PENGOPTIMUMAN EKSTRAKSI
ANDROGRAFOLIDA DARI SAMBILOTO DENGAN
RANCANGAN FRAKSIONAL FAKTORIAL
EULIS SITI NURASIAH
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
EULIS SITI NURASIAH. Pengoptimuman Ekstraksi Andrografolida dari Sambiloto
dengan Rancangan Fraksional Faktorial. Dibimbing oleh LATIFAH KOSIM
DARUSMAN dan MOHAMAD RAFI.
Andrografolida merupakan senyawa metabolit sekunder pada sambiloto
(
Andrographis paniculata
) yang digunakan sebagai antikanker, antiradang, dan
antimikrob. Pengkajian pada teknik dan kondisi ekstraksi perlu dilakukan untuk
memperoleh ekstrak yang maksimum dengan membandingkan tiga teknik ekstraksi
(maserasi, soxhlet, dan ultrasonikasi) dan menentukan kondisi optimum dari teknik
ekstraksi terbaik. Teknik terbaik untuk ekstraksi andrografolida adalah menggunakan
teknik maserasi. Kadar andrografolida hasil ekstraksi dengan teknik maserasi, soxhlet,
dan ultrasonikasi berturut-turut adalah 2.83%, 2.23%, dan 1.86%. Optimisasi kadar
andrografolida pada teknik maserasi menunjukkan bahwa nisbah dan frekuensi
berpengaruh nyata pada kadar andrografolida, sedangkan waktu ekstraksi tidak
berpengaruh nyata. Kondisi optimum ekstraksi andrografolida berdasarkan kadar prediksi
dari 27 kombinasi perlakuan adalah pada waktu ekstraksi 360 menit, nisbah bahan baku
dan pelarut 1 g/100 mL, dan frekuensi ekstraksi 5 kali dengan kadar yang diperoleh
4.83
℅
. Kondisi optimum ekstraksi andrografolida berdasarkan hasil analisis
menggunakan metode permukaan respons adalah pada waktu ekstraksi 300−352 menit,
nisbah bahan dan pelarut 1.25−1.28 g/100 mL, dan frekuensi ekstraksi 3−4 kali dengan
kadar 3.11−4.09
℅
.
ABSTRACT
EULIS SITI NURASIAH. Optimization for Extraction of Andrographolide from
Sambiloto by Fractional Factorial Design. Supervised by LATIFAH KOSIM
DARUSMAN and MOHAMAD RAFI.
PENGOPTIMUMAN EKSTRAKSI
ANDROGRAFOLIDA DARI SAMBILOTO DENGAN
RANCANGAN FRAKSIONAL FAKTORIAL
EULIS SITI NURASIAH
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Pengoptimuman Ekstraksi Andrografolida dari Sambiloto dengan
Rancangan Fraksional Faktorial
Nama : Eulis Siti Nurasiah
NIM : G44052962
Menyetujui
Pembimbing I, Pembimbing II,
Prof. Dr. Ir. Latifah K Darusman, MS
Mohamad Rafi, SSi, MSi
NIP 19530824 197603 2 001 NIP 19770316 200604 1010
Mengetahui
Ketua Departemen,
Prof. Dr. Ir. Tun Tedja Irawadi, MS
NIP 19501227 197603 2 002
PRAKATA
Segala puji senantiasa penulis panjatkan kepada Allah SWT karena atas rahmat,
hidayah, dan ridho-Nya penulis dapat menyelesaikan karya ilmiah ini. Shalawat serta
salam selalu penulis curahkan kepada Nabi Muhammad SAW, keluarga, sahabat, serta
pengikutnya hingga akhir zaman. Penulis melaksanakan penelitian sejak bulan April 2009
dengan tema penelitian optimisasi cara ekstraksi dan kondisinya, dengan judul
Pengoptimuman Ekstraksi Andrografolida dari Sambiloto dengan Rancangan Fraksional
Faktorial.
Penulis menyampaikan ucapan terima kasih kepada Ibu Prof. Dr. Ir. Latifah K.
Darusman, MS dan Bapak Mohammad Rafi, SSi, MSi sebagai pembimbing yang selalu
memberikan saran dan meluangkan waktu selama berkonsultasi; kepada Ibu Utami Dyah
Syafitri, SSi, MSi yang telah memberikan saran, kritik, dan bimbingan selama penelitian
dan penulisan karya ilmiah ini; kepada Pusat Studi Biofarmaka yang telah mendanai
sebagian biaya penelitian dan diikutsertakan dalam penelitian sambiloto. Terima kasih
kepada seluruh staf Departemen Kimia, staf Lab. Analitik, yaitu Ibu Nunung,
Om
Eman,
Pak Kosasih, Pak
Ridwan, dan Pak
Dede. Terima kasih kepada
Mbak
Wulan,
Mbak
Tuty,
dan Kak Zulhan atas arahannya yang sangat membangun; kepada seluruh staf Pusat Studi
Biofarmaka atas fasilitas, masukan, dan bantuan yang telah diberikan.
Terima kasih yang tak terhingga penulis sampaikan kepada Apa, Mamah, Atep, dan
semua Teteh serta Aa atas segala bantuan, baik doa, moril, materil, dan kasih sayangnya.
Semua keponakan Bibi terima kasih atas doa dan keceriaannya. Kepada Abi atas
dorongan semangat dan kesabarannya. Terima kasih kepada Ema, Ufa, Atih, Siti Uminah,
Wini, Widya, Riky, dan Kak Budi atas segala masukan dan dukungannya.
Semoga karya ilmiah ini bermanfaat.
Bogor, November 2009
RIWAYAT HIDUP
Penulis dilahirkan di Kumei, Kalimantan Tengah, pada tanggal 11 Januari 1987
dari ayah Djedjen Sujana dan Ibu Cumiati. Penulis merupakan putri ke-5 dari enam
bersaudara.
Tahun 2005 penulis lulus SMA Negeri 1 Cikampek dan pada tahun yang sama
lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih
Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan
Alam.
DAFTAR ISI
Halaman
DAFTAR TABEL... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN... viii
PENDAHULUAN ...
1
TINJAUAN PUSTAKA
Sambiloto (
Andrographis paniculata
) ... 1
Andrografolida ... 2
Maserasi ... 2
Soxhlet ... 3
Ultrasonikasi ... 3
Kromatografi Cair Kinerja Tinggi (KCKT) ... 3
Rancangan Acak Lengkap (RAL) ... 4
Rancangan 3
k-1Fraksional Faktorial... 4
BAHAN DAN METODE
Alat dan Bahan... 5
Metode Penelitian... 5
HASIL DAN PEMBAHASAN
Teknik Ekstraksi Terbaik ... 6
Kurva Standar dan Kadar Andrografolida Contoh... 8
Pemodelan dan Analisis Regresi ... 8
SIMPULAN DAN SARAN
Simpulan... 11
Saran ... 11
DAFTAR PUSTAKA ... 11
DAFTAR TABEL
Halaman
1 Rancangan 3
k-1fraksional faktorial ... 6
2 Sidik ragam RAL ... 8
3 Perbandingan kadar andrografolida hasil percobaan dengan dugaan ... 9
4 Pendugaan kadar andrografolida pada perlakuan yang tidak dicobakan ...10
DAFTAR GAMBAR
Halaman
1 Herba sambiloto ... 1
2 Struktur andrografolida... 2
3 Alat ekstraktor soxhlet ... 3
4 Skema alat KCKT ... 4
5 Kurva standar andrografolida... 8
6 Perilaku nisbah dan frekuensi pada kadar andrografolida ... 9
7 Kurva permukaan respons kadar pada nisbah dan frekuensi ekstraksi ...10
DAFTAR LAMPIRAN
Halaman
1 Diagram alir kerja ... 14
2 Kombinasi perlakuan pada tahap pengoptimuman teknik ekstraksi terbaik... 15
3 Kadar air serbuk herba sambiloto ... 16
4 Rendemen ekstrak contoh pada pemilihan teknik ekstraksi terbaik ...16
5 Kadar andrografolida contoh pada pemilihan teknik ekstraksi terbaik...17
6 Perhitungan teknik ekstraksi terbaik menggunakan RAL...18
7 Kromatogram pada pemilihan teknik ekstraksi terbaik ...20
8 Penentuan rendemen pada pengoptimuman teknik ekstraksi terbaik...20
9 Pengukuran standar andrografolida ...21
10 Penentuan kadar andrografolida pada teknik ekstraksi terbaik...21
PENDAHULUAN
Herba sambiloto (Andrographis paniculata) merupakan salah satu bahan obat tradisional yang paling banyak dipakai di Indonesia dan tumbuh subur di wilayah tropis Asia. Sambiloto dijuluki “The King of Bitter”
karena rasanya yang sangat pahit. Herba sambiloto memiliki khasiat sebagai diuretika, antipiretika, obat luka, serta diindikasikan sebagai obat kencing manis (Yulinah et al.
2001). Efek farmakologi sambiloto yang telah dilaporkan adalah sebagai antiradang, antikanker, antibakteri, serta menurunkan tekanan darah (Badan POM RI 2006).
Sambiloto mengandung 3 komponen utama, yaitu andrografolida, deoksi-andrografolida, dan neoandrografolida. Andrografolida merupakan komponen utama metabolit sekunder yang berguna sebagai bahan obat. Senyawa tersebut memiliki banyak aktivitas biologis, antara lain antiinflamasi, antialergi, hepatoprotektan, dan obat HIV (Liang et al. 2004).
Mengingat senyawa andrografolida memiliki banyak manfaat maka diperlukan pengkajian pada teknik ekstraksi dan kondisinya agar diperoleh ekstrak yang maksimum. Ekstraksi suatu komponen dari suatu bahan dipengaruhi oleh banyak faktor, antara lain jenis pelarut, konsentrasi pelarut, suhu, nisbah bahan−pelarut, frekuensi, dan waktu ekstraksi.
Berbagai teknik ekstraksi andrografolida telah dikembangkan, di antaranya ekstraksi klasik (maserasi, soxhlet, dan ultrasonikasi). Saat ini juga telah dikembangkan ekstraksi andrografolida menggunakan gelombang mikro (MAE) oleh Chen et al. (2008), kromatografi lawan arus kecepatan tinggi (Du
et al. 2003), dan ekstraksi dengan gas superkritik (Kumoro & Hasan 2007).
Beberapa metode telah dikembangkan untuk penentuan kadar andrografolida dalam herba sambiloto, di antaranya kromatografi cair kinerja tinggi (KCKT) dan high performance thin layer chromatography
(HPTLC) (Akowuoh et al. 2006; Lomlim et al. 2003), micellar electrokinetic capillary chromatography (MECC), micellar liquid chromatography (MLC), kromatografi mikroemulsi elektrokinetik (Yanfang et al.
2006), dan spektrofotometrik (Ruengsitagoon
et al. 2006).
Metode KCKT digunakan untuk menentukan kadar andrografolida pada penelitian ini. Berdasarkan Akowuoh et al.
(2006), metode KCKT lebih sensitif dibandingkan dengan metode HPTLC. Selain itu, metode KCKT memiliki limit deteksi yang lebih rendah dibandingkan dengan metode spektrofotometrik (Ruengsitagoon et al. 2006).
Penelitian ini bertujuan mencari teknik serta kondisi optimum pada ekstraksi andrografolida dari herba sambiloto menggunakan rancangan acak lengkap (RAL) dan fraksional faktorial. Teknik ekstraksi yang digunakan adalah maserasi, soxhlet, dan ultrasonikasi. Evaluasi dengan RAL digunakan untuk mengetahui teknik ekstraksi terbaik karena dianggap tidak ada faktor lain yang mempengaruhi ekstraksi selain teknik ekstraksi. Selanjutnya dilakukan pengoptimuman pada teknik ekstraksi terbaik dengan variasi nisbah antara jumlah bahan−pelarut, waktu, dan frekuensi ekstraksi. Tahap ini menggunakan rancangan fraksional faktorial untuk mengurangi jumlah kombinasi perlakuan yang dicobakan.
TINJAUAN PUSTAKA
Sambiloto (Andrographis paniculata)
Sambiloto (Gambar 1) tergolong tanaman terna yang tumbuh di berbagai habitat, seperti pinggiran sawah, kebun, atau hutan. Sambiloto banyak dijumpai hampir di seluruh kepulauan nusantara dan dikenal dengan beberapa nama daerah, seperti ki oray atau ki peurat (Jawa Barat), bidara, takilo, sambiloto (Jawa Tengah dan Jawa Timur), pepaitan atau ampadu (Sumatera). Tanaman ini terutama menyebar di Malaysia dan Indonesia (Sunardi 2008).
Gambar 1 Herba sambiloto.
2
sambiloto di daerah dengan curah hujan sebesar 2000-3000 mm/tahun dan tanaman ini dapat tumbuh hampir pada semua jenis tanah. Selama pertumbuhan tanaman sambiloto memerlukan banyak sinar matahari. Bunga dan buah sambiloto dapat dijumpai di India pada bulan Oktober atau antara Maret sampai Juli, di Australia bunga dan buah antara bulan Nopember sampai Juni, sedangkan di Indonesia bunga dan buah dapat ditemukan sepanjang tahun (Yusron et al. 2005).
Berdasarkan penelitian yang telah dilakukan diketahui bahwa herba sambiloto mengandung senyawa kimia antara lain diterpena lakton yang terdiri atas andrografolida, neoandrografolida, dehidro-andrografolida, flavonoid, tanin, dan saponin (Yusron et al. 2005). Kandungan kimia lain yang terdapat pada daun dan batang adalah panikulin, kalmegin, dan oksitosin yang memiliki rasa pahit (Sunardi 2008).
Herba sambiloto efektif untuk mengobati luka akibat gigitan ular dan serangga. Getah dari daun sambiloto yang dilumatkan dapat digunakan untuk pengobatan demam, sebagai tonik, dan untuk mengobati gatal-gatal pada kulit (Badan POM RI 2006). Saat ini sambiloto banyak diteliti untuk dikembangkan sebagai bahan baku obat modern, yaitu sebagai obat HIV (Liang et al. 2004).
Andrografolida
Andrografolida merupakan salah satu diterpena lakton utama pada herba sambiloto dan menjadi komponen utama yang berguna sebagai bahan obat. Studi farmakokinetik menunjukkan bahwa andrografolida diserap dan dapat dicerna dengan cepat oleh sistem metabolisme manusia dan tikus (Liang et al.
2004). Andrografolida terbukti memiliki efek sebagai antikanker sehingga memiliki potensi untuk dikembangkan sebagai sediaan terapi kanker. Selain itu andrografolida juga terbukti secara in vivo berpotensi sebagai antiradang (Badan POM RI 2006; Kumar et al. 2004) dan antimikrob (Singha et al. 2003).
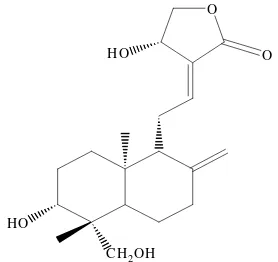
Andrografolida merupakan sebuah lakton trihidroksi takjenuh dengan rumus molekul C20H30O5 dan bobot molekul 350 g/mol (Gambar 2). Senyawa ini mudah larut dalam metanol, etanol, piridina, asam asetat, dan aseton, akan tetapi sedikit larut dalam air, yaitu kurang dari 1mg/g padatan terekstrak (Wongkittipong et al. 2004). Andrografolida merupakan serbuk pipih tak berwarna dengan titik leleh 228−230 °C (Du et al. 2003).
HO
CH2OH
O
HO O
Gambar 2 Struktur andrografolida.
Bagian tanaman yang paling banyak mengandung andrograpolida adalah daun, yaitu sebesar 2.15−2.95% (Akowuah et al. 2006). Hasil tersebut berasal dari 7 lokasi yang berbeda di Malaysia. Kadar andrografolida menurut Cheung et al. (2001) secara keseluruhan pada sambiloto adalah 3.54℅, pada bagian batang 1.11℅, dan bagian akar 0.61℅. Berdasarkan penelitian Yanfang
et al. (2006), kadar andrografolida pada sambiloto dari 2 lokasi berbeda di Cina sebesar 0.57 dan 1.27℅.
Maserasi
Maserasi adalah salah satu teknik ekstraksi yang bertujuan menarik suatu komponen tertentu dari sampel dengan pelarut tertentu. Maserasi dilakukan dengan me-rendam sampel dengan pelarut yang sesuai pada jangka waktu tertentu sehingga interaksi antara senyawa yang ingin diekstrak dengan pelarutnya dapat berlangsung maksimum (Houghton & Raman 1998). Pelarut akan berosmosis ke dalam sel melewati dinding sel. Isi sel akan berdifusi ke dalam pelarut. Umumnya pelarut ditambahkan sekurang-kurangnya sampai seluruh contoh tepat terendam. Pada isolasi produk alam dari jaringan tanaman, perendaman dihentikan jika uji fitokimia pada ekstrak telah memberikan hasil negatif bagi produk alam tersebut (Rahayu 2008).
3
bantuan gaya lain. Oleh karena itu, osmosis pelarut ke dalam padatan berlangsung statis dan rendemen biasanya rendah (Rahayu 2008).
Soxhlet
Ekstraksi soxhlet atau disebut juga ekstraksi sinambung merupakan teknik untuk mengekstrak komponen pada simplisia secara berkesinambungan. Dalam teknik ini, pelarut dididihkan perlahan-lahan dan uapnya akan bergerak melewati pipa samping alat soxhlet dan mengalami pendinginan saat melewati kondensor. Pelarut yang telah berkondensasi tersebut akan jatuh pada bagian dalam alat soxhlet yang berisi contoh yang telah dibungkus dengan kertas saring. Pelarut akan membawa serta bagian dari zat yang ingin diekstrak dari sampel tersebut serta ditampung pada labu tempat pelarut awal. Proses ini berlangsung terus-menerus sampai diperoleh hasil ekstraksi yang dikehendaki (Houghton & Raman 1998).
Pada teknik soxhlet suhu dibatasi oleh titik didih pelarut pada tekanan atmosfer. Kelebihan teknik ini adalah pelarut yang digunakan lebih sedikit dan selalu murni karena terjadi proses distilasi. Pelarut murni yang segar dapat menyaring senyawa dalam contoh lebih banyak dan membutuhkan waktu lebih singkat dibandingkan dengan maserasi atau perkolasi (Harvey 2000). Alat ekstraktor soxhlet dapat dilihat pada Gambar 3.
Gambar 3 Alat ekstraktor soxhlet.
Kekurangan teknik ini adalah tidak dapat digunakan untuk senyawa-senyawa termolabil. Selain itu, karena pelarut didaur ulang, ekstrak yang terkumpul pada labu bulat terus-menerus dipanaskan sehingga dapat menyebabkan reaksi peruraian oleh panas. Teknik ini terbatas pada ekstraksi dengan
pelarut murni dan tidak dapat digunakan untuk ekstraksi dengan campuran pelarut atau pelarut yang diasamkan atau dibasakan. Hal ini dikarenakan uapnya akan mempunyai komposisi yang berbeda dengan pelarut dalam labu bulat (Rahayu 2008).
Ultrasonikasi
Ultrasonikasi (ekstraksi ultrasonik) me-rupakan salah satu teknik yang dapat mempercepat dan menyederhanakan perlakuan pada contoh. Teknik ini mengandalkan energi gelombang yang menyebabkan proses kavitasi, yaitu suatu proses pembentukan gelembung-gelembung kecil akibat adanya transmisi gelombang ultrasonik. Ketika mengenai suatu larutan, energi ultrasonik menyebabkan timbulnya rongga akustik, dengan struktur bergelembung yang kemudian pecah. Proses tersebut membantu osmosis pelarut ke dalam dinding sel tanaman (Ashley et al. 2001).
Ultrasonikasi digunakan untuk ekstraksi senyawa organik nonatsiri dan semiatsiri dari padatan, seperti tanah, lumpur, dan limbah. Waktu kontak antara pelarut dan contoh terbatas. Oleh karena itu, penting untuk mengikuti prosedur, termasuk instruksi pengolahan untuk mencapai efisiensi ekstraksi. Ultrasonikasi dianjurkan untuk digunakan pada industri farmasi untuk mendapatkan ekstrak dengan kualitas yang baik dan memerlukan energi yang sedikit (Sulman et al. 2001).
Aplikasi ultrasonikasi telah di-kembangkan untuk tujuan ekstraksi analit utama dari matrik padatan yang diikuti pengukuran menggunakan AAS. Ultrasonikasi juga dikembangkan untuk preparasi contoh secara langsung dalam wadah contoh. Dengan demikian, hilangnya contoh dapat dicegah dan kemungkinan kontaminasi contoh dapat diminimumkan. Meskipun memiliki potensi yang sangat berguna, ultrasonikasi kurang berguna untuk proses analisis (Ashley et al.
2001).
Kromatografi Cair Kinerja Tinggi (KCKT)
4
jenis kromatografi cair adalah KCKT (Day & Underwood 1998).
Fase diam yang digunakan pada KCKT adalah padatan atau cairan, sementara fase geraknya adalah cairan. Teknik ini digunakan untuk pemisahan dan analisis secara kualitatif maupun kuantitatif pada senyawa yang tidak tahan panas atau tidak atsiri (Meyer 2004). Berdasarkan fase diamnya, KCKT terbagi menjadi KCKT fase normal dan fase terbalik. Fase normal jika menggunakan fase diam polar dan fase terbalik jika fase diam nonpolar (Harvey 2000). Komponen utama instrumen KCKT adalah reservoir fase gerak, sistem pompa, sistem injeksi sampel, kolom, dan detektor. Skema alat KCKT dapat dilihat pada Gambar 4.
Metode KCKT dapat digunakan untuk analisis kualitatif maupun kuantitatif pada bahan alam. Salah satunya seperti penentuan kadar andrografolida pada herba sambiloto yang telah dilakukan pada beberapa penelitian. Metode KCKT jauh lebih sensitif dan selektif dibandingkan dengan metode spektrofotometri pada penentuan kandungan komponen pada tanaman obat (Chen et al.
2007). Metode ini memiliki beberapa kelebihan, antara lain jumlah contoh yang digunakan sedikit (dalam skala mikroliter), waktu pemisahannya cepat dengan waktu retensi hanya beberapa menit, dan batas deteksi sampai ng/L (Day & Underwood 1998).
Gambar 4 Skema alat KCKT 1 = reservoir fase gerak, 2 = saluran transfer, 3 = pompa, 4 = sample injection, 5 = kolom, 6 = detektor, 7 = limbah, 8 = data (Meyer 2004).
Rancangan Acak Lengkap (RAL)
Rancangan acak lengkap (RAL) merupakan rancangan satu faktor yang menjaga faktor-faktor lain dalam kondisi tetap. Penerapan percobaan satu faktor dalam RAL biasanya digunakan jika kondisi unit
percobaan yang digunakan relatif homogen. Pada umumnya digunakan untuk percobaan yang dilakukan di laboratorium karena kehomogenan unit percobaan yang digunakan dapat dijamin. Pengacakan perlakuan dilakukan langsung pada unit percobaan. Model linear untuk RAL dapat dituliskan sebagai berikut (Matjik & Sumertajaya 2002):
Yij = + τi + εij
i = 1, 2, 3, ..., t dan j = 1, 2, 3, ..., r Yij = Respons pada perlakuan ke-i dan
ulangan ke-j
= Rataan umum
τi = Pengaruh perlakuan ke-i
εij = Pengaruh acak pada perlakuan ke-i
ulangan ke-j
Hipotesis: H0: τ1= τ2 = ... = τt = 0
H1: paling sedikit ada satu i dimana τi≠ 0
Hipotesis nol akan diterima bila nilai F-hitung lebih kecil dari F tabel atau nilai peluang nyatanya lebih besar dari taraf nyata (α) (Matjik & Sumertajaya 2002).
Rancangan 3k-1 Fraksional Faktorial
Rancangan faktorial merupakan salah satu cara yang digunakan dalam melakukan suatu percobaan untuk mengetahui pengaruh dua faktor atau lebih pada respons yang diharapkan. Salah satu perancangan percobaan dengan rancangan faktorial adalah rancangan 3k faktorial. Pada rancangan ini dilakukan penyusunan faktorial untuk k faktor pada level 3. Pada rancangan faktorial lengkap, semakin banyak faktor dan taraf yang dicobakan, jumlah kombinasi perlakuan akan meningkat. Akibatnya, membutuhkan waktu dan biaya penelitian yang besar (Montgomery 2001).
5
Rancangan fraksional faktorial umumnya akan menghasilkan beberapa kombinasi yang mungkin. Oleh karena itu, dari setiap kombinasi yang dihasilkan perlu diperiksa kelayakan kombinasi taraf atribut yang muncul. Salah satu fraksi percobaan yang sering digunakan pada rancangan fraksional faktorial 3k adalah fraksi sepertiga, yaitu mencobakan hanya sepertiga bagian dari kombinasi perlakuan lengkap. Bentuk rancangan percobaan ini adalah 3k-1 (Montgomery 2001).
BAHAN DAN METODE
Alat dan Bahan
Alat-alat yang digunakan antara lain KCKT La Chrome Elite dengan detektor UV-Vis L-2420 (Hitachi), kolom C-18, radas soxhlet, dan Ultrasonic Processor.
Bahan-bahan yang digunakan antara lain herba sambiloto yang diperoleh dari Kebun Cikabayan (Bogor) dan standar andrografolida
(Sigma Aldrich).
Metode Penelitian
Penelitian dilakukan melalui beberapa tahap, yaitu penentuan kadar air, pemilihan teknik ekstraksi, identifikasi, selanjutnya pengoptimuman pada teknik ekstraksi terbaik. Tahap identifikasi dilakukan dengan KCKT. Diagram alir kerja dapat dilihat pada Lampiran 1.
Penentuan Kadar Air ((((AOAC 1984)
Cawan porselen dikeringkan pada suhu 105 °C. Setelah didinginkan dalam eksikator, kemudian ditimbang. Sebanyak 3 g contoh herba sambiloto ditimbang (dicatat sampai 4 desimal dalam gram), dimasukkan dalam cawan, dan dikeringkan pada suhu 105 °C sampai diperoleh bobot yang konstan.
Maserasi (Akowuah et al. 2006)
Serbuk herba sambiloto ditimbang sebanyak 1 g, direndam dengan 100 mL metanol selama 300 menit pada suhu ruang, dan diaduk dengan alat kocok secara terus-menerus. Maserat kemudian disaring. Ekstraksi dilakukan sebanyak 1 kali kemudian ekstrak dipekatkan. Ekstrak yang diperoleh ditimbang dan dilarutkan kembali ke dalam metanol sampai volume total 10 mL untuk dilakukan analisis KCKT. Dilakukan 3 kali ulangan.
Cara Soxhlet (Wongkittipong et al. 2004)
Serbuk herba sambiloto ditimbang sebanyak 1 g. Setelah itu diekstraksi dengan 100 mL metanol menggunakan labu 125 mL. Ekstraksi dilakukan selama 210 menit pada suhu 75 °C tekanan normal dan dilakukan sebanyak 1 kali kemudian ekstrak dipekatkan menggunakan penguap putar. Ekstrak yang diperoleh ditimbang dan dilarutkan dengan metanol hingga volume 10 mL untuk dilakukan analisis KCKT. Dilakukan 3 kali ulangan.
Ultrasonikasi ((((Yanfang et al. 2006)
Serbuk herba sambiloto ditimbang sebanyak 1 g. Kemudian diekstraksi dengan 100 ml metanol selama 30 menit menggunakan Ultrasonic Processor pada suhu ruang. Setelah itu, didiamkan pada suhu kamar selama 30 menit kemudian ekstrak disaring. Ekstraksi diulang sebanyak 3 kali, dikumpulkan, kemudian dipekatkan. Ekstrak yang diperoleh ditimbang dan diencerkan dengan metanol hingga volume 10 mL untuk dilakukan analisis KCKT. Dilakukan 3 kali ulangan.
Penentuan Kadar Andrografolida dengan KCKT (Akowuah et al. 2006)
Andrografolida dipisahkan dengan menggunakan kolom fase terbalik. Suhu selama elusi dijaga 25 oC dengan volume injeksi 10 µL dan laju alir 1 mL/menit pada panjang gelombang 210 nm. Fase gerak yang digunakan adalah metanol−air (6:4 v/v) pada pH 2.8 yang diatur dengan asam fosfat. Larutan stok andrografolida disiapkan 1024 ppm dalam metanol. Larutan standar disiapkan dengan konsentrasi 10 ppm untuk tahap pemilihan teknik ekstraksi terbaik. Sementara untuk tahap pengoptimuman teknik ekstraksi terbaik digunakan 3 deret standar dengan konsentrasi 10, 100, dan 1024 ppm. Larutan standar dan ekstrak sambiloto diinjeksikan ke dalam sistem KCKT dan konsentrasi sampel ditentukan menggunakan metode standar eksternal.
Pengoptimuman pada Teknik Ekstraksi Terbaik
6
Evaluasi Data Analisis
Data hasil analisis pada pemilihan teknik ekstraksi dievaluasi menggunakan rancangan acak lengkap (RAL). Jika nilai F hitung < F tabel, maka H0 diterima. Artinya teknik ekstraksi tidak memengaruhi kadar andrografolida pada sambiloto. Sementara itu, jika F hitung > F tabel, maka H0 ditolak. Artinya, minimal ada 1 teknik ekstraksi yang memengaruhi kadar andrografolida. Selanjutnya dilakukan uji lanjut untuk me-ngetahui teknik yang paling berpengaruh pada kadar andrografolida, sehingga diperoleh teknik ekstraksi terbaik. Nilai Ftabel = 5.143 untuk 3 kali ulangan pada selang kepercayaan 95%.
Teknik ekstraksi terbaik yang diperoleh pada tahap pertama dioptimisasi meng-gunakan rancangan fraksional faktorial 3k-1 yang dapat dilihat pada Tabel 1. Data hasil analisis pada pengoptimuman kondisi ekstraksi diolah menggunakan perangkat lunak Minitab 14 dan SAS 9.1 dengan aplikasi metode permukaan respons. Tahap pertama adalah melihat korelasi antara rendemen ekstrak kental dan kadar andrografolida hasil analisis dengan metode KCKT. Jika nilai-p >
α maka tidak ada korelasi antara rendemen ekstrak kental dengan kadar andrografolida.
Tabel 1 Rancangan 3k-1 fraksional faktorial
Berdasarkan kadar yang diperoleh dari 9 percobaan hasil fraksionalisasi dibuat suatu model regresi. Setelah itu, dilihat pengaruh dari setiap peubah bebas menggunakan uji-t. Jika nilai-p >α maka pengaruh peubah relatif tidak ada. Berdasarkan persamaan yang diperoleh dapat dilakukan prediksi kadar andrografolida untuk kombinasi lain dari peubah yang dioptimisasi. Kemudian dilihat kedekatan hasil prediksi dengan hasil analisis. Jika R2 mendekati 1 maka model regresi yang dibuat cukup baik.
HASIL DAN PEMBAHASAN
Teknik Ekstraksi Terbaik
Tanaman sambiloto yang digunakan pada penelitian ini adalah campuran bagian batang dan daun. Serbuk herba sambiloto merupakan bahan yang berasal dari tumbuhan yang jika dianalisis sering mengandung kadar air dengan jumlah yang tidak menentu. Oleh karena itu, perlu dilakukan penentuan kadar air yang terkandung di dalam bahan untuk mengetahui umur simpan bahan dan sebagai faktor koreksi bagi rendemen dan kadar andrografolida.
Kadar air serbuk herba sambiloto yang diperoleh adalah 6.57% ± 0.1987 (Lampiran 3). Nilai yang diperoleh masih di bawah standar serbuk obat tradisional, yaitu kadar air harus di bawah 10% (Badan POM RI 2006). Nilai tersebut menunjukkan bahwa sampel tahan disimpan dalam jangka waktu yang lama. Semakin besar kadar air yang diperoleh, kemungkinan mikroba untuk tumbuh pada bahan akan semakin besar. Oleh karena itu, bahan tidak baik disimpan dalam jangka waktu yang lama sehingga bahan yang telah diekstrak dan dipekatkan harus segera dianalisis.
Serbuk herba sambiloto yang digunakan pada penelitian berukuran 100 mesh. Semakin kecil ukuran partikel, luas permukaan bahan akan semakin besar. Oleh karena itu, interaksi antara pelarut pengekstrak dan bahan yang diekstraksi akan semakin efektif sehingga pelarut pengekstrak akan lebih mudah berpenetrasi ke dalamnya. Diharapkan akan semakin banyak kadar andrografolida yang diperoleh. Metanol dipilih sebagai pengekstrak sambiloto karena hampir semua senyawa pada jaringan tumbuhan dapat terekstrak oleh metanol. Selain itu, sifat andrografolida yang semipolar cenderung polar karena adanya gugus hidroksil. Oleh karena itu, metanol cocok untuk digunakan sebagai pelarut andrografolida karena memiliki kemiripan kepolaran.
Teknik ekstraksi andrografolida yang digunakan pada penelitian ini adalah maserasi, soxhlet, dan ultrasonikasi. Perbedaan ketiga teknik tersebut berdasarkan jenis energi yang terlibat pada proses ekstraksi. Penelitian ini dilakukan untuk mengetahui keterlibatan jenis energi dari ketiga teknik pada ekstraksi andrografolida sehingga diperoleh kadar andrografolida yang tinggi.
Ekstrak yang diperoleh selanjutnya dipekatkan dengan rotavapor pada suhu 40 °C Observasi Nisbah
7
untuk mencegah kemungkinan terjadinya kerusakan komponen yang terkandung dalam ekstrak. Prinsip penguap putar adalah penurunan tekanan sehingga pelarut dapat menguap pada suhu di bawah titik didihnya. Jadi zat yang terkandung dalam pelarut tidak rusak oleh suhu tinggi. Ekstrak sambiloto yang diperoleh berwarna hijau pekat dan memiliki ciri bau yang menyengat.
Nilai rerata rendemen yang diperoleh pada maserasi, soxhlet, dan ultrasonikasi berturut-turut adalah 33.33, 30.78, dan 30.43% (Lampiran 4). Ekstraksi dengan cara maserasi menghasilkan rendemen paling besar dibandingkan dengan soxhlet dan ultrasonikasi. Ekstraksi dengan cara soxhlet menghasilkan ekstrak dengan warna hijau yang lebih cerah dibandingkan dengan maserasi. Hal ini dimungkinkan adanya senyawa tidak tahan panas yang terkandung dalam herba sambiloto. Sehingga senyawa tersebut rusak dan tidak terekstrak oleh metanol. Teknik ultrasonikasi menghasilkan ekstrak dengan warna yang hampir sama dengan ekstrak hasil soxhlet.
Identifikasi senyawa andrografolida dalam penelitian ini menggunakan teknik KCKT fase terbalik (reversed phase). Kondisi KCKT yang digunakan dikembangkan oleh Akowuoh et al. (2006) dengan menggunakan fase gerak yang bersifat polar, yaitu campuran metanol-air 6:4 (v/v) pada pH 2.8 yang diatur dengan asam fosfat. Suhu selama elusi dijaga 25 °C dengan volume injeksi 10 µL pada panjang gelombang 210 nm dan laju alir 1 mL/menit.
Pemisahan terbaik andrografolida diperoleh pada saat laju alir 1 mL/menit (Chen
et al. 2007) dan fase gerak campuran metanol-air 6:4 (v/v) (Cheung et al. 2001). Komposisi metanol lebih banyak dibandingkan dengan air untuk mencegah hidrolisis cincin lakton pada andrografolida. Nilai pH yang digunakan bersifat asam karena andrografolida tidak stabil pada pH basa. Pada kondisi basa cincin lakton pada andrografolida akan mengalami hidrolisis sehingga mengalami pembukaan cincin dan lakton akan cenderung berada dalam bentuk garam karboksilat (Ruengsitagoon et al. 2006; Cheung et al. 2001).
Kolom yang digunakan pada identifikasi andrografolida adalah kolom C18. Kolom ini bersifat nonpolar, sehingga dengan kondisi KCKT yang digunakan, senyawa yang memiliki sifat lebih polar akan terelusi lebih dahulu dan senyawa yang bersifat nonpolar akan lebih lama tertahan pada fase diam
(Skoog et al. 1998). Kolom C18 lebih cocok untuk pemisahan dan analisis kuantitatif senyawa-senyawa yang bersifat sedikit polar dan nonpolar (Meyer 2004).
Kadar androgafolida hasil ekstraksi dengan teknik maserasi, soxhlet, dan ultrasonikasi berturut-turut adalah 2.83, 2.23, dan 1.86%. Nilai simpangan baku untuk masing-masing teknik adalah 0.0954, 0.1474, dan 0.0681. Perhitungan kadar andrografolida dapat dilihat pada Lampiran 5. Kadar andrografolida hasil ekstraksi menggunakan radas soxhlet lebih sedikit dibanding hasil maserasi. Hal ini disebabkan andrografolida stabil pada suhu ruang (Ruengsitagoon et al. 2006).
Andrografolida memiliki cincin lakton pada strukturnya. Cincin tersebut merupakan bagian yang sangat rentan dari andrografolida. Bagian ini sangat reaktif dan mudah mengalami penataan ulang. Cincin lakton pada andrografolida akan terdestruksi jika mengalami pemanasan dengan suhu tinggi. Reaksi destruksi cincin lakton melalui mekanisme hidrolisis dan trans-esterifikasi. Suhu maksimum agar 98% andrografolida dapat terekstrak adalah 67 °C (Wongkittipong
et al. 2004).
Ekstraksi dengan gelombang ultrasonik menghasilkan kadar andrografolida paling kecil. Gelombang ultrasonik adalah gelombang dengan frekuensi lebih dari 20 kHz sehingga memiliki energi yang besar. Energi tersebut dapat menyebabkan cincin lakton pada andrografolida mengalami pembukaan cincin sehingga terdestruksi. Oleh karena itu, dihasilkan kadar andrografolida yang kecil pada ekstraksi menggunakan ultrasonikasi.
Hasil analisis data menggunakan rancangan acak lengkap (RAL) menunjukkan bahwa ketiga teknik berbeda dalam menghasilkan rerata kadar andrografolida pada taraf nyata 95%. Hal ini ditunjukkan dengan nilai F hitung = 60.6186 yang lebih besar dari F0.05 (2,6) = 5.143 (Lampiran 6). Uji lanjut diperlukan untuk mengetahui pengaruh teknik ekstraksi pada kadar andrografolida.
8
aman dan sederhana untuk menghasilkan kadar andrografolida yang besar. Koefisien keragaman dari data yang diperoleh adalah 4.71%. Hal ini menunjukkan unit-unit percobaan yang digunakan relatif homogen. Hasil analisis RAL dapat dilihat pada Tabel 2.
Tabel 2 Sidik ragam RAL
*SK: sumber keragaman, db: derajat bebas, JK: jumlah kuadrat, KT: kuadrat tengah.
Kromatogram pada pemilihan teknik ekstraksi terbaik dapat dilihat pada Lampiran 7. Berdasarkan kromatogram yang dihasilkan diketahui bahwa puncak andrografolida muncul dengan waktu retensi 3 menit. Setiap kromatogram yang dihasilkan menunjukkan adanya serapan pada waktu retensi kurang dari 2 menit. Serapan tersebut merupakan serapan dari pelarut, yaitu metanol. Hal ini disebabkan panjang gelombang yang digunakan dekat dengan daerah UV cutoff
metanol, yaitu 205 nm (Meyer 2004). Pada daerah UV cutoff pelarut murni akan memberikan serapan, sehingga akan ada puncak dari pelarut.
Kurva Standar dan Kadar Andrografolida Contoh
Maserasi merupakan teknik ekstraksi terbaik yang diperoleh pada tahap pertama. Selanjutnya dilakukan pengoptimuman pada teknik maserasi menggunakan rancangan fraksional faktorial 3k-1. Berdasarkan penelitian yang dilakukan, diketahui bahwa semakin lama waktu ekstraksi rendemen total yang diperoleh semakin besar. Semakin banyak frekuensi ekstraksi rendemen total yang dihasilkan semakin besar sampai ekstraksi dilakukan tiga kali. Namun, frekuensi ekstraksi 5 kali menghasilkan rendemen yang lebih kecil. Hal ini disebabkan komponen telah seluruhnya terekstrak. Semakin besar nisbah bahan−pelarut, semakin kecil rendemen yang dihasilkan. Hal ini disebabkan belum seluruhnya komponen dalam sambiloto terekstrak. Rendemen yang dihasilkan pada pengoptimuman ekstraksi menggunakan teknik ekstraksi diberikan pada Lampiran 8.
Kurva standar andrografolida dibuat dengan menginjeksikan larutan standar
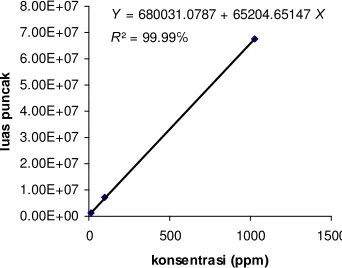
andrografolida pada 3 konsentrasi berdasarkan metode Akowuoh et al. (2006). Persamaan garis yang diperoleh untuk kurva standar andrografolida adalah Y = 680031.0787 + 65204.65147x dengan R2 = 99.99℅ (Gambar 5). Hasil tersebut menunjukkan bahwa konsentrasi mampu menerangkan keragaman luas puncak sebesar 99.99% dan hanya 0.01% yang diterangkan oleh faktor lain. Data luas puncak untuk pembuatan kurva standar diberikan pada Lampiran 9.
0.00E+00 1.00E+07 2.00E+07 3.00E+07 4.00E+07 5.00E+07 6.00E+07 7.00E+07 8.00E+07
0 500 1000 1500
konsentrasi (ppm) lu a s p u n c a k
Y = 680031.0787 + 65204.65147 X R² = 99.99℅
Gambar 5 Kurva standar andrografolida.
Konsentrasi andrografolida dalam contoh dapat ditentukan berdasarkan kurva standar yang diperoleh. Setelah itu dapat ditentukan kadar andrografolida pada contoh. Kadar andrografolida dari setiap perlakuan yang dicobakan dapat dilihat pada Lampiran 10.
Pemodelan dan Analisis Regresi
Tahap pengoptimuman dilakukan sebanyak 3 ulangan untuk setiap observasi pada 9 observasi hasil fraksionalisasi. Akan tetapi, diperoleh nilai simpangan baku relatif yang cukup besar. Setelah dilakukan uji Q pada data yang diperoleh dari 3 ulangan, terdapat pencilan. Oleh karena itu, pemodelan dilakukan dengan menggunakan 2 ulangan. Pencilan yang dihasilkan disebabkan terjadinya galat sistematik yang dapat bersumber dari galat pengukuran dan personal pada saat percobaan berlangsung.
Tahap awal pada pengoptimuman dan analisis data adalah penentuan korelasi antara rendemen ekstrak kental dengan kadar andrografolida yang diperoleh secara kuantitatif dengan metode KCKT. Hasil uji korelasi menunjukkan bahwa secara keseluruhan tidak ada korelasi yang baik antara rendemen ekstrak kental dengan kadar andrografolida. Hal ini dibuktikan dengan nilai-p = 0.595 yang lebih besar dari α = 0.05. Hasil uji korelasi terlihat pada Lampiran 11. SK* db* JK* KT*
9
Berdasarkan nilai kadar andrografolida yang diperoleh dari sembilan kombinasi hasil fraksionalisasi, dibuat suatu model regresi menggunakan metode permukaan respons. Persamaan yang diperoleh:
Kadar = 15.327778 + 7.707778 nisbah -0.099579 waktu -1.871111 frekuensi -1.676667 nisbah2 -0.008870 waktu.nisbah + 0.000153 waktu2 -0.156111 frekuensi.nisbah + 0.007125 frekuensi.waktu + ε
R2 = 95.61%
Hasil analisis regresi yang diperoleh menunjukkan bahwa frekuensi berpengaruh nyata secara linear dan nisbah berpengaruh nyata secara kuadratik. Hal ini terlihat dari nilai-p yang lebih kecil dari α = 0.05. Sementara itu, waktu ekstraksi tidak berpengaruh nyata karena nilai-p lebih besar dari α = 0.05. Perilaku nisbah dan frekuensi ekstraksi dapat dilihat pada Gambar 6.
nisbah (g/100 mL)
k a d a r A P 2.0 1.0 0.5 3.4 3.2 3.0 2.8 2.6 2.4 2.2
a
Frekuensi Ekstraksi K a d a r A P 5 3 1 3.0 2.9 2.8 2.7 2.6b
Gambar 6 Perilaku nisbah (a) dan frekuensi (b) pada kadar andrografolida.
Gambar 6 hanya menunjukkan pengaruh masing-masing faktor pada kadar tanpa memperhatikan pengaruh faktor lain. Berdasarkan gambar tersebut diketahui bahwa kadar andrografolida meningkat dengan ber-tambahnya frekuensi ekstraksi. Semakin banyak frekuensi ekstraksi maka semakin sering terjadi kontak antara contoh dan pelarut, sehingga semakin banyak
andrografolida yang terekstrak. Berdasarkan kadar prediksi diketahui bahwa kadar andrografolida terbesar diperoleh pada saat frekuensi ekstraksi 5 kali.
Nisbah bahan−pelarut berpengaruh nyata secara kuadratik pada kadar andrografolida. Gambar 6 menunjukkan kadar andrografolida meningkat dengan bertambahnya nisbah bahan−pelarut sampai nisbah yang digunakan 1 g/100 mL. Jika ekstraksi dilakukan kurang dari 1 g/100 mL, kadar andrografolida yang dihasilkan lebih kecil dibanding 1 g/100 mL. Hal ini disebabkan sudah seluruh andrografolida dalam contoh terekstrak. Jika lebih dari 1 g/100 mL, dimungkinkan andrografolida dalam sampel belum terekstrak sempurna.
Waktu ekstraksi tidak berpengaruh nyata pada kadar andrografolida. Hal ini menunjukkan bahwa berapapun lamanya waktu ekstraksi yang dilakukan, tidak menghasilkan kadar andrografolida yang berbeda nyata. Berdasarkan percobaan yang dilakukan dengan menggunakan waktu 240, 300, dan 360 menit diketahui bahwa kadar andrografolida terbesar diperoleh pada waktu ekstraksi 360 menit.
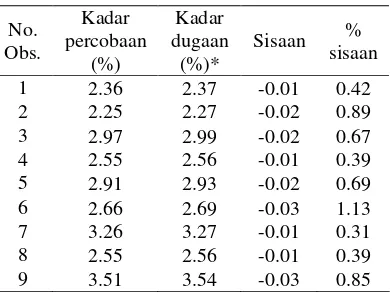
Berdasarkan model yang diperoleh dilakukan pendugaan kadar andrografolida untuk kombinasi perlakuan yang dicobakan. Perbandingan kadar andrografolida hasil percobaan dengan kadar dugaan terlihat pada Tabel 3. Berdasarkan Tabel 3 diketahui bahwa secara umum sisaannya relatif kecil dengan persentase kurang dari 2% dan keragaman dari sisaan sebesar 6.94×10-5. Hal ini memperlihatkan model yang digunakan memiliki keakuratan yang baik karena hasil percobaan mendekati hasil dugaan model.
Tabel 3 Perbandingan kadar andrografolida hasil percobaan dengan dugaan
*Diperoleh berdasarkan perhitungan dengan model regresi. No. Obs. Kadar percobaan (%) Kadar dugaan (%)*
Sisaan % sisaan
10
2.0 1.5 kadar 2.5 3.0 3.5 nisbah 1.0 1.0 2.5 0.5 4.0 5.5 frekuensiPemeriksaan sisaan merupakan salah satu cara mengetahui kebaikan model regresi. Sisaan merupakan selisih antara nilai hasil percobaan dengan nilai yang diramalkan oleh model regresi, dengan kata lain sisaan merupakan bagian yang tidak dapat dijelaskan oleh model regresi. Semakin kecil nilai sisaan berarti semakin baik model regresi yang diperoleh (Draper & Smith 1992).
Cara lain untuk mengetahui kebaikan model adalah melalui koefisien determinasi,
R2, dan koefisien keragaman model. Suatu model dikatakan baik jika nilai R2 yang diperoleh mendekati 1. Nilai koefisien keragaman berbeda untuk setiap bidang ilmu. Jika percobaan dilakukan di laboratorium nilai koefisien keragaman untuk model regresi yang baik adalah kurang dari 10% (Matjik & Sumertajaya 2002). Model regresi yang diperoleh cukup baik karena nilai R2 = 95.61% dan koefisien keragaman 4.30%.
Model regresi yang diperoleh digunakan untuk menduga kadar andrografolida pada 18 kombinasi perlakuan yang tidak dicobakan. Hasil pendugaan dapat dilihat pada Tabel 4.
Tabel 4 Pendugaan kadar andrografolida pada perlakuan yang tidak dicobakan Nisbah (g/100 mL) Waktu (menit) Frekuensi ekstraksi Kadar* (%b/b)
0.5 240 3 1.89
0.5 240 5 1.42
0.5 300 1 1.52
0.5 300 3 1.89
0.5 360 1 1.76
0.5 360 5 4.23
1 240 1 3.83
1 240 3 3.19
1 300 1 2.70
1 300 5 3.15
1 360 3 3.76
1 360 5 4.83
2 240 1 4.22
2 240 5 2.33
2 300 3 2.47
2 300 5 2.38
2 360 1 2.01
2 360 3 2.78
*Diperoleh berdasarkan perhitungan model regresi.
Berdasarkan hasil prediksi kadar andrografolida pada 27 kombinasi perlakuan menggunakan model regresi yang diperoleh, diketahui bahwa kondisi optimum ekstraksi andrografolida adalah pada waktu ekstraksi 360 menit dengan nisbah 1 g/100 mL dan frekuensi ekstraksi 5 kali. Kadar andrografolida yang diperoleh adalah 4.83%.
Kondisi optimum ekstraksi andrografolida hasil analisis menggunakan metode permukaan respons dapat dilihat berdasarkan kurva permukaan respons pada Gambar 7. Penentuan kondisi optimum ini berdasarkan kadar prediksi dari 9 kombinasi perlakuan yang dicobakan dengan dua ulangan.
Gambar 7 Kurva permukaan respons kadar pada nisbah dan frekuensi ekstraksi.
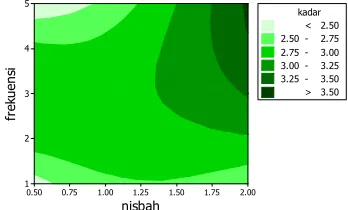
Kurva permukaan respons tersebut menunjukkan bahwa kadar optimum andrografolida berada pada kisaran 3.11-4.09℅. Kadar tersebut diperoleh pada waktu ekstraksi 300−352 menit, nisbah bahan−pelarut 1.25−1.28 g/100 mL, dan frekuensi ekstraksi 3−4 kali. Kisaran kondisi optimum berdasarkan peta kontur dapat dilihat pada Gambar 8.
Gambar 8 Peta kontur kadar pada frekuensi dan nisbah.
11
Kadar andrografolida hasil percobaan berada pada kisaran kadar andrografolida hasil penelitian sebelumnya, yaitu menurut Akowuah et al. (2006) andrografolida pada bagian daun 2.15-2.95%. Hasil tersebut berasal dari tujuh lokasi yang berbeda di Malaysia. Kadar andrografolida menurut Cheung et al. (2001) secara keseluruhan pada sambiloto adalah 3.54%, pada bagian batang 1.11℅, dan bagian akar 0.61%. Berdasarkan penelitian Yanfang et al. (2006) kadar andrografolida pada sambiloto dari dua lokasi berbeda di Cina sebesar 0.57 dan 1.27%. Perbedaan yang teramati disebabkan bahwa kadar andrografolida dipengaruhi oleh tempat tanaman tumbuh, perbedaan unsur hara dalam tanah, cuaca, serta keadaan lingkungan yang berbeda dapat menyebabkan perbedaan kadar andrografolida pada sambiloto.
SIMPULAN DAN SARAN
Simpulan
Pemilihan teknik ekstraksi terbaik untuk ekstraksi andrografolida dari herba sambiloto menunjukkan bahwa maserasi merupakan teknik ekstraksi terbaik. Kadar androgafolida hasil ekstraksi dengan teknik maserasi, soxhlet, dan ultrasonikasi berturut-turut adalah 2.83, 2.23, dan 1.86%. Pengoptimuman kadar andrografolida pada teknik ekstraksi terbaik menunjukkan nisbah dan frekuensi berpengaruh nyata, sedangkan waktu ekstraksi tidak berpengaruh nyata pada kadar andrografolida. Kondisi optimum ekstraksi andrografolida berdasarkan kadar prediksi dari 27 kombinasi perlakuan adalah pada waktu ekstraksi 360 menit, nisbah 1 g/100 mL, dan frekuensi ekstraksi 5 kali dengan kadar yang diperoleh 4.83%. Kondisi optimum ekstraksi andrografolida berdasarkan hasil analisis menggunakan metode permukaan respons adalah pada waktu ekstraksi 300−352 menit, nisbah bahan dan pelarut 1.25 g/100 mL−1.28 g/100 mL, dan frekuensi ekstraksi 3−4 kali dengan kadar 3.11−4.09℅.
Saran
Perlu dilakukan kisaran taraf yang lebih luas pada parameter waktu dan frekuensi karena kondisi optimum berdasarkan model regresi teramati pada ujung taraf. Selain itu perlu dilakukan validasi pada kondisi optimum yang diperoleh.
DAFTAR PUSTAKA
Akowuoh GA, Zhari I, Norhayati I, Mariam A. 2006. HPLC and HPTLC densitometric determination of andrographolides and antioxidant potential of Andrographis paniculata. Journal of Food Composition and Analysis 19:118-126.
Ashley K, Andrews RN, Cavazosa L, Demange M. 2001. Ultrasonic extraction as a sample preparation technique for elemental analysis by atomic spectrometry. Journal of Analytical Atomic Spectrometry 16:1147-1153. [AOAC] Association of Official Analytical
Chemist. 1984. Official Methods of Analysis of AOAC International. Washington DC: AOAC International. [Badan POM RI] Badan Pengawas Obat dan
Makanan. 2006. Serial Data Terkini Tumbuhan Obat: Sambiloto, Andrographis paniculata (Burm. F.) Ness. Jakarta: Badan Pengawas Obat dan Makanan Republik Indonesia.
Chen L, Yu A, Zhuang X, Zhang K, Wang X. 2007. Determination of andrographolide and dehydroandrographolide in rabbit plasma by on-line solid phase extraction of high-performance liquid chromatography.
Talanta 74:146-152.
Chen L et al. 2008. Application of on-line microwave sample-preparation techniques.
Trend in Analytical Chemistry 27:151-159.
Cheung HY, Cheng CS, Kong CK. 2001. Determination of bioactive diterpenoids from Andrographis paniculata by micellar electrokinetic chromatography. Journal of Chromatography A 930:171-176.
Christian GD. 1986. Analytical Chemistry 4th Editions. New York: Wiley.
Day RA, Underwood AL. 1998. Analisis kimia kuantitatif. Sofyan I, penerjemah; Wibi HH, Simarmata L, editor. Jakarta: Penerbit Erlangga. Terjemahan dari:
Quantitative Analysis.
Draper N, Smith H. 1992. Analisis Regresi Terapan. Ed ke-2. Sumantri B, penerjemah. Jakarta: Gramedia Pustaka Utama. Terjemahan dari: Applied Regression Analysis.
Du Q, Jerz G, Winterhalter P. 2003. Separation of andrographolide and neoandrographolide from the leaves of
12
Harvey D. 2000. Modern analytical chemistry. New York: McGraw-Hill. Houghton PJ, Raman A. 1998. Laboratory
Handbook for the Fractionation of Natural Extract. London: Chapman & Hall. Kumar RA, Sridevi K, Kumar NV, Nanduri S,
Rajagopal S. 2004. Anticancer and immunostimulatory compounds from
Andrographis paniculata. Journal of Ethnopharmacology 92:291-295.
Kumoro AC, Hasan M. 2007. Supercritical carbon dioxide extraction of andrographolide from Andrographis paniculatu: Effect of the solvent flow rate, pressure, and temperature. Chinese Journal of Chemical Engineering 15:877-883.
Liang C, Feng Q, Naili W, Xinsheng Y. 2004. Four new andrographolide metabolites in human urine. Chemical & Pharmaceutical Bulletin 52:772-775.
Lomlim L, Jirayupong N, Plubrukarn A. 2003. Heat-accelerated degradation of solid-state andrographolide. Chemical & Pharmaceutical Bulletin 51:24-26. Matjik AA, Sumertajaya IM. 2002.
Perancangan Percobaan dengan Aplikasi SAS dan Minitab. Vol I. Ed ke-2. Bogor: IPB P.
Meyer VR. 2004. Practical High-Performance Liquid Chromatography. Ed ke-4. New York: John Wiley.
Montgomery DC. 2001. Design and Analysis of Experimental. Ed ke-5. New York: Wiley.
Rahardo J, Rahardja S. 2001. Perbandingan metode 2k-p fractional factorial dengan Metode Taguchi pada proses pembuatan
fiber glass. Journal of Theological Interpretation 3:1-8.
Rahayu SS. 2008. Ekstraksi. [terhubung berkala]. http://medicafarma.com. [22 Okt 2009].
Ruengsitagoon W, Anuntakarun K, Aromdee C. 2006. Flow injection spectrophotometric determination of andrographolide from Andrographis paniculata. Talanta 69:900-905.
Singha PK, Roy S, Dey S. 2003. Antimicrobial activity of Andrographis paniculata.Fitoterapia 74:692-694. Skoog DA, Holler FJ, Nieman TA. 1998.
Principle of Instrumental Analysis. Ed ke-5. Florida: Saunders College Publishing. Sulman MG, Semagina NV, Ankudinova TV.
2001. Ultrasonic extraction of biologically active compounds from the vegetable raw material. Tver Technical University.
Sunardi. 2008. Teknik pembibitan sambiloto untuk menghasilkan bibit yang standar.
Buletin Teknologi Pertanian Vol. 13 No. 1.
Wongkittipong R, Plat L, Damlonglerd S, Gourdon C. 2004. Solid–liquid extraction of andrographolide from plants— experimental study, kinetic reaction and model. Separation and Purification Technology 40:147-154.
Yanfang Z, Xingping L, Zongde Z, Liren C, Yongmin L. 2006. Simultaneous determination of andrographolide and dehydroandrographolide in Andrographis paniculata and Chinese medicinal preparations by microemulsion electrokinetic chromatography. Journal of Pharmaceutical and Biomedical Analysis
40:157-161.
Yulinah E, Sukrasno, Fitri MA. 2001. Aktivitas antidiabetika ekstrak etanol herba sambiloto (Andrographis paniculata
Nees (Acanthaceae)). Journal of Mass Spectrometry 6:13-20.
Yusron M, Januwati M, Pribadi ER. 2005.
14
Perancangan percobaan
dengan 3
k-1Desain
Fraksional Faktorial (9
kombinasi yang
mewakili 27 kombinasi
yang ada)
Metode Terbaik
Sampel kering daun
sambiloto
Kadar Air
Ekstraksi
Maserasi
Soxhlet
Ultrasonikasi
Analisis dengan KCKT
Rendemen Ekstrak Kental dan Kadar Andrografolida
pada Sembilan Pengamatan yang Terwakili
Analisis Regresi
Kondisi Optimum Ekstraksi
Lampiran 1 Diagram alir kerja
15
Lampiran 2 Kombinasi perlakuan pada tahap pengoptimuman teknik ekstraksi
terbaik
Maserasi
0.5 g/100 mL
1 g/100 mL
2 g/100 mL
240
menit
300 menit
360 menit
1 kali
3 kali
5 kali
1 kali
3 kali
5 kali
1 kali
3 kali
5 kali
240 menit
300 menit
360 menit
1 kali
3 kali
5 kali
1 kali
3 kali
5 kali
1 kali
3 kali
5 kali
240 menit
300 menit
360 menit
16
Lampiran 3 Kadar air serbuk herba sambiloto
Ulangan
Bobot Basah (g)
Bobot Kering (g)
Kadar Air (%)
1
3.0063
2.8064
6.65
2
3.0022
2.8048
6.58
3
3.0048
2.8098
6.49
Rerata
6.57 ± 0.1987
Contoh perhitungan:
Kadar air
Batas galat
n
t
σ
=
1987
.
0
3
08
.
0
303
.
4
±
=
×
=
Keterangan:
t
= Nilai tabel t student selang kepercayaan 95%
σ
= Simpangan baku
n
= Banyaknya ulangan
Lampiran 4 Rendemen ekstrak contoh pada pemilihan teknik ekstraksi terbaik
Metode
Ulangan
Bobot
Contoh (g)
Bobot Ekstrak
Pekat (g)
Rendemen
(%)
Rerata
Rendemen (%)
Maserasi
Soxhlet
Ultrasonik
1
2
3
1
2
3
1
2
3
1.0015
1.0012
1.0051
1.0009
1.0045
1.0008
1.0000
1.0096
1.0032
0.3101
0.3212
0.3053
0.2890
0.2956
0.2800
0.2774
0.2888
0.2904
33.14
34.34
32.51
30.90
31.50
29.95
29.69
30.62
30.98
33.33
30.78
30.43
Contoh perhitungan:
Penentuan rendemen ekstrak dengan metode maserasi ulangan 1
17
Lampiran 5 Kadar andrografolida contoh pada pemilihan teknik ekstraksi terbaik
Kadar andrografolida serbuk herba sambiloto dengan teknik maserasi
Larutan
[andrografolida]
(ppm)
Luas Puncak Bobot Contoh
(g)
Kadar (%b/b)
Standar
10
957110
-
-
Ulangan 1
2597.16
2485769
1.0015
2.78
Ulangan 2
2746.08
2628303
1.0012
2.94
Ulangan 3
2597.20
2485810
1.0051
2.77
Kadar rerata
2.83
Kadar andrografolida serbuk herba sambiloto dengan teknik soxhlet
Larutan
[andrografolida]
(ppm)
Luas Puncak Bobot Contoh
(g)
Kadar
(%b/b)
Standar
10
1417341
-
-
Ulangan 1
2136.41
3028025
1.0009
2.28
Ulangan 2
2194.91
3110940
1.0045
2.34
Ulangan 3
1925.68
2729348
1.0008
2.06
Kadar rerata
2.23
Kadar andrografolida serbuk herba sambiloto dengan teknik ultrasonikasi
Larutan
[andrografolida]
(ppm)
Luas Puncak Bobot Contoh
(g)
Kadar
(%b/b)
Standar
10
1417341
-
-
Ulangan 1
1812.91
2569507
1
1.94
Ulangan 2
1732.49
2455526
1.0096
1.84
Ulangan 3
1692.83
2399316
1.0032
1.81
Kadar rerata
1.86
Contoh perhitungan: Larutan contoh ulangan 1 teknik maserasi
18
Lampiran 6 Perhitungan teknik ekstraksi terbaik menggunakan RAL
Perlakuan (Teknik Ekstraksi)
Ulangan
P1(Maserasi) P2(Soxhlet) P3(Ultrasonikasi)
1 2.78 2.28 1.94
2 2.94 2.34 1.84
3 2.77 2.06 1.81
Total Keseluruhan
Total Perlakuan
(Yi.) 8.49 6.68 5.59 20.76
i
Y
2.83 2.23 1.86Model Linear:
Y
ij= +
τ
i+
ε
iji
= 1, 2, 3, ...,
t
dan
j
= 1, 2, 3, ...,
r
Y
ij= Respons pada perlakuan ke-
i
dan ulangan ke-
j
= Rataan umum
τ
i= Pengaruh perlakuan ke-
i
ε
ij= Pengaruh acak pada perlakuan ke-
i
ulangan ke-
j
Hipotesis:
H
0:
τ
1=
τ
2= ... =
τ
t= 0
H
1: paling sedikit ada satu
i
dimana
τ
i≠ 0
Sidik ragam RAL
Sumber
Keragaman
Derajat
Bebas (db)
Jumlah
Kuadrat (JK)
Kuadrat
Tengah (KT)
F-Hitung
Perlakuan
Galat
Total
2
6
8
1.4305
0.0709
1.5014
0.7153
0.0118
60.6186
F hitung = 60.6186
F
0.05 (2,6)= 5.143
F hitung = 60.6186 > F
0.05 (2,6)19
Lanjutan Lampiran 6
Uji Beda Nyata Jujur (BNJ) atau disebut juga Uji Tukey
BNJ = q
α,p,dbgx
S
y= q
0.05,3,6x 0.0627
= 4.34 x 0.0627
= 0.2721
Urutan rerata kadar dari ketiga metode
Y
ultrasonik
soxhlet
maserasi
1.86
2.23
2.83
BNJ
60
.
0
Y
Y
BNJ
97
.
0
Y
Y
BNJ
37
.
0
Y
Y
A B
A C
B C
>
=
−
>
=
−
>
=
−
Disimpulkan bahwa ketiga teknik ekstraksi berbeda nyata pada taraf nyata 5
℅
.
KK
4
.
71
3067
.
2
0118
.
0
=
=
=
Y
KTG
℅
3
0118
.
0
=
0627
.
0
=
20
Lampiran 7 Kromatogram pada pemilihan teknik ekstraksi terbaik
Kromatogram larutan standar 10 ppm untuk teknik maserasi.
Kromatogram contoh pada teknik maserasi.
Lampiran 8 Penentuan rendemen pada pengoptimuman teknik ekstraksi terbaik
Observasi
Waktu
(menit)
Frekuensi
Ekstraksi
Ulangan
Bobot
Sampel
(g)
Bobot
Ekstrak
Pekat (g)
Rendemen
(%)
Rerata
Rendemen
(%)
1
240
1
1
0.5001
0.1914
40.96
2
0.5001
0.1869
40.00
40.48
2
300
5
1
0.5001
0.2221
47.53
2
0.5003
0.2094
44.80
46.17
3
360
3
1
0.5003
0.2196
46.98
2
0.5006
0.2172
46.44
46.71
4
240
5
1
1.0005
0.2990
31.99
2
1.0013
0.3042
32.52
32.26
5
300
3
1
1.0007
0.3131
33.49
2
1.0003
0.3419
36.58
35.04
6
360
1
1
1.0082
0.2360
25.05
2
1.0024
0.2527
26.98
26.02
7
240
3
1
2.0007
0.5300
28.35
2
2.0001
0.5977
31.98
30.17
8
300
1
1
2.0008
0.4068
21.76
2
2.0027
0.3518
18.80
20.28
9
360
5
1
2.0002
0.5839
31.24
21
Lampiran 9 Pengukuran standar andrografolida
Konsentrasi Standar
(ppm)
Luas Puncak
10
100
1024
1375514
7152829
67453825
Persamaan garis:
Y
= 680031.0787 + 65204.65147
X
R
2= 99.99℅
Lampiran 10 Penentuan kadar andrografolida pada teknik ekstraksi terbaik
Waktu
(menit)
Frekuensi
Ekstraksi
Ulangan
Bobot
Sampel (g)
Luas
Puncak
Konsentrasi
AP (ppm)
Kadar
AP (%)
Rerata
(%)
240
1
1
0.5001
1352525
1031.36
2.21
2
0.5001
1444123
1171.84
2.51
2.36
300
5
1
0.5001
1405330
1112.34
2.38
2
0.5003
1325598
990.06
2.12
2.25
360
3
1
0.5003
1600074
1411.01
3.02
2
0.5006
1568631
1362.79
2.91
2.97
240
5
1
1.0005
2178859
2298.65
2.46
2
1.0013
2283955
2459.83
2.63
2.55
300
3
1
1.0007
2423965
2674.55
2.86
2
1.0003
2479892
2760.33
2.95
2.91
360
1
1
1.0082
2258437
2420.70
2.57
2
1.0024
2350639
2562.10
2.74
2.66
240
3
1
2.0007
4670755
6120.31
3.27
2
2.0001
4640284
6073.57
3.25
3.26
300
1
1
2.0008
3855856
4870.55
2.61
2
2.0027
3707217
4642.59
2.48
2.55
360
5
1
2.0002
4926274
6512.18
3.48
2
2.0007
4989255
6608.77
3.54
3.51
Lampiran 11 Korelasi antara rendemen dan kadar pada pengoptimuman teknik
ekstraksi terbaik
Correlations: rendemen, kadar
Pearson correlation of Kadar AP (℅) and Rendemen (℅) = -0.206 P-Value = 0.595