PERANCANGAN PROSES DAN PENINGKATAN SKALA
EKSTRAKSI KITIN DARI KULIT UDANG
SECARA BIOLOGIS
JUNIANTO
.
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
SURAT PERNYATAAN
Dengan ini saya menyatakan bahwa disertasi yang berjudul
PERANCANGAN PROSES DAN PENINGKATAN SKALA
EKSTRAKSI KITIN DARI KULIT UDANG
SECARA BIOLOGIS
Adalah benar hasil karya saya sendiri dengan arahan komisi pembimbing dan belum pernah dipublikasikan. Disertasi ini belum pernah diajukan untuk memperoleh gelar pada program sejenis di perguruan tinggi lain. Semua sumber data dan informasi yang digunakan telah dinyatakan secara jelas dan dapat diperiksa kebenarannya
Bogor, September 2008
ABSTRACT
JUNIANTO. F361040011. Process Design and Scale Up of The Biological Extraction of Chitin from Shrimp Shells. Supervised by DJUMALI MANGUNWIDJADJA, SUPRIHATIN, MULYORINI RAHAYUNINGSIH, and BUDIASIH WAHYUNTARI.
Biologically chitin extraction was conducted by microbial process for deproteinization and demineralization. Lactobacillus acidophilus FNCC 116 was used for demineralization and Bacillus licheniformis F11.1 for deproteinization. The aim of the experiment was to design the biological extraction process of chitin from shrimp shells and to obtain the best scaling up criteria for the biological chitin extraction. The result of design of the biologically chitin extraction process from shrimp shells was as follow : The Shrimp shells was ground into pieces of 5 – 10 mm and followed by demineralization that was conducted by subsequent batch fermentation. The fermentation was done for 36 hours and 100 % medium was substituted at 24th hour. The best fermentation condition was 50 rpm agitation, at room temperature (30 ± 1oC), 10 % (v/v) inoculums (1 x 109 Cfu/ml cell density) and medium fermentation consisted of 0.5 g/L yeast extract and 60 g/L glucose. The demineralized shrimp shells was washed by running water. The final step was deproteinization of demineralized shrimp shells by batch fermentation and it was conducted for 96 hours. The best fermentation condition was 275 rpm agitation, 2.3 vvm aeration, pH adjusted in range of 7.8 – 8.2 and temperature of 55oC. The medium fermentation consisted of 5 g/L yeast extract; 5 g/L KH2PO4; 1 g/L CaCl2; 5 g/L NaCl and 0.5 g/L
MgSO4. By this design of the biologically chitin extraction process, 95.69 % ash
and 92.42 % protein could be removed. The ash, protein, and chitin content of chitin product was 0.84 % (db), 1.46 % (db), and 97.26 % (db) respetively whereas its viscosity was 15000 cps. The best criteria for scaling up for the biologically chitin extraction was the constant power given per unit volume for the demineralization as well as the deproteinization process.
RINGKASAN
JUNIANTO. F361040011. Perancangan Proses dan Peningkatan Skala Ekstraksi Kitin dari Kulit Udang Secara Biologis. Dibimbing oleh DJUMALI MANGUNWIDJADJA, SUPRIHATIN, MULYORINI RAHAYUNINGSIH, dan BUDIASIH WAHYUNTARI.
Ekstraksi kitin dari kulit udang dapat dilakukan secara kimiawi maupun biologis. Ekstraksi kitin secara kimiawi dapat menyebabkan hidrolisis polimer sehingga kitin yang dihasilkan viskositasnya rendah. Selain itu, ekstraksi secara kimiawi menghasilkan limbah yang memberi beban pencemaran lingkungan cukup besar. Ekstraksi kitin secara biologis tidak menyebabkan hidrolisis polimer sehingga viskositas kitinnya tinggi. Ekstraksi kitin secara biologis ramah lingkungan dan juga menghasilkan produk samping berupa protein dan kalsium yang mempunyai nilai tambah.
Tujuan penelitian ini adalah mendapatkan rancangan proses biologi untuk ekstraksi kitin dari kulit udang vannamei (Penaeus vannamei) menggunakan bakteri B. licheniformis F11.1 dan L. acidophillus FNCC 116. Selain itu bertujuan untuk mendapatkan kriteria terbaik dalam peningkatan skala ekstraksi kitin.
Tahapan ekstraksi kitin dari kulit udang dilakukan melalui demineralisasi dan deproteinasi. Demineralisasi dimaksudkan untuk menghilangkan kandungan mineral dalam bentuk abu sedangkan deproteinasi bertujuan untuk menghilangkan protein dari kulit udang. Bakteri Lactobacillus acidophillus FNCC 116 dan Bacillus licheniformis F11.1 digunakan untuk ekstraksi kitin secara biologis dari kulit udang. Kedua bakteri ini merupakan spesies baru yang digunakan untuk ekstraksi kitin. Setiap jenis bakteri memerlukan kondisi pertumbuhan yang spesifik, sehingga diperlukan perancangan proses biologis untuk ekstraksi kitin agar diperoleh tingkat penghilangan mineral dan protein maksimal dari kulit udang. Selain itu, pemilihan kriteria yang sesuai untuk peningkatan skala proses sangat diperlukan dalam rangka mendapatkan hasil yang tetap optimal.
pada proses demineralisasi dan B. licheniformis F11.1 pada deproteinasi adalah sebagai berikut: Pengecilan ukuran kulit udang dilakukan pada 0,5 – 1 cm. Selanjutnya didemineralisasi melalui proses fermentasi batch berturut-turut (subsequent batch), dengan penggantian 100 % medium yang dilakukan pada jam ke 24 jam. Fermentasi dilakukan pada suhu 30 ± 1oC selama 36 jam. Selama proses fermentasi dilakukan agitasi pada laju 50 rpm. Medium fermentasi terdiri atas 0,5 g/L ekstrak khamir dan 60 g/L glukosa. Jumlah inokulum bakteri sebanyak 10 % (v/v) dengan tingkat kepadatan 1 x 109 Cfu/ml. Kulit udang hasil demineralisasi dicuci bersih kemudian dideproteinasi. Deproteinasi dilakukan melalui proses fermentasi sistem batch selama 96 jam. Suhu dan pH fermentasi dipertahankan pada 55 oC dan kisaran 7,8 – 8,2, sedangkan aerasi dan agitasi masing-masing ditetapkan pada 2,3 vvm dan 275 rpm. Komposisi medium fermentasi terdiri dari ekstrak khamir 5 g/L; KH2PO4 5 g/L; CaCl2 1 g/L; NaCl 5
g/L dan MgSO4 0,5 g/L. pH awal medium diatur pada 7,3. Jumlah inokulum
bakteri sebanyak 20 % (v/v) dengan tingkat kepadatan 1 x 109 Cfu/ml.
@ Hak Cipta milik IPB, tahun 2008 Hak Cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan
karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu
masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya
PERANCANGAN PROSES DAN PENINGKATAN SKALA
EKSTRAKSI KITIN DARI KULIT UDANG
SECARA BIOLOGIS
JUNIANTO
Disertasi
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Doktor
Pada Program Studi Teknologi Industri Pertanian
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Disertasi : Perancangan Proses dan Peningkatan Skala Ekstraksi Kitin dari Kulit Udang Secara Biologis
Nama Mahasiswa : Junianto
NRP : F361040011
Disetujui Komisi Pembimbing
Prof. Dr. Ir. Djumali Mangunwidjaja, DEA Dr.-Ing.Ir. Suprihatin Ketua Anggota
Dr. Ir. Mulyorini Rahayuningsih, MS. Dr. Ir. Budiasih Wahyuntari, MSc. Anggota Anggota
Diketahui,
Ketua Program Studi Dekan Sekolah Pascasarjana Teknologi Industri Pertanian
Dr. Ir. Irawadi Jamaran Prof. Dr. Ir. Khairil Anwar Notodiputro, MS.
PRAKATA
Segala puji hanya bagi Allah SWT, Dialah pemilik segala ilmu dan atas kuasa-Nya disertasi dengan judul “Perancangan Proses dan Peningkatan Skala Ekstraksi Kitin Secara Biologis dari Kulit Udang” dapat diselesaikan. Sholawat dan Salam, semoga Alloh SWT limpahkan kepada Rasulallah Muhammad SAW dan ummatnya; Amien.
Ucapan terima kasih, rasa hormat dan penghargaan yang tinggi pada kesempatan yang tepat ini, penulis sampaikan kepada :
1. Prof. Dr. Ir. Djumali Mangunwidjadja, DEA selaku ketua komisi
pembimbing; Dr.-Ing.Ir. Suprihatin; Dr. Ir. Mulyorini Rahayuningsih, MS; dan Dr. Ir. Budiasih Wahyuntari, MSc masing-masing sebagai anggota komisi pembimbing yang telah memberikan bimbingan, arahan, saran, keluangan waktu dan dorongan moral yang tulus sehingga penulisan disertasi ini dapat diselesaikan.
2. Dr. Ir. Sukardi, MM di Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian IPB yang banyak memberikan masukan pada saat bertindak sebagai dewan penguji di ujian tertutup. Dr. Siswa Setyahadi, Kepala Bidang Biokatalis-Teknologi BioIndustri BPPT dan Prof (riset) Dr.Ir. Rosmawati Peranginangin, MS., Peneliti Utama Balai Besar Riset Pengolahan Produk dan Bioteknologi Perikanan Departemen Kelautan dan Perikanan atas masukan yang disampaikan pada saat menjadi penguji ujian terbuka
3. Dr. Ir. Koenandar, M.Eng selaku Direktur Pusat Teknologi BioIndustri; Dr. Ir. Siswa Setyahadi selaku Kepala Bidang Biokatalis; dan Ir. Trismilah, MS selaku Kepala Laboratorium BioIndustri – BPPT; atas segala biaya dan penggunaan fasilitas laboratorium yang diberikannya sehingga penelitian ini dapat diselesaikan.
4. Dekan Sekolah Pascasarjana IPB Prof. Dr. Ir. Khairil Anwar Notodipuro, MS;
staf pengajar yang telah memberi ilmu dan bimbingan kepada penulis selama menimba ilmu pengetahuan di IPB.
5. Rektor Universitas Padjadjaran Prof. Dr. Ir. Ganjar Kurnia, DEA; Dekan Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran Prof. Dr. Ir. H. Bachrulhayat Koswara, MS; Ketua Program Studi Perikanan Dr. Ir. H. Eddy Afrianto, MS dan Ketua Laboratorium Teknologi Industri Hasil Perikanan Ir. H. Evi Liviawaty, MP atas ijin dan kesempatan yang diberikan kepada penulis untuk melanjutkan jenjang pendidikan S3.
6. Tim Manajemen BPPS-Dikti atas bantuan dana pendidikan program doktor yang diberikan kepada penulis.
7. Staf peneliti laboratorium Bioindustri – BPPT antara lain Dr. Dadang, Deden
R Waltam, SSi; Drs. Djamil, MS; Ir. Djoni Prasetyo, MS; dan kelompok penelitian kitin antara lain Herwanto, SP; Siti Rahma , SP; M. Fajar, SPi; Iman Firmansyah, SPi, Rita Rahmawati, ST; Anugrah Luki Haryanto, SSi; Mufti., atas segala bantuan kekompakan dan kerjasamanya dalam penelitian ini.
8. Ayanda H. Ali Syukur, Ibunda H. Siti Rokayyah, dan Ibunda Mertua Siti Haniah, atas segala doa, kasih sayang dan pengorbanannya yang tiada tara. 9. Istriku Lilis Kusmayati, SPt dan anak-anakku Amir Mujahiduddien, Hadiati
Rabbani, Sayyid Irsyadul Ibad, Roja Fathlur Rahman, Hasyidah Hanifati Dieni, Najim Kharil Abidin dan Mufakir Falih Bayyinal Haq, atas segala doa, pengorbanan, pengertian, dan dorongan semangat. Begitu pula ucapan terima kasih kepada adik-adikku Drs. Junaidi dan istri, Junairi, SPd dan Istri, Junaiman dan Istri, Junarsih dan Suami, Junarni, Dipl.SPi dan Suami serta Jumadi, SPd; atas segala doa dan dorongan semangatnya.
10.Rekan-rekan dan semua pihak yang telah membantu penulis selama mengikuti
Semoga Allah SWT memberikan pahala kepada mereka semua atas segala yang diberikannya. Akhirnya, semoga disertasi ini dapat memberikan sumbangan pemikiran dan pengembangan ilmu pengetahuan yang bermanfaat.
Bogor, September 2008
RIWAYAT HIDUP
Penulis lahir di Madura Kabupaten Sampang, Propinsi Jawa Timur, tanggal 17 Agustus 1967. Anak pertama dari 8 bersaudara dari pasangan Bapak H. Ali Syukur dan Ibu H. Siti Rokayyah. Setelah lulus Sekolah Menengah Atas Negeri I di Sampang tahun 1986, penulis diterima di Program Studi Teknologi Hasil Pertanian, Fakultas Pertanian Universitas Padjadjaran melalui program Penelusuran Minat dan Kemampuan (PMDK). Selama studi di Fakultas Pertanian, penulis mendapatkan tunjangan ikatan dinas selama 1 tahun dari Dikti. Penulis menyelesaikan program sarjana S1 pada bulan Januari 1991 dan setelah itu bekerja di PT. Ultra Jaya Milk Industri selama 1 tahun sebagai Management Traineer.
Pada bulan April 1992, penulis diangkat sebagai calon pengawai negeri sipil dan ditempatkan sebagai staf pengajar Jurusan Perikanan Fakultas Pertanian Universitas Padjadjaran yang sekarang menjadi Fakultas Perikanan dan Ilmu Kelautan. Setahun kemudian yaitu 1993 penulis diangkat sebagai pegawai negeri sipil sampai sekarang. Pada tahun 1994, penulis melanjutkan studi ke program magister Teknologi Pascapanen Universitas Padjadjaran atas dana BPPS dan selesai tahun 1997. Setelah itu, pada tahun 2004 penulis melajutkan studi ke program doktor Teknologi Industri Pertanian IPB juga dengan dana BPPS. Selama menjadi staf pengajar, penulis disamping mengajar juga telah melakukan penelitian dan pengabdian kepada masyarakat, menulis di media cetak dan penerbitan buku. Akhirnya penulis sekarang menjadi lektor kepala dengan pangkat IVB.
Penulis menikah dengan Lilis Kusmayati, SPt tanggal 30 Juni 1993 di Garut. Alhamdulillah, penulis sampai saat ini masih dikarunia 7 orang anak yaitu Amir Mujahiduddien, Hadiati Rabbani, Sayyid Irsyadul Ibad, Roja Fathlur Rahman, Hasyidah Hanifati Dieni, Najim Kharil Abidin, dan Mufakir Falih Bayyinal Haq.
Penguji Sidang Tertutup: Dr. Ir. Sukardi, MM.
Dosen Fakultas Teknologi Pertanian IPB
Penguji Sidang Terbuka: 1. Dr.Ir. Siswa Setyahadi
Kepala Bidang Biokatalis Teknologi Bioindustri BPPT 2. Prof (R) Dr.Ir. Rosmawati Peranginangin, MS.
DAFTAR ISI
1.3 Ruang Lingkup Penelitian ...
1.4 Manfaat Penelitian ...
2.6 Optimasi dengan Response Surface Methodology ...
2.7 Perancangan Proses ...
III
IV
V
METODE PENELITIAN ... 3.1 Waktu dan Tempat Penelitian ...
3.2 Bahan dan Alat Penelitian ...
3.3 Metode Penelitian ...
HASIL DAN PEMBAHASAN ... 4.1 Perancangan Proses Biologis Ekstraksi Kitin dari Kulit Udang ....
4.1.1 Penentuan Kecepatan Agitasi pada Proses Demineralisasi Kulit Udang ...
4.1.2 Penentuan Kecepatan Agitasi dan Tingkat Aerasi pada Proses Deproteinasi Kulit udang ...
4.1.3 Penentuan Jalur Tahapan Ekstraksi Kitin dari Kulit Udang Secara Biologi ...
4.1.4 Penentuan Sistem Fermentasi pada Proses Demineralisasi Kulit
Udang ...
4.1.5 Optimasi Kecepatan Agitasi dan Tingkat Aerasi pada Proses Deproteinasi Kulit Udang Hasil Demineralisasi ...
4.1.6 Penentuan Sistem Fermentasi Proses Deproteinasi Kulit Udang
Hasil Demineralisasi ...
4.1.7 Hasil Rancangan Proses Ekstraksi Kitin dari Kulit Udang Secara Biologis ...
4.2 Penentuan Kriteria untuk Peningkatan Skala Ekstraksi Kitin Secara Biologi dari Kulit Udang ...
DAFTAR TABEL
Produksi dan ekspor udang Indonesia 2003 – 2007 ...
Mutu kitin niaga dari berbagai produk ...
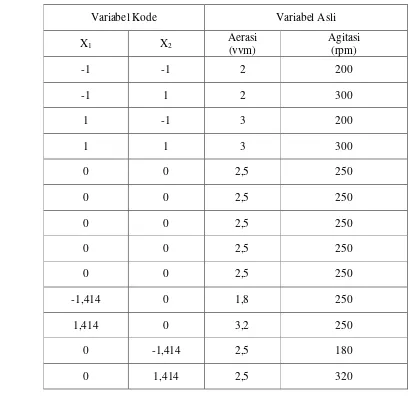
Kombinasi perlakuan dengan rancangan komposit pusat ...
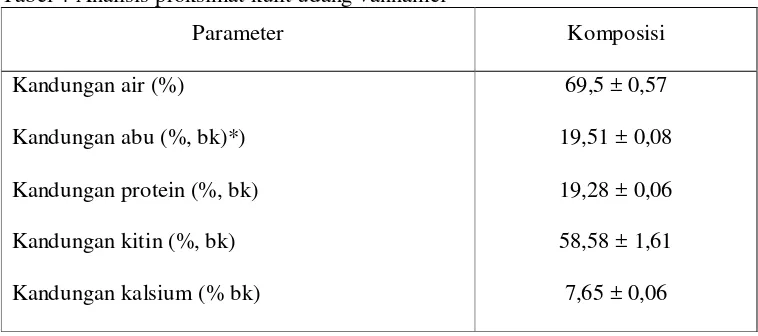
Analisis proksimat kulit udang vannamei ...
Tingkat hidrolisis protein kulit udang hasil demineralisasi pada berbagai kondisi proses untuk pendugaan ordo pertama ...
Tingkat hidrolisis protein kulit udang hasil demineralisasi pada berbagai kondisi proses untuk pendugaan ordo kedua ...
Kriteria Mutu Kitin ...
Karakteristik bioreaktor ...
Kondisi proses pada bioreaktor 13 liter dari berbagai kriteria penigkatan skala ...
Parameter geometrik bioreaktor 2 liter yang digunakan pada proses ekstraksi kitin dari kulit udang ...
Karakteristik rancang bangun dan kondisi proses pada berbagai skala bioreaktor untuk ekstraksi kitin ...
DAFTAR GAMBAR
Struktur kimia kitin, kitosan dan selulosa ...
Penerapan kitin dan turunannya di industri ...
Reaksi kimia pemutusan ikatan peptida dengan katalis enzim ...
Skematis deproteinasi kulit udang secara biologi ...
Skema proses biologi demineralisasi kulit udang dalam fermentasi asam laktat ...
Persamaan reaksi antara asam laktat dan kalsium karbonat ...
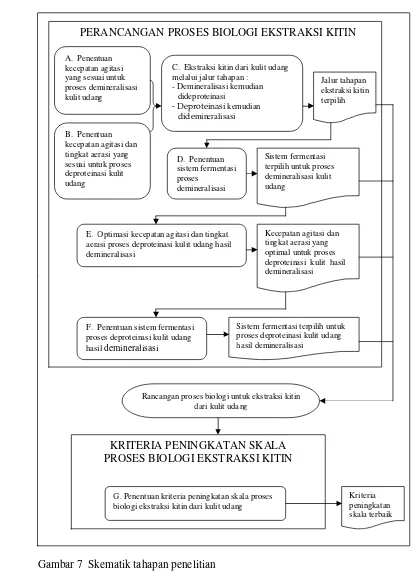
Skematik tahapan penelitian ...
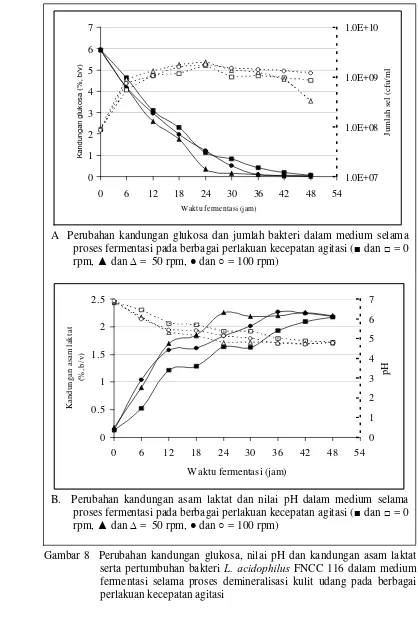
Perubahan kandungan glukosa, nilai pH dan kandungan asam laktat
serta pertumbuhan bakteri L. acidophilus FNCC 116 dalam
medium fermentasi selama proses demineralisasi kulit udang pada berbagai perlakuan kecepatan agitasi...
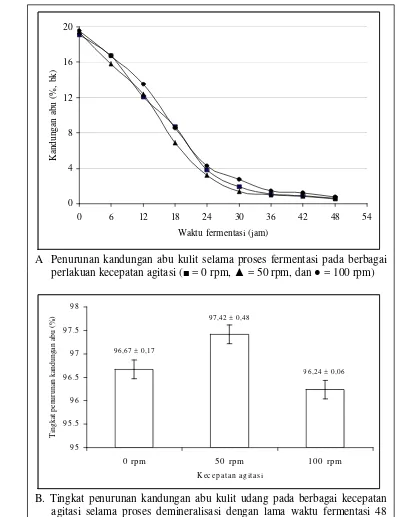
Kandungan abu kulit udang dan tingkat penurunannya selama proses demineralisasi pada berbagai perlakuan kecepatan agitasi ...
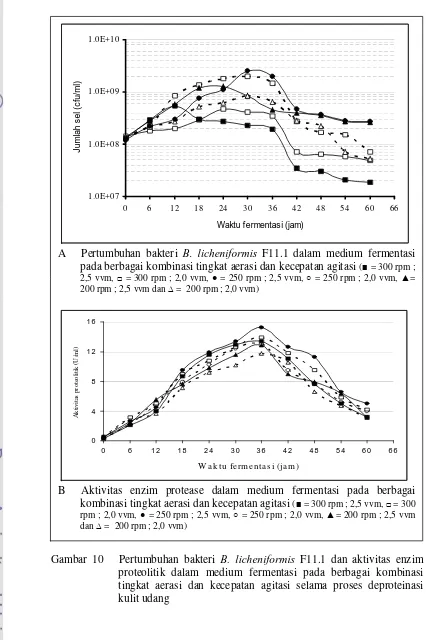
Pertumbuhan bakteri B. licheniformis F11.1 dan aktivitas enzim proteolitik dalam medium fermentasi pada berbagai kombinasi tingkat aerasi dan kecepatan agitasi selama proses deproteinasi kulit udang ...
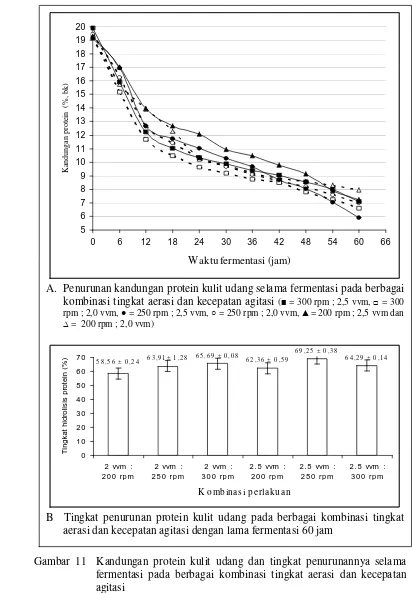
Kandungan protein kulit udang dan tingkat penurunannya selama fermentasi pada berbagai kombinasi tingkat aerasi dan kecepatan agitasi ...
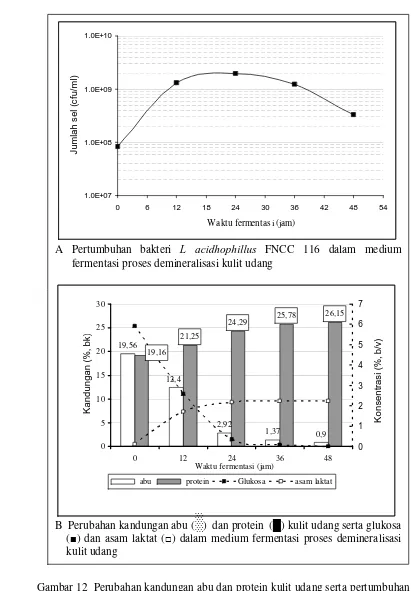
Perubahan kandungan abu dan protein kulit udang serta pertumbuhan bakteri L acidhophillus FNCC 116, glukosa dan asam laktat dalam medium fermentasi proses demineralisasi kulit udang .
Pertumbuhan bakteri B licheniformis F11.1, aktivitas enzim protease dalam medium fermentasi dan kandungan abu serta protein kulit udang hasil demineralisasi selama proses deproteinasi
14
Pertumbuhan bakteri B licheniformis F11.1, aktivitas enzim protease dalam medium fermentasi dan kandungan abu serta protein kulit udang selama proses deproteinasi ...
Perubahan kandungan abu dan protein kulit udang serta pertumbuhan bakteri L acidhophillus FNCC 116, glukosa dan asam laktat dalam medium fermentasi proses demineralisasi kulit udang hasil deproteinasi ...
Karakteristik kulit udang dan hasil ekstraksi kitin melalui dua jalur proses yang berbeda ...
Pertumbuhan bakteri L. acidophillus FNCC 116 dan perubahan kandungan glukosa dalam medium berbagai sistem fermentasi proses demineralisasi kulit udang ...
Perubahan kandungan asam laktat dan pH dalam medium berbagai sistem fermentasi proses demineralisasi kulit udang ...
Penurunan kandungan abu kulit udang selama proses fermentasi dari berbagai sistem fermentasi ...
Optimasi dan kontur respon tingkat hidrolisis protein terhadap tingkat aerasi dan kecepatan agitasi ...
Tingkat hidrolisis dan kandungan protein kulit udang hasil demineralisasi pada proses deproteinasi kondisi optimum (2,3 vvm : 275 rpm) ...
Pertumbuhan bakteri B.licheniformis F11.1 dan aktivitas enzim protease dalam berbagai medium sistem fermentasi proses deproteinasi kulit udang hasil demineralisasi ...
Pola penurunan kandungan protein kulit udang hasil demineralisasi pada proses deproteinasi dalam berbagai sistem fermentasi ...
Diagram blok ekstraksi kitin dari kulit udang secara biologis ...
Diagram alir proses ekstraksi kitin dari kulit udang secara biologis .
Pertumbuhan bakteri L acidophillus FNCC 116 dan perubahan kandungan glukosa, pH serta kandungan asam laktat dalam medium fermentasi pada bioreaktor 2 lt dan 13 lt ...
28
29
Pertumbuhan bakteri B.licheniformis F11.1 dan aktivitas enzim dalam medium fermentasi pada berbagai kriteria peningkatan skala
Pola penurunan kandungan protein selama proses deproteinasi kulit udang hasil demineralisasi dalam medium fermentasi pada berbagai kriteria peningkatan skala ...
121
DAFTAR LAMPIRAN
Pengukuran kandungan abu (AOAC 1984) ...
Pengukuran aktivitas enzim protease (azokasein) ………
Pengukuran pH (pH meter) ...
Pengukuran total asam dengan HPLC ...
Pengukuran kandungan glukosa (metode DNS, AOAC 1984) ...
Pengukuran viskositas ...
Pengukuran kandungan kitin melalui nitrogen total ...
Teknis Penentuan Nilai kLa (Metode dinamik, Scragg 1991) ...
Metode penghitungan jumlah bakteri (TPC) ...
Kurva standar jumlah bakteri Bacillus licheniformis F11.1 versus optical density (OD) ...
Kurva standar jumlah bakteri Lactobacillus acidhophilus FNCC 116 versus optical density (OD) ...
Hasil penghitungan jumlah bakteri dalam medium fermentasi proses demineralisasi kulit udang pada berbagai perlakuan kecepatan agitasi (Cfu/ml) ...
Hasil pengukuran pH dalam medium fermentasi proses demineralisasi kulit udang pada berbagai perlakuan kecepatan agitasi ...
Hasil pengukuran kandungan glukosa dalam medium fermentasi proses demineralisasi kulit udang dalam berbagai perlakuan kecepatan agitasi (%; b/v) ...
17 penurunannya selama proses demineralisasi pada berbagai perlakuan kecepatan agitasi serta analisis statistik ...
Hasil penghitungan jumlah bakteri dalam medium fermentasi proses deproteinasi kulit udang dalam berbagai kombinasi perlakuan kecepatan agitasi dan tingkat aerasi (Cfu/ml) ...
Hasil pengukuran aktivitas enzim protease dalam medium fermentasi proses deproteinasi kulit udang pada berbagai kombinasi perlakuan kecepatan agitasi dan tingkat aerasi (Unit/ml) ...
Hasil pengukuran kandungan protein dan penghitungan tingkat penurunannya pada proses deproteinasi kulit udang dalam berbagai kombinasi perlakuan kecepatan agitasi dan tingkat aerasi serta analisis statistik ...
Hasil pengukuran kandungan glukosa, asam laktat, abu, protein, dan jumlah bakteri pada proses demineralisasi kulit udang ...
Hasil pengukuran kandungan abu, protein, aktivitas enzim dan jumlah bakteri pada proses deproteinasi kulit udang hasil demineralisasi ...
Hasil pengukuran kandungan abu, protein, aktivitas enzim dan jumlah bakteri pada proses deproteinasi kulit udang ...
Hasil pengukuran kandungan abu, protein, glukosa, asam laktat dan jumlah bakteri pada proses demineralisasi kulit udang hasil deproteinasi ...
Hasil penghitungan jumlah bakteri dalam medium fermentasi pada proses demineralisasi kulit udang pada berbagai perlakuan sistem fermentasi (Cfu/ml) ...
Hasil pengukuran kandungan asam laktat dan pH dalam medium fermentasi pada proses demineralisasi kulit udang pada berbagai sistem fermentasi ...
Hasil pengukuran glukosa dan kandungan abu pada proses demineralisasi kulit udang pada berbagai sistem fermentasi ...
Analisis Statistik terhadap tingkat penurunan kandungan abu pada perancangan fermentasi (B) Fermentasi Subsequent Batch bertahap dengan pengantian media dan inokulum baru pada jam ke 24 ...
29
Matriks orde pertama respon tingkat hidrolisis protein kulit udang hasil demineralisasi terhadap tingkat aerasi dan kecepatan agitasi ...
Hasil analisis ragam tingkat hidrolisis protein kulit udang hasil demineralisasi terhadap tingkat aerasi dan kecepatan agitasi pada percobaan titik faktorial dan pusat ...
Analisis varian ordo pertama proses optimasi pengaruh tingkat aerasi dan kecepatan agitasi terhadap tingkat hidrolisis protein kulit udang hasil demineralisasi ...
Hasil analisis nilai estimasi, standar deviasi dan nilai t respon tingkat hidrolisis protein kulit udang hasil demineralisasi terhadap tingkat aerasi dan kecepatan agitasi ...
Hasil uji penyimpangan model pengaruh tingkat aerasi dan kecepatan agitasi terhadap hidrolisis protein kulit udang hasil demineralisasi ...
Hasil percobaan tingkat hidrolisis protein kulit udang hasil demineralisasi terhadap tingkat aerasi dan kecepatan agitasi ...
Hasil analisis ragam tingkat hidrolisis protein kulit udang hasil demineralisasi terhadap tingkat aerasi dan kecepatan agitasi pada titik faktorial, pusat dan bintang ...
Hasil analisis nilai estimasi, standar deviasi dan nilai t respon tingkat hidrolisis protein kulit udang hasil demineralisasi terhadap tingkat aerasi dan kecepatan agitasi agitasi pada titik faktorial, pusat dan bintang ...
Hasil uji penyimpangan model pengaruh tingkat aerasi dan kecepatan agitasi terhadap hidrolisis protein kulit udang hasil demineralisasi ...
Analisis kanonik pengaruh tingkat aerasi dan kecepatan agitasi terhadap tingkat hidrolisis protein kulit udang hasil demineralisasi ..
Hasil pengukuran reologi cairan kultivasi pada konsisi optimal (2,3 vvm ; 275 rpm) proses deproteinasi kulit udang hasil demineralisasi dalam bioreaktor 2 liter ...
Penentuan nilai kLa pada medium fermentasi kondisi optimal (2,3
vvm : 275 rpm) proses deproteinasi kulit udang hasil demineralisasi dalam bioreaktor 2 liter. ...
41
Hasil penghitungan jumlah bakteri dalam medium fermentasi proses deproteinasi kulit udang hasil demineralisasi pada berbagai perlakuan sistem fermentasi (Cfu/ml) ...
Hasil pengukuran aktivitas enzim dalam medium fermentasi proses deproteinasi kulit udang hasil demineralisasi pada berbagai perlakuan sistem fermentasi (U/ml) ...
Hasil pengukuran kandungan protein kulit udang hasil
demineralisasi selama proses deproteinasi pada berbagai perlakuan sistem fermentasi (%, bk) ...
Analisis Statistik terhadap tingkat penurunan kandungan protein kulit udang hasil demineralisasi pada berbagai perlakuan sistem fermentasi proses deproteinasi ...
Data geometris bioreaktor 2 dan 13 liter ...
Kriteria kesaamaan fisik bioreaktor 2 dan 13 liter ...
Penghitungan kecepatan agitasi pada bioreaktor 13 liter berdasarkan patokan peningkatan skala tenaga per unit volume tetap dari biorektor 2 liter ...
Hasil penghitungan jumlah bakteri dalam medium fermentasi proses demineralisasi kulit udang segar pada biorektor ukuran 13 liter (Cfu/ml)...
Hasil pengukuran kandungan asam laktat, glukosa, dan nilai pH dalam medium fermentasi serta kandungan abu kulit udang pada proses demineralisasi dalam biorektor ukuran 13 liter ...
Penghitungan nilai kecepatan agitasi dan aerasi pada biorektor 13 liter berdasarkan optimasi pada biorektor 2 liter pada berbagai kriteria peningkatan skala ...
Grafik hubungan antara bilangan Reynolds dengan bilangan tenaga (Wang et al. 1978) ...
Grafik hubungan antara perbandingan tenaga pengadukan pada sistem beraerasi dan tanpa earasi (Pg/P) dengan bilangan aerasi (Na) pada berbagai tipe impeler (Aiba et al. 1973) ...
Hasil penghitungan jumlah bakteri dalam medium fermentasi proses deproteinasi kulit udang hasil demineralisasi pada berbagai perlakuan kriteria peningkatan skala (Cfu/ml) ...
54
55
56
57
58
Hasil pengukuran aktivitas enzim dalam medium fermentasi proses deproteinasi kulit udang hasil demineralisasi dalam berbagai perlakuan kriteria peningkatan skala (Unit/ml) ...
Hasil pengukuran kandungan protein kulit udang pada proses deproteinasi dalam berbagai perlakuan kriteria peningkatan skala (%, bk) ...
Analisis statistik terhadap tingkat penurunan kandungan protein kulit udang hasil demineralisasi pada berbagai kriteria peningkatan skala ...
Penghitungan rancang bangun dan kondisi proses ekstraksi kitin secara biologi dari kulit udang dalam berbagai kapasitas biorektor ..
Hasil pengukuran analisis proksimat kulit udang dan kitin hasil ekstraksi ...
205
206
207
208
SINGKATAN
AOAC = Association of Official Analytical Chimestry
b/b = Berat per Berat
bk = Berat kering
BPPT = Badan Pengkajian dan Penerapan Teknologi
BSA = Bovine Serum Albumin
b/v = Berat per volume
Cfu = Coloni form unit
DCL = Dichloroisocoumarin
DD = Derajat Deasetilasi
DFP = Diisopropil Fluorophosfat
Di = diameter pengaduk
Dml = demineralisasi
DNS = Dinetrosolisilat
DOT = Dissolved oxygen tension
Dpr = Deproteinasi
Dpt = Diameter putaran (impeler)
Dt = Diameter bioreaktor
EDTA = Ethylene diamine tetraacetic acid
F/V = Tingkat aerasi
g/L = Gram per liter
HL = Tinggi cairan fermentasi
Hb = Tinggi baji pertama dari dasar tangki
HPLC = High performance liquid chromatography
Ht = Tinggi bioreaktor
Kag = kecepatan agitasi
kLa = koefisien transfer oksigen
L = Liter
LB = Luria Broth
LTB = Laboratorium Teknologi Bioindustri
MRS = Man Rogosa Sharpe
N = kecepatan agitasi
Ni = jumlah pengaduk
OD = Optical density
PMSF = Phenymethylsulfonylfluoride
Pg/v = tenaga per unit volume
PUSPIPTEK = Pusat Penelitian Ilmu Pengetahuan dan Teknologi
Rpm = Round per menit (putaran per menit)
TPC = Total plate count
U/ml = Unit per ml
V = Tingkat kecepatan ujung impeller
Vk = Volume kerja bioreaktor
Vvm = Volume udara per volume cairan per menit
I PENDAHULUAN
1.1 Latar Belakang
Udang merupakan komoditi perikanan Indonesia terbesar yang dieskpor,
setelah itu diikuti oleh ikan tuna. Realisasi ekspor perikanan pada tahun 2007
sebesar Rp 23 trilyun, 50 % dari udang dan 15 % dari ikan tuna. Volume ekspor
udang pada tahun 2007 adalah 160.797 ton dan 90 % dalam bentuk beku tanpa
kulit dan atau tanpa kepala (Pusat Data Statistik dan Informasi, Departemen
Kelautan dan Perikanan 2008; http://www.dkp.go.id).
Salah satu limbah yang dihasilkan dari industri pembekuan udang tersebut
adalah kulit udang. Menurut Dhewanto dan Kresnowati (2002) proporsi berat
kulit udang terhadap berat udang keseluruhannya adalah 45 %. Berdasarkan
proporsi tersebut, diperkirakan jumlah limbah kulit udang yang tersedia pada
tahun 2007 mencapai 100.188,9 ton.
Selama ini, pemanfaatan limbah kulit di Indonesia sebagian besar digunakan
untuk pakan ternak, campuran untuk pembuatan kerupuk udang, dan terasi
(Dhewanto dan Kresnowati 2002). Pengolahan limbah kulit udang menjadi
produk seperti pakan ternak, terasi maupun kerupuk mempunyai nilai tambah
yang relatif kecil.
Untuk meningkatkan nilai tambah kulit udang, diekstraksi menjadi kitin
sangat penting dilakukan, karena kitin mempunyai harga jual yang tinggi. Harga
kitin saat ini berkisar antara Rp 50.000,-/kg (untuk bahan penanganan limbah cair)
sampai Rp 1.000.000,-/kg (untuk bahan biomedik)
Kitin yang terdapat dalam kulit udang berkisar antara 20 sampai 60 % (berat
kering ), tergantung jenisnya (Muzzarelli 2000). Berdasarkan hasil penelitian
pendahuluan, kulit udang vannamei (Penaeus vannamei) mengandung kitin
sekitar 58 % (bk). Udang vannamei (P.vannamei) merupakan jenis udang yang
diekspor terbesar dalam bentuk beku tanpa kulit, yaitu hampir 75 % dari volume
ekspor udang beku (Pusat Data Statistik dan Informasi, Departemen Kelautan dan
Perikanan 2008; http://www.dkp.go.id).
Menurut Mangunwidjaja dan Harahap (2001), penanganan dan pengolahan
limbah udang melalui industri kitin menjadi sorotan, karena senyawa yang hampir
sama dengan selulosa ini ternyata menunjukkan keandalan di berbagai bidang dan
mempunyai prospek sebagai komoditi perdagangan. Kitin dan turunannya dapat
dimanfaatkan untuk kesehatan, industri tekstil, penanganan air limbah, farmasi,
biomedikal, kosmetik, teknologi pangan, fotografi dan lain-lain.
Saat ini produsen kitin dunia dikuasai oleh Jepang dan Amerika Serikat.
Sebenarnya, Indonesia mempunyai peluang untuk mengambil bagian dari pasar
kitin dunia karena memiliki sumber bahan baku kitin yang relatif lebih besar jika
dibandingkan dengan Jepang atau Amerika Serikat.
Ekstraksi kitin dari kulit udang di dunia industri dilakukan secara kimiawi
melalui tahapan deproteinasi yang menggunakan basa kuat dan demineralisasi
yang menggunakan asam kuat. Tahapan deproteinasi dimaksudkan untuk
menurunkan kandungan protein sedangkan demineralisasi dimaksudkan untuk
Menurut Yang et al. (2000), ekstraksi kitin secara kimiawi tersebut dapat
menyebabkan hidrolisis polimer terhadap kitin yang dihasilkan, sehingga
viskositasnya rendah dan mempengaruhi penggunaan kitin selanjutnya. Toan et
al. (2006), menyatakan bahwa ekstraksi secara kimia diperlukan penanganan
terhadap limbah cair yang dihasilkan yaitu harus dinetralisasi dan didetoksifikasi
agar tidak merusak lingkungan. Biaya penanganan limbah cair dari industri kitin
tersebut cukup besar yaitu dapat mencapai 40 % dari total biaya produksi. Selain
itu, ekstraksi kitin secara kimiawi berlangsung pada suhu yang relatif tinggi (
>100 oC) sehingga diperlukan energi yang cukup besar.
Alternatif lain untuk ekstraksi kitin dapat dilakukan dengan metode
biologis. Proses ekstraksi kitin secara biologis adalah memanfaatkan aktivitas
atau kemampuan mikroba baik dalam tahapan demineralisasi maupun
deproteinasinya. Proses demineralisasi dilakukan dengan memanfaatkan
fermentasi asam laktat sedangkan proses deproteinasi menggunakan kemampuan
mikroba proteolitik (Bustos dan Healy 1994)
Kitin hasil ekstraksi secara biologis mempunyai nilai viskositas yang lebih
tinggi daripada kitin yang diektraksi secara kimiawi (Beaney et al. 2005).
Keunggulan lain dari proses ekstraksi kitin secara biologis adalah dihasilkan
produk samping yang potensial. Produk samping tersebut antara lain protein dan
pigmen karotenoid sebagai suplemen pakan untuk ikan dan binatang lainnya, serta
kalsium laktat yang merupakan komponen mineral penting untuk makanan
suplemen (Healy et al. 2003). Limbah cairnya tidak perlu adanya penanganan
Beberapa penelitian ekstraksi kitin secara biologis telah dilakukan yaitu
Ekstraksi kitin dari limbah kulit udang windu (Penaeus monodon) melalui
fermentasi asam laktat menggunakan gabungan bakteri Streptococcus faecium,
Lactobacillus plantarum dan Pediococcus acidilactici (Hall dan Silva 1992).
Ekstraksi kitin dari kulit udang Duplin Bay (Nephrops norvegicus) menggunakan
gabungan bakteri Lactobacillus salvarius, Enteroccus facium dan Pediococcus
acidilactici (Beaney et al. 2005). Deproteinasi limbah kulit udang menggunakan
bakteri Pseudomonas aeruginosa K-187 (Wang dan Chio 1998), Pseudomonas
maltophilia LC-102 (Shimahara et al. 1984) dan Bacillus subtilis (Yang et al.
2000).
Semua hasil penelitian ekstraksi kitin secara biologis tersebut diperoleh
tingkat penghilangan kandungan abu dan protein dari kulit udang berkisar antara
30 – 85 %, yang masih rendah jika dibandingkan dengan metode kimia yang dapat
mencapai lebih dari 95 %. Menurut Healy et al. (2003), tingkat penghilangan
kandungan abu dan protein dari kulit dalam ekstraksi kitin adalah penting.
Semakin besar tingkat penghilangan kandungan abu dan protein dari kulit udang
akan dihasilkan kitin yang memiliki kandungan abu dan protein kecil. Makin
kecil kandungan abu dan protein kitin, harga jual kitin makin tinggi. Oleh karena
itu penggunaan mikroba baru yang lebih potensial untuk ekstraksi kitin perlu terus
dilakukan.
Beberapa bakteri yang potensial digunakan untuk ekstraksi kitin adalah
Bacillus licheniformis F11.1 dan Lactobacillus acidophilus FNCC 116. Bacillus
tidak memproduksi enzim kitinase, sehingga dapat digunakan dalam proses
deproteinasi pada tahapan ekstraksi kitin. B. licheniformis F11.1 adalah bakteri
derivat dari B. licheniformis F11 yang berhasil diisolasi dari limbah kulit udang.
Isolasi terhadap B. licheniformis F11 dilakukan atas kerjasama antara
Laboratorium Bioindustri, Badan Pengkajian dan Penerapan Teknologi (BPPT)
dengan Universitas Hamburg, Jerman dalam rangka mendapatkan strains baru
penghasil enzim protease.
L. acidophilus FNCC 116 adalah bakteri asam laktat yang bersifat
homofermentatif. Artinya, dalam proses fermentasi hanya asam laktat saja yang
dihasilkan oleh bakteri tersebut dari biokonversi glukosa, sehingga diharapkan
lebih efektif untuk menurunkan kandungan abu kulit udang dalam proses
demineralisasi pada tahapan ekstraksi kitin.
Berdasarkan penelusuran paten dan jurnal ilmiah, bakteri B. licheniformis
F11.1 dan L. acidophilus FNCC 116 belum pernah digunakan untuk ekstraksi
kitin dari kulit udang. Menurut Jung et al. (2005), penggunaan bakteri dengan
jenis dan strains yang berbeda untuk ekstraksi kitin diperlukan kondisi optimum
yang berbeda pula. Dengan demikian diperlukan perancangan proses biologis
untuk ekstraksi kitin dari kulit dengan menggunakan kedua bakteri tersebut agar
diperoleh tingkat penghilangan mineral dan protein yang maksimal. Dalam
kegiatan perancangan ini, hasil dari setiap tahapan yang dilakukan merupakan
pilihan yang paling baik dari beberapa pilihan yang dicanangkan.
Selain itu, penggunaan kedua bakteri tersebut untuk ekstraksi kitin dari kulit
optimal pertumbuhan 55oC, sehingga mikroba yang bersifat mesophilik yang
umumnya tumbuh di lingkungan suhu ruang tidak dapat mengkontaminasi proses
deproteinasi. Begitu pula dengan proses demineralisasi yang menggunakan L.
acidhophillus FNCC 116 yang bersifat acidophilik yaitu tumbuh optimal pada
lingkungan pH asam, sehingga mikroba non acidophilik yang banyak terdapat di
lingkungan suhu ruang tidak dapat mengkontaminasi. Keuntungan kondisi
ekstraksi kitin yang tidak perlu steril ini adalah dapat menghemat energi dan
waktu proses.
Agar ekstraksi kitin secara biologis ini dapat diterapkan dalam skala
komersial perlu dilakukan peningkatan skala. Peningkatan skala dalam bioproses
dilakukan dalam tiga tahapan yaitu skala laboratorium, pilot plant, dan industri.
Pada peningkatan skala bioproses ini harus diusahakan kondisi optimum tetap
terjaga. Masalah utama yang dijumpai pada peningkatan skala bioproses adalah
berubahnya faktor-faktor lingkungan fisik, seperti perpindahan massa,
kemampuan pencampuran, penyebaran tenaga dan laju geser. Oleh karena itu
harus dipilih kriteria peningkatan skala yang sesuai agar diperoleh hasil kitin yang
tetap optimal.
1.2 Tujuan Penelitian
Penelitian ini bertujuan mendapatkan rancangan proses biologis untuk
ekstraksi kitin dari kulit udang vannamei (P. vannamei) menggunakan bakteri B.
licheniformis F11.1 dan L. acidophilus FNCC 116, sehingga tingkat penghilangan
kriteria terbaik pada proses biologis ekstraksi kitin untuk peningkatan skala
proses.
1.3 Ruang Lingkup Penelitian
A. Perancangan proses ekstraksi kitin dari kulit udang secara biologis:
- Penentuan jalur tahapan proses ekstraksi kitin yang paling baik secara
biologis.
- Penentuan sistem fermentasi yang paling baik pada ekstraksi kitin dari kulit
udang secara biologis.
B. Penentuan kriteria peningkatan skala yang paling baik untuk proses ekstraksi
kitin dari kulit udang secara biologis.
1.4 Manfaat Penelitian
Manfaat penelitian ini adalah memperoleh informasi mengenai rancangan
proses dan kriteria peningkatan skala untuk ekstraksi kitin dari kulit udang secara
biologis. Informasi yang diperoleh tersebut diharapkan dapat digunakan sebagai
dasar untuk pengembangan ekstraksi kitin dari kulit udang secara biologi ke arah
II TINJAUAN PUSTAKA
2.1 Kulit Udang
Ekspor komoditi hasil perikanan dari Indonesia yang terbesar sampai saat
ini adalah udang. Realisasi ekspor udang pada tahun 2007 mencapai 160.797 ton
dengan nilai Rp 11,5 trilyun. Nilai ekspor udang ini adalah 50 % dari nilai ekspor
komoditi perikanan Indonesia pada tahun 2007 yaitu sebesar 23 trilyun (Pusat
Data Statistik dan Informasi, Departemen Kelautan dan Perikanan 2008
http://www.dkp.go.id)
Ekspor udang tahun 2003 sampai 2007 terus meningkat sebagaimana
ditunjukkan pada Tabel 1. Udang yang diekspor hampir 90 % nya adalah bentuk
beku tanpa kulit dan kepala. Jenis udang yang diekspor adalah udang vannamei
dan windu, untuk tiga tahun terakhir hampir 75 % adalah udang vannamei (Pusat
Data Statistik dan Informasi, Departemen Kelautan dan Perikanan 2008
http://www.dkp.go.id)
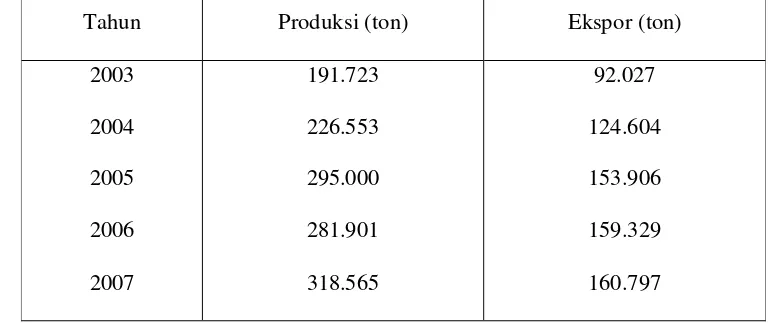
Tabel 1 Produksi dan ekspor udang Indonesia 2003 – 2007
Tahun Produksi (ton) Ekspor (ton)
2003
2004
2005
2006
2007
191.723
226.553
295.000
281.901
318.565
92.027
124.604
153.906
159.329
160.797
Salah satu limbah yang dihasilkan dari industri pembekuan udang tanpa
kulit dan kepala adalah kulit udang. Proporsi kulit udang dapat mencapai 45 %
dari berat udang keseluruhan (Dhewanto dan Kresnowati 2002). Berdasarkan
asumsi tersebut, ketersediaan kulit udang di Indonesia tiap tahunnya relatif besar.
Menurut Rao et al. (2000), kulit udang mengadung beberapa komponen
yaitu protein, pigmen, lemak, kitin dan mineral yang berupa kalsium karbonat.
Semua komponen ini dapat diisolasi atau diekstraksi sehingga mempunyai nilai
jual yang lebih tinggi dibandingkan dengan kulit udang. Tiga komponen yang
keberadaannya cukup besar dalam kulit udang adalah kitin, mineral dan protein.
Kandungan kitin pada kulit udang merah (Solenocera melantho) adalah
23,3 % (bk) (Chang dan Tsai 1997). Kandungan kitin pada udang Crangon
crangon adalah 17,8 % (bk) (Synowiecki dan Al-Khateeb 2000). Menurut
Muzzarelli (2000), kandungan kitin dalam kulit udang berkisar antara 20 – 60 %
(bk), tergantung jenisnya.
2.2 Kitin
Kitin merupakan senyawa biopolimer berantai panjang dan tidak bercabang.
Tiap rantai polimer pada umumnya terdiri dari 2000 hingga 5000 unit monomer
N-asetil-D-Glukosamin (2-acetamido-2-deoksi-D-Glukosa) yang terpaut melalui
ikatan β (1-4) glukosa. Unit monomer kitin mempunyai rumus molekul
C8H12NO5 dengan kadar C, H, N dan O berturut-turut 47%, 6%, 7% dan 40%
Struktur kitin dan kitosan serupa dengan selulosa, yaitu antara monomernya
terangkai dengan ikatan glukosida pada posisi β (1-4). Perbedaan dengan selulosa
adalah gugus hidroksil (-OH) yang terikat pada atom karbon nomor dua,
digantikan oleh gugus asetamina (-NHCOCH3) pada kitin sehingga kitin menjadi
sebuah polimer berunit N-Asetil glukosamin sedangkan pada kitosan digantikan
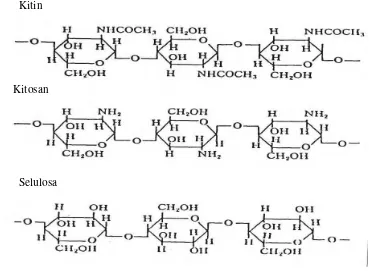
oleh gugus amin (NH2) (Tsugita 1990). Struktur kimia kitin, kitosan dan selulosa
dapat dilihat pada Gambar 1.
Gambar 1 Struktur kimia kitin, kitosan dan selulosa (Tsugita 1990)
Pengamatan dengan sinar X terhadap struktur kitin menunjukkan adanya
gugus amino yang tidak terasetilasi pada setiap 6 sampai 7 gugus asetil
glukosamida. Ditinjau dari segi fisik, struktur kitin tersusun atas unit-unit
berbentuk ortorombik, setiap sel dibangun oleh 8 residu asetil glukosamin, dan Kitin
Kitosan
mempunyai ukuran 94Ǻ x 10,5 Ǻ x 9,3 Ǻ. Berdasarkan struktur tersebut kitin
dapat dibedakan atas tiga jenis yaitu α kitin (rantai antipararel), β kitin (rantai
pararel) dan γ-kitin (rantai campuran) (Tsugita 1990).
Menurut Stephen (1995), kitin merupakan makromolekul berbentuk padatan
amorfatau kristal dengan panas spesifik 0,373 kal/g/oC, berwarna putih, dan dapat
terurai secara hayati (biodegradable), terutama oleh bakteri penghasil enzim
lisozim dan kitinase. Kitin bersifat tidak larut dalam air, asam anorganik encer,
asam organik, alkali pekat dan pelarut organik tetapi larut dalam asam pekat
seperti asam sulfat, asam nitrit, asam fosfat dan asam formiat anhidrous. Menurut
Austin (1988), kitin yang larut dalam asam pekat dapat terdegradasi menjadi
monomernya dan memutuskan gugus asetil.
Mutu niaga berbagai produk kitin berdasarkan spesifikasi kandungan air,
abu, dan proteinnya terdapat pada Tabel 2. Menurut Bustos dan Healey (1994),
harga kitin ditentukan oleh kandungan abu dan proteinnya. Semakin kecil
kandungan abu dan proteinnya harga kitin semakin tinggi.
Menurut Knorr (1984), sifat kitin yang penting untuk aplikasinya adalah
kemampuannya mengikat air dan minyak karena terdapat gugus hidrofobik dan
hidrofilik. Struktur polar kitin terdispersi membentuk misel, dan ekor
hidrokarbonnya tersembunyi di sebelah dalam membentuk fase hidrofobik,
sedangkan fase hidrofilik ada di sebelah luar. Jumlah air dan minyak yang dapat
diikat kitin masing-masing sebesar 385 % dan 315 %.
Kitin karena bersifat mengikat air dan minyak, sehingga dapat digunakan
sebagai surfaktan atau pengemulsi pada makanan, dan kosmetik. Selain itu kitin
dan turunannya dapat digunakan sebagai penstabil, pengental, kelengkapan ion
exchanger, membran pada kromatografi dan dialisis (Knorr 1984), untuk proses
penyembuhan luka bakar, pengobatan dermatitis, pengobatan infeksi jamur,
sebagai benang bedah dan sebagai bahan lensa kontak yang lunak dan bersih
(Alamsyah 2004). Hubungan antara penerapan dan nilai tambah kitin dan
turunannya dalam berbagai industri terdapat pada Gambar 2.
Gambar 2 Penerapan kitin dan turunannya di industri (Morrisey 2003). Nilai tambah tinggi dan volume pemakaian sedikit
- Biomedik dan Pharmaceutical
- Teknologi kimia
- Kosmetik
- Teknologi pangan
- Penjernih air
- Pertanian
- Tekstil
- Teknologi kertas
Kitin dengan proses deasetilasi (pengurangan gugus asetil) diturunkan
menjadi kitosan. Kitosan ini mempunyai sifat yang larut dalam asam-asam
organik encer dan tidak larut dalam air (Alamsyah 2004). Proses deasetilasi kitin
menjadi kitosan selama ini dilakukan secara termokimia menggunakan alkali kuat
pada suhu tinggi, perlakuan secara enzimatik belum memberikan hasil yang
memuaskan yaitu memperoleh derajat deasetilasi (DD) yang sangat rendah
(Emmawati 2005).
Penelitian yang dilakukan Tsigos dan Bouriotis (1995) pada kristal kitin dari
kulit udang yang dideasetilasi secara enzimatis mendapatkan kitosan dengan nilai
DD 54 %. Menurut Bartnicki-Gracia (1989), sulitnya dihasilkan kitosan dengan
DD tinggi diduga karena kitin secara alami berbentuk kristalin yang mengandung
rantai-rantai polimer kitin berkerapatan sangat tinggi, yang satu sama lain terikat
dengan ikatan hidrogen yang sangat kuat, sehingga menghalangi enzim
berpenetrasi mencapai subtrat spesifiknya.
2.3 Ekstraksi Kitin
Ekstraksi kitin dilakukan melalui dua tahapan proses yaitu penghilangan
protein (deproteinasi) dan penghilangan kalsium karbonat (demineralisasi) dari
kulit udang (Muzzarelli 2000). Kedua tahapan proses dalam ekstraksi kitin
tersebut dapat dilakukan secara kimia maupun biologi (Alamsyah 2004).
Ekstraksi kitin secara kimia dilakukan dengan menggunakan senyawa kimia
seperti asam klorida, atau asam laktat pada proses demineralisasinya. Sedangkan
(Bastaman 1989). Ekstraksi kitin secara biologi dilakukan melalui proses
fermentasi asam laktat pada tahapan demineralisasi sedangkan pada tahapan
deproteinasi menggunakan enzim protease baik yang ditambahkan langsung atau
enzim yang dihasilkan oleh bakteri selama proses kultivasi (Lee dan Tan 2002).
2.3.1 Proses Deproteinasi
Kulit udang selain mengandung kitin juga mengandung protein. Untuk
mendapatkan kitin dari kulit udang, maka protein tersebut harus dihilangkan atau
dideproteinasi. Protein yang terdapat pada kulit udang dapat berikatan secara fisik
dan kovalen. Protein yang terikat secara fisik dalam kulit udang dapat
dihilangkan dengan perlakuan fisik seperti pengecilan ukuran, dan pencucian
dengan air. Adapun protein yang terikat secara kovalen dapat dihilangkan dengan
perlakuan kimia yaitu pelarutan dalam larutan basa kuat atau dengan perlakuan
biologi (Lee dan Tan 2002).
Jumlah protein yang terikat secara kovalen dengan kitin setiap jenis
crustacea tidak sama. Protein yang terikat secara kovalen dalam kulit udang
sekitar 16 %. Perbedaan jumlah protein yang terikat secara kovalen akan
mempengaruhi mudah tidaknya proses deproteinasi (Austin 1988).
Deproteinasi secara kimia dari kulit udang dengan menggunakan larutan
natrium hidroksida atau larutan basa lainnya dapat menyebabkan kerusakan pada
asam amino protein yang direcovery. Kerusakan yang terjadi adalah pelepasan
amonia pada pemecahan group amida asparagin dan glutamin menjadi asam
threonin mengalami kerusakan sekitar 5 – 10 %, adapun sistin/sistein, asam
aspartat, asam glutamat, lisin, arginin, tirosin dan prolin terdegradasi sebagian
(Davidex et al. 1990).
Deproteinasi secara biologi dilakukan dengan menggunakan enzim protease.
Enzim protease adalah enzim yang mampu menghidrolisis ikatan peptida dalam
protein. Enzim protease tersebut dapat diperoleh baik dari jaringan tanaman,
hewan maupun hasil metabolik mikroba (Lee dan Tan 2002).
Pada proses hidrolisis ikatan peptida terdapat tiga perubahan. Perubahan
pertama yaitu struktur molekul polipeptida membentuk struktur hidrofobik yang
terbuka terhadap lingkungan berair. Perubahan kedua terjadi kenaikan jumlah
gugus terionisasi (NH4+, COO-) sehingga produk lebih bersifat hidrofilik.
Perubahan ketiga adalah penurunan ukuran molekul rantai polipeptida sehingga
sifat antigenisitas menurun tajam (Mahmoud 1994).
Menurut Stauffer (1989), salah satu enzim protease atau proteolitik ada
yang memiliki aktivitas endo-peptidolitik yaitu memutuskan ikatan peptida di
dalam rantai polipeptida protein. Proses pemutusan ikatan peptida dengan katalis
enzim terdapat pada Gambar 3 sedangkan secara skematis deproteinasi kulit
udang dengan enzim protease dapat dilihat pada Gambar 4.
Protein yang tersusun dari 20 jenis asam amino dapat memiliki 380 ikatan
peptida. Ikatan peptida inilah yang akan menjadi sasaran aksi enzim. Enzim
tertentu hanya memutuskan ikatan tertentu yang secara fisik cocok dengan enzim.
Proses hidrolisis protein secara enzimatis memerlukan kondisi yang sesuai
Faktor-faktor yang perlu dikondisikan dalam proses hidrolisis adalah temperatur,
jumlah dan jenis enzim yang digunakan, pH, dan waktu.
Enzim
CHR’- CO-NH-CHR” + H2O
→
–CHR’-COOH + NH2-CHR”Gambar 3 Reaksi kimia pemutusan ikatan peptida dengan katalis enzim (Mahmoud 1994)
Beberapa penelitian deproteinasi kulit udang secara biologi telah banyak
dilakukan, baik yang menggunakan enzim yang ditambahkan langsung maupun
enzim hasil metabolik sekunder dari proses kultivasi mikroba (Yang et al. 2000).
Bustos dan Healy (1994) telah membandingkan penggunaan enzim langsung
dengan enzim hasil metabolik kultivasi mikroba pada proses deproteinasi kulit
udang. Hasilnya menunjukkan tingkat hidrolisis protein kulit udang
menggunakan enzim hasil kultivasi mikroba (82 %) lebih baik dibandingkan
menggunakan enzim yang ditambahkan langsung (64 %). Menurut Gagne dan
Simpson (1993) rasio enzim papain terhadap kulit udang yang dibutuhkan untuk
memperoleh hasil maksimum pada proses deproteinasi adalah sangat tinggi yaitu
1 : 10 (b/b).
Buston dan Healey (1994) menyatakan penggunaan enzim langsung untuk
proses deproteinasi pada tahapan ekstraksi kitin dari kulit udang diperlukan dua
tahapan proses. Tahapan pertama dilakukan proses isolasi dan pemurnian
terhadap enzim proteolitik dari jaringan hewan dan tanaman atau hasil metabolik
sekunder mikroba. Tahapan kedua adalah enzim yang telah diisolasi dan
dimurnikan tersebut digunakan untuk proses hidrolisis protein terhadap kulit
proteolitik hanya dilakukan satu tahapan saja yaitu tidak diperlukan proses isolasi
dan permurnian enzim. Enzim hasil metabolik mikroba langsung menghidrolis
protein kulit udang yang terdapat dalam kultivasi tersebut.
Deproteinasi kulit udang melalui kultivasi mikroba telah banyak
dilakukan. Bustos and Healy (1994) melaporkan penggunaan campuran mikroba
B. subtilis, S. faecium, P. pentasaseus, dan A.oryzae dan mampu mendeproteinasi
81,7 % dari kulit udang yang telah didemineralisasi secara kimia. Yang et al.
(2000), menggunakan B. subtilis dan mampu mendeproteinasi 78 % dari kulit
udang segar.
Gambar 4 Skematis deproteinasi kulit udang secara biologi (Lee dan Tan 2000)
B. licheniformis mempunyai potensi untuk digunakan pada proses
deproteinasi kulit udang (Waldeck et al. 2006). B. licheniformis merupakan
bakteri gram positif, berbentuk batang dengan panjang antara 1,5 µm sampai 3
µm dan lebar antara 0,6 µm sampai 0,8 µm. Spora bakteri ini berbentuk batang
silindris atau elips dan terdapat pada sentral atau parasentral. Suhu maksimum
pertumbuhannya adalah 50 – 55 oC dan suhu minimumnya 15 oC (Mao et al.
1992).
B. licheniformis merupakan species bakteri yang mampu menghasilkan
protease dalam jumlah yang relatif tinggi. Jenis protease yang dihasilkan adalah Protein terasosiasi dalam kulit udang protein terlarut
hidrolisis enzim protease
enzim ekstraselular yang tergolong proteinase serin. Enzim ini bekerja sebagai
endopeptidase yaitu memutuskan ikatan peptida yang berada dalam rantai protein
sehingga dihasilkan peptida dan polipeptida (Fleming et al. 1995).
Sifat dari enzim protease serin adalah aktivitasnya dapat dihambat kuat oleh
senyawa diisopropil-fluorofosfat (DFP), 3,4-dichloroisocoumarin (3,4-DCL),
L-3-carboxytrans-2,3-epoxypropyl-leucylamido (4-guanidine), butane,
phenymethylsulfonylfluoride (PMSF), dan tosyl-L-lysine chlorometyl ketone
(TLCK). Selain itu, protease serin tahan terhadap EDTA (Ethylene diamine
tetraacetic acid) dan adanya ion Ca++ dapat menstabilkan enzim ini pada suhu
tinggi (Rao et al. 1998).
2.3.2 Proses Demineralisasi
Kulit udang mengandung mineral 30 – 50 % (berat kering), komposisi yang
utama adalah kalsium karbonat. Komponen mineral ini dapat dilarutkan dengan
penambahan asam seperti asam klorida, asam sulfat atau asam laktat (Bastaman
1989).
Menurut Lee dan Tan (2002), proses demineralisasi dapat dilakukan secara
kimia dan biologi. Demineralisasi secara kimia digunakan senyawa kimia seperti
asam klorida atau asam laktat. Demineralisasi secara biologi yaitu melarutkan
mineral yang terdapat dalam kulit udang melalui proses fermentasi asam laktat.
Proses demineralisasi secara biologi ini melibatkan dua proses utama yang
bersamaan dalam satu sistem. Proses pertama adalah pembentukan asam laktat.
karbonat dalam kulit udang membentuk kalsium laktat (Lee dan Tan 2002).
Proses biologi yang terjadi selama demineralisasi kulit udang dalam fermentasi
asam laktat ditunjukkan pada Gambar 5, sedangkan reaksi antara asam laktat dan
kalsium karbonat terdapat pada Gambar 6.
Menurut Healey et al. (2003), demineralisasi melalui fermentasi asam laktat
hampir sama dengan secara kimia yang menggunakan asam laktat. Akan tetapi
demineralisasi menggunakan asam laktat langsung diperlukan dua tahapan proses.
Proses pertama adalah pembentukan dan pemisahan asam laktat. Proses kedua
adalah reaksi antara asam laktat dengan kalsium karbonat dalam kulit udang
membentuk kalsium laktat.
Gambar 5 Skema proses biologi demineralisasi kulit udang dalam fermentasi asam laktat (Lee dan Tan 2000)
Fermentasi asam laktat merupakan proses perubahan bahan penghasil asam
laktat seperti glukosa, sukrosa, maltosa dan laktosa menjadi asam laktat oleh
enzim yang dihasilkan oleh bakteri asam laktat. Bakteri asam laktat termasuk
dalam golongan bakteri gram positif, tidak berspora, berbentuk batang atau bulat,
tidak berespirasi, dan suhu optimum pertumbuhan antara 20 – 40 oC. Sifat-sifat Glukosa
L. acidophilus FNCC 116
Asam laktat + kalsium karbonat dalam kulit udang
terbentuk produk akhir
Kalsium laktat + CO2 + air
khusus bakteri asam laktat adalah mampu tumbuh pada kadar gula, alkohol, dan
garam yang tinggi, tumbuh pada pH 3,8 sampai 8,0. Adapun bakteri yang
tergolong dalam bakteri asam laktat adalah Aerococcus, Corinobacterium,
Lactobacillus, Leuconostoc, Pediococcus, Streptococcus, Tetragenococcus, dan
Vagacoccus (Frazier dan Westhoff 1988).
Bakteri-bakteri yang mampu menghasilkan asam laktat dapat dibagi
menjadi dua kelompok yaitu bakteri homofermentatif dan heterofermentatif.
Bakteri heterofermentatif selain menghasilkan asam laktat, juga karbondioksida
dan etanol. Adapun bakteri homofermentatif hanya menghasilkan asam laktat
(Litchfield 1996).
Gambar 6 Persamaan reaksi antara asam laktat dan kalsium karbonat (Lee dan Tan 2000)
Seluruh anggota genus Pediococcus, dan Streptococcus merupakan bakteri
homofermentatif, sedangkan seluruh genus Leuconostoc merupakan bakteri
heterofermentatif. Genus bakteri Lactobacillus ada yang termasuk dalam bakteri
homofermentatif dan heterofermentatif (Sharpe 1981).
Beberapa penelitian proses demineralisasi kulit udang melalui fermentasi
asam laktat antara lain dilaporkan oleh Rao dan Stevens (2006), Beaney et al.
(2005), dan Jung et al. (2005). Bakteri asam laktat yang digunakan Rao dan
Stevens (2006) adalah L. plantarum, sedangkan Beaney et al. (2005)
CaCO3 + 2CH3CHOHCOOH (CH3CHOHCOO)2Ca + H2CO3
H2CO3 H2O + CO2
menggunakan gabungan bakteri L. salvarius, Enterococcus facium dan P.
acidilactici. Adapun Jung et al. (2005) menggunakan bakteri L. paracasei.
Menurut Rao dan Stevens (2006), pemilihan jenis bakteri untuk proses
demineralisasi pada tahapan ekstraksi kitin dari kulit crustacea didasarkan atas
kemampuannya membiokonversi gula menjadi asam laktat. Menurut Dash
(2002), salah satu bakteri asam laktat yang efisien membiokonversi gula menjadi
asam laktat adalah L. acidophilus. Bakteri ini bersifat homofermentatif, mampu
membiokonversi gula menjadi asam laktat lebih dari 85 %.
L. acidophilus secara spesifik ditemukan dan tumbuh di dalam susu skim,
termasuk golongan organisme gram positif dan non-motil. Bentuknya batang
bulat 0,6 – 0,9 µm dan panjang 1,5 – 6,0 µm serta ada dalam bentuk tunggal atau
berpasangan. Suhu pertumbuhan optimumnya adalah 37 oC dan tidak dapat
tumbuh pada temperatur di bawah 22 oC atau di atas 45 oC (Dash 2002).
L. acidophilus mempunyai kemampuan untuk berkembang dalam media
asam dan juga dalam ragi, amigdalin, selobiosa, dan salicin. L. acidophillus dapat
juga melakukan proses fermentasi pada rafinosa, trihalosa dan dekstrin.
Sedangkan xylosa, arabinosa, rhamnosa, gliserol, manitol, sorbitol, dulsitol, dan
inositol tidak dapat difermentasi oleh bakteri asam laktat ini. Selain itu,
Lactobacillus merupakan organisme probiotik yang memiliki banyak kemampuan
penting, salah satu diantaranya dapat bertahan dalam koloni sel karena
menghasilkan bacteriocins yang bekerja berlawanan terhadap pertumbuhan
2.4 Sistem Fermentasi
Proses deproteinasi maupun demineralisasi dalam ekstraksi kitin dari kulit
udang secara biologi dilakukan dengan memanfaatkan kemampuan mikroba
dalam suatu proses kultivasi. Kultivasi mikroba dilakukan bersama-sama dengan
kulit udang dalam suatu sistem fermentasi (Lee dan Tan 2000).
Untuk proses deproteinasi, kultivasi mikroba dimaksudkan untuk
memproduksi enzim protease yang selanjutnya enzim ini menghidrolisis protein
yang terikat secara kovalen dalam kulit udang (Healey et al. 2003). Adapun pada
proses demineralisasi, kultivasi mikroba dimaksudkan untuk memproduksi asam
laktat. Asam laktat yang terbentuk secara bersamaan akan bereaksi dengan
kalsium karbonat, komponen mineral yang terdapat dalam kulit udang (Rao et al.
2000).
Keberhasilan ekstraksi kitin secara biologi pada tahapan deproteinasi
dipengaruhi oleh kemampuan enzim untuk menghidrolis protein. Kemampuan
atau aktivitas enzim ini salah satunya dipengaruhi oleh jumlah enzim yang
dihasilkan dalam suatu kultivasi. Semakin banyak jumlah enzim yang dihasilkan
maka aktivitas enzim semakin tinggi pula, sehingga semakin banyak protein pada
kulit udang yang dihidrolisis (Bustos dan Healy 1994).
Keberhasilan ekstraksi kitin secara biologi pada tahapan demineralisasi
dipengaruhi oleh jumlah asam laktat. Semakin banyak jumlah asam laktat yang
dihasilkan maka semakin banyak kalsium karbonat pada kulit udang yang dapat
Menurut Stanbury dan Whitaker (1984), enzim dan asam laktat merupakan
produk metabolik mikroba yang dikultivasi dalam suatu sistem fermentasi. Enzim
merupakan produk metabolit sekunder sedangkan asam laktat termasuk metabolik
primer. Metabolit sekunder bakteri akan diproduksi maksimal pada saat bakteri
tersebut telah memasuki fase eksponensial sedangkan metabolit primer diproduksi
sejalan dengan meningkatnya pertumbuhan bakteri.
Strategi untuk memproduksi secara maksimal baik terhadap produk
metabolik primer maupun sekunder pada fermentasi medium cair telah banyak
dilaporkan. Fleming et al. (1995), menggunakan fermentasi batch untuk
mengoptimalkan sintesis enzim ektraseluler dari B. licheniformis DN286 dan B.
subtilis 168. Cromwick et al. (1996) menggunakan fermentasi fed batch untuk
memproduksi asam glutamat melalui kultivasi B licheniformis ATCC 9945.
Sedangkan Wee et al. (2006) menggunakan fermentasi batch untuk
mengoptimalkan produksi asam laktat melalui kultivasi Lactobacillus sp. RKY2.
2.5 Aerasi dan Agitasi
2.5.1 Aerasi
Perberian aerasi selalu dilakukan untuk sistem kultivasi cair mikroba yang
bersifat aerobik. Aerasi tersebut dimaksudkan untuk menyediakan oksigen dalam
medium fermentasi. Tingkat aerasi yang diberikan tergantung kepada jenis
bakteri yang digunakan (Cromwick et al. 1995).
Mikroba aerobik seperti B. licheniformis sangat memerlukan tingkat
licheniformis DSM 1969 dalam bioreaktor volume 3,5 L untuk memproduksi
protease dilakukan aerasi sampai 2 vvm dan pemberian aerasi kurang dari 1 vvm
menyebabkan pertumbuhan bakteri tidak optimal (Calik et al. 2000). Sementara
itu (Cromwick et al. 1995) melaporkan bahwa pembentukan asam glutamat oleh
B. licheniformis ATCC 9945A sangat dipengaruhi tingkat aerasi yang diberikan.
Tingkat aeasi 2 vvm menghasilkan asam glutamat yang lebih banyak dibadingkan
dengan pemberian aerasi 0,5 vvm; 1,0 vvm dan 1,5 vvm.
Menurut Calik et al. (2000), metabolisme bakteri akan terganggu jika
konsentrasi oksigen terlarut berada dibawah tingkat kritisnya. Selanjutnya,
peningkatan kelarutan oksigen dalam medium kultivasi akan meningkatkan laju
konsumsi oksigen spesifik oleh bakteri sampai nilai tertentu, setelah itu
peningkatan oksigen terlarut tidak berpengaruh terhadap laju konsumsi oksigen
spesifik. Dengan demikian ketersedian oksigen terlarut harus dipertahankan lebih
besar dari tingkat kritisnya.
2.5.2 Agitasi
Agitasi mempunyai peranan sangat penting pada sistem cair kultivasi
mikroba baik yang bersifat aerobik (Calik et al. 1998) maupun mikroaerofilik
seperti fermentasi asam laktat (Luis et al. 2003). Menurut Benz (2008), tingkat
agitasi yang diberikan berpengaruh terhadap pertumbuhan mikroba, sehingga
berakibat terhadap jumlah metabolik yang dihasilkan.
Menurut Calik et al. (1998), kultivasi mikroba B. licheniformis DSM 1969
dari 250 rpm. Karena B. licheniformis DSM 1969 adalah mikroba yang bersifat
aerobik yaitu sangat memerlukan oksigen untuk pertumbuhannya.
Sementara itu, Luis et al. (2003) melaporkan tingkat agitasi yang diberikan
untuk produksi asam laktat optimal melalui fermentasi asam laktat menggunakan
L. delbrueckii NRRL B 445 hanya 200 rpm. Dijelaskan bahwa pemberian agitasi
yang terlalu tinggi menyebabkan pertumbuhan bakteri tidak optimal sehingga
terjadi penurunan terhadap produksi asam laktat.
Pemberian agitasi juga dilakukan pada proses ekstraksi kitin secara biologi
(Bustos dan Healey 1994). Tingkat agitasi yang diberikan tergantung pada jenis
mikroba yang digunakan (Benz 2008). Jung et al. (2005) melalui kofermentasi L.
paracasei subsp dan S. marcescens FS-3 untuk ekstraksi kitin dari cangkang
kepiting, agitasi yang diberikan adalah 180 rpm. Selanjutnya (Rao dan Stevens
2005), melaporkan tingkat agitasi yang diberikan untuk ekstraksi kitin dari kulit
udang adalah 50 rpm. Bakteri yang digunakan adalah L. plantarum 541, bakteri
ini bersifat mikroaerofilik yaitu memerlukan oksigen dalam jumlah terbatas.
2.9 Optimasi dengan Response Surface Methodology
Penggunaan metode Response Surface Methodology (RSM) untuk optimasi
dalam proses-proses kimia, bioproses dan pengembangan pengolahan pangan
telah banyak dilaporkan (Mangunwijadja dan Harahap 2001; Santoso dkk 2002;
dan Luis et al. 2003). Optimasi adalah suatu pendekatan normatif untuk