Lampiran 2. Bagan pembuatan ekstrak daun jambu bol (Syzygium malaccense
dibiarkan selama 5 hari terlindung dari cahaya
sambil sesekali diaduk
Lampiran 3. Bagan pembuatan fraksi n-heksan, fraksi etilasetat dan fraksi air daun jambu bol (Syzygium malaccense L.Merr & Perry)
ditambahkan 10 ml akuades dihomogenkan
dimasukkan dalam corong pisah ditambah dengan 40 ml n- heksan dikocok dan didiamkan sampai terbentuk dua lapisan dan dipisahkan
dilakukan fraksinasi hingga diperoleh fraksi n-heksan yang jernih
Ekstrak etanol daun jambu bol (30g)
Lampiran 4. Gambar tanaman jambu bol (Syzygiun malaccense L. Merr & Perry) dan daun jambu bol
Tanaman jambu bol
Lampiran 6. Perhitungan hasil karakterisasi serbuk simplisia dan ekstrak etanol daun jambu bol
1. Penetapan kadar air
No
Berat sampel Volume awal Volume akhir
Simplisia Ekstrak Simplisia Ekstrak Simplisia Ekstrak
1 5,0500 g 5,0500 g 1,2 2,4 1,6 2,6
2 5,0500 g 5,0000 g 1,6 2,6 2,0 2,8
3 5,0300 g 5,0000 g 2,0 2,8 2,4 3,0
Kadar air simplisia
%Kadar air = , ,
, x 100% = 7,92 %
% Kadar air = , – ,
, x 100 % = 7,92 %
% Kadar air = , – ,
, x 100 % = 7,95 %
% Kadar air rata-rata = , % , % , % = 7,93 %
Kadar air ekstrak
Kadar air = , – ,
,
x 100% = 3,96 %
% Kadar air = , – ,
, x 100 % = 4 %
% Kadar air = ( )
Lampiran 6. (Lanjutan)
% Kadar air = , – ,&
, x 100 % = 4 %
% Kadar air rata-rata = , % , % , % = 3,98 %
2. Penetapan kadar sari larut air
No
Berat sampel Berat sari
Simplisia Ekstrak Simplisia Ekstrak
1 5,0000 g 5,0500 g 0,1300 g 0,4000 g
2 5,0000 g 5,0000 g 0,1200 g 0,3500 g
3 5,0500 g 5,0500 g 0,1500 g 0,3500 g
Kadar sari simplisia
% Kadar sari larut dalam air = ,
, x
x
100 % = 13,0 %% Kadar sari larut dalam air = ,
, x
x
100 % = 12,0 %% Kadar sari larut dalam air = ,
, x
x
100 % = 14,85 %% Kadar sari larut dalam air rata-rata = , % , % ,& % = 13,28 %
% kadar sari yang larut dalam air = " # $
Lampiran 6. (Lanjutan)
3. Penetapan kadar sari larut etanol No
Berat sampel Berat sari
Simplisia Ekstrak Simplisia Ekstrak
Lampiran 6. (Lanjutan)
Simplisia Ekstrak Simplisia Ekstrak
% Kadar abu tidak larut asam = " # " # . / # $
" # $ % x 100 %
Lampiran 6. (Lanjutan)
Kadar abu total ekstrak
% Kadar abu total = ,
,
x 100 % = 2 %
% Kadar abu total = ,
, x 100 % = 2,24 %
% Kadar abu total = ,
, x 100 % = 2,74 %
% Kadar abu total rata-rata = , % , % = 2,32 %
5. Penetapan kadar abu yang tidak larut asam
No
Berat sampel Berat sari
Simplisia Ekstrak Simplisia Ekstrak
1 2,0000 g 2,0000 g 0,0100 g 0,0065 g
2 2,0000 g 2,0000 g 0,0100 g 0,0041 g
3 2,0000 g 2,0000 g 0,0100 g 0,0045 g
Kadar abu simplisia
% Kadar abu tidak larut asam = ,
,
x 100 % = 0,5 %
% Kadar abu tidak larut asam = ,
, x 100 % = 0,5 %
% Kadar abu tidak larut asam = ,
Lampiran 6. (Lanjutan)
% Kadar abu tidak larut asam rata-rata = , % , % , % = 0,5 %
Kadar abu ekstrak
% Kadar abu tidak larut asam = ,
,
x 100 % = 0,11 %
% Kadar abu tidak larut asam = ,
,
x 100 % = 0,11 %
% Kadar abu tidak larut asam = ,
,
x 100 % = 0,12 %
Lampiran 7. Gambar sediaan gel ekstrak daun jambu bol
Keterangan:
F0 = Basis gel
FI = Formula mengandung 15% ekstrak daun jambu bol
Lampiran 8. Gambar hasil uji homogenitas gel ekstrak daun jambu bol
Keterangan:
F0 = Basis gel
FI = Formula mengandung 15% ekstrak daun jambu bol
Lampiran 9. Perhitungan nilai viskositas
Perhitungan viskositas = faktor koreksi x skala = cp = :100=p Nomor spindel : 64
Nomor speed : 30 Faktor koreksi : 200
Lampiran 14. Gambar hasil uji aktivitas antibakteri ekstrak etanol daun jambu bol terhadap bakteri Staphylococcus aureus
500mg/mL
200mg/mL 300mg/mL 400mg/mL
100mg/mL Blanko
75mg/mL
50mg/mL 6,25mg/mL
25mg/mL 12,5mg/mL
125mg/mL
Lampiran 15. Gambar hasil uji aktivitas antibakteri ekstrak etanol daun jambu bol terhadap bakteri Staphylococcus epidermidis
400mg/mL 500mg/mL
300mg/mL 200mg/mL
Blanko 50mg/mL
75mg/mL 100mg/mL
150mg/mL
Lampiran 16. Gambar hasil uji aktivitas antibakteri ekstrak etanol daun jambu bol terhadap bakteri Pseudomonas aeroginosa
500mg/mL
300mg/mL
400mg/mL
75mg/mL
50mg/mL
100mg/mL 200mg/mL
12,5mg/mL 25mg/mL
6,25mg/mL Blanko 125mg/mL
150mg/mL
Lampiran 17. Gambar hasil uji aktivitas antibakteri fraksi n-heksan daun jambu bol terhadap bakteri Staphylococcus aureus
500mg/mL
300mg/mL
400mg/mL
200mg/mL
25mg/mL 50mg/mL
75mg/mL 100mg/mL Blanko
Lampiran 18. Gambar hasil uji aktivitas antibakteri fraksi n-heksan daun jambu bol terhadap bakteri Staphylococcus epidermidis
500mg/mL 400mg/mL
200mg/mL 300mg/mL
25mg/mL 50mg/mL
75mg/mL 100mg/mL Blanko
Lampiran 19. Gambar hasil uji aktivitas antibakteri fraksi n-heksan daun jambu bol terhadap bakteri Pseudomonas aeroginosa
500mg/mL 300mg/mL
400mg/mL 200mg/mL
25mg/mL
50mg/mL 100mg/mL 75mg/mL
Blanko
150mg/mL
Lampiran 20. Gambar hasil uji aktivitas antibakteri fraksi etilasetat daun jambu bol terhadap bakteri Staphylococcus aureus
200mg/mL 300mg/mL
500mg/mL
400mg/mL
75mg/mL
12,5mg/mL
100mg/mL
50mg/mL Blanko
6,25mg/mL
Lampiran 21. Gambar hasil uji aktivitas antibakteri fraksi etilasetat daun jambu bol terhadap bakteri Staphylococcus epidermidis
500mg/mL
300mg/mL 200mg/mL
400mg/mL
100mg/mL
25mg/mL
75mg/mL
50mg/mL
12,5mg/mL
Blanko
Lampiran 22. Gambar hasil uji aktivitas antibakteri fraksi etilasetat daun jambu bol terhadap bakteri Pseudomonas aeroginosa
500mg/mL
300mg/mL
125mg/mL
200mg/mL
12,5mg/mL 100mg/m
75mg/mL 25mg/mL
50mg/mL
Blanko
6,25mg/mL 400mg/mL
150mg/mL
Lampiran 27. Perhitungan pembuatan variasi konsentrasi larutan uji
1. Konsentrasi 500 mg/mL 2 gram ekstrak
4 mL pelarut DMSO= 500 mg/mL
• Konsentrasi 500 mg/mL dibuat dengan melarutkan 2 g ekstrak dalam 4 mL DMSO
2. Konsentrasi 400 mg/mL 400 mg/mL
500 mg/mLx 1 mL = 0,8 mL larutan uji konsentrasi 500 mg/mL
• Konsentrasi 400 mg/mL dibuat dari 0,8 mL larutan uji konsentrasi 500 mg/mL dan dicukupkan dengan 0,2 mL pelarut DMSO.
3. Konsentrasi 300 mg/mL 300 mg/mL
500 mg/mLx 1 mL = 0,6 mL larutan uji konsentrasi 500 mg/mL
• Konsentrasi 300 mg/mL dibuat dari 0,6 mL larutan uji konsentrasi 500 mg/mL dan dicukupkan dengan 0,4 mL pelarut DMSO.
4. Konsentrasi 200 mg/mL 200 mg/mL
400 mg/mLx 1 mL = 0,5 mL larutan uji konsentrasi 400 mg/mL
• Konsentrasi 200 mg/mL dibuat dari 0,5 mL larutan uji konsentrasi 400 mg/mL dan dicukupkan dengan 0,5 mL pelarut DMSO.
5. Konsentrasi 150 mg/mL 150 mg/mL
300 mg/mLx 1 mL = 0,5 mL larutan uji konsentrasi 300 mg/mL
Lampiran 27. (Lanjutan) 6. Konsentrasi 125 mg/mL
125 mg/mL
500 mg/mLx 1 mL = 0,25 mL larutan uji konsentrasi 500 mg/mL
• Konsentrasi 125 mg/mL dibuat dari 0,25 mL larutan uji konsentrasi 500 mg/mL dan dicukupkan dengan 0,75 mL pelarut DMSO.
7. Konsentrasi 100 mg/mL 100 mg/mL
200 mg/mLx 1 mL = 0,5 mL larutan uji konsentrasi 200 mg/mL
• Konsentrasi 100 mg/mL dibuat dari 0,5 mL larutan uji konsentrasi 200 mg/mL dan dicukupkan dengan 0,5 mL pelarut DMSO.
8. Konsentrasi 75 mg/mL 75 mg/mL
150 mg/mLx 1 mL = 0,5 mL larutan uji konsentrasi 150mg/mL
• Konsentrasi 75 mg/mL dibuat dari 0,5 mL larutan uji konsentrasi 150 mg/mL yang diperoleh dari konsentrasi 300mg/mL dan dicukupkan dengan 0,5 mL pelarut DMSO.
9. Konsentrasi 50 mg/mL 50 mg/mL
100 mg/mLx 1 mL = 0,5 mL larutan uji konsentrasi 100 mg/mL
• Konsentrasi 50 mg/mL dibuat dari 0,5 mL larutan uji konsentrasi 100 mg/mL dan dicukupkan dengan 0,5 mL pelarut DMSO.
10. Konsentrasi 25 mg/mL 25 mg/mL
50 mg/mLx 1 mL = 0,5 mL larutan uji konsentrasi 50 mg/mL
Lampiran 27. (Lanjutan) 11. Konsentrasi 12,5 mg/mL
12,5 mg/mL
25 mg/mL x 1 mL = 0,5 mL larutan uji konsentrasi 25 mg/mL
• Konsentrasi 12,5 mg/mL dibuat dari 0,5 mL larutan uji konsentrasi 25 mg/mL dan dicukupkan dengan 0,5 mL pelarut DMSO.
12. Konsentrasi 6,25 mg/mL 6,25 mg/mL
12,5 mg/mLx 1 mL = 0,5 mL larutan uji konsentrasi 12,5 mg/mL
• Konsentrasi 6,25 mg/mL dibuat dari 0,5 mL larutan uji konsentrasi 12,5mg/mL dan dicukupkan dengan 0,5 mL pelarut DMSO.
13. Konsentrasi 3,125 mg/mL 3,125 mg/mL
6,25 mg/mL x 1 mL = 0,5 mL larutan uji konsentrasi 6,25 mg/mL
DAFTAR PUSTAKA
Anonim. (2014). Manfaat Jambu Bol Untuk Kesehatan. Tanggal akses 25 juli 2016.https://www.7manfaat.com/manfaat-jambu-bol-untuk-kesehatan. Achroni, K. (2012). (Semua Rahasia Kulit Cantik dan Sehat Ada Disini). Cetakan
I. Jogjakarta: javalitera. Halaman 57.
Anhira. (2011). Bisul dan Cara Mengatasinya. Tanggal akses pada 27 juli 2016. http//Annehira.com
Arifin, H., Rasyid R., dan Lucida H. (2009). Pengembangan Tumbuhan Jambu Bol (Eugenia malaccensis L.). Hasil Penelitian Tahun I Hibah Unggulan Strategis Nasional Tahun Anggaran 2009. Padang : Universitas Andalas. Brooks, G.F., Butel, J.S., dan Morse, S.A.(2001). Medical Microbiology Twenty
Second Ed. Penerjemah: Bagian Mikrobiologi Fakultas Kedokteran Universitas Airlangga. Mikrobiologi Kedokteran. Edisi I. Jakarta: Penerbit Salemba Medika. Halaman. 93,235,317, 371.
Depkes RI. (1979). Materia Medika Indonesia. Jilid III. Jakarta: Departemen Kesehatan RI. Halaman 33, 167-170.
Depkes RI. (1985). Cara Pembuatan Simplisia. Jakarta: Departemen Kesehatan RI. Halaman 10. Kesehatan Republik Indonesia. Halaman 9,12, 33.
Ditjen POM RI. (1985). Formularium Kosmetika Indonesia. Jakarta: Departemen Kesehatan RI. Halaman 32-36,86
Ditjen POM RI. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Departemen Kesehatan Republik Indonesia. Halaman 7,896-898,1112.
Ditjen POM RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Cetakan Pertama. Jakarta: Departemen Kesehatan RI Direktorat Jenderal Pengawasan Obat dan Makanan Direktorat pengawasan Obat Tradisional. Halaman 10-11, 14-17, 31-32.
Dwidjoseputro, D. (1978). Dasar-Dasar Mikrobiologi. Jakarta: Djambatan. Halaman 17,119.
Garg, A., D. Aggarwal, S. Garg, dan Sigla. A. K. (2002). Spreading of Semisolid Formulation. USA: Pharmaceutical Technology. Halaman 84-104.
Gibson, M., (2001), Pharmaceutical Preformulation and Formulation. United States of America: CRC Press. Halaman 546-550.
Harborne, J.B. (1987). Metode Fitokimia. Penerjemah: Kosasih Padmawinata dan Iwang Soediro. Edisi II. Bandung: Penerbit ITB. Halaman 152.
Jawetz, E., Joseph, M., Edward, A.A., Geo, F.B., Janet ,S.B., dan Nicholas, L.D. (2001). Mikrobiologi Kedokteran. Penerjemah: Mudihardi, E., Kuntaman.,Wasito,E.B., Mertamiasih, M., Harsono, S., Alimsardjono., L. Jakarta: Penerbit Salemba Medica. Halaman 357.
Lieberman, H.A. (1997). Pharmaceutical Dosage Form: Disperse System. Vol. 1. New York: Marcell Dekker Inc. Halaman 315-319.
Marliana, E dan Saleh, C. (2011). Uji Fitokimia dan Aktivitas Antibakteri Ekstrak Kasar Etanol, Fraksi n-Heksana, Etilasetat dan Metanol dari Buah Labu Air (Lagenari siceraria (Molina) Standl. Jurnal Kimia Mulawarman 8(2): 63-69.
Martin, A., Swarbrick. J, dan Cammarata. A. (1993). Farmasi Fisik: Dasar-dasar Farmasi Fisik dalam Ilmu Farmasetik. Edisi III. Penerjemah: Yoshita. Jakarta: UI-Press. Halaman 1176-1182.
Morton, J.F. (1987). Malay Apple in Fruits of Warm Climates. Creative Resource System Inc. Winterville, N.C. pp. 378-381
Mulyana, L. (2015). Uji Aktivitas Ekstrak Etanol Daun Jambu Bol (Syzygium Malaccense L. Merr & Perry) Sebagai Antikolesterol Menggunakan Tikus Jantan. Skripsi. Medan: Universitas Sumatera Utara.
Nurmalina, R. (2012). 24 Herbal Legendaris Untuk Kesehatan Anda. Jakarta: Alex Media Komputindo. Halaman 11.
Odugbemi, T. (2008). A Textbook of Medicinal Plants from Nigeria. Nigeria: University of Lagos Press. Halaman 219-220.
Oxoid. (1982). The Oxoid Manual. Edisi VIII. Basingtoke: Oxoid Limited. Halaman 223-224.
Panjaitan, E.N., Awaluddin, S., dan Djendakita, P. (2012). Formulasi Gel dari Ekstrak Rimpang Jahe Merah (Zingiber officinale Roscae). J of Pharmaceutics and Pharmacology. 1(1): 9-20.
Rahmawanty, D., Effionora, A., dan Anton, B. (2014). Formulasi Gel Menggunakan Serbuk Daging Ikan Haruan (Channa striatus) sebagai Penyembuh Luka. Media Farmasi. 11(1):29-40.
Robinson, T. (1995). Kandungan Organik Tumbuhan Tinggi. ITB, Bandung, Indonesia. Halaman 191-193.
Rogers, T.L., Hypromellose, Rowe, R. C., Paul J. S., dan Marian E. Q. (2009). Handbook of Pharmaceutical Excipient. Edisi VI. USA: Pharmaceutical Press. Halaman 326-329.
Rowe, R.C., Sheskey, P.J., and Owen, S.C. (2006). Handbook of Pharmaucetical Excipiens.Pharmaceutical Press, American pharmaceutical Association. Edisi V. Halaman 346, 466, 596 dan 624.
Sari, R., dan Isadiartuti, D. (2006). [Studi Efektivitas Sediaan Gel Antiseptik Tangan Ekstrak Daun Sirih (Piper betle Linn.)] 17(4): 163-169.
Soerartri, W. (2004). Pengaruh Penambahan Asam Glikolat Terhadap Efektivitas Sediaan Tabir Surya Kombinasi Anti UV-A dan UV-B Dalam Basis Gel. Surabaya: M. Farmasi Airlangga. 4(3):76.
Staf Pengajar FK UI. (1994). Buku Ajar Mikrobiologi Kedokteran. Edisi Revisi. Jakarta: Binarupa Aksara. Halaman 18-20, 103.
Suardi, M., Armenia, dan Maryawati, A. (2008) Formulasi dan Uji Klinik Gel Anti Jerawat Benzoil Peroksida-HPMC. Karya Ilmiah, Fakultas Farmasi Universitas Andalas, Sumatra Barat. Halaman 34.
Syamsuni, H. (2006).Farmasetika Dasar dan Hitungan Farmasi. Jakarta: EGC. Halaman 104.
Tim Mikrobiologi FK Brawijaya. (2003). Bakteriologi Medik. Cetakan I. Malang: Bayu Media Publishing. Halaman 29,32,33,132,133.
Venn, R.F. (2008). Principles and Practices of Bioanalysis. Edisi II. Prancis: Taylor and Francis Group Ltd. Halaman 23-25.
Verheij, E.W.M., dan Coronel, R.E. (1991). Buah-buahan yang dapat dimakan. Terjemahan dari Plant Resources of South-East Asia 2: Edible Fruits and Nuts oleh Daniminihardja, S ; Sutarno, H; Utami, N.W. ; dan Hoesen, D.S.H. PT. Gramedia Pustaka Utama. Halaman 376-379.
Voigt, R. (1984). Lehrbuch der Pharmaceutischen Technologie. Penerjemah: Soendani Noerono. (1995). Buku Pelajaran Teknologi Farmasi. Jogjakarta: UGM Press. Halaman 573.
Waluyo, L. (2010). Teknik dan Metode Dasar Dalam Mikrobiologi. Cetakan II. Malang: UPT Penerbitan Universitas Muhammadiyah. Halaman 40-42,185,186.
BAB III
METODE PENELITIAN
Metode penelitian ini menggunakan metode eksperimental dengan tahapan penelitian yaitu pengumpulan dan pengolahan bahan, pembuatan ekstrak, karakterisasi simplisia, pembuatan sediaan gel ekstrak dan fraksi daun jambu bol dengan menggunakan HPMC sebagai basis gel, evaluasi stabilitas sediaannya dan pengujian aktivitas antibakteri ekstrak dan fraksi daun jambu bol (Syzygium malaccense L.Merr & Perry) dan sediaan gel ekstrak daun jambu bol terhadap bakteri Staphylococcus aureus, Pseudomonas aeroginosa, Staphylococcus epidermidis. Penelitian ini dilakukan di Laboratorium Fitokimia, Laboratorium Mikrobiologi dan Laboratorium Farmasi Fisik Fakultas Farmasi Universitas Sumatera Utara.
3.1 Alat
3.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah serbuk simplisia daun jambu bol (Syzygium malaccense L.Merr & Perry), etanol 80%, aquadest, HPMC 4000, propilenglikol, metil paraben, bakteri uji: Staphylococcus aureus (ATCC 6358), Pseudomonas aeroginosa (ATCC 9027), Staphylococcus epidermidis (ATCC 11764), media Nutrient Agar (NA), media Nutrient Broth (NB), pereaksi Molish, pereaksi Dragendorf, pereaksi Bouchardat, pereaksi Mayer. Bahan kimia yang digunakan kecuali dinyatakan lain adalah berkualitas pro analisa yaitu: asam klorida pekat, asam asetat anhidrida, asam sulfat pekat, besi (III) klorida, etanol, amil alkohol, n-heksan, isopropanol, kloroform, metanol, natrium hidroksida, serbuk magnesium, timbal (II) asetat, toluen dan dimetil sulfoksida (DMSO).
3.3 Penyiapan Bahan
3.3.1 Pengambilan bahan tanaman
Pengumpulan bahan tumbuhan dilakukan secara purposive yaitu tanpa membandingkan dengan bahan tumbuhan yang sama dari daerah lain. Bahan diambil dari pohon yang tumbuh di Emplasmen, PTPN III Kebun Pulau Mandi, Kec.Buntu Pane Kab.Asahan. Daun yang diambil adalah helai daun yang masih segar, berwarna hijau, dalam keadaan baik dengan usia dewasa, tidak terlalu tua dan tidak terlalu muda.
3.3.2 Identifikasi tanaman
3.3.3 Pengolahan sampel
Daun yang sudah diambil dicuci dengan air yang mengalir dan dikeringkan sampai rapuh. Selanjutnya daun kering diblender menjadi serbuk.
3.4 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik, penetapan kadar air, penetapan kadar sari larut air, penetapan kadar sari larut etanol, penetapan kadar abu total dan penetapan kadar abu tidak larut asam.
3.4.1 Pemeriksaan makroskopik
Pemeriksaan makroskopik dilakukan dengan mengamati bentuk luar, ukuran serta warna dari simplisia daun jambu bol.
3.4.2 Penetapan kadar air
kandungan air yang terdapat dalam bahan yang diperiksa (WHO, 1998). 3.4.3 Penetapan kadar sari larut air
Sebanyak 5 g serbuk yang telah dikeringkan, dimaserasi selama 24 jam dalam 100 mL air-kloroform (2,5 mL kloroform dalam air suling 1000 mL) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, dibiarkan selama 18 jam, kemudian disaring, diuapkan 20 mL filtrat sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan di udara (Depkes RI, 1995). 3.4.4 Penetapan kadar sari larut etanol
Sebanyak 5 g serbuk simplisia yang telah dikeringkan dimaserasi selama 24 jam dalam 100 mL etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam lalu disaring, kemudian 20 mL filtrat diuapkan sampai kering dalam cawan dangkal berdasar rata yang telah ditara dan sisanya dipanaskan pada suhu 105oC sampai bobot tetap. Kadar sari larut dalam etanol dihitung terhadap bahan yang telah dikeringkan (Depkes RI, 1995).
3.4.5 Penetapan kadar abu total
3.4.6 Penetapan kadar abu tidak larut asam
Abu yang telah diperoleh dalam penetapan abu didinginkan dengan 25 mL asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring dengan kertas masir atau kertas saring bebas abu, cuci dengan air panas, dipijarkan sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut dalam asam dihitung terhadap bobot yang dikeringkan di udara (Depkes RI, 1995).
3.5 Skrining Fitokimia
Skrining fitokimia serbuk simplisia daun jambu bol meliputi pemeriksaan senyawa alkaloid, saponin, flavonoid, tanin, glikosida, steroid.
3.5.1 Pemeriksaan alkaloid
Serbuk simplisia ditimbang 0,5 g kemudian ditambahkan 1 mL asam klorida 2 N dan 9 ml air suling, dipanaskan diatas penangas air selama 2 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk uji alkaloida sebagai berikut:
a. Filtrat 3 tetes ditambah 2 tetes larutan pereaksi Mayer, maka akan terbentuk endapan menggumpal berwarna putih atau putih kekuningan.
b. Filtrat 3 tetes ditambah 2 tetes larutan pereaksi Bouchardat, maka akan terbentuk endapan berwarna coklat.
c. Filtrat 3 tetes ditambah 2 tetes larutan pereaksi Dragendorff, maka akan terbentuk endapan warna merah atau jingga.
3.5.2Pemeriksaan flavonoida
Sebanyak 10 g serbuk simplisia ditambahkan 10 mL air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, ke dalam 5 mL filtrat ditambahkan 0,1 g serbuk magnesium dan 1 mL asam klorida pekat dan 2 mL amil alkohol, dikocok dan dibiarkan memisah. Hasil menunjukan positif flavonoida jika terjadi warna merah atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.5.3Pemeriksaan glikosida
Sebanyak 3 g serbuk simplisia ditimbang, lalu disari dengan 30 mL campuran dari 7 bagian etanol 95% dan 3 bagian air suling, kemudian direfluks selama 10 menit, didinginkan, lalu disaring. Filtrat diambil 20 mL, ditambahkan 25 mL air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu disaring. Filtrat disari dengan 20 mL campuran 2 bagian isopropanol dan 3 bagian kloroform, perlakuan ini diulangi sebanyak 3 kali menghasilkan 2 lapisan. Dikumpulkan masing-masing sari (sari air dan sari pelarut organik). Sari pelarut organik dikumpulkan dan ditambahkan Na2SO4 anhidrat, disaring kemudian
3.5.4Pemeriksaan glikosida antrakuinon
Sebanyak 0,2 g serbuk simplisia ditimbang, kemudian ditambahkan 5 mL asam sulfat 2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml benzena, dikocok dan didiamkan. Lapisan benzena dipisahkan dan disaring, kocok lapisan benzena dengan 2 mL NaOH 2 N, didiamkan. Lapisan air menghasilkan warna merah dan pada lapisan benzena yang tidak berwarna menunjukan adanya senyawa antrakinon (Depkes RI, 1995).
3.5.5Pemeriksaan saponin
Sebanyak 0,5 g serbuk simplisia dimasukan ke dalam tabung reaksi, lalu ditambahkan 10 mL air panas, dinginkan kemudian dikocok kuat-kuat selama 10 detik. Jika terbentuk busa setinggi 1-10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan 1 tetes asam klorida 2 N menunjukan adanya saponin (Depkes RI, 1995).
3.5.6Pemeriksaan tanin
Sebanyak 0,5 g sampel disari dengan 10 mL air suling, disaring lalu filtratnya diencerkan dengan air suling sampai tidak berwarna. Filtrat yang diperoleh, diambil 2 mL larutan lalu ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida. Terjadi warna biru atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
3.5.7Pemeriksaan steroid/triterpenoid
3.6 Pembuatan Ekstrak Etanol Serbuk Simplisia Daun Jambu Bol
Pembuatan ekstrak etanol daun jambu bol dilakukan dengan cara maserasi menggunakan etanol 80% (Depkes RI, 1979).
Cara kerja :
Sebanyak 900 g serbuk simplisia daun jambu bol dimasukan ke dalam wadah berkaca berwarna gelap, kemudian dituangi dengan 8,5 L etanol 80%. Ditutup dan dibiarkan selama 5 hari terlindung dari cahaya sambil sering diaduk, diserkai dan diperas. Ampas dicuci dengan 2,5 L etanol 80%, dipindahkan ke dalam bejana tertentu, dibiarkan di tempat sejuk, terlindung dari cahaya selama 2 hari, selanjutnya dienap tuangkan. Maserat etanol yang diperoleh diuapkan denagn menggunakan rotary evaporator pada temperature ± 40oC sampai diperoleh ekstrak kental kemudian dikeringkan menggunakan hair dryer dan freezer.
3.7 Pembuatan Fraksi n-Heksan, Fraksi Etilasetat dan Fraksi Air
Sebanyak 10 g ekstrak etanol ditambahkan 10 mL aquadest lalu ditambahkan 40 ml n-heksan, dikocok dalam corong pisah dan dibiarkan sampai memisah, kemudian dipisahkan, selanjutnya difraksinasi kembali dengan menggunakan pelarut n-heksan hingga diperoleh fraksi n-heksan yang jernih (tidak memberikan reaksi positif dengan penambahan pereaksi Lieberman-Burchard), kemudian fraksi air ditambahkan 50 mL etilasetat, dikocok dan dibiarkan memisah. Lapisan etilasetat dipisahkan dan fraksinasi dilanjutkan sampai diperoleh fraksi etilasetat yang jernih (tidak memberikan hasil positif dengan penambahan pereaksi FeCl
pada temperatur ± 40°C sampai diperoleh ekstrak kental, kemudian dikeringkan dengan hair dryer dan freezer.
3.8 Pembuatan Media untuk Bakteri Uji 3.8.1 Nutrient agar (NA)
Sebanyak 28 g serbuk Nutrient Agar (NA) dilarutkan dalam 1 L air suling steril dan dipanaskan sampai semua bahan larut sempurna, kemudian disterilkan di autoklaf pada suhu 121oC selama 15 menit (Oxoid, 1982).
3.8.2 Nutrient broth (NB)
Sebanyak 13 g serbuk Nutrient Broth (NB) dilarutkan dalam 1 L air suling steril dan dipanaskan sampai semua bahan larut sempurna, kemudian disterilkan di autoklaf pada suhu 121oC selama 15 menit (Oxoid, 1982).
3.8.3. Pembuatan agar miring
3.9 Pembuatan Stok Kultur
3.9.1. Pembuatan stok kultur bakteri Staphylococcus aureus
Satu koloni bakteri Staphylococcus aureus diambil dengan jarum ose steril, lalu diinokulasikan pada permukaan media Nutrient Agar (NA) miring dengan cara menggores, kemudian diinkubasikan pada suhu 35 ± 2oC selama 24 jam (Ditjen POM RI, 1995).
3.9.2 Pembuatan stok kultur bakteri Staphylococcus epidermidis
Satu koloni bakteri Staphylococcus epidermidis diambil dengan jarum ose steril, lalu diinokulasikan pada permukaan media Nutrient Agar (NA) miring dengan cara menggores, kemudian diinkubasikan pada suhu 35 ± 2oC selama 24 jam (Ditjen POM RI, 1995).
3.9.3 Pembuatan stok kultur bakteri Pseudomonas aeroginosa
Satu koloni bakteri Pseudomonas aeroginosa diambil dengan jarum ose lalu diinokulasikan pada permukaan media Nutrient Agar (NA) miring dengan cara menggores, kemudian diinkubasikan pada suhu 35 ± 2oC selama 24 jam (Ditjen POM RI,1995).
3.10 Pembuatan Inokulum Bakteri
3.10.1 Pembuatan inokulum bakteri Staphylococcus aureus
3.10.2 Pembuatan inokulum bakteri Staphylococcus epidermidis
Koloni bakteri Staphylococcus epidermidis diambil dari stok kultur dengan menggunakan jarum ose steril, kemudian disuspensikan ke dalam 10 mL larutan Nutrient Broth (NB) steril lalu diinkubasikan pada suhu 35 ± 2oC sampai didapat kekeruhan dengan transmitan 25% menggunakan alat spektrofotometer UV panjang gelombang 580 nm (Ditjen POM RI, 1995).
3.10.3 Pembuatan inokulum bakteri Pseudomonas aeroginosa
Koloni bakteri Pseudomonas aeroginosa diambil dari stok kultur dengan menggunakan jarum ose steril, kemudian disuspensikan ke dalam 10 mL larutan Nutrient Broth (NB) steril lalu diinkubasikan pada suhu 35 ± 2oC sampai didapat kekeruhan dengan transmitan 25% menggunakan alat spektrofotometer UV panjang gelombang 580 nm (Ditjen POM RI, 1995).
3.11 Sterilisasi Alat dan Bahan
Alat-alat yang digunakan dalam uji aktivitas antibakteri ini disterilkan lebih dahulu sebelum dipakai. Media disterilkan di autoklaf pada suhu 121oC selama 15 menit dan alat-alat gelas lainnya disterilkan di oven pada suhu 160-170oC selama 2-3 jam. Jarum ose dibakar dengan lampu bunsen (Pratiwi, 2008).
3.12 Pembuatan Larutan Uji Ekstrak dan Fraksi Daun Jambu Bol dengan Berbagai Konsentrasi
pengenceran dengan konsentrasi 400 mg/mL; 300 mg/mL; 200 mg/mL; 100 mg/mL; 75 mg/mL; 50 mg/mL; 25 mg/mL; 12,5 mg/mL dan 6,25 mg/mL.
3.13 Pengujian Aktivitas Antibakteri terhadap Ekstrak dan Fraksi
Pengujian aktivitas antibakteri dilakukan terhadap ekstrak dan fraksi daun jambu bol dengan berbagai konsentrasi. Pengujian ini dilakukan dengan metode difusi agar menggunakan pencadang kertas.
3.13.1 Bakteri Staphylococcus aureus
Sebanyak 0,1 mL inokulum dimasukkan ke dalam cawan petri steril, setelah itu dituang media Nutrient Agar (NA) sebanyak 20 mL dengan suhu 45-50oC, selanjutnya cawan digoyang di atas permukaan meja agar media dan suspensi bakteri tercampur rata. Pada media yang telah padat diletakkan beberapa pencadang kertas yang telah dicelupkan dalam larutan uji ekstrak daun jambu bol dengan berbagai konsentrasi, kemudian diinkubasi dalam inkubator pada suhu 35 ± 2oC selama 18-24 jam, lalu diukur diameter daerah hambatan (zona jernih) pertumbuhan di sekitar pencadang dengan menggunakan jangka sorong.
3.13.2 Bakteri Stapyhlococcus epidermidis
3.13.3 Bakteri Pseudomonas aeroginosa
Sebanyak 0,1 mL inokulum dimasukkan ke dalam cawan petri steril, setelah itu dituang media Nutrient Agar (NA) sebanyak 20 mL dengan suhu 45-50oC, selanjutnya cawan digoyang di atas permukaan meja agar media dan suspensi bakteri tercampur rata. Pada media yang telah padat diletakkan beberapa pencadang kertas yang telah dicelupkan dalam larutan uji ekstrak daun jambu bol dengan berbagai konsentrasi, kemudian diinkubasi dalam inkubator pada suhu 35 ± 2oC selama 18-24 jam, lalu diukur diameter daerah hambatan (zona jernih) pertumbuhan di sekitar pencadang dengan menggunakan jangka sorong.
3.14 Pembuatan Formula Sediaan Gel Ekstrak Daun Jambu Bol 3.14.1 Pembuatan basis gel hingga mendidih, kemudian diangkat dan HPMC diikembangkan di dalamnya selama 15 menit, setelah kembang ditambahkan metil paraben dan propil paraben dilarutkan dalam propilen glikol sedikit demi sedikit sambil digerus sampai homogen, lalu dicukupkan dengan air suling hingga 100 g (Soerartri, 2004). 3.14.2 Komposisi formula
Sediaan dibuat ke dalam satu konsentrasi dan satu blanko dimana masing-masing sediaan memiliki bobot 100 g.
Tabel 3.1 Komposisi formula sediaan gel ekstrak etanol daun jambu bol
No Nama Bahan F0 (g) FI (g)
1 Ekstrak etanol jambu bol - 15
Keterangan:
F0 = Formula tanpa mengandung ekstrak daun jambu bol FI = Formula mengandung 15 % ekstrak daun jambu bol 3.14.3 Cara pembuatan sediaan gel
Cara pembuatan: ke dalam lumpang dimasukkan 15 g ekstrak etanol daun jambu bol ditambahkan 85 g basis gel sambil gerus sampai homogen.
3.15 Evaluasi Formula
Evaluasi formula meliputi evaluasi fisik dan biologi. Evaluasi fisik meliputi pemeriksaan stabilitas fisik sediaan, pemeriksaan homogenitas, penentuan pH, dan penentuan viskositas. Evaluasi biologi meliputi pengujian aktivitas antibakteri sediaan gel ekstrak daun jambu bol terhadap Staphylococcus epidermidis, Staphylococcus aureus dan Pseudomonas aeroginosa dengan metode difusi agar menggunakan pencadang kertas.
3.15.1 Pemeriksaan stabilitas fisik sediaan
Pemeriksaan stabilitas sediaan meliputi bentuk, warna dan bau yang diamati secara visual (Ditjen POM RI, 1985).
Sediaan dinyatakan stabil apabila bentuk, warna dan bau tidak berubah secara visual selama penyimpanan dan juga secara visual tidak ditumbuhi jamur. Pengamatan dilakukan pada suhu kamar pada setiap minggu dari minggu ke- 0 hingga minggu ke- 4.
3.15.2 Pemeriksaan homogenitas sediaan
(Ditjen POM RI, 1979). Pengamatan dilakukan pada suhu kamar setiap minggu dari minggu ke- 0 hingga minggu ke- 4.
3.15.3 Penentuan pH sediaan
Penentuan pH sediaan dilakukan dengan mengunakan pH meter Hanna. Alat terlebih dahulu dikalibrasi dengan menggunakan larutan dapar standar pH netral (pH 7,0) dan larutan dapar pH asam (pH 4,0), kemudian pH meter dicuci dengan air suling dan dikeringkan dengan kertas tisu. Pengukuran pH sediaan dengan mencelupkan pH meter ke dalam larutan sediaan. Dicatat nilai pH yang ditunjukkan pada pH meter. Pengamatan dilakukan pada suhu kamar setiap minggu dari minggu ke- 0 hingga minggu ke- 4.
3.15.4 Uji viskositas sediaan
Penentuan viskositas sediaan menggunakan viskometer Brookfield. Sediaan dimasukkan ke dalam pot plastik sampai mencapai volume 100 mL, lalu spindel diturunkan hingga spindel tercelup ke dalam formulasi, selanjutnya alat dihidupkan dengan menekan tombol ON. Kecepatan spindel diatur, kemudian dibaca skalanya (dial reading) dimana jarum merah yang bergerak stabil. Nilai viskositas dalam sentipise (cps) diperoleh dari hasil perkalian skala baca (dial reading) dengan faktor koreksi (f) khusus untuk masing-masing kecepatan spindel. Pengamatan dilakukan pada suhu kamar pada minggu 0, 1, 2, 3, 4.
3.15.5 Uji mikrobiologi sediaan
BAB IV
HASIL DAN PEMBAHASAN 4.1Hasil Identifikasi Sampel
Hasil identifikasi tumbuhan dilakukan di Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI) Bogor menunjukkan bahwa tumbuhan yang digunakan adalah daun jambu bol (Syzygiun malaccense L. Merr & Perry) suku Myrtaceae. Hasil identifikasi dapat dilihat pada Lampiran 1 halaman 51.
4.2 Hasil Ekstraksi Serbuk Daun Jambu Bol
Pembuatan ekstrak dilakukan dengan metode maserasi menggunakan pelarut etanol 96%. Hasil maserasi dari 900 g serbuk simplisia diperoleh ekstrak kental 113,7 g dan setelah di freezer diperoleh sebanyak 109,5 g.
4.3 Hasil Karakterisasi Simplisia Daun Jambu Bol
Hasil karakterisasi simplisia dapat dilihat pada Tabel 4.1 dan perhitungan dapat dilihat pada Lampiran 6 halaman 56–61.
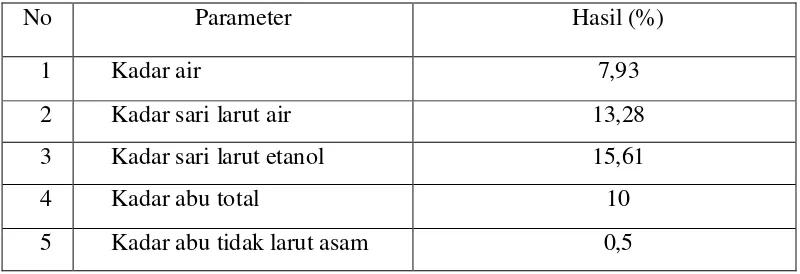
Tabel 4.1 Hasil karakterisasi simplisia
No Parameter Hasil (%)
1 Kadar air 7,93
2 Kadar sari larut air 13,28
3 Kadar sari larut etanol 15,61
4 Kadar abu total 10
5 Kadar abu tidak larut asam 0,5
lainnya (Depkes RI, 1985). Penetapan kadar air dilakukan untuk memberikan batasan minimal atau rentang tentang besarnya kandungan air dalam sampel karena tingginya kandungan air menyebabkan ketidakstabilan sediaan obat, bakteri dan jamur cepat tumbuh dan bahan aktif yang terkandung didalamnya dapat terurai.
Hasil penetapan kadar sari larut air simplisia daun jambu bol dan kadar sari larut etanol simplisia daun jambu bol adalah 13,28 dan 15,61. Penetapan kadari sari yang larut dalam air menyatakan jumlah zat yang tersari larut dalam air yaitu glikosida, gula, gom, protein, enzim, zat warna dan asam organik. Penetapan kadar sari yang larut dalam etanol menyatakan jumlah zat yang tersari dalam pelarut etanol seperti glikosida, antrakinon, steroid, flavonoid, klorofil, saponin, tanin dan dalam jumlah sedikit yang larut yaitu lemak (Depkes RI, 1995).
Penetapan kadar abu total dan kadar abu tidak larut asam bertujuan untuk memberikan jaminan bahwa simplisia tidak mengandung logam berat tertentu melebihi nilai yang ditetapkan karena dapat berbahaya (toksik) bagi kesehatan dan mengetahui kandungan mineral internal yang terdapat di dalam simplisia yang diteliti serta senyawa organik yang tersisa selama pembakaran. Abu total terbagi dua yang pertama abu fisiologis adalah abu yang berasal dari jaringan tumbuhan itu sendiri dan abu non fisiologis adalah sisa setelah pembakaran yang berasal dari bahan-bahan dari luar yang terdapat pada permukaan simplisia. Kadar abu tidak larut asam untuk menentukan jumlah silika, khususnya pasir yang ada pada simplisia dengan cara melarutkan abu total dalam asam klorida (WHO, 1998).
4.4Hasil Skrining Fitokimia Simplisia dan Ekstrak Etanol Daun Jambu Bol Skrining fitokimia terhadap simplisia dan ekstrak etanol daun jambu bol dilakukan untuk mendapatkan informasi golongan senyawa metabolit sekunder yang terdapat di dalam simplisia dan ekstrak etanol daun jambu bol. Skrining fitokimia yang dilakukan terhadap simplisia daun jambu bol meliputi pemeriksaan alkaloid, flavonoid, saponin, tanin, steroid/triterpenoid dan glikosida. Hasil skrining fitokimia simplisia dan ekstrak etanol daun jambu bol dapat dilihat pada Tabel 4.2 berikut.
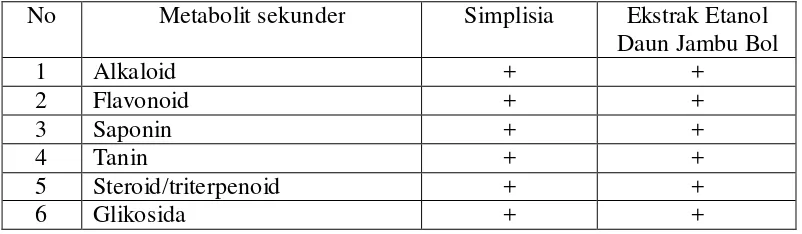
Tabel 4.2 Hasil skrining fitokimia ekstrak etanol daun jambu bol
No Metabolit sekunder Simplisia Ekstrak Etanol
Daun Jambu Bol
Keterangan: (+) = mengandung golongan senyawa metabolit sekunder (-) = tidak mengandung golongan senyawa metabolit sekunder Hasil skrining menunjukkan bahwa simplisia dan ekstrak etanol daun jambu bol mengandung senyawa golongan alkaloid, flavonoid, saponin, tanin, steroid/triterpenoid, dan glikosida.
4.5 Hasil Uji Aktivitas Antibakteri Ekstrak Etanol, Fraksi n-heksan, Fraksi etilasetat dan Fraksi air Daun Jambu Bol
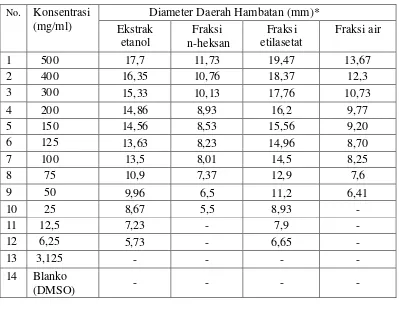
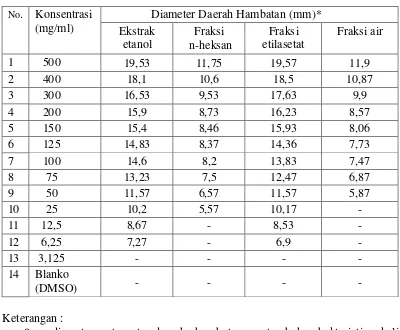
Tabel 4.3 Hasil pengukuran diameter rata-rata daerah hambatan pertumbuhan
Tabel 4.4 Hasil pengukuran diameter rata-rata daerah hambatan pertumbuhan
Berdasarkan hasil pengukuran diameter daerah hambatan pada konsentarsi 500 mg/mL memperlihatkan bahwa fraksi etilasetat dan ekstrak etanol daun jambu bol memberikan aktivitas antibakteri yang terkuat dalam menghambat pertumbuhan Staphylococcus epidermidis. Fraksi etilasetat pada konsentrasi 100 mg/mL memiliki diameter daya hambat adalah 14,93 mm dan ekstrak etanol konsentrasi 150 mg/mL dengan nilai diameter daerah hambat adalah 14,33 mm.
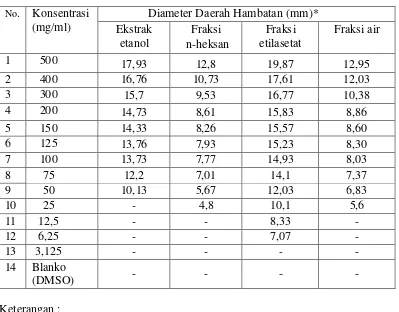
Tabel 4.5 Hasil pengukuran diameter rata-rata daerah hambatan pertumbuhan
Berdasarkan hasil pengukuran diameter daerah hambatan pada konsentrasi 500 mg/mL memperlihatkan bahwa fraksi etilasetat dan ekstrak etanol daun jambu bol memberikan aktivitas antibakteri yang terkuat dalam menghambat pertumbuhan Pseudomonas aeroginosa. Fraksi etilasetat pada konsentrasi 125 mg/mL memiliki diameter daerah hambat adalah 14,36 mm dan ekstrak etanol konsentrasi 150 mg/mL dengan nilai diameter daerah hambat adalah 15,4 mm.
Hasil pengujian aktivitas antibakteri fraksi etilasetat memberikan hasil efektif terhadap bakteri Staphylococcus aureus, Staphylococcus epidermidis dan Pseudomonas aeroginosa pada konsentrasi 125 mg/mL dengan nilai diameter hambatnya adalah 14,96 mm, 15,23 mm dan 14,36 mm.
Hasil pengukuran diameter hambat fraksi air dan dan fraksi n-heksan menunjukkan aktivitas antibakteri yang lemah bila dibandingkan dengan fraksi etilasetat dan ekstrak etanol dalam menghambat pertumbuhan bakteri Staphylococcus aureus, Staphylococcus epidermidis, Pseudomonas aeroginosa. Hasil pengukuran diameter hambat fraksi air terhadap bakteri Staphylococcus aureus, Staphylococcus epidermidis, Pseudomonas aeroginosa pada konsentrasi 500 mg adalah 13,67 mm, 12,95 mm dan 11,9 mm. Nilai ini tidak memenuhi persyaratan diameter hambatan efektif yang ditetapkan, sedangkan untuk fraksi n-heksan hasil pengukuran diameter hambatnya terhadap bakteri Staphylococcus aureus, Staphylococcus epidermidis, Pseudomonas aeroginosa pada konsentrasi 500 mg/ml adalah 11,73 mm, 12,8 mm dan 11,75 mm. Aktivitas antibakteri yang didapatkan dari fraksi etilasetat merupakan aktivitas antibakteri terkuat dalam menghambat pertumbuhan bakteri Staphylococcus aureus, Staphylococcus epidermidis, dan Pseudomonas aeroginosa, dikarenakan kandungan senyawa metabolit sekunder yang terdapat dalam fraksi etilasetat daun jambu bol (Syzygium malaccense L. Merr & Perry) adalah senyawa yang memiliki aktivitas antibakteri yang kuat yaitu flavonoid, tanin dan saponin.
dibandingkan dengan fraksi etilasetat dan juga untuk meminimalisir biaya yang digunakan serta membuat sediaan gel yang efektif sebagai antibakteri. Berdasarkan hasil skrining fitokimia dari ekstrak etanol menunjukkan senyawa metabolit sekunder yang lebih banyak dibandingkan dengan fraksi etilasetat namun menghasilkan zona hambatan yang lebih kecil dibandingkan dengan zona hambatan fraksi etilasetat. Menurut Marliana dan Saleh (2011), hal ini mungkin disebabkan karena adanya kerja yang tidak sinergis antara senyawa metabolit sekunder dalam ekstrak etanol dalam peranannya sebagai antibakteri..
Hasil uji aktivitas antibakteri fraksi air dan fraksi n-heksan lebih rendah dibandingkan fraksi etilasetat dan ekstrak etanol, hal ini disebabkan oleh kandungan senyawa yang terdapat dalam fraksi air yang merupakan fraksi sisa sangat sedikit karena senyawa metabolit sekunder yang memiliki aktivitas anti bakteri kuat telah ditarik oleh pelarut etil asetat sehingga hanya tersisa beberapa senyawa metabolit sekunder dengan kuantitas yang sedikit, sedangkan pada fraksi n-heksan disebabkan karena dari hasil skrining fitokimia fraksi n-heksan hanya memiliki senyawa triterpenoid, walaupun triterpenoid memiliki sifat antibakteri namun jumlahnya tidak mencukupi untuk menghasilkan daya antibakteri sehingga pada pengujian antibakteri hasilnya lebih rendah dibandingkan fraksi etilasetat dan ekstrak etanol.
4.6 Evaluasi Formula
4.6.1 Pemeriksaan stabilitas fisik sediaan
sedangkan dengan penambahan ekstrak gel berwarna hijau pekat serta menunjukkan adanya bau khas daun jambu bol.
Hasil uji stabilitas sediaan gel ekstrak daun jambu bol menunjukkan bahwa seluruh sediaan yang dibuat tetap stabil dalam penyimpanan pada suhu kamar selama 4 minggu. Hasil pemeriksaan stabilitas fisik sediaan gel ekstrak daun jambu bol dapat dilihat pada Tabel 4.6.
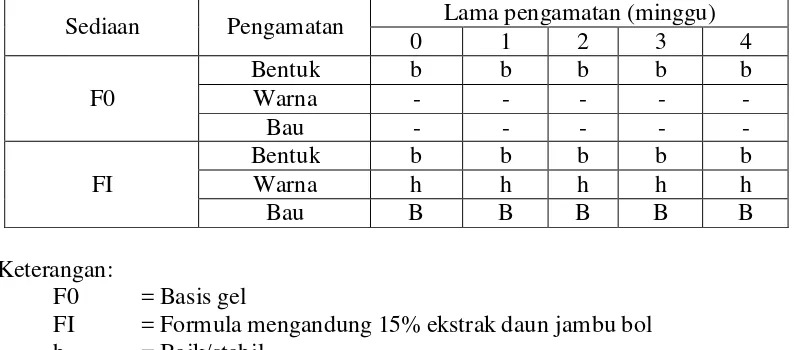
Tabel 4.6 Pengamatan perubahan bentuk, warna, dan bau sediaan gel ekstrak etanol daun jambu bol
Sediaan Pengamatan Lama pengamatan (minggu)
0 1 2 3 4
FI = Formula mengandung 15% ekstrak daun jambu bol b = Baik/stabil
h = Hijau tua
B = Bau khas daun jambu bol
Sediaan gel tidak menunjukkan adanya interaksi antara bahan aktif dan bahan pembawa sehingga tidak mengakibatkan perubahan apapun, hal ini menunjukkan bahan-bahan dalam formula gel tidak mengalami penguraian selama penyimpanan, ini dikarenakan sifat HPMC yang netral, tahan terhadap asam dan basa, punya pH stabil antara 3-11 dan tahan panas (Suardi, dkk., 2008). Sediaan gel yang baik mempunyai kestabilan dalam jangka waktu yang lama dan tidak dipengaruhi oleh lingkungan luar.
4.6.2 Pemeriksaan homogenitas sediaan
tidak boleh mengandung bahan kasar yang bisa diraba (Syamsuni, 2006). Homogenitas sedian gel dapat dilihat secara visual dengan hasil pengujian semua formula dihasilkan warna merata serta tidak ditemukan adanya partikel di dalam gel. Hasil pemeriksaan homogenitas sediaan gel ekstrak daun jambu bol dapat dilihat pada Tabel 4.7.
Tabel 4.7 Pengamatan homogenitas sediaan gel ekstrak etanol daun jambu bol
Sediaan Lama pengamatan (minggu)
FI = Formula mengandung 15% ekstrak daun jambu bol h = Homogen
4.6.3 Penentuan pH sediaan
Hasil penentuan pH sediaan gel ekstrak daun jambu bol dapat dilihat pada Tabel 4.8.
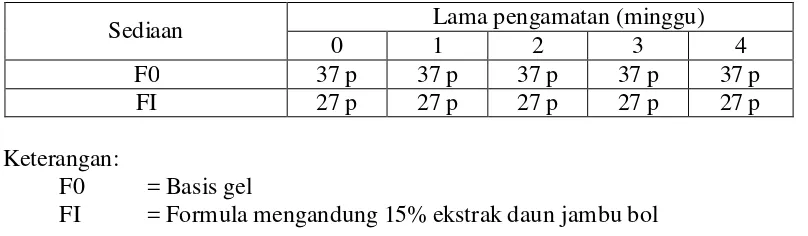
Tabel 4.8 Pengukuran pH sediaan gel ekstrak daun jambu bol
Sediaan Lama pengamatan (minggu)
FI = Formula mengandung 15% ekstrak daun jambu bol
menyebabkan iritasi kulit. Jika pH sediaan terlalu basa dapat menyebabkan kulit menjadi bersisik sehingga mengurangi nilai estetika kulit (Rahmawanty, dkk., 2014). Secara keseluruhan terlihat bahwa pH sediaan gel daun jambu bol stabil sampai minggu ke-4. Hasil uji stabilitas terhadap pH basis gel maupun sediaan gel ekstrak daun jambu bol menunjukkan pH sediaan tetap stabil pada penyimpanan. 4.6.4 Uji viskositas sediaan
Hasil penentuan viskositas gel dilakukan menggunakan viskometer brookfield pada seluruh sediaan. Hasil penentuan viskositas sediaan dapat dilihat pada Tabel 4.9.
FI = Formula mengandung 15% ekstrak daun jambu bol
sediaan akan bersifat lebih asam mengakibatkan jumlah gugus karboksilat yang terionkan berkurang sehingga tolak menolak antar gugus hidroksil yang menyebabkan pengembangan struktur gelling agent menurun, hal ini yang menyebabkan penurunan viskositas gel dengan meningkatnya jumlah ekstrak (Sari dan Isadiartuti, 2006).
4.7 Uji Mikrobiologi Sediaan Gel
Hasil uji aktivitas antibakteri sediaan gel ekstrak dilihat pada Tabel 4.10. Tabel 4.10 Hasil uji aktivitas antibakteri sediaan gel ekstrak etanol daun jambu
FI = Formula mengandung 15% ekstrak daun jambu bol - = Tidak ada hambatan
Sediaan gel ekstrak daun jambu bol memberikan daerah hambatan terhadap bakteri Staphylococcus aureus, Staphylococcus epidermidis dan Pseudomonas aeroginosa dengan diameter lebih besar dari 14. Menurut Ditjen POM RI (1995), suatu zat dikatakan memiliki daya hambat yang memuaskan bila diameter daerah hambatan 14 mm sampai 16 mm, sehingga dapat disimpulkan bahwa sediaan gel ekstrak daun jambu bol 15% memenuhi persyaratan.
yang menginaktifkan sistem enzim bakteri, sedangkan pada konsentrasi tinggi mampu merusak membran sitoplasma dan mengendapkan protein sel (Harborne, 1987; Volk dan Wheller, 1984).
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian yang dilakukan dapat disimpulkan bahwa :
a. Hasil uji aktivitas antibakteri daun jambu bol memberikan aktivititas bakteri yang efektif dalam menghambat pertumbuhan bakteri Staphylococcus aureus, Stapyhlococcus epidermidis dan Pseudomonas aeruginosa pada fraksi etil asetat yaitu pada konsentrasi 125 mg/ml dengan nilai diameter daerah hambat masing-masing adalah 14,96 mm; 15,23 mm; dan 14,36 mm, kemudian ekstrak etanol pada konsentrasi 150 mg/mL dengan nilai diameter daerah hambat masing-masing adalah 14,56 mm; 14,33 mm; dan 15,4 mm.
b. Ekstrak etanol daun jambu bol dapat diformulasikan dalam bentuk sediaan gel yang stabil dan efektif menghambat pertumbuhan bakteri.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi morfologi tumbuhan, sejarah tumbuhan, nama daerah tumbuhan, sistematika tumbuhan dan manfaat tumbuhan.
2.1.1 Morfologi tumbuhan
Jambu bol merupakan pohon yang tingginya 5 – 20 m, diameter pohonnya 20 – 45 cm. Perbungaan pada bagian ranting yang tidak berdaun, pendek dan menggerombol. Daun mahkota berbentuk lonjong sampai bundar telur, panjang 2 cm berwarna merah gelap. Daun berbentuk lonjong menjorong, agak tebal. Buah merupakan buah buni, berbentuk menjorong, berdiameter 5 – 8 cm, daging buah berwarna putih. Tiap buah hanya mempunyai satu biji (Verheij dan Coronel, 1991).
2.1.2 Sejarah tumbuhan
Jambu bol (Syzygium malaccense (L.) Merr & Perry) sudah dikenal luas di dunia dengan nama “Malay Apple”. Jambu bol termasuk family Myrtaceace dan genus Syzygium. Jambu bol diperkirakan berasal dari Malaysia, umumnya dibudidayakan mulai dari Jawa, Filipina, Vietnam, Bangladesh dan India Selatan (Morton, 1987).
2.1.3 Nama daerah
2.1.4 Sistematika tumbuhan
Sistematika dari tumbuhan pepaya adalah sebagai berikut: Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledonae Bangsa : Myrtales Suku : Myrtaceae Marga : Syzygium
Jenis : Syzygium malaccense (L.) Merr & Perry (Mulyana, 2015). 2.1.5 Manfaat tumbuhan
Jambu bol banyak manfaat bagi kesehatan tubuh, hal ini disebabkan karena kandungan gizi yang terdapat di dalamnya. Jambu bol dipercaya dapat mengatasi sembelit, diabetes, sakit kepala, batuk dan radang selaput lendir pada saluran napas. Sedangkan biji, kulit kayu dan daunnya memiliki sifat antibakteri dan memiliki efek terhadap tekanan darah dan pernapasan. Pada akar tanaman jambu bol memiliki manfaat untuk mengobati gatal-gatal (Anonim, 2014).
2.2 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Dengan diketahui senyawa aktif yang dikandung simplisia akan mempermudah pemilihan pelarut dengan cara ekstraksi yang tepat (Ditjen POM RI, 1995).
pengaruh cahaya matahari langsung (Ditjen POM RI, 1979).
Ekstraksi dengan menggunakan pelarut dapat dilakukan beberapa cara yaitu :
a. Cara dingin
1. Maserasi adalah cara penarikan simplisia dengan cara merendam serbuk simplisia tersebut dalam cairan penyari dengan beberapa kali pengocokkan atau pengadukan pada temperatur kamar, sedangkan remaserasi merupakan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama dan seterusnya (Ditjen POM RI, 2000).
2. Perkolasi ekstraksi dengan pelarut yang selalu baru sampai sempurna yang umumnya dilakukan pada temperatur ruangan. Proses terdiri dari tahapan pengembangan bahan, tahap maserasi antara dan tahap perkolasi sebenarnya (Ditjen POM RI, 2000).
b. Cara panas
1. Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan karena adanya pendingin balik (Ditjen POM RI, 2000).
2. Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur yang lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum dilakukan pada temperatur 40 – 500 C (Ditjen POM RI, 2000).
4. Infusa adalah sediaan cair yang dibuat dengan menyari simplisia nabati dengan air pada suhu 900 C selama 15 menit (Ditjen POM RI, 1979).
5. Dekok adalah sediaan cair yang dibuat dengan cara menyari simplisia dengan air bersuhu 900 C sambil diaduk berulang-ulang dengan pemanas air selama 30 menit (Voigt, 1984).
2.3 Fraksinasi
Proses pemisahan selanjutnya masih menggunakan prinsip ekstraksi yang dikenal dengan ekstraksi cair-cair atau yang biasa dikenal dengan nama fraksinasi. Fraksinasi adalah suatu metode pemisahan senyawa organik berdasarkan kelarutan senyawa-senyawa berdasarkan dua pelarut yang tidak saling bercampur, biasanya antara pelarut air dan pelarut organik (Dey, 2012).
Teknik pemisahan ekstraksi cair-cair ini biasanya dilakukan dengan menggunakan corong pisah. Kedua pelarut yang saling tidak bercampur tersebut dimasukkan ke dalam corong pisah, kemudian digojok dan didiamkan. Senyawa organik akan terdistribusi ke dalam fasenya masing-masing bergantung pada kelarutannya terhadap fase tersebut dan kemudian akan terbentuk dua lapisan, yaitu lapisan atas dan lapisan bawah yang dapat dipisahkan dengan membuka kunci pipa corong pisah (Odugbemi, 2008).
Aglikon pada umumnya terekstraksi pada fraksi non-polar seperti terpenoid dan steroid sedangkan flavonoid, glikosida, saponin dan gula ester ditemukan pada fraksi yang lebih polar dan fraksi air. Petroleum eter dan n-heksana juga dapat digunakan untuk menghilangkan lipid dan senyawa lemak (Dey, 2012).
2.4 Bakteri
2.4.1 Uraian umum
Nama bakteri berasal dari kata “bakterion” dari bahasa Yunani yang berarti tongkat atau batang, sekarang nama itu dipakai untuk menyebut sekelompok mikroorganisme yang bersel satu, berkembangbiak dengan pembelahan diri serta demikian kecilnya sehingga hanya tampak dengan mikroskop (Dwidjoseputro, 1978).
Menurut Waluyo (2010) morfologi bakteri dapat dibedakan atas tiga bagian yaitu :
a. Bacilli
Basil dari bacillus, merupakan bakteri yang mempunyai bentuk tongkat pendek/ batang kecil dan silindris. Sebagian bakteri berbentuk basil, yang dapat bergandeng-gandengan panjang, bergandeng-gandengan dua-dua atau terlepas satu sama lain. Berdasarkan jumlah koloni, basil dapat dibagi menjadi beberapa kelompok, yaitu :
- Monobasil (monobacillus), yakni basil yang hidup menyendiri atau tidak bergerombol.
b. Spiral
Spiral merupakan bakteri yang berbentuk bengkok atau berbengkok-bengkok seperti spiral. Bakteri yang berbentuk spiral sangat sedikit jumlahnya. Golongan ini merupakan golongan paling kecil jika dibandingkan dengan golongan basil dan golongan kokus.
c. Cocci/coccus
Kokus adalah bakteri yang berbentuk bulat seperti bola-bola kecil. Kelompok ini ada yang bergerombol dan bergandeng-gandengan membentuk koloni. Berdasarkan jumlah koloni, kokus dapat dibedakan menjadi beberapa kelompok, yaitu :
- Monokokus (monococcus), bila kokus hidup menyendiri.
- Diplokokus (diplococcus), bila kokus membentuk koloni terdiri dari dua kokus. - Streptococcus (streptococcus), bila koloni berbentuk rantai.
- Stafilokokus (staphylococcus), bila koloni bakteri kokus membentuk untaian seperti buah anggur.
- Sarsina (Sarcina), bila koloni bakteri mengelompok serupa kubus. - Tetrakokus (tetracoccus), bila koloni bakteri terdiri dari empat kokus. 2.4.2 Proses terjadinya infeksi pada kulit
Menurut Anhira (2011) proses berawal terjadinya infeksi pada kulit adalah : a. Bakteri masuk kedalam tubuh lewat jaringan kulit
b. Bakteri tersebut kemudian mengeluarkan toksin atau racun yang bisa membunuh sel-sel disektarnya
d. Secara otomatis, sel kulit akan menghalangi toksin tersebut menyebar dengan cara membentuk jaringan sehingga toksin tetap terkumpul disatu titik
e. Karena toksin ini mengumpul disatu titik kulit, maka terjadilah benjolan berisi nanah.
2.4.3 Bakteri yang memasuki tubuh melalui kulit
Kulit utuh adalah penghalang yang efektif yang mencegah banyak agen penginfeksi memperoleh jalan masuk ke tubuh. Akan tetapi, sepanjang kehidupan normal kulit tidak selalu utuh. Sobekan kulit yang begitu kecil sehingga tidak terlihat bisa memungkinkan bakteri masuk dan berlipat ganda. Beberapa organisme memasuki tubuh melalui kontak dengan kulit. Bakteri yang masuk melalui lecet kulit diantaranya Stapylococcus aureus, Staphylococcus epidermidis dan Pseudomonas aeruginosa (Volk dan Wheeler, 1984).
1. Staphylococcus aureus
Staphylococcus aureus adalah jenis kuman yang terutama menimbulkan penyakit pada manusia. Setiap jaringan ataupun alat tubuh dapat diinfeksi olehnya yang menyebabkan timbulnya penyakit dengan tanda-tanda yang khas yaitu, peradangan, nekrosis dan pembentukan abses (Staf Pengajar FK UI, 1994).
2. Staphylococcus epidermidis
Staphylococcus epidermidis merupakan bakteri gram positif, aerob atau aerob fakultatif, berbentuk bola atau kokus berkelompok tidak teratur, diameter 0,8 – 1,0 µm, tidak membentuk spora dan tidak bergerak, koloni berwarna putih. Bakteri ini tumbuh cepat pada suhu 370C. Koloni pada pembenihan padat berbentuk bulat halus, menonjol, berkilau, tidak menghasilkan pigmen, berwarna putih porselen sehingga Staphylococcus epidermidis disebut juga Staphylococcus alba (Jawetz, et al., 2001). Kuman ini terdapat pada kulit, selaput lendir, bisul dan luka (Dwijoseputro, 1978).
3. Pseudomonas aeruginosa
Pseudomonas aeruginosa merupakan bakteri berbentuk batang, ukurannya 0,6 x 2 µm. Merupakan bakteri gram negatif dan terlihat sebagai bentuk tunggal, ganda dan kadang-kadang dalam rantai pendek. Pseudomonas aeruginosa bersifat aerobik obligat yang tumbuh dengan cepat pada berbagai tipe media dan tumbuh baik pada suhu 37 – 420C (Brooks, et al., 2001). Organisme ini tidak membentuk sporula dan ditemukan baik sebagai bagian flora normal saluran usus maupun kulit manusia (Volk dan Wheeler, 1984).
2.5 Fase Pertumbuhan Mikroorganisme
Menurut Pratiwi (2008) ada empat macam fase pertumbuhan mikroorganisme, yaitu fase lag, fase log (fase esksponensial), fase stasioner dan fase kematian.
- Fase lag
sel, yang ada hanyalah peningkatan ukuran sel. Waktu penyesuaian ini umumnya berlangsung selama 2 jam. Kuman belum berkembang biak dalam fase ini, tetapi aktivitas metabolismenya sangat tinggi. Fase ini merupakan persiapan untuk fase berikutnya.
- Fase log (fase esksponensial)
Fase ini merupakan fase dimana mikroorganisme tumbuh dan membelah pada kecepatan maksimum, tergantung pada genetika mikroorganisme, sifat media, dan kondisi pertumbuhan. Sel baru terbentuk dengan laju konstan dan massa yang bertambah secara eksponensial. Hal yang dapat menghambat laju pertumbuhan adalah bila satu atau lebih nutrisi dalam kultur habis, sehingga hasil metabolisme yang bersifat racun akan tertimbun dan menghambat pertumbuhan bakteri. Hasil metabolisme bakteri yang bersifat racun dapat mengganggu pertumbuhan bakteri.
- Fase stationer
Pada fase ini pertumbuhan mikroorganisme berhenti dan terjadi keseimbangan antara jumlah sel yang membelah dengan jumlah sel yang mati, Pada fase ini terjadi akumulasi produk buangan yang toksik .
- Fase kematian
Pada fase ini jumlah sel yang mati meningkat. Konsentrasi produk buangan yang bersifat toksis meningkat dan ketersediaan makanan untuk bakteri menurun. Jumlah bakteri yang mati meningkat dengan cepat.
2.6 Pengukuran Aktivitas Antibakteri
dan metode dilusi cair. 1. Metode difusi agar
Metode yang paling sering digunakan adalah metode difusi agar. Cakram kertas saring berisi sejumlah tertentu obat ditempatkan pada permukaan medium padat yang sebelumnya telah diinokulasi bakteri uji pada permukaannya. Setelah inkubasi, diameter zona hambatan disekitar cakram dipergunakan mengukur kekuatan hambatan obat terhadap organisme uji (Brooks, et al., 2001).
2. Metode dilusi cair
Metode ini digunakan untuk mengukur kadar hambat minimum (KHM) dan kadar bunuh minimum (KBM). Cara yang dilakukan yaitu dengan membuat seri pengenceran agen antimikroba pada media cair yang telah ditambahkan dengan mikroba uji. Larutan uji agen antimikroba pada kadar terkecil yang terlihat jernih tanpa adanya pertumbuhan mikroba uji ditetapkan sebagai KHM. Larutan yang ditetapkan sebagai KHM tersebut selanjutnya dikultur ulang pada media cair tanpa penambahan mikroba uji ataupun agen antimikroba, dan diinkubasi selama 18 – 24 jam. Media yang tetap terlihat jernih setelah diinkubasi ditetapkan sebagai KBM (Pratiwi, 2008).
2.7 Uraian Gel
terdispersi dalam cairan (misalnya karbomer dan tragakan). Gel sistem dua fase, jika ukuran partikel dari fase terdispersi relatif besar, massa gel kadang-kadang dinyatakan sebagai magma (misalnya Magma Bentonit) (Ditjen, POM., 1995).
Keunggulan gel pada formulasi sediaan: 1. Waktu kontak lama
Kulit mempunyai barrier yang cukup tebal, sehingga dibutuhkan waktu yang cukup lama untuk zat aktif dapat berpenetrasi.
2. Kadar air dalam gel tinggi
Jumlah air yang banyak dalam gel akan menghidrasi stratum corneum sehingga terjadi perubahan permeabilitas stratum corneum menjadi lebih permeabel terhadap zat aktif yang dapat meningkatkan permeasi zat aktif.
3. Resiko timbulnya peradangan ditekan
Kandungan air yang banyak pada gel dapat mengurangi resiko peradangan lebih lanjut akibat menumpuknya lipida pada pori-pori, karena lipida tersebut merupakan makanan bakteri jerawat (Lieberman, 1997).
2.7.1 Hidroksipropil metilselulosa (HPMC)
HPMC merupakan turunan dari metil selulosa yang memiliki ciri-ciri serbuk atau butiran putih, tidak memiliki bau dan rasa, sangat sukar larut dalam eter, etanol atau aseton, dapat mudah larut dalam air panas dan akan segera menggumpal dan membentuk koloid. Mampu menjaga penguapan air sehingga secara luas banyak digunakan dalam aplikasi produk kosmetik dan aplikasi lainnya (Rowe, et al., 2006).
pembuatan sediaan farmasi dan kosmetik, khususnya untuk zat-zat yang tidak stabil atau tidak dapat larut dalam air. Propilen glikol adalah cairan bening, tidak berwarna, kental, hampir tidak berbau dan memiliki rasa manis sedikit tajam. Propilen glikol stabil dalam wadah yang tertutup baik dalam kondisi biasa, serta merupakan suatu zat kimia yang stabil bila dicampur dengan gliserin, air atau alkohol (Rowe, et al., 2006).
2.7.3 Metil paraben
Metil paraben memiliki ciri-ciri serbuk hablur halus, berwarna putih, hampir tidak berbau dan tidak mempunyai rasa kemudian agak membakar diikuti rasa tebal (Ditjen, POM., 1979). Metil paraben banyak digunakan sebagai pengawet dan antimikroba dalam kosmetik, produk makanan dan formulasi farmasi dan digunakan baik sendiri atau dalam kombinasi dengan paraben lain atau dengan antimikroba lain. Metil paraben adalah pengawet yang paling sering digunakan pada kosmetik,. Jenis paraben lainnya efektif pada kisaran pH yang luas dan memiliki aktivitas antimikroba yang kuat (Rowe, et al., 2006).
2.7.4 Propil paraben
BAB I PENDAHULUAN
1.1 Latar Belakang
Indonesia merupakan negara kepulauan yang mempunyai luas kurang lebih 35.000 pulau besar dan kecil dengan keanekaragaman jenis flora dan fauna yang sangat tinggi. Di Indonesia diperkirakan terdapat 100 sampai 150 familia tumbuh–tumbuhan dan dari jumlah tersebut sebagian besar mempunyai potensi untuk dimanfaatkan sebagai tanaman industri, rempah dan obat (Nurmalina, 2012).
Ramuan obat digunakan masyarakat sebagai salah satu alternatif pengobatan, diantaranya adalah tanaman daun jambu bol (Syzygium malaccense L. Merr & Perry) yang diduga dapat mengobati penyakit infeksi. Tanaman ini dimanfaatkan oleh masyarakat di desa Teluk Keijing Kota Sekayu, Sumatera Selatan, sebagai obat infeksi luka pada kulit. Penggunaan daunnya sebagai obat infeksi dengan cara menumbuk ataupun direbus, lalu air rebusan tersebut ditempelkan pada luka. Menurut penelitian Arifin dan kawan-kawan (2009) bahwa daun jambu bol memiliki khasiat sebagai antidiabetes dan hasil skrining fitokimia ekstrak daun jambu bol (Syzygium malaccense L. Merr & Perry) mengandung senyawa metabolit sekunder golongan alkaloid, flavonoid, tertepenoid/steroid, tanin, saponin.
Upaya untuk mengurangi resiko infeksi oleh bakteri Staphylococcus aureus, Staphylococcus epidermis dan Pseudomonas aeroginosa adalah dengan mengembalikan fungsi dari bagian tubuh yang terluka, mengurangi risiko terjadinya infeksi dengan cara melakukan beberapa tindakan dasar seperti mencuci tangan, membersihkan luka, membersihkan kulit disekitar luka, menutup luka, mengganti perban sesering mungkin dan pemakaian gel dari ramuan obat.
Sediaan topikal antibakteri telah banyak beredar di pasaran dalam bentuk krim, salep dan gel. Sediaan dalam bentuk gel lebih banyak digunakan karena bening, mudah mengering, membentuk lapisan film yang mudah dicuci dan memberikan rasa dingin dikulit. Gel mempunyai aliran pseudoplastik yaitu gel berbentuk padat apabila disimpan dan akan segera mencair bila dikocok. Sediaan gel mempunyai kadar air yang tinggi, sehingga dapat menghidrasi stratum corneum dan mengurangi resiko timbulnya peradangan lebih lanjut akibat menumpuknya minyak pada pori-pori (Gibson, 2001).
Hidroksipropil metilselulose (HPMC) adalah turunan selulosa eter semisintetik yang telah digunakan secara luas sebagai polimer hidrofilik dalam sistem pemberian obat oral dan topikal (Rogers, et al., 2009). Pemilihan basis HPMC dikarenakan penampakan gel jernih dan kompatibel dengan bahan-bahan lain, kecuali bahan-bahan yang oksidatif (Gibson, 2001) serta dapat mengembang terbatas dalam air sehingga merupakan bahan pembentuk hidrogel yang baik (Suardi, dkk., 2008).
Berdasarkan uraian di atas, maka dilakukan penelitian pembuatan sediaan gel dengan menggunakan ekstrak daun jambu bol dengan basis HPMC 3%, menguji aktivitas antibakteri dari ekstrak dan fraksi daun jambu bol dan menguji konstentrasi hambat minimum serta menguji sediaan gelnya terhadap bakteri Staphylococcus aureus, Staphylococcus epidermis dan Pseudomonas aeroginosa.
1.2 Perumusan Masalah
a. Apakah ekstrak dan fraksi daun jambu bol (Syzygium malacensse L. Merr & Perry) mempunyai aktivitas antibakteri terhadap bakteri Staphylococcus aureus, Staphylococcus epidermis dan Pseudomonas aeroginosa ?
b. Apakah ekstrak daun jambu bol (Syzygium malaccense L. Merr & Perry) dapat diformulasi dalam bentuk sediaan gel dan efektif sebagai obat infeksi pada kulit ?
1.3 Hipotesis
a. Ekstrak dan fraksi daun jambu bol dan sediaan gelnya mempunyai aktivitas antibakteri terhadap bakteri Staphylococcus aureus, Staphylococcus epidermis dan Pseudomonas aeroginosa.
b. Ekstrak daun jambu bol dapat diformulasi dalam bentuk sediaan gel dan efektif sebagai obat infeksi pada kulit.
1.4Tujuan Penelitian
gelnya terhadap bakteri Staphylococcus aureus, Staphylococcus epidermis dan Pseudomonas aeroginosa.
b. Untuk membuat sediaan gel dari ekstrak etanol daun jambu bol yang efektif.
1.5Manfaat Penelitian