Lampiran 1. Bagan kerja penelitian
1 g Serbuk sampel
Seduhan Teh Daun Sirsak Kemasan
Dimasukkan kedalam beaker glass, ditambahkan 100 ml air panas dan diletakkan diatas hot plate.
Didihkan.
Senyawa Flavonoid
Senyawa Polifenol Pemeriksaan Senyawa
Bersifat Antioksidan
Hasil
Lampiran 2. Data kemasan teh daun sirsak 2.1 K1: Kemasan
Nama Produk : Griya Herba Drink
Komposisi : Daun Sirsak (Annona muricata folium) Isi : 40 g (20 x 2 g)
Produksi : UD. Herba Sari Sukoharjo – Indonesia untuk CV. Griya Herba Semarang – Indonesia No. Registrasi : P.IRT No. 810331114343
Tgl. Produksi : 19 Januari 2016 Exp. Date : 19 Januari 2018
2.2 K2: Kemasan 2
Nama Produk : Teh Herbal Celup Laurico Daun Sirsak (Soursop leaf bag) Komposisi : Daun Sirsak (Annona muricata folium)
Isi : 50 g (25 x 2 g)
Produksi : PT. Palma Natura Sanat Depok – Jawa Barat No. Registrasi : Dinkes P.IRT No. 81327603115
Tgl. Produksi : -
Exp. Date : 28 November 2016 No. Batch : 1056
2.3 K3: Kemasan 3
Nama Produk : Gravila Teh Celup Daun Sirsak
Komposisi : Daun Sirsak (Annona muricata folium) Isi : 50 g (25 x 2 g)
Produksi : CV. Permana Putra Mandiri Jakarta - Indonesia No. Registrasi : Dinkes P.IRT No. 310321301554
Tgl. Produksi : -
Lampiran 3. Gambar kantongan dan serbuk teh daun sirsak.
Gambar 1. Kantongan dan serbuk teh daun sirsak K1
Gambar 2. Kantongan dan serbuk teh daun sirsak K2
Lampiran 4. Gambar seperangkat alat spektrofotometer UV-Visibel (UV 1800 - Shimadzu)
Lampiran 5. Perhitungan Pembuatan larutan blanko DPPH 0,5 mM
0,5 mM = mg
394,32 g/mol�
1000 100 ��
mg = 19,716 mg≈ 20 mg
Jadi, serbuk DPPH yang ditimbang adalah 20 mg untuk membuat larutan blanko DPPH 0,5 mM didalam volume 100 ml.
M = g
�� �
1000
Lampiran 6. Hasil Pengukuran Operating Time 6.1 Hasil Pengukuran Operating Time Tanpa Sampel.
Lampiran 7. Pemeriksaan senyawa Flavonoid dan Polifenol
1. Pemeriksaan Senyawa Flavonoid 2. Pemeriksaan Senyawa Polifenol
Identifikasi senyawa flavonoid K1 Identifikasi senyawa polifenol K1
Identifikasi senyawa flavonoid K2 Identifikasi senyawa polifenol K2
Lampiran 8. Hasil uji aktivitas antioksidan
5.1 Tabel hasil uji aktivitas antioksidan STDSK K1. Larutan
Uji
Konsentrasi (ppm)
Absorbansi % Pemerangkapan
I II III I II III
Rata-5.2 Tabel hasil uji aktivitas antioksidan STDSK K2. Larutan
Uji
Konsentrasi (ppm)
Absorbansi % Pemerangkapan
I II III I II III
Rata-5.3 Tabel hasil uji aktivitas antioksidan STDSK K3. Larutan
Uji
Konsentrasi (ppm)
Absorbansi % Pemerangkapan
Rata-Lampiran 9. Contoh perhitungan persen pemerangkapan dan perhitungan nilai IC50
9.1 Perhitungan persen pemerangkapan STDSK K1. Tabel data absorbansi DPPH pengukuran 1
No. Konsentrasi Larutan Uji (ppm) Absorbansi
1 0 0,846
Keterangan : Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
1. Konsentrasi 500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,846
0,736 -0,846
= 13,00
2. Konsentrasi 1000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,846
0,614 -0,846
= 27,42
3. Konsentrasi 1500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,846
0,509 -0,846
= 33,70
4. Konsentrasi 2000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,846
0,399 -0,846
= 44,70
5. Konsentrasi 2500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,846
0,267 -0,846
= 68,44
6. Konsentrasi 3000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,846
0,169 -0,846
= 80,02.
• Tabel data absorbansi DPPH pengukuran 2
No. Konsentrasi Larutan Uji (ppm) Absorbansi
1 0 0,844
Keterangan : Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
1. Konsentrasi 500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,844
0,731 -0,844
= 13,39
2. Konsentrasi 1000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,844
0,610 -0,844
= 27,73
3. Konsentrasi 1500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,844
0,510 -0,844
= 39,57
4. Konsentrasi 2000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,844
0,400 -0,844
= 52,61
5. Konsentrasi 2500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,844
0,270 -0,844
= 68,01
6. Konsentrasi 3000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,844
0,166 -0,844
= 80,33
• Tabel data absorbansi DPPH pengukuran 3
No. Konsentrasi Larutan Uji (ppm) Absorbansi
1 0 0,847
Keterangan : Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
1. Konsentrasi 500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,848
0,742 -0,847
= 12,40
2. Konsentrasi 1000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,848
0,618 -0,847
= 27,04
3. Konsentrasi 1500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,848
0,508 -0,847
= 40,02
4. Konsentrasi 2000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,848
0,398 -0,847
= 53,01
5. Konsentrasi 2500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,848
0,263 -0,847
= 68,95
6. Konsentrasi 3000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,848
0,172 -0,847
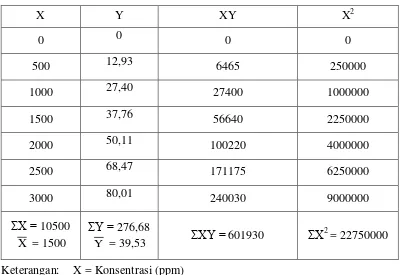
Perhitungan nilai IC50 Keterangan: X = Konsentrasi (ppm)
Y = % Pemerangkapan
Jadi, persamaan garis regresi Y = 0,026x – 0,526 Nilai IC50 = Y = 0,026x – 0,535
50 = 0,026x – 0,535 X = 1943
9.2 Contoh perhitungan persen pemerangkapan STDSK K2
• Tabel data absorbansi DPPH pengukuran 1
No. Konsentrasi Larutan Uji (ppm) Absorbansi
1 0 0,880
Keterangan : Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
1. Konsentrasi 500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,880
0,760 -0,880
= 13,63
2. Konsentrasi 1000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,880
0,656 -0,880
= 25,45
3. Konsentrasi 1500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,880
0,540 -0,880
= 38,64
4. Konsentrasi 2000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,880
0,409 -0,880
= 53,52
5. Konsentrasi 2500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,880
0,360 -0,880
= 59,09
6. Konsentrasi 3000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,880
0,249 -0,880
= 71,70
• Tabel data absorbansi DPPH pengukuran 2
No. Konsentrasi Larutan Uji (ppm) Absorbansi
1 0 0,877
Keterangan : Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
1. Konsentrasi 500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,877
0,753 -0,877
= 14,14
2. Konsentrasi 1000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,877
0,628 -0,877
= 28,39
3. Konsentrasi 1500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,877
0,545 -0,877
= 37,86
4. Konsentrasi 2000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,877
0,406 -0,877
= 53,71
5. Konsentrasi 2500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,877
0,365 -0,877
= 58,38
6. Konsentrasi 3000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,877
0,253 -0,877
= 71,15
• Tabel data absorbansi DPPH pengukuran 3
No. Konsentrasi Larutan Uji (ppm) Absorbansi
1 0 0,874
Keterangan : Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
1. Konsentrasi 500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,874
0,746 -0,874
= 14,65
2. Konsentrasi 1000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,874
0,600 -0,874
= 31,35
3. Konsentrasi 1500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,874
0,550 -0,874
= 37,07
4. Konsentrasi 2000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,874
0,403 -0,874
= 53,89
5. Konsentrasi 2500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,874
0,370 -0,874
= 57,67
6. Konsentrasi 3000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,874
0,257 -0,874
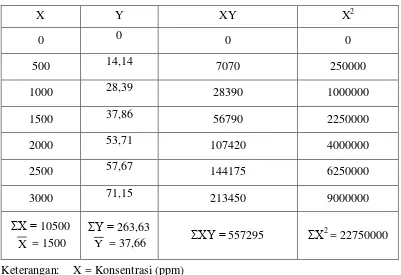
Perhitungan nilai IC50 Keterangan: X = Konsentrasi (ppm)
Y = % Pemerangkapan
Jadi, persamaan garis regresi Y = 0,023x + 2,601
Nilai IC50 = Y = 0,023x + 2,601 50 = 0,023x + 2,601
X = 2287
9.3 Contoh perhitungan persen pemerangkapan STDSK K3
• Tabel data absorbansi DPPH pengukuran 1
No. Konsentrasi Larutan Uji (ppm) Absorbansi
1 0 0,802
Keterangan : Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
1. Konsentrasi 500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,802
0,729 -0,802
= 9,10
2. Konsentrasi 1000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,802
0,628 -0,802
= 21,69
3. Konsentrasi 1500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,802
0,541 -0,802
= 32,54
4. Konsentrasi 2000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,802
0,480 -0,802
= 40,15
5. Konsentrasi 2500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,802
0,380 -0,802
= 52,61
6. Konsentrasi 3000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,802
0,279 -0,802
= 65,21
• Tabel data absorbansi DPPH pengukuran 2
No. Konsentrasi Larutan Uji (ppm) Absorbansi
1 0 0,803
Keterangan : Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
1. Konsentrasi 500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,803
0,724 -0,803
= 9,84
2. Konsentrasi 1000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,803
0,638 -0,803
= 20,55
3. Konsentrasi 1500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,803
0,550 -0,803
= 31,51
4. Konsentrasi 2000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,803
0,477 -0,803
= 40,60
5. Konsentrasi 2500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,803
0,370 -0,803
= 53,92
6. Konsentrasi 3000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,803
0,284 -0,803
= 64,63
• Tabel data absorbansi DPPH pengukuran 3
No. Konsentrasi Larutan Uji (ppm) Absorbansi
1 0 0,805
Keterangan : Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel
1. Konsentrasi 500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,805
0,720 -0,805
= 9,83
2. Konsentrasi 1000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,805
0,648 -0,805
= 19,50
3. Konsentrasi 1500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,805
0,564 -0,805
= 29,93
4. Konsentrasi 2000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,805
0,474 -0,805
= 41,11
5. Konsentrasi 2500 ppm
Aktivitas pemerangkapan (%) = x 100% 0,804
0,380 -0,805
= 55,28
6. Konsentrasi 3000 ppm
Aktivitas pemerangkapan (%) = x 100% 0,804
0,289 -0,805
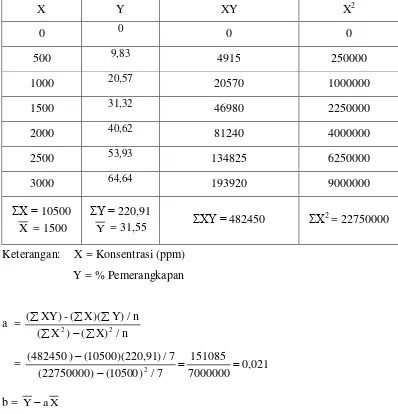
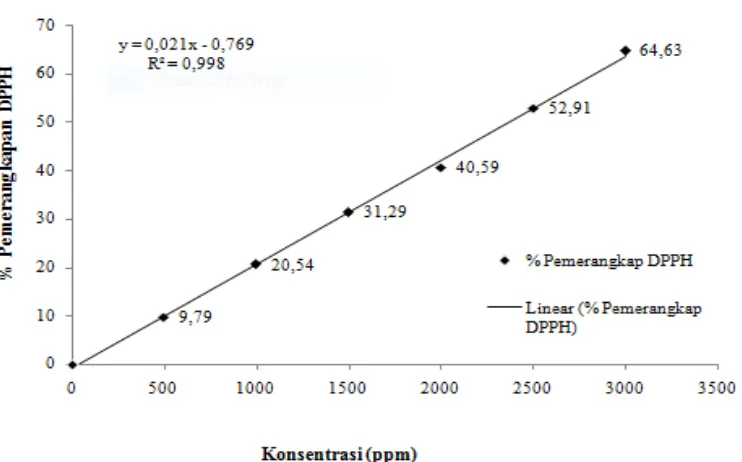
Perhitungan nilai IC50 Keterangan: X = Konsentrasi (ppm)
Y = % Pemerangkapan
Jadi, persamaan garis regresi Y = 0,021x – 0,05
Nilai IC50 = Y = 0,021x – 0,05 50 = 0,021x – 0,769
X = 2383
DAFTAR PUSTAKA
Adri, Delvi Dan Wikanastri Hesolisstyiorini. (2013). Aktivitas Antioksidan dan Sifat Organoleptik Teh Daun Sirsak ( Annona Muricata Linn )Berdasarkan Variasi Lama Pengeringan. Jurusan Teknologi Pangan. Fakultas Pertanian. Universitas Muhammadiyah Semarang. Semarang. Vol. 04 No 7 Tahun 2013. Halaman 1-4.
Budiarti, A., dkk. (2014). Aktivitas Antioksidan Fraksi Kloroform Ekstrak Etanol Daun Sirsak (Annona muricata L.) dan Identifikasi Kandungan Senyawa Kimianya. Jurusan Farmasi. Fakultas Farmasi. Universitas Wahid Hasyim Semarang. Prosiding SNST ke-5 Tahun 2014. Halaman 1; 4-5.
Cholisoh, Z. 2008. Aktivitas Penangkap Radikal Ekstrak Etanol 70% Biji Jengkol (Archidendron jiringa). Jurnal Fakultas Farmasi Universitas Muhamadiyah Surakarta. Halman 1-12
Daroini, O.S. (2006). Kajian Proses Pembuatan The Herbal Dari Campuran The Hijau (Camelia sinensis), Rimpang Bangle (Zingiber cassumunar Roxb.) dan Daun Ceremai (Phyllantus acidus (L.) Skeels). Fakultas Teknologi Pertanian IPB. Halaman 12.
Ditjen POM. (1979). Farmakope Indonesia. Edisi Ketiga. Jakarta: Depkes. Halaman 32.
Ditjen POM. (1995). Farmakope Indonesia. Edisi Keempat. Jakarta: Departemen Kesehatan RI. Halaman 796.
Fessenden, R. J., dan Fessenden, J. S. (1986). Organic Chemistry: Diterjemahkan oleh Pudjaatmakan, A.H. Kimia Organik. Edisi Ketiga. Jakarta: Penerbir Erlangga. Halaman 229-232.
Gandjar, I. G., dan Rohman, A. (2008). Kimia Farmasi Analisis. Cetakan Ketiga. Yogyakarta: Pustaka Pelajar. Halaman 222, 254-255.
Handayani, H., et al,. (2016). Ekstraksi Antioksidan Daun Sirsak Metode Ultrasonic Bath (Kajian Rasio: Pelarut dan Lama Ekstraksi). Jurusan Teknologi Hasil Pertanian, Universitas Brawijaya, Malang. Jurnal Pangan dan Agroindustri vol. 4 No. 1 Halaman: 262-272.
Harun, N., et al,. (2014). Penerimaan Panelis terhadap The Herbal Dari kulit Buah Manggis (Garcinia mangostana L.) Dengan Perlakuan Suhu Pengeingan. Universitas Riau Pekan Baru, Program Studi Teknologi Hasil Pertanian. ISSN Vol. 13 No. 2. Halaman: 7-18.
Pertanian, Fakultas Pertanian & LPPM UPN Veteran Jawa Timur. Halaman 1-8.
Mardiana L., et al,. (2013). Ramuan dan Khasiat Sirsak. Jakarta: Niaga Swadaya. Halaman 24-25.
Markham, K.R. (1988). Cara Mengidentifikasi Flavinoid. Bandung: Penerbit ITB. Halaman 10, 15, 38.
Molyneux, P. (2004). The Use of the Stable Free Radical Diphenylpicrylhydrazyl (DPPH) for Estimating Antioxidant Activity. Songklanakarin J. Sci. Technol. 26(2): 211-219.
Nihlati A.I., et al,. (2013). Daya Antioksidan Ekstrak Etanol Rimpang Temu Kunci (Boesenbergia pandurata (Roxb.) Schlecth) Dengan Metode Penangkapan Radikal DPPH (1,1-difenil-2-pikrilhidrazil). Fakultas Farmasi Universitas Gadjah Mada, Yogyakarta. Halaman 1-8.
Prakash, A., et al,. (2001). Antioxidant Activity. Medallion Laboratories-Analytical Progress. 19(2): 2.
Prtasetyorini, dkk., (2014). Potensi Antioksidan Berbagai Sediaan Buah Sirsak (Annona muricata Linn). Fakultas MIPA Universitas Pakuan Bogor. Panel Gizi Makan. Hol. 37 (2): Halaman: 137-144.
Ridho, E.A., et al., (2013). Uji Aktivitas Antioksidan Ekstrak Metanol Buah Lakum Dengan Metode DPPH. Program Studi Farmasi Fakultas Kedokteran, Universitas TanjungPura, Pontianak. Halaman
Rosidah, Yam, M.F., Sadikun, A., dan Asmawi, M.Z. (2008). Antioxidant Potential of Gynura procumbens. Pharmaceutical Biology. 46(9): 616-625. Salamah, N dan Erlinda W., (2015). Aktivitas Antioksidan Ekstrak Metanol Daun Kelengkeng Dengan Metode DPPH. Fakultas Farmasi Universitas Ahmad Dahlan, Yogyakarta. Pharmaciana, vol 5, No. 1, 2015: 25-34.
Satria, M.D. 2013. Uji Aktivitas Antioksidan Ekstrak n-Heksan dengan Metode DPPH (2,2-Difenil-1-pikrilhidrazil). Skripsi. Halaman 1-10.
Silalahi, J. (2006). Makanan Fungsional. Yogyakarta: Kanisius. Halaman 41, 47-48, 121.
Sirait, M. (2007). Penuntun Fitokimia dalam Farmasi. Bandung: Penerbit ITB. Halaman 129.
Winarsi, H. (2007). Antioksidan Alami dan Radikal Bebas. Yogyakarta: Kanisius. Halaman 12, 17.
Winarsi, H. (2014). Antioksidan Daun Kapulaga. Yogyakarta: Graha Ilmu. Halaman 38, 42-43.
Zuhra, C.F., et al,. (2008). Aktivitas Antioksidan Senyawa Flavonoid Dari Daun Katuk (Sauropus androgunus (L) Merr.). Departemen Kimia FMIPA USU Jurnal Biologi Sumatera Vol 3 No. 1. Halaman: 7-10
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan secara deskriptif. Penelitian meliputi pemeriksaan senyawa flavonoid dan polifenol serta pengujian aktivitas antioksidan dari masing-masing STDSK dengan metode aktivitas pemerangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazyl) yang diukur secara spektrofotometri visibel. Penelitian ini dilakukan di Laboratorium Penelitian Fakultas Farmasi, Universitas Sumatera Utara pada bulan Maret 2016 – Juni 2016.
3.1 Sampel
Pengambilan sampel dilakukan secara purposif yaitu pengambilan sampel dengan pertimbangan khusus sehingga layak dijadikan sampel. Sampel yang digunakan adalah sampel teh daun sirsak kemasan (Annona muricata Linn.) sebanyak 3 merek kemasan yaitu K1, K2, dan K3 yang berasal dari toko obat Hasan AS Jalan Letkol Iskandar No. 18 Ilir Barat 2 Palembang Sumatera Selatan. 3.2 Alat
Alat-alat yang digunakan pada penelitian ini terdiri dari alat-alat gelas laboratorium, neraca analitik (Boeco Germany), hot plate, vortex, spektrofotometer UV-Visible (Shimadzu UV-1800), dan stopwatch.
3.3 Bahan
suling.
3.4 Pembuatan Pereaksi
3.4.1 Pereaksi Besi (III) Klorida 1%
Sebanyak 1 g besi (III) klorida ditimbang, kemudian dilarutkan dalam air secukupnya hingga diperoleh larutan 100 ml (Ditjen RI, 1995).
3.5 Pemeriksaan Senyawa Antioksidan 3.5.1 Pemeriksaan Senyawa Flavonoid
Sebanyak 10 g serbuk simplisia ditambahkan 10 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, kedalam 5 ml filtrat ditambahkan 0,1 g serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika terjadi warna merah atau kuning atau jingga pada lapisan amil alkohol (Adri, 2013).
3.5.2 Pemeriksaan Senyawa Polifenol
5 ml minuman teh daun sirsak dimasukkan ke dalam tabung reaksi. Ditambahkan 5 tetes larutan FeCl3 1% dan dikocok kuat. Terbentuknya warna biru kehitaman atau hitam pekat setelah penambahan FeCl3 1% menunjukkan adanya senyawa fenolik (Adri, 2013 ).
3.6 Uji Aktivitas Antioksidan Metode Pemerangkapan DPPH 3.6.1 Prinsip metode DPPH (1,1 Diphenyl-2-picrylhydrazyl)
3.6.2 Pembuatan larutan blanko DPPH 0,5 mM
Timbang 20 mg DPPH (1,1-diphenyl-2-picrylhydrazyl) kemudian dilarutkan dalam methanol hingga volume 100 ml (Molyneux, 2004).
3.6.3 Pembuatan Larutan blanko C = 40 ppm
Larutan DPPH 0,5 mM dipipet sebanyak 5 ml, kemudian dimasukkan ke dalam labu tentukur 25 ml, lalu dicukupkan volumenya dengan metanol sampai garis tanda untuk mendapatkan konsentrasi 40 ppm (Molyneux, 2004).
3.6.4 Pengukuran panjang gelombang serapan maksimum DPPH
Larutan DPPH konsentrasi 40 ppm dihomogenkan dengan vortex dan diukur serapannya pada panjang gelombang 400-750 nm yang merupakan panjang gelombang sinar tampak (Gandjar, 2008).
3.6.5 Pembuatan larutan induk seduhan teh daun sirsak kemasan
Ditimbang sebanyak 1 g sampel uji, ditambahkan 100 ml air panas, kemudian diletakkan diatas hotplate, lalu didihkan. (Adri, 2013).
3.6.6 Pembuatan seduhan teh daun sirsak kemasan (STDSK)
3.6.7 Analisis persen pemerangkapan radikal bebas
Penentuan persen pemerangkapan radikal bebas dihitung dengan rumus sebagai berikut:
Aktivitas pemerangkapan radikal bebas (%) = x 100% kontrol
A
sampel A
-kontrol A
Keterangan: Akontrol = Absorbansi tidak mengandung sampel Asampel = Absorbansi sampel (Rosidah, 2008). 3.6.8 Analisis nilai IC50
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil pemeriksaan golongan senyawa flavonoid dan polifenol
Gambar hasil pemeriksaan golongan senyawa flavonoid dan senyawa polifenol pada masing-masing sampel uji STDSK dapat dilihat pada lampiran 7 halaman 48. Masing-masing sampel uji STDSK mengandung golongan senyawa flavonoid dan senyawa polifenol yang memiliki sifat sebagai antioksidan, hasil pemeriksaan golongan senyawa flavonoid dan senyawa polifenol tersebut dapat di lihat pada tabel 4.1 dibawah ini:
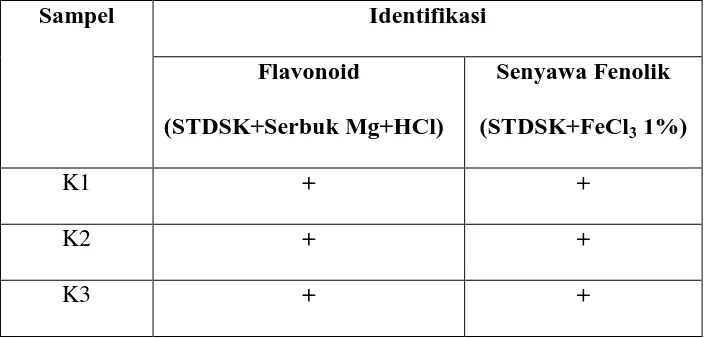
Tabel 4.1 Hasil Identifikasi secara kualitatif seduhan teh daun sirsak pada masing-masing kemasan.
Sampel Identifikasi
Flavonoid
(STDSK+Serbuk Mg+HCl)
Senyawa Fenolik (STDSK+FeCl3 1%)
K1 + +
K2 + +
K3 + +
Keterangan: (+) Positif : mengandung golongan senyawa 4.2 Hasil pengujian aktivitas antioksidan
4.2.1 Hasil penentuan panjang gelombang serapan maksimum
Visibel. Data hasil pengukuran panjang gelombang maksimum dapat dilihat pada Gambar 4.1 berikut ini:
Gambar 4.1 Kurva Serapan Maksimum Larutan DPPH ( 1,1-diphenyl-2-picrylhydrazyl) 40 ppm Dalam Metanol Menggunakan Spektrofotometer UV-Visibel.
Hasil pengukuran menunjukkan bahwa larutan DPPH ( 1,1-diphenyl-2-picrylhydrazyl) 40 ppm dalam metanol menghasilkan serapan maksimum pada panjang gelombang 516 nm. Panjang gelombang 516 nm, termasuk dalam kisaran panjang gelombang sinar tampak 400-800 nm (Gandjar, 2008), serta termasuk dalam rentang panjang gelombang DPPH (1,1-diphenyl-2-picrylhydrazyl) yang berkisar antara 515-520 nm (Molyneux, 2004).
4.2.2 Hasil analisis waktu pengukuran (operating time)
1,1-diphenyl-2-picrylhydrazyl) 0,5 mM dalam metanol dengan konsentrasi 40 ppm dan menggunakan sampel pada masing-masing STDSK dengan konsentrasi 500 ppm ditambahkan dengan 5 ml larutan DPPH (1,1-diphenyl-2-picrylhydrazyl) 0,5 mM dalam metanol, diukur selama 80 menit, menunjukkan bahwasanya pada mulai menit ke 60 masing-masing perlakuan sudah menunjukkan kestabilan dalam meredam radikal bebas. Menurut Salamah (2015), waktu operasional merupakan waktu pengukuran saat larutan menyerap sinar dengan serapan yang stabil. Serapan yang stabil ini menunjukkan bahwa DPPH ( 1,1-diphenyl-2-picrylhydrazyl) telah bereaksi optimal dengan senyawa uji. Hasil analisis waktu pengukuran (operating time) dapat dilihat pada lampiran halaman
4.2.3 Hasil analisis aktivitas antioksidan STDSK
Tabel 4.2 Penurunan absorbansi dan persen pemerangkapan DPPH oleh masing-masing STDSK
Larutan Uji
Konsentrasi (ppm)
Absorbansi % Pemerangkapan
I II III I II III
Rata-rata
K1 Blanko 0,846 0,844 0,847 0 0 0 0
500 0,736 0,731 0,742 13,00 13,39 12,40 12,93 1000 0,614 0,610 0,618 27,42 27,73 27,04 27,40 1500 0,509 0,510 0,508 33,70 39,57 40,02 37,76 2000 0,399 0,400 0,398 44,70 52,61 53,01 50,12 2500 0267 0,270 0,263 68,44 68,01 68,95 68,47 3000 0,169 0,166 0,172 80,02 80,33 79,69 80,01
K2 Blanko 0,880 0,877 0,874 0 0 0 0
500 0,760 0,753 0,746 13,63 14,14 14,65 14,14 1000 0,656 0,628 0,600 25,45 28,39 31,35 28,39 1500 0,540 0,545 0,550 38,64 37,86 37,07 37,85 2000 0,409 0,406 0,403 53,52 53,71 53,89 53,70 2500 0,360 0,365 0,370 59,09 58,38 57,67 58,38 3000 0,249 0,253 0,257 71,70 71,15 70,59 71,15
K3 Blanko 0,802 0,803 0,804 0 0 0 0
500 0,729 0,724 0,720 9,10 9,83 10,44 9,79 1000 0,628 0,638 0,648 21,69 20,54 19,40 20,54 1500 0,541 0,550 0,564 32,54 31,50 29,85 31,29 2000 0,480 0,477 0,474 40,14 40,59 41,04 40,59 2500 0,380 0,370 0,360 52,61 53,92 55,22 52,91 3000 0,279 0,284 0,289 65,21 64,63 64,05 64,63
kepada DPPH (1,1-diphenyl-2-picrylhydrazyl) sehingga atom dengan elektron yang tidak berpasangan mendapat pasangan elektron dan tidak lagi menjadi radikal (Silalahi, 2006).
Tabel 4.3 Hasil persamaan regresi linier dan hasil analisis IC50 (ppm) yang diperoleh dari masing-masing STDSK
Larutan Uji Persamaan regresi IC50 (ppm)
STDSK K1 y = 0,027x – 0,301 1943
STDSK K2 y = 0,023x + 1,978 2287
STDSK K3 y = 0,021x - 0,769 2383
Hasil perbandingan analisis IC50 (ppm) pada larutan uji STDSK masing-masing kemasan dapat dilihat pada gambar 4.5 dibawah ini:
Gambar 4.5 Grafik hasil analisis IC50 (ppm) yang diperoleh dari larutan uji STDSK masing-masing.
yang berikatan dengan senyawa tersebut dapat menurunkan aktivitas antioksidan. Aktivitas antioksidan akan meningkat dengan bertambahnya gugus hidroksil dan akan menurun dengan adanya gugus glikosida, dan dapat pula diduga karena glikosida flavonoid dalam bentuk aglikon yang bersifat non-polar memiliki aktivitas antioksidan yang lebih tinggi jika dibandingkan dengan bentuk glikonnya yang bersifat polar (Ridho 2013; Satria, 2013).
Tabel 4.4 Kategori nilai IC50 sebagai antioksidan
No. Kategori Konsentrasi (ppm)
1. Sangat kuat ≤ 50
2. Kuat 50 – 100
3. Sedang 101 – 150
4. Lemah ≥ 150
Sumber: Winarsi, 2014.
3132
menit ke-30 yaitu sebesar 117,86 ppm dan yang tertinggi pada menit ke-150 yaitu sebesar 82,16 ppm. Hasil perbandingannya dapat di lihat pada Gambar 4.6 grafik berikut ini:
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat disimpulkan: a. Hasil pemeriksaan golongan senyawa flavonoid dan polifenol sediaan
teh daun sirsak kemasan menunjukkan adanya kandungan golongan senyawa yang memiliki aktivitas sebagai antioksidan..
b. Hasil analisis antioksidan menunjukkan bahwa masing-masing STDSK memiliki aktivitas antioksidan dan nilai IC50 masing-masing STDSK adalah K1 sebesar 1943 ppm, K2 sebesar 2287 ppm, dan K3 sebesar 2383 ppm dan termasuk dalam kategori sangat lemah.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Sirsak
Sirsak merupakan tanaman buah yang dapat tumbuh dan berkembang dengan baik di dataran rendah sampai daerah berketinggian 500 meter dari permukaan laut (mdpl). Tanaman sirsak akan tumbuh dengan baik di daerah beriklim basah sampai daerah kering bersuhu 22-28oC, kelembapan udara (RH) 60-80%, dan curah hujan berkisar antara 1.500-2.500 mm/ tahun. Berbeda dengan tanaman buah pada umumnya, manfaat sirsak bagi kesehatan tidak hanya terletak pada daging buahnya. Namun khasiat sirsak tersebar ke bagian daunnya (Zuhud, 2011).
Dalam sistematika tumbuhan (taksonomi), tanaman sirsak diklasifikasikan sebagai anggota famili Annonaceae dengan nama ilmiah A. macrocarpa, A. bonplandiana, A. cearensis, dan Guanabanus muricatus. Tanaman sirsak berkerabat dekat dengan srikaya (Annona squamosa Linn) (Mardiana, 2013).
Daun sirsak merupakan bagian yang banyak mengandung zat di antaranya annocatalin, annohexocin, annonacin, annomuricin, annomurine, caclourine,
Daun sirsak memiliki panjang 6-18 cm, lebar 3-7 cm, betekstur kasar, berbentuk bulat telur terbalik bentuk eliptik, ujungnya lancip pendek, daun bagian atas mengilap hijau dan gundul pucat kusam di bagian bawah daun, berbentuk lateral saraf. Daun sirsak memiliki bau tajam menyengat dengan tangkai daun pendek sekitar 3-10 mm. Daun sirsak nomor 4 sampai 5 dari pucuk memiliki kandungan acetogenins tertinggi. Daun sirsak yang terlalu muda belum banyak mengandung acetogenins yang terbentuk, sedangkan kandungan acetogenins pada daun yang terlalu tua sudah mulai rusak sehingga kadarnya berkurang (Zuhud, 2011).
2.2 Teh
Teh adalah minuman yang paling banyak dikonsumsi oleh manusia sesudah air putih, dalam jumlah kira-kira 120 ml/ kapita per hari (Silalahi, 2006).
Teh herbal merupakan istilah umum yang digunakan untuk minuman yang bukan berasal dari tanaman teh (Camelia sinensis). Pengertian teh herbal sudah umum dikalangan masyarakat, sehingga masyarakat sudah menggunakan kata “teh” untuk minuman yang bukan berasal dari daun teh (Camelia sinensis). Teh herbal adalah sebutan untuk ramuan bunga, daun, biji, akar atau buah kering untuk membuat minuman yang juga disebut teh herbal (Harun, 2014).
pengemasan. Kondisi proses tersebut harus diperhatikan untuk menghindari hilangnya zat-zat penting yang berkhasiat dari bahan segar (Daroini, 2011).
Berbagai herbal atau tanaman obat sebenarnya dapat diolah menjadi herbal kering. Pada dasarnya, proses pengolahan semua jenis tanaman obat hampir sama. Biasanya, perbedaan terletak pada lama dan suhu pengeringan karena disesuaikan dengan karakteristik bahan segar. Herbal-herbal kering tersebut selanjutnya dicampur dengan komposisi tertentu sesuai dengan jenis teh herbal yang akan dihasilkan (Daroini, 2011).
Teh dapat dikelompokkan dalam tiga jenis, yaitu teh hijau (tidak difermentasikan), teh oolong (semi fermentasi), dan teh hitam (fermentasi penuh). Teh hijau dibuat melalui inaktivasi enzim polifenol oksidasenya didalam teh segar. Metode inaktivasi enzim polifenol oksidase teh hijau dapat dilakukan melalui pemanasan (udara panas) dan penguapan (steam/ uap air). Kedua metode itu berguna untuk mencegah terjadinya oksidasi enzimatis katekin. Teh hitam dibuat melalui oksidasi katekin dalam daun segar dengan katalis polifenol oksidase atau disebut dengan fermentasi. Proses fermentasi ini dihasilkan dalam oksidasi polifenol sederhana, yaitu katekin teh diubah menjadi molekul yang lebih kompleks dan pekat sehingga memberi ciri khas teh hitam, yaitu berwarna, kuat, dan berasa tajam. Teh oolong diproses melalui pemanasan daun dalam waktu singkat setelah penggulungan. Oksidasi terhenti dalam proses pemanasan, sehingga teh oolong disebut dengan teh semifermentasi. Karakteristik teh oolong berada diantara teh hitam dan teh hijau (Syah, 2006).
2.3 Radikal Bebas
elektron dengan jumlah yang ganjil (gassal, tidak genap). Karena jumlah elektron ganjil, maka tidak semua elektron dapat berpasangan. Meskipun suatu radikal bebas tidak bermuatan positif atau negatif, spesi semacam ini sangat reaktif karena adanya elektron yang tidak berpasangan. Suatu radikal bebas biasanya dijumpai sebagai zat antara yang tak dapat diisolasi dan berenergi tinggi (Fessenden, 1982).
Radikal bebas sangat berbahaya karena dapat mencuri elektron dari senyawa lain seperti seperti protein, lipid, karbohidrat, dan sangat mudah menyerang sel-sel yang sehat di dalam tubuh. Radikal bebas dapat dihasilkan dari metabolisme tubuh dan faktor eksternal seperti asap rokok. Hasil penyinaran ultra violet, zat kimia dalam makanan dan polutan lain (Hutahaean, 2011)
Menurut Fessenden (1982), mekanisme reaksi radikal bebas paling tepat dibayangkan sebagai suatu deret reaksi-reaksi bertahap, tiap tahap termasuk pada salah satu kategori berikut:
a. Inisiasi
Inisiasi adalah pembentukan awal radikal-radikal bebas. Dalam klorinasi metana, tahap inisiasi adalah pematahan (cleavage) homolitik molekul Cl2 menjadi dua radikal bebas klor. Energi untuk reaksi ini diberikan oleh cahaya ultraviolet atau oleh pemanasan campuran ke temperatur yang sangat tinggi.
Hv atau kalor
Cl-Cl + 58 kkal/mol 2Cl- radikal bebas b. Propagasi
tahap-tahap propogasi dari reaksi radikal bebas. Pada hakekatnya, pembentukan awal beberapa radikal bebas akan mengakibatkan perkembanganbiakan radikal-radikal bebas baru dalam suatu reaksi pengabdian diri (self perpetuating) yang disebut reaksi rantai. Proses ini dapat berlangsung terus tanpa batas. Banyaknya daur (cycle; yakni jumlah berulangnya tahap-tahap propogasi) disebut panjang rantai (chain length). Panjang rantai suatu reaksi radikal bebas bergantung sebagian pada energi radikal-radikal yang terlibat dalam propogasi.
Tahap propogasi:
CH4 + Cl* *CH3 + HCl *CH3 + Cl2 CH3Cl + Cl* c. Pengakhiran
Daur propogasi terputus oleh reaksi-reaksi pengakhiran (termination). Reaksi apa saja yang memusnahkan radikal bebas atau mengubah radikal bebas menjadi radikal bebas yang stabil dan tidak reaktif, dapat mengakhiri daur propogasi radikal bebas.
Tahap pengakhiran:
Cl* + *CH3 CH3Cl *CH3 + *CH3 CH3CH3
Reaksi kedua ini adalah contoh dari reaksi kopling (coupling reaction): penggabungan dua gugus alkil.
antioksidan endogen, keadaan inimengakibatkan kelebihan radikal bebas terjadi pada proses berikut:
1. Peroksidasi lemak
Dimana terjadi kerusakan pada membran sel yang kaya akan sumber poly unsaturated fatty acid (PUFA), yang mudah dirusak oleh bahan-bahan pengoksidasi; proses tersebut dinamakan peroksidasi lemak, hal ini sangat merusak karena merupakan suatu proses berkelanjutan, dimana pemecahan hiperperoksida lemak, sering melibatkan katalisis ion logam transisi.
2. Kerusakan protein
Dimana protein dan asam nukleat lebih tahan terhadap radikal bebas daripada PUFA, sehingga kecil kemungkinan dalam terjadinya reaksi berantai yang cepat. Serangan radikal bebas terhadap protein sangat jarang kecuali bila sangat ekstensif. Hal ini terjadi jika radikal tersebut mampu berakumulasi, atau bila kerusakannya terfokus pada daerah tertentu dalam protein, salah satu penyebab kerusakan adalah, jika protein berikatan dengan ion logam transisi. 3. Kerusakan DNA
Kerusakan di DNA menjadi suatu reaksi berantai, biasanya kerusakan terjadi bila ada delesi pada susunan molekul, apabila tidak dapat diatasi, dan terjadi sebelum replikasi maka akan terjadi mutasi, radikal oksigen dapat menyerang DNA jika terbentuk disekitar DNA seperti pada radiasi biologis.
2.4 Antioksidan
dapat mencegah dampak negatif yang diakibatkan oleh radikal bebas. Senyawa ini memiliki berat molekul kecil, tetapi mampu menginaktivasi berkembangnya reaksi oksidasi, dengan cara mencegah terbentuknya radikal atau dengan mengikat radikal bebas dan molekul yang sangat reaktif (Julyasih, 2009; Winarsi, 2007).
Antioksidan dalam makanan memainkan peranan penting sebagai faktor untuk melindungi kesehatan. Bukti ilmiah menunjukkan bahwa antioksidan mengurangi resiko penyakit kronis termasuk kanker dan penyakit jantung. Sumber utama alami antioksidan adalah biji-bijian, buah-buahan dan sayuran. Tanaman bersumber antioksidan seperti vitamin C, vitamin E, karoten, asam fenolik, fitat, dan fitoestrogen telah diakui memiliki potensi untuk mengurangi resiko penyakit. Beberapa senyawa seperti gallat memiliki aktivitas antioksidan yang kuat sementara yang lain seperti mono fenol merupakan antioksidan yang lemah (Prakash, 2001)
Menurut Silalahi (2006), antioksidan tubuh dikelompokkan menjadi 3 kelompok yakni:
1. Antioksidan primer yang bekerja dengan cara mencegah terbentuknya radikal bebas yang baru dan mengubah radikal bebas menjadi molekul yang tidak merugikan, misalnya glutation peroksidase.
2. Antioksidan sekunder yang berfungsi untuk menangkap radikal bebas untuk menghalangi terjadinya reaksi berantai, misalnya vitamin C, vitamin E, dan β -caroten.
Khasiat antioksidan untuk mencegah berbagai penyakit akibat pengaruh oksidatif akan lebih efektif jika kita mengkonsumsi sayur-sayuran dan buah-buahan yang kaya akan antioksidan daripada menggunakan antioksidan tungggal. Efek antioksidan dari sayur-sayuran dan buah-buahan, lebih efektif daripada suplemen antioksidan yang diisolasi. Hal ini mungkin dikarenakan oleh adanya komponen lain dan interaksinya dalam sayur-sayuran dan buah-buahan yang berperan secara positif.
2.5 Senyawa Polifenol
Polifenol merupakan salah satu kelas utama metabolit sekunder. Senyawa tersebut terdapat dalam berbagai struktur dan bertanggung jawab atas karakteristik organoleptik utama, yang diturunkan dari tanaman pangan. Karakteristik tersebut terutama dalam hal warna dan rasa, yang berkontribusi pada kualitas gizi buah-buahan dan sayuran. Di antara senyawa-senyawaa fenolat tersebut, flavonoid merupakan salah satu kelompok yang paling banyak. Hingga saat ini lebih dari 8.000 jenis flavonoid telah diidentifikasi, tetapi mekanisme kerjanya masih menjadi perdebatan (Winarsi, 2014)
2.6 Flavonoid
Flavonoid adalah senyawa yang terdiri dari C6-C3-C6, umumnya terdapat pada tubuhan sebagai glikosida dengan mengecualikan alga dan hornwort. Gugusan gula bersenyawa pada satu atau lebih grup hidroksil fenolik. Flavonoid terdapat pada seluruh bagian tanaman, termasuk pada daun, akar, kayu, kulit, tepung sari, nektar, bunga, buah buni, dan biji. (Markham, 1988; Sirait, 2007).
makanan berkisar antara 50-80 mg/ hari yang ditemukan dalam buah-buahan dan sayuran. Kelompok flavonoid termasuk di dalamnya flavon, flavan, flavonol, katekin dan antosianin. Perbedaan struktur dalam setiap anggota flavonoid menghasilkan berbagai variasi jumlah dan subsitusi gugus hidroksil dan glikosilasi kelompok tersebut (Silalahi, 2006).
Flavonoid menunjukkan manfaatnya bagi kesehatan melalui efeknya sebagai antioksidan fitokimia, yang berkaitan dengan gugus hidroksil fenolik yang terikat pada strukturnya. Radical scavenging tampaknya berperan cukup dominan dalam aktivitas antioksidan senyawa flavonoid (Winarsi, 2014).
Aglikon flavonoid adalah polifenol dan karena itu mempunyai sifat kimia senyawa fenol, yaitu bersifat agak asam sehingga dapat larut dalam basa. Karena mempunyai sejumlah gugus hidroksil yang tak tersulih, atau suatu gula, flavonoid merupakan senyawa polar maka umumnya flavonoid larut dalam pelarut polar seperti etanol, metanol, butanol, aseton, dimetil sulfoksida, dimetil formamida, air dan lain-lain. Adanya gula yang terikat pada flavonoid (bentuk yang umum ditemukan) cenderung menyebabkan flavonoid lebih mudah larut dalam air dan dengan demikian campuran pelarut di atas dengan air merupakan pelarut yang lebih baik untuk glikosida. Sebaliknya, aglikon yang kurang polar seperti isoflavon, flavonon, dan flavon serta flavonol yang termetoksilasi cenderung lebih mudah larut dalam pelarut seperti eter dan kloroform (Markham, 1988).
2.7 Penentuan Aktivitas Antioksidan dengan Metode DPPH
Interaksi antioksidan dengan DPPH baik secara transfer elektron atau radikal hidrogen pada DPPH akan menetralkan radikal bebas dari DPPH dan membentuk DPPH tereduksi. Jika semua elektron pada radikal bebas pada DPPH menjadi berpasangan, maka warna larutan berubah dari ungu menjadi kuning terang. Perubahan ini dapat diukur sesuai dengan jumlah elektron atau atom hidrogen yang ditangkap oleh molekul DPPH akibat adanya zat antioksida (Panjaitan, 2011).
Suatu senyawa menunjukkan efeknya sebagai antioksidan jika dapat menghambat reaksi peroksidasi lipid, yang secara in vitro dapat diketahui dari besarnya IC50 atau Inhibitor Concentration-50. Parameter yang dipakai untuk menunjukkan aktivitas antioksidan adalah harga konsentrasi efisiensi atau efficient concentration (EC50) atau Inhibitory Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat antioksidan yang memberikan persen peredaman sebesar 50%. Zat yang mempunyai aktivitas antioksidan tinggi, akan mempunyai harga EC50 atau IC50 yang rendah (Molyneux, 2004).
1,1-diphenil-2-picrylhydrazil radical), manfaat antioksidan diperoleh dari minuman teh herbal yang berasal dari daun, rimpang, daging buah, bunga dan kulit kayu (Winarsi, 2014).
2.8 Spektrofotometer Visibel
Spektroskopi serapan ultraviolet dan serapan tampak barangkali merupakan cara tunggal yang paling berguna untuk menganalisis struktur flavonoid. Kedudukan gugus hidroksil fenol bebas pada inti flavonoid dapat ditentukan dengan menambahkan pereaksi ke dalam larutan cuplikan dan mengamati pergeseran puncak serapan yang terjadi (Markham, 1988).
Panjang gelombang untuk sinar ultraviolet antara 200-400 nm sedangkan panjang gelombang untuk sinar tampak/ visibel antara 400-800 nm (Gandjar, 2008). Spektrofotometri serapan adalah pengukuran serapan radiasi elektromagnetik panjang gelombang tertentu yang sempit, mendekati monokromatik, yang diserap zat. Spektrofotometer pada dasarnya terdiri atas sumber sinar monokromator, tempat sel untuk zat yang diperiksa, detektor, penguat arus dan alat ukur atau pencatat. (Ditjen RI, 1979).
2.9 Pelarut
Metode ini akan bekerja dengan baik menggunakan pelarut methanol atau etanol karena kedua pelarut ini tidak mempengaruhi dalam reaksi antara sampel uji sebagai antioksidan dengan DPPH sebagai radikal bebas (Molyneux, 2004). 2.10 Pengukuran absorbansi-panjang gelombang
dalam praktiknya hasil pengukuran yang memberikan peak maksimum itulah panjang gelombangnya yaitu sekitar panjang gelombang yang disebutkan diatas. Nilai absorbansi yang mutlak tidaklah penting, karena panjang gelombang dapat diatur untuk memberikan absorbansi maksimum sesuai dengan alat yang digunakan (Molyneux, 2004).
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang yang mempunyai absorbansi maksimal. Untuk memilih panjang gelombang maksimal, dilakukan dengan membuat kurva hubungan antara absorbansi dengan panjang gelombang dari suatu larutan baku pada konsentrasi tertentu (Gandjar, 2008).
Menurut Gandjar (2008) Ada beberapa alasan mengapa harus menggunakan panjang gelombang maksimal, yaitu:
1. Pada panjang gelombang maksimal, kepekaannya juga maksimal karena pada panjang gelombang maksimal tersebut perubahan absorbansi untuk setiap satuan konsentrasi adalah yang paling besar.
2. Disekitar panjang gelombang maksimal, bentuk kurva absorbansi datar dan pada kondisi tersebut hukum lambert-Beer akan terpenuhi.
3. Jika dilakukan pengukuran ulang maka kesalahan yang disebabkan oleh pemasangan ulang panjang gelombang akan kecil sekali, ketika digunakan panjang gelombang maksimal.
2.11 Waktu pengukuran
BAB I PENDAHULUAN
1.1 Latar Belakang
Antioksidan adalah senyawa pemberi elektron (electron donor) atau reduktan yang memiliki berat molekul kecil, tetapi mampu menginaktivasi berkembangnya reaksi oksidasi, dengan cara mencegah terbentuknya radikal bebas dan dapat menghambat reaksi oksidasi dengan cara mengikat radikal bebas dan molekul yang sangat reaktif. Akibatnya, kerusakan sel akan dihambat (Winarsi, 2007).
Radikal bebas adalah setiap molekul yang mengandung satu atau lebih elektron yang tidak berpasangan. Radikal bebas sangat reaktif dan dengan mudah menjurus kereaksi yang tidak terkontrol, menghasilkan ikatan silang (cross-link) pada DNA, protein, lipida, atau kerusakan oksidatif pada gugus fungsional yang penting pada biomolekul ini, perubahan ini akan menyebabkan proses penuaan. Radikal bebas juga terlibat dalam patologi dari penyakit degenaratif, yakni kanker, aterosklerosis, rematik, jantung koroner, katarak, dan penyakit degenerasi saraf seperti parkinson (Silalahi, 2006).
Senyawa ini terbentuk didalam tubuh dipicu oleh bermacam-macam faktor, misalnya ketika komponen makanan diubah menjadi bentuk energi melalui proses metabolisme yang membentuk radikal bebas seperti anion superoksida, hidroksil dan lain-lain (Winarsi, 2007).
berlebihan antioksidan tubuh ini tidak akan mampu mengatasinya, sehingga tubuh memerlukan antioksidan dari luar yang diperoleh dari makanan maupun minuman (Cholisoh, 2008).
Antioksidan dikelompokkan menjadi dua kelompok yaitu antioksidan sintetik (antioksidan yang diperoleh dari hasil sintesa reaksi kimia) dan antioksidan alami (antioksidan hasil ekstraksi bahan alami). Senyawa antioksidan yang berasal dari bahan-bahan alami mendapat perhatian yang sangat besar, hal ini disebabkan atas Dasar penggunaan yang aman dibandingkan dengan antioksidan sintetik. Antioksidan sintetik mulai dibatasi karena dapat meracuni binatang percobaan dan bersifat karsinogenik (Julyasih, 2009; Zuhra, 2008).
Salah satu tanaman yang dapat dimanfaatkan sebagai antioksidan adalah sirsak (Annona Muricata L.). Bagian tanaman sirsak yang memiliki jumlah besar dalam satu pohon adalah daunnya. Daun sirsak mengandung senyawa bioaktif seperti tanin, flavonoid, polifenol, Annonaceous acetogenius dan saponin. Senyawa flavonoid dan polifenol merupakan senyawa yang berpotensi sebagai antioksidan (Budiarti, 2014; Handayani, 2016; Salamah, 2015).
Masyarakat Indonesia menggunakan daun sirsak secara tradisional sebagai minuman fungsional yang dapat difungsikan antara lain sebagai obat herbal, yaitu dengan cara meminum air rebusan daun sirsak segar (Adri, 2013). Meskipun air rebusan daun sirsak segar telah lama digunakan sebagai obat herbal, namun bentuk teh daun sirsak belum banyak digunakan oleh masyarakat. Karena itu perlu dilakukan kajian tentang aktivitas antioksidan dalam teh daun sirsak, untuk menggali potensi daun sirsak sebagai minuman fungsional yang dapat
Penelitian yang dilakukan Adri (2013), mengenai aktivitas antioksidan teh daun sirsak berdasarkan variasi lama pengeringan dilakukan dengan metode DPPH (1,1-diphenyl-2-picrylhydrazyl). Hasil penelitian menunjukkan bahwa semakin lama pengeringan, semakin tinggi aktivitas antioksidan.
Berdasarkan hal tersebut, maka peneliti tertarik untuk melakukan pemeriksaan senyawa flavonoid dan polifenol serta melakukan uji aktivitas antioksidan dari teh daun sirsak kemasan (Annona muricata Linn.) dengan menggunakan metode pemerangkapan DPPH (1,1-diphenyl-2-picrylhydrazyl). 1.2 Perumusan Masalah
Berdasarkan uraian diatas, maka permasalahan dalam penelitian ini dapat dirumuskan sebagai berikut:
a. Apakah seduhan teh daun sirsak kemasan mengandung senyawa flavonoid dan polifenol yang bersifat sebagai antioksidan ?
b. Apakah aktivitas antioksidan di dalam teh daun sirsak kemasan termasuk dalam kategori yang kuat ?
1.3 Hipotesis
Berdasarkan uraian diatas, maka hipotesis dalam penelitian ini adalah: a. Teh daun sirsak kemasan mengandung senyawa flavonoid dan
polifenol yang bersifat sebagai antioksidan.
b. Teh daun sirsak kemasan memiliki aktivitas antioksidan dalam kategori yang kuat.
1.4 Tujuan Penelitian
Berdasarkan uraian diatas, maka tujuan dari penelitian ini adalah:
senyawa flavonoid dan polifenol yang bersifat sebagai antioksidan. b. Untuk mengetahui kategori aktivitas antioksidan teh daun sirsak
kemasan. 1.5 Manfaat Penelitian
Pemeriksaan Flavonoid dan Polifenol Serta Uji Aktivitas Antioksidan Teh Daun Sirsak Kemasan (Annona muricata Linn.) Dengan Metode
Pemerangkapan DPPH (1,1-diphenyl-2-picrylhydrazyl)
ABSTRAK
Antioksidan berguna bagi kesehatan yakni untuk melindungi dan mengobati tubuh dari berbagai macam penyakit degeneratif dan kanker yang disebabkan oleh radikal bebas dengan cara menetralkannya. Salah satu tanaman yang dimanfaatkan sebagai antioksidan adalah daun sirsak (Annona muricata Linn.). Masyarakat Indonesia menggunakan daun sirsak secara tradisional sebagai minuman fungsional yang dapat difungsikan antara lain sebagai obat herbal, namun bentuk teh daun sirsak kemasan belum banyak digunakan oleh masyarakat. Karena itu perlu dilakukan kajian tentang aktivitas antioksidan dalam teh daun sirsak, untuk menggali potensi daun sirsak sebagai minuman fungsional yang dapat difungsikan antara lain sebagai obat herbal.
Tujuan penelitian ini untuk mengetahui golongan senyawa kimia yang berperan sebagai antioksidan dan mengukur aktivitas antioksidan pada ketiga sediaan teh daun sirsak kemasan.
Pemeriksaan flavonoid dan polifenol yang berperan sebagai antioksidan serta uji aktivitas antioksidan teh daun sirsak kemasan menggunakan metode pemerangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil) diukur pada panjang gelombang maksimum 516 nm setelah 60 menit pada suhu kamar.
Hasil pemeriksaan sediaan teh daun sirsak kemasan memberikan hasil positif terhadap golongan senyawa flavonoid dan polifenol dan hasil aktivitas antioksidan dalam memerangkap radikal bebas DPPH diperoleh nilai Inhibitory Concentration (IC50) masing-masing STDSK pada K1: 1943 ppm, K2: 2287 ppm, dan K3 sebesar 2383 ppm.
The flavonoids and polyphenols Inspection And Testing Antioxidant Activity Soursop Leaf Tea Packaging (Annona muricata Linn.) With the method of
trapping DPPH (1,1-diphenyl–2- picrylhydrazyl) ABSTRACT
Antioxidants are beneficial to health which is to protect and cure the body of a wide range of degenerative diseases and cancer are caused by free radicals in a way to neutralize it. One of the plant used as antioxidants are the leaves of the soursop (Annona muricata Linn.). Indonesian society soursop leaf is traditionally used as a functional beverage that can be used among others as a medicinal herb, but the form of soursop leaf tea packaging has not been widely used by people. Because it is necessary to study on the antioxidant activity in tea leaves of the soursop, to explore the potential of soursop leaves as a functional beverage that can be used among others as a medicinal herb.
The purpose of this study to determine the class of chemical compounds that act as antioxidants and measure the antioxidant activity in the third dosage soursop leaf tea packaging.
Examination of flavonoids and polyphenols that act as antioxidants as well as antioxidant activity assay soursop leaf tea packaging using free radical trapping methods DPPH (1,1-diphenyl-2-picrylhydrazil) measured at the maximum wavelength of 516 nm after 60 minutes at room temperature.
The results of examination preparation of tea leaves of the soursop packaging gives a positive result to the class of flavonoids and polyphenols and the results of antioxidant activity in trapping free radicals DPPH values obtained Inhibitory Concentration (IC50) each STDSK at K1: 1943 ppm, K2: 2287 ppm, and K3 by 2383 ppm.
The conclusion of this study is each steeping tea leaves of the soursop packaging showed antioxidant activity in the category of very weak.
PEMERIKSAAN FLAVONOID DAN POLIFENOL SERTA UJI
AKTIVITAS ANTIOKSIDAN TEH DAUN SIRSAK KEMASAN
(Annona muricata Linn.) DENGAN METODE
PEMERANGKAPAN DPPH (1,1-diphenyl-2-picrylhydrazyl)
SKRIPSI
OLEH:
CHINTY INDRIA M S
NIM 141524069
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMERIKSAAN FLAVONOID DAN POLIFENOL SERTA UJI
AKTIVITAS ANTIOKSIDAN TEH DAUN SIRSAK KEMASAN
(Annona muricata Linn.) DENGAN METODE
PEMERANGKAPAN DPPH (1,1-diphenyl-2-picrylhydrazyl)
SKRIPSI
Diajukan Sebagai Salah Satu Syarat Untuk Memperoleh Gelar
Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
CHINTY INDRIA M S
NIM 141524069
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PEMERIKSAAN FLAVONOID DAN POLIFENOL SERTA UJI
AKTIVITAS ANTIOKSIDAN TEH DAUN SIRSAK KEMASAN
(Annona muricata Linn.) DENGAN METODE
PEMERANGKAPAN DPPH (1,1-diphenyl-2-picrylhydrazyl)
OLEH:
CHINTY INDRIA M S NIM 141524069
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: September 2016
Pembimbing I, Panitia Penguji,
Dra. Sudarmi, M.Si., Apt. Prof. Dr. Ginda Haro, M.Sc., Apt. NIP. 195409101983032001 NIP. 195108161980031002
Pembimbing II, Dra. Sudarmi, M.Si., Apt.
NIP. 195409101983032001
Drs. Fathur Rahman Harun, M.Si., Apt. Nahitma Ginting, M.Si., Apt. NIP. 195310301980031002 NIP. 195406281983031002
Dr. Masfria, M.S., Apt. NIP. 195707231986012001 Medan, September 2016
Fakultas Farmasi,
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa yang telah memberikan karunia yang berlimpah sehingga penulis dapat menyelesaikan penyusunan skripsi yang berjudul Pemeriksaan Flavonoid dan Polifenol Serta Uji Aktivitas Antioksidan Teh Daun Sirsak Kemasan (Annona muricata Linn.) Dengan Metode Pemerangkapan DPPH (1,1-diphenyl-2-picrylhydrazyl). Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
juga mempersembahkan rasa terima kasih yang tak terhingga kepada keluarga, Bapak A. Sitorus, Ibu M. Sinaga dan kakak, abang serta adik-adikku tercinta atas limpahan kasih sayang, doa dan semangat yang tak ternilai dengan apa pun.
Terimakasih juga penulis ucapkan kepada teman-teman Farmasi Ekstensi angkatan 2014 untuk kebersamaan dan dorongan semangatnya, serta semua pihak yang tidak dapat disebutkan satu persatu yang telah banyak membantu hingga selesainya penulisan skripsi ini.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum sempurna, oleh karena itu penulis mengharapkan saran dan kritik yang membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, September 2016 Penulis,
SURAT PERNYATAAN BEBAS PLAGIAT Saya yang bertanda tangan dibawah ini :
Nama : Chinty Indria M Sitorus
NIM : 141524069
Program Studi : S-1 Ekstensi Farmasi
Judul Skripsi : Pemeriksaan Flavonoid dan Polifenol Serta Uji Aktivitas Antioksidan Teh Daun Sirsak Kemasan (Annona muricata Linn.) Dengan Metode Pemerangkapan DPPH ( 1,1-diphenyl-2-picrylhydrazyl).
Dengan ini menyatakan bahwa skripsi ini ditulis berdasarkan data dan hasil pekerjaan yang saya lakukan sendiri, dan belum pernah diajukan orang lain untuk memperoleh gelar kesarjanaan di perguruan tinggi lain, dan bukan plagiat karena kutipan yang ditulis setelah disebutkan sumbernya didalam daftar pustaka. Apabila dikemudian hari ada pengaduan dari pihak lain karena di dalam skripsi ini ditemukan plagiat karena kesalahan saya sendiri, maka saya bersedia menerima sanksi apapun oleh Program Studi Farmasi Fakultas Farmasi Universitas Sumatera Utara, dan bukan menjadi tanggng jawab pembimbing.
Demikian surat pernyataan ini saya perbuat dengan sebenarnya untuk dapat digunakan jika diperlukan sebagai mana mestinya.
Medan, September 2016 Yang Membuat Pernyataan
Pemeriksaan Flavonoid dan Polifenol Serta Uji Aktivitas Antioksidan Teh Daun Sirsak Kemasan (Annona muricata Linn.) Dengan Metode
Pemerangkapan DPPH (1,1-diphenyl-2-picrylhydrazyl)
ABSTRAK
Antioksidan berguna bagi kesehatan yakni untuk melindungi dan mengobati tubuh dari berbagai macam penyakit degeneratif dan kanker yang disebabkan oleh radikal bebas dengan cara menetralkannya. Salah satu tanaman yang dimanfaatkan sebagai antioksidan adalah daun sirsak (Annona muricata Linn.). Masyarakat Indonesia menggunakan daun sirsak secara tradisional sebagai minuman fungsional yang dapat difungsikan antara lain sebagai obat herbal, namun bentuk teh daun sirsak kemasan belum banyak digunakan oleh masyarakat. Karena itu perlu dilakukan kajian tentang aktivitas antioksidan dalam teh daun sirsak, untuk menggali potensi daun sirsak sebagai minuman fungsional yang dapat difungsikan antara lain sebagai obat herbal.
Tujuan penelitian ini untuk mengetahui golongan senyawa kimia yang berperan sebagai antioksidan dan mengukur aktivitas antioksidan pada ketiga sediaan teh daun sirsak kemasan.
Pemeriksaan flavonoid dan polifenol yang berperan sebagai antioksidan serta uji aktivitas antioksidan teh daun sirsak kemasan menggunakan metode pemerangkapan radikal bebas DPPH (1,1-diphenyl-2-picrylhydrazil) diukur pada panjang gelombang maksimum 516 nm setelah 60 menit pada suhu kamar.
Hasil pemeriksaan sediaan teh daun sirsak kemasan memberikan hasil positif terhadap golongan senyawa flavonoid dan polifenol dan hasil aktivitas antioksidan dalam memerangkap radikal bebas DPPH diperoleh nilai Inhibitory Concentration (IC50) masing-masing STDSK pada K1: 1943 ppm, K2: 2287 ppm, dan K3 sebesar 2383 ppm.
The flavonoids and polyphenols Inspection And Testing Antioxidant Activity Soursop Leaf Tea Packaging (Annona muricata Linn.) With the method of
trapping DPPH (1,1-diphenyl–2- picrylhydrazyl) ABSTRACT
Antioxidants are beneficial to health which is to protect and cure the body of a wide range of degenerative diseases and cancer are caused by free radicals in a way to neutralize it. One of the plant used as antioxidants are the leaves of the soursop (Annona muricata Linn.). Indonesian society soursop leaf is traditionally used as a functional beverage that can be used among others as a medicinal herb, but the form of soursop leaf tea packaging has not been widely used by people. Because it is necessary to study on the antioxidant activity in tea leaves of the soursop, to explore the potential of soursop leaves as a functional beverage that can be used among others as a medicinal herb.
The purpose of this study to determine the class of chemical compounds that act as antioxidants and measure the antioxidant activity in the third dosage soursop leaf tea packaging.
Examination of flavonoids and polyphenols that act as antioxidants as well as antioxidant activity assay soursop leaf tea packaging using free radical trapping methods DPPH (1,1-diphenyl-2-picrylhydrazil) measured at the maximum wavelength of 516 nm after 60 minutes at room temperature.
The results of examination preparation of tea leaves of the soursop packaging gives a positive result to the class of flavonoids and polyphenols and the results of antioxidant activity in trapping free radicals DPPH values obtained Inhibitory Concentration (IC50) each STDSK at K1: 1943 ppm, K2: 2287 ppm, and K3 by 2383 ppm.
The conclusion of this study is each steeping tea leaves of the soursop packaging showed antioxidant activity in the category of very weak.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
SURAT PERNYATAAN BEBAS PLAGIAT ... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Sirsak... 5
2.2 Teh ... 6
2.3 Radikal Bebas ... 7
2.4 Antioksidan ... ... 10
2.6 Flavonoid ... 12
2.7 Penentuan Aktivitas Antioksidan Metode DPPH (1,1-Diphenyl-2-Picrylhydrazyl) ... 13
2.8 Spektrofotometer Visibel ... 15
2.9 Pelarut ... 15
2.10 Pengukuran Absorbansi Panjang Gelombang Maksimum ... 15
3.5 Pemeriksaan Senyawa Antioksidan ... 19
3.5.1 Pemeriksaan Senyawa Flavonoid ... 19
3.5.2 Pemeriksaan Senyawa Polifenol ... 19
3.6 Uji Aktivitas Antioksidan Metode DPPH ... 19
3.6.1 Prinsip Metode DPPH (1,1-diphenyl-2-picrylhydrazyl) ... 19
3.6.7 Analisis Persen Pemerangkapan Radikal Bebas ... 21
3.6.8 Analisis Nilai IC50 ... 21
BAB IV HASIL DAN PEMBAHASAN ... 22
4.1 Hasil Pemeriksaan Senyawa Flavonoid dan Polifenol ... 22
4.2 Hasil Pengujian Aktivitas Antioksidan ... 22
4.2.1 Hasil Penentuan Panjang Gelombang Serapan Maksimum ... 22
4.2.2 Hasil Analisis Waktu Pengukuran (operating time) ... 23
4.2.3 Hasil Analisis Aktivitas Antioksidan STDSK ... 24
BAB V KESIMPULAN DAN SARAN ... 31
5.1 Kesimpulan ... 31
5.2 Saran ... ... 31
DAFTAR PUSTAKA ... 32
DAFTAR TABEL
Tabel Halaman
4.1 Hasil Identifikasi Secara Kualitatif
Seduhan Teh Daun Sirsak Kemasan ... 22 4.2 Penurunan Absorbansi dan Persen
Pemerangkapan DPPH oleh Masing-masing STDSK ... 25 4.3 Hasil Persamaan Regresi Linier dan Hasil Analisis
DAFTAR GAMBAR
Gambar Halaman
4.1 Kurva Serapan Maksimum Larutan DPPH 40 ppm Dalam
Metanol Menggunakan Spektrofotometer UV-Visibel ... 23 4.2 Grafik Hasil Uji Aktivitas
Antioksidan STDSK K1 ... 26 4.3 Grafik Hasil Uji Aktivitas
Antioksidan STDSK K2 ... 27 4.4 Grafik Hasil Uji Aktivitas
DAFTAR LAMPIRAN
Lampiran Halaman
1 Bagan Kerja Penelitian ... 35
2 Data Kemasan Teh Daun Sirsak ... 36
3 Gambar Kantongan dan Serbuk Teh Daun Sirsak ... 37
4 Gambar Seperangkat Alat Spektrofotometer UV-Visibel (UV-1800 Shimadzu) ... 38
5 Perhitungan Pembuatan Larutan Blanko DPPH 0,5 mM ... 39
6 Hasil Pengukuran Operating Time ... 40
7 Hasil Identifikasi Secara Kualitatif ... 48
8 Hasil Uji Aktivitas Antioksidan ... 49