PENETAPAN KADAR KALIUM DAN NATRIUM PADA AIR KELAPA HIJAU (Cocos nucivera L.Varietas viridis) DAN AIR KELAPA
GADING (Cocos nucivera L.Varietas eburnia) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH: MINAWATI NIM 050804038
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
▸ Baca selengkapnya: manfaat kelapa cengkir gading
(2)PENETAPAN KADAR KALIUM DAN NATRIUM PADA AIR KELAPA HIJAU (Cocos nucivera L. Varietas viridis) DAN AIR KELAPA
GADING (Cocos nucivera L. Varietas eburnia) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH MINAWATI NIM 050804038
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALIUM DAN NATRIUM PADA AIR KELAPA HIJAU (Cocos nucivera L. Varietas viridis) DAN AIR KELAPA
GADING (Cocos nucivera L. Varietas eburnia) SECARA SPEKTROFOTOMETRI SERAPAN ATOM
OLEH MINAWATI NIM 050804038
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Juni 2011
Disetujui Oleh:
Pembimbing I, Panitia Penguji,
Drs.Syahrial Yoenoes, SU.,Apt Drs. Muchlisyam, M.Si., Apt. NIP 195112061983031001 NIP 195006221980021001
Disetujui Oleh: Drs. Maralaut Batubara, M.Phill.,Apt. Pembimbing II, NIP 195001261983031002
Dra. Sudarmi, M.Si., Apt. NIP 195409101983032001 Drs. Fathur Rahman Harun, M.Si., Apt.
NIP 195201041980031002
Dekan,
KATA PENGANTAR
Bismillahirrahmanirrahiim,
Puji syukur penulis ucapkan kepada Allah SWT atas segala limpahan
rahmat dan karunianya, sehingga penulis dapat menyelesaikan penelitian dan
penyusunan skripsi ini, serta shalawat beriring salam untuk Rasulullah
Muhammad SAW sebagai suri tauladan dalam kehidupan.
Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar
Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, dengan
judul” Penetapan Kadar Kalium dan Natrium Pada Air kelapa Hijau (Cocos
nucivera L. Varietas viridis) dan Air Kelapa Gading (Cocos nucivera L. Varietas eburnia) Secara Spektrofotometri Serapan Atom”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan
terima kasih yang sebesar-besarnya kepada:
1. Ayahanda Aminuddin, S.Pd dan ibunda Asmawati yang telah memberikan cinta
dan kasih sayang yang tidak ternilai dengan apapun, pengorbanan baik materi
maupun motivasi beserta doa yang tulus yang tidak pernah berhenti.
2. Bapak Drs.Syahrial Yoenoes, SU.,Apt dan Drs. Fathur Rahman Harun, M.Si.,
Apt Bapak yang telah membimbing dan memberikan petunjuk serta
saran-saran selama penelitian hingga selesainya skripsi ini.
3. Bapak Drs. Muchlisyam, M.Si., Apt yang telah banyak membantu saya dalam
menyelesaikan skripsi ini.
4. Bapak Prof. Dr. Sumadio Hadisahputra, Apt selaku Dekan Fakultas Farmasi
USU Medan, yang telah memberikan pengarahan dan bimbingan dalam
5. Bapak Drs. syafruddin, MS, Apt. Dan Drs Salim Usman M.Si., Apt. selaku
penasehat akademik yang telah memberikan bimbingan dan motivasi kepada
penulis selama masa perkuliahan.
6. Ibu Dra. Sudarmi, M.Si, Apt selaku Kepala Laboratorium Kimia Farmasi
Kuantitatif Farmasi USU yang telah memberikan izin dan fasilitas untuk
penulis sehingga dapat mengerjakan dan menyelesaikan penelitian.
7. Bapak Masykur,M.Sc. dan Muksalmina MTA di Laboratorium Herbarium
Biologi FMIPA UNIVERSITAS SYIAH KUALA yang telah membantu
penulis dalam mengidentifikasi Kelapa. Bapak Hambali selaku Operator
Laboratorium Pusat Penelitian Kelapa Sawit (PPKS) Medan.
8. Adik ku tercinta (Hartati), dan Fatimah serta seluruh keluarga yang selalu
mendoakan dan memberikan semangat.
9. Sahabat-sahabat terbaikku Jack, Sofi, Dinda, Hilma, Vera, Ade, Sri, Risa ,Irma,
meli, fika dan kakak kakak kutercinta kak Ipeh, kak willy, kak mimi, kak
wina, kak yeni, kak Ira serta teman-teman Farmasi Reguler angkatan 2005
terima kasih untuk perhatian, semangat, doa, dan kebersamaannya selama ini.
10. Serta seluruh pihak yang telah ikut membantu penulis namun tidak tercantum
namanya.Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini
masih jauh dari kesempurnaan, oleh karena itu dengan segala kerendahan hati,
penulis menerima kritik dan saran demi kesempurnaan skripsi ini.Akhirnya,
penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, Maret 2011
Penulis,
PENETAPAN KADAR KALIUM DAN NATRIUM PADA
AIR KELAPA HIJAU (Cocos nucivera L. Varietas viridis) DAN AIR KELAPA GADING (Cocos nucivera L. Varietas eburnia) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM ABSTRAK
Air Kelapa merupakan salah satu bagian dari tanaman kelapa yang
bermanfaat bagi kesehatan, terutama Air kelapa hijau, yang dapat digunakan
sebagai obat seperti obat demam, demam berdarah, batu ginjal dan hipertensi.
Salah satu zat gizi dalam Air kelapa yang mempunyai kadar tinggi adalah Kalium
yaitu 3120 mg/L, dan Natrium 1050 mg/L. Banyak jenis tanaman kelapa yang
ada, tetapi hanya jenis kelapa tertentu yang sering digunakan sebagai obat yaitu
Air kelapa muda hijau, tujuan dari penelitian ini yaitu untuk mengetahui berapa
kadar kalium dan natrium dan apakah ada perbedaan kadar Kalium dan Natrium
Air kelapa hijau yang sering digunakan sebagai obat dan kelapa gading/kuning
yang banyak beredar dipasaran.
Sampel diambil dari kebun kelapa Desa lama Kecamatan Pancur batu Deli
serdang.Kelapa yang dipilih sebagai sampel berdasarkan ketebalan daging
buahnya yaitu ± 2 mm, Penentuan kadar Kalium dan Natrium pada sampel
dilakukan secara kuantitatif dengan metode spektrofotometri serapan atom pada
panjang gelombang yang berbeda yaitu 769,9 nm untuk Kalium dan 589,6 nm
untuk Natrium.
Dari hasil penelitian menunjukkan bahwa varietas kelapa berpengaruh
terhadap kadar Kalium dan Natrium pada Air kelapa. Kadar rata rata Kalium
pada Air kelapa hijau yaitu 2058,1 µ g/ml dan kelapa gading/kuning adalah
1666,4750 µg/ml sementara kadar rata rata Natrium pada Air kelapa hijau
67,4854 µg/ml dan kelapa gading/kuning 16,3126 µg/ml. Kadar Kalium dan
Natrium lebih tinggi pada Air kelapa muda hijau dari pada Air kelapa muda
gading/kuning.
DETERMINATION THE CONCENTRATION OF SODIUM AND POTASSIUM IN WATER GREEN COCONUT (Cocos nucivera
L. Variety viridis ) AND WATER OIL IVORY (Cocos nucivera L. Variety eburnia) USING ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Coconut water is one part of the coconut trees that are beneficial to health,
especially of green coconut water, which can be used to cure fever, dengue fever,
and kidney stones. One of the nutrients in coconut water is having high levels of
Potassium and Sodium, which is 3120 mg/L, and Sodium 1050 mg/L. many of
palm species that exist, so that there are people who use certain palm species of
plants as medicine is a young green coconut water, the purpose of this study is to
determine how many levels of potassium and sodium differences in levels of
Potassium and Sodium coconut green coconut water that is frequently used as a
medicine and palm ivory nice is used as a natural fresh drinks.
The samples taken from coconut garden Pancur Batu Deli serdang.
chosen as a sample based on the thickness of flesh that is ± 2 mm . Determination
of Potassium and Sodium on samples carried quantitatively atomic
absorption spectrophotometric method different wavelengths of 769,6 nm to589,6
nm for potassium and sodium.
The results showed that the significant effect of coconut varieties to
Potassium and Sodium levels in coconut water. Average levels of Potassium in
green cococnut water is 2058,1 µg/ml and palm invory is 1666.4750 µ g/ml, while
the average levels of sodium in green coconutwater 67.4854 µg/ml and palm ivory
16.3126 µg/ml.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
ABSTRAK ... iii
ABSTRACT ... iv
DAFTAR ISI ... v
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... ix
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian... 3
1.5 Manfaat Penelitian... 3
BAB II METODOLOGI PENELITIAN ... 4
2.1 Tempat dan Waktu Penelitian ... 4
2.2 Bahan dan Alat ... 4
2.2.1 Sampel ... 4
2.2.2 Pereaksi ... 4
2.2.3 Alat-alat ... 5
2.3 Pembuatan Pereaksi ... 5
2.4.1 Sampel ... 5
2.4.1.1 Pengambilan Sampel ... 5
2.4.1.2 Identifikasi Sampel ... 5
2.4.1.3 Penyiapan Sampel... 6
2.4.2 Proses Destruksi ... 6
2.4.3 Analisis Kuantitatif ... 6
2.4.3.1 Penentuan panjang Gelombang Maksimum ... 6
2.4.3.2 Penentuan Linearitas Kurva Kalibrasi Kalium ... 6
2.4.3.3 Penentuan Linearitas Kurva kalibrasi Natrium ... 6
2.4.4 Penentapan Kadar Kalium Dan Natrium Dalam Sampel ... 7
2.4.5 Analaisis Data Secara Statistik ... 8
2.4.5.1 Penolakan Hasil Pengamatan ... 8
2.4.5.2 Pengujian Nilai Rata-Rata ... 9
2.4.5.3 Pengujian Beda Nilai Rata Rata... 9
2.4.6 Penentuan Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)... 10
2.4.7 Uji Ketepatan (Recovery Test) ... 11
2.4.8 Uji ketelitian (presisi) ... 12
BAB III HASIL DAN PEMBAHASAN ... 13
3.1 Hasil identifikasi sampel ... 13
3.2 Pemeriksaan Kuantitatif... 13
3.2.1 Linearitas Kurva Kalibrasi kalium Dan Natrium ... 14
3.3.3 Pengujian Beda Nilai Rata Rata Kadar Logam Kalium
Dan Natrium Pada Sampel... 18
3.4 Uji Validasi... 19
3.4.1 Uji perolehan kembali(Recovery Test) ... 19
3.4.2 Uji Presisi (ketelitian) ... 19
3.6 Batas Deteksi (LOD) dan batas Kuantitasi(LOQ)... .... 20
BAB IV KESIMPULAN DAN SARAN... 21
4.1 Kesimpulan ... 21
4.2 Saran ... 21
DAFTAR PUSTAKA ... 22
DAFTAR TABEL
Halaman
Tabel 1. Harga koefisien penolakan t pada taraf
Kepercayaan 95%... 8
Tabel 2. Hasil penetapan kadar ... 14
DAFTAR GAMBAR
Halaman
Gambar 1. Kurva Kalibrasi Larutan Standar Kalium... 14
Gambar 2. Kurva Kalibrasi Larutan standar Natrium ... 14
Gambar 3. Kelapa Hijau ... 50
Gambar 4. Kelapa Gading/Kuning ... 50
Gambar 5. Proses Destruksi ... 51
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Bagan Proses destruksi logam Kalium dan Natrium ...23
Lampiran 2. Data Hasil pengukuran Larutan Standar Kalium... 24
Lampiran 3 Contoh Perhitungan Persamaan Regresi Logam Kalium... 24
Lampiran 4. Hasil Pengukuran Absorbansi Larutan Standar Natrium …….26
Lampiran 5. Contoh Perhitungan Persamaan Regresi Logam Natrium……26
Lampiran 6. Data Hasil Volum Sampel, Absorbansi, Kadar Rata Rata
dan Kadar Sebenarnya Sampel... 26
Lampiran 7. Contoh Perhitungan Hasil Penetapan Kadar Kalium Pada
Sampel Air Kelapa Gading/kuning ... 29
Lampiran 8. Perhitungan Statistik Kadar Logam Kalium Pada Air kelapa Gading/kuning... ... 31
Lampiran 9. Perhitungan Statistik Kadar Logam Kalium Pada Air kelapa hijau ... 33
Lampiran 10. Perhitungan Statistik Kadar Natrium Air kelapa
Gading/kuning... ... 35
Lampiran 11. Perhitungan Statistik Kadar Logam Natrium Air kelapa
hijau ... 35
Lampiran 12. Pengujian Beda Nilai Rata Rata Kalium Air kelapa Hijau dan Air kelapa gading/kuning ... ... 37
Lampiran 13. Pengujian Beda Nilai Rata Rata Natrium Air kelapa hijau dan
Air Kelapa gading/kuning... ...41
Lampiran 14. Contoh Perhitungan Kadar Kalium Untuk Recovery ... . 43
Lampiran 15. Contoh Perhitungan Kadar Natrium Untuk Recovery ... 44
Lampiran 16. Data % Recovery logam Kalium Air kelapa gading……… . 45
Lampiran 17 Data % Recovery logam Kalium Air kelapa gading…………. 45
Lampiran 19. Perhitungan Koefisien Variasi (%RSD) Natrium pada Air kelapa
Gading……….46
Lampiran 20. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi Logam (LOQ) Kalium ………. 47
Lampiran 21. Perhitungan Batas Deteksi (LOD) dan Batas Kuantitasi Logam (LOQ) Natrium………. 48
Lampiran 22. Daftra Komposisi Air kelapa Muda………..49
Lampiran 23. Sampel Kelapa Hijau Dan Kelapa Gading/Kuning... 50
Lampiran 24. Proses Destruksi Sampel ... ... 51
Lampiran 25. Alat Spektofotometri Serspsn Stom ... 52
Lampiran 26. Gambar Hasil Identifikasi Sampel kelapa gading ... 53
Lampiran 27. Gambar Hasil Identifikasi Sampel kelpa hijau ... 54
Lampiran 28. Tabel Distribusi t... 55
PENETAPAN KADAR KALIUM DAN NATRIUM PADA
AIR KELAPA HIJAU (Cocos nucivera L. Varietas viridis) DAN AIR KELAPA GADING (Cocos nucivera L. Varietas eburnia) SECARA
SPEKTROFOTOMETRI SERAPAN ATOM ABSTRAK
Air Kelapa merupakan salah satu bagian dari tanaman kelapa yang
bermanfaat bagi kesehatan, terutama Air kelapa hijau, yang dapat digunakan
sebagai obat seperti obat demam, demam berdarah, batu ginjal dan hipertensi.
Salah satu zat gizi dalam Air kelapa yang mempunyai kadar tinggi adalah Kalium
yaitu 3120 mg/L, dan Natrium 1050 mg/L. Banyak jenis tanaman kelapa yang
ada, tetapi hanya jenis kelapa tertentu yang sering digunakan sebagai obat yaitu
Air kelapa muda hijau, tujuan dari penelitian ini yaitu untuk mengetahui berapa
kadar kalium dan natrium dan apakah ada perbedaan kadar Kalium dan Natrium
Air kelapa hijau yang sering digunakan sebagai obat dan kelapa gading/kuning
yang banyak beredar dipasaran.
Sampel diambil dari kebun kelapa Desa lama Kecamatan Pancur batu Deli
serdang.Kelapa yang dipilih sebagai sampel berdasarkan ketebalan daging
buahnya yaitu ± 2 mm, Penentuan kadar Kalium dan Natrium pada sampel
dilakukan secara kuantitatif dengan metode spektrofotometri serapan atom pada
panjang gelombang yang berbeda yaitu 769,9 nm untuk Kalium dan 589,6 nm
untuk Natrium.
Dari hasil penelitian menunjukkan bahwa varietas kelapa berpengaruh
terhadap kadar Kalium dan Natrium pada Air kelapa. Kadar rata rata Kalium
pada Air kelapa hijau yaitu 2058,1 µ g/ml dan kelapa gading/kuning adalah
1666,4750 µg/ml sementara kadar rata rata Natrium pada Air kelapa hijau
67,4854 µg/ml dan kelapa gading/kuning 16,3126 µg/ml. Kadar Kalium dan
Natrium lebih tinggi pada Air kelapa muda hijau dari pada Air kelapa muda
gading/kuning.
DETERMINATION THE CONCENTRATION OF SODIUM AND POTASSIUM IN WATER GREEN COCONUT (Cocos nucivera
L. Variety viridis ) AND WATER OIL IVORY (Cocos nucivera L. Variety eburnia) USING ATOMIC ABSORPTION SPECTROPHOTOMETRY
ABSTRACT
Coconut water is one part of the coconut trees that are beneficial to health,
especially of green coconut water, which can be used to cure fever, dengue fever,
and kidney stones. One of the nutrients in coconut water is having high levels of
Potassium and Sodium, which is 3120 mg/L, and Sodium 1050 mg/L. many of
palm species that exist, so that there are people who use certain palm species of
plants as medicine is a young green coconut water, the purpose of this study is to
determine how many levels of potassium and sodium differences in levels of
Potassium and Sodium coconut green coconut water that is frequently used as a
medicine and palm ivory nice is used as a natural fresh drinks.
The samples taken from coconut garden Pancur Batu Deli serdang.
chosen as a sample based on the thickness of flesh that is ± 2 mm . Determination
of Potassium and Sodium on samples carried quantitatively atomic
absorption spectrophotometric method different wavelengths of 769,6 nm to589,6
nm for potassium and sodium.
The results showed that the significant effect of coconut varieties to
Potassium and Sodium levels in coconut water. Average levels of Potassium in
green cococnut water is 2058,1 µg/ml and palm invory is 1666.4750 µ g/ml, while
the average levels of sodium in green coconutwater 67.4854 µg/ml and palm ivory
16.3126 µg/ml.
BAB I PENDAHULUAN
1.1 latar Belakang
Kelapa merupakan salah satu tanaman yang umumnya terdapat di daerah
tropis. Tumbuhan ini dimanfaatkan hampir semua bagiannya oleh manusia
sehingga dianggap tumbuhan serba guna. Tanaman kelapa terdiri atas batang,
akar, daun, bunga dan buah. Buah kelapa terdiri atas kulit luar, kulit dalam, kulit
biji, putih lembaga, dan air (Suhadirman, 1998).
Salah satu bagian dari tanaman kelapa yang bermanfaat adalah Air
kelapa. air kelapa muda banyak dijual sebagai minuman penyegar, selain sebagai
minuman penyegar, air kelapa muda juga bermanfaat bagi kesehatan, yaitu dapat
digunakan sebagai obat demam, demam berdarah, batu ginjal dan hipertensi.
Menurut Balai penelitian dan pengembangan Industri, Departemen perindustrian
(1986) air kelapa merupakan cairan kaya gizi, dan salah satu zat gizinya adalah
Kalium yaitu 3120 mg/L dan Natrium adalah 1050 mg/L (Rendengan, 2009).
Kalium merupakan ion bermuatan positif, terutama terdapat di dalam sel
dan sebanyak 95% Kalium berada di dalam cairan intraseluler. Kalium berperan
dalam pemeliharaan keseimbagan cairan dan elektrolit serta keseimbangan asam
basa. Kebutuhan kalium minimum ditaksir sebanyak 2000 mg/hari. Peranan
Natrium mirip dengan Kalium, Natrium adalah kation utama dalam cairan
ekstraselular. Taksiran kebutuhan Natrium sehari adalah 500 mg/hari (Almatsier,
Secara umum jenis kelapa dapat digolongkan menjadi dua bagian yaitu
kelapa dalam dan kelapa genjah, salah satu bagian dari kelapa dalam adalah
kelapa hijau (Cocos nucisvera L. Varietas viridis) dimana kelapa ini mulai
berbuah 6-7 tahun atau lebih, buahnya lebih besar dari pada kelapa yang lain,
bagian dalam jika dikupas berwarna kemerah merahan, rasa airnya lebih kurang
manis. Sedangkan salah satu bagian dari kelapa genjah adalah kelapa gading
(Cocos nucisvera L.Varietas eburnia), Kelapa ini mulai berbuah lebih kurang 3-4
tahun, warna kuning kehijauan, bulat dan kecil (Nurul.P, 2007).
Berdasarkan informasi yang diperoleh dari masyarakat dan artikel, Air
kelapa yang sering digunakan adalah air kelapa hijau (air kelapa muda hijau) dan
terutama digunakan sebagai obat. Harga kelapa hijau lebih mahal dibandingkan
dengan kelapa gading/kuning. Dengan adanya berbagai jenis kelapa kemungkinan
kandungan Kalium dan Natrium mempunyai kadar yang berbeda, oleh karena itu
peneliti melakuka penelitian penentuan kadar Kalium dan Natrium pada Air
kelapa hijau (Cocos nucisvera L. Varietas viridis) dan Air kelapa gading/kuning
(Cocos nucisvera L. Varietas eburnia).
1.2 Perumusan Masalah
1. Apakah ada perbedaan kadar Kalium dan Natrium pada air kelapa
hijau dan air kelapa gading?
2. Apakah kadar Kalium dan Natrium pada air kelapa hijau dan air
1.3 Hipotesis
1. Terdapat perbedaan kadar Kalium dan Natrium pada air kelapa hijau
dan air kelapa gading
2. Terdapat perbedaan kadar kalium dan Natrium pada air kelapa hijau dan
air kelapa gading dengan literatur (Annisa.R., 2010)
1.4 Tujuan
1. Untuk mengetahui apakah terdapat perbedaan kadar Kalium dan
Natrium pada air kelapa hijau dan air kelapa gading
2. Untuk mengetahui kadar Kalium dan Natrium yang terdapat pada air
kelapa hijau dan air kelapa gading apakah sesuai dengan literatur
(Annisa.R., 2010)
1.5. Manfaat
1. Hasil penelitian ini dapat memberikan informasi kepada masyarakat
tentang perbedaan kadar Kalium dan Natrium pada air kelapa hijau dan
air kelapa gading
2. Hasil penelitian dapat dimanfaatkan oleh peneliti selanjutnya untuk
BAB II
TINJAUAN PUSTAKA 2.1. Pengenalan Tanaman Kelapa
Kelapa (Cocos nucifera L) merupakan salah satu anggota tanaman palmae
yang paling dikenal dan banyak tersebar di daerah tropis. Daunnya panjang dapat
mencapai 3-4 meter lebih dengan sirip-sirip lidi yang menopang tiap helaian.
Dalam taksonomi tumbuh-tumbuhan, tanaman kelapa dimasukkan ke dalam
klasifikasi sebagai berikut :
Kingdom : Plantae (tumbuh-tumbuhan)
Divisio : Spermatophyta (tumbuhan berbiji)
Sub-divisio : Angiospermae (Berbiji tertutup)
Kelas : Monocotyledonae (Biji berkeping satu)
Ordo : Palmales
Familia : Palmae
Genus : Cocos
Spesies : Cocos nucifera L (Nurul.P, 2007)
Ciri-ciri kelapa yang dapat diamati dari varietas viridis antara lain seperti
mulai berbuah pada umur 6-8 tahun dan setelah ditanam, umur pohon mencapai 50
tahun lebih. Batangnya tinggi sampai mencapai 35 m, pada umumnya tingginya 30 m.
Buahnya berukuran besar, yaitu rata-rata beratnya 2 kg dengan daging buah ½ kg dan
air ½ liter (Warisno,1998)
merah jingga bila tangkainya dilepas. Warna sabutnya pun kemerah-merahan (Anonim, 2011).
Kelapa gading mulai berbuah pada umur 3-4 tahun. Buahnya kecil-kecil,
beratnya rata-rata 1 kg dan daging buahnya 400 gram. Batang kelapa ini berukuran
kecil dan pangkal batangnya tidak besar, tinggi batang ± 5m. Umur kelapa gading
rata-rata 25 tahun atau lebih (Warisno, 1998).
2.1.1 Air kelapa
Volume air yang terdapat pada kelapa Dalam sekitar ±500 ml, kelapa
gading ± 230 ml. Air kelapa muda termasuk minuman yang alami dan higienis
serta memiliki komposisi gizi yang cukup baik. Oleh karena itu dengan minum
Air kelapa muda selain dapat memenuhi rasa haus juga dapat menyembuhkan
beberapa jenis penyakit, seperti demam, demam berdarah, hipertensi dan batu
ginjal. Ini dikarenakan Air kelapa muda memiliki unsur kalium yang tertinggi.
Oleh karena itu Air kelapa muda berperan penting dalam meningkatkan frekwensi
pembuangan urin (Rindengan, 2004).
Air kelapa sebagai pencegah penyakit gijal karena Air kelapa dapat
terbukti efektif mencegah penyakit ginjal dan mereduksi serta melarutkan semua
jenis batu ginjal (Milla dan Boceta, 1989). Selanjutnya dikemukakan oleh Oslon
et al 1984, dalam Karyadi dan Muhilal (1988) bahwa mengkonsumsi K yang
tinggi dapat menurunkan hipertensi. Dengan cara menyeimbangi kadar Natrium
sehingga tekanan darah kita terjaga (Anonom, 2011).
a. Mineral
Berdasarkan kebutuhan didalam tubuh mineral dapat digolongkan menjadi dua kelompok utama yaitu mineral makro dan mineral mikro. Mineral makro
sedangkan mineral mikro mineral yang dibutuhkan kurang dari 100 mg/hari
(Kartasapoetra, 2008).
2.2.1 Kalium
Kalium adalah suatu unsur kimia dalam tabel periodik yang memiliki
lambang K dan nomor atom 19; berat atom 39,102; titik lebur 36.38
o
C; dan titik didih
759
o
C. Kalium berbentuk logam lunak berwarna putih keperakan dan termasuk
golongan alkali tanah. Kalium teroksidasi dengan sangat cepat dengan udara, sangat
reaktif terutama dalam air , dan secara kimiawi memiliki sifat yang mirip dengan
natrium (Vogel, 1985).
Fungsi dari unsur K di dalam tubuh adalah sebagai berikut :
a. Merupakan unsur anorganik yang penting di dalam intraseluler.
b. Penting dalam transmisi impul-impul syaraf.
c. Penting untuk kontraksi otak.
d. Penting untuk pertumbuhan
Kerja kalium adalah mempertahankan stabilitas membran sel agar sel
dapat berfungsi, seperti syaraf menyalurkan sinyal, otot berkontraksi dan jantung
berdenyut. Kekurangan kalium mengakibatkan gangguan fungsi ini sehingga
kerjanya melemah, demikian juga pada keadaan kelebihan, jantung mengalami
hambatan untuk memompa darah keseluruh tubuh. Pada orang sehat, ginjal
merupakan organ yang membuang kalium yang berlebihan. Kalium adalah
mineral yang terdapat dalam sayur dan buah-buahan (Kartasapoetra, 2008).
2.2.2 Natrium
Natrium adalah logam putih perak yang lunak, yang melebur pada 97,5ºC.
Natrium teroksidasi dengan cepat dalam udara lembab. Sumber natrium adalah
natrium dalam jumlah besar. Fungsi natrium antara lain adalah berperan dalam
menghasilkan tekanan osmotik yang mengatur pertukaran cair an antara sel dan
cair an disekitarnya, untuk mempertahankan keseimbangan tubuh (Budianto,
2009).
2.3 Persiapan Sampel Untuk Penentapan Mineral
Untuk menentukan kandungan mineral bahan harus dihancurkan atau
didestruksi dulu. Cara yang biasa dilakukan yaitu pengabuan kering (dry ashing)
dan pengabuan basah (wet digestion). Pemilihan cara tersebut tergantung pada
sifat zat organic dalam bahan, mineral yang akan dianalisis serta sensitivitas cara
yang digunakan.
Pengabuan basah memberikan beberapa keuntungan. Suhu yang
digunakan tidak dapat melebihi tititk didih larutan dan pada umumnya karbon
lebih cepat hancur dari pada menggunakan cara pengabuan kering. Cara
pengabuan basah pada prinsipnya adalah penggunaan asam nitrat untuk
mendestruksi zat organic pada suhu rendah dengan maksud meghindari
kehilangan mineral akibat penguapan (Apriantono, 1989).
Teknik destruksi basah adalah dengan memanaskan sampel organik
dengan penambahan asam mineral pengoksidasi atau campuran dari asam asam
mineral tersebut. Penembahan asam mineral pengoksidasi dan pemanasan yang
cukup dalam beberapa menit dapat mengoksidasi sampel secara sempurna,
sehingga menghasilkan ion logam dalam larutan asam sebagai sampel anorganik
untuk dianalisis selanjutnya. Destruksi basah biasanya menggunakan HNO3,
2.4 Analisis Kalium Dan Natrium
Ada dua macam cara analisis kalium yaitu :
1. Analisis kualitatif
Suatu bahan yang mengandung unsur kalium dan natrium akan memberikan
gambaran khas terhadap penambahan reagen tertentu, misalnya dengan pemanbahan
asam pikrat maka akan terbentuk Kristal jarum besar jika terdapat kalium dan jarum
kecil jka terdapat natrium. Kemudian dengan reaksi nyala, jika sampel positif
mengandung kalium, dengan reaksi nyala akan memberikan warna ungu sedangkan
natrium akan meghasilkan warna kuning (Vogel, 1985).
2. Analisa kuantitatif
b. Metode SSA (Spekrofotometri Serapan Atom)
Spektrofotometri Serapan Atom adalah suatu teknik atau metode analisa
kimia bagi penentuan kadar unsur-unsur logam yang terdapat di dalam sampel dengan
kadar yang rendah (ppm, ppb). Dasar analisis pada metode ini adalah absorbs energi
radiasi elektromagnetik oleh atom.
2.5 Spektrofotometri Serapan Atom
Spektrofotometri serapan atom adalah suatu metode yang digunakan untuk
mendeteksi atom-atom logam dalam fase gas. Metode ini seringkali
mengandalkan nyala untuk mengubah logam dalam larutan sampel menjadi
atom-atom logam berbentuk gas yag digunakan untuk analisis kuantitatif dari logam
dalam sampel (Bender, 1987).
Prinsip dari spektofotometer serapan atom adalah atom atom pada keadaan
dasar mampu menyerap cahaya pada panjang gelombang tertentu, yang pada
umumnya adalah panjang gelombang radiasi yang akan dipancarkan atom atom
gelombang tertentu dilewatkan nyala yang mengandung atom atom yang
bersangkutan maka sebagian cahaya itu akan diserap dan banyaknya penyerapan
akan berbandig lurus dengan banyaknya atom keadaan dasar yang berada dalam
nyala (Bassett, 1994).
Metode spektrofotometri serapan atom berdasarkan pada absorbsi cahaya
oleh atom. Atom- atom akan menyerap cahaya pada panjang gelombang tertentu,
tergantung pada sifat unsurnya. Dasar analisis menggunakan teknik
spektrofotometri serapan atom adalah bahwa dengan mengukur besarnya absorbsi
oleh atom analit, maka konsentrasi analit tersebut dapat ditentukan
Ada 4 cara pembentukan atom dalam spektrofotometri serapan atom,
yaitu:
1. Dengan menggunakan nyala campuran gas (Flame-AAS).
2. Melalui pembentukan senyawa hidrida diikuti pemanasan.
3. Dengan tanpa nyala untuk analisis merkuri.
4. Menggunakan pemanasan oleh listrik (Electrothermal-AAS atau Graphite
Furnace-AAS) (Rohman, 2007)
Gambar 1. Komponen Spektrofotometer Serapan Atom 1. Sumber Sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow
cathoda lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Katoda berbentuk silinder berongga yang terbuat dari
logam atau dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas
mulia (neon atau argon). Bila antara anoda dan katoda diberi selisih tegangan
yang tinggi (600 volt), maka katoda akan memacarkan beras-berkas elektron yang
bergerak menuju anoda yang mana kecepatan dan energinya sangat tinggi.
Elektron-elektron dengan energi tinggi ini dalam perjalanannya menuju anoda
akan bertabrakan dengan gas-gas mulia yang diisikan tadi. Akibat dari
tabrakan-tabrakan ini membuat unsur-unsur gas mulia akan kehilangan elektron dan
menjadi bermuatan positif. Ion-ion gas mulia yang bermuatan positif ini
selanjutnya akan bergerak ke katoda dengan kecepatan dan energi yang tinggi
pula. Pada katoda terdapat unsur-unsur yang sesuai dengan unsur yang dianalisis.
Unsur-unsur ini akan ditabrak oleh ion-ion positif gas mulia. Akibat tabrakan ini,
unsur-unsur akan terlempar ke luar dari permukaan katoda. Atom-atom unsur dari
katoda ini mungkin akan mengalami eksitasi ke tingkat energi-energi elektron
yang lebih tinggi dan akan memancarkan spektrum pencaran dari unsur yang sama
dengan unsur yang akan dianalisis (Rohman, 2007).
2. Tempat Sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan
3. Monokromator
Monokromator dimaksudkan untuk memisahkan dan memilih panjang
gelombang yang digunakan dalam analisis. Dalam monokromator terdapat
chopper (pemecah sinar), suatu alat yang berputar dengan frekuensi atau
kecepatan perputaran tertentu (Rohman, 2007).
4. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui
tempat pengatoman (Rohman, 2007).
5. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang
menggambarkan absorbansi atau intensitas emisi (Rohman, 2007)
2.5.2 Atomisasi Dalam Spektrofotometer Serapan Atom
Untuk mengubah unsur metalik menjadi uap atau hasil disosiasi diperlukan energi
panas. Tempratur harus benar benar terkendali dengan sangat hati hati agar proses
atomisasinya sempurna.
Pembentuk atom atom logam gas dalam nyala dapat terjadibila suatu larutan
sampel yang mengandung logam dimasukkan kedalam nyala. Peristiwa ini terjadi
secara singkat setelah sampel dimasukkan kedalam nyala adalah:
1. Peguapan pelarut yang meninggalkan residu
2. Penguapan zat padat dengan disosiasi menjadi atom atom penyusunnya,
3. Beberapa atom dapat tereksitasi oleh tingkat energi panas nyala ke
tingkatan energi yang lebih tinggi, dan mencapai kondisi dimana atom
atom tersebut memancarkan energi (Basset,dkk., 1994).
2.5.3 Bahan Bakar dan Bahan Pengoksidasi
Pemilihan bahan bakar dan gas pengoksidasi serta komposisi
perbandingannya sangat mempengaruhi suhu nyala (Rohman, 2007). Umumnya
bahan bakar yang digunakan adalah propana, butana, hidrogen dan asetilen,
sedangkan oksidatornya adalah udara, oksigen dan N2O (Khopkar, 1990).
2.5.4 Gangguan Pada Spektrofotometer Serapan Atom
Gangguan-gangguan (interference) yang ada pada AAS adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang dianalisis
menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan konsentrasinya
dalam sampel (Rohman, 2007).
Menurut Rohman (2007), gangguan-gangguan yang dapat terjadi dalam
AAS adalah sebagai berikut:
1. Gangguan yang berasal dari matriks sampel yang dapat mempengaruhi
banyaknya sampel yang mencapai nyala.
Sifat-sifat tertentu matriks sampel dapat mengganggu analisis yakni
matriks tersebut dapat berpengaruh terhadap laju aliran bahan bakar/gas
pengoksidasi. Sifat-sifat tersebut adalah:viskositas, tegangan permukaan, berat
jenis, dan tekanan unsur.
Gangguan matriks yang lain adalah pengendapan unsur yang dianalisis
sehingga jumlah atom yang mencapai nyala menjadi lebih sedikit dari
2. Gangguan kimia yang dapat mempengaruhi jumlah/banyaknya atom yang
terjadi didalam nyala.
Terbentuknya atom-atom netral yang masih dalam keadaan azas di dalam
nyala sering terganggu oleh dua peristiwa kimia, yaitu :
a. Disosiasi senyawa-senyawa yang tidak sempurna
b. Ionisasi atom-atom di dalam nyala
3. Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi atom yang
dianalisis, yakni absorbansi oleh molekul-molekul yang tidak terdisosiasi di
dalam nyala
2.6 Validasi Metode Analisa
Validasi adalah suatu tindakan penilaian terhadap perameter tertentu pada
prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut
memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Beberapa parameter validasi diuraikan di bawah ini.
2.6.1 Uji Perolehan Kembali (Recovery Test)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil
analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan
ditentukan dengan dua cara, yaitu:
a. Metode Simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode yang
dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu
hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang
sebenarnya) (Harmita, 2004).
b. Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan metode
yang dilakukan dengan cara menambahkan sejumlah analit dengan konsentrasi
tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan
divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa
penambahan sejumlah analit. Persen perolehan kembali ditentukan dengan
menentukan berapa persen analit yang ditambahkan ke dalam sampel dapat
ditemukan kembali (Harmita, 2004).
Menurut Miller (2005), suatu metode dikatakan teliti jika nilai
recoverynya antara 80-120%. Recovery dapat ditentukan dengan menggunakan
metode standar adisi.
2.6.2 Keseksamaan (presisi)
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan
derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Kriteria seksama diberikan jika metode
memberikan simpangan baku relatif atau koefisien variansi 2% atau kurang.
(Harmita, 2004).
2.6.3 Batas Deteksi dan Batas Kuantitasi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
BAB III
METODOLOGI PENELITIAN
Metode penelitian yang dilakukan adalah penelitian deskriptif dengan
tujuan utama untuk memberikan deskripsi tentang perbedaan kandungan logam
Kalium dan Natrium dalam Air kelapa muda hijau (Cocos nucisvera L. Varietas
viridis) dan Air kelapa muda gading (Cocos nucisvera L. Varietas eburnia)
2.1 Lokasi dan Waktu Penelitian
Penelitian dilakukan di tiga lokasi yaitu identifikasi sampel dilakukan di
bagian Herbarium Fakultas MIPA Biologi Universitas syiah Kuala, Banda Aceh.
Penyiapan preparasi sampel dilakukan di laboratorium Kimia Farmasi Kuantitatif
Fakultas Farmasi USU, dan pengukuran sampel dilakukan di Laboratorium Pusat
Penelitian Kelapa Sawit (PPKS) Medan, dilakukan dari bulan Desember 2010 - April 2011.
2.2 Bahan Dan Alat 2.2.1 Sampel
Sampel yang diperiksa dalam penelitian ini adalah Air kelapa muda hijau
dan Air kelapa muda gading yang diperoleh dari kebun kelapa Desa lama
kecamatan Pancur batu, Deli serdang.
2.2.2 Pereaksi
Bahan yang digunakan semua pro analis keluaran E. Merck kecuali
disebutkan lain yaitu Asam Nitrat 65%, Asam Pikrat , aquabidest (IKA), larutan
2.2.3 Alat-alat
Spektrofotometer Serapan Atom (GBC Avanta ∑ ) dengan nyala
Propana-asetilen lampu lampu Kalium (GBC Avanta ∑, Australia), dengan nyala
Propana-asetilen lampu Natrium (GBC Avanta ∑ ), kertas whatman 42, neraca analitik
(shimadzu), Hot Plate (shott), pisau stainless, dan alat-alat gelas (pyrex)
2.3 Pembuatan Pereaksi 2.3.1 Larutan HNO3 5N
Larutan HNO3 65% sebanyak 340 ml diencerkan dengan air suling
hingga 1000 ml.
2.3.2 Larutan Asam pikrat 1%
Sebanyak 1 gram asam pikrat dilarutkan dalam air suling hingga 100 ml.
(Ditjen POM, 1979).
2.4 Prosedur Penelitian 2.4.1 Sampel
2.4.1.1 Pengambilan Sampel
Metode pengambilan sampel dilakukan dengan cara sampling purposif
yang dikenal juga sebagai sampling pertimbangan dimana sampel ditentukan atas
pertimbangan bahwa populasi sampel adalah homogen dan sampel yang tidak
diambil mempunyai karakteristik yang sama dengan sampel yang sedang Analisis
2.4.1.2 Identifikasi sampel
Identifikasi sampel dilakukan oleh bagian Herbarium Fakultas MIPA
Biologi Universitas syiah Kuala, Banda Aceh. Hasil identifikasi sampel yaitu
kelapa hijau (Cocos nucivera L. varietas viridis) dan kelapa gading/kuning
(Cocos nucivera L. varietas eburnia)
2.4.1.3 Penyiapan Sampel
Masing masing jenis kelapa disiapkan 3 buah, kemudian dibuka mulai
dari sabut bagian atas buah kelapa, sampai Air kelapa bisa dituangkan dan
kemudian diletakkan dalam wadah kaca atau plastik , Air kelapa digabung
menjadi satu bagian berdasarkan jenis varietas kelapa tersebut (Haswell, 1991).
2.4.2 Proses Destruksi Basah Untuk Air kelapa Muda
Sebanyak 5 ml sampel Air kelapa muda dimasukkan ke dalam
erlemeyer lalu ditambahkan 15 mL HNO3(p) dibiarkan selama ± 24 jam
Kemudian didestruksi dengan menggunakan hot plate sampai larutan berubah
menjadi jernih dan uap nitrat habis pada suhu 100°C didinginkan, dimasukkan ke
dalam labu tentukur 100 ml, dibilas erlemeyer dengan aquabidest sebanyak tiga
kali masing masing ± 5ml, hasil pembilasan disatukan dengan larutan dalam labu
tentukur ditepatkan dengan aquabidest sampai garis tanda. Disaring dengan kertas
saring Whatman no 42, dan 10% larutan pertama dibuang untuk menjenuhkan
kertas saring kemudian larutan selanjutnya ditampung ke dalam botol. Larutan ini
2.4.3 Pemeriksaan Kualitatif 2.4.3.1 Kalium
2.4.3.1.1 Uji Kristal Kalium dengan Asam Pikrat
Larutan sampel diteteskan 1-2 tetes pada object glass kemudian ditetesi
dengan larutan asam pikrat, dibiarkan ± 5 menit lalu diamati di bawah mikroskop.
Jika terdapat Kalium, akan terlihat kristal berbentuk jarum-jarum besar.
2.4.3.2 Natrium
2.4.3.2.1 Uji Kristal Natrium dengan Asam Pikrat
Larutan sampel diteteskan 1-2 tetes pada object glass kemudian ditetesi
dengan larutan asam pikrat, dibiarkan ± 5 menit lalu diamati di bawah mikroskop.
Jika terdapat Natrium, akan terlihat kristal berbentuk jarum halus (Vogel, 1990).
2.4.4 Pemeriksaan Kuantitatif
2.4.4.1 Penentuan Panjang Gelombang Maksimum
Penentuan panjang gelombang absorbsi maksimum dilakukan berdasarkan
pengaturan alat spektrofotometer serapan atom yang telah distandarisasi, yaitu
panjang gelombang untuk logam Kalium 769,9 nm dan Natrium 589,6 nm.
2.4.4.2 Penentuan Linearitas Kurva Kalibrasi Kalium
Larutan standar kalium (1000 µg/ml) sebanyak 1,0 ml, dimasukkan ke
dalam labu tentukur 100 ml, ditambah dengan 10 ml HNO3 5 N, dicukupkan
dengan aquabidest sampai garis tanda. Dari larutan tersebut (10µg/ml)
masing-masing dipipet 10 ml; 15 ml; 20 ml; 25 ml 30 ml; dimasukkan kedalam labu
tentukur 100 ml dan ditambahkan dengan 10 ml HNO3 5 N, diencerkan dengan
µg/ml; 1,5 µg/ml; 2 µg/ml; 2,5 µg/ml; 3,0 µg/ml, lalu dilakukan pengukuran pada
panjang gelombang 769,9 nm
2.4.4.3.Penentuan Linearitas Kurva Kalibrasi Natrium
Larutan standar Natrium (1000 µg/ml) sebanyak 1,0 ml dimasukkan ke
dalam labu tentukur 100 ml, ditambahkan dengan 10 ml HNO3 5 N lalu
diencerkan dengan aquabidest sampai garis tanda. Dari larutan tersebut (10
µg/ml) dipipet 3,0 ml; 6,0 ml; 9,0 ml; 12 ml; 15 ml; kedalam labu 100 ml
diencerkan dengan aquabidest sampai garis tanda sehingga diperoleh larutan
dengan konsentrasi 0,3 µg/ml; 0,6 µg/ml; 0,9 µg/ml; 1,2 µg/ml; dan 1,5 µg/ml.
lalu dilakukan pengukuran pada panjang gelombang 589,6nm.
2.5.4 Penentuan kadar logam kalium dan Natrium dalam Sampel
Larutan sampel yang telah didestruksi diukur absorbansinya dengan
spektrofotometer serapan atom pada panjang gelombang 769,9 nm dan 589,6 nm.
Pengukuran ini dilakukan terhadap keenam sampel perulangan yang telah
didestruksi. Nilai absorbansi yang diperoleh berada dalam rentang kurva kalibrasi.
Kadar natrium dapat dihitung dengan rumus :
Kadar (µg/ml) = W CxVxFp
Keterangan : C = Konsentrasi larutan sampel (µg/ml)
V = Volume larutan sampel (ml)
Fp = Faktor pengenceran
2.5.5 Analisis Statistik
2.5.5.1 Analisis Kadar Secara Statistik
Untuk mengetahui diterima atau tidaknya data penelitian, maka data yang
diperoleh dianalisis secara statistk, dengan cara kadar Kalium dan Natrium yang
diperoleh dari hasil pengukuran masing-masing 6 larutan sampel, diuji secara
statistik dengan uji t. Data diterima jika t hitung < t tabel pada interval kepercayaan
95% dengan nilai α 0,05 dengan metode standar deviasi dengan rumus :
SD =
( )
1 -n
X -Xi 2
∑
Keterangan : Xi = Kadar sampel
X = Kadar rata-rata sampel −
n = jumlah pengulangan
⅀ = jumlah
Untuk mencari t hitung digunakan rumus :
t hitung =
n SD
X X
/ −
Keterangan: X = Kadar sampel
SD = standar deviasi
n = jumlah pengulangan
X = kadar rata rata sampel
2.5.5.2 Rata – Rata Kadar Kalium dan Natrium
Kadar kalium dan natrium ditentukan rata-ratanya secara statistik dengan
taraf kepercayaan 95% dengan rumus sebagai berikut :
Keterangan : µ = interval kepercayaan
X = kadar rata-rata sampel
t = harga t tabel sesuai dengan dk = ( n-1)
dk = derajat kebebasan α = tingkat kepercayaan SD = standar deviasi
n = jumlah pengulangan (Sudjana, 2002)
2.5.5.3 Pengujian Beda Nilai Rata-Rata
Sampel yang dibandingkan adalah independen dan jumlah pengamatan
masing-masing lebih kecil dari 30 dan variansi (σ) tidak diketahui sehingga
dilakukan uji F untuk mengetahui apakah variansi kedua populasi sama (σ1 = σ2) atau berbeda (σ1≠ σ2) dengan menggunakan rumus:
Fo = 2 2 2 1
S S
Keterangan : Fo = Beda nilai yang dihitung
S1 = Standar deviasi sampel 1
S2 = Standar deviasi sampel 2
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F maka dilanjutkan dengan uji t dengan rumus:
(X1 – X2)
t
o =Sp √1/n1 + 1/n2
Keterangan : X1 = kadar rata-rata sampel 1
X2 = kadar rata-rata sampel 2
Sp = Simpangan baku
n 1 = Jumlah pengulangan sampel 1
n 2 = Jumlah pengulangan sampel 2
S1 = Standar deviasi sampel 1
dan jika Fo melewati nilai kritis F maka dilanjutkan dengan uji t dengan rumus :
(X1 – X2)
t
o =√S12/n1 + S22/n2
Keterangan : X1 = kadar rata-rata sampel 1
X2 = kadar rata-rata sampel 2
S1 = Standar deviasi sampel 1
S2 = Standar deviasi sampel 2
n 1 = Jumlah pengulangan sampel 1
n 2 = Jumlah pengulangan sampel 2
Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai kritis t,
dan sebaliknya.
(Sabri dan Hastono, 2006) 2.5.6 Metode Validasi
2.5.6.1 Uji Perolehan kembali (Recovery Ttest) 2.5.6.1.1 Pembuatan Larutan Standar
Larutan standar Kalium dan Natrium (1000 µg/ml) sebanyak 1,0 ml
dimasukkan ke dalam labu tentukur 100 ml, ditambahkan dengan 10 ml HNO3 5
N lalu diencerkan dengan aquabidest hingga garis tanda (konsentrasi 10 µg/ml).
a. Pembuatan Larutan standar 2 µg/ml
Larutan standar kalium (10µg/ml) sebanyak 20 ml dimasukkan kedalam labu
tentukur 100 ml, kemudian ditambahkan 10 ml larutan HNO3 5N ditepatkan
sampai garis tanda dengan aquabidest (konsentrasi 2 µg/ml).
b. Pembuatan Larutan standar 0,9 µg/ml
Larutan Standar Natrium (10 µ g/ml) sebanyak 9 ml dimasukkan kedalam labu 100
ml, ditambahkan dengan 10 ml larutan HNO3 5N, ditempatkan sampai garis tanda
2.5.6.1.2 Prosedur Uji Perolehan kembali (Recovery Test)
Uji perolehan kembali atau recovery dilakukan dengan metode
penambahan larutan standar (standard addition method). Dalam metode ini, kadar
logam dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan
kadar logam dalam sampel setelah penambahan larutan standar dengan
konsentrasi tertentu (Ermer, 2005). Larutan standar yang ditambahkan yaitu 10 ml
larutan standar Kalium (konsentrasi 2 µg/ml), dan 10 ml larutan standar Natrium
(konsentrasi 0,9 µg/ml).
Sampel yang telah dihomogenkan sebanyak 5 ml ditambahkan dengan
larutan standar Kalium sebanyak 10 ml (konsentrasi 2 µg/ml) kemudian
dilanjutkan dengan prosedur destruksi basah seperti yang telah dilakukan
sebelumnya. Dilakukan langkah kerja yang sama untuk uji perolehan kembali
logam natrium, dengan penambahan larutan baku masing-masing.
Perhitungan uji perolehan kembali dapat dihitung dengan rumus sebagai
berikut :
Persen perolehan kembali = − ×100%
A A F
C C C
Keterangan :
CF = konsentrasi total sampel
CA = konsentrasi sampel sebenarnya (awal)
CA = konsentrasi larutan baku yang ditambahkan
2.5.7 Uji ketelitian/keseksamaan (Precision)
Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat
kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang. Adapun uji ketelitian yaitu koefisien variasi atau Relative Standard
Deviation (% RSD). Harga persentase koefisien variasi (%RSD) ditentukan
dengan rumus:
RSD = x100%
x SD
Keterangan:
Keterangan : X − = Kadar rata-rata sampel SD = Standar Deviasi
RSD = Relative Standard Deviation (Harmita, 2004).
2.5.8 Penentuan Batas Deteksi dan Batas Kuantitasi
Batas deteksi atau Limit of Detection (LOD) adalah jumlah terkecil analit
dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan,
sedangkan batas kuantitasi atau Limit of Quantitation (LOQ) merupakan kuantitas
terkecil analit dalam sampel yang masih dapat memberikan kriteria cermat dan
seksama (Gandjar, I. G., dan Rohman, A. 2007).
Batas deteksi dapat dihitung berdasarkan pada Standar Deviasi (SD) dari
kurva antara respon dan kemiringan (slope) dengan rumus :
SD = 2 ) ( 2 − −
∑
n Yi Y LOD = slope SD x 3Sedangkan untuk penentuan batas kuantitasi dapat digunakan rumus :
BAB IV
HASIL DAN PEMBAHASAN 3.1 Hasil Identifikasi sampel
Berdasarkan hasil identifikasi Jenis kelapa yang diambil sebagai sampel
adalah kelapa hijau (Cocos nucisvera L. Varietas viridis) dan kelapa gading
(Cocos nucisvera L. Varietas eburnea) sampel yang diambil dari kebun kelapa
desa lama kecamatan Pancur batu, Deli Serdang. Kemudian dilakukan identifikasi
terhadap sampel tersebut. Kelapa yang digunakan sebagai sampel adalah kelapa
yang masih muda, diambil berdasarkan ketebalan daging buah kelapa yaitu 2 mm.
Hasil identifikasi dapat dilihat pada lampiran 1 dan 2
3.2 Pemeriksaan Kualitatif
Analisis kualitatif dilakukan sebagai analisis pendahuluan untuk
mengetahui ada atau tidaknya kalium dan natrium dalam sampel.
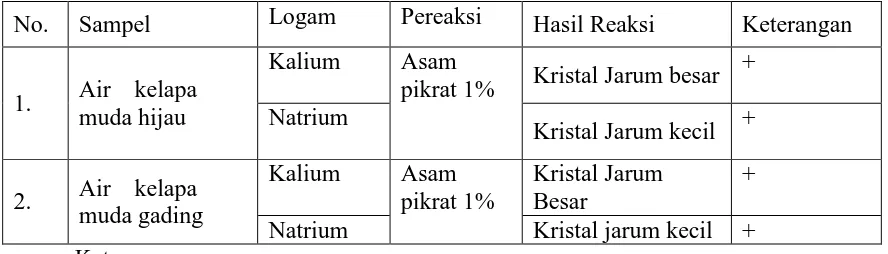
No. Sampel Logam Pereaksi Hasil Reaksi Keterangan
1. Air kelapa muda hijau
Kalium Asam
pikrat 1% Kristal Jarum besar +
Natrium
Kristal Jarum kecil +
2. Air kelapa muda gading
Kalium Asam pikrat 1%
Kristal Jarum Besar
+
Natrium Kristal jarum kecil + Keterangan:
+ = mengandung logam
[image:42.595.112.556.443.570.2]– = tidak mengandung logam
Tabel di atas menunjukkan bahwa Air kelapa muda hijau dan Air
kelapa muda gading mengandung logam kalium dan natrium. Sampel dikatakan
penambahan asam pikrat dan mengandung natrium jika menghasilkan kristal
jarum halus dapat dilihat pada Lampiran 5 (Vogel, 1979).
3.3 Pemeriksaan Kuantitatif
3.3.1 Linearitas Kurva Kalibrasi Kalium Dan Natrium
Kurva kalibrasi logam Kalium dan Natrium diperoleh dengan cara
mengukur absorbansi dari larutan standar kedua logam pada konsentrasi yang
berbeda-beda. Logam Kalium diukur pada panjang gelombang 769,9 nm dan
Natrium pada panjang gelombang 589,6 nm. Berdasarkan pengukuran kurva
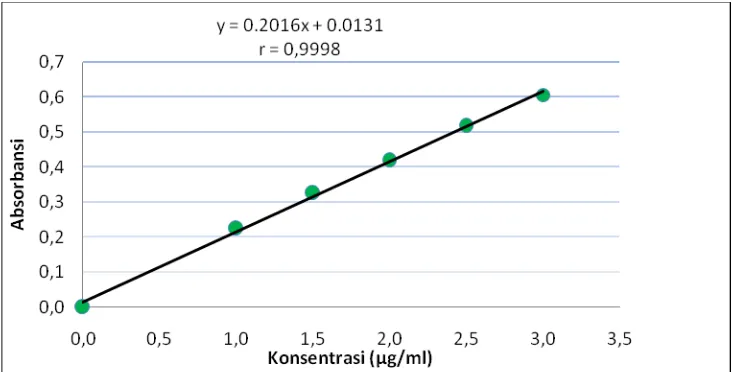
kalibrasi untuk logam kalium dengan rentang konsentrasi 0,5µg/ml sampai 3
µg/ml diperoleh persamaan garis regresi yaitu: Y= 0,2016X . Logam
Natrium pada rentang konsentrasi 0,3 µg/ml sampai 1,5µg/ml persamaan regresi
yang diperoleh adalah y = 0,3851x + 0,0068
Data hasil pengukuran absorbansi larutan standar kalium dan natrium serta
contoh perhitungan persamaan garis regresi dapat dilihat pada Lampiran 6
[image:43.595.113.479.526.712.2]sampai 10 dan, kurva kalibrasi larutan standar kalium dan natrium dapat dilihat pada Gambar 1 dan Gambar 2 berikut.
Gambar 2. Kurva Kalibrasi Larutan Standar Natrium
Berdasarkan gambar kedua kurva kalibrasi di atas diperoleh hubungan
antara konsentrasi logam dan serapannya dengan nilai koefisien korelasi (r)
0,9998 untuk kalium dan untuk natrium sebesar 0,9992. Nilai koefisien korelasi
yang diperoleh dari logam Kalium dan Natrium dapat diterima karena sesui
persyaratan yaitu: Nilai koefisien korelasi (r) terbaik adalah yang mendekati 1.
Hal ini sesuai dengan Hukum Lambert-Beer yaitu A = abc, dimana nilai
absorbansi (A) berbanding lurus dengan nilai konsentrasi (c) ( Rohman, A. 2007).
3.3.2 Kadar Kalium Dan Natrium Dalam Air kelapa hijau dan Air kelapa gading/kuning.
Penentuan kadar kalium dan natrium dilakukan secara spektrofotometri
serapan atom. Konsentrasi Kalium dan Natrium dalam sampel ditentukan
berdasarkan persamaan garis regresi linier kurva kalibrasi larutan standar. Analisis
kemudian dilanjutkan dengan perhitungan statistik dengan distribusi t pada taraf
kepercayaan 95% (α = 0,05). Berdasarkan hasil perhitungan statistik tersebut
dapat dilihat pada tabel 2 dibawah ini, dan contoh perhitungannya dapat dilihat
[image:45.595.112.524.167.311.2]pada Lampiran 8 samapai 11 sampai 14
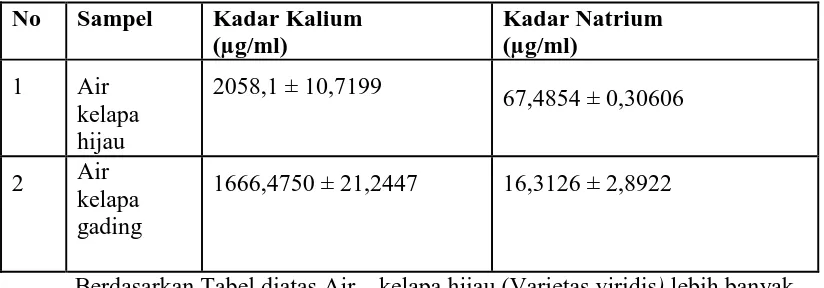
Tabel 2
No Sampel Kadar Kalium (µg/ml)
Kadar Natrium (µg/ml)
1 Air kelapa hijau
2058,1 ± 10,7199
67,4854 ± 0,30606
2 Air kelapa gading
1666,4750 ± 21,2447 16,3126 ± 2,8922
Berdasarkan Tabel diatas Air kelapa hijau (Varietas viridis) lebih banyak
megandung Kalium dan Natrium dibandingkan dengan Air kelapa
gading/kuning (Varietas eburnia). Ini menunjukkan bahwa kadar Kalium dan
Natrium pada Air kelapa sangat berpengaruh terhadapa varietas kelapa tersebut.
Menurut Rindengan, (1995) Komposisi nutrisi dari Air kelapa secara
lagsung dipengaruhi oleh jenis Varietas Kelapa dan perbedaan tingkat kemasakan
buah, secara tidak langsung dipengaruhi oleh lingkungan tumbuh dan
pemeliharaan seperti keadaan tanah dan iklim.
Jumlah kalium yang banyak terdapat dalam Air kelapa yang berasal dari
kelapa hijau yang muda. Kadar Kalium Air kelapa tua 312 mg/L, Air kelapa
Muda 3120 mg/L (child, 1964). Unsur mineral dalam Air kelapa termasuk
Kalium dan Natrium berasal dari penyerapan unsur hara tanah oleh akar
(Suhardiono, L 2000). Banyak sedikitnya unsur hara yang diserap dipengaruhi
3.4.3 Pengujian Beda rata rata
Pengujian beda nilai rata rata bertujuan untuk melihat apakah ada perbedaan
yang signifikan pada rata rata kadar logam Kalium dan Natrium antara Air
kelapa hijau dan Air kelapa gading. Berdasarkan asumsi bahwa sampel berasal
dari varians yang sama maka dilakukan uji F dengan taraf kepercayaan 95%, apa
bila dari hasil diperoleh Fo ≤ FkritisPerhitungan dilanjutkan dengan uji t pada taraf
kepercayaan 5%. Berdasarkan pengujian beda rata rata pada logam Kalium
dengan metode uji ini didapat bahwa kadar kalium pada Air kelapa muda
gading/kuning berbeda dengan kadar Kalium pada Air kelapa muda hijau,
Karena berada pada daerah penolakan, yaitu Fhitung > dari pata Ftabel, dengan nilai
Ftabel = 9,277, Fhitung = 26,5348 kemudian dilanjutkan dengan uji t taraf
kepercayaan 5%, hasil yang didapat berada pada daerah penolakan keritis karena
nilai t hitung lebih besar dari pada ttabel, dengan nilai ttabel = 2,447 dan thitung = 57,6
sehingga disimpulkan terdapat perbedaan yang signifikan antara kadar kalium
pada Air kelapa muda hijau dan Air kelapa muda gading/kuning. Contoh
perhitungan uji beda rata rata dapat dilihat pada lampiran 15 samapai 16
Sementara Untuk logam Natrium pada uji F hipotesis diterima, yang berarti
ada kesamaan/homogenitas antara logam Natrium pada Air kelapa muda hijau
dan Air kelapa muda gading dengan nilai Ftabel 9,277 dan Fhitung 3,0341
kemudian dilanjutkan dengan uji t pada taraf kepercayaan 5%, hasil yang didapat t
hitung lebih besar dari pada ttabel, sehingga hipotesis ditolak, dengan nilai thitung =
652,8 berarti terdapat perbedaan yang signifikan kadar logam Natrium pada Air
3.5 Uji Validasi
3.5.1 Uji Perolehan Kembali (Recovery test)
Akurasi prosedur ditentukan dengan uji perolehan kembali menggunakan
metode Adisi dengan menambahkan sejumlah analit dengan konsentrasi tertentu
pada sampel yang diperiksa lalu di analisis kembali (Harmita, 2004).
Hasil uji perolehan kembali logam Kalium dan Natrium dalam Air
kelapa Muda setelah penambahan larutan standar untuk logam Kalium memiliki
persen rata rata 104%, selanjutnya logam Natrium 84 %.
Contoh perhitungan dan data dapat dilihat pada Lampiran 17 samapai
20. Persen perolehan kembali tersebut menunjukkan ketepatan kerja pada saat pemeriksaan kadar logam dalam sampel. Karena ketepatan dalam kerja
merupakan validasi dari suatu metode yang sesuai penggunaannya sehingga
menghasilkan data analisis yang tepat.
Persen recovery tersebut menunjukkan ketepatan kerja pada saat
pemeriksaan kadar logam dalam sampel. Menurut Ermer (2005), suatu metode
dikatakan teliti jika nilai recovery antara 80-120%.
3.5.2 Uji Presisi
Pada koefisien Variasi (RSD) memberikan ketelitian yang memuaskan.
Hasil perhitungan Menunjukkan RSD untuk masing masing logam adalah 0,43%
untuk kalium dan 0,23% untuk Natrium, contoh perhitungannya dapat dilihat pada
lampiran 21 dan 22. Hasil ini telah memenuhi batas yang telah ditetapkan yaitu kriteria seksama atau diteliti yang diberikan jika metode memberikan koefisien
Variasi 2% atau kurang (Harmita, 2004).
3.5.3 Batas Deteksi dan Batas Kuantitasi
Berdasarkan hasil perhitungan standar deviasai (SD) yang dilakukan, maka
diperoleh batas deteksi (LOD) untuk logam Kalium dan Natrium masing masing
sebesar 0,1849 µg/ml dan 0,0738 µg/ml, Sedangkan batas kuantitasi (LOQ) dari
hasil perhitungan diperoleh sebesar 0,5604 µg/ml dan 0,2237 µg/ml, cara
perhitungan dapat dilihat pada Lampiran 23 samapai 24, sementara hasil
pengukuran batas deteksi dan batas kuantitasi untuk sampel Air kelapa
gading/kuning dengan nilai terendah yaitu 1,6373 µg/ml untuk kalium, dan
0,8113 µg/ml untuk natrium, demikian juga untuk sampel Air kelapa hijau
hasil pengukuran batas deteksi dan kuantitasi dengan nilai terendah yaitu 2,0487
untuk kalium, sedangkan untuk natrium 0,6699 µg/ml. Batas deteksi dan batas
kuantitasi umumnya menentukan suatu analisis sampel dimana konsentrasi analit
diketahui dan dengan menetapkan konsentrasi analit terkecil yang dapat dideteksi
BAB V
KESIMPULAN DAN SARAN
4.1 Kesimpulan
1. Berdasarkan hasil penelitian kadar Kalium pada Air kelapa muda hijau
dengan ketebalan kulit ± 2mm yaitu 2058,1 ± 10,7199 µg/ml dan Natrium
67,4854 ± 0,3060 µg/ml pada Air kelapa muda gading/kuning kadar
kalium1666,4750 ± 21,2447 µg/ml dan Natriumnya 16,3126 ± 2,8922µ g/ml .
2. Berdasarkan hasil penelitian terdapat perbedaan kadar Kalium dan Natrium
pada Air kelapa muda hijau dan Air kelapa muda kuning/gading, kadar
Kalium
dan Natrium pada Air kelapa hijau lebih besar dari pada Kadar Kalium dan
Natrium pada Air kelapa gading/kuning
4.2 Saran
Disarankan kepada peneliti selanjutnya agar memeriksa mineral lain pada
DAFTAR PUSTAKA
Anderson, R. (1987). Food Analysis. Edisi kedua. New York:Avi Book. Hal. 613-615.
Anonim, (2011)
Annisa.R.(2010). Perbedaan kadar kalium pada Air kelapa hijau (cocos viridis) didataran tinggi dan dataran rendah. Undegraduate Theses from
JTPTUNIMUS. Unimus Digital Library Universitas Muhammadiyah
Semarang. Hal 1-3
Almatsier, S. (2002). Prinsip Dasar Ilmu Gizi. Cetakan II. Jakarta: PT.Gramedia Pustaka Utama. Hal 228, 235-236.
Bender, G.T. (1987). Principal of Chemical Instrumentation. Philadhelphia:W.B. Sounders Company. Page. 98.
Budianto, A.K. (2009). Dasar Dasar Ilmu Gizi. Cetakan ke IV. Malang: UMM Press. Hal 88
Child,R.(1964). Tropical Agriculture Series. Logman. Group London. Page 77
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Departemen Kesehatan RI. Jakarta.
Gandjar, I. G., dan Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan Pertama. Yogyakarta: Pustaka Belajar. Hlm. 27, 463
Haswell, S.J. (1991). Atomic Absorption Spectrometry. Amsterdam: Elsevier. page.202
Harmita.(2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. Vol 1 (3): 117-135.
J. Ermer, J. H. McB. Miller. (2005). Method Validation in Pharmaceutical
Analysis. Weinheim : WILEY-VCH Verlag GmbH & Co. KGaA. Page.
117 -135
Kartasapotra,G. (2008).Ilmu Gizi Korelasi gizi, Kesehatan dan Produktivitas Kerja. Cetakan VII.Jakarta: rineka Cipta. Hal 94 – 95.
Kemala, D.C.B. (1978).Changes in The Chemical Composition of nut Water and
Kernel during development of coconut. P. 340 -346
Rendengan,B, (2004). Potensi Buah Kelapa Muda Untuk Kesehatan dan Pengolahannya. Manado:Balai penelitian kelapa dan Palma. Hal 2-4
Rony.p.(1999). Aneka Produk Olahan Kelapa. Cetakan VII. Jakarta: PT.Penebar Swadaya. Hal 1
Suhardiyono,L. (1989). Tanaman Kelapa Budidaya dan Pemanfaatannya. Yogyakarta: Kanisius.Hal 160-161
Sabri, L. dan Hastono, S.P. (2006). Statistik Kesehatan. Jakarta: PT Raja Grafindo Persada. Halaman 112-118
Sudjana. (2001). Metode Statistika. Edisi Keenam. Bandung : Tarsito. Hal 167,
206.
Suhadirman, (1999). Bertanam Kelapa Hibrida. Cetakan ke II. Jakarta: PT.Penebar Swadaya.Hal 15,27
Khopkar, S.M. (1990). Konsep Dasar Kimia Analitik. Penerjemah: Saptorahardjo, A. Jakarta: UI-Press. Hal. 283.
Mita.W. (1990). Bertanam Kelapa Kapyor. Cetakan ke III. Jakarta: PT.Peneber Swadaya.Hal 8-9
Nurul.P. (2007). Nyiur Melambai.cetakan I. Bandung: PT sinergi Pustaka Indonesia.Hal 21-29
Warisno. (2003). Budidaya Kelapa Genjah. Yogyakarta: Kanisius IKAPI. Hal 15
Woodroof ,J.G.,( 1979). Cococnut Production, Procesing Products.The Avi Publishing Company, Inc.Wesport,Connectic
Vogel, A. I. (1990). Analisis Anorganik Kualitatif Makro dan Semimikro. Bagian
I. Penerjemah: Setiono, L., dkk. Jakarta: Kalman Media Pustaka. Hal. 262,
Lampiran 3. Gambar Sampel Kelapa
Gambar 1. Kelapa Hijau (Cocos nucivera L. Varietas vieidis)
[image:54.595.119.385.421.637.2]Lampiran 4. Bagan Proses Destruksi Logam Kalium dan Natrium
Dimasukkan kedalam erlemeyer
5 ml
Ditambahkan 15 ml HNO3 (p)
Didiamkan selama ± 24 jam
Didestruksi sampai larutan
berwarna jernih pada suhu 100°C
Didinginkan
Dimasukkan kedalam labu tentukur
100 ml
Ditepatkan dengan aquabidest
sampai garis tanda
Disaring dengan kertas saring
whatman no.42 dengan membuang
10 ml larutan pertama hasil penyaringan
Diuji kualitatif untuk Kalium dan
Natrium dengan penambahan asam
pikrat
Di ukur dengan Spektrofotometer
Serapan atom pada panjang
Gelombang 769,9 untuk Kalium
dan 589,6 nm untuk Natrium. Campuran 3 buah Air
kelapa muda
Sampel + HNO3 (p)
100 ml larutan sampel
Larutan sampel
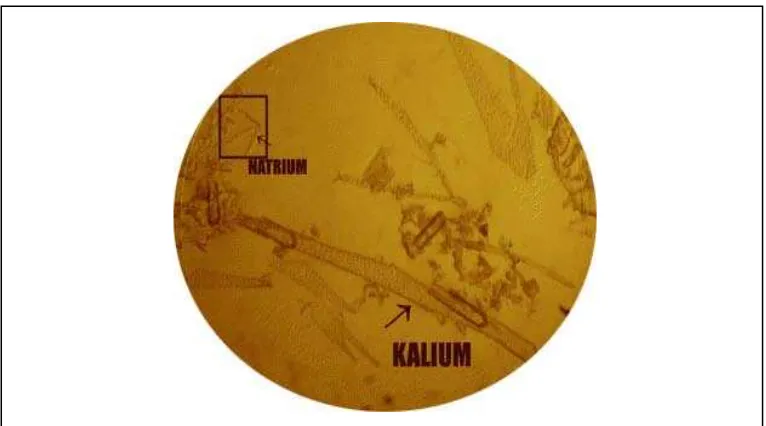
Lampiran 5. Hasil Analisi Kualitatif Kalium dan Natriumpada Air kelapa hijau NATRIUM
Gambar 3. Gambar Kristal Kalium dan Natrium dengan penambahan asam pikrat pada sampel Air kelapa Muda hijau
Gambar 4. Gambar Kristal Kalium dan Natrium dengan penambahan asam pikrat pada sampel Air kelapa Muda gading/kuning
[image:56.595.119.502.474.687.2]Lampiran 6. Data Hasil Pengukuran Absorbansi Larutan Standar Kalium
No Konsentrasi (µ g/ml) Absorbansi (A)
1
0.0000 0.0000
2
1.0000 0.2253
3
1.5000 0.3254
4
2.0000 0.4194
5
2.5000 0.5175
6
3.0000 0.6070
No X Y XY X2 Y2
1
0.0000 0.0000 0.0000 0.0000 0.0000
2
1.0000 0.2253 0.2253 1.0000 0.0508
3
1.5000 0.3254 0.4881 2.2500 0.1059
4
2.0000 0.4194 0.8388 4.0000 0.1759
5
2.5000 0.5175 1.2938 6.2500 0.2678
6
3.0000 0.6070 1.8210 9.0000 0.3684
∑ 10.0000 2.0946 4.6670 22.5000 0.9688
Rerata
a
a
a
a
a = 0,2016
b - a
b = 0,3491 – (0,2016) ( 1,6667)
b = 0,3491 – 0,3359
b = 0,0131
Maka persamaan regresinya adalah : Y= 0,2016
r
r
r
r
r
Lampiran 7. Data Hasil Pengukuran Absorbansi Larutan Standar Natrium
No Konsentrasi (µ g/ml) Absorbansi (A)
1
0.0000 0.0000
2
0.3000 0.1241
3
0.6000 0.2383
4
0.9000 0.3672
5
1.2000 0.4673
6
1.5000 0.5771
No X Y XY X2 Y2
1
0.0000 0.0000 0.0000 0.0000 0.0000
2
0.3000 0.1241 0.0372 0.0900 0.0154
3
0.6000 0.2383 0.1430 0.3600 0.0568
4
0.9000 0.3672 0.3305 0.8100 0.1348
5
1.2000 0.4673 0.5608 1.4400 0.2184
6
1.5000 0.5771 0.8657 2.2500 0.3330
∑ 4.5000 1.7740 1.9371 4.9500 0.7584
Rerata
a
a
a
a
a = 0,3851
b - a
b = 0,2957 – (0,3851) ( 0,7500)
b = 0,2957 – 0,288825
b = 0,0068
Maka persamaan regresinya adalah : Y= 0,3851 X
r
r
r
r
r
Lampiran 8. Data Volume Sampel, Absorbansi, kadar rata rata, kadar
logam Kalium, Natrium, dan kadar sebenarnya pada sampel Air kelapa gading dan Air kelapa hijau.
No
Sampel Logam
Volume
Sampel (ml)
Absorbansi Konsentrasi
(µg/ml)
Kadar sampel (µg/ml)
Kadar sebenarnya
(µg/ml)
1 Air kelapa gading
Kalium 5 0,3478 1,6603 1660,3000
5 0,3497 1,6692 1669,2000
5 0,3495 1,6687 1668,7000 1666,4750±21,2447
5 0,3432 1,6375 1637,5000
5 0,3485 1,6677 1667,7000
5 0,3416 1,6295 1629,5000
Kadar rata -rata 1655,4834
Natrium 5 0,3231 0,8214 16,4280
5 0,3242 0,8253 16,5060
5 0,3192 0,8113 16,2260 16,3126±2,8922
5 0,3222 0,8191 16,3820
5 0,3212 0,8165 16,3300
5 0,3194 0,8118 16,2360
Kadar rata- rata 16,3514
2. Air Kelapa hijau
Kalium 5 0,4381 2,1082 2108,2000
5 0,4273 2,0546 2054,6000 2058,1000 ±10,7199
5 0,4282 2,0591 2059,1000
5 0,4245 2,0606 2060,6000
5 0,4280 2,0581 2058,1000
5 0,4257 2,0467 2046,7000
Kadar rata rata 2064,5600
Natrium 5 0,2666 0,6747 67,4700
5 0,2648 0,6699 66,9999
5 0,2675 0,6769 67,6900
5 0,2710 0,6861 68,6100
5 0,2665 0,6744 67,4400 67,3126± 0,3060
5 0,2661 0,6734 67,3400
Lampiran 9. Contoh Perhitungan kadar logam Kalium dalam sampel Air kelapa gading.
Misalnya untuk kadar Kalium dalam sampel Air kelapa gading dengan volume 5
ml absorbansi 0,3478
X = Konsentrasi sampel
Y = Absorbansi sampel
Persamaan garis regresi yang diperoleh dari kurva kalibrasi adalah
y = 0,2016x + 0,0131
x =
x = 1,6603 µg/ml
Maka konsentrasi sampel tersebut adalah 1,6603 µg/ml
Kadar = <