JANTAN DEWASA YANG DIPAPARI TUAK (ALKOHOL)
T E S I S
O l e h: SION SEMBIRING NIM. 087008015/BM
PROGRAM STUDI MAGISTER ILMU BIOMEDIK FAKULTAS KEDOKTERAN
JANTAN DEWASA YANG DIPAPARI TUAK (ALKOHOL)
T E S I S
Diajukan Untuk Melengkapi Persyaratan Memperoleh Gelar Magister Biomedik Pada Program Studi Magister Ilmu Biomedik
Fakultas Kedokteran Universitas Sumatera Utara
O l e h:
SION SEMBIRING NIM. 087008015/BM
PROGRAM STUDI MAGISTER ILMU BIOMEDIK FAKULTAS KEDOKTERAN
PANITIA PENGUJI TESIS:
Ketua : Prof. Dr. Drs. Dwi Suryanto, M.Sc. Anggota : 1. dr. Betty, Sp.PA.
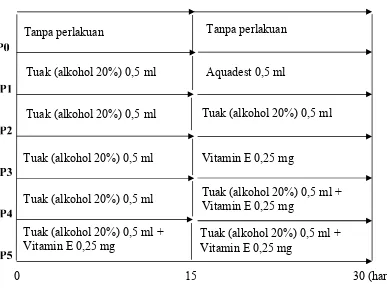
konsumsi tuak (alkohol 20%) dapat menyebabkan terjadinya peroksidasi lipid sel membran dan merusak organisasinya. Radikal bebas merupakan suatu atom atau molekul yang tidak mempunyai pasangan elektron dan dapat merusak molekul-molekul penting bagi fungsi seluler. Dalam penelitian ini, pemberian asupan antioksidan (vitamin E) diusulkan dapat menurunkan efek radikal bebas dalam tubuh.Tujuan penelitian ini adalah untuk mengetahui pengaruh pemberian vitamin E terhadap perubahan bobot dan gambaran mikroskopis tubulus proksimal ginjal mencit (Mus musculus, L.) jantan dewasa yang dipapari tuak (alkohol 20%). Mencit jantan dibagi dalam 6 kelompok, tiap kelompok terdiri dari 5 ekor; P0= Tanpa perlakuan; P1= Tuak (alkohol 20%) 0,5 ml 15 hari + Aquadest 0,5 ml 15 hari; P2= Tuak (alkohol 20%) 0,5 ml 30 hari; P3= Tuak (alkohol 20%) 0,5 ml 15 hari + Vitamin E 0,25 mg 15 hari; P4= Tuak (alkohol 20%) 0,5 ml 15 hari + Tuak (alkohol 20%) 0,5 ml & Vitamin E 0,25 mg 15 hari; P5= Tuak (alkohol 20%) 0,5 ml & Vitamin E 0,25 mg 30 hari. Pada akhir perlakuan sesuai dengan kelompok, dilakukan pemeriksaan terhadap histologis tubulus proksimal ginjal mencit. Hasil penelitian menunjukkan bahwa vitamin E mempunyai pengaruh terhadap perubahan bobot ginjal mencit jantan dewasa yang dipapari tuak (alkohol 20%) secara tidak bermakna (p>0,05). Pemberian vitamin E selama 15 hari setelah pemberian tuak (alkohol 20%) 15 hari (kolompok P3) berpengaruh bermakna dibandingkan dengan kelompok P0 (kontrol, p<0,05) dan berpengaruh tidak bermakna dibandingkan dengan kelompok P1 (tuak/alkohol 20% selama 15 hari ditambah aquadest selama 15 hari). Meskipun demikian pemberian vitamin E cenderung menurunkan sel ginjal (tubulus proksimal) yang mengalami nekrotik.
In the condition of oxidative stress, the existence of free radical caused by the consumption of fermented palm wine/tuak (alcohol 20%) may lead into the occurrence of membrane cell lipid peroxidation and it damaged its organization. Free radical is as an atom or the molecule without electron pair and it may damage the important molecules for the function of cellular. In this research, the proposed antioxidant administration (vitamin E) can reduce the effect of free radical in body. The objective of this research is to know the influence of vitamin E giving to the change of weight and the description of adult male mice kidney proximal tubulus microscopic (Mus musculus, L) with tuak exposure (alcohol 20%). Male mice are divided into 6 (six) groups and each contained 5 (five) mice; P0 = without treatment, P1= tuak (alcohol 20%) 0,5 ml for 15 days + aquadest 0,5 ml for 15 days; P2 = tuak (alcohol 20%) 0,5 ml for 30 days, P3 = tuak (alcohol 20%) 0,5 ml for 15 days + vitamin E 0,25 mg for 15 days; P4 = tuak (alcohol 20%) 0,5 ml for 15 days + vitamin E 0,25 mg for 15 days; P5 = tuak (alcohol 20%) 0,5 ml & vitamin E 0,25 mg for 30 days. At the end of the treatment in accordance with the group, checking was carried out to mice kidney proximal tubulus histology. The results of the research showed that vitamin E influenced of adult male mice weight with tuak exposure (alcohol 20%, p>0,05). Vitamin E administration for 15 days after administration the tuak (alcohol 20%) for 15 days (P3 group) has significant influenced compared to P0 group (control, p<0,05) and to P1 group (tuak/alcohol 20% for 15 days plus aquadest for 15 days). However, vitamin E tended to reduce the kidney cell (proximal tubulus) suffering from the necrotic.
N a m a : Sion Sembiring
N I P : 19711217 199603 1 004. Pangkat/Gol. Ruang : Penata, III/c
J a b a t a n : Lektor
Tempat dan Tgl. Lahir : Tanjung Keriahan, 17 Desember 1971 A g a m a : Kristen Protestan
A l a m a t : Jl. Empat Lima 175 Sidikalang, Kabupaten Dairi
SD Negeri 050610 Tanjung Keriahan Kab. Langkat, tamat tahun 1984. SMP Swasta Berdikari Tanjung Keriahan Kab. Langkat, tamat tahun 1987. SMA Swasta Taman Siswa Binjai Kota Madya Binjai, tamat tahun 1990. D-III Keperawatan (Akademi Perawat) Darmo Medan, tamat tahun 1994. D-IV Perawat Pendidik Universitas Sumatera Utara Medan, tamat tahun 2001. S-2 (Pascasarjana) Program Studi Magister Ilmu Biomedik Fakultas
Kedokteran Universitas Sumareta Utara Medan, 2008-2011.
1996-1997 : Staf Keperawatan di RSUD Sidikalang, Kab. Dairi.
1997-2000 : Staf Pendidik di Sekolah Perawat Kesehatan Pemerintah Kab. Dairi.
2001-2005 : Staf Pendidik di Akper Pemerintah Kab. Dairi. 2001-2005 : Bendahara Rutin di Akper Pemerintah Kab. Dairi. 2001-2005 : Pembantu Direktur I di Akper Pemerintah Kab. Dairi. 2005-2007 : Pelaksana Tugas Direktur di Akper Pemerintah Kab. Dairi. 2007-sekarang : Bendahara Rutin di Akper Pemerintah Kab. Dairi.
Puji dan syukur penulis sampaikan kehadirat Tuhan Yang Maha Kuasa atas berkat, rahmat dan anugerah-Nya sehingga penulis dapat menyusun dan menyelesaikan tesis ini. Penulisan tesis ini merupakan salah satu persyaratan dalam memperoleh Gelar Magister pada Program Studi Magister Ilmu Biomedik Fakultas Kedokteran Universitas Sumatera Utara Medan. Adapun judul penelitian ini adalah Pengaruh Pemberian Vitamin E Terhadap Perubahan Bobot Dan Gambaran Mikroskopis Tubulus Proksimal Ginjal Mencit (Mus musculus, L.) Jantan Dewasa Yang Dipapari Tuak (Alkohol) .
Proses penulisan tesis ini tidak terlepas dari bimbingan, bantuan, dukungan, doa dan perhatian dari berbagai pihak, serta pada kesempatan ini ucapan terima kasih saya sampaikan kepada yang terhormat:
1. Bapak Prof. Dr. dr. Syahril Pasaribu, DTM&H, M.Sc, (CTM), SpA(K)., Rektor Universitas Sumatera Utara.
2. Bapak Prof. dr. Gontar A. Siregar, SpPD-KGEH., Dekan Fakultas Kedokteran Universitas Sumatera Utara.
3. Ibu dr. Yahwardiah Siregar, Ph.D., Ketua Program Studi Magister Ilmu Biomedik Fakultas Kedokteran Universitas Sumatera Utara.
6. Ibu dr. Alya Amila Fitrie, M.Kes., Ketua Komisi Pembanding yang telah banyak memberi masukan dan saran untuk perbaikan dalam penyelesaian tesis ini.
7. Ibu dr. Jessy Chrestella, Sp.PA., Anggota Komisi Pembanding yang telah banyak memberi masukan dan saran untuk perbaikan dalam penyelesaian tesis ini.
8. Pimpinan dan seluruh staf Laboratorium Kimia Bahan Makanan (KBM) Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara (FMIPA USU) Medan, yang menyediakan tempat untuk penggunaan laboratorium dan bantuan tenaga laboran kepada penulis untuk menyelesaikan tesis ini.
9. Pimpinan, seluruh staf dan adik-adik mahasiswa Departemen Biologi FMIPA Universitas Sumatera Utara Medan, yang menyediakan tempat dan membantu penulis untuk penelitian dalam menyelesaikan tesis ini.
10. Pimpinan dan seluruh staf Laboratorium Patologi Anatomi Fakultas Kedokteran Universitas Sumatera Utara Medan, yang telah menyediakan tempat untuk pemeriksaan hasil penelitian tesis ini.
Kabupaten Dairi dan Bapak Direktur Akademi Keperawatan Pemerintah Kabupaten Dairi, yang telah memberikan kesempatan kepada penulis untuk mengikuti pendidikan pada Sekolah Pascasarjana Program Studi Magister Ilmu Biomedik Fakultas Kedokteran Universitas Sumatera Utara Medan. 13. Terima kasih yang tulus penulis ucapkan kepada Isteri tercinta Setyawati Br.
Ginting, AM.Keb. dan anak-anak yang senantiasa memberi dukungan moril dan materil sehingga penulis dapat menyelesaikan pendidikan di Sekolah Pascasarjana Program Studi Magister Ilmu Biomedik Fakultas Kedokteran Universitas Sumatera Utara Medan.
Akhir kata penulis berharap semoga tesis ini dapat bermanfaat bagi para pembaca dan mendapat penambahan ilmu dan wawasan serta menciptakan ide-ide untuk penelitian selanjutnya.
Medan, Juli 2011. Penulis
Halaman
2.1.2. Nira Aren (Arenga pinnata) ... 11
2.2. Radikal Bebas dan Antioksidan ... 12
2.2.1. Radikal Bebas ... 12
2.2.2. Antioksidan ... 13
2.2.3. Vitamin E ... 14
2.2.4. Fungsi Fisiologi dan Farmakokinetika Vitamin E ... 15
2.2.5. Efek Kimia Vitamin E Terhadap Ginjal ... 16
2.3. Ginjal ... 17
2.3.1. Anatomi dan Fisiologi Ginjal ... 17
2.3.2. Fungsi Ginjal ... 20
2.3.3. Tubulus Proksimal ... 22
BAB 3. METODOLOGI PENELITIAN ... 27
3.1. Tempat dan Waktu Penelitian ... 27
3.2. Rancangan, Populasi dan Sampel Penelitian ... 27
3.3. Bahan dan Alat Penelitian ... 28
3.3.1. Bahan Penelitian ... 28
3.5.1. Pelaksanaan Penelitian ... 29
3.5.2. Etika Penggunaan Hewan Coba ... 30
3.5.3. Pemberian Perlakuan ... 30
3.6. Prosedur Pemeriksaan dan Pengamatan ... 32
3.6.1. Pengamatan Makroskopis (Bobot Ginjal) ... 32
3.6.2. Prosedur Pembuatan Sediaan Histologi Jaringan Ginjal ... 32
3.6.2. Pemeriksaan Mikroskopis dan Penilaian Perubahan Pada Jaringan Ginjal (Tubulus Proksimal) ... 33
3.7. Analisis Data dan Pengujian Hipotesis ... 35
3.8. Jadual Penelitian ... 35
BAB 4. HASIL DAN PEMBAHASAN ... 37
4.1. Hasil Penelitian ... 37
4.1.1. Bobot Ginjal Mencit Jantan Dewasa ... 37
4.1.2. Penilaian Perubahan Tubulus Proksimal Ginjal (Sel Ginjal Nekrotik) Mencit Jantan Dewasa ... 38
4.2. Pembahasan ... 40
4.2.1. Bobot Ginjal Mencit Jantan Dewasa ... 40
4.2.2. Penilaian Perubahan Tubulus Proksimal Ginjal (Sel Ginjal Nekrotik) Mencit Jantan Dewasa ... 42
BAB 5. KESIMPULAN DAN SARAN ... 45
5.1. Kesimpulan ... 45
5.2. Saran ... 45
DAFTAR PUSTAKA
LAMPIRAN 1 : Penentuan Kadar Alkohol Secara Kualitatif Dan Kuantatif Dari Hasil Fermentasi
LAMPIRAN 2 : Bobot Ginjal Mencit Dan Penilaian Perubahan Tubulus Proksimal (Sel Ginjal Yang Mengalami Nekrotik)
LAMPIRAN 3 : Ethical ClearancePenggunaan Hewan Coba LAMPIRAN 4 : Sertifikat Vitamin E
LAMPIRAN 5 : Singkatan
Gambar Judul Halaman
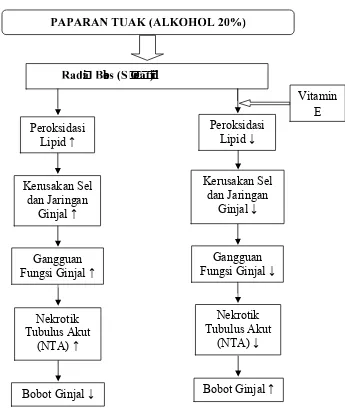
1.1. Kerangka Konsep Pengaruh Pemberian Vitamin E Terhadap Perubahan Bobot dan Gambaran Mikroskopis Ginjal Mencit
(Mus musculus,L.) Yang Dipapari Tuak (Alkohol) ... 5
2.1. Gambaran Makroskopis Ginjal ... 18
2.2. Gambaran Histologi Tubulus Proksimal Normal ... 23
2.3. Struktur Mikroanatomi Ginjal Mencit ... 25
4.1. Grafik Bobot Ginjal (g) ... 38
4.2. Grafik Sel Ginjal Yang Mengalami Nekrotik (%) ... 39
Tabel Judul Halaman
Pada kondisi stres oksidatif, keberadaan radikal bebas yang disebabkan konsumsi tuak (alkohol 20%) dapat menyebabkan terjadinya peroksidasi lipid sel membran dan merusak organisasinya. Radikal bebas merupakan suatu atom atau molekul yang tidak mempunyai pasangan elektron dan dapat merusak molekul-molekul penting bagi fungsi seluler. Dalam penelitian ini, pemberian asupan antioksidan (vitamin E) diusulkan dapat menurunkan efek radikal bebas dalam tubuh.Tujuan penelitian ini adalah untuk mengetahui pengaruh pemberian vitamin E terhadap perubahan bobot dan gambaran mikroskopis tubulus proksimal ginjal mencit (Mus musculus, L.) jantan dewasa yang dipapari tuak (alkohol 20%). Mencit jantan dibagi dalam 6 kelompok, tiap kelompok terdiri dari 5 ekor; P0= Tanpa perlakuan; P1= Tuak (alkohol 20%) 0,5 ml 15 hari + Aquadest 0,5 ml 15 hari; P2= Tuak (alkohol 20%) 0,5 ml 30 hari; P3= Tuak (alkohol 20%) 0,5 ml 15 hari + Vitamin E 0,25 mg 15 hari; P4= Tuak (alkohol 20%) 0,5 ml 15 hari + Tuak (alkohol 20%) 0,5 ml & Vitamin E 0,25 mg 15 hari; P5= Tuak (alkohol 20%) 0,5 ml & Vitamin E 0,25 mg 30 hari. Pada akhir perlakuan sesuai dengan kelompok, dilakukan pemeriksaan terhadap histologis tubulus proksimal ginjal mencit. Hasil penelitian menunjukkan bahwa vitamin E mempunyai pengaruh terhadap perubahan bobot ginjal mencit jantan dewasa yang dipapari tuak (alkohol 20%) secara tidak bermakna (p>0,05). Pemberian vitamin E selama 15 hari setelah pemberian tuak (alkohol 20%) 15 hari (kolompok P3) berpengaruh bermakna dibandingkan dengan kelompok P0 (kontrol, p<0,05) dan berpengaruh tidak bermakna dibandingkan dengan kelompok P1 (tuak/alkohol 20% selama 15 hari ditambah aquadest selama 15 hari). Meskipun demikian pemberian vitamin E cenderung menurunkan sel ginjal (tubulus proksimal) yang mengalami nekrotik.
In the condition of oxidative stress, the existence of free radical caused by the consumption of fermented palm wine/tuak (alcohol 20%) may lead into the occurrence of membrane cell lipid peroxidation and it damaged its organization. Free radical is as an atom or the molecule without electron pair and it may damage the important molecules for the function of cellular. In this research, the proposed antioxidant administration (vitamin E) can reduce the effect of free radical in body. The objective of this research is to know the influence of vitamin E giving to the change of weight and the description of adult male mice kidney proximal tubulus microscopic (Mus musculus, L) with tuak exposure (alcohol 20%). Male mice are divided into 6 (six) groups and each contained 5 (five) mice; P0 = without treatment, P1= tuak (alcohol 20%) 0,5 ml for 15 days + aquadest 0,5 ml for 15 days; P2 = tuak (alcohol 20%) 0,5 ml for 30 days, P3 = tuak (alcohol 20%) 0,5 ml for 15 days + vitamin E 0,25 mg for 15 days; P4 = tuak (alcohol 20%) 0,5 ml for 15 days + vitamin E 0,25 mg for 15 days; P5 = tuak (alcohol 20%) 0,5 ml & vitamin E 0,25 mg for 30 days. At the end of the treatment in accordance with the group, checking was carried out to mice kidney proximal tubulus histology. The results of the research showed that vitamin E influenced of adult male mice weight with tuak exposure (alcohol 20%, p>0,05). Vitamin E administration for 15 days after administration the tuak (alcohol 20%) for 15 days (P3 group) has significant influenced compared to P0 group (control, p<0,05) and to P1 group (tuak/alcohol 20% for 15 days plus aquadest for 15 days). However, vitamin E tended to reduce the kidney cell (proximal tubulus) suffering from the necrotic.
&' &(
)*+, '- ./ . ' +
( 0( 0/121 3&1 41 5el g
A67898 6 :;7< =;78>? @A? ; ABAC @><;y BDB7 E 87?;7 EB F9< =<C E @G@9 G< ; 7 ? BH< F<
6<> I?@>I A<@C @> E ; =<7 6<> I?@>I (J<> : <;E<> K 2003). L< 6<9 ? <E@ <7 ; G<E 7 8>? @A? ; < 67898 6 (BE <>8 6) GBF6BG; 9<> < =< 6<9 AB> ;>I7<E><y FB? ;78 I<I< 6 I;> : < 6 =<> I<I<6 D@> I?; 9<E;. MB> I78>?@ A?;BE<>8 6 ? <> I<E GB FG<9 <<y7 < FB> < FB<7? ; 7 ;A ;< ? B>< M<y ;> ; AB AGB>E@7 >B D F8E 87?;> 7 @<E 9 ;>II< AB>BG<G7<>y I<> II@<> D@> I? ; = <> 7B A<E;<> ? B6 (>B7 F8?;? N C< =< ?B 6 E @G@6 @? C F87?;A< 6. H<? ; 6 CB>B 6;E ;<> <>Iy =;6<7 @7<> C< =< 9B M<> CB FH8 G< <> E;7 @? C @E;9 I< 6@F M ;?E < F, y<>I =;GB F; <67898 6 20%, 30%, 40% =<> 50%? B G<><7y 2 A6 /9< F;? B 6< A< 15 9< F;, =;E B A@7<> >B7 F8? ;?
? B6E @G@6 @?C F87?;A< 6I;> :< 6 (G@><M<> K 2010).
LBCB FE; ?B G<I;<> GB? < F 8 F I<> =< 6<A E@G@9 < =< ?B : @A6<9 FBI@6< ? ; y<>I AB A @> I7 ;>7<> I;> :< 6 @>E @7 GB FD@>I? ; ?BH<F< > 8 FA< 6 =<> 8CE;A< 6, BE ; 6 < 67898 6 =<C<E AB> II<>II@ 78>EF8 6 ;> ;. EDB7 y<>I E BC<E EB FI<>E @>I C< =< :@A 6<9 < 67898 6 y
<>I < G? 8 FG?; =<> M<7 E@ =;78>?@A?;. A67898 6 EB 6<9 E B F6 ;9<E =<C <E A B> I@G<9 ? E F@7E @F =<> D@>I?; I;> :<6 ? B FE < AB F@?<7 7BA< AC@<>><y@>E@7 AB>I<E@F O8 6 @AB, 78 AC8?;? ; H< ;F<> =<> B6B7E F8 6;E =<6< A E @G@9 P JBF@G<9<> A;7 F8?78C ;? C<=< I;> :< 6
EB FA<?@7 CB F@G<9 <> ? E F@7E @F I68 AB F@6 @? K CB A GB > I7<7 <> <E< @ CB A GB? < F< > I;> :< 6
BTU TVWX W YU WZ WZ W[ zat kimia yang beredar dalam sirkulasi sistemik akan
dibawa ke ginjal dalam kadar yang cukup tinggi, sebagai akibatnya terjadi proses
reabsorbsi dan ekskresi dari zat-zat toksik tersebut. Salah satu manifestasi yang
sering ditemukan akibat zat nefrotoksik dalam ginjal adalah gagal ginjal akut
terutama dalam bentuk nekrosis tubular akut (NTA). Adanya kerusakan dalam
tubulus ginjal akibat zat nefrotoksik ini dilihat dengan adanya: penyempitan
tubulus kontortus proksimal, nekrosis sel epitel tubulus kontortus proksimal, dan
adanya hialin cast di tubulus distal (Manggarwati dan Susilaningsih, 2010). Salah
satu penyebab nekrosis (jejas sel) adalah bahan kimia dan obat-obatan, seperti:
obat-obatan terapeutik misalnya acetaminophen dan agen non-terapeutik misalnya
timah dan alkohol (Stanley dan Robbins, 2007).
Radikal bebas adalah sekelompok bahan kimia baik berupa atom maupun
molekul yang memiliki elektron tidak berpasangan pada lapisan luarnya. Radikal
bebas sangat reaktif, maka mempunyai spesifitas kimia yang rendah sehingga
dapat bereaksi dengan berbagai molekul lain seperti protein, lemak, karbohidrat
dan Deoxi Nucleic Acid (DNA) (Droge, 2002). Radikal bebas terpenting dalam tubuh adalah radikal derivat dari oksigen yang disebut kelompok oksigen reaktif
(reactive oxygen species atau ROS) termasuk didalamnya adalah triplet (3O2),
tunggal (singlet/1O2), anion superoksida (O2-), radikal hidroksil (-OH), nitrit oksida
(NO-), peroksinitrit (ONOO-), asam hipoklorus (HOCl), hidrogen peroksida
(H2O2), radikal alkoksil (LO-) dan radikal peroksil (LO-2). Radikal yang
mengandung hidrogen hasil penyerangan atom H (H-) dan bentuk lain adalah
radikal mengandung sulfur yang diproduksi pada oksidasi glutation menghasilkan
Semua organisme aerobik pada derajat tertentu dilengkapi dengan sistem
pertahanan yang mampu melindungi sel dari pengaruh metabolit oksigen yang
secara umum dikerjakan oleh beberapa kelompok enzim protektif seperti:
superoksida dismutase (SOD), katalase, reduktase, glutation peroksidase serta anti
oksidan endogen antara lain adalah seruloplasmin, transferin, asam askorbat, asam
urat, sistein, -tokoferol dan -karoten. Semua sistem perbaikan ini mencegah
akumulasi yang rusak akibat proses oksidatif (Wuryastuti, 2000; Wirakusumah,
2000).
Ketidakseimbangan antara produksi senyawa oksigen reaktif dengan
kemampuan pertukaran antioksidan mengalami gangguan sehingga menggoyahkan
rantai reduksi-oksidan normal, hal ini mengakibatkan kerusakan oksidatif jaringan.
Keadaan ini diduga sebagai salah faktor pendorong timbulnya beberapa penyakit
(Shahidi, 1997; Packer \] ^_ `a 1998; Wuryastuti, 2000). Radikal bebas ini akan
bereaksi dengan bc_ d-unsaturated fatty acid s (PUFAs) atau asam lemak tidak
jenuh ganda yang menyebabkan terbentuknya lemak peroksida. Ebrahim dan
Sakthisekaran (1997), menyatakan bahwa O2 merupakan faktor penting pada
beberapa kondisi patologi.
Vitamin E merupakan vitamin yang larut dalam lemak yang terdiri dari
campuran dan substansi tokoferol ( , , , dan ) pada manusia -tokoferol
merupakan vitamin E yang paling penting untuk aktifitas biologi tubuh (Linder,
1992; Dutta-Roy, 1994). Bentuk vitamin E ini dibedakan berdasarkan letak
berbagai grup metil pada cincin fenil rantai cabang molekul dan ketidakjenuhan
peroksida lemak pada membran dan e fg Density Lipoprotein (LDL), -karoten
sebagai scavangers atau pemulung oksigen tunggak dan vitamin C untuk pemulung superoksida radikal bebas yang lain (Krishnamurthy, 1993; Watson dan
Leonard, 1986; Packer, 1998).
Sehubungan dengan fakta-fakta di atas terlihat bahwa pemberian etil alkohol
dapat menyebabkan perubahan gambaran miokroskopis dan gangguan pada
tubulus proksimal ginjal. Sedangkan vitamin E dapat menetralisir hidroksil,
superoksida, radikal hidrogen peroksida dan mencegah kerusakan pada tubulus
proksimal ginjal. Penelitian ini bertujuan untuk mengetahui pengaruh pemberian
vitamin E terhadap perubahan bobot dan gambaran mikroskopis tubulus proksimal
ginjal mencit jantan dewasa yang dipapari tuak (alkohol).
hiji ker umul mnoml mp m h
Bagaimana pengaruh pemberian vitamin E terhadap perubahan bobot dan
gambaran mikroskopis tubulus proksimal ginjal mencit jantan dewasa yang
dipapari tuak (alkohol).
hiqi rermngkmseori
Pemberian tuak (alkohol) pada mencit baik secara akut atau kronis
menyebabkan toksik pada ginjal (nefron), yang menyebabkan peningkatan aktifitas
enzim katalase sehingga menimbulkan radikal bebas (stres oksidatif) ditandai
dengan kerusakan atau gangguan pada jaringan ginjal, yang akibatnya terjadi
Kerja vitamin E merupakan pemutus rantai peroksida lemak pada membran
dant uv Density Lipoprotein(LDL), -karoten sebagaiscavangers atau pemulung
oksigen tunggak dan vitamin C untuk pemulung superoksida radikal bebas yang
lain (Krishnamurthy, 1993; Watson dan Leonard, 1986; Packer, 1998).
wxyx zer{|gk{zonsep
Gambar 1.1. Kerangka konsep pengaruh pemberian vitamin E terhadap perubahan bobot dan gambaran mikroskopis tubulus proksimal ginjal mencit (Mus musculus,
L.) jantan dewasa yang dipapari tuak (alkohol).
ujueneliti
ujuumm
Untuk membuktikan bahwa vitamin E dapat memperbaiki dan menghambat
kerusakan jaringan ginjal (tubulus proksimal) mencit jantan dewasa yang dipapari
tuak (alkohol).
ujuhusus
1. Untuk mengetahui pengaruh pemberian vitamin E terhadap perubahan bobot
ginjal mencit jantan dewasa yang dipapari tuak (alkohol).
2. Untuk mengetahui pengaruh pemberian vitamin E terhadap perubahan
gambaran mikroskopis tubulus proksimal ginjal mencit jantan dewasa yang
dipapari tuak (alkohol).
3. Untuk mengetahui kemampuan vitamin E dalam memperbaiki dan menghambat
kerusakan tubulus proksimal ginjal mencit jantan dewasa yang dipapari tuak
(alkohol).
ipotesis
1. Pemberian vitamin E mempunyai pengaruh terhadap perubahan bobot ginjal
mencit jantan dewasa yang dipapari tuak (alkohol).
2. Pemberian vitamin E mempunyai pengaruh terhadap perubahan gambaran
mikroskopis tubulus proksimal ginjal mencit jantan dewasa yang dipapari tuak
¡¢f¡¡£¤eneliti¡¢
1. Hasil penelitian ini diharapkan dapat memberikan informasi ilmiah bagi ilmu
kedokteran dan bidang ilmu lainnya sebagai salah satu acuan untuk menjaga
kesehatan dan mencegah penyakit yang disebabkan oleh minum tuak.
2. Dapat dijadikan sebagai referensi untuk penelitian selanjutnya dimana dampak
¥¦ ¥§
¨©ª «¦¬ ¦ª¬ ® ¨ ¦¯ ¦
§°±°¦lkohol ²³t´µol¶
Secara umum tuak dikenal oleh masyarakat di Indonesia adalah jenis
minuman yang disebut arak. Bagi masyarakat Batak Toba tuak merupakan
minuman sehari-hari (Ikegami, 1997). Tuak merupakan minuman beralkohol yang
bahan dasarnya nira aren (·¸ ¹º»¼½¾ ºº¼¿ ¼) mengandung alkohol dengan kadar 4%
(Sunanto, 1993). Menurut Keputusan Menteri Kesehatan No.151/A/SK/V/81
bahwa minuman atau obat tradisional yang tergolong dalam minuman keras
mengandung alkohol >1%. Pengolahan nira aren menjadi etanol sudah umum
dilakukan petani aren, antara lain di daerah Minahasa Sulawesi Utara, dengan cara
menampung nira hasil sadapan dalam tangki selama 2-3 hari tanpa menggunakan
starter atau ragi, nira hasil fermentasi kemudian disuling dengan alat penyulingan
sederhana, akan menghasilkan bioetanol berkadar 25-35% (Lay¹¿¼À., 2004).
Alkohol terutama dalam bentuk etil alkohol (etanol), telah mengambil tempat
dalam sejarah umat manusia paling sedikit selama 8.000 tahun. Saat ini, alkohol
dikonsumsi secara luas. Sama seperti obat-obat sedatif-hipnotik lainnya, alkohol
dalam jumlah rendah sampai sedang dapat menghilangkan kecemasan dan
membantu menimbulkan rasa tenang atau bahkan euforia. Akan tetapi, alkohol
juga dikenal sebagai obat yang paling banyak disalahgunakan di dunia, suatu
alasan yang tepat atas kerugian besar yang mesti ditanggung masyarakat dan dunia
Kandungan alkohol minuman berkisar dari 4-6% (volume/volume) untuk bir,
10-15% untuk anggur, dan 40% dan lebih tinggi untuk spiritus hasil destilasi.
ÁÂÃÃÄ (kekuatan alkohol) minuman mengandung alkohol adalah dua kali persen
alkoholnya (sebagai contoh: alkohol 40% adalah 80ÅÂÃÃÄ) (FlemingÆÇÈÉÊË2007).
Di Amerika Serikat, sekitar 75% dari populasi dewasa mengkonsumsi
minuman beralkohol secara teratur. Mayoritas dari populasi peminum ini bisa
menikmati efek memuaskan yang diberikan alkohol tanpa menjadikannya sebagai
resiko terhadap kesehatan. Bahkan fakta baru menunjukkan bahwa konsumsi
etanol secukupnya dapat melindungi beberapa organ terhadap penyakit
kardiovaskuler. Akan tetapi, sekitar 10% dari populasi umum di Amerika Serikat
tidak mampu membatasi konsumsi etanol mereka, suatu kondisi yang dikenal
dengan penyalahgunaan alkohol. Individu-individu yang terus menerus meminum
alkohol tanpa memperdulikan adanya konsekuensi yang merugikan secara medis
dan sosial yang berkaitan langsung dengan konsumsi alkohol mereka tersebut
menderita alkoholisme, suatu gangguan kompleks yang tampaknya ditentukan oleh
faktor genetik dan lingkungan (Masters, 2002).
Alkoholisme sulit untuk menentukan jumlah alkohol yang dikonsumsi tetapi
dapat diketahui jika kebiasaan tersebut dalam beberapa cara mempengaruhi
kehidupan seseorang secara bertolak belakang. Alkoholisme menyebabkan
gangguan fungsi sosial dan pekerjaan, meningkatkan toleransi terhadap efek
ÌÍÎÍÎÍÏÐrmÐ ÑokinetikÐ Òlkohol
Setelah pemberian oral, etanol diabsorbsi dengan cepat dari lambung dan usus
halus ke dalam aliran darah dan terdistribusi ke dalam cairan tubuh total (Fleming
ÓÔ ÕÖ ×Ø 2007). Tingkat absorbsi paling tinggi pada saat lambung kosong. Adanya
lemak di dalam lambung menurunkan tingkat absorbsi alkohol (Chandrasoma dan
Taylor, 2005). Setelah minum alkohol dalam keadaan puasa, kadar puncak alkohol
di dalam darah dicapai dalam waktu 30 menit. Distribusinya berjalan cepat,
dengan kadar obat dalam jaringan mendekati kadar di dalam darah. Volume
distribusi dari etanol mendekati volume cairan tubuh total (0,5-0,7 L/Kg) (Masters,
2002). Alkohol didistribusikan di dalam tubuh (terutama dalam jaringan adiposa),
menyebabkan efek dilusi. Hal ini berkaitan dengan berat badan dan menerangkan
mengapa orang dengan obesitas memiliki kadar alkohol yang lebih rendah dari
pada orang yang kurus untuk jumlah alkohol yang sama (Chandrasoma dan
Taylor, 2005).
Pada dosis oral ekuivalen dari alkohol, kaum wanita mempunyai konsentrasi
puncak lebih tinggi dibandingkan kaum pria, sebagian disebabkan karena wanita
mempunyai kandungan cairan tubuh total lebih rendah. Di dalam sistem saraf
pusat, konsentrasi etanol meningkat dengan cepat karena otak menampung
sebagian besar aliran darah dan etanol melewati membran biologi dengan cepat.
Lebih dari 90% alkohol yang digunakan dioksidasi di dalam hati, sebagian besar
sisanya di keluarkan lewat paru-paru dan urin (Masters, 2002).
Ekskresi alkohol di urin dan udara yang dihembuskan biasanya sedikit, tetapi
(Blood Alcohol Concentration/BAC). Hal ini merupakan prinsip yang mendasari penggunaan pemeriksaan urin dan pernafasan pada forensik selain pemeriksaan
dengan menggunakan darah (Chandrasoma dan Taylor, 2005), juga sebagai prinsip
yang mendasari definisi legal dari mengemudi di bawah pengaruh (driving under influence) di berbagai negara. Pada umumnya orang dewasa dapat memetabolisme alkohol per-jam sebanyak 7-10 g (150-220 mmol), ini ekuivalen
dengan bir sekitar 10 oz, anggur 3,5 oz, atau minuman keras 1 oz yang disuling
dengan kadar murni 80 (Masters, 2002).
ÙÚÛÚÙÚÜirÝÞren ßàrenga pinnataá
Nira aren (Arenga pinnata (Wurmb.) Merr.) Sinonim: Arenga sacchrifera Labill (nama lama). Familia : Arecaceae (Palmae). Pada umumnya semua bagian aren ini dapat dipergunakan, tongkol bunga jantan yang disadap mengandung gula,
kemudian dibuat gula (gula Jawa), bila dikhamirkan dapat menghasilkan air sagu,
arak atau cuka; bijinya dapat dibuat makanan berupa manisan (kolang-kaling).
Tuak/legen adalah hasil peragian air nira dari tongkol bunga jantan dan akar.
Aren mempunyai berbagai istilah tergantung daerahnya, misalnya Aceh: Bak
juk, Bak jok; Batak: Pola, Paula, Bagot, Agaton, Bargot; Minangkabau: Anau,
Biluluk; Sunda: Kawung, Taren; Jawa: Aren, Lirang, Nanggung; Bali: Jaka, Hano;
Flores: Moke, Huwat; Sawu: Akel, Akere, Koito, Akol, Ketan; Bugis: Inru; Roti:
Bole; Ternate: Seho.
Komponen utama dari nira berupa air, karbohidrat dalam bentuk sukrosa,
aktifitas bakteri (âã äåæçèã åäé sp.) dan khamir (Saccharomyces sp.) yang dapat
menfermentasi sukrosa menjadi alkohol maupun asetat. Sadapan dari tandan
bungan aren jantan dapat dilakukan setelah tanaman berumur 5-12 tahun. Setiap
pohon tanaman aren ini dapat disadap selama 3 tahun, dan setiap tahun dapat
dilakukan sadap 3-4 tangkai bunga,dan dalam seharinya aren dapat menghasilkan
3-10 liter nira (Halim, 2008).
Komposisi beberapa nira dari berbagai tanaman palmae seperti pada Tabel
2.1. di bawah ini:
Tabel 2.1. Komposisi Nira dari Berbagai Tanaman Palmae (%) (Halim, 2008).
êënis ìíî íï ìíî íï ìíî íï ìíî íï ìíî íï
Radikal bebas merupakan spesies yang terdiri dari satu electron atau lebih
Salah satunya apabila dua radikal bebas bertemu maka elektron yang tidak
berpasangan tadi akan bergabung membentuk ikatan kovalen (Haliwell, 1994).
Radikal bebas sangat berbahaya jika menjadi sangat reaktif untuk
mendapatkan pasangan elektronnya, sehingga dapat bereaksi dengan berbagai
biomolekuler penting seperti enzim, DNA dan juga merusak sel lain yang akhirnya
dapat menimbulkan penyakit. Hal ini dapat dihambat dengan menggunakan
antioksidan. Ketidakseimbangan antara radikal bebas dengan antioksidan
menimbulkan stress oksidatif.
Tubuh manusia mempunyai beberapa mekanisme untuk bertahan terhadap
radikal bebas dan ÿ (ROS) lainnya. Pertahanan yang
bervariasi saling melengkapi satu dengan yang lain karena pada oksidan yang
berbeda atau dalam bagian seluler yang berbeda (Tuminah, 2000).
ntioksid
Antioksidan adalah senyawa yang mampu menangkal atau meredam efek
negatif oksidan dalam tubuh, bekerja dengan cara mendonorkan satu elektronnya
kepada senyawa yang bersifat oksidan sehingga aktifitas senyawa oksidan tersebut
dapat dihambat (Winarsih, 2007).
Antioksidan dikelompokkan menjadi dua yaitu antioksidan enzimatis dan
antioksidan non-enzimatis. ntioksid enzimtis : merupakan antioksidan
endogenus, yang termasuk di dalamnya adalah enzim superoksida dismutase
(SOD), katalase, glutation peroksidase PX), serta glutation reduktase
bekerja menghambat pembentukan radikal bebas, dengan cara memutuskan reaksi
berantai (polimerisasi), kemudian mengubahnya menjadi produk lain yang stabil,
sehingga antioksidan kelompok ini disebut juga -breaking-antioxidant
(Winarsih, 2007). Enzim katalase dan glutation peroksidase bekerja dengan cara
mengubah H2O2 menjadi H2O dan O2, sedangkan SOD bekerja dengan cara
mengkatalisis reaksi dismutasi dari radikal anion superoksida menjadi H2O2
(Langseth, 1995; Winarsih, 2007). ntioksid on nzimis disebut juga
antioksidan eksogenus, antioksidan ini bekerja secara preventif. Terbentuknya
senyawa oksigen reaktif dihambat dengan cara pengkelatan metal, atau dirusak
pembentukannya (Winarsih, 2007). Antioksidan non-enzimatis bisa didapatkan
dari komponen nutrisi sayuran, buah dan rempah-rempah. Komponen yang bersifat
antioksidan dalam sayuran, buah dan rempah-rempah meliputi vitamin C, vitamin
E, -karoten, flavonoid, isoflavon, flavon, antosianin, katekin dan isokatekin
(Kahkonenet al.,1999). Senyawa-senyawa fitokimia ini membantu melindungi sel dari kerusakan oksidatif yang disebabkan oleh radikal bebas.
! Vi"#
Vitamin E merupakan salah satu vitamin yang larut dalam lemak. Nama lain
dari vitamin E adalah tokoferol. Keaktifan vitamin E dalam beberapa senyawa
tokoferol berbeda. Bentuk -, -, dan -tokoferol menunjukkan keaktifan vitamin
E yang paling tinggi. Struktur kimia tokoferol adalah sebagai berikut, -tokoferol
alam memutar bidang polarisasi ke kanan, sedangkan -tokoferol buatan adalah
resemik (DL). Tokoferol lainnya (beta, gama dan delta) kurang penting karena
$%$%&% 'un() *'*)*+,+( *- ./'. 0 1.2 +2*/ 34*25 *4.1*/6
Vitamin E berperan sebagai antioksidan dan dapat melindungi aksi kerusakan
membran biologis akibat radikal bebas. Vitamin E melindungi asam lemak tidak
jenuh pada membran fosfolipid. Radikal peroksi bereaksi 1.000 kali lebih cepat
dengan vitamin E dari pada asam lemah tidak jenuh, dan membentuk radikal
tokoferoksil (Gunawan, 2007). Selanjutnya radikal tokoferoksil berinteraksi
dengan antioksidan lain seperti vitamin C, yang akan membentuk kembali
tokoferol. Vitamin E misalnya, paling penting untuk melindungi membran sel
darah merah yang kaya akan asam lemak tidak jenuh ganda dari kerusakan akibat
oksidan.
Selain itu vitamin E melindungi lipoprotein dalam sirkulasi 7 89 Density Lipoprotein (LDL) teroksidasi yang ternyata memegang peranan penting dalam menyebabkan arterosklerosis. LDL teroksidasi lebih mudah diambil oleh makrofag
dibanding dengan LDL yang tidak teroksidasi, selanjutnya membentuk sel
makrofag dengan sitoplasma yang berbusa (foam cell) yang berpengaruh buruk pada sel endotel, dan mungkin dapat menyebabkan vasokonstriksi. Vitamin E
dosis tinggi (1.600 mg/hari) dapat mencegah terjadinya oksidasi pada LDL.
Di samping efek antioksidannya, efek langsung terhadap sel endotel pembuluh
darah, sel otot polos atau pembekuan darah diduga ikut berperan. Vitamin E
mengatur proliferasi sel otot polos pembuluh darah, menyebabkan vasodilatasi dan
menghambat baik aktifasi trombosit maupun adhesi leukosit. Vitamin E juga
misalnya selenium, asam amino yang mengandung sulfur, koenzim Q dapat
menggantikan vitamin E (Gunawan, 2007).
:;:;<; => ?@AB CB DEB FDCB G=H?IJ D KD LMB G NDO
Pada penelitian yang dilakukan kepada manusia yang merokok dengan tujuan
untuk menentukan efek vitamin E baik secara sendiri-sendiri maupun kombinasi
terhadap kadar lipid peroksidasi secara P Q RP RS T ditemukan bahwa pemberian
vitamin E secara sendiri-sendiri dapat mereduksi lipid peroksidasi dengan kadar
yang sama. Sedangkan pemberian vitamin C dan vitamin E dengan cara kombinasi
juga memberikan efek yang sama tidak lebih dari pada pemberian secara
sendiri-sendiri (HuangUVWX YT2002).
Secara klinis, vitamin E juga bermanfaat melindungi membran dasar
glomerulus ginjal dan menghambat proses pengentalan darah (agregrasi platelet)
(Saran UV WXYT 2003). Jika kekurangan vitamin E dapat terjadi nefritis, dimana
tubulus tidak dapat dilewati urin yang ditandai dengan degenerasi basal yang
progresif. Jika keadaan ini berkepanjangan maka tubulus akan mengalami
kerusakan/hancur, namun pemberian vitamin E akan memperbaiki keadaan ini.
Vitamin E dapat membantu sel dalam mempertahankan kehidupan dengan cara
menurunkan kebutuhan terhadap oksigen, mencegah jaringan parut dan kerusakan
ginjal oleh karena bahan kimia beracun serta meningkatkan aliran urin (Crawford,
Z[\[]in^_`
Z[\[a[ bc_defgh _cig j g e` ekg]g c^_`
Ginjal adalah organ vital yang berperan sangat penting dalam
mempertahankan keseimbangan lingkungan dalam tubuh. Ginjal mengatur
keseimbangan cairan tubuh dan elektrolit dan asam basa dengan cara menyaring
darah yang melalui ginjal, reabsorbsi selektif air, elektrolit dan non-elektrolit serta
mengekskresi kelebihannya sebagai kemih. Ginjal juga mengeluarkan sampah
metabolisme (seperti urea, kreatinin dan asam urat) dan zat kimia asing. Selain
fungsi regulasi dan ekskresi, ginjal juga mensekresi renin (yang penting untuk
pengaturan tekanan darah), juga bentuk aktif vitamin D (untuk pengaturan
kalsium) serta eritropoietin (untuk sintesis darah) (Price, 1995).
Ginjal merupakan organ yang berbentuk kacang, terletak di kedua sisi
kolumna vertebralis. Ginjal sebelah kanan sedikit lebih rendah dibanding ginjal
sebelah kiri karena tertekan ke bawah oleh hati. Katup atasnya ginjal kanan
terletak setinggi kostal ke-12 dan ginjal kiri setinggi kostal ke-11.
Ginjal terletak di bagian belakang rongga abdomen, di belakang peritoneum,
di depan dua kosta terakhir dan tiga otot-otot besar (tranversus abdominis,
kuadratus lumborum dan psoas mayor). Kelenjar adrenal terletak di atas katup
masing-masing ginjal. Pada orang dewasa panjang ginjal antara 12-13 cm,
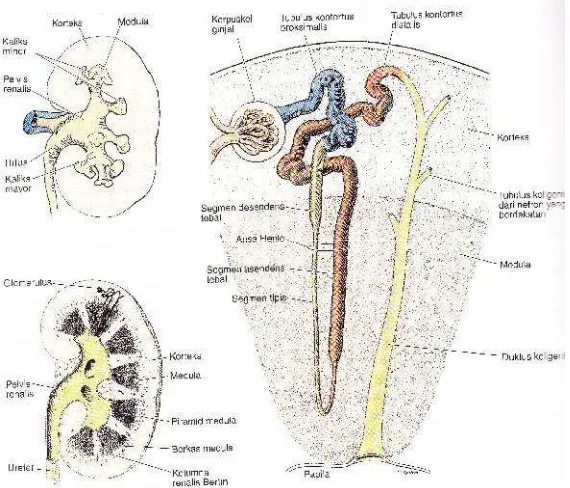
Gambar 2.1. Gambaran Makroskopis Ginjal (Junqueira, 2007).
Potongan logitudinal ginjal memperlihatkan dua daerah yang berbeda yaitu
korteks (bagian luar) dan medula (bagian dalam). Medula terbagi-bagi menjadi
baji segitiga yang disebut piramid. Piramid-piramid tersebut diselingi oleh bagian
korteks yang disebut dengan kolom lmn op qp. Piramid ini tampak bercorak karena
tersusun dari segmen-segmen tubulus dan duktus pengumpul nefron. Papila
(apeks) dari tiap piramid akan membentuk duktus papilaris belini yang terbentuk
dari persatuan bagian terminal dari banyak duktus pengumpul. Setiap duktus
papilaris masuk ke dalam suatu perluasan ujung pelpis ginjal berbentuk seperti
cawan yang disebut dengan kaliks minor. Beberapa kaliks minor bersatu yang
pelvis ginjal. Pelvis ginjal merupakan reservoar utama pada sistem pengumpul
ginjal. Ureter menghubungkan pelvis ginjal dengan kandung kemih (Price, 1995).
Nefron merupakan satu kesatuan unit fungsional dari ginjal, masing-masing
ginjal manusia terdiri dari kurang lebih 1 juta nefron, setiap nefron mempunyai
dua komponen utama, yaitu: rs tuvwxsx y (kapiler gromelurus) dan zx{xsx y
(Guyton, 2007). Nefron terdiri atas bagian yang melebar, korpuskulus renal;
tubulus kontortus proksimal, segmen tipis dan tebal ansa Henle; dan tubulus
kontortus distal. Pada kutub urinarius pada korpuskulus renal, epitel gepeng dari
lapisan parietal kapsul Bowman, berhubungan langsung dengan epitel silidris dari
tubulus kontortus proksimal. Tubulus ini lebih panjang dari tubulus kontortus
distal dan karenanya tampak lebih banyak dekat korpuskulus renalis dalam labirin
korteks. Tubulus ini juga memiliki lumen lebar dan dikelilingi oleh kapiler
peritubuler (Junqueira, 1995).
Pembentukan urin (kemih) dimulai dengan proses filtrasi plasma pada
glomerulus. Aliran darah ginjal (RBF: renal blood flow) adalah sekitar 25% dari
curah jantung atau sekitar 1.200 ml/menit. Bila hematokrit normal dianggap 45%,
maka aliran plasma ginjal (RPF: renal plasma flow) sama dengan 660 ml/menit
(0,55 x 1.200 = 660). Sekitar seperlima dari plasma atau 125 ml/menit dialirkan
melalui glomerulus ke kapsula Bowman. Ini dikenal dengan istilah laju filtrasi
glomerulus (GFR: glomerular filtrasion rate).
Tekanan-tekanan yang berperan dalam proses laju filtrasi glomerulus yang
cepat ini seluruhnya bersifat pasif, dan tidak membutuhkan energi metabolik untuk
antara kapiler glomerulus dan kapsula Bowman. Tekanan hidrostatik darah dalam
kapiler glomerulus mempermudah filtrasi dan kekuatan ini dilawan oleh tekanan
hidrostatik filtratsi dalam kapsula Bowman serta tekanan osmotik koloid darah.
Tekanan koloid osmotik kapiler pada hakekatnya adalah nol.
Zat-zat yang difiltrasi ginjal dibagi dalam 3 kelas yaitu: elektrolit,
nonelektrolit dan air. Beberapa jenis elektrolit yang paling penting adalah natrium
(Na+), kalium (K+), kalsium (Ca++), magnesium (Mg++), bikarbonat (HCO3-),
klorida (Cl-) dan fosfat (HPO4=). Sedangkan non-elektrolit yang penting adalah
glukosa, asam amino dan metabolit yang merupakan hasil akhir dari proses
metabolisme protein seperti: urea, asam urat dan kreatinin.
Setelah filtrasi, langkah kedua dalam proses pembentukan kemih adalah
reabsorbsi selektif zat-zat yang sudah difiltrasi. Kebanyakan dari zat yang difiltrasi
akan direabsorbsi melalui poro-pori kecil yang terdapat dalam tubulus sehingga
akhirnya zat-zat tersebut kembali lagi ke dalam kapiler peritubular yang
mengelilingi tubulus. Disamping itu beberapa zat disekresikan pula dari pembuluh
darah peritubular ke dalam tubulus (Price, 1995).
|}~}|}un
Ginjal menjalankan fungsi yang multipel, antara lain:
1. Pengaturan keseimbangan air dan elektrolit
Untuk mempertahankan homeostasis, ekskresi air dan elektrolit seharusnya
sesuai dengan asupan. Jika asupan melebihi ekskresi, jumlah zat dalam tubuh
natriumnya sebagai respon terhadap perubahan asupan natrium, jumlahnya
sangat besar.
2. Sekresi hasil buangan metabolik dan bahan kimia asing
Ginjal merupakan organ utama untuk membuang produk sisa metabolisme yang
tidak lagi diperlukan oleh tubuh. Produk ini meliputi: urea (dari metabolisme
asam amino), kreatinin (dari kreatin otot), asam urat (dari asam nukleat),
produk akhir dari pemecahan hemoglobin (bilirubin) dan metabolit dari
berbagai hormon. Ginjal juga membuang toksin dan zat asing lainnya yang
diproduksi oleh tubuh dan pencernaan seperti pestisida, obat-obatan dan
makanan tambahan.
3. Pengaturan tekanan arteri
Ginjal berperan penting dalam pengaturan tekanan arteri jangka panjang dengan
mengekskresikan sejumlah natrium dan air sedangkan jangka pendek dengan
mengekskresikan faktor atau zat vasoaktif, seperti renin yang menyebabkan
pembentukan produk vasoaktif (angiotensi II).
4. Pengaturan keseimbangan asam dan basa
Ginjal turut mengatur keseimbangan asam basa bersama dengan sistem dapar
paru dan cairan tubuh, dengan mengekskresikan asam dan mengatur
penyimpanan dapar cairan tubuh. Ginjal merupakan satu-satunya organ untuk
membuang tipe-tipe asam tertentu dari tubuh yang dihasilkan oleh metabolisme
protein, seperti asam fosfat atau sulfat.
5. Pengaturan produk eritrosit
Ginjal menyekresikan eritropoetin, yang merangsang pembentukan sel darah
6. Pengaturan produksi 1,25-dihidroksi vitamin D-3
Ginjal menghasilkan bentuk aktif vitamin D, yaitu 1,25-dihidroksi vitamin D3.
Dengan menghidroksi vitamin ini posisi nomor 1 , vitamin ini penting dalam
pengaturan kalsium dan fosfat.
7. Sistem glukosa
Ginjal mensitesis glukosa dari asam amino dan prekursor lainnya selama masa
puasa yang panjang, proses ini disebut (Guyton, 2007).
ubulu
¡¢£
Tubulus proksimal berjalan berkelok-kelok dan berakhir sebagai saluran yang
lurus di medula ginjal (pars desendens Ansa Henle). Tubulus kontortus proksimal
terdapat banyak pada korteks ginjal dengan diameter sekitar 60 m dan panjang
sekitar 14 mm. Tubulus kontortus proksimal terdiri dari pars konvulata yang
berada di dekat korpus kulus ginjal dan pars rekta yang berjalan turun di medula
dan korteks, kemudian berlanjut menjadi lengkung Henle di medula (Gartner dan
Hiatt, 2007). Fungsi tubulus kontortus proksimal adalah mengurangi isi filtrat
glomerulus 80-85% dengan cara reabsorpsi melalui transport dan pompa natrium.
Glukosa, asam amino dan protein seperti bikarbonat akan diresorpsi. Epitel yang
melapisi tubulus ini adalah selapis kuboid atau silindris yang menunjang dalam
mekanisme absorbsi dan ekskresi. Sel-sel epitel ini memiliki sitoplasma asidofilik
yang disebabkan oleh adanya mitokondria panjang dalam jumlah besar. Apeks sel
memiliki banyak mikrovili dengan panjang sekitar 1 m, yang membentuk suatu
Gambar 2.2. Histologi Tubulus Proksimal Nornal (Eroschenko, 2003)
Pada medula bagian luar, ruas tebal desenden, dengan garis tengah luar sekitar
60 m, secara mendadak menipis sampai sekitar 12 m dan berlanjut sebagai ruas
tipis desenden. Lumen ruas nefron ini lebar karena dindingnya terdiri atas sel
epitel gepeng yang intinya hanya sedikit menonjol ke dalam lumen. Bila ruas tebal
asenden lengkung Henle menerobos korteks, struktur histologisnya tetap
terpelihara tetapi menjadi berkelok-kelok disebut tubulus kontortus distal, yaitu
bagian terakhir nefron. Tubulus ini dilapisi oleh sel-sel epitel selapis kuboid
(Junqueiraª«¬., 2005). Sel epitel tubulus sangat peka terhadap anoksia dan rentan
terhadap toksin. Beberapa faktor memudahkan tubulus mengalami toksik,
termasuk permukaan bermuatan listrik yang luas untuk reabsorbsi tubulus, sistem
transpor aktif untuk ion dan asam organik, dan kemampuan melakukan pemekatan
secara efektif, selain itu kadar sitokrom P450 yang tinggi untuk mendetoksifikasi
¯°±²³ ´µ ´¶ · ¶¸´¹ º²± ·¹»¼bul° ¶ ½¹¼ ±¾¸»½ ¿
Zat yang dikeluarkan oleh tubuh melalui organ ekskresi, dan ginjal merupakan
organ yang paling penting (Guyton, 2007). Ekskresi ginjal dapat berefek samping,
baik karena toksin maupun karena konsentrasi zat yang tinggi yang potensial
merusak, dan dapat menyebabkan Nekrotik Tubulas Akut (NTA), nefritis
intersisialis akibat obat dan membrano glomerulo nephritis (MGN) (Underwood
JCE, 2004; Alpers, 2007). Beberapa obat atau zat kimia yang beredar dalam
sirkulasi sistemik akan dibawa ke ginjal dalam kadar yang cukup tinggi, sebagai
akibatnya terjadi proses reabsorbsi dan ekskresi dari zat-zat toksik tersebut. Salah
satu manifestasi yang sering ditemukan akibat zat nefrotoksik dalam ginjal adalah
gagal ginjal akut terutama dalam bentuk NTA. Adanya kerusakan dalam tubulus
ginjal akibat zat nefrotoksik ini dilihat dengan adanya: penyempitan pada tubulus
kontortus proksimal, nekrotik sel epitel tubulus kontortus proksimal, dan adanya
hialin cast pada tubulus distal (Manggarwati dan Susilaningsih, 2010).
Nekrosis (jejas ireversibel) adalah perubahan morfologik yang mengikuti
kematian sel pada jaringan atau organ hidup. Dua proses penyebab perubahan
morfologik dasar nekrosis adalah denaturasi protein dan digesti enzimatik organel
dan sitosol. Sel yang mengalami nekrotik berwarna eosinofolik, seperti kaca
(glassy), membran sel pecah-pecah. Perubahan inti sel nekrotik adalah
kariopiknosis (inti kecil, padat), kariolisis (inti pucat, larut) dan karioreksis (inti
pecah menjadi beberapa gumpalan) (Stanley dan Robbins, 2007). NTA adalah
kumpulan tanda dan gejala dari kegagalan ginjal tingkat kedua yang menghasilkan
gejala terlihat hanya pada sekitar tubulus interstisium dan sering mengakibatkan
organ tidak berfungsi (Seymour, 2008). NTA ditandai dengan berkurangnya fungsi
laju filtrasi glomerulus (glomerular filtrasi rate/GFR) secara tiba-tiba, penumpukan
sampah-sampah yang bersifat nitrogen dan ketidak mampuan ginjal untuk
meregulasi keseimbangan sodium, elektrolit-elektrolit, asam dan air (Matthew,
2002).
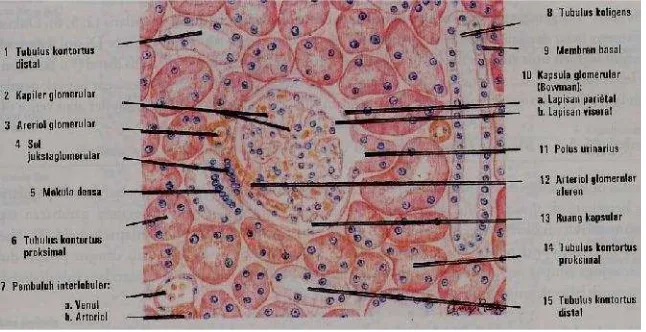
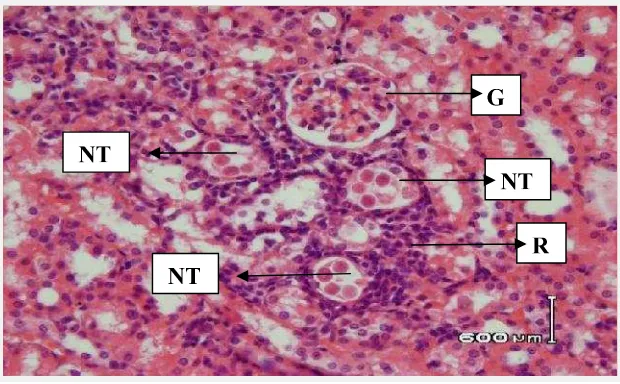
Gambar 2.3. Struktur mikroanatomi ginjal mencit, Perbesaran 400 x. Keterangan; G= Glomerulus; NT= Nekrosis Tubulus; R= Infiltrasi sel radang.
Pewarnaan H-E (Suhenti, 2007).
Pada NTA nefrotoksik, ginjal bengkak, berwarna merah, dan sering ditemukan
vakuolisasi sitoplasma sel epitel tubulus. Kerusakan terbanyak di tubulus
proksimal, jarang di tubulus distal. Tampak adanya degenerasi tubulus proksimal
yang mengandung debris, tetapi membran basalis utuh (Underwood JCE, 2004;
Alpers CE, 2007). NTA merupakan penyebab terpenting dari gagal ginjal akut.
Klinisnya adalah oliguria yang dilanjutkan diuresis. Peningkatan ketidakkebalan
À
Á Â
Ã
terhadap infeksi sehingga kurang lebih 25% kematian akibat NTA terjadi selama
ÄÅ ÄÆ
ÇÈÉÊ ËÊ ÌÊ ÍÎÏÈÐ ÈÌÎÉ ÎÅÐ
ÆÑÒÑÉÓ ÔÕem ÖÔ×ØÔÙ ÕÚÏÛ ×ÛÜ ÝÕÝ Ô×
Penelitian akan dilakukan di Laboratorium Biokimia/Kimia Bahan Makanan
(KBM) Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) Universitas
Sumatera Utara (USU) Medan, Laboratorium Biologi FMIPA Universitas
Sumatera Utara dan Laboratorium Patologi Anatomi Fakultas Kedokteran
Universitas Sumatera Utara. Penelitian dilakukan selama ± 2 (dua) bulan yaitu
Bulan Desember 2010 s.d Januari 2011.
ÆÑÞÑß Ô× àÔ× áÔ× âÏã ÓÚ Ü Ôä ÝÖÔ×åÔæÓÛÜÏÛ ×ÛÜÝÕÝ Ô ×
Penelitian ini dilakukan dengan rancangan eksperimental dengan desain
Rancangan Acak Lengkap (RAL). Mencit jantan (çèéê èéë èì èéíL) strain Double Distsch Webster (DDW) dewasa, sebanyak 30 ekor, dengan menggunakan rumus penghitungan Frederer (Frederer, 1963) yaitu: (t-1)(n-1) 15, t adalah jumlah
perlakuan (dalam penelitian ini ada 6 kelompok perlakuan) dan n adalah jumlah
ulangan perkelompok, maka jumlah yang diharapkan secara teoritis adalah 5 (6-1),
sehingga jumlah keseluruhan hewan coba yang diperlukan dalam penelitian ini
adalah 30 ekor mencit jantan dewasa yang dipilih dari hasil perbanyakan untuk
îïîïðñò ñó dñn ôlñõöeneliõ÷ ñó
îïîïøïðñò ñóöùó ùú ÷õ ÷ñó
Hewan coba yang akan digunakan dalam penelitian ini adalah mencit jantan
(ûüýþ üý ÿüüý L.) strain DDW dewasa sehat yang berumur 8-11 minggu dengan
berat 25-35 gram. Mencit jantan dewasa merupakan hasil pengembangan hewan
yang diperoleh dari Fakultas Matematika Ilmu Pengetahuan Alam (FMIPA)
Biologi Universitas Sumatera Utara, sebanyak 30 ekor mencit jantan dewasa yang
dipilih dari hasil perbanyakan untuk keperluan penelitian.
Bahan kimia yang dipergunakan dalam penelitian ini adalah, antara lain:
1. Sediaan vitamin E murni (Merck)
2. Reagensia: 2-thiobarbiturat acid (Merck; Cat No.1.08180.0025),
1,1,3,3-terramethoxypropane 99% (Sigma; Cat. No.108383) 500 µM, Acetic acid
glacial, sodium hydroxide (NaOH) dan aquades.
3. Preparat jaringan: Larutan formalin 10%, alkohol 70%, 96% dan 100%,
toluene, lilin cair, blok parafin, xylol, hematokxylin-eosin (H-E).
îïîï ïôúñõ-alat Penelitian
Alat utama yang dipergunakan dalam penelitian ini, antara lain: jarum oval
(Gauge), spuit 1 ml, bak bedah dan ý ýÿý gelas arloji, cawan petri, batang
pengaduk, timbangan, blender, rotavapor, þ sentrifuse,
spektropotometri, labu ukur, labu Erlen Meyer, buret, ÿ ý ý, mikrotom,
ir u d en !!
Air tuak didapat dari daerah Pancurbatu dengan cara mengambil air nira dari
pohon aren. Ada 4 (empat) air tuak yang diambil untuk menentukan kadar
alkoholnya yaitu: nira aren asli, nira ditambah raru "Rapistrum rugosum L), tuak
asli, tuak yang siap dipasarkan, masing-masing sebanyak 2 liter. Kemudian dibawa
ke Laboratorium Biokimia/Kimia Bahan Makanan FMIPA Universitas Sumatera
Utara untuk ditentukan kadar alkohol yang dikandungnya.
# $ % & & &
# ' $ % & (&b )
1. Tuak (alkohol 20%)
2. Vitamin E (Merck)
# * $i%el erg
1. Bobot ginjal
2. Gambaran mikroskopis tubulus proksimal ginjal
+ & ) & & &,
+ ' & ) & &
Mencit ditempatkan di dalam kandang yang terbuat dari bahan plastik dengan
ukuran 30 x 20 x 10 cm yang ditutup dibagian atasnya dengan kawat kasa. Dasar
kandang dilapisi dengan sekam padi setebal 0,5-1 cm dan diganti setiap 3 hari.
jam gelap (pukul 18.00 s.d 06.00 wib). Pakan (pelet komersial) dan minuman air
-./0 /12atau34530 .6 7disuplai setiap hari.
89:9;9<=> ? @ABC DDE C @@CF Bw@CG Hb@
Penggunaan dan penanganan hewan di laboratorium penelitian dilakukan
dengan aturan etika penelitian hewan. Etika penelitian hewan yang diatur dalam
Deklarasi Helsinki untuk memperoleh ethical clearance dari komite etika dan komite ilmiah penelitian FMIPA Biologi Universitas Sumatera Utara.
89:989Aemberi@CAerl@ ? E @C
Penelitian ini terdiri atas 6 kelompok (1 kelompok kontrol dan 5 kelompok
perlakuan), yaitu:
1. Kelompok 1 (P0) = Kelompok kontrol pertama, terdiri dari 5 ekor mencit jantan
dewasa tanpa perlakuan selama 30 hari.
2. Kelompok 2 (P1) = Kelompok perlakuan pertama, terdiri dari 5 ekor mencit
jantan dewasa yang diberi tuak (alkohol 20%) sebanyak 0,5 ml/hari/ekor secara
oral setiap hari selama 15 hari pertama dan 15 hari berikutnya pemberian tuak
dihentikan dan diganti dengan pemberian aquadest 0,5 ml secara oral.
3. Kelompok 3 (P2) = Kelompok perlakuan kedua, terdiri dari 5 ekor mencit
jantan dewasa yang diberi tuak (alkohol 20%) sebanyak 0,5 ml/hari/ekor secara
oral selama 30 hari.
4. Kelompok 4 (P3) = Kelompok perlakuan ketiga, terdiri dari 5 ekor mencit
oral selama 15 hari pertama dan 15 hari berikutnya tuak dihentikan dan diganti
dengan pemberian vitamin E sebanyak 25 mg/hari/ekor secara oral.
5. Kelompok 5 (P4) = Kelompok perlakuan keempat, terdiri dari 5 ekor mencit
jantan dewasa yang diberi tuak (alkohol 20%) sebanyak 0,5 ml/hari/ekor secara
oral selama 15 hari pertama dan 15 hari berukutnya pemberian tuak dan vitamin
E sebanyak 25 mg/hari/ekor secara oral.
6. Kelompok 6 (P5) = Kelompok perlakuan kelima, terdiri dari 5 ekor mencit
jantan dewasa yang diberi tuak (alkohol 20%) sebanyak 0,5 ml/hari/ekor secara
oral dan pemberian vitamin E sebanyak 25 mg/hari/ekor secara oral selama 30
hari.
PQRQSrTUVW X YSVZV Y[\ U ]]^W ]^SV^_] Z] `]^
Setelah dilakukan perlakuan selama 30 hari, masing-masing hewan percobaan
dikorbankan dengan cara dislokasi leher, selanjutnya dibedah dan isolasi ginjal,
kemudian dilakukan pengamatan sebagai berikut:
PQRQaQSV^_]Z] `]^b]\YTU\Tc[UdeTf T `g[^ h] i j
Setelah dilakukan semua isolasi ginjal (30 ekor mencit jantan dewasa) maka
ginjal kiri dan kanan diletakkan pada kertas ukur dan ditimbang pada timbangan
mikrogram, kemudian dicatat berat masing-masing ginjal.
PQRQk QSYTU VW XYSVZbu]`]^ledi]]^mU`T iT _[i n] Y[^_]^g[^ h] i
Pembuatan sediaan histologi menurut Suntoro (1983) dengan metode parafin
adalah: fiksasi, pencucian, dehidrasi, penjernihan, infiltrasi parafin, penanaman,
pengirisan, penempelan, deparafinasi, pewarnaan, penutupan dan pemberian label.
Organ ginjal (kiri dan kanan) yang telah dipotong-potong kemudian
dimasukkan ke dalam larutan fiksatif Bouin selama 2-10 jam. Setelah proses
fiksasi, kemudian dilakukan dehidrasi secara bertahap dengan menggunakan
alkohol 30%, 50%, 60%, 70%, 80%, 90%, 96% dan 100% (alkohol absolut)
masing-masing selama 60 menit dengan menggunakan shaker. Kemudian
dilanjutkan dengan penjernihan setelah proses dehidrasi dengan menggunakan
xylol murni. Proses infiltrasi parafin dilakukan di dalam oven dengan suhu 58oC.
Organ ginjal dimasukkan ke dalam campuran xylol-parafin dengan perbandingan
dimasukkan ke dalam kotak kecil (leu chart) sebagai cetakan, kemudian
dimasukkan parafin cair sehingga penuh dalam kotak dan dibiarkan parafin
memadat dan mengeras. Blok parafin yang telah mengeras ditempelkan pada
opqrst kayu sampai melekat erat, kemudian dilakukan pemotongan dengan pisau
mikrotom dipasangkan opqrst pada mikrotom. Pemotongan dilakukan dengan
ketebalan 6 µm. Kemudian hasil pemotongan pada puv swx y qz{ { diolesi dengan
larutan albumin mayer dan ditetesi dengan z| } zrs{ ~ Kemudian beberapa pita
parafin diletakkan dipermukaan aquades pada puvswx y q z{ {dan dibiarkan beberapa
saat, kemudianpuvswxy q z { {dipindahkan ke meja pemanasan hingga kering.
Pewarnaan dengan Hematoxylin Erlich-Eosin (H-E) dengan cara preparat
dideparafinasi dalam xylol sampai bebas parafin, kemudian dimasukkan ke dalam
alkohol 96%, 90%, 80%, 70%, 50%, 30% dan aquades, setelah itu ke dalam
larutan Hematoxylin Erlich dibiarkan selama 1 menit lalu dicuci dengan air
mengalir, dicelupkan ke dalam aquades, alkohol 30%, 50% dan 70%. Kemudian
ke dalam larutan Eosin 0,5% selama 1 menit, lalu kedalam alohol 70%, 80%, 90%
dan alkohol absolut, selanjutnya dimasukkan ke dalam xylol. Preparat ditutup
dengan gelas penutup setelah ditetesi dengan z zrz uzq{ z terlebih dahulu,
kemudian diberi label.
meri b inn
in bulu
Prosedur kerja: setiap mencit dibuat preparat ginjal (kiri dan kanan) dan tiap
preparat dibaca (dibagi) dalam 4 lapangan pandang yaitu keempat sudut bagian
jumlahnya setiap bagian lapangan pandang adalah 25 sel, kemudian disesuaikan
dengan tingkat/derajat kerusakan 0, 1, 2, 3 dan 4 selanjutnya dicari rata-ratanya di
4 lapangan pandang. Sasaran yang dibaca adalah perubahan struktur (gambaran)
histologis tubulus kontortus proksimal ginjal mencit, karena sel epitel tubulus
proksimal mencit merupakan tempat absorbsi dan mengkonsentrasikan racun
(Rubin, 2009).
Kriteria normal bila tidak ditemukan adanya perubahan sel pelapis tubulus
proksimal, berupa:
1. Degenerasi hidrofilik (pembengkakan pada sitoplasma)
2. Nekrosis (kematian sel), yang ditandai dengan perubahan sebagai berikut:
- ¡¢£¤ ¥ ¢¥(inti kecil dan padat)
- ¦ ¢¥¢¥(inti pucat dan terlarut)
- §£¥ ¢¥(inti pecah menjadi beberapa gumpalan)
Tingkat/derajat kerusakan sel epitel pelapis tubulus proksimal adalah sebagai
berikut:
0 = Sel dengan inti dan sitoplasma yang masih dalam batas normal
1 = Inti dalam batas normal dan sitoplasma dijumpai degenerasi hidrofilik
2 = Ditemukan nekrotik tubulus proksimal, dengan luas <25%
3 = Ditemukan nekrotik tubulus proksimal, dengan luas 26-50%
4 = Ditemukan nekrotik tubulus proksimal, dengan luas >50%
¨©ª©«n¬i® ¯ ®°¬±¬² ¬ ³´µ³ ¶· ¸¯¬ ³¹ ¯º »±µ® ¯®
Semua data dipresentasikan dalam bentuk rata-rata ± simpangan baku
(rata-rata ± SD). Dilakukan uji normalitas dan homogenitas dari hasil penelitian
didapatkan data dengan distribusi normal dan homogen maka dilakukan uji
parametrik¼½¾¿¼. Bila terdapat perbedaan yang nyata dilanjutkan dengan uji À¾ÁÂ
Ã¾Ä analisis Benferroni taraf 5% untuk melihat perbedaan antara kelompok
kontrol dari masing-masing perlakuan.
Jika distribusi data tidak normal dan tidak homogen maka dilakukan
trasformasi data. Kemudian diuji lagi normalitas dan homogenitas data. Apabila
masih tidak normal distribusinya dan data tidak homogen maka dilakukan uji
Mann-Whitney untuk membandingkan antara 2 kelompok perlakuan (kontrol vs
perlakuan). Pada kelompok data lebih dari 2 kelompok maka dilakukan uji
Friedman.
¨©Å©Æ¬ ² ·¬´µ³µ¯± ¯¬ ³
Keseluruhan kegiatan penelitian ini, mulai dari persiapan sampai pada
penulisan hasil penelitian adalah lebih kurang selama delapan (8) minggu. Urutan
kegiatan dan jadual pelaksanaan secara lengkap dapat dilihat pada Tabel 3.2.
Tabel 3.2. Jadual Penelitian
ÇÈÉ ÊËÌÍ ÎÏÎÇ
ÐÍÇÌ ÌÑÊ Ë
Ò Ó Ô Õ Ö 6 7 8
1. Persiapan
2. Pelaksanaan
3. Analisis Data
×Ø ×Ù
Ú ØÛ ÜÝÞØßàáâ×Ø Ú Ø Û Øß
Ù ãäãÚåæ çl àeneliè çåé
Berdasarkan hasil penelitian dan kumpulan data yang telah dilakukan selama
penelitian, maka dapat dibuat beberapa grafik histogram dan gambar dengan
parameter hasil pengukuran sebagai berikut:
Ù ãäãäã×êë êèìçé íåîâïé ðçèñå é èåéÞ ïwåæå
Data pengukuran bobot ginjal tiap-tiap mencit jantan dewasa seperti yang
ditunjukkan pada Lampiran 2, Tabel 1. Rata-rata hasil analisis data bobot ginjal
mencit jantan (òóôõ óôöó÷ óô øL.) strain DDW yang ditunjukkan pada Gambar 4.1.
Hasil analisis distribusi data dan homogenitas variansi yaitu; data bobot ginjal
distribusinya tidak normal tetapi variansi datanya homogen. Hasil ini tidak
memenuhi asumsi untuk dapat dilakukan uji parametrik. Kemudian dilakukan
transformasi data dan didapatkan data yang tidak normal dan variansinya tetap
homogen. Oleh karena itu dilakukan uji non parametrik Kruskal Wallis, dan
ditemukan tidak adanya perbedaan yang bermakna diantara masing-masing
perlakuan penelitian (p>0,05; Lampiran 2, Tabel 1.), oleh sebab itu tidak dilakukan
uji lanjutan.
Hasil uji didapatkan bahwa bobot ginjal yang tertinggi ditemukan pada
pada kelompok P2 (0,212±0,083 g), dimana tidak dijumpai perbedaan yang
bermakna (p>0,05) dengan kelompok P0, P1, P3, P4, dan P5.
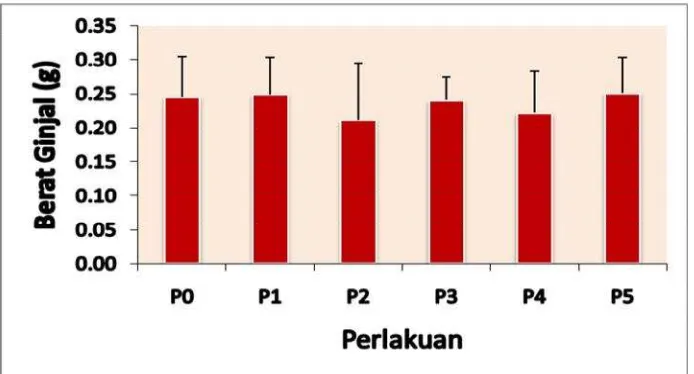
Gambar 4.1. Grafik Bobot Ginjal (g).
Keterangan; Grafik histogram pada perlakuan berbeda yang diikuti oleh huruf kecil yang sama berbeda tidak bermakna pada taraf uji 5%. P0= Tanpa perlakuan; P1= Tuak (alkohol 20%) 0,5 ml 15 hari + Aquadest 0,5 ml 15 hari; P2= Tuak (alkohol 20%) 0,5 ml 30 hari; P3= Tuak (alkohol 20%) 0,5 ml 15 hari + Vitamin E 0,25 mg 15 hari; P4= Tuak (alkohol 20%) 0,5 ml 15 hari + Tuak (alkohol 20%) 0,5 ml & Vitamin E 0,25 mg 15 hari; P5= Tuak (alkohol 20%) 0,5 ml & Vitamin E 0,25 mg 30 hari; = standar deviasi (SD).
ùúûúüú ýenilþÿ þ ý rubþ þ ubulu ýÿ þ ÿ þ ÿ þ ÿ
ÿþ þ wþþ
Hasil pengamatan perubahan jaringan ginjal atau sel ginjal (tubulus
proksimal) yang mengalami nekrotik pada mencit jantan dewasa ditunjukkan pada
Lampiran 2, Tabel 2. Rata-rata hasil analisis datanya ditunjukkan pada Gambar
4.2. Hasil analisis distribusi data dan homogenitas variansi adalah sebagai berikut;
semua data sel ginjal nekrotik distribusinya normal dan variansi datanya homogen.
dilakukan uji ANOVA pada taraf 5% dan ditemukan adanya perbedaan yang
bermakna antara masing-masing perlakuan penelitian (p<0,05) (Lampiran 2, Tabel
2.). Oleh sebab itu dilakukan Post Hoc test-Bonferroni untuk melihat ada/tidaknya
perbedaan rata-rata jarak sel ginjal nekrotik antara masing-masing kelompok
perlakuan (kelompok P0-P5).
Gambar 4.2. Grafik Sel Ginjal Yang Mengalami Nekrotik (%).
Keterangan; Grafik histogram pada perlakuan berbeda yang diikuti oleh huruf kecil yang sama berbeda tidak bermakna pada taraf uji 5%. P0= Tanpa perlakuan; P1= Tuak (alkohol 20%) 0,5 ml 15 hari + Aquadest 0,5 ml 15 hari; P2= Tuak (alkohol 20%) 0,5 ml 30 hari; P3= Tuak (alkohol 20%) 0,5 ml 15 hari + Vitamin E 0,25 mg 15 hari; P4= Tuak (alkohol 20%) 0,5 ml 15 hari + Tuak (alkohol 20%) 0,5 ml & Vitamin E 0,25 mg 15 hari; P5= Tuak (alkohol 20%) 0,5 ml & Vitamin E 0,25 mg 30 hari; = standar deviasi (SD).
Hasil uji terhadap sel ginjal (tubulus proksimal) nekrotik yang terluas
didapatkan pada kelompok P2 (73,50±10,89%), sedangkan sel ginjal nekrotik yang
paling minimal didapatkan pada kelompok P0 (1,00±0,004%), dari hasil uji ini
menunjukkan adanya perbedaan yang bermakna (p<0,05) dengan kelompok P1,
Pada Gambar 4.3. ini menunjukkan perubahan struktur histopatologi jaringan
ginjal dari beberapa kelompok perlakuan penelitian.
Gambar 4.3. Perubahan Struktur Histopatologi Jaringan Ginjal Mencit. Pembesaran 400 x, Pewarnaan H-E. Keterangan; G= glomerulus. P0= tanpa perlakuan; P1= Tuak (alkohol 20%) 0,5 ml 15 hari + Aquadest 0,5 ml 15 hari; P2= Tuak (alkohol 20%) 0,5 ml 30 hari; P3= Tuak (alkohol 20%) 0,5 ml 15 hari + Vitamin E 0,25 mg 15 hari; P4= Tuak (alkohol 20%) 0,5 ml 15 hari + Tuak (alkohol 20%) 0,5 ml & Vitamin E 0,25 mg 15 hari; P5= Tuak (alkohol 20%) 0,5 ml & Vitamin E 0,25 mg 30 hari; = standar deviasi (SD).
emb ! "
#$% $&'( " )*+," -( &. "& ",w!
Mencit jantan yang memiliki bobot ginjal paling tinggi adalah pada kelompok
P5 (0,251±0,053 g), tetapi tidak terdapat perbedaan yang bermakna dengan
kelompok perlakuan lainnya (kelompok P0-P4). Hal ini kemungkinan disebabkan
karena adanya penambahan vitamin E yang besamaan dengan pemberian tuak.
Vitamin E dapat menekan radikal bebas yang merupakan efek dari tuak (alkohol).