ABSTRACT
Antimicrobial Activity of Bacteriocins Produced by Lactobacillus plantarum against Patogenic Bacterias during Store at Cold Temperature
Bariyah, K., I.I. Arief and Z. Wulandari
Bacteriocins are antimicrobial substances produced by lactic acid bacteria (LAB) which can be used as a natural preservative. The preservative method which commonly used in storage under temperature of 4-10 °C. This method does not guarantee that it can inhibit the bacterial growth, such as psikrofil bacteria which still active on the refri temperature. The aim of this research was to study the stability of antimicrobia bacteriocins produced by L. plantarum 1A5, 1B1, 2B2, and 2C12 through its sensitivity during store at cold temperature (10 °C) againts the pathogenic bacteria that consists of Salmonella enteritidis ser. Typhimurium ATCC 14028, E. coli ATCC 25922, S. aureus ATCC 25923, P. aeruginosa ATCC 27853, and B. cereus. Plantaricin that was used is the result of cation exchange chromatography purification. Storage duration for 15 days and testing was done in intervals of 5 days. The antagonistic assay showed the antimicrobial activity against the pathogenic bacteria. The results showed that plantaricin 1A5, 1B1, 2B2, and 2C12 during cold storage temperature is still effective to be used for antagonistic assay to the pathogen indicator bacteria. Plantaricin of the four strains is able to inhibit bacterial growth indicators. Plantaricins has been stored for 15 days still have antimicrobial activity. This showed that the four plantaricins remained active after storage for 15 days at cool temperatures (10 °C).
1
PENDAHULUAN Latar Belakang
Masalah keamanan pangan (food safety) masih merupakan kendala utama
dalam produk makanan. Mutu dan keamanan pangan perlu diperhatikan karena dapat
membahayakan kesehatan bagi konsumen. Mikroorganisme patogen yang sering
terdapat di dalam bahan pangan diantaranya Salmonella enteritidis ser. Typhimurium, E. coli, S. aureus, P. aeruginosa, dan B. cereus. Bakteri patogen tersebut beresiko menimbulkan penyakit bahkan kematian. Alternatif dalam
mengatasi masalah tersebut adalah dengan pengolahan dan pengawetan pangan.
Metode pengawetan yang telah banyak diaplikasikan adalah penambahan
bahan pengawet pada makanan, baik bahan pengawet sintetis maupun alami.
Penggunaan pengawet sintetis dapat menyebabkan kemungkinan toksin akibat residu
yang masih aktif, bahaya mikroorganisme yang resisten dan dapat menimbulkan
infeksi pada konsumen. Penggunaan pengawet kimia yang dapat diserap bahan
organik mengakibatkan efektivitas bahan pengawet alami berupa antimikrob yang
dihasilkan oleh bakteri asam laktat berkurang. Penggunaan bahan pengawet alami
lebih berpotensi untuk diaplikasikan sebagai pengganti pengawet sintetis.
Bakteriosin merupakan salah satu substansi antimikrob yang dihasilkan
bakteri asam laktat dan memiliki aktivitas antagonistik, baik bakteriostatik maupun
bakterisidal. Bakteriosin berpotensi digunakan sebagai bahan pengawet pangan alami
yang aman untuk dikonsumsi, karena zat aktif yang terdapat dalam bakteriosin
adalah protein yang dapat didegradasi oleh enzim proteolitik. Galur L. plantarum
1A5, 1B1, 2B2, dan 2C12 diketahui menghasilkan suatu senyawa antimikrob sebagai
bakteriosin yang dapat menghambat pertumbuhan bakteri patogen di dalam bahan
pangan.
Pendinginan merupakan salah satu metode pengawetan bahan pangan. Suhu
pendinginan yang umum digunakan yaitu suhu refrigerator 4 – 10 °C. Metode pengawetan ini belum menjamin pertumbuhan bakteri pada bahan pangan, seperti
golongan bakteri psikrofil terhambat. Penambahan bakteriosin dalam bahan pangan
yang disimpan pada suhu dingin diharapkan mampu menjadi alternatif solusi dari
kasus tersebut. Penelitian ini menggunakan suhu penyimpanan 10 °C karena
2 penyimpanan makanan di refrigerator. Plantarisin galur L. plantarum 1A5, 1B1, 2B2 dan 2C12 diharapkan masih memiliki aktivitas antimikrob selama penyimpanan suhu
dingin (10 °C).
Tujuan
3
TINJAUAN PUSTAKA Bakteri Asam Laktat
Sifat yang terpenting dari bakteri asam laktat adalah memiliki kemampuan
untuk memfermentasi gula menjadi asam laktat. Berdasarkan tipe fermentasi, bakteri
asam laktat terbagi menjadi homofermentatif dan heterofermentatif. Kelompok
homofermentatif menghasilkan asam laktat sebagai produk utama dari fermentasi
gula, sedangkan kelompok heterofermentatif menghasilkan asam laktat dan senyawa
lain yaitu CO2, etanol, asetaldehid, diasetil. Bakteri yang termasuk ke dalam bakteri asam laktat adalah famili Lactobacillaceae, yaitu Lactobacillus, dan famili
Streptococcoceae, terutama Leuconostoc, Streptococcus dan Pediococcus. Streptococcus, Pediococcus dan beberapa spesies Lactobacillus bersifat homofermentatif, sedangkan Leuconostoc dan spesies Lactobacillus yang lain bersifat heterofermentatif (Fardiaz, 1992).
Bakteri asam laktat termasuk mikroorganisme yang aman jika ditambahkan
dalam pangan karena bersifat tidak toksik dan tidak menghasilkan toksin. Bakteri ini
secara luas didistribusikan pada susu, daging segar, sayuran dan produk-produk hasil
olahan. Bakteri asam laktat juga disebut sebagai biopreservatif karena dapat
menghambat pertumbuhan bakteri patogen dan mampu membawa dampak positif
bagi kesehatan manusia (Smid dan Gorris, 2007).
Bakteriosin banyak diteliti karena berpotensi sebagai pengawet makanan
alami dan dapat diaplikasikan di bidang farmasi. Beberapa jenis bakteriosin
mempunyai spektrum yang luas dan mempunyai aktivitas menghambat terhadap
pertumbuhan beberapa patogen makanan seperti Listeria monocytogenes dan S. aureus. Bakteri asam laktat didefinisikan sebagai bakteri pembentuk asam laktat dalam metabolisme karbohidrat dan terdiri atas berbagai macam kelompok bakteri
Gram positif (Frazier dan Westhoff, 1998). Satu atribut penting dari bakteri asam
laktat adalah memiliki kemampuan memproduksi komponen antimikrob, berupa
bakteriosin yang potensial menjadi biopreservatif menggantikan pengawet kimiawi
pada bahan makanan untuk memperpanjang umur simpan produk. Kemampuan
bakteriosin sebagai biopreservatif dicapai dengan efek penghambatan terhadap
4
L. plantarum
L. plantarum merupakan salah satu jenis BAL (Bakteri Asam Laktat) homofermentatif dengan temperatur optimal lebih rendah dari 37 oC (Frazier dan Westhoff, 1998). L. plantarum berbentuk batang dan tidak bergerak (non motil). Bakteri ini memiliki sifat katalase negatif, aerob atau fakultatif anaerob, cepat
mencerna protein, tidak mereduksi nitrat, toleran terhadap asam dan mampu
memproduksi asam laktat. L. plantarum dalam media agar, membentuk koloni berukuran 2 – 3 mm, berwarna putih opaque, conveks dan dikenal sebagai bakteri pembentuk asam laktat (Kuswanto dan Sudarmadji, 1988). L. plantarum mampu merombak senyawa kompleks menjadi senyawa yang lebih sederhana dengan hasil
akhir yaitu asam laktat. Menurut Buckle et al. (2007) asam laktat dapat menghasilkan pH yang rendah pada substrat sehingga menimbulkan suasana asam.
Pertumbuhan L. plantarum dapat menghambat kontaminasi mikrooganisme patogen dan penghasil racun karena memiliki kemampuan untuk menghasilkan asam laktat
dan menurunkan pH substrat. Selain itu bakteri asam laktat dapat menghasilkan
hidrogen peroksida yang dapat berfungsi sebagai antibakteri. L. plantarum juga mempunyai kemampuan menghasilkan bakteriosin yang berfungsi sebagai zat
antibiotik (Jenie dan Rini, 1995).
L. plantarum 1A5, 1B1, 2B2 dan 2C12 merupakan isolat indigenus yang diisolasi dari daging sapi lokal Indonesia (Arief et al., 2008). Senyawa antimikrob tersebut dapat menghambat pertumbuhan bakteri patogen E. coli, Salmonella enteritidis ser. Typhimurium, S. aureus. P. aeruginos dan B. cereus. Senyawa antimikrob yang diproduksi Lactobacillus sp. 1A5, 1B1, 2B2 dan 2C12 mengandung bakteriosin.
Bakteriosin
Bakteriosin adalah antibakteri protein kelompok heterogen yang berbeda
dalam spektrum aktivitas, pola kerja, berat molekul, asal genetik, dan sifat biokimia
(Omar et al., 2006). Bakteriosin umumnya dihasilkan oleh Bakteri Asam Laktat (BAL), yang memproduksi asam laktat sebagai produk utama metabolisme. Asam
laktat memiliki kemampuan menghambat pertumbuhan mikroba dalam makanan,
5 Bakteriosin merupakan substansi protein, umumnya mempunyai berat
molekul kecil serta memiliki aktivitas sebagai bakterisidal dan bakteriostatik.
Pengujian bakteriosin dapat menggunakan metode difusi sumur, dengan indikator
terdapat zona hambat di sekitar sumur. Diameter zona hambat yang terbentuk dapat
berupa diameter zona bening di sekeliling sumur yang menunjukkan sifat
bakterisidal (membunuh bakteri) maupun diameter zona semu yang merupakan sifat
bakteriostatik (menghambat pertumbuhan mikroba). Bakteriosin merupakan protein
atau peptida pada bakteri yang menunjukkan aksi bakterisidal ataupun bakteriostatik
terhadap spesies yang umumnya berkerabat dekat namun terdapat pula beberapa
jenis bakteriosin dapat menunjukkan spektrum yang lebih luas (Jimenez-diaz, 1993).
Sifat antagonistik bakteriosin telah banyak dimanfaatkan dalam bidang
biopreservatif pangan, karena memiliki kemampuan menghambat bakteri Gram
positif atau Gram negatif. Banyak bakteriosin dapat secara bakterisidal melawan
spesies-spesies dan strain yang berkerabat dekat dengan bakteriosin tersebut, namun
beberapa bakteriosin dapat secara efektif melawan banyak bakteri dari spesies dan
genus yang berbeda (Ray dan Bhunia, 2008). Saat ini bakteriosin sudah mulai
diterapkan sebagai salah satu biopreservatif karena bersifat alami dan tidak
menyebabkan efek negatif pada konsumen. Molekul protein bakteriosin mengalami
degradasi oleh enzim proteolitik dalam pencernaan manusia sehingga tidak
membahayakan. Bakteriosin telah digunakan di negara maju sebagai biopreservatif
pada bahan pangan karena memiliki kemampuan menghambat bakteri perusak dan
patogen, serta tidak meninggalkan residu yang menimbulkan efek negatif pada
manusia (Usmiyati et al., 2009).
Bakteri Patogen
Bakteri patogen merupakan mikroorganisme yang dapat menyebabkan
penyakit. Bakteri tertentu dapat menyebabkan penyakit pada manusia. Beberapa jenis
penyakit tersebut dapat dipindahkan melalui pangan, diantara penyakit yang
disebabkan kerusakan pangan yaitu keracunan makanan, kolera dan tifus (Gaman
dan Sherrington, 1992). Bakteri yang tumbuh di dalam bahan pangan terbagi menjadi
dua yaitu bakteri pembusuk yang dapat menyebabkan kerusakan makanan dan
bakteri patogen penyebab penyakit pada manusia. Jumlah bakteri pembusuk
6 yang diamati sebagai bakteri pembusuk dan patogen pada produk fermentasi adalah
dari famili Enterobactericeae (Fardiaz, 1992).
Terdapat dua cara bakteri dapat menularkan penyakit pada manusia yaitu 1)
intoksikasi, yaitu makanan mengandung toksin yang dihasilkan bakteri yang tumbuh
di dalam makanan tersebut, dan 2) infeksi, yaitu penyakit yang disebabkan bakteri
masuk ke dalam tubuh melalui makanan yang telah terkontaminasi dan ada reaksi
dari tubuh terhadap keberadaan atau metabolit-metabolit yang dihasilkan bakteri
selama tumbuh di dalam tubuh (Frazier dan Westhoff, 1998). Bakteri secara umum
dibedakan menjadi dua bagian berdasarkan sifat pewarnaan Gram yaitu Gram positif
dan Gram negatif. Bakteri Gram positif adalah bakteri yang memberi respon
berwarna biru keunguan jika dilakukan uji pewarnaan Gram, sedangkan Gram
negatif memberikan respon warna merah jika dilakukan uji pewarnaan Gram
(Tortora et al., 2006).
E. coli
Bakteri ini merupakan bakteri Gram negatif. E. coli secara normal terdapat di dalam alat-alat pencernaan manusia dan hewan. Bakteri ini memiliki ciri-ciri umum
yaitu bergerak, berbentuk batang, bersifat fakultatif anaerob dan termasuk golongan
Enterobacteriaceae. Suatu serotipe tertentu bersifat enterophatogenic dan dikenal sebagai penyebab diare pada bayi. Organisme ini berada di dapur dan tempat-tempat
persiapan bahan pangan melalui bahan baku kemudian masuk ke makanan yang telah
dimasak melalui tangan. Masa inkubasi bakteri ini yaitu selama 1 – 3 hari dan
gejala-gejala yang muncul menyerupai gejala-gejala-gejala-gejala keracunan bahan pangan yang tercemar
Salmonella atau disentri (Buckle et al, 2007).
E. coli merupakan salah satu spesies jenis Escherichia dan disebut koliform fekal karena ditemukan di saluran usus hewan dan manusia, sehingga sering terdapat
di dalam feses. Bakteri ini sering digunakan sebagai indikator kontaminasi kotoran
(Fardiaz, 1992). E. coli dapat tumbuh optimum pada pH 7 – 7,5 dengan pH minimum 4 dan pH maksimum 8,5. Bakteri ini sensitif terhadap panas dan pada makanan yang
mengalami pemanasan. Suhu optimum untuk pertumbuhan bakteri Escherichia coli
7
Salmonella enteritidis ser. Typhimurium
Salmonella merupakan bakteri Gram negatif. Salmonella memiliki ciri-ciri yaitu berbentuk batang, bergerak dan mempunyai tipe metabolisme yang bersifat
fakultatif anaerob. Salmonella termasuk kelompok bakteri Enterobacteriaceae.
Salmonella telah dibedakan secara serologis dan diberi nama khusus. Salmonella typhimurium, Salmonella agona, dan Salmonella panama hanya sebagian kecil dari berbagai jenis mikroorganisme penyebab keracunan bahan pangan tipe
gastroenteritis yang sudah lama dikenal. Salmonella penyebab gastroenteritis ditandai oleh gejala-gejala yang umumnya nampak 12 – 13 jam setelah makan bahan
pangan yang tercemar. Gejala-gejala tersebut adalah berak-berak (diarrhea), sakit
kepala, muntah-muntah, dan demam dan dapat berakhir selama 1-7 hari. Tingkat
kematian kurang dari 1%, tetapi jumlah ini dapat meningkat pada anak-anak, orang
tua, atau orang yang lemah. Tempat terdapatnya jenis mikroorganisme ini adalah
pada alat-alat pencernaan hewan dan burung, baik yang telah diternakkan ataupun
yang masih liar. Keracunan pangan karena Salmonella terutama berhubungan dengan daging sapi dan ayam yang baru dimasak, namun dapat beracun karena sesuatu hal
yaitu pemasakan serta pengolahan yang kurang sempurna sebelum dikonsumsi
(Buckle et al., 2007).
Salmonella sp. tumbuh pada tingkat keasaman antara 4,5 – 5,4 dengan pH optimumnya sekitar 7. Nilai pH minimum bervariasi tergantung pada suhu inkubasi,
komposisi media, aw dan jumlah sel. Pada pH kurang dari 4,0 dan lebih dari 9,0
Salmonella akan mati secara perlahan (Adam dan Moss, 2007).
S. aureus
S. aureus merupakan bakteri Gram positif. S. aureus memiliki ciri-ciri yaitu berbentuk bola berkelompok seperti buah anggur, bakteri ini tidak bergerak,
fakultatif anaerob dan banyak tumbuh pada produk-produk yang mengandung NaCl
sampai 16%. Produk-produk bahan pangan yang telah dimasak atau diasinkan,
dengan organisme-organisme yang telah rusak karena pemanasan atau
pertumbuhannya terhambat karena konsentrasi garam, sel-sel S. aureus dapat terus berkembang mencapai tingkat yang membahayakan. Gejala-gejala dari keracunan
8 termakan dapat menyebabkan serangan mendadak yaitu kekejangan pada perut dan
muntah-muntah yang hebat (Buckle et al,. 2007).
Kebanyakan galur S. aureus bersifat patogen dan memproduksi enterotoksin yang tahan panas, ketahanan panas bakteri ini melebihi sel vegetatifnya. Beberapa
galur, terutama yang bersifat patogenik, memproduksi koagulase (menggumpalkan
plasma), bersifat proteolitik, lipolitik dan betahomolitik. Spesies lain yaitu
Staphylococcus epidermidis, biasanya tidak bersifat patogen dan merupakan flora normal yang terdapat pada kulit tangan dan hidung (Fardiaz, 1992). Suhu minimum
pertumbuhan Staphylococcus aureus adalah 6 – 7 °C, suhu maksimum 45,5 °C, sedangkan suhu optimum pertumbuhan adalah 35 – 37 °C. Nilai pH optimum adalah
7 – 7,5 dengan kisaran pH 4 – 9,8. Bakteri ini memproduksi pigmen kuning sampai
orange (Fardiaz, 1992).
P. aeruginosa
Pseudomonas merupakan salah satu jenis dalam kelompok
Pseudomonadaceae yang sering menimbulkan kebusukan makanan. Bakteri ini bersifat motil dengan flagella polar. Sifat-sifat penting Pseudomonas yang mempengaruhi pertumbuhan pada makanan adalah (1) umumnya mendapatkan
sumber karbon dari senyawa yang bukan karbohidrat, (2) dapat menggunakan
senyawa-senyawa nitrogen sederhana, (3) kebanyakan spesies tumbuh baik pada
suhu rendah (bersifat psikrofilik, mesofilik dengan suhu optimum relatif rendah),
kecuali P. aeruginosa dan P. fluorescens yang dapat tumbuh pada suhu 37 °C, (4) memproduksi senyawa-senyawa yang bau busuk, (5) dapat mensintesa faktor-faktor
pertumbuhan dan vitamin, (6) beberapa spesies bersifat proteolitik (memecah
protein) dan lipolitik (memecah lemak) dan pektinolitik (memecah pektin), (7)
pertumbuhan pada posisi aerobik berjalan dengan cepat, dan biasanya membentuk
lender, (8) tidak tahan terhadap panas dan keadaan kering, oleh karena itu mudah
dibunuh dengan proses pemanasan dan pengeringan (Fardiaz, 1992).
B. cereus
9 menggumpalkan susu. Beberapa spesies Bacillus juga bersifat lipolitik (memecah lipid), sedangkan yang lain tidak bersifat lipolitik (Fardiaz, 1992).
Bakteri Bacillus merupakan Gram positif. B. cereus memiliki ciri-ciri berbentuk batang, bergerak, dapat membentuk spora, bersifat fakultatif anaerob dan
tersebar secara luas dalam tanah dan air. Organisme ini sampai saat ini belum dapat
dikatakan sebagai bakteri patogenik. Sejumlah keracunan akibat tercemarnya bahan
pangan dengan bakteri ini banyak ditemukan pada daging saus berempah dan nasi
goreng. Kemampuan Bacillus membentuk spora memungkinkan mikroorganisme ini tetap hidup pada operasi pengolahan dengan pemanasan. Gejala-gejala keracunan
bahan pangan yang tercemar karena bakteri ini termasuk diare, sakit perut dan
kadang muntah-muntah, tetapi belum jelas apakah ini merupakan suatu bentuk
10
MATERI DAN METODE Lokasi dan Waktu
Penelitian ini dilaksanakan di Laboratorium Terpadu Ilmu Produksi dan
Teknologi Peternakan, Fakultas Peternakan Institut Pertanian Bogor. Kegiatan
Penelitian dilaksanakan selama enam bulan dari April sampai September 2011.
Materi
Bahan-bahan yang digunakan dalam penelitian ini adalah isolat indigenus
bakteri asam dari daging sapi lokal Indonesia yaitu L. plantarum 1A5, 1B1, 2B2 dan 2C12 serta bakteri indikator Salmonellaenteritidis ser. Typhimurium ATCC 14028,
E. coli ATCC 25922, S. aureus ATCC 25923, P. aeruginosa ATCC 27853 dan B. cereus, media De Man Rogosa and Sharpe Broth (MRSB), De Man Rogosa Sharp
Agar (MRSA), Yeast Extract (YE) 3%, NaCl 1%, NaOH 1 N, ammonium sulfat,
buffer kalium fosfat, resin SP Sepharose – Fast flow, media Mueller Hinton Agar
(MHA), Bacto Agar (BA), dan aquadest.
Alat-alat yang digunakan dalam penelitian ini adalah tabung reaksi, jarum
Ose, cawan petri, tabung Erlenmeyer, membran saring Sartorius, gelas ukur, pipet volumetrik, mikro pipet, sentrifuse, incubator, refrigerator, membran dialisis, vortex, alumunium foil, kapas, bunsen, alkohol 70%, kertas saring, plastik PE, plastik wrap, oven, otoklaf, pH meter, neraca digital dan jangka sorong.
Prosedur
Pemeriksaan Kemurnian Bakteri Asam Laktat (Pelczar dan Chan, 2005)
Kultur starter yang telah diisolasi dari daging sapi pada penelitian sebelum-
nya dikonfirmasi kembali untuk memastikan kemurnian kultur dengan cara
ditumbuhkankan pada media De Man Rogosa Sharp Agar (MRSA) dengan metode
striking dan diinkubasi pada suhu 37 °C selama 24 jam, kemudian diambil satu koloni yang dianggap sebagai koloni bakteri asam laktat dan dimasukkan ke De Man Rogosa Sharp Broth (MRSB). Kultur ini disebut kultur stok. Setiap kultur stok dilakukan penyegaran pada media MRSB sebelum dilakukan pengujian. Sebanyak
satu ml kultur diinokulasikan ke dalam media MRSB. Kultur kemudian diinkubasi
11 yang digunakan untuk mengkonfirmasi bakteri uji. Uji yang dilakukan adalah uji
pewarnaan Gram.
Pewarnaan Gram (Hadioetomo, 1990). Sampel bakteri dari koloni yang homogeny
dioleskan pada kaca objek kemudian difiksasi panas. Satu ose bakteri kemudian
diteteskan dengan kristal violet selama satu menit, diratakan, dibilas dengan akuades
dan dikering udarakan. Setelah kering, olesan bakteri diteteskan iodium dan
diratakan kembali, kering udara selama dua menit, kemudian dibilas akuades dan
ditiriskan. Preparat dicuci dengan pemucat warna yaitu alkohol 95% setetes demi
setetes selama 30 detik, kemudian dicuci segera dengan akuades dan ditiriskan.
Setelah kering, preparat diteteskan minyak imersi dan diamati di bawah mikroskop
untuk melihat bentuk dan warna dinding sel setelah dilakukan pewarnaan. Bakteri
yang termasuk dalam kelompok Gram positif akan menunjukkan warna ungu,
sedangkan kelompok bakteri Gram negatif akan menunjukkan warna merah safranin.
Produksi Supernatan Netral Asal Isolat L. plantarum 1A5, 1B1, 2B2 dan 2C12 (Todorov dan Dicks, 2005)
Sebanyak 500 ml media MRS-broth ditambah yeast extrack 3% dan NaCl 1% diinokulasikan dengan 10% (v/v) kultur L. plantarum. Terdapat empat galur L. plantarum yang digunakan untuk diperoleh bakteriosin yaitu L. plantarum 2C12, 1A5, 1B1, dan 2B2 yang telah disegarkan, selanjutnya diinkubasi pada suhu 37 °C
selama 20 jam. Setelah selesai diinkubasi, L. plantarum disimpan pada refrigerator
suhu 4 °C selama dua jam dan dilakukan sentrifugasi pada kecepatan 10.000 rpm
selama 20 menit suhu 4 °C. Setelah selesai, dilakukan penyaringan dengan
menggunakan membran saring Sartorius berdiameter 0,22 µm yang selanjutnya
supernatan bebas sel dari setiap galur L. plantarum dinetralkan menjadi pH 5,8 – 6,2 dengan menggunakan 1 N NaOH. Pengecekan pH menggunakan kertas lakmus dan
pH meter dengan kalibrasi dua kali yaitu pH 7 dan pH 4. Supernatan bebas sel yang
telah dinetralkan kemudian dilakukan uji antagonistik terhadap bakteri patogen
Salmonella ATCC 14028, E. coli ATCC 25922, S. aureus ATCC 25923, B. cereus
dan P. aeruginosa ATCC 27853. Pengujian ini dilakukan untuk mengetahui aktivitas penghambatan supernatan bebas sel galur 1A5, 1B1, 2B2 dan 2C12 pada bakteri
12
Tabel 1. Penggunaan Padatan Ammonium Sulfat (% Penjenuhan)
Awal % 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100
Konsentrasi Akhir dari Padatan Ammonium Sulfat (g) / 1000 ml
0 10.6 13.4 16.4 19.4 22.6 25.8 29.1 32.6 36.1 39.8 43.6 47.6 51.6 55.9 60.3 65.0 69.7 10 5.3 8.1 10.9 13.9 16.9 20.0 23.3 26.6 30.1 33.7 37.4 41.2 45.2 49.3 53.6 58.1 62.7 20 0 2.7 5.5 8.3 11.3 14.3 17.5 20.7 24.1 27.6 31.2 34.9 38.7 42.7 46.9 51.2 55.7 25 0 2.7 5.6 8.4 11.5 14.6 17.9 21.1 24.5 28.0 31.7 35.5 39.5 43.6 47.8 52.2
30 0 2.8 5.6 8.6 11.7 14.8 18.1 21.4 24.9 28.5 32.3 36.2 40.2 44.5 48.8
35 0 2.9 5.7 8.7 11.8 15.1 18.4 21.8 25.8 29.6 32.9 36.9 41.0 45.3
40 0 2.9 5.8 8.9 12.0 15.3 18.7 22.2 26.3 29.6 33.5 37.6 41.8
45 0 3.0 5.9 9.0 12.3 15.6 19.0 22.6 26.3 30.2 34.2 38.3
50 0 3.0 6.0 9.2 12.5 15.9 19.4 23.5 26.8 30.8 34.8
55 0 3.1 6.1 9.3 12.7 16.1 20.1 23.5 27.3 31.2
60 0 3.1 6.2 9.5 12.9 16.8 20.1 23.9 27.9
65 0 3.2 6.3 9.7 13.2 16.8 20.5 24.4
70 0 3.2 6.5 9.9 13.4 17.1 20.9
75 0 3.3 6.6 10.1 13.7 17.4
80 0 3.4 6.7 10.3 13.9
85 0 3.4 6.8 10.5
90 0 3.4 7.0
95 0 3.5
100 0
13 Purifikasi Parsial dengan Menggunakan Presipitasi Ammonium Sulfat (Todorov dan Dicks, 2005)
Supernatan antimikrob yang telah disaring steril ditambahkan serbuk ammonium
sulfat sebanyak 80% secara bertahap (20%, 40%, 60%, dan 80%) untuk menghasilkan
endapan protein, kemudian dihomogenkan secara perlahan pada suhu 4 oC selama dua jam (Abo Amer, 2007). Tahapan ini dilakukan untuk menghasilkan endapan protein
yang selanjutnya disebut presipitat bakteriosin. Presipitat dikoleksi pada tabung steril.
Pengecekan protein dari presipitat bakteriosin diamati dengan menggunakan
spektrofotometer UV-Vis pada absorbansi 280 nm.
Dialisis. Dialisis dilakukan dengan tujuan untuk desalting atau menghilangkan garam ammonium sulfat yang masih bercampur dengan presipitat bakteriosin. Buffer yang digunakan adalah buffer kalium fosfat pH 6,8 (campuran KH2PO4 dan K2HP04) dengan perbandingan 1 : 1.000 (1 bagian presipitat dan 1.000 bagian buffer). Dialisis dilakukan dengan menggunakan membran dialisis berdiameter 20 pada buffer kalium fosfat selama 12 jam, dan dilakukan penggantian buffer sebanyak dua kali (2 dan 4 jam) pada suhu 4 °C. Setelah selesai, didapatkan ekstrak kasar bakteriosin. Pengecekan protein
plantarisin hasil dialisis diamati menggunakan spektrofotometer UV-Vis pada panjang
gelombang 280 nm.
Purifikasi dengan Menggunakan Kromatographi Pertukaran Kation (Hata et al., 2010)
Kolom diisi dengan resin SP Sepharose – fast flow. Buffer yang digunakan adalah buffer kalium fosfat pH 6,8. Kolom terlebih dahulu dipasangkan pada penjepit Bunsen kemudian buffer dituangkan ke dalam kolom. Setelah itu buffer dibuang secara perlahan. SP Sepharose secara perlahan dengan menggunakan pipet Pasteur dimasukkan ke dalam kolom, dan diusahakan supaya tidak ada udara (gas) yang masuk ke dalam
kolom. Selanjutnya resin akan menjadi gel. Kemudian di atas resin diberikan buffer dan kolom disimpan pada refrigerator (4 °C).
Plantarisin hasil dialisis dimasukkan ke dalam kolom secara perlahan-lahan, dan
di bawah kolom diberikan tabung penampung eluent yang keluar dari kolom. Eluent
14
dengan buffer kembali dan ditampung untuk mengambil eluent yang terikat pada gel (resin). Semua dilakukan pada suhu dingin (4 °C). Setelah selesai dalam beberapa
tabung koleksi didapatkan eluent yang berisi plantarisin murni. Plantarisin murni disimpan pada suhu dingin (4 °C) dan protein plantarisin murni diukur dengan
menggunakan spektrofotometer yang selanjutnya plantarisin murni siap untuk dianalisis
sifat dan karakteristiknya.
Karakteristik Plantarisin (Hata et al., 2010)
Ketahanan terhadap Suhu. Uji ketahanan terhadap suhu sangat penting untuk mengetahui karakteristik aktivitas plantarisin sebagai antimikrob yang dapat
diaplikasikan pada berbagai kondisi penanganan dan pengolahan pangan. Plantarisin
murni hasil kromatografi kolom diuji ketahanannya setelah mengalami penyimpanan
selama 15 hari yaitu 0, 5, 10, dan 15 hari pada suhu refrigerator (10 °C). Ketahanan terhadap suhu dilihat dengan menguji aktivitas antimikrob plantarisin murni hasil
perlakuan lama penyimpanan dengan metode sumur. Zona hambat (baik zona bening
maupun zona semu) yang terdapat disekitar sumur pada cawan yang berisikan bakteri
patogen dan pembusuk, menunjukkan bahwa plantarisin tersebut masih memiliki
aktivitas antagonistik selama penyimpanan terhadap bakteri patogen.
Aktivitas Antimikrob Plantarisin terhadap Bakteri Patogen dan Pembusuk Makanan (Salmonella enteritidis ser. Typhimurium ATCC 14028, E. coli ATCC 25922, S. aureus ATCC 25923, P. aeruginosa ATCC 27853, dan B. cereus).
Plantarisin murni hasil kromatografi kolom disiapkan dengan melarutkan 1:1
(v/v) plantarisin dengan buffer kalium fosfat. Metode yang digunakan adalah metode difusi sumur (Savadogo et al., 2006). Bakteri indikator (Patogen dan pembusuk makanan) sebanyak 106 cfu/ml yang berumur 24 jam diinokulasikan ke dalam cawan yang selanjutnya dituangkan media konfrontasi yaitu Mueller Hinton agar (MHA)
sebanyak 15 – 20 ml. Setelah agar mengeras dan dingin, dibuat sumur pada cawan pada
diameter lima mm.
Sumur yang telah dibuat, kemudian ke dalam sumur dituangkan 50 µl plantarisin
murni kemudian cawan disimpan dalam refrigerator selama 2 jam untuk memberikan
kesempatan plantarisin berdifusi kedalam agar. Setelah itu cawan diinkubasi pada suhu
15
plantarisin mampu menghambat bakteri indikator. Selanjutnya dilakukan pengukuran
diameter zona bening (mm).
Rancangan dan Analisis Data
Rancangan dan analisis data meliputi perlakuan dan model statistik rancangan
penelitian. Rancangan dan analisis data yang digunakan pada penelitian ini meliputi
produksi plantarisin, uji antagonistik plantarisin murni 1A5, 1B1, 2B2, dan 2C12
terhadap bakteri indikator selama penyimpanan suhu dingin.
Produksi Plantarisin
Nilai pH supernatan bebas sel netral dan konsentrasi protein plantarisin, analisis
data dilakukan secara deskriptif. Rancangan percobaan yang digunakan untuk peubah
hasil uji antagonistik supernatan bebas sel netral L. plantarum. adalah rancangan acak lengkap (RAL) faktorial dengan perlakuan 4 x 5 dan ulangan sebanyak tiga kali. Faktor
perlakuan adalah galur L. plantarum, dengan empat taraf perlakuan yaitu galur 1A5, 1B1, 2B2, dan 2C12 dan lima bakteri patogen indikator. Analisis data dilakukan secara
statistik. Model statistik rancangan acak lengkap (RAL) faktorial adalah sebagai berikut.
Yijk = µ + Pi + Yj + PYij+ €ijk Keterangan :
Yijk = Variabel respon akibat bakteri patogen indikator ke-i dan supernatan bebas sel ke- j pada ulangan ke-k.
µ = Nilai tengah umum.
Pi = Pengaruh perlakuan bakteri patogen indikator ke-i, i = 1, 2, 3, 4, 5 Yj = Pengaruh perlakuan jenis supernatan bebas sel ke-j, j = 1, 2, 3, 4
PYij= Pengaruh interaksi antara bakteri patogen indikator ke-i dengan jenis supernatan bebas sel ke- j
€ij = Pengaruh galat perlakuan ke-i dan ke-j, terhadap ulangan ke-k, k = 1, 2, 3
Peubah yang diamati adalah diameter zona hambat hasil uji antagonistik dari
supernatan bebas sel asal berbagai strain L. plantarum dengan bakteri patogen indikator
Salmonella enteritidis ser. Typhimurium ATCC 14028, E. coli ATCC 25922, S. aureus
16
memenuhi uji asumsi dianalisis dengan menggunakan analisa ragam yaitu uji
parametrik dan bila hasil yang diperoleh nyata maka dilanjutkan uji banding dengan
menggunakan uji Tukey (Steel dan Torrie, 1995). Jika data tidak memenuhi asumsi,
maka data dianalisis menggunakan uji Kruskal – Wallis (uji non parametrik), bila hasil
yang diperoleh menunjukkan pengaruh yang nyata pada non parametrik maka
dilanjutkan dengan uji pembanding berganda (Mattjik dan Sumertajaya, 2002).
Pengolahan data dilakukan dengan menggunakan software Minitab14 dan Statistix8.
Stabilitas Aktivitas Plantarisin selama Penyimpanan Suhu Dingin (10 °C)
Rancangan percobaan yang digunakan adalah rancangan faktorial dengan
rancangan dasar rancangan acak lengkap (RAL) 4 x 4. Faktor perlakuan yang pertama
adalah lama penyimpanan yang berbeda (0, 5, 10 dan 15 hari) pada suhu dingin (10 °C)
dan faktor perlakuan kedua adalah plantarisin asal L. plantarum galur yang berbeda (1A5, 1B1, 2B2, dan 2C12). Ulangan dilakukan sebanyak tiga kali. Model statistik
rancangan faktorial dengan rancangan dasar RAL adalah sebagai berikut.
Yijk = µ + Pi + Yj + PYij+ €ijk Keterangan :
Yijk = Variabel respon akibat pengaruh lama penyimpanan ke-i dan plantarisin ke- j pada ulangan ke-k.
µ = Nilai tengah umum.
Pi = Pengaruh perlakuan lama penyimpanan ke-i, i = 1, 2, 3, 4 Yj = Pengaruh perlakuan jenis plantarisin ke-j, j = 1, 2, 3, 4
PYij = Pengaruh interaksi antara lama penyimpanan ke-i dengan jenis plantarisin ke-j.
€ij = Pengaruh galat perlakuan ke-i dan ke-j, terhadap ulangan ke-k, k = 1, 2, 3
Peubah yang diamati adalah diameter zona hambat hasil uji antagonistik dari
plantarisin murni asal berbagai galur L. plantarum hasil purifikasi parsial dengan perlakuan lama penyimpanan yang berbeda yang dilakukan terhadap bakteri indikator
Salmonella enteritidis ser. Typhimurium ATCC 14028, E. coli ATCC 25922, S. aureus
17
memenuhi uji asumsi dianalisis dengan menggunakan analisa ragam yaitu uji
parametrik dan bila hasil yang diperoleh nyata maka dilanjutkan uji banding dengan
menggunakan uji Tukey (Steel dan Torrie, 1995). Jika data tidak memenuhi asumsi,
maka data dianalisis menggunakan uji Kruskal – Wallis (uji non parametrik), bila hasil
yang diperoleh menunjukkan pengaruh yang nyata pada non parametrik maka
dilanjutkan dengan uji pembanding berganda (Mattjik dan Sumertajaya, 2002). Model
statistik uji Tukey adalah sebagai berikut:
w = qα (p,fe) x (KTG/r)1/2
Keterangan :
qα = Taraf uji yang digunakan (95% atau 99%)
p = Jumlah taraf perlakuan
fe = Derajat bebas (db) galat
KTG = Kuadrat tengah galat
18 HASIL DAN PEMBAHASAN
Hasil yang diperoleh pada penelitian ini diawali dengan pemeriksaan
karakteristik morfologi dan kemurnian isolat bakteri yang digunakan. Isolat bakteri
yang digunakan adalah BAL indigenous daging sapi yaitu bakteriosin asal L. plantarum
1A5, 1B1, 2B2 dan 2C12 serta bakteri patogen indikator yang terdiri atas bakteri
Salmonella enteritidis ser. Typhimurium ATCC 14028, E. coli ATCC 25922, S. aureus
ATCC 25923, B. cereus, dan P. aeruginosa ATCC 27853. Karakteristik morfologis yang diamati meliputi bentuk dan susunan sel-sel bakteri secara mikroskopik, dilakukan
dengan bantuan pewarnaan Gram.
Pemeriksaan Kemurnian Isolat Bakteri Asam Laktat dan Bakteri Patogen Indikator
Pemeriksaan kemurnian Bakteri Asam Laktat (BAL) merupakan cara untuk
memastikan bahwa bakteri yang akan diuji merupakan kultur murni BAL hasil isolasi
dengan mengetahui karakteristik masing-masing kultur berdasarkan sifat yang tampak
pada setiap bakteri. Karakteristik tersebut berdasarkan profil fenotip seperti berdasarkan
dinding sel bakteri melalui pewarnaan Gram serta bentuk dari masing-masing isolat
BAL yang sudah diisolasi sebelumnya dari daging sapi yang beredar di Bogor
(Hidayati, 2006).
Morfologi Sel
Konfirmasi bakteri uji yang selanjutnya diuji adalah morfologi sel. Sebanyak
empat BAL dan lima bakteri patogen indikator dikarakterisasi berdasarkan morfologi
selnya untuk mengetahui bentuk bakteri dari masing-masing isolat menggunakan
mikroskop. Fardiaz (1992) menyatakan bahwa berdasarkan bentuk morfologinya bakteri
dibagi menjadi tiga golongan yaitu golongan batang (basil), bulat (kokus), dan golongan
spiral.
Hasil pengamatan morfologi sel empat isolat BAL yaitu 1A5, 1B1, 2B2 dan
2C12 adalah bakteri dengan bentuk batang (basil) dengan susunan tunggal atau pendek.
Isolat ini merupakan kelompok bakteri asam laktat genus Lactobacillus (Fardiaz, 1992). Menurut Buckle et al (2007), bakteri E. coli, Salmonella dan P. aeruginosa tergolong bakteri Gram negatif karena memiliki ciri-ciri morfologi yaitu berbentuk batang,
19
positf dengan ciri-ciri morfologi yaitu berbentuk kokus dan berkelompok menyerupai
buah anggur, tidak bergerak, dan tidak berspora (Holt et al., 1994). B. cereus juga merupakan bakteri Gram positif dengan ciri-ciri morfologi yaitu berbentuk batang dan
merupakan bakteri gram positif yang memiliki spora (Ray, 2000). Karakteristik keempat
isolat BAL dan bakteri patogen indikator dapat dilihat pada Tabel 2.
Tabel 2. Karakteristik L. plantarum 1A5, 1B1, 2B2 dan 2C12 serta Bakteri Patogen Indikator Berdasarkan Uji Morfologi dan Pewarnaan Gram
Bakteri Pewarnaan Gram Morfologi Bentuk dan Susunan
L. plantarum 1A5 Positif Batang, susunan tunggal dan berkoloni rantai pendek
L. plantarum 1B1 Positif Batang, susunan tunggal dan berkoloni rantai pendek
L. plantarum 2B2 Positif Batang, susunan tunggal dan berkoloni rantai pendek
L. plantarum 2C12 Positif Batang, susunan tunggal dan berkoloni rantai pendek
Salmonella enteritidis ser.
Typhimurium ATCC 14028 Negatif Batang tunggal dan berkoloni
E. coli ATCC 25922 Negatif Berbentuk batang, bergerak
S. aureus ATCC 25923 Positif Bulat tunggal dan berkoloni seperti buah anggur
P. aeruginosa ATCC 27853 Negatif Batang, susunan tunggal dan berkoloni rantai pendek
B. cereus Positif
Batang, susunan tunggal dan berkoloni serta terdapat kantung spora
Pewarnaan Gram merupakan metode uji untuk mengetahui makromolekul
dinding sel setiap isolat bakteri uji dan bakteri indikator. Bakteri berdasarkan reaksi
pewarnaan Gram dibedakan menjadi bakteri Gram positif dan Gram negatif. Sebanyak
empat isolat bakteri asam laktat dan lima bakteri patogen indikator dilakukan pengujian
pewarnaan Gram. Pewarnaan Gram dimaksudkan untuk mengetahui karakteristik
morfologis dan kemurnian kultur bakteri yang digunakan. Karakteristik morfologis
20
bervariasi dari panjang dan ramping sampai kokobacilus pendek (Pelczar dan Chan,
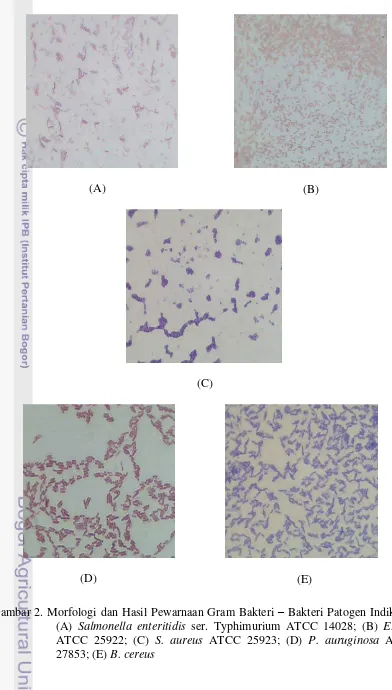
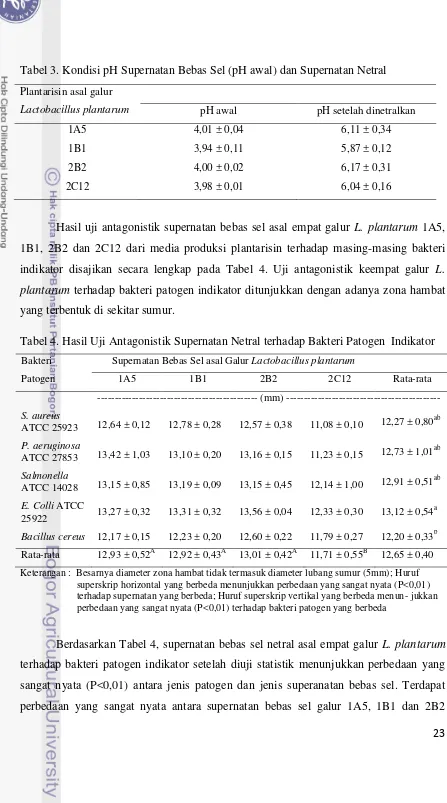
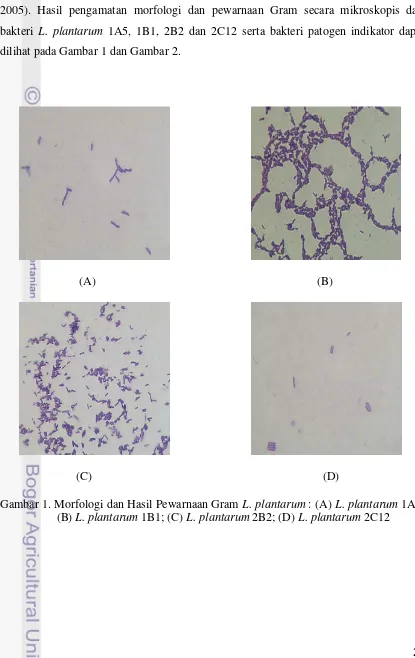
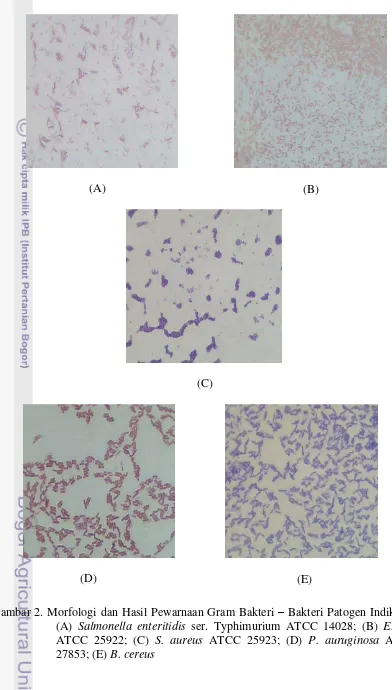
2005). Hasil pengamatan morfologi dan pewarnaan Gram secara mikroskopis dari
bakteri L. plantarum 1A5, 1B1, 2B2 dan 2C12 serta bakteri patogen indikator dapat dilihat pada Gambar 1 dan Gambar 2.
(A)
(B)
(C)
(D)
21
(A)
(B)
(C)
(D)
(E)
Gambar 2. Morfologi dan Hasil Pewarnaan Gram Bakteri – Bakteri Patogen Indikator: (A) Salmonella enteritidis ser. Typhimurium ATCC 14028; (B) E. coli
22
Hasil yang diperoleh berdasarkan pewarnaan Gram, ternyata bakteri L. plantarum 1A5, 1B1, 2B2 dan 2C12 serta bakteri patogen indikator S. aureus ATCC 25923 dan B. cereus yang digunakan merupakan bakteri Gram positif. Hal ini disebabkan keenam bakteri ini tetap mempertahankan warna ungu Kristal violet
meskipun telah diberi alkohol 95% dan zat warna lain yaitu safranin. Bakteri
Salmonella enteritidis ser. Typhimurium ATCC 14028, E. coli ATCC 25922 dan P. aeruginosa ATCC 27853 merupakan Gram negatif. Hal ini disebabkan ketiga bakteri tersebut tidak dapat mempertahankan warna ungu Kristal violet setelah diberi alkohol
95% dan bakteri ini menyerap warna merah yang berasal dari zat warna safranin.
Produksi Plantarisin
Produksi plantarisin dilakukan dengan menggunakan inducer berupa kombinasi NaCl 1% dan yeast extract 3% dengan media pertumbuhan kultur menggunakan MRS broth. Tabel 3 menunjukkan kondisi pH awal dari supernatan bebas sel dan kondisi pH
supernatan bebas sel yang telah dinetralkan menggunakan NaOH 1N. Berdasarkan nilai
pH pada Tabel 3 supernatan antimikrob yang telah dihasilkan dari media produksi
dengan inducer berada pada kondisi asam. Kondisi asam tersebut disebabkan oleh adanya asam-asam organik yang terbentuk sebagai metabolit primer dari bakteri asam
laktat. Asam organik tersebut mempunyai spektrum penghambatan yang luas terhadap
mikroorganisme yaitu dengan cara menyerang dinding sel, membran sel, metabolisme
enzim, sistem sintesis protein maupun secara genetik (Smid dan Gorris, 2007).
Asam-asam organik yang terdapat di dalam supernatan antimikrob L. plantarum
dapat menutupi aktivitas plantarisin yang terbentuk saat akan menghambat bakteri
indikator pada uji antagonistik. Asam-asam organik dihilangkan dengan cara dilakukan
penambahan buffer (NaOH 1N) agar supernatan antimikrob tersebut mencapai pH 5,8 – 6,2. Hal ini bertujuan untuk mengurangi pengaruh asam organik yang terdapat pada
supernatan antimikrob sehingga diharapkan dapat mengoptimalkan kerja plantarisin
23
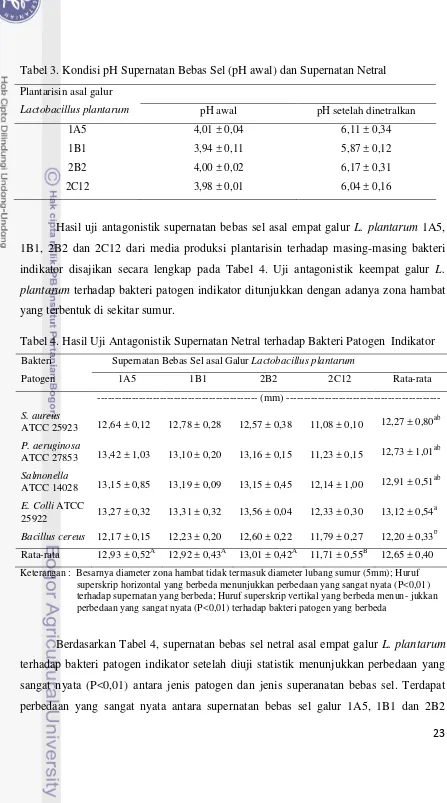
Tabel 3. Kondisi pH Supernatan Bebas Sel (pH awal) dan Supernatan Netral
Plantarisin asal galur
Lactobacillus plantarum pH awal pH setelah dinetralkan
1A5 4,01 ± 0,04 6,11 ± 0,34
1B1 3,94 ± 0,11 5,87 ± 0,12
2B2 4,00 ± 0,02 6,17 ± 0,31
2C12 3,98 ± 0,01 6,04 ± 0,16
Hasil uji antagonistik supernatan bebas sel asal empat galur L. plantarum 1A5, 1B1, 2B2 dan 2C12 dari media produksi plantarisin terhadap masing-masing bakteri
indikator disajikan secara lengkap pada Tabel 4. Uji antagonistik keempat galur L. plantarum terhadap bakteri patogen indikator ditunjukkan dengan adanya zona hambat yang terbentuk di sekitar sumur.
Tabel 4. Hasil Uji Antagonistik Supernatan Netral terhadap Bakteri Patogen Indikator
Bakteri
Patogen
Supernatan Bebas Sel asal Galur Lactobacillus plantarum
1A5 1B1 2B2 2C12 Rata-rata
Keterangan : Besarnya diameter zona hambat tidak termasuk diameter lubang sumur (5mm); Huruf superskrip horizontal yang berbeda menunjukkan perbedaan yang sangat nyata (P<0,01) terhadap supernatan yang berbeda; Huruf superskrip vertikal yang berbeda menun- jukkan perbedaan yang sangat nyata (P<0,01) terhadap bakteri patogen yang berbeda
Berdasarkan Tabel 4, supernatan bebas sel netral asal empat galur L. plantarum
terhadap bakteri patogen indikator setelah diuji statistik menunjukkan perbedaan yang
sangat nyata (P<0,01) antara jenis patogen dan jenis superanatan bebas sel. Terdapat
24
dengan supernatan bebas sel galur 2C12. Supernatan bebas sel galur 2C12
menghasilkan rataan zona hambat yang paling rendah dibandingkan dengan supernatan
asal galur lain. Hal ini dapat dikatakan bahwa 2C12 kurang efektif digunakan untuk uji
antagonistik terhadap kelima bakteri patogen indikator. Diameter zona hambat
supernatan bebas sel juga dipengaruhi oleh jenis bakteri patogen indikator, terdapat
perbedaan yang sangat nyata diameter zona hambat yang dihasilkan keempat supernatan
antara bakteri E. coli ATCC 25922 dengan bakteri B.cereus.
Pengamatan secara deskriptif menunjukkan bahwa supernatan asal empat galur
L. plantarum dapat menghambat pertumbuhan bakteri indikator Gram negatif (E. coli
ATCC 25922, Salmonella enteriditis ser. Typhimurium ATCC 14028, P. aeruginosa
ATCC 27853). Hasil ini dikuatkan oleh pernyataan Smaoui et al. (2010) bahwa bakteriosin yang dihasilkan oleh Lactobacillus plantarum sp. TN635 dapat menghambat pertumbuhan bakteri Gram negatif (Salmonella enterica ATCC43972, Pseudomonas aeruginosa ATCC 49189, Hafnia sp. and Serratia sp.) dan Candida tropicalis R2 CIP203 yang termasuk jamur (fungi) patogen.
Pengujian Konsentrasi Protein Plantarisin
Plantarisin murni diperoleh dari beberapa tahapan, diantara tahapan yang
digunakan yaitu tahap purifikasi. Tahap purifikasi terdiri atas purifikasi parsial yang
menggunakan ammonium sulfat dan dialisis, serta purifikasi menggunakan
kromatografi pertukaran kation. Hasil dari tahapan purifikasi menggunakan ammonium
sulfat disebut presipitat plantarisin dan hasil dari tahap dialisis disebut plantarisin kasar,
sedangkan hasil dari purifikasi menggunakan kromatografi pertukaran kation disebut
plantarisin murni.
Pengujian ini dilakukan bertujuan untuk mengetahui konsentrasi protein dari
presipitat plantarisin, plantarisin kasar dan plantarisin murni, sehingga dapat dilihat
perbedaan konsentrasi protein dari ketiga bentuk plantarisin tersebut. Pengujian protein
ini menggunakan spektrofotometer dengan panjang gelombang (λ) 280. Konsentrasi
25
Tabel 5. Konsentrasi Protein Plantarisin Asal L. plantarum pada Presipitat Plantarisin, Plantarisin Kasar dan Plantarisin Murni.
Berdasarkan Tabel 5, hasil kuantitatif presipitat plantarisin, plantarisin kasar dan
plantarisin murni, secara deskriptif dapat dikatakan bahwa nilai rataan konsentrasi
protein plantarisin kasar lebih tinggi dibandingkan presipitat plantarisin terhadap ketiga
plantarisin asal galur L. plantarum 1A5, 1B1, dan 2B2. Presipitat plantarisin merupakan hasil dari purifikasi parsial dengan konsentrasi yang tinggi namun masih mengandung
garam mineral yang digunakan untuk mengendapkan protein. Proses dialisis atau proses
pencucian yang bertujuan untuk menghilangkan pengotor pada permukaan
partikel-partikel protein sehingga dapat menghasilkan plantarisin kasar dengan konsentrasi
protein yang lebih tinggi dari presipitat plantarisin (Day dan Underwood, 2002). Nilai
konsentrasi protein plantarisin kasar galur L. plantarum 2C12 cenderung lebih rendah dari ketiga galur lainnya. Konsentrasi protein plantarisin kasar 2C12 mengalami
penurunan setelah tahap dialisis. Hal ini dapat disebabkan masih terdapat pengaruh
media MRSB di dalam presipitat plantarisin dan pada saat didialisis banyak yang
keluar. Proses purifikasi plantarisin dengan menggunakan kromatografi pertukaran
kation akan menghasilkan sejumlah fraksi plantarisin murni yang konsentrasi
proteinnya berbeda-beda. Fraksi dengan konsentrasi protein yang tidak terlalu tinggi
dipilih sebagai sampel untuk melakukan pengujian karakterisasi plantarisin terhadap
lamanya penyimpanan suhu dingin.
Konsentrasi protein plantarisin murni jika dibandingkan dengan plantarisin kasar
memiliki konsentrasi yang lebih rendah. Hal ini disebabkan konsentrasi protein yang
26
penghasil protein lain yaitu masih terdapat media MRSB yang memiliki kandungan
pepton dan yeast extract. Konsentrasi protein keempat plantarisin murni yang diperoleh cukup tinggi, sehingga keempat plantarisin tersebut dapat digunakan untuk uji
selanjutnya yaitu pengujian 1A5, 1B1, 2B2, dan 2C12 terhadap ketahanan suhu dingin
(10 °C).
Pengaruh Lama Penyimpanan Plantarisin Murni Galur 1A5, 1B1, 2B2 dan 2C12 melalui Aktivitas Penghambatan Antimikrob pada Suhu Dingin (10 °C)
Aktivitas penghambatan keempat plantarisin asal galur L. plantarum selama 15 hari pada suhu 10 °C diamati untuk mengetahui stabilitas plantarisin 1A5, 1B1, 2B2,
dan 2C12 selama penyimpanan suhu dingin. Stabilitas aktivitas penghambatan
ditentukan melalui diameter zona hambat (berupa zona bening atau zona semu) yang
dihasilkan terhadap kelima bakteri patogen indikator (S. aureus ATCC 25923,
Salmonella enteritidis ser. Thyphimurium ATCC 14028, P. aeruginosa ATCC 27853,
E. coli ATCC 25922 dan B. cereus).
S. aureus ATCC 25923. Stabilitas aktivitas penghambatan plantarisin murni asal L. plantarum 1A5, 1B1, 2B2 dan 2C12 terhadap bakteri indikator S. aureus yang disimpan selama 15 hari pada suhu dingin (10 °C) dapat dilihat pada Tabel 6.
Tabel 6. Diameter Zona Hambat Plantarisin Asal Empat Galur L. Plantarum selama Penyimpanan terhadap S. aureus ATCC 25923 pada Suhu Dingin (10 °C)
Plantarisin asal
Keterangan : Besarnya diameter zona hambat sudah termasuk diameter lubang sumur (5 mm); Huruf superskrip yang berbeda menunjukkan perbedaan yang nyata (P< 0,05)
Penyimpanan plantarisin murni asal empat galur yaitu 1A5, 1B1, 2B2, dan 2C12
yang disimpan pada suhu dingin selama 15 hari, setelah diujikan pada bakteri S. aureus
27
berdasarkan uji antagonistik yaitu terdapat diameter zona hambat di sekitar sumur.
Diameter zona hambat yang terbentuk berupa diameter zona semu. Menurut
Jimenez-Diaz (1993), Diameter zona hambat dapat berupa diameter zona bening di sekeliling
sumur yang menunjukkan sifat bakterisidal (membunuh bakteri) maupun diameter zona
semu yang merupakan sifat bakteriostatik (menghambat pertumbuhan mikroba).
Berdasarkan analisis ragam, diameter zona hambat yang diperoleh tidak terdapat
interaksi antara jenis plantarisin dengan umur simpan (P>0,05). Penghambatan bakteri
S. aureus ATCC 25923 tidak dipengaruhi oleh jenis plantarisin yang berbeda. Hal ini disebabkan bakteri S. aureus ATCC 25923 merupakan bakteri Gram negatif, menurut Jimenez-Diaz (1993), bakteriosin merupakan protein atau peptida pada bakteri yang
menunjukkan aksi bakterisidal ataupun bakteriostatik terhadap spesies yang umumnya
berkerabat dekat. Plantarisin 1A5, 1B1, 2B2 dan 2C12 berpengaruh nyata (P<0,05)
terhadap perlakuan umur simpan, sehingga dilakukan pengujian lanjut. Hasil pengujian
lanjut menunjukkan bahwa penyimpanan pada hari ke-5 berbeda nyata terhadap S. aureus ATCC 25923 jika dibandingkan dengan hari ke-10.
Perbedaan lamanya umur simpan keempat plantarisin asal galur L. plantarum
mengalami penurunan aktivitas penghambatan pada penyimpanan selama lima hari,
namun perpanjangan penyimpanan hingga 10 hari mampu mengembalikan aktivitas
penghambatan plantarisin murni dengan menghasilkan diameter zona hambat yang tidak
berbeda dengan H-0. Menurut Amanah (2011), penyimpanan 1 minggu pada suhu
refrigerator menyebabkan FBS (filtrat bebas sel) L. acidophilus Y-01 mengalami penurunan aktivitas penghambatan yang sangat nyata, namun perpanjangan
penyimpanan hingga 2 minggu mampu mengembalikan aktivitas penghambatan FBS L. acidophilus Y-01 dengan menghasilkan diameter zona hambat yang tidak berbeda dengan kontrol. Aktivitas plantarisin selama penyimpanan suhu dingin bersifat
fluktuatif. Penyimpanan plantarisin selama 10 hari efektif digunakan untuk uji
antagonistik terhadap bakteri S. aureus ATCC 25923 karena menghasilkan diameter zona hambat yang optimum.
28
bakteri indikator Salmonella yang disimpan selama 15 hari pada suhu dingin (10 °C)
dapat dilihat pada Tabel 7.
Tabel 7. Diameter Zona Hambat Plantarisin Asal Empat Galur L. Plantarum selama Penyimpanan terhadap Salmonella enteritidis ser. Typhimurium ATCC 14028 pada Suhu Dingin (10 °C)
Keterangan : Besarnya diameter zona hambat sudah termasuk diameter lubang sumur (5mm)
Penyimpanan plantarisin murni asal empat galur L. plantarum 1A5, 1B1, 2B2 dan 2C12 selama 15 hari pada suhu dingin, setelah diujikan pada bakteri Salmonella enteritidis ser. Typhimurium ATCC 14028 dapat menghambat pertumbuhan bakteri tersebut. Hasil yang diperoleh berdasarkan uji antagonistik yaitu terdapat diameter zona
hambat di sekitar sumur.
Analisis yang digunakan yaitu non parametrik karena data tersebut tidak
memenuhi uji asumsi, sehingga menggunakan Kruskal-Wallis. Hasil yang diperoleh
tidak berbeda nyata (P>0,05). Berdasarkan hasil uji antagonistik, diameter zona hambat
yang dihasilkan oleh plantarisin 1A5, 1B1, 2B2 dan 2C12 dari penyimpanan H-0
sampai H-15 terhadap bakteri Salmonella enteritidis ser. Typhimurium ATCC 14028 masih mempunyai aktivitas antimikrob sehingga dapat dikatakan bahwa keempat
plantarisin tersebut tetap stabil. Menurut Davis dan Stout (1971), rataan diameter zona
hambat yang dihasilkan oleh plantarisin 1A5, 1B1 dan 2B2 termasuk kategori sedang
dan plantarisin 2C12 termasuk kategori kuat. Kategori sedang yaitu plantarisin memiliki
aktivitas penghambatan yang sedang terhadap bakteri patogen indikator dilihat dari zona
hambat yang dihasilkan. Kategori kuat yaitu plantarisin memiliki aktivitas
penghambatan yang kuat terhadap bakteri patogen indikator dilihat dari zona hambat
yang dihasilkan. Plantarisin yang paling efektif digunakan untuk menghambat
29
plantarisin 2C12 karena 2C12 menghasilkan rataan diameter zona hambat terbesar dan
termasuk kategori kuat.
P. aeruginosa ATCC 27853. Stabilitas aktivitas penghambatan plantarisin murni asal
L. plantarum 1A5, 1B1 2B2 dan 2C12 terhadap bakteri indikator P. aeruginosa yang disimpan selama 15 hari pada suhu dingin (10 °C) dapat dilihat pada Tabel 8.
Tabel 8. Diameter Zona Hambat Plantarisin Asal Empat Galur L. plantarum selama
Keterangan : Besarnya diameter zona hambat tidak termasuk diameter lubang sumur (5mm); Huruf superskrip kapital yang sama menunjukkan tidak berbeda nyata (P>0,05) antara jenis plantarisin; Huruf superskrip (kecil) yang berbeda menunjukkan perbedaan yang nyata (P<0,05) antara umur simpan
Penyimpanan plantarisin murni asal empat galur yaitu 1A5, 1B1, 2B2, dan 2C12
yang disimpan pada suhu dingin selama 15 hari, setelah diujikan pada bakteri P. aeruginosa ATCC 27853 dapat menghambat pertumbuhan bakteri tersebut. Hasil yang diperoleh yaitu terdapat diameter zona hambat disekitar sumur.
Berdasarkan analisis ragam, hasil yang diperoleh berbeda nyata (P<0,05)
sehingga dilakukan pengujian lanjut. Terdapat interaksi antara kedua perlakuan yaitu
jenis plantarisin yang berbeda dengan lamanya umur simpan terhadap bakteri indikator
P. aeruginosa ATCC 27853. Pengujian berdasarkan pengaruh sederhana dari perlakuan jenis plantarisin dengan menggunakan uji Tukey, plantarisin 1A5, 1B1 dan 2B2 setelah mengalami penyimpanan (H-0, H-5, H-10 dan H-15) memberikan pengaruh yang sama
(tidak berbeda nyata) terhadap diameter zona hambat yang dihasilkan. Implikasi dari
pengujian pengaruh sederhana ini adalah penyimpanan ketiga plantarisin tersebut dapat
menggunakan salah satu umur simpan (H-0, H-5, H-10 atau H-15) untuk menghambat
30
1B1, dan 2B2 tetap stabil selama penyimpnan 15 hari pada suhu dingin (10 ºC).
Terdapat pengaruh yang berbeda nyata (P<0,05) terhadap plantarisin 2C12 selama
penyimpanan 15 hari. Plantarisin 2C12 efektif digunakan sebagai antimikrob bakteri P. aeruginosa ATCC 27853 setelah mengalami penyimpanan selama 10 hari karena aktivitas 2C12 meningkat dan menghasilkan diameter zona hambat yang paling besar.
Pengujian berdasarkan pengaruh sederhana dari perlakuan umur simpan yang
berbeda menggunakan uji Tukey, penyimpanan (H-0, H-5, H-10 dan H-15) memberikan
pengaruh yang sama (tidak berbeda nyata) pada keempat plantarisin terhadap diameter
zona hambat yang dihasilkan. Implikasi dari pengujian pengaruh sederhana ini adalah
keempat umur simpan tersebut dapat digunakan untuk salah satu jenis plantarisin (1A5,
1B1, 2B2, atau 2C12) sebagai penghambat pertumbuhan bakteri P. aeruginosa ATCC 27853.
E. coli ATCC 25922. Stabilitas aktivitas penghambatan plantarisin murni asal L. plantarum 1A5, 1B1, 2B2 dan 2C12 terhadap bakteri E. coli yang disimpan selama 15 hari pada suhu dingin (10 °C) dapat dilihat pada Tabel 9.
Tabel 9. Diameter Zona Hambat Plantarisin Asal Empat Galur L. plantarum selama Penyimpanan terhadap E. coli ATCC 25922 pada Suhu Dingin (10 °C) Plantarisin
Keterangan : Besarnya diameter zona hambat tidak termasuk diameter lubang sumur (5mm); Huruf superskrip horizontal yang berbeda menunjukkan perbedaan yang nyata (P<0,05) terhadap umur simpan; Huruf superskrip vertikal yang berbeda menunjukkan perbedaan yang nyata (P<0,05) terhadap plantarisin yang berbeda
Penyimpanan plantarisin murni asal empat galur L. plantarum yaitu 1A5, 1B1, 2B2 dan 2C12 yang disimpan selama 15 hari pada suhu dingin, setelah diujikan pada
31
Berdasarkan analisis ragam, hasil yang diperoleh berbeda nyata (P<0,05)
sehingga dilakukan pengujian lanjut. Interaksi diantara kedua faktor perlakuan (umur
simpan dan jenis plantarisin) tidak berpengaruh nyata, namun berpengaruh nyata
terhadap umur simpan dan jenis plantarisin yang berbeda. Hasil yang diperoleh
berdasarkan pengujian lanjut, keempat plantarisin asal galur L. plantarum yaitu terdapat perbedaan yang nyata antara plantarisin 2B2 dengan 2C12. Plantarisin 2C12 memiliki
rataan diameter zona hambat paling besar, sehingga plantarisin 2C12 lebih efektif jika
digunakan sebagai antimikrob terhadap bakteri E. coli ATCC 25922 dibandingkan ketiga plantarisin lainnya.
Berdasarkan faktor perlakuan umur simpan, terdapat perbedaan yang nyata
(P<0,05) antara H-5 dan H-10. Aktivitas keempat plantarisin setelah mengalami
penyimpanan suhu dingin selama 10 hari menghasilkan diameter zona hambat yang
paling besar, sehingga plantarisin yang telah disimpan selama 10 hari efektif digunakan
sebagai antimikrob terhadap bakteri E. coli ATCC 25922.
B. cereus. Stabilitas aktivitas penghambatan plantarisin murni asal L. plantarum 1A5, 1B1, 2B2 dan 2C12 terhadap bakteri indikator B. cereus yang disimpan selama 15 hari pada suhu dingin (10 °C) dapat dilihat pada Tabel 10.
Tabel 10. Diameter Zona Hambat Plantarisin Asal Empat Galur L. Plantarum selama Penyimpanan terhadap B. cereus pada Suhu Dingin (10 °C)
Plantarisin
Keterangan : Besarnya diameter zona hambat sudah termasuk diameter lubang sumur (5mm); Huruf superskrip kapital yang sama menunjukkan tidak berbeda nyata (P>0,05) antara jenis plantarisin; Huruf superskrip (kecil) yang berbeda menunjukkan perbedaan yang nyata (P<0,05) antara umur simpan
Penyimpanan plantarisin murni asal empat galur yaitu 1A5, 1B1, 2B2, dan 2C12
32
dapat menghambat pertumbuhan bakteri tersebut. Hasil yang diperoleh berdasarkan uji
antagonistik yaitu terdapat diameter zona hambat disekitar sumur.
Berdasarkan analisis ragam, hasil yang diperoleh berbeda nyata (P<0,05)
sehingga dilakukan pengujian lanjut. Terdapat interaksi antara kedua perlakuan yaitu
jenis plantarisin yang berbeda dengan lamanya umur simpan terhadap bakteri indikator
B. cereus. Pengujian berdasarkan pengaruh sederhana dari perlakuan jenis plantarisin dengan menggunakan uji Tukey, plantarisin 1A5, 1B1 dan 2B2 setelah mengalami penyimpanan (H-0, H-5, H-10 dan H-15) memberikan pengaruh yang sama (tidak
berbeda nyata) terhadap diameter zona hambat yang dihasilkan. Implikasi dari
pengujian pengaruh sederhana ini adalah penyimpanan ketiga plantarisin tersebut dapat
menggunakan salah satu umur simpan (H-0, H-5, H-10 atau H-15) untuk menghambat
pertumbuhan bakteri B. cereus. Hal ini disebabkan plantarisin 1A5, 1B1, dan 2B2 tetap stabil selama penyimpnan 15 hari pada suhu dingin (10 ºC). Terdapat pengaruh yang
berbeda nyata (P<0,05) terhadap plantarisin 2C12 selama penyimpanan 15 hari yaitu
pada H-15. Plantarisin 2C12 efektif digunakan sebagai antimikrob bakteri B. cereus
setelah mengalami penyimpanan selama 10 hari karena aktivitas 2C12 meningkat dan
menghasilkan diameter zona hambat yang paling besar.
Pengujian berdasarkan pengaruh sederhana dari perlakuan umur simpan yang
berbeda menggunakan uji Tukey, penyimpanan (H-0, H-5, H-10 dan H-15) memberikan
pengaruh yang sama (tidak berbeda nyata) pada keempat plantarisin terhadap diameter
zona hambat yang dihasilkan. Implikasi dari pengujian pengaruh sederhana ini adalah
keempat umur simpan tersebut dapat digunakan untuk salah satu jenis plantarisin (1A5,
33 KESIMPULAN DAN SARAN
Kesimpulan
Plantarisin dari empat galur L. plantarum 1A5, 1B1, 2B2 dan 2C12 setelah mengalami penyimpanan selama 15 hari pada suhu dingin (10 ºC) masih mempunyai
aktivitas antimikrob terhadap bakteri patogen indikator yaitu Salmonella enteritidis ser. Typhimurium ATCC 14028, E. coli ATCC 25922, S. aureus ATCC 25923, B. cereus
dan P. aeruginosa ATCC 27853. Plantarisin 2C12 memiliki tingkat sensitivitas paling tinggi dibandingkan 1A5, 1B1 dan 2C12 selama penyimpanan 15 hari pada suhu dingin.
Saran
Perlu dilakukan penelitian lebih lanjut untuk mengetahui sampai berapa hari
penyimpanan dingin (umur simpan) plantarisin murni 1A5, 1B1, 2B2 dan 2C12 masih
AKTIVITAS ANTIMIKROB BAKTERIOSIN ASAL
Lactobacillus
plantarum
TERHADAP BERBAGAI BAKTERI PATOGEN
SELAMA PENYIMPANAN SUHU DINGIN
SKRIPSI
KHAIRUL BARIYAH
DEPARTEMEN ILMU PRODUKSI DAN TEKNOLOGI PETERNAKAN FAKULTAS PETERNAKAN
AKTIVITAS ANTIMIKROB BAKTERIOSIN ASAL
Lactobacillus
plantarum
TERHADAP BERBAGAI BAKTERI PATOGEN
SELAMA PENYIMPANAN SUHU DINGIN
SKRIPSI
KHAIRUL BARIYAH
DEPARTEMEN ILMU PRODUKSI DAN TEKNOLOGI PETERNAKAN FAKULTAS PETERNAKAN
RINGKASAN
Khairul Bariyah D14070044. 2007. Aktivitas Antimikrob Bakteriosin asal Lactobacillus plantarum terhadap Berbagai Bakteri Patogen selama Penyimpanan Suhu Dingin. Skripsi. Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan, Institut Pertanian Bogor.
Pembimbing Utama : Dr. Irma Isnafia Arief S.Pt., M.Si. Pembimbing Anggota : Zakiah Wulandari S.TP., M.Si.
Masalah keamanan pangan masih merupakan kendala utama dalam produk makanan. Mutu dan keamanan pangan perlu diperhatikan karena dapat membahayakan kesehatan bagi konsumen. Alternatif dalam mengatasi masalah tersebut adalah dengan pengolahan dan pengawetan. Metode pengawetan yang telah banyak diaplikasikan adalah penambahan bahan pengawet pada makanan, baik bahan pengawet alami maupun yang sintetis. Pemilihan bahan pengawet yang sangat dianjurkan adalah bahan pengawet alami. Beberapa isolat asal daging seperti
Lactobacillus plantarum 1A5, 1B1, 2B2 dan 2C12 telah mampu menunjukkan aktivitas antimikrob melalui uji antagonistik terhadap bakteri patogen.
Penelitian ini bertujuan mempelajari aktivitas antimikrob plantarisin asal L. plantarum 1A5, 1B1, 2B2, dan 2C12 melalui sensitivitas plantarisin selama penyimpanan suhu dingin (10 °C) terhadap bakteri patogen yaitu Salmonella enteritidis ser. Typhimurium ATCC 14028, Eschericia coli ATCC 25922, Staphylococcus aureus ATCC 25923, Pseudomonas aeruginosa ATCC 27853 dan
Bacillus cereus. Penyimpanan di suhu dingin yang dilakukan selama 15 hari, melalui uji antagonistik dengan metode difusi sumur terhadap kelima bakteri indikator.
Proses karakterisasi diawali dengan pemeriksaan kemurnian isolat bakteri asam laktat dan bakteri patogen indikator melalui metode pewarnaan Gram. Proses selanjutnya yaitu memproduksi plantarisin1A5, 1B1, 2B2 dan 2C12 melalui tahapan purifikasi meliputi purifikasi parsial dengan menggunakan amonium sulfat, dialisis, dan purifikasi dengan menggunakan kromatografi pertukaran kation. Keempat galur
L. plantarum ditumbuhkan pada media de Man Rogosa and Sharpe broth (MRSB) yang disuplementasi dengan yeast extract (YE) 3%, lalu diinkubasi selama 20 jam, kemudian disentrifugasi pada kecepatan 10.000 rpm untuk mendapatkan supernatan antimikrob. Supernatan antimikrob disaring menggunakan membran saring Sartorius untuk mendapatkan supernatan bebas sel, yang kemudian pH supernatant dinetralkan menjadi 5,8 – 6,2. Proses purifikasi parsial siap dilakukan dengan menjenuhkan larutan dengan menggunakan amonium sulfat 80%. Presipitat plantarisin didapat dan didialisis dengan menggunakan membran dialisis. Proses dialisis akan menghasilkan plantarisin kasar, kemudian plantarisin kasar dimurnikan dengan teknik kromatografi pertukaran kation untuk memperoleh plantarisinmurni.
Hasil penelitian menunjukkan bahwa plantarisin asal galur L. plantarum 1A5, 1B1, 2B2, dan 2C12 setelah mengalami penyimpanan suhu dingin selama 15 hari masih mempunyai aktivitas antimikrob terhadap bakteri patogen indikator. Hal ini menunjukkan bahwa keempat plantarisin asal galur L. plantarum masih aktif setelah mengalami penyimpanan suhu dingin (10 °C).
ABSTRACT
Antimicrobial Activity of Bacteriocins Produced by Lactobacillus plantarum against Patogenic Bacterias during Store at Cold Temperature
Bariyah, K., I.I. Arief and Z. Wulandari
Bacteriocins are antimicrobial substances produced by lactic acid bacteria (LAB) which can be used as a natural preservative. The preservative method which commonly used in storage under temperature of 4-10 °C. This method does not guarantee that it can inhibit the bacterial growth, such as psikrofil bacteria which still active on the refri temperature. The aim of this research was to study the stability of antimicrobia bacteriocins produced by L. plantarum 1A5, 1B1, 2B2, and 2C12 through its sensitivity during store at cold temperature (10 °C) againts the pathogenic bacteria that consists of Salmonella enteritidis ser. Typhimurium ATCC 14028, E. coli ATCC 25922, S. aureus ATCC 25923, P. aeruginosa ATCC 27853, and B. cereus. Plantaricin that was used is the result of cation exchange chromatography purification. Storage duration for 15 days and testing was done in intervals of 5 days. The antagonistic assay showed the antimicrobial activity against the pathogenic bacteria. The results showed that plantaricin 1A5, 1B1, 2B2, and 2C12 during cold storage temperature is still effective to be used for antagonistic assay to the pathogen indicator bacteria. Plantaricin of the four strains is able to inhibit bacterial growth indicators. Plantaricins has been stored for 15 days still have antimicrobial activity. This showed that the four plantaricins remained active after storage for 15 days at cool temperatures (10 °C).
AKTIVITAS ANTIMIKROB BAKTERIOSIN ASAL
Lactobacillus
plantarum
TERHADAP BERBAGAI BAKTERI PATOGEN
SELAMA PENYIMPANAN SUHU DINGIN
KHAIRUL BARIYAH D14070044
Skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Peternakan pada
Fakultas Peternakan Institut Pertanian Bogor
DEPARTEMEN ILMU PRODUKSI DAN TEKNOLOGI PETERNAKAN FAKULTAS PETERNAKAN