ii
SEBAGAI ANTIOKSIDAN
ZULIA HAJLI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
i
mahagoni
Jacq.) yang Berpotensi sebagai Antioksidan. Dibimbing oleh DUDI
TOHIR dan GUSTINI SYAHBIRIN.
Biji mahoni daun kecil (
Swietenia mahagoni
Jacq.) mengandung senyawa
flavonoid yang memiliki potensi sebagai antioksidan. Penelitian ini bertujuan
mengisolasi senyawa flavonoid biji mahoni yang memberikan aktivitas
antioksidan yang tinggi. Aktivitas antioksidan ditentukan dengan menggunakan
metode 1,1-difenil-2-pikrilhidrazil. Ekstrak etil asetat biji mahoni difraksionasi
dengan menggunakan kromatografi lapis tipis preparatif dengan eluen etil
asetat-metanol (1:1) dan menghasilkan 4 fraksi. Ekstrak etil asetat memiliki aktivitas
antioksidan dengan nilai konsentrasi hambat 50% (IC
50) sebesar 117.73 mg L
-1.Fraksi teraktif dari biji mahoni ialah fraksi 3 dengan IC
50sebesar 65.18 mg L
-1,
tetapi aktivitasnya masih lebih kecil dari butil hidroksitoluena (BHT) sebesar 4.70
mg L
-1. Uji kemurnian fraksi 3 menggunakan kromatografi cair kinerja tinggi
(KCKT) menghasilkan satu puncak dengan waktu retensi 14.079 menit dan uji
golongan flavonoid menunjukkan senyawa flavonol atau flavon. Spektrum
inframerah fraksi 3 menunjukkan gugus fungsi OH, C=O, C-O, dan CH alifatik.
ABSTRACT
ZULIA HALI. Isolation of Flavonoid Compounds from Mahogany’s Seed
(
Swietenia mahagoni
Jacq.) Potential as An Antioxidant. Supervised by DUDI
TOHIR and GUSTINI SYAHBIRIN.
Small-leaves mahogany’s seed (
Swietenia mahagoni
Jacq.) contains
flavonoid compounds which are potential as an antioxidant. The purpose of this
research is to isolate flavonoid compounds from mahogany’s seed which give
high antioxidant activity. Antioxidant activity was determined by using
1,1-diphenyl-2-picrylhydrazyl method. Ethyl acetate extract of mahogany’s seed was
fractionated using preparative thin layer chromatography with ethyl
acetate-methanol (1:1) as eluent, resulting 4 fractions. Ethyl acetate extract had
antioxidant activity with the 50% inhibition concentration (IC
50) value of about
117.73 mg L
-1. The most active fraction of mahogany’s seed was the third fraction
with the IC
50value of 65.18 mg L
-1, but the activity was still lower than butyl
hydroxytoluene 4.70 mg L
-1. Purity assay of this fraction by high performance
liquid chromatography (HPLC) resulted one peak with retention time of 14.079
minutes and flavonoid group assay showed flavonol or flavone compound. The
infrared spectrum of the third fraction showed that it had OH, C=O, C-O, and
aliphatic CH functional groups.
ii
SEBAGAI ANTIOKSIDAN
ZULIA HAJLI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
iii
NIM : G44086025
Disetujui
Pembimbing I,
Pembimbing II,
Drs Dudi Tohir, MS
Dr Gustini Syahbirin, MS
NIP 19571104 198903 1 001
NIP 19600819 198903 2 001
Diketahui
Ketua Departemen,
Prof Dr Ir Tun Tedja Irawadi, M
S
NIP 19501227 197603 2 002
iv
sehingga penulis dapat menyelesaikan karya ilmiah yang berjudul “Isolasi
Senyawa Golongan Flavonoid Biji Mahoni (
Swietenia mahagoni
Jacq.) yang
Berpotensi sebagai Antioksidan” yang dilaksanakan sejak bulan Oktober 2010 di
Laboratorium Kimia Organik Departemen Kimia FMIPA IPB.
Penulis mengucapkan terima kasih kepada Drs. Dudi Tohir, MS dan Dr.
Gustini Syahbirin, MS selaku pembimbing yang telah memberikan pengarahan
dan bimbingannya kepada penulis. Penulis juga mengucapkan terima kasih
kepada orang tua, Bapak Abdul Jalil dan Ibu Halimah Damanik atas didikan, doa,
dan kasih sayangnya yang tiada terkira, serta untuk seluruh keluarga besar di
rumah, terima kasih atas dukungan dan dorongannya.
Penulis juga mengucapkan terima kasih kepada Bapak Sabur, Mba Nia, Ibu
Yenni Karmila, dan Ibu Siti Robiah, atas bantuan yang diberikan. Tak lupa,
ungkapan terima kasih penulis kepada teman-teman kosan (Nanda, Asih, Ayu, dan
Femy), seluruh rekan peneliti di Laboratorium Kimia Organik (Ina, Saki, Dinda,
Ela, Wulan, Yogi, Arif, Farid, dan Risal), serta teman-teman Ekstensi Kimia
angkatan 2008 atas bantuan, motivasi, diskusi, dan kebersamaan selama penulis
menempuh studi dan menjalankan penelitian.
Semoga karya ilmiah ini dapat bermanfaat.
Bogor, Oktober 2011
vi
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
BAHAN DAN METODE
Bahan dan Alat ... 2
Kadar Air ... 2
Isolasi Flavonoid ... 2
Uji Aktivitas Antioksidan ... 3
Uji Fitokimia ... 3
Uji Golongan Flavonoid ... 3
Uji Kemurnian dengan KCKT ... 3
Identifikasi Fraksi Aktif ... 4
HASIL DAN PEMBAHASAN
Kadar Air ... 4
Isolasi Senyawa Golongan Flavonoid ... 4
Aktivitas Antioksidan ... 5
Fitokimia dan Golongan Flavonoid ... 5
Analisis Spektrum Inframerah ... 6
SIMPULAN DAN SARAN
Simpulan ... 7
Saran ... 7
DAFTAR PUSTAKA ... 7
vii
1 Aktivitas antioksidan ... 5
2 Fitokimia ekstrak etil asetat ... 5
3 Golongan flavonoid ekstrak etil asetat dan fraksi 3 ... 5
DAFTAR GAMBAR
Halaman
1 Struktur senyawa limonoid, yaitu swietenolida (a) dan 2-hidroksi-3-
O
-tigloilswietenolida (b). ... 1
2 Biji mahoni daun kecil. ... 1
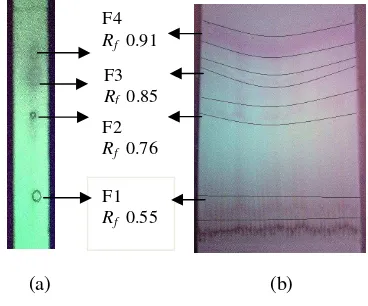
3 Noda pemisahan di bawah lampu UV 254 nm: KLT (a), KLT preparatif (b)
dengan eluen etil asetat-metanol (1:1) ... 4
4 KLT 2 dimensi fraksi 3 dengan eluen 1 etanol-etil asetat-heksana (3:2:0.5) dan
eluen 2 metanol-etil asetat (1:1) ... 6
5 Kromatogram fraksi 3 ... 6
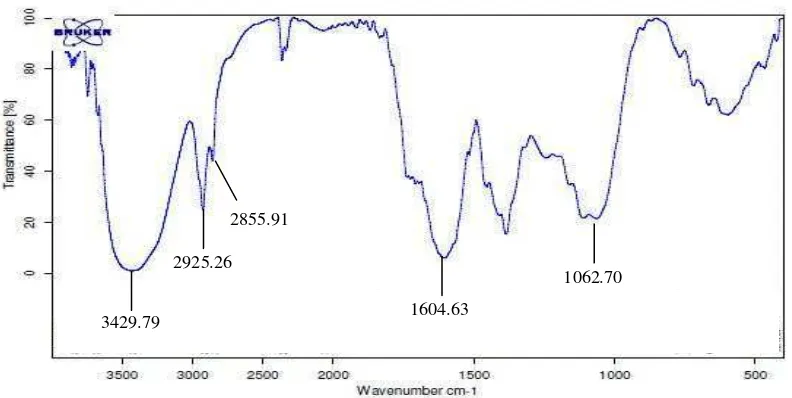
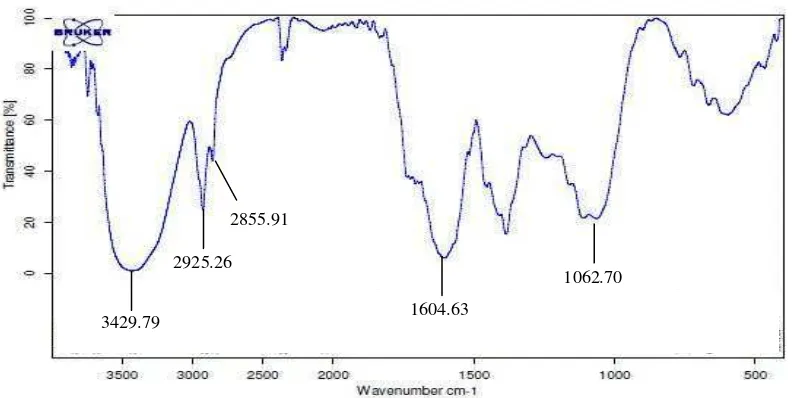
6 Spektrum inframerah fraksi 3 ... 6
DAFTAR LAMPIRAN
Halaman
1 Diagram alir penelitian ... 10
2 Kadar air serbuk biji mahoni ... 11
3 Rendemen hasil ekstraksi ... 11
4 Kromatogram pencarian eluen terbaik ... 12
PENDAHULUAN
Tumbuhan obat asli Indonesia sampai saat ini masih banyak digunakan oleh masyarakat dalam pengobatan berbagai jenis penyakit. Pengetahuan tentang tanaman berkhasiat obat berdasarkan pada pengalaman dan keterampilan yang diwariskan turun-temurun. Salah satu tanaman yang biasa digunakan sebagai obat tradisional adalah biji mahoni daun kecil (Swietenia mahagoni Jacq.). Mahoni daun kecil merupakan famili Meliaceae, lazim ditanam di tepi jalan sebagai pohon pelindung. Secara tradisional, bijinya berkhasiat sebagai obat tekanan darah tinggi, kencing manis, perangsang nafsu makan, obat rematik, demam, masuk angin, encok, dan eksim (Dalimartha 2007).
Beberapa penelitian telah dilakukan untuk penelusuran kandungan aktif dan bioaktivitas yang dimiliki biji mahoni. Biji mahoni mengandung senyawa bioaktif yang bersifat toksik terhadap larva udang Artemia salina Leach dan berpotensi sebagai obat (Sianturi 2001). Fraksi aktif biji mahoni dapat menghambat pertumbuhan Saccharomyces cerevisiae (Putri 2004). Ekstrak metanol, heksana, dan etil asetat biji mahoni terbukti mampu menghambat pertumbuhan bakteri
Escherichia coli dan Bacillus subtilis
(Haryanti 2002). Menurut Setiani (2009), biji mahoni juga dapat menghambat pertumbuhan sel kanker payudara T47D dengan nilai konsentrasi hambat 50% (IC50) sebesar 49.12 ppm dan mengandung senyawa alkaloid serta steroid/triterpenoid.
Ekstrak metanol batang kayu famili Meliaceae mengandung terpenoid yang bersifat toksik pada ikan Oryzias latipes pada konsentrasi 5 ppm dan dapat menghambat aktivitas bakteri Gram positif pada konsentrasi 5–20 ppm (Mulholland et al 1998). Ekstrak etanol dari biji mahoni Afrika mengandung tetranortriterpenoid dan berpotensi sebagai insektisida (Govindachari & Kumari 1998). Shahidur et al. (2009) melaporkan bahwa ekstrak metanol biji mahoni mengandung 2 jenis senyawa limonoid, yaitu swietenolida dan 2-hidroksi-3-O-tigloilswietenolida, dan memiliki aktivitas sebagai antibakteri (Gambar 1). Ekstrak kasar metanol biji mahoni berpotensi sebagai antimikrob yang dapat menghambat pertumbuhan Candida
albicans, Staphylococcus aureus,
Pseudomonas aeroginosa, Streptococcus
faecalis, dan Proteus mirabillase (Sahgal et al. 2009). Selain itu, ekstrak metanol-air (3:2) biji mahoni berpotensi menurunkan kadar gula
darah pada tikus dalam 21 hari (Debasis et al. 2010)
(a)
(b)
Gambar 1 Struktur senyawa limonoid, yaitu swietenolida (a) dan 2-hidroksi-3-O-tigloilswietenolida (b).
Kandungan senyawa kimia biji mahoni (Gambar 2) di antaranya flavonoid, saponin, alkaloid, steroid/triterpenoid, dan tanin (Sianturi 2001; Haryanti 2002; Setiani 2009). Flavonoid diketahui mampu berperan menangkap radikal bebas atau sebagai antioksidan alami (Amic et al. 2003; Lugasi et al. 2003).
Penggunaan antioksidan alami pada saat ini menjadi alternatif yang dipilih karena terdapat kekhawatiran terhadap efek samping antioksidan sintetik. Antioksidan alami mampu melindungi tubuh terhadap kerusakan yang disebabkan oleh spesies oksigen reaktif dan mampu menghambat penyakit degeneratif (Sunarni et al. 2007). Tanaman (buah, sayuran, tanaman herbal, dan lainnya) mengandung senyawa yang dapat menangkap molekul radikal bebas, contohnya senyawa fenolik (flavonoid, asam fenolat, kuinon, dan tanin) (Harnly et al. 2006).
Khasiat biji mahoni yang mengandung flavonoid sebagai antioksidan perlu diuji secara ilmiah. Penelitian ini bertujuan mengisolasi, mengidentifikasi golongan flavonoid, dan menguji aktivitas antioksidan. Selain itu, dilakukan juga analisis gugus fungsi senyawa yang terkandung dalam biji mahoni menggunakan spektrofotometer inframerah transformasi Fourier (FTIR).
Potensi antioksidan penangkap radikal ditentukan menggunakan radikal 1,1-difenil-2-pikrilhidrazil (DPPH). Metode uji ini dipilih karena sederhana, cepat, dan peka untuk evaluasi aktivitas antioksidan dari senyawa bahan alam (Hanani et al. 2005). Senyawa yang aktif sebagai antioksidan akan mereduksi radikal bebas DPPH menjadi difenilpikrilhidrazina (Amic et al. 2003). Uji kemurnian fraksi aktif menggunakan kromatografi lapis tipis (KLT) 2 dimensi dan kromatografi cair kinerja tinggi (KCKT). Flavonoid yang merupakan komponen fenolik memberikan serapan pada panjang gelombang 240 dan 270 nm, dan antara 320 dan 380 nm. Pada KCKT, digunakan detektor ultraviolet (UV) atau UV-tampak (Lee 2000). Spektrofotometer FTIR merupakan cara paling sederhana dalam menentukan golongan senyawa. Spektrum FTIR dapat menunjukkan adanya beberapa gugus fungsi yang merupakan pita-pita khas yang teramati dalam spektrum senyawaan fenolik (Silverstein et al. 2005).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah biji mahoni yang diambil dari Kebun Raya Purwodadi Jawa Timur, etanol 70%, metanol, etanol 96%, akuades, kloroform, eter, NH4OH, H2SO4 2M, FeCl3 1%, anhidrida asetat, amil alkohol, serbuk Mg, HCl pekat, CH3COONa, Na2CO3, CH3COOPb, H2SO4
pekat, butil hidroksitoluena (BHT), etil asetat, NaOH 0.1 N, n-heksana, HCl 2 N, DPPH, pereaksi Mayer, Wagner, Dragendorf, dan Lieberman-Buchard.
Alat-alat yang digunakan adalah peralatan kaca yang biasa digunakan di laboratorium, KLT preparatif, pelat KLT GF254, penguap putar, spektrofotometer UV-Tampak Pharmaspec 1700 Shimadzu, KCKT 20 AD.Prominance UFLC Shimadzu, dan spektrofotometer FTIR Bruker Trensor 37.
Kadar Air
Diagram alir penelitian ditunjukkan pada Lampiran 1. Cawan porselen dikeringkan pada suhu 105 oC selama 3 jam. Cawan kemudian didinginkan dalam eksikator dan ditimbang bobot keringnya. Sampel ditimbang sebanyak 3 g dimasukkan ke dalam cawan tersebut dan dipanaskan di dalam oven dengan suhu 105 oC selama 3 jam. Setelah itu, cawan didinginkan dalam eksikator dan ditimbang sampai bobotnya konstan.
Isolasi Flavonoid (Markham 1988)
Serbuk biji mahoni direndam dengan etanol 70% selama 24 jam pada suhu kamar. Ekstrak yang diperoleh disaring dan ampasnya direndam kembali dengan etanol 70% beberapa kali sampai ampas tidak berwarna kuning. Filtratnya dipekatkan dengan penguap putar.
Ekstrak etanol biji mahoni dipartisi dengan n-heksana, kemudian dihidrolisis dengan HCl 2 N pada suhu 100 °C selama 60 menit. Ekstrak etanol biji mahoni terhidrolisis dipartisi dengan etil asetat. Fraksi etil asetat dikumpulkan dan dipekatkan dengan penguap putar, lalu difraksionasi dengan KLT preparatif. Pemilihan eluen terbaik dilakukan dengan menggunakan pelat KLT GF254 sebagai fase diam.
Uji Aktivitas Antioksidan (Blois 1958 diacu dalam Hanani et al. 2005)
Larutan ekstrak dibuat dengan konsentrasi 10, 30, 50, 70, dan 90 mg L-1. Sebanyak 4.5 mL larutan ekstrak dimasukkan ke dalam tabung reaksi dan ditambahkan 1.5 mL larutan DPPH 0.1 mM dalam etanol. Campuran diinkubasi pada suhu 37 °C selama 30 menit, lalu diukur serapannya pada panjang gelombang 515 nm. BHT dengan konsentrasi 2, 4, 6, 8, dan 10 mg L-1 digunakan sebagai kontrol positif. Kemudian nilai IC50 dihitung menggunakan rumus persamaan regresi.
Uji Fitokimia (Harborne 1987)
Alkaloid
Sebanyak 0.1 g ekstrak dilarutkan dalam 10 mL CHCl3 dan 4 tetes NH4OH. Larutan disaring, filtratnya dimasukkan ke dalam tabung reaksi tertutup, dan dikocok dengan 10 tetes H2SO4 2 M. Lapisan asam dipisahkan ke dalam tabung reaksi yang lain, lalu diteteskan pada lempeng tetes dan ditambahkan pereaksi Mayer, Wagner, dan Dragendorf. Timbulnya endapan, berturut-turut berwarna putih, cokelat, dan merah jingga, menunjukkan keberadaan alkaloid.
Saponin
Sebanyak 0.1 g ekstrak ditambahkan 10 mL air panas dan dididihkan selama 5 menit. Setelah itu, disaring dan filtratnya digunakan untuk pengujian. Filtrat dimasukkan ke dalam tabung reaksi tertutup kemudian dikocok selama 10 detik dan didiamkan selama 10 menit. Adanya saponin ditunjukkan dengan terbentuknya buih yang stabil.
Triterpenoid dan Steroid
Sebanyak 0.1 g ekstrak dilarutkan dengan 25 mL etanol panas (50 °C). Larutan disaring dalam pinggan porselen dan diuapkan sampai kering. Residu ditambahkan eter dan ekstrak eter dipindahkan ke lempeng tetes untuk ditambahkan 3 tetes anhidrida asetat dan 1 tetes H2SO4 pekat (uji Lieberman-Buchard). Warna merah atau ungu menunjukkan kandungan triterpenoid, sedangkan warna hijau atau biru menunjukkan kandungan steroid.
Tanin
Sebanyak 0.1 g ekstrak ditambahkan 10 mL air panas, dididihkan selama 5 menit, dan disaring. Sebagian filtrat yang diperoleh
ditambahkan larutan FeCl3 1%. Hasil positif ditunjukkan oleh warna hijau kehitaman.
Flavonoid
Sebanyak 0.1 g ekstrak ditambahkan 10 mL air panas dan dididihkan selama 5 menit. Setelah itu, disaring dan filtratnya digunakan untuk pengujian. Filtrat dimasukkan ke dalam tabung reaksi lalu ditambahkan 0.5 g serbuk Mg, 1 mL HCl pekat, dan 1 mL amil alkohol, dan dikocok kuat. Uji positif flavonoid menghasilkan warna kuning atau jingga pada lapisan amil alkohol.
Uji Golongan Flavonoid (Harborne 1987)
Sebanyak 0.5 g ekstrak dilarutkan dengan 10 mL metanol-HCl 1 N (1:1) dan dipanaskan pada suhu 95 °C selama 1 jam. Setelah itu, didinginkan dan disaring, lalu filtratnya diekstraksi dengan etil asetat.
Antosianidin
Sebanyak 1 mL ekstrak etil asetat ditambahkan 3 tetes CH3COONa lalu diamati, kemudian ditambahkan 3 tetes FeCl3 dan diamati lagi. Antosianidin dengan CH3COONa memberikan warna merah atau ungu dan bila ditambahkan FeCl3 menjadi biru.
Uji lainnya, sebanyak 1 mL ekstrak etil asetat ditambahkan Na2CO3 lalu diamati. Antosianidin memberikan warna ungu, biru, atau hijau.
Flavon, Kalkon, Auron, dan Flavonol
Sebanyak 1 mL ekstrak etil asetat ditambahkan 3 tetes CH3COOPb lalu diamati warnanya. Flavon memberikan warna jingga hingga krem, kalkon jingga tua, dan auron merah.
Sebanyak 1 mL ekstrak etil asetat juga ditambahkan 3 tetes NaOH 0.1 N lalu diamati warnanya. Flavon memberikan warna kuning, flavonol memberikan warna kuning, jingga hingga krem, dan kalkon memberikan warna krem hingga merah tua.
Uji Kemurnian dengan KCKT (Hertog et al. 1992)
F1
Rf 0.55
F2
Rf 0.76
F3
Rf0.85
F4
Rf 0.91
akan melewati kolom Nova_pak C18, yang memiliki dimensi (150 × 3.9 mm ID). Detektor yang digunakan diatur pada 370 nm dan oven pada suhu 30 °C .
Identifikasi Fraksi Aktif
Padatan fraksi teraktif dicampurkan dengan 200 mg KBr. Campuran tersebut kemudian dibuat pelet dan dilakukan analisis spektrum FTIR.
HASIL DAN PEMBAHASAN
Kadar Air
Penentuan kadar air berguna untuk menyatakan kandungan zat dalam tumbuhan sebagai persen bahan keringnya. Selain itu, penentuan kadar air berfungsi untuk mengetahui ketahanan sampel terhadap penyimpanan (Harjadi 1993). Sampel yang baik disimpan dalam jangka waktu yang panjang adalah yang memiliki kadar air kurang dari 10% (Winarno 1992).
Kandungan air dalam serbuk biji mahoni dihilangkan dengan pemanasan pada suhu 105 °C. Air yang terikat secara fisik akan dihilangkan dengan pemanasan pada suhu 100–105 °C (Harjadi 1993). Kadar air rerata biji mahoni sebesar 4.82% (Lampiran 2). Kadar air yang didapat kurang dari 10%, hal ini menunjukkan bahwa sampel dapat disimpan dalam waktu yang relatif lama.
Isolasi Senyawa Golongan Flavonoid
Tahap pertama isolasi senyawa flavonoid adalah maserasi dengan menggunakan etanol 70%. Etanol 70% digunakan sebagai pelarut karena bersifat polar sehingga dapat mengekstraksi senyawa flavonoid. Flavonoid merupakan senyawa polar karena mempunyai sejumlah gugus hidroksil baik yang terikat ataupun yang tidak terikat gula (Markham 1988). Selain itu, aktivitas antioksidan tanaman obat dalam etanol 70% lebih tinggi dibandingkan dengan beberapa pelarut lainnya (Macari et al. 2006). Maserasi dilakukan berulang kali sampai filtrat tidak berwarna kuning lagi, sehingga dapat dianggap semua senyawa yang berbobot molekul rendah telah terekstraksi (Harbone 1987). Ekstrak kasar yang diperoleh dipekatkan dengan penguap putar. Rendemen ekstrak kasar yang didapat dari 200.02 g serbuk biji mahoni sebesar 15.35% (Lampiran 3).
Pemisahan senyawa flavonoid dari ekstrak etanol 70% dilakukan dengan ekstraksi cair-cair. Sebelum dilakukan pemisahan flavonoid, ekstrak etanol dipartisi dengan n-heksana terlebih dahulu untuk menghilangkan lemak yang mungkin ikut terekstraksi. Setelah itu, ekstrak bebas-lemak dihidrolisis menggunakan asam. Hidrolisis dilakukan untuk memecah flavonoid ke dalam bentuk aglikonnya. Hasil hidrolisis dipartisi dengan etil asetat untuk memisahkan aglikon flavonoid dengan gulanya (Markham 1988). Aglikon umumnya mempunyai daya antioksidan dan penangkap radikal lebih tinggi daripada glikosida flavonoid, sebab pada glikosida flavonoid gugus hidroksil fenolik yang merupakan gugus aktif antioksidan maupun penangkap radikal telah mengikat gugus gula (Cholisoh & Utami 2008).
Pemisahan aglikon flavonoid pada ekstrak etil asetat dilakukan dengan KLT preparatif dengan menggunakan eluen terbaik dari berbagai jenis pelarut yang berbeda kepolarannya (Lampiran 4). Perbandingan eluen yang menghasilkan pemisahan terbaik menggunakan eluen metanol-etil asetat (1:1). Noda dideteksi di bawah lampu UV 254 nm dan diperoleh 4 noda. Nilai Rf untuk fraksi 1,
2, 3, dan 4 berturut-turut ialah 0.55; 0.76; 0.85; dan 0.91 (Gambar 3).
(a) (b)
Gambar 3 Noda pemisahan di bawah lampu UV 254 nm: KLT (a), KLT preparatif (b) dengan eluen etil asetat-metanol (1:1).
dengan yang bersifat semipolar. Dalam sistem kromatografi, senyawa akan bergerak cepat terbawa oleh eluen karena memiliki sifat kepolaran yang hampir sama dengan eluen. Setiap fraksi dikerok dan dilarutkan dengan etanol hingga mencukupi untuk uji kualitatif, uji aktivitas antioksidan, dan analisis senyawa golongan flavonoid.
Aktivitas Antioksidan
Aktivitas antioksidan diukur menggunakan radikal DPPH dan dinyatakan dengan IC50, yaitu bilangan yang menunjukkan konsentrasi ekstrak yang mampu menghambat aktivitas radikal sebesar 50% (Molyneux 2004). Aktivitas antioksidan ekstrak etil asetat dan keempat fraksi hasil KLT preparatif ditunjukkan pada Lampiran 5.
Ekstrak etil asetat mempunyai nilai IC50 sebesar 117.73 mg L-1. Fraksi 3 (F3) memperlihatkan aktivitas antioksidan tertinggi dengan nilai IC50 sebesar 65.18 mg L-1. Semakin rendah nilai IC50, semakin tinggi aktivitas antioksidannya (Molyneux 2004). Radikal bebas diharapkan dapat ditangkap oleh senyawa antioksidan hanya dengan konsentrasi yang kecil.
Kontrol positif yang digunakan ialah BHT. Dalam industri, BHT digunakan sebagai zat aditif antioksidan pada makanan, kosmetik, farmasi, produk karet, dan sebagainya. Fungsi BHT hampir sama seperti vitamin E, yaitu sebagai zat yang mencegah reaksi autooksidasi atau oksidasi yang disebabkan oleh O2 dari udara (Sudirman 2011).
Nilai IC50 BHT yang didapat sebesar 4.7 mg L-1. Aktivitas antioksidan F3 masih lebih kecil bila dibandingkan dengan aktivitas antioksidan BHT tersebut (Tabel 1). Walaupun demikian, F3 memiliki aktivitas antioksidan yang kuat, karena mempunyai IC50 kurang dari 200 mg L-1 (Hanani et al. 2005).
Tabel 1 Aktivitas antioksidan
Salah satu senyawa yang memiliki aktivitas antioksidan yang kuat ialah flavonoid. Reaksi yang terjadi antara senyawa
flavonoid dan DPPH meliputi pemberian atom hidrogen dari senyawa flavonoid untuk mereduksi radikal DPPH. Hal tersebut dapat terjadi disebabkan adanya lebih dari satu gugus hidroksil pada struktur molekulnya (Sunarni et al. 2007). Radikal bebas DPPH akan ditangkap oleh senyawa flavonoid dan flavonoid akan dioksidasi oleh radikal bebas menghasilkan bentuk radikal yang lebih stabil dengan kereaktifan yang rendah. Flavonoid mendonorkan radikal hidrogen dari cincin aromatiknya untuk mengurangi radikal bebas yang bersifat toksik, dan menghasilkan radikal flavonoid yang terstabilkan resonans dan tidak toksik (Amic et al. 2003).
Fitokimia dan Golongan Flavonoid
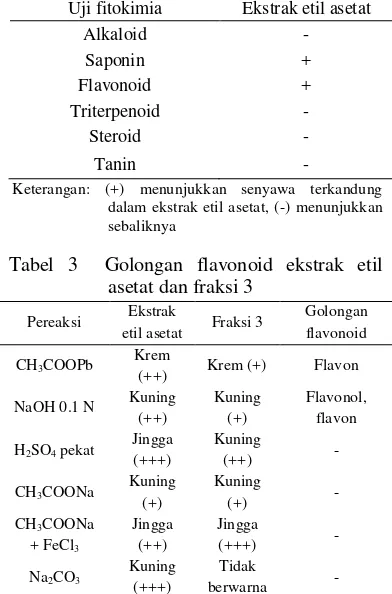
Uji fitokimia dilakukan pada ekstrak etil asetat (Tabel 2) dan uji golongan flavonoid dilakukan pada ekstrak etil asetat dan fraksi teraktif F3 (Tabel 3). Ekstrak etil asetat biji mahoni didapati positif saponin dan flavonoid. Uji golongan flavonoid pada ekstrak etil asetat dan F3 positif adanya golongan flavon atau flavonol.
Tabel 2 Fitokimia ekstrak etil asetat
Keterangan: (+) menunjukkan senyawa terkandung dalam ekstrak etil asetat, (-) menunjukkan sebaliknya
Tabel 3 Golongan flavonoid ekstrak etil asetat dan fraksi 3
Keterangan: (+) menunjukkan tingkat intensitas warna
Uji fitokimia Ekstrak etil asetat
Alkaloid -
Saponin +
Flavonoid +
Triterpenoid -
Steroid -
Tanin -
Larutan Uji IC50 (mg L-1)
BHT 4.7
Ekstrak etil asetat 117.73
F1 149.77
F2 93.11
F3 65.18
F4 94.41
Pereaksi Ekstrak
etil asetat Fraksi 3
Golongan flavonoid CH3COOPb
Krem
(++) Krem (+) Flavon NaOH 0.1 N Kuning
(++)
Kuning (+)
Flavonol, flavon H2SO4 pekat
Jingga (+++)
Kuning
(++) - CH3COONa
Kuning (+)
Kuning
(+) - CH3COONa
+ FeCl3
Jingga (++)
Jingga
(+++) - Na2CO3
Kuning (+++)
Tidak
Tingkat kemurnian F3 diuji dengan melakukan KLT 2 dimensi. Kromatogram dihasilkan dengan menggunakan eluen terbaik dan menghasilkan 1 noda tunggal (Gambar 4). Hasil KCKT juga memperlihatkan puncak tunggal dengan waktu retensi 14.079 menit (Gambar 5), maka fraksi yang didapat diduga sudah murni. Puncak kromatogram yang didapat melebar. Hal ini disebabkan konsentrasi dari senyawa yang terkandung kecil sehingga puncak tidak tajam dan puncak pelarut lebih terlihat daripada puncak senyawa dalam fraksi 3.
Eluen 1
Eluen 2
Gambar 4 KLT 2 dimensi fraksi 3 dengan eluen 1 etanol-etil asetat-heksana (3:2:0.5) dan eluen 2 metanol-etil asetat (1:1).
Gambar 5 Kromatogram fraksi 3.
Analisis Spektrum Inframerah
Analisis spektrum inframerah (Gambar 6) dengan menggunakan pelet KBr pada F3 menunjukkan adanya beberapa gugus fungsi. Menurut Silverstein et al. (2005), pita-pita khas yang teramati dalam spektrum senyawaan fenolik berasal dari vibrasi ulur O-H dan ulur C-O. Vibrasi ulur O-H dari F3 terlihat melebar di daerah 3500–3200 cm-1 dengan puncak serapan di 3429.76 cm-1. Vibrasi ini menunjukkan adanya gugus O-H yang membentuk ikatan hidrogen.
Serapan pada bilangan gelombang 1062.70 cm-1 menunjukkan adanya gugus C-O. Vibrasi ulur C-O dalam senyawaan fenolik menghasilkan pita kuat di daerah 1260–1050 cm-1. Serapan pada bilangan gelombang 2925.26 dan 2855.91 cm-1 menunjukkan vibrasi ulur C-H di dalam gugus CH alifatik. Pita-pita khas yang menunjukkan adanya gugus C=O dihasilkan oleh vibrasi ulur di daerah 1870–1540 cm-1. Spektrum FTIR F3 menunjukkan serapan pita ulur C=O heterosiklik pada 1604.63 cm-1. Gugus C=O pada umumnya berada pada di daerah 1700 cm-1, tetapi pada F3 mengalami pergeseran yang dapat disebabkan oleh pengaruh gugus fungsi OH yang berada disebelah C=O. Gugus C=O juga terdapat di daerah vibrasi ulur 1604 cm-1 pada ekstrak Chrysanthemum parthenium yang mengandung senyawa flavonoid (Shafaghat & Salimi 2008).
Gambar 6 Spektrum inframerah fraksi 3. 3429.79
2925.26 2855.91
1604.63
SIMPULAN DAN SARAN
Simpulan
Rendemen ekstrak etanol 70% biji mahoni sebesar 15.35%. Ekstrak etil asetat memiliki aktivitas antioksidan dengan nilai IC50 sebesar 117.73 mg L-1. Fraksi 3 (Rf 0.85; eluen
metanol-etil asetat 1:1) memiliki aktivitas antioksidan tertinggi dibandingkan dengan ketiga fraksi lainnya dengan IC50 sebesar 65.18 mg L-1. Uji golongan flavonoid pada fraksi 3 menunjukkan flavon atau flavonol. Hasil spektrum inframerah memperlihatkan bahwa senyawa tersebut mempunyai gugus fungsi OH, C=O, C–O dan CH alifatik.
Saran
Perlu dilakukan analisis lebih lanjut dengan menggunakan resonans magnetik inti 1
H, 13C, dan spektrometer massa untuk memastikan struktur senyawa dalam fraksi 3.
DAFTAR PUSTAKA
Amic D, Beslo D, Trinajstic N, Davidovic. 2003. Structure-radical scavenging activity relationships of flavonoids. Croatia Chem Acta 76:55-61.
Cholisoh Z, Utami W. 2008. Aktivitas penangkap radikal ekstrak etanol 70 % biji jengkol (Archidendron jiringa).
Pharmacon 9:33-40.
Dalimartha S. 2007. Atlas Tumbuhan Obat
Indonesia, Jilid 2. Jakarta: Trubus
Agriwidya.
Debasis De, Chatterjee K, Ali KM, Bera TK, Ghosh D. 2010. Antidiabetic potentiality of the aqueous-methanolic extract of seed
of Swietenia mahagoni (L.) Jacq. in
streptozotocin-induced diabetic male albino rat: A correlative and antihyperlipidemic activities. Evidence-Based Complementary and Alternative Med 2011:1-11.
Govindachari TR, Kumari GNK. 1998. Tetranortriterpenoid from Khaya
senegalensis. Phytochemistry
47:1423-1425.
Hanani E, Abdul M, Ryany S. 2005. Identifikasi senyawa antioksidan dalam Callyspongia sp dari Kepulauan Seribu.
Maj Ilmu Kefarmasian 2:127-133.
Harborne JB. 1987. Metode Fitokimia. Padmawinata K, Soediro I, penerjemah; Niksolihin S, editor. Bandung: ITB. Terjemahan dari: Phytochemical Methods. Harjadi W. 1993. Ilmu Kimia Analitik Dasar.
Jakarta: Gramedia Pustaka Utama.
Harnly JM, Doherty RF, Beecher GR, Holden JM, Haytowitz DB, Bhagwat S, Gebhardt S. 2006. Flavonoid content of U.S. fruits, vegetables, and nuts. J Agric Food Chem 54:9966-9977.
Haryanti F. 2002. Isolasi senyawa antibakteri dari biji mahoni (Swietenia mahagoni Jacq.) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Hertog MGL, Hollman PCH, Venema DP. 1992. Optimization of a quantitative HPLC determination of potentially anticarcinogenic flavonoid in vegetables and fruits. Agric Food 40:1591-1598. Lee HS. 2000. HPLC Analysis of Phenolic
Compounds. Di dalam: Food Analysis by HPLC. Nollet LML, editor. New York: Marcel Dekker.
Lugasi A, Hovari J, Sagi KV, Biro L. 2003. The role of antioxidant phytonutrients in the prevention of diseases. Acta Biol Szeged 47:119-125.
Macari PdAT, Portela CN, Polhit AM. 2006. Antioxidant, cytotoxic, and UVB-absorbing activity of Maynetus guyanensis Klotzch (Celastraceae) bark extract. Acta
Amazonica 36:513-518.
Markham KR. 1988. Cara Mengidentifikasi
Flavonoid. Padmawinata K, penerjemah.
Bandung: ITB. Terjemahan dari: Techniques of Flavonoid of Identification. Molyneux P. 2004. The use of stable free
radical diphenylpicryl-hydrazyl (DPPH) for estimazing antioxidant activity.
Songklanakarin J Sci Technol 26:211-219.
Mulholland DA, Iourine S, Taylor DAH. 1998. Sesquiterpenoids from Dysoxylum schiffnerri. Phytochemistry 47:1421-1422. Putri NE. 2004. Inhibisi fraksi aktif biji
Sahgal G, Ramanathan S, Sasidharan S, Mordi MN, Ismail S, Mansor SM. 2009. Phytochemical and antimicrobial activity of Swietenia mahagoni crude methanolic seed extract. Tropical Biol 26:274-279. Setiani RFC. 2009. Sitotoksisitas fraksi aktif
biji mahoni (Swietenia mahagoni) pada sel kanker payudara T47D [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Shafagat A, Salimi F. 2008. Extraction and determining of chemical structure of flavonoids in Tanacetum parthenium (L.) Schultz. Bip. from Iran. J Sci IAU 18:39-42.
Shahidur R, Azad C, Husne-Ara A, Sheikh ZR, Mohammad SA, Lutfun N, Satyajit DS. 2009. Antibacterial activity of two limonoids from Swietenia mahagoni against multiple-drug-resistant (MDR) bacterial strains. J Nat Med 63:41-45.
Sianturi AHM. 2001. Isolasi dan fraksinasi senyawa bioaktif dari biji mahoni
(Swietenia mahagoni Jacq.) [skripsi].
Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Silverstein RM, Webster FX, Kiemle DJ. 2005. Spectrometric Identification of Organic Compounds Ed ke-7. New York: J Wiley.
Sudirman S. 2011. Aktivitas antioksidan dan komponen bioaktif kangkung air (Ipomea
aquatica Forsk.) [skripsi]. Fakultas
Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Sunarni T, Pramono S, Asmah R. 2007. Flavonoid antioksidan penangkap radikal dari daun kepel Stelechocarpus burahol (BI.) Hook f. & Th. Maj Farmasi Indonesia 18:111-116.
Winarno FG. 1997. Kimia Pangan dan Gizi. Jakarta: Gramedia.
10
Lampiran 1 Diagram alir penelitian
Fraksionasi (KLTp)
Partisi dengan etil asetat
Hidrolisis HCl Serbuk biji mahoni
Penetapan kadar air Ekstraksi dengan etanol 70%
Residu Ekstrak etanol
Partisi dengan n-heksana
Fraksi n-heksana Fraksi etanol
Fraksi etanol terhidrolisis
Uji golongan flavonoid
dan antioksidan Fraksi etil asetat Fraksi etanol
Fraksi 2 Fraksi 3 Fraksi 4
Senyawa golongan flavonoid Uji antioksidan
Uji golongan flavonoid KLT 2 dimensi, KCKT, FTIR Fraksi teraktif
Lampiran 2 Kadar air serbuk biji mahoni
Ulangan
Bobot cawan kosong
(g)
Bobot cawan + contoh
(g)
Bobot contoh (g)
Bobot contoh kering
(g)
Kadar air (%b/b)
1 29.6484 32.5115 3.0065 2.8631 4.77
2 28.8422 31.6977 3.0001 2.8555 4.82
3 29.5506 32.4144 3.0077 2.8608 4.88
Rata-rata 4.82
Contoh perhitungan:
Lampiran 3 Rendemen hasil ekstraksi
Bobot serbuk biji mahoni (
W
contoh)
= 200.02 g
Bobot ekstrak (
W
ekstrak)
= 29.23 g
Kadar air
= 4.82%
Contoh perhitungan :
Lampiran 4 Kromatogram pencarian eluen terbaik
(a)
(b) (c) (d) (e) (f) (g)
(h) (i) (j) (k) (l) (m)
Keterangan: metanol (a), aseton (b), eter (c),
n-
heksana (d), etil asetat (e),
MeOH-EtOAc (1:3) (f), (3:1) (g), (1:6) (h), (6:1) (i), (1:9) (j), (9:1) (k), (2:3)
(l), (3:2) (m)
Lampiran 5 Hasil uji aktivitas antioksidan
a)
BHT
Konsentrasi
(mg/L)
ln
konsentrasi
% Inhibisi
2
0.6931
18.93
4
1.3863
48.83
6
1.7918
56.7
8
2.0794
67.72
10
2.3026
75.1
b)
Etil asetat
Konsentrasi (mg/L)
ln
konsentrasi % Inhibisi
10 2,3026 4,92
30 3,4012 17,78
50 3,912 28,23
70 4,2485 32,45
Lanjutan Lampiran 5
c)
F1
Konsentrasi (mg/L)
ln
konsentrasi % Inhibisi
10 2.3026 6.84
30 3.4012 16.19
50 3.912 25.71
70 4.2485 34.62
90 4.4998 49.39
d)
F2
Konsentrasi (mg/L)
ln
konsentrasi % Inhibisi
10 2.3026 26.52
30 3.4012 40.69
50 3.912 44.53
70 4.2485 47.57
Lanjutan Lampiran 5
e)
F3
Konsentrasi (mg/L)
ln
konsentrasi % Inhibisi
10 2.3026 19.84
30 3.4012 46.76
50 3.912 48.99
70 4.2485 48.78
90 4.4998 50.81
f)
F4
Konsentrasi (mg/L)
ln
konsentrasi % Inhibisi
10 2,3026 45,34
30 3,4012 47,77
50 3,912 48,79
70 4,2485 49,39
i
mahagoni
Jacq.) yang Berpotensi sebagai Antioksidan. Dibimbing oleh DUDI
TOHIR dan GUSTINI SYAHBIRIN.
Biji mahoni daun kecil (
Swietenia mahagoni
Jacq.) mengandung senyawa
flavonoid yang memiliki potensi sebagai antioksidan. Penelitian ini bertujuan
mengisolasi senyawa flavonoid biji mahoni yang memberikan aktivitas
antioksidan yang tinggi. Aktivitas antioksidan ditentukan dengan menggunakan
metode 1,1-difenil-2-pikrilhidrazil. Ekstrak etil asetat biji mahoni difraksionasi
dengan menggunakan kromatografi lapis tipis preparatif dengan eluen etil
asetat-metanol (1:1) dan menghasilkan 4 fraksi. Ekstrak etil asetat memiliki aktivitas
antioksidan dengan nilai konsentrasi hambat 50% (IC
50) sebesar 117.73 mg L
-1.Fraksi teraktif dari biji mahoni ialah fraksi 3 dengan IC
50sebesar 65.18 mg L
-1,
tetapi aktivitasnya masih lebih kecil dari butil hidroksitoluena (BHT) sebesar 4.70
mg L
-1. Uji kemurnian fraksi 3 menggunakan kromatografi cair kinerja tinggi
(KCKT) menghasilkan satu puncak dengan waktu retensi 14.079 menit dan uji
golongan flavonoid menunjukkan senyawa flavonol atau flavon. Spektrum
inframerah fraksi 3 menunjukkan gugus fungsi OH, C=O, C-O, dan CH alifatik.
ABSTRACT
ZULIA HALI. Isolation of Flavonoid Compounds from Mahogany’s Seed
(
Swietenia mahagoni
Jacq.) Potential as An Antioxidant. Supervised by DUDI
TOHIR and GUSTINI SYAHBIRIN.
Small-leaves mahogany’s seed (
Swietenia mahagoni
Jacq.) contains
flavonoid compounds which are potential as an antioxidant. The purpose of this
research is to isolate flavonoid compounds from mahogany’s seed which give
high antioxidant activity. Antioxidant activity was determined by using
1,1-diphenyl-2-picrylhydrazyl method. Ethyl acetate extract of mahogany’s seed was
fractionated using preparative thin layer chromatography with ethyl
acetate-methanol (1:1) as eluent, resulting 4 fractions. Ethyl acetate extract had
antioxidant activity with the 50% inhibition concentration (IC
50) value of about
117.73 mg L
-1. The most active fraction of mahogany’s seed was the third fraction
with the IC
50value of 65.18 mg L
-1, but the activity was still lower than butyl
hydroxytoluene 4.70 mg L
-1. Purity assay of this fraction by high performance
liquid chromatography (HPLC) resulted one peak with retention time of 14.079
minutes and flavonoid group assay showed flavonol or flavone compound. The
infrared spectrum of the third fraction showed that it had OH, C=O, C-O, and
aliphatic CH functional groups.
PENDAHULUAN
Tumbuhan obat asli Indonesia sampai saat ini masih banyak digunakan oleh masyarakat dalam pengobatan berbagai jenis penyakit. Pengetahuan tentang tanaman berkhasiat obat berdasarkan pada pengalaman dan keterampilan yang diwariskan turun-temurun. Salah satu tanaman yang biasa digunakan sebagai obat tradisional adalah biji mahoni daun kecil (Swietenia mahagoni Jacq.). Mahoni daun kecil merupakan famili Meliaceae, lazim ditanam di tepi jalan sebagai pohon pelindung. Secara tradisional, bijinya berkhasiat sebagai obat tekanan darah tinggi, kencing manis, perangsang nafsu makan, obat rematik, demam, masuk angin, encok, dan eksim (Dalimartha 2007).
Beberapa penelitian telah dilakukan untuk penelusuran kandungan aktif dan bioaktivitas yang dimiliki biji mahoni. Biji mahoni mengandung senyawa bioaktif yang bersifat toksik terhadap larva udang Artemia salina Leach dan berpotensi sebagai obat (Sianturi 2001). Fraksi aktif biji mahoni dapat menghambat pertumbuhan Saccharomyces cerevisiae (Putri 2004). Ekstrak metanol, heksana, dan etil asetat biji mahoni terbukti mampu menghambat pertumbuhan bakteri
Escherichia coli dan Bacillus subtilis
(Haryanti 2002). Menurut Setiani (2009), biji mahoni juga dapat menghambat pertumbuhan sel kanker payudara T47D dengan nilai konsentrasi hambat 50% (IC50) sebesar 49.12 ppm dan mengandung senyawa alkaloid serta steroid/triterpenoid.
Ekstrak metanol batang kayu famili Meliaceae mengandung terpenoid yang bersifat toksik pada ikan Oryzias latipes pada konsentrasi 5 ppm dan dapat menghambat aktivitas bakteri Gram positif pada konsentrasi 5–20 ppm (Mulholland et al 1998). Ekstrak etanol dari biji mahoni Afrika mengandung tetranortriterpenoid dan berpotensi sebagai insektisida (Govindachari & Kumari 1998). Shahidur et al. (2009) melaporkan bahwa ekstrak metanol biji mahoni mengandung 2 jenis senyawa limonoid, yaitu swietenolida dan 2-hidroksi-3-O-tigloilswietenolida, dan memiliki aktivitas sebagai antibakteri (Gambar 1). Ekstrak kasar metanol biji mahoni berpotensi sebagai antimikrob yang dapat menghambat pertumbuhan Candida
albicans, Staphylococcus aureus,
Pseudomonas aeroginosa, Streptococcus
faecalis, dan Proteus mirabillase (Sahgal et al. 2009). Selain itu, ekstrak metanol-air (3:2) biji mahoni berpotensi menurunkan kadar gula
darah pada tikus dalam 21 hari (Debasis et al. 2010)
(a)
(b)
Gambar 1 Struktur senyawa limonoid, yaitu swietenolida (a) dan 2-hidroksi-3-O-tigloilswietenolida (b).
Kandungan senyawa kimia biji mahoni (Gambar 2) di antaranya flavonoid, saponin, alkaloid, steroid/triterpenoid, dan tanin (Sianturi 2001; Haryanti 2002; Setiani 2009). Flavonoid diketahui mampu berperan menangkap radikal bebas atau sebagai antioksidan alami (Amic et al. 2003; Lugasi et al. 2003).
Penggunaan antioksidan alami pada saat ini menjadi alternatif yang dipilih karena terdapat kekhawatiran terhadap efek samping antioksidan sintetik. Antioksidan alami mampu melindungi tubuh terhadap kerusakan yang disebabkan oleh spesies oksigen reaktif dan mampu menghambat penyakit degeneratif (Sunarni et al. 2007). Tanaman (buah, sayuran, tanaman herbal, dan lainnya) mengandung senyawa yang dapat menangkap molekul radikal bebas, contohnya senyawa fenolik (flavonoid, asam fenolat, kuinon, dan tanin) (Harnly et al. 2006).
Khasiat biji mahoni yang mengandung flavonoid sebagai antioksidan perlu diuji secara ilmiah. Penelitian ini bertujuan mengisolasi, mengidentifikasi golongan flavonoid, dan menguji aktivitas antioksidan. Selain itu, dilakukan juga analisis gugus fungsi senyawa yang terkandung dalam biji mahoni menggunakan spektrofotometer inframerah transformasi Fourier (FTIR).
Potensi antioksidan penangkap radikal ditentukan menggunakan radikal 1,1-difenil-2-pikrilhidrazil (DPPH). Metode uji ini dipilih karena sederhana, cepat, dan peka untuk evaluasi aktivitas antioksidan dari senyawa bahan alam (Hanani et al. 2005). Senyawa yang aktif sebagai antioksidan akan mereduksi radikal bebas DPPH menjadi difenilpikrilhidrazina (Amic et al. 2003). Uji kemurnian fraksi aktif menggunakan kromatografi lapis tipis (KLT) 2 dimensi dan kromatografi cair kinerja tinggi (KCKT). Flavonoid yang merupakan komponen fenolik memberikan serapan pada panjang gelombang 240 dan 270 nm, dan antara 320 dan 380 nm. Pada KCKT, digunakan detektor ultraviolet (UV) atau UV-tampak (Lee 2000). Spektrofotometer FTIR merupakan cara paling sederhana dalam menentukan golongan senyawa. Spektrum FTIR dapat menunjukkan adanya beberapa gugus fungsi yang merupakan pita-pita khas yang teramati dalam spektrum senyawaan fenolik (Silverstein et al. 2005).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah biji mahoni yang diambil dari Kebun Raya Purwodadi Jawa Timur, etanol 70%, metanol, etanol 96%, akuades, kloroform, eter, NH4OH, H2SO4 2M, FeCl3 1%, anhidrida asetat, amil alkohol, serbuk Mg, HCl pekat, CH3COONa, Na2CO3, CH3COOPb, H2SO4
pekat, butil hidroksitoluena (BHT), etil asetat, NaOH 0.1 N, n-heksana, HCl 2 N, DPPH, pereaksi Mayer, Wagner, Dragendorf, dan Lieberman-Buchard.
Alat-alat yang digunakan adalah peralatan kaca yang biasa digunakan di laboratorium, KLT preparatif, pelat KLT GF254, penguap putar, spektrofotometer UV-Tampak Pharmaspec 1700 Shimadzu, KCKT 20 AD.Prominance UFLC Shimadzu, dan spektrofotometer FTIR Bruker Trensor 37.
Kadar Air
Diagram alir penelitian ditunjukkan pada Lampiran 1. Cawan porselen dikeringkan pada suhu 105 oC selama 3 jam. Cawan kemudian didinginkan dalam eksikator dan ditimbang bobot keringnya. Sampel ditimbang sebanyak 3 g dimasukkan ke dalam cawan tersebut dan dipanaskan di dalam oven dengan suhu 105 oC selama 3 jam. Setelah itu, cawan didinginkan dalam eksikator dan ditimbang sampai bobotnya konstan.
Isolasi Flavonoid (Markham 1988)
Serbuk biji mahoni direndam dengan etanol 70% selama 24 jam pada suhu kamar. Ekstrak yang diperoleh disaring dan ampasnya direndam kembali dengan etanol 70% beberapa kali sampai ampas tidak berwarna kuning. Filtratnya dipekatkan dengan penguap putar.
Ekstrak etanol biji mahoni dipartisi dengan n-heksana, kemudian dihidrolisis dengan HCl 2 N pada suhu 100 °C selama 60 menit. Ekstrak etanol biji mahoni terhidrolisis dipartisi dengan etil asetat. Fraksi etil asetat dikumpulkan dan dipekatkan dengan penguap putar, lalu difraksionasi dengan KLT preparatif. Pemilihan eluen terbaik dilakukan dengan menggunakan pelat KLT GF254 sebagai fase diam.
Penggunaan antioksidan alami pada saat ini menjadi alternatif yang dipilih karena terdapat kekhawatiran terhadap efek samping antioksidan sintetik. Antioksidan alami mampu melindungi tubuh terhadap kerusakan yang disebabkan oleh spesies oksigen reaktif dan mampu menghambat penyakit degeneratif (Sunarni et al. 2007). Tanaman (buah, sayuran, tanaman herbal, dan lainnya) mengandung senyawa yang dapat menangkap molekul radikal bebas, contohnya senyawa fenolik (flavonoid, asam fenolat, kuinon, dan tanin) (Harnly et al. 2006).
Khasiat biji mahoni yang mengandung flavonoid sebagai antioksidan perlu diuji secara ilmiah. Penelitian ini bertujuan mengisolasi, mengidentifikasi golongan flavonoid, dan menguji aktivitas antioksidan. Selain itu, dilakukan juga analisis gugus fungsi senyawa yang terkandung dalam biji mahoni menggunakan spektrofotometer inframerah transformasi Fourier (FTIR).
Potensi antioksidan penangkap radikal ditentukan menggunakan radikal 1,1-difenil-2-pikrilhidrazil (DPPH). Metode uji ini dipilih karena sederhana, cepat, dan peka untuk evaluasi aktivitas antioksidan dari senyawa bahan alam (Hanani et al. 2005). Senyawa yang aktif sebagai antioksidan akan mereduksi radikal bebas DPPH menjadi difenilpikrilhidrazina (Amic et al. 2003). Uji kemurnian fraksi aktif menggunakan kromatografi lapis tipis (KLT) 2 dimensi dan kromatografi cair kinerja tinggi (KCKT). Flavonoid yang merupakan komponen fenolik memberikan serapan pada panjang gelombang 240 dan 270 nm, dan antara 320 dan 380 nm. Pada KCKT, digunakan detektor ultraviolet (UV) atau UV-tampak (Lee 2000). Spektrofotometer FTIR merupakan cara paling sederhana dalam menentukan golongan senyawa. Spektrum FTIR dapat menunjukkan adanya beberapa gugus fungsi yang merupakan pita-pita khas yang teramati dalam spektrum senyawaan fenolik (Silverstein et al. 2005).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah biji mahoni yang diambil dari Kebun Raya Purwodadi Jawa Timur, etanol 70%, metanol, etanol 96%, akuades, kloroform, eter, NH4OH, H2SO4 2M, FeCl3 1%, anhidrida asetat, amil alkohol, serbuk Mg, HCl pekat, CH3COONa, Na2CO3, CH3COOPb, H2SO4
pekat, butil hidroksitoluena (BHT), etil asetat, NaOH 0.1 N, n-heksana, HCl 2 N, DPPH, pereaksi Mayer, Wagner, Dragendorf, dan Lieberman-Buchard.
Alat-alat yang digunakan adalah peralatan kaca yang biasa digunakan di laboratorium, KLT preparatif, pelat KLT GF254, penguap putar, spektrofotometer UV-Tampak Pharmaspec 1700 Shimadzu, KCKT 20 AD.Prominance UFLC Shimadzu, dan spektrofotometer FTIR Bruker Trensor 37.
Kadar Air
Diagram alir penelitian ditunjukkan pada Lampiran 1. Cawan porselen dikeringkan pada suhu 105 oC selama 3 jam. Cawan kemudian didinginkan dalam eksikator dan ditimbang bobot keringnya. Sampel ditimbang sebanyak 3 g dimasukkan ke dalam cawan tersebut dan dipanaskan di dalam oven dengan suhu 105 oC selama 3 jam. Setelah itu, cawan didinginkan dalam eksikator dan ditimbang sampai bobotnya konstan.
Isolasi Flavonoid (Markham 1988)
Serbuk biji mahoni direndam dengan etanol 70% selama 24 jam pada suhu kamar. Ekstrak yang diperoleh disaring dan ampasnya direndam kembali dengan etanol 70% beberapa kali sampai ampas tidak berwarna kuning. Filtratnya dipekatkan dengan penguap putar.
Ekstrak etanol biji mahoni dipartisi dengan n-heksana, kemudian dihidrolisis dengan HCl 2 N pada suhu 100 °C selama 60 menit. Ekstrak etanol biji mahoni terhidrolisis dipartisi dengan etil asetat. Fraksi etil asetat dikumpulkan dan dipekatkan dengan penguap putar, lalu difraksionasi dengan KLT preparatif. Pemilihan eluen terbaik dilakukan dengan menggunakan pelat KLT GF254 sebagai fase diam.
Uji Aktivitas Antioksidan (Blois 1958 diacu dalam Hanani et al. 2005)
Larutan ekstrak dibuat dengan konsentrasi 10, 30, 50, 70, dan 90 mg L-1. Sebanyak 4.5 mL larutan ekstrak dimasukkan ke dalam tabung reaksi dan ditambahkan 1.5 mL larutan DPPH 0.1 mM dalam etanol. Campuran diinkubasi pada suhu 37 °C selama 30 menit, lalu diukur serapannya pada panjang gelombang 515 nm. BHT dengan konsentrasi 2, 4, 6, 8, dan 10 mg L-1 digunakan sebagai kontrol positif. Kemudian nilai IC50 dihitung menggunakan rumus persamaan regresi.
Uji Fitokimia (Harborne 1987)
Alkaloid
Sebanyak 0.1 g ekstrak dilarutkan dalam 10 mL CHCl3 dan 4 tetes NH4OH. Larutan disaring, filtratnya dimasukkan ke dalam tabung reaksi tertutup, dan dikocok dengan 10 tetes H2SO4 2 M. Lapisan asam dipisahkan ke dalam tabung reaksi yang lain, lalu diteteskan pada lempeng tetes dan ditambahkan pereaksi Mayer, Wagner, dan Dragendorf. Timbulnya endapan, berturut-turut berwarna putih, cokelat, dan merah jingga, menunjukkan keberadaan alkaloid.
Saponin
Sebanyak 0.1 g ekstrak ditambahkan 10 mL air panas dan dididihkan selama 5 menit. Setelah itu, disaring dan filtratnya digunakan untuk pengujian. Filtrat dimasukkan ke dalam tabung reaksi tertutup kemudian dikocok selama 10 detik dan didiamkan selama 10 menit. Adanya saponin ditunjukkan dengan terbentuknya buih yang stabil.
Triterpenoid dan Steroid
Sebanyak 0.1 g ekstrak dilarutkan dengan 25 mL etanol panas (50 °C). Larutan disaring dalam pinggan porselen dan diuapkan sampai kering. Residu ditambahkan eter dan ekstrak eter dipindahkan ke lempeng tetes untuk ditambahkan 3 tetes anhidrida asetat dan 1 tetes H2SO4 pekat (uji Lieberman-Buchard). Warna merah atau ungu menunjukkan kandungan triterpenoid, sedangkan warna hijau atau biru menunjukkan kandungan steroid.
Tanin
Sebanyak 0.1 g ekstrak ditambahkan 10 mL air panas, dididihkan selama 5 menit, dan disaring. Sebagian filtrat yang diperoleh
ditambahkan larutan FeCl3 1%. Hasil positif ditunjukkan oleh warna hijau kehitaman.
Flavonoid
Sebanyak 0.1 g ekstrak ditambahkan 10 mL air panas dan dididihkan selama 5 menit. Setelah itu, disaring dan filtratnya digunakan untuk pengujian. Filtrat dimasukkan ke dalam tabung reaksi lalu ditambahkan 0.5 g serbuk Mg, 1 mL HCl pekat, dan 1 mL amil alkohol, dan dikocok kuat. Uji positif flavonoid menghasilkan warna kuning atau jingga pada lapisan amil alkohol.
Uji Golongan Flavonoid (Harborne 1987)
Sebanyak 0.5 g ekstrak dilarutkan dengan 10 mL metanol-HCl 1 N (1:1) dan dipanaskan pada suhu 95 °C selama 1 jam. Setelah itu, didinginkan dan disaring, lalu filtratnya diekstraksi dengan etil asetat.
Antosianidin
Sebanyak 1 mL ekstrak etil asetat ditambahkan 3 tetes CH3COONa lalu diamati, kemudian ditambahkan 3 tetes FeCl3 dan diamati lagi. Antosianidin dengan CH3COONa memberikan warna merah atau ungu dan bila ditambahkan FeCl3 menjadi biru.
Uji lainnya, sebanyak 1 mL ekstrak etil asetat ditambahkan Na2CO3 lalu diamati. Antosianidin memberikan warna ungu, biru, atau hijau.
Flavon, Kalkon, Auron, dan Flavonol
Sebanyak 1 mL ekstrak etil asetat ditambahkan 3 tetes CH3COOPb lalu diamati warnanya. Flavon memberikan warna jingga hingga krem, kalkon jingga tua, dan auron merah.
Sebanyak 1 mL ekstrak etil asetat juga ditambahkan 3 tetes NaOH 0.1 N lalu diamati warnanya. Flavon memberikan warna kuning, flavonol memberikan warna kuning, jingga hingga krem, dan kalkon memberikan warna krem hingga merah tua.
Uji Kemurnian dengan KCKT (Hertog et al. 1992)
F1
Rf 0.55
F2
Rf 0.76
F3
Rf0.85
F4
Rf 0.91
akan melewati kolom Nova_pak C18, yang memiliki dimensi (150 × 3.9 mm ID). Detektor yang digunakan diatur pada 370 nm dan oven pada suhu 30 °C .
Identifikasi Fraksi Aktif
Padatan fraksi teraktif dicampurkan dengan 200 mg KBr. Campuran tersebut kemudian dibuat pelet dan dilakukan analisis spektrum FTIR.
HASIL DAN PEMBAHASAN
Kadar Air
Penentuan kadar air berguna untuk menyatakan kandungan zat dalam tumbuhan sebagai persen bahan keringnya. Selain itu, penentuan kadar air berfungsi untuk mengetahui ketahanan sampel terhadap penyimpanan (Harjadi 1993). Sampel yang baik disimpan dalam jangka waktu yang panjang adalah yang memiliki kadar air kurang dari 10% (Winarno 1992).
Kandungan air dalam serbuk biji mahoni dihilangkan dengan pemanasan pada suhu 105 °C. Air yang terikat secara fisik akan dihilangkan dengan pemanasan pada suhu 100–105 °C (Harjadi 1993). Kadar air rerata biji mahoni sebesar 4.82% (Lampiran 2). Kadar air yang didapat kurang dari 10%, hal ini menunjukkan bahwa sampel dapat disimpan dalam waktu yang relatif lama.
Isolasi Senyawa Golongan Flavonoid
Tahap pertama isolasi senyawa flavonoid adalah maserasi dengan menggunakan etanol 70%. Etanol 70% digunakan sebagai pelarut karena bersifat polar sehingga dapat mengekstraksi senyawa flavonoid. Flavonoid merupakan senyawa polar karena mempunyai sejumlah gugus hidroksil baik yang terikat ataupun yang tidak terikat gula (Markham 1988). Selain itu, aktivitas antioksidan tanaman obat dalam etanol 70% lebih tinggi dibandingkan dengan beberapa pelarut lainnya (Macari et al. 2006). Maserasi dilakukan berulang kali sampai filtrat tidak berwarna kuning lagi, sehingga dapat dianggap semua senyawa yang berbobot molekul rendah telah terekstraksi (Harbone 1987). Ekstrak kasar yang diperoleh dipekatkan dengan penguap putar. Rendemen ekstrak kasar yang didapat dari 200.02 g serbuk biji mahoni sebesar 15.35% (Lampiran 3).
Pemisahan senyawa flavonoid dari ekstrak etanol 70% dilakukan dengan ekstraksi cair-cair. Sebelum dilakukan pemisahan flavonoid, ekstrak etanol dipartisi dengan n-heksana terlebih dahulu untuk menghilangkan lemak yang mungkin ikut terekstraksi. Setelah itu, ekstrak bebas-lemak dihidrolisis menggunakan asam. Hidrolisis dilakukan untuk memecah flavonoid ke dalam bentuk aglikonnya. Hasil hidrolisis dipartisi dengan etil asetat untuk memisahkan aglikon flavonoid dengan gulanya (Markham 1988). Aglikon umumnya mempunyai daya antioksidan dan penangkap radikal lebih tinggi daripada glikosida flavonoid, sebab pada glikosida flavonoid gugus hidroksil fenolik yang merupakan gugus aktif antioksidan maupun penangkap radikal telah mengikat gugus gula (Cholisoh & Utami 2008).
Pemisahan aglikon flavonoid pada ekstrak etil asetat dilakukan dengan KLT preparatif dengan menggunakan eluen terbaik dari berbagai jenis pelarut yang berbeda kepolarannya (Lampiran 4). Perbandingan eluen yang menghasilkan pemisahan terbaik menggunakan eluen metanol-etil asetat (1:1). Noda dideteksi di bawah lampu UV 254 nm dan diperoleh 4 noda. Nilai Rf untuk fraksi 1,
2, 3, dan 4 berturut-turut ialah 0.55; 0.76; 0.85; dan 0.91 (Gambar 3).
(a) (b)
Gambar 3 Noda pemisahan di bawah lampu UV 254 nm: KLT (a), KLT preparatif (b) dengan eluen etil asetat-metanol (1:1).
dengan yang bersifat semipolar. Dalam sistem kromatografi, senyawa akan bergerak cepat terbawa oleh eluen karena memiliki sifat kepolaran yang hampir sama dengan eluen. Setiap fraksi dikerok dan dilarutkan dengan etanol hingga mencukupi untuk uji kualitatif, uji aktivitas antioksidan, dan analisis senyawa golongan flavonoid.
Aktivitas Antioksidan
Aktivitas antioksidan diukur menggunakan radikal DPPH dan dinyatakan dengan IC50, yaitu bilangan yang menunjukkan konsentrasi ekstrak yang mampu menghambat aktivitas radikal sebesar 50% (Molyneux 2004). Aktivitas antioksidan ekstrak etil asetat dan keempat fraksi hasil KLT preparatif ditunjukkan pada Lampiran 5.
Ekstrak etil asetat mempunyai nilai IC50 sebesar 117.73 mg L-1. Fraksi 3 (F3) memperlihatkan aktivitas antioksidan tertinggi dengan nilai IC50 sebesar 65.18 mg L-1. Semakin rendah nilai IC50, semakin tinggi aktivitas antioksidannya (Molyneux 2004). Radikal bebas diharapkan dapat ditangkap oleh senyawa antioksidan hanya dengan konsentrasi yang kecil.
Kontrol positif yang digunakan ialah BHT. Dalam industri, BHT digunakan sebagai zat aditif antioksidan pada makanan, kosmetik, farmasi, produk karet, dan sebagainya. Fungsi BHT hampir sama seperti vitamin E, yaitu sebagai zat yang mencegah reaksi autooksidasi atau oksidasi yang disebabkan oleh O2 dari udara (Sudirman 2011).
[image:30.595.319.515.414.711.2]Nilai IC50 BHT yang didapat sebesar 4.7 mg L-1. Aktivitas antioksidan F3 masih lebih kecil bila dibandingkan dengan aktivitas antioksidan BHT tersebut (Tabel 1). Walaupun demikian, F3 memiliki aktivitas antioksidan yang kuat, karena mempunyai IC50 kurang dari 200 mg L-1 (Hanani et al. 2005).
Tabel 1 Aktivitas antioksidan
Salah satu senyawa yang memiliki aktivitas antioksidan yang kuat ialah flavonoid. Reaksi yang terjadi antara senyawa
flavonoid dan DPPH meliputi pemberian atom hidrogen dari senyawa flavonoid untuk mereduksi radikal DPPH. Hal tersebut dapat terjadi disebabkan adanya lebih dari satu gugus hidroksil pada struktur molekulnya (Sunarni et al. 2007). Radikal bebas DPPH akan ditangkap oleh senyawa flavonoid dan flavonoid akan dioksidasi oleh radikal bebas menghasilkan bentuk radikal yang lebih stabil dengan kereaktifan yang rendah. Flavonoid mendonorkan radikal hidrogen dari cincin aromatiknya untuk mengurangi radikal bebas yang bersifat toksik, dan menghasilkan radikal flavonoid yang terstabilkan resonans dan tidak toksik (Amic et al. 2003).
Fitokimia dan Golongan Flavonoid
Uji fitokimia dilakukan pada ekstrak etil asetat (Tabel 2) dan uji golongan flavonoid dilakukan pada ekstrak etil asetat dan fraksi teraktif F3 (Tabel 3). Ekstrak etil asetat biji mahoni didapati positif saponin dan flavonoid. Uji golongan flavonoid pada ekstrak etil asetat dan F3 positif adanya golongan flavon atau flavonol.
Tabel 2 Fitokimia ekstrak etil asetat
Keterangan: (+) menunjukkan senyawa terkandung dalam ekstrak etil asetat, (-) menunjukkan sebaliknya
Tabel 3 Golongan flavonoid ekstrak etil asetat dan fraksi 3
Keterangan: (+) menunjukkan tingkat intensitas warna
Uji fitokimia Ekstrak etil asetat
Alkaloid -
Saponin +
Flavonoid +
Triterpenoid -
Steroid -
Tanin -
Larutan Uji IC50 (mg L-1)
BHT 4.7
Ekstrak etil asetat 117.73
F1 149.77
F2 93.11
F3 65.18
F4 94.41
Pereaksi Ekstrak
etil asetat Fraksi 3
Golongan flavonoid CH3COOPb
Krem
(++) Krem (+) Flavon NaOH 0.1 N Kuning
(++)
Kuning (+)
Flavonol, flavon H2SO4 pekat
Jingga (+++)
Kuning
(++) - CH3COONa
Kuning (+)
Kuning
(+) - CH3COONa
+ FeCl3
Jingga (++)
Jingga
(+++) - Na2CO3
Kuning (+++)
Tidak
[image:30.595.132.285.615.704.2]Tingkat kemurnian F3 diuji dengan melakukan KLT 2 dimensi. Kromatogram dihasilkan dengan menggunakan eluen terbaik dan menghasilkan 1 noda tunggal (Gambar 4). Hasil KCKT juga memperlihatkan puncak tunggal dengan waktu retensi 14.079 menit (Gambar 5), maka fraksi yang didapat diduga sudah murni. Puncak kromatogram yang didapat melebar. Hal ini disebabkan konsentrasi dari senyawa yang terkandung kecil sehingga puncak tidak tajam dan puncak pelarut lebih terlihat daripada puncak senyawa dalam fraksi 3.
Eluen 1
Eluen 2
[image:31.595.108.301.184.498.2]Gambar 4 KLT 2 dimensi fraksi 3 dengan eluen 1 etanol-etil asetat-heksana (3:2:0.5) dan eluen 2 metanol-etil asetat (1:1).
Gambar 5 Kromatogram fraksi 3.
Analisis Spektrum Inframerah
Analisis spektrum inframerah (Gambar 6) dengan menggunakan pelet KBr pada F3 menunjukkan adanya beberapa gugus fungsi. Menurut Silverstein et al. (2005), pita-pita khas yang teramati dalam spektrum senyawaan fenolik berasal dari vibrasi ulur O-H dan ulur C-O. Vibrasi ulur O-H dari F3 terlihat melebar di daerah 3500–3200 cm-1 dengan puncak serapan di 3429.76 cm-1. Vibrasi ini menunjukkan adanya gugus O-H yang membentuk ikatan hidrogen.
Serapan pada bilangan gelombang 1062.70 cm-1 menunjukkan adanya gugus C-O. Vibrasi ulur C-O dalam senyawaan fenolik menghasilkan pita kuat di daerah 1260–1050 cm-1. Serapan pada bilangan gelombang 2925.26 dan 2855.91 cm-1 menunjukkan vibrasi ulur C-H di dalam gugus CH alifatik. Pita-pita khas yang menunjukkan adanya gugus C=O dihasilkan oleh vibrasi ulur di daerah 1870–1540 cm-1. Spektrum FTIR F3 menunjukkan serapan pita ulur C=O heterosiklik pada 1604.63 cm-1. Gugus C=O pada umumnya berada pada di daerah 1700 cm-1, tetapi pada F3 mengalami pergeseran yang dapat disebabkan oleh pengaruh gugus fungsi OH yang berada disebelah C=O. Gugus C=O juga terdapat di daerah vibrasi ulur 1604 cm-1 pada ekstrak Chrysanthemum parthenium yang mengandung senyawa flavonoid (Shafaghat & Salimi 2008).
Gambar 6 Spektrum inframerah fraksi 3. 3429.79
2925.26 2855.91
1604.63
[image:31.595.109.505.514.713.2]SIMPULAN DAN SARAN
Simpulan
Rendemen ekstrak etanol 70% biji mahoni sebesar 15.35%. Ekstrak etil asetat memiliki aktivitas antioksidan dengan nilai IC50 sebesar 117.73 mg L-1. Fraksi 3 (Rf 0.85; eluen
metanol-etil asetat 1:1) memiliki aktivitas antioksidan tertinggi dibandingkan dengan ketiga fraksi lainnya dengan IC50 sebesar 65.18 mg L-1. Uji golongan flavonoid pada fraksi 3 menunjukkan flavon atau flavonol. Hasil spektrum inframerah memperlihatkan bahwa senyawa tersebut mempunyai gugus fungsi OH, C=O, C–O dan CH alifatik.
Saran
Perlu dilakukan analisis lebih lanjut dengan menggunakan resonans magnetik inti 1
H, 13C, dan spektrometer massa untuk memastikan struktur senyawa dalam fraksi 3.
DAFTAR PUSTAKA
Amic D, Beslo D, Trinajstic N, Davidovic. 2003. Structure-radical scavenging activity relationships of flavonoids. Croatia Chem Acta 76:55-61.
Cholisoh Z, Utami W. 2008. Aktivitas penangkap radikal ekstrak etanol 70 % biji jengkol (Archidendron jiringa).
Pharmacon 9:33-40.
Dalimartha S. 2007. Atlas Tumbuhan Obat
Indonesia, Jilid 2. Jakarta: Trubus
Agriwidya.
Debasis De, Chatterjee K, Ali KM, Bera TK, Ghosh D. 2010. Antidiabetic potentiality of the aqueous-methanolic extract of seed
of Swietenia mahagoni (L.) Jacq. in
streptozotocin-induced diabetic male albino rat: A correlative and antihyperlipidemic activities. Evidence-Based Complementary and Alternative Med 2011:1-11.
Govindachari TR, Kumari GNK. 1998. Tetranortriterpenoid from Khaya
senegalensis. Phytochemistry
47:1423-1425.
Hanani E, Abdul M, Ryany S. 2005. Identifikasi senyawa antioksidan dalam Callyspongia sp dari Kepulauan Seribu.
Maj Ilmu Kefarmasian 2:127-133.
Harborne JB. 1987. Metode Fitokimia. Padmawinata K, Soediro I, penerjemah; Niksolihin S, editor. Bandung: ITB. Terjemahan dari: Phytochemical Methods. Harjadi W. 1993. Ilmu Kimia Analitik Dasar.
Jakarta: Gramedia Pustaka Utama.
Harnly JM, Doherty RF, Beecher GR, Holden JM, Haytowitz DB, Bhagwat S, Gebhardt S. 2006. Flavonoid content of U.S. fruits, vegetables, and nuts. J Agric Food Chem 54:9966-9977.
Haryanti F. 2002. Isolasi senyawa antibakteri dari biji mahoni (Swietenia mahagoni Jacq.) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Hertog MGL, Hollman PCH, Venema DP. 1992. Optimization of a quantitative HPLC determination of potentially anticarcinogenic flavonoid in vegetables and fruits. Agric Food 40:1591-1598. Lee HS. 2000. HPLC Analysis of Phenolic
Compounds. Di dalam: Food Analysis by HPLC. Nollet LML, editor. New York: Marcel Dekker.
Lugasi A, Hovari J, Sagi KV, Biro L. 2003. The role of antioxidant phytonutrients in the prevention of diseases. Acta Biol Szeged 47:119-125.
Macari PdAT, Portela CN, Polhit AM. 2006. Antioxidant, cytotoxic, and UVB-absorbing activity of Maynetus guyanensis Klotzch (Celastraceae) bark extract. Acta
Amazonica 36:513-518.
Markham KR. 1988. Cara Mengidentifikasi
Flavonoid. Padmawinata K, penerjemah.
Bandung: ITB. Terjemahan dari: Techniques of Flavonoid of Identification. Molyneux P. 2004. The use of stable free
radical diphenylpicryl-hydrazyl (DPPH) for estimazing antioxidant activity.
Songklanakarin J Sci Technol 26:211-219.
Mulholland DA, Iourine S, Taylor DAH. 1998. Sesquiterpenoids from Dysoxylum schiffnerri. Phytochemistry 47:1421-1422. Putri NE. 2004. Inhibisi fraksi aktif biji
ii
SEBAGAI ANTIOKSIDAN
ZULIA HAJLI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
SIMPULAN DAN SARAN
Simpulan
Rendemen ekstrak etanol 70% biji mahoni sebesar 15.35%. Ekstrak etil asetat memiliki aktivitas antioksidan dengan nilai IC50 sebesar 117.73 mg L-1. Fraksi 3 (Rf 0.85; eluen
metanol-etil asetat 1:1) memiliki aktivitas antioksidan tertinggi dibandingkan dengan ketiga fraksi lainnya dengan IC50 sebesar 65.18 mg L-1. Uji golongan flavonoid pada fraksi 3 menunjukkan flavon atau flavonol. Hasil spektrum inframerah memperlihatkan bahwa senyawa tersebut mempunyai gugus fungsi OH, C=O, C–O dan CH alifatik.
Saran
Perlu dilakukan analisis lebih lanjut dengan menggunakan resonans magnetik inti 1
H, 13C, dan spektrometer massa untuk memastikan struktur senyawa dalam fraksi 3.
DAFTAR PUSTAKA
Amic D, Beslo D, Trinajstic N, Davidovic. 2003. Structure-radical scavenging activity relationships of flavonoids. Croatia Chem Acta 76:55-61.
Cholisoh Z, Utami W. 2008. Aktivitas penangkap radikal ekstrak etanol 70 % biji jengkol (Archidendron jiringa).
Pharmacon 9:33-40.
Dalimartha S. 2007. Atlas Tumbuhan Obat
Indonesia, Jilid 2. Jakarta: Trubus
Agriwidya.
Debasis De, Chatterjee K, Ali KM, Bera TK, Ghosh D. 2010. Antidiabetic potentiality of the aqueous-methanolic extract of seed
of Swietenia mahagoni (L.) Jacq. in
streptozotocin-induced diabetic male albino rat: A correlative and antihyperlipidemic activities. Evidence-Based Complementary and Alternative Med 2011:1-11.
Govindachari TR, Kumari GNK. 1998. Tetranortriterpenoid from Khaya
senegalensis. Phytochemistry
47:1423-1425.
Hanani E, Abdul M, Ryany S. 2005. Identifikasi senyawa antioksidan dalam Callyspongia sp dari Kepulauan Seribu.
Maj Ilmu Kefarmasian 2:127-133.
Harborne JB. 1987. Metode Fitokimia. Padmawinata K, Soediro I, penerjemah; Niksolihin S, editor. Bandung: ITB. Terjemahan dari: Phytochemical Methods. Harjadi W. 1993. Ilmu Kimia Analitik Dasar.
Jakarta: Gramedia Pustaka Utama.
Harnly JM, Doherty RF, Beecher GR, Holden JM,