ISOLASI SENYAWA AKTIF ANTIOKSIDAN DARI
FRAKSI ETIL ASETAT TUMBUHAN PAKU
Nephrolepis falcata (Cav.) C. Chr
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
AGUNG PRIYANTO
NIM. 109102000011
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN PROGRAM STUDI FARMASI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH JAKARTA
Skripsi ini adalah hasil karya sendiri,
dan semua sumber yang dikutip maupun dirujuk
telah saya nyatakan dengan benar. `
Nama : Agung Priyanto
NIM : 109102000011
Tanda Tangan :
Nama : AgungPriyanto
NIM : 109102000011
Program Studi : Farmasi
Judul : Isolasi Senyawa Aktif Antioksidan Dari Fraksi Etil Asetat
Tumbuhan Paku Nephrolepis falcata (Cav.) C. Chr
Menyetujui,
Pembimbing I
Ismiarni Komala, M.Sc., Ph.D., Apt NIP : 197806302006042001
Pembimbing II
Puteri Amelia, M.Farm., Apt NIP : 198012042011012004
Mengetahui,
Kepala Program Studi Farmasi
Fakultas Kedokteran dan Ilmu Kesehatan
Universitas Islam Negeri Syarif Hidayatullah
Skripsi ini diajukan oleh :
Nama : Agung Priyanto
NIM : 109102000011
Program Studi : Farmasi
Judul : Isolasi Senyawa Aktif Antioksidan Dari Fraksi Etil Asetat Tumbuhan Paku Nephrolepis falcata (Cav.) C. Chr.
Telah berhasil dipertahankan di hadapan Dewan Penguji dan diterima sebagai bagian persyaratan yang diperlukan untuk memperoleh gelar Sarjana Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan, Universitas Islam Negeri Syarif Hidayatullah Jakarta
DEWAN PENGUJI
Pembimbing I : Ismiarni komala, M.Sc., Ph.D., Apt ( )
Pembimbing II : Putei Amelia, M.Farm., Apt ( )
Penguji I : Prof. Atiek Soemiati, M.Si., Apt ( )
Penguji II : Eka Putri, M.Si., Apt ( )
Nama : Agung Priyanto
Program studi : Farmasi
Judul :Isolasi Senyawa Aktif Antioksidan dari Fraksi Etil Asetat Tumbuhan Paku Nephrolepis falcata (Cav.) C. Chr.
Tumbuhan paku digunakan secara luas dalam pengobatan tradisional seperti pengobatan inflamasi, infeksi, impotensi dan permasalahan dalam kehamilan. Ekstrak etanol Nephrolepis falcata dilaporkan memiliki aktivitas antioksidan dengan nilai IC5072 µg/mL (Komala, 2012). Studi pendahuluan terhadap aktivitas
antioksidan, menunjukkan bahwa ekstrak n-heksan dan etil asetat dari Nephrolepis falcata aktif dalam menangkap radikal 2,2-diphenyl-1-picrylhydrazyl (DPPH). Studi lebih lanjut dalam mengisolasi komponen kimia dari ekstrak etil asetat, memperoleh senyawa aktif antioksidan, yang diduga sebagai senyawa
β-sitosterol. Struktur kimia di elusidasi dengan menggunakan metode spektroskopi antara lain (FTIR, UV-Visible dan 1H-RMI) dan data yang diperoleh di hubungkan dengan literatur data dari β-sitosterol. β-sitosterol telah diketahui memiliki aktivitas antioksidan dengan nilai IC50 389,5 µM (Baskar, et al., 2010)
Name : Agung Priyanto
Program study : Pharmacy
Title : Isolation of Active Antioxidant Compound from Ethyl Acetate
Fraction of Ferns Nephrolepis falcata (Cav) C. Chr..
Ferns widely used in traditional medicine against inflammation, infection, impotence and problems in pregnancy. Ethanol extract of Nephrolepis falcata was reported to have antioxidant activity with IC50 value31,72 µg/mL (Komala, 2012).
Preliminary study on the antioxidant activity, showed that n-hexane and ethyl acetate extracts of Nephrolepis falcata were active scavenging free radical 2,2-diphenyl-1-picrylhydrazyl (DPPH). Further study on the isolation of the chemical components of the Ethyl acetate extract gave the active antioxidant compound, which was suggested as β-sitosterol. The structure were elucidated by using spectroscopic data such as (FTIR, UV-Visible and 1H-NMR) and the data were compared to the reference data of β-sitosterol. β-sitosterol was known to have antioxidant activity with IC50 value389,5 µM (Baskar, et al., 2010).
Bismillahirahmaanirrahiim
Alhamdulillah, puji syukur kehadirat Allah SWT, karena atas segala
rahmat dan karunia-Nya penulis dapat menyelesaikan penelitian dan
penyusunan skripsi dengan judul “Isolasi Senyawa Aktif Antioksidan Dari Fraksi Etil Asetat Tumbuhan Paku Nephrolepis falcata (Cav.) C. Chr”. Skripsi
ini disusun sebagai salah satu syarat untuk menyelesaikan program pendidikan
tingkat Strata 1 (S1) pada Program Studi Farmasi, Fakultas Kedokteran dan
Ilmu Kesehatan, Universitas Islam Negeri (UIN) Syarif Hidayatulah Jakarta.
Pada kesempatan ini perkenankanlah penulis menyampaikan ucapan
terima kasih yang sebesar-besarnya kepada:
1. Ibu Ismiarni Komala, M.Sc., Ph.D., Apt dan Ibu Puteri Amelia, M.Farm.,
Apt. Selaku pembimbing yang telah memberikan bimbingan, waktu, serta
motivasi kepada penulis selama penelitian.
2. Prof.DR (hc). Dr. M. K Tadjudin, Sp. And. Selaku dekan Fakultas
Kedokteran dan Ilmu Kesehatan, Universitas Islam Negeri (UIN) Syarif
Hidayatulah Jakarta.
3. Drs. Umar Mansur, M.Sc. Selaku ketua Program Studi Farmasi Fakultas
Kedokteran dan Ilmu Kesehatan, Universitas Islam Negeri (UIN) Syarif
Hidayatulah Jakarta.
4. Dosen-dosen, staff, karyawan Program Studi Farmasi Fakultas Kedokteran
dan Ilmu Kesehatan, Universitas Islam Negeri (UIN) Syarif Hidayatulah
Jakarta serta karyawan Perpustakaan Fakultas Kedokteran dan Ilmu
Kesehatan, Universitas Islam Negeri (UIN) Syarif Hidayatulah Jakarta.
5. Kepada Ka Eris, Ka Tiwi, Ka Lisna, Ka Liken Ka Rani, Ka Yopi, Ka
Rahmadi yang telah memberi banyak bantuan kepada penulis selama
penelitian di kampus.
6. Kepada kedua orang tua penulis bapak Jasmo, dan Ibu Sudjinem, kakak
7. Kepada Dyah Mundir Sari yang telah memberikan motivasi, dukungan dan
semangat kepada penulis, sehingga dapat menyelesaikan skripsi ini.
8. Sahabat-sahabat Farmasi angkatan 2009. Muhammad Arif, Gian Pertela
Muchammad Irsyad, Wardah Nabiella, Fauziah Utami, Widya Larasaty
Risda Yulianti, Indah fadlul Maula dan seluruh teman-teman farmasi
angkatan 2009, Terima kasih untuk semangat dan motivasinya.
9. Sahabat-sahabat seperjuangan di laboratorium PHA, Ferry Indar
Ardiansyah, M. Muaffaq Zaki, Siti Zamilatul Azkiyah, Putri Assifa,
Maulida Putri Ahdaini.
10.Serta semua pihak yang tidak dapat disebutkan satu-persatu yang turut
membantu menyelesaikan skripsi.
Penulis menyadari bahwa skripsi ini masih memiliki banyak
kekurangan, oleh karena itu penulis dengan senang hati menerima segala saran
dan kritik.
Semoga kebaikan yang telah diberikan kepada penulis dicatat sebagai
amal ibadah dan dibalas oleh Allah SWT dan penulis berharap semoga
penelitian ini dapat bermanfaat bagi masyarakat dan dalam pengembangan
ilmu pengetahuan. Aamiin.
Ciputat, Juli 2013
Sebagai sivitas akademik Universitas Islam Negeri (UIN) Syarif
Hidayatullah Jakarta, Saya yang bertanda tangan di bawah ini :
Nama : Agung Priyanto
NIM : 109102000011
Program studi : Farmasi
Fakultas : Fakultas Kedokteran dan Ilmu Kesehatan (FKIK)
Jenis Karya : Skripsi
Demi pengembangan ilmu pengetahuan, saya menyetujui skripsi/karya
ilmiah saya dengan judul
ISOLASI SENYAWA AKTIF ANTIOKSIDAN DARI FRAKSI ETIL ASETAT TUMBUHAN PAKU Nephrolepis falcata (Cav.) C. Chr
untuk dipublikasikan atau ditampilkan di internet atau media lain yaitu Digital
Library Perpustakaan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta
untuk kepentingan akademik sebatas sesuai dengan Undang-Undang Hak Cipta.
Dengan demikian persetujuan publikasi karya ilmiah ini saya buat dengan
sebenarnya.
Dibuat di : Ciputat
Pada Tanggal : Juli 2013
Yang menyatakan,
HALAMAN JUDUL ... ii
HALAMAN PERNYATAAN ORISINALITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ... iv
HALAMAN PENGESAHAN ... v
ABSTRAK... vi
ABSTRACT ... vii
KATA PENGANTAR ... viii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... x
DAFTAR ISI ... xi
2.1.2 Penggunaan Tradisional Tumbuhan Paku ... 5
2.2 Nephrolepis falcata (Cav.) C. Chr ... 7
2.2.1 Klasifikasi... 7
2.2.2 Kandungan Kimia dan Aktivitas Biologis ... 7
2.3 Radikal Bebas ... 8
2.3.1 Reaksi Perusakan Radikal Bebas Terhadap Sel ... 9
2.4 Antioksidan ... 9
2.5 Uji Aktivitas Antioksidan Dengan Metode DPPH ... 10
2.6 Ekstrak dan Ekstraksi ... 12
2.6.1 Ekstraksi Cara Dingin ... 13
2.6.2 Ekstraksi Cara Panas ... 14
2.6.3 Macam-macam Teknik Ekstraksi Lain ... 15
2.7 Pelarut... 16
2.8 Vaccum Rotary Evaporator ... 18
2.9 Metode Isolasi ... 19
2.9.1 Kromatografi ... 19
2.9.2 Kromatografi Lapis Tipis ... 20
2.10 Elusidasi Struktur ... 26
2.10.1 UV-Visible ... 26
2.10.2 Spektrofotometri Infra Merah ... 27
2.10.3 Spektrofotometri Massa ... 28
2.10.4 Kromatografi Gas-Spektrofotometri Massa (KG-SM) ... 28
2.10.5 Resonansi Magnetik Inti (RMI) ... 29
2.11 Kerangka Konsep ... 30
BAB 3 METODOLOGI PENELITIAN ... 31
3.1 Lokasi dan Waktu Penelitian ... 31
3.2 ALAT DAN BAHAN ... 31
3.3.1 Pemeriksaan Sampel Tumbuhan ... 32
3.3.2 Penyiapan Simplisia ... 32
3.3.3 Pembuatan Ekstrak ... 32
3.3.4 Kromatografi Lapis Tipis ... 33
3.3.5 Skrining Fitokimia ... 34
3.3.6 Uji Kualitatif Aktivitas Antioksidan Dengan DPPH ... 35
3.3.7 Isolasi Senyawa Aktif Antioksidan Dengan Kromatografi Kolom ... 36
3.3.8 Pemurnian Kristal ... 37
3.3.9 Uji Kualitatif Aktivitas Antioksidan Senyawa Murni ... 37
3.3.10 Uji Kemurnian Senyawa Aktif Antioksidan ... 37
3.3.10.1 Kromatografi Lapis Tipis 2 Dimensi ... 38
3.3.10.2 Uji Titik Leleh ... 38
3.3.10.3 Kromatografi Cair Kinerja Tinggi (KCKT) ... 39
3.3.11 Penentuan Struktur Molekul ... 39
3.3.11.1 UV-Visible ... 39
4.3 Hasil Penapisan Fitokimia ... 41
4.4 Hasil Kromatografi Lapis Tipis (KLT) ... 42
4.5 Hasil Uji Kualitatif Aktivitas Antioksidan Dengan DPPH ... 43
4.6 Hasil Pemisahan Dengan Kromatografi Kolom ... 44
4.8 Penentuan Struktur Molekul Senyawa Fraksi F2.D ... 47
4.8.1 Hasil UV-Visible ... 47
4.8.2 Hasil Spektrofotometri Infra Merah ... 48
4.8.3 Hasil Resonansi Magnetik Inti Proton (1H-RMI) ... 48
BAB 5 KESIMPULAN DAN SARAN ... 53
5.1 Kesimpulan ... 53
5.2 Saran ... 53
Gambar 2.1.Nephrolepis falcata (Cav.) C. Chr ... 7
Gambar 2.2 Struktur molekul senyawa seskuiterpenoid tipe drimane ... 8
Gambar 2.3 Reaksi penghambatan antioksidan primer terhadap radikal lipid ... 10
Gambar 2.4 Reaksi penghambatan antioksidan terhadap radikal DPPH ... 12
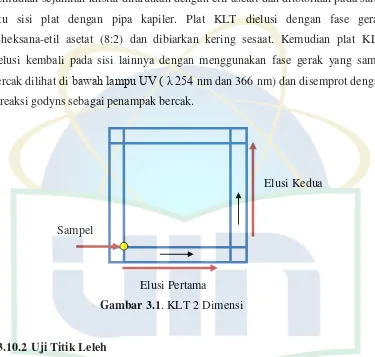
Gambar 3.1 KLT 2 dimensi ... 36
Gambar 4.1 Hasil uji kualitatif antioksidan ekstrak ... 42
Gambar 4.2 Hasil uji kualitatif antioksidan isolat ... 44
Gambar 4.3 Hasil KLT 2 dimensi dari senyawa fraksi F2.D ... 46
Tabel 2.1 Penggunaan Tumbuhan Paku Sebagai Bahan Obat Tradisional ... 6
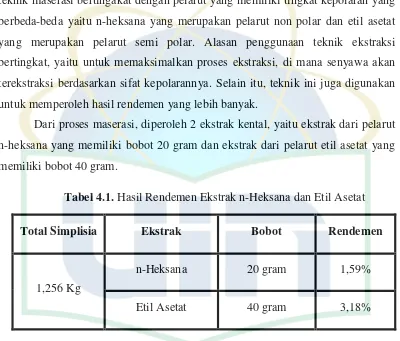
Tabel 4.1 Hasil Rendemen Ekstrak n-Heksana dan Etil Asetat ... 41
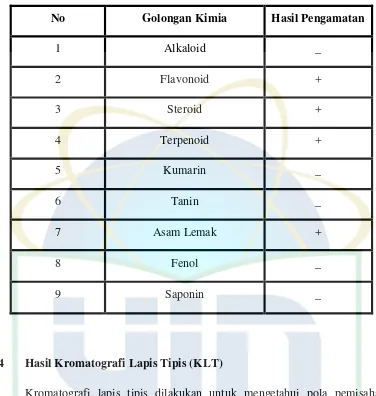
Tabel 4.2 Hasil Penapisan Fitokimia Ekstrak Etil Asetat ... 42
Tabel 4.3 Hasil Isolat Dari Ekstrak Etil Asetat ... 45
Tabel 4.4 Data Geseran Kimia Proton Senyawa Fraksi F2.D yang diukur pada frekuensi 500 MHz dengan pelarut CDCl3 ... 49
Tabel 4.5 Perbandingan Serapan Gugus Fungsi Senyawa Fraksi F2.D Dengan Senyawa β-sitosterol ... 50
Lampiran 1. Hasil determinasi tumbuhan paku Nephrolepis falcata ... 61
Lampiran 2. Bagan alur ekstraksi tumbuhan paku Nephrolepis falcata ... 62
Lampiran 3. Uji kromatografi lapis tipis ekstrak etil asetat dan n-heksana Nephrolepis falcata ... 63
Lampiran 4. Bagan isolasi senyawa aktif antioksidan tumbuhan paku Nephrolepis falcata ... 64
Lampiran 5. Hasil analisis senyawa fraksi F2.D dengan KCKT ... 67
Lampiran 6. Hasil analisis senyawa fraksi F2.D dengan UV-Visible ... 68
Lampiran 7. Hasil Spektrum IR Senyawa Fraksi F2.D ... 69
Lampiran 8. Hasil spektrum 1H-RMI senyawa Fraksi F2.D ... 70
Lampiran 9. Hasil Spektrum 1H-RMI Senyawa F2.D (Diperbesar) ... 71
Lampiran 10. Hasil Spektrum 1H-RMI Senyawa F2.D (Diperbesar) ... 72
Lampiran 11. Hasil Spektrum 1H-RMI Senyawa F2.D (Diperbesar) ... 73
Lampiran 12. Hasil Spektrum 1H-RMI Senyawa F2.D (Diperbesar) ... 74
Lampiran 13. Hasil Spektrum 1H-RMI Senyawa F2.D (Diperbesar) ... 75
Lampiran 14. Hasil Spektrum 1H-RMI Senyawa F2.D (Diperbesar) ... 76
1.1 Latar Belakang
Tumbuhan telah banyak digunakan sebagai bahan obat tradisional
sejak zaman dahulu. Berbagai jenis tumbuhan obat telah digunakan oleh
sekitar 80% dari populasi masyarakat dunia, meskipun dalam kebanyakan
kasus, tidak ada penelitian ilmiah yang telah dilakukan untuk membuktikan
khasiat tumbuhan obat tersebut (Verpoorte, et al., 2006). Setidaknya 80%
dari populasi masyarakat dunia diperkirakan masih akan menggunakan obat
tradisional seperti dalam perawatan kesehatan. Dari 40.000 sampai 70.000
jenis tumbuhan obat, sekitar 20% dari semua spesies adalah tumbuhan
tingkat tinggi (Verpoorte, et al., 2006).
Aktivitas farmakologi dari tumbuhan obat, sering tergantung dari
keberadaan senyawa bioaktif yang disebut metabolit sekunder
(Bruneton, 1999; Heinrich, et al., 2004). Dalam tumbuhan, metabolit
sekunder memiliki fungsi penting sebagai perlindungan terhadap predator,
mikroba patogen atas dasar sifatnya yang beracun, dan perlindungan
terhadap herbivora, mikroba, serta beberapa di antaranya juga terlibat dalam
pertahanan terhadap stres abiotik (misalnya paparan UV-B)
(Schafer, et al., 2009), metabolit sekunder juga penting untuk komunikasi
dari tumbuhan dengan organisme lain (Rosenthal, et al., 1991). Metabolit
sekunder dari tumbuhan yang memiliki aktivitas sebagai obat, dilaporkan
terdiri dari lilin, asam lemak, alkaloid, terpenoid, fenolat, antara lain fenolat
sederhana, flavonoid, glikosida, dan turunannya (Sarker, et al., 2006).
Indonesia adalah negara megabiodiversity yang kaya akan tumbuhan
obat, dan sangat potensial untuk dikembangkan, namun belum dikelola
secara maksimal. Kekayaan alam tumbuhan di Indonesia meliputi 30.000
jenis tumbuhan dari total 40.000 jenis tumbuhan di dunia, 940 jenis
diantaranya merupakan tumbuhan berkhasiat obat. Jumlah ini merupakan
penelitian, dari sekian banyak jenis tumbuhan obat, baru 20-22% yang
dibudidayakan (Pers, 2010). Potensi tumbuhan obat di Indonesia, termasuk
tumbuhan obat kehutanan, apabila dikelola dengan baik akan sangat
bermanfaat dari segi ekonomi, sosial, budaya maupun lingkungan.
Tumbuhan paku merupakan tumbuhan yang distribusinya tersebar
luas di Indonesia dan menjadi salah satu sumber kekayaan alam Indonesia.
Tumbuhan paku sangat mudah tumbuh di Indonesia karena iklim Indonesia
sangat cocok untuk pertumbuhan tumbuhan tersebut. Tumbuhan paku
merupakan tumbuhan yang dikenal pertama kali memiliki sistem pembuluh
sejati. Tumbuhan ini tidak menghasilkan biji dan mereka merupakan
tumbuhan yang paling sederhana diantara tumbuhan yang memiliki sistem
pembuluh sejati (Tracheophytes). Tumbuhan paku distribusinya tersebar
luas di seluruh dunia dan jumlahnya melimpah dalam studi geologi.
Tumbuhan paku tumbuh dengan baik di tempat lembab, dingin dan teduh
serta tersedianya air (Fathima, et al., 2007).
Berdasarkan studi fitokimia, tumbuhan paku telah dilaporkan
mengandung senyawa golongan flavonoid, terpenoid, senyawa fenol dan
xanton (Soeders, 1985). Beberapa tumbuhan paku juga telah dilaporkan
memiliki aktivitas biologis seperti antibakteri, antihelmintik, ekspektoran
dan antioksidan (Lai, 2011).
Antioksidan merupakan senyawa yang dapat mencegah oksidasi dari
molekul lain dengan cara menghalangi inisiasi atau propagasi dari reaksi
oksidasi berantai. Di dalam industri makanan, antioksidan digunakan sejak
lama sebagai bahan aditif untuk melindungi produk makanan dari reaksi
oksidasi yang berhubungan dengan penurunan kualitas makanan seperti
berbau tengik (Lee, et al., 2004).
Telah dilaporkan bahwa antioksidan alami terdapat dalam banyak
tumbuhan yang berfungsi dalam mengurangi kerusakan sel dan membantu
mencegah mutagenesis, karsinogenesis dan penuaan akibat aktivitas radikal
bebas (Lee, et al., 2004). Antioksidan alami telah diisolasi dari berbagai
macam buah-buahan, sayur-sayuran dan tumbuhan obat
Nephrolepis falcata merupakan salah satu tumbuhan paku yang sangat
mudah ditemukan di Indonesia yang banyak digunakan sebagai tanaman
hias. Berdasarkan penelusuran kepustakaan, penelitian mengenai tumbuhan
ini masih sangat sedikit, baik usaha dalam menentukan metabolit sekunder
maupun dalam penggunaannya sebagai bahan obat. Tetapi spesies lain dari
genus Nephrolepis, yaitu Nephrolepis radicans dilaporkan memiliki
aktivitas antioksidan (Dayanti & Suyatno, 2012), dan Nephrolepis bisserata
dilaporkan memiliki aktivitas sebagai antioksidan dengan nilai
lC50 0,53 mg/mL (Lai, 2011).
Dalam penelitian sebelumnya yang dilakukan oleh (Komala, 2012),
telah dilaporkan bahwa ekstrak etanol 70% dari tumbuhan
Nephrolepis falcata yang diambil dari wilayah kampus UIN Syarif
Hidayatullah Jakarta memiliki aktivitas antioksidan dengan nilai lC50 31,72
µg/mL. Untuk mengetahui jenis metabolit sekunder dalam tumbuhan ini
yang memberikan aktivitas antioksidan, maka dilakukan penelitian lebih
lanjut dalam mengisolasi kandungan metabolit sekunder dari tumbuhan
Nephrolepis falcata yang memiliki aktivitas antioksidan.
1.2 Rumusan Masalah
Berdasarkan penelusuran pustaka, belum diketahuinya senyawa yang
memberikan aktivitas antioksidan dalam tumbuhan paku
Nephrolepis falcata (cav,) C.Chr.
1.3 Tujuan Penelitian
a. Mengetahui senyawa aktif antioksidan dari fraksi etil asetat tumbuhan paku Nephrolepis falcata.
b. Menentukan struktur kimia dari senyawa murni hasil isolasi yang diduga memiliki aktivitas antioksidan dari tumbuhan paku
Nephrolepis falcata.
1.4 Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi kepada
masyarakat mengenai khasiat dari tumbuhan Nephrolepis falcata, sehingga
dapat digunakan sebagai bahan obat tradisional. Penelitian ini juga
diharapkan memberikan kontribusi bagi perkembangan ilmu pengetahuan
dengan memberikan informasi terhadap aktivitas antioksidan tumbuhan
Nephrolepis falcata. Mengingat tumbuhan ini belum pernah diteliti
sebelumnya, diharapkan ditemukan senyawa baru yang nantinya mungkin
didapatkan yang akan memperkaya pengetahuan dalam bidang kimia bahan
BAB 2
TINJAUAN PUSTAKA
2.1 Tumbuhan Paku
Secara taksonomi tumbuhan paku berada diantara tumbuhan tingkat tinggi
(gymnosperma dan angiosperma) dan tumbuhan lumut (bryophyta). Berbeda
dengan alga dan lumut, tumbuhan paku telah memiliki jaringan pengangkut
seperti xilem dan floem tetapi tidak menghasilkan biji untuk reproduksi
seksualnya (Pooja, 2004).
2.1.1 Habitat Tumbuhan Paku
Habitat tumbuhan paku terdiri dari kondisi iklim yang rendah dengan lokasi
khusus pada tempat-tempat lembab dan teduh. Gangguan kecil terhadap kondisi
iklim tempat tumbuh mereka, dapat menyebabkan hilangnya sejumlah besar
spesies.
Tumbuhan paku terdapat dalam jumlah besar di hutan tropis, subtropis,
temperatur dan kelembaban yang rendah dan siklus hidup mereka didasarkan pada
keberadaan hutan (Dudani, et al., 2010).
2.1.2 Penggunaan Tradisional Tumbuhan Paku
Tumbuhan paku telah banyak digunakan sebagai bahan obat tradisional di
beberapa negara, seperti di kepulauan Hawaii yang menggunakan tumbuhan paku
dari spesies Nephrolepis sebagai bahan obat dalam penyembuhan beberapa
penyakit, diantaranya penyakit diabetes, infeksi yang disebabkan jamur ataupun
bakteri. Selanjutnya tumbuhan paku spesies Nephrolepis tuberosa yang secara
tradisional digunakan untuk menurunkan demam. Bagian daun dari tanaman ini
digunakan untuk mengobati perdarahan pada luka dan akar dari tanaman ini
digunakan dalam mengobati infeksi serta sebagai obat batuk
(Ja & Sharma, 2012)
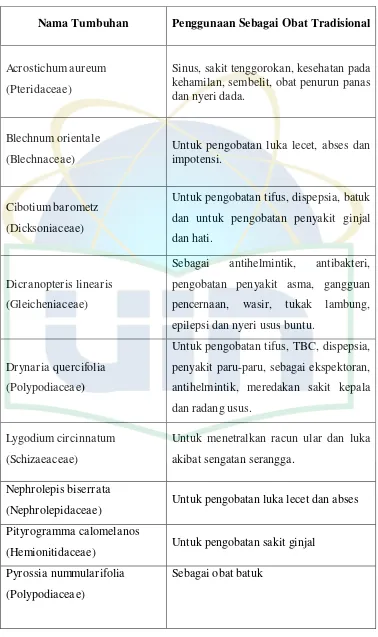
Beberapa tumbuhan paku yang digunakan sebagai bahan obat tradisional
Tabel 2.1. Penggunaan Tumbuhan Paku Sebagai Bahan Obat Tradisional.
Nama Tumbuhan Penggunaan Sebagai Obat Tradisional
Acrostichum aureum
dan untuk pengobatan penyakit ginjal
dan hati.
Dicranopteris linearis
(Gleicheniaceae)
Sebagai antihelmintik, antibakteri,
pengobatan penyakit asma, gangguan
pencernaan, wasir, tukak lambung,
epilepsi dan nyeri usus buntu.
Drynaria quercifolia
(Polypodiaceae)
Untuk pengobatan tifus, TBC, dispepsia,
penyakit paru-paru, sebagai ekspektoran,
antihelmintik, meredakan sakit kepala
dan radang usus.
(Nephrolepidaceae) Untuk pengobatan luka lecet dan abses
Pityrogramma calomelanos
(Hemionitidaceae) Untuk pengobatan sakit ginjal
Pyrossia nummularifolia
(Polypodiaceae)
2.2 Nephrolepis falcata (Cav.) C.Chr
Gambar 2.1. Nephrolepis falcata (Cav.) C.Chr (Sumber: Koleksi Pribadi, Februari 2013)
2.2.1 Klasifikasi
Kingdom : Plantae
Divisio : Pteridophyta
Class : Polypodiopsida = Filicopsida
Order : Polypodiales
Family : Davalliaceae
Genus : Nephrolepis
Species : Nephrolepis falcata (Cav.) C.Chr.
2.2.2 Kandugan Kimia dan Aktivitas Biologis
Belum ada penelitian sebelumnya yang mempublikasikan mengenai
kandungan kimia dari Nephrolepis falcata. Tetapi spesies lain dari genus
Nephrolepis yaitu Nephrolepis biserrata diketahui bahwa tumbuhan ini
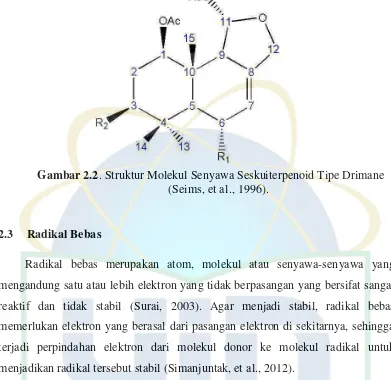
mengandung senyawa seskuiterpenoid tipe drimane (Seims, et al., 1996), dan
dilaporkan bahwa tumbuhan ini memiliki aktivitas sebagai antioksidan
(Lai, et al., 2011). Aktivitas biologis Nephrolepis falcata dilaporkan, bahwa
ekstrak etanol 70% dari tumbuhan tersebut memiliki aktivitas sebagai antioksidan
dengan nilai IC50 31,72 µg/mL (Komala, 2012).
Gambar 2.2. Struktur Molekul Senyawa Seskuiterpenoid Tipe Drimane (Seims, et al., 1996).
2.3 Radikal Bebas
Radikal bebas merupakan atom, molekul atau senyawa-senyawa yang
mengandung satu atau lebih elektron yang tidak berpasangan yang bersifat sangat
reaktif dan tidak stabil (Surai, 2003). Agar menjadi stabil, radikal bebas
memerlukan elektron yang berasal dari pasangan elektron di sekitarnya, sehingga
terjadi perpindahan elektron dari molekul donor ke molekul radikal untuk
menjadikan radikal tersebut stabil (Simanjuntak, et al., 2012).
Senyawa radikal yang terdapat dalam tubuh (prooksidan) dapat berasal dari
luar tubuh (eksogen) atau terbentuk di dalam tubuh (endogen) dari hasil
metabolisme zat gizi secara normal (Muchtadi, 2000). Secara eksogen, senyawa
radikal antara lain berasal dari polutan, makanan atau minuman, radiasi, ozon dan
pestisida (Supari, 1996). Sedangkan secara endogen, senyawa radikal dapat timbul
melalui beberapa macam mekanisme seperti autooksidasi, aktivitas oksidasi dan
sistem transpor elektron.
Radikal bebas dapat menyebabkan kerusakan pada sel dengan cara
mengoksidasi DNA, sehingga DNA mengalami mutasi dan dapat menyebabkan
penyakit degeneratif (Wang, et al., 2002), senyawa radikal bebas juga dapat
menyebabkan kerusakan pada jaringan tubuh sehingga terjadi proses penuaan dan
2.3.1 Reaksi Perusakan Radikal Bebas Terhadap Sel a. Peroksidasi Lemak
Membran sel kaya akan sumber poly unsaturated fatty acid (PUFA),
yang mudah dirusak oleh bahan-bahan pengoksidasi; proses tersebut
dinamakan peroksidasi lemak. Hal ini sangat merusak, karena merupakan
suatu proses berkelanjutan. Pemecahan hidroperoksida lemak sering
melibatkan katalisis ion logam transisi (Droge, 2002).
b. Kerusakan Protein
Protein dan asam nukleat lebih tahan terhadap radikal bebas daripada
PUFA, sehingga kecil kemungkinan terjadinya reaksi berantai yang cepat.
Serangan radikal bebas terhadap protein sangat jarang kecuali bila sangat
ekstensif. Hal ini terjadi hanya jika radikal tersebut mampu berakumulasi
(jarang pada sel normal), atau bila kerusakannya terfokus pada daerah
tertentu dalam protein. Salah satu penyebab kerusakan terfokus adalah jika
protein berikatan dengan ion logam transisi (Droge, 2002).
c. Kerusakan DNA
Seperti pada protein, kecil kemungkinan terjadinya kerusakan pada
DNA menjadi suatu reaksi berantai, biasanya kerusakan terjadi bila ada
lesi pada susunan molekul, apabila tidak dapat diatasi, dan terjadi sebelum
replikasi, maka akan terjadi mutasi. Radikal oksigen dapat menyerang
DNA jika terbentuk disekitar DNA seperti pada radiasi biologis
(Allen, et al., 2000).
2.4 Antioksidan
Antioksidan adalah zat yang dapat melawan pengaruh bahaya dari radikal
bebas atau Reactive Oxygen Species (ROS) yang terbentuk sebagai hasil dari
metabolisme oksidatif, yaitu hasil dari reaksi-reaksi kimia dan proses metabolik
sebagai penangkap radikal bebas, membentuk kompleks dengan logam-logam
peroksida dan berfungsi sebagai senyawa pereduksi (Andlauer, et al., 1989) .
Antioksidan dapat menangkap radikal bebas sehingga dapat menghambat
mekanisme oksidatif yang merupakan penyebab penyakit-penyakit degeneratif
seperti penyakit jantung, kanker, katarak, disfungsi otak dan artritis
(Miller, et al., 2000). Mekanisme kerja antioksidan memiliki dua fungsi, fungsi
pertama yaitu merupakan fungsi utama dari antioksidan yaitu sebagai pemberi
atom hidrogen. Antioksidan yang mempunyai fungsi utama tersebut sering disebut
sebagai antioksidan primer.
Antioksidan tersebut dapat memberikan atom hidrogen secara cepat ke
radikal lipida (R*,ROO*) atau mengubahnya ke bentuk lebih stabil, sementara
turunan radikal antioksidan (A*) tersebut memiliki keadaan lebih stabil
dibandingkan radikal lipida. Fungsi kedua merupakan mekanisme fungsi sekunder
antioksidan, yaitu memperlambat laju autooksidasi dengan berbagai mekanisme
diluar mekanisme pemutusan rantai autooksidasi dengan pengubahan radikal
lipida ke bentuk lebih stabil (Gordon, 1990).
Inisiasi : R* + AH RH + A*
Radikal lipid
Propagasi : ROO* + AH RH + A*
Gambar 2.3. Reaksi Penghambatan Antioksidan Primer Terhadap Radikal Lipid (Gordon, 1990).
2.5 Uji Aktivitas Antioksidan Dengan Metode DPPH
Metode DPPH merupakan salah satu metode untuk menentukan aktivitas
antioksidan yang sederhana dengan menggunakan 2,2-diphenyl-1-picrylhydrazyl
(DPPH) sebagai senyawa pendeteksi (Surai, 2003). DPPH
dengan atom hidrogen yang berasal dari suatu antioksidan membentuk DPPH
tereduksi (Surai, 2003).
Metode DPPH (2,2-diphenyl-1-picrylhydrazyl) digunakan secara luas untuk
menguji kemampuan senyawa yang berperan sebagai pendonor elektron atau atom
hidrogen. Metode DPPH merupakan metode yang dapat mengukur aktivitas total
antioksidan baik dalam pelarut polar maupun nonpolar. Beberapa metode lain
terbatas mengukur komponen yang larut dalam pelarut yang digunakan dalam
analisa. Metode DPPH mengukur semua komponen antioksidan, baik yang larut
dalam lemak maupun dalam air (Prakash, 2001).
Metode DPPH merupakan metode yang sederhana, mudah, cepat dan peka,
serta hanya memerlukan sedikit sampel. DPPH adalah senyawa radikal bebas
stabil kelompok nitrit oksida. Senyawa ini mempunyai ciri-ciri padatan berwarna
ungu kehitaman, larut dalam pelarut DMF atau etanol/metanol, dengan rumus
molekul C18H12N5O6 (Prakash, 2001).
Radikal bebas DPPH yang memiliki elektron tidak berpasangan memberikan
warna ungu dan menghasilkan absorbansi maksimum pada panjang gelombang
517 nm. Warna akan berubah menjadi kuning saat elektronnya berpasangan.
Pengurangan intensitas warna yang terjadi berhubungan dengan jumlah elektron
DPPH yang menangkap atom hidrogen. Sehingga pengurangan intensitas warna
mengindikasikan peningkatan kemampuan antioksidan untuk menangkap radikal
bebas (Prakash, 2001).
Aktivitas antioksidan dapat dinyatakan dengan satuan persen aktivitas. Nilai
ini diperoleh dengan rumus sebagai berikut (Molyneux, 2003).
% Inhibisi = X 100%
Absorbansi kontrol yang digunakan dalam prosedur DPPH ini adalah absorbansi
DPPH, sedangkan blanko yang digunakan adalah etanol 95%. Berdasarkan rumus
tersebut, semakin tinggi tingkat diskolorisasi (absorbansi semakin kecil) maka
semakin tinggi nilai aktivitas penangkapan radikal bebas (Molyneux, 2003). absorbansi kontrol – absorbansi sampel
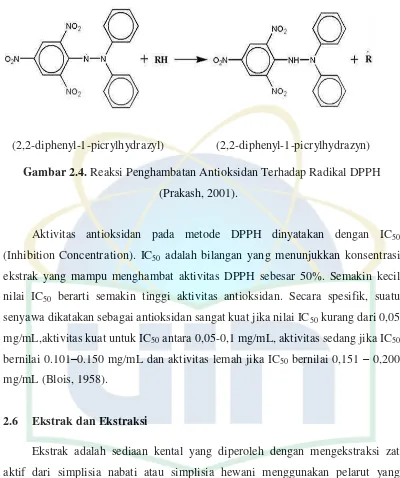
(2,2-diphenyl-1-picrylhydrazyl) (2,2-diphenyl-1-picrylhydrazyn)
Gambar 2.4. Reaksi Penghambatan Antioksidan Terhadap Radikal DPPH (Prakash, 2001).
Aktivitas antioksidan pada metode DPPH dinyatakan dengan IC50
(Inhibition Concentration). IC50 adalah bilangan yang menunjukkan konsentrasi
ekstrak yang mampu menghambat aktivitas DPPH sebesar 50%. Semakin kecil
nilai IC50 berarti semakin tinggi aktivitas antioksidan. Secara spesifik, suatu
senyawa dikatakan sebagai antioksidan sangat kuat jika nilai IC50 kurang dari 0,05
mg/mL,aktivitas kuat untuk IC50 antara 0,05-0,1 mg/mL, aktivitas sedang jika IC50
bernilai 0.101–0.150 mg/mL dan aktivitas lemah jika IC50 bernilai 0,151 – 0,200
mg/mL (Blois, 1958).
2.6 Ekstrak dan Ekstraksi
Ekstrak adalah sediaan kental yang diperoleh dengan mengekstraksi zat
aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang
sesuai, kemudian semua atau hampir semua pelarut dan massa atau serbuk yang
tersisa, diperlakukan sehingga memenuhi baku yang telah ditetapakan
(Soesilo, 1995). Ekstrak adalah sediaan kering, kental atau cair, dibuat dengan
menyari simplisia nabati atau hewani menurut cara yang sesuai diluar pengaruh
Parameter yang mempengaruhi kualitas dari ekstrak adalah (Tiwari, et al., 2011):
a) Bagian dari tumbuhan yang digunakan.
b) Pelarut yang digunakan untuk ekstraksi.
c) Prosedur ekstraksi
Selama proses ekstraksi, pelarut akan berdifusi sampai ke material padat dari
tumbuhan dan akan melarutkan senyawa dengan polaritas yang sesuai dengan
pelarutnya. Efektivitas ekstraksi senyawa kimia dari tumbuhan bergantung pada.
a) Bahan-bahan tumbuhan yang diperoleh
b) Keaslian dari tumbuhan yang digunakan
c) Proses ekstraksi
d) Ukuran partikel
Macam-macam perbedaan metode ekstraksi yang akan mempengaruhi
kuantitas dan kandungan metabolit sekunder dari ekstrak, antara lain :
a) Tipe ekstraksi
b) Waktu ekstraksi
c) Suhu ekstraksi
d) Konsentrasi pelarut
e) Polaritas pelarut
Beberapa metode ekstraksi dengan menggunakan pelarut dibagi menjadi dua
cara, yaitu cara panas dan cara dingin (Ditjen POM, 2000).
2.6.1 Ekstraksi Cara Dingin a) Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan
pelarut dengan beberapa kali pengocokan atau pengadukan pada
temperatur kamar (Ditjen POM, 2000). Keuntungan ekstraksi dengan cara
maserasi adalah pengerjaan dan peralatan yang digunakan sederhana,
sedangkan kerugiannya yakni cara pengerjaannya lama, membutuhkan
pelarut yang banyak dan penyarian kurang sempurna. Dalam maserasi,
serbuk halus atau kasar dari tumbuhan obat yang kontak dengan pelarut
yang sering, sampai zat tertentu dapat terlarut. Metode ini paling cocok
digunakan untuk senyawa yang termolabil (Tiwari, et al., 2011).
b) Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
penyarian sempurna (exhaustive extraction) yang umumnya dilakukan
pada temperatur ruang. Proses terdiri dari tahapan pengembangan bahan,
tahap maserasi antara, tahap perkolasi sebenarnya
(penetesan/penampungan ekstrak), terus sampai diperoleh ekstrak
(perkolat) yang jumlahnya 1-5 kali dari bahan (Ditjen POM, 2000).
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
terjadi penyarian sempurna yang umumnya dilakukan pada temperatur
kamar. Proses perkolasi terdiri dari tahap pengembangan bahan, tahap
perendaman, tahap perkolasi antara, tahap perkolasi sebenarnya
(penampungan ekstrak) secara terus menerus sampai diperoleh ekstrak
(perkolat). Untuk menentukan akhir dari pada perkolasi dapat dilakukan
pemeriksaan zat secara kualitatif pada perkolat akhir. Ini adalah prosedur
yang paling sering digunakan untuk mengekstrak bahan aktif dalam
penyusunan tincture dan ekstrak cairan (Tiwari, et al., 2011).
2.6.2 Ekstraksi Cara Panas a) Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru,
dengan menggunakan alat soklet sehingga terjadi ekstraksi kontinyu
dengan jumlah pelarut relatif konstan dengan adanya pendingin balik
(Ditjen POM, 2000).
b) Refluks
Refluks adalah ekstraksi dengan menggunakan pelarut pada
temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut
terbatas yang relatif konstan dengan adanya pendingin balik
c) Infusa
Infusa adalah ekstraksi menggunakan pelarut air pada temperatur
penangas air dimana bejana infus tercelup dalam penangas air mendidih,
temperatur yang digunakan (96-980C) selama waktu tertentu (15-20 menit) (Ditjen POM, 2000). Cara ini menghasilkan larutan encer dari komponen
yang mudah larut dari simplisia (Tiwari, et al., 2011).
d) Dekok
Dekok adalah infus pada waktu yang lebih lama (≥300C) dan temperatur sampai titik didih air (Ditjen POM, 2000). Dekok adalah
ekstraksi dengan pelarut air pada temperatur 90oC selama 30 menit. Metode ini digunakan untuk ekstraksi konstituen yang larut dalam air dan
konstituen yang stabil terhadap panas (Tiwari, et al., 2011).
e) Digesti
Digesti adalah maserasi kinetik pada temperatur lebih tinggi dari
temperatur suhu kamar, yaitu secara umum dilakukan pada temperatur
40-50oC (Ditjen POM, 2000).
Digesti adalah maserasi dengan pengadukan kontinyu pada temperatur
lebih tinggi dari temperatur ruang (umumnya 25-30oC). Ini adalah jenis ekstraksi maserasi di mana suhu sedang digunakan selama proses ekstraksi
(Tiwari, et al., 2011).
2.6.3 Macam-macam Teknik Ekstraksi Lain 1) Sonikasi
Prosedur ekstraksi ini melibatkan penggunaan gelombang ultrasonik
dengan frekuensi mulai dari 20 kHz sampai 2000 kHz. Teknik ini
meningkatkan permeabilitas dinding sel dan menghasilkan kavitasi.
Meskipun proses ini berguna dalam beberapa kasus, tetapi pada skala
besar aplikasinya terbatas karena biayanya yang tinggi. Satu kelemahan
dari 20 KHz) yang menyebabkan konstituen tanaman membentuk radikal
bebas yang tidak diharapkan (Tiwari, et al., 2011).
2) Supercritical Fluid
Teknik ekstraksi supercritical fluid memberikan fakta bahwa gas
dapat berperilaku sebagai cairan ketika berada dibawah tekanan. Salah
satu contohnya adalah karbon dioksida yang dapat digunakan untuk
mengekstrak biomassa dan memiliki keuntungan bahwa setelah tekanan
dihilangkan, molekul gas akan meninggalkan ekstrak. Karbon dioksida
bertindak sebagai pelarut non polar, tetapi polaritas ekstraksi dengan
supercritical fluid dapat ditingkatkan dengan menambahkan agen tertentu,
yang biasanya berupa pelarut lain seperti metanol atau diklormetan
(Heinrich, 2004).
2.7 Pelarut
Pelarut adalah zat yang digunakan sebagai media untuk melarutkan zat lain.
kesuksesan penentuan senyawa biologis aktif dari bahan tumbuhan sangat
tergantung pada jenis pelarut yang digunakan dalam prosedur ekstraksi
(Ncube, et al., 2008). Sifat pelarut yang baik untuk ekstraksi yaitu toksisitas dari
pelarut yang rendah, mudah menguap pada suhu yang rendah, dapat
mengekstraksi komponen senyawa dengan cepat, dapat mengawetkan dan tidak
menyebabkan ekstrak terdisosiasi (Tiwari, et al., 2011).
Pemilihan pelarut juga akan tergantung pada senyawa yang ditargetkan.
Faktor-faktor yang mempengaruhi pemilihan pelarut adalah jumlah senyawa yang
akan diekstraksi, laju ekstraksi, keragaman senyawa yang akan diekstraksi,
kemudahan dalam penanganan ekstrak untuk perlakuan berikutnya, toksisitas
Berbagai pelarut yang digunakan dalam prosedur ekstraksi antara lain:
1) Air
Air adalah pelarut universal, biasanya digunakan untuk mengekstraksi
produk tumbuhan dengan aktivitas antimikroba. Meskipun pengobatan
secara tradisional menggunakan air sebagai pelarut, tetapi ekstrak tumbuhan
dari pelarut organik telah ditemukan untuk memberikan aktivitas
antimikroba lebih konsisten dibandingkan dengan ekstrak air
(Tiwari, et al., 2011).
Air juga melarutkan flavonoid (kebanyakan antosianin) yang tidak
memiliki aktivitas signifikan terhadap antimikroba dan senyawa fenolat
yang larut dalam air yang mempunyai aktivitas sebagai antioksidan.
2) Aseton
Aseton melarutkan beberapa komponen senyawa hidrofilik dan lipofilik
dari tumbuhan. Keuntungan pelarut aseton yaitu dapat bercampur dengan
air, mudah menguap dan memiliki toksisitas rendah. Aseton digunakan
terutama untuk studi antimikroba (Tiwari, et al., 2011).
3) Alkohol
Aktivitas antioksidan yang lebih tinggi dari ekstrak etanol dibandingkan
dengan ekstrak air dapat dikaitkan dengan adanya jumlah polifenol yang
lebih tinggi pada ekstrak etanol dibandingkan dengan ekstrak air.
Konsentrasi yang lebih tinggi dari senyawa flavonoid terdeteksi dengan
etanol 70% karena polaritas yang lebih tinggi daripada etanol murni
(Tiwari, et al., 2011).
Etanol lebih mudah untuk menembus membran sel untuk mengekstrak
bahan intraseluler dari bahan tumbuhan. Metanol lebih polar dibanding
etanol namun karena sifatnya yang toksik, sehingga tidak cocok digunakan
4) Kloroform
Terpenoid lakton telah diperoleh dengan ekstraksi berturut-turut
menggunakan n-heksana, kloroform dan metanol dengan konsentrasi
aktivitas tertinggi terdapat dalam fraksi kloroform. Kadang-kadang tanin
dan terpenoid ditemukan dalam fase air, tetapi lebih sering diperoleh dengan
pelarut semipolar (Tiwari, et al., 2011).
5) Eter
Eter umumnya digunakan secara selektif untuk ekstraksi kumarin dan
asam lemak (Tiwari, et al., 2011).
6) n-Heksana
n-Heksana mempunyai karakteristik sangat tidak polar, volatil,
mempunyai bau khas yang dapat menyebabkan pingsan. Berat molekul
n-heksana adalah 86,2 gram/mol dengan titik leleh 94,3°C sampai 95,3°C.
Titik didih n-heksana pada tekanan 760 mmHg adalah 66°C sampai 71°C
(Daintith, 1994). n-Heksana biasanya digunakan sebagai pelarut untuk
ekstraksi minyak nabati.
7) Etil Asetat
Etil asetat merupakan pelarut dengan karakteristik semipolar. Etil asetat
secara selektif akan menarik senyawa yang bersifat semipolar seperti fenol
dan terpenoid.
2.8 Vacuum Rotary Evaporator
Vacuum rotary evaporator adalah alat yang berfungsi untuk memisahkan
suatu larutan dari pelarutnya sehingga dihasilkan ekstrak dengan kandungan kimia
tertentu sesuai yang diinginkan. Cairan yang ingin diuapkan biasanya ditempatkan
dalam suatu labu yang kemudian dipanaskan dengan bantuan penangas dan
diputar. Uap cairan yang dihasilkan didinginkan oleh suatu pendingin (kondensor)
akan dihasilkan ekstrak yang dapat berbentuk padatan atau cairan
(Nugroho, et al., 1999).
Kelebihan dari alat ini adalah diperolehnya kembali pelarut yang diuapkan.
Penggunaan vacuum rotary evaporator meningkatkan presentase plarut yang
terevaporasi dibandingkan dengan menggunakan waterbath
(Mutairi & Jasser, 2012). Prinsip kerja alat ini didasarkan pada titik didih pelarut
dan adanya tekanan yang menyebabkan uap dari pelarut terkumpul, serta adanya
kondensor yang menyebabkan uap ini mengembun dan akhirnya jatuh ke tabung
penerima (receiver flask).
2.9 Metode Isolasi
Suatu ekstrak yang telah dihasilkan dari suatu protokol ekstraksi yang sesuai
dan pengujian aktivitas biologis telah dilakukan (contohnya aktivitas antibakteri),
langkah selanjutnya adalah fraksinasi ekstrak menggunakan metode pemisahan
sehingga komponen biologis aktif dapat diisolasi (Heinrich, et al., 2004).
Pemisahan dan pemurnian kandungan tumbuhan terutama dilakukan dengan
menggunakan salah satu dari keempat teknik kromatografi atau gabungan teknik
tersebut. Keempat teknik kromatografi itu adalah: kromatografi kertas (KKt),
kromatografi lapis tipis (KLT). Kromatografi gas cair (KGC), dan kromatografi
cair kinerja tinggi (KCKT) (Harborne, 1987).
2.9.1 Kromatografi
Kromatografi merupakan metode pemisahan fisikokimia untuk memisahkan
campuran senyawa berdasarkan perbedaan waktu huni komponen campuran
dalam sistem fase diam dan fase gerak (Hostettman, et al., 1995). Prinsip
pemisahan dari kromatografi adanya distribusi komponen-komponen dalam fase
diam dan fase gerak berdasarkan sifat fisik komponen yang akan dipisahkan. Pada
dasarnya semua cara kromatografi menggunakan dua fase, yaitu fase diam
(stationer) dan fase gerak (mobile).
Menurut (Adrianingsih, 2009), persyaratan utama kromatografi antara lain:
2. Komponen sampel harus larut dalam fase gerak dan berinteraksi dengan fase diam.
3. Fase gerak harus bisa mengalir melewati fase diam, sedangkan fase diam harus terikat kuat di posisinya.
2.9.2 Kromatografi Lapis Tipis
Kromatografi lapis tipis (KLT) merupakan salah satu metode pilihan
kromatografi secara fisikokimia (Gandjar & Rohman, 2007). KLT merupakan
bentuk kromatografi planar, selain kromatografi kertas dan elektroforesis. Pada
KLT fase diamnya berupa lapisan yang seragam (uniform) pada permukaan
bidang datar yang didukung oleh lempeng kaca, pelat alumunium atau plat plastik.
Meskipun demikian, kromatografi planar ini merupakan bentuk terbuka dari
kromatografi kolom (Gritter, et al., 1991).
KLT dapat dipakai dengan dua tujuan. Pertama, dipakai untuk mencapai
hasil kualitatif, kuantitatif atau preparatif. Kedua dipakai untuk menjajaki sistem
pelarut dan sistem penyangga yang akan dipakai dalam kromatografi kolom
(Gritter, et al., 1991).
Kromatografi lapis tipis (KLT) dapat digunakan untuk tujuan analitik dan
preparatif. KLT analitik digunakan untuk menganalisa senyawa-senyawa organik
dalam jumlah kecil, misalnya menentukan jumlah komponen dalam campuran dan
menentukan pelarut yang tepat untuk pemisahan dengan KLT preparatif.
Sedangkan KLT preparatif digunakan untuk memisahkan campuran senyawa dari
sampel dalam jumlah besar berdasarkan fraksinya, yang selanjutnya fraksi-fraksi
tersebut dikumpulkan dan digunakan untuk analisa berikutnya
(Townshend, 1995).
Plat KLT yang umum digunakan adalah plat KLT analitik dengan ketebalan
0,1-0,2 mm dengan ukuran 20x20 cm yang dilapisi dengan adsorben silika gel 60
F254 dengan ketebalan 0,2 mm. Plat kemudian ditempatkan ke dalam bejana
dengan fase gerak yang sesuai, dimana ketinggian fase gerak cukup untuk
membasahi bagian bawah plat dan tidak sampai membasahi dimana sampel
diaplikasikan. Fase gerak kemudian bermigrasi melewati adsorben dengan gaya
KLT merupakan teknik yang benar-benar menguntungkan karena tingkat
sensitivitasnya sangat besar dengan jumlah sampel lebih sedikit
(Brain & Turner, 1975). Fase gerak yang dikenal sebagai pelarut pengembang
atau cairan pengelusi, akan bergerak sepanjang fase diam karena pengaruh kapiler
pada pengembangan secara menaik (ascending), atau karena pengaruh gravitasi
pada pengembangan secara menurun (descending) (Gritter, et al., 1991).
Jumlah volume fase gerak harus mampu mengelusi lempeng sampai
ketinggian lempeng yang telah ditentukan. Setelah lempeng terelusi, dilakukan
deteksi bercak (Gandjar & Rohman, 2007). Laju pergerakan fase gerak terhadap
fase diam dihitung sebagai retardation farctor (Rf). Nilai Rf diperoleh dengan
membandingkan jarak yang ditempuh oleh zat terlarut dengan jarak yang
ditempuh oleh fase gerak (Gandjar & Rohman, 2007).
Fase gerak harus memiliki kemurnian yang tinggi. Hal ini dikarenakan KLT
merupakan teknik yang sensitif. Fase gerak yang digunakan adalah pelarut
organik yang memiliki tingkat polaritas tersendiri, melarutkan senyawa contoh,
dan tidak bereaksi dengan penjerap (Gritter, et al., 1991). Adsorben umumnya
digunakan dalam KLT meliputi partikel silika gel ukuran 12 µm, alumina, mineral
oksida, selulosa, poliamida, polimer penukar ion (Gocan, 2002).
a) Silika Gel
Silika gel adalah yang paling banyak digunakan sebagai adsorben dan
fase stasioner yang dominan untuk KLT. Sebagian besar analisa dengan
KLT dilakukan dengan menggunakan fase normal lapisan silika gel.
Fase diam ini dapat digunakan sebagai fase polar maupun non polar.
Untuk fase polar, merupakan silika yang dibebaskan dari air dan bersifat
sedikit asam. Silika gel perlu ditambah gips (kalsium sulfat) untuk
memperkuat pelapisannya pada pendukung. Sebagai pendukung biasanya
lapisan tipis digunakan kaca dengan ukuran 20x20 cm, 10x20 cm, atau
5x10 cm. Pendukung yang lain berupa lembaran alumunium atau plastik
seperti ukuran di atas yang umumnya dibuat oleh pabrik.
Silika gel kadang-kadang ditambah senyawa fluoresensi, agar bila
dikenal dengan silika gel 60 F254 yang berarti silika gel dengan fluoresen
yang berpendar pada panjang gelombang 254 nm. Silika gel untuk fase non
polar terbuat dari silika yang dilapisi dengan senyawa non polar misalnya,
lemak, parafin, minyak silikon, raber gom, atau lilin, dengan fase gerak air
yang bersifat polar dapat digunakan sebagai eluen. Fase diam ini dapat
memisahkan banyak senyawa namun elusinya sangat lambat dan
keterulangannya kurang bagus (Sumarno,2001).
b) Alumina
Alumina merupakan adsorben yang paling banyak digunakan dalam
KLT (Gocan, 2002). Fase diam ini bersifat sedikit basa, lebih jarang
digunakan. Saat akan digunakan harus diaktifkan kembali dengan
pemanasan. Alumina yang digunakan sebagai fase diam untuk KLT
umumnya yang bebas air, sehingga mempunyai aktivitas penjerapan lebih
tinggi (Sumarno, 2001).
Fase diam ini sebenarnya merupakan asam silika yang berbentuk amorf,
berasal dari kerangka diatomae, maka lebih dikenal dengan nama tanah
diatomae, kurang bersifat adsorptif dibanding silika (Sumarno, 2001).
e) Magnesium Silikat
Fase diam ini hanya digunakan bila adsorben atau penjerap lain tidak
dapat digunakan. Nama lain dalam perdagangan dikenal dengan floresil
(Sumarno, 2001). Floresil (magnesium silikat) adalah endapan silika dan
magnesium. Sifat dan aplikasi dari floresil pada KLT dan KCKT ditinjau
f) Selulosa
Polaritasnya tinggi sehingga dapat digunakan sebagai pemisahan secara
partisi, baik dengan bentuk kertas maupun bentuk lempeng. Kedua bentuk
tersebut masih sering digunakan untuk pemisahan flavonoid. Ukuran
partikel yang digunakan kira-kira 50 m. Fase diam ini sekarang sudah
diganti dengan bubuk selulosa yang dapat dilapiskan pada kaca seperti
halnya fase diam yang lain sehingga lebih efisien dan lebih banyak
digunakan untuk memisahkan senyawa-senyawa polar atau isomernya
(Sumarno, 2001).
g) Resin
Fase diam resin digunakan pada KLT penukar ion. Resin merupakan
polimer dari stirendivenil yang mengalami kopolimerisasi dan bersifat non
polar. Fase diam ini sangat berguna untuk memisahkan senyawa berbobot
molekul tinggi dan bersifat amfoter seperti asam amino, protein, enzim,
nukleotida. Sebagai fase gerak digunakan larutan asam kuat atau basa kuat
(Sumarno, 2001).
2.9.3 Identifikasi Kromatogram
Ada beberapa cara untuk mendeteksi senyawa yang tidak berwarna pada
kromatogram. Deteksi paling sederhana adalah jika senyawa menunjukkan
penyerapan di daerah UV gelombang pendek (radiasi utama kira-kira 254 nm)
atau jika senyawa itu dapat dieksitasi pada radiasi UV gelombang pendek dan
gelombang panjang (365 nm). Pada senyawa yang mempuyai dua ikatan rangkap
atau lebih dan senyawa aromatik seperti turunan benzena, mempunyai serapan
kuat di daerah 230-300 nm (Stahl, 1985).
Identifikasi dari senyawa-senyawa yang terpisah dari lapisan tipis yaitu
dengan menggunakan nilai Rf. Nilai Rf didefinisikan sebagai berikut
(Sastrohamidjojo, 2005).
Nilai Rf untuk senyawa-senyawa murni dapat dibandingkan dengan harga
standar. Nilai Rf yang diperoleh hanya berlaku untuk campuran tertentu dari
pelarut dan penjerap yang digunakan, meskipun demikian daftar dari harga-harga
Rf untuk berbagai campuran dari pelarut dan penjerap dapat diperoleh
(Sastrohamidjojo, 2005).
2.9.4 Sistem Fase Gerak Pada KLT
Polaritas fase gerak perlu diperhatikan pada analisa dengan KLT, sebaiknya
digunakan campuran pelarut organik yang mempunyai polaritas serendah
mungkin. Campuran yang baik memberikan fase gerak yang mempunyai kekuatan
bergerak sedang. Secara umum dikatakan bahwa fase diam yang polar akan
mengikat senyawa polar dengan kuat sehingga bahan yang kurang sifat
kepolarannya akan bergerak lebih cepat dibandingkan bahan-bahan polar
(Gritter, et al., 1991).
Fase gerak harus memiliki kemurnian yang tinggi. Hal ini dikarenakan KLT
merupakan teknik yang sensitif. Fase gerak yang digunakan adalah pelarut
organik yang memiliki tingkat polaritas tersendiri, melarutkan senyawa contoh,
dan tidak bereaksi dengan penjerap (Gritter, et al., 1991).
Pelarut yang ideal harus melarutkan linarut dan harus cukup baik sebagai
pelarut yang bersaing dengan daya serap penjerap. Keadaan yang ideal tersebut
mungkin terjadi jika pelarut tidak berproton seperti hidrokarbon, eter dan senyawa
karbonil dipakai sebagai pelarut pengembang (Gritter, et al., 1991).
2.9.5 Kromatografi Gas
Kromatografi gas merupakan metode yang dinamis untuk pemisahan
senyawa-senyawa organik yang mudah menguap dan senyawa-senyawa gas
anorganik dalam suatu campuran. Sampel yang mudah menguap dan stabil
terhadap panas akan bermigrasi melalui kolom yang mengandung fase diam
dengan suatu kecepatan yang terantung pada rasio distribusinya. Pada umumnya
solut dari ujung kolom menghantarkan ke detektor (McNair, et al., 1998).
Kromatografi gas penggunaan utamanya ialah pada pemisahan senyawa
dapat diperbesar dengan mengubahanya menjadi ester dan/atau eter trimetil-silil
sehingga hanya sedikit saja golongan yang sama sekali tidak cocok untuk
dipisahkan dengan cara KGC (Harborne, 1987).
Kromatografi gas dapat digunakan untuk analisia kualitatif dan kuantitatif.
Untuk analisia kualitatif dilakukan dengan cara membandingkan waktu retensi
dari komponen yang akan dianalisa dengan waktu retensi zat baku pembandig
(standar) pada kondisi analisa yang sama. Untuk analisa kuantitatif dilakukan
dengan cara perhitungan relatif dari tinggi atau luas puncak kromatogram
komponen yang dianalisa terhadap zat baku pembanding (standar) yang dianalisa
(McNair, et al., 1998).
Untuk pemisahan bahan-bahan yang mudah menguap, kromatografi gas
merupakan metode yang tepat karena kecepatannya, resolusinya yang tinggi dan
mudah digunakan (McNair, et al., 1998).
2.9.6 Kromatografi Kolom
Kromatografi kolom merupakan metode kromatografi klasik yang
digunakan untuk memisahkan senyawa-senyawa dalam jumlah banyak
berdasarkan adsorpsi dan partisi (Gritter, et al., 1991). Kromatografi kolom
membutuhkan zat terlarut yang terdistribusi diantara dua fase, satu diantaranya
fase diam dan yang lainnya fase gerak. Fase gerak membawa zat terlarut melalui
media, hingga terpisah dari zat terlarut lain yang terelusi lebih awal atau akhir.
Umumnya zat terlarut dibawa melewati media pemisah oleh aliran suatu pelarut
berbentuk cairan atau gas (Harborne, 1987).
Pada kromatografi kolom, tabung pemisah diisi penjerap. Penjerap yang
biasa digunakan ialah silika gel. Pengisian ini harus dilakukan secara berhati-hati
dan merata. Penjerap dapat dikemas dalam tabung dengan cara basah maupun
kering (Harborne, 1987). Cara basah, silika gel terlebih dahulu dijenuhkan dengan
cairan pengelusi yang akan digunakan. Kemudian dimasukkan ke dalam kolom
melalui dinding kolom secara kontinyu sedikit demi sedikit, sambil kran kolom
dibuka.
Kemudian pelarut dialirkan hingga silika gel mampat. Setelah silika gel
ditutup dan sampel dimasukkan, sampel yang dimasukkan terlebih dahulu
dilarutkan dalam pelarut hingga diperoleh kelarutan yang spesifik. Kemudian
sampel dipipet dan dimasukkan ke dalam kolom melalui dinding kolom sedikit
demi sedikit hingga semua sampel masuk. Selanjutnya kran dibuka dan diatur
tetesannya, serta ditambahkan dengan cairan pengelusi. Tetesan yang keluar
ditampung sebagai fraksi-fraksi (Gritter, et al., 1991).
Sedangkan cara kering, yaitu dengan memasukkan silika gel ke dalam
kolom yang telah diberi kapas sedikit demi sedikit dan diratakan dengan alat
pemampat kemudian ditambahkan dengan cairan pengelusi (Gritter, et al., 1991).
2.10 Elusidasi Struktur
Elusidasi struktur umumnya menggunakan teknik spektroskopi klasik
seperti spektrofotometri masa (SM) dan resonansi magnetik inti (RMI). Langkah
pertama, bagaimanapun harus memperoleh rekaman spektrum sinar inframerah
dan ultraviolet untuk menentukan adanya kelompok gugus fungsi tertentu dalam
suatu molekul (Heinrich, 2004).
2.10.1 UV-Visible
Spektrum serapan kandungan tumbuhan dapat diukur dalam larutan yang
sangat encer dengan pembanding blanko pelarut serta menggunakan
spektrofotometer yang merekam otomatis. Senyawa tanwarna diukur pada jangka
200-400 nm, senyawa berwarna pada jangka 200-700 nm. Prinsip kerja
spektrofotometer UV-Vis ialah interaksi sinar ultraviolet atau tampak dengan
molekul sampel. Energi cahaya akan mengeksitasi elektron terluar molekul ke
orbital lebih tinggi (Harborne, 1987).
Pada kondisi ini, elektron tidak stabil dan dapat melepas energi untuk
kembali ke tingkat dasar, dengan disertai emisi cahaya. Besarnya penyerapan
(Day & Underwood, 1980).
Sumber radiasi pada spektrofotometer UV-Vis berdasarkan panjang
gelombang terbagi menjadi 2, yaitu lampu deuterium dan tungstent. Lampu
deuterium menghasilkan sinar 160-500 nm. Lampu tungstent digunakan di daerah
sinar tampak 350-3500 nm. Sumber radiasi dikatakan ideal jika memancarkan
spektrum radiasi yang kontinyu, intensitasnya tinggi dan stabil pada semua
panjang gelombang.
2.10.2 Spektrofotometri Infra Merah
Spektrofotometri infra merah merupakan suatu metode yang mengamati
interaksi molekul dengan radiasi elektromagnetik yang berada pada daerah
panjang gelombang 0,75–1.000 m atau pada bilangan gelombang
13.000–10 cm-1. Spektrofotometer infra merah merupakan alat untuk mendeteksi gugus fungsi, mengidentifikasi senyawa dan menganalisis campuran. Banyak pita
absorbsi yang terdapat dalam daerah yang di sebut daerah ”sidik jari” spektrum
(Harborne, 1987).
Spektrum infra merah suatu sampel dapat di ketahui letak pita serapan
yang dikaitkan dengan adanya suatu gugus fungsi tertentu
(Day & Underwood, 1999). Spektrofotometer infra merah digunakan sebagai
analisa kualitatif untuk menentukan gugus fungsi. Gugus fungsi dapat
diintepretasi dengan memeriksa puncak absorbsi dari spektrum infra merah.
Daerah pada spektrum inframerah diatas 1200 cm-1 menunjukkan pita spektrum atau puncak yang disebabkan oleh getaran ikatan kimia atau gugus
fungsi dalam molekul yang telah ditelaah. Daerah dibawah 1200 cm-1 menunjukkan pita yang disebabkan oleh getaran seluruh molekul, dan karena
secara subjektif pada skala sederhana yaitu kuat, menengah atau lemah
(Harborne, 1987).
2.10.3 Spektrofotometri Massa
Teknik ini memungkinkan untuk mengukur berat molekul dari senyawa
dan ion molekular yang diidentifikasi, teknik ini memungkinkan untuk mengukur
ion secara akurat, untuk memastikan jumlah dari atom hidrogen, karbon, oksigen
dan atom lain yang terdapat dalam suatu molekul. Teknik ini akan memberikan
hasil data berupa rumus molekul (Heinrich, 2004).
Sejumlah teknik ionisasi terdapat dalam Spektrofotometri massa, yang
mana electron impact digunakan secara luas. Teknik ini memberikan fragmentasi
yang baik dari molekul dan berguna untuk menentukan struktur dengan
menetapkan fragmentasi untuk kelompok gugus fungsi yang terdapat dalam
senyawa (Heinrich, 2004).
2.10.4 KG-SM (Kromatografi Gas-Spektrofotometri Massa)
Kromatografi gas dan spektrofotometri massa dapat digunakan untuk
memisahkan komponen dengan memberikan waktu retensi dan puncak elusi yang
dapat dimasukkan ke dalam spektrofotometer massa untuk memperoleh berat
molekul, karakteristik dan informasi fragmentasi (Heinrich, 2004). Teknik ini juga
dapat digunakan untuk komponen yang polar (senyawa yang larut dalam air)
seperti calistegines dan polihidroksil alkaloid jika dibuat turunannya dengan
komponen yang sesuai (trimetilsilil klorida) untuk meningkatkan volatilitasnya
(Heinrich, 2004).
Kromatografi gas saat ini merupakan metode analisa yang penting dalam
kimia organik untuk menentukan senyawa tunggal dalam campuran.
Spektrofotometri massa sebagai metode deteksi yang memberikan data bermakna,
yang diperoleh dari penentuan langsung molekul zat atau fragmen
2.10.5 Resonansi Magnetik Inti (RMI)
Radiasi pada daerah frekuensi radio digunakan untuk mengeksitasi
atom-atom, biasanya proton-proton (1H-RMI) atau atom-atom karbon-13 (13C-RMI), sehingga spinnya berubah dari sejajar menjadi sejajar melawan medan magnet yang digunakan. Rentang frekuensi yang dibutuhkan untuk eksitasi dan
pola-pola pembagian kompleks yang dihasilkan sangat khas pada struktur kimia
molekul tersebut (Watson, 2009).
Spektra RMI biasanya ditentukan dari larutan substansi yang akan
dianalisa. Untuk itu pelarut yang digunakan tidak boleh mengandung atom
hidrogen karena akan mengganggu puncak spektrum. Ada dua cara untuk
mencegah gangguan oleh pelarut. Pertama dapat digunakan pelarut seperti
tetraklormetana, CCl4 yang tidak mengandung hidrogen atau pelarut yang atom
hidrogennya telah diganti dengan isotopnya yaitu deuterium, sebagai contoh
2.11 Kerangka Konsep
Tumbuhan Paku Nephrolepis falcata
Determinasi
Ekstraksi Bertingkat Dengan Pelarut n-Heksana dan Etil Asetat
Ekstrak n-Heksana Ekstrak Etil Asetat
Uji Aktivitas Antioksidan Dengan DPPH
Ekstrak Aktif Antioksidan
Fraksinasi Dengan Kromatografi kolom
Senyawa Hasil Isolasi
Uji Kemurnian Senyawa
BAB 3
METODOLOGI PENELITIAN
3.1 Lokasi dan Waktu Penelitian
Penelitian dilaksanakan di (Laboratorium Analisis Obat dan Pangan) dan
(Laboratorium Farmakognosi dan Fitokimia) Program Studi Farmasi, Fakultas
Kedokteran dan Ilmu Kesehatan, Universitas Islam Negeri Syarif Hidayatullah
Jakarta. Waktu penelitian ini berlangsung selama 6 bulan, yaitu pada bulan
Januari 2013 sampai dengan bulan Juni 2013.
3.2 ALAT DAN BAHAN
3.2.1 Alat
Alat yang digunakan dalam penelitian ini antara lain: Ayakan No.40,
blender, timbangan analitik, kertas label, alumunium foil, kertas saring, kapas,
labu erlenmeyer (Duran), beker gelas (Duran), gelas ukur (Duran), corong
(Eyela), tabung reaksi, kolom kromatografi, spatula, batang pengaduk, pipet tetes,
seperangkat alat vaccum rotary evaporator, kaca arloji, cawan penguap, alat
melting point, pipa kapiler, vial, plat KLT dan bejana KLT.
3.2.2 Sampel Tumbuhan
Sampel tumbuhan yang digunakan adalah tumbuhan paku
Nephrolepis falcata (Cav.) C. Chr yang diperoleh di wilayah kampus FKIK UIN
Syarif Hidayatullah Jakarta, yang selanjutnya dideterminasi di Herbarium
Bogoriense ( LIPI), Cibinong, Bogor.
3.2.3 Bahan Kimia
Bahan kimia yang digunakan dalam penelitian ini antara lain: n-heksana
(Brataco), etil asetat (Brataco), aquades, metanol grade HPLC, aquabides, silika
KLT (whatman, 250 µm 20 x 20 cm AL SIL G/UV, Felxible Plates for TLC, Cat
No. 4420222, coating silica gel) (Merck). Reagen kimia antara lain: Dragendorff,
Mayer, Wagner, ferri klorida, asam sulfat, natrium hidroksida, asam asetat,
kloroform, Liberman Buchardat, asam kloroda, natrium klorida, gelatin, Vanilin ,
dan asam perklorat.
3.2.4 Instrumen
Instrumen yang digunakan antara lain: spektrofotometer infra merah,
kromatografi cair kinerja tinggi (KCKT), resonansi magnetik inti proton
(1H-RMI), lampu UV 254 nm dan 366 nm ( bioinstrument atta), UV-Visible.
3.3 PROSEDUR KERJA
3.3.1 Pemeriksaan Sampel Tumbuhan
Sampel tumbuhan Nephrolepis falcata sebanyak 10,1 kg yang diperoleh dari
halaman kampus Universitas Islam Negeri Syarif Hidayatullah Jakarta, dilakukan
determinasi di Pusat Penelitian Herbarium Bogoriense (LIPI), Cibinong, Bogor.
3.3.2 Penyiapan Simplisia
Sampel daun tumbuhan Nephrolepis falcata sebanyak 10,1 kg disortasi
basah dan dilakukan pencucian dengan menggunakan air mengalir hingga bersih.
Selanjutnya sampel dikeringkan dengan cara diangin-anginkan dan terhindar dari
cahaya matahari, pengeringan dilakukan selama satu minggu hingga sampel
benar-benar kering. Sampel yang telah kering, disortasi kering kemudian
dihaluskan dengan menggunakan blender dan diayak dengan ayakan no.40.
Serbuk simplisia yang diperoleh kemudian ditimbang, Selanjutnya simplisia
disimpan dalam wadah tertutup rapat dan terhindar dari cahaya matahari.
3.3.3 Pembuatan Ekstrak
Prosedur ekstraksi menggunakan metode ekstraksi cara dingin dengan
teknik maserasi bertingkat. Pelarut yang digunakan antara lain, n-heksana dan etil
sehingga terhindar dari cahaya matahari. Selanjutnya dimasukkan pelarut
n-heksana ke dalam wadah yang berisi serbuk simplisia hingga serbuk terendam
±3 cm di atas permukaan simplisia. Pelarut n-heksana yang digunakan untuk
maserasi sebanyak 4,5 liter.
Maserasi dilakukan selama 1-2 hari dengan beberapa kali pengadukan. Hasil
maserasi disaring untuk memisahkan filtrat dengan ampas. Filtrat yang diperoleh
diuapkan dengan vaccum rotary evaporator hingga diperoleh ekstrak kental.
Ampas yang tersisa, kembali ditambahkan n-heksana dan proses maserasi
dilakukan kembali. Maserasi dengan menggunakan pelarut n-heksana dilakukan
sebanyak 15 kali hingga pelarut yang digunakan terlihat bening yang menandakan
senyawa telah terekstraksi seluruhnya.
Selanjutnya maserasi diganti dengan perlarut etil asetat, volume etil asetat
yang digunakan sebanyak 4,5 liter. Prosedur ekstraksi sesuai dengan kegiatan
ekstraksi sebelumnya. Maserasi dengan menggunakan pelarut etil asetat dilakukan
sebanyak 10 kali hingga pelarut yang digunakan terlihat bening. Total pelarut
n-heksana yang digunakan untuk maserasi sebanyak 18 liter dan pelarut etil asetat
yang digunakan sebanyak 10 liter.
3.3.4 Kromatografi Lapis Tipis (KLT)
Ekstrak yang diperoleh, dianalisa dengan menggunakan kromatografi lapis
tipis untuk mengamati pola pemisahannya. Lempeng KLT dengan ukuran
5x10 cm, pada bagian atas dan bawah plat, dibuat garis tepi sepanjang 1 cm.
Selanjutnya dibuat sistem fase gerak yang terdiri dari n-heksana dan etil asetat
dengan berbagai perbandingan, setiap perbandingan kepolarannya ditingkatkan
10%. Fase gerak yang telah dibuat, dimasukkan ke dalam bejana KLT dan
dijenuhkan dengan memasukkan kertas saring ke dalamnya, hingga kertas saring
terbasahi semua. Selanjutnya, 10 mg ekstrak dilarutkan dengan 1 mL pelarut etil
asetat dan ditotolkan pada garis tepi bagian bawah plat dengan menggunakan pipa
kapiler.
Plat KLT dielusi di dalam masing-masing bejana KLT yang berisi fase
gerak, hingga fase gerak mencapai garis tepi bagian atas, kemudian diangkat. Plat