POTENSl Spirulinaplatensis SEBAGAI IMUNOSTIMULAN PADA IKAN PATIN (Pangasius djambal Bleeker)
OLEH: J U N I T A
ABSTRAK
JUNITA. Potensi Spirulina platensis Sebagai Imunostimulan pada Ikan Patin (Pangusius djarnbal Bleeker). Dibimbing oleh DARNAS DANA, FACHRIYAN H. PASARlBU dan HAMBALI SUPRIYADl
Penelitian dilakukan untuk mengetahui dosis dan waktu pemberian Spirulina platensis yang dapat meningkatkan kekebalan ikan clan melihat efektifitas Spirulina platensis terhadap serangan bakteri patogen. Ikan patin dengan berat 12-14 gram diberi Spirulina platensis melalui pakan dengan dosis
0%, 2%, 4% clan 6% serta LPS 0.06% sebagai kontrol positif dengan pemberian
secara kontinyu dan diskontinyu. Penelitian dilakukan dengan rancangan acak lengkap pola faktorial (RAL 2 x 5 ~ 3 ) Pemberian dosis secara kontinyu dilakukan setiap hari selama ernpat minggu, sedstngkan untuk pemberian dosis diskontinyu diberikan dengan interval waktu selang satu minggu selama ernpat minggu. Efektifitas proteksi imunogenik dilakukan dengan uji tantang pada hari ke-29 dengan penyuntikan patogen aktif A.hydrophila Parameter yang diamati meliputi total leukosit, jenis leukosit, indeks fagositik, nilai hematokrit dan tingkat kelangsungan hidup ikan uji. Pengamatan dilakukan pa& hari ke-O,7, 14,21,28, 36, dan 43.
Hasil pengamatan menunjukkan bahwa total leukosit, jenis leukosit (limfosit, monosit dan netrofil) dan indeks fagositik mengalami peningkatan selama pemberian Spirulinu platensis dan L P S ; ha1 ini menujukkan bahwa Spirulina platensis merupakan imunostimulan yang dapat meningkatkan kekebalan ikan. Peningkatan kekebalan ikan yang diberi imunostimulan secara diskontinyu lebih tinggi dibandingkan pemberian secara kontinyu pada dosis yang sama. Peningkatan kekebalan ikan patin yang tertinggi dari perlakuan Spirulina platensis diperoleh pada pemberian 4% secara diskontinyu dengan rataan total leukosit berkisar antara 22866
-
30908 sel/mm3, limfosit antara 15092-
21738sel/mm3, monosit antara 876
-
2068 sel/mm3, netrofil antara 854 -1987 sel/mm3 , nilai indeks fagositik antara 5.67-
10.67% clan tingkat kelangsungan hidup sebesar 76.6%. Narnun, tingkat kekebalan ikan den- pemberian Spirulina platensis 4% secara diskontinyu ini lebih rendah dibandingkan tingkat kekebalan ikan yang diberi LPS 0.06% secara diskontinyu yang mencapai tingkat kelangsungan hidup 83.3% setelah dilakukan uji tantang dengan A.bdrophila. Rataan kadar hematokrit ikan selarna perlakuan berkisar antara 30.33 - 33.33%;SURAT PERNYATAAN
Dengin ini saya menyatakan bahwa tesis yang berjudul
P O T E N S I Spirulina pidensis S E B A G A I IMUNOSTIMULAN P A D A IKAN PATIN (Pangmius djambaf Bleeker)
Adalah benar merupakan hasil karya saya sendiri dan belum pernah dipublikasikan. Semua sumber data dan informasi yang digunakan telah dinyatakan secara jelas dan dapat diperiksa kebenarannya.
P O T E N S I Spirulina platensis S E B A G A I IMUNOSTIMULAN P A D A I K A N PATIN (Pangasius djnmbal Bleeker)
J U N I T A
Tesis
Sebagai salab satu syarat memperoleh gelar
Magister Sains pada
Program Studi Ilmu Perairan
PROGRAM PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis : Potensi S p i r u l m a p l a t e n . ~ ~ ~ sebagai ImunostimuIan
.
( pada Ikan Patln (Pangas~us djambal Bleeker)Nama Mahasls~va : J u n i t a
NRP : 99451
Program Studi : Ilmu Perairan
(ACR)
Menyetujui
1 . Komisi Pembimbing
[Dr.Ir. Darnas Dana. M.Sc) Ketua
(Dr.Drh. Fachriyan H.Pasaribu)
--
Mengetahui(Drs. .Hambali Supriyadi, M. Sc) h g g o t a
2 Ketua Program Studi Ilmu Perairan
IDr.Ir.Kusman Sumawidiaia M.Sc )
Jua
Nar Non pro^
: Potensi Spirulina platemis sebagai Imunostimulan pada Ikan Patin (Pungusius djambal Sleeker)
: J u n i t a
: 99451
: Ilmu Perairan (AIR)
Menyetujui
1 . Komisi Pembimbing
(Dr.Ir. Darnas Dana. M.Sc] Ketua
rs. d a l i Suurivadi. M. Sc) Anggota
Mengetahui -
2 . Kei Ilm
(Dr.Ir.Kusman Sumawidjaja, M. Sc) a hhnuwoto, M.Sc)
RIWAYAT HIDUP
PRAKATA
Puji Syukur penulis kehadirat Allah Subhanahuwata'ala atas rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan perkuliahan, penelitian sarnpai rampungnya penulisan tesis ini.
Selesainya pendidikan dan penelitian ini tidak terlepas dari bantuan dan dukungan berbagai pihak. Untuk itu, ucapan terima kasih dan penghargaan penulis tujukan kepada kepada ibunda, ayahanda, uni, adik-adik dan Kang Suherman atas segala do'a, kasih sayang, dorongan dan semangatnya yang teIah diberikan selama penulis menjalani pendidikan Program Pascasa jana, Bapak Dr. H. Ir. Damas Dana, M.Sc., Dr. Drh. Fachriyan H. Pasaribu dan Drs. Supriyadi, M.Sc. yang berkenan membimbing selama persiapan, pelaksanaan dan penyelesaian tesis; Bapak Dr. IT. Kusman Sumawidjaja, M.Sc. selaku ketua Program Studi Ilmu Perairan yang telah memberikan bimbingan dan arahan selama mengikuti perkuliahan; Rektor Universitas Abulyatama, Dekan beserta staf Fakultas Perikanan Universitas Abulvatama dan Koordinator Komrtis Wilayah X yang telah memberikan kesempatan untuk mengikuti pendidikan; Departemen Pendidikan Nasional dalam hal ini Badan Penyelenggara Pendidikan ~aicasarjana (BPPS) yang telah membantu pembiayaan p&didi&; Kepala Balai Penelitian Perikanan Air t a w Sukamandi beserta staf dan Kepala Laboratorium Penyakit Ikan Fakultas Perikanan IPB beserta staf yang telah membantu dan memberikan fasilitas selama penelitian, rekan-rekan Program Studi flmu Perairan, Rini, Nunnahadi, Fitma, Lely, Oning, Ela, Detin, serta semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah membantu baik moril maupun matefit selama ini.
DAFTAR IS1
Halaman PRAKATA ... v DAFTAR TABEL ... vi DAFTAR GAMBAR ... v ii DAFTAR LAMPZRAN ... viii PENDAHULUAN ... I
Latar Belakang ... 1 Rumusan Masalah ...
.
.
3Tujuan Penellt~an ... 4 Hipotesis ... 4 Kegunaan Penelitian ... 4
TINJAUAN PUSTAKA
...
5 Kekebalan Ikan...
5 Organ Pembentuk Respon Kekebalan ... 5 Sistem Kekebalan Ikan...
6 Imunostimulan...
8 Spirulina piatensis ... 9 Darah Ikan ... 10BAHAN dan METODE PENELITIAN
...
12...
Ternpat dan Waktu Penelitian
... Bahan dan Mat Penelitian
. .
Rancangan Penelitran
. .
... ....-
Pelaksanaan Penellban...
Pengujian LDso Aeromonas Iydrophila pada Ikan Patin
...
Pengaruh Spirulinapiatensis terhadap Kekebalan nEan Patin Pemeriksaan Parameter Penelitian ......
LDm Aeromonns hydrophila pada &an Patin...
...Pemeriksaan Respon Kekebalan Ikan Patin :
....
...
Penghitungan Total Leukosit...
Penghitungan Jenrs Leukosit... Pengukuran Indekss Pagositik
...
Pengukuran Kadar Hematobit... LDso Aerornonas hydrophila pada Ikan Patin
... Respon Kekebalan &an Patin yang diberi Spirulina platensis
DAFTAR TABEL
Halaman
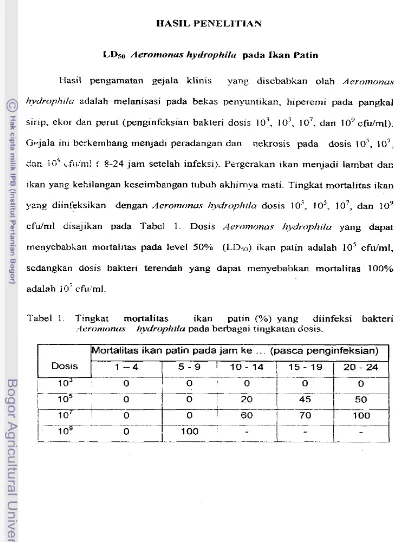
1 . Tingkat mortalitas ikan patin (%) yang diinfeksi bakteri
Aerornonas hidrophila pada berbagai tingkatan dosis
...
192. Gejala klinis ikan patin setelah uji tantang dengan
DAFTAR GAMBAR
Halaman
1 . Rataan total leukosit ikan paiin per waktu pengarnatan ... 21
2 . Rataan jumlah lirnfosit ikan patin) per waktu pengarnatan ... 23
3
.
Rataan j u i l a h rnonosit ikan patin per waktu pengamatan ... 25DAFTAR LAMPIRAN
1. Hasil analisis ragam nilai total leukosit pada tingkat waktu dan
dosis Spirulina platensis ... 42
2. Hasil analisis ragam rataan jurnlah limfosit pada tingkat waktu
dan dosis Spirulina platensis) ...
.
.
... 4 33. Hasil analisis ragam rataan jumlah monosit pada tingkat waktu
dan dosis Spirulina platensis) ... 44 4. Hasil analisis ragam rataan jumlah netrofil pada tingkat waktu
dan dosis Spirulina platensis
...
....
...
455. HasiI analisis ragam nilai rataan indeks fagositik pa& tingkat
waktu dan dosis Spiruiinuplatensis ... 46 6 . Hasil analisis ragam kadar hematokrit pada tingkat walctu dan
...
dosis Spiruiina platensis
.
.
.
477. Hasil analisis ragam tingkat kelangsungan hidup ikan patin
...
PENDAHULUAN
Ikan patin (Pangasius djambal Bleeker) termasuk famili Pangasidae. Ikan ini merupakan ikan lokal yang mempunyai pertumbuhan yang cepat dan harga
yang lebih mahal dibandingkan jenis ikan jambal introduksi dari luar negeri
(Legendre et al. 1999), sehingga mempunyai prospek dan potensi untuk dikembangkan. Seperti ikan lainnya, ikan patin juga menjadi objek dan tidak
lepas dari berbagai penyakit.
Ikan hidup di lingkungan perairan yang juga mempakan tempat hidup
berbagai jenis patogen seperti bakteri, virus, parasit, dan jamur. Pada kondisi lingkungan normal, keberadaan patogen ini tidak menimbulkan penyakit. Namun, dalam kegiatan budidaya dengan kondisi lingkungan yang terbatas, kepadatan
yang tinggi dan pengelolaan kualitas air yang kurang tepat dapat menyebabkan keseimbangan lingkungan terganggu. Kondisi ini mengakibatkan ikan mudah
sues clan patogen dapat berkernbang menimbulkan penyakit. Respon fisiologis ikan terhadap penyakit dapat diamati melalui penyimpangan tingkah lakq
anatomi, hematologis, dan respon kekebalan. Penyimpangan-penyimpangan *-
tersebut merupakan indikasi terjadinya perubahan status kesehatan ikan dari
kondisi normal menjadi abnormal.
Pengendalian penyakit perlu dilakukan secara dini agar tidak terjadi
kerugian ekonomi. Pemakaian antibiotik merupakan pilihan m u m yang sering dilakukan untuk menghindari serangan akut suatu jenis penyakit. Namun, pemakaian antibiotik un& jangka panjang dapat menimbulkan damp& negatif
kimia yang dapat berdampak buruk pa& kesehatan konsumen serta pernasaran.
Cara lain untuk pencegahan penyakit adalah dengan pemberian vaksin.
Penggunaan vaksin dapat memperkecil resiko mortalitas yang diakibatkan oleh
suatu jenis penyakit tertentu, tetapi belurn ada vaksin yang efektif untuk
menangkal beberapa jenis panyakit bakterial dan virus sekaligus.
Tidak seperti halnya vaksin yang memicu produksi antibodi spesifik terhadap satu patogen tertentu, sekelompok senyawa biologi dan sintetis yang disebut imunostimulan dapat meningkatkan kekebalan non-spesifik. Penggunaan
imunostimulan pa& ikan dapat dijadikan salah satu alternatif untuk
perlindungan terhadap infeksi patogen. Imunostimulan yang dapat digunakan
antara lain lipopolisakarida (LPS), gldcan, levamisol, vitamin C dan Sprrulina
(Sakai 1998).
Pengunaan imunostimulan dalarn budidaya perikanan di Indonesia masih
merupakan ha1 yang baru, sehingga informasi mengenai jenis dan dosis yang efektif untuk meningkatkan respon kekebalan jenis ikan lokal belum banyak
diketahui. Sehubungan dengan h d tersebut, maka kajian tentang potensi imunostimulan (Spirulinaplatensis) untuk meningkatkan sistem kekebalan jenis
Rumusan Masalah
Penyakit infeksi sewaktu-waktu dapat te ja d i pada ikan karena patogen seIalu
ada dalam media hidupnya. Penyakit ini rnerupakan salah satu kendala dalam
kegiatan budidaya ikan karena dapat menyebabkan kerugian ekonomi. Untuk itu,
pencegahan dan pengendalian penyakit h a w dilakukan sedini mungkin. Penemuan imunostimulan sebagai suatu bahan yang dapat meningkatkan
kekebalan non-spesifik dapat dijadikan sebagai alternatif pencegahan penyakit
pa& ikan. Aplikasi imunostimulan yang tepat &pat menstimulasi kekebalan
tubuh ikan terhadap penyakit infeksi. Namun, pemberian imunostimulan
berlebihan dan tidak tepat waktunya sering mengurangi efek yang diingini
sehingga tidak efesien. Hasil-hasil penelitian menunjukkan bahwa Spirulina berpotensi dalam meningkatkan sistem kekebalan beberapa jenis hewan seperti
ayarn, tikus, kelinci, kucing. dan ikan ( Quereshi er al. 1995, Duncan dan Klesius 1996, Sakai 1998 clan Hendrikson 2000). Sejauh ini, penelitian mengenai penggunaan Spirulina platensis sebagai imunostimulan untuk ikan di Indonesia belum pernah dilakukan, sehingga informasi mengenai peranan Splrulina platensis dalam sistem kekebalan ikan-ikan lokal belum diketahui. Langkah awal perlu dilakukan untuk meningkatkan sistem kekebalan ikan patin ialah menjajaki
Tujuan Penelitian Penelitian yang dilakukan ini bertujuan untuk:
1. Mengetahui peranan Spirulina platensis terhadap kekebalan ikan patin yang ditelaah dari respon seluler (total leukosit, jenis leukosit dan aktifitas sel-sel
fagositik)
2. Mengetahui kebutuhan dosis dan waktu pemberian Spirulina platensis yang efektif untuk meningkatkan kekebalan ikan patin.
I Pemberian Splrullna platensrs rqalalui
p*n
dapat menstimulasi sistem kekebalan ikan sehingga meningkatkan respon ketahanan terhadap penyakitinfeksi
2. Pemberian Sprrullna platensls dengan dosis dan lama waktu berbeda memberi pengaruh yang berbeda pula terhadap respon kekebalan ikan.
Kegunaan Penelitian
TINJAUAN PUSTAKA
Kekebalan Ikan
Organ Pembentuk Respon Kekebalan
Jaringan pembentuk respon kekebalan dan darah dikenal sebagai jaringan
limfoid dan mieloid (Anderson 1974). Pada ikan, jaringan limfoid dan rnieloid
menyatu rnembentuk organ iimfomieloid (Fange 1982). Selanjutnya disebutkan,
organ limfomieloid pada ikan sangat bervariasi bergantung kepada kelasnya.
Pada ikan teleost organ ini terdiri atas lirnpa, timus dan ginjal bagian depan. Limpa terletak dekat lengkung lambung, berwarna merah tua atau hitam
Jan dibalut oleh Iapisan tipis jaringan ikat (Roberts 1989; Ellis 1989). Pulpa putih Iimpa banyak mengandung limfosit; antigen yang diikat berlokasi pada
limfosit yang terlihat mengelornpok pa& bagian elipsoid l i m p sebagai suatu
perangkap antigen yang nantinya berpengaruh &lam proses pembentukan dan rnemori respon humoral, sedangkan pulpa merah banyak mengandung eritrosit
(Lamers dan Muiswinkel 1986).
Timus ikan teleost merupakan pusat organ limfoid (Lamers dan de Haas
1985), terletak pada faring dalam rongga insang (Ferguson 1989). Parenkhimnya
mengandung limfosit (Hibiya 1982), seI timosit, sel eosinofilik, dan komponen sel lainnya yang terdiri dari netrofil (Anderson 1974). Limfosit umumnya timbul setelah timus berdiferensiasi menjadi jarigan Iimfoid, biasanya te jadi pada hari ke
tiga setelah penetasan telur (Ellis 1982). Secara makroskopis, timus jelas terlihat
Ginjal merupakan jaringan haemopoietik, kaya akan sel Iimfosit,
granulosit d m sel fagosit (Rijkers 1981), terletak retroperitonial di bawah
kolomna vertebralis (Ferguson 1989). Jaringan limfoidnya merupakan kelompok
pulpa putih mengandung sel retikulosit yang a k a membentuk sel plasma, sedangkan pembentukan eritrosit dan granulosit te rjadi di pulpa merah (Lamers
clan Muiswinkel 1986).
Sistem Kekebalan lkan
Sistem kekebalan pada ikan hampir sama dengan hewan mamalia yang
terdiri dari sistem kekebalan spesifik dan non-spesifik (Anderson 1974). Ellis
(1988) menjelaskan bahwa pada a w l kehidupannya sistem pertahanan tubuh
yang mula-mula berfungsi adalah sistem pertahanan non-spesifik, sedangkan
pertahanan spesifik baru berkembang clan dapat berfungsi dengan baik sekitar beberapa minggu setelah telur menetas. Mekanisme k e j a kedua sistem pertahanan ini saling menunjang satu sama lain melalui mediator dan
komunikator seperti sitokin dan limfokin (Anderson 1974). Sistem pertahanan
tersebut diperlukan untuk perlindungan tubuh terhadap serangan patogen seperti virus, bakteri, cendawan dan parasit.
--
Sistem kekebalan non-spesifik meliputi barrier mekanik clan kimiawi (mukus, kulit, sisik clan insang), dan pertahanan seIuler ( m a k r o h dan leukosit seperti monosit, netrofil, eosinofil
dan
basofil ) (Ingram 1980). Mukus yangmenyelimuti permukaan tubuh ikan, insang
dan
juga terdapat pada lapisan mukosa usus berperan sebagai perangkap patogen secara mekanik dan mengeliminasi patogen secara kimiawi dengan lisosim dan enzim proteolitik lainnya. Kulit danproses penebalan kutikel ataupun hiperplasia sel-sel malpigi (Roberts 1989).
Pertahanan seluler merupakan respon pertahanan yang diperantarai sel (Walczak
1985). Rijkers (1 98 1) menjelaskan bahwa kekebalan berperantara sel pa& ikan
dapat terlihat dalam bentuk reaksi leukosit, pembentukan limfokin, transformasi
limfosit oleh mitogen sel T secara in vitro, imunitas transplantasi dan
penghambatan migrasi makrofag. Kekebalan berperantara sel sangat penting
dalam pertahanan tubuh melalui aktivitas sel-sel fagositik (Woo 1995). Sel
pagositik berfirngsi melakukan pogositosis terhadap benda asing yang masuk ke
dalam tubuh ikan. Proses pagositosis ini mempakan langkah awal untuk sistem
pertahanan berikutnya (Ellis 1988).
Proses pembentokan respon kekebalan, dimulai oleh stimulasi patogen
yang mempakan protein asing dikenal sebagai antigen. Anderson (1990)
mengemukakan, dalam proses imunomodulasi melibatkan dua mekanisme
kekebalan. Pertarna, sistem kekebalan ''afferent" yang dimulai dengan kontak,
seleksi dan penghancuran antigen. Kedua, sistem kekebalan "efferent" yang mengbasilkan aktivasi limfosit, antibodi, dan sei-sel pagositik Setelah terjadi
aktivasi antigenik, makrofag yang merupakan pertahanan pertama melalui proses
pagosistosis akan menghancurkan bahan asing yang masuk ke dalam tubuh
dan
mengirim sandi-sandi ke set-sel limfosit. Selanjumya, sel-sel limfositberproliferasi dan membentuk dua subpopulasi limfosit yaitu limfosit T dan B. Roitt (1985) menjelaskan sel T dan B mengalami proses sirkulasi dan resirkulasi daIam tubuh. Keadaan ini bertujuan untuk mencari adanya patogen atau bahan asing yang masuk ke dalam tubuh. Apabila ditemukan patogen, sel T
akan berdiferensiasi menjadi Iimfoblas, selanjutnya membentuk sel T yang aktif
dan masuk lagi dalam sistem sirkulasi (darah). Sel T yang &if akan ke luar dari darah menuju situs infeksi. Sel ini akan menghasilkan lirnfokin yang dapat
mengaktiflcan makrofag, sehingga aktivitas pagositik makrofag tersebut
meningkat. Sebaliknya, sel B yang berada dalam jaringan tidak kembali ke
jaringan limfoid melainkan akan mengikat antigen yang selanjutnya diambil clan diproses oleh makrofag. Di samping itu, stimulasi antigen mengakibatkan Iimfosit B membentuk plasmablas, sel ini kemudian berkembang menjadi sel plasma yang
akan memproduksi antibodi. Sel plasma yang kembali sebagai limfosit B dan
tetap dalam jaringan limfoid akan berperan sebagai memori. Adanya sel memori ini akan mempercepat respon ketahanan pada infeksi berikutnya (Ellis 1988).
Imunostirnulan merupakan suatu senyawa biologi, sintetis atau bahan
lainnya yang &pat meningkatkan sistem kekebalan tubuh @?st et al. 1992). Galeotti (1998) mengungkapkan bahwa imunostimulan dapat meningkatkan
respon kekebalan spesifik dan non-spesifik ikan. Apabila masuk ke dalam tubuh
ikan, imunostimulan akan merangsang makrofag untuk memproduksi interleukin -
yang akan menggiatkan sel limfosit yang kemudian membelah menjadi limfosit-T dan B (Raa et al. 1992). Selanjutnya dijelaskan bahwa limfosit-T memproduksi interferon yang menggiatkan kembali (meningkatkan kemampuan) makrofag
sehingga dapat memfagositosis bakteri, virus, dan partikel asing lainnya yang
imunostimuIan dapat berasal dari komponen bakteri, ekstrak tumbuhan dan hewan, serta faktor nutrisi (Galeotti 1998). Sakai (1998) menyebutkan komponen
karbohidrat dan asam nukleat yang terdapat pa& dinding bakteri gram-negatif dipercaya sebagai imunostimulan, bila dicampur ke dalam pakan akan
memberikan respon kekebalan. Dari beberapa hasil penelitian diketahui bahwa
Sprrulina platensis juga berpotensi dalam menstimulasi sistem kekebalan beberapa hewan terrnasuk ikan (Henrikson 2000). Alifuddin (1999) menyatakan
bahwa pemberian imunostimulan &pat meningkatkan respon kekebalan ikan
terhadap penyakit infeksi, sehingga peng-nnya dalam budidaya sangat
dianjurkan.
Spirulina platensis
Spirulina platenszs adalah alga biru-hijau multiseluler dengan ukuran sel
11 0 pm d m diameter 1 - 12 pm , berbentuk spiral yang merupakan filamen tidak bercabang (Richmond 1987). Alga ini banyak terdapat pada danau-danau yang airnya bersifat basa, &pat tumbuh pada perairan tawar, payau, dan laut (Sze
1993). Alga ini dapat dikultur secara massal (Vonshak 1997). Menurut Allen (2000), Spirulina platensis terdiri dari 65-72% protein, 8% Iemak, 19% karbohidrat, sumber vitamin, B-karoten, phycocianin, gamma linolenic acid
(GLA), dan lebih dari 2000 enzirn-enzim aktif. Komponen utama dinding sel SpiruIinu platensis sama dengan dinding sel bakteri Gram-negatif yang mengandung peptidoglikan clan lipopolisakarida (Sze 1993). Lipopolisakarida menurut Jawetz et a [ . (1982) terdiri atas t i p bagian yaitu lipid A, polisakarida 0
merupakan antigen permukaan yang dapat menginduksi kekebalan spesifik dan
non-spesifik. Hal inilah yang menjadi landasan digunakannya lipopolisak-arida
sebagai imunostimulan yang potensial dalam meningkatkan respon kekebalan
pada ikan. Vonshak (1997) menyebutkan lipopolisakarida pada Spirulina
sebesar 1.5% dari bobot kering sel.
Hasil-hasil penelitian menunjukkan bahwa Spirulina berpotensi dalam
meningkatkan sistem kekebalan beberapa jenis hewan seperti ayam, tikus,
kelinci, kucing,
dan
juga ikan (Quereshi et al. 1995, Duncan dan Klesius 1996, Sakai 1998 dan Henrikson 2000). Besednova (1979) adalah peneliti pertama dariRusia yang mempublikasikan pengaruh lipopolisakarida Spiruiina terhadap
stimulasi kekebalan kelinci. Tikus yang diberi ekstrak Spirulina platensis terbukti meningkatkan fungsi makrofag, produksi antibodi dan sel T terhadap paparan infeksi ( Boajiang 1994). Duncan dan Klesius (1996) telah mengevaluasi
pengaruh Spirulina terhadap peningkatan respon kekebalan ikan chanel catfish
(Ichtaluruas punctatus)
.
Darah Ikan
Darah ikan tersusun dari sel-sel &ah yang tersuspensi dalam plasma dan diedarkan ke seluruh tubuh melalui sistem sirkulasi tertutup. Sel dan plasma
d a d mempunyai peran fisiologis yang sangat penting. Perubahan gambaran darah dan kimia darah baik secara kualitatif maupun kuantitatif dapat
menentukan kondisi kesehatan ikan (Wedemeyer et al. 1990).
Pemeriksaan darah penting artinya untuk memantapkan diagnostik suatu
penyakit (Ellsaeser et a2. 1985). Pada penelitian hematologi ikan, parameter darah
jenis Ieukosit, titer antibodi, aktivitas fagositik, dan protein plasma plasma (Anderson d m Siwicki 1993).
Sel darah putih (Ieukosit) kelimpahannya kurang dari sel darah merah di
dalam darah ikan (20000 - 150000/mrn3) dan fungsinya membersihkan tubuh dari
benda asing (Moyle
dan
Chech 1988). Chinabut et al. (1991) membagi Ieukositmenjadi dua grup yaitu agranulosit dan granulosit berdasarkan ada tidaknya butir- butir halus (granula) di sitoplasma. Agranulosit terdiri atas limfosit, monosit, dan
trombosit; sedangkan granulosit terdiri atas netrofil, eosinofil, clan basofil.
Menurut Moyle dan Chech (1988), limfosit mempunyai diameter yang berkisar
antara 4.5 - 12.0 prn. Kelimpahan limfosit paling banyak yaitu bejumlah antara
71.12 - 82.88% dari total sel darah putih dalam darah ikan (Blaxhall 1971). Monosit mempunyai jumlah sedikit dari populasi sel
darah
putih kecuali kalau ada benda asing rnasuk ke jaringan atau aliran darah (Moyle dan Chech 1988); bersama dengan rnakrofag jaringan setempat, monosit mempagositosis sisa-sisajaringan dan penyebab-penyebab penyakit (Nabib
dan
Pasaribu 1989). Adapun ne.trofil adalah sel darah putih yang dapat meninggalkan pembuluh darah, mengandung vakuola yang berisi enzirn yang digunakan oleh sel tersebut untukB A H A N
dan METODE PENELlTIANTempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Patologi Balai Penelitian
Perikanan Air Tawar Sukamandi. Peneiitian dilaksanakan selama lima bulan.
sejak bulan Pebruari sampai Juni 200 1
Bahan dan Alat Penelitian
Ikan yang digunakan adalah ikan patin (Pangasius djambal) yang diperoleh dari produksi Balai Penelitian Perikanan Air T a w Sukamandi berumur 1 minggu. Ikan dikarantina selama 1 bulan' dalam fiber glass yang telah
disucihamakan dengan KMn04. Pemberian pakan dilakukan 2 kati sehari.
Bahan untuk imunostimulan adalah SpimZirzap2atensi.s yang diperoleh dari Laboratorium Mikroalga, Pusat Penelitian dan Pengembangan Bioteknologi-LIPI,
Cibinong clan Lipopolisakarida (LPS) yang diekstrak dari bakteri Vibrio h ~ e y i produksi Balitkanwar Sukamandi. Pakan yang digunakan adalah pelet CP 781 dengan kandungan protein sebesar 35%. Pakan perlakuan dibuat dengan cara meiarutkan Spimlina platemis bentuk powder dm LPS cair ke daiarn air aquades
steril sampai homogen, suspensi Spirulinaplatensis d m LPS dicarnpurkan sedikit
.-
demi sedikit pada pakan sesuai dosis perlakuan. Pakan dikeringkan dibawah sinarmatahari selama 4 - 5 jam. Pelet dikemas dalam kantong plastik dan disimpan dalam kulkas.
Bakteri untuk uji tantang adalah bakteri Aeromonas hydrophila isolat no.26 koleksi laboratorium Patologi Balitkanwar Sukamandi. Untuk keperluan ini
Wadah yang digunakan adalah akuarium clan bak fiber yang dilengkapi
peralatan aerasi. Untuk mencegah berkembangnya potogen dan membersihlcan kotoran yang menempel dalam wadah, maka sebelum digunakan wadah
disuciharnakan dengan KMn04 sebanyak 5 ppm seIama 24 jam, selanjutnya
dibilas dengan air bersih dan dikeringkan. Alat untuk pemerikasaan respon
kekebaIan adaIah jarurn suntik, tabung reaksi, obyek dan gelas penutup, hemasitometer, mikropipet, pipet pasteur, pipet berskala, tabung hematokrit kapiler. sentxifirs, alat penghitung, mikroskop, petridish, gelas beker, elemeyer, penangas air, autoklaf, jarum ose, inkubator, spektrofotometer dan kulkas. Bahan kimia untuk analisis parameter pengamatan adalah akuades, alkohol, metanol,
HCl, Na-slhat, pewama Giemsa, media TSA, PBS, larutan Hayem, lamtan Turks,
dan K h h 0 4
Rancangan Penelitian
Penelitian ini dilakukan dengan metode eksperimen yang terdiri atas 2
tahapan penelitian yaitu pengujian dosis Aeromonas hydrophila yang dapat menyebabkan mortalitas 50%
(ID-)
pada ikan patin clan pengaruh Spirul~na platensis terhadap sistem kekebalan ikan patin. Pada pengujian LDm, diterapkan--
Penelitian ini menggunakan rancangan acak Iengkap (RAL) pola faktorial 2x5
dengan 3 ulangan (Steel dan Torrie 1989). Adapun kombinasi perlakuan adalah sebagai berikut:
Keterangan: I = kontinyu, I1 = diskontinyu
A = Wh(kontro1-),
8 = 0.06% LPS (Kontrol +),
C = 2% Spimlinaplatensis , D = 4% Spirulina platensis,
E = 6 O h Spirulina platensis
Waktu pernberian 1
II
Pelaksanaan Penelitian
Pengujian LDso Aeromonas hydrophih pada Ikan Patin
Ikan uji dengan bobot rata-rata 12 gram dipelihara &lam akuarium Dosis
dengan kepadatan I 0 ekor per wad& Masing-masing ikan diinfeksikan dengan dosis Aerornonas hydrophila
lo3, lo5, lo7,
danlo9 cfulml.
Penginfeksian dilakukan dengan cara penyuntikan bakteri ke dalam tubuh ikan secara intra muscdar. Setelah diinfeksikan, diadakan pengamatan terhadap perkembanganE IE IIE
gejala klinis dan jumlah mortalitas ikan uji -
Pengaruh SpiruCi~pZatensis terhadap Sistem Kekebalan Ikan Patin D
ID
IIDIkan uji dengan bobot rab-rata 12
-
14 gram dipelihara &lam bak frber C IC IIC A 1'4 IIAdengan kepadatan 25 ekor per wadah. Ikan dipetihara selama enam minggu; pemberian pakan dilakukan 2 kali sehari sebanyak 5% bobot tubuh. Pada
B
IB
IIE?
pemeliharaan; pa& pemeliharaan selanjutnya diberikan pakan CP 781 yang tidak
mengandung Spirulina platensis dan LPS. Sedangkan pada perlakuan dosis dengan waktu diskontinyu, pakan yang mengandung Spirulina platensis dan LPS diberikan dengan interval waktu selang satu minggu selama empat minggu; pada
pemeliharaan seianjutnya juga diberikan pakan CP 781 yang tidak mengandung
SpiruIina platensis dm L P S . Penyiponan dilakukan setiap pagi hari dan dilakukan penambahan air sampai setinggi semula Pemeriksaan gambaran respon
kekebalan dan hematologis ikan uji dilakukan pa& hari ke-0, 7, 14, 21, 28 (setelah pemberian Spirulina platensis), 36 dan 43 (setelah uji tantang). Efektivitas proteksi imonologik dilakukan melalui uji tantang dengan penyuntikan
patogen aktif Aeromonas hydrophila dengan kepadatan sesuai hasil penentuan LDSO. Uji tantang ini dilakukan pada hari ke-29 setelah pemberian Spirulina platensis. Pengamatan gejala klinis dan tingkat kelangsungan hidup ikan uji
dilakukan setiap hari terutama setelah dilakukan uji tantang.
Pemeriksaan Parameter Penelitian
Parameter yang diperiksa &lam pengujian LD50 Aerornonas 1:ydrophila
pada ikan patin meliputi patofisiologi (gejala klinis
d m
tingkah laku ikan) serta -pengamatan tingkat kelangsungan hidup ikan. A h p u n parameter yang diperiksa
LD50 Aeromonas hydrophila pada Ikan Patin
LD50 ditentukan dengan adanya tingkat mortalitas ikan 50% selama 24
jam pengamatan. Perneriksaan LDso dilakukan dengan cara menghitung
persentase mortalitas ikan setelah diinfeksikan dengan Aeromonas hydrophila pada berbagai tingkat kepadatan bakteri mengikuti rumus Hazen (1978) dalam
Sanusi (1 988):
Keterangan : M = mortalitas ikan (Oh)
Nt = jumlah ikan hidup pada hari ke-t (ekor) No = j d a h ikan hidup pada hari k e o (ekor)
Pemeriksaan Respon Kekebalan Ikan Patin
Pemeriksaan respon kekebalan meliputi jumlah total leukosit, jenis
leukosit, dan aktivitas pagositik dan kadar hematoloit. Untuk pemeriksaan ini,
pengambilan darah dilakukan sebagai berikut: darah &an diambil dari bagian kaudal dengan spuit 1 ml yang ditambahkan dengan antikoagulan ( Na-sitrat
3.8% ) dengan perbandingan 1:4. Darah ikan yang telah diambil ditampung dalam tabung Efpendorfuntuk pemeriksaan selanjutnya.
Penghitungan Total Leukosit
Total leukosit dihitung menurut Blaxhall dan Daisley (1973), yaitu sampel darah dihisap dengan pipet pencampur) sampai skala 0.5, dilanjutkan dengan
-
menghisap larutan Turk s sampai skala 11. Pipet digoyangkan sampai campuran
homogen. Tetesan pertama dibuang, tetesan berikutnya diteteskan di
hernasitometer, ditutup dengan gelas penutup kemu&an dilakukan penghitungan jumlah sel darah putih. Pengllltungan dilakukan pada 5 kotak besar hemasitometer
Penghitungan Jenis Leukosif
Penghitungan jenis leukosit dilakukan menurut Blaxhall dan Disley
(1973) yaitu dengan mengamati preparat ulas darah. Preparat ulas darah Qbuat dengan cara menempatkan setetes darah pada gelas objek yang bersih, di atas
gelas objek pertama ini ditempatkan ujung gelas objek kedua membentuk sudut
45', gelas objek kedua di geser ke arah belakang menyentuh tetesan darah hingga
menyebar kemudian gelas objek kedua digeser ke arah berlawanan hingga
terbentuk lapisan darah yang tipis clan dibiarkan hingga kering. Selanjutnya dilakukan fiksasi dengan metanol selama 5 menit, dibiarkan kering udara dan
diwarnai dengan larutan Giemsa selama 15 menit, dibilas dengan air mengalir
dan dibiarkan hingga kering. Preparat diamati dibawah mikroskop dan dilakukan
penghitungan jenis leukosit.
Pengukuran Indeks Pagositik
Pengukuran indeks pagositik untuk mengetahui aktivitas sel-sel pagositik Pengukuran ini dilakukan dengan metode ulasan indeks fagositik mengikuti
Anderson dan Siwicki (1993), yaitu sebanyak 100 p1 darah dimasukkan ke dalam
mikrotiter plat dan ditambahkan sebanyak 100 pl suspensi StaphyZZococcus aureus &lam PBS (10' sel), dicampurkan secara homogen dan diinkubasi selama 20 menit. Selanjutnya dibuat ulasan darah, dikeringkan dengan udara, difiksasi dengan metanol selama 5 menit d m diwarnai dalam larutan Giemsa selama 15
menit, dicuci dengan air mengalir dan keringkan. Preparat diamati di bawah
mikroskop setiap 100 sel diukur aktifitas fogositiknya. Aktivitas pagositik didasarkan atas prosentase jumlah sel polimorfnuklear (PMN) yang menunjukkan
Kadar Hematokrit (We)
Kadar hematokrit diukur mengikuti Anderson dan Siwicki (1993), yaitu
Sarnpel darah dimasukkan ke tabung mikrohematokrit dengan sistem kapiler
Seteiah darah mencapai 4/5 bagian tabung, kemudian ujung tabung (bertanda
merah) disumbat dengan kretoseal. Tabung kapiler yang telah berisi darah di
sentrifise seIama 15 menit dengan kecepatan 3500 rpm. Pengukuran kadar hematokrit dilakukan dengan membandingkan volome padatan sel darah terhadap
volume seluruh darah menggunakan skala hematokrit.
Kelangsungan Hidup Ikan
Tingkat kelangsungan hidup ikan dihitung berdasarkan Effendi (1997)
rumus sebagai berikut:
Keterangan : S = tingkat kelangsungan hidup (%)
N, = jumlah ikan hidup pada hari ke-t (ekor)
No
= jumlah ikan hidup pa& hari ke-o (ekor)Analisa Data
Data pemeriksaan parameter respon kekebalan
dan
tingkat kelangsunganhidup ikan uji dianalisis dengan sidik ragam dan untuk mengetahui respon yang terbaik dari interaksi perlakuan terhadap parameter menggunakan uji Duncan (Steel dan Tome 1989). Data gejala klinis dianalisis secara desknptif, data
HASIL PENELIT1.QR:
LDSo Aeron~onus hyrlrophifiz pada Zkan Patin
Nasil pengarnatan gejala klinis yane disebahkan olah Acrr>monu.t
/~ydrophilo adalah melanisasi pada bekas psnyuntikan, hiperemi pada pangkal
sirip, ekor dan perut (penginfeksian bakleri dosis lo:, 105, lo7, dan 10'cfuiml).
Grjala ini berkembang menjadi peradangan dan nekrosis pada dosis lo5, lo7, dar,
icy
L ~ ~ L ~ E ! ! 8-24 jam setelah infeksi). Pergerakan ikan menjadi lambat dar. ikan yang kehilangan keseimbangan tubuh akhimya mati. Tingkat mortalitas ikanyeng diinfeksikan dengan Aeromonu.~ I?-vdrophila dosis 1 o', 1
o',
I o', dan l o 9cfu/ml diszjikan pada Tabel 1. Dosis Ac.rumonos Iz~ydr~pIzrlu yang dapat
menyebabkan mortalitas pada level 50% (LD50) ikan patin adalah 10' cfulml, sedangkan dosis bakteri terendah yang dapat menyebabkan mortalitas 100%
adalah 10' cfui'ml
Tabel 1. Tingkat mortalitas ikan pntin (%) yang diinfeksi bakteri ..lrronzonus l~vdrophilu ~ a d a berbaga~ t ~ n g k a t a n ciosis.
I
l~ortalitas ikan patin pada jam k e.
(pasca penginfeksianfl Dosis 1 - 4-- - I
[image:103.520.52.446.52.594.2]Respon Kekebalan Ikan Patin dengan Pemberian SpimIina pfafemis
Total Leukosit
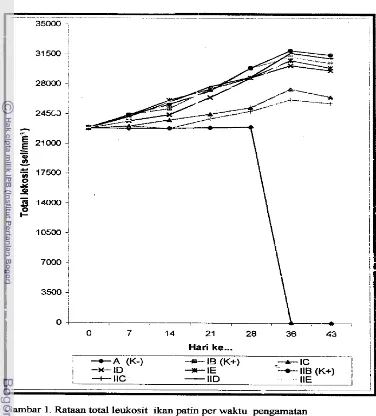
Raban total leukosit ikan uji per waktu pengamatan ditampilkan pada
Garnbar 1.Total leukosit cenderung meningkat sampai hari ke- 36 dan menurun hari ke- 43. Total leukosit ikan (hari ke-7 sampai ke-28) pada kontrol negatif
antara 22825 - 23008 sel/mm3, kontrol positif berkisar antara 24383 - 29925
sel/mm3 dan ikan perlakuan Spirulina platensis antara 22825 - 28852 sevmm3.
Pa& pengamatan hari ke- 36 clan 43 untuk perlakuan kontrol negatif tidak terdapat nilai total leukosit karena pada saat pengamatan ikan uji teIah mengalami
mortalitas 100%.
Peningkatan total leukosit ikan yang diberi Spirulzna platensis lebih tinggi dibandingkan nilai peningkatan leukosit ikan kontrol negatif, namun lebih rendah
bila dibandingkan dengan nilai leukosit ikan kontrol positif. Pada perlakuan dosis Spirulina platensis yang sama, peningkatan total leukosit ikan dengan waktu
pemberian diskontinyu lebih tinggi dibandingkan dengan pemberian secara
kontinyu. Peningkatan total leukosit tertinggi perlakuan Spirulina platensis diperoleh pada pemberian dosis 4% secara diskontinyu. Berdasarkan hasil uji Duncan, ti& terdapat perbedaan yang nyata (P>0.05) antara pemberian Sprrulina platensis 4% dengan 6% secara diskontinyu terhadap peningkatan total leukosit namun berbeda nyata dengan perlakuan yang lainnya nyata (PK0.05) mulai
pengamatan hari ke-14 sampai akhir pengamatan. Hasil analisis statistik pengaruh masing-masing perlakuan terhadap nilai total leukosit per waktu pengamatan
Gambar 1. Rataan total leukosit ikan patin per waktu pengamatan Keterangan: I = kontinyu,
II
= diskontinyuA (K-) = 0% Spiruiina platemis,
B (K+) = 0.06% LPS,
C = 2% Spirulina platensis, D = 4% Spirulina platensis,
[image:105.514.56.432.49.465.2]Jenis Leu kosit
Pemeriksaan dan identifikasi ulas darah diketahui jenis-jenis leukosit ikan
patin yang terdiri dari sel limfosit, monosit, netrofil d m trombosit.
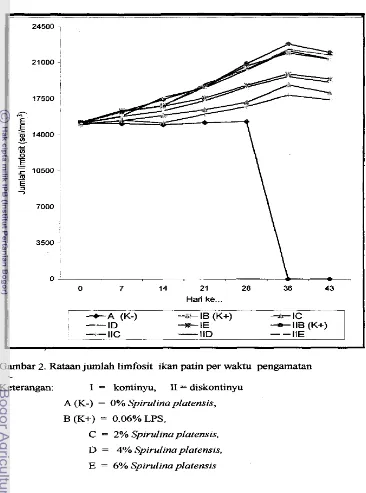
Rataan jurnlah limfosit ikan uji per waktu pengamatan ditampilkan pada
Gambar 2. Rataan jurnlah limfosit cenderung meningkat sampai hari ke- 36 dan menurun hari ke- 43. Rataan jumlah Iimfosit ikan (hari ke-7 sampai ke-28) pada
kontrol negatif antara 15102-15300 sel/mm3, kontrol positif berkisar antara
16243-20897 sel/mm3, dan perlakuan Spirulina platensis antara 15377-20380 sel/mm3. Peningkatan jumlah limfosit ikan yang diberi SpiruZina pZatenszs lebih tinggi dibandingkan jumlah limfosit ikan kontrol negatif, namun lebih rendah bila
dibandingkan dengan jumlah limfosit ikan kontrol positif. Pada perlakuan dosis
Spzdina platensis yang sama, peningkatan jumlah limfosit ikan dengan waktu pemberian diskontinyu lebih tinggi dibandingkan dengan pemberian secara
kontinyu. Peningkatan jumlah limfosit tertinggi perlakuan Spirulina platensis diperoleh pada pemberian dosis 4% secara diskontinyu. Berdasarkan analisis
ragarn terdapat perbedaan yang nyata antara dosis, waktu pemberian seria adanya
-
interaksi antara dosis dengan waktu pemberian (P-=0.05) terhadap peningkatan jumlah limfosit ikan uji Berdasarkan uji Duncan, tidak terdapat perbedaan yang
nyata (P>0.05) antara pemberian Spirulina platemis 4%, 6% clan LPS secara diskontinyu terhadap peningkzttan total leukosit pada hari ke-28. Hasil analisis
pengarub perlakuan terhadap nilai jumlah limfosit per waktu pengamatan
Gambar 2. Rataan jumlah limfosit ikan patin per waktu pengamatan
--
Keterangan: I = kontinyu, I1 = diskontinyu A ( K - ) = 0% Spirulina platensis,
B (K+) = 0.06% LPS,
24500 ;
I
i
i
21000-1
I
1
i
27500
1
C = 2% Spirulina platensis, I
D = 4% Spirulina plafensrs.
.-,
E E 14000-
-
.- V )1
I
e
E .-lOSO0
4
m -
S
7 7000I
3500 i
0 '
0 7 14 21 28 36 43
Hari ke ...
+A (K-) -!v- .+ I6 (K+) I C
8
--
ID-
If-
1 I 3 (K+)---
IIC-
l ID--
I1E2. Monosit
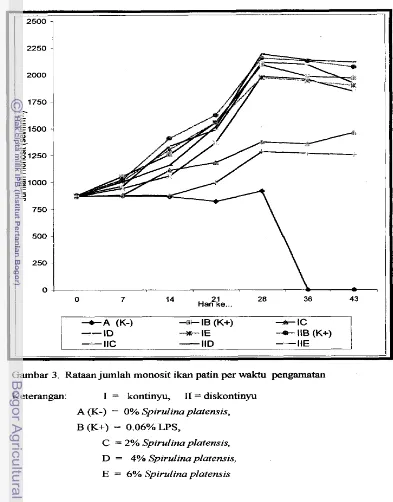
Rataan jumlah monosit ikan uji per waktu pengamatan disajikan pada
Gambar 3. Rataan jumlah monosit cenderung meningkat sampai hari ke- 28 dan
menurun mulai hari ke- 36. Rataan jurnlah monosit ikan (hari ke-7 sampai ke-28)
pada kontrol negatif antara 887-920 sel/mm3, kontrol positif berkisar antara 1027-
2 19 1 se~rnm3, dan perlakuan Spirulina p l a t e m ~ s antara 880-2 154 sel/mm3. Pada pengarnatan hari ke- 36 dan 43 untuk perlakuan kontrol negatif tidak terdapat nilai monosit karena pada saat pengamatan ikan uji telah mengalami mortalitas 100%.
Peningkatan jumlah monosit ikan yang diberi SpzruIina platensis lebih tinggi dibandingkan nilai peningkaian monosit ikan kontrol negatif, namun lebih
rendah bila dibandingkan dengan nilai monosit ikan kontrol positif. Pada
perlakuan dosis Spiruiina platensis yang sama, peningkatan jurnlah monosit ikan dengan waktu pemberian diskontinyu lebih tinggi dibandingkan dengan
pemberian secara kontinyu. Peningkatan jumlah monosit tertinggi perlakuan
Spirulrna platensis diperoleh pada pemberian dosis 4% secara diskontinyu. Berdasarkan uji Duncan, tidak terdapat perbedaan yang nyata ( m . 0 5 ) antara pernberian Spirulina platensis 496, 6% dan LPS secara diskontinyu terhadap peningkatan jumlah rnonosit mulai pengamatan hari ke-14 sampai ke-28. HasiI
analisis pengaruh masing-masing perlakuan terhadap nilai jumlah monosit per
Gambar 3. Rataan jumlah monosit ikan patin per waktu pengamatan Keterangan: I = kontinyu, I1 = diskontinyu
A (K-) = 0% SpiruZina platensis,
B
( K t ) = 0.06%LPS,
C = 2% Spirulina piatensis, D = 4% Spirulina platensis,
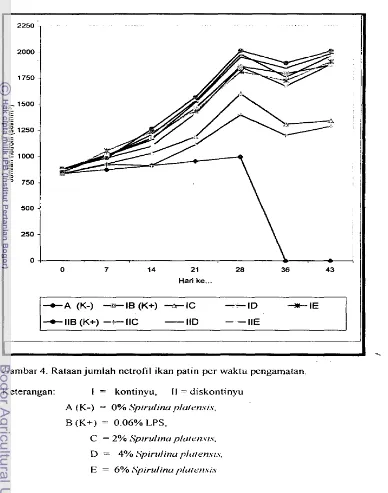
[image:109.522.48.441.53.555.2]3- Netrofii
Rataan jumlah netrofil ikan uji selama pengamatan disajikan pada
Garnbar 4. Rataan jumlah netrofii cenderung meningkat sampai hari ke- 28,
menurun hari ke- 36 dan meningkat Iagi pada hari ke-43. Rataan jurnlah netrofil
ikan (hari ke-7 sampai ke-28) pada kontrol negatif antara 874-997 sel/mm3,
kontrol positif berkisar antara 987-2016 sel/mm3, dan perlakuan SpiruZina
platensis antara 992-1982 sel/mm3. Pada pengamatan hari ke- 36 dan 43 untuk perlakuan kontrol negatif tidak terdapat nilai netrofil karena pada saat pengamatan ikan uji telah mengalami mortalitas 100%.
Peningkatan jumlah netrofil ikan yang diberi Spirulina piatensis lebih
tinggi dibandingkan nilai peningkatan netrofil ikan kontrol negatif, narnun Iebih rendah bila dibandingkan dengan netrofil ikan kontrol positif. Pada perlakuan
dosis Spirulina platensis yang sama, peningkatan j u d a h netrofil ikan dengan waktu pemberian diskontinyu lebih tinggi dibandingkan dengan pemberian
secara. Peningkatan jumlah netrofil tertinggi perlakuan Spirulina platensis
diperoleh pada pemberian dosis 4% secara diskontinyu. Berdasarkan uji Duncan,
tidak terdapat perbedaan yang nyata (PXl.05) antara pemberian Spirulznu plufensis 4%, 6% dan LPS secara diskontinyu terhadap peningkatan total netrofil pada hari ke-14 sampai ke-28. Hasil analisis pengaruh masing-masing perlakuan
terhadap nilai jumlah netrofil per waktu pengamatan selengkapnya disajikan pada
Gambar 4. Rataan jumiah netrofil ikan patin per waktu pengamatan.
2250
2000
1750
-
15000.
E
E 5
1 1250
-
E2
-
Keterangan: I = kontinyu, 11
-
diskontinyu A (K-)
= 0% Spirzilinu plu/r,z.s~.v. 3 (K+) = 0.06% LPS,C = 2% Spirulinu p/u/er~.vrs.
D = 4% Spirulinu p/trtc.n.srs.
E = 6% Spirulinu plu/c.n.\i.s
.-
I
s
1000C
-
S
750 500I
250 i 00 7 14 21 28 36 43
Hari ke
...
&A (K-)
-*
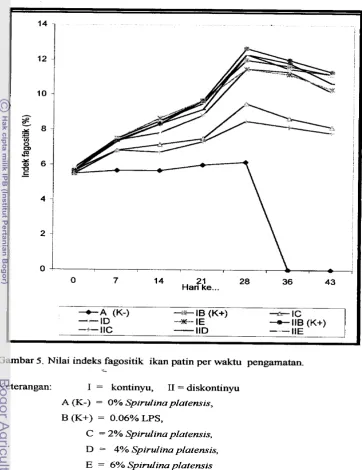
lB (K+) -'slCIndeks Fagositik
Rataan indeks fagositik per waktu pengamatan dsajikan pada Gambar 5.
Rataan indeks fagositik cenderung meningkat sampai hari ke- 28 dan menurun mulai hari ke- 36. Rataan indeks fagositik ikan (hari ke-7 sampai ke-28) pada
kontrol negatif antara 5.67-6.17 sel/mm3, kontrol positif berkisar antara 7.40-
12.67 sel/mm3, dan perlakuan Spirulzna piatensis antara 6.73- 12.33 seL/mm3. Peningkatan indeks fagositik ikan yang diberi Spirulina platensis lebih tinggi dibandingkan nilai peningkatan indeks fagositik ikan kontrol negatif,
namun lebih rendah bila dibandingkan dengan indeks fagositik ikan kontrol positif. Pada perlakuan dosis Spirulina platensis yang sama, peningkatan jumlah indeks fagositik ikan dengan wakku pemberian diskontinyu lebih tinggi
dibandingkan dengan pemberian secara kontinyu. Peningkatan jumlah indeks
fagositik tertinggi perlakuan Spirulina plafensis diperoleh pada pemberian dosis 4% secara diskontinyu. Berdasarkan uji Duncan, tidak terdapat perbedaan yang
nyata (P>0.05) antara pemberian Spirulina platensis 4%, 6% dan LPS secara diskontinyu terhadap peningkatan indeks fagositik pada hari ke-7 sampai ke-28.
Hasil analisis pengaruh masing-masing perlakuan terhadap nilai indeks fagositik
Gambar 5 . Nilai indeks fagositik ikan patin per waktu pengamatan. -
Keterangan: I = kontinyu, I1 = diskontinyu A ( K - ) = 0% Sprrulinaplatensis,
B (K+) = 0.06% LPS,
Kadar Hematokrit
Kadar hematolait ikan patin disajikan pada Lampiran 6. Nilai hematokrit
cenderung meningkat sampai pengamatan hari ke- 28 dan menurun pada hari ke-
36. Pada pengamatan hari ke- 36 clan 43 untuk kontrol negatif tidak terdapat nilai
hematokrit karena pada saat pengamatan tersebut ikan uji telah mengalami
mortalitas 100%. Rataan nilai hematokrit (hari ke-7 sampai ke-28) pada kontrol
positif berkisar antara 3 1.33-33.67 sel/mm3, kontrol negatif antara 30.00-3 1 .OO
sel/mm3 dan perlakuan Spirulina platensis antara 30.00-33.33 sel/mm3 Berdasarkan uji Duncan, tidak terdapat perbedaan yang nyata antara pemberian
Spirulina platensis 496, 6% dan LPS baik yang dberikan secara kontinyu maupun diskontinyu terhadap nilai hematolait per waktu pengamatan (F'Xl.05).
Gejala Klinis dan Tingkat KeIangsuogan Hidup
Perkembangan gejala klinis ikan uji diamati setelah dilakukan uji tantang
dengan Aeroinonas hydrophila. Ikan uji kontrol positif dan ikan yang diberi perlakuan Spirulina platensis mengalami kemerahan (hiperemi), peradangan (inflamasi),' nekrosis dan ulser. Ikan uji kontrol negatif mengalami mortalitas 100% (jam ke- 10 - 24 pasca penginfeksian). Pada jam ke-10 pasca
--
penginfeksian, ikan yang diberi Spirulina platensis clan LPS terlihat timbulnya nekrosis yang diikuti ulser pada jam ke-24. Selanjutnya ulser semakin melebar
dan &lam serta pergerakan ikan menjadi lambat. Ikan dengan sistem kekebalan rendah mengalami mortalitas, sedangkan ikan yang memiliki respon kekebalan tinggi bertahan hidup. GejaIa klinis setelah dilakukan uji tantang setiap perlakuan
Tabel 2. Gejala klinis ikan patin (Pangasiurr djambaZ) setelah uji tantang dengan Aeromonas hydrophila
Hari ke.. . Gejala Klinis
Hiperemi dan inflamasi, mortalitas total ikan konirol negatif
U s e r mulai terbentuk, daging berwama merah pucat, perut
membusung; mortaLitas mulai terjadi pada perlakuan Spirulina platensis clan konirol positif
Ulser membesar dan dalam, warna daging merah tua, skip
mengalami kerusakan, perut membusung; mortalitas terbanyak
pada perlakuan dosis Spirulina platensis 2%
Perkembangan ulser menurun, warna daging menjadi merah
P U d
Ulser menyempif warna daging kuning pucat
Ulsa semakin kecil, warna d@ng makin pucat
Ulser pada sebagian ikan menghilang dan pergerakan ikan
menjadi normal
Tingkat kelangsungan hidup ikan patin yang diberi Spirulina platensis dan LPS setelah dilakukan uji tantang dengan Aeromonas hydrophila diperoieh nilai seperti disajikan pada Lampiran 7. Tingkat kelangsungan hidup ikan uji
tertinggi diperoleh pada pemberian LPS secara diskontinyu (83.3%) diikuti
pemberian SpiruZina platensis 4% diskontinyu ( 76.7%) sedangkan pada perlakuan kontrol negatif, ikan uji mengalami mortalitas 100% setelah uji tantang
[image:115.524.57.450.50.597.2]PEMBAEIASAN
Penambahan Spirulina platensis dalam pakan ikan sebanyak 296, 4% dan 6% baik secara kontinyu maupun diskontinyu dapat meningkatkan respon kekebalan ikan patin. Peningkatan ini dapat dilihat dari meningkatnya total
leukosit, jenis leukosit, nilai indeks fagositik serta adanya perbedaan tingkat
kelangsungan hidup ikan setelah dilakukan uji tantang dengan Aeromonas hydrophila, seperti yang disebutkan Sakai (1998) dan Hendrikson (2000) bahwa Spirulina platensis berpotensi dalam meningkatkan sistem kekebalan beberapa jenis hewan termasuk ikan.
Peningkatan kekebalan ikan patin dengan pemberian Spirulina platensis lebih rendah dibandingkan dengan pemberian lipopolisakarida (LPS) yang
digunakan sebagai kontrol positif. Hal ini dimungkinkan karena lipopolisakarida
yang terkandung dalam Spirulina platensis masih lebih rendah dibanding dosis lipopolisakarida yang digunakan dalam kontrol positif. Ikan yang tidak diberi
Spzrulina platensis sebagi kontrol negatif menunjukkan respon kekebalan paling rendah dari semua perlakuan, ha1 ini diketahui dari nilai total leukosit paling
rendah dan tingkat mortalitas ikan mencapai 100% setelah uji tantang. Kondisi ini membuktikan bahwa ikan yang tidak diberi Spirulina platemis tidak tejadi stimulasi imunogenik yang cukup untuk merespon masuknya patogen dan menghambat perkembangan infeksinya.
(pengarnatan hari ke-7 setelah uji tantang) rnerupakan pengaruh imunostimulan
dan adanya infeksi bakteri. Sesuai penjelasan Anderson dan Siwicki (1995) bahwa peningkatnya total leukosit dapat terjadi karena adanya infeksi, stress ataupun
penyakit darah. Peningkatnya total leukosit pada ikan patin yang diberi Spirulina platensis dapat digunakan sebagai suatu tanda rneningjcatnya sistem pertahanan
seluler ikan tersebut
Jenis leukosit ikan patin terdiri dari limfosit, monosit, netrofil dan
trornbosit. Ferguson (1989) menjelaskih bahwa selain keempat jenis leukosit tersebut kadang-kadang dijumpai eosinofiI dan basofil, namun dari hasil pemeriksaan clan identifikasi ulas darah ikan patin tidak 'ditemukan adanya eosinofil dan basofil. Adanya peningkatan total leukosit dan jumlah jenis leukosit karena adanya aktivitas pernbelahan sel. Hal ini dimungkinkan karena Spirulina platensis mengandung Iipopolisakarida yang bersifat imunogenik. Rorstad et al. (1993) dalam Alifiddin (1999) menyebutkan bahwa senyawa Iipopolisakarida (LPS) bersifat imunogenik dan telah terbukti secara invitro dapat rneningkatkan
jumlah sel leukosit. Senyawa imunogenik akan mengaktifkan sel pertahanan untuk berdiferensiasi, rnenyebabkan te jadinya sintesa DNA pada sel limfosit
yang berakibat meningkatkan total Ieukosit
dan
jumlah jenis leukosit.Peningkatan dan penurunan jumlah netrofil dan monosit erat kaitannya
dengan perannya sebagai garis pertahanan ikan. Netrofil mernpunyai ke j a yang
cepat namun tidak mampu bertahan lama karena mernpunyai cadangan energi yang terbatas. Hal ini diduga penyebab turunnya jumlah netrofil lebih besar
menghrtsilkan makrofag (monosit); aktivitas monosit bertahan lebih lama dan
mampu mengolah antigen sebagai persizpan proses tanggap kebal berikutnya.
Kondisi ini menyebabkan meningkatnya jumlah monosit dan bertahan relatif
stabil setelah dilakukan uji tantang hingga akhir pengamatan.
Indeks fagositik merupakan manifestasi dari aktifitas fagositosis respon
seluler. Respon seluler ini dilakukan oleh sel-sel fagositik seperti monosit,
netrofil dan makrofag. Sel fagositik akan memfagosit benda asing atau bakteri
yang masuk ke dalam tubuh ikan meldui proses kemotaksis, perlekatan,
penelanan, dan pencemaan (Tizard 1988). Peningkatan nilai indeks fagositik
mengindikasikan terjadinya periingkatan aktifitas fagositosis pada ikan yang
diberi
S'irulina
plafensis. Hal ini menunjukan bahwa ikan yang diberi Spirulina platensis mempunyai kemampuan pertahanan non-spesifik yang lebih besar dibandingkan dengan ikan yang tidak diberi S p i d i n a p l a t e m i s ( kontroI negatif). Nilai indeks fagositik ikan patin meningkat diduga karena Spirulina platensis mengandung lipopolisakarida yang akan dikenali set makrofag dan merangsangmakrofag untuk mengaktifkan limfosit T. Limfosit T akan memproduksi lebih banyak interferon (limfokin) yang akan membentuk dan mengaktifkan rnakrofag
kembaii, sehingga kemarnpuannya memfagosit bahan asing meningkat. T-ya
.
nilai indeks fagositik setelah uji tantang (hari ke -36 dan hari ke-43) dimungkinkan karena adanya beMeri patogen yang menyebabkan beban ke rja sel
fagosit menjadi lebih besar, sehingga kemampuan memfhgosit bakteri menjadi menurun. Selain itu juga terjadi karena jumlah sel netrofil yang aktif mengalami
Kondisi kesehatan ikan dapat juga diamati melalui pengukuran kadar
hematokrit (Anderson dan Siwiclu 1995). Kadar hematokrit selama pemaparan Spiml~naplatemis berkisar antara 29.67
-
33.33%. Kisaran nilai ini menunjukan kondisi ikan cukup baik, sesuai penjelasan Wedemeyer dan Yasutake (1977)bahwa hematokrit ikan berkisar antara 24-43%. Tejadinya penurunan kadar
hematokrit pada pengamatan minggu pertama (hari ke-36) setelah diinfeksikan dengan Aeromonas hydrophila disebabkan karena meluasnya kerusakan sel dan jaringan oleh produk ekstraseluler (ECP) yang dihasilkan oleh bakteri. Menurut
BIaxhall (1972), nilai hematokrit cenderung menjadi rendah apabila ikan
terserang penyakit atau kehilangan nafsu makan. Peningkatan nilai hematokrit
te ja d i iagi pada akhir pengamam karena kondisi ikan telah membaik.
Setelah dilakukan uji tantang dengan bakteri Aeromonas hydrophila dengan kepadatan bakteri 10' cfu/ml terlihat adanya melanisasi pada bekas penyuntikan dan timbulnya hiperemi kemudian berkembang menjadi nekrosis
yang akhirnya terbentuk ulser. Timbulnya hiperemi pada pmgkal sirip ekor,
dada, dan perut menunjukkan terjadinya mobilisasi leukosit ke jaringan tempat
berkembangnya patogen. Leukosit yang berfungsi sebagai pertahan non-spesifik
akan melokalisasi dan mengeliminasi patogen melalui proses fagositosis pada jaringan. Timbunya nekrosis dan ulser karena adanya substansi ekstraseluler
bakteri seperti protease dan sitotoksin yang dapat menghidrolisa clan melisis jaringan inang. Seperti yang disebutkan Huizinga dan Brenden (1986) bahwa nekrosis dapat timbul akibat aktifitas enzim protease. Enzim ini akan memecah
protein menjadi senyawa-senyawa yang lebih sederhana sehingga akan merusak
Diantara variasi perlakuan Spirulina platensis yang telah dicobakan,
tingkat kelangsungan hidup ikan pemberian 4% lebih baik dari 6% pada
pemberian diskontinyu dengan nilai masing-masing adalah 76.6% dan 73.3%, sedangkan pada pemberian 4% dan 6% secara kontinyu diperoleh nilai
kelangsungan hidup ikan yang sama (66.7%). Tingkat kelangsungan hidup ikan
uji berkaitan dengan waktu dan dosis yang diberikan. Pemberian dosis yang tinggi dan waktu yang lama dapat menyebabkan penekanan mekanisme
pertahanan, sebaliknya pernberian dosis rendah dan waktu yang singkat menjadi tidak efektif. Hal ini diduga karena pada konsentrasi tinggi LPS bersifat toksik
seperti yang dijelaskan oIeh Hannesse dan Bakeer (1997), bahwa penggunaan
preparat LPS sebagai terapeutik dibatasi ol