UJI SITOTOKSISITAS DAN AKTIVITAS EKSTRAK
DAUN LEUNCA (
Solanum nigrum
L) TERHADAP
KELARUTAN KALSIUM OKSALAT
DENI SUHENDAR
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Uji Sitotoksisitas dan Aktivitas Ekstrak Daun Leunca (Solanum nigrum L) terhadap Kelarutan Kalsium Oksalat adalah benar karya saya denganarahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
ABSTRAK
DENI SUHENDAR. Uji Sitotoksisitas dan AktivitasEkstrak Daun Leunca (Solanum nigrum L.) Terhadap Kelarutan Kalsium Oksalat. Dibimbing oleh EMAN KUSTAMAN dan DIMAS ANDRIANTO.
Berbagai penelitian membuktikan bahwa tanaman leunca terutama bagian buah dan daunnya memiliki banyak aktivitas farmakologi. Penelitian ini bertujuan menguji komponen-komponen bioaktif ekstrak daun leunca secara kualitatif,sitotoksisitas dan aktivitas ekstrak daun leunca terhadap kelarutan kalsium oksalat yang merupakan bahan utama penyusun batu ginjal. Ekstraksi daun leunca dilakukan secara maserasi menggunakan berbagai macam pelarut, yaitu air, etanol (30%, 70% dan 96%). Berdasarkan hasil ekstraksi diperoleh rendemen ekstrak pelarut air, etanol30%, etanol 70% dan etanol 96% berturut-turut sebesar 39.7, 19.0, 17.7 dan 26.6%. Komponen fitokimia yang terdapat dalam daun leunca adalah alkaloid, flavonoid, tannin dan saponin. Hasil pengukuran kadar kalsium menggunakan turbidimetri dan metode AAS menunjukkan penurunan kadar kalsium. Penurunan terbaik terdapat pada penambahan ekstrak pelarut air dengan konsentrasi 1.5 %.Hasil uji potensi hayati menunjukkan bahwa ekstrak terbaik dimiliki oleh ekstrak air dengan nilai LC50 sebesar 136.44 ppm.
ABSTRACT
DENI SUHENDAR. Leunca Leaf Extract Activity (Solanum nigrum L.) Through Calcium Oxalate Solubility. Supervised by EMAN KUSTAMAN and DIMAS ANDRIANTO.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Biokimia
UJI SITOTOKSISITASDAN AKTIVITAS EKSTRAK
DAUN LEUNCA (
Solanum nigrum
L) TERHADAP
KELARUTAN KALSIUM OKSALAT
DENI SUHENDAR
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
Judul Skripsi :Uji Sitotoksisitas dan AktivitasEkstrak Daun Leunca (Solanum nigrum L) Terhadap Kelarutan Kalsium Oksalat
Nama : Deni Suhendar NIM : G84080020
Disetujui oleh
Ir Eman Kustaman Pembimbing I
Diketahui oleh
Dimas Andrianto, MSi Pembimbing II
Dr Ir I Made Artika, MAppSc Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Februari 2012 ini ialah aktivitas daun leunca, dengan judul Uji Sitotoksisitas dan AktivitasEkstrak Daun Leunca (Solanum nigrum L) terhadap Kelarutan Kalsium Oksalat.
Terima kasih penulis ucapkan kepada BapakIr Eman Kustaman dan Bapak Dimas Andrianto, M.Si selaku pembimbingyang telah banyak memberi saran dalam penyusunan karya ilmiah ini. Di samping itu, Di samping itu, terima kasih pula kepada Dhian Anugerah, Hana Filya dan Aneisti Septiani yang telah banyak membantu dalam pengerjaan penelitian ini. Ungkapan terima kasih juga disampaikan kepada ayah, ibu, serta seluruh keluarga, atas segala doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
METODE 2
Bahan dan Alat 2
Prosedur Percobaan 2
HASIL DAN PEMBAHASAN 4
SIMPULAN DAN SARAN 9
Simpulan 10
Saran 10
DAFTAR PUSTAKA 10
LAMPIRAN 12
DAFTAR TABEL
1 Rendemen ekstrak daun leunca (Solanum nigrum L.) ... 5
2 Hasil Uji Fitokimia ... 5
3 Hasil Analisis Probit ... 6
DAFTAR GAMBAR
1 Hasil Pengukuran Kadar Kalsium Metode Turbidimetri ... 62 Hasil Pengukuran Kadar Kalsium Metode AAS ... 7
DAFTAR LAMPIRAN
1 Strategi Penelitian ... 122 Prosedur Ekstraksi (BPOM 2005)... 13
3 Rendemen Ekstrak ... 14
4 Kadar Air Daun Leunca ... 14
5 Uji Fitokimia ... 15
6 Hasil Pengukuran Kadar Kalsium dengan Turbidimetri ... 15
7 Hasil Pengukuran Kadar Kalsium dengan AAS ... 16
8 Uji Sitotoksisitas ... 17
PENDAHULUAN
Data badan kesehatan dunia (WHO) pada tahun 2008 mencatat bahwa penyakit batu ginjal di Amerika Serikat dilaporkan 0,1-0,3% penduduknya per tahun dan sekitar 5-10% penduduknya sekali dalam hidupnya pernah menderita penyakit tersebut. Di Eropa Utara, ada 3-6% penduduknya menderita batu ginjal, sedangkan di Eropa Bagian Selatan, di sekitar Laut Tengah 6-9% penduduknya per tahun juga menderita penyakit ini.. Di Jepang sendiri terdapat 7% penduduknya juga mengalami penyakit batu ginjal per tahunnya dan di Taiwan terdapat 9,8% dari penduduknya per tahun. Sedangkan di Indonesia sampai saat ini angka kejadian batu ginjal yang sesungguhnya belum diketahui secara pasti, diperkirakan 170.000 kasus per tahun (Wahyuni 2008).
Pengobatan yang dilakukan untuk mengatasi batu ginjal ini bisa dengan operasi, teknologi laser, ultrasonikasi, penggunaan obat-obatan sintetik, maupun herbal. Pengobatan dengan operasi dapat dilakukan dalam kurun waktu yang cukup singkat. Akan tetapi, alternatif dengan pengobatan ini terbentur akan masalah finansial. Sedangkan pengobatan dengan obat-obatan sintetik umumnya akan memiliki efek samping yang dapat muncul dalam kurun waktu tertentu, seperti akumulasi zat kimia yang dapat memicu kanker. Pengobatan dengan bahan alami atau herbal yang telah diketahui dan dikembangkan oleh masyarakat adalah dengan penggunaan tanaman kumis kucing. Kandungan ortosifonin glikosida dan garam kalium (terutama pada daunnya) dapat mencegah terjadinya endapan batu ginjal. Selain itu, ada tanaman lain yang diduga berpotensi meluruhkan batu ginjal yaitu leunca (Solanum nigrum L).
Populasi yang banyak dan syarat hidup atau kultur yang relatif sederhana menyebabkan tanaman leunca mudah diperoleh di Indonesia. Selain buahnya dipakai untuk sayuran, tanaman ini sudah lama dikenal bisa dipakai sebagai obat,terutama daunnya. Daun memiliki efek sedatif (menenangkan), diuretik (memperlancar air seni), dan ekspektoran (mengencerkan dahak). Daun leunca bisa dimanfaatkan sebagai tonik dan diuretik. Daun leunca juga dapat digunakan sebagai obat anti bakteri yang dapat mengobati penyakit gonorhoe dan anti kanker. Tanaman leunca ini juga dapat digunakan sebagai obat pembengkakan, peradangan, rematik dan wasir. Selain buah dan daunnya, getahnya dapat digunakan untuk obat kulit dan kutilan. Daun dan buah tanaman leunca banyak mengandung senyawa glikoalkaloid solanin, solasonin, solamargin, solasodin, solanidin, diosgenin, tigogenin, atropin, saponin, kalsium, fosfor, zat besi, vitamin A dan vitamin C. Adanya aktivitas dari senyawa metabolit sekunder tanaman leunca khususnya pada daun diduga dapat meluruhkan batu ginjal.
2
METODE
Bahan dan Alat
Bahan yang digunakan, yaitu daun leunca, akuades, etanol 30%, etanol 70%, etanol 96%, obat herbal, obat sintetik, kloroform, kristal kalsium oksalat, pereaksi Dragendorf, pereaksi Mayer, pereaksi Wagner, pereaksi Liebermann-Buchard, pereaksi Molisch, H2SO4 pekat, metanol, kristal NaOH, NaCl, FeCl3, NH4OH, MgSO4, buffer fosfat, KCl, CaCO3, Urea, dan HNO3 pekat.
Alat-alat yang digunakan, yaitu labu Erlenmeyer, gelas piala, labu takar, rotary evaporator, sudip, pengaduk gelas, eksikator, spektrofotometer serapan atom, turbidimeter, botol kaca bertutup, pipet Mohr, pipet tetes, tabung reaksi, gegep, oven, pH meter, blender, saringan, corong, kertas saring Whatman 40, neraca analitik, penangas air, cawan Petri, cawan porselen, gelas ukur, mortar, plastik, dan alumunium foil.
Prosedur Percobaan
Pembuatan Simplisia Daun Leunca (Solanum nigrum L)
Proses pembuatan simplisia daun leunca diawali dengan pemilihan daun leunca yang masih segar. Daun leunca kemudian dicuci bersih dan dirajang. Perajangan dilakukan untuk membantu mempercepat proses pengeringan. Rajangan dikeringkan di bawah sinar matahari sampai daun kering. Setelah itu daun dimasukkan dalam oven selama semalam (over night) untuk menghilangkan uap air yang masih tersisa dari proses pengeringan. Daun tersebut dihancurkan dengan blender untuk memperbesar luas permukaan partikel agar kontak antara bahan dan pelarut lebih besar.
Ekstraksi Daun Leunca (Solanum nigrum L) (BPOM 2005)
Simplisia daun tanaman leunca (Solanum nigrum L) yang sudah dikeringkan, timbang. sampai mencukupi sebanyak 30 gram. Simplisia dimaserasi menggunakan 150 mL pelarut uji, yaitu akuades, etanol 30%, etanol 70% dan etanol 96% di dalam labu Erlenmeyer 250 mL sambil diaduk menggunakan shaker selama 24 jam kemudian di saring. Filtrat dipisahkan dan proses diulang dua kali dengan jenis dan jumlah pelarut yang sama. Filtrat dievaporasi menggunakan rotary evaporator pada suhu 50°C hingga diperoleh ekstrak yang kering.
3 diperoleh dari pengurangan bobot cawan ditambah bahan uji dengan bobot cawan kosong.
Uji Fitokimia pada Ekstrak Daun Leunca (Harbone 1987)
Uji Alkaloid. Sebanyak 500 mg masing-masing bahan uji digerus kemudian ditambahkan 5 mL kloroform dan 3 tetes ammonia 25%. Filtrat diambil dan ditambahkan pereaksi Dragendorff, Mayer dan Wagner dalam tabung terpisah. Alkaloid dalam sampel ditandai dengan terbentuknya endapan merah setelah ditambah pereaksi Dragendorff, terbentuk endapan putih setelah penambahan pereaksi Mayer dan endapan coklat setelah penambahan pereaksi Wagner.
Uji Flavonoid. Sebanyak 500 mg masing-masing bahan uji ditambahkan 5 mL metanol 30% lalu dipanaskan selama 5 menit dan saring. Sebanyak 5 tetes NaOH 10% atau H2SO4 pekat ditambahkan ke dalam filtrat. Flavonoid ditunjukkan oleh warna merah yang terbentuk setelah penambahan asam sulfat pekat.
Uji Saponin. Timbang masing-masing 500 mg bahan uji dan dalam 100 mL air panas selama 5 menit. Pipet sebanyak 10 mL dan masukkan ke dalam tabung reaksi. Kocok kuat secara vertikal selama 10 detik. Saponin ditunjukkan oleh terbentuknya busa setinggi 1 sampai 10 cm yang stabil selama kurang 10 menit dan tidak hilang dengan penambahan asam klorida 2 N.
Uji Tanin. Sebanyak 500 mg dari masing-masing bahan uji ditambahkan 5 mL aquades. Setelah itu, campuran dididihkan selama 5 menit. Campuran disaring dan filtratnya ditambahkan 5 tetes FeCl3 1%. Tanin ditunjukkan oleh terbentuknya warna biru tua atau hijau-kehitaman.
Uji Steroid dan Triterpenoid. Sebanyak 50 mg ekstrak ditambah asam asetat anhidrida sampai terendam dalam tabung reaksi dan dipanaskan selama 5 menit. Setelah dipanaskan, campuran ekstrak didinginkan dan kemudian ditambahkan 1 tetes H2SO4 pekat melalui sisi tabung. Cincin berwarna coklat akan terbentuk pada dua lapisan cairan. Warna hijau pada lapisan atas menunjukkan adanya steroid, sedangkan warna merah pada lapisan bawah menunjukan adanya triterpenoid.
Uji Fenolik. Sebanyak 0.1 gram masing-masing bahan uji ditimbang dan dimasukkan ke dalam tabung reaksi. Kemudian ditambahkan 2 ml etanol 20 % ke dalamnya lalu dipanaskan dan disaring. Filtrat ditambahkan dengan 3 tetes NaOH. Larutan berubah menjadi merah menunjukan positif mengandung polifenol.
Uji Molisch. Sebanyak 1 gram masing-masing bahan uji ditimbang dan ditambahkan 5 ml akuades ke dalam tabung reaksi. Pereaksi Molisch ditambahkan sebanyak 2 tetes dan dicampurkan merata. Kemudian ditambahkan perlahan-lahan melalui dinding tabung sebanyak 3 ml asam sulfat pekat. Warna violet (ungu) kemerahan pada batas kedua cairan menunjukkan reaksi positif.
Analisis Kadar Kalsium Oksalat
4
etanol 96 % 0.5 gram, obat herbal 0.5 ml, dan obat sintetik 0.5 gram. Masing-masing bahan uji ditambahkan ke dalam 50 ml larutan kalsium oksalat 4000 ppm pada botol penyimpanan. Sebanyak 2 ml campuran kalsium oksalat dan bahan uji dimasukkan ke dalam botol dan ditambahkan 18 ml urin buatan sehingga konsentrasinya menjadi 400 ppm. Kemudian larutan sebanyak 20 ml tersebut diukur dengan turbidimeter. Sisa larutan di dalam botol penyimpanan didiamkan selama 6 jam. Nilai turbiditas diukur setiap penambahan jam dengan interval 1 jam.
Analisis Kadar Kalsium Oksalat metode AAS. Penentuan kadar kalsium oksalat dengan spektrofotometer serapan atom dilakukan pada ekstrak terbaik dari hasil turbidimetri. Sebanyak 0.64 gram kristal kalsium oksalat dilarutkan dengan urin buatan dalam labu takar 50 ml. Ulangi prosedur sebelumnya sebanyak 5 kali. Sebuah botol berisi larutan digunakan sebagai blanko. Siapkan ekstrak terbaik sebanyak 0.25 gram, 0.5 gram, 0.75 gram dan 1 gram. Masing-masing ekstrak dimasukkan ke dalam 50 ml larutan kalsium oksalat 4000 ppm pada botol penyimpanan. Sebanyak 10 ml campuran larutan kalsium oksalat dan ekstrak disaring. Filtrat sebanyak 0.125 ml dimasukkan ke dalam labu takar 50 ml dan ditera dengan menggunakan urin buatan. Larutan tersebut diukur kadar kalsiumnya dengan spektrofotometer serapan atom. Sisa larutan dalam botol penyimpanan didiamkan selama 6 jam. Ulangi prosedur yang sama untuk filtrat setelah 6 jam perlakuan.
Uji Sitotoksisitas Ekstrak Daun Leunca terhadap A. salina
Penetesan kista. Kista larva udang (A. salina) yang sudah ditetaskan ditimbang sebanyak 50 mg kemudian dimasukkan ke dalam wadah yang berisi air laut yang sudah disaring, dan kemudian diaerasi. Kista dibiarkan selama 48 jam di bawah pencahayaan lampu agar menetas sempurna. Larva yang sudah menetas diambil untuk uji toksisitas.
Uji sitotoksisitas. Sebanyak 10 ekor larva udang dimasukkan ke dalam vial yang berisi air laut kemudian ditambahkan larutan ekstrak kasar dan ditepatkan volumenya dengan air laut sehingga konsentrasi akhirnya menjadi 50, 200, 500, dan 1000 ppm. Pengamatan dilakukan setelah 24 jam dengan menghitung jumlah larva yang mati dari total larva yang dimasukkan ke dalam vial. Pengamatan memakai bantuan cahaya lampu neon. Pengolahan data persen mortalitas kumulatif digunakan analisis probit LC50 dengan selang kepercayaan 95%.
HASIL DAN PEMBAHASAN
Hasil
Kadar Air dan Kandungan Ekstrak
5 Tabel 1 Rendemen ekstrak daun leunca (Solanum nigrum L.)
Pelarut Rendemen (%)
Air 39.67
Etanol 30% 19.00
Etanol 70% 17.66
Etanol 96% 26.63
Hasil maserasi ekstrak air, etanol 30%, etanol 70% dan etanol 96% dari 30 gram simplisia daun leunca masing-masing dihasilkan maserat (ekstrak) sebesar 11.9, 5.7, 5.3 dan 7.9 gram. Berdasarkan hasil tersebut, ekstrak air memiliki persentase rendemen tertinggi dibandingkan ketiga jenis ekstrak lainnya, yaitu sebesar 39.67% sedangkan persentase rendemen terendah dimiliki oleh ekstrak etanol 70% dengan nilai sebesar 5.3% (Tabel 1).
Uji Fitokimia
Hasil pengujian fitokimia ekstrak daun leunca berbagai pelarut dapat dilihat pada tabel 2. Berdasarkan hasil uji fitokimia ekstrak daun leunca memiliki senyawa golongan alkaloid, flavonoid, tanin dan saponin. Sedangkan dari hasil pengujian fitokimia semua ekstrak tidak mengandung senyawa steroid, triterpenoid dan fenolik karena tidak menunjukan warna hijau pada steroid, warna mereah pada triterpenoid dan warna merah pada fenolik.
Tabel 2 Hasil uji fitokimia Uji
Brine Shrimp Lethality Test (BSLT)
6
Tabel 3 Hasil analisis probit
Sampel LC50 (ppm)
Ekstrak air 136.435
Ekstrak etanol 30% 247.937
Ekstrak etanol 70% 154.338
Ekstrak etanol 96% 146.623
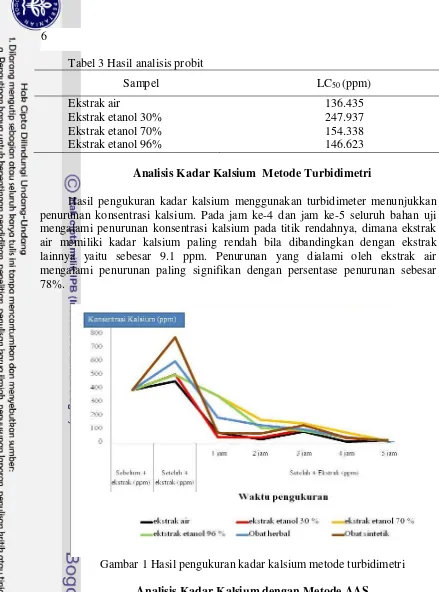
Analisis Kadar Kalsium Metode Turbidimetri
Hasil pengukuran kadar kalsium menggunakan turbidimeter menunjukkan penurunan konsentrasi kalsium. Pada jam ke-4 dan jam ke-5 seluruh bahan uji mengalami penurunan konsentrasi kalsium pada titik rendahnya, dimana ekstrak air memiliki kadar kalsium paling rendah bila dibandingkan dengan ekstrak lainnya yaitu sebesar 9.1 ppm. Penurunan yang dialami oleh ekstrak air mengalami penurunan paling signifikan dengan persentase penurunan sebesar 78%.
Gambar 1 Hasil pengukuran kadar kalsium metode turbidimetri Analisis Kadar Kalsium dengan Metode AAS
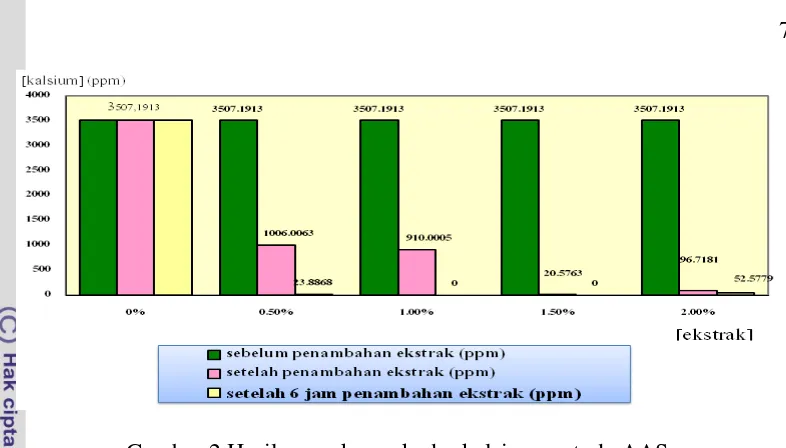
7
Gambar 2 Hasil pengukuran kadar kalsium metode AAS Pembahasan
Kadar Air dan Kandungan Ekstrak
Simplisia daun leunca ditentukan kadar airnya agar dapat diperkirakan cara penyimpanan terbaik bagi sampel untuk menghindari pengaruh aktivitas mikroba.Analisis kadar air dilakukan untuk menentukan masa simpan dari serbuk simplisa. Berdasarkan Keputusan Menteri Kesehatan RI nomor 661/MENKES/SK/VII/1994 tentang persyaratan obat tradisional, kadar air simplisia yang diperbolehkan adalah kurang dari 10%. Rerata kadar air simplisia daun leunca yang diperoleh sebesar 8.3%. Hasil tersebut menunjukan bahwa simplisia daun leunca dapat digunakan sebagai obat tradisional.Penentuan kadar air juga digunakan sebagai faktor koreksi dalam perhitungan rendemen ekstrak.
Tahap ekstraksi dilakukan menggunakan empat pelarut dengan satu kali ulangan, yaitu air, etanol 30 %, etanol 70% dan etanol 96%.Hasil maserasi ekstrak air, etanol 30%, etanol 70% dan etanol 96% dari 30 gram simplisia daun leunca masing-masing dihasilkan maserat (ekstrak) sebesar 11.9, 5.7, 5.3 dan 7.9 gram.Berdasarkan hasil tersebut, ekstrak air memiliki persentase rendemen tertinggi dibandingkan ketiga jenis ekstrak lainnya, yaitu sebesar 39.67%, sedangkan persentase rendemen terendah dimiliki oleh ekstrak etanol 70% dengan nilai sebesar 5.3%. Senyawa bioaktif yang terlarut dalam keempat pelarut tersebut diharapkan memiliki aktivitas sebagai obat herbal peluruh batu ginjal yang akan diuji pada tahap selanjutnya. Perbedaan jumlah rendemen pada setiap ekstrak tersebut dikarenakan pada ekstrak dengan rendemen tertinggi mengandung lebih banyak senyawa yang mudah larut dalam air, sedangkan ekstrak dengan rendemen yang lebih rendah yaitu ekstrak etanol 70% mengandung sejumlah senyawa yang kurang larut dalam etanol.
8
keuntungan, diantaranya dapat menyebabkan komponen senyawa yang terkandung di dalam sampel dapat terekstrak lebih banyak, karena dapat mengekstrak komponen kimia yang tahan panas dan tidak tahan panas (Harborne 1987).
Etanol dapat melarutkan secara keseluruhan semua zat aktif yang terkandung di dalam simplisia, baik yang bersifat polar, semi polar, maupun kurang polar. Etanol dapat menarik senyawa alkaloid, steroid, saponin, flavonoid, antakuinon, dan glikosida. Sedangkan akuades digunakan sebagai pelarut karena umum digunakan dalam proses ekstraksi pada kehidupan sehari-hari. Sampel daun leunca yang digunakan pada penelitian ini berbentuk daun segar(Harborne 1987).
Uji Fitokimia
Metode pengujian untuk melihat secara kualitatif senyawa-senyawa bioaktif dari suatu tanaman dikenal dengan istilah uji fitokimia. Efek farmakologi yang ditimbulkan oleh ekstrak kasar tanaman diduga bersinergi dengan senyawa-senyawa bioaktif yang terdapat di dalam tanaman tersebut. Senyawa-senyawa-senyawa bioaktif dari suatu tanaman yang sering diidentifikasi diantaranya adalah alkaloid, flavonoid, tannin, steroid, terpenoid, saponin (Vagashiya et al 2011).
Perbedaan jenis pelarut yang digunakan dalam proses ekstraksi memberikan hasil yang berbeda terhadap senyawa fitokimia yang terdapat pada daun leunca. Berbagai aktivitas biologis yang ditimbulkan oleh tumbuhan sangat dipengaruhi oleh komponen-komponen fitokimia yang terkandung didalamnya, seperti flavonoid dan fenol (antimikroba, antioksidan, antikanker).
Hasil pengujian fitokimia ekstrak daun leunca pada berbagai pelarut menunjukkan adanya senyawa golongan alkaloid, flavonoid, tanin dan saponin. Sedangkan dari hasil pengujian fitokimia semua ekstrak tidak mengandung senyawa steroid, triterpenoid dan fenolik karena tidak menunjukan warna hijau pada steroid, warna mereah pad;a triterpenoid dan warna merah pada fenolik. Metabolit sekunder merupakan senyawa kimia yang berasal dari tumbuhan. Metabolit sekunder dapat berupa flavonoid, alkaloida, steroid, terpenoida, fenolik, tannin, saponin, dan glikosida. Senyawa ini di antaranya berfungsi sebagai pelindung terhadap serangan atau gangguan yang ada di sekitarnya dan sebagai antibiotika (Tamin dan Arbain 1995) selain itu juga berpotensi sebagai antioksidan (Pokomi 2001).
Brine Shrimp Lethality Test (BSLT)
Brine Shrimp Lethality Test (BSLT) adalah suatu metode pengujian dengan menggunakan hewan uji yaitu Artemia salina Leach, yang dapat digunakan sebagai bioassay yang sederhana untuk meneliti toksisitas akut suatu senyawa, dengan cara menentukan nilai LC 50 yang dinyatakan dari komponen aktif suatu simplisia maupun bentuk sediaan ekstrak dari suatu tanaman.
9 terganggu. Selain itu, senyawa ini menghambat reseptor perasa pada daerah mulut larva. Hal ini mengakibatkan larva gagal mendapatkan stimulus rasa sehingga tidak mampu mengenali makanannya sehingga larva mati kelaparan.
Penentuan nilai LC50 dilakukan dengan menggunakan analisis probit pada software SPSS 16. Melalui perangkat tersebut dapat ditentukan hubungan linearitas antara konsentrasi sampel terhadap probit kematian dari larva udang. Jumlah letalitas larva udang dihitung secara manual. Kematian larva udang, disebabkan oleh perlakuan pemberian sampel pada konsentrasi 50, 200, 500, dan 1000 ppm.Hasil uji potensi hayati menunjukkan bahwa efek farmakologis terbaik dimiliki oleh ekstrak air dengan nilai LC50 sebesar 136.435 ppm, kemudian diikuti dengan ekstrak etanol 96% dengan nilai LC50 sebesar 146.623 ppm dan ekstrak etanol 70% dengan nilai LC50 sebesar 154.338 ppm. Efek farmakologi terendah dimiliki oleh ekstrak etanol 30% dengan nilai LC50 247.937 ppm. Rendahnya nilai LC50 pada ekstrak air diduga disebabkan oleh banyaknya senyawa bioaktifitas yang terkandung didalam sampel.
Analisis Kadar Kalsium Metode Turbidimetri
Hasil pengukuran kadar kalsium menggunakan turbidimeter menunjukkan penurunan konsentrasi kalsium. Pada jam ke-4 dan jam ke-5 seluruh bahan uji mengalami penurunan konsentrasi kalsium pada titik rendahnya, dimana ekstrak air memiliki kadar kalsium paling rendah bila dibandingkan dengan ekstrak lainnya yaitu sebesar 9.1 ppm. Pada jam ke-6 konsentrasi kalsium kembali mengalami peningkatan. Namun, peningkatan konsentrasi kalsium pada penambahan ekstrak dengan pelarut air cenderung tidak signifikan. Oleh karena itu, ekstrak dengan pelarut air merupakan ekstrak terbaik berdasarkan hasil pengukuran turbidimeter untuk penurunan kadar kalsium. Ekstrak air kemudian dilanjutkan dengan analisis kadar kalsium dengan menggunakan metode AAS.
Ekstrak air merupakan ekstrak terbaik disebabkan karena pada pelarut air memiliki senyawa fitokimia yang lebih banyak dibandingkan dengan pelarut lain, sehingga efek yang ditimbulkan oleh pelarut air menjadi lebih baik dibandingkan pelarut lain. Berdasarkan uji kualitatif salah satu senyawa fitokimia yang terdapat dalam ekstrak air adalah flavonoid. Flavonoid memiliki berbagai khasiat yang salah satunya adalah sebagai perluruh batu ginjal yang berasal dari kalsium. Mekanismenya yaitu dengan cara membentuk kompleks khelat yang stabuil antar logam-logam dengan senyawa flavonoid yang memiliki gugus hidroksil dan gugus karbonil (Pramono 1993).
Analisis Kadar Kalsium dengan Metode AAS
10
SIMPULAN DAN SARAN
Simpulan
Ekstrak air daun leunca memiliki senyawa alkaloid, flavonoid, tanin dan saponin. Hasil pengujian metode turbidimetri menunjukkan bahwa aktivitas terbaik dimiliki oleh ekstrak air yang memiliki kadar kalsium terendah dan memiliki nilai LC50 136.435 ppm. Analisis kadar kalsium melalui Spektrofotometri Serapan Atom didapatkan hasil ekstrak air dengan konsentrasi 1.5% yang merupakan komposisi terbaik.
Saran
Perlu dilakukan penelitian lebih lanjut agar dapat mengetahui secara spesifik senyawa bioaktif yang terkandung dalam daun leunca serta perlu juga dilakukan analisis terhadap ekstrak daun leunca secara in vivo.
DAFTAR PUSTAKA
Basset et al. 1994. Kimia Analisis KualitatifAnorganik. Jakarta : Penerbit BukuKedokteran EGC.
Bintang M. 2010. Biokimia Teknik penelitian.Jakarta : Erlangga.
[BPOM RI] Badan Pengawas Obat dan Makanan Republik Indonesia. 2005.Gerakan Nasional Minum Temulawak. Jakarta : BPOM RI.
Cahyono & Suharjo. 2009. BatuGinjalBagaimana Mencegah dan Mengobatinya. Yogyakarta: Kanisius.
Day RA dan Underwood AL.1986. AnalisisKimia Kuantitatif. Jakarta : Erlangga Harbone JB. 1987. Metode Fitokimia. KosasihPadmawinata dan Iwang Soediro,
penerjemah. Bandung: Institut Tekhnologi Bandung. Terjemahan dari: PhytochemicalMethod.
Harjadi W. 1993. Ilmu Kimia Analitik Dasar.Jakarta : Erlangga.
Herbert RB. 1995. Biosintesis MetabolitSekunder. Semarang: IKIP Press.
Karel M. 1979. Physical Principals of Food Preservation. New York : Marcel Dekker Publ.
Kartesz J. 2004. National Plant Database USA [terhubung berkala]
Kavanagh JP, Jones L, Rao PN. 2000. Calsium oxalate crystallization kinetics studied by oxalate induced turbidity in fresh human urine and artificial urine. Clin Sci 98:151–158.
Khopkar. 2003. Konsep Dasar Kimia Analitik. Jakarta : UI Press
Pokorni. 2001. Antioxidant in Food; Practical Applications. New York : CRC Press.
11 Siemonsma JS and Jansen PCM. 1994. Solanum americanum Merrill, p. 252- 255. In: J.S Siemonsma and K. Piluek (Eds.). Plant Resources of South- East Asia. PROSEA (8): Vegetables. Prosea. Bogor
Sumardjo. 2006. Pengantar Kimia: Buku Panduan Kuliah Mahasiswa Kedokteran dan Program Strata I Fakultas Bioeksakta. Jakarta : Gramedia.
Sundoyo, Bambang S. 2006. Buku AjarPenyakit Dalam Edisi IV . Jakarta : PP Departemen ilmu penyakit dalam.
Skoog DA et al. 2000. Fundamentals of Analytical Chemistry. Philadelphia : Brooks Cole
[SNI] Standar Nasional Indonesia. 1992. SNI 01-2891-1992. Cara uji makanan dan minuman. Jakarta (ID) : Dewan Standarisasi Nasional
Tamin R & D Arbain. 1995. Biodiversityand Survey Etnobotani. Makalah Lokakarya Isolasi Senyawa Berkhasiat Obat. Madang: Kerjasama HEDS-FMIPA Universitas Andalas.
Vaghasiya et al. 2011. Phytochemical analisis of some medical plants from western region of India. J. Med. Plant 5 : 567-576
Wahyuni. 2008. Pemanasan Global Berpotensi Picu Prevalensi Batu Ginjal. Suara Karya 17 Mei 2008
12
Lampiran 1 Strategi Penelitian
Daun Leunca
Ekstraksi dengan air, etanol 30%, etanol 70% dan etanol 96% Pembuatan Simplisia Daun
Leunca
Uji Fitokimia Uji Sitotoksisitas
BSLT dan Analisis LC50 Analisis Kadar
Kalsium Metode Turbidimetri
13 Lampiran 2 Prosedur Ekstraksi (BPOM 2005)
Daun leunca
Pembuatan simplisia daun leunca
Direndam dan diaduk dalam maserator selama 6 jam
Didiamkan selama 24 jam
Maserat dipisahkan dan filtrat diuapkan hingga kental dengan
evaporator pada suhu 50°C
Ekstrak kental ditimbang 15 gram simplisia dilarutkan dalam
14
Lampiran 3 Rendemen Ekstrak
Tabel 2 Rendemen ekstrak daun leunca (Solanum nigrum L) Pelarut Bobot simplisia
(g)
Bobot ekstrak (g) Rendemen ekstrak (%)
15 Lampiran 5 Uji fitokimia
Uji
Lampiran 6 Hasil pengukuran kadar kalsium dengan turbidimetri Sampel
Setelah + Ekstrak (ppm)
16
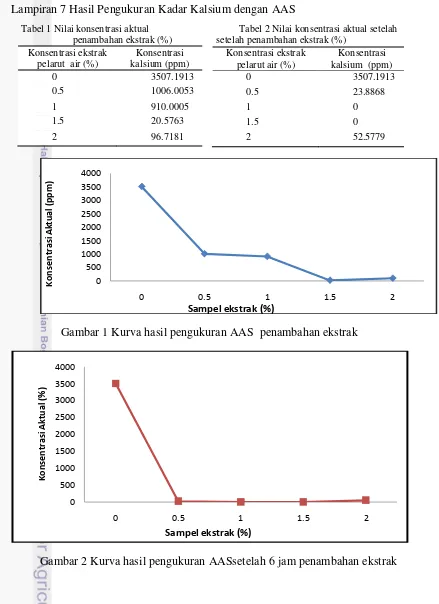
Lampiran 7 Hasil Pengukuran Kadar Kalsium dengan AAS
Tabel 1 Nilai konsentrasi aktual Tabel 2 Nilai konsentrasi aktual setelah penambahan ekstrak (%) setelah penambahan ekstrak (%)
Konsentrasi ekstrak
Gambar 1 Kurva hasil pengukuran AAS penambahan ekstrak
Gambar 2 Kurva hasil pengukuran AASsetelah 6 jam penambahan ekstrak
17
10 ekor larva udang diambil dan dimasukkan dalam plate uji
Di tambahkan larutan sampel yang akan diuji masing-masing
sebanyak 100 μL.
sampel dengan konsentrasi 1000 ppm, 500 ppm, 200 ppm, dan 50 ppm
Diinkubasi selama 24 jam dan dihitung jumlah udang yang mati
Telur udang diteteskan dalam media air laut selama 24 jam
0.02 gram sampel dari masing-masing ekstrak di encerkan dengan 10
mL air laut
18
Lampiran 9 Hasil perhitungan analisis probit
Sampel Ulangan Konsentrasi LC50
19
RIWAYAT HIDUP
Deni Suhendar merupakan anak kedua dari tiga bersaudara dengan ayah Ujang Kosim dan Ibu Suhastini yang lahir pada 15 Desember 1990. Penulis menyelesaikan pendidikan jenjang menengah atas di SMA Negeri 4Kota Jambi, Provinsi Jambi pada tahun 2008. Pada tahun yang sama penulis melanjutkan pendidikan di Departemen Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor (IPB) melalui jalur Ujian Saringan Masuk IPB(USMI).
Selama mengikuti kegiatan perkuliahan,pada pertengahan tahun 2011 hingga tahun 2012 penulis mendapat kesempatan untuk mengajar sebagai guru privat di Jakarta. Pada tahun 2011 penulis melaksanakan kegiatan praktik lapang di Balai Besar Penelitian dan Pengembangan Pascapanen Pertanian Bogor dengan karya ilmiah yang berjudul Teknologi Kemasan Aktif Berbasis 1-Methylcyclopropene (1-MCP) untuk Memperlambat Kematangan Pisang.Penulis juga pernah mengikuti pelatihan Keamanan dan Keselamatan Kerja (K3) yang diselenggarakan oleh Merck pada tahun 2011, dan mengikuti kegiatan IPB goes to field di Cibinong, Bogor.