Lampiran 3. Bagan alur penelitian Dibiarkan selama 3 jam Dimasukkan kedalam alat Dipekatkan dengan rotary
evaporator 3. Penetapan Kadar
Air
300 gram serbuk simplisia
Ekstrak kental 69,15 g
47
Lampiran 5. Gambar Hasil Pemeriksaan Makroskopik
Gambar : Daun mahkota dewa
49
Lampiran 6. Gambar Mikroskopik dengan Perbesaran 10 x 40
Daun mahkota dewa (Phaleria macrocarpa (Scheff) Boerl) Keterangan :
1. Stomata
2. Hablur Kristal Oksalat bentuk prisma 3. Rambut Penutup
4. Silem 4
1
3
Lampiran 8. Gambar hewan
Gambar : Mencit Jantan
53 Lampiran 9. Gambar alat
Gambar : Pipet mikro 5 – 50 µl/ml
55
Lampiran 10. Perhitungan Hasil Pemeriksaan Karakteristik Simplisia Perhitungan Penetapan Kadar Air
a. Sampel I
Berat sampel = 5,054 g Volume air = 0,4 ml Kadar air = 0,4𝑚𝑙
5,054𝑔 𝑥 100 %
= 7,915 % b. Sampel II
Berat sampel = 5,080 g Volume air = 0,35 ml Kadar air = 0,35𝑚𝑙
5,080𝑔 𝑥 100 %
= 6,890 % c. Sampel III
Berat sampel = 5,029 g Volume air = 0,3 ml Kadar air = 0,3𝑚𝑙
5,054𝑔 𝑥 100 %
= 5,965 %
Kadar air rata-rata = 𝑘𝑎𝑑𝑎𝑟𝑎𝑖𝑟 (𝑠𝑎𝑚𝑝𝑒𝑙𝐼+𝑠𝑎𝑚𝑝𝑒𝑙𝐼𝐼+𝑠𝑎𝑚𝑝𝑒𝑙𝐼𝐼𝐼)% 3
= 7,915+6,890+5,965
3 = 6,923 %
Kadar air simplisia = 𝒗𝒐𝒍𝒖𝒎𝒆𝒂𝒊𝒓 (𝒎𝒍)
Perhitungan Penetapan Kadar Sari yang Larut Dalam Air
dalam air rata-rata
57
Penetapan Kadar Sari yang Larut Dalam Etanol
a. Sampel I
dalam air rata-rata
Perhitungan Penetapan Kadar Abu Total
a. Sampel I
Berat sampel = 2,001 g Berat abu = 0,194 g Kadar abu = 0,194𝑔
2,001𝑔 𝑥 100 %
= 9,69% b. Sampel II
Berat sampel = 2,005 g Berat abu = 0,149 g Kadar abu = 0,149𝑔
2,005𝑔 𝑥 100 %
= 7,43% c. Sampel III
Berat sampel = 2,004 g Berat abu = 0,095 Kadar abu = 0,095𝑔
2,004𝑔 𝑥 100 %
= 4,74%
Kadar abu total rata-rata =kadar sari (sampel I + sampel II + sampel III) % 3
= 9,69+7,43+4,74 3
= 7,28% Kadar abu total = 𝒃𝒆𝒓𝒂𝒕𝒂𝒃𝒖 (𝒈)
59
Perhitungan Penetapan Kadar Abu yang Tidak Larut Asam
a. Sampel I
dalam asam rata-rata
= 0,19+0,49+0,29
3
= 0,32%
Kadar abu yang tidak larut dalam asam = 𝒃𝒆𝒓𝒂𝒕𝒂𝒃𝒖 (𝒈)
Lampiran 11. Perhitungan Uji Ketahanan Sel (Cell Viability Test) digunakan Rumus Sebagai Berikut :
% 𝑉𝐶 =� 1− 𝑈𝑉𝐶
𝑇𝐶𝐶� 𝑥 100 %
% 𝑉𝐶 =� 1− 27
287� 𝑥 100 %
= 90,59 % Dimana :
61
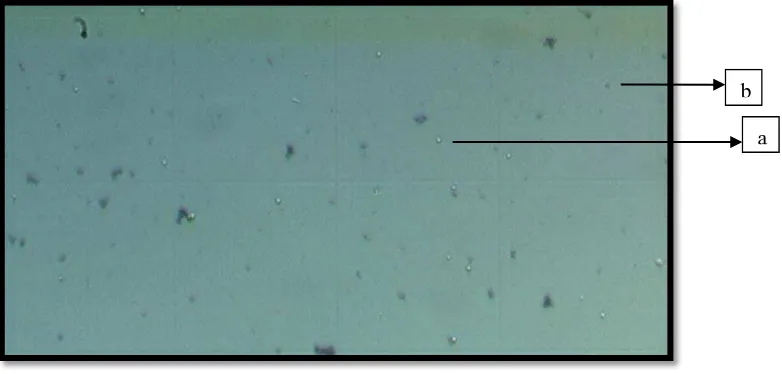
Lampiran 12. Gambar Sel Mastosit Pada Pengujian
Uji Ketahanan Sel (Cell Viability Test) dengan metode trypan blue exclusion Keterangan : (a) = sel mastosit yang tidak terdegranulasi (tidak berwarna)
(b) = sel mastosit yang terdegranulasi (berwarna biru)
Pengujian dengan menggunakan pewarnaan biru toluidin dengan pembesaran 10x 40
Gambar : Sel mastosit yang tidak terdegranulasi
b
63 Lampiran 14. Hasil SPSS Data Normalitas
Tests of Normality
Kolmogorov-Smirnova Shapiro-Wilk
Statistic df Sig. Statistic df Sig.
Hewan 1 .134 8 .200* .975 8 .931 Hewan 2 .192 8 .200* .852 8 .099 Hewan 3 .290 8 .046 .832 8 .062 Hewan 4 .152 8 .200* .956 8 .767 Hewan 5 .202 8 .200* .914 8 .380
a. Lilliefors Significance Correction
*. This is a lower bound of the true significance.
Lampiran 15. Hasil SPSS Data Persen Degranulasi
Within Groups 3366.911 32 105.216
65 Lampiran 16. Hasil SPSS Data Tukey HSD
Post Hoc Tests
67
Kontrol positif Normal 20.96800 6.48740 .051 -.0466 41.9826
Kontrol
% Degranulasi
Tukey HSDa
Perlakuan
N
Subset for alpha = 0.05
1 2 3 4 5
Normal 5 .0000
Kontrol positif 5 20.9680 20.9680
Uji 500 µg/ml 5 29.3400 29.3400
Uji 400 µg/ml 5 40.9160 40.9160 40.9160
Uji 300 µg/ml 5 50.1180 50.1180 50.1180
Uji 200 µg/ml 5 57.1960 57.1960
Uji 100 µg/ml 5 63.1660
Kontrol negatif 5 69.3720
Sig. .051 .073 .054 .228 .092
41
DAFTAR PUSTAKA
Agoes, A. H., (2010). Tanaman Obat Indonesia. Buku 2. Jakarta: Penerbit Salemba Medika. Halaman 71.
Alvianti, F., Mukhtar, R., dan Marianne., (2012). Penghambatan Degranulasi Mastosit Tersensitisasi Aktif oleh Curcuma Mangga Val. & Zijp Pada Mencit Secara In Vitro. Journal of Pharmaceutics and Pharmacology. Medan: Jurusan Farmasi. Universitas Sumatera Utara.1 (1): 44-54.
Baratawidjaja, G.K., (1996). Imunologi Dasar. Edisi III. Jakarta: Gaya Baru. Halaman 16-17.
Campbell, Reece dan Mitchell, L., (2000).Biologi. Edisi Kelima. Jilid 1. Jakarta: Penerbit Erlangga. Halaman 77,78,85.
Choudary, G.P., (2010). In Vitro Mast Cell Stabilization Activity of Onosma
Bracteatum Wall.J. Pharm. & Bio Sci. 6(2):54-60.
Ditjen POM., (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Halaman 33.
Depkes RI., (1999). Inventaris Tanaman Obat Indonesia.Jilid V. Jakarta: Departemen Kesehatan RI dan Kesejahteraan Sosial RI Badan Penelitian dan Pengembangan Kesehatan. Halaman 147.
Depkes RI., (1995). Materia Medika Indonesia. Jilid VI. Jakarta : Depkes RI. Halaman. 321,325,333-334,336.
Depkes RI., (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Halaman 1-11.
Dowd. John, A. Marotti. Nedle danYogiela., (2011). Pharmacology and
Therapeutic for Dentistry.Sixth Edition.Mosty Elsevier.Halaman 329, 359,
361.
Dyah, N dan Firman., (2007). Mahkota Dewa dan Manfaatnya. Bekasi: Ganeca Exact. Halaman.5-7.
Farnsworth, N.R. (1966). Biologycal and Phytochemical Screening of Plants.Journal of Pharmaceutical Sciense.55:264.
Gunawan, G.S., (2007). Farmakologi dan Terapi.Edisi V. Jakarta: Gaya Baru. Halaman 255.
Handayani, D., Aldi, Y., dan Zumiati. (2008). Uji Aktivitas Penghambatan Degranulasi Mastosit yang Tersensitisasi terhadap Ekstrak Metanol Spon Laut ( Acathodendrilla SP.). Jurnal Sains dan Teknologi Farmasi. Padang: Jurusan Farmasi FMIPA Universitas Andalas Padang. 13(1): 43-48.
Hariana, A. H., (2009). Tumbuhan Obat dan Khasiatnya. Seri kedua, Jakarta: Penerbit Penebar Swadaya. Halaman 109.
Harr. Robert. R., (2002).Resensi Ilmu Laboratorium Klinis. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 53.
Hermanto, N., (2004). Mahkota Dewa. Jakarta: Agro Media Pustaka. Halaman 52. Ibrahim, J., Harun, N.H., Septama, A.W.,Murad, S., dan Mesaik, M.A.,(2010).
Inhibition of Chemiluminescence and Chemotactic Activity of Pagocytes In-Vitro by The Extracts of Selected Medical Plant. J. Nat. Med. 65(2): 400-405.
Katzung, G., Bertram., (2001). Farmakologi Dasar dan Klinik. Edisi Pertama. Jakarta: Salemba Medika. Halaman 357;358.
Katzung and Trevors., (2008). Pharmacology.Eighth Edition. America: Mc Graw Hill Companies. Halaman 168.
Kimura, M., I., dan Kobuko, M. (1978).Inhibition Of Compound 48/80 Mediated Histamin Release From Isolated Rat Mast Cell By Oosponol Related Compounds (4-acyl-isocoumarins).Japan. J. Pharmacol. 28(1): 639-673. Kresno, S. B. (2010). Imunologi,Diagnosis dan Prosedur Laboratorium. Edisi V.
Jakarta: Balai Penerbit Fakultas Kedokteran Universitas Indonesia. Halaman 162,163.
Louis, K.S., dan Siegel, A.C. (2011). Cell Viability Analysis Using Trypan Blue: Manual and Automated Methods. Mamalia Cell Viability: Methode in Molecular Biology.740; 7-10.
Muttaqin.A., (2008).Buku Ajar Asuhan Keperawatan dengan Gangguan Sistem
Pernapasan.Jakarta: Penerbit Salemba Medika. Halaman 172,173.
Nahak, M. M., (2013). Shock Anafilaksis Akiba Anastesi Lokal Menggunakan
Lidocaine. Jurnal Kesehatan Gigi. Denpasar.1(2):106-108.
43
Rohyami, Y., (2008). Penentuan Kandungan Flavanoid dari Ekstrak Metanol
Daging Buah Mahkota Dewa (Phaleria macrocarpa Scheff Boerl.
Program DIII, Kimia Analisis, UII, Yogyakarta: Jurusan FMIPA. 5(1):1-8. Sari, K, L.O.R., (2006).Pemanfaatan Obat Tradisional dengan Pertimbangan
Manfaat dan Keamanannya.Majalah Ilmu Farmasi, 3(1):1-2.
Sukandar, E.Y. (2006). Trend dan Paradigma Dunia Farmasi, Industri Klinik
Teknologi Kesehatan, Disampaikan Dalam Orasi Ilmiah Dies Natalis ITB.
http//ac.id./focus/focus_file/orasi-ilmiah-dies-45.pdf.
Tambayong, J., (2000). Patofisiologi Keperawatan. Jakarta: Pernerbit EGC. Halaman 52.
Tan, H.T., dan Rahardja, K., (2007). Obat-Obat Penting. Edisi ke-4. Jakarta: Elex Media Komputindo. Halaman 813.
Wahab, A., Samik dan Julia, Madarina., (2002). Sistem Imun, Imunisasi, dan
Penyakit Imun. Jakarta: Widya Medika. Halaman 67;69;75;79;84.
WHO., (1998). Quality Control Methods for Medicinal Plant
Material.Switzerland: Geneva press. Halaman 31-33.
Vogel, H. G., (2008). Methods for Testing Immunological Factors.Editor: Hans Gerhard Vogel. Dalam: Drug Discovery and Evaluation Pharmacological
Essays,Edisi ke-3. Jilid2. Berlin Springer.Halaman 1143.
BAB III
METODE PENELITIAN
Metode penelitian ini dilakukan secara eksperimental parametrik meliputi pengumpulan bahan, pengolahan bahan, pembuatan ekstrak etanol daun mahkota dewa, penyiapan hewan percobaan (mencit), dan pengujian penghambatan degranulasi mastosit pada hewan percobaan secara in-vitro dengan menggunakan alat Improved neubauer hemocytometer. Data hasil penelitian dianalisis secara ANAVA dua arah (two way anava) dan dilanjutkan dengan uji bedaTukey HSD menggunakan program SPSS (Statistical and Product Service Solution) versi 18.
3.1 Alat dan Bahan 3.1.1 Alat - alat
Alat-alat yang digunakan dalam penelitian ini meliputi alat-alat gelas laboratorium, perkolator, blender, rotary evaporator, seperangkat alat destilasi penetapan kadar air, kertas saring, spot plat, penjepit tabung, spatula, kertas perkamen, lumpang dan stamper,aluminium foil, seperangkat alat bedah, spuit 1 ml dan spuit 10 ml, kandang mencit, neraca listrik, mikroskop (Boeco), neraca hewan (Presica Geniweigher GW-1500), pipet mikro, alat sentrifuge, waterbath,
microtube, pipet mikro, kamar hitung improved Neubauer hemocytometer
(Marienfeld).
3.1.2 Bahan - bahan
19
asam nitrat dan kalium iodida), pereaksi Bourchardat (iodium dan kalium iodida), serbuk Zn, asam klorida pekat, amil alkohol, asam sulfat pekat, pereaksi Molish (∝- naftol dan asam nitrat), pereaksi besi (III) klorida, n-heksana,pereaksi Liebermann Burchat ( asam asetat anhidrat dan asam sulfat pekat), kloroform, kloralhidrat, larutan NaCl 0,9%, Aminofilin 24 mg/ml, dimetil sulfoksida (DMSO), asam asetat glasial, formaldehid 37%, biru toluidin, natrium klorida,kalim klorida, dinatrium hidrogen fosfat, kalium dihidrogen fosfat, akuabidest, trypan blue 0,4 %,
3.2 Hewan Percobaan
Hewan percobaan yang digunakan dalam penelitian adalah mencit jantan dengan berat 20-30 gram sebanyak 5 ekor. Sebelum digunakan sebagai hewan percobaan, semua mencit dipelihara terlebih dahulu selama dua minggu untuk penyesuaian lingkungan.
3.3 Penyiapan Tanaman
Penyiapan tanaman meliputi pengumpulan tanaman, identifikasi tanaman dan pengolahan tanaman.
3.3.1 Pengumpulantanaman
3.3.2 Identifikasi tanaman
Identifikasi tanaman dilakukan di Herbarium Bogoriense, Bidang Botani, Pusat Penelitian Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI).
3.3.3 Pengolahan tanaman
Daun mahkota dewa yang telah dikumpulkan dibersihkan dari pengotoran, selanjutnya dicuci dibawah air mengalir beberapa kali hingga bersih, kemudian ditiriskan lalu disebarkan diatas perkamen sampai merata hingga airnya terserap, setelah itu ditimbang diperoleh daun sebanyak 2,5 kg, kemudian dikeringkan dilemari pengering. Setelah sampel kering ditimbang berat keringnya, diperoleh berat kering sebanyak 1 kg. Kemudian sampel yang sudah kering dihaluskan sampai menjadi serbuk dengan menggunakan blender, selanjutnya dimasukkan dalam wadah plastik tertutup, serbuk sebelum dipakai disimpan ditempat kering terlindung dari cahaya.
3.4 Pemeriksaan Karakteristik Simplisia
Pemeriksaan karakteristik simplisia meliputi pemeriksaan makroskopik dan mikroskopik, penetapan kadar air, kadar sari larut air, kadar sari larut etanol, kadar abu total dan kadar abu tidak larut asam (Depkes, RI., 1995).
3.4.1 Pemeriksaan makroskopik
21 3.4.2 Pemeriksaan mikroskopik
Pemeriksaan mikroskopik terhadap serbuk simplisia daun mahkota dewa dilakukan dengan cara menaburkan simplisia diatas gelas preparat yang telah diteteskan dengan larutan kloralhidrat dan ditutup dengan gelas penutup kemudian dilihat dibawah mikroskop.
3.4.3 Penetapan kadarair
Penetapan kadar air dilakukan menurut metode Azeotropi (destilasi toluen). Alat terdiri dari labu alas bulat 500 ml, pendingin, tabung penyambung, tabung penerima 5 ml berskala 0,05 ml, alat penampung dan pemanas listrik. Cara Kerja :
3.4.4 Penetapan kadarsari larut air
Sebanyak 5 g serbuk yang telah dikeringkan, dimaserasi selama 24 jam dalam 100 ml air-kloroform (2,5 ml kloroform dalam air suling 1000 ml) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, dibiarkan selama 18 jam, kemudian disaring. Diuapkan 20 ml filtrat sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Hitung kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan diudara (Depkes, RI.,1995).
3.4.5 Penetapan kadarsari larut etanol
Sebanyak 5 g serbuk simplisia yang telah dikeringkan dimasersi selama 24 jam dalam 100 ml etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Kemudian disaring, 20 ml filtrat diuapkan sampai kering dalam cawan dangkal berdasar rata yang telah ditara dan sisanya dipanaskan pada suhu 105oC sampai bobot tetap. Kadar sari larut dalam etanol dihitung terhadap bahan yang telah dikeringkan diudara (Depkes, RI., 1995).
3.4.6 Penetapan kadarabu total
23 3.4.7 Penetapan kadarabu tidak larut asam
Abu yang telah diperoleh dalam penetapan abu didinginkan dengan 25 ml asam klorida encerselama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring dengan kertas saring bebas abu, cuci dengan air panas, dipijarkan sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut asam dihitung terhadap bobot yang dikeringkan diudara (Depkes, RI., 1995).
3.5 Skrining Fitokimia
Skrining fitokimia serbuk simplisia daun mahkota dewa meliputi : pemeriksaan senyawa golongan alkaloid, flavanoid, glikosida, tanin, saponin dan steroid/triterpenoid.
3.5.1 Pemeriksaan alkaloid
Serbuk simplisia daun mahkota dewa ditimbang sebanyak 0,5 g kemudian ditambahkan 1 ml asam klorida 2 N dan 9 ml air suling, dipanaskan diatas penangas air selama 2 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk uji alkaloida: diambil 3 tabung reaksi, lalu kedalamnya dimasukkan 0,5 ml filtrat.
Pada masing-masing tabung reaksi:
a. Tabung 1 ditambahkan 2 tetes pereaksi Mayer b. Tabung 2 ditambahkan 2 tetes pereaksi Bauchardat c. Tabung 3 ditambahkan 2 tetes pereaksi Dragendorff
3.5.2 Pemeriksaan flavonoid
Sebanyak 10 g serbuk simplisia daun mahkota dewa ditambahkan 100 ml air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas. Filtrat yang diperoleh kemudian diambil 5 ml lalu ditambahkan 0,1 g serbuk Mg dan 1 ml HCL pekat dan 2 ml amil alkohol, dikocok, dan dibiarkan memisah. Flavonoid positif jika terjadi warna merah, kuning, jingga pada lapisan amil alkohol(Farnsworth, 1966).
3.5.3 Pemeriksaan glikosida
Serbuk simplisia daun mahkota dewa ditimbang sebanyak 3 g, lalu disari dengan 30 ml campuran etanol 95 % dengan air (7:3) dan 10 ml asam klorida 2 N, direfluks selama 2 jam, didinginkan dan disaring. Diambil 20 ml filtrat ditambahkan 25 ml air suling dan 25 ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu disaring. Filtrat disari sebanyak 3 kali, tiap kali dengan 20 ml campuran isopropanol dan kloroform (2:3). Pada kumpulan sari tambahkan natrium sulfat anhidrat, disaring dan uapkan pada suhu 500C. Sisanya dilarutkan dalam 2 ml metanol. Larutan ini digunakan untuk percobaan berikut : 0,1 ml larutan percobaan dimasukkan dalam tabung reaksi dan diuapkan di atas penangas air. Pada sisa ditambahkan 2 ml air dan 5 tetes pereaksi Molish. Kemudian secara perlahan-lahan ditambahkan 2 ml asam sulfat pekat melalui dinding tabung, terbentuknya cincin berwarna ungu pada batas kedua cairan menunjukkan ikatan gula (Depkes, RI., 1995).
3.5.4 Pemeriksaan tanin
25
larutan lalu ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida. Terjadi warna biru atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966). 3.5.5 Pemeriksaan saponin
Sebanyak 0,5 g serbuk simplisia daun mahkota dewa dimasukkan ke dalam tabung reaksi ditambahkan 10 ml air panas, didinginkan kemudian dikocok selama 10 detik. Jika terbentuk buih yang mantap setinggi 1-10 cm yang stabil tidak kurang dari 10 menit dan tidak hilang dengan penambahan satu tetes asam klorida 2 N menunjukkan adanya saponin (Depkes, RI., 1995).
3.5.6 Pemeriksaan steroid/triterpenoid
Sebanyak 1 g serbuk simplisia daun mahkota dewa dimaserasi dengan 20 ml eter selama 2 jam, disaring, setelah itu filtrat yang diperoleh diuapkan dengan menggunakan cawan penguap dan pada sisanya ditambahkan 2 tetes pereaksi Lieberman-Bourchard. Apabila terbentuk warna ungu atau merah yang berubah menjadi biru atau hijau menunjukkan adanya steroid/triterpenoid yang terkandung di dalam simplisia atau ekstrak (Farnsworth, 1966).
3.6 Pembuatan Ekstrak Etanol Daun Mahkota Dewa (EEDMD)
Pembuatan ekstrak etanol daun mahkota dewa dilakukan secara perkolasi menggunakan etanol 96%
dihentikan bila 500 mg perkolat terakhir diuapkan tidak lagi meninggalkan sisa. Perkolat yang diperoleh kemudian dipekatkan dengan alat rotary evaporator pada suhu kurang lebih 60oC sampai diperoleh ekstrak kental (Ditjen POM., 1979).
3.7 Uji Aktivitas Penghambatan Degranulasi Mastosit
Uji aktivitas penghambatan degranulasi mastosit meliputi penyiapan sediaan, penyiapan hewan percobaan dan uji degranulasi mastosit tersensitisasi aktif.
3.7.1 Penyiapan sediaan
Penyiapan sediaan meliputi penyiapan larutan putih telur ayam 50%, penyiapan larutan phosphate buffered saline (PBS), penyiapan larutan trypan
blue 0,4%,penyiapan larutan uji, penyiapan larutan Aminofilin konsentrasi 100
µg/ml,penyiapan larutan biru toluidindanekstrak etanol daun mahkota dewa (EEDMD) dengan berbagai konsentrasi.
3.7.1.1Pembuatanlarutan putih telur ayam 50%
Sebanyak 5 ml putih telur ayam ditambahkan dalam 5 ml salin fisiologis, kemudian dilakukan pengenceran dengan mengambil 5 ml larutan diatas lalu dicukupkan volumenya hingga 10 ml dengan larutan salin fisiologis sehingga diperoleh larutan induk, kemudian diambil 5 ml larutan induk dan dicukupkan volumenya hingga 10 ml dengan larutan salin fisiologis sehingga diperoleh konsentrasi 50%.
3.7.1.2 Pembuatan larutan phosphate buffered saline (PBS)
Phosphate Buffered Saline (PBS) adalah larutan penyangga yang umum
27
gram NaCl, 0,2 gram KCL, 1,44 gram Na2HPO4, 0,24 gram KH2PO4, dilarutkan
dalam 800 ml akuabidest, kemudian dicek pH ± 7 dan dapat disesuaikan dengan penambahan HCL atau NaOH, tambahkan akuabidest hingga 1 L(Sambrook dan Maniatis, 1989).
3.7.1.3 Pembuatan larutan trypan blue 0,4 %
Sebanyak 200 mg serbuk trypan blue dilarutkan dalam 50 ml larutan PBS dengan pH ± 7 dan dikocok hingga larut.
3.7.1.4Pembuatan larutan uji
Sebanyak 1 g ekstrak etanol daun mahkota dewa dilarutkan dalam 10 ml larutan DMSO 1% sehingga didapatkan konsentrasi 100 mg/ml, kemudian dilakukan pengenceran dengan mengambil 1 ml larutan ekstrak etanol daun mahkota dewa konsentrasi 100 mg/ml diatas lalu ditambahkan dengan larutan DMSO 1 % hingga 10 ml sehingga diperoleh konsentrasi 10000 µg/ml, kemudian diambil 1 ml larutan ekstrak etanol daun mahkota dewa konsentrasi 10000 µg/ml diatas dan tambahkan dengan larutan DMSO 1% hingga volume 10 ml sehingga diperoleh konsentrasi 1000 µg/ml, lalu diambil 5 ml larutan ekstrak etanol daun mahkota dewa konsentrasi 1000 µg/ml ditambahkan dengan larutan DMSO 1 % hingga 10 ml sehingga diperoleh konsentrasi 500 µg/ml, demikian seterusnya sampai diperoleh konsentrasi 400 µg/ml, 300 µg/ml, 200 µg/ml dan 100 µg/ml. 3.7.1.5 Pembuatan larutan Aminofilin konsentrasi 100 µg/ml
1% hingga 5 ml sehingga diperoleh konsentrasi 100 µg/ml (Handayani,dkk.,2008).
3.7.1.6 Pembuatan larutan biru toluidin
Sebanyak 39 ml larutan NaCl fisiologis 0,9% dicampur dengan 1 ml asam asetat glasial, 10 ml formaldehid 37% (v/v) dan 50 ml etanol 95% (v/v), kemudian campuran dikocok dan ditambahkan biru toluidin sebanyak 100 mg dan dikocok lagi hingga larut (Handayani,dkk., 2008).
3.7.2 Penyiapan hewan percobaan
Hewan yang digunakan adalah mencit jantan sehat dengan berat berkisar 20-30 gsebanyak 5 ekor yang dapat perlakuan yang sama. Tiap 1 ekor mencit diambil cairan intraperitonealnya dan dibagi atas 8 kelompok:
Kelompok 1 (Normal): suspensi mastosit yang tidak diberi penambahan larutan antigen (putih telur ayam) maupun EEDMD dan Aminofilin.
Kelompok 2 (Kontrol Positif): suspensi mastosit yang diberikan larutan antigen putih telur ayam 50% dan Aminofilin 100 µg/ml.
Kelompok 3 (Kontrol Negatif): suspensi mastosit yang diberikan larutan antigen putih telur ayam 50% dan DMSO 1% tetapi tidak diberikan EEDMD ataupun Aminofilin.
Kelompok 4 (Uji 1): suspensi yang diberikan larutan antigen putih telur ayam 50% dan EEDMD 100 µg/ml.
Kelompok 5 (Uji 2): suspensi yang diberikan larutan antigen putih telur ayam 50% dan EEDMD 200 µg/ml.
29
Kelompok 7 (Uji 4): suspensi yang diberikan larutan antigen putih telur ayam 50% dan EEDMD 400 µg/ml.
Kelompok 8 (Uji 5): suspensi yang diberikan larutan antigen putih telur ayam 50% dan EEDMD 500 µg/ml.
3.7.2.1 Pembuatan suspensi mastosit tersensitisasi
3.7.3 Pengujian Mastosit
3.7.3.1 Uji ketahanan sel (cell viability test)
Uji ketahanan sel dilakukan untuk melihat sel uji yang tetap utuh dengan penambahan larutan uji dosis maksimal dan diinkubasi selama beberapa jam. Pengujian ini menggunakan metode pewarnaan oleh trypan blue.
Sebanyak 50 µl suspensi mastosit yang telah diisolasi dari peritonial mencit dengan jumlah sel permililiternya 1 x 106 dimasukkan kedalam tabung reaksi. Kemudian ditambahkan 50 µl larutan uji EEDMD 500 µg/ml dan ditepuk-tepuk secara perlahan sampai homogen. Inkubasi pada suhu 370C selama 1 jam. Diambil 100 µl larutan tersebut kemudian ditambahkan 100 µl larutan trypan blue 0,4 % dan ditepuk-tepuk secara perlahan sampai homogen. Teteskan larutan di atas hemositometer dan hitung sel yang berwarna biru dibawah mikroskop 10 x 40. Persen ketahanan sel dihitung dengan rumus sebagai berikut :
% sel yang utuh = 1,00−𝐽𝑢𝑚𝑙𝑎ℎ𝑠𝑒𝑙𝑦𝑎𝑛𝑔𝑡𝑒𝑟𝑑𝑒𝑔𝑟𝑎𝑛𝑢𝑙𝑎𝑠𝑖 (𝑏𝑖𝑟𝑢)
𝑗𝑢𝑚𝑙𝑎ℎ𝑡𝑜𝑡𝑎𝑙𝑠𝑒𝑙 𝑥 100%
3.7.3.2 Uji degranulasi mastosit tersensitisasi aktif
Sebanyak 5 ekor mencit yang diambil cairan intraperitonealnya mendapat perlakuan yang sama sebagai berikut:
a. Penghitungan jumlah mastosit tersensitisasi (kelompok normal).
Sebanyak 50 µl suspensi mastosit ditambahkan 40 µl PBS, 10 µl biru toluidin.
b. Penghitungan jumlah mastosit yang tidak terdegranulasi oleh DMSO 1% (kelompok kontrol negatif ).
31
c. Pengujian aktivitas penghambatan degranulasi mastosit oleh Aminofilin 100 µg/ml.
Sebanyak 50 µl suspensi mastosit ditambahkan 30 µl Aminofilin 100 µg/ml, 10 antigen putih telur ayam 50% dan 10 µl biru toluidin.
d. Pengujian aktivitas penghambatan degranulasi mastositoleh ekstrak etanol daun mahkota dewa (kelompok uji) dengan konsentrasi sebagai berikut :
i. Sebanyak 50 µl suspensi mastosit ditambahkan 30 µl EEDMD 100 µl/ml, 10 antigen putih telur ayam 50% dan 10 µl biru toluidin. ii. Sebanyak 50 µl suspensimastosit ditambahkan 30 µl EEDMD 200
µl/ml, 10 antigen putih telur ayam 50% dan 10 µl biru toluidin. iii. Sebanyak 50 µl suspensi mastosit ditambahkan 30 µl EEDMD 300
µl/ml, 10 antigen putih telur ayam 50% dan 10 µl biru toluidin. iv. Sebanyak 50 µl suspensi mastosit ditambahkan 30 µPl EEDMD
400 µl/ml, 10 antigen putih telur ayam 50% dan 10 µl biru toluidin. v. Sebanyak 50 µl suspensi mastosit ditambahkan 30 µl EEDMD 500
3.7.3.3 Penghitungan persen jumlah mastosit terdegranulasi
Efek penghambatan degranulasi mastosit oleh ekstrak etanol daun mahkota dewa ditentukan dengan menghitung jumlah mastosit yang tidak terdegranulasi menggunakan alat hemositometer. Kemudian dari jumlah mastosit yang didapat , dihitung persentase degranulasi mastosit dengan cara sebagai berikut (Handayani, dkk., 2008).
% Degranulasi = 𝑝 − 𝑠
𝑝 𝑥 100 %
Dimana :
P = Jumlah mastosit sebelum perlakuan S = Jumlah mastosit setelah perlakuan
3.8 Analisis Data
33 BAB IV
HASIL DAN PEMBAHASAN 4.1 Simplisia
Tumbuhan yang digunakan adalah daun mahkota dewa yang telah diidentifikasi Herbarium Bogoriense,Bidang Botani Pusat Penelitian Biologi-LIPI Bogor, dengan nama lain Phaleria macrocarpa (Scheff.) Boerl, suku
Thymelaeaceae. Hasil identifikasi tumbuhan dapat dilihat pada Lampiran 2.
Hasil pemeriksaan makroskopik dari daun mahkota dewa Lampiran 4, adalah sebagai berikut : daun mahkota dewa berwarna hijau, daun tunggal berbentuk lonjong, ujung dan pangkal runcing, tepi rata, panjang 7-10 cm, lebar 2-5 cm, permukaan licin dan memiliki pertulangan menyirip(Depkes, 1999).
Hasil pemeriksaan mikroskopik serbuk simplisia Lampiran 5, terlihat fragmen stomata, fragmen rambut penutup, fragmen spiral,fragmen palisade, dan fragmen hablur kristal oksalat.
Hasil skrining fitokimia serbuk simplisia menunjukkan adanya kandungan alkaloida, flavanoid, tanin dan steroid/triterpenoid. Hasil karakteristik simplisia daun mahkota dewa yaitu penetapan kadar air 6,92%, kadar sari yang larut dalam air 25,05%, kadar sari yang larut dalam etanol 54,77%, kadar abu total 7,29%, kadar abu tidak larut asam 0,32% Hasil karakterisasi simplisia daun mahkota dewa dan skrining fitokimia dapat dilihat pada Tabel 4.1 dan Tabel 4.2.
Tabel 4.1 Hasil karakterisasi simplisia daun mahkota dewa
No Parameter Hasil
1. Penetapan kadar air 6,92%
2. Penetapan kadar sari larut dalam air 25,05% 3. Penetapan kadar sari larut dalam etanol 54,77%
4. Penetapan kadar abu total 7,29%
Tabel 4.2 Hasil skrining fitokimia simplisia daun mahkota dewa
No Skrining Hasil
1 Alkaloida +
2 Flavanoida +
3 Glikosida -
4 Saponin -
5 Tanin +
6 Steroid/Triterpenoid +
Keterangan :+ =Mengandung golongan senyawa
- = Tidak mengandung golongan senyawa
Ektrak cair dari 455,04 g serbuk simplisia daun mahkota dewa yang diperkolasi, dipekatkan dengan menggunakan rotary evaporator diperoleh ekstrak kental 69,15 gram.
4.2 Pengujian Efek Antialergi
Pada penelitian ini pengujian dilakukan menggunakan ekstrak daun mahkota dewa dengan metode isolasi mastosit dari cairan intraperitoneal mencit jantan secara in vitroyang digunakan untuk melihat pengaruh ekstrak daun mahkota dewa terhadap aktivitas penghambatan degranulasi mastosit yang tersensitisasi aktif.
35
Pemberian antigen untuk pertama kali dilakukan secara intaperitoneal, hal ini ditunjukkan agar proses pengenalan antigen lebih cepat oleh sel limposit. Proses pengenalan ini dilakukan oleh sel makrofag karena sel ini merupakan sel antigen Precenting cell (APC) dan banyak terdapat pada rongga perut (Kimura, 1978).
Antigen adalah molekul yang mencetuskan pembentukan antibodi yang mampu berikatan dengan antigen spesifik, dimana antigen dapat menimbulkan respon kekebalan dengan cara mengaktifkan sel B untuk mensekresi protein sehingga sel B dan sel T dapat mengenali antigen spesifik karena adanya reseptor antigen yang berikatan pada membran plasmanya (Campbell, 2000).
Alergen yang masuk melalui saluran pernapasan, kulit dan saluran cerna akan ditangkap oleh makrofag yang bekerja sebagai Antigen precenting cell (APC) setelah alergen diproses oleh APC lalu sel tersebut dipresentasikan oleh sel Th melalui pelepasan interleukin II oleh sel Th yang diaktifkan kepada sel B sehingga dapat berproliferasi menjadi sel plasma dan membentuk IgE.
Berdasarkan penelitian yang telah dilakukan oleh Handayani, dkk, (2008) didapatkan efek maksimal antigen putih telur ayam dalam degranulasi mastosit adalah pada konsentrasi 50%.Pengujian dilakukan dengan cara menginduksi mencit jantan secara intraperitoneal dengan menggunakan putih telur ayam konsentrasi 50%. Antigen yang diberikanpada hari pertama dilakukan secara intraperitoneal dengan tujuan untuk proses pengenalan antigen lebih cepat dilanjutkan pada hari ketiga dan kelima secara subkutan pada telapak kaki mencit dengan tujuan pembosteran untuk memperbanyak terbentuknya antibodi IgE, sehingga reaksi alerginya semakin hebat (Alvianty,2012).
Sebelum pengujian ekstrak dengan berbagai konsentrasi dilakukan terlebih dahulu uji ketahanan sel dimana untuk mengetahui sitoksisitas ekstrak tanaman, hasil dari pengujian ketahanan sel didapat 90,59% pada dosis 500 µg/ml yang mengindikasikan sel dapat tetap hidup (> 90,0%) setelah diinkubasi selama 1 jam (Ibrahim, et al., 2010).
Pada uji pendahuluan digunakan dengan metode tradisional dengan menggunakan pewarnaan trypan blue.Trypan blue adalah pewarnaan yang tertinggal pada sel yang mati dengan warna biru yang khas ketika dilihat dibawah mikroskop, sedangkan sel yang sehat tidak menunjukkan warna.Sel yang sehat memiliki membran yang utuh karena tidak menyerap medium disekitarnya, tetapi pada sel yang tidak sehat tidak mempunyai membran yang utuh dan dapat menyerap medium disekitarnya (Louis, 2011).
37
reaksi anafilaksis yang sebelumnya telah diinduksi oleh antigen putih telur ayam pada konsentrasi 50%.
Bentuk sel mastosit normal dibawah mikroskop terlihat warna ungu dan bagian tengahnya bergranul.Sel mastosit yang telah terdegranulasi tidak terlihat lagi karena telah hancur dan tidak mengikat lagi.Semakin banyak sel yang terdegranulasi maka semakin sedikit sel yang terlihat.
Data yang diperoleh dari hasil pengujian degranulasi mastosit dinyatakan dalam bentuk persen degranulasi, yaitu perbandingan jumlah sel sebelum perlakuan dikurangi jumlah sel sesudah perlakuan. Persentase degranulasi mastosit dihitung dengan cara sebagai berikut :
% 𝐷𝑒𝑔𝑟𝑎𝑛𝑢𝑙𝑎𝑠𝑖 = 𝑝 − 𝑠
𝑝 𝑥 100 %
Dimana :
P = jumlah sel mastosit sebelum perlakuan S = jumlah sel mastosit setelah perlakuan
Dalam pengujian penghambatan degranulasi mastosit oleh ekstrak daun mahkota dewa, dilakukan terlebih dahulu uji pendahuluan dengan tujuan untuk mengetahui konsentrasi terkecil dan konsentrasi terbesar yang dapat menghambat degranulasi. Dari hasil pendahuluan tersebut diperoleh konsentrasi terkecil 100 µg/ml dan konsentrasi terbesar adalah 500 µg/ml, Diperoleh konsentrasi pengujian tersebut yaitu 100 µg/ml, 200 µg/ml, 300 µg/ml, 400 µg/ml, 500 µg/ml. Hasil pengujian degranulasi sel mastosit dengan variasi 5 konsentrasi dapat dilihat pada Lampiran 4.
aminofilin.Pemilihan ini didasarkan kepada senyawa yang telah diketahui mekanismenya dalam menghambat degranulasi mastosit dan mudah didapat. Berdasarkan penelitian dilakukan oleh Handayani, dkk., (2008), efek maksimal yang memberikan efek yaitu 100 µg/ml.
Proses penghambatan degranulasi sel mastosit secara in-vitrosecara teoritis dapat dilakukan dengan menghambat masuknya ion Ca, seperti senyawa kromolin atau menghambat kerja enzim fosfodiesterase sehingga kadar cAMP tinggi. Hal ini akan mengakibatkan pendorongan granul-granul ke pinggir tidak berlangsung sehingga sel mastosit menjadi stabil. Senyawa yang dapat mempertahankan kadar cAMP didalam sel mastosit adalah Aminofilin dan kortikosteroid (Katzung, 2001).
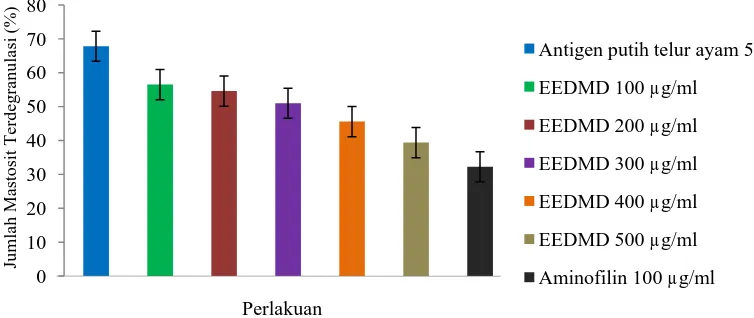
Grafik persen degranulasi mastosit sebagai respon penghambatan degranulasi mastosit yang tersensitisasi aktif dapat dilihat Gambar 4.1.
Gambar 4.1 Grafik persen degranulasi mastosit
Berdasarkan Gambar 4.1 tampak bahwa EEDMD dosis 100, 200, 300, 400 dan 500 µg/ml dan aminofilin dosis 100 µg/ml menunjukkan persen, degranulasi
0
39
yang lebih kecil dan jauh berbeda dengan antigen putih telur ayam 50% sebagai kontrol negatif yang tidak diberi apapun, kemampuan Aminofilin dosis 100 µg/ml dalam menghambat degranulasi mastosit dengan persen 32,28% lebih besar dibandingkan EEDMD dosis 500 µg/ml dengan persen degranulasi mastosit 39,39%. Ekstrak etanol daun mahkota dewa dosis 500 µg/ml dengan persen degranulasi mastosit 39,39% menunjukkan persen degranulasi mastosit yang lebih kecil dibandingkan dengan EEDMD dosis 400 µg/ml (45,58%), 300 µg/ml (51,02%), 200 µg/ml (54,59%), 100 µg/ml (56,51%). Hal ini menunjukkan bahwa adanya hubungan antara peningkatan dosis dengan persen degranulasi mastosit yaitu semakin besar peningkatan dosis maka mastosit yang terdegranulasi semakin sedikit.
Analisis variasi (ANAVA) digunakan untuk melihat ada tidaknya perbedaan dari setiap perlakuan pada tiap kelompok hewan coba dengan menggunakan program SPSS terhadap persen gegranulasi mastosit. Hasil analisis yang didapat pada variasi diperoleh harga (F=26,197, P= 0,000).
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Berdasarkan penelitian yang telah dilakukan dapat disimpilkan bahwa: a. Hasil karakteristik serbuk simplisia daun mahkota dewa pada penetapan
kadar air yaitu 6,92%, penetapan kadar sari larut dalam air yaitu 25,05%, penetapan kadar sari larut dalam etanol yaitu 54,77%, penetapan kadar abu total yaitu 7,29%, penetapan kadar abu tidak larut dalam asam yaitu 0,32%.
b. Efek penghambatan degranulasi mastosit ekstrak etanol daun mahkota dewa pada konsentrasi 400 µg/ml, 500 µg/ml dan Aminofilin 100 µg/ml dapat menghambat degranulasi mastosit tersensitisasi aktif secara
in-vitroterhadap control negatif (P<0,05). Penghambatan maksimal diberikan
pada ekstrak dengan konsentrasi 500µg/ml.
5.2 Saran
6 BAB II
TINJAUAN PUSTAKA 2.1 Uraian Tanaman
Tanaman mahkota dewa (Phaleria macrocarpa (Scheff) Boerl) merupakan salah satu tanaman asli Indonesia yang akhir-akhir ini populer sebagai tanaman yang secara empiris dapat mengobati berbagai macam penyakit. Tanaman ini memiliki batang utama yang bercabang-cabang setinggi 1,5-2,5 meter, daunnya tunggal berbentuk lonjong dan berujung lancip. Buahnya bulat dan berwarna merah tua jika matang.Tanaman mahkota dewa berasal dari Irian dan tumbuh subur pada ketinggian 10-1.200 m diatas permukaan laut (Agoes, 2010).
2.1.1 Sistematika Tanaman
Menurut Depkes (1999), sistematika tanaman mahkota dewa adalah sebagai berikut:
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledoneae Ordo : Thymelaeales Famili : Thymelaeaceae Genus : Phaleria
Spesies : Phaleria macrocarpa (Scheff.) Boerl. 2.1.2 Nama Daerah
2.1.3 Bagian yang digunakan
Menurut Hariana (2009) daun dan kulit buah dapat digunakan dalam keadaan segar atau setelah dikeringkan. Pemanfaatan tanaman mahkota dewa khususnya buah sebagai pengobatan tidak memisahkan antara daging buah dan kulitnya, artinya kulit tidak perlu dikupas terlebih dahulu, bagian buah lainnya yang juga bermanfaat adalah cangkang buah. Kulit dan daging buah dikonsumsi secara langsung dengan cara direbus dahulu.
Bagian dari buah mahkota dewa yaitu biji yang merupakan bagian tanaman yang paling berbahaya karena memiliki sifat yang sangat beracun. Pemanfatan biji dilakukan dengan cara dikeringkan dan disangrai sampai gosong. Daun mahkota dewa yang berwarna hijau dengan permukaan licin juga sering digunakan sebagai pengobatan dengan cara direbus seperti alergi (Dyah, 2007). 2.1.4 Penggunaan Tanaman
Daun mahkota dewa (Phaleria macrocarpa (Scheff.) Boerl) digunakan sebagai antikanker, astringent, antimikroba, antiperadangan dan antihistamin (Agoes, 2010).
2.2 Ekstraksi
8
(kemudahan diabsorpsi, rasa, dan pemakaian) dan disimpan dibandingkan simplisia asal, dan tujuan pengobatannya lebih terjamin (Syamsuni, 2006).
Hasil ekstraksi disebut dengan ekstrak, yaitu sediaan pekat yang diperoleh dengan mengektraksi zat aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan. Simplisia yang digunakan dalam proses pembuatan ekstrak adalah bahan alamiah yang belum mengalami pengolahan apapun juga dan kecuali dinyatakan lain berupa bahan yang telah dikeringkan (Depkes, 2000).
2.2.1 Metode Ekstraksi
Menurut Depkes (2000) metode ekstraksi menggunakan pelarut dapat dilakukan dengan beberapa cara yaitu:
a. Cara dingin i. Maserasi
Maserasi adalah proses ekstraksi simplisia dengan menggunakan pelarut dengan beberapa kali pengadukan pada temperatur ruangan.
ii. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses ini terdiri dari tahapan pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak).
b. Cara panas i. Refluks
konstandengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama sampai 3-5 kali sehingga dapat termasuk proses ekstraksi sempurna.
ii. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
iii. Digesti
Digesti adalah maserasi dengan pengadukan kontinu pada temperatur yang lebih tinggi dari temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40-50oC.
iv. Infudasi
Infudasi adalah sediaan cair yang dibuat dengan menyari simplisia nabati dengan air pada suhu 90oC selama 15 menit, Hasil infudasi disebut dengan infus.
v. Dekoktasi
Dekoktasi adalah sediaan cair yang dibuat dengan menyari simplisia nabati dengan air pada waktu yang lebih lama ± 30 menit dengan temperatur sampai titik didih air.
2.3 Reaksi Hipersensitivitas
10
kemudian terpapar lagi untuk kedua kalinya atau lebih dapat menimbulkan respon imun sekunder (Nahak,2013).
Respon imun sekunder atau kontak selanjutnya degan antigen yang sama akan menimbulkan respon imun lebih kuat. Pada hipersentivitas, respon sekunder tersebut terjadi secara menyimpang atau berlebihan sehingga menyebabkan reaksi radang atau kerusakan jaringan.Coombs dan Gell telah mengidentifikasi empat tipe reaksi hipersentivitas (Tipe I, II, III, dan IV).Kerusakan jaringan pada penyakit infeksi juga dapat ditimbulkan oleh satu atau lebih reaksi hipersensitivitas ini (Wahab, 2002).
2.3.1 Hipersensitivitas Tipe I
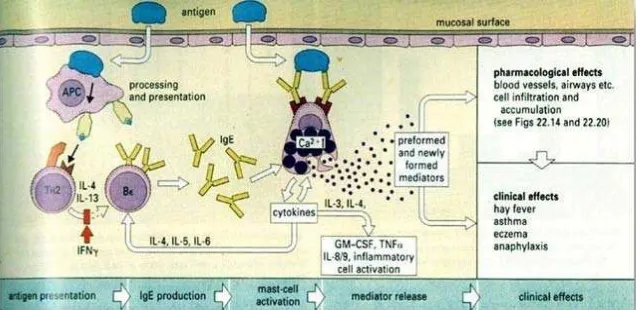
Hipersensitivitas tipe I ditandai dengan reaksi alergi yang terjadi segera setelah kontak dengan antigen yang disebut alergen.Istilah alergi sendiri berarti perubahan reaktivitas tanda klinis.Pada tipe hipersensitivitas ini, antigen bereaksi dengan antibodi yang terikat pada sel mast jaringan atau basofil dalam sirkulasi.Antibodi yang dihasilkan biasanya IgE, dapat dilihat pada Gambar 2.1 (Wahab,2002).
Molekul IgE menempel pada sel mast melaluai reseptor Fc, hubungan silang IgE pada permukaan sel mast disebabkab oleh pengikatan alergen yang menyebabkan sel mast mengalami degranulasi melepaskan histamine dan mediator alergi kimia lain. Tanda klinis hipersensitivitas tipe I meliputi asma, hay
fever dan urtikaria (Harr,2002).
2.3.2 Hipersensitivitas Tipe II
Hipersensitivitas tipe II dimediasi oleh antibodi IgG dan IgM yang berikatan pada sel atau jaringan tertentu.Dengan demikian, kerusakan yang terjadi terbatas pada sel atau jaringan yang membawa antigen yang dituju oleh IgG dan/atau IgM tersebut. Pada hipersensitivitas tipe ini, antibodi terhadap antigen permukaan suatu sel melekat pada sel tersebut dan mengakibatkan kehancuran sel dengan cara mengaktifkan sel pembunuh sitotoksik, meningkatkan fagositosis atau menyebabkan lisis melalui aktivasi komplemen (Wahab, 2002).
Hipersensitivitas tipe II disebabkan pembentukan komplek antigen-antibodi di antara antigen asing dan immunoglobulin IgG atau IgM.Jenis hipersensitivitas ini biasanya terjadi selama reaksi transfusi darah dan terjadi pada penyakit hemolisis bayi baru lahir (Katzung, 2001).
2.3.3 Hipersensitivitas Tipe III
12
hipersensitivitas ini ditemukan pada infeksi mikroba persisten tertentu yang membentuk sejumlah besar kompleks dan tidak dapat dibersihkan secara sempurna oleh sistem retikuloendotelial.Komplek ini mengendap pada jaringan seperti glomerulus, sinovium, dinding pembuluh darah, serta mengakibatkan kehancuran jaringan tersebut (Wahab, 2002).
2.3.4 Hipersensitivitas Tipe IV
Reaksi hipersensitivitas tipe IV merupakan hipersensitivitas tipe lambat akan muncul setelah lebih dari 12 jam dan terutama melibatkan reaksi imun seluler dan bukan reaksi imun imun humoral. Hipersensitivitas tipe IV tergantung pada limfosit T yang yang tersensitisasi saat kontak dengan antigen yang terkait makrofag.Limfosit T kemudian berproliferasi dan melepaskan berbagai sitokin.Reaksi ini mengakibatkan akumulasi sel-sel radang yang terlokalisasi dan kerusakan jaringan (Wahab, 2002).
2.4 Aminofilin
Aminofilin (suatu komplek teofilin-etilendiamin) merupakan preparat teofilin yang paling umum digunakan untuk penyakit asma.Aminofilin memiliki kelarutan yang lebih besar dari pada teofilin sehingga senyawa ini lebih sering digunakan untuk sediaan asma.Struktur aminofilin dapat dilihat pada Gambar 2.2.
Nama kimia : 1H-Purin-2,6-dione, 3,7-dihidro-1,3- dimetil dengan 1,2- etilendiamin (2:1)
Rumus molekul : C16H24N20O4.2H2O
Pemerian : Butir atau serbuk putih atau agak kekuningan, bau ammoni lemah, rasa pahit. Jika dibiarkan di udara terbuka, perlahan-lahan kehilangan etilen-diamin dan menyerap karbon dioksida dengan melepaskan teofilin.
Kandungan : Tidak kurang dari 84% dan tidak lebih dari 87,4% teofilin anhidrat, C6H8N4O2 dihitung terhadap zat anhidrat.
Kelarutan : 1g aminofilin larut dalam 25 ml air (Depkes RI., 1995). Mekanisme kerja dari teofilin yaitu dengan cara menghambat enzim fosfodiesterase sehingga mencegah pemecahan cAMP dan cGMP masing-masing menjadi 5-AMP dan 5-GMP. Penghambatan fosfodiesterase menyebabkan akumulasi cAMP dan cGMP dalam sel sehingga menyebabkan relaksasi otot polos, termasuk otot polos bronkus (Gunawan, 2007).
2.5 Imunoglobulin
14
tersebut.Antibodi meliputi sekitar 20% protein dalam plasma darah (Wahab, 2002).
a. IgG
IgG mempunyai rantai γ (G), dalam serum orang dewasa normal, IgG
merupakan 75% dari imunoglobulin total, dan dijumpai dalam bentuk monomer. IgG merupakan imunoglobulin pertama dibentuk atas rangsangan antigen. IgG dapat menembus plasentadan masuk ke dalam peredaran darah janin,sehingga pada bayi baru lahir IgG yang berasal dari ibu yang melindungi bayi terhadap infeksi.Diantara semua kelas imunoglobulin, IgG paling mudah berdifusi ke dalam jaringan ekstravaskuler dan melakukan aktivitas antibodi di jaringan.
b. IgA
IgA mempunyai rantai α (A), kelas imunoglobulin kedua terbanyak dalam
serum, walaupun demikian IgA terutama berfungsi dalam cairan sekresi dan diproduksi dalam jumlah besar oleh sel plasma dalam jaringan limfoid yang terdapat sepanjang saluran cerna, saluran nafas.
c. IgM
kemudian menurun.Selain itu karena IgM tidak dapat menenbus plasenta, adanya antibodi kelas IgM dalam darah bayi baru lahir menunjukkan bahwa IgM dibentuk oleh bayi sebagai respon terhadap infeksi.
d. IgD
IgD mempunyai rantai δ (D), merupakan monomer dan konsentrasi dalam serum sangat sedikit, peran biologiknya sebagai antibodi humoral belum jelas, yang telah diketahui adalah perannya sebagai antibodi dalam reaksi hipersensitifitas terhadap penisilin.Imunoglobulin D (IgD) dapat dijumpai pada permukaan sel B.
e. IgE
IgE mempunyai rantai ε (E), dapat dijumpai dalam serum dengan kadar
16 2.6 Sistem Imunitas
Sistem imunitas ialah semua mekanisme yang digunakan badan untuk mempertahankan keutuhan tubuh sebagai perlindungan terhadap bahaya yang dapat ditimbulkan berbagai bahan dalam lingkungan hidup.Lingkungan hidup manusia yang tercemar berbagai bahan organik dan anorganik, baik yang hidup seperti bakteri, virus, jamur, parasit maupun yang mati.Debu dan polusi yang setiap saat dapat masuk kedalam tubuh dapat menimbulkan kerusakan jaringan atau penyakit (Baratawidjaja, 1996).
2.7 Respon Imunitas Tubuh
Lingkungan di sekitar manusia mengandung berbagai jenis unsur pathogen, misalnya bakteri, virus, fungus, protozoa dan parasit yang dapat menyebabkan infeksi pada manusia.Infeksi yang terjadi pada orang normal umumnya singkat dan jarang meninggalkan kerusakan permanen.Hal ini disebabkan tubuh manusia memiliki suatu sistem yang disebut sistem imun yang memberikan respon dan melindungi tubuh terhadap unsur-unsur patogen tersebut.Bila Respon imun terpapar pada zat yang dianggap asing, maka ada dua jenis respon imun yang mungkin terjadi (Kresno, 2010).
2.7.1 Respon imun nonspesifik (bawaan)
2.7.2 Respon imun spesifik
Respon imun spesifik merupakan mekanisme pertahanan tubuh yang ditujukan khusus terhadap satu jenis antigen, karena itu dapat berperan terhadap antigen jenis lain. Imun spesifik mampu mengenali kembali antigen yang pernah dijumpainya, sehingga paparan berikutnya akan meningkatkan efektifitas mekanisme pertahanan tubuh (Kresno, 2010).
2.8 Mastosit
Sel mastosit merupakan sel efektor reaksi hipersensitivitas cepat dari penyakit alergi.Mastosit mengandung granula sitoplasmik yang isinya merupakan mediator utama reaksi alergi, granula mastosit merupakan komponen utama dari semua penyakit alergi.Kandungan utama granula mastosit ini adalah heparin dan histamin. Perkembangan sel mastosit tidak bergantung sel T, sel mastosit diaktifkan oleh cross-linking dengan reseptor FceRI yang terjadi akibat pengikatan antigen pada molekul IgE (Kresno,2010).
1 BAB I PENDAHULUAN 1.1 Latarbelakang
Penggunaan obat tradisional telah lama digunakan diseluruh dunia dan menurut World Health Organization (WHO), sekitar 65% dari penduduk negara maju dan 80% dari penduduk negara berkembang telah menggunakan obat herbal sebagai obat tradisional. Dukungan WHO terhadap konsep back to nature dibuktikan dengan adanya rekomendasi untuk menggunakan obat tradisional termasuk herbal kedalam pemeliharaan kesehatan masyarakat dan pencegahan penyakit, terutama untuk penyakit infeksi yaitu sistem imun yang kurang baik penyakit degeneratif dan kanker (Sukandar, 2006).
Bangsa Indonesia mengenal dan menggunakan tanaman berkhasiat obat sebagai salah satu upaya dalam menanggulangi masalah kesehatan. Pengetahuan tentang tanaman berkhasiat obat berdasarkan pada pengalaman dan keterampilan yang secara turun temurun telah diwariskan dari satu generasi kegenerasi berikutnya (Sari,2006).
Seiring dengan perkembangan zaman tanaman mahkota dewa semakin penting untuk diteliti karena hampir seluruh bagian tanamannya dapat dimanfaatkan untuk pengobatan, kosmetik dan lain-lain.Menurut De Padua, dkk., (1999) dalam daun terkandung alkaloid, saponin, serta polifenol dan ekstrak daunnya dapat memberikan efek antihistamin (Rohyami, 2008).
berfungsi sebagai antihistamin. Zat lain yang terdapat pada tumbuhan mahkota dewa adalah tanin, sterol dan terpen (Agoes,2010).Pembudidayaan mahkota dewa tidak terlalu sulit, karena dapat diperbanyak dengan cara vegetatif maupun generatif. Daun mahkota dewa sering direbus untuk menyembuhkan penyakit disentri, alergi dan tumor.
Menurut Sumastuti, berhasil membuktikan bahwa mahkota dewa mengandung zat antihistamin. Zat ini merupakan penangkal alergi yang bisa menyembuhkan penyakit alergi yang disebabkan oleh histamin seperti biduran gatal-gatal dan sesak napas (Harmanto,2004).
Reaksi alergi terjadi jika seseorang telah memproduksi antibodi IgE akibat terpapar suatu antigen (alergen), terpapar kembali oleh antigen yang sama. Alergen memicu terjadinya aktivitas sel mast yang mengikat IgE pada jaringan. IgE merupakan antibodi yang sering terlihat pada reaksi melawan parasit, oleh karena alergi menjadi masalah kesehatan yang cukup penting sehingga patofisiologi yang ditimbulkan oleh IgE lebih diketahui dari pada peran IgE pada fisiologi normal.Alergi merupakan salah satu respon sistem imun yang disebut reaksi hipersensitif (Rifa’i, 2010).
3
melalui reseptor Fc pada permukaan sel bersangkutan yang mengikat fragmen Fc IgE. Sekali terikat, IgE dapat melekat pada permukaan mastosit dan basofil selama beberapa minggu dan IgE yang terikat inilah yang berperan besar pada reaksi anafilaktik (Kresno, 2010).
Bila suatu protein asing (antigen) masuk berulang kali kedalam aliran darah seseorang terjadi hipersensitif, maka limfosit B akan membentuk antibodi dari tipe IgE, sehingga IgE akan mengikat diri pada membran sel mast tanpa menimbulkan gejala. Apabila kemudian antigen (alergen) yang sama atau mirip rumus bangunnya memasuki darah lagi, maka IgE akan mengenali dan mengikat diri padanya. Hasilnya adalah suatu reaksi alergi akibat pecahnya membran sel mast. Sejumlah zat perantara (mediator) dilepaskan yakni histamin bersama serotonin, bradikinin dan asam arakidonat yang kemudian diubah menjadi prostaglandin dan leukotrien. (Tan dan Rahardja, 2007).
Salah satu tumbuhan yang berkhasiat obat adalah tanaman mahkota dewa (Phaleria macrocarpa (Scheff) Boerl), sukuThymelaeaceae, merupakan salah satu tanaman asli Indonesia yang akhir-akhir ini populer sebagai tanaman yang secara empiris dapat mengobati berbagai macam penyakit, yaitu kanker, antimikroba, penyakit kulit seperti alergi dan astrigent (Hariana, 2009).
1.2 Perumusan Masalah
Berdasarkan latarbelakang diatas, maka perumusan masalah pada penelitian ini adalah:
a. apakah simplisia daun mahkota dewa dapat ditentukan karakteristiknya? b. apakah ekstrak etanol daun mahkota dewa dapat menghambat degranulasi
mastosit pada mencit yang diinduksi dengan putih telur ayam? 1.3 Hipotesis
Berdasarkan perumusan masalah diatas, maka hipotesis pada penelitian ini adalah:
a. karakteristik simplisia daun mahkota dewa dapat ditentukan dengan menggunakan prosedur karakteristik simplisia pada Materia Medika Indonesia.
b. ekstrak etanol daun mahkota dewa dapat menghambat degranulasi mastosit pada mencit yang diinduksi dengan putih telur ayam.
1.4 Tujuan Penelitian
Berdasarkan hipotesis di atas, maka tujuan penelitian ini adalah : a. untuk mengetahui karakteristik simplisia daun mahkota dewa
b. untuk mengetahui efek penghambatan degranulasi mastosit ekstrak etanol daun mahkota dewa pada mencit yang diinduksi dengan putih telur ayam 1.5 Manfaat Penelitian
a. mengembangkan daun mahkota dewa menjadi suatu sediaan herbal terstandar dengan efek antialergi
5 1.6 Kerangka Pikir
Subjek yang digunakan dalam penelitian ini adalah mencit jantan yang telah disensitisasi aktif dengan menginduksi putih telur ayam 50% secara in
vitro. Terdapat 5 variabel bebas yaitu EEDMD dengan konsentrasi 500µg/ml,
400µg/ml, 300µg/ml, 200µg/ml dan 100µg/ml digunakan untuk uji penghambatan degranulasi mastosit dengan cara menghitung persen penurunan jumlah terdegranulasi dapat dilihat pada Gambar 1.1 berikut:
Variabel Bebas Variabel Terikat Parameter
UJI PENGHAMBATAN DEGRANULASI MASTOSIT
TERSENSITISASI AKTIF OLEH EKSTRAK ETANOL DAUN
MAHKOTA DEWA (Phaleria macrocarpa (Scheff.) Boerl)
PADA MENCIT JANTAN
ABSTRAK
Reaksi alergi merupakan respon tubuh seseorang menjadi hipersensitif dan bereaksi secara imunologi terhadap bahan-bahan imunogenik. Mastosit secara luas dianggap sebagai sel efektor penting dalam respon imun yang bertanggungjawab atas terjadinya reaksi alergi yang dimediasi oleh imunoglobulin E (IgE). Tanaman mahkota dewa (Phaleria macrocarpa (Scheff) Boerl) merupakan salah satu tanaman yang daunnya diduga memiliki aktivitas sebagai anti alergi. Tujuan penelitian ini adalah untuk mengetahui efek penghambatan pada degranulasi mastosit ekstrak etanol daun mahkota dewa (EEDMD) pada mencit jantan yang diinduksi putih telur ayam konsentrasi 50%.
Metode ditentukan dengan menghitung jumlah mastosit yang tidak terdegranulasi yang berasal dari cairan intraperitoneal mencit yang diisolasi menggunakan alat improved Neubauer hemocytometer. Mastosit yang terdegranulasi diwarnai dengan larutan biru toluidin. EEDMD dengan konsentrasi 100 µg/ml, 200 µg/ml, 300 µg/ml, 400 µg/ml, 500 µg/ml sebagai bahan uji. Aminofilin dosis 100 µg/ml sebagai kontrol positif dan larutan DMSO 1% sebagai kontrol negatif. Kemampuan EEDMD dalam menghambat degranulasi mastosit dilihat dari persen penurunan jumlah mastosit yang terdegranulasi. Dari hasil penelitian menunjukkan bahwa kemampuan ektrak daun mahkota dewa 500 µg/ml (39,39%), 400 µg/ml (45,58%), 300 µg/ml (51,02%), 200 µg/ml (54,59%), 100 µg/ml (56,51%), Aminofilin 100 µg/ml (32,28%). Dari hasil Analisis satistik pemberian EEDMD pada konsentrasi 500 µg/ml, 400 µg/ml mampu menghambat degranulasi mastosit tersensitisasi aktif secara signifikan terhadap kontrol negatif (p < 0,05).
Dengan demikian disimpulkan bahwa EEDMD konsentrasi 500 µg/ml dan 400 µg/ml dengan aminofilin 100 µg/ml mempunyai aktivitas penghambatan degranulasi mastosit tersensitisasi aktif pada mencit jantan secara in-vitro.
vii
INHIBITING TEST OF ACTIVE SENSITIZED MASTOCYTE
DEGRANULATION BY MAHKOTA DEWA
(Phaleria macrocarpa (Scheff.) Boerl) LEAVES
ETHANOL EXTRACT IN MALE MICE
ABSTRACT
An allergic reaction is a response to a person's body becomes hypersensitive and reacts immunologically to the immunogenic material. Mastosit is widely regarded as an important effector cells in the immune response is responsible for the occurrence of allergic reactions mediated by immunoglobulin E (IgE). Plant mahkota dewa (Phaleria macrocarpa (Scheff) Boerl) is a plant whose leaves are thought to have activity as an anti-allergy. The purpose of this study was to determine the inhibitory effect on degranulation of mast cells ethanol extract of mahkota dewa (EEDMD) in male mice induced egg white chicken concentration of 50%.
The method is determined by counting the number of mast cells were not terdegranulasi intraperitoneal fluid derived from mice that were isolated using a Neubauer hemocytometer improved. Mastosit which terdegranulasi stained with toluidine blue solution. EEDMD with a concentration of 100 µg/ml, 200 µg/ml, 300 µg/ml, 400 µg/ml, 500 µg/ml as the test material. Aminophylline dose of 100 µg/ml as a positive control and a solution of 1% DMSO as a negative control. EEDMD ability to inhibit the degranulation of mast cells per cent decline seen from the number of mast cells terdegranulasi. The results showed that the ability of the extracts ethanol mahkota dewa 500 µg/ml (39.39%), 400 µg/ml (45.58%), 300 µg/ml (51.02%), 200 µg/ml (54.59%), 100 µg/ml (56.51%), Aminofilin 100 µg/ml (32.28%). Statistical analysis of the results of the EEDMD administration at a concentration of 500 µg/ml, 400 µg/ml was able to inhibit degranulation of mast cells actively sensitized significantly to the negative control (p <0.05).
Thus concluded that EEDMD concentration of 500 µg/ml and 400 µg/ml with aminophylline 100 µg/ml had inhibitory activity degranulation of mast cells in male mice sensitized active in vitro.
UJI PENGHAMBATAN DEGRANULASI MASTOSIT
TERSENSITISASI AKTIF OLEH EKSTRAK ETANOL
DAUN MAHKOTA DEWA (Phaleria macrocarpa (Scheff) Boerl)
PADA MENCIT JANTAN
SKRIPSI
OLEH:
DWI YUNITA HAREFA
NIM 111501005
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI PENGHAMBATAN DEGRANULASI MASTOSIT
TERSENSITISASI AKTIF OLEH EKSTRAK ETANOL
DAUN MAHKOTA DEWA (Phaleria macrocarpa (Scheff) Boerl)
PADA MENCIT JANTAN
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
DWI YUNITA HAREFA
NIM 111501005
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI PENGHAMBATAN DEGRANULASI MASTOSIT
TERSENSITISASI AKTIF OLEH EKSTRAK ETANOL
DAUN MAHKOTA DEWA (Phaleria macrocarpa (Scheff) Boerl)
PADA MENCIT JANTAN
OLEH:
DWI YUNITA HAREFA NIM 111501005
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 05 Januari 2016
iv
KATA PENGANTAR
Puji dan syukur kehadirat Allah SWT yang telah memberikan karunia yang berlimpah sehingga penulis dapat menyelesaikan penyusunan skripsi yang berjudul “Uji Penghambatan Degranulasi Mastosit Tersensitisasi Aktif Oleh Ekstrak Etanol Daun Mahkota Dewa (Phaleria macrocarpa (Scheff) Boerl) Pada Mencit Jantan”. Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini, dengan segala kerendahan hati penulis mengucapkan terima kasih yang sebesar-besarnya kepada Ibu Masfria, M.S., Apt., selaku Pejabat Dekan Fakultas Farmasi yang telah menyediakan fasilitas kepada penulis selama perkuliahan di Fakultas Farmasi. Penulis juga mengucapkan terima kasih kepada Ibu Prof. Dr. Rosidah, M.Si., Apt dan Ibu Poppy Anjelisa Z. Hsb., M.Si., Apt yang telah meluangkan waktu dan tenaga dalam membimbing penulis dengan penuh kesabaran dan tanggung jawab, memberikan petunjuk dan saran-saran selama penelitian hingga selesainya skripsi ini. Ucapan terima kasih juga penulis sampaikan kepada Bapak Prof. Dr. Urip Harahap , Apt., selaku ketua penguji, Bapak Drs. Saiful Bahri, M.S., Apt, Ibu Aminah Dalimunthe, S.Si., M.Si., Apt dan dan Ibu Marianne, S.Si, M.Si., Apt selaku anggota penguji yang telah memberikan saran untuk menyempurnakan skripsi ini, dan Bapak Chairul Azhar Dalimunthe, Drs., M.Sc., Apt selaku dosen pembimbing akademik serta Bapak dan Ibu staf pengajar Fakultas Farmasi USU yang telah banyak membimbing penulis selama masa perkuliahan hingga selesai.
Adikku Diah Tria Chantika Harefa dan Dava Aisy Nabillah Harefa., atas limpahan kasih sayang, semangat dan doa yang tak ternilai dengan apapun. Penulis juga mengucapkan terima kasih kepada teman-teman asisten Teknologi Sediaan Farmasi III Farmasi USU dan sahabat tercinta, Nurhasanah, Cindy, Lisa, Wulan, Suli, Qisthi, Maal, Aini, Dwiluti, Hera, Ame dan Falah serta Mahasiswa/i angkatan 2011 Fakultas Farmasi USU yang selalu mendoakan dan memberi semangat.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum sempurna, oleh karena itu penulis mengharapkan saran dan kritik yang membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, Januari 2016 Penulis,
vi
UJI PENGHAMBATAN DEGRANULASI MASTOSIT
TERSENSITISASI AKTIF OLEH EKSTRAK ETANOL DAUN
MAHKOTA DEWA (Phaleria macrocarpa (Scheff.) Boerl)
PADA MENCIT JANTAN
ABSTRAK
Reaksi alergi merupakan respon tubuh seseorang menjadi hipersensitif dan bereaksi secara imunologi terhadap bahan-bahan imunogenik. Mastosit secara luas dianggap sebagai sel efektor penting dalam respon imun yang bertanggungjawab atas terjadinya reaksi alergi yang dimediasi oleh imunoglobulin E (IgE). Tanaman mahkota dewa (Phaleria macrocarpa (Scheff) Boerl) merupakan salah satu tanaman yang daunnya diduga memiliki aktivitas sebagai anti alergi. Tujuan penelitian ini adalah untuk mengetahui efek penghambatan pada degranulasi mastosit ekstrak etanol daun mahkota dewa (EEDMD) pada mencit jantan yang diinduksi putih telur ayam konsentrasi 50%.
Metode ditentukan dengan menghitung jumlah mastosit yang tidak terdegranulasi yang berasal dari cairan intraperitoneal mencit yang diisolasi menggunakan alat improved Neubauer hemocytometer. Mastosit yang terdegranulasi diwarnai dengan larutan biru toluidin. EEDMD dengan konsentrasi 100 µg/ml, 200 µg/ml, 300 µg/ml, 400 µg/ml, 500 µg/ml sebagai bahan uji. Aminofilin dosis 100 µg/ml sebagai kontrol positif dan larutan DMSO 1% sebagai kontrol negatif. Kemampuan EEDMD dalam menghambat degranulasi mastosit dilihat dari persen penurunan jumlah mastosit yang terdegranulasi. Dari hasil penelitian menunjukkan bahwa kemampuan ektrak daun mahkota dewa 500 µg/ml (39,39%), 400 µg/ml (45,58%), 300 µg/ml (51,02%), 200 µg/ml (54,59%), 100 µg/ml (56,51%), Aminofilin 100 µg/ml (32,28%). Dari hasil Analisis satistik pemberian EEDMD pada konsentrasi 500 µg/ml, 400 µg/ml mampu menghambat degranulasi mastosit tersensitisasi aktif secara signifikan terhadap kontrol negatif (p < 0,05).
Dengan demikian disimpulkan bahwa EEDMD konsentrasi 500 µg/ml dan 400 µg/ml dengan aminofilin 100 µg/ml mempunyai aktivitas penghambatan degranulasi mastosit tersensitisasi aktif pada mencit jantan secara in-vitro.
INHIBITING TEST OF ACTIVE SENSITIZED MASTOCYTE
DEGRANULATION BY MAHKOTA DEWA
(Phaleria macrocarpa (Scheff.) Boerl) LEAVES
ETHANOL EXTRACT IN MALE MICE
ABSTRACT
An allergic reaction is a response to a person's body becomes hypersensitive and reacts immunologically to the immunogenic material. Mastosit is widely regarded as an important effector cells in the immune response is responsible for the occurrence of allergic reactions mediated by immunoglobulin E (IgE). Plant mahkota dewa (Phaleria macrocarpa (Scheff) Boerl) is a plant whose leaves are thought to have activity as an anti-allergy. The purpose of this study was to determine the inhibitory effect on degranulation of mast cells ethanol extract of mahkota dewa (EEDMD) in male mice induced egg white chicken concentration of 50%.
The method is determined by counting the number of mast cells were not terdegranulasi intraperitoneal fluid derived from mice that were isolated using a Neubauer hemocytometer improved. Mastosit which terdegranulasi stained with toluidine blue solution. EEDMD with a concentration of 100 µg/ml, 200 µg/ml, 300 µg/ml, 400 µg/ml, 500 µg/ml as the test material. Aminophylline dose of 100 µg/ml as a positive control and a solution of 1% DMSO as a negative control. EEDMD ability to inhibit the degranulation of mast cells per cent decline seen from the number of mast cells terdegranulasi. The results showed that the ability of the extracts ethanol mahkota dewa 500 µg/ml (39.39%), 400 µg/ml (45.58%), 300 µg/ml (51.02%), 200 µg/ml (54.59%), 100 µg/ml (56.51%), Aminofilin 100 µg/ml (32.28%). Statistical analysis of the results of the EEDMD administration at a concentration of 500 µg/ml, 400 µg/ml was able to inhibit degranulation of mast cells actively sensitized significantly to the negative control (p <0.05).
Thus concluded that EEDMD concentration of 500 µg/ml and 400 µg/ml with aminophylline 100 µg/ml had inhibitory activity degranulation of mast cells in male mice sensitized active in vitro.
viii DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB 1 PENDAHULUAN ... 1
1.1 Latar belakang ... 1
1.2 Perumusan masalah ... 4
1.3 Hipotesis ... 4
1.4 Tujuan ... 4
1.5 Manfaat penelitian ... 4
1.6 Kerangka pikir ... 5
BAB 2 TINJAUAN PUSTAKA ... 6
2.1 Uraian Tumbuhan ... 6
2.1.1 Sistematika Tumbuhan ... 6
2.1.2 Nama Daerah ... 6
2.1.3 Bagian yang Digunakan ... 7
2.2 Ekstraksi ... 7
2.2.1 Metode Ekstraksi ... 8
2.3 Reaksi Hipersensitivitas ... 9
2.3.1 Hipersensitivitas Tipe I ... 10
2.3.2 Hipersensitivitas Tipe II ... 11
2.3.3 Hipersensitivitas Tipe III ... 11
2.3.4 Hipersensitivitas Tipe IV ... 12
2.4 Aminofilin ... 12
2.5 Imunoglobulin ... 13
2.6 Sistem Imun ... 16
2.7 Respon Imunitas Tubuh ... 16
2.7.1 Respon Imun Nonspesifik ... 16
2.7.2 Respon Imun Spesifik ... 17
2.8 Mastosit ... 17
BAB 3 METODE PENELITIAN ... 18
3.1 Alat dan bahan ... 18
3.1.1 Alat ... 18
3.1.2 Bahan ... 18
3.2 Hewan Percobaan ... 19
3.3 Penyiapan tanaman... ... ……. 19
3.3.1 Pengumpulan tanaman ... 19
3.3.2 Identifikasi tanaman ... 20
3.3.3 Pengolahan simplisia ... 20
x
3.4.1 Pemeriksaan Makroskopik ... 20
3.4.2 Pemeriksaan Mikroskopik ... 21
3.4.3 Penetapan Kadar Air ... 21
3.4.4 Penetapan Kadar Sari Larut Air ... 22
3.4.5 Penetapan Kadar Sari Larut Etanol ... 22
3.4.6 Penetapan Kadar Abu Total ... 22
3.4.7 Penetapan Kadar Abu Tidak Larut Asam ... 23
3.5 Skrining Fitokimia ... 23
3.5.1 Pemeriksaan Alkaloida ... 23
3.5.2 Pemeriksaan Flavonoid ... 24
3.5.3 Pemeriksaan Glikosida ... 24
3.5.4 Pemeriksaan Tanin ... 24
3.5.5 Pemeriksaan Saponin ... 25
3.5.6 Pemeriksaan Steroid/triterpenoid ... 25
3.6 Pembuatan Ekstrak EEDMD ... 25
3.7 Uji Aktivitas Penghambatan Degranulasi Mastosit ... 26
3.7.1 Penyiapan Sediaan ... 26
3.7.1.1 Pembuatan Larutan Putih Telur Ayam 50% ... 26
3.7.1.2 Pembuatan Larutan PBS ... 26
3.7.1.3 Pembuatan Larutan Trypan Blue 0,4% ... 27
3.7.1.4 Pembuatan Larutan Uji ... 27