KONSENTRASI, VIABILITAS SPERMATOFOR DAN
KARAKTERISTIK MORFOLOGI SPERMATOZOA
KEPITING BAKAU MERAH (Scylla olivacea
HERBEST 1796)
ASAL JAWA, SULAWESI DAN PAPUA
NURIL FARIZAH
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
ii
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis Konsentrasi,Viabilitas Spermatofor dan Karakteristik Morfologi Spermatozoa Kepiting Bakau Merah
(Scylla olivacea Herbest 1796) Asal Jawa, Sulawesi dan Papua adalah karya saya
dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, 11 Agustus 2009
iii
ABSTRACT
NURIL FARIZAH. Concentration, Viability Of Spermatophores And Morphology Characteristic Of Mud Crab Spermatozoa (Scylla Olivacea Herbest 1796 ) From Java, Celebes and Papua. Under Direction of ARIEF BOEDIONO and R. IIS ARIFIANTINI
Mud crab (Scylla olivacea) is fishery commodity posses a high economic value in Indo-Pacific region. Market supply depends on the seasons, so the continuity product is not available in all years. It effect the aquaculture development of mud crab. The successful of hatchery have influenced by broodstock quality, including the role of male broodstock. The research aim to study the biology reproduction of male mud crab from three locations (Java, Celebes, and Papua). Studies were conducted based on the macro and micro morphology of male reproduction characteristics. The result obtained, that carapace size, weight and color of Scylla olivacea in Java (6.8 ± 0.8 and 10.0 ± 1.0 mm), weight (208.1 ± 59.7 g) and color of body is green to brown. Sample from Celebes (8.4 ± 0.6 and 11.9 ± 0.9 mm), weight (486.9 ± 100.6 g), and Papua (8.9 ± 0.5 and 12.3 ± 0.8 mm), weight (566.3 ± 138.1 g) with color of body is green to red. The weight of testes is 0.8 ± 0.5 g with GSI; 0.06 - 0.82 %, for Java. Celebes, testes weight is 1.9 ± 0.8 g with GSI; 0.12 - 0.72 % and for sample from Papua showed weight of testes is 2.3 ± 0.9 g with GSI; 0.13 – 1.07%. Scylla olivacea is produce simple spermatophores and have aflagellate spermatozoa and non-motile.
iv
RINGKASAN
NURIL FARIZAH. Konsentrasi, Viabilitas Spermatofor dan Karakteristik Morfologi Spermatozoa Kepiting Bakau Merah ( Scylla olivacea Herbest 1796 ) Asal Jawa, Sulawesi dan Papua. Dibimbing oleh ARIEF BOEDIONO dan R. IIS ARIFIANTINI.
Kepiting bakau merah (Scylla olivacea) merupakan salah satu dari ke empat spesies kepiting bakau di dunia. Kepiting ini memiliki keunggulan dari ketiga spesies kepiting lainnya, yakni proses reproduksinya lebih singkat dan dapat bertahan hidup dalam kondisi ekstrim. Usaha pembenihan yang dilakukan belum memberikan hasil yang maksimal karena survival rate dari benih yang dihasilkan masih sangat rendah. Hal ini mungkin disebabkan oleh penyediaan indukan yang berkualitas rendah sehingga berdampak pada kualitas benih yang dihasilkan. Keberhasilan kegiatan pembenihan dipengaruhi oleh kualitas induk, yaitu induk yang memiliki sel telur atau sel spermatozoa berkualitas baik. Informasi mengenai induk betina maupun jantan yang ideal untuk kegiatan pembenihan kepiting bakau masih sangat minim. Induk jantan yang berkualitas tinggi adalah induk jantan yang memiliki jumlah dan viabilitas spermatozoa yang tinggi, sehingga mempengaruhi keberhasilan dalam fertilisasi yang tinggi. Penelitian ini bertujuan mengkaji performans reproduksi kepiting bakau merah jantan (Scylla olivacea) pada daerah Jawa Barat, Sulawesi Selatan dan Papua Barat. Performans reproduksi yang dikaji, meliputi; konsentrasi, viabilitas spermatofor dan karakteristik morfologi spermatozoa.
Studi yang dilakukan berdasarkan pengamatan morfologi secara makro dan mikro dari karakteristik reproduksi jantan kepiting bakau merah (Scylla
olivacea). Hasil yang diperoleh menunjukkan tiap daerah memiliki performans
reproduksi yang berbeda hal ini diduga karena perbedaan lokasi yang mempengaruhinya. Untuk ukuran karapas, bobot tubuh dan warna tubuh dari
Scylla olivacea asal Jawa (6.8 ± 0.8 dan 10.0 ± 1.0 mm), bobot tubuh (208.1 ±
59.7 g) dan warna tubuh hijau kecoklatan sampai kemerahan. Sampel dari Sulawesi memiliki ukuran karapas (8.4 ± 0.6 dan 11.9 ± 0.9 mm), dan bobot tubuh (486.9 ± 100.6 g), untuk sampel Papua memiliki ukuran karapas (8.9 ± 0.5 dan 12.3 ± 0.8 mm), bobot badan (566.3 ± 138.1 g) dengan warna tubuh yang agak kemerahaan. Bobot dari testis adalah 0.8 ± 0.5 g dengan GSI; 0.06 - 0.82 %, untuk Jawa. Sampel Sulawesi, bobot testes adalah 1.9 ± 0.8 g dengan GSI; 0.12 - 0.72 % dan untuk sampel dari Papua menunjukkan bobot testes 2.3 ± 0.9 g dengan GSI; 0.13 – 1.07 %.
v konsentrasi spermatofor dari 7.37 x 10 ³ - 61.63 x 10 ³, kemudian diikuti sampel dari Jawa Barat 1.67 x 10 ³ - 52. 40 x 10 ³ dan Sulawesi Selatan 5.53 x 10 ³ - 45.13 x 10³.
Hasil preservasi spermatofor yang diperoleh dari ketiga lokasi pengambilan sampel, menunjukkan adanya penurunan viabilitas spermatofor seiring dengan waktu preservasi atau penyimpanan spermatofor. Diameter spermatofor sangat bervariasi baik antar sampel, antar individu maupun antar lokasi pengambilan sampel. Spermatofor Scylla olivacea asal Jawa Barat, menunjukkan diameter terkecil 33.75µm dan terbesar 210µm dengan distribusi spermatofor terpusat pada ukuran diameter ≤ 50 sampai dengan ≤ 150µm dan ukuran spermatofor yang paling banyak ditemukan adalah 72.5µm sampai dengan 120µm. Spermatofor dari Scylla olivacea asal Sulawesi Selatan, menunjukkan diameter yang lebih kecil yaitu 18.75µm dan spermatofor terbesar 362.5µm. Distribusi spermatofor pada sampel dari Sulawesi, yaitu terpusat pada ukuran diameter ≤ 50 sampai dengan ≤ 250µm. Jumlah diameter yang paling banyak ditemukan antara 87.5µm sampai dengan 125µm. Diameter spermatofor
Scylla olivacea asal Papua Barat, menunjukkan diameter terkecil 45µm tetapi
spermatofor terbesar hanya 277.5µm, range nilai diameter spermatofor yang sama dengan sampel dari Sulawesi yaitu terpusat pada diameter ≤ 50 sampai dengan ≤ 250µm. diameter spermatofor yang paling sering ditemukan adalah 92.5µm – 152.5µm, lebih tinggi kisarannya dari sampel asal Jawa dan Sulawesi.
Konsentrasi spermatozoa per spermatofor Scylla olivacea menunjukkan nilai yang signifikan, jumlah spermatozoa meningkat seiring dengan bertambahnya ukuran diameter spermatofor. Untuk spermatopor dengan diameter (40-70) μm, diperoleh konsentrasi spermatozoa per spermatopor ; 6.67 x 10⁶, kisaran diameter spermatopor (70-100)μm, diperoleh konsentrasi spermatozoa 10.12 x 10⁶, kisaran diameter spermatopor (100-130)μm, diperoleh konsentrasi 15.96 x 10⁶, kisaran diameter spermatopor (130-160) μm, diperoleh konsentrasi 15.88 x 10⁶ dan kisaran diameter spermatopor (160-190) μm, diperoleh konsentrasi spermatozoa 16.14 x 10⁶. Scylla olivacea menghasilkan spermatofor tunggal dan terpisah satu sama yang lain berada dalam medium cair dari seminal plasma. Memiliki spermatozoa yang berflagela dan tidak bergerak.
vi
© Hak Cipta milik IPB, tahun 2009
Hak Cipta dilindungi Undang-undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk
kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan
laporan, penulisan kritik atau tinjauan suatu masalah; dan pengutipan
tersebut tidak merugikan kepentingan yang wajar IPB.
vii
KONSENTRASI, VIABILITAS SPERMATOFOR DAN
KARAKTERISTIK MORFOLOGI SPERMATOZOA
KEPITING BAKAU MERAH (Scylla olivacea
HERBEST 1796)
ASAL JAWA, SULAWESI DAN PAPUA
NURIL FARIZAH
TESIS
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Biologi Reproduksi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
ix Judul Tesis : Konsentrasi, Viabilitas Spermatofor dan Karakteristik
Morfologi Spermatozoa Kepiting Bakau Merah
(Scylla olivacea Herbest 1796 ) Asal Jawa, Sulawesi
dan Papua
Nama : Nuril Farizah
N R P : B351060051
Disetujui
Komisi Pembimbing
Prof. Dr. drh. Arief Boediono Dr.Dra. R. Iis Arifiantini, M.Si Anggota Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Biologi Reproduksi
Dr. drh. Iman Supriatna Prof.Dr. Ir. Khairil A. Notodiputro, M.S.
x
PRAKATA
Alhamdulillahirabbil Alamin, Tiada kata yang paling tulus
dipersembahkan kepada Allah SWT. atas rahmat dan hidayah serta kasih
sayang-Nya sehingga tesis dengan judul ‘Konsentrasi, Viabilitas Spermatofor dan
Karakteristik Morfologi Spermatozoa Kepiting Bakau Merah (Scylla olivacea
Herbest 1796 ) Asal Jawa, Sulawesi dan Papua’dapat diselesaikan. Salam serta
shalawat senantiasa dituturkan untuk Baginda Rasullullah S.A.W, pembawa
rahmat bagi semua makhluk.
Tesis ini berisikan tentang kajian biologi reproduksi kepiting bakau yang
dihubungan dengan performans reproduksinya. Hasil dari penelitian ini nantinya
akan menjadi informasi dasar mengenai calon indukan jantan yang baik untuk
digunakan dalam kegiatan pembenihan. Kendala dan permasalahan dari awal
sampai akhir penelitian dan penulisan, dapat terselesaikan dengan baik berkat
bantuan, dukungan, dorongan dan kerjasama dari semua pihak yang telah
membantu hingga berakhirnya semua kegiatan penelitian.
Terima kasih dan penghargaan besar penulis ucapkan kepada:
1. Dosen pembimbing : Bapak Prof. Dr. drh. Arief Boediono dan Ibu Dr. Dra. R.
Iis Arifiantini, M.Si, disela kesibukannya bersedia meluangkan waktu dalam
membimbing dalam penelitian dan penulisan tesis ini.
2. Prof. Dr. Yushinta Fujaya, M.Si, yang membantu membimbing dalam
penulisan tesis ini.
3. Program Mitra Bahari-Coral reef Management Program II (PMB-COREMAP
II) Tahun 2008, atas beasiswa bantuan penulisan tesis Tahun 2008. Pemerintah
Provinsi Kaltim atas bantuan stimulan penulisan tesis tahun 2008 dan
Pemerintah Kotamadya Samarinda atas bantuan beasiswa tahun 2007.
4. drh. Wahono Esthi P, M.Si, Nurmila Anwar, S.Pi, M.Si, Nur Alam, S.Pi, Ari
Nurhayati, S.Pt atas bantuannya selama pelaksanaan penelitian. Teman-teman
xi 5. Serta tidak lupa juga pada rekan-rekan P.S. BRP 2004-2008 serta rekan-rekan
P.S. SVT 2006 atas masukan dan dukungannya, sehingga memudahkan
penulisan tesis ini.
Akhir kata, semoga tesis ini dapat berguna dalam rangka pengembangan
budidaya perikanan khususnya pembenihan kepiting bakau.
Bogor, 11 Agustus 2009
xii
RIWAYAT HIDUP
Penulis dilahirkan di Samarinda Kalimantan Timur pada tanggal 03
September 1981, dari Ayahanda H. Dhamrah Bakrie, BA dan Ibunda Hj. Siti
Normasyam. Penulis merupakan putri ketiga dari empat bersaudara.
Tahun 2000 penulis lulus dari SMU Negeri 2 Samarinda dan pada tahun
yang sama, penulis melanjutkan pendidikan di program Budidaya Perairan (BDP),
Jurusan Perikanan, Fakultas Ilmu Kelautan dan Perikanan Universitas Hasanuddin
Makassar dan selesai pada tahun 2005 dengan gelar Sarjana Perikanan.
Selama mengikuti perkuliahan di Universitas Hasanuddin, pernah aktif di
berbagai organisasi kemahasiswaan, baik yang bersifat intern sebagai Anggota
dalam lingkup Keluarga Mahasiswa Perikanan (KEMAPI) UNHAS di jurusan
perikanan, maupun yang bersifat eksternal, diantara yang pernah aktif di ikuti
adalah Anggota Aquatic Study Club Makassar (ASCM) (2001-2005), Anggota
Rohis Perikanan Unhas (2001-2004). Dibidang akademik penulis, sebagai asisten
mata kuliah Histologi (2004/2005), asisten mata kuliah Dasar-Dasar Ilmu Tanah
xiii Klasifikasi, Morfologi, dan Anatomi Scylla olivacea... 5
Penyebaran dan Habitat... 6
Siklus Hidup... 6
Sistem Reproduksi Kepiting Bakau Merah Jantan... 7
Testes ... 9
Vas Deferen ... 9
Spermatofor... 10
Spermatozoa ... 11
Fisiologi dan Perkembangan Gonad... 12Mekanisme Hormonal pada Individu ... 12
Fase-Fase Reproduksi... 13
Kopulasi... 14
Perkembangan Gonad ... 14
Proses Spermatogenesis pada Kepiting ... 16
Tahap Spermatogonia ... 17
Tahap Spermatosit Primer ... 18
Tahap Reduksi... 19
Tahap Spermatosit Sekunder ... 20
Transformasi dari Spermatid menjadi Spermatozoa... 21
Pengeluaran dari Spermatozoa Matang ... 22
xiv MATERI DAN METODE PENELITIAN
Waktu dan Tempat ... 28
Prosedur Penelitian ... 28
Sampling Hewan Uji ... 28
Koleksi Testes dan Penghitungan Kons. Spermatofor... 29
Pengukuran Diameter dan Koleksi Spermatofor... 29
Penghitungan Jumlah Spermatozoa per Spermatofor ... 30
Preservasi Spermatofor ... 30
Pengamatan Struktur & Morfologi Spermatofor dan Spermatozoa dengan SEM ... 30
Rancangan Penelitian dan Analisis Data... 30
HASIL DAN PEMBAHASAN Karakteristik Umum Kepiting Bakau Merah Jantan... 31
Konsentrasi Spermatofor Kepiting Bakau Merah ... 37
Preservasi Spermatofor Kepiting Bakau Maerah ... 39
Kisaran Diameter Spermatofor ... 41
Konsentrasi Spermatozoa Dihubungkan dengan Ukuran Spermatofor .. 43
Morfologi Spermatofor dan Spermatozoa... 45
PEMBAHASAN UMUM ... 47
SIMPULAN DAN SARAN Simpulan ... 51
Saran ... 51
DAFTAR PUSTAKA ... 52
xv DAFTAR GAMBAR
Halam
an
1.Perbedaan morfologi dari keempat spesies Scylla spp……… 5
2.Siklus hidup kepiting bakau (Scylla spp)... 7
3.Sistem reproduksi kepiting jantan secara umum………. 8
4.Anatomi organ kelamin jantan kepiting bakau (Scylla spp)... 8
5. Spermatofor dari kelas crustacea... 10
6. Morfologi umum spermatozoa kepiting... 11
7. Kontrol endokrin pada reproduksi jantan... 13
8. Gambaran histologi testis kepiting Telmessus cheiragonus……… 16
9.Tahap spermatogonia pada kepiting... 23
10.Tahap spermatosit primer pada kepiting... 24
11.Tahap spermatosit sekunder pada kepiting... 25
12.Transformasi spermatid menjadi spermatozoa... 26
13.Karakteristik umum S. olivacea asal Jawa, Sulawesi dan Papua…… 31
14.Ciri karakteristik Scylla olivacea………. 32
15.Konsentrasi spermatofor per individu Scylla olivacea... 36
16. Kisaran diameter spermatofor asal Jawa Scylla olivacea... 36
17. Kisaran diameter spermatofor asal Sulawesi Scylla olivacea.... 37
18. Kisaran diameter spermatofor asal Papua Scylla olivacea... 38
19. Morfologi spermatofor dan spermatozoa S. olivacea dengan SEM.... 40
20. Sistem reproduksi Scylla olivácea……… 41
21. Ruas abdomen dan alat kopulasi dari Scylla olivácea………. 42
22. Berbagai ukuran dan bentuk spermatofor dari Scylla olivácea……… 43
xvi DAFTAR TABEL
Halam
an
1. Aktivitas reproduksi kepiting bakau Scylla spp ...14
2. Karakteristik umum Scylla olivacea jantan...32
3. Rataan konsentrasi spermatozoa per spermatofor S. olivacea...39
DAFTAR LAMPIRAN Halam an 1. Prosedur pembuatan larutan pembilas testes...57
2. Komposisi larutan medium spermatofor dan spermatozoa...58
3. Prosedur SEM dari spermatozoa kepiting bakau merah ...59
PENDAHULUAN
Latar Belakang
Kepiting bakau adalah komoditas perikanan pantai yang mempunyai nilai ekonomis cukup tinggi di wilayah Indo-Pasifik dan banyak digemari masyarakat karena rasanya lezat dan kandungan gizinya yang cukup tinggi (Kasri 1982).
Kepiting bakau merah (Scylla olivacea) merupakan salah satu dari ke empat
spesies kepiting bakau di dunia (Keenan 1999). Kepiting bakau merah ini memiliki keunggulan dari ketiga spesies kepiting lainnya, yakni proses reproduksi dari kepiting ini lebih singkat (lebih cepat bertelur) dan dapat bertahan hidup dalam kondisi yang ekstrim kekurangan air.
Permintaan pasar yang terus meningkat, telah menjadikan komoditas ini
sebagai salah satu andalan ekspor non migas. Selama ini permintaan pasar akan
kepiting bakau sebagian besar masih dipenuhi dari hasil penangkapan di alam yang jumlahnya terbatas dan sangat bergantung kepada musim sehingga kontinuitas produksi tidak dapat dipertahankan sepanjang tahun. Hal ini berimbas pada tuntutan yang mendesak untuk pengembangan budidaya kepiting bakau (Karim et al. 2002).
Upaya budidaya mulai dari pembenihan (Rustam 1989), pembesaran (Sulaeman & Hanafi 1992), penggemukan, pematangan gonad untuk betina bertelur (Gunarto 1990; Fattah 1998; Fujaya 2004) yang memiliki nilai jual tinggi di luar serta dikembangkannya budidaya kepiting lunak (soft shelled) yang memiliki prospek cerah (Fujaya 2007). Namun semua kegiatan budidaya tersebut sebagian besar masih mengandalkan bibit yang berasal dari alam, yang kita ketahui sekarang jumlahnya sudah berkurang. Hal ini disebabkan oleh kegiatan eksploitasi (penangkapan) di alam serta terjadinya pengerusakan pada habitat asli dari kepiting bakau. Aktivitas manusia yang mengeksploitasi hutan mangrove tanpa terkendali, antara lain; penebangan untuk pemukiman, areal budidaya dan lain-lainya.
2 Hal ini mungkin disebabkan oleh penyediaan indukan yang berkualitas rendah sehingga berdampak pada kualitas benih yang dihasilkan. Keberhasilan kegiatan pembenihan dipengaruhi oleh kualitas induk, yaitu induk yang memiliki sel telur atau sel spermatozoa berkualitas baik (Fujaya 2007). Beberapa penelitian yang telah dilaporkan lebih banyak mengarah pada induk betina yang bisa menghasilkan kualitas telur yang baik (Fattah 1998; Jalil 1999), tetapi penelitian mengenai kualitas induk betina dan sel telur yang baik juga belum banyak dilakukan sedangkan kualitas benih yang baik bukan hanya tergantung pada induk betina tetapi juga pada induk jantan.
Induk jantan yang berkualitas tinggi adalah induk jantan yang memiliki jumlah dan viabilitas spermatozoa yang tinggi, sehingga mempengaruhi
keberhasilan dalam pembuahan (fertilisasi) yang tinggi (Akarasanon et al. 2004).
Sampai saat ini informasi mengenai induk jantan kepiting bakau merah yang baik sangat terbatas, karena penelitian yang berkaitan dengan spermatozoa dan sistem reproduksi jantan kepiting bakau masih sedikit dilakukan (Bhavanishankar & Subramoniam 1997).
Daerah migrasi kepiting bakau tidak luas, sehingga diperkirakankepiting
bakau dari suatu daerah dengan daerah yang lainnya memiliki kualitas berbeda, hal ini berhubungan dengan kondisi lingkungan, sumber makanan yang tersedia
dan lainnya. Performans reproduksi pada golongan krustacea dipengaruhi
berbagai faktor, yaitu ; faktor lingkungan, makanan, dan hormonal (Sulaeman 1992).
Faktor lingkungan, tempat dimana spesies itu hidup berkaitan pula dengan distribusi makanannya. Selain itu faktor hormonal juga memegang peran penting dalam suatu siklus reproduksi. Faktor hormonal juga berkaitan dengan lingkungan, jika lingkungan kurang mendukung akan memberikan tekanan pada individu tersebut sehingga proses reproduksi yang biasanya terjadi mengalami gangguan atau berhenti sama sekali, ini berkaitan dengan sistem endokrin
(Pickering et al. 1987; Pankhurst & Dedual 1994; Haddy & Pankhurst 1999;
3 paparan yang satu dengan lainnya, karena dibatasi oleh palung laut yang dalam. Pemilihan tiga daerah di Indonesia yakni: Jawa Barat, Sulawesi Selatan dan Papua Barat diasumsikan bahwa ketiga daerah tersebut mewakili Indonesia. Dengan demikian diduga kepiting dari ketiga daerah tersebut memiliki performans reproduksi berbeda, sehingga penelitian ini bertujuan mengkaji performans reproduksi kepiting bakau merah jantan (Scylla olivacea) pada daerah Jawa Barat, Sulawesi Selatan dan Papua Barat.
Kerangka Pemikiran
Kegiatan pembenihan pada kepiting bakau, khusus kepiting bakau merah (Scylla olivacea) belum optimal. Fekunditas, hatcing rate, dan survival rate larva serta anakan yang dihasilkan masih rendah. Kualitas indukan yang digunakan dalam kegiatan pembenihan belum memenuhi standar. Penyediaan dan penggunaan indukan yang berkualitas masih disuplai dari alam, jadi diperlukan informasi mengenai induk yang berkualitas tinggi. Sehingga usaha pembenihan dapat optimal dari segi kualitas telur dan spermatozoa, khususnya untuk induk jantan berpotensi sebagai indukan yang memiliki kualitas spermatozoa baik. Penyediaan induk jantan yang berkualitas memegang peran penting dalam kegiatan pembenihan selain induk betina. Penelitian yang berkaitan dengan spermatozoa dan sistem reproduksi jantan kepiting bakau masih sedikit dilakukan.
Pendekatan masalah dalam mengatasi hal tersebut diatas adalah mencari informasi sumber induk jantan berkualitas tinggi dari beberapa daerah. Kualitas induk jantan kepiting bakau yang baik dapat diduga berdasarkan morfologi makro dan mikro dari karakteristik reproduksi jantan; ukuran karapas dan bobot tubuh, ukuran dan jumlah spermatofor yang diproduksi oleh setiap pejantan, jumlah spermatozoa dalam setiap spermatofor, viabilitas spermatozoa, normal dan abnormalitas spermatozoa. Sehingga memberikan informasi dasar (database)
untuk induk jantan yang berkualitas baik. Oleh karena itu, diperlukan penelitian
yang berkaitan dengan kepiting bakau merah jantan. Mengkaji performans reproduksi kepiting bakau merah jantan yang berasal dari beberapa lokasi
4 jantan kepiting bakau merah berkualitas tinggi. Parameter lain yang dapat
digunakan sebagai indikator mutu induk jantan adalah hatching rate, survival
rate, laju perkembangan dan pertumbuhan namun demikian parameter ini selain
dipengaruhi oleh jantan juga dipengaruhi oleh betina.
Tujuan dan Manfaat Penelitian
Tujuan umum dari penelitian ini adalah mengkaji performans reproduksi kepiting bakau merah jantan (Scylla olivacea) pada daerah Jawa Barat, Sulawesi Selatan dan Papua Barat. Performans reproduksi yang dikaji, meliputi; konsentrasi, viabilitas spermatofor dan karakteristik morfologi spermatozoa. Data ini akan digunakan sebagai informasi dasar (database) mengenai induk jantan yang berkualitas dan bermutu tinggi. Hasil penelitian ini diharapkan dapat memberikan informasi sumber calon induk kepiting bakau merah yang lebih baik untuk digunakan dalam pembenihan secara buatan di hatchery. Selain itu, menambah wawasan ilmu pengetahuan khususnya reproduksi kepiting bakau jantan.
Hipotesis
1. Perbedaan ukuran tubuh (panjang dan lebar karapas) dan bobot tubuh
tidak berpengaruh pada tingkat kematangan gonad pada individu jantan kepiting bakau merah (Scylla olivacea).
2. Gonad stomatik indeks (GSI) berpengaruh pada konsentrasi spermatofor.
3. Spermatofor yang berukuran besar diduga menyimpan jumlah atau masa
TINJAUAN PUSTAKA
Klasifikasi, Morfologi, dan Anatomi Scylla olivacea
Berdasarkan faktor ekologi dan faktor fisik perkembangan larva dari
kepiting bakau, diklasifikasikan ke dalam filum Arthropoda, sub filum
Mandibula, kelas Crustacea, sub kelas Malacostraca, super ordo Eucarida, ordo
Decapoda, sub ordo Reptantia, seksi Brachyura, sub seksi Branchyrhyncha,
famili Portuninae, genus Scylla dan spesies Scylla serrata, Scylla tranquebarica
dan Scylla ocenica (Joel & Raj 1983; Stephenson & Champbell 1960 dalam
Watanabe et al. 2001). Lebih lanjut menurut Keenan et al. 1999, bahwa
berdasarkan perbedaan sifat morfologi dan ekologi kepiting bakau yang hidup di
alam terdiri atas empat spesies yaitu ; Scylla serrata, Scylla tranquebarica, Scylla
paramamosain, dan Scylla olivacea. Keempat jenis kepiting ini memiliki
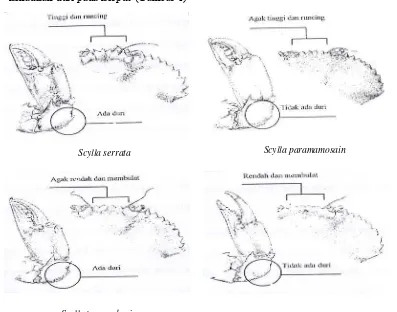
perbedaan pada bentuk morfologinya, yakni pada bentuk duri antara mata dan
kehadiran duri pada korpus (Gambar 1)
Gambar 1 Perbedaan morfologi dari keempat spesies Scylla (Keenan et al. 1999)
Scylla tranquabarica Scylla olivacea
6 Bentuk badan kepiting secara umum adalah badan yang pendek dengan
abdomen yang tereduksi. Badan yang pendek diakibatkan oleh fusi antara kepala
dan torak membentuk cefalotorak dan ditutupi oleh karapas. Sedangkan abdomen
tereduksi menjadi tipis, rata dan terlipat dibawah cefalotorak. Oleh sebab itu,
kepiting dinamakan brachyuna atau ekor pendek (Garth & Abbott 1980).
Kepiting bakau ditutupi oleh karapas yaitu kulit yang terdiri atas kitin bercampur
bahan kapur yang telah mengeras. Karapas berbentuk bulat pipih, dilengkapi
dengan sembilan duri pada sisi kiri dan kanan. Empat duri yang lain terdapat
diantara kedua matanya. Mempunyai sepasang kaki jalan yang bentuknya besar
disebut capit yang berfungsi untuk memegang, tiga pasang kaki jalan dan
sepasang kaki renang berbentuk bulat telur dan pipih seperti alat pendayung
(Karim 1998 ).
Penyebaran dan Habitat
Scylla olivacea hidup pada berbagai habitat dan sebagian besar hidup di
laut, sebagian hidup di perairan bakau atau di estuari. Pada masa juvenil sampai
menjelang dewasa atau dewasa, kepiting hidup di pantai, muara-muara sungai dan
hutan bakau dengan cara membuat lubang (Kasry 1986). Sebagian besar siklus
hidup kepiting bakau dilalui di sekitar muara sungai dan hutan bakau (Sulaeman
& Hanafi 1992). Kemampuannya yang tinggi untuk beradaptasi pada perubahan
kualitas air seperti salinitas, menyebabkan kepiting sering dijumpai di sungai yang
jauh dari laut dengan salinitas rendah (sekitar 5 ppt). Kepiting bakau
melangsungkan perkawinan di perairan hutan bakau, selanjutnya kepiting betina
beruaya ke laut untuk memijah dan kepiting jantan tetap di perairan hutan bakau
atau muara sungai (Hill 1979).
Siklus Hidup
Kepiting bakau betina yang matang kelamin akan beruaya dari perairan
pantai ke perairan laut untuk memijah (Brick 1974). Kemudian kepiting bakau
betina dan anak-anaknya tersebut akan berusaha kembali ke perairan pantai,
muara sungai atau perairan hutan bakau untuk berlindung, mencari makanan atau
7 telah dewasa berada di perairan bakau, di tambak atau disela-sela akar bakau atau
paling jauh sekitar perairan pantai yaitu pada bagian-bagian yang berlumpur yang
makanannya melimpah. Mosa et al. (1985), menyatakan bahwa kepiting bakau
mengalami beberapa tingkatan perkembangan mulai telur sampai dewasa.
Tingkat perkembangan tersebut dimulai dari telur, zoea, megalopa,
kepiting muda dan kepiting dewasa. Telur yang telah dibuahi menetas dalam
waktu 2-4 minggu menjadi larva dengan lima tingkatan zoea dan satu megalopa.
Larva tersebut akan terbawa arus ke pantai. Hill (1974) menemukan bahwa larva
kepiting bakau tahap zoea I tidak dapat mentolerin salinitas dibawah 14 ppt.
Setelah tahap zoea, perkembangan selanjutnya adalah megalopa. Megalopa akan
berenang dan masuk kembali ke muara sungai atau mangrove untuk mencari
makanan dan perlindungan. Selanjutnya megalopa akan berkembang menjadi
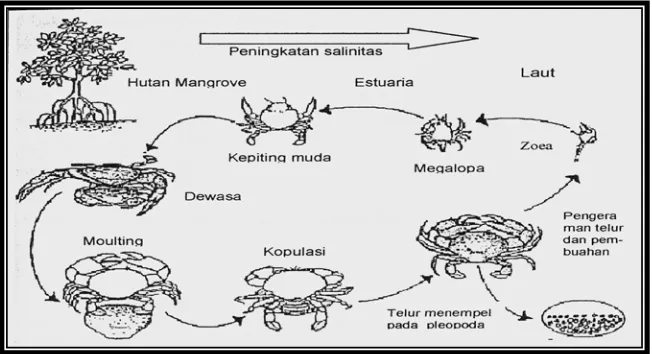
kepiting bakau muda yang bersifat bentik kemudian menjadi dewasa. Siklus hidup
kepiting bakau dapat dilihat pada Gambar 2.
Gambar 2 Siklus Hidup Kepiting Bakau (Scylla spp) Modifikasi Kanna (2000)
Sistem Reproduksi Kepiting Bakau Jantan
Kepiting merupakan organisme dioecious, artinya mempunyai jenis
kelamin jantan dan betina pada individu yang berbeda. Berdasarkan struktur organ
reproduksinya kepiting bakau tergolong kepiting yang melakukan internal
fertilization (pembuahan di dalam). Sistem reproduksi pada jantan terdiri atas
testis, saluran spermatozoa, dan alat ejakulasi. Sedangkan pada reproduksi
8 kepiting jantan dan betina adalah pada ruas-ruas abdomennya. Untuk jantan
memiliki ruas-ruas abdomen yang lebih sempit dibandingkan dengan betina yang
memiliki ruas-ruas abdomen yang lebar dan membulat (Mossa et al. 1985).
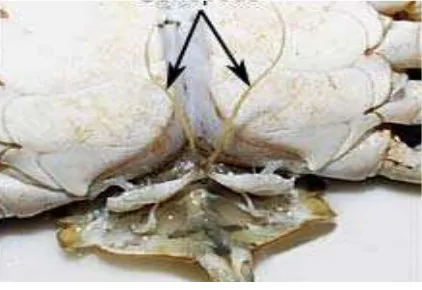
Kepiting betina memiliki empat pasang pleopod yang digunakan untuk membawa
telur selama musim reproduksi sedangkan jantan hanya memiliki dua pasang
pleopod yang digunakan sebagai organ kopulasi.
Gambar 3 Skema dari Sistem Reproduksi Kepiting Jantan Secara Umum. Anterior Testis (AT) bergabung dengan Commissure (C),Posterior Testis (PT), Ekspansi (EX) dan Posterior Vas Deferens (PV)
Gambar 4 Anatomi Organ Kelamin Jantan Kepiting Bakau (Scylla sp)
Sistem reproduksi kepiting jantan secara umum terdiri atas testis, saluran
spermatozoa, dan alat ejakulasi (Gambar 3). Kepiting bakau jantan memiliki
ruas-ruas abdomen yang lebih sempit dibandingkan dengan betina, dua pasang pleopod
9
Testes
Susunan sistem reproduksi kepiting bakau jantan dari Scylla spp,
terdapat dibawah cefalotorak. Terdiri dari sepasang testes dan vas deferen sama
halnya dengan sistem reproduksi yang telah digambarkan untuk ordo
Decapoda secara umum. Organ reproduksi jantan pada sub kelas
Malacostraca, ditemukan dalam cefalotorak atau torak (Krol et al. 1992).
Saluran reproduksi jantan pada beberapa Decapoda, terdiri dari sepasang
testis dan saluran genital (Johnson, 1980 pada C. Sapidus &Leite, 2002 pada U.
Cordatus). Tiap saluran genital terdiri dari suatu kumpulan pipa, bagian vas
deferen, dan suatu saluran ejakulator yang berakhir dalam seminal vesicle
atau suatu ampoule terminal, bergantung pada masing-masing spesies (Krol et al.
1992).
Vas Deferen
Bagian vas deferen dari Scylla olivacea terdiri dari dua bagian utama
secara umum seperti halnya pada Decapoda lainnya, namun tidak selalu sama
bergantung spesies. Pada kasus lainnya, vas deferen pada L. emarginata
(Hinsch & Walker 1974), C. sapidus (Johnson 1980), dan T. orientalis (Burton
1995) membagi vas deferen menjadi tiga bagian, sedangkan pada S. chacei
(Hinsch & Mcknight 1988), vas deferen terbagi menjadi empat bagian dan pada
D. pugilator (Manjon-Cabeza & Evenness 2000) vas deferen terbagi menjadi
delapan bagian. Kriteria perbedaannya ditentukan secara mikroskopis dan
makroskopis bergantung spesies.
Binford (1913), menggambarkan struktur dari vas deferen berupa garis
lurus dengan epithelium kolumnar yang mensekresikan bahan kimia yang
diperlukan untuk menghasilkan dinding dari spermatofor. Cronin (1947) meneliti
bahwa kebanyakan bagian anterior dari vas deferen berperan dalam pengeluaran
bahan-bahan kimia yang diperlukan untuk membungkus dan penyimpanan
spermatofor. Hinsch dan Mcknight (1988) juga memberikan pernyataan pada
pembentukan awal dari spermatofor dan produksi cairan seminal terjadi di
bagian anterior dari vas deferen. Namun menurut Marie (1999) bahwa sel
sperma meninggalkan testes dan memasuki vas deferen untuk berkembang
10 menyelesaikan pematangan mereka di dalam spermateka. Sedangkan penelitian
pada cairan seminal plasma dari crustacea menunjukkan bahwa seminal plasma
beberapa spesies antara lain; Cirripede (Barnes 1962) dan kepiting (Jeyalectumie &
Subramoniam 1987) memiliki kesamaan dengan semen dari mamalia.
Spermatofor
Kepiting atau Brachyuran menghasilkan spermatofor tunggal yang berada
dalam medium cair dari seminal plasma (Jeyalectumie & Subramoniam 1997).
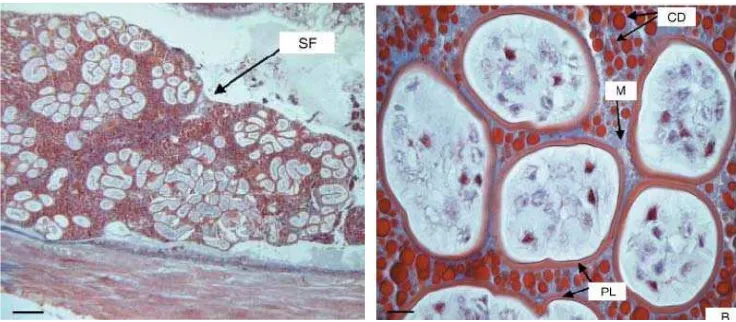
Spermatofor crustacea memiliki bentuk yang bervariasi (Gambar 5), namun
pengetahuan mengenai komposisi kimiawi dari spermatofor sangat sedikit.
Beberapa peneliti memberikan pernyataan bahwa dinding dari spermatofor
tersusun dari kitin (Spalding 1942; King 1948).
Uma dan Subramoniam (1979) tidak menemukan kitin pada Brachyuran,
kepiting bakau Scylla serrata. Sedangkan spermatofor yang terdapat dalam individu
betina pada crustacea laut, pada membran spermatozoanya terdapat kantung yang
melekat, diduga mengandung gelatin kental (Berry & Heydorn 1970). Walaupun
begitu ada beberapa substrat pada selaput membran dari spermatozoa dalam transport
spermatozoa, namun komposisi kimianya belum diketahui (Subramoniam 1984).
Gambar 5 Spermatofor dari C. quadricarinatus A: Gambar secara umum dari
spermatofor (stained with Masson-Trichrome; bar: 286 μm). B: Gambaran
detail dari spermatofor (stained with Masson-Trichrome; bar: 26 μm).CD:
11 Spermatofor yang baik ditunjukkan dengan jumlah spermatozoa yang
tinggi di dalamnya. Spermatofor memelihara kemampuan fertilisasi
spermatozoa yang sudah pasti mengarah pada tingginya angka pembuahan
yang tinggi, berdampak, pada kesempatan yang tinggi bagi embrio untuk
bertahan hidup, menetas dan hidup sebagai larva (Akarasanon et al. 2004).
Spermatozoa
Spermatozoa dari crustacea (udang dan kepiting), memiliki suatu
flagelate, tidak memiliki midpiece, dan tidak bergerak (non-motile), serta
berbagai macam bentuknya. Spermatozoa dari Natant (udang) bentuknya
seperti paku tunggal, sebaliknya pada spermatozoa Decapoda Reptalia
(kepiting) dalam bentuk multistellate (Gambar 6).
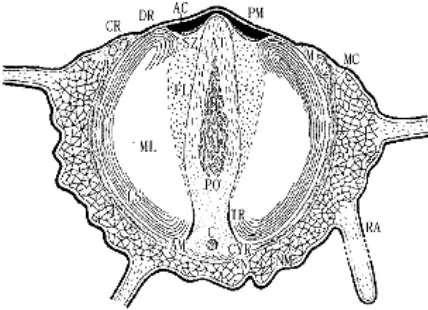
Gambar 6 Morfologi umum spermatozoa kepiting, keterangan gambar : AC (apical
cap); AM (akrosomal membran); AT (akrosomal tubule); C (sentriole); CR
(convex ring); CYR(cytoplasmic region); DR (ditch ring); FL (fibrous
layer); LS (lamellar structure); M (mitochondria); MC (membrane
complex); ML (middle layer); N (nucleus); NM. (nuclear membrane);
PM.(plasma membrane); PO (percutor organ); RA. (radial arm); SZ
(subcap zone); TR (thickened ring) (Shan et al. 1999).
Spermatozoa dari Echinodermata, Mollusca, Polychaetes dan Crustacea
menunjukkan variasi yang besar dalam morfologi spermatozoanya, dan semua
Crustacea memiliki akrosom yang khas (Qamieson et al. 1995; Gwo et al. ;
1996, 1997, 2000). Akrosom terletak pada bagian anterior dari kepala
spermatozoa lebih rendah dari membran plasma. Akrosom mengandung enzim
yang berfungsi dalam exocytosis dan penetrasi spermatozoa ke telur selama
12 perubahan dalam bagian akrosom sebelum menuju telur dan penetrasi secara
ekstraseluler yang membutuhkan waktu (Clark et al. 1981; Jamieson et al.
1995; Gwo et al. 2000). Kelangsungan hidup spermatozoa secara umum dapat
diperkirakan dari motilitas spermatozoa tetapi metode evaluasi ini tidak dapat
diaplikasikan untuk spermatozoa dari crustacea, Decapoda. Spermatozoa
crustacea, Decapoda tidak bergerak (Clark et al. 1981). Untuk menentukan
kelangsungan hidup dari spermatozoa crustacea menggunakan metode pewarnaan
eosin-nigrosin (Jeyalectumie & Subramoniam 1989) atau pewarnaan trypan
blue (Bhavanishankar & Subramoniam 1997). Spermatozoa hidup tidak
terwarnai, sedangkan sperma mati terwarnai dengan baik. Untuk kelangsungan
hidup viabilitas dari spermatozoa Scylla serrata, bervariasi antara 95% - 67%
dari suhu -196°C sampai -4°C (Jeyalectumie & Subramoniam 1997). Produksi,
kualitas spermatozoa, dan pembentukan spermatofor merupakan variabel penting
dalam reproduksi jantan (Leung-Trujillo & Lawrence 1987; Díaz et al. 2001).
Pembentukan karbohidrat sebagai substrat utama yang digunakan dalam
pemeliharaan spermatozoa sampai didalam spermateka kepiting betina matang
gonad (Jeyalectumie 1989).
Fisiologi dan Pertumbuhan Gonad
Seluruh Decapoda termasuk kepiting bakau pada ukuran kepiting muda
(juvenil) memiliki gonad yang belum berdiferensiasi, artinya terdapat saluran sperma
(vas deferen) dan saluran telur (oviduct) bersama-sama. Perkembangan ke arah jenis
kelamin jantan atau betina ditentukan oleh berkembangnya atau tidak berkembangnya
kelenjar androgen. Testis dan karakteristik seksual jantan dirangsang oleh hormon
androgenik yang disekresikan oleh kelenjar androgen. Sedangkan ovarium akan
berkembang apabila tidak adanya kelenjar androgen (Meussy & Payen 1988;
Lockwood 1996).
Mekanisme Hormonal pada Individu Jantan
Informasi mengenai peranan hormon dalam pengontrolan proses
spermatogenesis pada kepiting bakau masih sedikit, tetapi untuk golongan crustacea
secara umum digambarkan peranan dan pengontrolan dari kelenjar androgen
13 Gambar 7 Diagram Sistematik dari kontrol endokrin pada reproduksi jantan dalam udang. Keterangan : AH: hormone kelenjar androgenic, MF: methyl
farnesoate, MOIH: mandibular organ-inhibiting hormone (Okumura 2004)
Methyl farnesoate merupakan substansi yang memiliki fungsi dalam
reproduksi jantan disertai beberapa faktor yang ada dalam system saraf pusat,
otak, dan ganglion torak juga berperan dalam memelihara spermatogonia dan
perkembangan dari testes. Untuk reproduksi jantan pada udang, hormon kelenjar
androgen berperan dalam kontrol differensiasi seksual (Okumura 2004).
Ada dua neurohormon yang berperan dalam siklus kematangan gonad,
Gonad Inhibiting Hormone (GIH), yang dilepaskan dari kelenjar sinus, dan Gonad
Stimulating Hormone (GSH) yang ditemukan pada otak dan ganglion torak kepiting
(Sarojini et al. 1995).
Fase-Fase Reproduksi
Fase – fase reproduksi kepiting dimulai dari kopulasi (transfer spermatofor),
perkembangan testes, kopulasi, pembuahan dan penetasan. Aktivitas reproduksi
14 Tabel 1 Aktivitas Reproduksi Kepiting Bakau
Aktivitas Reproduksi Waktu (hari)
Kopulasi
Proses Perkembangan Testes 30
Telur keluar sampai menetas 17
Kopulasi
Kopulasi hanya terjadi pada kepiting betina dan jantan yang telah dewasa
kelamin. Kegiatan kopulasi dilakukan setelah betina berganti kulit sebelum
pemijahan. Fermon yang dikeluarkan oleh kepiting betina pada saat ganti kulit
mampu menarik kepiting jantan untuk mendekatinya (Primavera 1985; Soim 1994).
Setelah karapak betina mulai mengeras, kepiting jantan membalikkan tubuh betina
sehingga perut dan alat kelaminnya saling berhadapan dan selanjutnya kepiting
jantan akan mentransfer spermatofor kedalam saluran reproduksi betina, yang
disebut dengan spermateka dengan bantuan pleopod jantan yang berfungsi sebagai
alat kopulasi (Barnes 1987).
Perkembangan Gonad
Tahap perkembangan lobul testikular pada kepiting Telmessus
cheiragonus, dilaporkan oleh Nagoa dan Munehara (2003), yang dibagi menjadi
6 tahapan berdasarkan studi histologi, yaitu :
Tahap I: Tahap Proliferasi Spermatogonia
Tahap ini ditunjukkan dalam Gambar 8a, lobul mengandung
spermatogonia dengan sitoplasma tipis dan nukleus berbentuk bulat panjang.
Terdapat kromatin sekitar membran nuklear. Spermatogonia dalam lobul
testikular memperlihatkan mitosis asynchronous. Diameter nuklei dari
spermatogonia adalah 9.9 ± 1.3 x 8.0 ± 0.8mm.
Tahap II: Tahap Spermatosit Pertama
Tahap ini ditunjukkan pada Gambar 8b, sel-sel germ dalam lobul testikular
selama tahap ini tidak mencapai fase zygoten dari meiosis. Sitoplasma dari
15 nuklei menunjukkan berbagai bentuk dengan aglutinasi dari kromatin.
Diameter dari nuklei sebelum hilangnya membran nuklear adalah 9.4 ± 1.1 x 8.1
± 0.7 mm. Terjadinya meiosis secara sikronisasi pada tiap lobul individu.
Tahap III: Tahap Pembelahan Reduksi (Reduction division stage)
Tahap ini ditunjukkan pada Gambar 8c dan 8d, lobul testikular selama
tahap ini termasuk dalam spermatosit pertama setelah fase diploten dari meiosis
atau spermatosit sekunder sebelum telofase dari bagian kedua. Pada tahap ini,
spermatosit menunjukkan bentuk irregular. Nukleus dari spermatid terlihat
seperti bola dengan rata-rata diameter 4.2 ± 0.6 mm.
Tahap VI : Tahap Spermatogenesis
Tahap ini ditunjukkan pada Gambar 8e, spermiogenesis terjadi di dalam
lobul testikular. Penampakan kantung akrosomal sekitar nuklei saat
spermiogenesis dimulai. Nukleus secara bertahap memanjang pada kantung
akrosomal dan berada di sekitar area kantung saat proses spermigenesis
sempurna.
Tahap V : Tahap Spermatozoa Bebas
Tahap ini ditunjukkan pada Gambar 8f, spermatozoa terpisah dari sel
nutrisi di lapisan lumen dari lobul testikular. Spermatozoa memiliki suatu
kantung akrosomal dan nukleus dengan tiga lengan nuklear yang memanjang
membentuk jari-jari lingkaran. Sel nutrisi menyerupai sel-sel epitelia dari saluran
seminiferus, spermatozoa yang diobservasi dalam lumen serta yang di dalam
saluran seminiferus dikelilingi oleh sel nutrisi. Saluran seminiferus dianggap
sebagai suatu lobul.
Pada brachyuran, spermatosit berkembang secara sikronisasi pada tiap
lobul testikular. Lobul yang paling berkembang adalah pada tahap VI, dimana
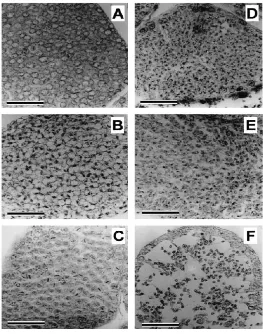
16 Gambar 8 Gambaran Histologi dari lobul testikular pada saat tahap perkembangan. (a) Tahap I (spermatogonia proliferation stage). (b) Tahap II (first spermatocyte stage). (c) Tahap III (reduction division stage). (d) Tahap IV (spermatid stage). (e) Tahap V (spermiogenesis stage). (f) Tahap VI (free sperm stage). Bar 50 mm (Nagoa & Munehara 2003).
Proses Spermatogenesis pada Kepiting
Studi histologi pada sistem reproduksi kepiting jantan Callinectes sapidus
telah dilaporkan, bahwa testis Brachyuran mengandung sel kelamin selama fase
spermatogenesis yang berbeda-beda dari spermatogonia ke spermatozoa.
Fluktuasi presentase kehadiran dari sel germ selama fase spermatogenesis
ditemukan pada beberapa Brachyuran dan perubahan tersebut berhubungan
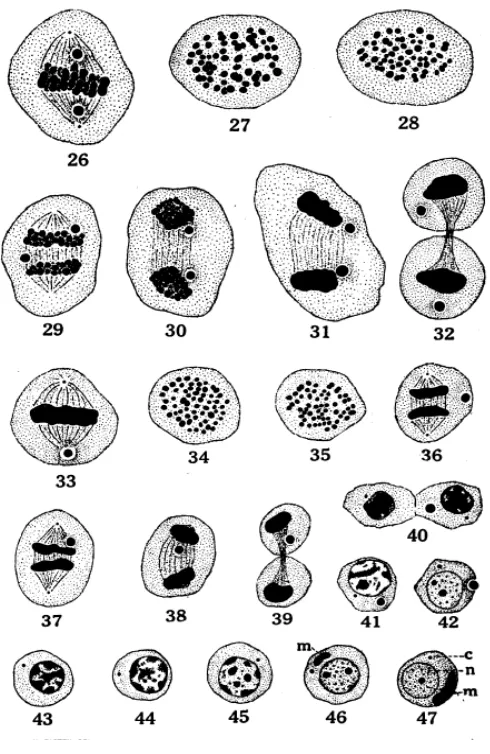
17 Spermatogenesis pada brachyuran telah dilaporkan secara mendetail,
pada kepiting Cancer magister oleh Fasten (1918) dapat dilihat pada Gambar 9,
10, 11, dan 12, yaitu :
Tahap Spermatogonia
Sel spermatogonia merupakan sel yang berukuran besar, dengan garis
sitoplasmik yang jelas serta nuklei menonjol. Tahap spermatogonia primer dan
sekunder bisa dibedakan. Spermatogonia primer ukurannya lebih besar
dibandingkan dengan spermatogonia sekunder.
Spermatogonia primer mengandung sejumlah besar kromatin dengan
nukleus. Ketika sel terbagi menjadi kumpulan besar kromatin pada nukleus,
dimulai proses pembelahan. Proses ini berlanjut sampai kromatin tersusun ke
dalam sejumlah besar sel berbentuk bulat panjang (elliptical) yang tebal,
terdistribusi di seluruh nukleus. Jumlah dari kumpulan kromatin yang diamati
berbeda-beda, dengan jumlah ber kisaran 40 - 65. Binford (1913) melaporkan
pada Menippe mercenaria dan Cambarus virilis, menemukan sequence yang
sama pada proses tersebut. Beberapa kumpulan kromatin sebagai kromosom
yang masuk kedalam piringan equator dari tahap metafase spermatogonia.
Jumlah kromosom akhir ditentukan pada tahap metafase. Penampakan
kumpulan kromatin menunjukkan lebih banyak kromosom tunggal.
Keadaan sekitar dinding nuklear dikelilingi oleh kumpulan kromatin yang
masuk kedalam sel pada tahap metafase. Kromosom berada dalam garis equator
dengan bentuk dumb-bell shaped dan munculnya kumparan serabut halus.
Sentromer secara mudah dipisahkan pada kutub yang berlawanan. Penyebaran
kromosom pada seluruh bidang equator. Penampakan kromosom kecil, bulat dan
jumlahnya banyak tidak bisa dihitung. Tahap anafase, kemudian diikuti oleh
tahap telofase, kemudian sel membagi kedalam spermatogonia sekunder.
Pembelahan spermatogonia sekunder serupa dengan spermatogonia primer,
pembelahan berlanjut pada pola yang sama. Pembelahan pokok dari spermatogonia
sekunder menghasilkan spermatosit primer dorman. Pada bidang spermatogonia
dari tubular, beberapa sel ditemukan mengalami reduksi. Perubahan struktur
nuklei ke bentuk irregular yang lebih besar dengan penonjolan (
18 Beberapa sel yang terdapat di tubuli disebut dengan sel nutrisi "nutritive
cells", telah dipelajari pada spermatozoa matang Cambarus virilis. Sel-sel
nutrisi, memiliki struktur yang unik. Nuklei dari sel nutrisi mengandung masa
kromatin, sementara pada sitoplasmanya memiliki banyak butiran lemak.
Umumnya penelitian awal pada Decapoda seperti : Grobben 1978;
Gilson 1986; Hermann 1990, yang melaporkan bahwa spermatogonia berasal
dari sel nutrisi. Sebaliknya, Keppen (1906) dan George (1992) melaporkan hal
yang berlawanan bahwa sel nutrisi berasal dari perubahan spermatogonia. Hal
ini sama yang didapatkan pada Cancer magister. Saat potongan sel nutrisi diuji
coba, terjadi amitosis. Fakta bahwa terjadi pembelahan dalam sel-sel nutrisi.
Studi nuklei yang menunjukkan bahwa sel-sel nutrisi menjadi ambceoid
dalam penampakannya.
Tahap Spermatosit Primer
Tahap ini menunjukkan pembelahan spermatogonia. Setelah periode
waktu pertumbuhan dan sinapsi, terjadi reduksi. Selama dua periode
pertumbuhan terbentuk body spherical, dikelilingi oleh ruang kosong yang
membuat spermatosit primer terlihat penampakannya dalam sitoplasma.
a. Periode Pertumbuhan
Periode ini meliputi: tahap persiapan, sinapsi dan pembentukan tetra.
Awal dari fase profase, kromatin di dalam nukleus dari spermatosit yang dorman
terdiri dari kumpulan kromatin yang sedikit. Beberapa spermatosit yang
jumlahnya sedikit terlihat benang-benang berupa garis tipis dan adanya
penampakan granular. Kromatin pada nukleus membelah ke dalam struktur yang
lebih kecil dan kemudian mulai masuk ke dalam. Pada waktu yang bersamaan
sel mengalami peningkatan dalam ukuran. Tahap ini merupakan awal
dimulainya periode pertumbuhan dan peningkatan ukuran sel dengan jelas.
Spireme terbentuk, benang-benang leptoten terpisah dan bisa dibedakan antara
satu dengan yang lainnya.
Benang leptotene berpindah ke salah satu kutub dari nukleus, disebut
pula dengan "synaptic pole" dalam garis lintang sejajar yang berpasangan.
19 dengan "chromatoid body." Pada Cambarus virilis, ditemukan sepasang
badan kromatoid yang terlihat juga pada tahap yang sama dalam perkembangan
spermatosit Cancer magister.
Benang-benang yang terdapat pada garis lintang menjadi lebih dekat
dan berpasangan pada kutub synaptic dan sel masuk pada tahap pachyten,
dimana sepasang dari benang leptoten menyatu ke dalam gemini thick. Setelah
penyatuan yang konstan untuk beberapa lama, komponen dari tiap geminus mulai
terurai. Tiap geminus membelah membujur, dan secara serempak pembukaan
dari benang-benang yang dempet pada akhirnya, menghasilkan penampakan
seperti 8, V, atau kurang lebih seperti U. Batang yang lain membagi secepatnya
seluruh lengan dari tiap geminus. Dimulai dari potongan dua bidang yang
membujur dan mengkerut secara jelas terlihat dalam dua lengan dari 8 yang
terletak ditengah pada nukleus.
Dua bidang pembelahan yang membujur, empat benang kromatid
terbentuk. Dua pasang dari beberapa benang melanjutkan kembali untuk
bercabang saling berlawanan sampai akhirnya mereka berbentuk X. Sepasang
benang yang berada pada posisi berlawanan dari titik penyatuan pusat. Tiap X
kemudian berpindah mendekat satu sama lain, sampai pada garis lintang sejajar.
Titik penyatuan pusat kemudian hilang, dan empat benang tipis tersusun dalam
dua garis lintang sejajar yang dihasilkan.
Tiap benang menjadi tipis dan bertambah tipis setelah masuk ke dalam
masa kromatid yang berbentuk kumparan bola dan segera tiap geminus
mengalami perubahan kedalam bentuk empat spherical kromosom,
menggambarkan empat serangkai. Tiap tetra mengandung empat univalen
kromosom. Selanjutnya sepasang dari beberapa penyatuan univalen kromosom
menghasilkan dua bivalen yang besar yang berdempetan antara satu dengan yang
lainnya. Kondensasi dari bivalen berlanjut sampai mereka berubah ke dalam
struktur dumb-bell shaped. Proses pertumbuhan ini telah selesai dan sel siap
untuk mengalami pengurangan.
b. Pembelahan Reduksi (reduction division)
Tahap akhir periode pertumbuhan, dinding nuklear mulai membelah.
20 ke kutub yang berlawanan, dan terlihat kumparan serabut tipis antara sentromer
dan kromosom. Kromosom segera tertarik ke bidang equator, mengalami reduksi.
Bivalen yang berbentuk dumb-bell shaped terlihat tersusun. Terlihat badan
kromatid pada kutub yang berlawanan. Tiap badan dikelilingi dan dikarakteristik
oleh ruang kosong dan lebih mudah dikenali.
Periode metafase, semua kromosom berkelompok pada bidang equator
dan penampakannya seperti lonceng tumpul (large dumb-bells). Pada tahap
metafase terdapat enam puluh kromosom yang telah dibedakan. Secara umum
berbentuk oval, ada beberapa ukuranya lebih besar dibandingkan yang lain dan
terdistribusi pada bidang equator. Badan kromatid selalu berpindah ke kutub
yang berlawanan dari sel. Kedudukan badan kromatid berada pada kumparan
serabut, sementara pada kasus lainnya badan kromatid terlihat dalam sitoplasma.
Anafase adalah tahap setelah tahap metafase. Bivalen berbentuk
lonceng dumb-bells terpisah dan tertarik pada kutub yang berlawanan. Badan
kromatid berpindah dalam beberapa arah. Proses pembelahan berlanjut dan
setahap demi setahap spermatosit primer masuk pada tahap telofase. Pada akhir
telofase, kromosom yang lengkap berpindah ke kutub yang berlawanan
kemudian dikelilingi oleh dinding nuklear yang tipis. Sitoplasma tertarik
kedalam dua bagian dan selama proses itu, kumparan serabut juga ikut tertarik
pada pusatnya dan terbentuk "zwischenkorper". Ketika tahap ini selesai dua
spermatosit sekunder dihasilkan.
Tahap Spermatosit Sekunder
Spermatosit sekunder terbentuk pada tahap telofase, terjadinya
pembelahan reduksi. Tidak ada periode istirahat, sel diasumsikan pada tahap
metafase, dan kromosom pada garis atas equator berbentuk lonceng
(dumb-bells). Tahap anafase dan telofase dengan urutan sistematik, menghasilkan
pembelahan spermatosit sekunder ke bentuk spermatid. Dua tipe dari spermatid
yang terbentuk, satu tipe yang mengandung badan kromatid tunggal dalam
21
Transformasi dari Spermatids menjadi Spermatozoa
Produksi spermatid pada pertama kali adalah kecil dan nukleinya
mengandung masa yang sebagian besar material kromatid. Sitoplasma homogen
dan sentromer yang menonjol ditemukan.
Pada tipe kedua dari perkembangan spermatid, sitoplasma mengandung
sentrosomer juga memiliki badan kromatid. Perubahan yang dialami oleh
spermatid dalam pergantian bentuk ke spermatozoa terjadi dalam nukleus.
Masa kromatin dari nukleus berkurang secara bertahap. Pertama pada
kumpulan besar dari khromatin yang membelah ke dalam masa granular dan
beberapa bagian diperlengkap sampai tahap akhir, tiga badan kromatin yang
bundar. Struktur kromatin tetap spherical. Spermatid menampakan struktur
yang jelas, yaitu; 1) nukleus yang homogen dengan suatu karyosome sebagai
tubuh pusat, 2) sitoplasma ditemukan, 3) sentromer, dan 4) masa
mitokondria.
Nukleus mengembara pada satu kutub spermatid, sementara pada
kutub yang berlawanan terdapat vakuola. Pada saat bersamaan masa
mitokondria berkelilingi di antara nukleus dan vakuola dan akhirnya mengisi
seluruh ruangan. Peningkatan ukuran sentrosomer dan mengambil bagian dalam
pusat massa mitokondria. Masa mitokondria kemudian ditransformasi ke dalam
kumparan, dan sentrosomer menempati pusat pada bagian dalam. Bagian atas
dari nukleus terletak pada ruang ini. Bersamaan badan karyosome terletak pada
pusat nukeus pindah ke atas bagian tengah dari nukleus secara langsung di
bawah sentrosomer. Perubahan terakhir pada vakuola dalam anterior. Pada
vakuola terlihat seperti gelembung kecil yang berupa cairan.
Selama sentrosomer dan badan karyosome berada pada nukleus, dalam
bentuk memanjang menyerupai batang yang disebut dengan badan sentral. Pada
awal, badan sentral berbentuk seperti lonceng (a dumb-bell), panjangnya
tidak diketahui. Tahap ini terjadi pembukaan pada bagian tengah dari terluar
atau akhir distal dari kantung kedua dan bersamaan dengan badan sentral lebih
memanjang dan bagian luar berbentuk pipa tipis yang terhubung dengan
pembukaan distal dalam kantung kedua.
22 Kumparan kromatid terlihat lebih jelas sebagai akhir distal pada badan
sentral. Penyatuan dua elemen kedalam struktur tunggal, nuklear-mitokhondrial
menjadi pendek. Perubahan berlanjut kantung kedua tersusun rapat ke dalam
kantung pertama. Bagian terluar dari badan sentral secara lengkap berubah ke
bentuk tabung yang berlubang dengan dinding yang tipis. Menunjukkan
beberapa struktur, mulai dari jari-jari yang berbentuk lingkaran pada penampilan
spermatozoa. Setelah transformasi spermatid secara lengkap ke bentuk
spermatozoa yang matang, dan pada tahap ini spermatid terlihat berbentuk oval
atau bulat dengan lengan yang berbentuk lingkaran sangat rapat mengelilingi
nuklear-mitokhondria.
Spermatozoa matang, menunjukkan badan sentral terletak pada bagian
tengah, dikelilingi kantung kedua, kantung pertama, dan nuklear-mitokhondria.
Struktur spermatozoa berupa badan sentral terdiri dari akhir distal dan akhir
proksimal. Khromatin-ring, terletak pada bagian atas dari kantung kedua.
Spermatozoa lepas pada saat matang, kemudian spermatozoa masuk ke dalam
vas deferen, dan dikelilingi oleh kantung membran atau spermatofor.
Pengeluaran dari Spermatozoa Matang
Tahap pertama dalam pengeluaran spermatozoa adalah ektrusi dari
kantung kedua. Kantung ini secara normal mengelilingi badan sentral dan melekat
dalam kantung pertama. Ketika kantung kedua mulai dilepaskan pada ukuran dan
waktu yang sama. Kantung ini dibawa kebagian atas dari kantung pertama dan
terlihat seperti lingkaran yang tipis. Bersamaan dengan akhir distal dari badan
sentral yang juga extruded, mendesak kantung tersebut pada bagian padat
proximal, perubahan ke bentuk seperti duri. Ketika kantung kedua telah
kompleks untuk bebas, kemudian kantung pertama memulai untuk evert dan
melanjutkan proses ini sampai lengkap pada bagian luar. Selama eversi, pada
akhir proximal dari badan sentral mendorong ke atas pada bagian tubular distal
sampai yang kedua akhirnya bebas ke luar.
Pelepasan sempurna spermatozoa dapat terlihat pada Gambar 10, bagian
atas terdiri dari kantung kedua, bagian dalam mengandung kantung pertama,
dengan bentuk tubuh yang cenderung keatas seperti duri. Bagian bawah terdiri
23 Pada beberapa kasus, tahap ini ditunjukkan pada Gambar terakhir dari proses
spermatogenesis pada kepiting Cancer magister.
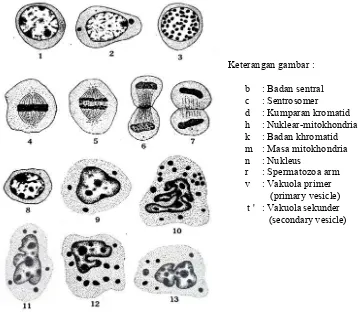
Gambar 9 Tahap spermatogonia pada kepiting Cancer magister (Fasten 1918)
1. Tahap spermatogonia primer yang beristirahat
2. Profase awal spermatogonia, menunjukkan pembagian kromatin dengan dua
sitoplasma
3. Profase akhir spermatogonia prophase, kumpulan kromatin dengan
nukleus
4. Metafase, spermatogonium primer
5. Anafase, spermatogonium primer
6-7. Telofase, spermatogonium primer
8. Tahap spermatogonia sekunder yang beristirahat
9-12. Sel nutrisi, nuklei irregular dan globul lemak dengan sitoplasma
13. Sel nutrisi, nukleus menunjukkan keadaan terdesak ke tengah terlihat peristiwa
amitosis.
Keterangan gambar :
b : Badan sentral c : Sentrosomer d : Kumparan kromatid h : Nuklear-mitokhondria k : Badan khromatid m : Masa mitokhondria n : Nukleus
r : Spermatozoa arm v : Vakuola primer (primary vesicle) t ' : Vakuola sekunder
24
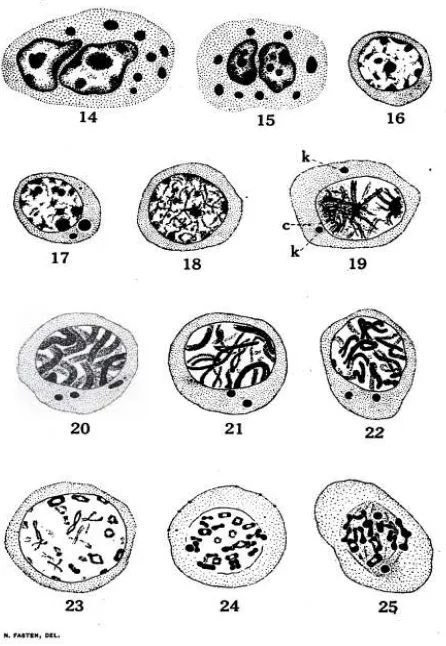
Gambar 10 Tahap Spermatosit Primer pada kepiting Cancer magister
(Fasten 1918)
14-15. Sel nutrisi, dengan dua nuklear diduga amitosis.
16-17. Awal profase, tahap spermatosit primer pada gambar 17. Dua masa kromatid
dengan sitoplasma terwarnai dengan gelap.
18. Tahap leptoten
19. Tahap sintesis dan sinapsis. Tahap leptoten ini, berupa benang-benang yang
berpasangan, tersusun pada equator yang terbagi pada kutub synaptic dari sel.
Keterangan : badan khromatid (k), dan sentrosome (c),terlihat dalam sitoplasma.
20. Tahap pachyten dan leptoten, sepasang benang membentuk geminius ditengah.
21-22. Tahap diploten.
23. Tahap post diploten
24. Pembentukan tetra, pada tahap ini dinding inti (nuklear) mulai membagi.
25. Perubahan tetra ke bentuk dumb-bells, sel masuk ke fase metafase
25
Gambar 11 Tahap Spermatosit Sekunder pada kepiting Cancer magister
(Fasten 1918)
26. Metafase, spermatosit primer menunjukkan badan khromatid pada kumparan
serabut pada kutub yang berlawanan.
27-28. Kutub spermatosit primer, menunjukkan 60 kromosom.
29-32. Tahap anafase dan telofase dari spermatosit primer menunjukkan badan kromatid pada kutub yang berlawanan. Gambar 32, badan kromatid yang diamati tetap berada pada sitoplasma.
33. Metafase spermatosit sekunder, menunjukkan badan kromatid tunggal
pada satu kutub.
34-35. Kutub spermatosit sekunder, menunjukkan 60 kromosom.
36-37. Tahap anafase dari spermatosit sekunder, menunjukkan kedudukan yang
berbeda, dimana badan kromatid mungkin menempati bagian dalam dinding sel.
38-39. Tahap telofase spermatosit sekunder, badan kromatid tunggal pada
26
40. Dua tipe spermatid yang terbentuk, satu tanpa badan kromatid dan yang
lainnya mengandung badan kromatid. Sentromer berwarna gelap ditemukan di sitoplasma pada kedua tipe spermatid.
41. Tahap awal dalam perubahan spermatid yang berisi badan kromatid
42. Pada tahap ini badan kromatid dikeluarkan dari spermatid
43-47. Tahap perubahan awal dari spermatid yang minus akan badan khromatid, reduksi
dari khromatin dan penampakan dari masa mitokhrondria (m) dalam sitoplasma. Pada gambar 47, karyosom tunggal menempati pusat dari nukleus.
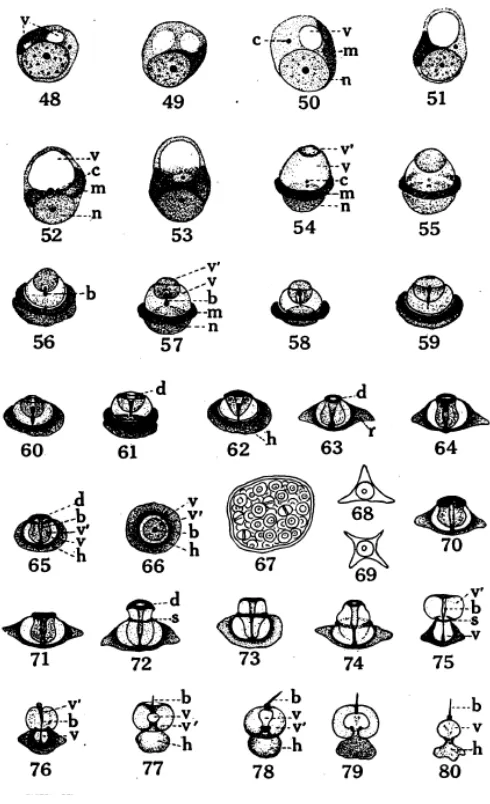
Gambar 12 Transformasi Spermatid menjadi Spermatozoa pada kepiting
Cancer magister (Fasten 1918)
48-53. Perubahan spermatid secara bertahap, dihasilkan dalam vakuola primer. terbentuk pada satu kutub, sementara nukleus (n) menempati kutub yang berlawanan, dan masa mitokhrondria (m) dan sentrosomer (c) juga menempati
27
54. Vakuola sekunder (t/) terlihat penampakan akhir distal pada vakuola primer.
55-58. Tahap transformasi dari spermatid dalam vakuola primer dan sekunder berubah ke dalam bentuk kantung, dan central body(b) terlihat seperti lonceng.
59-62. Perubahan spermatid menunjukkan lubang terluar akhir distal dari central body.
pembentukan ring kromatin (d), dan penyatuan inti dan masa mitokondria kedalam bentuk nuclear-mitochondria (a).
63-64. Pembentukan arm dari spermatozoa.
65-66. Bagian sisi samping dan bawah menunjukkan secara detail struktur spermatozoa matang
67. Spermatofor, berisi spermatozoa matang.
68-69. Tipe spermatozoa, yang terdiri dari tiga dan empat bagian yang terlihat menggantung pada cancer magister.
70-78. Secara bertahap mengeluarkan spermatozoa matang ketika dipenuhi tekanan osmotik dengan larutan garam dari air laut.
79. Spermatozoa terlepas.
80. Keluarnya spermatozoa dari kantung sekunder dengan sempurna.
Pengaruh Lingkungan Terhadap Siklus Reproduksi
Faktor lingkungan seperti suhu, cahaya, dan ketersediaan pakan adalah faktor
luar yang umum mempengaruhi reproduksi (Sastry 1983). Namun faktor-faktor ini
mempunyai pengaruh yang berbeda terhadap rangkaian tahap-tahap gametogenesis
maupun fase lain dalam siklus reproduksi. Primavera (1985) mengemukakan bahwa
pakan berpengaruh terhadap pematangan gonad Penaeid, tetapi tidak demikian
terhadap perkawinan dan pemijahan. Sedangkan suhu, salinitas, dan cahaya tidak
saja berpengaruh terhadap pematangan gonad, tetapi juga terhadap kopulasi,
BAHAN DAN METODE PENELITIAN
Waktu dan Tempat
Penelitian dilakukan pada bulan Juni 2008 sampai Februari 2009.
Tahapan penelitian, dibagi dua tahap. Tahap I, meliputi; 1) Sampling hewan uji,
2) Koleksi testes dan penghitungan konsentrasi spermatofor, 3) Pengukuran
diameter dan koleksi spermatofor, 4) Penghitungan jumlah spermatozoa dalam
spermatofor, dan 5) Preservasi spermatofor. Tahap II, preparasi Scanning
Electron Microscope (SEM). Penelitian dilakukan di Laboratorium Embriologi,
Laboratorium Unit Rehabilitas Reproduksi (URR) dan Laboratorium Histologi
FKH-IPB. Pengamatan morfologi spermatofor dan spermatozoa (Scylla olivacea)
dengan SEM dilakukan di Lembaga Ilmu Pengetahuan Indonesia (LIPI), Cibinong.
Hewan Uji
Hewan uji yang digunakan dalam penelitian ini adalah kepiting bakau
merah jantan (Scylla olivacea) sebagai sumber testes, spermatofor, dan
spermatozoa yang berasal dari tiga lokasi pengambilan sampel (Jawa Barat,
Sulawesi Selatan, dan Papua Barat) yang memiliki kisaran ukuran karapas
berkisar 8-15 cm dan bobot tubuh 200-500 gr.
Tahapan Penelitian I Sampling Hewan Uji
Pengambilan hewan uji dari tiga daerah, yaitu; Jawa (Blanakan, Jawa
Barat), Sulawesi (Maros, Sulawesi Selatan) dan Papua (Fak-Fak, Papua Barat),
yang diperoleh dari pengumpul lokal. Pemilihan spesimen berdasarkan morfologi
tubuh yang normal, sehat, serta kondisi badan yang lengkap. Spesimen yang
diambil sebanyak ± 16 ekor tiap lokasi penelitian. Spesimen ditampung
sementara untuk adaptasi di URR-FKH IPB. Pengukuran karakteristik
morfometrik kepiting bakau merah mengikuti petunjuk Warner (1977),
29 ketelitian 0.05 mm. Pengukuran karapas diukur dari letak antara gigi median
sampai tepi posterior karapas dalam bentuk garis lurus, sedangkan lebar karapas
diukur dari kedua gigi anterolateral. Berat kepiting secara individual dihitung
dengan menggunakan timbangan.
Koleksi Testes dan Penghitungan Konsentrasi Spermatofor
Kepiting bakau terlebih dahulu dibersihkan, selanjutnya dipingsankan
dalam freezer (-30oC). Setelah pingsan, kepiting dibedah pada bagian cefalatorak
untuk pengambilan jaringan testes. Jaringan testes, ditimbang dengan timbangan
elektrik (Electonic Analytical Balance, ANDGR-200). Setelah itu dicuci dalam
larutan NaCl fisiologis 0.82 %, dan dikeringkan dengan kertas saring.
Untuk penghitungan konsentrasi spermatofor, testes dicacah dengan
gunting steril, cairan yang keluar diambil dengan mikropipet sebanyak 10 μL dan
dilarutkan dengan 990 μL larutan Ca ++Saline (1:10) dalam mikrotube 1.5 mL.
Kedua larutan dihomogenkan, sebanyak 10 μL dari campuran tersebut diteteskan
ke gelas objek dan dilakukan penghitungan seluruh spermatofor yang terlihat
dibawah mikroskop dan dilakukan pengulangan sebanyak tiga kali. Penghitungan
konsentrasi spermatofor per individu menggunakan rumus : (∑ spermatofor yang
teramati X 10 μL larutan yang diambil dari mikrotube berisi kedua larutan yang
telah dihomogen tersebut).
Pengukuran Diameter dan Koleksi Spermatofor
Pengukuran diameter spermatofor kepiting bakau merah menggunakan
mikroskop yang dilengkapi mikrometer okuler. Spermatofor yang diukur berkisar
± 250 buah untuk tiap individu. Setiap spermatofor diukur berdasarkan ukuran
terbesar sampai terkecil, hal ini dilakukan untuk mengetahui kisaran ukuran
diameter spermatofor.
Koleksi spermatofor dilakukan dengan mengambil spermatofor segar dari
bagian tengah vas deferen pada jaringan testes dengan cara menusuk dinding tipis
dari bagian tengah vas deferen, seminal plasma yang mengandung spermatofor
dikoleksi dalam petri dish (Bhavanishankar & Subramonian 1997; Sato et al.
30
Penghitungan Jumlah Spermatozoa
Penghitungan konsentrasi spermatozoa dilakukan dengan cara
mengeluarkan spermatozoa dari spermatofor (Bhavanishankar & Subramonian
1997). Pengeluaran spermatozoa dari spermatofor dilakukan dengan pronase
dengan prosedur, sebagai berikut; 1) Spermatofor dikoleksi sesuai dengan
klasifikasi ukuran yang telah ditentukan, diletakkan dalam objek gelas dan
diteteskan dengan 2 μL pronase 0.05 % dan ditambahkan 8 μL larutan medium
spermatozoa (Ca++ free saline). 2) Didiamkan selama 15-20 menit kemudian
dihomogenkan 3) Larutan yang berisi spermatozoa diambil menggunakan pipet
sebanyak 5 μL, kemudian diteteskan pada Neubauer Chamber untuk dilakukan
penghitungan sel spermatozoa.
Preservasi Spermatofor
Preservasi spermatofor dengan memberikan perlakuan pada lama
penyimpanan spermatofor (0,5,10,15, dan 20 hari) dalam refreigator 4◦ C untuk
menguji viabilitas dari spermatofor Scylla olivacea.
Tahapan Penelitian II
Pengamatan Struktur dan Morfologi Spermatozoa Dengan SEM
Pengamatan SEM untuk melihat morfologi permukaan spermatofor dan
spermatozoa secara detail dari kepiting bakau merah menggunakan SEM
mengikuti prosedur standar yang ada.
Rancangan Penelitian dan Analisis Data
Data yang diperoleh disajikan dalam bentuk tabel, histogram, grafik, dan
scaterplot menggunakan program Excell untuk melihat rataan dan sd dari
masing-masing karakteristik umum Scylla olivacea yang berasal dari tiga lokasi,
konsentrasi spermatofor per individu, viabilitas spermatofor, kisaran ukuran
spermatofor, konsentrasi spermatozoa per spermatofor. Untuk gambar morfologi
HASIL DAN PEMBAHASAN
Karakteristik Umum Kepiting Bakau Merah Jantan Scylla olivacea
Gambar 13 Karakteristik umum Scylla olivacea, Keterangan; A = Blanakan, Jawa Barat
B = Maros, Sulawesi Selatan dan C = Fak-Fak, Papua Barat
Berdasarkan pengamatan diperoleh hasil yang menunjukkan kepiting
bakau merah jantan (Scylla olivacea) yang berasal dari tiga lokasi pengambilan
sampel penelitian, memiliki perbedaan morfometrik yang cukup signifikan ini
terlihat dari ukuran dan warna tubuh (Gambar 13). Kepiting bakau merah jantan
yang berasal dari Blanakan, Jawa Barat memiliki ukuran tubuh yang relatif lebih
kecil dibandingkan dengan kepiting bakau merah jantan dari Maros, Sulawesi
Selatan dan Fak-Fak, Papua Barat. Selain itu, memiliki warna tubuh yang lebih
terang dibandingkan dengan kepiting dari kedua daerah lainnya. Hal ini
disebabkan perbedaan hábitat yang berhubungan langsung dengan wilayah
geografi masing-masing lokasi, sehingga merupakan suatu indikator yang dapat