MEMPELAJARI PENGGUNAAN AIR KELAPA SEBAGAI
MEDIA UTAMA DALAM PRODUKSI BAHAN AKTIF
.
BIOJNSEKTISIDA DAM
Bacillus thuringiensis subsp. Israelensis
Oleh
TEGUH PRIATNO
1999
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
TEGUH PRIATNO. F 31.0924. Mempelajari Penggunaan Air Kelapa Sebagai Media Dalam Produksi Bahan Aktif Bioinsektisida Dan BaciNus thuringiensis subsp.
isruelensis. Di bawah bimbingan Khaswar Syamsu.
Penggunaan insektisida kimia dalam memberantas vektor pembawa penyakit, seperti nyamuk dan lalat hitam di negara tropis mempunyai efek yang tidak baik karena insektisida hmia bersifat tidak selektif dan menyebabkan terganggunya keseimbangan ekosistem. Sebagai alternatif lain adalah dip.akannya insektisida mikroba dari Bacillus thuringiensis yang bersifat selektif terhadap serangga tertentu.
Indonesia termasuk negara yang banyak menghasilkan kelapa sehingga dengan demikian juga menghasilkan limbah berupa air kelapa. Air kelapa mengandung gula, protein, mineral, vitamin, dan zat turnbuh yang memungkinkan sebagai media dalam fermentasi mikroba.
Tujuan penelitian ini adalah untuk mengetahui kombinasi optimal antara air kelapa yang berkadar gula tertentu sebagai media utama dengan kedua jenis sumber nitrogen yang digunakan yaitu pupuk urea dan ekstrak kharnir dalam medium fermentasi untuk produksi bahan aktif bioinsektisida dari B. thuringiensis subsp. isruelensis dan untuk mengetahui toksisitas produk yang dihasilkan terhadap larva nyamuk Culex sp.
Penelitian pendahuluan memberikan hasil bahwa air kelapa yang digunakan mempunyai kadar abu 0.466 persen, kadar protein 0.238 persen, dan kadar gula 1.77 persen. Untuk mencapai kadar pula optimum bagi pertumbuhan B.t.i. (sebesar 1.25 persen) maka air kelapa yang digunakan diencerkan hingga 70,5 persen. Air kelapa
100 persen digunakan sebagai pembanding untuk mengetahui mana yang lebih baik. Laju pertumbuhan tercepat terjadi pada kisaran jam ke-6 hingga jam ke-9 dimana air kelapa 70.5 persen menghasilkan laju pertumbuhan yang lebih cepat daripada air kelapa 100 persen. Demikian pula sumber nitrogen urea memberikan laju perhmbuhan yang lebih cepat daripada sumber nitrogen ekstrak khamir.
P e n m a n nilai pH terjadi mulai dari jam ke-0 hingga jam ke-9, setelah itu nilai pH naik kernbali. Semakin banyak gula yang dikandung di dalam cairan kultur (media) semakin besar rentang penurunan nilai pH yang dihasilkan. Konsentrasi nitrogen juga mempengaruhi penurunan nilai pH cairan kultur.
Pembentukan spora dimulai pada kisaran jam ke-9 hingga jam ke-12 dan pembentukan spora secara cepat terjadi pada jam ke-12 hingga jam ke-30, kemudian mengalami perlambatan hingga jam ke-48.
Sumber karbon dan sumber nitrogen yang digunakan memberikan pengaruh yang nyata terhadap nilai total sel, jumlah spora hidup, dan berat kering yang dihasilkan, sedangkan konsentrasi sumber nitrogen tidak memberikan pengaruh yang nyata terhadap nilai total sel, jumlah spora hidup, dan berat kering yang dihasilkan.
Produk dengan sumber nitrogen ekstrak khamir mempunyai daya bunuh (toksisitas) yang lebih besar daripada sumber nitrogen urea. Nilai berat kering biomassa atau jumlah spora hidup yang dihasilkan tidak mempengaruhi tingkat mortalitas larva Culex sp. oleh produk yang dihasilkan.
MEMPELAJARI PENGGUNAAN AIR KELAPA SEBAGAI MEDIA
DALAM PRODUKSI BAHAN AKTIF BIOINSEKTISIDA DARI
Bacillus thuringiensis subsp. Israelensis
Oleh
TEGUH PRIATNO
F 31.0924
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
pada Jumsan TEKNOLOGI MDUSTRI PERTANIAN,
Fakultas Teknologi Pertanian,
Institut Pertanian Bogor
FAKULTAS TEKNOLOGI PERTANIAN
.- -, ,-
/.<.
\"* INSTITUT PERTANIAN BOGOR dj.
.<
O.-:,:
.) ,..",a v . >;\..,-, \ -., ,+
,
..a. -
'
? a \, *..,, & ,
BOGOR
i/'2
-;
.,:. ,j2T .. .,.::-: .*
I1,
--
.,$, ,: .!;\ ; ,-,
,
..:.
. . . ' ..# i ?/:..? ,"9 r.
'"'
?,$1 l Z ,:.L,!a.,. i j . ' ; . 0,. :#
,-a- I.:&*#* / >
I , \ .>.-. '~,:**; <-#>.j
3 ., -. - -.. / ',' ' . , > , .
,,,
..
,
.
, , , i.I
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PERTANIAN
MEMPELAJARI PENGGUNAAN AIR KELAPA SEBAGAI MEDIA DALAM PRODUKSI BAHAN AKTIF BIOINSEKTISDA DARI
Raci1lu.s tl~uringiensis subsp. Isrue1en.si.s
SKRIPSI
Sebagai salah satll syarat ut~tuk niemperoleh gelar SARJANA TEKNOLOGI PERTANIAN
pada J U N S ~ ~ TEKNOLOGI INDUATRI PERTANIAN, Fakultas Teknologi Pertanian,
Institut Pertanian Bogor
Oleh
TEGUH PRIATNO F 31.0924
Dilahirkan pada tanggal 26 Desember 1976 di Jakarta
Tanggal Lulus : 14 Man,t 1949
%
+-T-=-M
-'KATA PENGANTAR
Alhamdulillah, penulis memanjatkan puji dan syukur ice hadirat Allah
SWT yang telah memberikan rahnlat dan karunia-Nya sehingga penulis dapat
menyelesaikan skripsi ini dengan baik.
Pada keselnpatan ini penulis menyampaikan ucapan terima kasih yang
sebesar-besarnya kepada :
1. Bapak (aim) dan Ibu, serta kakak-kakakku tercinta yang telah dengan tulus
ikhlas memberikan kasih sayang, restu, dan dorongan spirituii seiaina ini
sehingga tanpanya penulis tidak berarti apa-apa.
2. Dr. IT. Khaswar Syamsu, MSc. sebagai dosen pembimbing yang teiah
memnberikan berbagai bimbingan, pengarahan, dan saran seiarna penelitiaii
sampai penyusunan skripsi.
3. Dr. Ir. Tajuddin Bantacut, MSc. dan Drs. Chiiwan Panciji, Apth. MSc. sehagai
dosen penguji.
4. Zulfikar Muin, 'Dik Nova Fiiria Andyani, Dian Kusuma Hendrawati dan
Martyasari Aziya, yang telah banyak memberikan saran, bantuan, dan
persahabatannya.
5 . Mbak Peppy, Mbak Emi, Pak Alfi, Pak Jacksen, Vivi, Kristian, Arnanto,
Rifa'i, Jamal , Rairi, Devi, Ranti, Yennita, dan teman-ieman di Laboratoriuin Rekayasa Bioproses yang telah banyak lnembantu selama penulis melakukan
6. Indriawan, Akri, Togar, Budi (TIN 16), Woro, Aboet, Ita yang teiah banyak membantu ljenuiis baik selbma peneiitian, penyusunan skripsi, hingga
persiapan ujian sidang.
7. Teman-teman TN-15 atas segala ha1 yang telah kita laiui bersama sela~na
kuiiah di Fateta-PB.
8. Tenian-temari satu kost Fitrian, Azis, Hendra, Akrie, Indri, Zakir, Priyo,
Yitno, Budi, Yogi, Rozal, Bang Dedi Naufal, Toha, dan Eka serta teman-
teinan kost di Wisma Sriwijaya lainnya yang telah meinberikan arti dan wanla
kehidupan seiama. penulis menjaiani masa pendidikan di P B .
9. Semua pihak yang telah membantu penulis selama ini nalnun tidak dapat
disebutkan satu-.persatu
Penulis mengharapkan kritik clan saran yang ine~nbangun dari senlua
pihak berkaitan dengan skripsi ini. Akhirnya penulis berharap agar skripsi ini
dapat membcrikan miinfakt bagi semua pihak yang memc~iukannya.
DAFTAR IS1
Halaman
KATA PENGANT I
DAFTAR IS1 ....
.
. .. . . .. . ... . . ....
......
.. ..
. . .. . .
.
. . .. . . .
. . . ..
,.
iiiDAFTAR TABE
DAFTAR GAMBAR
DAFTAR LAMPIRAN
....
... viiI. PENDAHULUAN ... 1
A. LATAR BELAKAN 1
B. TUJUAN PENELITIAN ... 3
C. RUANGLINGK 3
Di. TEYJAUAN PUSTA 4
A. AIR KELAPA ... . . . . . . . ... 4
B. PENGGUNAAN Bacillus thuring~ensis SEBAGAI BAHAN
AKTIF INSEKTISIDA MIKROBA 5
C. FEFSdENTASI B. :/zuringiensi 7
D. PENENTUAN AKTIVITAS TNSEKTISIDA MIKROBA ... 9
III.
BAEAN DAN METOD 10A. BAHAN DAN ALAT 10
B. METODE PENELITIAN i 1
. .
1. Penelltlan Pendahuluan ... 11
2. Penelitian Utam 11
b . Persiapan Inokulum ... 12
c . Fermentasi 13 d . Penentuan Aktivitas Insektisida Mikroba ... 14
C . ANAiISA PARAMETEIi
...
15D . PENGAMBLAN CONTOH (SAMPLING) ... 16
E
.
RANCANGAN PERCOBAAN...
171 . Penentuan Jumlah Sel clan Spora Hidup ... 17
... 2 . Penentuan Aktivitas Insektisida Mkroba (Bioassay) 18
IV
.
HAS= DAN PEMBAHASAN ... 19A . PENELITIAN PENDAHULUAN ... 19
. B . PERTUMBUKAN SEL Bacillus thuringiensis subsp israelensis
...
20C . NILAIp 25 D . PEMBENTUKAN SPORA 27 ... E . BERAT KERING BIOMASSA (SEL-SPORA-KRISTAL) 33 F . BIAYA BAHAN BAKU (SUMl3ER NITROGEN) ... 33
G
.
PENGUJIAN AKTIVITAS PRODUK PRIMER TEKHADAP MORTALITAS LARVA 3 5 V.
KESIMPULAN DAN SARAN ... 38A . KZSWIPULAN
...
38B . SARAlU
...
40DAFTAR PUSTAKA ... 41
DAFTAR TABEL
Tabel 1
.
Perubahan koinposisi air kelapa ... 5Tabel 2 . Komposisi nutrisi air ketapa ... 6
Tabel 3
.
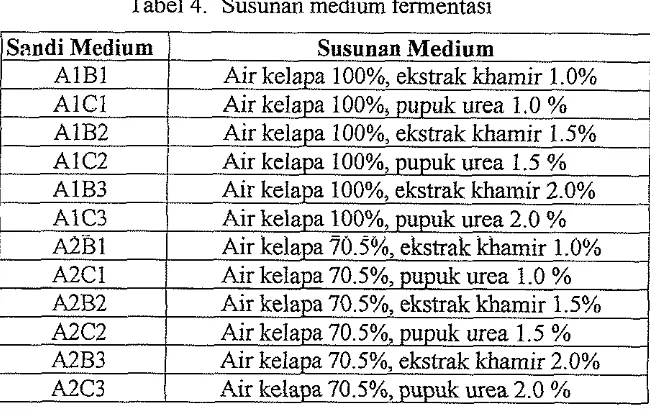
Kandungan mineral air kelapa ... 6Tabel 4 . Susunan medium fermentasi ... 12
Tabel 5 . Kadar gula. nitrogen clan abu dari air kelapa yang digunakan ... 18
Tabel 6
.
Berat kering biomassa (sel-spora-kristal) untuk berbagai konsentrasi sumber karbon clan sumber nitrogen ... 34Tabel 7 . Dafiar harga sumber karbon dan sumber nitrogen ... 34
Tabel 8 . Tingkat mortalitas larva Culex sp
.
untuk berbagai konsentrasi sumber karbon dan sumber nitrogen ... 36DAFTAR G M A R
Eaiaman
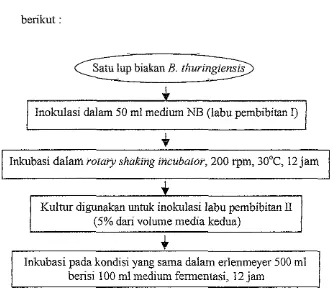
Gambar 1. Diagram alir persiapan inoMum (Vandekar dan dulmage,
1982) ... 13 Gambar 2. Diagram aiir proses fermentasi (Vandekar dan Dulmage, 1982) ... 14
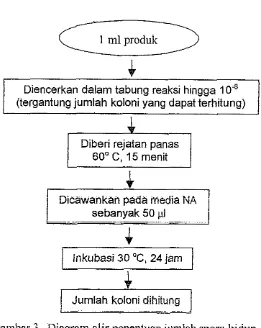
Gambar 3. Diagram alir penentuan jum1ah spora hiciup (Mummigatti dan
Raghunathan, 1990) ... 16 Gambar 4. G r a f i hubungan antara waktu dengan log total sel untuk sumber
karbon air kelapa 100 persen dan 70.5 persen dengan sumber
...
nitrogen ekstrak khamir (a) dan sumber nitrogen urea (b) 22 Gambar 5. Grafik hubungan antara waktu dengan iog total sei untuk sumber
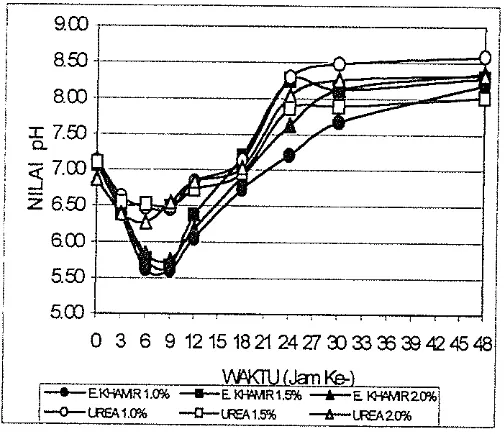
karbon air kelapa 70.5 persen ... 23 Gainbar 6. Grafik hubungan antara waktu dengan nilai pH untuk sumber
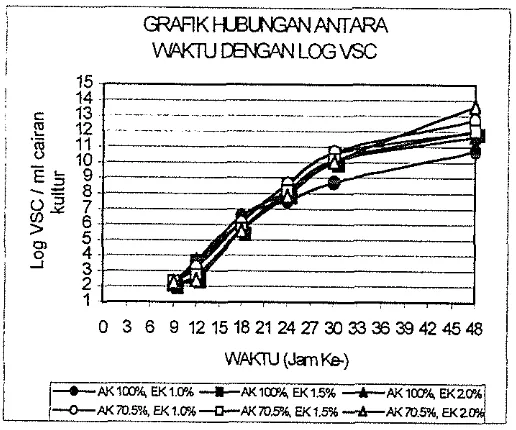
karbon air keiapa 100 persen (a) dan air kelapa 70.5 persen (bj ... 28 Gambar 7. Grafik hubungan antar waktu dengan log VSC untuk sumber
karbon air kelapa dengan sumber nitrogen ekstrak khamir (a) dan urea (b). ... 3 1
DAPTAR LAMPIRAN
Lampiran 1 . Data log total sel Bacillus thuringiensis subsp . isruelensis
...
selama fermentasi 45
Lampiran 2 . Data laju pertumbuhan Bacillus thuringiensis subsp
.
isruelensis selama fermentasi ... 46 Lampiran 3.
Data nilai pH cairan kultur selama fementasi ... 47Lampiran 4 . Data log jumlah spora hidup (VSC) selama fermentasi
...
48Lampiran 5 . Data berat kering bioinassa (sel-spora-kristal)
selama fermentasi ... 49
...
Lampiran 6 . Uji statistik untuk log total sel 50
Lampiran 7 . Uji statistik untuk log VSC ... 52
Lampiran 8 . Uji statistik untuk berat kering biomassa
...
(sel-kristal-spora)
Lampiran 9
.
Analisa kadar protein metode Lowry (Lowry. 1951) ... 56...
.
Lampiran 10 Analisa kadar abu 57
Lampiran 11 . Analisa kadar gula total (metode fenol) ... 58
...
I. PENDAHULUAN
A. LATAR BELAKANG
Insektisida kimia masih banyak digunakan di negara-negara tropis
dalam usaha memberantas vektor pembawa penyakit, seperti nyamuk dan lalat
hitam. Namun ha1 tersebut kurang menguntungkan, karena penggunaan
insektisida kimia dengan dosis dan frekuensi yang tinggi meiljadikan serangga
vektor p e n y k t menjadi resisten terhadap insektisida kimia tersebut, dan
insektisida kimia bersifat tidak selektif sehingga menyebabkan terganggunya
keseimbangan ekosistem (Philip, et. al., 1993).
Penggunaan B. tlzuringiensis dalam memproduksi bioinsektisida telah
dilakukan terutama sebagai pengendali hama pertanian dan serangga vektor
beberapa penyakit pada hewan dan manusia (Hofte dan Whiteley, 1989). Adapun
insektisida bakten yang paling banyak digunakan umumnya berasal dari genus
Bacillus (Khachatourians,l989). Dengan ditenemukannya Bacillus tlzuringiensis
subsp. isruelensis (Rucillz~s tizuringiensis isruelensis) pada tahun 1976 membuka
babak bam dalam pengendalian serangga vektor penyakit (Goldberg dan
Margalit, 1977; Margalit dan Dean, 1985).
Di Indonesia telah beredar produk berbahan aktif B. tlzuringiensis
dengan merk dagang Turex WP, Florbac FG, Centuri G, Bactis S, Bactimos,
Beempe, Teknar, Vectobas-AS, Bactospeine, Delfin, Dipel dan Thuricide
karena bioinsektisida bermerk yang ada di Indonesia di impor dari luar negeri.
Hal ini kemungkinan dapat matasi jika bioinsektisida berbahan aktif B.
thuringiensis dapat diproduksi sendiri.
Indonesia adalah urutan ketiga negara penghasil kelapa terbesar di dunia
setelah Philipina dan India sebagai (Woodroof, 1979). Produksi kelapa di
Indonesia pada tahun 1988 mencapai 2,143,978 ton kopra. Jika menggunakan
angka konversi 5 buah kelapa perkilogram kopra dan 200 ml air kelapa per buah
kelapa, maka didapatkan jumlah air kelapa yang dihasilkan pada tahun 1988
mencapai dua miliar liter (Badan Pusat Statistik, 1991).
Air kelapa mengandung gula, vitamin, mineral, senyawa nitrogen dan
zat-zat tumbuh seperti asam nikotinat, auksin, giberelin, piridoksin dan thiamin
(Tuleckle, 1961). Komponen nutrisi yang lengkap dari air kelapa ini sangat
cocok untuk pertumbuhan bakteri. Oleh karena itu dalam penelitian ini
digunakan air kelapa sebagai media utama dalam memproduksi bahan aktif
bioinsektisida dari B. tlzuringiensis.
Galur
H.
rizuringie~sis dan medium fementasi yang digunakan sangatberpengaruh terhadap keberhasilan produksi bioinsektisida (Dulmage dan
Rhodes, 1971). Demikian pula perlu diperhatikan faktor lingkungan yang
mempengaruh proses fermentasi.
Penelitian ini menggunakan air kelapa sebagai media utama dengan
penambahan urea atau ekstrak khamir sebagai sumber nitrogen. Hal tersebut
dikarenakan mengingat masih banyaknya air kelapa yang masih belum
media pengganti dalam produksi bioinsektisida dari B. thuringiensis secara
fermentasi terendam sehingga akan mengurangi biaya produksi. Dengan
demikian kemungkinan harga jual pun dapat ditekan menjadi lebih murah.
B. TUJUAN PENELITIAN
Tujuan umum penelitian ini adalah memanfaatkan air kelapa sebagai salah satu hasil sampingllimbah pertaniadindustri pertanian untuk menghasilkan
produk yang mempunyai nilai tambah. Tujuan khusus penelitian ini adalah
untuk mengetahui kombinasi optimal antara air kelapa yang berkadar gula
tertenty sebagai media utama, dengan kedua jenis sumber nitrogen yang
digunakan yaitu pupuk urea dan ekstrak khamir dalam medium fermentasi untuk
produksi bahan aktif bioinsektisida dari B. thuringiensis isruelensis dan untuk
mengetahui toksisitas produk yang dihasilkan terhadap larva nyamuk Culex sp.
C. RUANG LINGKUP
Ruang lingkup penelitian adalah :
1. Mencari kombinasi optimal antara sumber karbon dan nitrogen untuk
fermentasi B. thuringiensis israelensis.
II.
TINJAUAN PUSTAKA_
Produksi kelapa di Indonesia pada tahun 1988 mencapai 2 143 987 tonkopra. Dengan menggunakan angka konversi 5 buah kelapa perkilogram
kopra dan 200 ml air kelapa per buah kelapa, maka jumlah air kelapa yang
dihasilkan di Indonesia pada tahun 1988 mencapai dua milyar liter yang
terbuang percurna (Badan Pusat Statistik, 199 1).
Air kelapa adalah cairan jemih yang mengisi lebih kurang % bagian
rongga sebelah dalam daging kelapa. Air kelapa di dalam buah mencapai
jumlah maksimum pada waktu buah berumur 6 sampai 9 bulan (Freemond
dan Ziller, 1966). Air kelapa mengandung gula yang terdiri dari sukrosa,
glukosa, dan fiuktosa (Alaban, 1962). Kandungan gula air kelapa adalah
sekitar 5 persen dengan nilai kalori 17.4 kalori per 100 gram bahan
(Direktorat Gizi Depkes, 1988) Kandungan gula invert meningkat dan
mencapai maksimal ketika bemmur kira-kira 220 hari, setelah periode ini
sukrosa mulai terbentuk clan konsentrasi total gula menurun [Thampan,
1982). Dengan bertambahnya umur buah kelapa, wama sabut berubah
menjadi coklat dan jumlah aimya berkurang bersama-sama dengan turunnya
kadar gula menjadi sekitar 2 persen dan setengahnya adalah gula
Air kelapa memiliki pH yang beragam dari 4.8 sarnpai 5.3 (Thampan,
1982). Adanya asam-asam organik dan anorganik dalam air kelapa Tabel 1. Pembahan komposisi air kelapa3
menyebabkan pH air kelapa agak rendah. Asam-asam tersebut antara lain
asam amino, asam-asam organik non volatil, asam nukleat, asain shikinat dan Komponen Air Protein Lemak Karbohidrat Abu
asam kuinat (Tuleckle, 1961). Asam amino yang terdapat dalam air kelapa
antara lain adalah alanin, arginin, sistein, dan serin (Woodroof, 1979).
Nilai nutrisi yang dikandung air kelapa cukup lengkap, karena
mengandung pula vitamin, mineral serta zat-zat tumbuh seperti terlihat pada
*' Subrahmanyan dan Swaminathan (1959)
Kelapa Muda (YO)
95.01 0.13 0.12 4.11 0.63
Tabel 2. Zat-zat tumbuh tersebut antara lain asam nikotinat, auksin, giberelin,
piridoksin dan thiamin (Tuieckle, 1961). Air kelapa mengandung 0.7 sampai
3.7 persen vitamin C dan sedikit vitamin B kompleks (Child, 1962). Air Kelapa Tua (%)
91.23 0.29 0.i5 7.27 1.06
keiapa juga mengandung kalium, natrium, kalsium dan mineral-mineral
lainnya seperti terlihat pada Tabel 3
B. PENGUNAAN Bacillus thuringiettsis SEBAGAI BAHAN AKTIF INSEKTISIDA MlKROBA
Bacillus thuringiensis adalah bakteri yang paling banyak digunakan
[image:17.564.157.468.68.197.2]hama (Quinlan dan Lisansky, 1985; Feitelson, el. al., 1992). Penggunaan
B. thuringiensis sebagai insektisida mikroba diharapkan semakin meningkat
dan berkembang dengan ditemukannya galur-galur B. thuringiensis yang
mempunyai aktivitas tinggi dan spektrum inang yang lebih luas (Rupar, et.
al., 1991; Jhonson, el. al., 1993).
Tabel 3. Kandungan Mineral Kalium Natrium Kalsium Magnesium Besi Teinbaga fosfor
Tabel 2. Komposisi nutrisi air kelapaS)
rineral air kelapa')
Kindungan (mg1100 ml) 312.00 Komponen Asam nikotinat Asam pantotenat Biotin fiboflavin Asam folat Thiamin Piridoksin Auksin Giberelin 1-3 difenil urea Sorbitol
Mvoinositol
Jumlah 0.6 mgll 0.52 mg/l 0.02 mdl 0.01 mg/l 0.003 mg/l
sedikit sedikit 0.07 mg/l sedikit 5.8 mg!l 15.0 mg/l 0.01mdl
Bacillus thuringiensis adalah bakteri berbentuk batang, bersifat gram
Belerang
positif dan berflagelum. Bakteri ini membentuk spora secara aerob dan 24.00
[image:18.559.152.421.224.474.2] [image:18.559.141.429.467.620.2]7
insektisida, yang disebut juga dengan 6 endotoksin (Shieh, 1994). Disamping
endotoksin, B. thuringiensis juga menghasilkan eksotoksin, yaitu
a eksotoksin,
P
eksotoksin d m faktor kutu yang bersifat sangat toksikterhadap kutu mamalia (Bovicola sp.) (Dulmage, 1981).
Proses reaksi kristai protein sebagai bahan aktif bioinsektisida dimulai
dengan termakannya kristal protein oleh serangga yang akan dipecah oleh
enzim protease pada kondisi basa dalam usus tengah serangga, dan akan
melepaskan protein toksik yana disebut 6 endotoksin. Toksin ini akan
berinteraksi dengan reseptor-reseptor pada sel-sel epitelium usus tengab larva
serangga yang rentan. Setelah toksin ini bereaksi maka akan menyebabkan
terbentuknya lubang-lubang pada membran sel, sehingga mengganggu
keseimbangan osmotik. Akibatnya sel usus serangga yang rentan menjadi
bengkak dan mengalami lisis. Karena tejadi pembengkakan maka larva
berhenti makan dan akhirnya mati (Hofte dan Whiteley, 1989; Gill, el. a/.,
1992).
Fennentasi untuk memproduksi bioinsektisida B. thuringiensis terdiri
dari dua tipe yaitu fermentasi semi padat (semi solid fermentation) dan
fermentasi terendam (submerged ferntentation). Fermentasi terendam yaitu
fermentas B. tlzuringiensis dimana biakan murni B. thuringiensis
ditumbuhkan dalam medium cair dengan dispersi yang merata. Fermentasi
skala kecil dalam labu kocok dilakukan dengan menggunakan labu ukuran
dengan menggunakan labu erlenmeyer ukuran 500 ml yang diisi 100 - 125 ml
medium (Vandekar dan Dulmage, 1982; Mummigatti dan Raghunathan,
1990).
Beberapa faktor sangat mempenganh fermentasi B. thuringiensis,
diantaranya adalah komposisi medium dan kondisi untuk pertumbuhan mikroba seperti pH, oksigen dan temperatur (Dulmage dan Rhodes, 1971).
Untuk pertumbuhannya mikroorganisme membutuhkan surnber air, sumber
karbon, nitrogen, unsur mineral dan faktor pertumbuhan dalam medium
pertumbuhannya (Vandekar dan Dulmage, 1982). Beberapa sumber karbon
dapat digunakan untuk fermentasi B. thuringiensis secara terendam antara
lain glukosa, simp jagung, tepung jagung, dekstrosa, sukrosa, laktosa, pati,
minyak kedelai dan moiases dari bit dan tebu. Sumber nitrogen yang dapat
digunakan adalah tepung kedelai, tepung biji kapas (proflo), corn steep,
gluten jagung, ekstrak kharnir, pepton, kedelai, tepung ikan, tripton dan
kasein (Dulmage dan Rhodes, 1971; Quinlan dan Lisansky, 1985).
Garam-garam anorganik yang dibutuhkan untuk pertumbuhan
miliroba nieliputi K, Mg, P, S, dan yang diperlukan daiam jumiah sedikit
yaitu Ca, Zn, Fe, Co, Cu, Mo dan Mn (Dulmage dan Rhodes, 1971). Dalam
medium fermentasi ditambahkan 0.3 g/l MgS04.7H20, 0.02 g/l ZnS04.7H20,
0.02 g/l FeS04.7H20 dan 1.0 gfl CaC03 (Vandekar dan Dulmage, 1982).
Fermentasi B. tlzuringiensis dalam labu kocok dilakukan pada suhu
28 - 32 OC, dengan pH awal medium diatur sekitar pH 6.8 - 7.2, agitasi
142 - 340 rpm dan dipanen pada waktu inkubasi 24
-
48 jam (Vandekar danD. PENENTUAN AKTJMTAS INSEKTISIDA MlKROBA
Insektisida mikroba ditentukan aktivitasnya dengan menghitung
jumlah spora hidup, dan melalui bioassai untuk menentukan kadar letal
(LCso) dan International Unit (IU) (Vandekar .. dan Dulmage, 1982) atau dosis
letal (LDso), Diet Dilution Unit (DDU50) dan IU (Dulmage dan Rhodes,
1971). LC50, LD50, dan DDUSO sebenarnya hanya menunjukkan potensi
relatif produk, karena dlpengamhi oleh spesies dan umur serangga. Oleh
karena it-, maka disepakati potensi produk insektisida mdcroba
(B. tlzuringiensis) dinyatakan dalam satuan internasional (SI).
LC50 standnr
A. BAHAN DAN ALAT
Isolat Bacillus tlzuringiensis yang digunakan adalah E. tlzuringiensis
israelensis yang diperoleh dari B. thuringiensis israelensis komersial
(Vectobac). Media fementasi yang digunakan adalah air kelapa yang
didapatkan dari pasar Gunung Batu di daerah Bogor. Sumber nitrogen yang
digunakan adalah pupuk urea dan ekstrak khamir.
Bahan-bahan yang digunakan adalah nutrien broth (NB), HCl 1 N,
NaOH 1 N, larutan garam fisiologis, medium nutrient agar (NA), napthol blue
black, methanol 98 persen, air suling, asam asetat, basic fuchsin, ethanol
95 persen, fenol, air destilata, Na-K-Tartarat, larutan fenol 5 persen,
Na~C03-anhidrat, H2S04 pekat, protein BSA, NaOH 0.1 N, CuS04.5H20,
folin ciocalteu, larutan glukosa standar, produk komersial Vectobac, dan
produk kimia Abate.
Alat-alat yang digunakan adalah rotat-)? shaking incubator, otoklaf,
pemanas berpengaduk, batang magnetik, pH meter, labu erlenmeyer,
sentrifuse, loop inkubasi, tabung reaksi, pipet, lemari pendingin, oven,
spektrofotometer, timbangan analitik, cawan petri, gelas kimia, gelas piala,
kertas saring, bunsen, keranjang tabung, kertas serap, desikator, tanur dan
B. METODE PENELITIAN
Penelitian ini terdiri dari dua bagian, yaitu penelitian pendahuluan dan
penelitian utama.
1. Penelitian Pendahuluan
Penelitian pendahuluan bertujuan untuk menganalisa komposisi
awal air kelapa. Analisa komposisi kimia air kelapa yang dilakukan
adalah analisa kadar protein (metoda L o w ) , kadar abu, kadar gula
total (metoda fenol).
2. Penelitian Utarna
a. Persiapan medium fermentasi
Susunan medium fermentasi yang akan digunakan dalam
penelitian ini adalah air kelapa sebagai media utama dengan
penambahan sumber karbon lain dan nitrogen seperti terlihat pada
Tabel 4. Susunan medium fermentasi tersebut dibuat 2 kali
ulangan.
Jenis dan jumlah mineral sesuai dengan yang digunakan oleh
Dulmage dan Rhodes (1971), yaitu 0.3 g MgS04.7H20, 0.02 g
FeS04.7H20, 0.02 g ZnSO4.7H20, 0.02 MnS04H20 dan 1.0 g
12
Tabel 4. Susunan medium fermentasi
Adapun persiapan medium fermentasi adalab sebagai berikut :
air kelapa dan CaC03 masing-masing dilamtkan dan disterilkan
secara terpisah dari bahan-bahan media yang lain, seperti mineral
dan sumber nitrogen, di dalam otoklaf. Bahan-bahan medium yang
lain langsung dimasukkan ke dalam erlenmeyer dan disterilkan di
dalam otoklaf. Setelah didinginkan sampai F 50°C, medium campuran air kelapa dan CaC03 dibagi-bagi dalam beberapa labu
erlenmeyer yang telah berisi bahan-bahan media lain kemudian pH
medium disesuaikan menjadi sekitar pH 6.8
-
7.2. Semua babandisterilkan dalam autoklaf pada suhu 121°C dan 15 lbs selama i 5
menit.
b. Persiapan Inokulum
Inokulum (kultur bibit) untuk menginokulasi medium
[image:24.567.153.478.74.280.2]dan Dulinage (1982). Persiapan inokuium dilakukan sebagai
berikut :
lup biakan R. tltur
+
Inokulasi dalam 50 rnl memum NB (labu pembibitan I)
I I
t
Mcubasi dalam roluly shakifig incltbulot, 200
rpm,
30°C, 12 jamI I
+
Kultur di,gmakan untuk inokulasi labu pembibitan
II
(5% dari volume mema kedua)
Inkubasi pada kondisi yang sama daiam erlenmeyer 500 ml berisi 100 ml medium fermentasi, 12 jam
Gambar 1. Diagram alir persiapan inokulum (Vandekar dan Dulmage, 1982)
c. Fermentasi
Fermentasi dilakukan dalam beberapa iabu erlenmeyer 500 mi
yang masing-masing berisi 125 mi medium fermentasi, dengan
konsentrasi sumber kaioon dan nitrogen yang sesuai dengan
perlakuan yang dicobakan (Tabel 2). Masing-masing labu tersebut
diinokulasi dengan kultur inokulum dari labu pembibitan kedua
sebanyak 2% secara aseptik. Kemudian diinkubasi dalam rotavy
shaking incubator pada 200 rpm dan suhu 30" C selama 48 jam.
Selama inkubasi, biakan diamati pada interval waktu tertentu.
[image:25.564.130.463.86.383.2]Labu erlenmeyer 500 ml berisi 125 ml medium
I
Masing-masing labu diinokulasi dengan kuitur inoMum dari labu pembibitan I1 (2%)I
~
5
II
Inkuljasi dalsuii 200 rpm, 30' rotary shaking incubator, C, 48 jam1
Biakan diamati ~ a d a interval walctu tertentu1
Gambar 2. Diagram alir proses fermentasi (Vandekar dan Dulmage, 1982)
d. Penentuan Aktivitas Inseictisida Wkroba
Penentuan aktivitas insektisida mikroba adalah sebagai
berikut : sampel cairan produk bahan aktif bioinsektisida
B. thuringiensis dari tiap-tiap perlakuan disuspensikan dalam air
destiiata sebanyak 10 tingkat konsentrasi. Sebanyak 25 ekor larva
nyamuk Culex sp. masing-masing dimasukkan ke &lam larutan
bioinsektisida yang telah dibuat sebeiumnya. Sebagai pembanding
dibuat pula lamtan bionsektisida dari produk komersiai Vectobac
dan produk insektisida kimia Abate dengan konsentrasi yang sama.
Setiap perlakuan diulang sebanyak dua kali. Setelah 24 jam,
mortalitas iarva diamati. Nilai LC50 produk untuk tiap perlakuan
ditentukan dengan menggunakan metode analisis probit program
[image:26.559.135.433.79.288.2]C. ANALISA PARAMETER
Analisa parameter dalam penelitian ini meliputi analisa pendahuluan
(pra-fementasi), analisa fermentasi dan analisa pasca fermentasi. Analisa
pendahuluan meliputi : (1) penentuan kadar protein, (2) kadar abu dan
( 3 ) kadar gula dari air kelapa yang digunakan. Analisa selama fennentasi
meliputi pengamatan terhadap : (1 ) perturnbuhan sel bakteri dengan metode
hitungan cawan, (2) pengukuran pH dengan pH meter, (3) pengamatan
sporulasi, dan (4) pengukuran berat kering biomassa (Sel-spora-knstal).
Analisa pasca fermentasi adalah dengan menguji bioinsektisida atau komplek
spora kristal hasil fermentasi untuk semua jenis perlakuan, dengan
menentukan jumlah spora yang terkandung dan toksisitasnya terhadap larva
nyamuk yang dinyatakan dalam LCso. Metode penentuan jumlah spora hidup
(viable spore count) adalah sebagai berikut :
Larutan fermentasi diambil dan diencerkan di dalam tabung reaksi hingga
pengenceran 10.' (tergantung pada julnlah koloni yang dapat dihitung). Lalu
diberi rejatan panas pada suhu 65" C selama 15 menit untuk membunuh sel-
sel vegetatif (Mummigatti dan Rashunathan, 1990). Selanjutnya sebanyak
0.05 mi dari pengenceran yang sesuai dicawankan dengan metode cawan
sebar pada medium NA. Setelah diinkubasi pada suhu 30" C selama 24 jam,
jumlah koloni masing-masing cawan diamati dan dihitung. Spora hidup yang
terkandung dalam satnpel serbuk spora kristal, ditentukan dengan cara
mengalikan jumlah koloni yang terbentuk dengan faktor pengencerannya.
1 ml produk
-
Diencerkan dalarn tabung reaksi hingga 1 O9
(tergantung jurnlah koloni yang dapat terhitung)
I
+
I
Diberi rejatan panas/
60' C, 15 rnenitDiawankan pada media NA sebanyak 50 p1
,
I
lnkubasi 30 "C, 24 jamI
(
Jurnlah koloni dihitungI
Gambar 3. Diagram alir penentuan jumlah spora hiaup (Mummigatti dan Raghunathan, 1990)
Pengambiian contoh (satnpling) dilakukan sebanyak 9 kali dan dila'mkan
pada saat inkubasi 0,3,6, 9, i2, i s , 24,30, dan 48 jam. Pengambilan contoh
(sampiingj ini dilakukan untuk mengetahui pertumbuhan bakteri
B. Tizuringiensis dengan menggunakan hitungan cawan, pengukuran terhadap
pH, pengukuran terhadap pembentukan spora dan mengukur berat kering
[image:28.567.157.418.61.389.2]E. RANCANGAN PERCOBAAN
1. Penentuan Jumlah Sel dan Spora Hidup
Rancangan percobaan yang digunakan untuk menentukan jumlah
sel dan spora hidup adalah eksperimen faktorial tersarang 2 x ?. Faktor
pertama menunjukkan sumber karbon dengan 2 taraf faktor. Sedangkan
faktor kedua menunjukkan sumber nitrogen yang terdiri atas 2 taraf
faktor dengan konsentrasi yang terdiri dari 3 taraf faktor tersarang
didalam sumber nitrogen yang digunakan, sehingga terdapat 12 unit
percobaan dengan replikasi sebanyak 3 kali. Model yang digunakan
untuk desain faktorial tersebut adalah :
Dengan i = 1,2 j = 1,2
k = 1,2,3 untuk semua j ; dan 1 = 1,2,3
Y
= Variabel respon dari hasil observasi ke-1 yang terjadi karena pengaruh bersama taraf ke-i faktor A dan taraf ke-J faktor Bserta taraf ke-k faktor C yang tersarang di dalam faktor B
P = Rata-rata sebenamya Ai = Sumber karbon ke-i
Bj = Sumber nitrogen ke-j
Ckgl = Konsentrasi ke-k tersarang dalam sumber nitrogen ke-j
18
ACiliti) = Efek interaksi antara sumber karbon ke-i dan konsentrasi ke-k
tersarang dalarn surnber nitrogen ke-j
~l(ijk) = Kekeliruan
2. Penentuan Aktivitas Insektisida Milcroba (Bioassay)
Aktivitas insektisida mikroba terhadap serangga dinyatakan
dengan LC50 (ietai concentration). Nilai LC50 merupakan nilai yang
menunjukkan konsentrasi insektisida yang dapat mematikan separuh
dari populasi larva setelah jangka waktu tertentu.
Untuk menentukan aktivitas insektisida mikroba tersebut, data
berat kering lamtan campuran spora kristal dan nilai log jurnlah spora
hidup (Viable Spore Count/'KSC) yang diperoleh untuk masing-masing
perlakuan dianalisa dengan analisis ragam uji F. Apabila hasiinya
menunjukkan perbedaan nyata, analisis dilanjutkan dengan uji
Duncan's klultiple Range Test. Ijntuk hasil pengujian toksisitas,
Iaruian cainpuran spora-kristai dari tiap periakuan ditentukan niiai
Peneiitian pendahuluan dilakukan sebagai langkah awal u~kiuk
L - L . . : ,.-Ae- - . I - -:&*-
' u r ; l q p a u u z haual gum, ill~vgez serfa mineral yang terkandung di dalam
i
L - ~ . ualrarl - yaug digunakan. Dan penelitian pendahuluan ini, diketahui kadar gula,
iiiii-"geii &ail ~ i i i ~ i e ~ a ; yiiiig ieikaiid-ui~g di dalam air keiapa yang digunakan,
seperti teriihat pada Tabel 5.
Tabei 5. Kadar gula, nitrogen dan abu dari air kelapa
y ang digunakanW)
g
1
Gula1
1.770 ii
II
1
Protein
i
0.244I
I
1
A ~ Ui
0.466i
I i
Kadar gula pada bahan yang digunakan ini lebih kecil dari yang
diiaporkan oieh Cniid (i962) bahwa kadar gula maksirnum 5 persen. Hal ini
disebabkan karena air kelapa yang digunakan berasal dari kelapa yang sudah
iua. D ~ r ~ g a t l scrrrakir~ beriarrivaiu~ya umur kelapa, maka kadar gula di
dalamnya pun akan semakin berkurang hingga sekitar 2 persen dan
setengahnya acialah gula bukan pereduksi (Child, 1962). Sedangkan kadar
p~otein air kelapa yang diguiiakan tidak jauh berbeda dengan kadar protein
yang dilaporkan oieh Subrainanyan dan Swaminathan (1959), sehingga dapat
dikatakan bahwa air ketapa yang digunakan masih termasuk air kelapa yang
- segar (tidak rusak) terutama kadar proteinnya.
" Data didapat dari penelitian bersarna Teguh Priatno dengan Depi Arpita dan Ranthi
20
Air kelapa banyak mengandung mineral, vitamin dan zat tumbuh,
sehingga air kelapa baik untuk digunakan sebagai media pertumbuhan
Bacillus thuringiensis subsp. israelensis (l3.t.i.). Dengan banyaknya vitamin,
mineral dan zat tumbuh kemungkinan dapat mempengaruhi kualitas produk
yang dihasilkan. Berdasarkan penelitian sebelumnya, konsentrasi sumber
nitrogen yang optimum untuk perhmbuhan B.t.i. adalah 1.5 persen (Sukmadi,
1996). Dalam penelitian ini chgunakan konsentrasi sumber nitrogen 1.0, 1.5,
dan 2.0 persen (bh). Berdasarkan penelitian sebelumnya, kadar gula yang
optimum untuk perhmbuhan B.t.i. adalah 1.25 persen (Sukmadi, 1996).
Dengan kadar guia pada air kelapa 1.77 persen, maka air kelapa yang
digunakan perlu diencerkan hingga memiliki kadar gula 1.25 persen. Dengan
demikian air kelapa yang digunakan sebanyak 70.62 ml atau sekitar 70.5 ml
di dalam 100 mi media, atau dengan kata lain sebesar70.5 persen air kelapa.
Namun demikian dalam penelitian digunakan juga 100 persen air kelapa
sebagai pembanding.
B. PERTUMBUEAN SEE Bacillus tltzcrilzgieitsis subsp. Isrnelensis
Penelitian terhadap pertumbuhan sel B.t.i menunjuicitan bahwa untuk
tiap faktor yang diujikan (air kelapa dengan sumber nitrogemya)
memperlihatkan pola pertumbuhan yang sama, yaitu fase lambat (fase lag)
tejadi sangat pendek. Hal ini terjadi karena kultur B.t.i. ditumbuhkan
terlebih dahulu di dalam media nutrien brotlz (sebagai inokulum pertama) dan
kemudian ditumbuhkan lagi di dalam media fermentasi (sebagai inokulum
21
menyebabkan kulixr dapat beradaptasi terhadap lingkungail pertumbuhan
ketika mtumbuhkan pada media fermentasi utama.
Seperti yang terlihat pada Gambar 1 dan Lampiran i, bahwa
penggunaan media air kelapa 100 persen (tanpa penambahan air destilata)
maupun air kelapa 70.5 persen (air keiapa 70.5 ml
+
air destilata 29.5 mi)dengan sumber nitrogen ekstrak khamir menghasilkan fase stasioner pada jam
ke-12, sedangkan untuk sumber nitrogen urea fase stasioner terjadi pada jam
ke-9. Hal ini disebabkan karena untuk berat yang sama, kandungan nitrogen
urea lebih sedikit daripada ekstrak khamir sehingga jumlah nitrogen (urea)
dalam media iebih cepat habis yang menyebabkan fase stasioner menjadi
lebih cepat. Ekstrak khamir juga mengandung sumber karbon sehingga
media yang menggunakan sumber nitrogen ekstrak khamir mengandung
sumber karbon yang lebih banyak daripada media yang inenggunakan urea
sebagai sumber karbon.
Baik pada sumber nitrogen ekstrak khamir maupun urea,
penggunaan sumber karbon air kelapa 70.5 persen menghasilkan nilai log
total sel yang iebih tinggi daripada j i ~ a inenggunakan air kelapa 100 persen.
Hal ini dapat terlihat jelas pada Gambar 2. Perbedaan yang sangat nyata ini
juga diperkuat dengan uji analisa ragam untuk log total sei yang
menghasilkan nilai F hitung sebesar 96.9341 dengan nilai F Tabel
( a
= 0.05)sebesar 4.75. Nilai ini menunjukkan bahwa konsentrasi sumber karbon
terhadap nilai log total sel yang dihasilkan. Lebih tingginya nilai log total sel
yang dihasilkan pada media dengan sumber karbon air kelapa 70.5 persen
daripada air kelapa 100 persen disebabkan karena air kelapa 100 persen
mengandung kadar gula yang lebih tinggi sehingga setelah terjadi proses
metabolisme dihasilkan asam-asam yang lebih banyak. Produksi asam yang
lebih banyak pada air kelapa 100 persen menyebabkan penurunan nilai pH
yang lebih besar pada saat proses fenentasi berlangsung sehingga
pertumbuhan sel menjadi terhambat.
Dengan menggunakan air kelapa 70.5 persen, pada dasamya
penggunaan sumber nitrogen urea menghasilkan log total sel yang lebih
tinggi daripada menggunakan sumber nitrogen ekstrak khamir. Hasil ini
dapat terlihat nyata pada Gambar 2, dan diperkuat dengan pengolahan analisa
ragam yang menghasilkan nilai F hitung sebesar 7.4696 dengan nilai F Tabel
[image:35.570.144.407.466.651.2]24
(a = 0.05) sebesar 4.75 yang berarti penggunaan sumber nitrogen yang
berbeda memberikan efek yang signifikan terhadap log total sel yang
dihasilkan. Lebih tingginya nilai log total sel yang dihasilkan pada media
dengan sumber nitrogen urea daripada ekstrak kharnir dikarenakan pada awal
fermentasi sampai dengan jam ke-6 selama fermentasi pada media dengan
sumber nitrogen ekstrak khamir terjadi p e n m a n nilai pH yang sangat tajam
yaitu 1.2 - 1.43, sedangkan pada urea terjadi penurunan pH berkisar antara
0.19 - 0.43. Pada media dengan sumber nitrogen ekstrak khamir nilai pH
terendah berkisar antara 5.75 - 5.84, sedangkan pada urea nilai pH terendah
berkisar antara 6.67 - 6.81. Besarnya penurunan pH dan rendahnya nilai pH
yang dihasilkan pada jam ke-6 pada ekstrak khamir menyebabkan
pertumbuhan kultur menjadi terhambat. Namun demikian nilai pH ini tidak
sampai menghentikan pertumbuhan kultur B.t.i. karena nilai pH ini masih
dalam batas toleransi nilai pH minimum untuk pertumbuhan B.t.i. yaitu
5.6 - 5.8 (Vandekar dan Dulmage, 1982).
Laju pertumbuhan kultur B.t.i. tercepat terjadi pada kisaran jam ke-6
hingga jam ke-9. Laju pertumbuhan B.t.i.. secara lengkap dapat dilihat pada
Lampiran 2. Jika dibandingkan antara sumber karbon air kelapa 100 persen
dengan air kelapa 70.5 persen, pada kisaran jam ke-6 atau jam ke-9 air kelapa
70.5 persen menghasilkan laju pertumbuhan yang lebih tinggi daripada air
kelapa 100 persen. Hal ini disebabkan pada air kelapa 100 persen terdapat
kandungan gula yang lebih banyak daripada air kelapa 70.5 persen, sehingga
setelah terjadi fermentasi air kelapa 100 persen menghasilkan asam yang
25
pH secara tajam ini menyebabkan terhambatnya pertumbuhan kultur sehingga
laju pertumbuhan menjadi lebib lambat.
Demikian pula halnya dengan sumber nitrogen, pada kisaran jam
ke-6 atau jam ke-9 sumber nitrogen urea menghasilkan laju pertumbuhan
yang lebih tinggi daripada sumber nitrogen ekstrak khamir. Cepatnya laju
pertumbuhan yang terjadi pada jam ke-6 atau terutama jam ke-9 dikarenakan
pada kisaran waktu ini kadar gula pada media mulai habis sedangkan kultur
masih menggunakan sumber nitrogen dalam proses metabolismenya.
Penggunaan sumber nitrogen oleh kultur menyebabkan terbentuknya zat yang
bersifat alkali. Sedikitnya gula menyebabkan asam yang dihasilkan tidak
dapat menetralkan semua basa (zat yang bersifat alkali) yang terbentuk
sehingga menyebabkan pH meningkat kembali menuju nilai pH yang normal
untuk pertumbuhan E3.t.i. yaitu pada nilai pH mendekati 8.0 dimana pada nilai
pH ini kultur mulai mengalami pertumbuhan yang stabil (fase stasioner)
(Vandekar dan Dulmage, 1982). Namun demikian pada penelitian ini kultur
sudah mengala~lli fase stasioner walaupun nilai pH belum mencapai 8.0. Hal
ini keinungkinan disebabkan karena pada media sumber karbon sudah mulai
sedikit sehingga kultur sudah mulai kekurangan sumber makanan untuk
pertumbuhannya dan pada fase ini biasanya kultur mulai memakan sel-sel
yang lisis sehingga dikatakan laju pertumbuhan sama dengan laju kematian.
Pada media dengan sumber nitrogen ekstrak khamir, sumber karbon
26
sedangkan pada air kelapa 70.5 persen menghasilkan nilai pH terendah pada
jam ke-6. Hal ini dapat disebabkan karena pada air kelapa 100 persen
terdapat kandungan gula yang lebih banyak daripada air kelapa 70.5 persen
sehingga penggunaan sumber karbon (gula) untuk proses fermentasi menjadi
lebih lama dan semakin banyak gula yang dikonsumsi oleh B.t.i. maka
semakin banyak jumlah asam yang dihasilkan. Penurunan PI-I terbesar terjad
pada air kelapa 100 persen dengan sumber nitrogen ekstrak khamir 1.0 persen
yaitu 1.47. Hal ini disebabkan karena kadar nitrogen yang ada dalam media
yang bersumber ekstrak khamir 1.0 persen lebih kecil daripada media yang
bersumber nitrogen ekstrak khamir 1.5 dan 2.0 persen sehingga basa yang
dihasilkan dari proses metabolisme tidak mampu menetralkan seinua asam
yang dihasilkan dari proses fermentasi gula oleh kultur B.t.i.
Untuk media dengan sumber nitrogen urea, baik sumber karbon air
kelapa 100 persen maupun sumber air kelapa 70.5 persen menghasilkan nilai
pH terendah pada jam ke-6 kecuali pada media dengan sumber air kelapa 100
persen dan urea 1.5 persen yang menghasilkan nilai pH terendah pada jam ke-
9. Penumnan pH terjadi karena pada jam ke-0 hingga jam ke-6 atau jam ke-9
yaitu pada fase eksponensial, B.t.i. menggunakan air kelapa (gula) sebagai
sumber makanannya sehingga menghasilkan asam asetat serta asan~ piruvat
yang menyebabkan nilai pH kultur m e n m . Setelah jam ke-6 atau jam ke-9
nilai pH kembali meningkat karena pada kisaran jam ke-6 hingga jam ke-9
sumber karbon mulai meningkat sedangkan B.t.i. masih menggunakan
sumber nitrogen dalam proses metabolismenya dan menghasilkan zat alkali
27
dihasilkan sedikit sehingga tidak dapat menetralkan semua basa yang
terbentuk.
Pada dasarnya penurunan pH selaina proses fermentasi B.t.i.
tergantung pada konsentrasi sumber nitrogen yang digunakan (Sukmadi et.
al., 1997). Keadaan ini terlihat jelas pada Gambar 3 dan Lampiran 3 bahwa
penurunan pH pada media sumber nitrogen yang konsentrasinya lebih kecil
menghasilkan nilai penurunan pH yang lebih besar daripada sumber nitrogen
yang konsentrasinya lebih besar. Hal ini disebabkan karena pada
metabolisme sumber nitrogen yang konsentrasinya lebih kecil akan dihasilkan
zat alkali yang lebih sedikit daripada sumber nitrogen yang konsentrasinya
lebih banyak. Semakin banyak zat alkali yang dihasilkan dari proses
metabolisme maka semakin banyak asam yang dapat dinetralkan sehingga
penurunan pH semakin kecil.
D. PEMBENTUKAN SPORA
Proses pembentukan spora pada fermentasi B.t.i. dengan media air
kelapa dimulai pada jam ke-9 atau jam ke-12 yaitu pada saat fase log mulai
berakhir dengan jumlah spora hidup pada akhir fermentasi paling banyak
dihasilkan pada media dengan sumber karbon air kelapa 70.5 persen dan
sumber nitrogen ekstrak khamir 2.0 persen yaitu dengan jumlah log VSC
i
w m (Jam ~ e )! I - - C E ~ I R l . O ) b - - C E M R l . S % +EKWVRRZ.Wb
1 --0--UREA$.% +UREA2.(Pb
1
[image:40.559.136.388.83.304.2]i
Gambar 6. Grafik hubungan antara waktu dengan nilai pH untuk
29
Pada dasamya pembentukan spora ini mulai terlihat nyata pada saat fase log
mulai berakhir yaitu pad* saat dimulainya fase stasioner (Sukmadi et. al.,
1997). Pembentukan spora secara cepat tejadi pada jam ke-12 hingga jam
ke-30, setelah itu pembentukan spora muiai mengalami perlambatan hingga
jam ke-48. Hal ini disebabkan karena seteiah sumber karbon difermentasi
.
menjah asam-asam yaitu asam laictat, asam piruvat, asam asetat dan asetain
maka asam asetat yang dihasiikan digunaitan 1.agi untuk mensintesis poli-beta-
hidroksibutirat (PHB) untuk proses spomlasi (Benoit et. al., 1990).
Cepat atau lambatnya pembentukan spora tergantung pada kondisi
lingkungan kultur. Biasanya spora akan tumbuh pada kondisi lingkungan di
sekitar sel yang kurang sesuai bagi sel. Hal ini dapat disebabkan karena
kultur yang pH yang ekstrim, suhu yang ekstrim dan kurangnya suplai
inakanan bagi sel, atau kemungkinan lainnya yang dapat menyebabkan
kondisi lingkungan tidak sesuai bagi sel sehingga sel membentuk spora.
Sedangkan proses cepatnya pelepasan spora dari sel (lisis) tergantung pada
konsentrasi gula yang digunakan yaitu semakin kecil konsentrasi gula yang
digunakan maka seinakin cepat iejadi iisis sei yang meiepas spora dan kristai
(Suionadi el. al., 1996). Demiiuan pula halnya dengan keberhasilan proses
sporuiasi dan pembentukan iaistal, tergantung pada keseimbangan antara
konsentrasi sumber karbon clan konsentrasi sumber nitrogen. Semahn rendah
konsentrasi sumber nitrogen maka sporulasi dan pembentukan kristal tejadi
lebih cepat, namun jumlah spora dan kristal yang dihasilkan lebih sedikit
sedangkan jika konsentrasi sumber nitrogen terlalu tinggi akan mengganggu
30
demikian pada peneiitian ini konsentrasi nitrogen rertinggi tidak sampai
mempengaruhi proses sporuiasi seperti terlihat dari uji analisa ragam yang
memperlihatkan bahwa konsentrasi sumber nitrogen tidak memberikan efek
yang signifikan terhadap nilai log spora hidup yang dihasilkan yaitu dengan
nilai F hitung sebesar 0.279 dan nilai F Tabel
( a
= 0.05) sebesar 3.24.Pembentukan spora selama proses fermentasi berlangsung seperti
terlihat pada Gambar 4 dan 5 menunjukkan bahwa pada dasamya baik pada
media dengan sumber nitrogen urea atau ekstrak khamir maupun pada
sumber karbon air kelapa 100 persen atau 70.5 persen didapatkan
pertumbuhan spora yang tidak jauh befbeda. Namun dari uji analisa ragam
terlihat bahwa sumbe: karbon
dan
interaksi antara sumber karbon denganjenis sumber nitrogen memberikan efek yang signifikan terhadap jurnlah
spora hidup yang dihasilkan. Untuk sumber karbon dihasilkan niiai F hitung
dan F Tabel ( a = 0.05) masing-masing sebesar 8.349 dan 4.75, sedangkan
untuk interaksi antara sumher karbon dan jenis sumber nitrogen menghasiikan
nilai F hitung dan F Tabel (a = 0.05) masing-masing sebesar 4.852 dan 4.75.
Seteiah diiakukan uji Duncan's, hanya pada interaksi antara sumber karbon
70.5 persen dengan sumber nitrogen ekstrak khamir yang signifikan terhadap
interaksi antara sumber karbon air kelapa 100 persen dengan sumber nitrogen
W W(Jan
a)
11-PXlWh EKl WA t M l W A EK1.596 --CPXlW EK209L
I
[image:43.564.135.393.109.324.2]I - O - - ~ ~ ~ ~ A E K ~ . W - - ( ~ . - - M ~ ~ ~ ~ E K ~ . ~ + I U ( I O ~ , E K Z
Gambar 7. Grafik hubungan antara waktu dengan log VSC untuk
GRAnKHLIBUW;nNANTPRA
W ~ L C G V S C (AIR W AIOSO/)
WPKN (Jan Ke)
/
+ E W R l . W - C E W R I . %i- 4 L R A ' . C % -O--m1.5?6
GRAnK H U B U W ANTAR4
WAKN D E W LCG VSC
(AIR KELAPA 100%)
0 3 6 9 12151821242730333639424548
w m (Jan I(*)
&E. I J X U ( R ~ . ( P ~ -C E . W R I . S
% &E. W R Z . ~
[image:44.567.141.386.103.568.2]- d
Gambar 8. Grafik hubungan antara waktu dengan log VSC untuk
i3erat kering akhir (pada jam ke-48) yang diperoleh teriihat pada
Tabel 6. Dari Tabel tersebui dapat terlihat bahwa berat kering yang
dihasilkan berkisar antara 2.791 - 6.362 gl1 cairan kuitur. Hasil ini~tidak jauh
berbeda dengan penelitian yang telah dilakukan oleh Sikdar et. uZ. (1991).
Sikdar et. al. (1991) meneliti pengaruh mineral terhadap produksi
6 - endotoksin oleh i3.t.i. dan mendapatkan berat kering sel yang berkisar
antara 0.8 sampai 4.0 g/l cairan kultur.
Dari Tabel 6 terlihat bahwa penggunaan sumber karbon 70.5 persen
dengan sumber nitrogen urea 1.5 persen memberikan hasii berat kering
terbesar yaiiu 6.362 gil cairan kultur. Berdasafkan hasil analisa ragam,
sumber kaibon dan jenis sumber nitrogen memberikan efek yang sangat
signifikan terhadap nilai log berat kering yang dihasilkan ( a = 0.05).
Demikian pula interaksi antara sumber karbon dengan jenis surnber nitrogen,
untuk a = 0.05 me~nberikan efek yang signifikan terhadap nilai log berat
kering yang dihasilkan. Sedangkan konsentrasi sumber nitrogen dan interaksi
antara sumber karbon dengan konsentrasi sumber nitrogen tidak memberikan
efek yang signifikan terhadap nilai berat kering yang dihasil~an ( a = 0.05).
F. BAYA BAHAN BAKU (SUMBER NITROGEN)
Media air keiapa 70.5 persen dengan sumber nitrogen urea 1.0
persen ( b h ) merupakan media yang sesuai untuk pertumbuhan B.t.i. Hal ini
terlihat dengan besamya nilai berat kering yang dihasilkan. Dalam penelitian
ekstrak khamir, karena selain memberikan hasil yang lebih baik juga
membutuhkan biaya yang lebih murah. Perincian harga tiap bahan yarlg
digunakan terlihat dalarn Tabel 7.
Tabel 7. Daftar barga sumber karbon dan sumber nitrogen
Bahan I Harga
1
Air kelapa I Rp. 2000 I20 1
I
Air destilata
1
Rp. 300ilEkstrak khamir
I
Rp. 800 0001500 gI
I
I
Tabel 6. Berat kering biomassa (sel-spora-kristal) untuk berbagai konsentrasi
-e n .
Urea
1
Rp. 1500 / k gI
Surnber1
Sumbe. Nitmgen
Berat kering (pa cairan knltur) Rata-rata 3.450 2.966 2.791 4.168 4.834 3.169 Ulangan 1 Illangan
II
4.041
I
3.3212.678 4.387 4.566 3.547 karbon - I
i
Air kelapa 100 persen1
Ekstrak khamir 1.0 persen
Ekstrak kharnir 1.51 2.612
I
persen
Ekstrak khamir 2.0
'
2.904ersen
Urea 1.0 persen 3.950 Urea 1.5 persen
1
5.102I
Urea 2.0 persen/
2.792 I ji
i
i
iEkstrak khamir 1.0 1 4.179 4.201
1
4.191persen
i
Ipersen
I
Ekstrak khamir 2.0
1
4.424 3.983 4.203persen I I I
Urea 1.0 persen
/
6.4161
6.015 6.215!
1
Urea 1.5 persen1
6.735/
5.9881
6.362 [image:46.564.111.509.191.507.2] [image:46.564.145.467.549.661.2]35
Untuk membuat i liter media dibutuhkan urea sebanyak 7.5 g, air
kelapa 0.705 I, dan air destilata 0.295 1, maka dibutuhkan biaya sebesar Rp.
81.8385,- atau sekitar Rp. loo,-. Sedangkan jika menggunakan sumber
nitrogen ekstrak khamir, dibutuhkan 7.5 g ekstrak kharnir, air kelapa 0.705 1,
dan air destilata 0.295 1; maka dibutahkan biaya sebesar Rp. 12 000,-. Jadi
terlihat jelas bahwa akan tejadi penghematan biaya yang sangat besar yaitu
sekitar Rp. 11 900,- jika rnenggunakan sumber nitrogen urea untuk fermentasi
B.t.i., dan keuntungan ini akan menjadi lebih besar lagi jika diperhltungkan
perbedaan berat produk akhir yang didapatkan per liter rneda.
G. PENGUJLAN AKTNLTAS PRODUK PRIMER TERHADAP
MORTALITAS LARVA
Pengujian terhadap aktivitas produk primer terhadap iarva Culex sp
dilakukan dengan memasukkan masing-masing 25 ekor larva Culex sp ke
dalam sepuluh tingkat konsentrasi untuk tiap perlakuan. Tingkat mo~ialitas
larva Cu1e.x sp untuk tiap perlakuan ini terlihat pada Tabel 8.
Dari Tabel terlihat bahwa air kelapa I00 persen dengan sumber
nitrogen ekstrak khamir 1.5 persen memiliki daya bunuh yang paling bark
karena pada konsentrasi i0-" masih dapat membunuh larva Culex sp lebih
dari 10 persen. Bardasarkan Tabel 8 tersebut maka dapat dihitung LCso-nya
dengan menggunakan program Quant seperti teriihat pada Tabel 9.
Dari Tabel 9 terlihat bahwa produk yang dihasilkan dengan surnber
karbon air kelapa 100 persen dan surnber nitrogen ekstrak khamir 1.5 persen
merupakan produk yang paling baik karena rnemiliki nilai LC50 yang paling
sebanyak 50 persen dari populasi yang ada diperlukan produk sebanyak
Tabel 8. Tingkat mortalitas larva Culex sp untuk berbagai konsentrasi sumber karbon dan sumber nitrogen.
I
Mortalitas (%) pada konsentrasi -- II
SumberHitmgenI
krrbon
1
10.'i
10"1
10"j
10"/
lo-=i
lo4/
1
loa/
1 0 - ~/
lo-'0IE.khamirl.Openen 1 9 6 1 9 6 1 9 2 1 5 2 1 2 8 1 2 4
/
161
8/
8I
8L h \ a m i i i . 5 p e r s e o
I
I 0 9 I 0 9 96 96 76 52:
:
32 32 20I
l
l
i
l
l
l
l
i
I
I
I
Air kelapa
I
E khamirZ.0 p e n n1
100I
100I
100I
I 361
20/
161
12/
81
4/
100 persen
1
e
Urea 1.0 persenl
1
Urea 1.5 persen I O O ( 8 4 1 6 4 1 2 4 1 1 2I
I
I . I . - /‘ / I
8 4I
1 4/
OI
i
I
Urea 2.0 persen ~ 9 6 1 8 8 ~ 8 0 1 1 6 ~ 1 6 1 1 2 ] 81
81
81
41
1
{
i
I I I I I/
E. khamir 1.5persen/
100/
100/
100/
96/
64/
48/
32/
16/
4/
01
Air kelapa
/
E. khamirZ.0 persen1
100 100/
96/
441
28/
161
81
8/
4/
41
70.5 persen
/
Urea i . 0 pervert / i 0 0 / 9 6 / 6 0 / 2 0 / 1 2 1 S/
S/
8 8/
4I I i
j
Urea 1.5 persen i 1 0 0 i 8 4 i j ~ i 3 6 1 2 8i
8i
4j
4 4j
0i
Produk komersinl Vectobac j - j - -
1
- - ) 1 0 0 / 9 0 / 6 0 / 4 0 1 10Jika dibandingkan antara air kelapa 100 persen dengan 70.5 persen
terlihat bahwa air kelapa 100 persen menghasilkan kualitas produk yang lebih
baik karena menghasilkan nilai LCso yang lebih kecil. Jika dibandingkan
antara sumber nitrogen ekstrak khamir dengan urea, maka produk dengan
sumber nitrogen ekstrak khamir mempunyai kualitas yang lebih baik karena
mempunyai nilai LC50 yang lebih kecil, kecuali pada urea 2.0 persen. Hal ini
menunjukkan kemungkinan komposisi sumber nitrogen mempengaruhi
[image:48.559.88.534.161.453.2]Dan Tabel 9 terlihat tidak adanya hubungan antara berat kering
biomassa atau jumlah spora terhadap nilai LC5o. Ini berarti berat kering
biomassa atau jumlah spora yang dihasilkan tidak mempengaruhi tingkat
mortalitas larva Culex sp oleh produk yang dihasilkan
Air kelapa
100 persen
Tabel 9. Berat kering biomassa (sel-spora-kristal) untuk berbagai konsentrasi sumber karbon dan sumber nitrogen.
Air kelapa
70.5 persen karbon
/
E. kharnir 1.5 persenI
E. khamir 2.0 persen
Surnber Nitrogen
E. khamir 1.0 persen
/
Urea 1.5 persenI
Urea 2.0 persen
!
1
E 1&amir 1.0 persenE. kharnir 1.5 persen
i
E. khamir 2.0 persenUrea 1.0 persen
I
Berat kering
(gn kultur) 3.450
/
Urea 1.5 persenI
I
I
/
Urea 2.0 persen1
Log VSC
(sporalml) 10.7340
Lcso ( p g L 94.406 1
[image:49.559.75.543.199.485.2]V. KESIMPULAN DAN SARAN
A. KESIMPULAN
Penelitian pendahuluan memberikan hasil bahwa kadar protein dari
air kelapa yang digunakan masih relatif besar yaitu 0.244 dan memiliki
kadar gula sebesar 1.77 persen. Dengan kadar gula tersebut, maka untuk
mencapai kadar gula optimum bagi pertumbuhan B.t.i. (sebesar 1.25 persen)
air kelapa diencerkan hingga 70.5 persen.
Penggunaan air kelapa 70.5 persen menghasilkan nilai log total sel
yang lebih tinggi daripada sumber karbon air kelapa 100 persen. Berdasarkan
uji ragam, konsentrasi surnber karbon memberikan efek yang signifikan
terhadap nilai log total sel yang dihasilkan.
Pada penggunaan air kelapa 70.5 persen dengan urea sebagai surnber
nitrogen menghasilkan log total sel yang lebih tinggi daripada air kelapa
70.5 persen dengan ekstrak khamir sebagai sumber nitrogen. Berdasarkan uji
analisa ragam, penggunaan sumber nitrogen yang berbeda memberikan efek
yang signifikan terhadap log total sel yang dihasilkan.
.
.
Laju pertumbuhan tercepat terjadi pada kisaran jam ke-6 hingga jam
ke-9, dimana air kelapa 70.5 persen sebagai sumber karbon menghasilkan laju
pertumbuhan yang lebih cepat daripada air kelapa 100 persen. Demikian pula
dengan urea sebagai sunber nitrogen menghasilkan laju pertumbuhan yang
lebih cepat daripada ekstrak khainir sebagai sumber nitrogen.
Penumnan nilai pH terjadi mulai dari jam ke-0 hingga pada kisaran
39
banyak gula yang dikandung di dalam cairan kultur (media), semakin besar
rentang penurunan nilai pH yang dihasilkan. Selain itu, konsentrasi nitrogen
juga mempengamhi penurunan nilai pH cairan kultur.
Pembentukan spora pada fermentasi B.t.i. dimulai pada kisaran jam
ke-9 hingga jam ke-12 dan pembentukan spora secara cepat tejadi pada jamn
ke-12 hingga jam ke-30, kemudian mengalami perlambatan hingga jam
ke-48. Berdasarkan uji analisa ragam, konsentrasi sumber nitrogen tidak
memberikan efek yang signifikan terhadap nilai log jumlah spora hidup yang
dihasilkan. Tetapi sumber karbon dan interaksi antara sumber karbon
dengan jenis sumber nitrogen memberikan efek yang signifikan terhadap log
jumlah spora hidup yang dihasilkan.
Berat kering yang dihasilkan pada fermentasi b.t.i. berkisar antara
2.791 sampai 6.362 gll cairan kultur. Sumber karbon dan jenis sumber
nitrogen
.
serta interaksi antara sumber karbon dengan jenis sumber nitrogen menghasilkan efek yang signifikan terhadap nilai berat kering yangdihasilkan. Sedangkan konsentrasi sumber nitrogen dan interaksi sumber
karbon dengan konsentrasi sumber nitrogen tidak memberikan efek yang
signifikan terhadap nilai berat kering yang dihasilkan.
Produk dengan sumber nitrogen ekstrak khamir mempunyai daya
bunuh yang lebih besar daripada sumber nitrogen urea. Nilai berat kering
biomassa atau jumlah spora yang dihasilkan tidak mnempengaruhi tingkat
B. SARAN
Dari hasil penelitian yang telah dilakukan maka perlu dilakukan :
(1) penelitian lebih lanjut mengenai konsentrasi air kelapa yang optimum
untuk pertumbuhan B.t.i., (2) penelitian lebih lanjut mengenai kombinasi
sumber nitrogen yang sesuai untuk sumber karbon air kelapa, (3) pengaruh
konsentrasi nitrogen dan kandungan vitamin, asam amino dalaln media
terhadap kualitas produk yang dihasilkan, clan (4) penelitian terhadap
DAFTAR PUSTAKA
Apriyantono, A. 1989. Analisis Pangan. Pusat Antar Universitas Pangan dan Gizi-PB, Bogor.
Alaban, C.A. 1962. Studies on Optimum Conditions for Nata De Coco Bacterium or Nata Formation In Coconut Water. Philipine Agric. 96(2j :
490 - 5i5.
Badan Pusat Statistik. 1991. Statistik Perkebunan. Badan Pusat Statistik, Jakarta.
Benoit, T.G. Wiison, dan C.L. Baugh. 1990. Fermentation During Growth and Sporulation of Bacillus thuringiensis HD-I. Lett. Appl. Microbial. (10) :
15 - 18. Di dalam Sukmadi, B., Haryanto, B., dan W n a , S.H. 1996. Pengaruh Konsentrasi Dekstrosa Pada Produksi Bahan Aktif Bioinsektisida Bacilius thuringiensis subsp. aizawai. Majaiah BPP- Teknologi No. LXXII : 17 - 23.
Child. 1962. Coconuts. Longrnans Green and. Co., London.
Direktorat Gizi Departemen Kesehatan R.I. 1988. Daftar Komposisi Bahan Makanan. Bharata Karya Aksara, Jakarta.
Duimage, H.T. l98i. insecticidal Activity of Isolates of Bacilr'us tiiuringiensis and T'heir Potential for Pest Control, pp. 193-22 1. Di dalam H.D. Bueges, ed. Microbial Control of Pest and Plant Diseases. Acad. Press, New York.
Dulmage, H.T. dan R.A. Rhodes. 1971. Production of Pathogens in Artificial Media, pp. 507-540. Di dalam H.D. Burges dan N.W. Eiussey, eds. Microbial Controi of insect and Mites. Acad. Press, New York.
Feitelson, J.S., J. Fayne, dan L. Kim. 1992. Buciir'us tiiuringiensis : insects and Beyond Biotechnol. 10 : 271-275.
Freemond, Y. dan R. Zilier. 1966. The Coconut Palm. International Potash Institute, Berne.
Gill, S.S., E.A. Cowles, dan P.V. Pietrantonio. 1992. The Mode of Action of Bacillus tizuringiensis Endotoxins. Annu. Rev. Entomol. 37 : 615-636.
Hofte, H. dan H.R. Whiteley. 1989. Insecticidal Crystal Proteins of Bacillus thuringiensis Iviicrobial. Rev. 53(2) : 242-255.
Johnson, T.B., A.C. Slaney, W.P. Donovan, dan M.J. Rupar. 1993. Insecticidal Activity of EG4961, a Novel Strain of Bacillus tizuringhnsis Toxic to Larvae and Adults of Southern Corn Rootworm (Coleoptera :
Chrysomelidae) and Colorado Potato Beetie (Coieoptera : Chrysomelidae). J. Econ. Entomol. 86(2) : 330-333.
Ketaren, S. 1978. Daya Guna Hasil Kelapa. Dept. Teknologi hasil Pertanian, Fatemeta-IPB, Bogor.
Khachatourians, G.G. 1989. Production and Use of Biological Pest Controi Agents. Tibtech, 5 : 120-124.
Kimia Pestisida. 1993. Pestisida Untuk Pertanian dan Kehutanan. Departemen Pertanian, Jakarta.
Krieg, A. dan H.G. Miltenburger. 1984. Bioinsecticides Bacillus thuringiensis. Advances in Biotechnoiogical Procesess. 3:273-290.
Lowry, O.H., N.J. Rosenbrough, A.L. Farm, dan R.J. Randaii. 1951. Protein Measurement With Folin Phenol Reagent. J. Biochemistry. 193,265.
Margalit, J. dan D. Dean. 1985. The Story of Bacillus tizuringiensis israeleiwis. Di dalam J. Am. Mosquitos Control Assessment, 1 : 1-7.
Mummigatti, S.G. dan A.N. Raghunathan. 1990. Influence of Media Composition on The Production of 6-endotoxin by Bacillus thuringiensis var. tlzuringiensis. J. Inveriebr. Pathoi. 5 5 : 147-1 5 1.
Philip, F.E., J.S. Cory, 1vl.J. Baiiey, dan S. Higgs. i993. Bacillus tizuringiensw, Ar, Envirormental Biopesiicide : Tiieon and Practice, pp. 148. Jo'nn Wiley and Sons, New York.
Quinlan, R.J. dan S.G. Lisansky. 1985. Microbial Insecticides, pp. 233-254.
2
daiarn
H. Dellweg, ed. Biotechnoiogy voi. 3. Veriag Chemis, Weinheim.Rupar, M.J., W.P. Donovan, R.G. Groat, A.C. Sianey, J.W. Mattison, T.B. Johnson, J.F. Charles, V.C. Dumanoir, dan H. de Barjac. 1991. Two Novel Strains of Bacillus tlzuringiensis Toxic to Coleopterans. App. Environ. Microbial. 57(11 j : 3337-3344.
Shieh, T.R. 1994. Indification and Clasification of Bacilius tizuringiensis. QI
Sikdar, D.P., M.K. IvIajumdar, dan S.K. Majumdar. 1993. Optimization of Process for Production of Delta Endotoxin by Bacillus tizuringierzsis var. isruelensis in a Five Litre Fermentor. Biochemical Archive:. 9 : 119-123.
Subrahmanyan, V. dan Swaminathan, D.