ABSTRACT
DISTRIBUTION OF HEAVY METAL Cd AND Ni IN SEDIMENT OF PANJANG PORT BY ATOMIC ABSORPTION SPECTROPHOTOMETER
(SSA) METHOD
By
Rini Handayani Rotua P
Distribution of heavy metals Cd and Ni in sediment of Panjang port Bandar Lampung was conducted . Metals concentration of Cd and Ni was determined by using
spectrophotometer atomic absorption. validation method was performed by limit of detection, linearity, accuracy, and precision. The result showed that the concentration of Cd ranged from 152,4434 ± 0,2089 ppm to 153,2679 ± 0,1152 ppm, indicating above the quality standards set of the National Sediment Quality Survey USEPA (0,6 - 2,49 ppm). Heavy metal concentration of Ni ranged from 427,4125 ± 0,1020 ppm to 443,7875 ± 1,5444 ppm. The result showed that the concentration of Ni have exceeded the quality standard of USEPA (23,77 – 80,07 ppm). Validation of the method on determining the level of Cd and Ni metal in the sediments showed the high precision performing the relative standard deviation values (RSD) < 5%, accuracy in ranging 85,2153 - 98,7500 %, limit of detection for heavy metal Cd and Ni of 0,00047 ppm and 0,13258 ppm and corelation coefisient value for Cd and Ni metal of 0,99887 and 0,99964, respectively.
ABSTRAK
DISTRIBUSI LOGAM BERAT Cd DAN Ni PADA SEDIMEN DI SEKITAR PERAIRAN PELABUHAN PANJANG DENGAN METODE
SPEKTROFOTOMETER SERAPAN ATOM (SSA)
Oleh
Rini Handayani Rotua P
Penelitian tentang distribusi logam berat Cd dan Ni pada sedimen telah dilakukan di sekitar perairan Pelabuhan Panjang Bandar Lampung. Konsentrasi logam Cd dan Ni ditentukan menggunakan spektrofotometer serapan atom dengan empat parameter validasi metode yaitu linieritas, limit deteksi, presisi, dan akurasi. Hasil penelitian menunjukkan konsentrasi logam berat Cd berada pada rentang (152,4434 ± 0,2089) ppm sampai (153,2679 ± 0,1152) ppm, berada di atas baku mutu yang ditetapkan oleh National Sediment Quality Survey USEPA. Konsentrasi logam berat Ni berada pada rentang (427,4125 ± 0,1020) ppm sampai (443,7875 ± 1,5444) ppm, berdasarkan National Sediment Quality Survey USEPA, baku mutu konsentrasi logam Ni yaitu 23,77- 80,07 ppm, hasil analisis menunjukan logam Ni telah melebihi baku mutu. Validasi metode pada penentuan kadar Cd dan Ni dalam sedimen menunjukan presisi dengan nilai relatif standar deviasi (RSD) < 5 %, akurasi pada rentang 85,2153 - 98,7500 %, limit deteksi untuk masing-masing logam Cd dan Ni adalah 0,00047 ppm dan 0,13258 ppm dan nilai koefisien korelasi untuk logam Cd dan Ni adalah 0,99887 dan 0,99964.
DISTRIBUSI LOGAM BERAT Cd DAN Ni PADA SEDIMEN DI SEKITAR PERAIRAN PELABUHAN PANJANG DENGAN METODE
SPEKTROFOTOMETER SERAPAN ATOM (SSA)
(Skripsi)
Oleh
RINI HANDAYANI ROTUA P
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
DAFTAR GAMBAR
Gambar Halaman
1. Pelabuhan Panjang ... ... 10
2. Spektrofotometer Serapan Atom ... ...25
3. Electrodless Discharge lamp ... ...26
4. Sumber Atomisasi .... ... ...27
5. Skema Instrumentasi Spektrofotometer Serapan Atom . ...29
6. Lokasi Pengambilan sampel...36
7. Perairan Pelabuhan Panjang... 42
8. Titik Koordinat Garis Lintang dan Garis Bujur titik pengambilan sampel.... 44
9. Parameter Temperatur Air PelabuhanPanjang……….46
10. Parameter pH Air Pelabuhan Panjang……….……….. 48
11. Kurva Regresi larutan standar Cd ………...58
i
A. Gambaran Umum Pesisir Teluk Lampung ………. 5
1. Letak Geografis ……… 5
2. Kondisi Wilayah ………. 6
3. Kondisi Fisik dan Kimia Perairan ……….. 7
ii
2. Toksisitas Nikel ……….………….. 21
G. Logam Cadmium……… 22
1. Sumber Pencemaran Logam Cd……….………… 23
2. Toksisitas Logam Cd………..………… 23
3. Sifat Fisik dan kimia logam Cd……….…………. 24
H. Spektrofotometer Serapan Atom ... ... … 25
1. Prinsip Dasar ……….……….. 25
2. Instrumentasi Spektrofotometer Serapan Atom ……….. 26
3. Analisis Kuantitatif ……… ……… 30
a. Persiapan Pengambilan Sampel... 35
b. Titik Pengambilan Sampel ... 36
3. Preparasi Sampel... 37
a. Preparasi Sampel Untuk Menentukan Logam Cd... ... 37
b. Preparasi Sampel Untuk Menentukan Logam Ni... 37
4. Penentuan Konsentrasi Cd dan Ni pada Sedimen……… 38
IV. HASIL PENGAMATAN DAN PEMBAHASAN ... 41
A. Gambaran Umum Pelabuhan Panjang ………... 41
B. Pengambilan Sampel ... 43
iii
1. Parameter Temperatur PerairanPelabuhan Panjang ... 46
2. Parameter pH Perairan Pelabuhan Panjang ... 47
D. Distribusi Logam Berat Cd dan Ni di Perairan Pelabuhan Panjang... 49
1. Distribusi Logam Berat Cd pada Sedimen di Pelabuhan Panjang….. 49
2. Distribusi Logam Berat Ni pada Sedimen di Pelabuhan Panjang…… 52
E. Validasi Metode ... ……… 56
1. Limit Deteksi………..………… 55
2. Presisi(Ketelitian)………. 57
3. Linieritas ...……….. 58
4. Akurasi ...………. 60
V. KESIMPULAN ………. 61 DAFTAR PUSTAKA
DAFTAR TABEL
Tabel Halaman
1. Kualitas air Teluk Lampung ... 8
2. Baku mutu kandungan logam berat dalam sedimen ... ... 17
3. Sifat Fisik Logam Cd ... ... 24
4. Kondisi visual sampel sedimen... 45
5. Konsentrasi Rata-rata Logam Cd pada Sedimen……… …… 50
6. konsentrasi Rata- rata logam berat Ni pada sedimen………... 53
7. Nilai SD dan RSD Hasil Analisis Logam Cd dan Ni pada Sedimen……… 57
MOTO
Percayalah kepada Tuhan dengan segenap
hatimu, dan janganlah bersandar kepada
pengertianmu sendiri
(Amsal 3 : 5)
"segala perkara dapat kutanggung di dalam
Dia yang memberi kekuatan kepadaku "
(filipi 4 : 13 )
Kuatkan dan teguhkanlah hatimu, janganlah takut
dan jangan gemetar karena mereKa, sebab Tuhan ,
Allah mu Dialah yang berjalan menyertai engkau ;
Dia tidak akan membiarkan engkau dan tidak akan
meninggalkan engkau.
(Ulangan 31 : 6)
"
Nikmati kesulitannya, nikmati beratnya, nikmati Proses yang Tuhan Kasih karena dia menuntun kita bukan untuk kegagalan
Waktu Tuhan Tidak pernah terlalu Cepat dan terlalu lambat, melainkan selalu Tepat
PERSEMBAHAN
Kupersembahkan karya kecil ini sebagai wujud tanda cinta,
kasih, bakti, dan tanggung jawabku
Kepada
Kedua orang tua ku Bapak Pardamean Panjaitan dan Ibu Sustra
Dewi Ananda Sitinjak,
Adik-adikku tersayang Feresia Panjaitan, dan Danil Andreas
Panjaitan,
Segenap Keluarga Besar yang selalu mendoakan keberhasilanku,
Sahabat dan teman-temanku yang selalu berbagi kebahagiaan
dan berjuang bersamaku,
Seseorang yang kelak akan mendampingiku
RIWAYAT HIDUP
Penulis dilahirkan di Tanjung Karang pada tanggal 10 Februari 1992, sebagai
anak pertama dari 4 bersaudara, putri dari Bapak Pardamean Panjaitan dan Ibu Sustra Dewi Ananda Sitinjak.
Penulis memulai jenjang pendidikan dari TK Bina Kasih Siak Sri Indrapura,
menyelesaikan pendidikan Sekolah Dasar di SDN 002 Siak pada tahun 2004, Sekolah Menengah Pertama di SMP Negeri 1 Siak pada tahun 2007, dan Sekolah Menengah Atas di SMA Negeri 1 Siak pada tahun 2010. Tahun 2010 Penulis
diterima di Universitas Lampung, Fakultas Matematika dan Ilmu Pengetahuan Alam Jurusan Kimia melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN).
Selama menjadi mahasiswa, penulis pernah menjadi asisten praktikum Kimia
Dasar untuk Fakultas Pertanian Unila pada tahun 2012-2013, asisten praktikum Sains Dasar untuk jurusan Biologi pada tahun 2013-2014, koordinator asisten
praktikum Kimia Dalam Kehidupan untuk jurusan Kimia pada tahun 2013-2014, dan asisten praktikum Kimia Analitik Jurusan Kimia FMIPA Unila pada tahun
sosial masyarakat. Penulis juga aktif di lembaga pers mahasiswa fakultas
“Natural” sebagai Reporter pada tahun 2010 – 2012. Pada tahun 2013 penulis
melakukan Praktek Kerja Lapangan di Laboratorium Kimia Analitik Universitas
SANWACANA
Salam sejahtera,
Puji dan syukur penulis panjatkan kepada Tuhan Yesus Kristus , karena atas
anugrah dan kebaikan-Nya penulis dapat menyelesaikan skripsi ini.
Skripsi dengan judul “Distribusi Logam Berat Cd dan Ni pada Sedimen di Sekitar Perairan Pelabuhan Panjang dengan metode Spektrofotometer Serapan Atom (SSA)” merupakan syarat untuk mencapai gelar Sarjana Sains pada Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung.
Pada kesempatan ini penulis mengucapkan terima kasih dan penghargaan yang
tulus kepada:
1. Bapak Diky Hidayat, M.Sc., selaku Pembimbing Utama yang telah banyak
membimbing penulis dengan sabar, memberikan banyak ilmu
pengetahuan, saran, arahan, dukungan dan motivasi sehingga penulis dapat menyelesaikan skripsi ini.
2. Ibu Rinawati, Ph.D., selaku pembimbing Kedua yang telah membimbing penulis dengan sabar, memberikan banyak ilmu pengetahuan, saran, dan
3. Bapak Dr. Hardoko Insan Qudus, M.S selaku Pembahas yang telah banyak
memberikan banyak arahan, kritik, saran, dan motivasi demi terselesaikannya skripsi ini.
4. Bapak Dr. Rudy T Mangapul Situmeang, M.Sc., selaku Pembimbing Akademik yang telah memberikan bimbingan, motivasi, nasehat dan
dukungan.
5. Bapak Prof. Dr. Suharso, Ph.D selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
6. Bapak Dr. Eng. Suripto Dwi Yuwono, M.T. selaku Ketua Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
7. Mba Iin,mas Udin,dan mba Karlina selaku Laboran di Laboratorium Kimia Analitik dan Instrumentasi yang telah banyak berbagi ilmu dan pengalaman dalam pelaksanaan Penelitian.
8. Mba Nora, Pak Gani, Mba liza, Uni Kidas, Mas Nomo, Pak Man, serta seluruh staf pengajar dan Karyawan Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
9. Keluarga Tercinta, Bapak dan Mamak untuk setiap cinta yang tercurah , perjuangan, jerih payah serta doa yang tidak pernah putus dan perhatian
yang takkan pernah habis demi keberasilan penulis. Kedua adikku Feresia Panjaitan dan Danil Andreas Panjaitan yang selalu mendoakan ku. 10.Opung Rafael (opung E.Manalu ), tante Kiki Maria Sitinjak dan Bapa uda
serta doa tulus yang tiada henti, dan perhatian yang takkan pernah habis
demi keberhasilan penulis.
11.Kedua Adik- adik ku yang selalu menghiburku disaat aku jenuh dan
mendoakan untuk keberhasilan ujian kelulusanku Febi Priskilla Pandegirot, dan adik ku yang kece,usil, dan lucu Michael Marselo
Pandegirot.
12.Keluarga besarku tante Rutiah Sitinjak, Tulang dan Nantulang Claudia, Tante Lena, Bapa uda Kristian Panjaitan, namboru dan Amang Boru Faisal
Manalu dan Opung Rini Panjaitan(S.Panjaitan) atas bantuan, dukungan, nasehat, dan doanya untuk keberhasilan Penulis.
13.Sahabat, sekaligus Patner setia ku dari awal perkuliahan, penelitian serta penulisan skripsi ini Martha Selvina Gultom atas segala kebersamaannya selama ini, dukungan, doa, motivasi serta bantuannya selama ini kepada
Penulis.
14.Patner Penelitan kak.Ignatius Sandy Ellen Prianda dan kak. Delphiana atas kebersamaannya. Lorentius Agung Setyo atas bantuannya dan telah
bersedia dengan tulus menemani saat penelitian.
15.Chyntia Gustianda Patraini yang telah sabar menghadapi kegupekan ku
serta bantuan dan kebersamaanya selama ini.
16.Siti Marfuah( Fuah) Sahabat setia yang selalu menemani ku dan
menghiburku susah, senang, sedih, dan tempat ku berbagi keluh,kesah,dan
17.Spesial thanks to Fransiskus Maruli Pasaribu atas kebersamaan, perhatian,
kesabaran, dukungan, bantuan, doa yang tulus dan semua hal yang telah diberikan tanpa lelah untuk penyelesaian skripsi ini.
18.Teman seperjuangan di Lab. Kimia Anorganik Fisik, Silvana Maya Pratiwi, Sevina Silvi, Widya Afriliani, Fauziyyah , Agung Supriyanto,
Wynda Dwi Anggraini, dan Hapin Afriyani, terimah kasih atas kebersamaanya, keceriaan, canda tawa yang selalu hadir disetiap hari penulis disaat penelitian.
19.Teman-teman se-angkatan 2010, Agung Supriyanto, S.Si., Ariyanti, Chintia Yolanda, S.Si., Hapin Afriyani, S.Si., Hayu Prita Anjani, Kristi
Arina, M. Nurul Fajri, Sifa Kusuma W., Surtini Karlina S., Aditya Putra P., Ely Setiawati, Fajria Faiza, Faradilla Syani, S.Si., Fauziyyah S.Si., Fitri Yani, Hanif Amrulloh S.Si., Indah Aprianti, Juni Zulhijjah, Lailatul
Hasanah, Leni Astuti S.Si., Lolita Napatilova, M. Prasetyo, Purniawati S.Si., Rahmat Kurniawan, S.Si., Sevina Silvi, S.Si., Silvana Maya Pratiwi, Widya Afriliani S.Si., Wynda Dwi S.Si., Yussi Fitria, Desi Meriyanti
S.Si., Desi Sujatana, Funda Elisyia, S.Si., Maria Anggraini, Martha Selvina, Nur Robiah, Putri Heryani, S.Si., Putri Rahmatika, Putri Sari
Dewi, Rani Anggraini, Rina Rachmawati, S.Si., Ruli Prayetno, Sunarmo, Ucep Saifulloh. Terimah Kasih untuk kebersamaan dan keceriaan selama menjalani perkuliahan, tetap semangat dan jangan menyerah, perjuangan
kita masih panjang, sukses selalu untuk kita.
20.Kakak-kakak tingkat 2008-2009, Adik-adik tingkat 2011-2012, atas
21.Kakak, Abang, dan Saudara- saudara ku di POMMIPA kak. Eflin
Pasaribu, kak. Adelina Sianturi, kak. Delphiana Sidabalok, kak. Santi Nababan,kak Leni, Kak Riri Napitupulu, bang Abe, bang Johar sitohang,
bang Alez, Anna Sirait, Togu Situmorang, Novaria Situmorang, Citra Saragih, Tina Zebua, Billy Andreas, Widamay Fresha, Pita Utari, Freddy
Sidauruk, Daniel Siagian, Leo, Diniyanti Hasibuan,Pandapotan Tambunan.
22.Teman-teman KKN Tematik Periode Juli 2013 daerah Lampung Timur
Kecamatan Pasir Sakti Desa Purworejo, TaufiQ, Okta, Rahmad, Fajar, Egha, Riana, Putri Ariesta, Puput, dan Septina Maulida.
23.Teman-teman di Kosn Wisma Rizki icha Sagala, Lusiana Simamora, Ana Sirait, Natalia Devi, Intan, Azrin, dian, Wika Pasaribu, Ayu, Sevi, Dian, Lilis, vina.
24.Semua pihak yang tidak dapat penulis sebutkan satu persatu yang secara tulus memberikan bantuan moril dan materil kepada penulis.
Akhir kata, penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan,
akan tetapi sedikit harapan semoga skripsi ini dapat berguna dan bermanfaat bagi kita semua. Aamiin.
Bandar Lampung, November 2014 Penulis
I. PENDAHULUAN
A. Latar Belakang
Bandar Lampung merupakan ibu kota provinsi Lampung, secara geografis terletak pada 5°20’ sampai dengan 5°30’ lintang selatan dan 105°28’ sampai dengan
105°37’ bujur timur. Kota tersebut berada pada Teluk Lampung di ujung selatan pulau Sumatra. Berdasarkan kondisi ini, kota Bandar Lampung menjadi pintu
gerbang utama pulau Sumatra tepatnya kurang lebih 165 km sebelah barat laut Jakarta dan memiliki peran sangat penting selain dalam kedudukannya sebagai ibu kota Provinsi Lampung juga merupakan pusat pendidikan, kebudayaan dan
perekonomian bagi masyarakat. Selain itu, karena merupakan wilayah pesisir, pemerintah kota Bandar Lampung mengembangkan wilayah pesisir untuk
meningkatkan dan menunjang ekonomi dan kesejahteraan masyarakat. Upaya-upaya pengembangan ini diantaranya melalui pemukiman, jasa transportasi laut, pelabuhan niaga dengan aktivitas kapal-kapalnya, pariwisata dan industri.
Berdasarkan data Badan Pusat Statistik (BPS) 2012, industri merupakan sektor tertinggi yang berperan dalam pengelolaan perekonomian Lampung yaitu sebesar
2
yang dapat merusak lingkungan apabila terdapat kesalahan dalam pengelolaan dan
pengawasannya.
Salah satu aktivitas utama di wilayah pesisir adalah aktivitas pelabuhan.
Pelabuhan Panjang Bandar Lampung dikenal dengan pelabuhan samudera karena
merupakan salah satu pelabuhan yang sangat strategis di Indonesia dan berada pada titik persilangan antara pulau Jawa dengan pulau Sumatra. Pelabuhan
Panjang berada dalam pengelolaan PT. Pelabuhan Indonesia II (Persero) dan merupakan pelabuhan bongkar muat, ekspor impor, dan lalu lintas kapal peti kemas utama di Lampung yang mempunyai peran penting bagi perindustrian,
sehingga tuntutan akan jasa pelabuhan semakin meningkat. Selain itu di sekitar wilayah pelabuhan Panjang terdapat beberapa perusahaan industri mulai dari
industri batu bara, industri makanan, dan lain-lain. Perusahaan-perusahaan ini membuang limbah pabriknya ke sungai yang muaranya mengarah ke perairan Teluk Lampung di sekitar pelabuhan Panjang. Padatnya aktivitas dan kegiatan di
wilayah pelabuhan Panjang berpotensi terjadinya pencemaran di perairan sekitar pelabuhan dan dapat menimbulkan ancaman terhadap kelestarian lingkungan.
Salah satu penyebab pencemaran di wilayah perairan khususnya wilayah pesisir pelabuhan Panjang adalah logam berat. Semakin tinggi aktivitas masyarakat (industri maupun rumah tangga), dan aktivitas kapal yang bersandar di sekitar
3
Melalui berbagai perantara, seperti udara, makanan, maupun air yang
terkontaminasi oleh logam berat, logam tersebut dapat terdistribusi ke bagian tubuh manusia dan sebagian terakumulasi. Jika keadaan ini berlangsung terus
menerus dalam jangka waktu lama dapat mencapai jumlah yang membahayakan.
Keracunan logam berat Cadmium dapat menyebabkan tekanan darah tinggi,
kerusakan jaringan testikular, kerusakan ginjal dan kerusakan sel-sel darah merah. Dalam jumlah yang melebihi ambang batas Ni bersifat toksik jika terakumulasi di dalam tubuh, dapat menyebabkan terjadinya mutasi genetik, gangguan pernapasan
dan kanker paru-paru (Pallar, 1994).
Daerah aliran sungai Way Kuala secara geografi berdekatan dengan pelabuhan
Panjang, dan paling banyak dikelilingi oleh industri, setidaknya terdapat sekitar 22 macam industri, seperti industri batu bara, industri kimia, industri konstruksi, industri pergudangan dan peti kemas. Sisa hasil produksi industri disekitar
Pelabuhan Panjang ini berupa limbah B3(Bahan berbahaya dan Beracun) yang mengalir dan terakumulasi didalam perairan . Selain dikelilingi oleh wilayah industri, daerah aliran sungai Way Kuala merupakan daerah pemukiman padat
penduduk yang menghasilkan limbah rumah tangga dan domestik. Limbah-limbah tersebut dibawa oleh arus sungai yang mengalir menuju pantai sehingga
menimbulkan pencemaran lingkungan.
Berdasarkan penelitian yang dilakukan Novita (2010), diketahui bahwa kandungan logam berat Cd pada sedimen di muara sungai Way Kuala adalah
4
Berdasarkan hasil penelusuran pustaka data tentang cemaran logam berat Cd dan
logam berat Ni pada sedimen di perairan pelabuhan Panjang belum tersedia. Oleh karena itu perlu dilakukan penelitian mengenai distribusi pencemaran logam berat
Cd dan Ni pada Sedimen di Pelabuhan Panjang. Logam berat Cd dan Ni akan dianalisis menggunakan Spektrofotometer Serapan Atom (SSA), alat ini dapat
digunakan karena dapat menentukan unsur di dalam suatu bahan dengan kepekaan, ketelitian serta selektifitas yang tinggi.
B. Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui distribusi logam berat Cd dan Ni di pelabuhan Panjang, kota Bandar Lampung.
C. Manfaat Penelitian
Manfaat dari penelitian ini adalah sebagai sumber informasi tentang distribusi
logam berat Cd dan Ni di perairan Pelabuhan Panjang, Bandar Lampung sehingga dapat dijadikan masukan bagi pemerintah daerah, pihak industri dan masyarakat
II. TINJAUAN PUSTAKA
A. Gambaran Umum Pesisir Teluk Lampung
1. Letak geografis
Teluk Lampung merupakan salah satu dari dua teluk di ujung paling selatan pulau
Sumatra, Kota Bandar Lampung terletak pada pangkal teluk, dan bagian mulut teluk (arah selatan-tenggara) berhadapan langsung dengan Selat Sunda yang
merupakan perairan penghubung antara Laut Jawa di sebelah utara dan Samudera Hindia di selatan. Pesisir Teluk Lampung meliputi daratan dan perairan, dengan
posisi geografis terletak antara 104o56’-105o45’ BT dan 5o25’-5o59’ LS. Luas
total wilayah daratan adalah 127.902 ha, dan luas perairan adalah 161.178 ha (Helfinalis, 2000).
Daratan wilayah pesisir Teluk Lampung tergolong sebagai dataran pantai sempit
dan perbukitan, dengan batuan dominan meliputi endapan aluvium dan rawa, batu gamping terumbu, dan endapan gunung api muda berumur quarter (Qhv). Wilayah yang berbatasan langsung dengan laut (Teluk Lampung) memiliki kelerengan
6
sampai dengan sangat curam (>40%), dengan elevasi beragam mulai dari 10
sampai dengan >1.000 m dpl. Kelompok relief pada wilayah ke arah laut tergolong dataran (flat); dan ke arah daratan beragam yaitu berombak
(undulating), bergelombang (rolling), dan berbukit (hummocky, hillocky, dan hilly) (Wiryawan et al., 1999).
2. Kondisi Wilayah
Wilayah pesisir Teluk Lampung memiliki potensi ekonomi wilayah yang besar, Secara ekologis wilayah ini merupakan kesatuan fungsional yang relatif dapat
dibatasi dari wilayah lainnya di Provinsi Lampung. Wilayah pesisir Teluk Lampung, dipisahkan oleh daerah aliran sungai (DAS) tersendiri, dan memiliki
perairan teluk yang semi tertutup dengan tubuh air lainnya. Nilai strategis lain dari wilayah pesisir Teluk Lampung adalah lokasi geografisnya sebagai pintu
gerbang antar Pulau Sumatra dan Jawa, serta dari sisi pertahanan sebagai calon pusat armada barat TNI-AL. Berdasarkan kondisi wilayah dan nilai strategis kawasan, maka terdapat cukup alasan untuk memberikan status sebagai kawasan
strategis provinsi pada wilayah pesisir Teluk Lampung. Dengan status tersebut maka penataan ruang dan pengelolaan wilayah pesisir Teluk Lampung, dapat
7
3. Kondisi Fisik dan Kimia Perairan Teluk Lampung
a. Arus dan sedimen
Arus di Teluk Lampung terdiri dari arus pasut yang dibangkitkan oleh pasut, dan
arus non pasut yang utamanya dibangkitkan oleh angin. Kekuatan arus berkisar antara 0,02-0,87 knot. Pada musim barat antara bulan November hingga Maret, arus mengalir dengan kecepatan 0,52-0,87 knot dan mencapai kecepatan
maksimum pada bulan Desember. Arus pada musim barat ini mengalir dengan tetap menuju ke arah tenggara. Sedangkan arus pada musim timur antara bulan
April hingga Oktober melemah dengan kisaran kecepatan 0,02-0,70 knot. Pada bulan Juli arus mencapai minimum, berkisar antara 0,02-0,10 knot.
Sebaran sedimen di Teluk Lampung cukup bervariasi mengikuti pola arus yang
terjadi. Hasil penelitian Helfinalis (2000) di Teluk Lampung, menunjukkan bahwa pada lokasi-lokasi dasar perairan yang dipengaruhi oleh arus pasut yang cepat akan didominasi pasir; dan sebaliknya yang dipengaruhi oleh pergerakan arus
pasut lemah akan didominasi sedimen lumpur. Sedimen pasir yang berasal dari aliran sungai akan diendapkan di sekitar muara sungai.
b. Kualitas Air
Kualitas air adalah kondisi kualitatif air yang diukur dan di uji berdasarkan parameter- parameter tertentu dan metode tertentu. Parameter ini meliputi
parameter fisik, kimia, dan mikrobiologis. Kualitas air Teluk Lampung
ditunjukkan dengan penggambaran beberapa parameter yang dirujuk dari berbagai
8
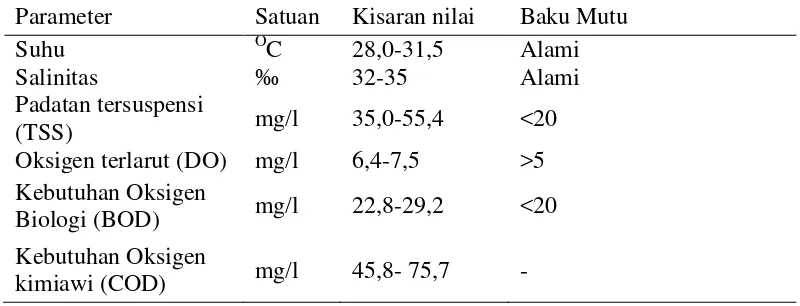
Tabel 1. Kualitas air Teluk Lampung
Parameter Satuan Kisaran nilai Baku Mutu
Suhu OC 28,0-31,5 Alami
Sumber : Kep-Men-LH No. 51 tahun 2004 tentang Baku Mutu Air Laut
Padatan tersuspensi (TSS) merupakan indikasi beban pencemaran berupa padatan
tersuspensi yang dapat berasal dari berbagai sumber. Pada perairan Teluk Lampung, padatan tersuspensi dapat berasal dari berbagai sumber seperti limbah permukiman (perkotaan), industri, dan suspensi yang dibawa oleh aliran sungai.
Secara umum, TSS perairan Teluk Lampung sudah melampaui ambang batas baku mutu kualitas air laut untuk biota laut, dan dapat dindikasikan sudah tercemar
(Helfinalis, 2000).
Oksigen terlarut (DO) merupakan indikasi ketersediaan oksigen di dalam air yang dibutuhkan oleh mahluk hidup. Secara umum peraian Teluk Lampung
menunjukkan indikasi DO masih memenuhi prasyarat yang dapat mendukung kehidupan biota laut. Kebutuhan oksigen biologi (BOD) dan kimiawi (COD) merupakan parameter kualitas perairan yang mengindikasikan tingkat
pencemaran. BOD dan COD merupakan jumlah oksigen (dalam satuan mg/l) yang diperlukan untuk mendegradasi (oksidasi) polutan di dalam air secara
9
sebaliknya bila nilai BOD sudah melebihi nilai ambang tersebut. Secara umum
terlihat bahwa perairan Teluk Lampung sudah melampaui ambang batas baku mutu BOD, dan dapat diindikasikan sudah tercemar (Bapelda, 2003) .
B. Pelabuhan Panjang
Kecamatan Panjang merupakan kawasan pesisir Teluk Lampung. Pelabuhan
Panjang berada di Jalan Yos Sudarso di daerah Panjang kota Bandar Lampung. Secara administratif batas wilayah kecamatan Panjang adalah (1) Sebelah Utara : kecamatan Tanjung Karang Timur; (2) Sebelah Selatan : Teluk Lampung; (3)
Sebelah Timur : kabupaten Lampung Selatan; (4) Sebelah Barat : Teluk Betung Selatan. Pelabuhan Panjang berada dalam lingkungan PT. Pelabuhan Indonesia II
(Persero). letak pelabuhan Panjang, disajikan pada Gambar 1(Anonim, 2013).
10
Gambar diatas memperlihatkan aktivitas pelabuhan Panjang. Pelabuhan ini
beraktivitas selama 24 jam penuh melayani ekspor impor dan pelabuhan ini juga merupakan gerbang masuknya barang dari pulau Jawa ke pulau Sumatra atau pun
sebaliknya (Pelindo, 2001). Selain itu juga pelabuhan ini dekat dengan wilayah perindustrian, seperti industri kayu lapis, batu bara, semen, pertamina dan
beberapa industri di sekitar pelabuhan Panjang seperti industri konstruksi (PT Darma Putra Konstruksi, PT Jaya Persada Konstruksi, PT Husada Baja), industri kimia (PT Golden Sari, PT Garuntang), industri pergudangan dan peti
kemas (PT Inti Sentosa Alam Bahtera). Berdasarkan data Badan Pusat Statistik (BPS) 2012, dari aktivitas kepelabuhan, jumlah kunjungan kapal laut baik dari
maupun ke Pelabuhan Panjang mengalami peningkatan, pada tahun 2010
berjumlah 2051 kunjungan kapal, dan pada tahun 2011 meningkat menjadi 2061 kunjungan kapal. Seiring dengan meningkatnya volume kunjungan kapal laut
tersebut, volume eksport dari Lampung juga meningkat sebesar 2,05% .
C. Pencemaran
Pencemaran lingkungan hidup menurut Undang-Undang No 23 tahun 1997 adalah
masuknya atau dimasukkannya makhluk hidup, zat, energi, dan atau komponen lain ke dalam lingkungan hidup oleh kegiatan manusia, sehingga kualitasnya turun sampai ke tingkat tertentu yang menyebabkan lingkungan hidup tidak dapat
berfungsi sesuai dengan peruntukkannya. Menurut Odum (1971) pencemaran perairan adalah suatu perubahan fisika, kimia dan biologi yang tidak dikehendaki
11
kehidupan, kondisi kehidupan dan proses industri. Sedangkan menurut definisi
GESAMP (Group of Expert on Scientific Aspect on Marine Pollution)
pencemaran laut diartikan sebagai masuknya zat-zat (substansi) atau energi ke
dalam lingkungan laut dan estuaria baik langsung maupun tidak langsung akibat adanya kegiatan manusia yang menimbulkan kerusakan pada lingkungan laut,
kehidupan di laut, kesehatan manusia, mengganggu aktivitas di laut (usaha penangkapan, budidaya, alur pelayaran) serta secara visual merusak keindahan (estetika). Fardiaz (2006) mengistilahkan pencemaran air dengan istilah yang
berbeda, yaitu polusi air. Polusi air yang dimaksud disini adalah penyimpangan sifat-sifat air dari keadaan normal.
Darmono (1995) mengklasifikasikan sumber pencemaran logam berat berdasarkan
lokasinya yaitu :
1. Pada perairan estuaria, pencemaran memiliki hubungan yang erat dengan penggunaan logam oleh manusia.
2. Pada perairan laut lepas kontaminasi logam berat biasanya terjadi secara langsung dari atmosfer atau karena tumpahan minyak dari kapal-kapal tanker
yang melaluinya.
12
D. Sedimen
Pipkin (1977) menyatakan bahwa sedimen adalah pecahan, mineral, atau material
organik yang ditranspartasikan dari berbagai sumber dan diendapkan oleh media udara, angin, es, atau air dan juga termasuk didalamnya material yang diendapkan
dari material yang melayang dalam air atau dalam bentuk larutan kimia. Sedangkan Gross (1990) mendefinisikan sedimen laut sebagai akumulasi dari mineral-mineral dan pecahan-pecahan batuan yang bercampur dengan hancuran
cangkang dan tulang dari organisme laut serta beberapa partikel lain yang
terbentuk lewat proses kimia yang terjadi di laut. Sedimen yang dijumpai di dasar
lautan dapat berasal dari beberapa sumber dan dibedakan menjadi empat yaitu (Ward and Stanley, 2004):
1. Lithougenus sedimen yaitu sedimen yang berasal dari erosi pantai dan
material hasil erosi daerah up land. Material ini dapat sampai ke dasar laut
melalui proses mekanik, yaitu tertransport oleh arus sungai dan atau arus laut dan akan terendapkan jika energi tertransforkan telah melemah.
2. Biogeneuos sedimen yaitu sedimen yang bersumber dari sisa-sisa organisme
yang hidup seperti cangkang dan rangka biota laut serta bahan-bahan organik
yang mengalami dekomposisi.
3. Hidreogenous sedimen yaitu sedimen yang terbentuk karena adanya reaksi
kimia di dalam air laut dan membentuk partikel yang tidak larut dalam air laut
13
4. Cosmogerous sedimen yaitu sedimen yang bersal dari berbagai sumber dan
masuk ke laut melalui jalur media udara atau angin. Sedimen jenis ini dapat bersumber dari luar angkasa , aktifitas gunung api atau berbagai partikel darat
yang terbawa angin. Material yang berasal dari luar angkasa merupakan sisa-sisa meteorik yang meledak di atmosfir dan jatuh ke laut. Sedimen yang
berasal dari letusan gunung berapi dapat berukuran halus berupa debu
volkanin, atau berupa fragmen-fragmen aglomerat. Sedangkan sedimen yang berasal dari partikel di darat dan terbawa angin banyak terjadi pada daerah
kering dimana proses aeolian dominan namun demikian dapat juga terjadi pada daerah sub tropis saat musim kering dan angin bertiup kuat.
Dalam suatu proses sedimentasi, zat-zat yang masuk ke laut berakhir menjadi
sedimen. Dalam hal ini zat yang ada terlibat proses biologi dan kimia yang terjadi di sepanjang kedalaman laut. Sebelum mencapai dasar laut dan menjadi sedimen, zat tersebut melayang-layang di dalam laut. Setelah mencapai dasar laut pun
sedimen tidak diam tetapi sedimen akan terganggu ketika hewan laut mencari makan. Sebagian sedimen mengalami erosi dan tersuspensi kembali oleh arus
bawah sebelum kemudian jatuh kembali dan tertimbun. Terjadi reaksi kimia antara butir-butir mineral dan air laut sepanjang perjalannya ke dasar laut dan reaksi tetap berlangsung, yaitu ketika air laut terperangkap di antara butiran
mineral.
Perairan pesisir banyak didominasi oleh substrat lunak seperti lumpur dan butir-butir pasir. Clark (1986) menyatakan bahwa air sungai mengangkut partikel
14
dengan air laut partikel lumpur akan membentuk partikel yang lebih besar dan
mengendap di dasar perairan. Menurut Fardiaz (2006) adanya sedimen dalam jumlah tinggi di perairan dapat merugikan karena:
1. Menyebabkan pendangkalan dan penyumbatan sehingga mengurangi volume air yang ditampung.
2. Mengurangi populasi ikan dan hewan air lainnya karena telur dan sumber makanan terendam oleh sedimen.
3. Mengurangi penetrasi cahaya ke dalam perairan sehingga mengurangi
kecepatan fotosintesis.
E. Logam Berat
1. Pengertian Logam Berat
Logam berat adalah unsur-unsur kimia dengan densitas lebih besar dari 5g/cm3 terletak di sudut kanan bawah pada sistem periodik unsur, mempunyai afinitas yang tinggi terhadap S dan biasanya bernomor atom 22 sampai 92 Dari periode 4
sampai 7 (Ernawati, 2010). Karena afinitasnya yang tinggi terhadap S
menyebabkan logam ini menyerang ikatan S dalam enzim, sehingga enzim yang
bersangkutan menjadi tidak aktif ( Manahan, 1994).
Logam berat adalah unsur alami dari kerak bumi. Logam yang stabil dan tidak bisa rusak atau hancur, oleh karena itu mereka cenderung menumpuk dalam tanah dan sedimen. Banyak istilah logam berat telah diajukan, berdasarkan kepadatan,
15
antimony (Sb), Arsen (As), kadmium (Cd), kobalt(Co), kromium (Cr), tembaga
(Cu), nikel (Ni), timbal (Pb), mangan (Mn), merkuri (Hg), molybdenum (Mo), skandium (Sc), selenium (Se), titanium (Ti), tungsten (W), timah (Sn), dan
vanadium (V).
2. Karakteristik Logam Berat
Berdasarkan daya hantar panas dan listrik, semua unsur kimia yang terdapat dalam susunan berkala unsur-unsur dapat dibagi atas dua golongan yaitu logam dan non logam. Golongan logam mempunyai daya hantar panas dan listrik yang
tinggi, sedangkan golongan non logam mempunyai daya hantar listrik yang rendah . Berdasarkan densitasnya, golongan logam di bagi atas dua golongan,
yaitu golongan logam ringan dan logam berat. Golongan logam ringan ( light metals ) mempunyai densitas < 5, sedangkan logam berat mempunyai densitas > 5
(Hutagalung, 1991).
Sedangkan (Palar, 1994) memberi karakteristik logam berat sebagai berikut :
a. Memiliki spesifikasi gravitasi yang sangat besar ( > 4).
b. Mempunyai nomor atom 22-34 dan 40-50 serta unsur lantanida dan aktanida.
c. Mempunyai respon biokimia yang spesifik pada organisme hidup.
Berbeda dengan logam biasa, logam berat biasanya menimbulkan efek khusus pada makhluk hidup. Dapat dikatakan bahwa semua logam berat dapat menjadi
16
makhluk hidup dalam jumlah sedikit, yang juga apabila tidak terpenuhi akan
berakibat fatal terhadap kelangsungan hidup dari makhluk hidup tersebut.
3. Toksisitas Logam Berat
Sedikitnya terdapat 80 jenis dari 109 unsur kimia di muka bumi ini yang telah teridentifikasi sebagai jenis logam berat. Berdasarkan sudut pandang toksikologi,
logam berat dapat dibagi dalam dua jenis. Pertama, logam berat esensial, di mana keberadaannya dalam jumlah tertentu sangat dibutuhkan oleh organisme hidup, namun dalam jumlah yang berlebihan dapat menimbulkan efek racun. Contoh
logam berat ini adalah Zn, Ni, Cu, Fe, Co, Mn dan lain sebagainya. Sedangkan jenis kedua, logam berat tidak esensial atau beracun, di mana keberadaannya
dalam tubuh masih belum diketahui manfaatnya atau bahkan dapat bersifat racun, seperti Hg, Cd, Pb, Cr dan lain-lain (Connel dan Miller 1995).
Berdasarkan sifat kimia dan fisikanya, maka tingkat atau daya racun logam berat terhadap hewan air dapat diurutkan (dari tinggi ke rendah) yaitu merkuri (Hg),
kadmium (Cd), seng (Zn), timah hitam (Pb), krom (Cr), nikel (Ni), dan kobalt (Co) (Sutamihardja dkk, 1982). Menurut Darmono (1995) daftar urutan
toksisitas logam paling tinggi ke paling rendah terhadap manusia yang
mengkomsumsi ikan adalah sebagai berikut Hg2+ > Cd2+ >Ag2+ > Ni2+ > Pb2+ > As2+ > Cr2+ Sn2+ > Zn2+ . Sedangkan menurut Kementrian Negara Kependudukan
dan Lingkungan Hidup (2004) sifat toksisitas logam berat dapat dikelompokkan ke dalam 3 kelompok, yaitu :
17
2. Bersifat toksik sedang (Cr, Ni, dan Co).
3. Bersifat tosik rendah (Mn dan Fe).
4. Logam Berat Dalam Lingkungan Air
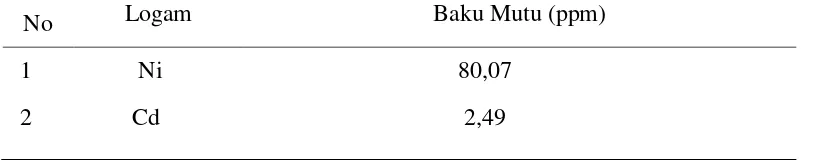
Berdasarkan National Sediment Quality Survey USEPA (2004) baku mutu logam
berat Cd dan Ni dapat dilihat pada Tabel 2.
Tabel 2. Baku mutu kandungan logam berat dalam sedimen
No Logam Baku Mutu (ppm)
Pada saat buangan limbah industri masuk ke dalam suatu perairan maka akan terjadi proses pengendapan dalam sedimen. Hal ini menyebabkan konsentrasi
bahan pencemar dalam sedimen meningkat.
Adanya logam berat di perairan, berbahaya baik secara langsung terhadap
kehidupan organisme, maupun efeknya secara tidak langsung terhadap kesehatan
manusia. Hal ini berkaitan dengan sifat-sifat logam berat yaitu (Efendi, 2003): 1. Sulit didegradasi, sehingga mudah terakumulasi dalam lingkungan perairan
dan keberadaannya secara alami sulit terurai (dihilangkan).
2. Dapat terakumulasi dalam organisme termasuk kerang dan ikan, dan akan membahayakan kesehatan manusia yang mengkomsumsi organisme tersebut.
18
4. Mudah tersuspensi karena pergerakan masa air yang akan melarutkan kembali
logam yang dikandungnya ke dalam air, sehingga sedimen menjadi sumber pencemar potensial dalam skala waktu tertentu.
Secara alamiah, kandungan logam berat dalam air adalah kurang dari 1 g/L.
Menurut Pallar (1994) faktor-faktor yang mempengaruhi kelarutan logam berat dalam suatu badan air antara lain :
a. pH air
Dalam lingkungan perairan, bentuk logam antara lain berupa ion bebas, pasangan ion organik, dan ion kompleks. Kelarutan logam dalam air dikontrol oleh pH air.
Kenaikan pH menurunkan kelarutan logam dalam air, karena kenaikan pH mengubah kestabilan dari bentuk karbonat menjadi hidroksida yang membentuk ikatan dengan partikel pada badan air, sehingga akan mengendap membentuk
lumpur.
b. Suhu air
Kenaikan suhu air dan penurunan pH akan mengurangi adsorpsi senyawa logam
berat pada partikulat. Suhu air yang lebih dingin akan meningkatkan adsorpsi logam berat ke partikulat untuk mengendap di dasar. Sementara saat suhu air naik, senyawa logam berat akan melarut di air karena penurunan laju adsorpsi ke
dalam partikulat. Logam yang memiliki kelarutan yang kecil akan ditemukan di permukaan air selanjutnya dengan perpindahan dan waktu tertentu akan
19
Hal ini ditentukan antara lain oleh massa jenis air, viskositas (kekentalan) air,
temperatur air, arus air serta faktor lainnya.
c. Konsentrasi oksigen dalam badan air
Pada daerah yang kekurangan oksigen, misalnya akibat kontaminasi bahan-bahan
organik, daya larut logam berat akan menjadi lebih rendah dan mudah mengendap. Logam berat yang terlarut dalam air akan berpindah ke dalam
sedimen jika berikatan dengan materi organik bebas atau materi organik yang melapisi permukaan sedimen, dan penyerapan langsung oleh permukaan partikel sedimen.
Keberadaan logam dalam perairan terutama muara dapat berasal dari sumber alamiah dan aktifitas manusia (Pallar, 1994). Masuknya logam berat kedalam muara secara alamiah dapat digolongkan sebagai berikut :
1. Pasokan dari daerah hulu sungai karena erosi yang disebabkan oleh gerakan gelombang air.
2. Pasokan dari laut dalam yang meliputi logam yang dilepaskan gunung berapi di
laut dalam dan dari partikel atau endapan oleh adanya proses kimiawi. 3. Pasokan yang berasal dari lingkungan dekat muara dan meliputi logam yang
diangkat ke dalam atmosfer sebagai partikel debu.
Sedangkan keberadaan logam-logam berat dalam muara yang disebabkan oleh aktifitas manusia dapat berasal dari:
1. Buangan rumah tangga.
20
3. Lumpur minyak yang kadang-kadang juga mengandung logam berat dengan
konsentrasi yang tinggi yang terbuang sampai ke muara dan mengendap jadi sedimen. Pembakaran hidrokarbon dan batu bara diantaranya ada yang
melepaskan senyawa logam berat ke udara kemudian bercampur dengan air hujan dan mengalir melalui sungai yang pada akhirnya sampai di muara.
F. Nikel (Ni)
Nikel ditemukan oleh A. F. Cronstedt pada tahun 1751. Nikel dengan nomor
atom 28 dan massa atom 58,69, dalam sistem periodik unsur terletak pada periode 4, golongan VIII B. Nikel adalah logam putih perak yang keras,bersifat liat, dapat
ditempa dan sangat kokoh. Logam ini melebur pada suhu 1455oC, dan bersifat sedikit magnetis (Svehla, 1999). Nikel di alam dalam bentuk ion heksaquo [Ni(H2O6]+2 dan garam terlarut dalam air. Aliran alami, sungai, dan danau
mengandung total 0,2-10 µgL-1 nikel terlarut. Air yang dekat dengan permukaan pada daerah pertambangan dan peleburan mengandung nikel sampai 6, 4 mg L-1.
Air laut mengandung kira-kira 1,5 µgL-1 dimana merupakan sekitar 50% bentuk ion bebasnya (Wright, 2002). Ni memasuki atmosfer dari pembakaran bahan bakar fosil, proses peleburan dan alloying (paduan logam), sampah pembakaran,
21
1. Manfaat dan Penggunaan Nikel
Nikel digunakan dalam berbagai aplikasi komersial dan industri, seperti : pembuatan baja tahan karat, alloy yang bersifat tahan korosi, pelindung baja (stainless steel), pelindung tembaga, industri baterai, elektronik, aplikasi industri
pesawat terbang, industri tekstil, turbin pembangkit listrik bertenaga gas, pembuat magnet kuat,pembuatan alat-alat laboratorium (nikrom), kawat lampu listrik,
katalisator lemak, pupuk pertanian, dan berbagai fungsi lain (Anonim 2, 2013).
2. Toksisitas Nikel
Nikel dalam jumlah kecil dibutuhkan oleh tubuh, tetapi bila terdapat dalam jumlah yang terlalu tinggi dapat berbahaya untuk kesehatan manusia, yaitu :
menyebabkan kanker paru-paru, kanker hidung, kanker pangkal tenggorokan,
kanker prostat, merusak fungsi ginjal, meyebabkan kehilangan keseimbangan, menyebabkan kegagalan respirasi, kelahiran cacat,menyebabkan penyakit asma dan bronkitis kronis serta merusak hati.
Berdasarkan hasil autopsi terhadap korban yang meninggal akibat paparan Ni(CO)4, diketahui bahwa kadar Ni tertinggi adalah di paru-paru selanjutnya dalam jumlah rendah terdapat di ginjal, hati, dan otak. Paparan nikel (Ni) bisa
terjadi melalui inhalasi, oral, dan kontak kulit . Paparan akut Ni dosis tinggi melalui inhalasi bisa mengakibatkan kerusakan berat pada paru-paru dan ginjal
22
kronis bisa menimbulkan gejala, antara lain dermatitis nikel berupa eksema (kulit
kemerahan, gatal) pada jari-jari, tangan, pergelangan tangan, serta lengan (Mukono, 2009).
Berdasarkan uji toksisitas akut pada hewan, diketahui bahwa tingkat toksisitas nikel bervariasi dipengaruhi oleh tingkat kelarutan senyawa Ni. Senyawa larut seperti nikel asetat lebih toksik dibandingkan senyawa Ni yang tidak larut, seperti
nickel powder .
Darmono (1995) melaporkan bahwa dalam konsentrasi tinggi nikel di tanah berpasir merusak tanaman dan di permukaan air dapat mengurangi tingkat
pertumbuhan alga. Lebih lanjut dikatakan bahwa nikel juga dapat menghambat pertumbuhan mikroorganisme, tetapi mereka biasanya mengembangkan
perlawanan terhadap nikel setelah beberapa saat. Ketoksikan nikel pada
kehidupan akuatik bergantung pada spesies, pH, kesadahan dan faktor lingkungan lain .
G. Kadmium (Cd)
Kadmium biasanya merupakan produk sampingan dari peristiwa peleburan dan refining bijih-bijih Zn (seng). Cd banyak digunakan sebagai stabilizer dalam
23
ikan, mesin pengolahan air minum dan mesin industri tekstil meskipun dalam
konsentrasi rendah (Pallar, 1994).
1. Sumber Pencemaran Logam Cd
Kandungan logam Cd dapat di jumpai di daerah-daerah penimbunan sampah dan aliran air hujan. Menurut National Research Council dalam Yuliasari (2003),
sampah dari kota mengandung Cd yang cukup besar sehingga penggunaan sampah yang mengandung Cd tinggi untuk pemupukan tanaman, baik tanaman untuk manusia atau hewan memperlihatkan peningkatan kandungan Cd secara
substansial ke dalam makanan hewan dan manusia.
Selain dari aktivitas manusia, organisme yang hidup di perairan tersebut juga dapat meningkatkan konsentrasi melalui biomagnifikasi. Biomagnifikasi adalah
kemampuan yang dimiliki oleh organisme perairan untuk meningkatkan
konsentrasi bahan pencemar baik dalam bentuk logam berat atau persenyawaan kimia beracun lainnya, yang melebihi keseimbangan penyerapan dalam tubuh
organisme tersebut (Gobas et al., 1999).
2. Toksisitas Logam Cd
Dampak keracunan Cd dapat menyebabkan tekanan darah tinggi, kerusakan jaringan testikular, kerusakan ginjal dan kerusakan sel darah merah.
24
Jepang yaitu itai-itai disease di sepanjang sungai Jinzo di pulau Honsyu
(Darmono, 1995).
3. Sifat Fisik dan Kimia Cd
Kadmium (Cd) adalah salah satu logam berat dengan penyebaran yang luas di alam; logam ini bernomor atom 48; berat atom 112,40 dengan titik leleh 321oC
dan titik didih 765oC. Di alam Cd bersenyawa dengan belerang (S) sebagai Greennocckite (CdS) yang ditemui bersamaan dengan senyawa Spalerite (ZnS).
Kadmium merupakan logam lunak (Ductile) berwarna putih perak dan mudah
teroksidasi oleh udara bebas dan gas amoniak. Di perairan Cd akan mengendap karena senyawa sulfitnya sukar larut (Pallar, 2004). Beberapa sifat fisik dari
logam Cd dapat dilihat pada Tabel 3.
Tabel 3. Sifat Fisik Logam Cd
Nomor atom 48
Titik lebur (0C) 321,07
Kalor peleburan (kJ/mol) 6,21
Kalor penguapan (kJ/mol) 99,87
25
H. Spektrofotometer Serapan Atom
Spektrofotometer Serapan Atom (SSA) adalah alat yang digunakan pada metode
analisis untuk penentuan unsur-unsur logam dan metaloid yang pengukurannya berdasarkan penyerapan cahaya dengan panjang gelombang tertentu oleh atom
logam dalam keadaan bebas (Ellwel, 1996).
1. Prinsip dasar
Jika cahaya dengan panjang gelombang resonansi dilewatkan nyala yang
mengandung atom-atom yang bersangkutan, maka sebagian cahaya akan
diserap,dan jauhnya penyerapan akan berbanding lurus dengan banyaknya atom
keadaan dasar yang berada dalam nyala. Cahaya pada panjang gelombang ini mempunyai cukup energi untuk mengubah tingkat elektronik suatu atom yang mana transisi elektronik suatu atom bersifat spesifik. Dengan menyerap suatu
energi, maka atom akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat ditingkatkan energinya ke tingkat eksitasi. Hal ini merupakan dasar
26
2. Instrumentasi Pada Spektrofotometer Serapan Atom
Instrumentasi spektrofotometer serapan atom disajikan pada Gambar 2.
Gambar 2. Spektrofotometer Serapan Atom (Anonim 3, 2010).
Spektrofotometer Serapan atom memiliki komponen-komponen sebagai berikut : (Slavin, 1987).
a. Sumber Sinar
Sumber radiasi Spektofotometer Serapan Atom (SSA) adalah Hallow Cathode Lamp (HCL). Setiap pengukuran dengan SSA harus menggunakan Hallow
Cathode Lamp khusus misalnya untuk menentukan konsentrasi tembaga dari
suatu cuplikan, maka digunakan Hallow Cathode khusus untuk tembaga. Hallow Cathode akan memancarkan energi radiasi yang sesuai dengan energi yang
diperlukan untuk transisi elektron atom. Hallow Cathode Lamp terdiri dari katoda cekung silindris yang terbuat dari unsur yang sama dengan unsur yang
akan dianalisis dan anoda yang terbuat dari tungsten. Sumber radiasi lain yang
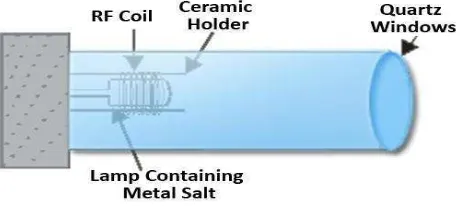
sering dipakai adalah ”Electrodless Dischcarge Lamp”, lampu ini mempunyai
27
tetapi mempunyai output radiasi lebih tinggi dan biasanya digunakan untuk
analisis unsur-unsur As dan Se, karena lampu HCL untuk unsur-unsur ini
mempunyai signal yang lemah dan tidak stabil yang bentuknya dapat dilihat pada
Gambar 3.
Gambar 3. Electrodless Dischcarge Lamp
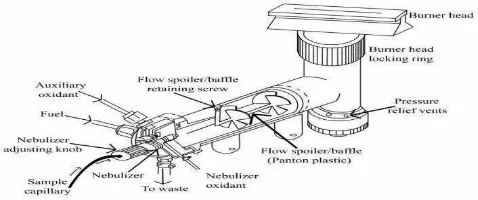
b. Sumber atomisasi
Sumber atomisasi dibagi menjadi dua yaitu sistem nyala dan sistem tanpa nyala. Kebanyakan instrumen sumber atomisasinya adalah nyala dan sampel
diintroduksikan dalam bentuk larutan. Sampel masuk ke nyala dalam bentuk
aerosol. Aerosol biasa dihasilkan oleh nebulizer (pengabut) yang dihubungkan ke nyala oleh ruang penyemprot (chamber spray). Jenis nyala yang digunakan
secara luas dan umum untuk pengukuran analitik adalah udara-asetilen dan nitrous oksida-asetilen. Dengan kedua jenis nyala ini, kondisi analisis yang sesuai untuk
28
Gambar 4. Sumber Atomisasi (Slavin, 1978)
Adapun beberapa jenis nyala yang digunakan dalam proses atomisasi yaitu :
Nyala udara - asetilen
Biasanya menjadi pilihan untuk analisis mengunakan SSA (Spektrofotometer
Serapan Atom). Temperatur nyalanya yang lebih rendah mendorong terbentuknya atom netral dan dengan nyala yang kaya bahan bakar pembentukan oksida dari banyak unsur dapat diminimalkan.
Nitrous oksida-asetilen
Suhu nyala ini sangat tinggi karena nitrous oksida mempunyai daya pereduksi
yang kuat sehingga dapat digunakan untuk unsur yang sulit diuraikan oleh nyala lain. Biasanya digunakan untuk penentuan unsur-unsur yang mudah membentuk oksida dan sulit terurai. Hal ini disebabkan karena temperatur nyala yang
dihasilkan relatif tinggi. Unsur-unsur tersebut adalah Al, B, Mo, Si, So, Ti dan V.
Nyala Udara- Hidrogen
29
Nyala Argon- Hidrogen
Nyala ini mempunyai transmitan pada daerah panjang gelombang pendek, nyala
ini sesuai untuk analisis unsur As (192,7 nm) dan Se (196 nm). Akan tetapi karena suhu nyala yang sangat rendah memungkinkan adanya interferensi yang besar.
c. Monokromator
Monokromator merupakan alat yang berfungsi untuk memisahkan radiasi yang
tidak diperlukan dari spektrum radiasi lain yang dihasilkan oleh Hallow Cathode Lamp.
d. Detektor
Detektor merupakan alat yang mengubah energi cahaya menjadi energi listrik, yang memberikan suatu isyarat listrik berhubungan dengan daya radiasi yang
diserap oleh permukaan yang peka.
e. Sistem pengolah
Sistem pengolah berfungsi untuk mengolah kuat arus dari detektor menjadi
besaran daya serap atom transmisi yang selanjutnya diubah menjadi data dalam sistem pembacaan.
f. Sistem pembacaan
Sistem pembacaan merupakan bagian yang menampilkan suatu angka atau gambar yang dapat dibaca oleh mata. Skema instrumentasi spektrofotometer serapan atom mulai dari sumber radiasi hingga recorder yang menampilkan sistem
30
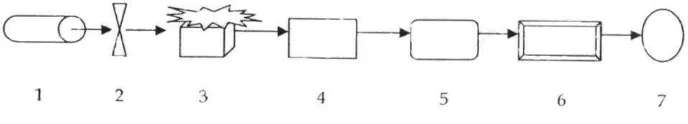
Gambar 5. Skema Instrumentasi Spektrofotometer Serapan Atom
Keterangan :
1. Sumber sinar 5. detektor 2. Pemilah (Chopper) 6. Amplifier
3. Nyala 7. recorder
4. Monokromator
3. Analisis Kuantitatif
Pada dasarnya hubungan antara absorpsi atom dengan konsentrasi di dalam metode SSA dapat dinyatakan dengan hukum Lambert-Beer, yaitu secara matematika persamaannya adalah sebagai berikut:
………. (1) Keterangan:
Io : Interaksi cahaya yang datang (mula-mula) I : Interaksi cahaya yang ditransmisikan a : Absorpsitivitas (g/L)
b : Panjang jalan cahaya atau tebalnya medium penyerap (cm) c : Konsentrasi atom yang mengabsorpsi
31
Dari persamaan 1, nilai absorbansi sebanding dengan konsentrasi untuk panjang
jalan penyerapan dan panjang gelombang tertentu. Ada dua cara untuk
mengetahui konsentrasi cuplikan yang telah diketahui nilai absorbansinya yaitu :
1. Cara deret waktu dengan membandingkan nilai absorbansi terhadap Kurva kalibrasi dari standar-standar yang diketahui.
2. Cara penambahan standar dengan membandingkan konsentrasi dengan perpotongan grafik terhadap sumbu dengan konsentrasi dari data absorbansi.
I. Validasi Metode
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter
tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya. Parameter validasi metode antara lain :
1. Limit Deteksi
Batas deteksi atau limit deteksi adalah jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Berdasarkan Batas
deteksi, maka limit deteksinya dapat ditentukan dengan Persamaan 2.
Q = 3 x SD ……….(2) SI
Keterangan :
LOD : limit of detection (limit deteksi) K : 3
32
2. Presisi (ketelitian)
Presisi merupakan ukuran derajat keterulangan dari metode analisis yang memberikan hasil yang sama pada beberapa perulangan, dinyatakan simpangan baku relatif (RSD) dan simpangan baku (SD). Metode dengan presisi yang baik
ditunjukan dengan simpangan baku relatif (RSD) < 5 %. Simpangan baku (SD) dan simpangan baku relatif (RSD) dapat ditentukan dengan Persamaan 3 dan 4.
………(3)
Keterangan :
SD : Standar Deviasi (simpangan baku) M : Konsentrasi hasil analisis
n : Jumlah pengulangan analisis konsentrasi rata-rata hasil analisis
………..(4)
Keterangan :
RSD : simpangan baku relative : konsentrasi hasil analisis SD : Standar Deviasi
3. Kecermatan (Akurasi)
33
dinyatakan sebagai persen perolehan kembali (Recovery) analit yang
ditambahkan. Persen perolehan kembali dapat ditentukan dengan Persamaan 5. (AOAC, 1993) :
………(5)
Keterangan :
CF : konsentrasi total sampel yang diperoleh dari pengukuran CA : konsentrasi sampel sebenarnya
C*A : konsentrasi analit yang ditambahkan
4. Linieritas
Linieritas adalah kemampuan metode analisis memberikan respon proporsional
terhadap konsentrasi analit dalam sampel. Linieritas suatu metode merupakan ukuran seberapa baik kurva kalibrasi yang menghubungkan antara respon (y) dengan konsentrasi (x).
Linieritas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi yang berbeda –beda. Data yang diperoleh selanjutnya diproses dengan metode kuadrat terkecil, untuk selanjutnya dapat ditentukan nilai slope, intersep, dan
34
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan April sampai dengan bulan Juli 2014 di laboratorium Kimia Analitik Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Lampung dan Laboratorium Kimia Analitik Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Gadjah Mada.
B. Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini adalah : Spektrofotometer Serapan Atom (SSA) , eckmen grab Wildco Wildlife Supply Company ®, orbital shaker
gallenhamp®, neraca analitik, botol sampel, kertas saring, Oven, pH-meter, termometer, saringan mess ukuran 150, mortar dan peralatan gelas yang umum digunakan di laboratorium.
Bahan-bahan yang digunakan adalah sampel sedimen, HCl pekat, HNO3 pekat,
35
C. Prosedur kerja
1. Pembuatan Larutan
a. Larutan HNO3 1 N
Sebanyak 31,25 mL HNO3 pekat dimasukkan ke dalam labu ukur 500 mL, kemudian ditambahkan akuades sampai tanda batas dan dihomogenkan.
b. Larutan induk Ni 1000 ppm.
Sebanyak 0,43 gram Ni(NO3)2.4 H2O dimasukkan ke dalam labu ukur 100 mL, kemudian ditambahkan akuades hingga tanda batas dan dihomogenkan.
c. Larutan induk Cd 1000 ppm
Sebanyak 0,2744 gram Cd(NO3)2.4H2O dimasukkan ke dalam labu ukur 100 mL, kemudian ditambahkan akuades hingga tanda batas dan dihomogenkan.
2. Metode Pengambilan Sampel
a. Persiapan Pengambilan Sampel
Sebelum melakukan pengambilan sampel, semua wadah dicuci dengan sabun
dan dibilas merata dengan air sampai busanya habis, kemudian dicuci dengan HNO3 1 N untuk menghilangkan kontaminasi logam yang menempel dalam wadah sampel.
36
b. Titik pengambilan Sampel
Penentuan titik sampel dilakukan secara Stratified Sampling, proses
pengambilan sampel dilakukan pada titik-titik yang telah ditentukan secara
terstruktur (Novita, 2010). Keunggulan dari metode ini yaitu sampel dapat terambil dari semua populasi yang ada, sehingga ada jaminan bahwa tidak
ada populasi yang terabaikan. Pengambilan sampel dilakukan dengan menggunakan perahu nelayan menuju lokasi pengambilan sampel. Sampel sedimen diambil di bagian tepi pelabuhan yang berjarak 50 - 200 m dari
pinggir pelabuhan pada 9 titik dengan empat kali pengulangan pengambilan sampel sedimen diambil dengan menggunakan eckman grab dan dimasukan kedalam plastik transparan, selanjutnya disimpan dalam coolbox. Kemudian
sampel sedimen dibawa ke laboratorium untuk dianalisis. Lokasi pengambilan sampel sedimen di Pelabuhan Panjang dapat dilihat pada
Gambar 6.
37
3. Preparasi Sampel
a. Preparasi Sampel Untuk Menentukan Kadar Logam Cd
Sedimen basah dikeringkan dalam oven 110 oC hingga diperoleh berat konstan. Sedimen kering dihaluskan dan disaring dengan ukuran pori 125 mess,
kemudian ditimbang dengan teliti 20 g. Sedimen yang telah disaring
dimasukkan ke dalam elenmeyer kemudian ditambahkan 30 ml HNO3 pekat
dan digoyangkan selama 30 menit, kemudian didiamkan selama 3 jam pada suhu ruang. Setelah didiamkan selama 3 jam ditambahkan 100 ml akuades kemudian disaring dengan menggunakan kertas saring. Sisa sedimen pada
kertas saring dicuci dengan 10 ml akuades sebanyak lima kali pengulangan sampai pH berkisar 2-3. Filtrat yang dihasilkan kemudian dianalisis dengan
Spektrofotometer Serapan Atom
c. Preparasi Sampel Untuk Menentukan Kadar Logam Ni
Sedimen basah dikeringkan dalam oven 110 oC hingga diperoleh berat konstan. Sedimen kering dihaluskan dan disaring dengan ukuran pori 125
mess, kemudian ditimbang dengan teliti 20 g . Sedimen yang telah
dihaluskan dimasukkan ke dalam gelas piala kemudian ditambahkan HCl dan
HNO3 dengan perbandingan 3 :1 dan total jumlah volume 50 mL sampai pH berkisar antara 2-3 dan digoyangkan selama 30 menit, kemudian didiamkan selama 3 jam pada suhu ruang. Setelah didiamkan selama 3 jam,
38
sebanyak lima kali pengulangan. Filtrat yang dihasilkan kemudian diukur
dengan Spektrofotometer Serapan Atom untuk menentukan kadar logam Ni.
4. Penentuan Konsentrasi Cd dan Ni pada Sedimen dengan Spektrofotometer Serapan Atom (SSA)
Penentuan konsentrasi logam Cd dan Ni pada sampel dilakukan dengan teknik
kurva kalibrasi. Masing-masing konsentrasi larutan standar, serapannya diukur dengan Spektrofotometer Serapan Atom pada kondisi optimum. Dari grafik kurva standar terdapat korelasi antara Konsentrasi (x) dengan Absorbansi (y). Dengan
menggunakan persamaan regresi linier maka konsentrasi dari sampel dapat diketahui :
y = a + bx ………..(1)
Keterangan :
y : Absorbansi Sampel x : Konsentrasi dari kurva kalibrasi a : Intersep b : Slope
Setelah konsentrasi dari kurva kalibrasi atau Creg diketahui dari persamaan 1, maka konsentrasi sebenarnya dari Cd dan Ni dalam sampel kering dapat
ditentukan dengan persamaan berikut (Siaka, 2008) :
Keterangan :
M : Konsentrasi logam dalam sampel (mg/Kg)
39
B : Bobot sampel (g) F : Faktor Pengenceran
5. Validasi Metode
Penelitian ini menggunakan 4 validasi metode yaitu limit deteksi, presisi, akurasi dan Linearitas.
a. Limit Deteksi
Pada penelitian ini batas deteksi ditentukan dengan mengukur respon blanko sebanyak 5 kali dan dihitung simpangan baku respon blangko.
b. Presisi
Presisi dilakukan dengan mengukur konsentrasi sampel dengan 4 kali pengulangan. Nilai absorbansi yang diperoleh kemudian ditentukan nilai konsentrasi (persamaan regresi larutan standar), lalu nilai simpangan baku
(SD) dan simpangan baku relatif (RSD) dapat ditentukan. Metode dengan presisi yang baik yaitu dengan perolehan simpangan baku relatif (RSD) <5 %
(Christian, 1994).
c. Akurasi
Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Pada penelitian ini, persen perolehan kembali ditentukan
40
d. Linieritas
Linieritas dapat diukur dengan melakukan pengukuran tunggal pada
konsentrasi yang berbeda –beda. Data yang diperoleh selanjutnya diproses
61
V. KESIMPULAN
A. Simpulan
Berdasarkan hasil analisis dan Pembahasan pada penelitian ini, maka diperoleh kesimpulan
sebagai berikut :
1. Distribusi logam Cd hampir merata yaitu pada titik Ax, Ay,Az, Bx,By, Bz dan Cx
masing- masing konsentrasi logam berat Cd sebesar (152,7391 ± 0,0239 ) ppm, (153,0370 ± 0,0674) ppm, (153,2679 ± 0,1152) ppm, (152,9886 ± 0,0622) ppm, (153,0238 ± 0,0519) ppm, (152,4434 ± 0,2089) ppm, (152,5259 ± 0,0999) ppm.
Berdasarkan hasil yang diperoleh konsentrasi logam berat Cd berada di atas baku mutu yang telah ditetapkan oleh National sediment Quality Survey USEPA, yaitu pada rentang
Cd 0,65 – 2,49 ppm
2. Berdasarkan National sediment Quality Survey USEPA, baku mutu konsentrasi logam berat Ni pada sedimen adalah sebesar 23,77 – 80,07 ppm. Hasil analisis logam Ni pada
sedimen di Pelabuhan Panjang menunjukan bahwa distribusi logam berat Ni terdapat pada titik pengambilan sampel Ax, Ay, Az, Bx, By, Bz, dan Cx telah melebihi baku
62
3. Konsentrasi logam Cd dan Ni pada sedimen dipengharui oleh jenis sedimen yang didapat 4. Analisis logam Cd dan Ni pada sampel sedimen dapat dilakukan dengan menggunakan
alat spektrofotometer serapan atom (SSA) karena pada analisis dengan metode ini menghasilkan validasi yang yang baik yang masih dalam batas standar yang ditentukan.
B. Saran
Keberadaan Logam berat Cd dan Ni yang telah melebihi baku mutu yang telah ditetapkan
oleh National Sediment Quality Survey USEPA, secara langsung memiliki dampak negatif terhadap biota perairan maupun kesehatan masyarakat yang tinggal disekitar Pelabuhan
Panjang. Untuk selanjutnya, perlu dilakukan penanggulangan terhadap keberadaan logam berat pada sedimen di perairan pelabuhan Panjang baik dengan proses kimiawi yaitu penambahan senyawa kimia seperti penyerapan menggunakan karbon aktif,elektrodialisis,
63
DAFTAR PUSTAKA
Anonim 1. 2013. Profil Pelabuhan Panjang Bandar Lampung. Diakses pada tanggal 20 Oktober 2013 pukul 10.00 WIB. http: //www. panjangport.co.id
Anonim 2. 2013. Penggunaan Logam Berat Nikel Dalam Bidang Industri. Diakses pada tanggal 20 Oktober 2013 pukul 11.00 WIB. http: //www.
wikipedia.org/wiki/Industri.
Anonim 3. 2010. Pelatihan Instrumental Kimia AAS dan X-R.Diaksespadatanggal 20 oktober 2013 pukul 15.00 WIB.http://www.stembatema.com
AOAC.1993. Peer Verified Methods Program, Manual on Policies and Procedures. Arlington. VA
Astuti, D. P. 2012.KajianSebaranLogamBerat Cd dan Cr PadaSedimen di Pesisir Pantai Way Kuala Bandar Lampung.Skripsi.UniversitasLampung.Bandar Lampung.
Bapeldalda Kota Bandar Lampung. 2003. Pengawasan Sumber-Sumber Potensi Pencemaran di Kota Bandar Lampung. BPPLH. Bandar Lampung
BPS. 2012. Lampung DalamAngka. BadanPusatStatistik. Provinsi Lampung. Buchanan, J. B. 1984. Sediment Analysis and Suspended Particulated Matter,
Fisheries and Marine Service Technical Report No. 700, Environmental. Canada.
Clark, D. V. 1986. Heavy Metal in Sediment. Butterworth-Heinemann. USA. Connel, DW. dan GJ. Miller. 1995. Kimia dan Ekotoksikologi
Pencemaran.Terjemahan Yanti Koestoer. 1995.Universitas Indonesia Press.Jakarta.
64
Darmono. 1995. Logam dalam Sistem Biologi Makhluk Hidup. Universitas Indonesia pers. Jakarta.
Effendi, H. 2003.TelaahKualitas Air
bagiPengolahanSumberDayadanLingkunganPerairan.PenerbitKanisius. Yogyakarta.
Ellwel, W. T. danJ.A. Gidley. 1996. Atomic Adsorption Spectrophotometry. Research Departemen Imperial Metal Industries Ltd. England.Ied.
Ernawati. 2010. Kerangbulu (Anadarainflata)
SebagaiBioindikatorPencemaranLogamBeratTimbal (Pb) dan Cadmium (Cd) di Muara Sungai Asahan. Tesis. Program Studi Magister Biologi, FMIPA, Universitas Sumatera Utara. Medan.
Fardiaz,S., 2006.Polusi Air danUdara.Kanisius.Yogyakarta.
Gobas, F.A.P.C., J.B. Wilcockson, R.W. Russeldan G.D. Haffner. 1999. Mechanism of Biomagnification in Fish Under Laboratory and Field Condition.
Enviromental Science and Technology.
Gross, M.G.1990.Oceanography : A View of Earth. Prentice Hall, Inc. Englewood Cliff .
New Jersey
Helfinalis.2000. AspekOseonografiBagiPeruntukanLahan di Wilayah PantaiTelukLampung.PPPLO-LIPI, Jakarta.
Hutagalung, H. P. 1991. PencemaranLautolehLogamBerat: Status Pencemaranlaut di Indonesia
danTeknikPemantauannya.PusatPenelitiandanPengembanganOseanologiLem bagaIlmuPengetahuan Indonesia. Jakarta.
KMNLH.2004. PedomanPenetapan Baku MutuLingkungan. Kantor Menteri Negara KependudukanLingkunganHidup. KeputusanMenteri Negara
KependudukandanLingkunganHidup.Kep-51/MNLH/2004.Sekretariat Negara, Jakarta.
Kusnoputranto, H. 2006. ToksikologiLingkungan, LogamToksikdanBerbahaya. FKM-UI Press danPusatPenelitianSumberDayaManusiadanLingkungan. Jakarta.
65
Mukono. 2009. ToksologiLogamBerat B3 danDampaknyaTerhadapkesehatan. FakultasKesehatanUniversitasairlangga. Surabaya.
Novita, N. P. 2010. Kajian Sebaran Logam Berat Pb dan Cd di Muara Sungai Way Kuala Bandar Lampung. Universitas Lampung. Bandar Lampung.
Odum, E. P. 1971. Dasar-DasarEkologi.EdisiKetigaGadjahMadaUniversty Press. Yogyakarta.
Pallar, H. 1994.PencemarandanToksikologiLogamBerat.Rineka Cipta. Jakarta. Pariwono, J.I. 1999. KondisiOseanografiPerairanPesisir Lampung. ProyekPesisir
Publish. Jakarta.
Pelindo II, PT. 2001. RencanaStrategisPelabuhanPanjang 2002-2006.Pelindo II CabangPanjang. Bandar Lampung.
Pipkin, B.W.1977.Laboratory Exercise in Oceanography. W.H Freeman and Company. San Fransisco.
Ructiyatun,E.,Edward, dan A.Rozak.2007.Pemantauan Kadar LogamBeratdalam Sedimen di PerairanTeluk
Jakarta.PusatPenelitianOseonegrafi-LIPI.Jakarta.
Ruiz, F. 2001. Trace Metal in Estuarime Sediments From The Southwestern Spanish Coast.Marine Pollution Bulletin. Huelva University
Slavin, M. 1987.Atomic Absorption Spectroscopy Second Edition.United State of America. New York.
Siaka, M. I. 1998. The Application of Atomic Absorption Spectroscopy to the Determation of Selected Trace Element in Sediment of the Coxs River Catchement. Departement of Chemistry.Faculty of Science and Technology.University of Western Sydney Nepean.
Sulistiani, W. S. 2009. AnalisisSimultanLogamBeratPb, Cu, Zn, Cr, Mn, Ni, Fe dan Cd
PadaBioindikatorRemis (Eremopyrguseganensis) di Sungai Kuripan Lampung Menggunakan ICP-OES.Skripsi.FMIPA.Universitas Lampung
Sutamihardja, R.T.M.,dan K. Adnan . 1982. PerairanTeluk Jakarta Ditinjaudari Tingkat Pencemaran. FakultasPascasarjana. Jurusan PSL- IPB. Bogor.
66
USEPA. 2004. The Incidence and Severity of Sediment Contamination in Surface Waters of United States, National Sediment Quality Survey :Second Edition. EPA-823-R-04-2007.U. S. Enviromental Protection Agency, Washington D.C.
Ward, A. D. dan W. Stanley .Trimble. 2004. EviromentalHidrology 2nd Edition.United States of Amerika. New York.
Wiryawan, B., B. Marsden, H.A. Susanto, A.K. Mahi, M. Ahmad dan H. Poespitasari (Editor). 1999. Atlas Sumberdaya Wilayah Pesisir Lampung. Kerjasama PEMDA Propinsi Lampung denganProyekPesisir (CoastalResources Center, University of Rhode Island dan PusatKajianSumberdayaPesisir dan Lautan, InstitutPertanianBogor). Bandar Lampung. Indonesia.
Wiryawan, B., B. Marsden, H.A. Susanto, A.K. Mahi, M. Ahmad,dan H.
Poespitasari. 2002. RencanaStrategisPengelolaan Wilayah Pesisir Lampung. PKSPL IPB. Bandar Lampung.
Wright, D.A dan W. Pamela. 2002. Enviromental Toxicology, Cambridge Environmetal Chemistry series 11, Cambridge University Press.
Yudha, I. G. 2007. KajianPencemaranLogamBerat di Wilayah Pesisir Kota Bandar Lampung.Universitas Lampung. Bandar Lampung.