ANALISIS KADAR LOGAM KADMIUM (Cd), KROMIUM (Cr), TIMBAL (Pb), DAN BESI (Fe) PADA HEWAN UNDUR-UNDUR DARAT (Myrmeleon Sp.) DENGAN METODE SPEKTROFOTOMETRI SERAPAN
ATOM (SSA)
SKRIPSI
SRININGSIH HUTAGALUNG 090802009
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
ANALISIS KADAR LOGAM KADMIUM (Cd), KROMIUM (Cr), TIMBAL (Pb), DAN BESI (Fe) PADA HEWAN UNDUR-UNDUR DARAT (myrmeleon Sp.)
DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar sarjana sains
SRININGSIH HUTAGALUNG 090802009
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGEAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : ANALISIS KADAR LOGAM KADMIUM (Cd), KROMIUM (Cr), TIMBAL (Pb), DAN BESI (Fe) PADA HEWAN UNDUR-UNDUR DARAT ( Myrmeleon Sp. ) DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM (SSA).
Kategori : SKRIPSI
Nama : SRININGSIH HUTAGALUNG Nomor Induk Mahasisw : 090802009
Program Studi : SARJANA (S1) KIMIA Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
Disetujui di Medan, Januari 2014
Komisi Pembimbing :
Dosen Pembimbing II Dosen Pembimbing I
Drs.Ahmad Darwin Bangun, M.Sc Dr. Tini Sembiring, MS
NIP.19521116198003001 NIP.194805131971072001
Diketahui / disetujui oleh
Departemen Kimia FMIPA USU Ketua
PERNYATAAN
ANALISIS KADAR LOGAM Cd, Cr, Pb, DAN Fe PADA HEWAN UNDUR-UNDUR DARAT (myrmeleon Sp.) DENGAN METODE
SPEKTROFOTOMETRI SERAPAN ATOM (SSA)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Januari 2014
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yesus Kristus untuk setiap kasih karuniaNya penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini. Banyak hal yang penulis rasakan disetiap penyertaannya sehingga semakin merasakan kebaikan dan kebesaranNya yang sangat luar biasa. Dalam pelaksanaan penelitian ini hingga penyelesaian skripsi ini, penulis menyadari banyak mendapat bantuan, dukungan, maupun motivasi dari berbagai pihak. Untuk itu pada kesempatan ini penulis mengucapkan terimakasih Kepada :
1. Ibu Dr.Tini Sembiring, MS sebagai pembimbing I dan Bapak Drs. Ahmad Darwin Bangun, M.Sc sebagai pembimbing II yang dengan sbar telah memberikan dorongan, bimbingan, dan asaran sehingga skripsi ini dapat selesai. 2. Ibu Dr. Rumondang Bulan, MS dan Bapak Drs. Albert Pasaribu, M.Sc sebagai ketua dan sekretaris departemen Kimia FMIPA USU.
3. Bapak Prof. Harlem Marpaung selaku kepala Laboratorium bidang kimia
analitik FMIPA USU. 4. Seluruh Dosen Departemen Kimia FMIPA USU yang telah memberikan waktunya untuk memberikan bimbingan selama penulis mengikuti kuliah di Departemen Kimia FMIPA USU , terkusus kepada Ibu Dra. Saur Lumban Raja, M,Si sebagai Dosen Wali yang tlah menyediakan waktunya untuk memberikan pengarahan dalam menyelesaikan studi selama perkuliahan dan penelitian
berlangsung. 5. Laboran dan seluruh asisten Kimia Analitik FMIPA USU yang
telah membantu penulis dalam menyelesaikan penelitian. 6. Seluruh Teman-teman stambuk 2009 dan teman-teman alumni SMA Sipahutar (terkhusus Mattatias, Usowan, Rivana)
7.Teman-teman KMK terkhusus keluarga kedua Thabita, buat dukungan , perhatian dan semangat yang tidak habis-habisnya diberikan kepada penulis 8. Pihak-pihak yang tida disebutkan namun dengan tulus membantu penulis dalam menyelesaikan skripsi ini.
Akhirnya penulis mengucapkan terimakasih dan penghargaan yang sebesar-besarnya kepda kedua orang tua saya ( Alm. B. Hutagalung dan M. Pakpahan Amd) yang telah member seluruh dkungan sarana prasarana dan semangat bahkan dengan setia selalu membawa penulis dalam doa, saudara-saudaraku ( Hendra Hutagalung, Minarty Hutagalung Amd, Hermanto Hutagalung SPd, Erwinton Hutagalung, Hasan Ht.galung, dan Benni Ht.galung) dan seluruh keluarga Hutagalung dan Pakpahan atas doa dan dukugannya. Penulis menyadari skripsi ini masih jauh dari sempurna, oleh karena itu, saya mengharapkan saran dan masukan yang membangun demi kesempurnaan skripsi ini dan semoga skripsi ini dapat bermanfaat bagi kita semua .
ANALISIS KADAR LOGAM KADMIUM (Cd), KROMIUM (Cr), TIMBAL (Pb), DAN BESI (Fe) PADA HEWAN UNDUR-UNDUR
DARAT (Myrmeleon Sp.) DENGAN METODE SPEKTROFOTOMETRISERAPAN
ATOM (SSA)
ABSTRAK
Telah dilakukan penelitian tentang analisis kandungan logam berat Kadmium (Cd), Kromium (Cr), Timbal (Pb), Besi (Fe), didalam Undur-undur Darat. Sampel destruksi kering diikuti dengan pelarutan abunya dengan HNO3(p) dan H2O2 30 %.
Uji kualitatif dilakukan dengan alat Inductively Coupled Plasma – Optical Emission (ICP-OES) dan penentuan kandungan logam Cd,Cr, Pb, dan Fe dilakukan dengan metode Spektrofotometri Serapan Atom (SSA) pada panjang gelombang untuk logam Cd λ = 228,8 nm; Cr λ = 359,3 nm; Pb λ = 283,3 nm; dan
ANALYSIS LEVELS METALS CADMIUM (Cd), CROMIUM (Cr), PLUMBUM (Pb), AND IRON (Fe) OF LAND ANT-LION
(Myrmeleon SP.) WITH METHODS ATOMIC ADSORPTION SPECTROPHOTOMETRY
ABSTRACT
The analisis of heavy metals Cadmium (Cd), Cromium (Cr), Plumbum (Pb). And Iron (Fe),in Lnd Ant-Lion. The Land Ant-Lion was dry digestion and than the ash of land ant-lion dissolved with HNO3(p) and H2O2 30 % concentrated, Quatatif
test using Inductivelyn Coupled Plasma – Optical Emission ( ICP-OES) and determination of Cd, Cr, Pb, and Fe content using Atomic Absorption Spectrophotometry (AAS) at wavelength for Cd λ = 228,8 nm; Cr λ = 359,3 nm;
DAFTAR ISI
2.5. Inductively Coupled Plasma-Optical Emission Spectrometry 19
b. Larutan Standar Cd2+ 100 mg/L 28
4.1.3.3. Penentuan Kadar Cadmium Dalam Sampel 45
4.1.3.3.1. Penentuan Kadar Cd Metode SSA 45
dalam mg/L 4.1.3.3.2. Penentuan Kadar Cd Metode SSA 46
dalam mg/kg 4.1.4. Logam Kromium (Cr) 46
4.1.4.1. Penurunan Persamaan Garis Regresi 47
4.1.4.2. Penentuan Koefisien Korelasi Kromium 48
4.1.4.3. Penentuan Kadar Kromium Dalam Sampel 49 4.1.4.3.1. Penentuan Kadar Cr Metode SSA 50 dalam mg/L 4.1.4.3.2. Penentuan Kadar Cr Metode SSA 51 dalam mg/kg 4.1.5. Logam Timbal (Pb) 51
4.1.5.1. Penurunan Persamaan Garis Regresi 52
4.1.5.2. Penentuan Koefisien Korelasi Timbal 53
4.1.5.3. Penentuan Kadar Timbal Dalam Sampel 54
4.1.5.3.1. Penentuan Kadar Pb Metode SSA 54
dalam mg/L 4.1.5.3.2. Penentuan Kadar Pb Metode SSA 56
dalam mg/kg 4.2. Pembahasan 56
Bab 5. KESIMPULAN DAN SARAN 5.1. Kesimpulan 59
5.2. Saran 59
DAFTAR TABEL
No. Tabel Judul Halaman
1. Tabel 4.1 Kandungan Logam yang Terdapat dalam 36 Sampel Untuk Uji Kualitatif dengan ICP – OES
2. Tabel 4.2 Data Pengukuran Absorbansi Larutan Seri 37 Standar Besi
3. Tabel 4.3 Penurunan Persamaan Garis Regresi untuk 38 Penentuan Konsentrasi Logam Besi (Fe)
Berdasarkan Pengukuran Absorbansi Larutan Standar Besi (Fe)
4. Tabel 4.4 Data Absorbansi Larutan Standar Tembaga (Cd) 42 5. Tabel 4.5 Penurunan Persamaan Garis Regresi untuk 43
Penentuan Konsentrasi Logam Cadmium (Cd) Berdasarkan Pengukuran Absorbansi
Larutan Standar Cadmium (Cd).
6. Tabel 4.6 Data Absorbansi Larutan Standar Kromium (Cr) 47 7. Tabel 4.7 Penurunan Persamaan Garis Regresi untuk 47
Penentuan Konsentrasi Logam Kromium (Cr) Berdasarkan Pengukuran Absorbansi Larutan Standar Kromium (Cr)
8. Tabel 4.8 Data Absorbansi Larutan Standar Timbal (Pb) 52 9. Tabel 4.9 Penurunan Persamaan Garis Regresi untuk 52
DAFTAR GAMBAR
No. Gambar Judul Halaman
1. Gambar 2.1 Undur-undur Darat 6
2. Gambar 2.2 Sarang Undur-undur Darat 7
3. Gambar 2.3 Metamrfosa Undur-undur Darat 8
4. Gambar 2.4 Pupa Undur-undur Darat 8
5. Gambar 2.5 Capung Undur-undur Darat 8
6. Gambar 2.6 Komponen utama dan susunan dari peralatan 21
Inductively Coupled Plasma – Optical Emission Spectrometry 7. Gambar 4.1 Kurva kalibrasi larutan seri standar logam Fe 39
8. Gambar 4.2 Kurva kalibrasi larutan seri standar logam Cd 45
9. Gambar 4.3 Kurva kalibrasi larutan seri standar logam Cr 49
DAFTAR LAMPIRAN
No. Lampiran Judul Halaman
1. Lampiran 1 Kondisi Alat SSA Pada Pengukuran 64
Konsentrasi Fe
2. Lampiran 2 Data Hasil Pengukuran Absorbansi 64 Larutan Seri Standar Fe dengan
Spektrofotometer Serapan Atom
3. Lampiran 3 Kondisi Alat SSA Pada Pengukuran 64 Konsentrasi Cd
4. Lampiran 4 Data Hasil Pengukuran Absorbansi 65 Larutan Seri Standar Cd dengan
Spektrofotometer Serapan Atom
5. Lampiran 5 Kondisi Alat SSA Pada Pengukuran 65 Konsentrasi Cr
6. Lampiran 6 Data Hasil Pengukuran Absorbansi 65 Larutan Seri Standar Cr dengan
Spektrofotometer Serapan Atom
7. Lampiran 7 Kondisi Alat SSA Pada Pengukuran 66 Konsentrasi Pb
8. Lmpiran 8 Data Hasil Pengukuran Absorbansi 66 Larutan Seri Standar Pb dengan
Spektrofotometer Serapan Atom
9. Lampiran 9 Perbandingan Konsentrasi Logam Cd, Cr, Pb dan 66 Fe Dalam Sampel Undur-undur Darat Dengan
Standart BPOM Tentang Ambang Batas Logam Dalam Obat yang Bisa Dikomsumsi
10. Lampiran 10 Kondisi Alat ICP – OES Merek Varian pada Uji 67 Kualitatif Cd, Cr, Pb, dan Fe dalam Undur-undur
ANALISIS KADAR LOGAM KADMIUM (Cd), KROMIUM (Cr), TIMBAL (Pb), DAN BESI (Fe) PADA HEWAN UNDUR-UNDUR
DARAT (Myrmeleon Sp.) DENGAN METODE SPEKTROFOTOMETRISERAPAN
ATOM (SSA)
ABSTRAK
Telah dilakukan penelitian tentang analisis kandungan logam berat Kadmium (Cd), Kromium (Cr), Timbal (Pb), Besi (Fe), didalam Undur-undur Darat. Sampel destruksi kering diikuti dengan pelarutan abunya dengan HNO3(p) dan H2O2 30 %.
Uji kualitatif dilakukan dengan alat Inductively Coupled Plasma – Optical Emission (ICP-OES) dan penentuan kandungan logam Cd,Cr, Pb, dan Fe dilakukan dengan metode Spektrofotometri Serapan Atom (SSA) pada panjang gelombang untuk logam Cd λ = 228,8 nm; Cr λ = 359,3 nm; Pb λ = 283,3 nm; dan
ANALYSIS LEVELS METALS CADMIUM (Cd), CROMIUM (Cr), PLUMBUM (Pb), AND IRON (Fe) OF LAND ANT-LION
(Myrmeleon SP.) WITH METHODS ATOMIC ADSORPTION SPECTROPHOTOMETRY
ABSTRACT
The analisis of heavy metals Cadmium (Cd), Cromium (Cr), Plumbum (Pb). And Iron (Fe),in Lnd Ant-Lion. The Land Ant-Lion was dry digestion and than the ash of land ant-lion dissolved with HNO3(p) and H2O2 30 % concentrated, Quatatif
test using Inductivelyn Coupled Plasma – Optical Emission ( ICP-OES) and determination of Cd, Cr, Pb, and Fe content using Atomic Absorption Spectrophotometry (AAS) at wavelength for Cd λ = 228,8 nm; Cr λ = 359,3 nm;
BAB 1 PENDAHULUAN
1.1. Latar Belakang
Akhir-akhir ini masyarakat Indonesia banyak yang beralih pada pengobatan
tradisional. Kepercayaan masyarakat terhadap pengobatan tradisional semakin
tinggi karena mulai banyak ahli pengobatan tradisional yang berhasil dan menjadi
populer lewat media massa. Pengobatan tradisional juga dirasa lebih murah
dibandingkan dengan pengobatan modern. Selain itu, masyarakat beralih pada
pengobatan tradisional karena takut akan efek samping dari obat-obatan sintetis
yang dibuat di pabrik. Akhirnya, banyak masyarakat yang meminimalisir
mengkonsumsi obat buatan dan memanfaatkan pengobatan tradisional
(http://blogspot.com/2012/10/karya-tulis-undur-undur-darat-myrmeleon.html#)
Salah satu pengobatan tradisional untuk penyakit diabetes mellitus adalah
dengan mengkonsumsi undur-undur darat (myrmeleon sp.). Di samping karena khasiatnya, harganya juga terbilang cukup murah. Kepopulerannya terbukti dari
semakin banyaknya kalangan pebisnis yang membudidayakan dan menjual
serangga yang berjalan mundur ini. Binatang kecil yang biasa dijumpai di sekitar
rumah berhalaman pasir itu telah terbukti ampuh menurunkan gula darah
(Hidayatul dkk, 2003) .
Undur-undur darat dengan nama latin Myrmeleon sp hewan ini adalah hewan yang unik sesuai dengan namanya undur-undur hewan ini dapat berjalan
mundur hewan ini merupakan “anak” Kinjeng Dom atau Capung jarum. Capung
Jarum merupakan capung kecil yang mirip jarum.Hewan sekecil kutu anjing yang
biasa dijumpai di sekitar rumah berhalaman pasir ini ampuh menurunkan gula
darah.Dalam bahasa mandarin undur-undur darat bernama di-gu-niu dan dalam
bahasa Inggris disebut
termasuk dalam keluarga Myrmeleontidae, yang berasal dari Yunani dari
mempunyai mulut penggigit dan dua pasang sayap yang urat-uratnya berbentuk
seperti jala (Nugroho, 2008).
Berdasarkan penelitian yang diketuai oleh Tyas Kurniasih,dkk dari
Universitas Gajah Mada yang berjudul Kajian Potensi Undur-Undur Darat
(Myrmeleon sp.) 2006, diketahui bahwa binatang tersebut mengandung zat sulfonylurea. Kerja sulfonylurea pada undur-undur darat adalah melancarkan kerja pankreas dalam memproduksi insulin. Dalam hal ini, insulin digunakan untuk
menurunkan kadar gula darah yang menjadi masalah bagi penderita DM, dan
penelitian Femi Dwi Aldini,dkk menunjukkan bahwa terdapat pengaruh yang
cukup signifikan antara penggunaan undur-undur dengan terjadinya kerusakan sel
pada jaringan hepar.
Toksisitas logam pada manusia menyebabkan beberapa akibat negatif
tetapi yang terutama adalah timbulnya kerusakan pada jaringan, terutama jaringan
ekskresi (hati dan ginjal) (Darmono. 1995).
Seperti pada umumnya jika kita minum obat apapun tidak boleh berlebihan.
Demikian juga yang terjadi pada undur-undur yang dikonsumsi untuk
menurunkan gula darah juga tidak boleh berlebihan karena mengkonsumsi
undur-undur terlalu banyak bisa menyebabkan badan panas, diare , dan pusing. Cara
mengonsumsinya ada dua macam. Pertama, langsung ditelan sebanyak 3-5 ekor,
sehari dua kali. Kedua, dimasukkan ke dalam kapsul, lalu diminum sehari dua kali
(pagi dan sore)
Masyarakat sering tidak mengetahui kandungan dan reaksi tubuh terhadap
bahan yang dikonsumsinya, tetapi mereka tetap mengkonsumsi karena dirasakan
adanya perbaikan. Berdasarkan hal tersebut, maka diperlukan dasar-dasar ilmiah
tentang kandungan, efek pada tubuh dalam jangka panjang dan korelasi dengan
reaksi tubuh terhadap berbagai zat yang terkandung. Upaya untuk menyembuhkan
gejalanya saja, tetapi juga harus memperhitungkan efek samping yang muncul
dari pengobatan tersebut.
Metode yang sangat umum digunakan unuk penentuan kadar logam berat
dalam jumlah kecil biasanya menggunakan SSA, ICP, dan lain sebagainya.
Namun penggunaan SSA lebih umum karena penggunaannya yang mudah, cepat,
sensitif dan biaya pengoperasian relatif murah. Tetapi alat ini hanya dapat
digunakan untuk uji kuantitatif. Metode ICP-OES memiliki beberapa kelebihan
disbanding metode SSA karena metode ini sangat selektif dan dapat digunakan
untuk analisa kulitatif dan kuantitatif beberapa unsur sekaligus di dalam sampel
pada saat pengukuran , namun metode ini lebih rumit iay pengoperasian reatif
mahal dan ketersediaan alat yang masih terbatas .
Berdasarkan latar belakang diatas peneliti tertarik untuk melakukan
penelitian tentang kandungan logam Cr, Cd, Pb, dan Fe pada undur-undur darat
(myrmeleon sp.) karena logam tersebut dapat menimbulkan keracunan dalam tubuh dan bahkan menimbulkan kematian jika tidak memenuhi standar yang
ditentukan.
1.2. Permasalahan
a. Apakah Undur-undur Darat (myrmeleon sp.) mengandung logam Cd, Cr, Pb, dan Fe ?
b. Berapakah kandungan logam Cd, Cr, Pb, dan Fe yang terkandung pada
undur Darat (myrmeleon sp.) ?
c. Apakah kadar logam Cd, Cr, Pb, Fe, dan Zn yang terdapat pada undur-undur
darat (myrmeleon sp.) masih memenuhi standar ambang batas BPOM.?
d. Apakah dengan mengonsumsi 3-5 ekor Undur-undur Darat masih memenuhi
1.3. Pembatasan Masalah
a. Dalam penelitian ini Undur-undur yang di analisis adalah Undur-undur Darat
(myrmeleon sp.)
b. Sampel diambil dari Silantom Jae Kecamatan Pangaribuan Kabupaten
Tapanuli Utara dengan beberapa kali pengambilan.
c. Ukuran dan berat Undur-undur Darat dianggap sama.
d. Logam yang dianalisis adalah logam Cd, Cr, Pb, dan Fe
e. Uji kualitatif dilakukan dengan metode ICP-OES
f. Uji kuantitatif dilakukan dengan menggunakan metode Spektrometer Serapa
Atom (SSA)
1.4. Tujuan Penelitian
a. Penelitian ini bertujuan untuk mengetahui apakah logam Cd, Cr, Pb, dan Fe
terkandung dalam Undur-undur Darat (myrmeleon sp.) .
b. Untuk mengetahui berapa kadar logam Cd, Cr, Pb, dan Fe yang terkandung
dalam Undur-undur Darat (myrmeleon sp.) .
c. Untuk mengetahui apakah kadar logam Cd, Cr, Pb, dan Fe masih memenuhi
standar ambang batas BPOM.
d. Untuk mengetahui apakah dengan mengonsumsi Undur-undur Darat 3-5
masih memenuhi standart ambang batas BPOM.
1.5. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi kepada masyarakat
mengenai kandungan logam yg terdapat pada Undur-undur Darat (myrmeleon sp.) sebagai salah satu upaya untuk mengetahui kadar logam tersebut masih sesuai
1.6. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik Fakultas Matematika dan
Ilmu Pengetahuan Alam Universitas Sumatera Utara Medan dan di Laboratorium
Penelitian Fakultas Farmasi USU serta di Laboratorium Balai Teknik Kimia
Lingkungan Medan.
1.7. Metodologi
a. Penelitian ini adalah merupakan eksperimen laboratorium
b. Metode pengambilan sampel dilakukan secara acak dan dalam beberapa kali
pengambilan.
c. Sampel Undur-undur Darat kemudian dihilangkan kadar airnya dengan
pemanasan dalam oven pada suhu 105-110o C kemudian dihaluskan
d. Dekstruksi Sampel Undur-undur Darat yang telah dihaluskan dilakukan dengan
metode dekstruksi kering dengan pemanasan dalam tanur 550 – 600o C selama
2 jam dan dilanjutkan dengan pelarutan sampel menggunakan HNO3(p), dan
H2O2 30 %.
e. Uji kualitatif dilakukan dengan metode ICP-OES
f. Uji kualitatif dengan penentuan kandungan logam Cd, Cr, Pb, dan Fe pada
Undur-undur Darat dilakukan dengan metode Spektrofotometri Serapan Atom
(SSA) dengan panjang gelombang untuk logam Cd λ = 228,8 nm; Cr λ =
BAB 2
TINJAUAN PUSTAKA
2.1. Undur-undur Darat
Undur-undur adalah kelompok binatang holometabola, yaitu serangga yang mengalami metamorfosis sempurna. Tahapan dari daur serangga yang mengalami
metamorfosis sempurna adalah telur, larva, pupa, lalu menjadi imago. Larva adalah hewan muda yang bentuk dan sifatnya berbeda dengan hewan dewasa.
Pupa adalah kepompong dimana pada saat itu serangga tidak melakukan kegiatan. Akan tetapi, pada saat itu terjadi penyempurnaan dan pembentukan organ.
Sedangkan imago adalah fase dewasa atau fase perkembangbiakan (Nugroho,
2008).
Gambar 2.1. Undur undur darat (Myrmeleon sp.)
Undur-undur yaitu mempunyai Ordo Neuroptera (serangga bersayap jala),
famili myrmeleontidae. Ciri-ciri: serangga ini mempunyai mulut menggigit, dan
mempunyai dua pasang sayap yang urat-uratnya berbentuk seperti jala. Dalam
bahasa latinnya : Myrmeleon formicarius atau lion ant dalam bahasa inggris.
Dalam versi yang lain Undur-undur juga mempunyai family Myrmecoleonidae
Undur-undur darat diklasifikasikan sebagai berikut:
Kerajaan : Animalis
Devisi : Magnoliophyza
Kelas : Insecta
Ordo : NeuropteraFamili : Myrmeleontidae
Genus : MyrmeleonSpesies : Myrmeleon Sp.
Undur-undur termasuk binatang pemangsa, membuat sarangnya di tanah
yang kering dan cukup mendapat cahaya. Sarang yang berbentuk tirus atau
kerucut itu juga berfungsi sebagai perangkap. Sarang undur-undur sering dijumpai
diketeduhan atap rumah, atau dibawah lantai rumah yang tinggi. Larva dari
undur-undur mirip sebuah kantung yang berbuku-buku dan memiliki rahang melengkung
yang sangat besar. Ia membuat lubang dalam tanah pasir yang gembur dengan
gerakan spiral ekornya. Tanah yang terlepas dibuang keluar lubang dengan
kepalanya. Pada dasar lubang tersembunyi, rahangnya siap menangkap serangga
kecil yang terperangkap dan menjadi mangsanya.
Gambar 2.2. Sarang undur-undur darat. (Widjajanto, dkk.2007)
Undur-undur memiliki tahapan kehidupan seperti kupu-kupu yaitu
bermetamorfosa. Tahapan dari daur serangga yang di alami undur-undur adalah
Gambar 2.3. Metamorfosa undur-undur
Gambar 2.4. pupa undur-undur
Larva adalah hewan muda yang bentuk dan sifatnya berbeda dengan
dewasa. Pupa adalah kepompong dimana pada saat itu pula terjadi
penyempurnaan dan pembentukan organ. Imago adalah fase dewasa atau fase
perkembangan . Jadi undur-undur merupakan larva dari suatu fase dalam
metamorphosis sempurna serangga.
Undur-undur berkhasiat mengobati penyakit diabetes, terbukti secara
medis, bahkan para dokter menganjurkan pasiennya untuk memakan binatang
undur-undur yang masih hidup tanpa harus dibersihkan air terlebih dahulu. Kalau
terkena air khasiatnya akan hilang. Yang dapat dipercaya menyembuhkan diabetes
dari binatang undur-undur ini salah satunya adalah bulunya. Undur-undur juga
tidak boleh dimakan dalam keadaan mati. Jika merasa jijik, pasien bisa
memasukkan ke kapsul kosong lalu dimakan dengan dorongan air. Kekuatan
hidup undur-undur jika di tempat terbuka (bukan di tanah gembur) bisa bertahan
selama dua hari, jika disediakan tanah gembur, akan bertahan hidup cukup lama.
2.2. Mineral
Dari dalam tanah tumbuhan hijau menghisap zat-zat tertentu melalui akarnya.
Zat-zat ini masuk kedalam tumbuhan dalam bentuk terlarut didalam air. Zat-Zat-zat ini
biasanya berupa garam-garaman dan dinamakan mineral. Mineral ini berlainan
halnya dengan bahan organik seperti karbohidrat, protein, dan lemak tidak dapat
dibuat oleh tumbuh-tumbuhan. Karena itu mineral tergolong bahan tak-organik,
yaitu tidak berasal dari mahluk hidup.
Kalau bahan tumbuhan seperti kayu bakar atau arang kita bakar, akan
tersisa abu. Abu ini terdiri atas bahan mineral yang telah diserap oleh tumbuhan
kedalam bagian tubuhnya. Sewaktu pembakaran, semua bahan organik habis
terbakar menjadi karbon dioksida dan air. Tetapi bahan tak-organik tersisa sebagai
garam-garaman yang bentuknya berupa abu. Didalam abu ini dapat ditemukan
antara lain logam Natrium (Na), Kalsium (Ca), Magnesium (Mg), Seng (Zn), Besi
(Fe), Mangan (Mn), dan Molibden (Mo). Logam-logam ini ada dalam bentuk
senyawa garam Fosfat yang mengandung Fosfor (P), Klorida yang mengandung
Klor (Cl), Yodida yang mengandung Yod (J), Fluorida yang mengandung Fluor
Kalau kita makan tumbuh-tumbuhan, sudah tentu garam-garam inipun akan
memasuki tubuh kita. Didalam tubuh kita mineral seperti kalsium fosfat terdapat
didalam bagian tubuh seperti tulang dan gigi. Demikian pula mineral seperti besi
menjadi bagian hemoglobin, atau juga disebut butir darah merah. Hemoglobin
adalah suatu protein yang kerjanya mengangkut oksigen di dalam darah ke
seluruh bagian tubuh kita.
Di dalam daun-daunan hijau juga ada protein yang bentuknya hampir sama
dengan hemoglobin, yaitu klorofil. Klorofil atau hijau daun tidak mengandung
logam besi, tetapi logam Magnesium. Selain itu mineral seperti natrium dalam
bentuk garam natrium klorida, kalsium dalam bentuk kalsium hidrofosfat, serta
magnesium, dapat terlarut didalam cairan sel tubuh kita. Perananya mengatur
berbagai proses kehidupan. Kalsium misalnya diperlukan sedikit agar darah dapat
mengggumpal. Demikian pula kalsium berperan dalam peristiwa menegang dan
melemasnya otot seperti otot jantung. Sedangkan magnesium diperlukan sebagai
bahan pembentuk enzim. Natrium dan kalium diperlukan untuk mengatur tekanan
cairan tubuh di dalam sel-sel tubuh.
Jadi, mineral-mineral didalam tubuh kita mempunyai dua macam tugas.
Yang pertama ialah sebagai bahan pembentuk bagian-bagian tubuh, seperti tulang
dan gigi. Yang kedua ialah sebagai zat pengatur kelangsungan hidup. Mineral
yang diperlukan oleh manusia ialah kalsium, fosfor, magnesium, kalium, natrium,
mangan, besi, tembaga, kobalt, yodium, belerang, dan seng. Ada mineral yang
diperlukan dalam jumlah yang cukup banyak, yaitu pada kadar 100 g atau lebih
sehari bagi setiap orang dewasa. Mineral seperti ini disebut unsur hara makro.
Termasuk kedalam golongan ini ialah kalium, natrium, kalsium, fosfor,
magnesium, dan klor. Ada pula mineral yang kita perlukan dalam kadar yang
lebih rendah, yaitu tidak lebih dari beberapa mg setiap hari untuk orang dewasa.
Mineral seperti ini disebut unsur hara mikro. Termasuk kedalam golongan ini
Mineral sangat penting bagi metabolisme tubuh. Mineral dapat diibaratkan
sebagai “busi” dari kehidupan karena mineral diperlukan untuk mengaktifkan
ribuan reaksi enzimatis dalam tubuh. Masing-masing mineral tidak bekerja
sendiri, tetapi bekerja secara seimbang satu sama lainnya. Oleh karena itu, bila
kita kelebihan satu mineral akan berakibat defisiensi (kekurangan) mineral
lainnya. Misalnya, kelebihan kalsium akan berakibat hilangnya magnesium dan
seng. Kelebihan natrium dan kalium akan berakibat defisiensi kalsium dan
magnesium. Kelebihan kalsium dan magnesium akan menyebabkan defisiensi
natrium dan kalium. Kelebihan natrium akan menyebabkan kehilangan kalium.
Kelebihan kalium akan berakibat hilangnya natrium. Kelebihan tembaga akan
mengakibatkan kehilangan seng. Kelebihan seng akan berakibat hilangnya
tembaga dan besi. Kelebihan fosfat akan mengakibatkan hilangnya kalsium.
Semuanya itu disebut reaksi berantai defisiensi.(Sembiring. 2000)
2.3. Logam Berat
Logam berat mengacu pada setiap logam yang berat atomnya lebih besar dari
berkisar 50. Ketika terserap kedalam tubuh, secara langsung logam berat beracun
(Eugene. 1990).Unsur logam berat adalah unsur yang mempunyai densitas lebih
dari 5 gr/cm3 (Fardiaz. 1992).
Hg mempunyai densitas 13,55gr/cm3. Diantara semua unsur logam berat,
Hg menduduki urutan pertama dalam hal sifat racunnya, dibandingkan dengan
logam berat lainnya, kemudian diikuti oleh logam berat antara lain Cd, Ag, Ni,
Pb,As, Cr, Sn, Zn (Fardiaz, 1992).
Logam berat termasuk golongan logam dengan kriteria yang sama dengan
logam lain, yaitu:
a. Memiliki kemampuan yang baik sebagai penghantar panas
b. Memiliki kemampuan yang baik sebagai penghantar daya listrik
d. Dapat membentuk alloy dengan logam lain
e. Untuk logam yang padat dapat ditempa
Perbedaannya terletak pada pengaruh yang dihasilkan bila logam berat ini
berikatan dan atau masuk ke dalam tubuh organisme hidup. Logam berat esensial
seperti Zn, Fe, dan Cu, bila masuk ke dalam tubuh dalam jumlah berlebih akan
menimbulkan pengaruh-pengaruh buruk terhadap fungsi fisiologis tubuh. Dan jika
yang masuk adalah logam berat beracun, seperti Pb, Cd, Cr, dan Hg, maka
dipastikan organisme tersebut akan keracunan. Dalam sistem biologi logam berat
bersift toksik, sebab dapat bereaksi dengan protein, enzim dan asam amino.
Logam berat dalam senyawa organic dapat terikat sebagai bio anorganik, yaitu
senyawa logam yang terikat dalam sistem biologi (Heryando Palar, 1994).
2.3.1. Logam Cd
Unsur Cd tanah terkandung dalam bebatuan beku, sedimen, dll. Kadar Cd dalam
tanah dipengaruhi oleh reaksi tanah dan fraksi-fraksi tanah yang bersifat dapat
mengikat ion Cd. Senyawa-senyawa tertentu seperti bahan ligand dapat
mempengaruhi aktivitas ion Cd, yaitu membentuk kompleks Cd-ligan yang stabil
(Lahuddin,2007)
Kadmium (Cd) merupakan salah satu jenis logam berat yang berbahaya karena unsur ini berisiko tinggi terhadap pembuluh darah. Logam ini memiliki tendensi untuk bioakumulasi. Keracunan yang disebabkan oleh kadmium dapat bersifat akut dan keracunan kronis. Logam Cd merupakan logam asing dalam tubuh dan tidak dibutuhkan dalam proses metabolisme. Logam ini teradsorbsi oleh tubuh manusia yang akan menggumpal di dalam ginjal, hati dan sebagian dibuang keluar melalui saluran pencernaan. Keracunan Cd dapat mempengaruhi otot polos pembuluh darah. Akibatnya tekanan darah menjadi tinggi yang kemudian bisa menyebabkan terjadinya gagal jantung dan kerusakan ginjal.
2.3.2. Logam Fe
Besi yang murni adalah logam berwarna putih-perak, yang kukuh dan liat. Besi
membentuk dua deret garam yang penting. Garam-garam besi(II) atau fero
diturunkan dari besi (II) oksida, FeO. Garam-garam ini mengandung kation Fe2+
dan berwarna sedikit hijau. Garam-garam besi(III) atau feri diturunkan dari oksida
besi(III), Fe2O3. Mereka lebih stabil daripada garam besi (II). Zat-zat pereduksi
mengubah ion besi(III) menjadi besi(II). (Svehla, 1990).
Besi merupakan mikroelemen esensial dalam system mahluk hidup.
Logam ini banyak digunakan dalam pabrik dan merupakan logam multiguna. Besi
banyak ditemukan dalam bahan makanan yang jumlahnya bervariasi dari yang
rendah (dalam sayuran) dan yang tinggi (dalam daging). Kandungan ya g rendah
dari Fe dalam makanan akan menyebabkan naiknya efisiensi absorpsi Fe,
disamping itu absorpsi logam lain juga meningkat baik esenssial (Co, Mn,Zn)
maupun toksik (Cd, Pb). Tetapi sebaliknya makanan yang banyak mengandung Fe
dapat menurunkan absorpsi Zn pada manusia dan Cu pada ruminansia.
(Darmono,1995).
Salah satu alasan mengapa Fe toksik pada sel adalah karena Fe
mengkatalis pembentukan hidroksi radikal. Radikal oksigen terkenal toksik pada
sel – sel hidup karena mampu menginduksi peroksida membrane lisosom yang
menyebabkan kerusakan endotel dan paru – paru serta agregasi platelet darah.
(Merian,1994)
2.3.3. Logam Pb
Timbal-senyawa yang mengandung toksik yang tinggi dan lebih dikenal dalam
masyarakat daripada arsenik saat ini. Polusi timbal dianggap oleh para ahli
menjadi masalah lingkungan utama yang dihadapi dunia modern (Meyer. 1990).
tinggi(11,48 gr/ml pada suhu kamar). Ia mudah terlarut dalam asam nitrat yang
sedang pekatnya (8 M). (Svehla, 1990).
1. Sumber dari Alam
Kadar Pb yang secara alami dapat ditemukan dalam bebatuan sekitar 13 mg/kg.
Khusus Pb yang tercampur dengan batu fosfat dan terdapat didalam batu pasir
(sand stone) kadarnya lebih besar yaitu 100 mg/kg. Pb yang terdapat di tanah
berkadar sekitar 5 -25 mg/kg dan di air bawah tanah (ground water) berkisar
antara 1- 60μg/liter.
Secara alami Pb juga ditemukan di air permukaan. Kadar Pb pada air
telaga dan air sungai adalah sebesar 1 -10 μg/liter. Dalam air laut kadar Pb lebih
rendah dari dalam air tawar. Laut Bermuda yang dikatakan terbebas dari
pencemaran mengandung Pb sekitar 0,07 μg/liter. Kandungan Pb dalam air danau
dan sungai di USA berkisar antara 1-10 μg/liter.
2. Sumber dari Industri
Industri yang perpotensi sebagai sumber pencemaran Pb adalah semua industri
yang memakai Pb sebagai bahan baku maupun bahan penolong, misalnya:
Industri pengecoran maupun pemurnian. Industri ini menghasilkan timbal konsentrat (primary lead), maupun secondary lead yang berasal dari potongan
logam (scrap). Industri batery. Industri ini banyak menggunakan logam Pb terutama lead antimony alloy dan lead oxides sebagai bahan dasarnya. Industri bahan bakar. Pb berupa tetra ethyl lead dan tetra methyl lead banyak dipakai sebagai anti knock pada bahan bakar, sehingga baik industry maupun bahan bakar
yang dihasilkan merupakan sum ber pencemaran Pb. Industri kabel. Industri kabel memerlukan Pb untuk melapisi kabel. Saat ini pemakaian Pb di industri kabel
mulai berkurang, walaupun masih digunakan campuran logam Cd, Fe, Cr, Au dan
arsenik yang juga membahayakan untuk kehidupan makluk hidup. Industri kimia,
toksisitasnya relatif lebih rendah jika dibandingkan dengan logam pigmen yang
lain. Sebagai pewarna merah pada cat biasanya dipakai red lead, sedangkan untuk
warna kuning dipakai lead chromate.
3. Sumber dari Transportasi
Hasil pembakaran dari bahan tambahan (aditive) Pb pada bahan bakar kendaraan
bermotor menghasilkan emisi Pb in organik. Logam berat Pb yang bercampur
dengan bahan bakar tersebut akan bercampur dengan oli dan melalui proses di
dalam mesin maka logam berat Pb akan keluar dari knalpot bersama dengan gas
buang lainnya.
Daya racun didalam tubuh diantaranya disebabkan oleh penghambatan
enzim-enzim oleh ion Pb2+. Enzim yang diduga dihambat adalah yang dibutuhkan
untuk pembentukan hemoglobin . penghambatan tersebut diakibatkan karena
terbentuknya ikatan yang kuat (ikatan kovalen) antara Pb2+ dengan grup sulfur
yang terdapat dalam asam-asam amino (misalnya cistein) dari enzim tersebut
.(Fardiaz. 1992).
2.3.4. Logam Cr
Logam berat krom (Cr) merupakan logam berwarna abu-abu, tahan terhadap
oksidasi meskipun pada suhu tinggi, mengkilat, keras, bersifat paramagnetik, dan
mempunyai bentuk senyawa-senyawa berwarna.
Krom merupakan elemen yang terdapat dalam kehidupan sehari-hari dan
merupakan unsur esensial bagi manusia dan hewan pada konsentrasi yang rendah,
krom tersedia sebagai krom (II), krom (III), dan krom (VI) atau di kenal dengan
Cr (III) merupakan mikronutrien bagi makhluk hidup, tetapi bersifat toksik
dalam dosis tinggi. Cr (III) dibutuhkan untuk metabolisme hormone insulin dan
pengaturan kadar glukosa darah. Defisiensi Cr (III) bisa menyebabkan
hiperglisemia, glukosoria, meningkatnya cadangan lemak tubuh , dan menurunkan
jumlah sperma
(widowati, W.2008)
Dalam bentuk makanan, kromium diserap 10-25 %. Kromium digunakan
dalam pembuata
meningkatkan ketahanan logam da
produk atau bahan kimia yang mengandung kromium dan bahan bakar
menyebabkan terjadinya pembakaran ke udara, tanah, dan air. Partikel menetap di
udara dalam waktu kurang dari 10 hari, akan menempel pada partikel tanah, dan
dalam air dengan sedikit larut. Efek racun akan timbul, jika menghirup udara
tempat kerja yang terkontaminasi, misalnya dalam pengelasan stainless steel,
kromat atau produksi pigmen krom, pelapisan krom, dan penyamakan kulit.
Selain itu, jika menghirup serbuk gergaji dari kayu yang mengandung kromium
akan menimbulkan efek keracunan. Efek toksik kromium dapat merusak dan
mengiritasi hidung, paru-par
tinggi dari kromium menyebabkan kerusakan pada hidung dan paru-paru.
Mengonsumsi makanan berbahan kromium dalam jumlah yang sangat besar,
menyebabkan gangguan perut
kematia
2.4. Destruksi Kimia
Destruksi merupakan suatu cara perlakuaan ( perombakan ) senyawa menjadi
unsur – unsur sehingga dapat dianalisa. Metode destruksi materi organik dapat
1. Metode destruksi basah
2. Metode destruksi kering
Destruksi basah pada prinsipnya adalah penggunaan asam nitrat untuk
mendestruksi zat organik pada suhu rendah dengan maksud menghindari
kehilangan mineral akibat penguapan. Pada tahapan selanjutnya, proses ini
seringkali berlangsung sangat cepat akibat pengaruh asam perklorat atau hidrat
peroksida. Destruksi basah pada umumnya digunakan untuk menganalisa arsen,
timah hitam, timah putih, seng, dan tembaga.
Ada tiga macam cara kerja destruksi basah dapat dilakukan, yaitu :
1. Destruksi basah menggunakan HNO3 dan H2SO4
2. Destruksi basah menggunkana HNO3, H2SO4, dan HClO4
3. Destruksi basah menggunakan HNO3, H2SO4, dan H2O2 . (Apriyanto,1989).
Destruksi kering merupakan penguraian ( perombakan ) senyawa organik
dalam sampel menjadi anorganik dengan jalan pengabuan sampel dan
memerlukan suhu pemanasan tertentu. (Raimon, 1992).
Destruksi kering merupakan perombakan organic logam di dalam sampel
menjadi logam-logam anorganik dengan jalan pengabuan sampel dalam muffle
furnace dan memerlukan suhu pemanasan tertentu. Pada umumnya dalam
destruksi kering ini dibutuhkan suhu pemanasan antara 400-800oC, tetapi suhu ini
sangat tergantung pada jenis sampel yang akan dianalisis. Untuk menentukan
suhu pengabuan dengan system ini terlebih dahulu ditinjau jenis logam yang akan
dianalisis. Bila oksida-oksida logam yang terbentuk bersifat kurang stabil, maka
perlakuan ini tidak memberikan hasil yang baik. Untuk logam Fe, Cu, dan Zn
oksidanya yang terbentuk adalah Fe2O3, FeO, CuO, dan ZnO. Semua oksida
logam ini cukup stabil pada suhu pengabuan yang digunakan. Oksida-oksida ini
kemudian dilarutkan ke dalam pelarut asam encer baik tunggal maupun campuran,
setelah itu dianalisis menurut metode yang digunakan. Contoh yang telah
Metode yang digunakaan untuk penentuan logam-logam tersebut yaitu metode
Spektrofotometer Serapan Atom (Raimon, 1993).
Bahan yang mempunyai kadar air tinggi sebelum pengabuan harus
dikeringkan terlebih dahulu. Bahan yang mempunyai kandungan zat yang mudah
menguap dan berlemak banyak pengabuan dilakukan dengan suhu mula-mula
rendah sampai asap hilang, baru kemudian dinaikkan suhunya sesuai dengan yang
dikehendaki. Untuk bahan yang membentuk buih waktu dipanaskan harus
dikeringkan dulu dalam oven dan ditambahkan zat anti buih misalnya olive atau
parain. Bahan yang akan diabukan ditempatkan dalam wadah khusus yang disebut
krusibel dengan berbagai kapasitas dan pemilihan wadah ini disesuaikan dengan
bahan yang akan diabukan. Temperatur pengabuan harus diperhatikan
sungguh-sungguh karena banyak element abu yang dapat menguap pada suhu yang tinggi.
Lama pengabuan tiap bahan berbeda-beda dan berkisar antara 2-8 jam.
Pengabuan dianggap selesai apabila diperoleh sisa pengabuan yang umumnya
berwarna putih abu-abu dan beratnya konstan dengan selang waktu pengabuan 30
menit. Penimbangan terhadap bahan dilakukan dalam keadaan dingin, untuk itu
maka cawan krusibel yang berisi abu yang diambil dari dalam alat pengabuan
(muffle) harus lebih dahulu dimasukkan ke dalam oven bersuhu 105oC agar
suhunya turun, baru kemudian dimasukkan ke dalam desikator sampai dingin.
Desikator yang digunakan harus dilengkapi dengan zat penyerap uap air misalnya
silika gel atau kalsium klorida, natrium hidroksida. Penentuan abu yang tidak larut
dalam asam dilakukan dengan mencampurkan abu dalam asam klorida 10%.
Setelah diaduk kemudian dipanaskan selanjutnya disaring dengan kertas whatman
no.42. Residu merupakan abu yang tidak larut dalam asam yang terdiri atas pasir
dan silika. Apabila abu banyak mengandung bahan jenis ini maka dapat
diperkirakan proses pencucian bahan tidak sempurna ataupun terjadinya
kontaminasi dari tanah selama proses pengolahan bahan tersebut .(Sudarmadji.
Metode ini digunakan secara luas untuk penentuan kadar unsur logam
dalam jumlah kecil atau trace level ( Kealey, D. 2002).
2.5. Inductively Coupled Plasma – Optical Emission Spectrometry 2.5.1. Definisi Umum
Inductively Coupled Plasma – Optical Emission Spectrometry ( ICP/OES ) adalah
instrumen yang sangat baik untuk penentuan logam dalam berbagai matriks
sampel yang berbeda. Dengan teknik ini, sampel cair di injeksikan ke dalam
Radio Frequency (RF)-induksi plasma argon menggunakan satu jenis nebulizer.
Sampel dalam bentuk kabut mencapai plasma dengan cepat dan mengering,
menguap, dan menghasilkan energy selama proses eksitasi pada suhu tinggi .
Emisi atom yang berasal dari plasma dianggap baik pada konfigurasi radial atau
aksial , yang dikumpulkan dengan lensa atau cermin , dan dilewatkan masuk ke
celah pada panjang gelombang yang selektif. Pengukuran unsur tunggal dapat
dilakukan dengan efektif menggunakan kombinasi sederhana tabung
monokromator /photomultiplier (PMT), dan penentuan multiunsur secara simultan
dilakukan hingga 70 unsur dengan kombinasi polychromator dan array detektor.
Kinerja analisa sistem tersebut kompetitif dengan teknik analisis anorganik
lainnya, terutama berkaitan dengan throughput dan sensitivitas sampel.
Sampel cair dan gas dapat diinjeksikan secara langsung ke dalam
instrumen , sedangkan sampel padat memerlukan ekstraksi atau pelarutan dengan
asam sehingga analit berbentuk larutan . Larutan sampel diubah menjadi aerosol
dan bergerak ke saluran pusat plasma . Pada bagian inti Inductively Coupled
Plasma (ICP) temperatur mencapai 10.000 K, sehingga aerosol menguap dengan
cepat. Unsur analit dibebaskan sebagai atom-atom bebas dalam keadaan gas.
Tumbukan eksitasi lebih lanjut dalam plasma memberikan energi tambahan pada
atom, yang menyebabkan atom-atom pada keadaan tereksitasi. Energi yang ada
memungkinkan untuk mengubah atom menjadi ion-ion dan kemudian menjadikan
Atom dan ion pada keadaan tereksitasi dengan lambat menuju keadaan
dasar melalui emisi foton. Foton memiliki energi yang karakteristik yang
ditentukan oleh struktur tingkat energi terkuantisasi untuk atom atau ion. Dengan
demikian panjang gelombang dari foton dapat digunakan untuk mengidentifikasi
unsur-unsur dari keadaan awal. Jumlah foton berbanding lurus dengan konsentrasi
unsur yang ada pada sampel (Hou, X. and Jones, B. T. 2000).
Instrumentasi yang terkait dengan sistem ICP/OES relatif sederhana.
Sebagian dari foton yang diemisikan oleh ICP dikumpulkan dengan sebuah lensa
atau cermin cekung. Optik pemokus ini memberi gambaran ICP pada jalur masuk
perangkat penyaring panjang gelombang seperti monokromator. Panjang
gelombang partikel melewati sebuah monokromator yang akan diubah menjadi
sinyal listrik oleh photodetektor. Sinyal diperkuat dan diproses oleh elektronik
detektor, kemudian ditampilkan dan disimpan oleh komputer (Hou, X. and Jones,
B. T. 2000).
2.5.2. Karakteristik ICP-OES
Keuntungan utama dari analisis menggunakan ICP dibanding dengan instrument
yang menggunakan sumber eksitasi lainnya adalah kemampuannya untuk efisiensi
dan kebolehulangan pada penguapan, atomisasi, eksitasi, dan ionisasi untuk
berbagai unsur dalam berbagai sampel yang berbeda. Hal ini terutama disebabkan
oleh suhu yang tinggi, 6000-7000 K pada ICP. Suhu ini jauh lebih tinggi dari suhu
maksimum pada flame atau tungku (3300 K). Suhu yang tinggi pada ICP
membuatnya mampu untuk mengeksitasi unsur yang tahan terhadap panas, dan
2.5.3. Instrumentasi ICP-OES
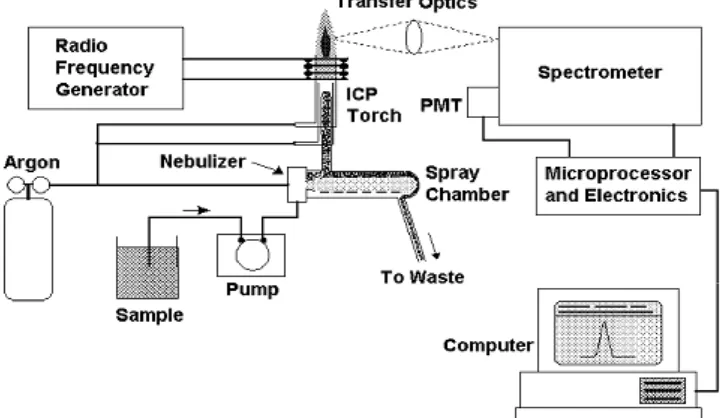
Representasi dan tampilan dari ICP-OES dapat dilihat dari gambar berikut:
Gambar 2.6.Komponen utama dan susunan dari peralatan Inductively Coupled Plasma - Optical Emission Spectrometry.
1. Pemasukan Sampel
a. Nebulizer
Nebulizer adalah perangkat yang digunakan untuk mengkonversi cairan menjadi
aerosol yang kemudian dialirkan ke plasma. Sistem pemasukan sampel yang ideal
untuk semua sampel pada plasma adalah kemampuan plasma untuk mensolvasi,
vaporisasi, atomisasi atau ionisasi, dan eksitasi. Karena hanya tetesan kecil dalam
ICP yang dianalisa, kemampuan untuk menghasilkan tetesan kecil untuk berbagai
sampel sangat menentukan kegunaan dari nebulizer pada ICP-OES. Banyak
perangkat yang dapat digunakan untuk memecah cairan menjadi aerosol, namun
hanya dua yang dapat digunakan pada ICP, yaitu pneumatik force dan ultrasonic
b. Pompa
Pompa adalah perangkat yang digunakan untuk mengalirkan sampel larutan
kedalam nebulizer. Dengan adanya pompa maka laju aliran konstan dan tidak
tergantung pada parameter larutan seperti viskositas dan tegangan permukaan
larutan. Selain itu laju aliran dapat dikontrol dan memungkinkan washout lebih
cepat dari nebulizer dan ruang semprot.
c. Spray Chamber (Tempat Penyemprot)
Setelah sampel aerosol terdapat pada nebulizer, harus segera dialirkan pada torch
sehingga dapat diinjeksikan ke dalam plasma. Karena hanya tetesan kecil aerosol
cocok untuk diinjeksikan ke dalam plasma, spray chamber ditempatkan antara
nebulizer dan torch. Fungsi utama dari spray chamber adalah untuk
menghilangkan tetesan besar dari aerosol. Tujuan kedua dari spray chamber
adalah untuk melancarkan keluaran pulsa yang terjadi selama nebulisasi, karena
spray chamber ikut memompa larutan.
d. Drains
Drains pada ICP berfungsi untuk membawa kelebihan sampel dari spray chamber
menuju ke tempat pembuangan. Selain itu, system drains memberikan tekanan
balik yang dibutuhkan untuk memaksa aerosol pada nebulizer melalui aliran gas
pada tungku injector tube kedalam plasma discharge. Jika sistem drains tidak
membuang habis sampel dan memungkinkan masih adanya gelembung, maka
injeksi sampel kedalam plasma dapat terganggu dan menyebabkan gangguan pada
2. Penghasil Emisi
a.Torches (Tungku)
Dari spray chamber aerosol diinjeksikan melalui torch kedalam plasma yang akan
terdesolvasi, menguap, teratomisasi, tereksitasi dan terionisasi oleh plasma. Torch
terdiri dari tiga tabung konsentrik, untuk aliran argon dan injeksi aerosol. Tiga
tabung itu terdiri dari plasma flow, auxiliary flow dan nebulizer flow.
b. Radio Frequency Generator.
Radio frequency (RF) generator adalah peralatan yang menyediakan daya untuk
pembangkit dan pemeliharaan debit plasma. Daya ini biasanya berkisar antara 700
sampai 1.500 watt, yang ditransfer ke gas plasma melalui kumparan yang terdapat
pada sekitar bagian atas torch. Kumparan, yang bertindak sebagai antena untuk
mentransfer daya RF ke plasma, biasanya terbuat dari pipa tembaga dan
didinginkan oleh air atau gas selama operasi.
3. Pengumpulan dan Pendeteksian Emisi.
a. Optik
Radiasi biasanya dikumpulkan oleh fokus optik seperti lensa cembung atau
cermin cekung. Optik ini bersifat mengumpulkan sinar, sehingga sinar difokuskan
menuju celah pada monokromator atau polikromator.
b. Monokromator
Monokromator digunakan untuk memisahkan garis emisi sesuai dengan panjang
gelombangnya. Monokromator digunakan dalam analisa multi unsur dengan cara
memindai cepat dari satu garis emisi ke garis emisi lainnya. Kisi difraksi
merupakan inti dari spectrometer, kisi memecah cahaya putih menjadi beberapa
panjang gelombang yang berbeda. Untuk menganalisa multi unsur secara simultan
c. Detektor
Detektor digunakan untuk mengukur intensitas garis emisi setelah garis emisi
dipisahkan oleh monokromator/polikromator. Jenis deteiktor yang paling banyak
digunakan pada ICP-OES adalah tabung photomultiplier (PMT).
4. Pemrosesan Sinyal dan Instrumen Kontrol
a. Pemrosesan Sinyal
Setelah emisi dideteksi oleh detector (PMT), maka arus anoda PMT dapat
dikonversi, yang mewakili intensitas emisi menjadi sinyal tegangan yang diubah
menjadi informasi digital. Informasi digital inilah yang mewakili intensitas emisi
relative atau konsentrasi dari sampel.
b. Komputer dan Processor
Komputer digunakan sebagai instrument untuk mengontrol, memanipulasi dan
mengumpulkan data analisis. Pada komputer kita dapat memilih parameter operasi
yang tepat untuk analisis seperti panjang gelombang, tegangan PMT, mengkoreksi
background pengukuran dan konsentrasi larutan standar. Kemampuan untuk
melihat data spectral pengukuran dengan waktu analisis yang sangat cepat
merupakan tujuan utama penggunaan computer dalam setiap instrumentasi (Boss,
C. B. and Freeden, K. J. 1997).
2.6. Spektrofotometri Serapan Atom.
2.6.1. Prinsip Dasar Spektrofotometri Serapan Atom
Spektroskopi serapan atom adalah spektroskopi atomik yang disertai penyerapan
sebagai suatu emisi atau pancaran. Di dalam beberapa dekade spektroskopi
serapan atom menjadi salah satu dari cara yang yang paling luas digunakan untuk
Metode spektrofotometri serapan atom berprinsip pada adsorbsi cahaya
oleh atom. Atom-atom menyerap cahaya tersebut pada panjang gelombang
tertentu. Misanya natrium menyerap pada 589 nm, uranium pada 358,5 nm,
sedangkan kalium pada 766,5 nm. Cahaya pada panjang gelombang ini mempuyai
cukup energy untuk mengubah tinkat elektonik suatu atom. Transisi elektronik
suatu unsure bersifat spesifik. Dengan adsorbsi energy, berarti memperoleh lebih
banyak energi, suatu atom pada keadaan dasar dinaikkn energinya ke tingkat
eksitasi
Umumnya bahan bakar yang digunakan adalah propane, butane, hydrogen,
dan asetilen, sedangkan oksidatornya adalah udara, oksigen, N2O dan asetilen.
Logam-logam yang mudah diuapkan seperti Cu, Pd, Zn, Cd umumnya ditentukan
ada suhu rendah sedangkan unsurunsur yang tak mudah diatomisasi diperlukan
suhu tinggi. Suhu tinggi dapat dicapai dengan menggunakan suatu oksidator
bersama dengan gas pembakar, contohnya atomisasi unsur seperti Al, Ti, Be tanah
jarang perlu menggunakan nyala oksiasetilena atau nyala nitrogen oksidaasetilena
sedangkan atomisasi unsur alkali hatus menggunakan campuran asetilena udara
(Khopkar, S.M. 2007).
Spektroskopi serapan atom digunakan untuk analisis kuantitatif unsur-unsur
logam dalam jumlah sekelumit dan sangat kelumit. Cara analisis ini memberikan
kadar total unsur logam dalam suatu sampel dan tidak tergantung pada bentuk
molekul dari logam dalam sampel tersebut. Spektroskopi serapan atom didasarkan
pada penyerapan energi sinar oleh atom-atom netral, dan sinar yang diserap
biasanya sinar tampak atau ultraviolet. Metode spektroskopi serapan atom
berdasarkan pada prinsip absorbsi cahaya oleh atom. Atom-atom akan menyerap
cahaya pada panjang gelombang tertentu, tergantung pada sifat unsurnya. Cahaya
pada panjang gelombang ini mempunyai cukup energi untuk mengubah tingkat
elektronik suatu atom yang mana transisi elektronik suatu atom bersifat spesifik.
Dengan menyerap suatu energi, maka atom akan memperoleh energi sehingga
suatu atom pada keadaan dasar dapat ditimgkatkan energinya ke tingkat eksitasi
2.6.2. Instrumentasi Spektrofotometri Serapan Atom
Komponen penting yang membentuk spektrofotometer serapan atom
diperlihatkan pada skema di bawah ini:
A = Lampu Katoda Berongga
B = Chopper
C = Tungku
D = Monokromator
E = Detektor
F = Recorder (Khopkar,S.M,2007)
BAB 3
METODE PENELITIAN
3.1. Alat dan Bahan 3.1.1. Alat
- Spektrofotometer Serapan Atom Z-2000 Series
- ICP – OES Varian
- Neraca analitik Mettler PM 400
- Peralatan gelas Pyrex
- Hot plate Fisher
- Bola karet
- Cawan krusibel
- Oven Fisher
- Desikator
- Spatula
- Botol aquadest
- Kertas`saring Whatman No.42
- Tanur listrik Fisher
- Matt Pipet Pirex
- Cawan penguap
3.1.2. Bahan
- Undur-undur
- HNO3(p) p.a ( E. Merck )
- H2SO4(p) p.a ( E. Merck )
- H2O2 30 % p.a ( E. Merck )
- NH4OH (p) p.a ( E. Merck )
- Aquadest
- Fe(NH4)2(SO4)2.6H2O p.a ( E. Merck )
- CrCl3.5H2O p.a ( E. Merck )
- Pb(NO3)2 p.a ( E. Merck )
- Cd(NO3).5H2O p.a ( E. Merck )
3.2. Prosedur Penelitian
3.2.1. Pembuatan Larutan standart Cd2+
a. Larutan Standart Cd2+ 1000 mg/L
Sebanyak 2,9107 g Cd(NO3).5H2O dimasukkan ke dalam labu Erlenmeyer yang
telah berisi akuades, diaduk hingga seluruh kristal larut sempurna, dimasukkan ke
dalam labu ukur 1000 mL, ditambahkan aquadest hingga garis tanda dan
dihomogenkan.
b. Larutan Standart Cd2+ 100 mg/L
Dipipet sebanyak 10 mL larutan induk Cd2+ 1000 mg/L dan dimasukkan kedalam
labu ukur 100 ml, ditambahkan aquadest hingga garis tanda dan dihomogenkan.
c. Larutan Standart Cd2+ 10 mg/L
Dipipet sebanyak 10 mL larutan induk Cd2+ 100 mg/L dan dimasukkan kedalam
d. Larutan Standart Cd2+ 0,10; 0,20; 0,30; 0,40; dan 0.50 mg/L
Dipipet sebanyak 1,0; 2,0; 3,0; 4,0; dan 5,0 mL larutan standart Cd2+ 10 mg/L
dimasukkan labu ukur 50 mL, ditambahkan aquadest sampai garis tanda dan
dihomogenkan.
3.2.2. Pembuatan Larutan Standart Fe3+
a. Larutan Standart Fe3+ 1000 mg/L
- Sebanyak 50 mL aquadest dimasukkan kedalam labu Erlenmeyer, ditambahkan
20 mL H2SO4 pekat secara perlahan – lahan kedalama labu Erlenmeyer.
- Sebanyak 7 g Fe(NH4)2(SO4)2.6H2O dimasukkan ke dalam labu Erlenmeyer
yang telah berisi campuran aquadest dan H2SO4, diaduk hingga seluruh Kristal
larut sempurna, dimasukkan ke dalam labu ukur 1000 mL, ditambahkaan
KMnO4 0,1 N setetes demi setetes sampai diperoleh warna merah muda,
ditambahkan aquadest hingga garis tanda dan dihomogenkan.
b. Larutan Standart Fe3+ 100 mg/L
Dipipet sebanyak 10 mL larutan induk Fe3+ 1000 mg/L dan dimasukkan kedalam
labu ukur 100 ml, ditambahkan aquadest hingga garis tanda dan dihomogenkan.
c. Larutan Standart Fe3+ 10 mg/L
Dipipet sebanyak 10 mL larutan induk Fe3+ 100 mg/L dan dimasukkan kedalam
d. Larutan Seri Standart Fe3+ 0,10; 0,30; 0,50; 0,70; dan 0,80 mg/L
Dipipet sebanyak 0,10 ; 0,30; 0,50; 0,70; dan 0,90 mL larutan standart Fe3+ 10
mg/L dan dimasukkan labu ukur 50 mL, ditambahkan aquadest sampai garis tanda
dan dihomogenkan
e. KMnO4 0,1 N
Sebanyak 0,32 g KMnO4 dimasukkan ke dalam labu ukur 100 mL, ditambahkan
akuades hingga garis tanda dan dihomogenkan
3.2.3. Pembuatan larutan standart Pb2+
a. Pembuatan larutan standart Pb2+ 1000 mg/L
Sebanyak 1,5990 g Pb(NO3)2 dimasukkan ke dalam labu Erlenmeyer yang telah
berisi aquadest, diaduk hingga seluruh kristal larut sempurna, dimasukkan ke
dalam labu ukur 1000 mL, ditambahkan aquadest hingga garis tanda dan
dihomogenkan
b. Pembuatan larutan standart Pb2+ 100 mg/L
Dipipet sebanyak 10 mL larutan standart Pb2+ 1000 mg/L dan dimasukkan
kedalam labu ukur 100 mL, ditambahkan akuades hingga garis tanda dan
c. Pembuatan larutan standart Pb2+ 10 mg/L
Dipipet sebanyak 10 mL larutan standart Pb2+ 100 mg/L dan dimasukkan kedalam
labu ukur 100 mL, ditambahkan akuades sampai garis tanda dan dihomogenkan.
d. Pembuatan larutan seri standart Pb2+ 0,10; 0,20; 0,30; 0,40; dan 0,50 mg/L
Sebanyak 1,0; 2,0; 3,0; 4,0; dan 5,0 mL larutan standart Pb2+ 10 mg/L dan
dimasukkan kedalam labu ukur 50 mL, ditambahkan akuades hingga garis tanda
dan dihomogenkan.
3.2.4. Pembuatan Larutan standart Cr2+
a. Larutan Standart Cr2+ 1000 mg/L
Sebanyak 4,750 g CrCl3.5H2O dimasukkan ke dalam labu Erlenmeyer yang telah
berisi akuades, diaduk hingga seluruh kristal larut sempurna, dimasukkan ke
dalam labu ukur 1000 mL, ditambahkan aquadest hingga garis tanda dan
dihomogenkan.
b. Larutan Standart Cr2+ 100 mg/L
Dipipet sebanyak 10 mL larutan induk Cr2+ 1000 mg/L dan
dimasukkankedalamlabu ukur 100 ml, ditambahkan aquadest hingga garis tanda
c. Larutan Standart Cr2+ 10 mg/L
Dipipet sebanyak 10 mL larutan induk Cr2+ 100 mg/L dan dimasukkan kedalam
labu ukur 100 ml, ditambahkan aquadest hingga garis tanda dan dihomogenkan.
d. Larutan Standart Cr2+ 0,10; 0,20; 0,30; 0,40; dan 0,50 mg/L
Dipipet sebanyak 1,0; 2,0; 3,0; 4,0; dan 5,0 mL larutan standart Cr2+ 10 mg/L dan
dimasukkan labu ukur 50 mL, ditambahkan aquadest sampai garis tanda dan
dihomogenkan.
3.2.5. Pembuatan Kurva Kalibrasi Larutan Standart Cd2+
Sebanyak 50 mL larutan seri standart Cd2+ 0,10 mg/L diukur absorbansinya
dengan Spektrofotometri Serapan Atom (SSA) pada λ = 228,8 nm dan dilakukan
hal yang sama untuk larutan seri standar Cd2+0,20; 0,30; 0,40; dan 0,50 mg/L.
3.2.6.Pembuatan Kurva Kalibrasi Larutan Standart Fe3+
Sebanyak 50 mL larutan seri standart Fe3+ 0,10 mg/L diukur absorbansinya
dengan Spektrofotometer Serapan Atom (SSA) pada λ = 248,3 nm dan dilakukan
hal yang sama untuk larutan seri standar Fe3+ 0,30; 0.50; 0,70 dan 0.90 mg/L.
3.2.7. Pembuatan Kurva Kalibrasi Larutan Standart Pb2+
Sebanyak 50 mL larutan seri standart Pb2+ 0,10 mg/L diukur absorbansinya
dengan Spektrofotometer Serapan Atom (SSA) pada λ = 283,3 nm dan dilakukan
3.2.8. Pembuatan Kurva Kalibrasi Larutan Standar Cr2+
Sebanyak 50 mL larutan seri standart Cr2+ 0,10 mg/L diukur absorbansinya
dengan Spektrofotometer Serapan Atom (SSA) pada λ = 359,3 nm dan dilakukan
hal yang sama untuk larutan seri standart 0,20; 0,30; 0,40; dan 0,50 mg/L.
3.2.9. Pengabuan sampel
Undur-undur yang telah dipisahkan dari abu tanah dimasukkan dalam cawan
crusibel lalu di oven hingga berat konstan, kemudian, diabukan pada suhu 550 –
600 OC selama 2 jam dalam tanur listrik lalu didinginkan di dalam desikator.
3.2.10. Penyediaan Larutan Sampel ( SNI 01-3551-2000)
Abu sampel yang diperoleh pada destruksi kering dimasukkan kedalam beaker
glass 250 mL kemudian ditambahkan 10 mL HNO3 pekat dan 2 mL H2SO4 pekat
dicampur ratakan sehingga diperoleh larutan sampel dan dipanaskan selama 30
menit dan didinginkan. Larutan sampel tersebut ditambahkan 5 mL HNO3 pekat
dan 3 mL H2O2 30% kemudian dipanaskan diatas hot plate hingga setengah
volume awal, disaring dengan kertas saring whatman No.42, dicuci residu dengan
akuades panas, kemudian filtrat dimasukkan kedalam labu ukur 50 mL dan diatur
pH = 3 dan ditambahkan akuades hingga garis tanda lalu dihomogenkan.
3.2.11. Penentuan Penentuan Cd2+, Fe3+, Zn2+, Pb2+ dan Cr2+ dalam sampel
Larutan sampel yang telah didestruksi diuji secara kualitatif dengan ICP –OES
kemudian dianalisa secara kuantitatif dengan alat Spektrofotometer Serapan Atom
(SSA) ) dengan panjang gelombang untuk logam Cd λ = 228,8 nm; Cr λ = 359,3
3.3. Bagan Penelitian
3.3.1. Penentuan kurva kalibrasi
3.3.1.1. Penentuan kurva kalibrasi Cd2+; Pd2+; Cr2+
50 mL larutan seri standart Cd2+ 0,10 mg/L
Ditentukan absorbansinya pada panjang gelombang = 228,8 nm dengan
menggunakan alat Spektrofotometer Serapan Atom.
Hasil
dilakukan hal yang sama untuk larutan seri standart 0,20; 0,30 ; 0,40; dan 0,50 mg/L. dibuat pada pH = 3
NB : Dilakukan prosedur yang sama pada penentuan kurva kalibrasi pada larutan
seri standar Pb2+; dan Cr2+ dengan panjang gelombang masing-masing λ =
283,3 nm; λ = 359,3 nm.
3.3.1.2. Penentuan kurva kalibrasi Fe3+
50 mL larutan seri standart Fe3+ 0,10 mg/L
Ditentukan absorbansinya pada panjang gelombang = 248,3 nm dengan
menggunakan alat Spektrofotometer Serapan Atom.
Hasil
3.3.2. Penentuan logam dalam sampel
9,005 gram sampel undur-undur
dipisahkan dari abu tanah
dimasukkan ke dalam cawan penguap dikeringkan dalam oven hingga berat konstan
diabukan dalam tanur listrik
abu sampel
dimasukkan ke dalam beaker gelas 250 mL ditambahkan 10 mL HNO3(p)
dipanaskan di atas hot plate selama 30 menit didinginkan
larutan sampel
ditambahkan 5 mL HNO3(p) ditambahkan 3 mL H2O2 30 %
larutan kuning kecoklatan
dipanaskan di atas hot plate hingga setengah volume awal
didinginkan
disaring dengan kertas saring whatman no.42 didinginkan dalam desikator
Filtrat Residu
dibilas dengan aquadest panas
dikumpulkan ke dalam labu takar 50 mL diatur pH hingga mencapai pH=3
diencerkan dengan aquadest sampai garis tanda diuji secara kualitatif dengan ICP - OES kemudian ditentukan kandungan Cd, Cr, Pb, dan Fe pada panjang gelombang berturut-turut 228,8 nm; 359,3 nm; 283,3 nm; dan 248,3 nm dengan SSA.
Hasil
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Uji Kualitatif Sampel
Uji kualitatif sampel dilakukan dengan menggunakan alat ICP – OES sehingga
diperoleh kandungan logam yang terdapat dalam sampel adalah seperti yang
ditunjukkan pada tabel 4.1 berikut ini:
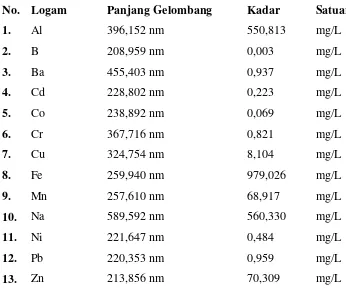
Tabel 4.1. Kandungan Logam yang Terdapat dalam Sampel Untuk Uji Kualitatif dengan ICP – OES
No. Logam Panjang Gelombang Kadar Satuan
1. Al 396,152 nm 550,813 mg/L
2. B 208,959 nm 0,003 mg/L
3. Ba 455,403 nm 0,937 mg/L
4. Cd 228,802 nm 0,223 mg/L
5. Co 238,892 nm 0,069 mg/L
6. Cr 367,716 nm 0,821 mg/L
7. Cu 324,754 nm 8,104 mg/L
8. Fe 259,940 nm 979,026 mg/L
9. Mn 257,610 nm 68,917 mg/L
10. Na 589,592 nm 560,330 mg/L
11. Ni 221,647 nm 0,484 mg/L
12. Pb 220,353 nm 0,959 mg/L
4.1.2 Logam Besi (Fe)
Pembuatan kurva larutan standar logam Besi (Fe) dilakukan dengan membuat
larutan standar denga berbagai konsentrasi yaitu pada pengukuran 0,00; 0,10;
0,30; 0,50; 0,70; dan 0,90 mg/L, kemudian di ukur absorbansinya dengan alat
SSA (kondisi alat pada lampiran 1). Data absorbansi untuk larutan standar Besi
(Fe) dapat dilihat pada table 4.1 di bawah ini:
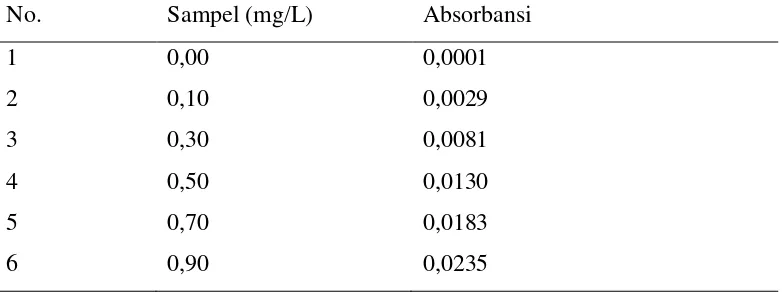
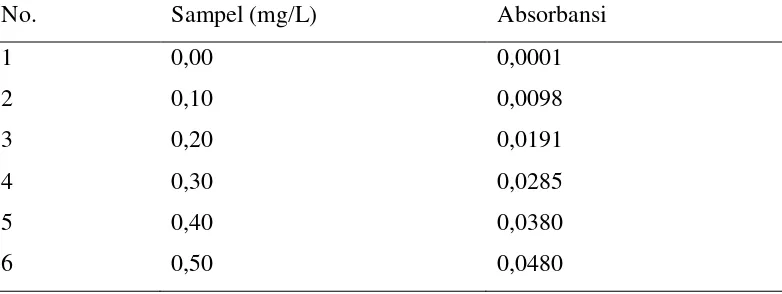
Tabel 4.2. Data pengukuran absorbansi larutan seri standar Besi (Fe)
No. Sampel (mg/L) Absorbansi
1 0,00 0,0001
2 0,10 0,0029
3 0,30 0,0081
4 0,50 0,0130
5 0,70 0,0183
6 0,90 0,0235
4.1.2.1. Penurunan Persamaan Garis Regresi Dengan Metode Least Square
Data absorbansi yang diperoleh untuk suatu seri larutan standar Fe diplotkan
terhadap konsentrasi larutan standar sehingga diperoleh kurva kalibrasi berupa
garis linear seperti pada gambar 4.1. Persamaan garis regresi ini diturunkan
dengan metode least square, dimana konsentrasi dari larutan standar dinyatakan
Tabel 4.3. Penurunan persamaan garis regresi untuk penentuan konsentrasi
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
garis :
Y = aX + b
Dimana :
a = slope
b = intersept
Selanjutnya harga slope dapat ditentukan dengan menggunakan metode least
square sebagai berikut :
� =∑(�� − ��)(�� − ��)
∑(�� − ��)2
b = Y – aX
Dengan mensubstitusikan harga-harga yang tercantum pada tabel pada persamaan
maka diperoleh :
� =15,719.10
−3
0,608 = 0,0258
= 0,0109 – 0,0107
= 0,0002
Maka persamaan garis yang diperoleh adalah :
Y = 0,0258X + 0,0002
4.1.2.2. Penentuan koefisien korelasi untuk logam besi (Fe)
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut :
�= ∑(�� − ��)(�� − ��)
�(�� − ��)2(�� − ��)2
Koefisien korelasi untuk logam Besi (Fe) adalah :
�= 15,719.10
−3
�(0,608)(4,057.10−4) = 0,9999
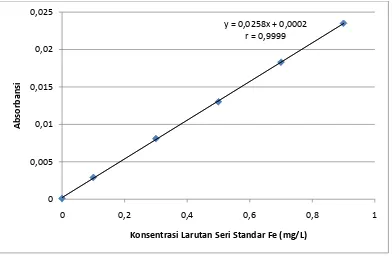
Selanjutnya absorbansi diplotkan terhadap konsentrasi larutan seri standar
sehingga diperoleh suatu kurva kalibrasi berupa garis linear seperti pada gambar
berikut:
Gambar 4.1. Kurva Kalibrasi Larutan Seri Standart Logam Fe (mg/L)
y = 0,0258x + 0,0002
4.1.2.3. Penentuan Kadar Besi (Fe) dalam Sampel
Kadar Besi (Fe) dapat ditentukan dengan menggunakan metode kurva kalibrasi
dengan mensubstitusikan nilai Y (absorbansi) yang diperoleh dari hasil
pengukuran terhadap persamaan garis regresi dari kurva kalibrasi.
4.1.2.3.1. Penentuan kadar Besi (Fe) yang terkandung dalam Undur-undur dengan metode Spektrofotometri Serapan Atom dalam mg/L.
Dari data pengukuran absorbansi Besi (Fe) untuk sampel Undur-undur Darat
diperoleh serapan (A) sebagai berikut :
A1 = 0,0180
A2 = 0,0181
A3 = 0,0179
Dengan mensubstitusikan nilai Y (Absorbansi) ke persamaan garis regresi
Y = 0,0258X + 0,0002, maka diperoleh:
X1 = 0,6899
X2 = 0,6937
X3 = 0,6860
Dengan demikian kadar Besi pada Undur-undur yang adalah :
����������ℎ����,�� = �
Dari data hasil distribusi student untuk n = 3, derajat kebebasan (dk) = n- 1 = 2
untuk derajat kepercayaan 95% (p=0,05), t= 4,30
Maka, d = t(0,05 x n-1)Sx
d = 4,30 x 0,1 x 0,0049 = 0,0021
Dari data hasil pengukuran kadar Besi pada Undur-undur Darat adalah sebesar :
0,6898 ± 0,0021 mg/L
4.1.2.3.2 Penentuan Kadar Besi (Fe) yang Terkandung dalam Undur-undur Darat dengan Metode Spektrofotometri Serapan Atom dalam mg/Kg.
��������������= ����������������
����������ℎ �106��/��
Dengan mengkalikan hasil penentuan Besi dari sampel di atas, maka diperoleh
hasil pengukuran kadar Besi dari 9,0050 gram sampel sebesar :
Kadar Besi pada 9,0050 gram sampel dapat dihitung sebagai berikut :
�����= 0,6898 ��/��0,05 �
9,0050 �� � 10
6��/��
= 3,8300 mg/Kg
Kadar Besi dalam 1 ekor Undur-undur dapat dihitung sebagai berikut:
�������������� 1 ���� = 3,800 ��/��
20
4.1.3. Logam Cadmium (Cd)
Pembuatan kurva larutan standar logam Cadmium (Cd) dilakukan dengan
membuat larutan standar denga berbagai konsentrasi yaitu pada pengukuran 0,00;
0,10; 0,20; 0,30; 0,40; dan 0,50 mg/L, kemudian di ukur absorbansinya dengan
alat SSA ( kondisi alat pada lampiran 3 ). Data absorbansi untuk larutan standar
Cadmium (Cd) dapat dilihat pada table 4.1 di bawah ini:
Tabel 4.4. Data Absorbansi Larutan Standar Tembaga (Cd)
No. Sampel (mg/L) Absorbansi
1 0,00 0,0001
2 0,10 0,0098
3 0,20 0,0191
4 0,30 0,0285
5 0,40 0,0380
6 0,50 0,0480
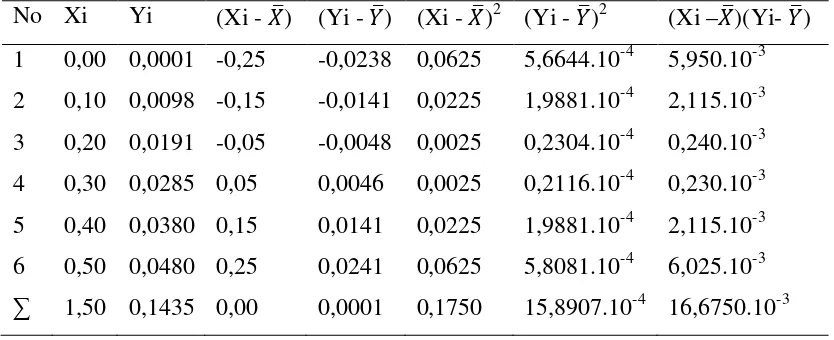
4.1.3.1. Penurunan Persamaan Garis Regresi dengan Metode Least Square
Data absorbansi yang diperoleh untuk suatu seri larutan standar Cd diplotkan
terhadap konsentrasi larutan standar sehingga diperoleh kurva kalibrasi berupa
garis linear seperti pada gambar 4.2. Persamaan garis regresi ini diturunkan
dengan metode least square, dimana konsentrasi dari larutan standar dinyatakan
Tabel 4.5. Penurunan persamaan garis regresi untuk penentuan konsentrasi
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
garis :
Maka persamaan garis yang diperoleh adalah :