1
PENETAPAN KADAR KALSIUM DAN BESI
DALAM UMBI UBI KAYU (Manihot esculenta Crants)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
OLEH:
DINDA NADYA
NIM 131524100
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2
PENETAPAN KADAR KALSIUM DAN BESI
DALAM UMBI UBI KAYU (Manihot esculenta Crants)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
DINDA NADYA
NIM 131524100
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
3
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALSIUM DAN BESI
DALAM UMBI UBI KAYU (Manihot esculenta Crants)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
OLEH: DINDA NADYA
NIM 131524100
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 03 September 2015
Disetujui oleh
Pembimbing I, Panitia Penguji,
Drs. Fathur Rahman Harun, M.Si., Apt. Prof. Dr. Jansen Silalahi, M.App.Sc., Apt.
NIP 195201041980031002 NIP195006071979031001
Pembimbing II, Drs. Fathur Rahman Harun, M.Si., Apt.
NIP 195201041980031002
Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt. Dra. Sudarmi, M.Si., Apt.
NIP 195306191983031001 NIP 195409101983032001
Drs. Nahitma Ginting, M.Si., Apt. NIP 1954062811983031002
Medan, September 2015 Fakultas Farmasi
Universitas Sumatera Utara Pejabat Dekan,
iv
KATA PENGANTAR
Bismillahirrahmanirrahim,
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala limpahan berkat, rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini. Skripsi ini disusun untuk melengkapi salah satu syarat mencapai gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara, yang berjudul “Penetapan Kadar Kasium dan Besi dalam Umbi Ubi Kayu (Manihot esculanta Crants ) secara Spektrofotometri Serapan Atom (AAS)”.
Pada kesempatan ini dengan segala kerendahan hati penulis mengucapkan terima kasih yang sebesar-besarnya kepada Ibu Dr. Masfria, M.S., Apt., selaku Pejabat Dekan Fakultas Farmasi Universitas Sumatera Utara Medan, yang telah memberikan fasilitas sehingga penulis dapat menyelesaikan pendidikan. Bapak Drs. Fathur Rahman Harun, M.Si., Apt., dan Bapak Prof. Dr. rer. nat. Effendy De Lux Putra, S.U., Apt., selaku pembimbing yang telah membimbing dan memberikan petunjuk serta saran-saran selama penelitian hingga selesainya skripsi ini. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., Ibu Dra. Sudarmi, M.Si., Apt., dan Bapak Drs. Nahitma Ginting, M.Si., Apt., selaku selaku dosen penguji yang telah memberikan kritik, saran dan arahan kepada penulis dalam menyelesaikan skripsi ini.
v
ayahanda Basaruddin dan ibunda Sri Hidayati, kedua adik penulis Popo Mogana Abdi dan Mifta Hujannah beserta keluarga besar yang telah memberikan doa dan dukungannya serta keridhaannya bagi penulis dalam menempuh dan menyelesaikan pendidikan, nasehat serta pengorbanan baik moril maupun materil dalam penyelesaian penelitian dan bahan skripsi ini. Penulis juga mengucapkan terima kasih kepada teman-teman Farmasi Ekstensi 2013 dan rekan-rekan penelitian atas doa dan dukungannya
Penulis menyadari sepenuhnya bahwa dalam penulisan skripsi ini masih jauh dari kesempurnaan, oleh karena itu penulis menerima kritik dan saran demi kesempurnaan skripsi ini. Akhirnya penulis berharap semoga skripsi ini dapat memberi manfaat bagi kita semua.
Medan, September 2015 Penulis,
vi
PENETAPAN KADAR KALSIUM DAN BESI DALAM UMBI UBI KAYU (Manihot esculenta Crants)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Umbi ubi kayu merupakan tanaman yang murah dan cukup populer di Indonesia. Umbi ubi kayu yang telah dipanen biasanya diawetkan dengan cara dibuat menjadi gaplek karena selama penyimpanan ubi kayu cepat rusak. Umbi ubi kayu ada dua jenis yaitu umbi ubi kayu kuning dan umbi ubi kayu putih. Umbi ubi kayu dan berbagai olahannya mengandung zat gizi yang cukup tinggi. Zat gizi yang terdapat dalam umbi ubi kayu yaitu karbohidrat, lemak, protein, vitamin (A dan B1), mineral (kalsium, besi dan fosfor). Penelitian ini bertujuan untuk mengetahui kadar kalsium dan besi pada umbi ubi kayu kuning, umbi ubi kayu putih dan umbi ubi kayu yang telah diawetkan (dikeringkan) yaitu gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih serta mengetahui persentase peningkatan kadar kalsium dan besi pada gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih.
Sebelum dilakukan analisis terlebih dahulu sampel didestruksi kering, kemudian analisis kuantitatif kalsium dan besi dilakukan dengan menggunakan metode spektrofotometri serapan atom (AAS) yaitu kalsium pada panjang gelombang 422,7 nm dan besi pada panjang gelombang 248,3 nm dengan nyala udara-asetilen. Keuntungan dari metode ini yaitu mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm) dan pelaksanaannya relatif sederhana.
Hasil penelitian menunjukkan kadar kalisum dalam umbi ubi kayu kuning sebesar (29,6768 ± 0,5899) mg/100 g, umbi ubi kayu putih sebesar (33,6412 ± 0,4633), gaplek umbi ubi kayu kuning sebesar (60,5842 ± 0,5701) mg/100 g dan gaplek umbi ubi kayu putih sebesar (61,7633 ± 0,8617). Kadar besi dalam umbi ubi kayu kuning sebesar (0,4212 ± 0,0065) mg/100 g, umbi ubi kayu putih sebesar (0,4396 ± 0,00171) mg/100 g, gaplek umbi ubi kayu kuning sebesar (0,8690 ± 0,0055) mg/100 g dan gaplek umbi ubi kayu putih sebesar (0,8081 ± 0,0981) mg/100 g.
Kata kunci: umbi ubi kayu kuning, umbi ubi kayu putih, gaplek umbi ubi kayu
vii
DETERMINATION OF CALCIUM AND IRON LEVELS IN CASSAVA TUBER (Manihot esculenta Crants) BY SPECTROPHOTOMETRY ATOMIC ABSORPSTION
ABSTRACT
Cassava tuber is a plant that is inexpensive and quite popular in Indonesia. The cassava tuber that have been harvested usually preserved became cassava chips because during storage they are perishable. There are two types of cassava tuber namely yellow cassava tuber and white cassava tuber. Cassava tuber and various processed products containing high nutrient. Nutrients contained in the cassava tuber namely carbohydrates, fats, proteins, vitamins (A and B1), minerals (calcium, iron and phosphorus). This research aims to determine levels calcium and iron in yellow cassava tuber, white cassava tuber and cassava tuber have been preserved or dried namely yellow cassava chips and white cassava chips also to determine persentage increase in the mineral contens of yellow cassava chips and white cassava chips.
Before analysis sample have destructed using dry destruction method, then the quantitative analysis of calcium and iron were done using atomic absorption spectrophotometry (AAS) at the wavelength of 422.7 nm for calcium and 248.3 nm for iron with air-acetylene flame. Advantages of this method are to have a high sensitivity (limit of detection of lesst han1ppm) and the implementation is relatively simple.
The results show that calcium levels in yellow cassava tuber (29.6768 ±0.5899) mg/100g, white cassava tuber (33.6412 ±0.4633), yellow cassava chips (60.5842 ± 0.5701) mg/100g and white cassava chips (61.7633± 0.8617) mg/100 g. Ironlevelsinyellow cassava tuber (0.4212 ±0.0065) mg/100g, white cassava tuber (0.4396 ±0.00171) mg/100 g, yellow cassava chips (0.8690 ± 0.0055) mg/100g and white cassava chips (0.8081 ±0.0981) mg/100 g.
Keywords: yellow cassava tuber, white cassava tuber, yellow cassava chips and
viii
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... viii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 3
1.2 Perumusan Masalah ... 3
1.3 Hipotesi ... 3
1.4 Tujuan Penelitian ... 4
1.4 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Ubi Kayu ... 5
2.2 Gaplek ... 6
2.3 Kandungan zat gizi dalam umbi ubi kayu dan produk olahnanya ... 6
2.4 Mineral ... 6
ix
2.4.2 Besi ... 8
2.5 Kadar Air ... 9
2.6 Dekstruksi ... 11
2.7 Spektrofotometri Serapan Atom (AAS) ... 12
2.7.1 Gangguan- gangguan Pada AAS ... 15
2.8 Validasi Metode Analisis ... 16
BAB III METODE PENELITIAN ... 19
3.1 Tempat danWaktu Penelitian ... 19
3.2 Bahan-bahan ... 19
3.2.1 Sampel ... 19
3.2.2 Pereaksi ... 19
3.3 Alat-alat ... 19
3.4 Pembuatan Pereaksi ... 20
3.4.1 Larutan HNO3 (1:1) ... 20
3.5 Prosedur Penelitian ... 20
3.5.1 Pengambilan sampel ... 20
3.5.2 Penyiapan sampel ... 20
3.5.2.1 Ubi kayu kuning dan ubi kayu putih ... 20
3.5.2.2 Gaplek ubi kayu kuning dan gaplek ubi kayu putih ... 21
3.5.3 Penetapan kadar air ... 21
3.5.4 Proses destruksi ... 22
3.5.5 Pembuatan larutan sampel ... 22
x
3.5.6.1 Pembuatan kurva kalibrasi kalsium ... 22
3.5.6.2 Pembuatan kurva kalibrasi besi ... 23
3.5.6.3 Penetapan kadar kalsium ... 23
3.5.6.4 Penetapan kadar besi ... 24
3.5.7 Analisis data secara statistik ... 24
3.6.7.1 Penolakan hasil pengamatan ... 24
3.6.7.2 Pengujian beda nilai rata-rata antar sampel 25
3.6.8 Analisis validasi metode ... 25
3.6.8.1 Uji perolehan kembali (recovery) ... 25
3.6.8.2 Simpangan baku relatif ... 26
3.6.8.3 Batas deteksi dan batas kuantitasi ... 27
BAB IV HASIL DAN PEMBAHASAN ... 28
4.1 Hasil Identifikasi Tumbuhan ... 28
4.2 Analisis Kuantitatif ... 28
4.2.1 Kurva kalibrasi kalsium dan besi ... 28
4.2.2 Penetapan kadar kalsium dan besi dalam sampel .. 30
4.2.3 Uji beda rata-rata ... 33
4.2.4 Uji perolehan kembali (recovery) ... 34
4.2.5 Simpangan baku relatif ... 35
4.2.6 Batas deteksi dan batas kuantitasi ... 36
BAB V KESIMPULAN DAN SARAN ... 37
5.1 Kesimpulan ... 37
xi
xii
DAFTAR TABEL
Tabel Halaman
2.1 Kandungan zat gizi dalam umbi ubi kayu dan produk
olahnnya ... 7 2.2 Rentang persen perolehan kembai yang diizinkan pada
analit sampel ... 17 4.1 Hasil penetapan kadar kalsium dalam sampel ... 31 4.2 Hasil Peningkatan Kadar Kalsium dan Besi pada umbi ubi
kayu kuning (uk) menjadi gaplek umbi ubi kayu kuning (gk) ... 32 4.3 Hasil Peningkatan Kadar Kalsium dan Besi pada umbi ubi
kayu Putih (up) menjadi gaplek umbi ubi kayu putih (gp) .. ... 32 4.4 Hasil Perhitungan Kadar kalsium dan Besi jika Kadar air 0% ... 33 4.5 Pengujian beda nilai rata-rata kalsium dan besi ... 34 4.6 Persen uji perolehan kembali (recovery) kadar kalsium
dan besi ... 35 4.7 Simpangan baku relatif kalsium dan besi dalam sampel dan besi .. 35 4.8 Batas deteksi dan batas kuantitasi kalsium dan besi dalam
xiii
DAFTAR GAMBAR
Gambar Halaman
xiv
DAFTAR LAMPIRAN
Lampiran Halaman
1. Identifikasi tumbuhan ... 40
2. Gambar Sampel ... 41
2. Gambar Alat ... 43
4. Bagan alir penyiapan sampel umbi ubi kayu kuning dan umbi ubi kayu putih ... 44
5. Bagan alir penyiapan sampel gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih ... 45
6. Bagan alir proses destruksi kering ... 46
7. Bagan alir pembuatan larutan sampel ... 47
8. Perhitungan kadar air ... 48
9. Data kalibrasi kalsium dengan spektrofotometer serapan atom perhitungan persamaan garis regresi dan koefisien korelasi (r) ... 52
10. Data kalibrasi besi dengan spektrofotometer serapan atom, perhitungan persamaan garis regresi dan koefisien korelasi (r) . ... 54
11. Hasil Analisis Kadar Kalsium dan Besi Pada sampel ... 56
12. Contoh perhitungan kadar kalsium dan besi ... 59
13. Perhitungan statistik kadar kalsium dan besi dalam sampel .... 64
14. Perhitungan peningkatan kadar kalsium dan besi dalam sampel ... 81
15. Perhitungan Kadar Kalsium dan besi jika Kadar air 0% ... 83
xv
penambahan masing-masing larutan baku ... 91 18. Perhitungan jumlah baku yang ditambahkan ... 93 19. Pehitungan uji perolehan kembali kadar kalsium dan besi
` dalam sampel ... 95 20. Perhitungan simpangan baku relatif (RSD) kadar kalsium
dan besi ... 98 21. Perhitungan batas deteksi (LOD) dan batas kuantitasi
vi
PENETAPAN KADAR KALSIUM DAN BESI DALAM UMBI UBI KAYU (Manihot esculenta Crants)
SECARA SPEKTROFOTOMETRI SERAPAN ATOM
ABSTRAK
Umbi ubi kayu merupakan tanaman yang murah dan cukup populer di Indonesia. Umbi ubi kayu yang telah dipanen biasanya diawetkan dengan cara dibuat menjadi gaplek karena selama penyimpanan ubi kayu cepat rusak. Umbi ubi kayu ada dua jenis yaitu umbi ubi kayu kuning dan umbi ubi kayu putih. Umbi ubi kayu dan berbagai olahannya mengandung zat gizi yang cukup tinggi. Zat gizi yang terdapat dalam umbi ubi kayu yaitu karbohidrat, lemak, protein, vitamin (A dan B1), mineral (kalsium, besi dan fosfor). Penelitian ini bertujuan untuk mengetahui kadar kalsium dan besi pada umbi ubi kayu kuning, umbi ubi kayu putih dan umbi ubi kayu yang telah diawetkan (dikeringkan) yaitu gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih serta mengetahui persentase peningkatan kadar kalsium dan besi pada gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih.
Sebelum dilakukan analisis terlebih dahulu sampel didestruksi kering, kemudian analisis kuantitatif kalsium dan besi dilakukan dengan menggunakan metode spektrofotometri serapan atom (AAS) yaitu kalsium pada panjang gelombang 422,7 nm dan besi pada panjang gelombang 248,3 nm dengan nyala udara-asetilen. Keuntungan dari metode ini yaitu mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm) dan pelaksanaannya relatif sederhana.
Hasil penelitian menunjukkan kadar kalisum dalam umbi ubi kayu kuning sebesar (29,6768 ± 0,5899) mg/100 g, umbi ubi kayu putih sebesar (33,6412 ± 0,4633), gaplek umbi ubi kayu kuning sebesar (60,5842 ± 0,5701) mg/100 g dan gaplek umbi ubi kayu putih sebesar (61,7633 ± 0,8617). Kadar besi dalam umbi ubi kayu kuning sebesar (0,4212 ± 0,0065) mg/100 g, umbi ubi kayu putih sebesar (0,4396 ± 0,00171) mg/100 g, gaplek umbi ubi kayu kuning sebesar (0,8690 ± 0,0055) mg/100 g dan gaplek umbi ubi kayu putih sebesar (0,8081 ± 0,0981) mg/100 g.
Kata kunci: umbi ubi kayu kuning, umbi ubi kayu putih, gaplek umbi ubi kayu
vii
DETERMINATION OF CALCIUM AND IRON LEVELS IN CASSAVA TUBER (Manihot esculenta Crants) BY SPECTROPHOTOMETRY ATOMIC ABSORPSTION
ABSTRACT
Cassava tuber is a plant that is inexpensive and quite popular in Indonesia. The cassava tuber that have been harvested usually preserved became cassava chips because during storage they are perishable. There are two types of cassava tuber namely yellow cassava tuber and white cassava tuber. Cassava tuber and various processed products containing high nutrient. Nutrients contained in the cassava tuber namely carbohydrates, fats, proteins, vitamins (A and B1), minerals (calcium, iron and phosphorus). This research aims to determine levels calcium and iron in yellow cassava tuber, white cassava tuber and cassava tuber have been preserved or dried namely yellow cassava chips and white cassava chips also to determine persentage increase in the mineral contens of yellow cassava chips and white cassava chips.
Before analysis sample have destructed using dry destruction method, then the quantitative analysis of calcium and iron were done using atomic absorption spectrophotometry (AAS) at the wavelength of 422.7 nm for calcium and 248.3 nm for iron with air-acetylene flame. Advantages of this method are to have a high sensitivity (limit of detection of lesst han1ppm) and the implementation is relatively simple.
The results show that calcium levels in yellow cassava tuber (29.6768 ±0.5899) mg/100g, white cassava tuber (33.6412 ±0.4633), yellow cassava chips (60.5842 ± 0.5701) mg/100g and white cassava chips (61.7633± 0.8617) mg/100 g. Ironlevelsinyellow cassava tuber (0.4212 ±0.0065) mg/100g, white cassava tuber (0.4396 ±0.00171) mg/100 g, yellow cassava chips (0.8690 ± 0.0055) mg/100g and white cassava chips (0.8081 ±0.0981) mg/100 g.
Keywords: yellow cassava tuber, white cassava tuber, yellow cassava chips and
1
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Di Indonesia dikenal dua jenis umbi ubi kayu yaitu umbi ubi kayu putih dan umbi ubi kayu kuning. Umbi ubi kayu yang telah dipanen tidak dapat bertahan lama terutama bila terkena umbinya karena adanya senyawa HCN yang menyebabkan daging umbinya berwarna kehitaman. Oleh karena itu masyarakat mengolahnya menjadi bentuk yang lebih tahan lama yaitu dibuat menjadi gaplek. Gaplek adalah umbi ubi kayu (singkong) yang dipotong tipis-tipis dan dijemur dibawah sinar matahari (Sediaoetama, 1999).
Sebagai produksi hasil pertanian pangan kedua terbesar setelah padi, umbi ubi kayu mempunyai potensi sebagai bahan baku bagi berbagai produk pangan dan industri. Dalam bentuk segar umbi ubi kayu dapat diolah menjadi berbagai makanan seperti tapai, getuk dan keripik. Sedangkan dalam bentuk yang telah diawetkan (gaplek) umbi ubi kayu dapat diolah menjadi tiwul, serta dibuat menjadi tepung gaplek dicampur dalam berbagai olahan kue dan bahan baku pembuatan mie. Dalam bidang industri umbi ubi kayu biasa digunakan sebagai bahan baku dalam membuat tapioka dan tepung ubi kayu (tepung gaplek) (Koswara, 2015).
2
Dalam umbi ubi kayu putih tiap 100 gram mengandung 146 kalori, 1,20 g protein, 0,30 g lemak, 34,70 g karbohidrat, 40 mg fosfor, 33 mg kalsium, 0,7 mg zat besi, 0,06 mg vitamin B1, 30 mg vitamin C dan 62,5 g air. Dalam bentuk gaplek tiap
100 gram mengandung 338 kalori, 1,5 g protein, 0,7 g lemak, 81,3 g karbohidrat, 60 mg fosfor, 80 mg kalsium, 1,9 mg zat besi, 0,04 mg vitamin B1 dan 14,5 g air
(Direktorat Gizi Depkes RI, 1981).
Mineral merupakan bagian dari tubuh dan memegang peranan penting dalam pemeliharaan fungsi tubuh, seperti untuk pengaturan kerja enzim-enzim, pemeliharaan keseimbangan asam basa, membantu transfer ikatan-ikatan penting melalui membran sel dan pemeliharan kepekaan otot dan saraf terhadap rangsangan (Almatsier, 2002).
Besi penting bagi manusia untuk pembentukan eritrosit, sehingga kekurangan besi dalam tubuh akan mempengaruhi pembentukan hemoglobin (Hb). Besi yang terikat dengan hemoglobin mempunyai beberapa fungsi esensial di dalam tubuh, yaitu sebagai alat angkut oksigen dari paru-paru ke jaringan tubuh, pemindahan/transfer elektron di dalam sel (Almatsier, 2002).
Kalsium merupakan salah satu mineral makro jumlahnya didalam tubuh 1,5 -2 % berat badan orang dewasa. Dari jumlah ini 99% berada dalam tulang dan gigi selebihnya kalsium tersebar didalam tubuh. Kalsium berfungsi pembentukan struktur tulang dan gigi. Kalsium juga diperlukan dalam kontraksi otot dan berperan dalam proses pembekuan darah (Almatsier, 2002).
3
Penetapan kadar kalsium dan besi dilakukan dengan Spektrofotometri Serapan Atom (AAS). Adapan alasan pemilihan metode ini adalah karena pelaksanaannya relatif sederhana, mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm) (Gandjar dan Rohman, 2007).
1.2Rumusan Masalah
Berdasarkan latar belakang, maka permasalahan dalam penelitian ini dapat
dirumuskan sebagai berikut:
1. Berapa kadar kalsium dan besi pada umbi ubi kayu kuning, umbi ubi kayu putih, gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih.
2. Berapakah persentase peningkatan kadar kalsium dan besi pada gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih.
1.3 Hipotesa
Berdasarkan rumusan masalah, maka hipotesa dalam penelitian ini dapat
dirumuskan sebagai berikut:
1. Pada umbi ubi kayu kuning, umbi ubi kayu putih, gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih mengandung kalsium dan besi dalam jumlah tertentu.
2. Terjadi peningkatan kadar kalsium dan besi pada gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih.
4
1.4 Tujuan Penelitian
Tujuan dalam penelitian ini dapat dirumuskan sebagai berikut:
1. Untuk mengetahui kadar kalsium dan besi pada umbi ubi kayu kuning, umbi ubi kayu putih, gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih.
2. Untuk mengetahui berapakah persentase peningkatan kadar kalsium dan besi pada gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih.
1.5Manfaat Penelitian
5
BAB II
TINJAUAN PUSTAKA
2.1 Ubi Kayu
Menurut Herbarium Bogorianse (2015) dan Rahmawati (2010), taksonomi ubi kayu adalah sebagai berikut:
Kingdom : Plantae (tumbuh-tumbuhan) Divisio : Spermatophyta (tumbuhan berbiji) Sub Divisio : Angiospermae (berbiji tertutup) Classis : Dicotyledoneae
Ordo : Euphorbiales Familia : Euphorbiaceae Genus : Manihot
Spesies : Manihot esculenta Crants
Ubi kayu (Manihot esculenta Crants) merupakan tanaman pangan berupa perdu dengan nama lain ketela pohon, singkong, atau kasape. Ubi kayu berasal dari benua Amerika, tepatnya dari negara Brasil. Penyebarannya hampir ke seluruh dunia, antara lain Afrika, Madagaskar, India, dan Tiongkok. Ubi kayu diperkirakan masuk ke Indonesia pada tahun 1852 (Rahmawati, 2010).
6
ubi kayu di Indonesia adalah bahan makanan pokok untuk dikonsumsi langsung (Barret dan Damardjati, 2015).
Berdasarkan sifat ubi kayu digolongkan dalam dua golongan yaitu golongan pahit (kandungan HCN tinggi) dan golongan manis (golongan HCN rendah). Umumnya yang dikonsumsi adalah varietas manis sedangkan varietas pahit digunakan untuk tujuan industri (Barret dan Damardjati, 2015).
2.2 Gaplek
Salah satu cara pengawetan singkong adalah dengan cara pengeringan, hasilnya disebut gaplek. Cara-cara pengeringan di berbagai negara berbeda-beda. Di beberapa daerah dilakukan dengan cara dibelah dua atau dengan sistem gelondongan. Cara pengeringan ini dapat memakan waktu dari 1 sampai 3 minggu, tergantung dari keadaan cuaca (Koswara, 2015).
2.3 Kandungan Zat Gizi dalam Umbi Ubi Kayu dan Produk Olahnnya
7
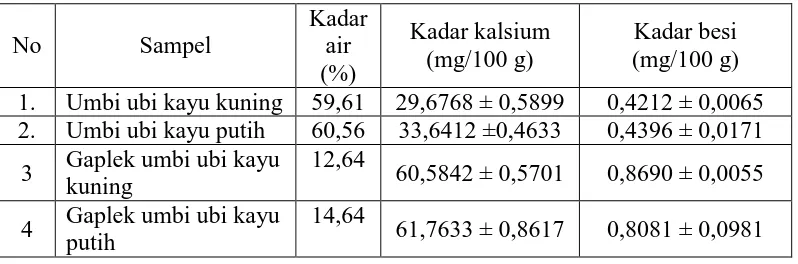
Tabel 2.1 Kandungan zat gizi dalam umbi ubi kayu dan produk olahannya tiap 100g
Zat Gizi Umbi Ubi kayu putih
Umbi ubi kayu Kuning
Gaplek
Kalori 146 kalori 157 kalori 338 kalori
Protein 1,20 g 0,8 g 1,5 g
Lemak 0,3 g 0,3 g 0,7 g
Karbohidrat 34,7 g 37,9 g 81,3 g
Mineral Fosfor Kalsium Besi 40 mg 33 mg 0,7 mg 40 mg 33 mg 0,7 mg 60 mg 80 mg 1,9 mg Vitamin B1
Vitamin C 0,06 mg 30 mg 0,06 mg 30 mg 0,04 mg
Kadar air 62,5 g 60 g 14,5 g
2.4 Mineral
Mineral merupakan bagian dari tubuh dan memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ maupun fungsi tubuh secara keseluruhan, juga berperan dalam berbagai tahap metabolisme, terutama sebagai kofaktor dalam aktivitas enzim-enzim, serta menjaga keseimbangan ion-ion tubuh (Almatsier, 2002).
Mineral digolongkan ke dalam mineral makro dan mineral mikro. Mineral makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg sehari, sedangkan mineral mikro dibutuhkan kurang dari 100 mg sehari. Jumlah mineral mikro dalam tubuh kurang dari 15 mg. Yang termasuk mineral makro adalah natrium, kalium, kalsium, fosfor, magnesium dan sulfur. Adapun yang termasuk mineral mikro adalah besi, seng, mangan dan tembaga (Almatsier, 2002).
2.4.1 Kalsium
8
yaitu 1,5-2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg. Dari jumlah ini, sebanyak 99% berada di dalam jaringan keras, yaitu tulang dan gigi, selebihnya tersebar luas di dalam tubuh. Kalsium mempunyai berbagai fungsi didalam tubuh yaitu pembentukan tulang dan gigi, mengatur pembekuan darah, katalisator reaksi-reaksi biologik dan kontraksi otot (Almatsier, 2002).
Kalsium diekskresikan lewat urin serta feses dan untuk mencegah kehilangan ini diperlukan kalsium melalui makanan. Kalsium tambahan diperlukan dalam keadaan tertentu seperti pada masa pertumbuhan mulai dari anak-anak hingga usia remaja dan pada saat hamil untuk memenuhi kebutuhan janin (Budiyanto, 2004).
Angka kecukupan rata-rata sehari untuk kalsium bagi orang Indonesia yang ditetapkan adalah 300 mg – 400 mg pada bayi, 500 mg pada anak-anak, 600 mg – 700 mg pada remaja, 500 mg – 800 mg pada orang dewasa, serta lebih besar 400 mg pada ibu hamil dan menyusui. Kekurangan kalsium pada masa pertumbuhan dapat menyebabkan gangguan pertumbuhan seperti tulang kurang kuat, mudah bengkok dan rapuh (Almatsier, 2002).
Sumber kalsium utama adalah susu dan hasil olahan susu seperti keju. Ikan yang dimakan dengan tulang, termasuk ikan kering merupakan sumber kalsium yang baik. Serealia, kacang-kacangan dan hasil kacang-kacangan, tahu, tempe, serta sayuran hijau merupakan sumber kalsium yang baik (Almatsier, 2002).
2.4.2 Besi
9
angkut elektron di dalam sel dan sebagai bagian terpadu berbagai reaksi enzim di dalam jaringan tubuh (Almatsier, 2002).
Kebutuhan akan zat besi untuk berbagai jenis kelamin dan golongan usia adalah sebagai berikut: untuk laki-laki dewasa 10 mg/hari, wanita yang mengalami haid 12 mg/hari dan anak-anak 8 mg – 15 mg/hari. Zat besi yang tidak mencukupi bagi pembentukan sel darah, akan mengakibatkan anemia, menurunkan kekebalan tubuh, sehingga sangat peka terhadap serangan penyakit. Sumber besi diantaranya adalah telur, daging, ikan, tepung, gandum, roti, sayuran hijau, hati, bayam, kacang-kacangan, kentang, jagung (Budiyanto, 2004).
2.5 Kadar Air
Menurut Sudarmadji dkk (1989), Kadar air dalam bahan makanan dapat
ditentukan dengan berbagai cara antara lain: 1. Metode Pengeringan (Thermogravimetri)
Prinsipnya menguapkan air yang ada dalam bahan dengan cara pemanasan kemudian menimbang bahan sampai berat konstan yang berarti semua air sudah diuapkan. Cara ini relatif mudah dan murah. Namun, cara ini memiliki kelemahan yaitu:
- Bahan lain disamping air juga ikut menguap dan ikut hilang bersama dengan uap air misalnya alkohol, asam asetat, minyak atsiri dan lain-lain.
10
- Bahan yang mengadung bahan yang dapat mengikat air sacara kuat sulit melepaskan airnya meskipun sudah dipanaskan.
2. Metode Destilasi (Thermovolumetri)
Prinsip penentuan kadar air dengan destilasi adalah menguapkan air dengan “pembawa” cairan kimia yang mempunyai titik didih lebih tinggi daripada air dan tidak dapat bercampur dengan air serta mempunyai berat jenis lebih rendah dari pada air. Zat kimia yang yang dapat digunakan antara lain: toluen, xylen, benzen dan lain-lain.
Cara destilasi ini baik untuk menentukan kadar air dalam zat yang kandungan airnya kecil yang sulit ditentukan dengan cara Thermogravimetri. Penentuan kadar air dengan cara ini hanya memerlukan waktu ± 1 jam (Sudarmadji dkk, 1989).
Penentuan kadar air dengan cara destilasi juga dapat digunakan untuk bahan-bahan yang kadar airnya tinggi dan mengandung senyawa-senyawa yang mudah menguap seperti sayuran dan susu (Winarno, 1995).
3. Metode Khemis
Ada beberapa cara penentuan kadar air dengan cara kimiawi antara lain: - Cara titrasi Karl Fisher (1935)
Cara ini adalah dengan menitrasi sampel dengan larutan iodin dalam metanol.
- Cara Kalsium Karbid
Cara ini berdasarkan reaksi antara kalsium karbid dan air menghasilkan gas asetilen.
11
penentuan kadar air cara ini berdasarkan reaksi asetil khorida dan air menghasilkan asam yang dapat dititrasi menggunakan basa.
4. Metode Fisis
Penetuan kadar air dengan cara fisis ini antara lain: a. Berdasarkan tetapan dielektrikum
b. Berdasarkan konduktivitas listrik (daya hantar listrik) atau resistansi
2.6 Dekstruksi
Destruksi merupakan suatu perlakuan pemecahan senyawa menjadi unsur-unsurnya sehingga dapat dianalisis. Istilah destruksi ini disebut juga perombakan, yaitu dari bentuk organik logam menjadi bentuk logam-logam anorganik. Pada dasarnya ada dua jenis destruksi yang dikenal dalam ilmu kimia yaitu destruksi basah dan destruksi kering. Kedua destruksi ini memiliki teknik pengerjaan dan lama pemanasan atau pendestruksian yang berbeda (Kristianingrum, 2012). 1. Metode Destruksi Basah
12 2. Metode Destruksi Kering
Destruksi kering merupakan perombakan organik logam di dalam sampel menjadi logam-logam anorganik dengan jalan pengabuan sampel dalam muffle furnace dan memerlukan suhu pemanasan tertentu. Pada umumnya dalam destruksi kering ini dibutuhkan suhu pemanasan antara 400-800 oC, tetapi suhu ini sangat tergantung pada jenis sampel yang akan dianalisis. Untuk menentukan suhu pengabuan dengan sistem ini terlebih dahulu ditinjau jenis logam yang akan dianalisis. Bila oksida-oksida logam yang terbentuk bersifat kurang stabil, maka perlakuan ini tidak memberikan hasil yang baik. Untuk logam Fe, Cu, dan Zn oksidanya yang terbentuk adalah Fe2O3, FeO, CuO, dan ZnO. Semua oksida
logam ini cukup stabil pada suhu pengabuan yang digunakan. Oksida-oksida ini kemudian dilarutkan ke dalam pelarut asam encer baik tunggal maupun campuran, setelah itu dianalisis menurut metode yang digunakan (Kristianingrum, 2012).
2.7 Spektrofotometri Serapan Atom
Spektroskopi serapan atom digunakan untuk analisis kuantitatif
unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrace). Cara analisis ini memberikan kadar total unsur logam dalam suatu sampel dan tidak tergantung pada bentuk molekul dari logam dalam sampel tersebut. Cara ini cocok untuk analisis logam karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaannya relatif sederhana dan interferensinya sedikit (Gandjar dan Rohman, 2007).
13
tertentu, dan hal itu tergantung dari unsurnya. Cahaya pada panjang gelombang tertentu memiliki energi yang cukup untuk mengubah tingkat elektronik suatu atom. Dengan adanya absorbsi energi, berarti diperoleh energi yang lebih banyak sehingga suatu atom yang berada pada keadaan dasar dinaikkan tingkat energinya ke tingkat eksitasi (Khopkar, 1985).
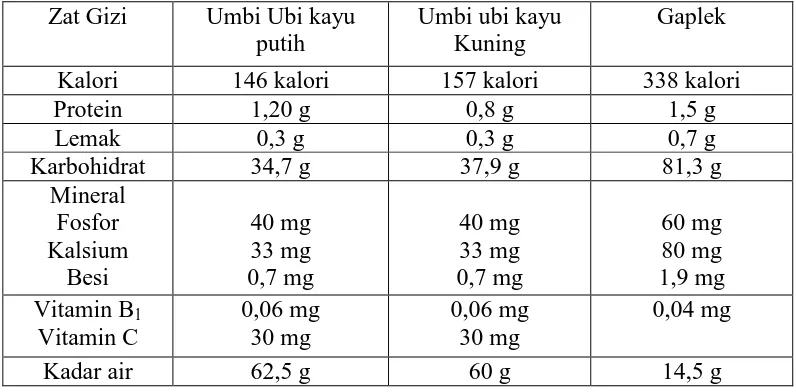
[image:30.595.125.513.295.459.2]Menurut Gandjar dan rohman (2007), bagian instrumentasi spektrofotometer serapan atom dapat dilihat pada Gambar 2.1 berikut ini:
Gambar 2.1 Sistem Peralatan Spektrofotometri Serapan Atom (Gandjar dan
Rohman, 2007). a. Sumber sinar
Sumber sinar yang umum dipakai adalah lampu katoda berongga (hollow
cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Katoda berbentuk silinder berongga yang terbuat dari unsur atau dilapisi unsur yang sama dengan unsur yang akan dianalisis. Tabung logam ini diisi dengan gas mulia dengan tekanan rendah yang jika diberikan tegangan pada arus tertentu, katoda akan memancarkan elektron-elektron yang bergerak menuju anoda dengan kecepatan dan energi yang tinggi. Elektron dengan
14
energi tinggi ini akan bertabrakan dengan gas mulia sehingga gas mulia kehilangan elektron dan menjadi ion bermuatan positif. Ion gas mulia bermuatan positif akan bergerak menuju katoda dengan kecepatan dan energi yang tinggi sehingga menabrak unsur-unsur yang terdapat pada katoda. Akibat tabrakan ini, unsur-unsur akan terlempar ke luar permukaan katoda dan mengalami eksitasi ke tingkat energi elektron yang lebih tinggi (Gandjar dan Rohman, 2007).
b. Tempat sampel
Dalam analisis dengan spektrofotometer serapan atom, sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan dasar. Ada berbagai macam alat yang digunakan untuk mengubah sampel menjadi uap atom-atomnya, yaitu:
- Dengan nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi bentuk uap atomnya dan untuk proses atomisasi. Suhu yang dapat dicapai oleh nyala tergantung pada gas yang digunakan, misalnya untuk gas asetilen-udara, suhunya sebesar 2200°C. Sumber nyala asetilen-udara ini merupakan sumber nyala yang paling banyak digunakan. Pada sumber nyala ini asetilen sebagai bahan pembakar, sedangkan udara sebagai bahan pengoksidasi. Sedangkan dengan gas dinitrogen oksida-asetilen suhunya sebesar 3000°C (Gandjar dan Rohman, 2007).
- Tanpa nyala (Flameless)
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil sedikit (hanya beberapa μL), lalu diletakkan dalam tabung grafit,
15
melewatkan arus listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga terjadilah proses penyerapan energi sinar yang memenuhi kaidah analisis kuantitatif (Gandjar dan Rohman, 2007).
c. Monokromator
Monokromator merupakan alat untuk memisahkan dan memilih spektrum sesuai dengan panjang gelombang yang digunakan dalam analisis dari sekian banyak spektrum yang dihasilkan lampu katoda berongga (Gandjar dan Rohman, 2007).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman (Gandjar dan Rohman, 2007).
e. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman, 2007).
2.7.1 Gangguan-gangguan pada spektrofotometri serapan atom
Gangguan-gangguan (interference) pada Spektrofotometri Serapan Atom adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan konsentrasinya dalam sampel (Gandjar dan Rohman, 2007).
16
tumpangasuh absorpsi antara spesies pengganggu dan spesies yang diukur. Interferensi kimia disebabkan adanya reaksi kimia selama atomisasi, sehingga mengubah sifat absorpsi (Khopkar, 1985).
Menurut Gandjar dan Rohman (2007), gangguan-gangguan yang terjadi pada spektrofotometri serapan atom adalah:
a. Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi banyaknya sampel yang mencapai nyala.
b. Gangguan kimia yang dapat mempengaruhi jumlah atau banyaknya atom yang terjadi di dalam nyala.
c. Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi atom yang dianalisis, yakni absorbansi oleh molekul-molekul yang tidak terdisosiasi di dalam nyala.
d. Gangguan oleh penyerapan non-atomik
2.8 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis menurut Harmita (2004) adalah sebagai berikut:
a. Kecermatan (accuracy)
17
persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan ditentukan dengan dua cara, yaitu:
1. Metode simulasi
Metode simulasi (Spiked-placebo recovery) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang sebenarnya).
2. Metode penambahan baku
Metode penambahan baku (standard addition method) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa penambahan sejumlah analit. Persen perolehan kembali ditentukan dengan menentukan berapa persen analit yang ditambahkan ke dalam sampel dapat ditemukan kembali. Rentang persen perolehan kembali yang diizinkan pada setiap konsentrasi analit pada matriks dapat dilihat pada Tabel 2.2 berikut ini:
Tabel 2.2 Rentang persen perolehan kembali yang diizinkan pada analit
sampel Jumlah analit pada
sampel
Persen perolehan kembali yang diizinkan (%)
1 ppm 80-110
100 ppb 80-110
10 ppb 60-115
1 ppb 40-120
18
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan.
Nilai simpangan baku relatif (RSD) untuk analit dengan kadar part per
million (ppm) adalah tidak lebih dari 16% dan untuk analit dengan kadar part per
billion (ppb) RSD-nya adalah tidak lebih dari 32% (Harmita, 2004)
c. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain yang ada di dalam sampel.
d. Linearitas dan rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon baik secara langsung maupun dengan bantuan transformasi matematika, menghasilkan suatu hubungan yang proporsional terhadap konsentrasi analit dalam sampel. Rentang merupakan batas terendah dan batas tertinggi analit yang dapat ditetapkan secara cermat, seksama dan dalam linearitas yang dapat diterima. e. Batas deteksi dan batas kuantitasi
19
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilakukan dilaboratorium penelitian Fakultas Farmasi USU pada bulan Maret-Mei 2015.
3.2 Bahan-Bahan
3.2.1 Sampel
Sampel yang digunakan adalah umbi ubi kayu kuning, umbi ubi kayu putih, gaplek umbi ubi kayu kuning, dan gaplek umbi ubi kayu putih yang diperoleh dari huta III Gunung Maligas Kecamatan Gunung Maligas Kabupaten Simalungun.
3.2.2 Pereaksi
Semua bahan yang digunakan dalam penelitian ini berkualitas pro analisa keluaran E. Merck (larutan baku kalsium konsentrasi 1000 µg/ml, larutan baku besi konsentrasi 1000 µg/ml, asam nitrat 65% b/v) dan akua demineralisata (Laboratorium Penelitian Fakultas Farmasi USU).
3.3 Alat-Alat
20
tanur, alat-alat gelas (Pyrex dan Oberol), pisau, parutan, blender, kertas saring Whatman no.42, alat destilasi.
3.4 Pembuatan Pereaksi
3.4.1 Larutan HNO3 (1:1)
Asam Nitrat 65% sebanyak 100 ml diencerkan dengan akuademineralisata 100 ml (Ditjen POM, 1979).
3.5 Prosedur Penelitian
3.5.1 Pengambilan Sampel
Sampel yang digunakan adalah umbi ubi kayu kuning dan umbi ubi kayu putih yang diambil secara purposif di Huta III Gunung Maligas Kecamatan Gunung Maligas Kabupaten Simalungun.
Metode pengambilan sampel dilakukan dengan cara sampling purposif yang dikenal juga sebagai sampling pertimbangan, dimana sampel ditentukan atas dasar pertimbangan bahwa semua sampel mempunyai karakteristik yang sama dengan yang diteliti (Sudjana, 2005).
3.5.2 Penyiapan Sampel
3.5.2.1 Sampel Umbi Ubi Kayu Kuning dan Umbi Ubi Kayu Putih
21
3.5.2.2 Sampel Gaplek Umbi Ubi Kayu kuning dan Gaplek Umbi Ubi Kayu Putih
Umbi ubi kayu putih dan umbi ubi kayu kuning dikupas dan dibuang kulitnya, dicuci bersih, ditiriskan, diparut dengan parutan keju, dijemur dibawah sinar matahari selama 7 hari, kemudian diblender hingga halus dan disimpan diwadah plastik
3.5.3 Penetapan Kadar Air
a. Penjenuhan toluen
Toluen sebanyak 200 ml dimasukkan kedalam labu alas bulat, lalu ditambahkan 2 ml air suling, kemudian alat dipasang dan dilakukan destilasi selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama ± 30 menit, kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,05 ml. b. Penetapan kadar Air
22
3.5.4 Proses Dekstruksi
Sampel yang telah dihomogenkan ditimbang sebanyak 25 gram diatas krus porselin, diarangkan diatas hot plate, diabukan dalam tanur dengan temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit, dilakukan selama 48 jam dan dibiarkan hingga dingin didalam tanur. Abu yang diperoleh ditambahkan 5 ml HNO3 (1:1), diuapkan pada hotplate sampai kering, dimasukkan kembali dalam
tanur dengan temperatur awal 100oC dan perlahan-lahan temperatur dinaikkan hingga suhu 500oC dengan interval 25oC setiap 5 menit, dilakukan selama 1 jam dan dibiarkan hingga dingin didalam tanur (suhu ± 27ºC) (Isaac, 1990).
3.5.5 Pembuatan Larutan Sampel
Sampel yang telah didekstruksi dilarutkan dengan 5 ml HNO3 (1:1),
dipindahkan kedalam labu tentukur 50 ml, dibilas krus sebanyak 3x dengan aquademineralisata, dicukupkan dengan akuademineralisata hingga garis tanda. Disaring dengan kertas saring Whatman No. 42, dibuang 2,5 ml filtrat pertama untuk menjenuhkan kertas saring. Filtrat yang diperoleh dimasukkan kedalam botol.
3.5.6 Pemeriksaan Kuantitatif
3.5.6.1 Pembuatan Kurva Kalibrasi Kalsium
23
Dipipet 0.5, 1, 1.5, 2, dan 2,5 ml dari LIB II dimasukkan kedalam labu ukur 25 ml (konsentrasi 2, 4, 6, 8,10 µg/ml) diadkan dengan akuademirelisata hingga garis tanda. Diukur pada panjang gelombang 422,7 nm dengan nyala udara asetilen.
3.5.6.2 Pembuatan Kurva Kalibrasi Besi
Larutan baku besi (1000 µg/ml) dipipet 5 ml, dimasukkan kedalam labu 50 ml, diadkan dengan aquademineralisata hingga garis tanda (Konsentrasi 100 µg/ml) (LIB II).
Dipipet 0.5, 1, 1.5, 2, dan 2,5 ml dari LIB II dimasukkan kedalam labu ukur 50 ml (konsentrasi 1, 2, 3, 4, 5 µg/ml) diadkan dengan aquademineralisata hingga garis tanda. Diukur pada panjang gelombang 248,3 nm dengan nyala udara asetilen.
3.5.6.3 Penetapan Kadar Kalsium dalam Sampel
Larutan sampel hasil dekstruksi masing-masing dipipet 1 ml dimasukkan kedalam labu tentukur 50 ml dan dicukupkan dengan aquademiralisata hingga garis tanda (faktor pengenceran 50 kali). Lalu diukur absorbansinya dengan spektrofotometri serapan atom pada panjang gelombang 422,7 nm. Nilai absorbansi yang diperoleh berada didalam rentang nilai kurva kalibrasi larutan baku. Dengan demikian konsentrasi kalsium dapat dihitung.
Menurut Gandjar dan Rohman (2007) kadar kalsium dapat dihitung dengan rumus: Kadar (µ g/g) = ������
�
Keterangan: C = Konsentrasi Larutan Sampel (µg/ml) V = Volume Larutan Sampel (ml)
24 W= Berat Sampel (g)
3.5.6.4 Penetapan Kadar Besi dalam Sampel
Larutan sampel diukur absorbansinya dengan spektrofotometri serapan atom pada panjang gelombang 248,3 nm. Nilai absorbansi yang diperoleh berada didalam rentang nilai kurva kalibrasi larutan baku. Dengan demikian konsentrasi besi dapat dihitung.
Menurut Gandjar dan Rohman (2007), kadar besi dapat dihitung dengan rumus:
Kadar (µg/g) = ������
�
Keterangan: C = Konsentrasi Larutan Sampel (µg/ml) V = Volume Larutan Sampel (ml)
Fp = Faktor Pengenceran W = Berat Sampel (g)
3.5.7 Analisis Statistik
3.5.7.1 Penolakan Hasil Pengamatan
Kadar kalisum dan besi yang diperoleh dari hasil pengukuran masing masing larutan sampel dianalisis secara statistik. Dimana menurut Sudjana (2005) Standar deviasi dapat dihitung dengan rumus:
SD = �∑(��−�)2
�−1
Keterangan:
Xi = kadar sampel (mg/100g)
25 n = jumlah pengulangan Untuk mencari t hitung digunakan rumus:
t hitung = | Xi−X | SD / √n
Untuk menentukan kadar mineral di dalam sampel dengan interval kepercayaan 99%, α = 0.01, dk = n-1, dapat digunakan rumus:
Kadar Mineral: μ = X ± (t(α/2, dk) x SD / √n ) Keterangan:
X = kadar rata-rata sampel (mg/100g) SD = standar deviasi (mg/100g)
dk = derajat kebebasan (dk = n-1) α = interval kepercayaan
n = jumlah pengulangan
3.5.7.2 Pengujian Beda Nilai Rata-Rata
Untuk mengetahui perbedaan rata-rata kadar kalsium dan besi antar sampel dilakukan analisis statistik menggunakan uji ANOVA dengan Statistical
Services Solution (SPSS) dengan taraf kepercayaan 95%, dengan menggunakan
uji tambahan uji Tukey. Teknik ini merupakan analisis yang fungsinya untuk menguji perbedaan lebih dari dua beda rerata sampel (Alhusin, 2003).
3.6.8 Validasi Metode
3.6.8.1 Uji Perolehan Kembali (recovery)
26
mineral dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar mineral dalam sampel yang sudah ditambahkan larutan standar dengan konsentrasi tertentu, kemudian dihitung berapa jumlah analit yang ditambahkan (Ermer dan McB. Miller, 2005).
Sampel umbi ubi kayu putih yang telah dihaluskan, ditimbang sebanyak 25 g di dalam krus porselin sebanyak 6 krus, lalu masing-masing krus ditambahkan 1 ml larutan baku kalsium (konsentrasi 1000 µ g/ml) dan 1 ml larutan baku besi (konsentrasi 10 µg/ml), perhitungan jumlah baku yang ditambahkan dapat dilihat pada Lampiran 18 halaman 92, kemudian dilanjutkan dengan prosedur dekstruksi kering seperti yang telah dilakukan pada sampel sebelumnya. Prosedur pengukuran uji perolehan kembali dilakukan sama dengan prosedur pengukuran penetapan kadar sampel.
Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
Persen Perolehan Kembali = ���−��
�∗ � 100 %
Keterangan:
CA = kadar logam dalam sampel sebelum penambahan baku (mg/100g)
CF = kadar logam dalam sampel setelah penambahan baku (mg/100g)
C*A = kadar larutan baku yang ditambahkan (mg/100g) 3.6.8.2 Simpangan Baku Relatif
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
27
berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan. Menurut Harmita (2004), rumus untuk menghitung simpangan baku relatif adalah sebagai berikut:
RSD = ×100%
X SD
Keterangan: X = kadar rata-rata sampel (%) SD = standar deviasi (%)
RSD = relative standard deviation (%)
3.6.8.3 Batas Deteksi dan Batas Kuantitasi
Menurut Harmita (2004), batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan. Sebaliknya batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama.
Batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku �SY� �X =�∑(�−���− )2 2
Batas Deteksi (LOD) = 3��������/�
28
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan oleh Herbarium Bogoriense, Bidang Botani, Pusat Penelitian dan Pengembangan Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI), Bogor, Jalan Raya Jakarta–Bogor Km.46, Cibinong. Disebutkan bahwa tumbuhan yang digunakan adalah umbi ubi kayu kuning dan umbi ubi kayu putih (Manihot esculenta Crants). Surat hasil identifikasi tumbuhan dapat dilihat pada Lampiran 1 halaman 40.
4.2 Analisis Kuantitatif
4.2.1 Kurva Kalibrasi Kalsium dan Besi
Kurva kalibrasi kalsium dan besi diperoleh dengan cara mengukur absorbansi dari larutan baku kalsium dan besi pada panjang gelombang masing- masing.
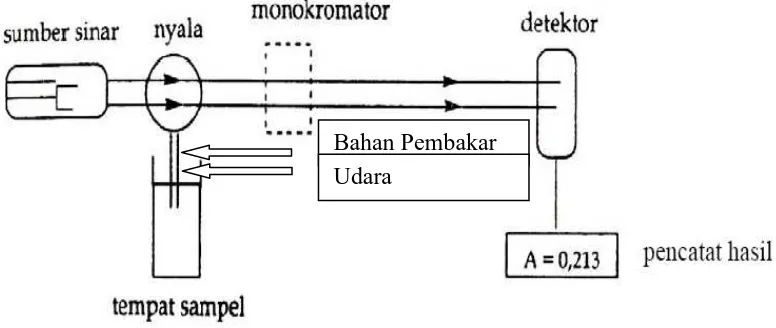
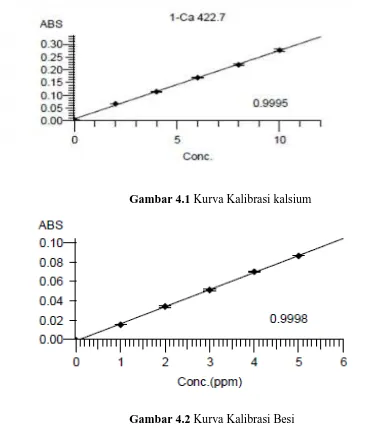
Dari pengukuran kurva kalibrasi untuk kedua mineral tersebut diperoleh persamaan garis regresi yaitu Y = 0,0268X + 0,0079 untuk kalsium dan Y = 0,01758X - 0,0013 untuk besi.
29
[image:46.595.128.502.86.525.2]Gambar 4.1 Kurva Kalibrasi kalsium
Gambar 4.2 Kurva Kalibrasi Besi
Keterangan:
X = Konsentrasi (µ�/��) Y = Absorbansi
30
Data hasil pengukuran absorbansi larutan baku dan perhitungan persamaan garis kalsium dapat dilihat pada Lampiran 9 halaman 52 dan besi dapat dilihat pada Lampiran 10 halaman 54
4.2.2 Penetapan Kadar Kalsium dan Besi dalam Sampel
Penetapan kadar kalsium dan besi dilakukan secara spektrofotometri serapan atom. Sumber nyala yang dipakai adalah udara-asitilen dengan suhu nyala 2200oC yang dapat mengatomisasi hampir semua elemen. Kalsium pada dasarnya merupakan logam alkali yang dapat terionisasi sempurna dengan udara dinitrogen oksida tetapi dalam hal keterbatasan alat dan bahan sangat diperhitungkan, sedangkan besi terionkan sempurna dengan udara asetilen (Gandjar dan Rohman, 2007). Konsentrasi kalsium dan besi dalam sampel ditentukan berdasarkan persamaan garis regresi kurva kalibrasi larutan baku masing-masing. Konsentrasi kalsium belum berada dalam rentang kalibrasi sehingga perlu diencerkan (pengenceran 50 kali) dan besi dalam sampel sudah berada pada rentang kurva kalibrasi maka sampel tidak diencerkan lagi (faktor pengenceran = 1).
31
Tabel 4.1 Hasil penetapan kadar kalsium dan besi dalam sampel
No Sampel
Kadar air (%)
Kadar kalsium (mg/100 g)
Kadar besi (mg/100 g) 1. Umbi ubi kayu kuning 59,61 29,6768 ± 0,5899 0,4212 ± 0,0065 2. Umbi ubi kayu putih 60,56 33,6412 ±0,4633 0,4396 ± 0,0171
3 Gaplek umbi ubi kayu kuning
12,64
60,5842 ± 0,5701 0,8690 ± 0,0055 4 Gaplek umbi ubi kayu
putih
14,64
61,7633 ± 0,8617 0,8081 ± 0,0981
Dari Tabel 4.1 diketahui bahwa kadar kasium dan besi pada sampel umbi ubi kayu kuning dan kadar besi pada umbi ubi kayu putih lebih kecil dibandingkan dengan yang disebutkan oleh Derektorat Gizi Depkes RI (1981) namun kadar kalsium pada umbi ubi kayu putih lebih besar dibandingkan dengan yang disebutkan oleh Derektorat Gizi Depkes RI (1981) yakni 33 mg/100g untuk kalsium dan 0,7 mg/100g untuk besi. Menurut Fitriani, dkk (2012) perbedaan kadar mineral ini disebabkan karena perbedaan umur tanaman, tempat tumbuh dan kesuburan tanah yang ditentukan oleh interaksi sejumlah sifat fisika, kimia dan biologi bagian tubuh tanah.
Kadar mineral kalsium dan besi pada gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih lebih kecil dibandingakan dengan yang disebutkan oleh Derektorat Gizi Depkes RI (1981) yaitu 80 mg/100g untuk kalisum dan 1,9 mg/100g untuk besi. perbedaan kadar ini dapat disebabkan karena proses pengeringan yang kurang sempurna.
32
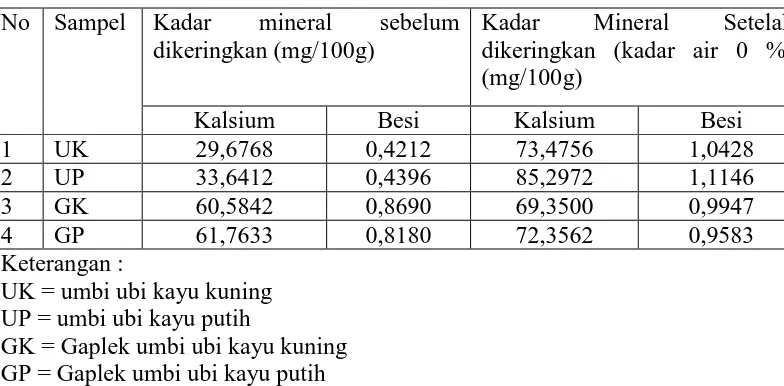
[image:49.595.113.513.180.242.2]umbi kayu putih menjadi gaplek umbi ubi kayu putih (perhitungan dapat dilihat pada Lampiran 14 pada halaman 81).
Tabel 4.2 Hasil peningkatan kadar kalsium dan besi pada umbi ubi kayu kuning (uk) menjadi gaplek umbi ubi kayu kuning (gk)
Mineral Kadar Sampel (mg/100 g) Peningkatan Kadar (%)
Uk Gk
Kalsium 29,6768 60,5842 104,13
Besi 0,4212 0,8690 106,32
Tabel 4.3 Hasil peningkatan kadar kalsium dan besi pada umbi ubi kayu putih (up) menjadi gaplek umbi ubi kayu putih (gp)
Mineral Kadar Sampel (mg/100 g) Peningkatan Kadar (%)
Up Gp
Kalsium 33,6412 61,7633 83,59
Besi 0,4396 0,8081 83,83
[image:49.595.114.512.317.378.2]33
Untuk mengetahui kandungan kalsium dan besi pada sampel yang lebih besar maka dilakukan perhitungan konversi diangkap bahwa sampel setelah dikeringkan memiliki kadar air 0%. Perhitungan dapat dilihat pada Lampiran 15 halaman 83.
Tabel 4.4 Hasil Perhitungan Kadar kalsium dan besi Jika dianggap kadar airnya
0%
No Sampel Kadar mineral sebelum dikeringkan (mg/100g)
Kadar Mineral Setelah dikeringkan (kadar air 0 %) (mg/100g)
Kalsium Besi Kalsium Besi
1 UK 29,6768 0,4212 73,4756 1,0428
2 UP 33,6412 0,4396 85,2972 1,1146
3 GK 60,5842 0,8690 69,3500 0,9947
4 GP 61,7633 0,8180 72,3562 0,9583
Keterangan :
UK = umbi ubi kayu kuning UP = umbi ubi kayu putih
GK = Gaplek umbi ubi kayu kuning GP = Gaplek umbi ubi kayu putih
Dari Tabel 4.4 diketahui bahwa jika dianggap sampel memiliki kadar air 0% maka kadar kalsium dan besi pada umbi ubi kayu putih kering lebih besar dari pada umbi ubi kayu kuning kering.
4.2.3 Pengujian Beda Nilai Rata-rata Kadar Kalsium dan Besi pada Sampel
Pengujian beda nilai rata-rata kalsium dan besi pada sampel dilakukan dengan uji statistik ANOVA dengan tingkat kepercayaan 95% untuk mengetahui apakah variasi antar populasi sama atau berbeda mengunakan sofware SPSS.
Menurut Hartono (2004), pengujian beda nilai rata-rata dapat dilakukan dengan membuat hipotesa terlebih dahulu yaitu:
a. H0 : diduga bahwa keempat dari rata-rata populasi adalah sama.
[image:50.595.113.505.233.426.2]34
Untuk menentukan H0 dan H1 yang diterima maka ketentuan yang berlaku adalah:
a. Bila F hitung sama dan atau lebih kecil dari F tabel maka H0 diterima
dan H1 ditolak.
b. Bila F hitung lebih besar dari F tabel maka H0 ditolak dan H1 diterima.
Hasil pengujian beda nilai rata-rata kadar kalsium dan besi dapat dilihat pada lampiran 16 halaman 85. Hasil Pengujian beda nilai rata-rata kalsium dan besi dapat dilihat pada Tabel 4.5.
Tabel 4.5 Pengujian beda nilai rata-rata kalsium dan besi pada umbi ubi kayu
kuning, umbi ubi kayu putih, gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih.
No Mineral F hitung F table Hasil
1 Kalsium 12073,733 4,30 Beda
2 Besi 8440,780 4,30 Beda
Berdasarkan Tabel 4.5 maka diketahui bahwa terdapat perbedaan kadar kalsium dan besi yang signifikan antara umbi ubi kayu kuning, umbi ubi kayu putih, gaplek umbi ubi kayu kuning dan gaplek umbi ubi kayu putih.
4.2.4 Uji Perolehan Kembali (recovery)
Hasil uji perolehan kembali (recovery) kadar kalsium dan besi setelah penambahan masing-masing larutan baku kalsium dan besi dalam sampel dapat dilihat pada Lampiran 17 halaman 91.
[image:51.595.108.509.333.379.2]35
Tabel 4.6 Persen uji perolehan kembali (recovery) kadar kalsium dan besi dalam
sampel
No. Mineral yang Dianalisis
Rata-Rata Recovery (%)
Syarat Rentang Recovery (%)
1. Kalsium 101,15
80 – 120
2. Besi 106,30
Berdasarkan Tabel 4.6 diatas, dapat dilihat bahwa rata-rata hasil uji perolehan kembali (recovery) tersebut menunjukkan kecermatan kerja yang memuaskan pada saat pemeriksaan kadar kalsium dan besi dalam sampel. Hasil uji perolehan kembali (recovery) ini memenuhi syarat akurasi yang telah ditetapkan, jika rata-rata hasil perolehan kembali (recovery) berada pada rentang 80 – 120% (Ermer dan McB. Miller, 2005).
4.2.5 Simpangan Baku Relatif
Perhitungan simpangan baku relatif kalsium dan besi dalam sampel dapat dilihat pada Lampiran 20 halaman 98. Simpangan baku relatif kalsium dalam sampel dapat dilihat pada Tabel 4.7 berikut:
Tabel 4.7 Simpangan baku relatif kalsium dan besi dalam sampel
No. Mineral yang Dianalisis Simpangan Baku (%) Simpangan Baku Relatif (%) Syarat Simpangan Baku Relatif(%)
1. Kalsium 5,18 5,12
16
2. Besi 7,52 7,07
Nilai simpangan baku relatif (RSD) untuk analit dengan kadar part per
million (ppm) adalah tidak lebih dari 16% dan untuk analit dengan kadar part per
billion (ppb) RSD-nya adalah tidak lebih dari 32% (Harmita, 2004). Dari hasil
[image:52.595.116.513.537.606.2]36
4.2.6 Batas Deteksi dan Batas Kuantitasi
Berdasarkan data kurva kalibrasi kalsium diperoleh batas deteksi dan batas kuantitasi dari kalsium dan besi yang perhitungannya dapat dilihat pada Lampiran 21 halaman 100. Batas deteksi dan batas kuantitasi dari kalsium dan besi dalam sampel dapat dilihat pada Tabel 4.8 berikut:
Tabel 4.8 Batas deteksi dan batas kuantitasi kalsium dan besi
No. Mineral yang
Dianalisis Batas Deteksi (µ g/ml) Batas Kuantitasi (µg/ml)
1. Kalsium 0,4096 1,3654
2. Besi 0,1329 0,4429
37
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Hasil penetapan kadar kalsium dan besi secara spektrofotometri serapan atom sebagai berikut, kadar kalisum dalam umbi ubi kayu kuning sebesar (29,6768 ± 0,5899) mg/100 g, umbi ubi kayu putih sebesar (33,6412 ± 0,4633) mg/100 g, gaplek umbi ubi kayu kuning sebesar (60,5842 ± 0,5701) mg/100 g dan gaplek umbi ubi kayu putih sebesar (61,6412 ± 0,8617) mg/100 g. Kadar besi dalam umbi ubi kayu kuning sebesar (0,4212 ± 0,0065) mg/100 g, umbi ubi kayu putih sebesar (0,4396 ± 0,00171) mg/100 g, gaplek umbi ubi kayu kuning sebesar (0,8690 ± 0,0055) mg/100 g dan gaplek umbi ubi kayu putih sebesar (0,8081 ± 0,0981) mg/100 g.
2. Persentase peningkatan kadar mineral pada gaplek umbi ubi kayu kuning adalah 104,13% untuk kalsium dan 106,32% untuk besi dan pada gaplek umbi ubi kayu putih adalah 83,59% untuk kalsium dan 83,83% untuk besi.
5.2 Saran
38
DAFTAR PUSTAKA
Alhusin, S. (2003). Aplikasi Statistik dengan SPSS 10 For Windows. Yogyakarta: Graha Ilmu. Halaman 123
Almatsier, S. (2002). Prinsip Dasar Ilmu Gizi. Jakarta: Gramedia Pustaka Utama. Halaman 239-243, 249-251.
Barret, D.M dan Damardjjati, D.S. (2015). Peningkatan Mutu Hasil Ubi Kayu di
Indonesia. Sukamandi: Balai Penelitian Tanaman Pangan Sukamandi.
Budiyanto, M. A.K. (2004). Dasar-dasar Ilmu Gizi. Malang: UMM Press. Hal. 60-62.
Direktorat Gizi Depkes RI. (1981). Daftar Komposisi Bahan Makanan. Jakarta: Penerbit Bhratara.
Ditjen POM. (1979). Farmakope Indonesia Edisi Ketiga. Jakarta. Depkes RI. Halaman 692.
Ermer, J., dan McB. Miller, J.H. (2005). Method Validation in Pharmaceutical
Analysis. Weinheim: Wiley-Vch Verlag GmbH & Co. KGaA. Halaman
171.
Fitriani, N.L.C., Walanda, D.K., dan Rahmad, N. (2012). Penetapan Kadar
Kalium (K) dan Kalsium ( Ca) dalam Labu Siam (Sechium Edule) serta Pengaruh Tempat Tumbuuhnya. Pendidikan Kimia/FKIP – University of
Tadulako, Palu. J. Akad. Kim. 1(4): 174-180, November 2012 ISSN 2302-6030
Gandjar, I.G dan Abdul, R. (2007). Kimia Farmasi Analisis.Yogyakarta: Pustaka pelajar. Halaman 298-299.
Harmita. (2004). Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. Review Artikel. Majalah Ilmu Kefarmasian. 1(3). 117 – 119, 121, 122, 127, 128, 130.
Hartono. (2004). Statistika untuk Penelitian. Yogyakarta: Pustaka pelajar. Halaman 243-244.
39
Isaac, R.A. Plants. Dalam: Helrich, K. (1990). Offfcial Methods of Analysis
Association of Official Analytical Chemist. Edisi Kelimabelas. Arlington:
AOCA Internasional. Halaman 42.
Khopkar, S.M. (1985). Basic Concepts of Analytical Chemistry. Penerjemah: Saptorahardjo, A. (2008). Konsep Dasar Kimia Analitik. Jakarta: UI Press. Halaman 298.
Koswara, S. (2015). Teknologi Pengolahan Umbi-Umbian Bagian 6: Pengolahan
Singkong. Bogor: Southeast Asian Food and Agricultural Sciens and
Technology (SEAFAST) Center. Halaman 2-5.
Kristianigrum, S. (2012). Kajian Berbagai Proses Dekstruksi Sampel. Yogyakarta: Prosiding Seminar Nasional Penelitian, Pendidikan dan Penerapan MIPA, Fakultas MIPA, Universitas Negeri Yogyakarta.
Putri, A. R. (2012). Pengaruh Kadar Air terhadap Tekstur dan Warna Keripik
Pisang Kepok. Skripsi. Makasar: Fakultas Pertanian Universitas
Hasanuddin.
Rahmawati, A. (2010). Pemanfaatan Limbah Kulit Ubi Kayu (Manihot esculenta
Crants) dan Kulit Nanas (Ananas comosus L.) pada Produksi Bioetanol Menggunakan Aspergillus niger.Skripsi. Surakarta: Jurusan Biologi
Fakultas Matematika dan Ilmu Pengetahuan Alam Uninersitas Sebelas Maret.
Sediaoetama, A. D. (1999). Ilmu Gizi untuk Mahasiswa dan Profesi Jilid II. Jakarta: PT Dian rakyat. Halaman 104-105.
Sudarmadji, S., Bambang, H dan Suhardi. (1989). Analisa Bahan Makanan dan
Pertanian. Yogyakarta: Liberty. Halaman 63-86.
Sudjana. (2005). Metode Statistika. Edisi Keenam. Bandung: Tarsito. Hal. 93, 168, 239.
WHO. (1998). Quality Control Menthonds For Medicinal plant Material. Switzerland: WHO. Pages 19-25.
40
41
Lampiran 2. Gambar Sampel
Pohon umbi ubi kayu putih Pohon umbi ubi kayu kuning
42
Umbi ubi kayu putih umbi ubi kayu kuning
43
Lampiran 3. Gambar alat spektrofotometer serapan atom (AAS) dan alat tanur
alat spektrofotometer serapan atom (AAS)
44
Lampiran 4. Bagan alir penyiapan sampel ubi kayu kuning dan ubi kayu putih
Umbi ubi kayu putih dan umbi ubi kayu kuning dikupas dan dibuang kulitnya
Dicuci dengan aquademineralisata Ditiriskan
Dihaluskan dengan cara diparut Disimpan dalam wadah plastik
Sampel Yang telah Dihaluskan
45
Lampiran 5. Bagan alir penyiapan sampel gaplek ubi kayu kuning dan gaplek ubi
kayu p utih
Umbi ubi kayu putih dan umbi ubi kayu kuning dikupas dan dibuang kulitnya
Dicuci dengan aquademineralisata Ditiriskan
Dihaluskan dengan cara diparut
Dijemur dibawah sinar matahari selama 7 hari Diblender hinggga halus
Disimpan dalam wadah plastik Sampel yang telah
46
Lampiran 6. Bagan alir proses destruksi kering
Ditimbang 25 gram di dalam krus porselen Diarangkan diatas hot plate
Diabukan dalam tanur dengan temperatur awal 100°C dan perlahan-lahan temperatur dinaikkan hingga suhu 500°C dengan interval 25°C setiap 5 menit
Dilakukan selama 48 jam dan dibiarkan hingga dingin di dalam tanur
Ditambahkan 5 ml HNO3 (1:1) dan diuapkan pada
hot plate sampai kering
Dimasukkan kembali dalam tanur dengan temperatur awal 100°C dan perlahan-lahan temperatur dinaikkan hingga suhu 500°C dengan interval 25°C setiap 5 menit.
Dilakukan selama 1 jam
Dibiarkan hingga dingin didalam tanur (suhu ± 27ºC)
Sampel yang telah dihaluskan
Sampel yang telah mengarang
Abu
47
Lampiran 7. Bagan Alir Pembuatan Larutan Sampel
Dilarutkan dalam 5 ml HNO3 (1:1)
Dipindahkan ke dalam labu tentukur 50 ml
Dibilas krus porselen sebanyak tiga kali dengan 10 ml akua demineralisata, lalu dicukupkan dengan akua demineralisata hingga garis tanda.
Disaring dengan kertas saring Whatman No. 42 Dibuang 2,5 ml untuk menjenuhkan kertas saring
Dimasukkan ke dalam botol
Dilakukan analisis kuantitatif dengan Spektrofotometer Serapan Atom pada λ 422,7 nm untuk kadar kalsium dan pada λ 248,3 nm untuk kadar besi dengan nyala udara -asetilen
sampel hasil deksruksi
filtrat
Larutan Sampel
48
Lampiran 8. Perhitungan Penetapan Kadar Air
1. umbi ubi kayu kuning
- Berat sampel 1 = 5,0053 g Volume air = 2,95 ml Kadar air 1 = ������ ���
����� ������ x 100 %
= 2,95 ��
5,0053 � x 100% = 58,93%
- Berat sampel 2 = 5,0008 g Volume air = 3 ml
Kadar air 1 = ������ ���
����� ������ x 100 %
= 3 ��
5,0008 � x 100% = 59,99%
- Berat sampel 3 = 5,0076 g Volume air = 2,95 ml Kadar air 1 = ������ ���
����� ������ x 100 %
= 2,95 ��
5,0076 � x 100% = 58,91%
- Kadar air rata-rata = 58,93%+59,99%+58,91 3
49
Lampiran 8 (Lanjutan) .
2. gaplek umbi ubi kayu kuning
- Berat sampel 1 = 5,0036 g Volume air = 0,65 ml Kadar air 1 = ������ ���
����� ������ x 100 %
= 0,65��
5,0036 � x 100% = 12,99%
- Berat sampel 2 = 5,0054 g Volume air = 0,65 ml Kadar air 1 = ������ ���
����� ������ x 100 %
= 0,65 ��
5,0054 � x 100% = 12,98%
- Berat sampel 3 = 5,0090 g Volume air = 0,6 ml Kadar air 1 = ������ ���
����� ������ x 100 %
= 0,6��
5,0090 � x 100% = 11,97%
- Kadar air rata-rata = 12,99%+13,98%+11,97% 3
50
Lampiran 8 ( Lanjutan)
3. umbi ubi kayu putih
- Berat sampel 1 = 5,0062 g Volume air = 3, 05 ml Kadar air 1 = ������ ���
����� ������ x 100 %
= 3,05��
5,0062 � x 100% = 60,92%
- Berat sampel 2 = 5,0058 g Volume air = 3 ml
Kadar air 1 = ������ ���
����� ������ x 100 %
= 3 ��
5,0058 � x 100% = 59,93%
- Berat sampel 3 = 5,0124 g Volume air = 3,05 ml Kadar air 1 = ������ ���
����� ������ x 100 %
= 3 ��
5,0124 � x 100% = 60,56%
- Kadar air rata-rata = 60,92%+59,93%+60,56% 3
51
Lampiran 8 (Lanjutan)
4. Gaplek umbi ubi kayu putih
- Berat sampel 1 = 5,0092 g Volume air = 0,75 ml Kadar air 1 = ������ ���
����� ������ x 100 %
= 0,75 ��
5,0092 � x 100% = 14,97%
- Berat sampel 2 = 5,0108 g Volume air = 0,75 ml Kadar air 1 = ������ ���
����� ������ x 100 %
= 30,75��
5,0108 � x 100% = 14,96%
- Berat sampel 3 = 5,0020 g Volume air = 0,7 ml Kadar air 1 = ������ ���
����� ������ x 100 %
= 0,7 ��
5,0020 � x 100% = 13,99%
- Kadar air rata-rata = 14,97%+14,96%+13,99% 3
52
Lampiran 9. Data kalibrasi kalsium dengan spektrofotometer serapan atom,
perhitungan persamaan garis regresi dan koefisien korelasi (r)
No Konsentrasi (µ g/ml) (X)
Absorbansi (Y)
1. 0,0000 0,0044
2. 2,0000 0,0672
3. 4,0000 0,1142
4. 6,0000 0,1689
5. 8,0000 0,2197
6. 10,0000 0,2770
No X Y XY X² Y²
1 0,0000 0,0044 0,0000 0,0000 0,00001936
2 2,0000 0,0672 0,1344 4,0000 0,00451584
3 4,0000 0,1142 0,4568 16,0000 0,01304164
4 6,0000 0,1689 1,0134 36,0000 0,02852721
5 8,0000 0,2197 1,7576 64,0000 0,04826809
6 10,0000 0,2770 2,7700 100,0000 0,0767290 ∑X = 30 ∑Y =
0,8514
∑XY=
6,1322 ∑ X²= 220
∑ Y² = 0,17110114
X= 5 Y= 0,1419
�= ∑�� −((∑ �� ∑ �)/ �)
∑ �²−( (∑ �)² / � )
�= 6,1322 −((30,0000 � 0,8514)/ 6) 220,0000 −((30,0000)2/ 6)
�= 0,0268
Y = a X + b b = Y – a x
53
Lampiran 9 (Lanjutan)
Maka persamaan garis regresinya adalah: Y = 0,0628 X + 0,007
r = ∑XY− [
(∑X )(∑Y ) n ]
��∑X²–(∑X)² / n � (∑Y²−(∑Y)² / n )
r = 6,1322 –�
(30)(0,8514 ) 6 �
��220−(30)2
6 ��0,17110114−
(0,8514 )2 6 � r = 1,87