UJI RASIO LAJU ABSORPSI IBUPROFEN PADA USUS
HALUS KELINCI (Oryctolagus cuniculus) YANG DIKERINGKAN
DENGAN FREEZE DRYER DIBANDINGKAN
DENGAN USUS HALUS KELINCI
(Oryctolagus cuniculus) SEGAR
SKRIPSI
jra Uta
OLEH:
Asni Zahara Rambe
NIM 091501021
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI RASIO LAJU ABSORPSI IBUPROFEN PADA USUS
HALUS KELINCI (Oryctolagus cuniculus) YANG DIKERINGKAN
DENGAN FREEZE DRYER DIBANDINGKAN
DENGAN USUS HALUS KELINCI
(Oryctolagus cuniculus) SEGAR
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh
gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
jra Uta
OLEH:
ASNI ZAHARA RAMBE
NIM 091501021
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI RASIO LAJU ABSORPSI IBUPROFEN PADA USUS
HALUS KELINCI (Oryctolagus cuniculus) YANG DIKERINGKAN
DENGAN FREEZE DRYER DIBANDINGKAN
DENGAN USUS HALUS KELINCI
(Oryctolagus cuniculus) SEGAR
OLEH:
ASNI ZAHARA RAMBE NIM 091501021
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 21 Desember 2013
Pembimbing I, Panitia Penguji,
Prof. Dr. M. T. Simanjuntak, M.Sc., Apt. Dr. Kasmirul Ramlan Sinaga, M.S., Apt. NIP 195212041980021001 NIP 195504241983031003
Pembimbing II, Prof. Dr. M. T. Simanjuntak, M.Sc., Apt. NIP 195212041980021001
KATA PENGANTAR
Puji syukur kehadirat Allah SWT yang telah memberikan karunia yang
berlimpah sehingga penulis dapat menyelesaikan penyusunan skripsi yang berjudul
Uji Rasio Laju Absorpsi Ibuprofen pada Usus Halus Kelinci (Oryctolagus cuniculus)
yang Dikeringkan dengan Freeze Dryer Dibandingkan dengan Usus Halus Kelinci
(Oryctolagus cuniculus) Segar. Skripsi ini diajukan untuk melengkapi salah satu
syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas
Sumatera Utara.
Pada kesempatan ini, dengan segala kerendahan hati penulis mengucapkan
terima kasih kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan
Fakultas Farmasi yang telah menyediakan fasilitas kepada penulis selama perkuliahan
di Fakultas Farmasi. Penulis juga mengucapkan terima kasih yang sebesar-besarnya
kepada Bapak Prof. Dr. M. T. Simanjuntak, M.Sc., Apt., dan Bapak Prof. Dr.
Karsono, Apt., yang telah membimbing penulis dengan penuh kesabaran dan
tanggung jawab, memberikan petunjuk dan saran-saran selama penelitian hingga
selesainya skripsi ini. Ucapan terima kasih juga penulis sampaikan kepada Bapak Dr.
Kasmirul Ramlan Sinaga, M.S., Apt., selaku ketua penguji, Bapak Drs. Fathur
Rahman Harun, M.Si., Apt., dan Bapak Drs. Saiful Bahri, M.S., Apt., selaku anggota
penguji yang telah memberikan saran untuk menyempurnakan skripsi ini, dan Ibu
Dra. Suwarti Aris, M.Si., Apt., selaku dosen penasehat akademik yang telah banyak
membimbing penulis selama masa perkuliahan hingga selesai.
Penulis mengucapkan terima kasih sebesar-besarnya kepada keluarga tercinta,
Ayahanda Alm. Hajopan Rambe dan Ibunda Roslena Nasution, dan kakakku Ade
Rambe, yang telah memberikan semangat dan kasih sayang yang tak ternilai dengan
apapun. Penulis juga mengucapkan terima kasih kepada teman-teman mahasiswa/i
Farmasi angkatan 2009 yang selalu mendoakan dan memberi semangat.
Penulis menyadari sepenuhnya bahwa penulisan skripsi ini masih belum
sempurna. Oleh karena itu, penulis mengharapkan saran dan kritik yang membangun
demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini
bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, Desember 2013 Penulis,
UJI RASIO LAJU ABSORPSI IBUPROFEN PADA USUS HALUS KELINCI
(Oryctolagus cuniculus) YANG DIKERINGKAN DENGANFREEZE DRYER
DIBANDINGKAN DENGAN USUS HALUS KELINCI (Oryctolagus cuniculus) SEGAR
Abstrak
Usus halus mempunyai karakteristik anatomi dan fisiologi yang lebih menguntungkan untuk penyerapan obat. Namun, metode in vitro pada usus halus mempunyai kekurangan yang disebabkan oleh ketidakmampuan usus halus untuk mempertahankan strukturnya dalam jangka waktu yang lama. Pengeringan beku
(freeze dryer) adalah salah satu metode pengeringan yang mempunyai keunggulan
dalam mempertahankan mutu hasil pengeringan, khususnya untuk produk-produk yang sensitif terhadap panas. Tujuan penelitian ini adalah untuk mengetahui perbedaan antara usus halus kelinci segar dan usus halus kelinci yang dikeringkan dengan freeze dryer terhadap laju absorpsi ibuprofen baku, ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®) dan untuk mengetahui perbedaan laju absorpsi ibuprofen baku, ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®) pada usus halus kelinci yang dikeringkan maupun usus halus kelinci segar sehingga dapat diketahui kelayakan pengeringan usus dengan teknik freeze dryer agar dapat digunakan pada penelitian absorpsi suatu obat.
Penelitian ini dilakukan dengan metode usus halus terbalik kelinci, menggunakan alat Crane dan Wilson yang telah dimodifikasi. Jenis sediaan ibuprofen yang dibandingkan adalah ibuprofen baku, ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®) dengan media larutan dapar fosfat pH 6,4 isotonis. Kadar ibuprofen yang terabsorpsi diperiksa dalam larutan dapar fosfat dengan menggunakan spektrofotometer ultraviolet pada panjang gelombang 222,5 nm dan data yang diperoleh dianalisis dengan menggunakan Statistical Program Service
Solution (SPSS).
Hasil penelitian menunjukkan bahwa laju absorpsi ibuprofen dipengaruhi oleh jenis sediaan dan keadaan usus. Pada usus halus kelinci segar laju absorpsi ibuprofen tablet merek dagang (Proris®) (0,764 mcg/ml.menit) > ibuprofen baku (0,679 mcg/ml.menit) > ibuprofen tablet generik (0,540 mcg/ml.menit) dan pada usus halus kelinci yang dikeringkan laju absorpsi ibuprofen tablet merk dagang (Proris®) (0,686 mcg/ml.menit) > ibuprofen baku (0,516 mcg/ml.menit) > ibuprofen tablet generik (0,438 mcg/ml.menit). Berdasarkan hasil uji statistik dengan menggunakan uji
Independent Sample T Test untuk laju absorpsi diketahui tidak terdapat perbedaan
yang signifikan antara usus halus kelinci segar dan usus halus kelinci yang dikeringkan dengan nilai signifikansi 0,059 dan terdapat perbedaan yang signifikan antara laju absorpsi ibuprofen baku, ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®) dengan nilai signifikansi 0,001 dengan menggunakan uji One
Way ANOVA.
RATIO OF IBUPROFEN ABSORPTION RATE TEST IN FREEZE-DRIED AND FRESH RABBIT SMALL INTESTINE (Oryctolagus cuniculus)
Abstract
The intestine has advantageous anatomy and physiological characteristic for drug absorption. However,the in vitro method for intestine has a disadvantage caused by its inability to mantain its structure in a long period of time. Freeze drying is a drying method which has advantageous for maintaining the quality of the dried materials especially for heat-sensitive products.The purpose of this study is to determine differences of fresh and freeze dried small intestine in standard ibuprofen, generic tablet ibuprofen and brand name tablet (Proris®) absorption rate and to determine differences of standard ibuprofen, generic tablet ibuprofen and brand name tablet (Proris®) absorption rate in freeze-dried and fresh small intestine so as to know the feasibility of dried of freeze dryer intestine that can be used to absorption of a drug study.
This study was done with everted sac of rabbit’s intestine, used Crane and Wilson apparatus which have been modified. The type of preparation of ibuprofen compared to is standard ibuprofen, generic tablet ibuprofen and brand name tablet ibuprofen (Proris®) in buffer phosphate at pH 6,4 isotonis medium. Determination of absorpted ibuprofen which was checked in buffer phosphate isotonic solution by using ultraviolet spectrophotometer at wavelength 222,5 nm and obtained data was analyzed by using Statistical Program Service Solution (SPSS).
The result of this study showed that the rate of ibuptofen absorption is influenced by the type of ibuprofen preparation and intestine conditions. In fresh rabbit small intestine the rate of brand name tablet ibuprofen (Proris®) (0.764 mcg/ml.menit) > standard ibuprofen (0.679 mcg/ml.menit) > generic tablet ibuprofen (0.540 mcg/ml.menit) and in dried rabbit small intestine the rate of brand name tablet ibuprofen (Proris®) (0.686 mcg/ml.menit) > standard ibuprofen (0.516 mcg/ml.menit) > generic tablet ibuprofen (0.438 mcg/ml.menit). Based on the results of statistical test using Independent Sample T Test for the rate of absorption is known that there are no significant differences between fresh and dried rabbit small intestine with a significance value of 0.059 and there are differences significantly between standard ibuprofen, generic tablet ibuprofen and brand name tablet ibuprofen (Proris®) absorption rate with a significance value of 0.001 using One Way ANOVA test.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BA I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
1.6 Kerangka Pikir Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 6
2.1 Ibuprofen ... 6
2.1.1 Sifat fisikokimia ... ... 6
2.1.2 Farmakokinetik ... ... 6
2.1.3 Farmakodinamik ... ... 7
2.2 Absorpsi ... 7
2.2.1 Membran sel ... 9
2.2.2 Struktur membran sel ... 10
2.2.3 Cara penembusan obat melalui membran biologis ... 11
2.3 Usus Halus ... 14
2.4 Metode Kantung Terbalik (Everted Sac) ... 17
2.5 Kinetika Laju Absorpsi ... 18
2.6 Pengeringan Beku (Freeze Dryer) ... 19
2.7 Spektrofotometri Ultraviolet-visibel ... 20
BAB III METODE PENELITIAN ... 22
3.1 Rancangan Penelitian ... 22
3.2 Tempat dan Waktu Penelitian ... 23
3.3 Alat dan Bahan ... 23
3.3.1 Alat ... ………. 23
3.3.2 Bahan ... ………. 23
3.4 Hewan Percobaan ... 23
3.5 Prosedur ... 24
3.5.1 Pembuatan pereaksi ... 24
3.5.1.1 Pembuatan air bebas karbondioksida ... 24
3.5.1.2 Pembuatan kalium dihidrogenfosfat 0,2 M ... 24
3.5.1.3 Pembuatan larutan natrium hidroksida 0,2 N ... 24
3.5.1.4 Pembuatan dapar fosfat pH 6,4 isotonis ... 24
3.5.1.5 Pembuatan larutan thyrode ... 24
3.5.3 Pembuatan kurva kalibrasi ibuprofen dalam medium dapar
fosfat pH 6,4 isotonis ... 25
3.5.4 Pembuatan larutan obat ibuprofen baku dengan konsentrasi
2 mmol/L ... 25
3.5.5 Pembuatan larutan obat ibuprofen generik dengan konsen-
trasi 2 mmol/L ... 25
3.5.6 Pembuatan larutan obat Proris® dengan konsentrasi 2
mmol/L ... 25
4.1 Penentuan Panjang Gelombang Maksimum Ibuprofen dalam
Larutan Dapar Fosfat pH 6,4 Isotonis ... 30
4.2 Pembuatan Kurva Kalibrasi dan Penentuan Persamaan Regresi Ibuprofen Baku dalam Larutan Dapar Fosfat pH 6,4 Isotonis.. 30
4.3 Pengecatan Membran Usus Halus Kelinci ... 30
4.5 Pengaruh Perbedaan Jenis Usus dan Jenis Sediaan Ibuprofen Terhadap Laju Absorpsi Ibuprofen pada Usus Halus Terbalik
Kelinci ... 35
4.6 Pengaruh Perbedaan Jenis Usus dan Jenis Sediaan Ibuprofen Terhadap Harga AUC (Area Under The Curve) Ibuprofen pada Usus Halus Terbalik Kelinci ... 38
BAB V KESIMPULAN DAN SARAN ... 40
5.1 Kesimpulan ... 40
5.2 Saran ... 40
DAFTAR PUSTAKA ... 41
DAFTAR TABEL
Halaman
Tabel 4.1 Data konsentrasi kumulatif ibuprofen pada interval waktu tertentu dalam mcg/ml pada usus halus kelinci segar ... 33
Tabel 4.2 Data konsentrasi kumulatif ibuprofen pada interval waktu tertentu dalam mcg/ml pada usus halus kelinci yang dike-
ringkan ... 34
Tabel 4.3 Data laju absorpsi ibuprofen pada usus halus kelinci segar dan usus halus kelinci yang dikeringkan (mcg/ml.menit)
... 37
Tabel 4.4 Data perbandingan harga AUC (area under the curve) berbagai sediaan ibuprofen dalam cairan serosa usus halus terbalik kelinci segar dalam mcg.menit/ml ... 38
DAFTAR GAMBAR
Halaman
Gambar1.1 Kerangka pikir penelitian ... 5
Gambar 2. Rumus bangun ibuprofen ... 6
Gambar 2.2 Struktur membran sel ... 10
Gambar 2.3 Difusi pasif melalui pori ... 11
Gambar 2.4 Sistem pengangkutan aktif ... 14
Gambar 2.5 Sistem pengangkutan secara pinositosis ... 14
Gambar 2.6 Skema usus halus dengan villi dan perfusinya ... 17
Gambar 4.1 Pengecatan membran hematoksilin-eosin usus halus kelinci segar ... 31
Gambar 4.2 Grafik konsentrasi kumulatif terhadap waktu dari ibuprofen baku ... 35
Gambar 4.3 Grafik konsentrasi kumulatif terhadap waktu dari ibuprofen generik ... 36
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Bagan alur penelitian ... 43
Lampiran 2 Flowsheet pembuatan larutan induk baku ibuprofen dalam larutan dapar fosfat pH 6,4 isotonis ... 44
Lampiran 3 Flowsheet penentuan panjang gelombang maksimum ibuprofen baku dalam larutan dapar fosfat ph 6,4 isotonis 45
Lampiran 4 Penentuan kurva serapan ibuprofen baku dalam larutan dapar fosfat pH 6,4 isotonis ... 46
Lampiran 5 Flowsheet pembuatan kurva kalibrasi ibuprofen baku dalam larutan dapar fosfat pH 6,4 isotonis.. ... 47
Lampiran 6 Penentuan persamaan regresi dan kurva kalibrasi ibuprofen baku dalam larutan dapar fosfat pH 6,4 isotonis ….. ... 48
Lampiran 7 Flowsheet pembuatan usus halus terbalik kelinci ... 50
Lampiran 8 Flowsheet penentuan pola penembusan membran oleh berbagai sediaan ibuprofen pada usus halus terbalik kelinci 51
Lampiran 9 Contoh perhitungan pembuatan larutan obat ibuprofen 2 mmol/L ... 52
Lampiran 10 Contoh perhitungan penentuan harga konsentrasi ibuprofen baku dalam cairan serosa usus halus terbalik kelinci dalam mcg/ml... 53
Lampiran 11 Contoh perhitungan penentuan harga konsentrasi kumulatif ibuprofen baku dalam cairan serosa usus halus terbalik kelinci dalam mcg/ml ... 54
Lampiran 12 Contoh perhitungan penentuan harga konsentrasi kumulatif ibuprofen baku dalam cairan serosa usus halus terbalik kelinci dalam mcg/ml ... 55
Lampiran 13 Data absorbansi berbagai sediaan ibuprofen dalam cairan serosa usus halus terbalik kelinci segar dan usus halus terbalik kelinci yang dikeringkan ... 56
Lampiran 15 Data konsentrasi kumulatif berbagai sediaan ibuprofen dalam cairan serosa usus halus terbalik kelinci segar dan
usus halus terbalik kelinci yang dikeringkan ... 64
Lampiran 16 Hasil analisis uji independent sample t test dan uji one way anova laju absorpsi ibuprofen ... 66
Lampiran 17 Sertifikat analisa bahan baku ibuprofen ... 68
Lampiran 18 Gambar alat-alat yang digunakan ... 69
UJI RASIO LAJU ABSORPSI IBUPROFEN PADA USUS HALUS KELINCI
(Oryctolagus cuniculus) YANG DIKERINGKAN DENGANFREEZE DRYER
DIBANDINGKAN DENGAN USUS HALUS KELINCI (Oryctolagus cuniculus) SEGAR
Abstrak
Usus halus mempunyai karakteristik anatomi dan fisiologi yang lebih menguntungkan untuk penyerapan obat. Namun, metode in vitro pada usus halus mempunyai kekurangan yang disebabkan oleh ketidakmampuan usus halus untuk mempertahankan strukturnya dalam jangka waktu yang lama. Pengeringan beku
(freeze dryer) adalah salah satu metode pengeringan yang mempunyai keunggulan
dalam mempertahankan mutu hasil pengeringan, khususnya untuk produk-produk yang sensitif terhadap panas. Tujuan penelitian ini adalah untuk mengetahui perbedaan antara usus halus kelinci segar dan usus halus kelinci yang dikeringkan dengan freeze dryer terhadap laju absorpsi ibuprofen baku, ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®) dan untuk mengetahui perbedaan laju absorpsi ibuprofen baku, ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®) pada usus halus kelinci yang dikeringkan maupun usus halus kelinci segar sehingga dapat diketahui kelayakan pengeringan usus dengan teknik freeze dryer agar dapat digunakan pada penelitian absorpsi suatu obat.
Penelitian ini dilakukan dengan metode usus halus terbalik kelinci, menggunakan alat Crane dan Wilson yang telah dimodifikasi. Jenis sediaan ibuprofen yang dibandingkan adalah ibuprofen baku, ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®) dengan media larutan dapar fosfat pH 6,4 isotonis. Kadar ibuprofen yang terabsorpsi diperiksa dalam larutan dapar fosfat dengan menggunakan spektrofotometer ultraviolet pada panjang gelombang 222,5 nm dan data yang diperoleh dianalisis dengan menggunakan Statistical Program Service
Solution (SPSS).
Hasil penelitian menunjukkan bahwa laju absorpsi ibuprofen dipengaruhi oleh jenis sediaan dan keadaan usus. Pada usus halus kelinci segar laju absorpsi ibuprofen tablet merek dagang (Proris®) (0,764 mcg/ml.menit) > ibuprofen baku (0,679 mcg/ml.menit) > ibuprofen tablet generik (0,540 mcg/ml.menit) dan pada usus halus kelinci yang dikeringkan laju absorpsi ibuprofen tablet merk dagang (Proris®) (0,686 mcg/ml.menit) > ibuprofen baku (0,516 mcg/ml.menit) > ibuprofen tablet generik (0,438 mcg/ml.menit). Berdasarkan hasil uji statistik dengan menggunakan uji
Independent Sample T Test untuk laju absorpsi diketahui tidak terdapat perbedaan
yang signifikan antara usus halus kelinci segar dan usus halus kelinci yang dikeringkan dengan nilai signifikansi 0,059 dan terdapat perbedaan yang signifikan antara laju absorpsi ibuprofen baku, ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®) dengan nilai signifikansi 0,001 dengan menggunakan uji One
Way ANOVA.
RATIO OF IBUPROFEN ABSORPTION RATE TEST IN FREEZE-DRIED AND FRESH RABBIT SMALL INTESTINE (Oryctolagus cuniculus)
Abstract
The intestine has advantageous anatomy and physiological characteristic for drug absorption. However,the in vitro method for intestine has a disadvantage caused by its inability to mantain its structure in a long period of time. Freeze drying is a drying method which has advantageous for maintaining the quality of the dried materials especially for heat-sensitive products.The purpose of this study is to determine differences of fresh and freeze dried small intestine in standard ibuprofen, generic tablet ibuprofen and brand name tablet (Proris®) absorption rate and to determine differences of standard ibuprofen, generic tablet ibuprofen and brand name tablet (Proris®) absorption rate in freeze-dried and fresh small intestine so as to know the feasibility of dried of freeze dryer intestine that can be used to absorption of a drug study.
This study was done with everted sac of rabbit’s intestine, used Crane and Wilson apparatus which have been modified. The type of preparation of ibuprofen compared to is standard ibuprofen, generic tablet ibuprofen and brand name tablet ibuprofen (Proris®) in buffer phosphate at pH 6,4 isotonis medium. Determination of absorpted ibuprofen which was checked in buffer phosphate isotonic solution by using ultraviolet spectrophotometer at wavelength 222,5 nm and obtained data was analyzed by using Statistical Program Service Solution (SPSS).
The result of this study showed that the rate of ibuptofen absorption is influenced by the type of ibuprofen preparation and intestine conditions. In fresh rabbit small intestine the rate of brand name tablet ibuprofen (Proris®) (0.764 mcg/ml.menit) > standard ibuprofen (0.679 mcg/ml.menit) > generic tablet ibuprofen (0.540 mcg/ml.menit) and in dried rabbit small intestine the rate of brand name tablet ibuprofen (Proris®) (0.686 mcg/ml.menit) > standard ibuprofen (0.516 mcg/ml.menit) > generic tablet ibuprofen (0.438 mcg/ml.menit). Based on the results of statistical test using Independent Sample T Test for the rate of absorption is known that there are no significant differences between fresh and dried rabbit small intestine with a significance value of 0.059 and there are differences significantly between standard ibuprofen, generic tablet ibuprofen and brand name tablet ibuprofen (Proris®) absorption rate with a significance value of 0.001 using One Way ANOVA test.
BAB I
PENDAHULUAN
1.1Latar Belakang
Absorpsi atau penyerapan zat aktif adalah masuknya molekul-molekul obat
kedalam tubuh atau menuju ke peredaran darah tubuh setelah melewati sawar
biologik (Aiache, et al., 1993). Absorpsi obat adalah peran yang terpenting untuk
akhirnya menentukan efektivitas obat (Joenoes, 2002). Agar suatu obat dapat
mencapai tempat kerja di jaringan atau organ, obat tersebut harus melewati berbagai
membran sel. Membran sel mempunyai pori yang bergaris tengah antara 3,5 - 4,2 Ǻ, merupakan saluran berisi air dan dikelilingi oleh rantai samping molekul protein yang
bersifat polar. Zat terlarut dapat melewati pori ini secara difusi karena kekuatan
tekanan darah (Siswandono dan Soekardjo, 2000). Sebelum obat diabsorpsi, terlebih
dahulu obat itu larut dalam cairan biologis. Kelarutan serta cepat-lambatnya melarut
menentukan banyaknya obat terabsorpsi. Dalam hal pemberian obat per oral, cairan
biologis utama adalah cairan gastrointestinal, dari sini melalui membran biologis obat
masuk ke peredaran sistemik (Joenoes, 2002).
Laju disolusi atau kecepatan melarut obat yang relatif tidak larut dalam air
telah lama menjadi masalah pada industri farmasi. Ibuprofen termasuk pada senyawa
model biopharmaceutical classification system (BCS) II, permeabilitas tinggi
kelarutan rendah (Dahan dan Amidon, 2009). Untuk obat yang mempunyai kelarutan
rendah laju disolusi merupakan tahap penentu pada proses absorpsi obat (Shargel dan
Yu, 2005).
Usus halus mempunyai karakteristik anatomi dan fisiologi yang lebih
usus halus terutama karena banyaknya lipatan-lipatan mukosa yang terutama banyak
terdapat di daerah duodenum dan jejunum (Aiache, et al., 1993). Metode in vitro pada
usus halus mempunyai kekurangan yang disebabkan oleh ketidakmampuan usus
halus untuk mempertahankan strukturnya dalam jangka waktu yang lama.
Beberapa metode pengeringan seperti pengeringan dengan sinar matahari,
pengeringan dengan oven, pengeringan beku dan lain sebagainya sering digunakan
untuk mengeringkan suatu zat dengan tujuan agar zat tersebut tidak rusak dalam
penyimpanannya. Pengeringan beku (freeze drying) adalah salah satu metode
pengeringan yang mempunyai keunggulan dalam mempertahankan mutu hasil
pengeringan, khususnya untuk produk-produk yang sensitif terhadap panas.
Keunggulan pengeringan beku dibandingkan metode lainnya yaitu dapat
mempertahankan stabilitas produk, dapat mempertahankan stabilitas struktur bahan
dan dapat meningkatkan daya rehidrasi sehingga dapat kembali ke sifat fisiologis,
organoleptik dan betuk fisik yang hampir sama dengan sebelum pengeringan
(Tambunan dan Lamhot, 2000). Proses pengeringan usus halus kelinci dengan
menggunakan freeze dryer diharapkan dapat mempertahankan struktur dari usus halus
kelinci dalam jangka waktu yang lama dan dapat memberikan hasil pengujian yang
sama dengan usus halus kelinci segar.
Metode kantung terbalik merupakan teknik in vitro yang mudah dan cepat
dilaksanakan serta dapat ditemukan seluruh tipe sel dan lapisan mukosa sehingga
mencerminkan proses/lingkungan sebenarnya saat obat mengalami proses absorpsi di
usus (Barthe, et al., 1999). Metode ini baik digunakan untuk menentukan absorpsi
pada tempat yang berbeda pada usus halus. Hal ini sangat berguna untuk
mengestimasi first-pass metabolism dari obat dalam sel epithelial intestinal
Ibuprofen merupakan obat yang termasuk ke dalam kelompok AINS (anti
inflamasi non steroid). Ibuprofen dapat digunakan untuk mengurangi nyeri yang
ringan hingga sedang, khususnya nyeri oleh karena inflamasi seperti yang terdapat
pada arthritis dan gout (Trevor, et al., 2005; Anderson, et al., 2002). Ibuprofen
diabsorpsi dengan cepat dalam saluran cerna, kadar serum tertinggi terjadi dalam 1-2
jam setelah pemberian oral, waktu paruh 1,8-2 jam (Siswadono dan Soekardjo, 2000).
Studi biofarmasetika menyatakan bahwa metode fabrikasi dan formulasi akan
mempengaruhi ketersediaan hayati suatu obat (Shargel dan Yu, 2005). Pada
pembuatan sediaan obat tablet generik dan tablet merk dagang terdapat perbedaan
pada metode fabrikasi dan formulasi. Oleh karena itu dilakukan pengujian pada
ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®).
Berdasarkan hal-hal tersebut, peneliti tertarik untuk memeriksa rasio laju
absorpsi ibuprofen baku, ibuprofen tablet generik dan ibuprofen merk dagang
(Proris®) pada usus halus kelinci (oryctolagus cuniculus) yang dikeringkan dengan
freeze dryer dan usus halus kelinci segar.
1.2 Perumusan Masalah
Berdasarkan latar belakang di atas, maka yang menjadi perumusan masalah
dalam penelitian ini adalah:
- Apakah ada perbedaan antara usus halus kelinci segar dan usus halus kelinci
yang dikeringkan dengan freeze dryer terhadap laju absorpsi ibuprofen baku,
ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®)
- Apakah ada perbedaan laju absorpsi ibuprofen baku, ibuprofen tablet generik
dan ibuprofen tablet merk dagang (Proris®) pada usus halus kelinci yang
1.3Hipotesis
Berdasarkan perumusan masalah di atas, maka yang menjadi hipotesis dalam
penelitian ini adalah:
- Tidak terdapat perbedaan antara usus halus kelinci segar dan usus halus
kelinci yang dikeringkan dengan freeze dryer terhadap laju absorpsi ibuprofen
baku, ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®)
- Tidak terdapat perbedaan laju absorpsi ibuprofen baku, ibuprofen tablet
generik dan ibuprofen tablet merk dagang (Proris®) pada usus halus kelinci
yang dikeringkan maupun usus halus kelinci segar
1.4Tujuan Penelitian
Berdasarkan hipotesis di atas, maka yang menjadi tujuan dalam penelitian ini
adalah :
- Untuk mengetahui perbedaan antara usus halus kelinci segar dan usus halus
kelinci yang dikeringkan dengan freeze dryer terhadap laju absorpsi ibuprofen
baku, ibuprofen tablet generik dan ibuprofen tablet merk dagang (Proris®)
- Untuk mengetahui perbedaan laju absorpsi ibuprofen baku, ibuprofen tablet
generik dan ibuprofen tablet merk dagang (Proris®) pada usus halus kelinci
yang dikeringkan maupun usus halus kelinci segar
1.5 Manfaat Penelitian
Adapun manfaat penelitian ini adalah untuk pengembangan metode absorpsi
1.6 Kerangka Pikir Penelitian
Penelitian dimulai dengan pembuatan usus halus kelinci segar dan usus halus
kelinci yang dikeringkan, pengecatan membran, dan penentuan absorpsi ibuprofen
pada kedua usus tersebut.
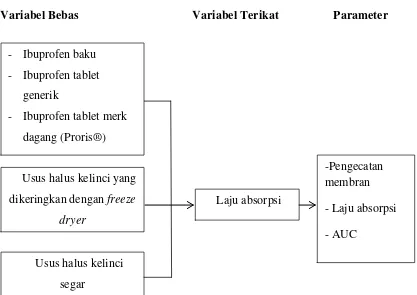
Secara skematis kerangka pikir penelitian ini ditunjukkan pada Gambar 1.1.
sebagai berikut:
Variabel Bebas Variabel Terikat Parameter
Gambar 1.1 Kerangka pikir penelitian Usus halus kelinci yang
dikeringkan dengan freeze
dryer
Usus halus kelinci
segar - Ibuprofen baku
- Ibuprofen tablet
generik
- Ibuprofen tablet merk
dagang (Proris®)
-Pengecatan membran
- Laju absorpsi
BAB II
TINJAUAN PUSTAKA
2.1 Ibuprofen
2.1.1 Sifat fisikokimia
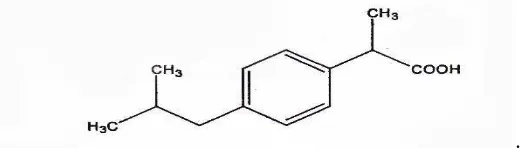
Ibuprofen ((±)-2-(p-isobutilfenil) asam propionat) dengan rumus molekul
C13H18O2 dan berat molekul 206,28. Rumus bangun ibuprofen seperti yang
ditunjukkan pada Gambar 2.1.
.
Gambar 2.1 Rumus bangun ibuprofen
Ibuprofen berupa serbuk hablur, putih hingga hampir putih, berbau khas
lemah. Ibuprofen praktis tidak larut dalam air, sangat mudah larut dalam etanol,
metanol, aseton dan dalam kloroform, sukar larut dalam etil asetat (Ditjen POM,
1995). Larut dalam larutan alkali hidroksida dan karbonat. Senyawa ini mempunyai
titik lebur 75-77º C dengan pKa 4,4; 5,2 dan log P (oktanol/air) 4,0 (Moffat, et al.,
2005).
2.1.2 Farmakokinetik
Ibuprofen diabsorpsi dengan cepat melalui saluran pencernaan dengan
bioavailabilitas lebih besar dari 80%. Puncak konsentrasi plasma dapat dicapai
setelah 1-2 jam. Ibuprofen menunjukkan pengikatan (99%) yang menyeluruh dengan
protein plasma (Anderson, 2002). Pada manusia sehat volume distribusi relatif rendah
90% dari dosis yang diabsorpsi akan dieksresi melalui urin sebagai metabolit atau
konyugatnya. Metabolit utama merupakan hasil hidroksilasi dan karboksilasi
(Stoelting, 2006; Sinatra, et al., 1992).
2.1.3 Farmakodinamik
Mekanisme kerja ibuprofen melalui inhibisi sintesa prostaglandin dan
menghambat siklooksigenase-I (COX I) dan siklooksigenase-II (COX II). Namun
tidak seperti aspirin hambatan yang diakibatkan olehnya bersifat reversibel. Dalam
pengobatan dengan ibuprofen, terjadi penurunan pelepasan mediator dari granulosit,
basofil dan sel mast, terjadi penurunan kepekaan terhadap bradikinin dan histamin,
mempengaruhi produksi limfokin dan limfosit T, melawan vasodilatasi dan
menghambat agregasi platelet (Stoelting, 2006).
2.1.4 Indikasi dan dosis terapi
Ibuprofen dapat digunakan untuk mengurangi nyeri yang ringan hingga
sedang, khususnya nyeri oleh karena inflamasi seperti yang terdapat pada arthritis dan
gout (Trevor, et al., 2005; Anderson, et al., 2002). Untuk mengurangi nyeri ringan
hingga sedang dosis dewasa penggunaan ibuprofen per oral adalah 200-400 mg,
untuk nyeri haid 400 mg per oral kalau perlu. Untuk arthritis rheumatoid 400-800 mg.
Untuk demam pada anak-anak 5 mg/kg berat badan, untuk nyeri pada anak-anak 10
mg/ kg berat badan, untuk arthritis juvenil 30-40 mg/ kg berat badan/hari (Anderson,
et al., 2002).
2.2 Absorpsi
Yang dimaksud dengan absorpsi atau penyerapan suatu zat aktif adalah
masuknya molekul-molekul obat ke dalam tubuh atau menuju peredaran darah tubuh
Untuk dapat diserap, semua zat aktif harus terlarut lebih dahulu. Oleh sebab
itu laju penyerapan merupakan fungsi dari laju pelarutan zat aktif didalam cairan
tubuh (saluran cerna misalnya) dan laju difusi molekul-molekul yang terlarut dalam
cairan tersebut melintasi membran seluler, sesuai dengan skema sebagai berikut:
Proses penyerapan tersebut berkaitan dengan prinsip: sebelum melintasi
membran biologik, zat aktif harus terlarut lebih dahulu didalam cairan disekitar
membran.
Bila zat aktif berada dalam suatu bentuk sediaan, maka sebelum melarut zat
aktif harus terlepas dari sediaan, dan selanjutnya berdifusi dan diserap menurut
tahapan sebagai berikut:
Bila proses pelepasan terjadi sangat lambat, maka pelepasan akan
mempengaruhi seluruh waktu dan tahapan proses pelarutan, difusi dan penyerapan zat
aktif. Jadi tahapan yang paling lambat dari rangkaian predisposisi zat aktif sediaan
obat didalam tubuh merupakan tahap penentu.
Dengan demikian, penyerapan zat aktif akan bergantung pada : laju pelarutan
zat aktif dalam cairan biologik disekitar membran, karakter fisikokimia yang dapat
mempengaruhi proses penyerapan (pKa, koefisien partisi, stabilitas, dan lain-lain)
2.2.1 Membran sel
Membran sel merupakan bagian sel yang mengandung komponen-komponen
yang terorganisasi dan dapat berinteraksi dengan mikromolekul secara khas. Struktur
membran biologis sangat kompleks dan dapat mempengaruhi intensitas dan masa
kerja obat. Sesudah pemberian secara oral, obat harus melewati sel epitel saluran
cerna, membran sistem peredaran tertentu, melewati membran kapiler menuju sel-sel
organ atau reseptor obat.
Menurut Siswandono dan Soekarjo (2000) membran sel terdiri dari
komponen-komponen yang terorganisasi, yaitu:
1. Lapisan lemak bimolekul.
Tebal lapisan lemak bimolekul ± 35 Ǻ, mengandung kolesterol netral dan fosfolipid terionkan, yang terdiri dari fosfatidiletanolamin, fosfatidilkolin,
fosfatidilserin dan spingomielin. Berdasarkan sifat kepolarannya lapisan lemak
bimolekul dibagi menjadi dua bagian yaitu bagian non polar, terdiri dari rantai
hidrokarbon, dan bagian polar yang terdiri dari gugus hidroksil kolesterol dan gugus
gliserilfosfat fosfolipid.
2. Protein.
Bentuk protein bervariasi, ada yang besar, berat molekulnya ± 300.000 dan
ada pula yang sangat kecil. Protein bersifat ampivil karena mengandung gugus
hidrofil dan hidrofob.
3. Mukopolisakarida.
Jumlah mukopolisakarida pada membran biologis kecil dan strukturnya tidak
dalam keadaan bebas tetapi dalam bentuk kombinasi dengan lemak, seperti
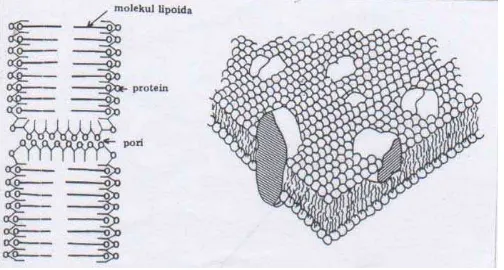
2.2.2 Struktur membran sel
Penelitian Dawson dan Danielli (1936-1943) serta Stein dan Danielli (1956),
mengemukakan suatu lembaran lipida protein sebagai model membran. Model
membran tersebut terdiri dari dua basal lipida monomolekular (yang terdiri dari
fosfolipida, tetapi juga kolesterol) yang kutub hidrofobnya menghadap ke bagian
dalam, dan kutub hidrofilnya merupakan basal protein berada di fasa berair. Dua
kutub hidrofil mengandung protein dan ujung fosfolipid yang polar (salah satu
diantaranya yang berada pada permukaan luar mempunyai lapisan protein globular)
mengelilingi daerah pusat hidrofob. Tetapi tampaknya susunan statis tersebut bukan
merupakan protein dan lipida dalam membran seluler yang hidup. Struktur membran
sel dapat dilihat pada Gambar 2.2.
Dalam konsep mosaik cair, matrik membran terdiri atas dua lapisan lipida
protein globular yang tidak berkesinambungan dan saling menyesuaikan menurut
susunan yang teratur atau tidak teratur. Gugusan polarnya terletak pada permukaan
membran yang kontak dengan cairan intra atau ekstraseluler, sedangkan gugus non
polar menghadap ke arah dalam. Pori-pori yang tampak pada sumbu utama protein
globuler tebalnya ± 85 Angstrom. Model ‘Mosaik Cair’ konsisten tentang eksistensi
dari chanel-chanel ion khusus dan reseptor-reseptor di dalam dan di sepanjang
permukaan membran (Syukri, 2002).
2.2.3 Cara penembusan obat melalui membran biologis
Pada umumnya obat menembus membran biologis secara difusi. Mekanisme
difusi dipengaruhi oleh struktur kimia, sifat fisika kimia obat dan sifat membran
biologis.
Cara penembusan obat ke dalam membran biologis dibagi atas:
1. Difusi pasif
Penembusan membran biologis secara difusi pasif dibedakan menjadi tiga,
yaitu difusi pasif melalui pori (cara penyaringan), difusi pasif dengan cara melarut
dalam lemak penyusun membran dan difusi pasif dengan fasilitas.
a. Difusi Pasif Melalui Pori
Penembusan air terjadi karena adanya perbedaan tekanan hidrostatik atau
osmotik; semua senyawa yang berukuran cukup kecil dan larut dalam air dapat
melewati kanal membrane. Sebagian besar membran (membran seluler, epitel usus
halus dan lain-lain) berukuran kecil (4-7oA) dan hanya dapat dilalui oleh molekul
dengan bobot molekul yang kecil yaitu lebih kecil dari 150 untuk senyawa yang
bulat, atau lebih kecil dari 400 jika molekulnya terdiri atas rantai panjang (Aiache, et
al., 1993). Untuk lebih jelasnya difusi pasif melalui pori dapat dilihat pada Gambar
2.3.
b. Difusi Pasif dengan Cara Melarut pada Lemak Penyusun Membran
Penembusan terjadi karena adanya perbedaan konsentrasi atau elektrokimia
tanpa memerlukan energi, sehingga mencapai keseimbangan di kedua sisi membran.
Bila molekul semakin larut lemak, maka koefisien partisinya semakin besar dan
difusi transmembran terjadi lebih mudah. Kebanyakan zat aktif merupakan basa atau
asam organik, maka dalam keadaan terlarut sebagian molekul berada dalam bentuk
terionkan dan sebagian dalam bentuk tak terionkan. Hanya fraksi zat aktif yang
terionkan dan larut dalam lemak yang dapat melalui membran dengan cara difusi
pasif.
Untuk obat yang zat aktifnya merupakan garam dari asam kuat atau basa kuat,
derajat ionisasi berperan pada hambatan difusi transmembran. Sebaliknya untuk
elektrolit lemah berupa garam yang berasal dari asam lemah atau basa lemah yang
sedikit terionisasi, maka difusi melintasi membran tergantung kelarutan bentuk tak
terionkan di dalam lemak, jumlah bentuk yang tak terionkan (satu-satunya yang
bergantung pada konsentrasi), serta derajat ionisasi molekul.
c. Difusi Pasif dengan Fasilitas
Beberapa bahan obat dapat melewati membran sel karena ada tekanan
osmosa, yang disebabkan adanya perbedaan kadar antar membran, pengangkutan ini
berlangsung dari daerah dengan kadar tinggi ke daerah dengan kadar yang lebih
rendah dan berhenti setelah mencapai kesetimbangan, gerakan ini tidak memiliki
energi dan terjadi secara spontan.
Diduga molekul obat membentuk kompleks dengan suatu molekul pembawa
dalam membran, yang bersifat mudah larut dalam lemak, sehingga dengan mudah
bergerak menembus membran. Pada sisi membran yang lain kompleks akan terurai
Pembawa dapat berupa enzim atau ion yang muatannya berlawanan dengan
muatan molekul obat. Penembusan obat ke dalam membran biologis dapat berjalan
dengan cepat bila ada katalisator enzim dan ukuran bentuk kompleks cukup kecil.
Penyerapan pasif terjadi hingga tercapainya keseimbangan dan proses akan berhenti
bila aliran darah tidak lagi mengangkut zat aktif dalam jumlah yang setara dengan
jumlah yang diserap (Aiache, et al., 1993).
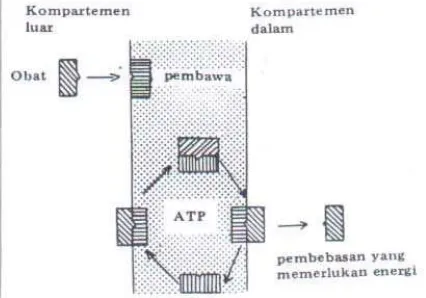
2. Transpor Aktif
Pada transpor aktif diperlukan adanya pembawa. Pembawa ini merupakan
suatu bagian dari membran, berupa enzim atau paling tidak senyawa protein dengan
molekul yang dapat membentuk kompleks pada permukaan membran. Kompleks
tersebut melintasi membran dan selanjutnya molekul dibebaskan pada permukaan
lainnya, lalu pembawa kembali menuju permukaan asalnya (transpor selalu terjadi
dalam arah tertentu, pada bagian usus perjalanan terjadi dari mukosa menuju serosa).
Sistem transpor aktif bersifat jenuh, artinya jika semua molekul pembawa telah
digunakan maka kapasitas maksimalnya tercapai. Sistem ini menunjukkan adanya
suatu kekhususan untuk setiap molekul atau suatu kelompok molekul. Oleh sebab itu
dapat terjadi persaingan beberapa molekul yang berafinitas sama pada pembawa
tertentu, dan molekul yang mempunyai afinitas tinggi dapat menghambat kompetisi
transpor dari molekul yang afinitasnya lebih rendah.
Transpor dari satu sisi membran ke sisi yang lain dapat terjadi dengan
mekanisme perbedaan konsentrasi. Transpor aktif ini memerlukan energi yang
diperoleh dari hidrolisa adenosintrifosfat (ATP) di bawah pengaruh suatu ATP-ase.
Gambar 2.4 Sistem pengangkutan aktif
3. Pinositosis
Pinositosis merupakan tipe khas pengangkutan aktif dari obat yang
mempunyai ukuran molekul besar dan misel-misel seperti lemak, amilum, gliserin,
vitamin A,D,E dan K. Pengangkutan ini digambarkan seperti sistem fagositosis pada
bakteri (Siswandono dan Soekarjo, 2000)). Mekanisme pinositosis dapat dilihat pada
Gambar 2.5.
Gambar 2.5 Sistem pengangkutan secara pinositosis
Kebanyakan dari obat melewati membran biologis dengan cara difusi pasif.
Senyawa obat yang berbobot molekul kecil dengan bebas melewati mikroporus dari
sel. Dengan catatan mungkin obat larut diluar fase membran plasma menembus
membran dan masuk ke dalam sitoplasma sel. Karena bersifat lipid membran sel
lipid. Obat asam lemah dan basa lemah mungkin berada dalam keadaan tak terion
pada harga pH dari fasa berair pada bagian eksternal dan internal membran. Selama
bentuk tak terion dari obat lebih mudah larut dalam lipid dari pada bentuk terion,
bentuk tak terion larut ke dalam membran dan seterusnya maka difusi akan lebih
cepat dari pada bentuk terion (Wolf, 1994)..
2.3 Usus Halus
Usus halus merupakan lanjutan lambung yang terdiri atas tiga bagian yaitu;
duodenum, jejunum dan illeum yang bebas bergerak. Diameter usus halus beragam
tergantung pada letaknya yaitu 2 – 3 cm dan panjang keseluruhan antara 5 - 9 m.
Panjang tersebut akan berkurang oleh gerakan regangan otot yang melingkari
peritonium (Aiache, et al., 1993). Duodenum dengan panjang sekitar 25 cm, terikat
erat pada dinding dorsal abdomen, dan sebagian besar terletak retroperitoneal.
Jalannya berbentuk –C, mengitari kepala pankreas dan ujung distalnya menyatu
dengan jejenum, yang terikat pada dinding dorsal rongga melalui mesenterium.
Jejenum dapat digerakkan bebas pada mesenteriumnya dan merupakan 2/5 bagian
proksimal usus halus, sedangkan ileum merupakan sisa 3/5 nya. Kelokan-kelokan
jejenum menempati bagian pusat abdomen, sedangkan ileum menempati bagian
bawah rongga (Fawcett, 2002). Mukosa usus halus, kecuali yang terletak pada bagian
atas duodenum berbentuk lipatan-lipatan atau disebut juga valvula conniventes.
Lipatan-lipatan inilah yang berfungsi sebagai permukaan penyerapan dan penuh
dengan villi yang tingginya 0,75 – 1,00 mm dan selalu bergerak. Adanya villi ini
lebih memperluas permukaan mukosa penyerapan hingga 40 – 50 m (Aiache, et al,
Bahan obat dari lambung masuk ke duodenum, fungsi utama duodenum dan
bagian pertama jejenum adalah untuk sekresi, sedangkan fungsi bagian kedua dari
jejenum dan illeum ialah untuk absorpsi. pH usus halus meningkat dari duodenum 4-
6, jejenum 6-7, illeum 7-8. pH dalam usus halus berperan besar dalam hal absorpsi
obat sebagai akibat disolusi berbagai bentuk sediaan (Aiache, et al., 1993).
Karakteristik anatomi dan fisiologi usus (dengan makrovilli dan
mikrovillinya) lebih menguntungkan untuk penyerapan obat, seperti halnya juga
penyerapan zat makanan.
Pentingnya permukaan penyerapan terutama karena banyaknya lipatan-lipatan
mukosa usus yang berupa valvula conniventes atau lipatan kerckring, yang terutama
banyak terdapat di daerah duodenum dan jejunum. Di daerah tersebut villi-villi usus
tertutup oleh epitel bagaikan sikat yang terdiri dari bulu-bulu halus (mikrovilli) dan
mempunyai aktivitas yang kuat. Adanya anyaman kapiler darah dan getah bening
pada setiap lipatan memungkinkan terjadinya penyerapan yang besar. Gerakan usus
dan gerakan villi usus di sepanjang saluran cerna akan mendorong terjadinya
penembusan menuju pembuluh darah. Keadaan pH serta tebal dinding yang beragam
di setiap bagian usus menyebabkan perbedaan penembusan yang cukup besar pada
molekul zat aktif terutama molekul asam yang penyerapannya dipengaruhi oleh pH
lambung.
Bagian lain dari usus halus juga merupakan tempat terjadinya pelintasan
membran dengan intensitas yang besar, dan disini lebih banyak terjadi difusi pasif.
Difusi pasif berkaitan dengan sejumlah senyawa yang larut lemak atau
fraksi-fraski tak terionkan yang larut lemak.
Difusi pasif terutama terjadi pada bagian pertama usus halus, karena
hal yang sama terjadi pula pada bagian usus sebelah bawah dan pada penyerapan
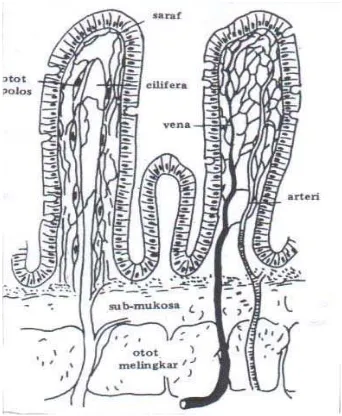
susjacent. Skema usus halus dengan villi dan perfusinya dapat dilihat pada Gambar
2.6.
Transpor aktif juga berperan di usus halus dan di sini terjadi persaingan
terhadap pembawa yang sama atau terjadi penjenuhan sistem transpor yang dapat
membatasi pelintasan membran. Pinositosis juga berperan terutama di ileum terhadap
molekul-molekul yang tidak larut (Aiache, et al., 1993).
Gambar 2.6 Skema usus halus dengan villi dan perfusinya
2.4 Metode Kantung Terbalik (Everted Sac)
Preformulasi melibatkan sejumlah pemeriksaan untuk menghasilkan informasi
yang bermanfaat untuk tahap formulasi selanjutnya meliputi kestabilan fisikokimia
dan kecocokan dosis obat secara biofarmasi.
Penelitian awal biofarmasi dari senyawa obat juga dilakukan selama
preformulasi. Uji-uji ini didesain untuk menelusuri karakteristik ketersediaan
senyawa obat secara in vitro. Hasil penelitian ini mengkontribusikan suatu produk
Suatu teknik dengan menggunakan everted intestinal sac dapat digunakan
dalam mengevaluasi karakteristik absorpsi dari zat obat (Ansel,1989).
Pada persiapannya, teknik everted sac menggunakan bagian dari intestin,
disayat dari bagian omentum dan sirkulasi mesenterikum. Intestin ini dibalik
sehingga permukaannya berada pada bagian luar dan ujung dari bagian ini diikat,
larutan buffer dimasukkan melalui kateter pada bagian lainnya, dan bagian luar usus
direndam dalam larutan berisis obat dengan suhu 37oC, dialiri oksigen 95% dan CO2
50%. Kedua bagian, baik serosa maupun mukosa dapat dijadikan sampel untuk
analisis.
Everted sac merupakan teknik yang sederhana yang menghadirkan kerumitan
yang lebih sedikit bila dibandingkan dengan pengujian konsentrasi obat secara in
vivo.
Kondisi dari temperatur, oksigen, ketersediaan makanan sebagai sumber
energi dapat diatur dalam metode ini, namun tidak ada lagi sirkulasi mesenterikum
dan kehadiran obat secara total pada bagian dalam kantung pada difusi melalui serosa
(Swarbrick and Boylan, 1992).
2.5 Kinetika Laju Absorpsi
a. Reaksi orde nol
Laju peruraian obat secara matematis dapat digambarkan sebagai berikut :
Laju pengurangan konsentrasi
=
−��� ��=k
Dimana; Ca = Konsentrasi zat A yang bereaksi
k = faktor perbandingan = laju reaksi
Bila data dari suatu studi stabilitas mengikuti reaksi orde nol, grafik x (jumlah
yang bereaksi) versus t (waktu) merupakan garis lurus dengan kelandaian menyamai
k. Nilai k menyatakan jumlah obat yang terurai per satuan waktu, dan titik potong
garis pada waktu nol sama dengan konstanta.
b. Reaksi ode pertama
Laju pengurangan konsentrasi = - ���
��
=kCa
Dengan memakai persamaan tersebut untuk reaksi orde pertama dihasilkan
garis lurus bila dibuat grafik logaritma konsentrasi Ca terhadap waktu. Kecepatan
atau konstanta laju reaksi, k, dapat dihitung dari kelandaian garis dikalikan 2,303
(Armstrong, 1995).
2.6 Pengeringan Beku (Freeze Dryer)
Pengeringan beku (freeze drying) adalah salah satu metode pengeringan yang
mempunyai keunggulan dalam mempertahankan mutu hasil pengeringan, khususnya
untuk produk-produk yang sensitif terhadap panas. Keunggulan pengeringan beku
dibandingkan metode lainnya yaitu dapat mempertahankan stabilitas produk, dapat
mempertahankan stabilitas struktur bahan dan dapat meningkatkan daya rehidrasi
sehingga dapat kembali ke sifat fisiologis, organoleptik dan betuk fisik yang hampir
sama dengan sebelum pengeringan (Tambunan dan Manalu, 2000).
Untuk proses pengeringan beku, bahan yang dikeringkan terlebih dahulu
dibekukan kemudian dilanjutkan dengan pengeringan menggunakan tekanan rendah
sehingga kandungan air yang sudah menjadi es akan langsung menjadi uap, dikenal
dengan istilah sublimasi. Pengeringan menggunakan alat freeze dryer lebih baik
dibandingkan dibandingkan dengan oven karena kadar airnya lebih rendah dan dapat
2.7 Spektrofotometri Ultraviolet - visibel
Radiasi elektromagnetik, yang mana sinar ultraviolet dan sinar tampak
merupakan salah satunya, dapat dianggap sebagai energi yang merambat dalam
bentuk gelombang. Beberapa istilah dan hubungan digunakan untuk menggambarkan
gelombang ini. Panjang gelombang merupakan jarak linier dari suatu titik pada satu
gelombang ke titik yang bersebelahan pada gelombang yang berdekatan. Sinar
ultraviolet mempunyai panjang gelombang antara 200 - 400 nm, sementara sinar
tampak mempunyai panjang gelombang 400 – 750 nm (Gandjar dan Rohman, 2009).
Sinar ultraviolet dan sinar tampak memberikan energi yang cukup untuk
terjadinya transisi elektronik. Dengan demikian, spektra ultraviolet dan spektra
tampak dikatakan sebagai spektra elektronik. Keadaan energi yang paling rendah
disebut dengan keadaan dasar (ground state). Transisi – transisi elektronik akan
meningkatkan energi molekuler dari keadaan dasar ke satu atau lebih tingkat energi
tereksitasi (Gandjar dan Rohman, 2009).
Jika suatu molekul sederhana dikenakan radiasi elektromagnetik maka
molekul tersebut akan menyerap radiasi elektromagnetik yang energinya sesuai.
Interaksi antara molekul dengan radiasi elektromagnetik ini akan meningkatkan
energi potensial elektron pada tingkat keadaan tereksitasi. Apabila pada molekul yang
sederhana tadi hanya terjadi transisi elektronik pada satu macam gugus yang terdapat
pada molekul, maka hanya akan terjadi satu absorbsi. Pada kenyataannya, spektrum
UV – Vis yang merupakan korelasi antara absorbansi (sebagai ordinat) dan panjang
gelombang (sebagai absis) bukan merupakan garis spektrum akan tetapi merupakan
pita spektrum. Terbentuknya pita spektrum UV – Vis tersebut disebabkan oleh
terjadinya eksitasi elektronik lebih dari satu macam pada gugus molekul yang sangat
Spektra UV – Vis dapat digunakan untuk informasi kualitatif dan sekaligus
dapat digunakan untuk analisis kuantitatif.
a. Aspek Kualitatif
Data spektra UV – Vis secara tersendiri tidak dapat digunakan untuk
identifikasi kualitatif obat atau metabolitnya. Akan tetapi jika digabung dengan cara
lain seperti spektroskopi infra merah, resonansi magnet inti, dan spektroskopi massa,
maka dapat digunakan untuk maksud identifikasi/ analisis kualitatif suatu senyawa
tersebut. Data yang diperoleh dari spektroskopi UV dan Vis adalah panjang
gelombang maksimal, intensitas, efek pH, dan pelarut; yang kesemuanya itu dapat
diperbandingkan dengan data yang sudah dipublikasikan (Gandjar dan Rohman,
2009).
b. Aspek Kuantitatif
Dalam aspek kuantitatif, suatu berkas radiasi dikenakan pada cuplikan
(larutan sampel) dan intensitas sinar radiasi yang diteruskan diukur besarnya. Radiasi
yang diserap oleh cuplikan ditentukan dengan membandingkan intensitas sinar yang
diteruskan dengan intensitas sinar yang diserap jika tidak ada spesies penyerap
lainnya. Intensitas atau kekuatan radiasi cahaya sebanding dengan jumlah foton yang
melalui satu satuan luas penampang perdetik. Serapan dapat terjadi jika foton/radiasi
yang mengenai cuplikan memiliki energi yang sama dengan energi yang dibutuhkan
untuk menyebabkan terjadinya perubahan tenaga. Kekuatan radiasi juga mengalami
penurunan dengan adanya penghamburan dan pemantulan cahaya, akan tetapi
penurunan karena hal ini sangat kecil dibandingkan dengan proses penyerapan.
Hukum Lambert – Beer menyatakan bahwa intensitas yang diteruskan oleh larutan
zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan (Gandjar dan
BAB III
METODE PENELITIAN
Metode yang digunakan dalam penelitian ini adalah penelitian eksperimental
(experimental research). Penelitian dimaksudkan untuk mengetahui pengaruh atau
hubungan antara variabel bebas dengan variabel terikat. Dalam penelitian ini yang
termasuk variabel bebas adalah: ibuprofen, usus halus kelinci yang dikeringkan dan
usus halus kelinci segar. Sedangkan variabel terikat adalah laju absorpsi.
3.1 Rancangan Penelitian
Penelitian ini dilakukan dengan pembuatan usus halus kelinci yang
dikeringkan dan usus halus kelinci yang segar. Setelah itu dilakukan pengecatan
membran usus halus kelinci yang dikeringkan dan usus halus kelinci yang segar.
Kemudian dilanjutkan dengan pemeriksaan laju absorpsi pada usus halus kelinci yang
dikeringkan dan usus halus kelinci yang segar serta dilakukan pengecatan membran
untuk usus halus kelinci segar dan yang dikeringkan pada waktu pengujian.
Hewan terbagi dalam tiga kelompok dan tiap kelompok terdiri dari tiga
pengulangan dengan uraian sebagai berikut:
1. Kelompok pertama diberi ibuprofen baku yang dilarutkan dalam larutan buffer
fosfat pH 6,4 isotonis dengan konsentrasi 2 mmol/L.
2. Kelompok kedua diberi ibuprofen tablet Generik yang dilarutkan dalam buffer
fosfat pH 6,4 dengan konsentrasi 2 mmol/L.
3. Kelompok ketiga diberi ibuprofen tablet merk dagang (Proris®) yang dilarutkan
3.2 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Biofarmasetika dan Farmakokinetika
dan Laboratorium Farmakologi dan Toksikologi, Fakultas Farmasi, Universitas
Sumatera Utara, Medan, Provinsi Sumatera Utara, Indonesia.
3.3 Alat dan Bahan
3.3.1 Alat
Alat-alat yang digunakan adalah alat freeze dryer (Virtis), alat uji absorpsi
(alat Crane dan Wilson yang telah dimodifikasi), beaker gelas, gelas ukur, kotak
kelinci, labu ukur, neraca analitik (Metler Toledo), pH meter (Hanna), pipet volume,
spektrofotometer UV-visibel (Shimadzu UV-Mini 1240), stopwatch, tabung oksigen
dan regulator, tabung reaksi, termometer, termostat, satu set alat bedah, vial dan alat
lain yang dibutuhkan.
3.3.2 Bahan
Bahan-bahan yang digunakan adalah akuades, carbogen, d-glukosa
monohidrat (E.Merck), ibuprofen baku, ibuprofen tablet Generik (Kimia Farma),
kalium dihidrogenfosfat (E.Merck), kalium klorida (E.Merck), kalsium klorida
(E.Merck), magnesium klorida (E.Merck), natrium bikarbonat (E.Merck), natrium
dihidrogenfosfat (E.Merck), natrium klorida (E.Merck), dan ibuprofen tablet merk
dagang (Proris(R)) (Pharos).
3.4 Hewan Percobaan
3.5 Prosedur Kerja
3.5.1 Pembuatan pereaksi
3.5.1.1 Pembuatan air bebas karbondioksida
Air murni dididihkan selama 5 menit atau lebih dan didiamkan sampai dingin
dan tidak boleh menyerap karbondioksida dari udara (Ditjen POM, 1995).
3.5.1.2 Pembuatan kalium dihidrogenfosfat 0,2 M
Dilarutkan 27,218 g kalium dihidrogenfosfat P dalam air bebas
karbondioksida P hingga 1000 ml (Ditjen POM, 1979).
3.5.1.3 Pembuatan larutan natrium hidroksida 0,2 N
Dilarutkan 8,001 natrium hidroksida P dalam air hingga 1000 ml (Ditjen
POM, 1979).
3.5.1.4 Pembuatan dapar fosfat pH 6,4 isotonis
Dicampur 50,0 ml kalium dihidrogenfosfat 0,2 M dengan 11,6 ml natrium
hidroksida 0,2 N dan diencerkan dengan air bebas karbondioksida P secukupnya
hingga 200 ml (Ditjen POM, 1979).
3.5.1.5 Pembuatan larutan thyrode
Dilarutkan 8,0 g natrium klorida; 0,2 g kalium klorida; 0,2 g kalsium klorida;
0,1 g magnesium klorida; 0,05 g natrium dihidrogenfosfat; 1,0 g natrium bikarbonat;
dan 2,0 g d-glukosa monohidrat dalam 1000 ml akuades (Anonim1, 2009).
3.5.2 Pembuatan kurva serapan ibuprofen dalam medium dapar fosfat pH 6,4 isotonis
Ditimbang seksama 50 mg ibuprofen dan dimasukkan ke dalam labu tentukur
250 ml kemudian ditambahkan dapar fosfat pH 6,4 isotonis sampai garis tanda. Di
pipet 0,45 ml kemudian dimasukkan ke dalam labu tentukur 10 ml, lalu ditambahkan
menggunakan spektrofotometer UV. Panjang gelombang yang dipilih adalah panjang
gelombang dimana ibuprofen memperlihatkan serapan paling tinggi.
3.5.3 Pembuatan kurva kalibrasi ibuprofen dalam medium dapar fosfat pH 6,4 isotonis
Ditimbang seksama 50 mg ibuprofen dan dimasukkan ke dalam labu tentukur
250 ml kemudian ditambahkan larutan dapar fosfat pH 6,4 isotonis sampai garis
tanda. Dari larutan tersebut di pipet 0,075 ml; 0,2 ml; 0,325 ml; 0,45 ml; 0,575 ml;
0,7 ml; 0,825 ml. Dimasukkan ke dalam labu tentukur 10 ml, kemudian
masing-masing diencerkan dengan larutan dapar fosfat pH 6,4 isotonis sampai garis tanda.
Serapan diukur pada panjang gelombang maksimum yang diperoleh dari kurva
serapan ibuprofen menggunakan spektrofotometer UV dan sebagai blanko digunakan
dapar fosfat pH 6,4 isotonis. Kurva kalibrasi antara jumlah serapan dan konsentrasi
dibuat dari data yang diperoleh, lalu dihitung persamaan regresi dan koefisien
korelasinya.
3.5.4 Pembuatan larutan obat ibuprofen baku dengan konsentrasi 2 mmol/L
Ditimbang seksama 20,628 mg ibuprofen baku, dimasukkan ke dalam labu
tentukur 50 ml. Dilarutkan dengan dapar fosfat pH 6,4 isotonis, dicukupkan sampai
garis tanda sehingga diperoleh konsentrasi 2 mmol/L.
3.5.5 Pembuatan larutan obat ibuprofen tablet generik dengan konsentrasi 2 mmol/L.
Ditimbang seksama 27,6054 mg ibuprofen generik yang telah diserbukkan,
dimasukkan ke dalam labu tentukur 50 ml. Dilarutkan dengan dapar fosfat pH 6,4
isotonis, dicukupkan sampai garis tanda sehingga diperoleh konsentrasi 2 mmol/L.
3.5.6 Pembuatan larutan obat ibuprofen tablet merk dagang (Proris®) dengan konsentrasi 2 mmol/L.
Ditimbang seksama 29,044 mg Proris® yang telah diserbukkan, dimasukkan
ke dalam labu tentukur 50 ml. Dilarutkan dengan dapar fosfat pH 6,4 isotonis,
3.5.7 Pembuatan usus halus kelinci
3.5.7.1 Pembuatan usus halus kelinci segar
Hewan percobaan berupa kelinci jantan dipuasakan selama 20-24 jam. Setelah
itu kelinci tersebut dianestesi, kemudian dilakukan pembedahan pada bagian perut
tetapi jangan sampai mengenai tulang dada. Setelah usus halus dikeluarkan dan
dibersihkan bagian dalamnya dari kotoran dan bagian luar dari jaringan yang
mengikat pembuluh darah halus, dan sebagainya dengan bantuan pinset dan gunting,
dan dicuci dengan larutan thyrode dingin. Lalu diangkat dan dibalik dengan
menggunakan batang pengaduk berpenampang 2 mm. Lalu diikat pada bagian ujung
dengan benang dan dilepaskan dari batang pengaduk, dicelupkan ke dalam larutan
Thyrode dingin.
3.5.7.2 Pembuatan usus halus kelinci yang dikeringkan
Hewan percobaan berupa kelinci jantan dipuasakan selama 20-24 jam. Setelah
itu kelinci tersebut dianestesi, kemudian dilakukan pembedahan pada bagian perut
tetapi jangan sampai mengenai tulang dada. Setelah usus halus dikeluarkan dan
dibersihkan bagian dalamnya dari kotoran dan bagian luar dari jaringan yang
mengikat pembuluh darah halus, dan sebagainya dengan bantuan pinset dan gunting,
dan dicuci dengan larutan thyrode dingin. Lalu diangkat dan dibalik dengan
menggunakan batang pengaduk berpenampang 2 mm. Lalu diikat pada bagian ujung
dengan benang dan dilepaskan dari batang pengaduk, dicelupkan ke dalam larutan
Thyrode dingin. Kemudian dikeringkan dengan menggunakan freeze dryer pada suhu
3.5.8 Pengecatan membran
3.5.8.1 Pengecatan membran usus halus kelinci segar
Pengecatan membran usus halus kelinci segar dilakukan dengan teknik
pengecatan menggunakan hematoksilin-eosin.
3.5.8.2 Pengecatan membran usus halus kelinci yang dikeringkan
Pengecatan membran usus halus kelinci yang dikeringkan dilakukan dengan
teknik pengecatan menggunakan hematoksilin-eosin.
3.5.9 Penentuan absorpsi ibuprofen
3.5.9.1 Penentuan absorpsi ibuprofen dalam usus halus kelinci segar dalam larutan dapar fosfat pH 6,4 isotonis
Usus halus terbalik kelinci dengan panjang efektif masing-masing 7 cm diikat
pada kanula dan masing-masing diisi dengan cairan serosa 3 ml ke dalamnya berupa
larutan dapar fosfat pH 6,4 isotonis yang tidak mengandung bahan obat. Usus Halus
terbalik bagian atas yang digunakan sebagai kontrol, dimasukkan ke dalam tabung
berisi 75 ml cairan mukosa berupa larutan buffer posfat pH 6,4 isotonis yang tidak
mengandung bahan obat. Sedangkan untuk usus halus terbalik bagian bawah yang
digunakan sebagai percobaan, dimasukkan ke dalam tabung berisi 75 ml cairan
mukosa berupa larutan buffer posfat pH 6,4 isotonis yang mengandung bahan obat
ibuprofen baku dengan konsentrasi 2 mmol. Selanjutnya dimasukkan tabung ke
dalam termostat dengan temperatur 37 ± 0,5°C. Selama berlangsung percobaan dijaga
agar seluruh bagian usus tetap terendam dalam cairan mukosa serta terus menerus
dialiri aliran oksigen dengan kecepatan kira-kira 1 gelembung per detik.
Pada menit 5, 10, 15, 30, 60, 90, 120, 150 cairan serosa diambil 1 ml melalui
kanula dan selanjutnya diencerkan dengan larutan buffer fosfat pH 6,4 isotonis
serosa. Serapan larutan yang diperiksa, diukur pada panjang gelombang maksimum
yaitu 222,5 nm dengan spektrofotometer ultraviolet. Dilakukan cara yang sama
dengan cara diatas untuk larutan obat ibuprofen tablet Generik dan ibuprofen tablet
merk dagang Proris®.
3.5.9.2 Penentuan absorpsi ibuprofen dalam usus halus kelinci yang dikeringkan dalam larutan dapar fosfat pH 6,4 isotonis
Usus halus terbalik kelinci yang telah dikeringkan dengan panjang efektif
masing-masing 7 cm diikat pada kanula dan masing-masing diisi dengan cairan
serosa 3 ml ke dalamnya berupa larutan dapar fosfat pH 6,4 isotonis yang tidak
mengandung bahan obat. Usus Halus terbalik bagian atas yang digunakan sebagai
kontrol, dimasukkan ke dalam tabung berisi 75 ml cairan mukosa berupa larutan
buffer posfat pH 6,4 isotonis yang tidak mengandung bahan obat. Sedangkan untuk
usus halus terbalik bagian bawah yang digunakan sebagai percobaan, dimasukkan ke
dalam tabung berisi 75 ml cairan mukosa berupa larutan buffer posfat pH 6,4 isotonis
yang mengandung bahan obat ibuprofen baku dengan konsentrasi 2 mmol.
Selanjutnya dimasukkan tabung ke dalam termostat dengan temperatur 37 ± 0,5oC.
Selama berlangsung percobaan dijaga agar seluruh bagian usus tetap terendam dalam
cairan mukosa serta terus menerus dialiri aliran oksigen dengan kecepatan kira-kira 1
gelembung per detik.
Pada menit 5, 10, 15, 30, 60, 90, 120, 150 cairan serosa diambil 1 ml melalui
kanula dan selanjutnya diencerkan dengan larutan buffer fosfat pH 6,4 isotonis
hingga 25 ml. Dimasukkan kembali sebanyak 1 ml untuk setiap pengambilan cairan
serosa. Serapan larutan yang diperiksa, diukur pada panjang gelombang maksimum
dengan cara diatas untuk larutan obat ibuprofen tablet Generik dan ibuprofen tablet
merk dagang Proris®.
3.6 Analisis Data
Data hasil penelitian dianalisis dengan menggunakan program SPSS 15. Data
hasil penelitian di tentukan homogenitas dan normalitasnya untuk menentukan
analisis statistik yang digunakan. Hasil analisis dapat dilihat pada lampiran 16 pada
BAB IV
HASIL DAN PEMBAHASAN
4.1 Penentuan Panjang Gelombang Maksimum Ibuprofen dalam Larutan Dapar Fosfat pH 6,4 Isotonis
Untuk mengetahui panjang gelombang maksimum ibuprofen dalam larutan
dapar fosfat pH 6,4 isotonis maka dilakukan pengukuran pada larutan induk baku
ibuprofen (9 mcg/ml) dengan menggunakan alat spektrofotometer ultraviolet. Dari
pengukuran diperoleh panjang gelombang ibuprofen dalam larutan dapar fosfat pH
6,4 isotonis adalah 222,5 nm. Panjang gelombang yang diperoleh mendekati dengan
panjang gelombang ibuprofen yang tertera pada U. S. P 29 yaitu 221 nm. Hasil
pengukuran dapat dilihat pada Lampiran 4 halaman 46.
4.2 Pembuatan Kurva Kalibrasi dan Penentuan Persamaan Regresi Ibuprofen Baku dalam Larutan Dapar Fosfat pH 6,4 Isotonis
Untuk menentukan kurva kalibrasi dari ibuprofen baku dalam larutan dapar
fosfat pH 6,4 isotonis dilakukan pengukuran absorbansi dari larutan induk ibuprofen
pada konsentrasi 1,5; 4; 6,5; 9; 11,5; 14; dan 16,5 mcg/ml sehingga diperoleh
absorbansi dari masing-masing konsentrasi dan persamaan regresi y = 0,0468x –
0,00755.
4.3 Pengecatan Membran Usus Halus Kelinci
Untuk mengetahui pengaruh freeze dryer pada usus halus kelinci, maka
dilakukan pengecatan membran hematoksilin-eosin pada usus halus kelinci segar dan
tersebut, maka diperoleh hasil berupa gambar membran usus yang terdapat pada
Gambar 4.1.a s/d 4.1.l sebagai berikut :
Gambar 4.1.a. Usus halus kelinci segar sebelum digunakan dengan perbesaran 4x10
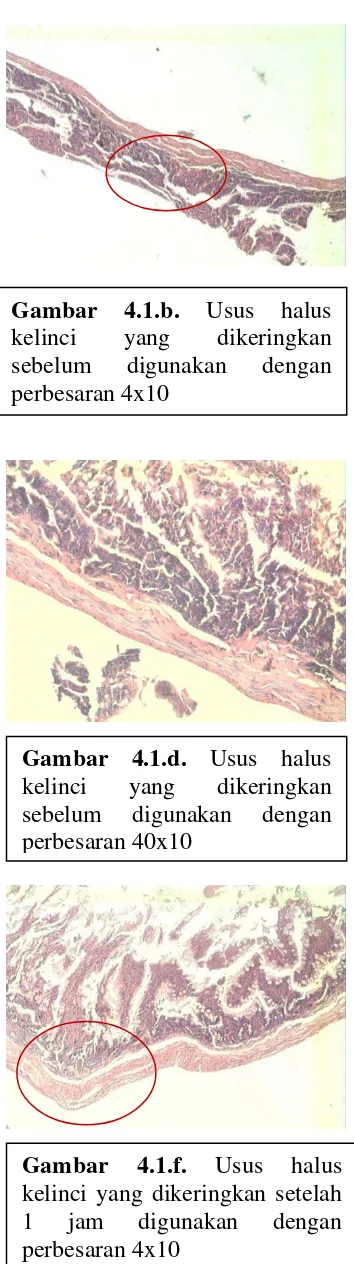
Gambar 4.1.b. Usus halus
kelinci yang dikeringkan
sebelum digunakan dengan
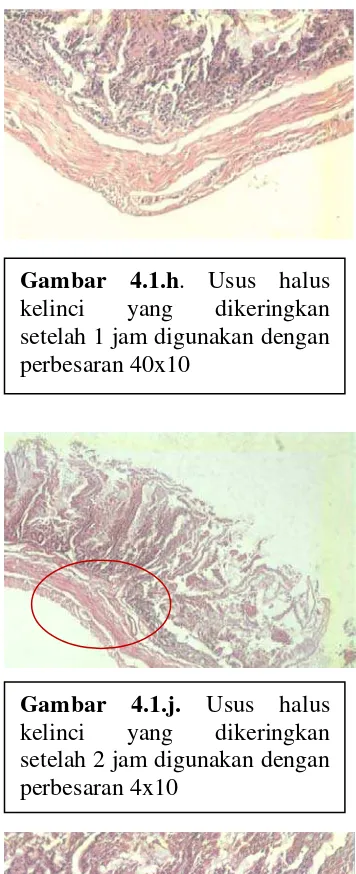
Gambar 4.1.f. Usus halus kelinci yang dikeringkan setelah
1 jam digunakan dengan
perbesaran 4x10 Gambar 4.1.c. Usus halus
kelinci segar sebelum digunakan dengan perbesaran 40x10
Keterangan : merupakan area gambar yang dilihat dengan perbesaran 40x10.
Gambar 4.1. Pengecatan membran hematoksilin-eosin usus halus kelinci segar dan usus halus kelinci yang dikeringkan
Gambar 4.1.i. Usus halus kelinci segar setelah 2 jam digunakan dengan perbesaran 4x10
Gambar 4.1.j. Usus halus kelinci yang dikeringkan setelah 2 jam digunakan dengan perbesaran 4x10 kelinci yang dikeringkan setelah
2 jam digunakan dengan
Dari hasil pengecatan membran hematoksilin-eosin pada usus halus kelinci
segar dan usus halus kelinci yang dikeringkan, dapat dilihat bahwa terdapat
perbedaan pada kedua usus halus kelinci tersebut. Perbedaan tersebut berupa semakin
besarnya pori-pori pada membran usus halus kelinci yang dikeringkan dibandingkan
dengan pori-pori pada usus halus kelinci yang segar. Hal ini menunjukkan bahwa
freeze dryer berpengaruh pada struktur membran usus halus kelinci tersebut.
4.4 Pengaruh Perbedaan Jenis Usus dan Jenis Sediaan Ibuprofen Terhadap Konsentrasi Kumulatif Ibuprofen yang Terabsorpsi pada Usus Halus Terbalik Kelinci
Untuk mengetahui pengaruh perbedaan jenis usus dan jenis sediaan ibuprofen
terhadap konsentrasi kumulatif ibuprofen, dilakukan pengujian dalam larutan dapar
fosfat pH 6,4 isotonis pada temperatur 37 ± 0,5ºC dengan hasil seperti yang terlihat
pada Tabel 4.1 dan Tabel 4.2.
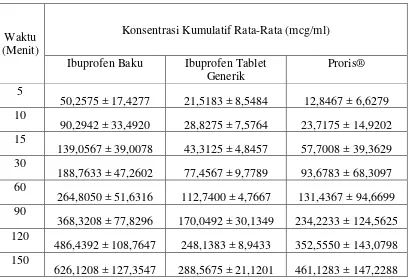
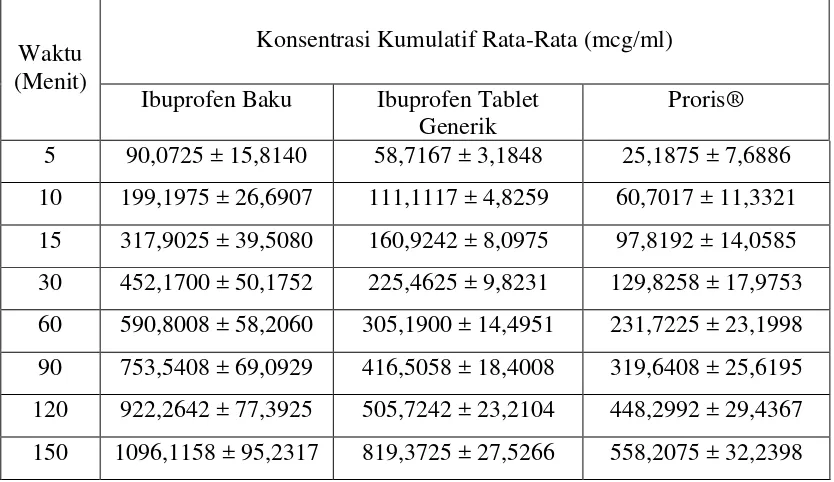
Tabel 4.1. Data konsentrasi kumulatif ibuprofen pada interval waktu tertentu dalam mcg/ml pada usus halus kelinci segar
Waktu (Menit)
Konsentrasi Kumulatif Rata-Rata (mcg/ml)
Ibuprofen Baku Ibuprofen Tablet Generik
139,0567 ± 39,0078 43,3125 ± 4,8457 57,7008 ± 39,3629 30
188,7633 ± 47,2602 77,4567 ± 9,7789 93,6783 ± 68,3097 60
264,8050 ± 51,6316 112,7400 ± 4,7667 131,4367 ± 94,6699 90
368,3208 ± 77,8296 170,0492 ± 30,1349 234,2233 ± 124,5625 120
486,4392 ± 108,7647 248,1383 ± 8,9433 352,5550 ± 143,0798 150