SEBARAN TERITIP INTERTIDAL DAN HUBUNGANNYA
DENGAN KONDISI LINGKUNGAN PERAIRAN
DI PELABUHAN KOTA DUMAI
AL MUDZNI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Sebaran Teritip Intertidal dan Hubungannya dengan Kondisi Lingkungan Perairan di Pelabuhan Kota Dumai adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Oktober 2014
Al Mudzni
RINGKASAN
AL MUDZNI. Sebaran Teritip Intertidal dan Hubungannya dengan Kondisi Lingkungan Perairan di Pelabuhan Kota Dumai. Dibimbing oleh DIETRIECH GEOFFREY BENGEN dan ISDRADJAD SETYOBUDIANDI.
Teritip Baran merupakan biota yang hidupnya menempel secara permanen pada substrat seperti tiang penyangga dermaga. Secara alami teritip banyak dijumpai pada perairan pesisir Kota Dumai. Penempelan teritip pada substrat diketahui dapat merusak dan memperpendek umur suatu bangunan. Tujuan penelitian ini untuk mengetahui sebaran kepadatan teritip intertidal pada jenis dan warna media penempelan yang berbeda. Selain itu, juga untuk mengetahui sebaran kepadatan teritip intertidal secara vertikal dan horizontal di perairan pelabuhan Kota Dumai, Provinsi Riau.
Penelitian dilaksanakan pada bulan September sampai November 2013 di Pelabuhan Pelindo I, Pelabuhan Pendaratan Ikan (PPI) Purnama dan Pelabuhan Angkatan Laut Kota Dumai. Data parameter biofisika kimiawi diukur di Laboratorium Ekologi dan Manajemen Lingkungan Perairan Universitas Riau. Contoh teritip diidentifikasi di Laboratorium Biologi Laut Institut Pertanian Bogor.
Hasil penelitian menunjukkan bahwasannya teritip jenis Amphibalanus spp.
memiliki kepadatan yang tidak merata pada jenis dan warna media penempelan yang berbeda. Tingkat kepadatan teritip ditemukan tertinggi pada media kayu yang tidak diberi warna dengan kisaran 265-506 ind/m2 dan terendah pada media
fiber putih dengan kisaran 25-68 ind/m2. Kedua stasiun Pelabuhan Pelindo I dan
stasiun 2 PPI Purnama merupakan stasiun yang memiliki tingkat kepadatan teritip tertinggi. Stasiun tersebut dicirikan dengan pH (7-8), salinitas (27-28 ‰), kekeruhan (2 NTU) yang tinggi dibandingkan stasiun lainnya. Sedangkan kedua stasiun Pelabuhan Angkatan Laut Bangsal Aceh merupakan stasiun yang memiliki tingkat kepadatan teritip terendah. Stasiun tersebut dicirikan dengan kecepatan arus (0,3-0,5 m/dtk) yang tinggi dibandingkan stasiun lainnya.
Kata kunci: Amphibalanus spp., sebaran, tiang pelabuhan, kondisi lingkungan,
SUMMARY
AL MUDZNI. Distribution of Barnacle (Amphibalanus spp.) And Its Relation to
Marine Environment Conditions in The Port of Dumai. Supervised by DIETRIECH GEOFFREY BENGEN and ISDRADJAD SETYOBUDIANDI.
Acorn barnacle lives permanently to attached a substrate such as a pillar of port. Naturally, barnacles were found in coastal waters of Dumai. Attachment of barnacles on the pillar of the port known to damage and shorten the life of a building. This study aim was to determine the distribution and density of the intertidal barnacle on the different type and colors of media attachment. Its were also to determine vertically and horizontally distribution of the intertidal barnacles density in the port of Dumai, Riau Province.
Survey was conducted in September to November 2013 at Port of Pelindo I, PPI Purnama and LANAL Port in Dumai. Data of biophysical chemistry parameters were measured at the Laboratory of Ecology and Aquatic Environmental Management, University of Riau. Barnacles were identified at the Marine Biological Laboratory, Bogor Agricultural University.
The results showed the inequality of Amphibalanus spp. density on the
different types and colors of media attachment. The highest density of barnacles were found in colorless timber (265-506 ind/m2) and in white fiber were a lowest
density (25-68 ind/m2). Both stations of Pelindo I port and station 2 of PPI
Purnama have the highest density of barnacles. These stations were characterized by the highest pH (7-8), salinity (27-28 ‰), turbidity (2 NTU) compared to the other stations. While both stations of LANAL Port have the lowest density of barnacles. These stations were characterized by highest current speed (0.3-0.5 m/s) compared to the other stations.
Keywords: Amphibalanus spp., distribution, the pole of port, marine
© Hak Cipta Milik IPB, Tahun 2014
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Ilmu Kelautan
SEBARAN TERITIP INTERTIDAL DAN HUBUNGANNYA
DENGAN KONDISI LINGKUNGAN PERAIRAN
DI PELABUHAN KOTA DUMAI
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2014
Judul Tesis : Sebaran Teritip Intertidal Dan Hubungannya Dengan Kondisi Lingkungan Perairan Di Pelabuhan Kota Dumai
Nama : Al Mudzni NIM : C551110061
Disetujui oleh Komisi Pembimbing
Prof Dr Ir Dietriech G. Bengen, DEA
Ketua Dr Ir Isdradjad Setyobudiandi, MSc Anggota
Diketahui oleh
Ketua Program Studi Ilmu Kelautan
Dr Ir Neviaty P. Zamani, MSc
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MScAgr
Tanggal Ujian:
PRAKATA
Puji dan syukur penulis ucapkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga penulis dapat menyelesaikan tesis dengan judul ” Sebaran Teritip Intertidal dan Hubungannya dengan Kondisi Lingkungan Perairan di Pelabuhan Kota Dumai”. Fokus kajian dalam tesis ini mencakup sebaran teritip pada jenis dan warna media penempelan yang berbeda yang dipasang pada 3 pelabuhan di Kota Dumai yang memiliki aktivitas yang berbeda.
Terima kasih penulis ucapkan kepada Prof Dr Ir Dietriech Geoffrey Bengen, DEA dan Dr Ir Isdradjad Setyobudiandi, MSc selaku Komisi Pembimbing yang telah memberi saran dan bimbingan dalam penyusunan tesis ini. Ucapan terima kasih juga disampaikan kepada ayah, ibu, adik-adik tercinta atas segala doa, motivasi dan kasih sayangnya. Salam hangat penulis sampaikan kepada teman-teman kampus khususnya IKL 2011. Ucapan terima kasih juga ucapkan kepada General Manager PT. PELINDO I, Komandan DAN LANAL dan Kepala PPI Purnama Kota Dumai atas izin dan dukungannya kepada penulis selama penelitian di lapangan.
Penulis menyadari bahwa isi tesis ini masih jauh dari sempurna, namun penulis berharap setidaknya tesis ini bisa memberikan kontribusi pada khasanah keilmuan terutama kepedulian terhadap pelestarian dan pemanfaatan biota kekerangan laut. Akhir kata, penulis mohon maaf apabila ada kekurangan dan kesalahan di dalam tesis ini. Kritik dan saran dari semua pihak sangat diharapkan demi kebaikan di masa mendatang. Salam hangat, selamat membaca dan semoga memberi inspirasi.
Bogor, Oktober 2014
DAFTAR ISI
Tujuan dan Manfaat Penelitian 2
Asumsi 2
Pengambilan dan Pengawetan Contoh Plankton 8
Parameter Kondisi Lingkungan Perairan 8
Analisis Data 8
Analisis Kepadatan Teritip 8
Identifikasi dan Perhitungan Kelimpahan Plankton 9 Keterkaitan Karakteristik Lingkungan dan Sebaran Spasial
Kepadatan Teritip 9
Sebaran Kepadatan Teritip Secara Vertikal pada 3 Jenis Media 11
4 HASIL DAN PEMBAHASAN 12
Teritip Amphibalanus spp. 12
Kepadatan Teritip Amphibalanus spp. 14
Keterkaitan Karakteristik Lingkungan dan Sebaran Spasial Kepadatan
Teritip Amphibalanus spp. 18
Sebaran Kepadatan Teritip Amphibalanus spp. Secara Vertikal pada 3
vi
1.1 Pendekatan Penelitian dalam Bagan Alir 4
2.1 Peta lokasi penelitian di Kota Dumai, Riau 5
2.2 Penentuan serta Pembagian Stasiun dan Substasiun Berdasarkan
Bahan Media Penempelan 6
2.3 Penentuan Pemasangan Media Penempelan atau Titik
Pengamatan pada Substasiun 7
3.1 Morfologi Cangkang Teritip Amphibalanus spp. a = Keseluruhan
Cangkang, b = Scuta (Kiri = Eksternal, Kanan = Internal), c =
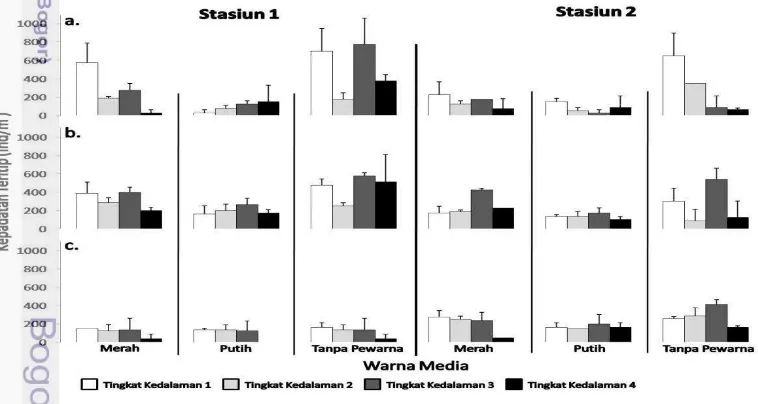
Terga (Kiri = Eksternal, Kanan = Internal) 13 3.2 Kepadatan Teritip Amphibalanus spp. pada Media Kayu, (a.) di
Pelabuhan Pelindo I, (b.) di Pelabuhan Pendaratan Ikan (PPI)
Purnama, (c.) di Pelabuhan Angkatan Laut Bangsal Aceh 14 3.3 Kepadatan Teritip Amphibalanus spp. pada Media Fiber, (a.) di
Pelabuhan Pelindo I, (b.) di Pelabuhan Pendaratan Ikan (PPI)
Purnama, (c.) di Pelabuhan Angkatan Laut Bangsal Aceh 15 3.4 Kepadatan Teritip Amphibalanus spp. pada Media Besi, (a.) di
Pelabuhan Pelindo I, (b.) di Pelabuhan Pendaratan Ikan (PPI)
Purnama, (c.) di Pelabuhan Angkatan Laut Bangsal Aceh 16 3.5 Diagram lingkaran korelasi antara parameter biofisika kimiawi
lingkungan pada sumbu 1 dan sumbu 2 (kiri) dan diagram
sebaran stasiun penelitian pada sumbu 1 dan 2 (kanan) 18 3.6 Hasil analisis koresponden pada sumbu 1 (F1) dan sumbu 2 (F2) 19 3.7 Grafik Pengelompokan Kepadatan Teritip Amphibalanus spp.
pada Setiap Media Penempelan 23
DAFTAR LAMPIRAN
1 Parameter Bio Fisika Kimiawi Perairan Lokasi Penelitian 31 2 Kepadatan Teritip Amphibalanus spp. pada Pelabuhan Pelindo I 32
3 Kepadatan Teritip Amphibalanus spp. pada PPI Purnama 33
4 Kepadatan Teritip Amphibalanus spp. pada Pelabuhan Angkatan
Laut Bangsal Aceh 34
5 Gambar Pemasangan dan Pengangkatan Media Pelabuhan pada
Tiang Pelabuhan 35
6 Hasil Analisis Komponen Utama (PCA) 36
7 Hasil Analisis Faktorial Koresponden (CA) 36
1
PENDAHULUAN
Latar Belakang
Perairan laut mengandung berbagai sumberdaya hayati yang menjadi penyusun struktur biota lingkungan perairan. Beberapa diantaranya adalah biota yang hidupnya menempel pada substrat, baik yang terendam maupun terdedah di permukaan laut. Secara alami kehadirannya adalah peristiwa yang wajar, dimana biota-biota penempel tersebut umumnya berasal dari kelompok bakteri, tumbuhan dan hewan. Penempelan biota tidak hanya terjadi pada substrat alami, dapat juga terjadi pada berbagai sarana kepentingan manusia seperti pada kapal dan bangunan pantai. Penempelan tersebut menimbulkan pengotoran biologis yang disebut dengan biofouling (Peterson et al. 1983).
Teritip adalah salah satu jenis biota yang hidupnya menempel secara permanen pada dinding tiang penyangga dermaga, sedangkan jenis lainnya memiliki kemampuan berpindah tempat. Secara alami teritip banyak dijumpai di laut. Sudah sejak lama teritip merupakan masalah yang sangat serius, kemampuannya dan tempat hidupnya yang menempel pada substrat ternyata memiliki sifat yang dapat merusak dan memperpendek umur suatu bangunan (Nontji 2001).
Penempelan atau biofouling teritip ini terjadi di Pesisir Timur Pulau
Sumatera yang berbatasan langsung dengan Selat Malaka. Padatnya akvitivitas laut di Pulau Sumatera Bagian Timur didukung oleh keberadaan pelabuhan atau dermaga yang dapat dijumpai di sepanjang Pesisir Timur Pulau Sumatera salah satunya di pelabuhan Kota Dumai, Provinsi Riau. Dalam pengelolaan dan pemanfaatannya, pelabuhan-pelabuhan tersebut tidak terlepas dari permasalahan-permasalahan, salah satunya adalah keberadaan organisme yang hidup menempel pada tiang pelabuhan seperti teritip.
Dari hasil observasi pra-penelitian, secara visual pelabuhan-pelabuhan di Pesisir Timur Pulau Sumatera mengalami biofouling dengan kepadatan teritip
yang lebih tinggi dibandingkan pelabuhan-pelabuhan di Pesisir Barat Pulau Sumatera. Penempelan teritip tidak merata pada sisi kiri dan kanan tiang pelabuhan. Selain itu, Distribusi kepadatan teritip tersebut juga tidak merata baik secara horizontal maupun vertikal pada tiang-tiang pelabuhan. Menurut Mudzni (2010), Rata-rata kepadatan teritip (Balanus spp) pada tiang Pelabuhan
Pendaratan Ikan (PPI) Purnama Kota Dumai secara vertikal ke bawah perairan semakin meningkat. Sedangkan secara horizontal, kepadatan teritip (Balanus spp)
lebih tinggi pada bagian tiang pelabuhan yang terlindung dari perairan laut lepas dibandingkan pada bagian tiang pelabuhan yang menghadap ke perairan laut lepas (Fauzi 2010).
Namun observasi pra-penelitian dan penelitian yang telah dilakukan tersebut terbatas pada kepadatan teritip dari jenis Balanus spp. Oleh karena itu perlu
2
Hal ini apabila diteliti lebih lanjut secara ruang (spasial), dapat diketahui penyebab terjadinya ketidakmerataan distribusi kepadatan teritip pada tiang-tiang pelabuhan dan bermanfaat bagi penanganan masalah biofouling yang terjadi pada
pelabuhan khususnya yang terdapat di kota pesisir timur Pulau Sumatera seperti Kota Dumai. Sehingga pada bagian tiang pelabuhan atau kapal yang ditempeli oleh teritip dalam jumlah tinggi dapat diberi penanganan yang lebih intensif seperti pemberian bahan yang dapat menghambat (antifouling) penempelan dan
pertumbuhan teritip.
Perumusan Masalah
Tingginya aktivitas maritim di pesisir timur Pulau Sumatera sebagai bagian dari perairan laut Selat Malaka, menuntut keberadaan pelabuhan laut. Pelabuhan laut menjadi penghubung antara aktivitas darat dan aktivitas perairan. Namun pada tiang-tiang pelabuhan di daerah yang terdapat di sepanjang pesisir timur Pulau Sumatera terdapat organisme-organisme yang menempel dan bersifat merusak. Teritip merupakan salah satu spesies hewan yang umum dijumpai di tiang pelabuhan-pelabuhan di Kota Dumai yang sejak dulu sudah meresahkan, hal ini disebabkan dari waktu ke waktu pertumbuhan teritip terus meningkat dan dikhawatirkan akan merusak tiang-tiang pada pelabuhan ini.
Penempelan teritip tersebut tidak merata pada tiang-tiang pelabuhan. Diperkirakan hal ini dipengaruhi oleh karakteristik lingkungan perairan yang berasal dari parameter biofisika kimiawi air laut. Ketidakmerataan tersebut dapat menyebabkan pengeroposan pada bagian tiang-tiang pelabuhan yang memiliki kepadatan teritip yang tinggi. Sehingga dapat mengancam usia penggunaan tiang pelabuhan tersebut.
Tujuan dan Manfaat Penelitian
Tujuan dari penelitian ini adalah untuk mengetahui sebaran kepadatan teritip intertidal pada jenis dan warna media penempelan yang berbeda. Selain itu, juga untuk mengetahui sebaran kepadatan teritip intertidal secara vertikal dan horizontal di perairan pelabuhan Kota Dumai.
Dengan mengetahui hasil dari penelitian ini diharapkan dapat bermanfaat untuk penanganan masalah biofouling yang terjadi pada bangunan di pesisir pantai
dan kapal-kapallaut khususnya di perairan laut Kota Dumai.
Asumsi
Dalam penelitian ini terdapat beberapa asumsi, yaitu:
1. Biofouling teritip merupakan penyebab utama terjadinya pengeroposan tiang
dermaga.
2. Letak geografis dari setiap pelabuhan dianggap memberikan pengaruh yang sama terhadap kepadatan teritip.
3
Kerangka Pemikiran
4
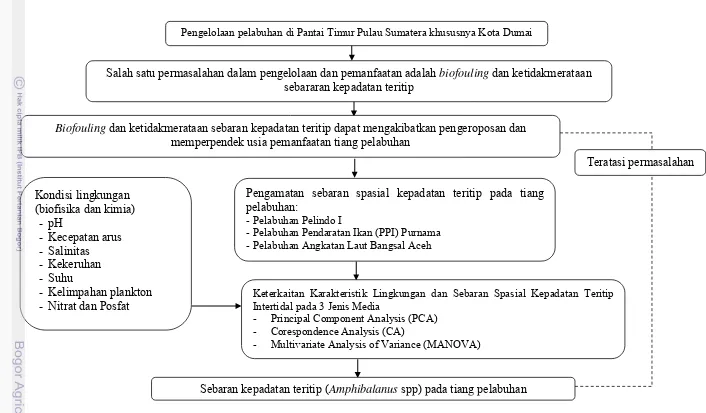
Gambar 1.1 Pendekatan Penelitian dalam Bagan Alir
Pengelolaan pelabuhan di Pantai Timur Pulau Sumatera khususnya Kota Dumai
Salah satu permasalahan dalam pengelolaan dan pemanfaatan adalah biofouling dan ketidakmerataan
sebararan kepadatan teritip
Pengamatan sebaran spasial kepadatan teritip pada tiang pelabuhan:
-Pelabuhan Pelindo I
-Pelabuhan Pendaratan Ikan (PPI) Purnama -Pelabuhan Angkatan Laut Bangsal Aceh Kondisi lingkungan
(biofisika dan kimia) - pH
- Kecepatan arus - Salinitas - Kekeruhan - Suhu
- Kelimpahanplankton
- Nitrat dan Posfat Keterkaitan Karakteristik Lingkungan dan Sebaran Spasial Kepadatan Teritip Intertidal pada 3 Jenis Media - Principal Component Analysis (PCA)
- Corespondence Analysis (CA)
- Multivariate Analysis of Variance (MANOVA)
Sebaran kepadatan teritip (Amphibalanus spp) pada tiang pelabuhan
Teratasi permasalahan
Biofouling dan ketidakmerataan sebaran kepadatan teritip dapat mengakibatkan pengeroposan dan
5
II. METODE PENELITIAN
Lokasi dan Waktu Penelitian
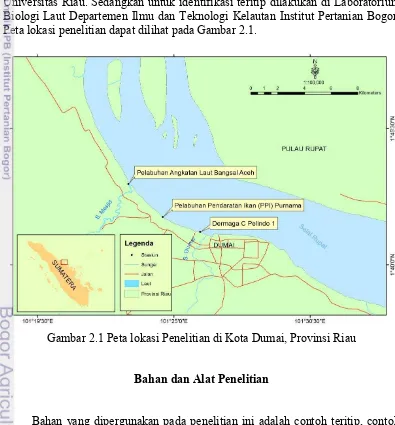
Penelitian ini dilaksanakan pada Bulan September sampai dengan Bulan November 2013. Lokasi penelitian merupakan tiga pelabuhan yang berada di Kota Dumai yaitu Pelabuhan Pelindo 1, Pelabuhan Pendaratan Ikan (PPI) Purnama dan Pelabuhan Angkatan Laut Bangsal Aceh. Untuk identifikasi plankton dan pengukuran parameter kualitas air dilakukan di Laboratorium Ekologi dan Manajemen Lingkungan Perairan Jurusan Manajemen Sumberdaya Perikanan Universitas Riau. Sedangkan untuk identifikasi teritip dilakukan di Laboratorium Biologi Laut Departemen Ilmu dan Teknologi Kelautan Institut Pertanian Bogor. Peta lokasi penelitian dapat dilihat pada Gambar 2.1.
Gambar 2.1 Peta lokasi Penelitian di Kota Dumai, Provinsi Riau
Bahan dan Alat Penelitian
Bahan yang dipergunakan pada penelitian ini adalah contoh teritip, contoh air, contoh plankton, lugol dan alkohol. Untuk alat yang dipergunakan sebagai media penempelan teritip adalah 3 jenis media/plat (besi, kayu dan fiber) dengan ukuran 20 x 20 cm2, mikroskop dan cawan petri. Sedangkan alat yang
-6
refractometer, thermometer, kertas lakmus, botol contoh, plankton net, dan spectrophotometer. Adapun peralatan lain yang mendukung dan digunakan pada
penelitian ini adalah meteran, Self Contained Underwater Breathing Apparatus
(SCUBA), kamera digital, serta perahu.
Prosedur Penelitian
Penentuan Titik Pengamatan
Metode penarikan contoh yang digunakan untuk melihat kepadatan teritip adalah metoda penarikan contoh acak stratifikasi (stratified random sampling method) yang mengacu pada Tanjung (2010). Pengamatan dilakukan pada tiang
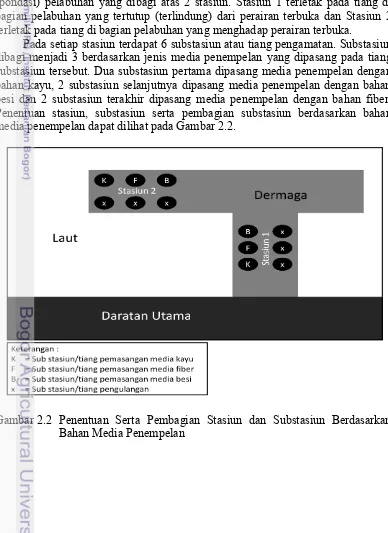
(pondasi) pelabuhan yang dibagi atas 2 stasiun. Stasiun 1 terletak pada tiang di bagian pelabuhan yang tertutup (terlindung) dari perairan terbuka dan Stasiun 2 terletak pada tiang di bagian pelabuhan yang menghadap perairan terbuka.
Pada setiap stasiun terdapat 6 substasiun atau tiang pengamatan. Substasiun dibagi menjadi 3 berdasarkan jenis media penempelan yang dipasang pada tiang substasiun tersebut. Dua substasiun pertama dipasang media penempelan dengan bahan kayu, 2 substasiun selanjutnya dipasang media penempelan dengan bahan besi dan 2 substasiun terakhir dipasang media penempelan dengan bahan fiber. Penentuan stasiun, substasiun serta pembagian substasiun berdasarkan bahan media penempelan dapat dilihat pada Gambar 2.2.
7
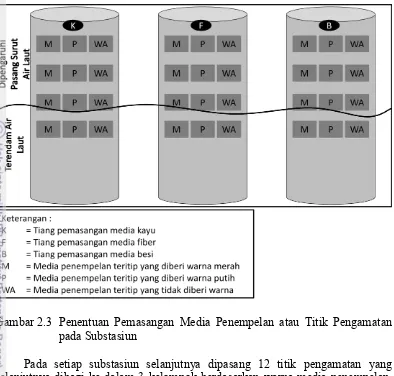
Gambar 2.3 Penentuan Pemasangan Media Penempelan atau Titik Pengamatan pada Substasiun
Pada setiap substasiun selanjutnya dipasang 12 titik pengamatan yang selanjutnya dibagi ke dalam 3 kelompok berdasarkan warna media penempelan. Empat titik pengamatan pertama adalah media penempelan berwarna merah. Empat titik pengamatan selanjutnya adalah media penempelan berwarna putih. Sedangkan 4 titik pengamatan terakhir adalah media penempelan yang tidak diberi warna.
Secara vertikal pada substasiun atau tiang pengamatan, setiap warna media penempelan dibagi kembali menjadi 2 kelompok. Kelompok pertama berada pada bagian tiang yang dipengaruhi pasang surut air laut. Sedangkan kelompok kedua berada pada bagian tiang yang selalu terendam air laut. Penentuan pemasangan media penempelan atau titik pengamatan pada substasiun dapat dilihat pada Gambar 2.3.
Pengamatan Kepadatan Teritip
Untuk menghitung kepadatan teritip yang menempel diperlukan media (plat) penempelan teritip yang dipasang atau diikat pada tiang (pondasi) pelabuhan yang telah ditentukan sebagai tiang pengamatan. Penghitungan kepadatan teritip dengan cara melihat dan menghitung kepadatan yang terfokus pada individu teritip yang berada dalam media (plat) penempelan teritip.
8
pada tiang pelabuhan. Media tersebut diangkat atau dilepaskan dari tiang (pondasi) pelabuhan setelah 60 hari.
Beberapa contoh teritip yang menempel dilepaskan dari media penempelan dan dimasukkan ke dalam botol contoh untuk diawetkan. Pada botol contoh telah diberi larutan alkohol 90%. Pengawetan dilakukan agar bentuk cangkang dan tubuh teritip dalam kondisi baik pada saat identifikasi berlangsung. Selain itu, penghitungan dilakukan pada saat permukaan laut berada pada rata-rata pasang surut terendah di hari pengambilan data.
Pengambilan dan Pengawetan Contoh Plankton
Pengambilan contoh plankton yang ada di permukaan menggunakan plankton net No.25 dengan cara penyaringan menggunakan water sampler
sebanyak 100 l air. Contoh air yang telah disaring kemudian ditampung atau dimasukkan ke dalam botol contoh bervolume 30 ml. Pada botol contoh, sebelumnya telah diberi larutan formalin 40% sampai konsentrasinya menjadi 4% dan diberi lugol sebanyak 2-3 tetes.
Parameter Kondisi Lingkungan Perairan
Pada penelitian ini, data parameter fisika, kimia dan biologi yang diamati adalah kecepatan arus, salinitas, kekeruhan, suhu, pH, nitrat, posfat dan kelimpahan plankton. Pengambilan data kondisi lingkungan perairan tersebut dilakukan pada hari Rabu tanggal 16 Oktober 2013 pukul 13.00 WIB. Pada saat pengambilan data, permukaan laut lokasi penelitian berada dalam kondisi peralihan surut menuju pasang. Data tersebut berguna untuk mendapatkan gambaran pengaruh kondisi lingkungan terhadap ketidakmerataan distribusi kepadatan teritip pada tiang pelabuhan.
Analisis Data
Analisis Kepadatan Teritip
Data penghitungan kepadatan teritip yang diperoleh, mula-mula disajikan dalam bentuk tabel. Untuk menghitung rata-rata kepadatan teritip digunakan metode penghitungan yang mengacu pada English et al. (1994).
= � � ... (1) Dimana:
Di : Kepadatan jenis (ind/m2)
ni : Jumlah individu jenis i
9
Dalam identifikasi jenis teritip digunakan buku Darwin (1851a; 1851b; 1854a; 1854b) dan Newman et al. (1976). Identifikasi dilakukan di Laboratorium
Biologi Laut Departemen Ilmu dan Teknologi Kelautan Institut Pertanian Bogor.
Identifikasi dan Perhitungan Kelimpahan Fitoplankton
Pengamatan plankton dilakukan mulai botol contoh dihomogenkan secara merata, diambil 1 tetes diletakkan di object glass dan ditutup dengan cover glass.
Contoh yang ada diamati dengan menggunakan mikroskop dengan perbesaran 100x sebanyak 25 lapang pandang, sedangkan untuk identifikasi plankton diamati pada perbesaran 400x. Setiap contoh diulang sebanyak dua kali. Plankton diidentifikasi menggunakan buku dari Davis (1955), Thompson (1959), Sachlan (1982), dan Yamaji (1976). Untuk menghitung kelimpahan fitoplankton, terlebih dahulu dihitung volume air laut yang tersaring dengan mengikuti rumus dari
Kelimpahan plankton secara kuantitatif dinyatakan dalam jumlah sel per liter yang ditentukan menggunakan rumus:
Keterkaitan Kondisi Lingkungan Dan Sebaran Spasial Kepadatan Teritip
Kondisi perairan pesisir Kota Dumai sebagai habitat teritip Amphibalanus
spp. berdasarkan variasi parameter biofisika kimiawi lingkungan pada setiap stasiun, dianalisa dengan menggunakan analisis statistik multivariabel yang didasarkan pada analisis komponen utama (Principle Component Analysis, PCA).
Parameter fisik kimia lingkungan yang terdiri atas salinitas, pH, kekeruhan, suhu, kecepatan arus, kelimpahan plankton, nitrat (NO3-N) dan posfat (PO4-P)
10 bersangkutan (Ludwig and Reynolds 1988 dalam Bengen 2000).
Bsxn = Axsn . Atnxs
Dimana:
Bsxn = Matriks korelasi
Axsn = Indeks matrik sintesis
Atnxs = Matriks transformasi Axsn
Pada prinsipnya Analisis Komponen Utama menggunakan jarak Euclidean.
Semakin kecil jarak Euclidean antar stasiun pengamatan, maka semakin mirip
karakteristik antara stasiun tersebut. Jarak Euclidean yang digunakan mengacu padaLegendre dan Legendre (1998) dan Bengen (2000).
� ( ,′) = √∑ = � − �′ ... (5) Dimana:
d(i,i’) = jarak antara pusat data dengan titik data
i & i’ = indeks untuk baris, dari baris ke-i sampai dengan ke-i’ j = indeks untuk kolom
Analisa sebaran kepadatan teritip secara spasial dilakukan dengan menggunakan analisis faktorial koresponden/ corespondence analysis, CA
(Bengen 2000). Analisis ini merupakan salah satu bentuk analisis statistik multivariabel yang didasarkan pada matrik data I baris (stasiun penelitian) dan j
kolom (kepadatan tetitip pada media penempelan). Matrik data yang digunakan merupakan tabel kontingensi stasiun pengamatan dengan modalitas kepadatan teritip pada media penempelan. Tabel kontingensi i dan j mempunyai peranan
yang simetris, yakni membandingkan unsur-unsur i (untuk tiap j) sama dengan
membandingkan hukum probabilitas bersyarat yang diestimasi dari nij/ni (untuk masing-masing nij/nj), dengan ni = jumlah subjek i yang memiliki semua karakter
j, dan nj = jumlah jawaban karakter j. Pengukuran kemiripan antar dua unsur I1 dan I2 dari I dilakukan melalui pengukuran jarak Chi-Square dengan persamaan:
11
Xj = Jumlah dari kolom j untuk keseluruhan baris
Xij,Xi’j = Jumlah dari baris i untuk kolom j
P = Banyaknya baris atau kolom (mulai dari 1 sampai p)
Pengolahan data Analisis Komponen Utama (Principal Component Analysis) dan Analisis Faktorial Koresponden (Correspondence Analysis) digunakan perangkat lunak program Statistika 6.
Sebaran Kepadatan Teritip Secara Vertikal pada 3 Jenis Media
Analisis Ragam Respon Ganda atau Multivariate Analysis of Variance
(MANOVA) digunakan untuk mengeksplor hubungan diantara variabel independen yang bersifat kategorikal (perlakuan atau lokasi) dari dua atau lebih variabel independen metrik. Analisis MANOVA menguji hipotesis nol (Ho) yang menyatakan tidak ada perbedaan rata-rata (mean) dari variabel tak bebas (Y)
dalam kelompok yang berbeda. Hipotesis alternatifnya (Ha) menyatakan, ada perbedaan rata-rata (mean) dari variabel tak bebas (Y) dalam kelompok yang
berbeda. Persamaan Manova adalah sebagai berikut (Mattjik dan Sumertajaya 2011):
Xij = μ + di + eij ... (7)
Tabel 2.1 Persamaan Manova
Sumber Variasi Jumlah Kuadrat Df
Perlakuan (between
W = Jumlah kuadrat residual seluruh kelompok B = Jumlah kuadrat antar kelompok
S1 = Ragam X1
12
kedalaman dan stasiun pengamatan) digunakan nilai Wilk’s Lambda, yang tingkat signifikansinya dibandingkan dengan tingkat signifikansi yang telah ditetapkan yaitu a 0,05 (5 %). Kriteria yang diberikan adalah jika nilai signifikansi Wilk’s Lambda > 0.05 maka hipotesis Ho diterima, yang menyatakan bahwa tidak terdapat pengaruh dari semua perlakuan yang diterapkan terhadap respon yang diamati. Selanjutnya, untuk melihat perlakuan-perlakuan yang berpengaruh nyata terhadap perbedaan respon digunakan analisis varian (uji F), dengan membandingkan nilai signifikansi uji F terhadap nilai signifikansi yang ditetapkan yaitu a 0,05 (5 %). Hipotesis H0 adalah variable independen (kepadatan teritip
pada media yang berbeda-beda jenis dan warnanya) secara parsial tidak berpengaruh nyata terhadap perbedaan variabel dependen (tingkat kedalaman dan stasiun pengamatan). Namun apabila H0 ditolak, dilakukan Uji Lanjut Duncan.
Kriteria penolakan H0 jika nilai signifikansi Fhitung < a 0,05. Untuk menganalisa
data dengan Analisis Manova digunakan perangkat lunak program SAS.
III. HASIL DAN PEMBAHASAN
Teritip Amphibalanus spp.
Teritip yang menempel pada setiap media penempelan selama pengamatan berlangsung, secara keseluruhan merupakan teritip dari genera Amphibalanus spp.
Identifikasi terhadap teritip Amphibalanus spp. dilakukan hingga tahap genera
saja. Hal ini dikarenakan sulitnya untuk melakukan identifikasi lanjut hingga tahap spesies bagi teritip dari genera Amphibalanus spp. yang masih dalam tahap juvenile. Menurut Henry dan McLaughlin (1975), kekeliruan dalam
mengidentifikasi teritip dari genus Amphibalanus yang masih dalam fase juvenile
sangat sering terjadi. Hal ini dikarenakan masih banyak kesamaan morfologi teritip jenis ini ketika dalam tahap juvenile. Beberapa spesies yang sangat potensial mengalami kekeliruan dalam identifikasinya adalah Amphibalanus improvisius, Amphibalanus reticulatus, Amphibalanus subalbidus dan Amphibalanus venustus.
Dominasi teritip jenis Amphibalanus spp. ini cukup beralasan. Menurut
Boesono (2008), teritip dari genus Amphibalanus memiliki senyawa arthropodine
yang berguna untuk menarik atau mengundang teritip dari jenis yang sama untuk menempel bahkan menumpuk pada substrat yang sama. Selain itu, dari keseluruhan famili Balanidae, larva Amphibalanus spp. memiliki laju
pertumbuhan yang paling cepat, mudah untuk dibudidayakan serta dapat diduga penempelannya pada kondisi statis khususnya jenis A. amphitrite, sehingga Amphibalanus spp. merupakan jenis teritip yang paling sering dijumpai dan
digunakan pada penelitian ekologi organisme intertidal dan studi antifouling (Anil et al. 2012). Pada media penempelan ditemukan juga biota-biota lain yang
menempel seperti alga cokelat (Phaeophyta), spons (Porifera) dan Ooyster
13
Gambar 3.1 Morfologi Cangkang Teritip Amphibalanus spp. a = Keseluruhan
Cangkang, b = Scuta (Kiri = Eksternal, Kanan = Internal), c = Terga (Kiri = Eksternal, Kanan = Internal)
Amphibalanus spp. merupakan jenis teritip baran (acorn barnacle) yang
dicirikan dengan cangkang yang dibangun dan langsung menempel pada substrat. Secara garis besar, habitat Amphibalanus spp. adalah perairan intertidal di daerah
beriklim tropis (Darwin 1854; Jones et al. 2000). Namun pada beberapa kasus,
teritip ini ditemukan di perairan laut lepas. Teritip tersebut menempel pada benda-benda terapung seperti sampah-sampah plastik dan patahan batang (Hansen 1990). Adapun klasifikasi dari Amphibalanus spp. menurut Darwin (1854); Newman dan
Abbot (1980) dan Pitombo (2004) adalah sebagai berikut: Superordo : Thoracica
Cangkang teritip Amphibalanus spp. umumnya berbentuk kerucut atau
cenderung silinder dan memiliki 6 bagian cangkang (plates) yang mengelilingi
dan melindungi tubuhnya (Gambar 3.1). Pada bagian puncak terdapat lubang yang melingkar dan sedikit bergerigi. Umumnya perbandingan tinggi cangkang
Amphibalanus spp. dengan lebar keseluruhan cangkang adalah 1:2. Pada
punggung cangkang terdapat garis lebar permanen yang membujur dan menyempit pada puncak cangkang yang disebut radii (Pitombo 2004). Beberapa
jenis Amphibalanus spp. seperti A. reticulatus dan A. amphitrite terdapat
perbedaan warna yang nyata antara cangkang yang memiliki warna lebih cerah dibandingkan radii. Berbeda halnya dengan A. improvisius, warna cangkang
serupa dengan warna radii (Zullo 1979). Bagian operculum, pada bagian
permukaan scutum terdapat adductor yang mencuat keluar dan sangat mencolok.
Panjang diameter dasar keseluruhan cangkang (basal margin) pada genera
Amphibalanus sangat beragam. Untuk diameter maksimal basal margin jenis A. reticulatus dan A. Improvisius adalah 18 mm, sedangkan jenis A. amphitrite
14
Kepadatan Teritip Amphibalanus spp.
Kepadatan Amphibalanus spp. pada setiap lokasi penelitian sangat beragam,
baik pada media penempelan atau pun pada pemberian warna media penempelan yang berbeda. Selain itu, keragaman kepadatan Amphibalanus spp. juga terjadi
pada pemasangan media penempelan secara vertikal (perbedaan tingkat pasang surut) dan horizontal (perbedaan stasiun penelitian). Secara keseluruhan, rata-rata kepadatan Amphibalanus spp. tertinggi terdapat pada media penempelan dengan
jenis kayu yang tidak diberi pewarna atau warna asli. Secara horizontal, rata-rata kepadatan tertinggi terdapat pada stasiun 1 pelabuhan Pelindo I dan stasiun 1 PPI Purnama. Sedangkan secara vertikal, rata-rata kepadatan tertinggi terjadi pada tingkat kedalaman 3 (tinggi rata-rata surut harian) dan tingkat kedalaman 2 (tinggi rata-rata pasang harian). Hasil penghitungan rata-rata kepadatan Amphibalanus
spp. pada setiap stasiun penelitian dapat dilihat pada Lampiran 2, 3 dan 4.
Sedangkan untuk mengetahui grafik hasil penghitungan kepadatan Amphibalanus
spp. pada media kayu, media fiber dan media besi dapat dilihat pada Gambar 3.2;
3.3 dan 3.4.
Rata-rata kepadatan Amphibalanus spp. tertinggi pada media kayu terdapat
pada stasiun 2 pelabuhan Pelindo I yaitu 506,25 ind/m2. Kepadatan tertinggi
tersebut terdapat pada media kayu yang tidak diberi pewarna (Gambar 3.2a). Sedangkan rata-rata kepadatan terendah terdapat pada stasiun 2 pelabuhan Pelindo I yaitu 78,125 ind/m2. Kepadatan terendah tersebut terdapat pada media kayu
dengan warna putih (Gambar 3.2a).
Gambar 3.2 Kepadatan Teritip Amphibalanus spp. pada Media Kayu, (a.) di
Pelabuhan Pelindo 1, (b.) di Pelabuhan Pendaratan Ikan (PPI) Purnama, (c.) di Pelabuhan Angkatan Laut Bangsal Aceh.
Kepadatan teritip Amphibalanus spp. pada beberapa media kayu
dipengaruhi oleh adanya kompetisi perebutan ruang dengan biota lain. Biota yang memiliki pengaruh besar terhadap kepadatan Amphibalanus spp. pada media kayu
dalam penelitian ini adalah cacing laut (marine borer worm). Ini ditandai dengan
15
lobang gerek (bore holes). Selain itu, serangan cacing laut juga berpengaruh
terhadap usia media kayu (Lampiran 5). Keberadaan serangan cacing laut ditandai oleh adanya penggerekan yang mula-mula tegak lurus terhadap serat kayu, kemudian membelok sejajar serat kayu. Secara terus menerus organisme ini memperpanjang lubang gereknya di dalam kayu dan dinding salurannya dilapisi zat kapur. Intensitas serangan yang tinggi pada kayu akan menunjukkan kepadatan populasi organisme tersebut di dalam kayu. Serangan ini disebut dengan serangan
Teredinidae (Muslich and Sumarni 2005).
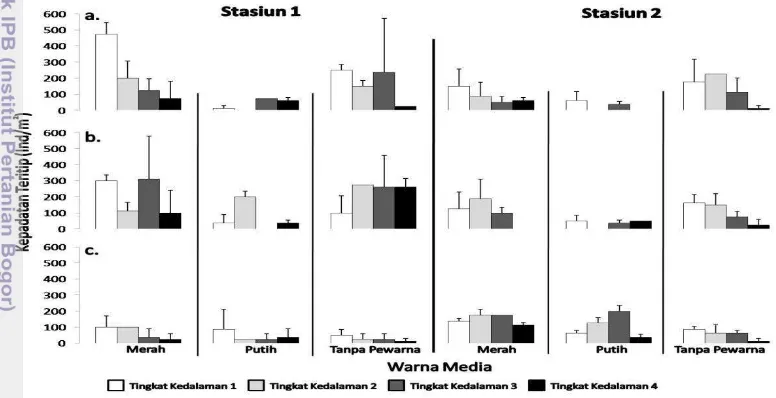
Rata-rata kepadatan Amphibalanus spp. tertinggi pada media fiber terdapat
pada stasiun 1 pelabuhan Pelindo I yaitu 218,75 ind/m2. Kepadatan tertinggi
tersebut terdapat pada media fiber dengan warna merah (Gambar 3.3a). Sedangkan rata-rata kepadatan terendah terdapat pada stasiun 2 pelabuhan Pelindo I yaitu 25 ind/m2. Kepadatan terendah tersebut terdapat pada media fiber dengan
warna putih (Gambar 3.3a).
Gambar 3.3 Kepadatan Teritip Amphibalanus spp. pada Media Fiber, (a.) di
Pelabuhan Pelindo 1, (b.) di Pelabuhan Pendaratan Ikan (PPI) Purnama, (c.) di Pelabuhan Angkatan Laut Bangsal Aceh.
Secara keseluruhan, rata-rata kepadatan pada media fiber adalah yang terendah dibandingkan dua media penempelan lainnya yaitu media kayu dan besi. Berdasarkan grafik Gambar 3.3 terlihat bahwa beberapa media fiber tidak memiliki nilai kepadatan atau sama dengan nol. Hal ini disebabkan karena pada saat pengamatan akhir atau pengangkatan media terdapat beberapa media fiber yang hilang dari tiang pengamatan, sehingga tidak diketahui nilai kepadatan teritip yang telah menempel pada media tersebut. Selain itu, media fiber yang memiliki nilai kepadatan yang tinggi pada umumnya terdapat alga yang telah menempel dan menutupi sebagian permukaan media fiber (Lampiran 5). Hal ini mengindikasikan bahwasannya terdapat hubungan antara kepadatan teritip dan alga pada suatu substrat.
16
2012). Hal ini disebabkan oleh karena beberapa alga menghasilkan zat pencegah pertumbuhan (inhibitor) bagi larva teritip seperti alga cokelat Fucus vesiculosus
yang memiliki kandungan phlorotannin (Brock et al. 2007) dan alga merah
Sphaerococcus coronopifolius yang memiliki kandungan LC50 yang juga
merupakan antifouling bagi larva teritip Amphibalanus amphitrite (Piazza 2010).
Namun hasil penelitian tersebut berbeda dengan hasil penelitian yang dilakukan oleh Nylund (1999) yang menyebutkan bahwa senyawa yang dihasilkan oleh alga
merah seperti Dilsea carnosa dan Delesseria sanguine yaitu Dimethylsulphoxid
(DMSO) justru menjadi stimulant bagi penempelan larva teritip Amphibalanus improvisius.
Pada beberapa studi yang lain, bakteri biofilm yang bersimbiosis dengan
alga berpengaruh nyata terhadap penempelan larva biota invertebrata seperti
teritip bahkan melindungi alga dari serangan epibionts (Lau and Qian 1997;
Steinberg et al. 1998; Lachnit et al. 2010). Namun begitu, beberapa bakteri
biofilm juga memiliki pengaruh netral terhadap penempelan larva teritip
(Wieczorek et al. 1995). Hal ini juga diperkirakan berpengaruh terhadap
kepadatan penempelan teritip Amphibalanus spp.pada media penempelan fiber di
penelitian ini, dimana kandungan bakteri biofilm yang berkemungkinan masih
rendah, sehingga dapat ditemukan teritip yang menempel pada media fiber.
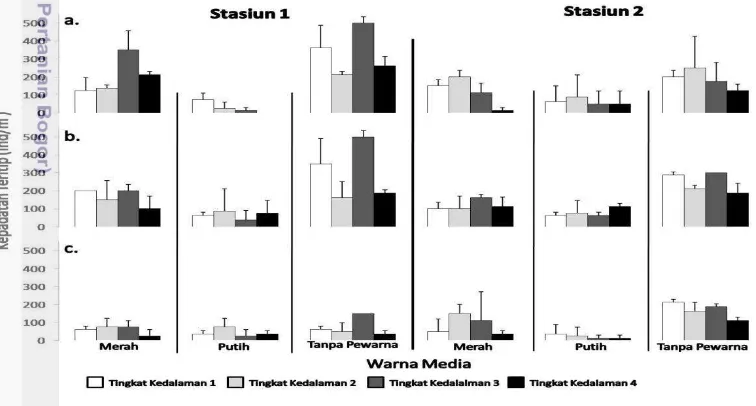
Gambar 3.4 Kepadatan Teritip Amphibalanus spp. pada Media Besi, (a.) di
Pelabuhan Pelindo 1, (b.) di Pelabuhan Pendaratan Ikan (PPI) Purnama, (c.) di Pelabuhan Angkatan Laut Bangsal Aceh.
Selanjutnya berdasarkan Gambar 3.4, rata-rata kepadatan Amphibalanus
spp. tertinggi pada media besi terdapat pada stasiun 1 pelabuhan Pelindo I yaitu 334.375 ind/m2. Kepadatan tertinggi tersebut terdapat pada media besi yang tidak
diberi pewarna atau warna asli (Gambar 3.4a). Sedangkan rata-rata kepadatan terendah terdapat pada stasiun 2 pelabuhan AL Bangsal Aceh yaitu 21,875 ind/m2.
17
Tabel 3.1 Ringkasan Kepadatan Teritip Amphibalanus spp. pada 3 Jenis Media
Jenis
*Jenis dan warna media serta tingkat kedalaman yang memiliki kepadatan teritip tertinggi
Keterangan : + + + + = Rata-rata kepadatan teritip > 350 ind/m2
+ + + = Rata-rata kepadatan teritip 200 – 350 ind/m2
+ + = Rata-rata kepadatan teritip 100 – 250 ind/m2
+ = Rata-rata kepadatan teritip < 100 ind/m2
Secara keseluruhan media penempelan, nilai kepadatan teritip
Amphibalanus spp. sangat beragam secara vertikal. Kepadatan tertinggi terdapat
pada tingkat kedalaman 2 (rata-rata tinggi permukaan laut saat pasang harian) dan 3 (rata-rata tinggi permukaan laut saat surut harian) yang termasuk ke dalam kategori pasang surut harian (mid intertidal zone) di perairan Kota Dumai. Hasil
ini sesuai dengan hasil penelitian yang dilakukan oleh Minchinton dan Scheibling (1993) yang menyatakan bahwa dari tiga tingkat pasang surut di Nova Scotia Kanada, kepadatan tertinggi teritip jenis Semibalanus balanoides terdapat pada
zona mid intertidal atau tinggi pasang surut harian.
Keragaman kepadatan teritip secara vertikal dipengaruhi oleh faktor abiotik dan biotik lingkungan (Scheletema 1974; Rittschof and Bonaventura 1986; Rittschof et al. 1998, Khandeparker and Anil 2007). Namun lebih khusus lagi,
keragaman kepadatan secara vertikal ini diperkirakan berkaitan dengan sifat fototaksis negatif atau kecenderungan menjauhi keberadaan cahaya larva teritip yang juga termasuk dalam kategori plankton-hewani (zooplankton)
(Rohmimohtarto dan Juwana 2009; Setyobudiandi et al. 2009). Dimana
keberadaan cahaya merupakan ancaman bagi penglihatan larva teritip untuk melakukan penempelan pada substrat. Hasil penelitian Hung et al. (2005)
18
bentuk adaptasi terhadap peristiwa pasang surut. Hal tersebut ditandai dengan tertutupnya cangkang teritip yang berguna untuk menyimpan volume air di dalam cangkang dan menurunnya metabolisme tubuh teritip hingga 70 %. Selanjutnya perbedaan kecepatan arus antara permukaan dan kolom perairan serta konsentrasi makanan secara vertikal juga mempengaruhi populasi teritip secara vertikal (Anil
et al. 2012).
Keterkaitan Kondisi Lingkungan dan Sebaran Spasial Teritip Amphibalanus spp.
Hasil analisis komponen utama terhadap parameter biofisika kimiawi lingkungan pesisir Kota Dumai pada matrik korelasi menunjukkan informasi penting yang menggambarkan korelasi antar parameter terpusat pada dua sumbu utama yaitu F1 dan F2. Kualitas informasi yang disajikan oleh kedua sumbu masing-masing sebesar 44,67% dan 26,60% (Gambar 3.5). Sehingga ragam karakteristik habitat teritip Amphibalanus spp. menurut stasiun penelitian
berdasarkan parameter biofisika kimiawi lingkungan dapat dijelaskan melalui dua sumbu utama sebesar 71,27% dari ragam total. Hasil analisis komponen utama juga disajikan ke dalam bentuk tabel yang dapat dilihat pada Lampiran 6.
Gambar 3.5 Diagram lingkaran korelasi antara parameter biofisika kimiawi lingkungan pada sumbu 1 dan sumbu 2 (kiri) dan diagram sebaran stasiun penelitian pada sumbu 1 dan 2 (kanan).
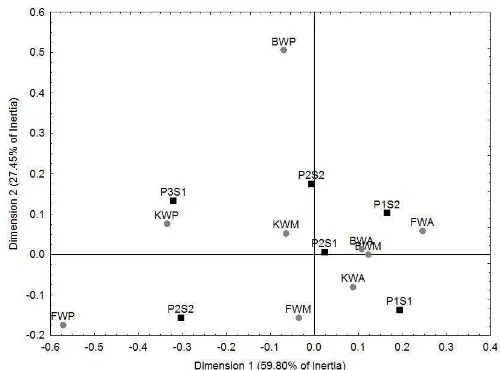
Analisis mengenai sebaran spasial kepadatan teritip Amphibalanus spp.
Berdasarkan kepadatan pada perlakuan jenis dan warna media yang berbeda dilakukan dengan Analisis Koresponden (Correspondent Analysis, CA). Hasil
analisis menunjukkan bahwa informasi distribusi spasial kepadatan teritip
Amphibalanus sp. terpusat pada dua sumbu utama, yaitu F1 dan F2.
Masing-masing sumbu memberikan kontribusi sebesar 59,80% (F1) dan 27,45% (F2). Sehingga nilai ragam total dari data yang membentuk kedua sumbu tersebut adalah sebesar 87,25%. Diagram analisis koreponden antara stasiun penelitian dan kepadatan teritip amphibalanus sp. pada setiap media penempelan dapat dilihat
19
Gambar 3.6 Hasil analisis koresponden pada sumbu 1 (F1) dan sumbu 2 (F2) Berdasarkan Gambar 3.5 dan 3.6, dapat diketahui bahwasannya terdapat 3 kelompok stasiun penelitian yang terbentuk karena memiliki karakteristik lingkungan dan kepadatan teritip Amphibalanus spp. yang berbeda. Kelompok
individu I (pertama) terdiri atas stasiun 1 (P1S1) dan stasiun 2 pelabuhan Pelindo I (P1S2) yang dicirikan oleh salinitas (28 ‰), pH (8) dan kekeruhan (2 NTU) yang tinggi. Rata-rata kepadatan teritip Amphibalanus spp. pada kelompok ini
memiliki kepadatan teritip tertinggi dibandingkan kelompok lainnya, yang terdapat pada media-media penempelan seperti media kayu yang tidak diberi warna (KWA = 506 ind/m2), media fiber yang tidak diberi warna (FWA = 165
ind/m2), media besi yang tidak diberi warna (BWA = 334 ind/m2) dan media besi
bewarna merah (BWM = 206 ind/m2).
Tingginya salinitas, pH dan kekeruhan pada kelompok individu I tidak terlepas dari adanya rutinitas kegiatan bongkar muat bahan CPO kering di Pelabuhan Pelindo I. Namun begitu, kondisi lingkungan tersebut sangat mendukung untuk kehidupan teritip. Kekeruhan perairan diketahui memiliki kaitan erat terhadap ketersediaan makanan bagi larva teritip dalam fase nauplii, yaitu fitoplankton dan tingginya kekeruhan perairan dapat melindungi larva nauplii yang belum mampu untuk berenang dengan baik dari kanibalisme yang dilakukan oleh teritip dewasa (Barnes 1962).
Konsentrasi salinitas perairan berpengaruh terhadap tekanan osmotik biota-biota yang hidup di dalamnya. Umumnya biota-biota-biota-biota tersebut memiliki kandungan garam pada sel-selnya yang nilainya mendekati nilai salinitas perairan, sehingga apabila sel-sel tersebut berada pada lingkungan perairan dengan nilai salinitas berbeda, maka akan berdampak langsung terhadap osmoregulasi dari sel-sel tersebut. Salinitas pada Pelabuhan Pelindo I masih merupakan kisaran optimum bagi kehidupan teritip. Kisaran salinitas yang dapat ditoleransi oleh teritip adalah 10 ‰ (Anil et al. 1995) hingga 52 ‰ (Cohen 2005). Dari hasil
percobaan Anil et al. (1995), tingkat kematian larva teritip jenis Amphibalanus amphitrite pada salinitas 10 ‰ mencapai 99%. Hal ini memiliki kaitan erat
20
‰. Teritip yang hidup pada salinitas tersebut adalah jenis Amphibalanus amphitrite dan ditemukan pada saat pengamatan lapangan yang dilakukan oleh
Cohen pada tahun 2005 di pesisir barat San Fransisco.
Konsentrasi pH pada Pelabuhan Pelindo I juga masih berada dalam kisaran optimum bagi kehidupan teritip Amphibalanus spp. Konsentrasi pH di perairan
memiliki pengaruh terhadap kehidupan organisme bentik (Kurihara et al. 2007;
Beesley et al. 2008; Wood et al. 2008; Dupont et al. 2008) khususnya teritip
(McDonald et al. 2009). Konsentrasi pH memiliki hubungan erat dengan
konsentrasi calcium carbonate (CaCO3) di perairan yang berguna sebagai bahan
pembentuk cangkang bagi beberapa organisme moluska dan crustacea. Menurut McDonald et al. (2009), penurunan pH perairan laut dari 8.2 hingga 7.4 tidak memberikan pengaruh terhadap kondisi larva, ukuran cyprid, penempelan cyprid serta metarmofosis dari tahap juvenile hingga menjadi dewasa bagi teritip jenis
Amphibalanus amphitrite. Perubahan ditemukan pada saat pH berada di bawah
nilai 7.4 yang ditandai dengan perusakan, penurunan laju pertumbuhan dan kalsifikasi pada cangkang teritip yang selanjutnya menyebabkan individu teritip rentan terhadap serangan predator.
Kelompok individu II (kedua) terdiri atas stasiun 1 PPI Purnama (P2S1), stasiun 1 (P3S1) dan stasiun 2 pelabuhan AL Bangsal Aceh (P3S2) yang dicirikan oleh kecepatan arus (0,7 m/dtk), nitrat (0,35 mg/l) dan posfat (0,0088 mg/l)yang tinggi. Namun berdasarkan sebaran kepadatan teritip Amphibalanus spp.,
kelompok ini memiliki perbedaan pengelompokan. Stasiun 1 PPI Purnama merupakan stasiun pengamatan yang memiliki rata-rata kepadatan teritip yang tinggi dan termasuk ke dalam kelompok yang sama dengan kedua stasiun Pelabuhan Pelindo I. Sementara kedua stasiun Pelabuhan Angkatan Laut Bangsal Aceh merupakan stasiun pengamatan yang memiliki rata-rata kepadatan terendah dibanding stasiun pengamatan lainnya, yang terdapat pada media-media penempelan seperti media kayu berwarna merah (KWM = 112 ind/m2), media
kayu berwarna putih (KWP = 100 ind/m2), media fiber berwarna merah (FWM =
65 ind/m2), media fiber berwarna putih (43 ind/m2) dan media besi berwarna putih
(BWP = 21 ind/m2).
Perbedaan pengelompokan tersebut tidak terlepas dari adanya pengaruh letak geografis masing-masing stasiun pengamatan. Kedua stasiun Pelabuhan Angkatan Laut Bangsal Aceh terletak pada muara Sungai Mesjid, sehingga menyebabkan tingginya kandungan nitrat posfat dan kecepatan arus (Hutagalung
et al. 1997). Sedangkan stasiun 1 PPI Purnama berada pada daerah yang tidak
berdekatan dengan muara sungai. Namun begitu, kandungan nitrat dan posfat pada stasiun itu memiliki nilai yang tidak jauh berbeda dengan kedua stasiun Pelabuhan Angkatan Laut Bangsal Aceh yaitu 0,2938 mg/l dan 0,0066 mg/l. Hal ini diperkirakan terjadi karena adanya aktivitas pendaratan dan pelelangan ikan yang mempengaruhi pasokan nutrien di perairan.
Kecepatan arus memiliki pengaruh yang besar terhadap kehidupan organisme sessilefilter feeder seperti halnya teritip. Hal ini terlihat dari rendahnya
kepadatan teritip Amphibalanus spp. pada kedua stasiun Pelabuhan Angkatan Laut
21
1989) dan pemberian makanan di perairan sekitar individu teritip (Cancino and Hughes 1987; Best 1988; Okamura 1992). Bagi larva cyprid, kecepatan arus berpengaruh pada tingkat keberhasilan penempelan larva terhadap substrat (Gambi et al. 1990; Irlandi and Peterson 1991).
Kisaran kecepatan arus di lokasi penelitian selama pengukuran masih berada dalam rentang toleransi bagi teritip. Menurut Anil et al. (2012), kisaran kecepatan
arus 1-2 knots (0.5-1 m/detik) merupakan titik kritis bagi larva teritip jenis
Eliminius modestus untuk melakukan penempelan. Namun setelah kecepatan arus
berada di atas 2 knots, tingkat keberhasilan penempelan tersebut perlahan mulai menurun. Hasil penelitian Qian et al. (2000) menambahkan bahwasannya
persentase penempelan larva teritip jenis Amphibalanus spp. terjadi pada kisaran
kecepatan arus 4.2 sampai 21.2 cm/detik, dimana penempelan tertinggi terjadi pada kecepatan arus sebesar 10.6 cm/s.
Penelitian terkait pengaruh kecepatan arus terhadap ketersediaan makanan bagi teritip di perairan pernah dilakukan oleh Sanford et al. (1994). Hasil
penelitiannya menunjukkan bahwasannya perairan yang tidak memiliki kecepatan arus atau relatif tenang dapat menyebabkan rendahnya persentase keberhasilan pemberian makan terhadap larva maupun teritip dewasa jenis Semibalanus balanoides. Sedangkan untuk persentase tertinggi dalam keberhasilan pemberian
makan ketika kecepatan arus berada pada nilai 21 cm/detik dengan suhu 15 0C.
Kecepatan arus 21 cm/detik tersebut umumnya terjadi pada kolom perairan di pesisir yang terjal berbatu.
Konsentrasi nutrien di perairan juga memiliki pengaruh langsung terhadap tingkat keberhasilan larva teritip untuk melakukan penempelan kepada substrat (Anderson 1996; Faimali et al. 2004). Hasil uji laboratorium yang dilakukan oleh
Minchinton and Mckenzie (2008) menyebutkan dalam 2 minggu, penempelan larva teritip meningkat secara nyata setelah diberi peningkatan konsentrasi nutrien di kolom perairan secara berkala.
Selanjutnya, kelompok individu III (ketiga) hanya terdiri dari satu stasiun pengamatan, yakni stasiun 2 PPI Purnama (P2S2) yang dicirikan kelimpahan plankton (4800 sel/L) yang rendah dan suhu permukaan laut (30 oC) yang tinggi
dibandingkan stasiun pengamatan lainnya. Berdasarkan pengelompokan kepadatan teritip, stasiun 2 PPI Purnama termasuk ke dalam kelompok dengan kepadatan teritip yang rendah. Rendahnya kepadatan tersebut dipengaruhi oleh bentuk atau struktur bangunan dari dermaga PPI Purnama yang lebih terbuka dan mudah terpapar cahaya matahari, sehingga mempengaruhi aktivitas larva teritip yang bersifat fototaksis negatif dan suhu permukaan perairan.
Kelimpahan dan keragaman jenis fitoplankton sangat berpengaruh dengan kepadatan teritip di perairan. Hal ini dikarenakan fitoplankton merupakan sumber makanan bagi teritip. Setiap fase hidup teritip memiliki jenis dan ukuran fitoplankton yang beragam sebagai makanannya. Secara keseluruhan, teritip lebih banyak mencerna fitoplankton dari jenis diatom. Diatom jenis Skeletonema costatum dengan ukuran 2-16 µm merupakan makanan yang paling disukai oleh
larva nauplii Balanus amphitrite dibandingkan Chaetoceros calcitrans dengan
ukuran 4-6 µm (Desai and Anil 2004). Hasil studi lain yang dilakukan oleh Thiyagarajan et al. (1996) menyebutkan bahwasannya diatom Chaetoceros gracilis diindikasikan lebih banyak dicerna oleh larva teritip Balanus amphitrite
22
Namun hasil kedua penelitian di atas berbeda dengan hasil penelitian terdahulu yang dilakukan oleh Moyse (1963) dan Moyse and Knight-Jones (1967) yang menyebutkan bahwa larva teritip Chtalamus stellatus, Lepas anatifera dan Lepas pectinata lebih bersifat omnivora yang tidak hanya mencerna diatom
(phytoplankton), tetapi juga mencerna flagellata (zooplankton). Hal ini cukup
beralasan karena didukung oleh ukuran tubuh dan mekanisme pencernaan larva teritip yang mampu untuk mencerna picoplankton dengan ukuran < 5 µm dan
bahan-bahan makanan lainnya selain diatom (Vargas et al. 2006).
Sebaran Teritip Amphibalanus spp. Secara Vertikal Pada 3 Jenis Media Penempelan
Rata-rata kepadatan teritip Amphibalanus spp. pada setiap perlakuan selama
penelitian sangat beragam baik secara vertikal maupun horizontal. Berdasarkan penempelan pada jenis media, rata-rata kepadatan pada media kayu merupakan yang tertinggi dibandingkan media fiber dan besi. Sedangkan berdasarkan pemberian warna, rata-rata kepadatan tertinggi dijumpai pada media yang tidak diberi warna dibandingkan media yang diberi warna merah dan putih. Keragaman kepadatan tersebut selanjutnya dianalisis menggunakan Analisis Ragam Peubah Ganda (MANOVA). Hasil analisis menunjukkan nilai p dalam statistik Wilk’s Lambda adalah <0,05, yang berarti terdapat minimal satu jenis media atau
pemberian warna pada media yang berpengaruh nyata terhadap kepadatan teritip
Amphibalanus spp. baik secara vertikal maupun horizontal, sehingga dengan ini
hipotesis awal (H0) dari analisa ini ditolak. Hasil penghitungan dari Analisa
Ragam Peubah Berganda (MANOVA) dapat dilihat pada Lampiran 8.
Pemasangan media penempelan dengan jenis dan warna yang berbeda, secara visualisasi dari Gambar 3.2; 3.3 dan 3.4 menunjukkan adanya beberapa pengelompokan media penempelan dengan rata-rata kepadatan teritip
Amphibalanus spp. yang sama. Namun gambaran tersebut belum dapat mewakili
ada-tidaknya pengelompokan secara kuantitatif inferensial. Oleh karena itu perlu dilakukan uji lanjut yaitu Uji Perbandingan Berganda Duncan yang berfungsi sebagai uji lanjut dari hasil analisa Analisa Ragam Peubah Ganda (MANOVA) di atas. Hasil Uji Duncan pada penelitian ini dapat dilihat pada Gambar 3.7.
Hasil Uji Duncan menunjukkan lebih dari satu perlakuan yang memberi pengaruh nyata terhadap kepadatan teritip Amphibalanus spp. Pada setiap
23
Gambar 3.7 Grafik Pengelompokan Kepadatan Teritip Amphibalanus spp. pada
Setiap Media Penempelan.
*Grafik batang kepadatan teritip yang memiliki huruf yang sama tidak berbeda nyata satu sama lain (Uji Perbandingan Berganda Duncan, σ = 0,05)
Pengelompokan rata-rata kepadatan teritip pada setiap stasiun penelitian di atas menunjukkan bahwasannya tingkat kesuksesan penempelan larva teritip juga bergantung kepada jenis dan warna substrat. Berdasarkan Gambar 3.9, teritip tampak memiliki kecenderungan memilih media dengan permukaan kasar seperti kayu. Berbeda halnya dengan media fiber dan besi yang memiliki permukaan yang lebih halus dibandingkan media kayu. Selama pengamatan berlangsung, penempelan teritip juga ditemukan pada tiang pelabuhan dan batu-batu di tepi pelabuhan dengan kepadatan yang tinggi secara visual. Permukaan substrat yang kasar diperkirakan dapat melindungi larva teritip yang bersifat planktonik dari pergerakan arus pada saat melakukan penempelan dan memudahkan teritip untuk melepaskan semen sebagai perekat tubuh teritip terhadap substrat (Abbot 1990). Selain itu, kayu juga memiliki daya tahan yang rendah terhadap biota penempel.
Berdasarkan Gambar 3.9, pemberian warna pada media juga memberi pengaruh yang nyata terhadap kepadatan teritip selama penelitian. Kepadatan teritip secara keseluruhan lebih tinggi pada media dengan warna yang lebih gelap dibandingkan media dengan warna cerah. Media penempelan yang memiliki kecerahan yang tinggi secara visual pada penelitian ini adalah media fiber. Oleh karena itu, media fiber merupakan media dengan rata-rata kepadatan terendah dibandingkan media kayu dan besi. Sebagaimana halnya larva invertebrata, larva cyprids teritip (tahap sebelum penempelan) juga memiliki sifat fototaksis negatif yang cenderung untuk menjauhi cahaya, sehingga media atau substrat yang memiliki warna cerah merupakan media yang tidak disukai oleh larva teritip (Hung et al. 2005).
24
alga pada permukaan substrat dapat menutup warna cerah yang dimiliki oleh media fiber dan juga membentuk lapisan baru di atas permukaan media fiber, sehingga warna dan permukaan substrat yang dibentuk oleh alga dapat menjadi pemicu bagi larva teritip untuk melakukan penempelan. Namun di sisi lain, keberadaan alga dapat menjadi pembatas perkembangan hidup teritip. Hal ini dikarenakan adanya beberapa bakteri biofilm yang bersimbiosis dengan alga dan
25
V. SIMPULAN DAN SARAN
Simpulan
Kepadatan teritip Amphibalanus spp. pada tiang pelabuhan tertinggi terdapat
pada media penempelan kayu yang tidak diberi warna yaitu sebesar 506,25 ind/m2, sedangkan kepadatan terendah terdapat pada media penempelan besi
berwarna putih (21, 875 ind/m2) dan fiber berwarna putih (25 ind/m2). Secara
horizontal, rata-rata kepadatan teritip tertinggi dijumpai pada kedua stasiun Pelabuhan Pelindo I, sedangkan kepadatan terendah dijumpai pada stasiun 1 Pelabuhan Angkatan Laut Bangsal Aceh. Secara vertikal, tingkat kedalaman yang memilki kepadatan teritip tertinggi adalah tingkat kedalaman 3 yaitu tinggi rata-rata permukaan laut saat surut terendah harian dan kepadatan terendah dijumpai pada tingkat kedalaman 1 yaitu tinggi permukaan laut saat pasang tertinggi di Kota Dumai.
Saran
Kajian dalam jangka waktu yang lebih panjang (temporal) di perairan pesisir Kota Dumai perlu dilakukan untuk mengetahui siklus dan pola kebiasaan hidup teritip sebelum dan sesudah melakukan penempelan.
Kajian adanya kompetisi dan simbiosis antar biota dengan teritip juga perlu dilakukan, mengingat tidak hanya teritip yang menjadi sumber biofouling di
26
DAFTAR PUSTAKA
Abbot A. 1990. Bioadhesives: Potential for Exploitation. Sci Prog 74: 131-46 Anderson MJ. 1986. A Chemical Cue Induces Settlement of Sydney Rock
Oysters, Saccrostrea commercialis in The Laboratory and in The Field.
Biol Bull 190: 350-358
Anil AC, Chiba K, Okamoto K, Kurokura H. 1995. Influence of Temperature and Salinity on The Larval Development of Balanus amphitrite: Implications
in The Fouling Ecology. Mar Ecol Prog Ser 118: 159-166
Anil AC, Desai DV, Khandepaker L, Gaonkar AC. 2012. Barnacle and Their Significance In Biofouling. In: Rajagopal S, Jenner HA, Venugopalan VP, editor. Operational and Environmental Consequences of Large Industrial Cooling Water Systems. Springer Science and Business Media. New York (USA). 65-94 p.
Barnes H. 1962. Note on The Variations in The Release of Nauplii of Balanus balanoides with Special Reference to The Spring Diatom Outburst.
Crustacea 4: 118-122
Bengen DG. 2000. Sinopsis teknik pengambilan contoh dan analisis data biofisik sumberdaya pesisir. Bogor (ID): Pusat Kajian Sumber Daya Pesisir dan
Laut IPB. 88 p.
Beesley A, Lowe DM, Pascoe CK, Widdicombe S. 2008. Effects of CO2-Induced Seawater Acidification on The Health of Mytilus edulis. Clim Res 37:215–
225
Best. BA. 1988. Passive Suspension Feeding in A Sea Pen: Effects of Ambient Flow on Volume Flow Rate and Filtering Efficiency. Biol Bull mar, Biol. Lab, Woods Hole 175: 332-342
Boesono H. 2008. Pengaruh Lama Perendaman Terhadap Organisme Penempel dan Modulus Elastisitas pada Kayu. Jurnal Ilmu Kelautan 13: 177-180 Brock E, Nylund GM, Pavia H. 2007. Chemical Inhibition of Barnacle Larval
Settlement by The Brown Alga Fucusvesiculosus. Mar Ecol Prog Ser 337:
165-174
Cancino, JM, Hughes RN. 1987. The Effect of Water Flow on Growth and Reproduction of Celleporella hyalina (L.) (Bryosoa: Cheilosotomata). J
Exp Mar Biol Ecol 112: 109-130
Cohen AN. 2005. Rapid Assessment Shore Survey for Exotic Species in San Francisco Bay - May 2004, San Francisco Estuary Institute, Oakland. 32 p. Crisp DJ. 1974. Factors Influencing The Settlement of Marine Invertebrate Larvae. In: Grant PT, Mackie AM editor. Chemoreception in Marine Organisms. Academic, New York. 177-265 p.
Darwin C. 1851a. A Monograph on The Subclass Cirripedia with Figures of All The Species. The Lepadidae; or, Pedunculated Cirripedes. London (ENG): Ray. Soc. Publ. 400 p.
. 1851b. A monograph on the fossil Lepadidae, or Pedunculated Cirripedes of Great Britain. London (ENG): Palaentograph Soc. 88 p. . 1854a. A Monograph on The Subclass Cirripedia with Figures of All
27
. 1854b. A monograph on the fossil Balanidae and Verrucidae of Great Britain. London (ENG): Palaentograph Soc. 88 p.
Davis CC. 1955. The Marine and Freshwater Plankton. Michigan State University Press, Chicago.
Desai DV, Anil AC. 2004. The Impact of Food Type, Temperature and Starvation Threshold of Nauplii Barnacle Balanus Amphitrite Darwin (Cirripedia:
Thoracica). Ind J Mar Sci 29: 69-72
Dupont S, Havenhand J, Thorndyke W, Peck L, Thorndyke M. 2008. Near-Future Level of CO2-Driven Ocean Acidification Radically Affects Larval Survival and Development in The Brittlestar Ophiothrix fragilis. Mar Ecol
Prog Ser 373:285–294
Eckman J, Duggins DO, Sewell AT. 1989. Ecology of Understory Kelp Environments. I. Effects of Kelps on Flow and Particle Transport Near The Bottom. J Exp Mar Biol Ecol 129: 173-187
English S. Wilkinson, C. and Baker, V. 1994. Survay Manual For Tropical Marine Resources. Australia Institule Of Marine Science. Townsville. 367 p. Faimali M, Garaventa F, Terlizzi A, Chiantore M, Cattaneo-Vietti R. 2004. The
Interplay of Substrate Nature and Biofilm Formation in Regulating
BalanusAmphitrite Darwin, 1954 Larval Settlement. J Exp Mar Biol Ecol
306: 37-50
Fauzi R. 2010. Distribusi Kepadatan Teritip (Balanus spp) pada Tiang Pelabuhan
Penyeberangan Purnama Kota Dumai [skripsi]. Pekanbaru (ID): Universitas Riau. 67 p.
Gambi MC, Nowell ARM, Jumars PA. 1990. Flume Observations on Flow Dynamics in Zostera Marina (Eelgrass) Beds. Mar Ecol Prog Ser 61: 159-169
Henry DP, McLaughlin PA. 1975. The Barnacles of The Balanus amphitrite
complex (Cirripedia: Thoracica). Zoologische Verhandelingen 141: 1-203 Hung OS, Gosselin LA, Thiyagarajan V, Wu RSS, Qian PY. 2005. Do Effects
Ultraviolet Radiation on Microbial Film have Indirect Effects of Larval Attachment of The Barnacle Balanusamphitrite? J Exp Mar Bio Ecol 323:
16-26
Hutagalung HP, Rozak A. 1997. Penentuan kadar nitrat dan fosfat. Dalam Hutagalung HP, Setiapermana D, Riyono. Metode Analisis Air laut, Sedimen dan Biota. Buku 2. Puslitbang Oseanologi. LIPI.
Irlandi EA, Peterson CH. 1991. Modification of Animal Habitat by Large Plants: Mechanisms by Which Seagrasses Influence Clam Growth. Oecologia 87: 307-318
Jones DS, Hewitt MA, Sampey A. 2000. Checklist of the Cirripedia of the South China Sea, Raffles Bulletin of Zoology Supplement 8: 233-307
Khandepaker L, Anil AC. 2007. Under Water Adhesive: The Barnacle Way. Int J Adh Adhesives 27: 165-172.
Kurihara H, Kato S, Ishimatsu A. 2007. Effects of Increased Seawater pCO2 on
Early Development of The Oyster Crassostrea gigas. J Aquat Biol 1:
91-98
28
Lau SCK, Qian PY. 1997. Phlorotannins and Related Compounds as Larval Settlement Inhibitors of The Tube-Building Polychaete Hydroides elegans.
Mar Ecol Prog Ser 159:219–227
Legendre P, LegendreL.1998. Numerical Ecology: Development in Environmental Modelling 2nd edition. Amsterdam (NL):Elsevier Scientific Publishing
Company.853 p.
Maki JS, Rittshcof D, Mitchell R. 1992. Inhibition of Larval Barnacle Attachment to Bacterial Films: An Investigation of Physical Properties. Microb Ecol 23: 97-106
McDonald MR, McClintock JB, Amsler CD, Rittschop D, Angus RA, Orihuela B, Lutostanski K. 2009. Effects of Ocean Acidfication Over The Life History of The Barnacle Amphibalanusamphitrite. Mar Ecol Prog 385: 179-187
Minchinton TE, McKenzie LA. 2008. Nutrient Enrichment Affects Recruitment Oyster and Barnacles in A Mangrove Forest. Mar Ecol Prog Ser 354: 181-189
Mudzni A. 2010. Distribusi Kepadatan Teritip (Balanus spp) Secara Vertikal pada
Tiang Pelabuhan Pendaratan Ikan (PPI) Purnama Kota Dumai [skripsi]. Pekanbaru (ID): Universitas Riau. 60 p.
Moyse J. 1963. Comparison of The Value of Various Flagellates and Diatoms as Food for Barnacle Larvae. J du Conseil Permanent International pour I’Exploration de la Mer 28: 175-187
Moyse J, Knight-Jones EW. 1967. Biology of Cirripede Larvae. In Proc Symp Crustacea Ernakulam, 1965, Part I. Marine Biology Society of India. Bangalore Press. Bangalore, 595-611 p.
Muslich M, Sumarni G. 2005. Keawetan 200 jenis kayu Indonesia terhadap penggerek di laut. Jurnal Penelitian Hasil Hutan 23(3):163-176. Pusat Litbang Hasil Hutan. Bogor.
Nasrolahi A. 2012. Stress Ecology: Interactive Effect of The Temperature and Salinity on Early Life Stages of Barnacle Amphibalanus amphitrite
[dissertation]. Kiel (Ger). Helmholtz-Zentrum fur Ozeanforschung (GEOMAR).
Newman WA, Zullo VA, and Withers TH. 1967. Origin and Evolution of Cirripedia. Conference on The Evolution of Crustacea. Crustaceana Vol. 4. 166 p.
Nontji A. 2001. Laut Nusantara. Djambatan. Ed rev, Cetakan 5. Jakarta. 300 hal. Nylund GM. 1999. Epibiosis of Red Algae and Algal Metabolites as Settlement
Inhibitors of The Barnacle Balanusimprovisius Darwin [thesis]. Goteborg
(Swe): Goteborg University
Okamura B. 1992. Microhabitat Variation and Patterns of Colony Growth and Feeding in A Marine Bryozoan. Ecology 73: 1502–1513.
Peterson H, Colburn T, and Downing D. 1983. Spatial and Temporal Patterns in Hebivory on a Caribbean Fringing Reef: The Effects on Plant Distribution. Oecologia 58:299–308
Piazza V, Roussis V, Garaventa F, Greco G, Smyrniotopoulos V, Vagias C, Faimali M. 2009. Terpenes from The Red Alga Sphaerococus coronopifolius Inhibit The Settlement of Barnacles. Mar Biotechnol.