INHIBITOR TOPOISOMERASE I
DARI KABLANG (Nerita albicilla)
DANI SJAFARDAN ROYANI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis yang berjudul “Komposisi kimia dan aktivitas inhibitor topoisomerase I dari Kablang (Nerita albicilla)” adalah karya saya sendiri dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Desember 2007
Inhibitor Activity of Kablang (Nerita albicilla). Supervised by LINAWATI HARDJITO and JOKO SANTOSO.
ABSTRAK
DANI SJAFARDAN ROYANI. Komposisi Kimia dan Aktivitas Inhibitor Topoisomerase I dari Kablang (Nerita albicilla). Dibimbing oleh LINAWATI HARDJITO dan JOKO SANTOSO.
DNA topoisomerase I dan II adalah enzim inti sel esensial untuk proliferasi sel dan merupakan target dalam pengembangan obat antikanker. Dalam penelitian ini dipelajari kadar proksimat dan komposisi asam amino serta aktivitas inhibisi dari ekstrak Kablang (Nerita albicilla) terhadap kerja dari enzim DNA topoisomerase I.
Tahapan penelitian meliputi penentuan kadar proksimat dan asam amino Kablang, ekstraksi sampel dengan pelarut heksana, etil asetat dan metanol, penentuan aktivitas inhibitor topoisomerase I dengan menggunakan drug screening kit topoisomerase I dari TopoGen. Aktivitas inhibisi DNA topoisomerase I dianalisis dengan menggunakan gel elektroforesis.
@ Hak cipta milik IPB, tahun 2007 Hak cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan, karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar IPB.
KOMPOSISI KIMIA DAN AKTIVITAS
INHIBITOR TOPOISOMERASE I
DARI KABLANG (Nerita albicilla)
DANI SJAFARDAN ROYANI
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Teknologi Hasil Perairan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
NRP : C351050031
Disetujui
Komisi Pembimbing
Dr. Ir. Linawati Hardjito, M.Sc Dr. Ir. Joko Santoso, M.Si
Ketua Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Teknologi Hasil Perairan
Dr. Ir. Sri Purwaningsih, M.Si Prof. Dr. Ir. Khairil Anwar Notodiputro, MS
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini dapat diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Nopember 2006 ini adalah Inhibitor topoisomerase I dengan judul “Komposisi kimia dan aktivitas inhibitor topoisomerase I dari Kablang (Nerita albicilla)”.
Terima kasih penulis ucapkan kepada Ibu Dr. Ir. Linawati Hardjito, M.Sc sebagai pembimbing I dan Bapak Dr. Ir. Joko Santoso, M.Si sebagai pembimbing II yang telah banyak memberikan bimbingan, arahan dan saran sehingga penelitian dan penulisan ini dapat diselesaikan. Juga kepada Ibu Prof.Dr.drh. Maria Bintang, MS, sebagai penguji luar komisi yang telah banyak memberikan masukan dalam penyempurnaan tesis ini. Ucapan terima kasih tak lupa penulis sampaikan juga kepada :
1. Direktur Politeknik Perikanan Negeri Tual Maluku Tenggara yang telah memberikan kepercayaan kepada penulis untuk melanjutkan studi di IPB Bogor.
2. Dekan Pascasarjana dan pengelola Program Studi Teknologi Hasil Perairan IPB atas kesempatan yang telah diberikan untuk mengikuti pendidikan pascasarjana.
3. Kepada ketua tim Program Hibah Penelitian Tim Pasacasarjana-HPTP (Hibah Pasca) dengan judul: ”Screening, Isolasi dan Identifikasi Inhibitor topoisomerase untuk target penemuan anti kanker dari organisme pesisir/laut yang telah digunakan sebagai obat tradisional” (2006-2007) yang telah mendanai penelitian ini.
4. Hasil karya ini juga penulis persembahkan kepada istri tercinta Nyai Hanubun, SE dan kedua anakku yaitu Muhammad Farhan Royani dan Muhammad Haidar Abyan atas segala pengertian, ketabahan, kesabaran serta pengorbanan yang diberikan selama Penulis menjalani studi S-2.
kerjasamanya selama perkuliahan serta semua pihak yang telah membantu baik secara langsung maupun tidak langsung.
8. Rekan-rekan seperjuangan di Laboratorium Bioteknologi Hasil Perairan (kang cecu, bu Niken, bu Dewi, mas Agus dan mas Fajar) atas segala bantuan dan kerjasama yang kompak.
9. Teman-teman dari Tual (Usman, Beni, Yula) atas segala bantuan dan kerjasama yang solid.
Semoga bimbingan, dorongan dan bantuan yang diberikan mendapat balasan dari Allah SWT.
Bogor, Desember 2007
RIWAYAT HIDUP
Penulis dilahirkan di Ambon-Maluku pada tanggal 7 April 1970 dari ayah Maad Yusuf Royani dan ibu Muhannah, dan merupakan putra kedua dari lima bersaudara.
Tahun 1990 penulis lulus SMA Negeri 3 Ambon dan pada tahun yang sama lulus seleksi masuk Universitas Pattimura Ambon melalui jalur Penerimaan Siswa-Siswi Berbakat (PSSB). Penulis memilih Program Studi Pengolahan Hasil Perikanan, Jurusan Pengolahan Hasil Perikanan, Fakultas Perikanan dan lulus pada tahun 1996.
ix
DAFTAR TABEL ...
xi
DAFTAR GAMBAR ...
xii
DAFTAR LAMPIRAN ... xiii
1. PENDAHULUAN ...
1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ...
3
1.3 Tujuan Penelitian dan Manfaat Penelitian ...
4
1.3 Hipotesis Penelitian ...
4
2. TINJAUAN PUSTAKA ...
5
2.1 Deskripsi Kablang (
Nerita
albicilla
) ...
5
2.2 Bahan Aktif Siput Laut Kablang (
Nerita albicilla
)...
6
2.3 Asam Amino ...
7
2.4 Ekstraksi Bahan Aktif ...
9
2.5 Kanker, Antikanker dan Uji Antikanker ...
10
2.6 Topoisomerase dan Inhibitor Topoisomerase I ...
12
2.7 Elektroforesis ...
15
2.5 Alkaloid dan Steroid ... 16
3. METODOLOGI PENELITIAN ...
20
3.1 Waktu dan Tempat Penelitian ...
20
3.2 Bahan dan Peralatan ...
20
3.2.1 Bahan ...
20
3.2.2 Peralatan ...
20
3.3 Prosedur Penelitian...
21
3.3.1 Penentuan kadar proksimat dan asam amino Kablang ...
21
3.3.2 Ekstraksi bahan aktif Kablang (
Nerita albicilla
) ...
26
3.3.3 Uji aktivitas inhibitor topoisomerase I (TopoGen 2006) ...
28
3.3.4 Karakterisasi ekstrak aktif inhibitor topoisomerase I ...
30
x
4. HASIL DAN PEMBAHASAN ...
35
4.1 Kandungan Gizi Kablang ...
35
4.1.1 Analisis proksimat ...
35
4.1.2 Komposisi asam amino ...
39
4.2 Ekstraksi Bahan Aktif ...
42
4.3 Aktivitas Inhibitor Topoisomerase I ...
43
4.4 MIC Inhibitor Topoisomerase I dari Ekstrak Metanol ...
44
4.5 Karakterisasi Ekstrak Aktif Inhibitor Topoisomerase I ...
45
4.6 Isolasi Senyawa Aktif Inhibitor Topoisomerase I ...
48
4.6.1 Isolasi alkaloid ...
49
4.6.2 Isolasi steroid ...
50
5. KESIMPULAN DAN SARAN ...
53
DAFTAR PUSTAKA ...
54
xi
Halaman
1 Hasil analisis proksimat daging kering Kablang dibandingkan dengan produk
perikanan lainnya ...
35
2 Hasil analisis komposisi asam amino Kablang dan ikan tuna, kerang sebagai
pembanding ...
39
3 Analisis asam amino esensial dan nonesensial dari
Nerita albicilla
(mg/g
protein) ...
41
4 Skor kimia asam amino Kablang ...
41
5 Rendemen hasil ekstraksi Kablang (
Nerita albicilla
) ...
42
6 Hasil elektroforesis uji inhibisi enzim DNA toposiomerase I dari ekstrak
Kablang. ...
43
7 Hasil uji inhibisi ekstrak metanol terhadap enzim topoisomerase I pada
berbagai konsentrasi ...
44
8 Hasil uji kimiawi ekstrak aktif inhibitor topoisomerase I dari Kablang (
Nerita
albicilla
) ...
46
9 Hasil isolasi alkaloid ekstrak aktif metanol (Metode Harborne) ...
49
xii
DAFTAR GAMBAR
Halaman
1 Kablang
(
Nerita albicilla
) ...
5
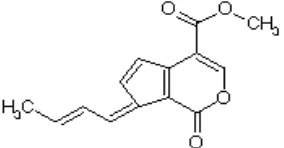
2 Struktur fulvoplumierin (Sanduja
et al.
1985) ...
6
3 Sruktur lamellarin D (Facompre
et al.
2003) ...
7
4 Struktur
beberapa
topoisomerase poison (Ammon dan Osheroff 1995) ...
14
5 Perbedaan antara inhibitor katalitik dan poison (TopoGen 2006) ...
14
6 Kerangka inti steroid (Litwack dan Schmidt 2002) ...
18
7 Struktur
7-dehidrokolesterol dan ergosterol ...
18
8 Diagram alir penelitian komposisi kimia dan aktivitas inhibitor
topoisomerase I dari siput laut
Nerita
albicilla
...
21
9 Diagram alir proses ekstraksi bahan aktif Kablang ...
27
10 Tahapan dalam uji inhibitor topoisomerase I ...
29
11 Bagan alir ekstraksi alkaloid (Harborne 1987) ...
33
12 Bagan alir ekstraksi steroid (Bahti
et al.
1983) ...
34
13 Kandungan asam amino Kablang (
Nerita albicilla
) ...
40
14 Hasil elektroforesis uji inhibisi ekstrak terhadap enzim DNA topoisomerase
I pada konsentrasi 50µg/ml ... 44
15 Hasil elektroforesis uji inhibisi ekstrak terhadap enzim DNA topoisomerase I
ekstrak metanol
Nerita albicilla
pada berbagai konsentrasi ...
45
16 Hasil uji alkaloid ekstrak aktif inhibitor topo I Kablang (
Nerita albicilla
) ...
47
17 Hasil uji steroid ekstrak aktif inhibitor topo I Kablang ...
48
18 Struktur
5
α
-cholestane-hexaol
...
51
xiii
Halaman
1
Road map
penelitian penapisan dan uji aktivitas inhibitor topoisomerase I
dari Kablang (
Nerita albicilla
) ...
60
2 Contoh perhitungan rendemen ekstrak Kablang (
Nerita albicilla
) ...
61
3 Contoh perhitungan asam amino Kablang (
Nerita albicilla
) ...
62
4 Kurva standar analisis asam amino ...
63
5 Hasil analisis asam amino Kablang (
Nerita albicilla
) ...
64
1. PENDAHULUAN
1.1 Latar Belakang
Kabupaten Maluku Tenggara yang sebagian besar wilayahnya terdiri atas
lautan (± 87%) dan memiliki 123 pulau, mempunyai potensi sumberdaya laut dan
keanaekaragaman hayati yang cukup tinggi. Berdasarkan Data Statistik Dinas
Perikanan dan Kelautan Kabupaten Maluku Tenggara (2004) jumlah produksi
perikanan pada tahun 2003 sebesar 94.599,3 ton, terdiri dari komoditas perikanan
tuna, pelagis besar, pelagis kecil, demersal dan komoditas perikanan lainnya. Hasil
analisis potensi sumberdaya ikan di Kabupaten Maluku Tenggara pada wilayah
pengelolaan 4 mil laut adalah sebesar 13.379,7 ton dengan nilai maximum
sustainable yield (MSY) sebesar 6.689,8 ton dan total allowable catch (TAC)
sebesar 5.351,9 ton. Dengan demikian, ikan yang masih dapat dieksploitasi lagi
sebesar 781,6–2.265,6 ton per tahun. Keanekaragaman hayati perairan pesisir pada
tingkat spesies terdiri atas filum moluska : 160 spesies (kelas gastropoda), kelas
bivalvia (41 spesies), kelas holothuridae (8 spesies), kelas ekinoidea (3 spesies), 9
spesies ekinodermata, 14 spesies alga, 256 spesies ikan karang, 69 spesies terumbu
karang.
Organisme hidup tidak terkecuali biota laut menghasilkan berbagai produk
alami yang terdiri atas metabolit primer dan sekunder. Senyawa ini dihasilkan oleh
organisme berupa metabolit primer yaitu yang dihasilkan bersamaan dengan
tumbuhnya organisme dan metabolit sekunder yang dihasilkan ketika organisme
sudah memasuki fase stasioner (non-growth associated product). Pemanfaatan
metabolit sekunder dari laut sebagai zat aktif dalam obat belum banyak diteliti
khususnya di Indonesia. Banyak zat-zat berdaya obat dari beberapa organisme laut
telah diketahui ratusan tahun, tetapi eksplorasi sumberdaya hayati laut sebagai
sumber obat-obatan hampir tidak pernah berlanjut. Untuk mengekstraksi
komponen bioaktif dari sumberdaya hayati laut, diperlukan berbagai cara yang
tepat, agar dapat dihasilkan produk secara efisien dan berdaya guna. Aplikasi
bioteknologi dalam pengembangan sumberdaya pesisir dan lautan akan
Menurut Darusman et al. (1995) umumnya obat yang berasal dari produk
alam hasil laut merupakan metabolit sekunder dari berbagai kelompok alkaloid,
terpenoid, flavonoid dan juga berasal dari senyawa pembangun metabolit primer
seperti dipeptida. Faulkner (2000) menjelaskan bahwa senyawa hasil laut tersebut
dapat larut dalam pelarut organik (organic soluble) atau pelarut air (water soluble).
Banyak upaya pencarian obat baru yang ditujukan khusus untuk kanker baik
dari sumberdaya laut maupun darat. Aneka sumberdaya laut yang menjadi obyek
riset di negara-negara maju berupa invertebrata laut seperti spons, tunicate, dan
moluska menempati urutan pertama dengan target utama sebagai antikanker (Russel
2003 diacu dalam Purwaningsih 2007). Prospek penemuan obat dan produk farmasi
dari biota laut diperkirakan 300 sampai dengan 400 kali lebih besar dibanding
dengan isolasi dari eksosistem darat (Bruckner 2002 diacu dalam Purwaningsih
2007).
Salah satu moluska laut yang dimanfaatkan sebagai obat adalah siput laut
Nerita albicilla (Kablang). Secara tradisional masyarakat Desa Sather di Kepulauan
Kei, Kabupaten Maluku Tenggara, memanfaatkan Kablang sebagai bahan pangan
lauk (pengganti ikan pada musim paceklik) dan untuk mengobati penyakit hati
dengan cara dimakan dagingnya dan air rebusannya diminum. Hasil penelitian
Martin et al. (1986) menyatakan bahwa Nerita albicilla mengandung oksiindol
alkaloid yang dikenal sebagai isopteropodin. Selanjutnya Lee et al. (1999)
melaporkan bahwa isopteropodin dari tanaman Uncaria tamentosa dapat
menghambat topoisomerase I.
Topoisomerase adalah enzim yang terdapat dalam inti sel yang berperan
dalam replikasi DNA. Enzim ini ditemukan dalam jumlah yang berlebihan pada sel
kanker dibandingkan sel sehat/normal. Oleh karena itu inhibitor topoisomerase
menjadi salah satu target penemuan antikanker baru oleh berbagai industri obat
dunia (Yanagihara et al. 2005). Enzim DNA Topoisomerase digunakan sebagai
molekul target untuk pencarian dan penemuan obat antikanker yang rasional dan
lebih selektif. Cara ini sangat baik untuk mengevaluasi senyawa bioaktif antikanker
yang positif dan pada pengujian in-vivo menunjukkan aktivitas antikanker
3
Penyakit kanker masih menjadi salah satu penyakit yang paling ditakuti
masyarakat dan merupakan salah satu penyakit mematikan. Di Indonesia, penyakit
ini telah menduduki peringkat kelima penyebab kematian. Padahal dekade
sebelumnya hanya di peringkat sembilan. Bahkan di negara-negara maju, kanker
menjadi penyebab kematian nomor dua. Di dunia, setiap tahun ada penambahan 6 -
10 juta orang yang menderita kanker, sedangkan di Indonesia jumlah penderita
kanker mencapai 6% dari populasi. Lima besar penyakit kanker yang sering terjadi
di Indonesia adalah kanker leher rahim, payudara, kelenjar getah bening, nasofaring,
dan kulit (Supari 2007).
Menurut Siswandono dan Soekardjo (1995) sampai saat ini masih sedikit
sekali obat antikanker yang bekerja secara selektif untuk pengobatan jenis kanker
tertentu. Berbagai usaha telah dilakukan untuk menanggulangi penyakit kanker
seperti pembedahan, terapi radiasi dan kemoterapi. Namun hingga kini masih belum
ditemukan cara yang dapat mengatasi penyakit tersebut secara memuaskan. Cara
lain yang dipilih sebagian penderita penyakit ini adalah dengan memanfaatkan
bahan alam yaitu dengan menggunakan tanaman obat dan hewan. Hal ini
disebabkan adanya keinginan masyarakat sendiri untuk kembali menggunakan
bahan dari alam (back to nature).
Penelitian ini difokuskan pada aktivitas ekstrak yang dapat menghambat
kerja dari enzim topoisomerase I serta karakteristik dari senyawa aktif inhibitor
topoisomerase yang dihasilkan oleh ekstrak Kablang. Pengetahuan akan
kandungan nutrisi dan senyawa bioaktif dari Kablang adalah penting karena
berkaitan dengan pengembangan dan pemanfaatannya di bidang pangan dan
farmasi. Road map penelitian Kablang (Nerita albicilla) dapat dilihat pada
Lampiran 1.
1.2 Perumusan Masalah
Di Indonesia berbagai hasil laut berupa alga laut, vertebrata maupun
invertebrata laut telah berabad-abad digunakan sebagai obat untuk meningkatkan
kesehatan (promotif), memulihkan kesehatan (rehabilitatif), pencegahan penyakit
(preventif) dan penyembuhan (kuratif). Namun eksistensinya belum dapat
kimia, karena memang belum teruji keamanan dan manfaatnya. Selama ini
kebanyakan manfaat dan pengembangannya hanya dari data empiris dan dari
pengalaman yang diwariskan dari generasi ke generasi.
Dalam usaha mengembangkan obat tradisional, salah satu biota laut yang
menarik perhatian dan diduga mempunyai aktivitas antikanker adalah Kablang
(Nerita albicilla) yang berasal dari Kepulauan Kei Provinsi Maluku. Penelitian
antikanker dari Kablang belum dilakukan secara ilmiah. Untuk itu perlu dilakukan
penelitian mengenai aktivitas enzim topoisomerase I terhadap ekstrak Kablang
(Nerita albicilla).
1.3 Tujuan Penelitian dan Manfaat Penelitian Penelitian ini bertujuan adalah untuk:`
Hasil penelitian ini diharapkan dapat memberikan kontribusi pada bidang
perikanan khususnya pengembangan produk alam dari laut yang berkhasiat obat.
1.4 Hipotesis Penelitian
Ekstrak dari Kablang (Nerita albicilla) mengandung senyawa inhibitor
topoisomerase I.
(1) Mengetahui komposisi kimiawi termasuk asam amino dari Kablang.
(2) Mendapatkan ekstrak yang memiliki aktivitas sebagai inhibitor
topoisomerase I.
(3) Mengetahui golongan senyawa ekstrak aktif inhibitor topoisomerase I.
2. TINJAUAN PUSTAKA
2.1 Deskripsi Kablang (Neritia albicilla)
Kablang merupakan nama lokal untuk siput laut Nerita albicilla di daerah
Kei Besar Kabupaten Maluku Tenggara. Selanjutnya Wilson (1993)
mengklasifikasikan Kablang (Nerita albicilla) sebagai berikut :
Kingdom : Animal
Filum : Molusca
Klas : Gastropoda
Subklas : Prosobranchia
Ordo : Neritimorpha
Superfamili : Neritoidea
Famili : Neritidae
Genus : Nerita
Spesies : Nerita albicilla
Nerita mempunyai cangkang kecil sampai sangat kecil, membulat sampai
bentuk mangkuk memipih. Pada siput dewasa dinding bagian dalam membentuk
ruangan membulat yang tidak melingkar di dalam cangkang. Operkulum
mengapur, sedikit terpilin, agak bulat dengan tempat gantungan lateral pada sisi
bagian dalam. Habitat berkisar dari laut, payau dan air tawar. Kebanyakan marga
dari famili ini hidup di atas dasar yang keras, kecuali Smaragdia yang hidup di
atas tanaman laut (Matsuura et al. 2000). Gambar 1 menunjukkan siput laut
Kablang (Nerita albicilla).
2.2 Bahan Aktif Siput Laut Kablang (Nerita albicilla)
Selain dikonsumsi sebagai sumber makanan di daerah Kei Besar, Kablang
(Nerita albicilla) dapat dimanfaatkan sebagai sumber senyawa bioaktif. Goad
(1978) menyatakan bahwa Nerita peloronta mengandung sterol yang umumnya
dari jenis kolesterol. Senyawa sterol dari jenis moluska telah banyak dianalisis
kandungan dan komposisi kimianya, bahkan lebih banyak daripada sterol dari
filum yang lain. Lebih lanjut Sanduja et al. (1985) melaporkan bahwa Nerita
albicilla mengandung pigmen antibakteri fulvoplumierin (Gambar 2).
Gambar 2 Struktur fulvoplumierin(Sanduja et al. 1985).
Martin et al. (1986) telah berhasil mengisolasi suatu senyawa oksiindol
alkaloid yang disebut isopteropodin dari moluska laut Nerita albicilla.
Selanjutnya Laus dan Keplinger (1994) melaporkan bahwa isopteropodin pada
tanaman Uncaria tomentosa menunjukkan efek sitotoksik pada fibroblast tikus
dan manusia (nonmikroseluler karsinoma paru-paru, karsinoma serviks dan
karsinoma prostat). Kandungan isopteropodin pada tanaman Uncaria tomentosa
terutama pada akar, dan dalam jumlah yang kecil pada batang dan kulit.
Isopteropodin juga dapat ditemukan pada beberapa spesies yang lain dari famili
Rubiaceae. Isopteropodin dari Uncaria tomentosa juga diketahui mempunyai
aktivitas inhibitor topoisomerase I (Lee et al. 1999) .
Sakai (1995) menjelaskan bahwa umumnya isopteropodin dicirikan oleh
beberapa aktivitas biologi yang khas dan banyak digunakan di dalam pengobatan
atau diharapkan memecahkan masalah pengobatan. Garcia et al. (2004)
melaporkan bahwa isopteropodin dari Uncaria tomentosa diketahui mempunyai
aktivitas antibakteri terhadap bakteri Gram positif.
Olivera (1995) melaporkan siput laut dari jenis Conus geographus
7
dibanding morfin dan telah dipatenkan pada Desember 2004 dan diberi nama
Prialt (ziconotide intratechal infusion).
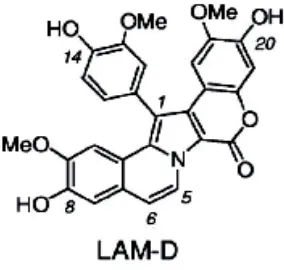
Facompre et al. (2003) melaporkan telah mengidentifikasi dan
mengkarakterisasi potensi inhibitor topoisomerase I yang baru yang diberi nama
lamellarin D (Gambar 3). Lamellarin D (LAM-D) diisolasi dari moluska laut
subklas Prosobranchia yaitu Lamellaria sp dan merupakan senyawa alkaloid.
Alkaloid ini diketahui memiliki aktivitas terhadap sel lestari tumor yang resisten
terhadap berbagai obat dan sitotoksik yang sangat tinggi terhadap sel kanker
prostat.
Gambar 3 Struktur lamellarin D(Facompre et al. 2003).
2.3 Asam Amino
Asam amino merupakan komponen utama penyusun protein dan dibagi
dalam dua kelompok utama yaitu asam amino esensial dan nonesensial. Asam
amino esensial tidak dapat diproduksi oleh tubuh sehingga harus disuplai lewat
makanan, sedangkan asam amino nonesensial dapat diproduksi dalam tubuh.
Menurut Belitz dan Grosch (1999) asam amino dibedakan menjadi tiga
grup, yaitu (1) asam amino netral tidak bermuatan (glisin, serin, treonin, aspargin,
glutamin) dan asam amino yang mengandung sulfur (sistin,sistein dan metionin);
(2) asam amino dengan rantai samping asam (asam aspartat dan asam glutamat)
dan asam amino dengan rantai samping gugus alifatik (alanin, valin, leusin,
isoleusin dan prolin); (3) asam amino dengan rantai samping gugus aromatik
(fenilalanin, tirosin dan triptofan) dan asam amino dengan rantai samping basa
larut dalam air, namun tidak larut dalam pelarut organik. Menurut Lehninger
(1997), berdasarkan polaritasnya asam amino dibedakan menjadi tiga bagian,
yaitu asam amino hidrofilik (asam aspartat, asam glutamat, asparagin, glutamin,
lisin, arginin dan histidin), asam amino hidrofobik (fenilalanin, leusin, isoleusin,
metionin, valin dan triptofan), dan asam amino antara (prolin, treonin, serin,
sistin, alanin, glisin dan tirosin). Asam amino hidrofilik adalah asam amino yang
pada struktur protein globular terdapat di permukaan luar. Asam amino yang
disebut hidrofobik adalah asam amino yang terdapat di bagian dalam struktur
pada struktur globular, sedangkan yang disebut asam amino dengan polaritas
antara adalah asam amino yang dapat ditemukan baik pada bagian luar maupun
dalam pada struktur protein globular (Lehninger 1997).
Dari sekitar 20 jenis asam amino yang dibutuhkan tubuh, sembilan
diantaranya disebut sebagai asam amino esensial atau penting karena tubuh tidak
bisa membentuknya dan harus didapat dari makanan. Histidin penting untuk
pertumbuhan fisik dan mental yang sempurna dan dilaporkan dapat
menanggulangi penyakit rematik. Isoleusin penting bagi pertumbuhan bayi dan
keseimbangan nitrogen bagi orang dewasa. Leusin, penting untuk pertumbuhan.
Lisin dapat menolong menyembuhkan penyakit herpes kelamin. Metionin
diperlukan bagi produksi sulfur, menjaga kenormalan metabolisme, dan
merangsang serotonin sehingga dapat menghilangkan kantuk. Metionin juga
berperan sebagai antioksidan, membantu menguraikan lemak dan mengurangi
kemorosotan otot serta baik untuk kesehatan kulit dan kuku. Fenilalanin
dibutuhkan untuk produksi tirosin yang penting bagi pertumbuhan. Treonin dan
valin, menyeimbangkan nitrogen, triptofan untuk produksi serotonin pada otak
(Anonim 2004). Asam amino yang berperan sebagai antioksidan adalah asam
amino metionin, triptofan, histidin, sistein, sistin dan arginin.
Asam amino yang lain disebut sebagai nonesensial karena tubuh dapat
membentuknya. Fungsinya antara lain untuk menjaga fungsi ginjal dan fungsi
seksual pria seperti arginin, berguna menjaga fungsi hati seperti alanin,
pengaturan tekanan darah dan fungsi seksual pria. Asam glutamat dan kolin
menjaga fungsi kesehatan otak. Prolin untuk pembentukan kolagen dan
9
2.4 Ekstraksi Bahan Aktif
Ekstraksi merupakan salah satu cara pemisahan satu atau lebih komponen
dari suatu bahan yang merupakan sumber komponen tersebut. Komponen yang
dipisahkan dengan ekstraksi dapat berupa padatan atau cairan. Metode ekstraksi
yang digunakan tergantung pada beberapa faktor antara lain (1) tujuan dilakukan
ekstraksi, (2) skala ekstraksi, (3) sifat-sifat komponen yang akan diekstrak, dan
(4) sifat-sifat pelarut yang akan digunakan. Ada beberapa metode umum ekstraksi
yang dapat dilakukan yaitu ekstraksi dengan pelarut, distilasi, supercritical fluid
extraction (SFE), pengepresan mekanik dan sublimasi. Diantara metode-metode
yang telah diaplikasikan, metode yang banyak digunakan adalah distilasi dan
ekstraksi menggunakan pelarut (Hougton dan Raman 1998).
Prinsip metode ekstraksi menggunakan pelarut organik adalah bahan yang
akan diekstrak kontak langsung dengan pelarut pada waktu tertentu, kemudian
diikuti dengan pemisahan dari bahan yang telah diekstrak (Hougton dan Raman
1998).
Metode ekstraksi tergantung pada polaritas senyawa yang akan diekstrak.
Suatu senyawa menunjukkan kelarutan yang berbeda-beda dalam pelarut yang
berbeda. Hasil ekstraksi yang diperoleh akan tergantung pada kandungan
komponen yang terdapat pada sampel dan jenis pelarut yang dipakai. Prinsip
kelarutan yang dipakai dalam metode ekstraksi ini adalah like dissolve like artinya
pelarut polar akan melarutkan senyawa polar, sedangkan pelarut nonpolar akan
melarutkan senyawa nonpolar (Khopkar 1990).
Hal yang perlu diperhatikan dalam pemilihan pelarut adalah selektivitas,
kemampuan untuk mengekstrak, toksisitas, kemudahan untuk diuapkan dan harga
pelarut. Ketaren (1986) menyatakan bahwa jenis dan mutu pelarut yang
digunakan sangat menentukan keberhasilan proses ekstraksi. Pelarut yang
digunakan harus memenuhi persyaratan sebagai berikut : harus dapat melarutkan
zat yang diinginkan, mempunyai titik didih yang cukup rendah, titik didihnya
seragam, murah, tidak toksik dan tidak mudah terbakar.
Menurut Suryandri (1981), semakin besar volume pelarut maka jumlah
bahan yang akan terekstrak akan semakin besar sampai larutan menjadi jenuh
pemisahan pelarut harus diperhatikan titik didihnya. Pelarut bertitik didih rendah
biasanya banyak hilang karena penguapan, sedangkan pelarut bertitik didih tinggi
baru dapat dipisahkan pada suhu tinggi (Sabel dan Warren 1973).
Secara umum ekstraksi bertingkat dilakukan berturut-turut dimulai dengan
pelarut nonpolar (kloroform atau heksana), lalu dengan pelarut yang kepolarannya
menengah (etil asetat), kemudian dengan pelarut polar (metanol atau etanol).
Dengan demikian akan diperoleh ekstrak awal (crude extract) yang mengandung
berturut-turut senyawa nonpolar, kepolaran menengah dan polar (Hostettmann et
al. 1997).
2.5 Kanker, Antikanker dan Uji Antikanker
Kanker adalah pertumbuhan jaringan yang baru sebagai akibat dari
proliferasi (pertumbuhan berlebihan) sel abnormal secara terus menerus yang
memiliki kemampuan untuk menyerang dan merusak jaringan lainnya. Kanker
digolongkan berdasarkan jaringan dan jenis sel asal : (1) Sarkoma, yang tumbuh
dari jaringan penyambung dan penyokong, seperti tulang, tulang rawan, saraf,
pembuluh darah, otot dan lemak; (2) Karsinoma, bentuk kanker yang paling
umum menyerang manusia, tumbuh dari jaringan epitelial (jaringan bersel yang
menutupi permukaan), seperti kulit dan lapisan rongga dan organ tubuh, dan
jaringan kelenjar, seperti jaringan payudara dan prostat. Karsinoma dengan
struktur berlapis-lapis yang menyerupai kulit disebut sebagai karsinoma sel
skuamosa (sel tanduk), sedangkan yang menyerupai jaringan kelenjar disebut
sebagai adenokarsinoma; (3) Leukemia dan limfoma, merupakan bentuk kanker
yang menyerang jaringan pembentuk darah dan dicirikan oleh pembesaran
kelenjar getah bening, penyerangan terhadap limpa dan sumsum tulang, dan
produksi sel darah putih yang belum matang secara berlebihan (Anonim 2006).
Menurut Mulyadi (1997) sel kanker mempunyai sistem enzim yang
berbeda yaitu jumlah dan macam enzim pada sel kanker lebih sedikit jika
dibandingkan dengan sel normal, dan enzim – enzim untuk pertumbuhan pada sel
kanker aktivitasnya lebih besar dibandingkan dengan sel normal. Dalam keadaan
normal, sel hanya akan membelah diri bila tubuh membutuhkannya seperti
mengganti sel yang rusak atau mati. Sebaliknya sel kanker akan membelah diri
11
Faktor-faktor penyebab kanker belum diketahui secara pasti. Pola makan
dan gaya hidup yang salah dapat memicu pertumbuhan sel kanker yang
meningkat. Selain itu, faktor seperti radiasi serta adanya virus disinyalir dapat
turut berkontribusi terhadap pertumbuhan sel kanker (Dalimartha 1999).
Antikanker adalah zat yang dapat menghambat atau membunuh sel kanker.
Penelitian untuk pengobatan penyakit kanker telah banyak dilakukan. Hasil
penelitian yang telah digunakan pada terapi kanker antara lain terapi radiasi,
pembedahan dan terapi dengan bahan kimia (kemoterapi). Terapi kanker dapat
dilakukan dengan satu macam terapi atau dikombinasikan. Kesulitan pada
kemoterapi terutama untuk menghasilkan dosis letal yang bersifat sitotoksik pada
sel tumor tapi tidak merusak sel normal (Mycek et al. 2000).
Akhir-akhir ini kemoterapi menjadi salah satu terobosan dalam
pengendalian kanker. Meskipun penemuan dan pemakaian kemoterapi menunjang
hasil yang bagus tetapi toksisitas dan efek sampingnya sangat besar (Siswandono
1993). Terapi kanker seperti kemoterapi maupun radiasi kerap membuat sel yang
sehat ikut terbunuh, sehingga daya tahan tubuh bisa melemah. Upaya pendukung
yang banyak dilakukan oleh penderita kanker adalah menggunakan obat-obatan
alami. Obat-obatan tersebut mempunyai kemampuan meningkatkan sistem imun.
Rivory (2002) menyatakan bahwa kerja obat anti antikanker dibagi dalam
beberapa mekanisme yaitu :
a) Merusak DNA secara langsung (agen pengkelat), melalui protein (misalkan
topoisomerase poison) dan kehilangan siklus basa (nukleusida analog).
b) Mengganggu sintesis kofaktor penting dan prekusor protein/DNA/RNA
(antimetabolit, asparginase).
c) Mengganggu struktur seluler dan proses (obat antimikrotubul seperti
docetaxel, paclitaxel dan vinca alkaloid)
d) Penghambatan pertumbuhan/penanda antikematian (inhibitor tirosin kinase
seperti imatinib mestylate, trastuzumab).
Mekanisme ini menyebabkan kematian sel-sel akut (nekrosis), kematian sel
terprogram (apoptosis), penghentian pertumbuhan atau diferensiasi.
Ada empat jenis uji daya antikanker suatu senyawa, yaitu prescreen test,
Prescreen digunakan untuk mengetahui apakah suatu senyawa merupakan
senyawa bioaktif. Uji ini harus memiliki kapasitas yang tinggi dengan biaya yang
rendah dan waktu yang cepat. Dalam screen test dipilih ekstrak untuk digunakan
pada secondary test, sedangkan monitor test berguna sebagai panduan pada
pemisahan ekstrak pekat melalui isolasi ekstrak murni sebagai senyawa bioaktif.
Uji ini harus cepat, murah, berkapasitas tinggi, dan mudah diperoleh. Secondary
test dilakukan untuk menguji ekstrak murni yang diperoleh pada beberapa model
dan kondisi untuk memilih ekstrak yang akan dikembangkan sebagai obat pada
terapi antikanker. Uji ini berkapasitas rendah, lambat dan mahal. Prescreen test
dilakukan untuk mendapatkan nilai LC50, yaitu konsentrasi yang dapat mematikan
50% hewan uji dalam waktu 24 jam. Uji yang paling sering dilakukan adalah uji
kematian larva udang (BSLT= brine shrimp lethality test).
Uji antikanker dapat dilakukan secara in vivo dan in vitro. Uji in-vivo
secara spesifik dapat dilakukan secara mekanik maupun seluler, untuk mencari
kemampuan sitotoksik, antimitotik dan antimetastatik. Uji ini juga dapat
dilakukan dengan melihat interaksinya dengan DNA (Suffnes dan Pezzuto 1991).
Salah satu uji yang didasarkan pada interaksi dengan DNA adalah dengan cara
melihat kemampuan senyawa uji untuk menghambat topoisomerase I dan II yang
digunakan pada replikasi DNA.
2.6 Topoisomerase dan Inhibitor Topoisomerase I
Topoisomerase adalah enzim yang mengatur perubahan topologi DNA
yang dilakukan dengan cara meningkatkan atau menurunkan jumlah pilinan pada
heliks ganda. Terdapat dua jenis topoisomerase yaitu topoisomerase I yang
membuat pilinan positif atau meningkatkan jumlah pilinan heliks, dan
topoisomerase II yang membuat pilinan negatif atau menurunkan pilinan heliks
ganda (Jusuf 2001). Lebih lanjut dijelaskan bahwa peningkatan atau penurunan
jumlah pilinan tersebut dilakukan topoisomerase dengan cara memotong rantai
fosfodiester antara dua nukleutida dari salah satu heliks ganda. Hengstler et al.
(2002) mengelompokkan enzim topoisomerase ke dalam dua klas utama yaitu
topoisomerase I yang berperan pada pemotongan DNA utas tunggal dan
13
Enzim DNA topoisomerase (topo) I dan II adalah target molekuler dari
beberapa zat antikanker yang potensial, dengan demikian inhibitor dari enzim ini
potensial untuk obat antikanker. Pertumbuhan tumor dapat dihambat dan
dijinakkan ke tahap dorman melalui pemblokiran proses angiogenesisnya.
Angiogenesis adalah proses terbentuknya pembuluh darah baru dari pembuluh
darah yang telah ada. Komponen antiangiogenesis mampu menurunkan laju
pertumbuhan tumor/kanker. Dengan dihambatnya aktivitas enzim DNA
topoisomerase oleh senyawa inhibitor, maka proses terjadinya ikatan antara enzim
dengan DNA sel kanker semakin lama. Hal ini menyebabkan terbentuknya
Protein Linked DNA Breaks (PLDB), akibatnya terjadi kerusakan DNA sel kanker
dan selanjutnya berpengaruh terhadap proses dalam sel khususnya proses
replikasi, yang diakhiri dengan kematian sel kanker (Hsiang 1989, Joseph 1989
diacu dalam Sukardiman et al. 2002).
Enzim topoisomerase adalah enzim yang berperan dalam proses replikasi,
transkripsi dan rekombinasi DNA dan juga proses proliferasi dan diferensiasi sel
normal dan sel kanker. Enzim ini merupakan target bahan bioaktif yang memiliki
aktivitas antikanker, karena dengan dihambatnya enzim DNA topoisomerase
maka proses dalam sel akan terhenti dan akhirnya akan terjadi kematian sel
tersebut (Andreas et al. 1995).
Aplikasi untuk pencarian bahan-bahan aktif antikanker dari alam dapat
menggunakan molekul target enzim DNA Topoisomerase. Enzim tersebut
digunakan sebagai molekul target, karena mempunyai fungsi cukup penting dalam
proses intraseluler dari sel kanker yang berperan dalam proses replikasi,
transkripsi, rekombinasi DNA dan proses proliferasi dari sel kanker (Pommier
1993). Dewasa ini telah banyak senyawa dari bahan alam yang telah diisolasi
yang bersifat antikanker dan memiliki molekul target enzim DNA topoisomerase
antara lain camptothecin dari tanaman Camptotheca acuminata (Famili
Nyssaceae), andriamycin, doxorubicin, mitoxantron dan etoposide VP-16),
Gambar 4 Struktur beberapa topoisomerase poison (Ammon dan Osheroff 1995).
Aktivitas inhibisi terhadap kerja dari enzim DNA topoisomerase sebagai
target obat antikanker melalui dua mekanisme yaitu penghambatan katalitik
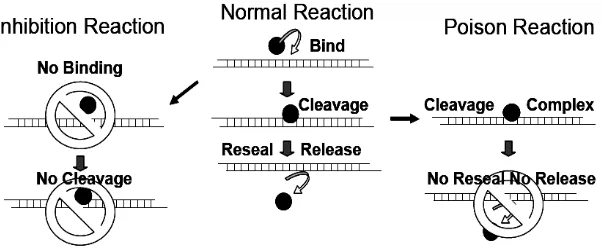
(catalytic inhibitor) dan poison (cleavable complex). Perbedaan mekanisme
keduanya ditunjukkan pada Gambar 5.
Gambar 5 Perbedaan antara inhibitor katalitik dan poison (Topogen 2006).
15
Pada Gambar 5 reaksi normal sekuen (diagram tengah) melibatkan
pengikatan DNA diikuti oleh pembelahan DNA (untai tunggal maupun ganda),
pelekatan kembali dan pelepasan enzim. Inhibitor (diagram kiri) memblokir tahap
pengikatan awal atau dengan kata lain mengganggu kemampuan enzim untuk
menggunakan DNA dalam pembelahan. Dalam hal ini, tidak ada relaksasi DNA
atau dekantanasi DNA (hanya topo 2) ketika aktivitas katalitik diblok oleh obat.
Topo poison (diagram kanan) bekerja pada tahap pembelahan yang menstabilkan
kompleks pembelahan dan menghambat tahap pelekatan kembali. Dengan kata
lain agen ini bertujuan “meracuni” reaksi melalui penstabilan pembelahan
intermediet dan pemanjangan umur dari kompleks pembelahan (normalnya sangat
pendek).
Inhibisi dari kerja topoisomerase mungkin melibatkan penghambatan
“konvensional” dimana aktivitas enzim dihambat atau diperlambat. Sebagai
contoh pengikatan inhibitor pada sisi aktif atau perubahan sifat pengikatan dari
enzim dengan substrat. Tipe penghambatan ini umumnya ditunjukkan sebagai
aktivitas penghambatan katalitik (relaksasi) (Webb dan Ebeler 2004).
2.7 Elektroforesis
Elektroforesis dengan gel agarosa merupakan metode yang sederhana dan
sangat efektif untuk memisahkan, mengidentifikasi dan memurnikan fragmen
DNA dengan panjang 0,5 hingga 25 kilo pasang basa (pb). Metode elektroforesis
ini meliputi tiga langkah : persiapan gel agarosa dengan konsentrasi agarosa yang
disesuaikan dengan ukuran DNA fragmen yang akan dipisahkan; DNA sampel
dimasukkan ke dalam sumur gel dan gel ditaruh di bak elektroforesis yang dialiri
listrik dengan tegangan dan waktu tertentu sehingga menghasilkan pemisahan
yang baik; gel direndam dalam etidium bromida atau etidium bromida yang telah
digunakan pada gel dan penyangga elektroforesis. Hasil elektroforesis ini dapat
dilihat langsung pada penyinaran dengan UV (Ausubel et al. 1990)
Menurut Muladno (2002) pada prinsipnya DNA dapat berintegrasi di
dalam gel dalam bentuk padat yang diletakkan dalam penyangga yang dialiri arus
listrik. Salah satu gel yang biasa digunakan adalah gel agarosa. Gel agarosa
penyangga sampai jernih. Larutan yang masih cair (dengan temperatur sekitar
60 oC) dituangkan ke dalam pencetak gel. Segera setelah itu, sisir ditempatkan
didekat tepian gel dan gel dibiarkan mengeras. Apabila telah mengeras, sisir
diangkat sehingga akan membentuk lubang-lubang yang digunakan untuk
menempatkan larutan DNA. Jika gel ditempatkan ke dalam bak elektroforesis
yang mengandung larutan penyangga dan bak tersebut dialiri listrik, molekul
DNA yang bermuatan negatif pada pH netral akan bergerak (bermigrasi) ke arah
positif (anoda). Kecepatan migrasi DNA ditentukan oleh beberapa faktor, salah
satunya adalah ukuran molekulnya. Migrasi molekul DNA berukuran besar lebih
lambat daripada migrasi molekul berukuran kecil.
2.8 Alkaloid dan Steroid 2.8.1 Alkaloid
Alkaloid adalah senyawa organik berbasis nitrogen yang banyak ditemui
pada tumbuhan tetapi juga dapat ditemui dalam jumlah yang sedikit pada
mikroorganisme dan hewan. Nama alkaloid berarti menyerupai alkali, tingkat
kebasaannya bergantung pada struktur molekul serta keberadaan dan lokasi gugus
fungsinya (Dewick 2001 diacu dalam Putri 2004). Menurut Suradikusumah
(1989) alkaloid umumnya dinyatakan sebagai senyawa basa yang mengandung
satu atau lebih atom nitrogen yang merupakan bagian dari sistem siklik. Atom
nitrogennya hampir selalu dalam bentuk nitro atau diazo. Subtituen oksigen
umumnya dalam bentuk gugus fenol, metoksil atau metilendioksida.
Klasifikasi alkaloid atas dasar struktur molekul sulit dilakukan, hal ini
dikarenakan terlalu banyak struktur yang ada. Penggolongan lain berdasarkan
jumlah cincin nitrogen dan biosintesis yang terjadi dibagi atas tiga golongan yaitu
(1) alkaloid sejati, (2) protoalkaloid dan (3) pseudoalkaloid (Pelletier 1983;
Bruneton 1993).
Alkaloid sejati merupakan senyawa nitrogen yang memiliki struktur yang
kompleks dan bersifat basa. Atom nitrogen yang terdapat di dalam struktur
merupakan bagian dari sistem heterosiklik yang menentukan aktivitas
farmakologis. Untuk alkaloid jenis ini terbentuk secara biosintesis dari asam
17
Protoalkaloid merupakan senyawa amina sederhana yang memiliki atom
nitrogen bukan merupakan bagian dari sistem heterosiklik. Senyawa ini juga
bersifat basa dan dapat terbentuk secara in vivo dari asam amino. Senyawa yang
termasuk dalam golongan ini antara lain adalah senyawa amina sederhana seperti
serotonin dan betain.
Pseudoalkaloid memiliki atom nitrogen yang merupakan bagian dari
sistem heterosiklik tetapi bukan merupakan turunan dari asam amino.
Senyawa-senyawa yang termasuk dalam golongan ini antara lain Senyawa-senyawa isoprenoid,
senyawa alkaloid terpenoid dan senyawa nitrogen heterosiklik yang muncul dari
metabolisme asetat.
Alkaloid memiliki bobot molekul antara 100-900. Umumnya alkaloid
tidak mengandung atom oksigen, berbentuk cair pada suhu kamar, sedangkan
alkaloid yang memiliki atom oksigen berbentuk kristal padat (Harborne 1987).
Hampir seluruh senyawa yang berbentuk kristal memiliki titik leleh dibawah 200
o
C. Alkaloid umumnya tidak berwarna, tetapi alkaloid yang lebih kompleks
terutama yang mengandung gugus aromatis akan berwarna (Robinson 1995).
Alkaloid lebih mudah diekstrak oleh pelarut polar seperti air yang
diasamkan, atau pada kondisi basa menggunakan natrium karbonat dan basa
bebas. Filtrat yang diperoleh selanjutnya diekstrak dengan pelarut organik seperti
eter dan pelarut yang bersifat polar (Maldoni 1991 diacu dalam Robinson 1995).
Umumnya alkaloid dapat diendapkan dengan pereaksi Meyer (kalium raksa II
iodida). Pereaksi Wagner (iodium dalam kalium iodida), asam silikotungstat 5%,
asam tanat 5%, pereaksi Dragendorff (kalium tetraiodobismutat), iodopainat dan
larutan asam pikrat jenuh juga dapat digunakan untuk mengetahui keberadaan
senyawa alkaloid.
2.8.2 Steroid
Steroid adalah salah satu jenis asam lemak yang merupakan turunan
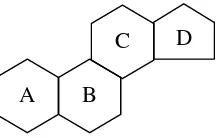
perihidroksiklopentanofenantrena, yang terdiri atas 3 cincin sikloheksana terpadu
seperti bentuk fenantrena (cincin A, B dan C) dan sebuah cincin siklopentana
A B
[image:33.612.263.372.74.143.2]C D
Gambar 6 Kerangka inti steroid (Litwack dan Schmidt 2002).
Menurut Fahi et al. (2005) sterol atau steroid alkohol merupakan bagian dari
steroid dengan group hidroksil pada posisi 3 dari cincin A. Sterol dari tumbuhan
disebut fitosterol dan sterol dari hewan disebut zoosterol. Zoosterol yang utama
adalah kolesterol dan beberapa hormon steroid. Sedangkan Poejiadi dan
Supriyanti (2006) menggolongkan senyawa steroid ke dalam kolesterol, 7
dehidrokolesterol, ergosterol, asam-asam empedu dan hormon steroid.
Menurut Linder (2006) kolesterol adalah senyawa golongan steroid dan
hanya terdapat dalam lemak hewan, mempunyai peranan penting sebagai
penyusun plasma sel, lipoprotein plasma dan merupakan prekusor pembentukan
asam empedu, hormon-hormon dan vitamin D. Selanjutnya Poejiadi dan Suryanti
(2006) menyatakan bahwa senyawa 7-dehidrokolesterol terdapat di bawah kulit
dan hanya berbeda sedikit dari kolesterol. Sedangkan ergosterol mempunyai
struktur inti sama dengan 7-dehidrokolesterol, tetapi berbeda pada rantai samping
(Gambar 7). Senyawa 7-dehidrokolesterol dan ergosterol dapat membentuk
vitamin D bila dikenai sinar ultra violet sehingga kedua steroid ini disebut juga
provitamin D.
[image:33.612.135.480.516.647.2]19
Evans (2002) menyatakan bahwa asam empedu dibuat dalam hati dan
dikumpulkan dalam empedu yang merupakan hasil degradasi kolesterol menjadi
C24-karboksil. Asam empedu utama yang dihasilkan hati yaitu asam kholat dan
asam khenodeoksikholat. Sedangkan asam empedu yang tidak dihasilkan hati,
namun dalam usus dengan bantuan mikroba yaitu asam deoksikholat (dari asam
kholat) dan asam lithokholat (dari asam khenodeoksikholat).
Davlin (1993) menyatakan bahwa hormon steroid dibentuk dari jaringan
tertentu di dalam tubuh dan dibagi ke dalam dua klas yaitu hormon adrenal dan
hormon seks (testosteron, estrogen dan progesteron). Antara ketiga hormon seks
ini saling berhubungan, testosteron berperan dalam pengaturan perilaku seksual
jantan, sedangkan estrogen dan progesteron berperan dalam pengaturan perilaku
seksual betina.
Sterol dari organisma laut terdiri atas campuran yang sangat kompleks.
Lebih dari 200 monohidroksi sterol telah dilaporkan dan lebih dari 70 sterol
berasal dari satu spesies organisme laut (Riccio et al. 1993). Sedangkan Menurut
Kanazawa (2001) komposisi sterol dari hewan invertebrata laut telah
menunjukkan campuran kompleks yang mencakup banyak jenis sterol baru
dengan inti steroid yang tidak biasa atau rantai samping yang tidak konvensional.
Sterol dapat ditemukan baik sebagai sterol bebas (lanosterol, vitamin D3/
cholecalciferol, desmosterol/24-dehydrocholesterol, stigmasterol, fukosterol), sterol
ester (cholesterol glucuronide), teralkilasi (steryl alkil ethers), sterol sulfat
(squalamine, annosterol) atau separuh glikosida (steryl glycosides) yang dapat
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Nopember 2006 sampai dengan Juni 2007 bertempat di Laboratorium Bioteknologi Hasil Perairan, Departemen Teknologi Hasil Perairan, FPIK. Analisis proksimat di lakukan di Laboratorium Kimia Pangan Departemen Ilmu dan Teknologi Pangan dan analisis asam amino dilakukan di Laboratorium Kimia Pangan Balai Besar Penelitian dan Pengembangan Pascapanen Pertanian, Cimanggu Bogor.
3.2. Bahan dan Peralatan 3.2.1 Bahan
Bahan baku yaitu Kablang (Nerita albicilla) kering diperoleh dari Desa Sather Kabupaten Maluku Tenggara, Propinsi Maluku. Bahan kimia untuk ekstraksi yaitu heksana, etil asetat dan metanol. Bahan untuk uji inhibitor topoisomerase I yaitu drug screening kit topoisomerase I dari TopoGen (Port Orange/USA) yang tersedia di Laboratorium Bioteknologi Hasil Perairan. Bahan untuk uji proksimat dan asam amino antara lain H2SO4, HCl, KOH, NaOH, Na2S2O3, H3BO3, asetonitril 60%, asam amino standar. Bahan untuk karakterisasi ekstrak aktif inhibitor topoisomerase I antara lain pereaksi ninhidrin, Molish, Lieberman Burchard, NH4OH, pereaksi Dragendorff, Meyer dan Wagner. Bahan untuk isolasi senyawa target antara lain CHCl3, dietil ater, NaHCO3, NaCl, Na2SO4.
3.2.2. Peralatan
21
3.3. Prosedur Penelitian
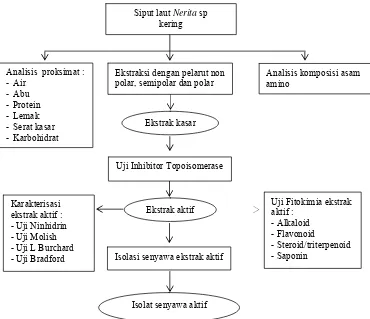
[image:36.612.135.505.227.546.2]Penelitian ini meliputi: penentuan kadar proksimat dan komposisi asam amino dari siput laut kering, ekstraksi bahan aktif, pengujian inhibitor topoisomerase I, karakterisasi ekstrak aktif inhibitor topoisomerase I untuk mengetahui kelompok senyawa yang terdapat pada ekstrak aktif, isolasi senyawa target dengan metode spesifik. Gambar 8 menunjukkan diagram alir penelitian komposisi kimia dan aktivitas inhibitor topoisomerase dari Kablang.
Gambar 8 Diagram alir penelitian komposisi kimia dan aktivitas inhibitor topoisomerase I dari Kablang (Nerita albicilla)
3.3.1 Penentuan kadar proksimat dan asam amino Kablang 3.3.1.1 Analisis proksimat Kablang (Nerita albicilla)
Analisis proksimat yang dilakukan meliputi penentuan kadar air, abu, protein, lemak, serat kasar dan karbohidrat.
Analisis proksimat : - Air
- Abu - Protein - Lemak - Serat kasar - Karbohidrat
Siput laut Nerita sp kering
Analisis komposisi asam amino
Uji Inhibitor Topoisomerase
Isolasi senyawa ekstrak aktif
Isolat senyawa aktif Ekstraksi dengan pelarut non polar, semipolar dan polar
Ekstrak aktif Ekstrak kasar
Karakterisasi ekstrak aktif : - Uji Ninhidrin - Uji Molish - Uji L Burchard - Uji Bradford
Uji Fitokimia ekstrak aktif :
- Alkaloid - Flavonoid
Analisis kadar air (AOAC 1995)
Cawan kosong yang digunakan dikeringkan dalam oven selama 15 menit atau sampai diperoleh berat tetap, kemudian didinginkan dalam desikator selama 30 menit dan ditimbang. Sampel sebanyak 2 g ditimbang dan diletakkan dalam cawan kemudian dipanaskan dalam oven sampai berat tetap pada suhu 105 – 110 o
C. Cawan kemudian didinginkan dalam desikator dan setelah dingin ditimbang kembali. Persentase kadar air dapat dihitung dengan rumus sebagai berikut :
Keterangan :
B = berat sampel (g)
B1 = berat (sampel + cawan) sebelum dikeringkan (g) B2 = berat (sampel + cawan) setelah dikeringkan (g)
Analisis kadar abu (AOAC 1995)
Pengukuran kadar abu ditentukan dengan gravimetri. Cawan porselin dipanaskan dalam oven kemudian didinginkan dalam desikator dan ditimbang. Sebanyak 3 – 5 g sampel dimasukkan dalam cawan porselin lalu dibakar sampai tidak berasap lagi lalu diabukan pada suhu 600 oC sampai berwarna putih (semua contoh menjadi abu) dan berat konstan. Setelah itu didinginkan dalam desikator dan ditimbang.
Perhitungan kadar abu adalah sebagai berikut :
Analisis kadar protein (AOAC 1995)
Ditimbang sejumlah kecil contoh (1 - 2 g) lalu dimasukkan ke dalam labu Kjeldahl. Setelah itu ditambahkan 1,9 g K2SO4: 40 mg HgO dan 2,0 ± 0,1 ml H2SO4 dan kemudian contoh dididihkan sampai cairan jernih. Larutan jernih ini lalu dipindahkan ke dalam alat destilasi. Labu Kjeldahl dicuci dengan air (1 – 2) ml kemudian air cucian dimasukkan ke dalam alat destilasi dan ditambahkan 8 – 10 ml larutan NaOH-Na2S2O3. Di bawah kondensor diletakkan erlenmeyer yang berisi 5 ml larutan H3BO3 dan 2 - 4 tetes indikator (campuran 2 bagian metil merah 0,2 % dan
% 100 x B B B (%) air
Kadar = 1− 2
23
1 bagian metilen biru 0,2 % dalam alkohol). Ujung tabung kondensor harus terendam dalam larutan H3BO3. Setelah itu isi erlenmeyer diencerkan sampai 50 ml dan dititrasi dengan HCl 0,02 N sampai terjadi perubahan warna menjadi abu-abu. Proses yang sama dilakukan terhadap blanko. Kadar nitrogen ditentukan sebagai berikut :
% Protein = % N x 6,25 Keterangan:
14,007 = berat atom Nitrogen
6,25 = faktor konversi protein-nitrogen untuk ikan dan produk sampingannya
Analisis kadar lemak (AOAC 1995)
Metode yang digunakan dalam analisis lemak adalah metode ekstraksi soxhlet. Pertama kali labu lemak yang akan digunakan dikeringkan di dalam oven, kemudian didinginkan dalam desikator dan ditimbang beratnya. Contoh sebanyak 5 g dibungkus dengan kertas saring, setelah itu kertas saring yang berisi contoh tersebut dimasukkan dalam alat ekstraksi soxhlet. Alat kondensor diletakkan di atasnya dan labu lemak diletakkan di bawahnya. Pelarut heksana dimasukkan ke dalam labu lemak secukupnya. Selanjutnya dilakukan refluks selama minimal 5 jam sampai pelarut yang turun kembali ke dalam labu lemak berwarna jernih.
Pelarut yang ada dalam labu lemak didestilasi, dan pelarut ditampung kembali. Labu lemak yang berisi lemak hasil ekstraksi kemudian dipanaskan di dalam oven pada suhu 105 oC hingga mencapai berat tetap dan setelah itu didinginkan dalam desikator. Selanjutnya labu beserta lemak didalamnya ditimbang dan berat lemak dapat diketahui. Kadar lemak ditentukan sebagai berikut : 100% x (g) sampel berat (g) lemak berat (%) lemak Kadar =
Analisis serat kasar (AOAC 1995)
Sebanyak 1 g sampel kering dilarutkan dengan 100 ml H2SO4 1,25%, dipanaskan hingga mendidih lalu didestruksi selam 30 menit. Selanjutnya larutan disaring menggunakan kertas saring dengan bantuan corong Buchner. Residu hasil saringan dibilas dengan 20-30 ml air mendidih dan dengan 25 ml air
mg) ( sampel berat 100% x 14,007 x HCl N x blanko) HCl ml sampel ml ( (%)
sebanyak 3 kali. Residu didestruksi kembali dengan 100 ml NaOH 1,25% selama 30 menit. Larutan disaring dengan cara seperti di atas dan dibilas berturut-turut dengan 25 ml H2SO4 1,25% mendidih, 2,5 ml air sebanyak tiga kali dan 25 ml alkohol. Residu beserta kertas saring dipindahkan ke cawan porselin dan dikeringkan dalam oven 130 °C selama 2 jam. Setelah dingin residu beserta
cawan porselin ditimbang (A), lalu dimasukkan dalam tanur 600 °C selama 30 menit, didinginkan dan ditimbang kembali (B). Kadar serat kasar ditentukan sebagai berikut:
100% x W2
W1 -W3 (%) kasar serat
Kadar =
Keterangan :
W1 = bobot residu setelah dibakar dalam tanur = B – (bobot cawan) ; B : bobot residu + cawan W2 = berat contoh (gram)
W3 = bobot residu sebelum dibakar dalam tanur
= A – (bobot kertas saring+cawan); A: bobot residu+kertas saring+cawan.
Analisis kadar karbohidrat (Apriyantono et al. 1989)
Perhitungan kadar karbohidrat dilakukan menggunakan metode by difference, yaitu pengurangan 100 % dengan jumlah dari hasil analisis kadar air, kadar abu, kadar protein, kadar lemak dan serat kasar). Perhitungannya adalah sebagai berikut:
3.3.1.2 Analisis asam amino (AOAC 1995)
Komposisi asam amino ditentukan dengan menggunakan High Performance Liquid Chromatography (HPLC). Sebelum dipakai, perangkat HPLC harus dibilas dulu dengan eluen yang akan digunakan selama 2-3 jam. Begitu pula dengan syringe yang akan digunakan harus dibilas dengan akuades. Analisis asam amino dengan menggunakan HPLC terdiri atas 4 tahap, yaitu: (1) tahap pembuatan hidrolisat protein; (2) tahap pengeringan; (3) tahap derivatisasi; (4) tahap injeksi serta analisis asam amino.
25
(1) Tahap pembuatan hidrolisat protein
Untuk preparasi sampel yaitu tahap pembuatan hidrolisat protein, sampel ditimbang sebanyak 0,1 g dan dihancurkan. Sampel yang telah hancur ditambah dengan HCl 6 N sebanyak 5-10 ml yang kemudian dipanaskan dalam oven pada suhu 100 oC selama 24 jam. Hal ini dilakukan untuk menghilangkan gas atau udara yang ada pada sampel agar tidak mengganggu kromatogram yang dihasilkan. Setelah pemanasan selesai, hidrolisat protein disaring dengan menggunakan milipore berukuran 45 mikron.
(2) Tahap pengeringan
Hasil saringan diambil sebanyak 10 µl dan ditambah dengan 30 µl larutan pengering. Larutan pengering dibuat dari campuran antara metanol, natrium asetat, dan trietilamin dengan perbandingan 2:2:1. Setelah ditambahkan larutan pengering, dilakukan pengeringan dengan pompa vakum untuk mempercepat proses dan mencegah oksidasi.
(3) Tahap derivatisasi
Larutan derivatisasi sebanyak 30 µl ditambahkan pada hasil pengeringan. Larutan derivatisasi dibuat dari campuran antara larutan metanol, pikoiodotiosianat, dan trimetilamin dengan perbandingan 3:3:4. Proses derivatisasi dilakukan agar detektor mudah untuk mendeteksi senyawa yang ada pada sampel. Selanjutnya dilakukan pengenceran dengan cara menambahkan 10 ml asetonitril 60% dan natrium asetat 1 M lalu dibiarkan selama 20 menit. Hasil pengenceran disaring kembali dengan menggunakan milipore berukuran 0,45 µm.
(4) Injeksi ke HPLC
Hasil saringan diambil sebanyak 20 µl untuk diinjeksikan ke dalam HPLC. Untuk perhitungan konsentrasi asam amino pada bahan, dilakukan pembuatan kromatogram standar dengan menggunakan asam amino standar yang telah siap pakai yang mengalami perlakuan yang sama dengan sampel.
Kondisi alat HPLC saat berlangsungnya analisis asam amino: Temperatur Kolom : 38 oC
Jenis kolom : Pico tag 3.9 x 150 nm column Kecepatan alir eluen : 1 ml/menit
Program : Gradien
Fase gerak : Asetonitril 60 % dan Natrium asetat 1 M 40 % Detektor : UV/ 254 nm
Merk : Waters
Kandungan asam amino pada bahan dapat dihitung dengan rumus yaitu presentase asam amino dalam 100 g sampel :
luas area sampel x 2,5 mol/ml x 5 ml x BMA x 100 luas area standar
Asam amino (%) =
Bobot sampel (0,25 g)
Keterangan :
BMA = berat molekul asam amino
3.3.2 Ekstraksi bahan aktif Kablang (Nerita albicilla)
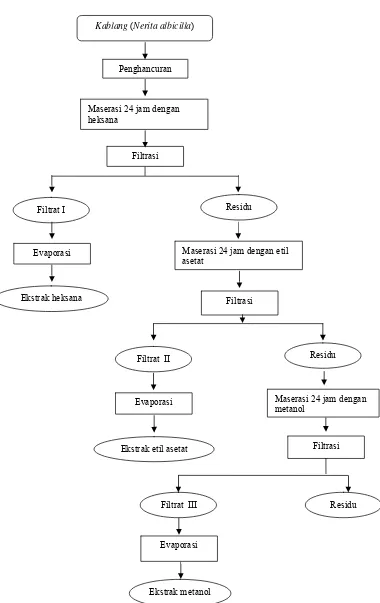
Metode ekstraksi bahan aktif yang digunakan adalah metode bertingkat. Pelarut yang digunakan adalah heksana sebagai pelarut nonpolar, etil asetat sebagai pelarut semipolar dan metanol sebagai pelarut polar. Pekerjaan ekstraksi bahan aktif Kablang dimulai dari penghalusan sampel yang telah kering dengan blender. Diagam alir proses ekstraksi bahan aktif Kablang dapat dilihat pada Gambar 9.
27
Gambar 9 Diagam alir proses ekstraksi bahan aktif Kablang
Penghancuran
Maserasi 24 jam dengan heksana
Filtrasi
Filtrat I Residu
Evaporasi
Ekstrak heksana
Maserasi 24 jam dengan etil asetat
Filtrasi
Filtrat II Residu
Evaporasi
Filtrasi Ekstrak etil asetat
Filtrat III Residu
Evaporasi
Ekstrak metanol
Maserasi 24 jam dengan metanol
Masing-masing filtrat yang dihasilkan dievaporasi dengan suhu yang sesuai dengan pelarut yang digunakan sampai terbentuk ekstrak yang berupa pasta, selanjutnya ekstrak dari masing-masing pelarut disebut ekstrak heksana, ekstrak etil asetat dan ekstrak metanol. Masing-masing ekstrak dikerok dan dimasukkan ke dalam botol sampel, kemudian disimpan pada suhu 4 °C. Selanjutnya ketiga ekstrak tersebut dicuci untuk membersihkan ekstrak dari pengotor dengan cara melarutkan dalam pelarut masing-masing dan didiamkan selama semalam di lemari es. Bagian yang terlarut dievaporasi untuk menguapkan pelarutnya. Bila sudah tidak terbentuk endapan maka ekstrak disebut ekstrak bersih.
3.3.3 Uji aktivitas inhibitor topoisomerase I (TopoGen 2006)
Uji inhibisi enzim DNA topoisomerase dari ekstrak dan fraksi-fraksi dengan metode elektroforesis. Substrat yang digunakan adalah DNA plasmid superkoil 25 μg dalam 100 μl buffer TAE (tris base-glacial acetic acid-EDTA) yang terdiri dari 0,25 μg/μl TE (Tris HCl-EDTA) : 10 mM Tris-HCl (pH 7,5), 1 mM etilen diamin tetra asetat (EDTA), kemudian ditambah 3 μl enzim DNA topoisomerase I. Volume reaksi akhir menjadi 20 μl. Penambahan dilakukan secara berurutan, yang terakhir ditambahkan adalah enzim topoisomerase, selanjutnya aquades ditambahkan untuk mencapai volume 20 μl.
29
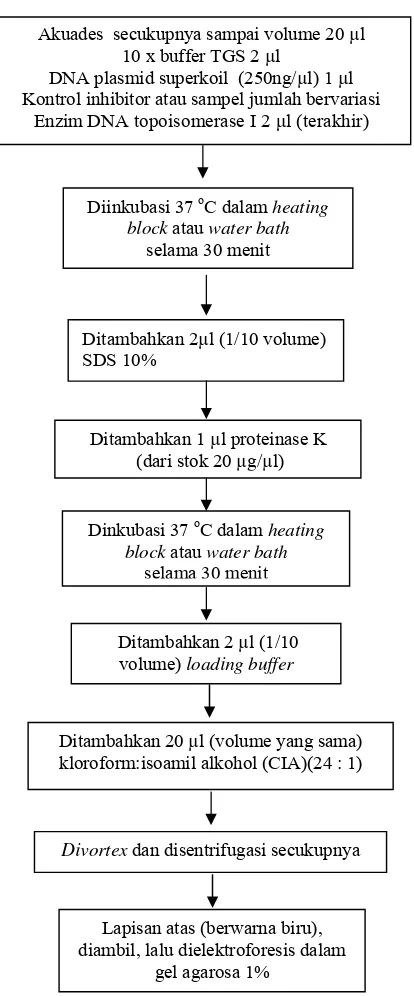
[image:44.612.208.415.177.675.2]Screening Kit topoGen. Kontrol positif inhibitor topoisomerase I adalah Camptothecin. Selain untuk sampel disertakan juga reaksi yang berfungsi sebagai kontrol (Lampiran 6). Gambar 10 menunjukkan tahapan dalam uji aktivitas inhibitor topoisomerase I.
Gambar 10 Tahapan dalam uji inhibitor topoisomerase I.
Diinkubasi 37 oC dalam heating block atau water bath
selama 30 menit
Ditambahkan 2µl (1/10 volume) SDS 10%
Ditambahkan 1 µl proteinase K (dari stok 20 µg/µl)
Dinkubasi 37 oC dalam heating block atau water bath
selama 30 menit
Ditambahkan 2 µl (1/10 volume) loading buffer
Ditambahkan 20 µl (volume yang sama) kloroform:isoamil alkohol (CIA)(24 : 1)
Divortex dan disentrifugasi secukupnya
Lapisan atas (berwarna biru), diambil, lalu dielektroforesis dalam
gel agarosa 1%
Akuades secukupnya sampai volume 20 µl 10 x buffer TGS 2 µl
DNA plasmid superkoil (250ng/µl) 1 µl Kontrol inhibitor atau sampel jumlah bervariasi
3.3.4 Karakterisasi ekstrak aktif inhibitor topoisomerase I
Tujuan karakterisasi adalah untuk mengetahui kelompok senyawa yang terdapat pada ekstrak aktif inhibitor topoisomerase I. Uji yang dilakukan adalah Ninhidrin, Molish, Lieberman Burchard dan Bradford (Bintang 1999). Sebanyak 0,1 g ekstrak dilarutkan dalam pelarut masing-masing. Ekstrak heksana dilarutkan dalam 5 ml heksana, ekstrak etil asetat dilarutkan dalam 5 ml etil asetat dan ekstrak metanol dilarutkan dalam 5 ml metanol.
Uji Ninhidrin
Uji ninhidrin dilakukan untuk menentukan adanya asam amino bebas dalam suatu bahan. Ninhidrin bereaksi dengan gugus amino pada asam amino bebas membentuk senyawa berwarna ungu, sedangkan dengan prolin dan hidroksiprolin ninhidrin berwarna kuning. Cara pengujian adalah sebagai berikut : ekstrak kasar Kablang 1 ml dalam tabung reaksi ditambah larutan ninhidrin 1 (satu) ml, lalu dipanaskan dalam penangas air mendidih selama lima menit. Bila terlihat warna ungu berarti positif. Uji ini dilakukan secara duplo.
Uji Molish
Uji ini adalah uji umum untuk menentukan adanya karbohidrat dalam suatu bahan. Karbohidrat akan dipecah oleh asam sulfat pekat menjadi gugus furfural yang akan bereaksi dengan sulfonat alfa-naftol membentuk senyawa berwarna ungu. Pereaksi molish terdiri atas alfa-naftol 5% dalam etanol 95% yang selalu dibuat segar. Uji ini dilakukan secara duplo. Cara pengujiannya dalam 1 ml ekstrak dibubuhi 2 tetes pereaksi molish lalu ditambahkan 1 ml asam sulfat pekat melalui dinding tabung secara hati-hati. Bila terbentuk lapisan berwarna ungu, berarti positif mengandung karbohidrat. Bila tidak ada karbohidrat akan berwarna hijau.
Uji Lieberman Burchard
31
menit. Bila terbentuk warna biru, berarti positif menunjukkan adanya steroid. Uji ini dikerjakan secara duplo.
Uji Bradford
Uji ini untuk mengetahui adanya protein dalam suatu bahan. Uji Bradford menggunakan pereaksi coomassie blue yang terdapat dalam reagen bradford. Coomassie blue tersebut mengikat protein membentuk kompleks berwarna biru.
Ekstrak 0,1 ml ditambah dengan 1 ml pereaksi Bradford. Tabung ditutup rapat dengan parafilm dan dikocok dengan cara membalikkan tabung perlahan-lahan beberapa kali. Jika menghasilkan warna biru cerah berarti positif mengandung protein. Kemudian didiamkan selama lima menit atau paling lama satu jam. Bila terbentuk warna biru, berarti positif mengandung protein.
Uji alkaloid
Uji ini untuk mengetahui adanya alkaloid dalam suatu bahan dengan menggunakan pereaksi logam berat. Pereaksi didasarkan pada kesanggupan alkaloid untuk bergabung dengan logam yang memiliki berat atom tinggi seperti merkuri, bismut dan iod. Ion logam pada senyawa pereaksi cenderung berikatan koordinasi dengan nitrogen (ligan) membentuk senyawa komplek yang menyebabkan terjadi perubahan warna dan terbentuknya endapan. Sebanyak 1 g ekstrak dilarutkan dengan 10 ml kloroform dan beberapa tetes NH4OH kemudian disaring ke dalam tabung reaksi bertutup. Ekstrak kloroform dalam tabung reaksi dikocok dengan 10 tetes H2SO4 2 M dan lapisan asamnya (bagian atas) dipisahkan ke dalam tabung reaksi yang lain. Lapisan asam ini diteteskan pada papan uji (spot plate) dan ditambahkan pereaksi Dragendorf KBiI4, Meyer K2(HgI4) dan Wagner KI(I2) yang akan menimbulkan endapan dengan warna berturut-turut merah jingga, putih dan coklat menunjukkan alkaloid positif.
Uji saponin
Uji flavonoid dan hidrokuinon
Uji flavonoid dan fenolik hidrokuinon dilakukan dengan prosedur sebanyak 1 g contoh ditambah metanol 30% sampai terendam lalu dipanaskan. Selanjutnya dilakukan penyaringan dan filtrat yang diperoleh ditaruh kedalam spot plate (papan uji) dan kemudian ditambahkan NaOH 10% (b/v) atau H2SO4 pekat. Terbentuknya warna merah akibat penambahan H2SO4 menunjukkan adanya flavonoid dan fenolik hidrokuinon ditandai dengan terbentuknya warna merah karena penambahan NaOH.
Uji triterpenoid dan steroid
Uji Liebermann Burchard dilakukan berdasarkan asetilasi 3 β hidroksi oleh
asam anhidrida dalam H2SO4. Ester asetil 3 β hidroksi sterol yang mengandung
ikatan ganda didalam asam akan mengalami epimerisasi menjadi bentuk 3α dan reaksi eliminasi yang menimbulkan produk berwarna. Uji triterpenoid ditandai dengan warna ungu atau merah, sedangkan steroid warna hijau atau biru. Sebanyak 2 g ekstrak ditambah 25 ml etanol 30% dipanaskan (50 oC) dan disaring, filtratnya diuapkan kemudian ditambah eter. Lapisan eter dipipet dan diujikan pada spot plate dengan menambahkan pereaksi Liebermen Burchard (3 tetes asam asetat anhidrat dan 1 tetes H2SO4 pekat) kemudian diamati warna yang terbentuk.
3.3.5 Isolasi senyawa target dengan metode spesifik
Isolasi senyawa target dengan metode spesifik dimaksudkan untuk memperoleh senyawa yang terdapat pada ekstrak aktif inhibitor topoisomerase I. Metode spesifik yang dimaksud adalah ekstraksi alkaloid dan steroid.
Ekstraksi alkaloid
33
Gambar 11 Bagan alir ekstraksi alkaloid (Harborne 1987).
Ekstraksi steroid
Ekstraksi setroid mengacu pada Bahti et al. (1983) yang dikutip oleh Heryani (2002). Penghilangan lemak dilakukan dengan cara partisi dengan
Ekstrak
Direndam dengan metanol air (4:1) (24 jam)
Filtrat diuapkan
(sampai 1/10 volume awal, suhu 40 oC)
Diasamkan (pH 3-4) dengan H2SO4 2M
Diekstraksi dengan kloroform (3x)
diuapkan
Dibasakan sampai pH 10 (+NH4OH)
Diekstraksi dengan CHCl 3-MeOH (3:1) (2x)
Diuapkan lapisan CHCl3-MeOH
Diekstraksi dengan MeOH Ekstrak Polar
Pertengahan (EPP)
Lapisan kloroform Lapisan air
Ekstrak Basa (EB)
Ekstrak Polar (EP) Lapisan air
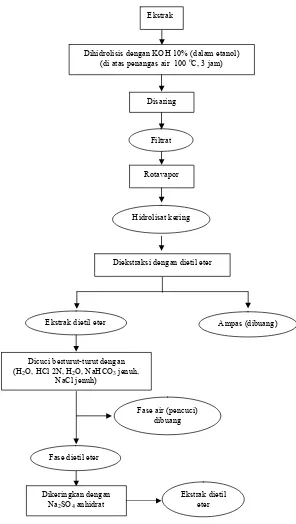
pelarut heksana. Diagram proses ekstraksi steroid secara skematis disajikan pada Gambar 12.
Gambar 12 Bagan alir ekstraksi steroid (Bahti et al. 1983 diacu dalam Heryani 2002).
Ekstrak
Dihidrolisis dengan KOH 10% (dalam etanol) (di atas penangas air 100 oC, 3 jam)
Disaring
Rotavapor Filtrat
Diekstraksi dengan dietil eter Hidrolisat kering
Ekstrak dietil eter Ampas (dibuang) Dicuci berturut-turut dengan
(H2O, HCl 2N, H2O, NaHCO3 jenuh,
NaCl jenuh)
Fase dietil eter
Fase air (pencuci) dibuang
Dikeringkan dengan Na2SO4 anhidrat
[image:49.612.169.465.117.641.2]4. HASIL DAN PEMBAHASAN
4.1 Kandungan Gizi Kablang 4.1.1 Analisis proksimat
Nilai gizi dari suatu produk merupakan parameter yang sangat penting karena merupakan salah satu pertimbangan konsumen dalam menentukan pilihan terhadap makanan. Salah satu cara untuk menentukan kandungan gizi suatu produk adalah analisis proksimat.
[image:50.612.130.510.354.463.2]Analisis proksimat terhadap daging Kablang (Nerita albicilla) meliputi pengukuran kadar air, protein, lemak, abu, serat kasar dan karbohidrat (by difference). Hasil analisis proksimat daging Nerita albicilla disajikan pada Tabel 1.
Tabel 1 Hasil analisis proksimat daging kering Kablang dibandingkan dengan produk perikanan lainnya
Komposisi Kablang (Nerita
albicilla) Bekicot (Achatina fulita)** Kerang darah (Anadara granosa)** Teripang batu (Holothuria. scabra)** Air (%) Protein (%) Lemak (%) Abu (%) Serat kasar (%) Karbohidrat * (%)
12,44 62,05 5,58 9,17 6,60 4,16 5,69 72,47 4,55 11,25 - 11,72 6,32 79,92 6,78 5,64 - 1,34 10,34 54,05 6,30 28,02 - 1,29 * by difference
** Sumber : Witjaksono (2005).
Tabel 1 memperlihatkan bahwa Kablang memiliki kadar air sebesar 12,44%, kadar protein 62,05%, kadar lemak 5,58%, kadar abu 9,17%, serat kasar 6,60% dan karbohidrat 4,16%. Walaupun dibandingkan dengan kandungan protein komoditas invertebrata perikanan lainnya yaitu bekicot (72,47%) dan kerang darah (79,92%) terlihat lebih rendah dan sedikit lebih tinggi dari kandungan protein teripang batu akan tetapi kandungan protein Kablang dapat meningkat lagi disebabkan kadar airnya yang masih cukup tinggi.