ANALISIS SEGREGASI GEN HPT (Hygromisin Phosphotransferase)
PADA TANAMAN TEMBAKAU TRANSGENIK GENERASI T0
NIKSON HALOMOAN
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
NIKSON HALOMOAN. Analisis Segregasi Gen hpt (hygromisin phosphotransferase) pada Tanaman Tembakau Transgenik Generasi T0. Dibimbing oleh SUHARSONO dan UTUT WIDYASTUTI.
Higromisin fosfotransferase yang disandi oleh gen hpt merupakan salah satu penanda seleksi yang digunakan pada perakitan tanaman transgenik. Tanaman yang membawa gen hpt mampu menghasilkan enzim higromisin fosfotransferase, sehingga toleran terhadap higromisin. Penelitian ini bertujuan untuk melakukan analisis segregasi gen hpt pada tanaman tembakau transgenik generasi T0. Tanaman T0 ditanam di pot dan diletakkan di rumah kaca. Biji yang dihasilkan tanaman T0 dari penyerbukan sendiri ditanam di media MS0 yang mengandung 50mg/l higromisin selama satu bulan. Perbandingan antara jumlah tanaman yang toleran dan sensitif terhadap higromisin adalah 3:1 berdasarkan uji Khi-kuadrat. Hal ini menunjukkan bahwa gen hpt
terintegrasi di genom tanaman T0, diwariskan mengikuti hukum Mendel untuk satu gen dan genotipe tanaman T0 adalah heterozigot untuk gen hpt. Gen hpt difusikan dengan gen MmCu-Zn-SOD, maka tanaman T0 juga mengandung gen MmCu-Zn-SOD.
Kata kunci : segregasi, higromisin, analisis khi-kuadrat.
ABSTRACT
NIKSON HALOMOAN. Segregation Analysis of hpt (hygromycin phosphotransferase) Gene in T0 Generation Transgenic Tobacco Plants. Supervised by SUHARSONO and UTUT WIDYASTUTI.
Hygromycine phosphotransferase encoded by hpt gene is one of commonly used as a selectable marker for the production of transgenic plants
.
The plants harbored the hpt gene were able to synthesize hygromycine phosphotransferase enzymes, therefore they are tolerant to higromicine.The objective of this research is to analyze the segregation of hpt gene in T0 generation transgenic tobacco plants. T0 transgenic plants were cultivated in the pot and placed in the green house. The seeds produced by selfing of T0 plants were cultivated on the MS0 media containing 50mg/l higromycine for one month. The rasio between the number of tolerant and sensitive plants to higromycine is 3:1 based on Khi-square. This result indicated that hpt gene is integrated in genom of T0 plants, inherited as Mendelian pattern for one gene, and the genotype of T0 plants is heterozigous for hpt gene. As hpt gene linked to MmCuZn-SOD gene, so T0 plants contain also MmCuZn-SOD gene.ANALISIS SEGREGASI GEN HPT (Hygromisin Phosphotransferase)
PADA TANAMAN TEMBAKAU TRANSGENIK GENERASI T0
NIKSON HALOMOAN
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul
: Analisis Segregasi Gen
hpt
(
Hygromisin Phosphotransferase
) pada
Tanaman Tembakau Transgenik Generasi T0
Nama : Nikson Halomoan
NRP : G34051052
Menyetujui :
Pembimbing I, Pembimbing II,
Prof. Dr. Ir. Suharsono, DEA
Dr. Ir. Utut Widyastuti, M. Si
NIP 196104281987031003
NIP 196405171989032001
Mengetahui :
Ketua Departemen Biologi
Dr. Ir. Ence Darmo Jaya Supena, M. Si
NIP 196410021989031002
PRAKATA
Puji syukur penulis panjatkan kehadirat Tuhan atas segala rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini. Penelitian ini berjudul Analisis Segregasi Gen HPT (Hygromisin Phosphotransferase) pada Tanaman Tembakau Transgenik Generasi T0 yang dilaksanakan pada bulan Mei sampai bulan Desember 2011 bertempat di Laboratorium BIORIN (Biotechnology Research Indonesia-The Netherlands) dan Biologi Sel dan Molekular Tanaman, Pusat Penelitan Sumberdaya Hayati dan Bioteknologi IPB (PPSHB-IPB) kampus IPB Dramaga, Bogor.
Terima kasih penulis ucapkan kepada Prof. Dr. Ir. Suharsono, DEA dan Dr. Ir. Utut Widyastuti, M. Si selaku pembimbing yang telah memberikan saran dan bimbingannya selama melaksanakan penelitian serta kepada Dra. Hilda Akmal, M. Si sebagai penguji atas saran yang telah diberikan. Terima kasih kepada Ditjen Dikti Depdiknas atas Hibah Kompetensi dengan judul: “Isolasi dan ekspresi gen dalam rangka perakitan tanaman yang toleran terhadap cekaman asam dan aluminium” an. Dr. Suharsono, DEA dengan nomor kontrak 039/HIKOM/DP2M/2008/ tanggal 13 Agustus 2008, 219/SP2H/PP/DP2M/V/2009 tanggal 30 Mei 2009, dan 224/SP2H/PP/DP2M/III/2010 tanggal 1 Maret 2010, terima kasih atas bantuannya dalam menyediakan biaya pendidikan dan penelitian. Terima kasih penulis ucapkan juga kepada Bu Hanum, Bu Ratna, Pak Ulung, Pak Muzuni, Pak Radit, Bu Srilis, Pak Mulya, Mbak Peppy, Mbak Nia, Mbak Ara, Pak Adi, Pak Yusman, Kak Muchdar, Kak Nurul, Kak Anita, Kak Novi, Lulu, Goto, Fajri, Lita, Indah, dan Ila yang telah banyak membantu dalam penelitian ini.
Ucapan terima kasih penulis sampaikan kepada Ibuku Rolas Purba yang selalu sabar mendidikku, Bapakku Jackson Anwar Hasudungan yang selalu menasihatiku, Abangku; Ruben serta kedua adikku; Fandry dan Fransiskus yang selalu mendoakanku. Terima kasih penulis ucapkan juga kepada sahabatku Henrikus, Budi dan Ayi yang selalu mengerti akan diriku, karibku Yanto, Yono, Aldion, Leo, Robin, Hardi, Mulya, Agus dan Bonar yang selalu ada dan dekat. Teman-teman Biologi angkatan 41, 42 dan 43 yang lain atas kebersamaan selama penelitian. Teman-teman Perwira 99 dan Kartika yang selalu memberi semangat. Tak lupa penulis ucapkan terimakasih kepada Bu Tri pembimbing akademikku, Bu Rita pembimbing Studi Lapanganku, Pak Aris pembimbing Praktik Lapanganku, Pak Tri, Pak Ence, Bu Nissa, Bu Agustin, Bu Rini, Bu Nunik, Bu Wita, Pak Achmad, Pak Bambang, Pak Alex, dan Bu Dorly. Keluarga Departemen Biologi yang selalu membantu Bu Eti, Mbak Yenny, Mbak Yunny, Pak Rusna, dan Paman Jonny.
Semoga karya ilmiah ini bermanfaat.
Bogor, 12 Juni 2012
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta tanggal 15 Juni 1987, putra kedua dari empat bersaudara dari Bapak Jackson Anwar Hasudungan dan Ibu Rolas Purba. Pada tahun 2005 penulis lulus dari SMUN 26 Jakarta dan pada tahun yang sama penulis melanjutkan kuliah di Institut Pertanian Bogor melalui jalur PMDK (Penelusuran Minat dan Bakat). Tahun 2006 penulis masuk program studi Biologi, Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... viii
DAFTAR TABEL... viii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan ... 1
Waktu dan Tempat ... 1
BAHAN DAN METODE ... 1
Bahan dan Alat ... 1
Metode Penelitian Penyerbukan sendiri pada tanaman tembakau ... 1
Uji resistensi tanaman tembakau terhadap higromisin secara in vitro ... 1
Analisis Data ... 2
HASIL ... 2
PEMBAHASAN ... 3
SIMPULAN ... 3
SARAN ... 3
DAFTAR PUSTAKA ... 4
viii
DAFTAR GAMBAR
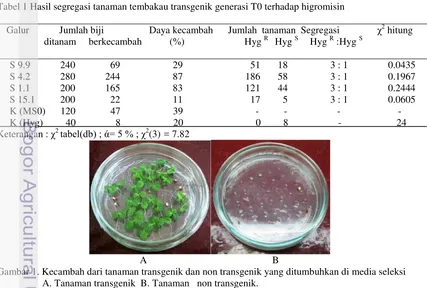
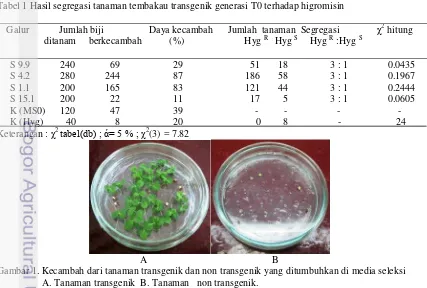
Halaman 1 Kecambah dari tanaman transgenik dan non transgenik yang ditumbuhkan di media
seleksi. A. Tanaman transgenik B. Tanaman non transgenik... ... ... 2 2 Tanaman non transgenik yang ditumbuhkan di media MS0. A. Mengandung higromisin 50 mg/l dan B. Tanpa higromisin………..3
DAFTAR TABEL
Halaman 1 Hasil segregasi tanaman tembakau transgenik generasi T0 terhadap higromisin ... 2
DAFTAR LAMPIRAN
1
PENDAHULUAN
Latar Belakang
Hukum Mendel mengenai segregasi menyatakan bahwa kedua alel dari masing-masing sifat individu terpisah selama pembentukan gamet sehingga gamet masing-masing individu hanya mendapat satu dari dua alel. Alel berpadu bebas pada saat pembuahan (Mendel 1865). Ratio hasil persilangan mengikuti hukum Mendel dapat dianalisis dengan menggunakan sebaran khi-kuadrat (χ2) (Mood et al. 1974). Untuk menguji hipotesis hasil persilangan digunakan formula: H0: α1 =
α2 vs H1 : α1 ≠ α2; χ2 = Σ [(oi – ei)2/ei]: dimana oi : hasil observasi dan ei : nilai
harapan observasi. Jika χ2 hitung ≤ χ2 tabel terima H0 dan χ2 hitung > χ2 tabel tolak H0. Penerimaan H0 berarti hasil persilangan mengikuti hukum Mendel, sedangkan penolakan H0 berarti tidak mengikuti hukum Mendel (Winchester 1958; Mendenhall & Scheaffer 1973).
Gen penanda hasil transformasi pada tanaman Nicotiana tabacum yang berasal dari
daerah pengkode protein pada Tn5
aminoglikosida jenis phosphotransferase II gen yang terdapat pada virus mosaik kembang kol VI telah disisipkan ke dalam protoplas tanaman sebagai bagian dari plasmid biner. Gen tersebut stabil terintegrasi di dalam genomik DNA dan terekspresi sebagai penanda, serta dapat diturunkan pada klon sel. Hasil analisis persilangan genetik pada tanaman transformasi memiliki sifat resisten terhadap kanamisin sebagai penanda seleksi dan bersegregasi sesuai hukum Mendel pada generasi F1 (Paszkowski et al. 1984).
Higromisin dihasilkan oleh Streptomyces hygroscopicus, sebuah bakteri yang diisolasi dari sampel tanah. Sejak penemuan pada tahun delapan puluhan higromisin telah menjadi agen seleksi standar dalam percobaan transfer gen dalam berbagai sel prokariotik dan eukariotik (Gritz & Davies 1983; Kaster et al. 1983). Higromisin menghambat sintesis protein pada proses penerjemahan mRNA (Cabanas et al. 1987; Lacal & Carrasco 1983). Higromisin juga mempengaruhi proses translokasi ribosom (Cabanas et al. 1987; Gonzalez et al. 1978; Hausner et al. 1988). Seperti antibiotik aminoglikosida lainnya, higromisin menginduksi salah membaca aminoasil-tRNA dengan mengikat situs ribosom A (decoding site) (Cabanas et al. 1987; Davies & Davis 1968; Moazed & Noller 1987; Spahn & Prescott 1996).
Tujuan
Penelitian ini bertujuan melakukan analisis segregasi gen hpt (hygromycin phosphotransferase) pada tanaman tembakau transgenik generasi T0.
Waktu dan Tempat
Penelitian ini dilakukan pada bulan Mei sampai dengan Desember 2011. Penelitian dilaksanakan di laboratorium BIORIN (Biotechnology Research Indonesia-The Netherlands), Biologi Sel dan Molekular Tanaman, Pusat Penelitan Sumberdaya Hayati dan Bioteknologi (PPSHB) IPB Dramaga.
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan yaitu tanaman tembakau transgenik yang mengandung gen
MmCuZn-SOD dan gen hpt yang resisten terhadap higromisin sebagai penanda seleksi (Hannum 2012), media tanam, media dasar Murashige dan Skoog (MS0), dan antibiotik higromisin. Cawan petri, timbangan analitik, kotak pindah (Laminar Air Flow Cabinet) dan alat laboratorium lainnya.
Metode Penelitian
Penyerbukan sendiri pada tanaman tembakau
Tanaman tembakau transgenik diperbanyak secara in vitro di dalam media MS0 di ruang kultur dengan fotoperiode 16
jam pada suhu 25oC. Tanaman yang
mempunyai akar yang baik, dipindahkan ke media sekam dalam ruang kultur selama seminggu. Selanjutnya tanaman yang tumbuh dengan baik dipindahkan ke media tanam yang berisi campuran tanah, kompos, sekam bakar (1:1:1) di dalam pot dan diletakkan di luar ruangan selama seminggu. Selanjutnya tanaman dipindahkan dan dipelihara di rumah kaca sampai dewasa. Tanaman tembakau dibiarkan melakukan penyerbukan sendiri dengan ditutup pada bunganya sampai menghasilkan biji.
Uji resistensi tanaman tembakau terhadap higromisin secara in vitro
2
Sebanyak 40 biji tembakau steril ditumbuhkan dalam media Murashige dan Skoog yang mengandung garam-garam MS, vitamin, 30 g/L sukrosa, 3 g/L agar, dan antibiotik higromisin 50 mg/L di dalam cawan petri yang berdiameter 10 cm, dan diletakkan di ruangan gelap selama 3 hari dan kemudian dipindahkan ke ruangan bercahaya, dengan suhu 25ºC selama satu bulan. Setelah berumur satu bulan, tanaman yang hidup dan yang mati dihitung. Tanaman yang hidup adalah tanaman yang resisten terhadap higromisin dan yang mati adalah yang sensitif terhadap higromisin.
Analisis Data
Segregasi gen hpt dianalisis dengan menggunakan uji khi-kuadrat (χ2) dengan rumus : χ2= Σ [(oi – ei)2/ei]. Adanya ekspresi gen hpt
menyebabkan tanaman resisten terhadap higromisin dan tidak adanya ekspresi gen hpt
menyebabkan tanaman sensitif terhadap higromisin sehingga gen hpt bersifat dominan pada tanaman transgenik.
HASIL
Tanaman transgenik hasil regenerasi dari sel atau jaringan disebut dengan generasi T0.
Tanaman T0 menghasilkan biji generasi T1. Pada penelitian ini empat galur T0 telah berhasil ditumbuhkan sehingga mendapatkan biji T1. Sebagian besar tanaman tembakau pada penelitian ini menghasilkan biji yang mempunyai daya kecambah yang rendah. Daya kecambah tanaman tembakau transgenik T0 berkisar antara 11 sampai 87% dan tanaman kontrol non transgenik 20-39% (Tabel 1).
Baik biji dari tanaman transgenik maupun non transgenik dapat berkecambah di media yang mengandung higromisin (Gambar 1). Kecambah yang resisten higromisin dapat tumbuh terus menghasilkan daun dan berwarna hijau setelah kotiledon tumbuh sedangkan kecambah yang sensitif hanya dapat menghasilkan kotiledon, berhenti tumbuh dan berwarna kuning keputih-putihan.
[image:10.595.88.515.460.748.2]Empat tanaman transgenik T0 menghasilkan keturunan tanaman resisten dan sensitif terhadap higromisin dengan perbandingan sekitar 3 resisten dan 1 sensitif dengan nilai (χ2) antara 0.0435 dan 0.2444. Tanaman non transgenik menghasilkan keturunan yang tumbuh bagus di media tanpa higromisin tetapi mati semua di media yang mengandung higromisin (Gambar 2).
Tabel 1 Hasil segregasi tanaman tembakau transgenik generasi T0 terhadap higromisin
Galur Jumlah biji Daya kecambah Jumlah tanaman Segregasi χ2 hitung ditanam berkecambah (%) Hyg R Hyg S Hyg R :Hyg S
S 9.9 240 69 29 51 18 3 : 1 0.0435 S 4.2 280 244 87 186 58 3 : 1 0.1967 S 1.1 200 165 83 121 44 3 : 1 0.2444 S 15.1 200 22 11 17 5 3 : 1 0.0605 K (MS0) 120 47 39 - - - - K (Hyg) 40 8 20 0 8 - 24 Keterangan : χ2 tabel(db) ; ά= 5 % ; χ2(3) = 7.82
A
B
3
A
B
Gambar 2. Tanaman non transgenik yang ditumbuhkan di media MS0. A. Mengandung higromisin 50 mg/l dan B. Tanpa higromisin.
PEMBAHASAN
Tanaman transgenik yang resisten terhadap higromisin yang diperoleh melalui infeksi
Agrobacterium tumefaciens menghasilkan keturunan tanaman yang resisten dan sensitif terhadap higromisin. Hal ini menunjukkan bahwa gen hpt yang menyandi sifat resisten terhadap higromisin terintegrasi ke dalam genom tanaman transgenik T0; karena tidak semua keturunannya resisten terhadap higromisin, maka tanaman transgenik T0 mempunyai genotipe heterozigot untuk gen hpt. Hasil analisis (χ2) terhadap keturunan dari empat tanaman transgenik generasi T0 menunjukkan bahwa populasi T1 terdiri dari tanaman yang resisten dan sensitif terhadap higromisin dengan perbandingan 3:1. Perbandingan ini menunjukkan bahwa selain tanaman tetuanya adalah heterozigot, tetapi juga tanaman tetuanya mengandung 1 gen hpt fungsional. Umumnya gen yang diintroduksikan ke tanaman dengan perantara A. tumefaciens diwariskan ke generasi berikutnya mengikuti pola pewarisan Mendel monohibrid (Travella et al. 2005).
Warna putih pada kecambah yang
ditumbuhkan di media seleksi yang mengandung antibiotik higromisin disebabkan oleh adanya penghambatan metabolisme sel tumbuhan oleh antibiotik (Braun & Bennett 2001) (Gambar 1 & 2 A dan B). Penghambatan proses metabolisme oleh antibiotik higromisin terjadi karena adanya pengikatan ribosom A pada subunit 30S oleh antibiotik yang menyebabkan terjadinya kesalahan membaca oleh aminoasil-tRNA terhadap mRNA pada proses translasi. Pada tumbuhan, ribosom subunit 30S berada di organel kloroplas dan mitokondria. Pada kloroplas pengikatan ribosom
A pada subunit 30S oleh antibiotik
menyebabkan rusaknya klorofil dan
menghambat pembentukan asam amino (Wajtania et al. 2005).
Tanaman transgenik yang membawa gen
hpt akan mampu menghasilkan enzim
hygromycin phosphotransferase, yaitu kinase yang akan memfosforilasi higromisin sehingga menjadi tidak toksik bagi tanaman tersebut (Holme et al. 2008).
Gen hpt difusikan dengan gen
MmCuZn-SOD maka kedua gen ini mempunyai
kecenderungan diwariskan ke generasi berikutnya secara bersama-sama (Lampiran 1). Gen hpt dan gen MmCuZn-SOD terletak berdampingan, maka kedua gen tersebut sangat kecil kemungkinannya untuk bersegregasi. Untuk mengetahui peranan gen SOD pada tanaman transgenik, maka genotipe tanaman transgenik lebih baik dalam keadaan homozigot. Untuk mendapatkan tanaman transgenik homozigot, maka seleksi harus dilakukan terhadap tanaman T1 karena tanaman T1 terdiri dari tanaman homozigot dan heterozigot untuk transgen dengan perbandingan 1:2.
SIMPULAN
Hasil segregasi pada tanaman tembakau transgenik yang mengandung gen MmCuZn-SOD dan gen hpt berdasarkan analisis khi-kuadrat mengikuti pola pewarisan Mendel dengan hasil segregasi 3:1. Semua tanaman T1 adalah heterozigot dan mengandung 1 gen hpt.
SARAN
4
DAFTAR PUSTAKA
Braun R, Bennett DJ. 2001. Antibiotic resistence in genetically modified (GM) crops. EFB Task GroupPub Prec Biotec
10: 1-4.
Cabanas MJ, Vasquez D, Modelell J. 1987. Dual interference of hygromycin B with ribosomal translocation and with aminoacyl-tRNA recognition. Eur J Biochem 87(1): 21-27.
Davies J, Davis BD. 1968. Misreading of ribonucleic acid code words indiced by aminoglycoside antibiotics. The effect of drug concentration. J Biol Chem 243 (12): 3312-3316.
Gonzalez A, Jimenez A, Vazquez D, Davies JE, Schindler D. 1978. Studies on the mode of action of hygromycin B,an inhibitor of translocation in eukaryotes. J Biochem Biophys Act 521(2): 459-469.
Gritz L, Davies J. 1983. Plasmid-encoded hygromycin B resistance : the sequence of hygromycin B phosphotransferase gene and its expression in Escherichia coli and
Saccharomyces cerevisiae. Gene 25(2-3): 179-188.
Hannum S. 2012. Isolasi, pengklonan dan analisis ekspresi gen penyandi Copper-Zinc Superoxide Dismutase [disertasi]. Bogor: Sekolah Pascasarjana, Institut Pertanian Bogor.
Hausner TP, Geigenmuller U, Nierhaus KH. 1988. The allosteric three-site model for the ribosomal elongation cycle. New insights into the inhibition mechanisms of aminoglycosides, hiostrepton, and viomycin. J Biol Chem 263(26): 13103-13111.
Holme IB, Brinch-Pedersen H, Lange M, Holm PB. 2008. Transformation of different barley (Hordeum vulgare L.) Cultivars by
Agrobacterium tumefaciens infection of in vitro cultured ovules. Plant Cell Rep 27: 1833-1840
Kaster KR, Burgett SG, Rao RN, Ingolia TD. 1983. Analysis of a bacterial hygromycin B resistance gene by transcriptional and translational fusions and by DNA sequencing. Nucleic Acids Res 11(19): 6895-6911.
Lacal JC, Carrasco L. 1983. Antiviral effects of hygromycin B, a translation inhibitor nonpermeant to uninfected cells.
Antimicrobiol Agents Chemother 24(2): 273-275.
Mendel G. 1865. Mendel's paper in English: Experiments in Plant Hybridization. Druery CT, the translator; Great Britain: the Royal Horticultural Society. translation ofMendel's paper.
Mendenhall W, Scheaffer R. 1973. Mathematical Statistics and Applications. University of Florida. Massachusctts. Duxbury Press Scituate. p. 501
Moazed D, Noller HF .1987. Interaction of antibiotics with functional sites in 16S ribosomal RNA. Nature 327(6121): 389-394.
Mood AM, Graybill FA, Boes DC. 1974. Introduction to the theory of statistics. 3nd. MC Graw-Hill Kagarusha. Tokyo. LTD. p. 107
Paszkowski J et al.1984. Direct gene transfer to plant. EMBO J 3(12): 2717-2722
Spahn CM, Prescott CD.1996. Throwing a spanner in the works: antibiotics and the translation apparatus. J Mol Med 74(8): 423-439.
Travella S, Ross SM, Harden J, Everett C, Snape JW, Harwood WA. 2005. A comparison of transgenic barley lines produced by particle bombardment and Agrobacterium-mediated technique. Plant Cell Rep 23: 780-789.
Wajtania A, Pulawka J, Gabryszewska E. 2005. Identification and elimination of bacterial contaminants from Pelargonium tissue cultures. J Fruit and Ornamental Plant Res
13: 101-108.
5
6
RB
LB
Lampiran 1 Konstruksi plasmid biner yang membawa gen MmCuZn-SOD dan gen hpt (Hannum 2012)
NosP NPT II
ABSTRAK
NIKSON HALOMOAN. Analisis Segregasi Gen hpt (hygromisin phosphotransferase) pada Tanaman Tembakau Transgenik Generasi T0. Dibimbing oleh SUHARSONO dan UTUT WIDYASTUTI.
Higromisin fosfotransferase yang disandi oleh gen hpt merupakan salah satu penanda seleksi yang digunakan pada perakitan tanaman transgenik. Tanaman yang membawa gen hpt mampu menghasilkan enzim higromisin fosfotransferase, sehingga toleran terhadap higromisin. Penelitian ini bertujuan untuk melakukan analisis segregasi gen hpt pada tanaman tembakau transgenik generasi T0. Tanaman T0 ditanam di pot dan diletakkan di rumah kaca. Biji yang dihasilkan tanaman T0 dari penyerbukan sendiri ditanam di media MS0 yang mengandung 50mg/l higromisin selama satu bulan. Perbandingan antara jumlah tanaman yang toleran dan sensitif terhadap higromisin adalah 3:1 berdasarkan uji Khi-kuadrat. Hal ini menunjukkan bahwa gen hpt
terintegrasi di genom tanaman T0, diwariskan mengikuti hukum Mendel untuk satu gen dan genotipe tanaman T0 adalah heterozigot untuk gen hpt. Gen hpt difusikan dengan gen MmCu-Zn-SOD, maka tanaman T0 juga mengandung gen MmCu-Zn-SOD.
Kata kunci : segregasi, higromisin, analisis khi-kuadrat.
ABSTRACT
NIKSON HALOMOAN. Segregation Analysis of hpt (hygromycin phosphotransferase) Gene in T0 Generation Transgenic Tobacco Plants. Supervised by SUHARSONO and UTUT WIDYASTUTI.
Hygromycine phosphotransferase encoded by hpt gene is one of commonly used as a selectable marker for the production of transgenic plants
.
The plants harbored the hpt gene were able to synthesize hygromycine phosphotransferase enzymes, therefore they are tolerant to higromicine.The objective of this research is to analyze the segregation of hpt gene in T0 generation transgenic tobacco plants. T0 transgenic plants were cultivated in the pot and placed in the green house. The seeds produced by selfing of T0 plants were cultivated on the MS0 media containing 50mg/l higromycine for one month. The rasio between the number of tolerant and sensitive plants to higromycine is 3:1 based on Khi-square. This result indicated that hpt gene is integrated in genom of T0 plants, inherited as Mendelian pattern for one gene, and the genotype of T0 plants is heterozigous for hpt gene. As hpt gene linked to MmCuZn-SOD gene, so T0 plants contain also MmCuZn-SOD gene.1
PENDAHULUAN
Latar Belakang
Hukum Mendel mengenai segregasi menyatakan bahwa kedua alel dari masing-masing sifat individu terpisah selama pembentukan gamet sehingga gamet masing-masing individu hanya mendapat satu dari dua alel. Alel berpadu bebas pada saat pembuahan (Mendel 1865). Ratio hasil persilangan mengikuti hukum Mendel dapat dianalisis dengan menggunakan sebaran khi-kuadrat (χ2) (Mood et al. 1974). Untuk menguji hipotesis hasil persilangan digunakan formula: H0: α1 =
α2 vs H1 : α1 ≠ α2; χ2 = Σ [(oi – ei)2/ei]: dimana oi : hasil observasi dan ei : nilai
harapan observasi. Jika χ2 hitung ≤ χ2 tabel terima H0 dan χ2 hitung > χ2 tabel tolak H0. Penerimaan H0 berarti hasil persilangan mengikuti hukum Mendel, sedangkan penolakan H0 berarti tidak mengikuti hukum Mendel (Winchester 1958; Mendenhall & Scheaffer 1973).
Gen penanda hasil transformasi pada tanaman Nicotiana tabacum yang berasal dari
daerah pengkode protein pada Tn5
aminoglikosida jenis phosphotransferase II gen yang terdapat pada virus mosaik kembang kol VI telah disisipkan ke dalam protoplas tanaman sebagai bagian dari plasmid biner. Gen tersebut stabil terintegrasi di dalam genomik DNA dan terekspresi sebagai penanda, serta dapat diturunkan pada klon sel. Hasil analisis persilangan genetik pada tanaman transformasi memiliki sifat resisten terhadap kanamisin sebagai penanda seleksi dan bersegregasi sesuai hukum Mendel pada generasi F1 (Paszkowski et al. 1984).
Higromisin dihasilkan oleh Streptomyces hygroscopicus, sebuah bakteri yang diisolasi dari sampel tanah. Sejak penemuan pada tahun delapan puluhan higromisin telah menjadi agen seleksi standar dalam percobaan transfer gen dalam berbagai sel prokariotik dan eukariotik (Gritz & Davies 1983; Kaster et al. 1983). Higromisin menghambat sintesis protein pada proses penerjemahan mRNA (Cabanas et al. 1987; Lacal & Carrasco 1983). Higromisin juga mempengaruhi proses translokasi ribosom (Cabanas et al. 1987; Gonzalez et al. 1978; Hausner et al. 1988). Seperti antibiotik aminoglikosida lainnya, higromisin menginduksi salah membaca aminoasil-tRNA dengan mengikat situs ribosom A (decoding site) (Cabanas et al. 1987; Davies & Davis 1968; Moazed & Noller 1987; Spahn & Prescott 1996).
Tujuan
Penelitian ini bertujuan melakukan analisis segregasi gen hpt (hygromycin phosphotransferase) pada tanaman tembakau transgenik generasi T0.
Waktu dan Tempat
Penelitian ini dilakukan pada bulan Mei sampai dengan Desember 2011. Penelitian dilaksanakan di laboratorium BIORIN (Biotechnology Research Indonesia-The Netherlands), Biologi Sel dan Molekular Tanaman, Pusat Penelitan Sumberdaya Hayati dan Bioteknologi (PPSHB) IPB Dramaga.
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan yaitu tanaman tembakau transgenik yang mengandung gen
MmCuZn-SOD dan gen hpt yang resisten terhadap higromisin sebagai penanda seleksi (Hannum 2012), media tanam, media dasar Murashige dan Skoog (MS0), dan antibiotik higromisin. Cawan petri, timbangan analitik, kotak pindah (Laminar Air Flow Cabinet) dan alat laboratorium lainnya.
Metode Penelitian
Penyerbukan sendiri pada tanaman tembakau
Tanaman tembakau transgenik diperbanyak secara in vitro di dalam media MS0 di ruang kultur dengan fotoperiode 16
jam pada suhu 25oC. Tanaman yang
mempunyai akar yang baik, dipindahkan ke media sekam dalam ruang kultur selama seminggu. Selanjutnya tanaman yang tumbuh dengan baik dipindahkan ke media tanam yang berisi campuran tanah, kompos, sekam bakar (1:1:1) di dalam pot dan diletakkan di luar ruangan selama seminggu. Selanjutnya tanaman dipindahkan dan dipelihara di rumah kaca sampai dewasa. Tanaman tembakau dibiarkan melakukan penyerbukan sendiri dengan ditutup pada bunganya sampai menghasilkan biji.
Uji resistensi tanaman tembakau terhadap higromisin secara in vitro
2
Sebanyak 40 biji tembakau steril ditumbuhkan dalam media Murashige dan Skoog yang mengandung garam-garam MS, vitamin, 30 g/L sukrosa, 3 g/L agar, dan antibiotik higromisin 50 mg/L di dalam cawan petri yang berdiameter 10 cm, dan diletakkan di ruangan gelap selama 3 hari dan kemudian dipindahkan ke ruangan bercahaya, dengan suhu 25ºC selama satu bulan. Setelah berumur satu bulan, tanaman yang hidup dan yang mati dihitung. Tanaman yang hidup adalah tanaman yang resisten terhadap higromisin dan yang mati adalah yang sensitif terhadap higromisin.
Analisis Data
Segregasi gen hpt dianalisis dengan menggunakan uji khi-kuadrat (χ2) dengan rumus : χ2= Σ [(oi – ei)2/ei]. Adanya ekspresi gen hpt
menyebabkan tanaman resisten terhadap higromisin dan tidak adanya ekspresi gen hpt
menyebabkan tanaman sensitif terhadap higromisin sehingga gen hpt bersifat dominan pada tanaman transgenik.
HASIL
Tanaman transgenik hasil regenerasi dari sel atau jaringan disebut dengan generasi T0.
Tanaman T0 menghasilkan biji generasi T1. Pada penelitian ini empat galur T0 telah berhasil ditumbuhkan sehingga mendapatkan biji T1. Sebagian besar tanaman tembakau pada penelitian ini menghasilkan biji yang mempunyai daya kecambah yang rendah. Daya kecambah tanaman tembakau transgenik T0 berkisar antara 11 sampai 87% dan tanaman kontrol non transgenik 20-39% (Tabel 1).
Baik biji dari tanaman transgenik maupun non transgenik dapat berkecambah di media yang mengandung higromisin (Gambar 1). Kecambah yang resisten higromisin dapat tumbuh terus menghasilkan daun dan berwarna hijau setelah kotiledon tumbuh sedangkan kecambah yang sensitif hanya dapat menghasilkan kotiledon, berhenti tumbuh dan berwarna kuning keputih-putihan.
[image:17.595.88.515.460.748.2]Empat tanaman transgenik T0 menghasilkan keturunan tanaman resisten dan sensitif terhadap higromisin dengan perbandingan sekitar 3 resisten dan 1 sensitif dengan nilai (χ2) antara 0.0435 dan 0.2444. Tanaman non transgenik menghasilkan keturunan yang tumbuh bagus di media tanpa higromisin tetapi mati semua di media yang mengandung higromisin (Gambar 2).
Tabel 1 Hasil segregasi tanaman tembakau transgenik generasi T0 terhadap higromisin
Galur Jumlah biji Daya kecambah Jumlah tanaman Segregasi χ2 hitung ditanam berkecambah (%) Hyg R Hyg S Hyg R :Hyg S
S 9.9 240 69 29 51 18 3 : 1 0.0435 S 4.2 280 244 87 186 58 3 : 1 0.1967 S 1.1 200 165 83 121 44 3 : 1 0.2444 S 15.1 200 22 11 17 5 3 : 1 0.0605 K (MS0) 120 47 39 - - - - K (Hyg) 40 8 20 0 8 - 24 Keterangan : χ2 tabel(db) ; ά= 5 % ; χ2(3) = 7.82
A
B
3
A
B
Gambar 2. Tanaman non transgenik yang ditumbuhkan di media MS0. A. Mengandung higromisin 50 mg/l dan B. Tanpa higromisin.
PEMBAHASAN
Tanaman transgenik yang resisten terhadap higromisin yang diperoleh melalui infeksi
Agrobacterium tumefaciens menghasilkan keturunan tanaman yang resisten dan sensitif terhadap higromisin. Hal ini menunjukkan bahwa gen hpt yang menyandi sifat resisten terhadap higromisin terintegrasi ke dalam genom tanaman transgenik T0; karena tidak semua keturunannya resisten terhadap higromisin, maka tanaman transgenik T0 mempunyai genotipe heterozigot untuk gen hpt. Hasil analisis (χ2) terhadap keturunan dari empat tanaman transgenik generasi T0 menunjukkan bahwa populasi T1 terdiri dari tanaman yang resisten dan sensitif terhadap higromisin dengan perbandingan 3:1. Perbandingan ini menunjukkan bahwa selain tanaman tetuanya adalah heterozigot, tetapi juga tanaman tetuanya mengandung 1 gen hpt fungsional. Umumnya gen yang diintroduksikan ke tanaman dengan perantara A. tumefaciens diwariskan ke generasi berikutnya mengikuti pola pewarisan Mendel monohibrid (Travella et al. 2005).
Warna putih pada kecambah yang
ditumbuhkan di media seleksi yang mengandung antibiotik higromisin disebabkan oleh adanya penghambatan metabolisme sel tumbuhan oleh antibiotik (Braun & Bennett 2001) (Gambar 1 & 2 A dan B). Penghambatan proses metabolisme oleh antibiotik higromisin terjadi karena adanya pengikatan ribosom A pada subunit 30S oleh antibiotik yang menyebabkan terjadinya kesalahan membaca oleh aminoasil-tRNA terhadap mRNA pada proses translasi. Pada tumbuhan, ribosom subunit 30S berada di organel kloroplas dan mitokondria. Pada kloroplas pengikatan ribosom
A pada subunit 30S oleh antibiotik
menyebabkan rusaknya klorofil dan
menghambat pembentukan asam amino (Wajtania et al. 2005).
Tanaman transgenik yang membawa gen
hpt akan mampu menghasilkan enzim
hygromycin phosphotransferase, yaitu kinase yang akan memfosforilasi higromisin sehingga menjadi tidak toksik bagi tanaman tersebut (Holme et al. 2008).
Gen hpt difusikan dengan gen
MmCuZn-SOD maka kedua gen ini mempunyai
kecenderungan diwariskan ke generasi berikutnya secara bersama-sama (Lampiran 1). Gen hpt dan gen MmCuZn-SOD terletak berdampingan, maka kedua gen tersebut sangat kecil kemungkinannya untuk bersegregasi. Untuk mengetahui peranan gen SOD pada tanaman transgenik, maka genotipe tanaman transgenik lebih baik dalam keadaan homozigot. Untuk mendapatkan tanaman transgenik homozigot, maka seleksi harus dilakukan terhadap tanaman T1 karena tanaman T1 terdiri dari tanaman homozigot dan heterozigot untuk transgen dengan perbandingan 1:2.
SIMPULAN
Hasil segregasi pada tanaman tembakau transgenik yang mengandung gen MmCuZn-SOD dan gen hpt berdasarkan analisis khi-kuadrat mengikuti pola pewarisan Mendel dengan hasil segregasi 3:1. Semua tanaman T1 adalah heterozigot dan mengandung 1 gen hpt.
SARAN
ANALISIS SEGREGASI GEN HPT (Hygromisin Phosphotransferase)
PADA TANAMAN TEMBAKAU TRANSGENIK GENERASI T0
NIKSON HALOMOAN
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
4
DAFTAR PUSTAKA
Braun R, Bennett DJ. 2001. Antibiotic resistence in genetically modified (GM) crops. EFB Task GroupPub Prec Biotec
10: 1-4.
Cabanas MJ, Vasquez D, Modelell J. 1987. Dual interference of hygromycin B with ribosomal translocation and with aminoacyl-tRNA recognition. Eur J Biochem 87(1): 21-27.
Davies J, Davis BD. 1968. Misreading of ribonucleic acid code words indiced by aminoglycoside antibiotics. The effect of drug concentration. J Biol Chem 243 (12): 3312-3316.
Gonzalez A, Jimenez A, Vazquez D, Davies JE, Schindler D. 1978. Studies on the mode of action of hygromycin B,an inhibitor of translocation in eukaryotes. J Biochem Biophys Act 521(2): 459-469.
Gritz L, Davies J. 1983. Plasmid-encoded hygromycin B resistance : the sequence of hygromycin B phosphotransferase gene and its expression in Escherichia coli and
Saccharomyces cerevisiae. Gene 25(2-3): 179-188.
Hannum S. 2012. Isolasi, pengklonan dan analisis ekspresi gen penyandi Copper-Zinc Superoxide Dismutase [disertasi]. Bogor: Sekolah Pascasarjana, Institut Pertanian Bogor.
Hausner TP, Geigenmuller U, Nierhaus KH. 1988. The allosteric three-site model for the ribosomal elongation cycle. New insights into the inhibition mechanisms of aminoglycosides, hiostrepton, and viomycin. J Biol Chem 263(26): 13103-13111.
Holme IB, Brinch-Pedersen H, Lange M, Holm PB. 2008. Transformation of different barley (Hordeum vulgare L.) Cultivars by
Agrobacterium tumefaciens infection of in vitro cultured ovules. Plant Cell Rep 27: 1833-1840
Kaster KR, Burgett SG, Rao RN, Ingolia TD. 1983. Analysis of a bacterial hygromycin B resistance gene by transcriptional and translational fusions and by DNA sequencing. Nucleic Acids Res 11(19): 6895-6911.
Lacal JC, Carrasco L. 1983. Antiviral effects of hygromycin B, a translation inhibitor nonpermeant to uninfected cells.
Antimicrobiol Agents Chemother 24(2): 273-275.
Mendel G. 1865. Mendel's paper in English: Experiments in Plant Hybridization. Druery CT, the translator; Great Britain: the Royal Horticultural Society. translation ofMendel's paper.
Mendenhall W, Scheaffer R. 1973. Mathematical Statistics and Applications. University of Florida. Massachusctts. Duxbury Press Scituate. p. 501
Moazed D, Noller HF .1987. Interaction of antibiotics with functional sites in 16S ribosomal RNA. Nature 327(6121): 389-394.
Mood AM, Graybill FA, Boes DC. 1974. Introduction to the theory of statistics. 3nd. MC Graw-Hill Kagarusha. Tokyo. LTD. p. 107
Paszkowski J et al.1984. Direct gene transfer to plant. EMBO J 3(12): 2717-2722
Spahn CM, Prescott CD.1996. Throwing a spanner in the works: antibiotics and the translation apparatus. J Mol Med 74(8): 423-439.
Travella S, Ross SM, Harden J, Everett C, Snape JW, Harwood WA. 2005. A comparison of transgenic barley lines produced by particle bombardment and Agrobacterium-mediated technique. Plant Cell Rep 23: 780-789.
Wajtania A, Pulawka J, Gabryszewska E. 2005. Identification and elimination of bacterial contaminants from Pelargonium tissue cultures. J Fruit and Ornamental Plant Res
13: 101-108.
5
6
RB
LB
Lampiran 1 Konstruksi plasmid biner yang membawa gen MmCuZn-SOD dan gen hpt (Hannum 2012)
NosP NPT II