PENGARUH RATIO Dt/Di DAN KECEPATAN PENGADUKAN
TERHADAP HIDROLISIS ENZIMATIK MINYAK IKAN
LEMURU MENGGUNAKAN LIPASE
Aspergillus niger
UNTUK
PRODUKSI ASAM LEMAK OMEGA-3
SKRIPSI
ANASTASIA CHRISTINA
F34080090
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Dt/Di RATIO AND STIRRING SPEED EFFECT OF LEMURU FISH OIL
ENZYMATIC HYDROLYSIS USING LIPASE
Aspergillus niger
FOR OMEGA-3
FATTY ACID PRODUCTION
Anastasia Christina and Sapta RaharjaDepartement of Agroindustrial Technology, Faculty of Agricultural Technology, Bogor Agricultural University, IPB Darmaga Campus, PO Box 220, Bogor, West Java, Indonesia.
Phone 62 856 9565 5318, e-mail : [email protected]
ABSTRACT
Lemuru is one of fish that found in Indonesia which can be processed into canned fish (sardine), cue, and fish meal. Fish oil is by- product of fish meal processing that is containing unsaturated fatty acid named omega-3, specially eicosapentanoic acid (EPA) and docosahexanoic acid (DHA). Research objectives are obtaining the optimum process conditions for enzymatic hydrolysis of lemuru fish oil using lipase from Aspergillus niger and determining the Dt/Di ratio and optimum stirring speed for enzymatic hydrolysis of fish oils produce omega-3 fatty acids.. Hexane added into 527,625ml of fish oil that have been rinsed by nitrogen and lipase enzyme that is dissolved with phosphat buffer 0,1 M and hydrolyzed at optimum condition for 48 hour. Product separated from water and analyzed with Gas Chromatography Mass Spectromerty. Scales that used in this research are 5, 10, 20, and 50, which each volumes are 52,7625 ml; 105,525 ml; 211,05 ml; and 527,625 ml. The product at last scale contain 1,16% EPA. DHA does not formed at this scale caused by non-ideal parameter. Stirring speed and ratio of stirrer diameter and container diameter are the parameters that influence production of omega-3. Ideal stirring speed using propeller with 3 blades calculated based on 250 rpm as initial stirring speed. Ideal ratio of container diameter and stirrer diameter is 1,1538.
Anastasia Christina. F34080090. Pengaruh Ratio Dt/Di dan Kecepatan Pengadukan terhadap Hidrolisis Minyak Ikan Lemuru Menggunakan Lipase Aspergillus niger untuk Produksi Asam Lemak Omega-3. Di bawah bimbingan Sapta Raharja. 2013.
RINGKASAN
Indonesia memiliki potensi hasil tangkapan ikan laut yang sangat melimpah. Produksi ikan hingga triwulan II tahun 2012 mencapai 14,86 juta ton dengan potensi perikanan tangkap di perairan umum mencapai 6,4 juta ton ikan per tahun
.
Pengolahan ikan yang banyak berkembang menghasilkan limbah yang belum termanfaatkan dan berpotensi untuk diolah kembali. Ikan lemuru tergolong ikan berlemak (fatty fish) karena kandungan lemaknya relatif tinggi pada saat tertentu dan bervariasi dari tahun ke tahun. Lemak ikan lemuru mengandung cukup banyak asam-asam lemak polienoat penting (EPA dan DHA) yang dianggap bermanfaat bagi kesehatan manusia. Ikan lemuru dapat diolah menjadi ikan lemuru kaleng (sarden), ikan pindang (cue), ikan asin, dan tepung ikan. Minyak ikan merupakan hasil samping pengolahan tepung ikan yang belum dimanfaatkan lebih lanjut. Minyak ikan merupakan sumber asam lemak tidak jenuh berupa eicosapentanoat (EPA) dan asam dokosaheksaenoat (DHA) yang penting bagi pertumbuhan dan kesehatan. Asam lemak omega-3 merupakan salah satu kelompok asam lemak tidak jenuh yang memiliki ikatan rangkap pertama pada posisi atom C (karbon) nomor tiga yang dihitung dari gugus metil terujung. Asam-asam lemak alami yang terdapat dalam asam lemak omega-3 adalah asam linolenat, EPA, dan DHA. Namun, hanya dua macam asam lemak omega-3 yang dominan dalam minyak ikan, yaitu EPA dan DHA. Pemaksimalan produksi asam lemak omega-3 dengan kualitas yang terbaik dari hasil samping pengolahan ikan berupa minyak ikan menjadi tantangan yang harus dihadapi.Tujuan penelitian adalah untuk mengetahui pengaruh rasio Dt/Di dan kecepatan pengadukan terhadap produksi asam lemak omega-3 dengan metode hidrolisis enzimatik minyak ikan menggunakan enzim lipase dari Aspergillus niger. Penelitian ini juga bertujuan untuk mengetahui ratio Dt/Di dan kecepatan pengadukan optimum untuk hidrolisis enzimatik minyak ikan menghasilkan asam lemak omega-3.
PENGARUH RATIO Dt/Di DAN KECEPATAN PENGADUKAN
TERHADAP HIDROLISIS ENZIMATIK MINYAK IKAN
LEMURU MENGGUNAKAN LIPASE
Aspergillus niger
UNTUK
PRODUKSI ASAM LEMAK OMEGA-3
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar
SARJANA TEKNOLOGI PERTANIAN
pada Departemen Teknologi Industri Pertanian,
Fakultas Teknologi Pertanian,
Institut Pertanian Bogor
Oleh:
ANASTASIA CHRISTINA
F34080090
FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR
Judul Skripsi
: Pengaruh Ratio Dt/Di dan Kecepatan Pengadukan terhadap
Hidrolisis Enzimatik Minyak Ikan Lemuru Menggunakan Lipase
Aspergillus Niger
untuk Produksi Asam Lemak Omega-3
Nama
: Anastasia Christina
NIM
: F34080090
Menyetujui,
Pembimbing Akademik,
NIP. 19631026 199002 1 001
Dr. Ir. Sapta Raharja, DEA
Mengetahui,
Ketua Departemen
Teknologi Industri Pertanian
NIP. 19621009 198903 2 001
Prof. Dr. Ir. Nastiti Siswi Indrasti
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER
INFORMASI
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul “Pengaruh Ratio Dt/Di dan Kecepatan Pengadukan terhadap Hidrolisis Enzimatik Minyak Ikan Lemuru Menggunakan Lipase Aspergillus Niger untuk Produksi Asam Lemak Omega-3” adalah hasil karya saya sendiri dengan arahan Dosen Pembimbing Akademik, dan belum diajukan dalam bentuk apapun pada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, April 2013
Yang membuat pernyataan,
© Hak Cipta milik Anastasia Christina, tahun 2013
Hak cipta dilindungi
Dilarang mengutip dan memperbanyak tanpa izin tertulis dari
Institut Pertanian Bogor, sebagian atau seluruhnya dalam bentuk apapun, baik
cetak, foto kopi,
BIODATA PENULIS
Bilangan asam minyak ikan sebelum hidrolisis adalah 2,718 mg KOH/g sampel. Hidrolisis enzimatik menghasilkan sejumlah asam lemak, sehingga menaikkan nilai bilangan asam produk. Bilangan asam produk hidrolisis pada skala 50 kali adalah 81,3843 mg KOH/g sampel. Peningkatan bilangan asam memiliki hubungan berbanding lurus dengan tingkat hidrolisis. Semakin tinggi nilai bilangan asam, maka semakin tinggi tingkat hidrolisis. Tingkat hidrolisis produk pada skala 50 kali adalah sebesar 43,301%. Tingkat hidrolisis mempengaruhi total asam lemak omega-3 yang terbentuk. Asam lemak omega-3 yang secara khusus diamati adalah EPA dan DHA. EPA yang dihasilkan adalah 1,16%. Tidak ada DHA yang terbentuk pada penggandaan skala hidrolisis 50 kali. Parameter dalam penggandaan skala hidrolisis enzimatik ini terdiri atas dua, yaitu kecepatan pengadukan dan rasio antara diameter pengaduk dan diameter wadah yang digunakan. Penelitian menunjukkan kecepatan pengadukan yang ideal untuk penggandaan skala adalah menggunakan basis perhitungan kecepatan awal sebesar 250 rpm. Rasio antara diameter pengaduk dan diameter wadah yang ideal adalah sebesar 1,1538.
KATA PENGANTAR
Puji syukur kepada Tuhan Yang Maha Esa, sehingga skripsi ini dapat diselesaikan dengan baik. Penelitian dengan judul Penggandaan Skala Hidrolisis Enzimatik Minyak Ikan Lemuru Menggunakan Lipase A. niger untuk Produksi Omega-3 yang dilaksanakan di Laboratorium Bioindustri Departemen Teknologi Industri Pertanian sejak bulan Februari hingga Desember 2012.
Dengan telah selesainya penelitian hingga tersusunnya skripsi ini, penulis ingin menyampaikan penghargaan dan terima kasih yang sebesar-besarnya kepada:
1. Dr. Ir. Sapta Raharja, DEA selaku dosen pembimbing yang telah memberikan banyak bimbingan dan bantuan selama pelaksanaan penelitian.
2. Prof. Dr. Ir. Khaswar Syamsu, M.Sc.St dan Dr. Ir. Liesbetini Hartoto, MS selaku dosen penguji skripsi yang telah banyak memberikan masukan untuk perbaikan skripsi.
3. Prof. Dr. Ir. Nastiti Siswi Indrasti yang telah banyak memberikan bimbingan moral selama penulis melakukan studi di Departemen Teknologi Industri Pertanian.
4. Seluruh dosen dan staff pengajar dari Departemen Teknologi Industri Pertanian yang telah memberikan ilmu dan pengetahuan yang bermanfaat.
5. Bapa, Nenek, Fani, Ua Osin, Tante Nur, Ua Leo dan seluruh keluarga besar DJ.F. Sinaga yang telah memberikan kasih sayang, semangat, bimbingan dan bantuan moril, material, dan spiritual kepada penulis sejak dulu hingga sekarang.
6. Ida Nur Rakhmi, Shiella Fanny Erawati, dan Fahrudin yang telah membantu penulis selama penelitian berlangsung.
7. Rekan-rekan TIN 45 dan Himpunan Solidaritas Laboratorium atas kerjasama, keakraban, dan kekerabatan selama menjalankan perkuliahan dan penelitian di Teknologi Industri Pertanian. 8. Antonius Hari Kristanto yang telah memberikan perhatian, kasih sayang, dukungan moril,
penghiburan, semangat dan pengertian kepada penulis.
9. Sahabat-sahabat terbaik Rida, Icha, Trio, Angga, Hazi, Sarinah, Ganis, Melisa, Riska, Citra, Isma, Bunga, Alya, dan Ista yang telah memberikan semangat dan dukungan, menemani dan berbagi dalam suka maupun duka selama menjalani pendidikan di IPB.
10. Seluruh keluarga besar Tim Pendamping dan adik-adik dampingan yang telah memberikan semangat dan dukungan moril, kekeluargaan, dan pengalaman berharga selama menjalani pendidikan di IPB.
11. Ibu Egnawati, Bapak Edy Sumantry, Bapak Sugiardi, Ibu Rini, Ibu Sri, Ibu Diah dan seluruh staff Tata Usaha yang telah memberikan bimbingan, dukungan dan bantuan moril kepada penulis.
Akhir kata penulis berharap semoga tulisan ini bermanfaat dan memberikan kontribusi nyata terhadap perkembangan ilmu pengetahuan di bidang teknologi pertanian.
Bogor, April 2013
DAFTAR ISI
Halaman
KATA PENGANTAR ... iii
DAFTAR ISI ... iv
DAFTAR TABEL ... v
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN ... vii
I. PENDAHULUAN ... 1
1.1. Latar Belakang... 1
1.2. Tujuan ... 2
II. TINJAUAN PUSTAKA ... 3
2.1. Minyak Ikan Lemuru ... 3
2.2. Asam Lemak Omega-3 ... 5
2.3. Hidrolisis Enzimatik ... 9
2.4. Lipase Aspergillus niger... 11
2.5. Penggandaan Skala Hidrolisis ... 12
III. METODOLOGI PENELITIAN ... 15
3.1. Alat dan Bahan ... 15
3.2. Waktu dan Tempat Penelitian ... 15
3.3. Metode Penelitian ... 15
3.3.1. Karakterisasi Minyak Ikan ... 16
3.3.2. Penentuan Desain Penggandaan Skala ... 16
3.3.3. Penentuan Pengaruh Ratio Dt/Di dan Kecepatan Pengadukan terhadap Bilangan Asam ... 16
3.3.4. Penentuan Pengaruh Ratio Dt/Di dan Kecepatan Pengadukan terhadap Tingkat Hidrolisis ... 17
3.3.5. Penentuan Hubungan antara Tingkat Hidrolisis Tertinggi dengan Omega-3 yang Dihasilkan ... 17
IV. HASIL DAN PEMBAHASAN ... 18
4.1. Karakterisasi Minyak Ikan ... 18
4.2. Penggandaan Skala Hidrolisis Enzimatik ... 19
4.2.1 Formulasi Media dan Kondisi Hidrolisis Enzimatik ... 19
4.2.2 Pengaruh Penggandaan Skala terhadap Tingkat Hidrolisis ... 26
4.2.3 Hubungan antara Tingkat Hidrolisis Tertinggi dengan Total Omega-3 ... yang Dihasilkan ... 27
V. PENUTUP ... 30
5.1. Simpulan ... 30
5.2. Saran ... 31
DAFTAR PUSTAKA ... 32
DAFTAR TABEL
Halaman
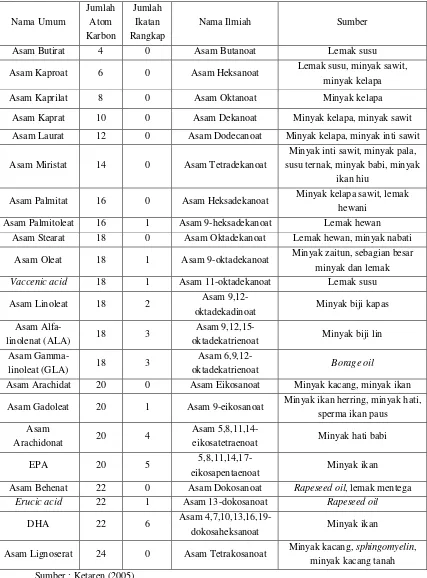
Tabel 1. Jenis-jenis asam lemak dan sumbernya ... 5
Tabel 2. Hasil karakterisasi sifat fisikokimia minyak ikan... 18
Tabel 3. Desain penggandaan skala hidrolisis enzimatik ... 22
Tabel 4. Bobot sampel berdasarkan perkiraan bilangan asam sampel ... 35
DAFTAR GAMBAR
Halaman
Gambar 1. Sardinella lemuru ... 4
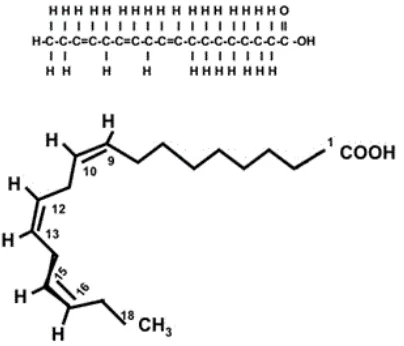
Gambar 2. Struktur kimia asam alfa-linoleat (ALA) ... 7
Gambar 3. Struktur kimia EPA dan DHA ... 7
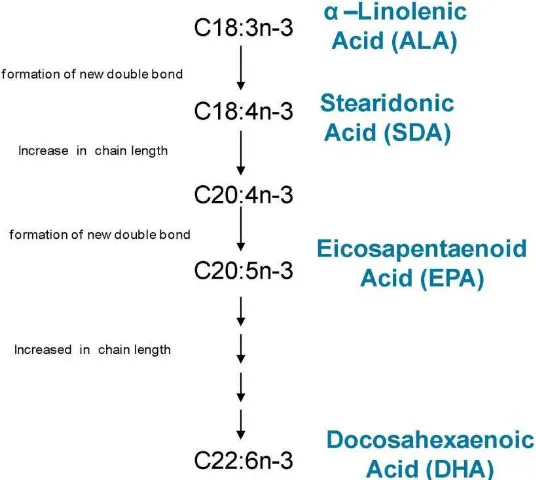
Gambar 4. Sintesis EPA dan DHA ... 8
Gambar 5. Metabolisme asam lemak ... 9
Gambar 6. Tahapan hidrolisis triasilgliserol ... 10
Gambar 7. Diagram alir tahapan penelitian ... 15
Gambar 8. Diagram alir hidrolisis enzimatik minyak ikan lemuru ... 15
Gambar 9. Pemisahan produk dalam corong pemisah ... 23
Gambar 10. Lapisan atas yang telah terpisah ... 23
Gambar 11. Kurva pengaruh ratio Dt/Di terhadap bilangan asam ... 23
Gambar 12. Kurva pengaruh kecepatan pengaduk terhadap bilangan asam ... 24
Gambar 13. Kurva pengaruh ratio Dt/Di terhadap tingkat hidrolisis ... 26
Gambar 14. Diagram hubungan antara tingkat hidrolisis terhadap total omega-3 ... 27
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Prosedur analisa sifat fisikokimia minyak ikan ... 33 Lampiran 2. Desain penggandaan skala hidrolisis ... 35 Lampiran 3. Metode Penentuan Tingkat Hidrolisis ... 38 Lampiran 4. Data pengaruh penggandaan skala terhadap bilangan asam dan tingkat
I.
PENDAHULUAN
1.1
Latar Belakang
Indonesia memiliki potensi hasil tangkapan ikan laut yang sangat melimpah. Produksi ikan hingga triwulan II tahun 2012 mencapai 14,86 juta ton dengan potensi perikanan tangkap di perairan umum mencapai 6,4 juta ton ikan per tahun (Malau, 2012). Salah satu jenis ikan laut yang terdapat di perairan Indonesia adalah ikan lemuru. Ikan lemuru adalah ikan berlemak (fatty fish) karena kandungan lemaknya relatif tinggi pada saat tertentu dan bervariasi dari tahun ke tahun. Ikan mengandung berbagai nutrisi yang diperlukan oleh tubuh diantaranya adalah protein, asam lemak omega-3, vitamin, mineral, komponen bio-active, dan asam lemak tak jenuh (Anonim, 2012). Lemak ikan lemuru mengandung cukup banyak asam-asam lemak polienoat penting (EPA dan DHA) yang dianggap bermanfaat bagi kesehatan manusia. Ikan lemuru dapat diolah menjadi ikan lemuru kaleng (sarden), ikan pindang (cue), ikan asin, dan tepung ikan. Minyak ikan merupakan hasil samping pengolahan tepung ikan yang belum dimanfaatkan lebih lanjut.
Proses produksi minyak ikan meliputi proses ekstraksi dan proses pemurnian. Proses ekstraksi yang umum digunakan adalah ekstraksi basah (wet rendering) yang mencakup proses pemasakan ikan dengan menggunakan uap air panas guna merusak struktur sel dan pengepresan minyak yang telah dipanaskan. Fraksi cair yang dihasilkan dari proses pengepresan merupakan fraksi kaya minyak ikan. Fraksi cair hasil pengepresan mengandung komponen-komponen minor tersuspensi sebagai padatan protein, air, dan minyak. Pada beberapa industri, fraksi cair kaya minyak yang merupakan hasil samping proses pengolahan diambil dan dijual. Umumnya, minyak ikan ini dimanfaatkan untuk keperluan pengolahan petis, pakan ternak, dan industri kulit.
Minyak hasil samping pengalengan dan penepungan ikan masih mengandung asam lemak omega-3 dalam jumlah tinggi. Asam lemak omega-3 adalah PUFAs yang memiliki lebih dari satu ikatan rangkap dalam konfigurasi cis. Minyak ikan merupakan sumber asam lemak tidak jenuh berupa eikosapentanoat (EPA) dan asam dokosaheksanoat (DHA) yang penting bagi pertumbuhan dan kesehatan. Asam lemak omega-3 merupakan salah satu kelompok asam lemak tidak jenuh yang memiliki ikatan rangkap pertama pada posisi atom C (karbon) nomor tiga yang dihitung dari gugus metil terujung. Asam-asam lemak alami yang tergolong asam lemak omega-3 adalah asam linolenat, asam eikosapentanoat (EPA), dan asam dekosaheksanoat (DHA). Asam lemak yang dominan dalam omega-3 adalah EPA dan DHA. Sebagai contoh, Estiasih (1996) menunjukkan bahwa minyak ikan hasil samping pengalengan ikan lemuru yang diambil dari Muncar-Banyuwangi pada bulan Juni 1995 mengandung asam lemak omega-3 sebesar 26,79% dengan asam eikosapentaenoat (EPA=eicosapentaenoicacid, C20:5 omega-3) sebesar 13,70% dan asam dokosaheksaenoat (DHA =
45o
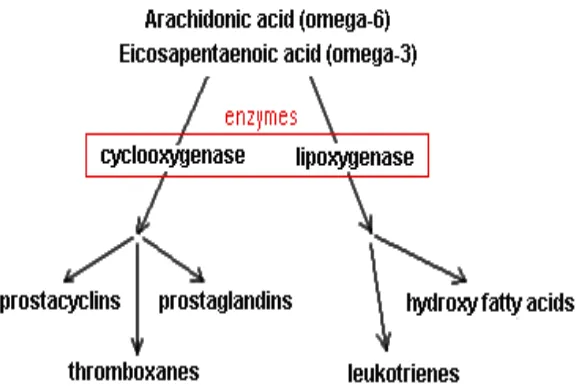
Manusia dan beberapa jenis mamalia dapat mensintesis asam lemak jenuh dan beberapa asam lemak tak jenuh tunggal dari gugus karbon yang terkandung dalam bahan pangan seperti karbohidrat dan protein. Namun, manusia tidak dapat mensintesis asam lemak omega-3. Hal ini dikarenakan manusia tidak memiliki enzim yang dapat memutuskan ikatan pada rantai karbon nomor tiga dari asam lemak tak jenuh jamak sumbernya. Untuk memenuhi kebutuhan omega-3, manusia umumnya mengkonsumsi suplemen omega-3 atau kosentrat asam lemak omega-3 yang telah mengalami proses pengolahan lebih lanjut seperti proses enkapsulasi. DHA berperan penting dalam fungsi kerja sistem saraf dan membran sel retina yang mempengaruhi penglihatan (Etherton, 2002). EPA berperan penting dalam sistem kekebalan tubuh dan respon terhadap luka. EPA dalam membran sel dapat dimetabolisme oleh enzim cyclooxynase dan lipoksigenase untuk membentuk prostaglandins dan leukotrienes (Calder, 2002). Minyak ikan ini belum dimanfaatkan secara optimal sebagai sumber asam lemak omega-3, padahal sampai saat ini Indonesia masih mengimpor minyak ikan untuk sumber asam lemak omega-3.
C dapat dilakukan untuk menghasilkan asam lemak omega-3 dari minyak hasil samping penepungan ikan lemuru yang telah diperkaya dengan pelarut organik heksana.
1.2
Tujuan
Penelitian hidrolisis minyak ikan lemuru dengan lipase A. niger bertujuan untuk :
1. Mendapatkan kondisi proses optimum untuk metode hidrolisis enzimatik minyak ikan lemuru menggunakan lipase dari Aspergillus niger.
II. TINJAUAN PUSTAKA
2.1
Minyak Ikan Lemuru
Minyak ikan merupakan minyak hasil ekstraksi komponen lemak dalam jaringan tubuh ikan. Minyak terdapat pada daging ikan, baik ikan yang memiliki daging berwarna putih maupun ikan yang memiliki daging berwarna merah. Minyak juga terdapat pada bagian tubuh ikan yang lain terutama hati dengan kadar garam yang beragam (Estiasih, 2009). Tiap ikan mengandung daging putih dan daging merah dalam proporsi yang berbeda-beda bergantung pada jenis ikan. Daging merah pada ikan terdapat di bawah permukaan kulit bagian samping. Daging merah pada ikan kurang disukai karena menimbulkan rasa pahit dan memiliki kadar lemak lebih tinggi. Tingginya kadar lemak daging merah pada ikan menyebabkan terjadinya proses penurunan mutu dan menimbulkan aroma tengik lebih cepat, sehingga daging ini umumnya dibuang dalam proses pengalengan ikan. Ikan yang memiliki daging berwarna putih diantaranya ikan kakap, ikan kerapu, ikan tenggiri, dan ikan cunang. Ikan yang memiliki daging berwarna merah adalah ikan salmon. Ikan laut dikelompokkan menjadi dua, yaitu ikan pelagik dan ikan demersal. Ikan pelagik adalah kelompok ikan yang hidup di permukaan air, seperti ikan tongkol, makarel, lemuru, dan hering. Ikan demersal adalah ikan yang hidup di dasar laut, seperti ikan cod, kakap, dan hiu.
Sebagian besar minyak ikan terdiri atas trigliserida dan sebagian kecil terdiri atas fosfolipid. Semua jenis ikan memiliki sejumlah kecil fosfolipid dalam sel tubuhnya. Sebagian besar fosfolipid pada ikan laut adalah fosfatidilkolin (lesitin) atau fosfatidiletanolamin (sefalin). Fosfolipid pada ikan laut dalam jumlah kecil adalah inositol fosfatida, serebrosida, dan sfingomielin. Minyak ikan mengandung sejumlah senyawa seperti hidrokarbon, sterol, vitamin, dan pigmen (Estiasih, 2009). Sifat minyak ikan ditentukan oleh jenis asam lemak penyusunnya.
Minyak ikan dapat diperoleh dari beberapa jenis ikan laut, salah satunya yang hidup di perairan Indonesia adalah ikan lemuru. Ikan lemuru (Sardinella lemuru) adalah jenis ikan yang mempunyai nilai ekonomis dan potensi cukup besar, serta mempunyai prospek pemanfaatan yang baik. Klasifikasi ikan lemuru adalah sebagai berikut :
Kingdom : Animalia Filum : Chordata Subfilum : Vertebrata Kelas : Actinopterygii Ordo : Clupeiformes Famili : Clupeidae Genus : Sardinella Spesies : Sardinella lemuru
Sumber : University of Michigan (2012)
Gambar 1. Sardinella lemuru (Hakim, 2012)
Daerah penyebaran ikan lemuru adalah daerah pantai yang berhadapan dengan laut bebas, diantaranya adalah Selat Bali, perairan bagian timur Sumba, perairan bagian utara Kalimantan, Pantai India, Thailand, Kamboja, Australia, dan Afrika Timur. Konsentrasi terbesar terdapat di Selat Bali dan sekitarnya (Direktorat Jenderal Perikanan, 1990).
Dalam pemanfaatannya, ikan lemuru dapat diolah menjadi ikan lemuru kaleng (sardencis), ikan pindang (cue), ikan asin, dan limbahnya dapat diolah menjadi tepung ikan. Ikan lemuru juga dapat digunakan sebagai umpan. Ikan lemuru adalah ikan berlemak (fatty fish) dengan kandungan lemak relatif tinggi pada saat tertentu dan bervariasi dari tahun ke tahun. Hal ini sering menjadi kendala dalam usaha pengolahan ikan lemuru.Menurut Winarno (1993) ikan lemuru termasuk kelompok ikan berlemak medium yaitu kelompok ikan dengan kandungan lemak berkisar 2-5%. Semakin besar ukuran tubuh ikan dan masak gonadanya kandungan lemak total ikan lemuru semakin rendah. Lemuru mengandung lebih dari 10% lemak dan sebagian besar lemak disimpan di dalam rongga perut (belly cavity). Tingkat kandungan lemak mencapai titik minimum menjelang dan sesudah memijah, sementara di dalam rongga perut tidak terdapat cadangan lemak. Ikan lemuru yang hidup di perairan Indonesia yang beriklim tropis menyebabkan kandungan lemaknya lebih rendah dibandingkan ikan sardine dari daerah beriklim sedang.
Dalam kehidupan ikan lemuru faktor lingkungan sangat berpengaruh. Pada saat musim.angin Tenggara arus Equator Selatan mengalir ke arah Barat di sepanjang pantai Selatan Lombok - Bali - Jawa sehingga menyebabkan terjadinya satu fenomena alam, yang dikenal sebagai up-welling. Keadaan ini menyebabkan perairan selat Bali menjadi sangat subur dan menyediakan banyak makanan bagi ikan lemuru selama musim ikan. Akibatnya, kandungan lemak total dan kandungan asam lemak polienoat ikan lemuru relatif tinggi. Sedangkan sebelum musim ikan, kesuburan perairan dan kandungan lemak total relatif rendah. Kesuburan perairan dianggap sebagai faktor lingkungan utama yang penting. Peranan up-welling terhadap kandungan lemak total dan profil asam lemaknya dapat dilihat dari komposisi asam lemak maupun variasi kandungan lemak total. Selama up-welling
sebagai pakan ternak. Minyak mentah ikan lemuru mengandung fraksi tersabunkan, sejumlah besar produk primer dan sekunder dari oksidasi lemak yang berikatan dengan warna, bau, rasa, dan kotoran. Minyak ikan sebagai hasil samping industri penepungan ikan lemuru memiliki kandungan asam lemak omega-3 sebesar 19,29% dan mutunya masih memenuhi standar International Association of Fish Meal Manufacturer (Kurniasari, 2005).
2.2
Asam Lemak Omega-3
Lipid dapat dikelompokkan menjadi empat kelas, yaitu lipid netral, fosfatida, spingolipid, dan glikolipid. Minyak dan lemak termasuk salah satu golongan lipid yaitu lipid netral. Minyak dan lemak yang telah diekstrak dari sumbernya mengandung sejumlah kecil komponen selain trigliserida, seperti lipid kompleks (lesithin, cephalin, fosfatida, dan glikolipid), sterol (baik bebas maupun terikat dengan asam lemak), asam lemak bebas, lilin, pigmen larut lemak, dan hidrokarbon. Komponen-komponen tersebut mempengaruhi warna dan flavor produk turunannya serta berperan dalam proses ketengikan. (Ketaren, 2005).
Minyak atau lemak terbentuk dari tiga asam lemak atau disebut trigliserida. Trigliserida yang menyusun lemak atau minyak merupakan trigliserida campuran yaitu asam lemak rantai panjang yang berikatan dengan ester dari gliserol. Asam lemak terdiri atas komponen karbon, hidrogen, dan oksigen yang tersusun menjadi rangka rantai karbon dan berikatan dengan gugus karboksil (-COOH) pada salah satu ujungnya. Berdasarkan pada jenis ikatannya, asam lemak dapat dikelompokkan menjadi dua, yaitu asam lemak jenuh dan asam lemak tak jenuh. Asam lemak jenuh adalah asam lemak yang tersusun atas ikatan tunggal atom karbon pada rantai karbonnya. Contoh asam lemak jenuh ialah asam laurat, asam palmitat, dan asam stearat. Asam lemak tak jenuh adalah asam lemak yang tersusun atas sejumlah ikatan rangkap atom karbon pada rantai karbonnya. Contoh asam lemak tak jenuh adalah asam oleat, asam linoleat, dan asam linolenat. Berdasarkan pada jumlah ikatan rangkapnya, asam lemak tak jenuh dapat dikelompokkan menjadi dua, yaitu asam lemak tak jenuh tunggal atau
Monounsaturated Fatty Acid (MUFAs) dan asam lemak tak jenuh jamak atau Polyunsaturated Fatty Acid (PUFAs). MUFAs merupakan asam lemak tak jenuh yang hanya terdiri atas satu ikatan rangkap. PUFAs merupakan asam lemak tak jenuh yang terdiri atas lebih dari satu ikatan rangkap. Jenis-jenis asam lemak yang umum dan sumbernya disajikan dalam Tabel 1.
Asam lemak tak jenuh jamak yang penting diantaranya adalah asam lemak omega-3. Omega-3 adalah PUFAs yang memiliki lebih dari satu ikatan rangkap dalam konfigurasi cis. Pada rantai asam lemak yang memiliki satu atau lebih ikatan rangkap dapat terbentuk isomer geometris. Ikatan rangkap akan mengikat karbon secara erat dan mencegah terjadinya perputaran atom karbon di sepanjang sumbu ikatan. Hal ini menyebabkan terbentuknya konfigurasi isomer. Konfigurasi isomer terdiri atas dua kelompok, yaitu konfigurasi isomer cis dan konfigurasi isomer trans. Kedua konfigurasi isomer tersebut menggambarkan orientasi atom hidrogen yang berhubungan dengan ikatan rangkap. Konfigurasi isomer cis merupakan konfigurasi isomer dengan orientasi atom hidrogen berada pada sisi yang sama. Konfigurasi isomer trans merupakan konfigurasi isomer dengan orientasi atom hidrogen pada sisi yang berlawanan atau berseberangan.Isomer cis bersifat tidak stabil, sedangkan isomer trans
Tabel 1. Jenis-jenis asam lemak dan sumbernya Nama Umum Jumlah Atom Karbon Jumlah Ikatan Rangkap
Nama Ilmiah Sumber
Asam Butirat 4 0 Asam Butanoat Lemak susu
Asam Kaproat 6 0 Asam Heksanoat Lemak susu, minyak sawit,
minyak kelapa
Asam Kaprilat 8 0 Asam Oktanoat Minyak kelapa
Asam Kaprat 10 0 Asam Dekanoat Minyak kelapa, minyak sawit
Asam Laurat 12 0 Asam Dodecanoat Minyak kelapa, minyak inti sawit
Asam Miristat 14 0 Asam Tetradekanoat
Minyak inti sawit, minyak pala, susu ternak, minyak babi, minyak
ikan hiu
Asam Palmitat 16 0 Asam Heksadekanoat Minyak kelapa sawit, lemak
hewani
Asam Palmitoleat 16 1 Asam 9-heksadekanoat Lemak hewan
Asam Stearat 18 0 Asam Oktadekanoat Lemak hewan, minyak nabati
Asam Oleat 18 1 Asam 9-oktadekanoat Minyak zaitun, sebagian besar
minyak dan lemak
Vaccenic acid 18 1 Asam 11-oktadekanoat Lemak susu
Asam Linoleat 18 2 Asam
9,12-oktadekadinoat Minyak biji kapas
Asam
Alfa-linolenat (ALA) 18 3
Asam
9,12,15-oktadekatrienoat Minyak biji lin
Asam
Gamma-linoleat (GLA) 18 3
Asam
6,9,12-oktadekatrienoat Borage oil
Asam Arachidat 20 0 Asam Eikosanoat Minyak kacang, minyak ikan
Asam Gadoleat 20 1 Asam 9-eikosanoat Minyak ikan herring, minyak hati,
sperma ikan paus Asam
Arachidonat 20 4
Asam
5,8,11,14-eikosatetraenoat Minyak hati babi
EPA 20 5
5,8,11,14,17-eikosapentaenoat Minyak ikan
Asam Behenat 22 0 Asam Dokosanoat Rapeseed oil, lemak mentega
Erucic acid 22 1 Asam 13-dokosanoat Rapeseed oil
DHA 22 6 Asam
4,7,10,13,16,19-dokosaheksanoat Minyak ikan
Asam Lignoserat 24 0 Asam Tetrakosanoat Minyak kacang, sphingomyelin,
minyak kacang tanah Sumber : Ketaren (2005)
(18:03 n-3, ALA), asam stearidonic (18:04 n-3, SDA), asam eikosapentanoat (20:05 n-3, EPA), dan asam dokosaheksanoat (22:06 n-3, DHA) (Collins, 2010). Asam alfalinolenat umumnya terkandung dalam benih, minyak yang berasal dari tumbuhan (canola, flaxseed, dan kacang kedelai), tumbuhan berdaun hijau, kacang-kacangan, dan biji-bijian.
Manusia dan beberapa jenis mamalia dapat mensintesis asam lemak jenuh dan beberapa asam lemak tak jenuh tunggal dari gugus karbon yang terkandung dalam bahan pangan seperti karbohidrat dan protein. Namun, manusia tidak dapat mensintesis asam lemak omega-3. Hal ini dikarenakan manusia tidak memiliki enzim yang dapat memutuskan ikatan pada rantai karbon nomor tiga dari asam lemak tak jenuh jamak sumbernya. Asam lemak omega-3 merupakan nutrisi penting bagi manusia. Asam lemak yang dapat disintesis oleh manusia adalah asam lemak rantai panjang. Asam lemak rantai panjang yang merupakan sumber omega-3 adalah asam alfa-linolenat atau ALA. Struktur kimia ALA ditunjukkan pada Gambar 2. Asam lemak turunan ALA adalah EPA (eicosapentaenoic acid; 20:5; n-3) dan DHA (docosahexaenoic acid; 22:6; n-3). Struktur kimia EPA dan DHA ditunjukkan pada Gambar 3.
Gambar 2. Struktur kimia asam alfa-linolenat (ALA) (Anonim, 2012)
Gambar 3. Struktur kimia EPA dan DHA (Anonim, 2012)
dicerna di dalam tubuh dan diubah melalui sejumlah tahapan menjadi EPA dan DHA seperti yang ditunjukkan pada Gambar 4. ALA dapat berperan sebagai prekursor sintesis EPA dan DHA dalam tubuh manusia, tetapi jalur sintesis ini memiliki kapasitas yang terbatas dan bervariasi antar individu (King, 2013).
Gambar 4. Sintesis EPA dan DHA (Anonim, 2012)
Asam lemak omega-3 merupakan komponen struktural penting dari membran sel. Omega-3 yang berikatan dengan fosfolipid mempengaruhi sejumlah sifat membran, seperti fluiditas, fleksibilitas, permeabilitas, dan aktivitas enzim dalam membran (Stillwell, 2003). DHA berperan penting dalam fungsi kerja sistem saraf dan membran sel retina yang mempengaruhi penglihatan. DHA merupakan nutrisi bagi otak yang mempengaruhi kinerja otak dalam pengendalian sistem saraf dan penglihatan pada manusia dan hewan (Etherton, 2002). EPA berperan penting dalam sistem kekebalan tubuh dan respon terhadap luka. EPA dalam membran sel dapat dimetabolisme oleh enzim
Gambar 5. Metabolisme asam lemak C20 cis (Zamora, 2013)
Asam lemak omega-3 dalam ikan dipengaruhi oleh beberapa faktor, seperti jenis makanan, jenis ikan, tahap perkembangan, dan tahap pemijahan ikan. Perbedaan spesies ikan menyebabkan perbedaan kadar asam lemak omega-3. Ikan dari perairan tropis mempunyai kadar asam lemak omega-3 yang lebih rendah dibandingkan ikan yang hidup di perairan subtropis dan dingin. Ikan yang berasal dari perairan dalam cenderung mengandung asam lemak omega-3 lebih tinggi dibandingkan ikan yang hidup di permukaan air (Estiasih, 2009).
2.3
Hidrolisis Enzimatik
Hidrolisis merupakan reaksi pembentukan gliserol dan asam lemak bebas melalui pemecahan molekul lemak dan penambahan elemen air. Hidrolisis merupakan salah satu reaksi yang terjadi pada produk atau bahan pangan berlemak (Zarevucka dan Wimmer, 2008). Reaksi hidrolisis pada trigliserida terdiri atas tiga tahapan reaksi maju dan mundur. Pada setiap reaksi maju, satu molekul air dikonversi menjadi asam lemak. Pada reaksi mundur gliserol bereaksi dengan asam lemak menjadi monogliserida (Minami, 2006). Hidrolisis dapat digolongkan menjadi hidrolisis murni, hidrolisis katalis asam, hidrolisis katalis basa, hidrolisis gabungan (alkali dan air), dan hidrolisis dengan katalis enzim. Berdasarkan pada fase reaksi, hidrolisis dikelompokkan menjadi dua, yaitu hidrolisis fase cair dan hidrolisis fase gas. Pada hidrolisis fase gas, air berperan sebagai senyawa penghidrolisis dan reaksi berlangsung pada fase uap. Hidrolisis fase cair terdiri atas empat jenis hidrolisis, yaitu hidrolisis murni, hidrolisis asam berair, hidrolisis alkali berair, dan hidrolisis enzimatik (BeMiller, 2009).
Faktor-faktor yang mempengaruhi reaksi hidrolisis antara lain katalisator, suhu dan tekanan, pencampuran (pengadukan), dan perbandingan zat pereaksi. Katalisator merupakan senyawa atau bahan yang digunakan untuk mempercepat terjadinya suatu reaksi. Katalisator yang umum digunakan adalah enzim, karena bekerja secara cepat. Selain enzim, katalisator yang juga banyak digunakan ialah asam. Jenis asam yang digunakan tidak memberikan pengaruh secara signifikan terhadap kecepatan reaksi. Faktor yang mempengaruhi kecepatan reaksi adalah konsentrasi ion H+ yang terkandung dalam asam yang digunakan sebagai katalisator. Pemilihan jenis asam berdasarkan pada sifat garam yang terbentuk, sehingga diupayakan penggunaan konsentrasi asam yang rendah. Asam klorida merupakan jenis asam yang banyak digunakan dalam industri. Suhu berpengaruh terhadap kecepatan reaksi. Pengaruh suhu ini mengikuti persamaan Arhenius, dimana semakin tinggi suhu, maka reaksi berjalan semakin cepat. Pencampuran atau pengadukan menyebabkan atom-atom dalam zat pereaksi saling bertumbukkan. Pada sistem curah, pencampuran dilakukan dengan bantuan pengaduk atau alat pengocok. Sedangkan pada proses kontinyu, pencampuran dilakukan dengan mengatur aliran dalam tangki reaktor. Perbandingan zat pereaksi mempengaruhi jalannya reaksi. Pereaksi dalam jumlah berlebih dapat menggeser keseimbangan reaksi ke arah kanan.
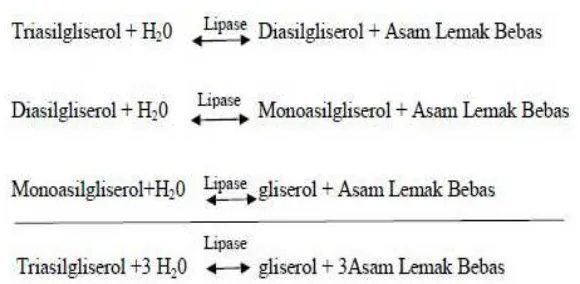
Trigliserida merupakan ester dari asam lemak dan gliserol. Asam lemak dapat dihasilkan dengan memecah ikatan esternya. Salah satu cara untuk memecah ikatan ester tersebut adalah dengan proses hidrolisis atau yang dikenal dengan istilah hidrolisis trigliserida. Hidrolisis trigliserida dapat dilakukan pada kondisi asam dan basa. Hidrolisis oleh asam bersifat bolak-balik (reversible). Hidrolisis oleh basa bersifat tidak dapat balik (irreversible) pada akhir reaksi, yaitu asam yang terbentuk selama reaksi tidak dapat bereaksi kembali dengan alkohol. Teknik lain yang dapat diterapkan adalah metanolisis atau penggunaan metanol yang dikatalisis oleh basa. Produk yang dihasilkan dari proses metanolisis ialah cairan-cairan heterogen (Dvorak, 2001). Cairan ini terbentuk dari pembentukan senyawa baru yang bersifat larut air dan minyak yaitu metil ester asam lemak. Asam lemak dapat dihasilkan melalui proses hidrolisis lanjutan. Hidrolisis lanjutan menghasilkan asam lemak dengan tingkat kemurniaan yang tinggi (Morrison, 1992). Komers et al.(1998) menyatakan bahwa reaksi hidrolisis pada trigliserida berlangsung secara bertahap, sehingga semua ikatan ester terputus dan diperoleh asam lemak bebasnya. Tahapan hidrolisis triasilgliserol menggunakan katalis enzim lipase ditunjukkan pada Gambar 6.
Gambar 6. Tahapan hidrolisis triasilgliserol (Brockman, 1984)
yang diperoleh secara alami. Hidrolisis enzimatik memberikan beberapa kemudahan dan keuntungan. Reaksi enzimatik membutuhkan kondisi yang ringan, sedikit pelarut, dan menghasilkan produk yang memenuhi konsep produksi bersih dan green chemistry. Kemudahan dan keuntungan ini menarik minat dan memberikan peluang pada proses hidrolisis minyak dan lemak dalam skala besar. Hal ini dimungkinkan karena reaksi umumnya terjadi pada kondisi reaksi yang ringan dengan kebutuhan suhu dan pH yang relatif aman, sehingga bahaya yang mungkin ditimbulkan menjadi relatif berkurang (Gunstone, 2004).
2.4
Lipase Aspergillus niger
Enzim adalah senyawa organik berupa protein yang berfungsi sebagai katalis pada proses metabolisme tubuh (biokatalisator). Enzim tersusun dari apoenzim, kofaktor, dan koenzim. Apoenzim ialah sisi enzim yang aktif. Apoenzim tersusun atas protein yang bersifat labil atau mudah berubah terhadap faktor lingkungan. Kofaktor adalah komponen non enzim. Kofaktor dapat berupa ion-ion anorganik (aktivator) maupun gugus prostetik. Aktivator berupa ion-ion logam yang berikatan lemah dengan enzim. Gugus prostetik berupa senyawa organik yang berikatan kuat dengan enzim. Contoh gugus prostetik adalah FAD (Flavin Adenin Dinucleotide). Koenzim adalah molekul organik non protein kompleks yang berfungsi untuk memindahkan gugus kimia, atom, maupun elektron dari satu enzim ke enzim lainnya. Enzim yang terikat dengan kofaktor disebut holoenzim.
Faktor-faktor yang mempengaruhi kerja enzim antara lain temperatur, derajat keasaman, aktivator dan inhibitor, konsentrasi enzim, dan konsentrasi substrat. Enzim merupakan protein yang sangat peka terhadap perubahan suhu. Peningkatan suhu dapat meningkatkan energi kinetik molekul substrat dan enzim. Peningkatan energi kinetik substrat dan enzim menyebabkan kecepatan reaksi meningkat. Namun, pada suhu yang terlalu tinggi enzim mengalami denaturasi atau kerusakan enzim. Suhu yang terlalu rendah dapat menghambat kerja enzim. Derajat keasaman (pH) mempengaruhi perubahan asam amino kunci pada sisi aktif enzim dan mempengaruhi kemampuan sisi aktif enzim untuk berikatan dengan substrat. Aktivator adalah molekul yang mempermudah enzim berikatan dengan substratnya. Inhibitor adalah molekul yang menghambat ikatan enzim dengan substratnya. Konsentrasi enzim mempengaruhi kecepatan reaksi, dimana kecepatan reaksi berbanding lurus dengan konsentrasi enzim. Peningkatan konsentrasi substrat pada jumlah enzim tetap dapat meningkatkan kecepatan reaksi. Namun, jika semua sisi aktif enzim telah berikatan dengan substrat, maka penambahan konsentrasi substrat tidak memberikan pengaruh pada peningkatan kecepatan reaksi.
Enzim diproduksi oleh sel hidup. Enzim yang bekerja di dalam sel disebut enzim intraseluler. Contoh enzim intraseluler adalah enzim katalase, yaitu enzim yang menguraikan senyawa peroksida (H2O2
Lipase (triacylglycerol acylhydrolase, E.C.3.1.1.3) adalah jenis enzim yang berperan dalam mengkatalisis sejumlah reaksi, seperti hidrolisis, interesterifikasi, esterifikasi, alkoholisis, asidolisis, dan aminolisis (Paiva, 2000). Lipase dihasilkan oleh hewan, tumbuhan, dan mikroorganisme. Lipase yang dihasilkan dari mikroorganisme memiliki potensi yang besar untuk penggunaan secara komersial karena memiliki stabilitas, selektivitas, dan permukaan substrat yang spesifik. Sejumlah literatur menyebutkan bahwa hanya beberapa lipase yang memiliki stabilitas dan kemampuan biosintesis dalam reaksi senyawa organik. Spesies mikroorganisme yang dapat menghasilkan lipase secara produktif adalah Geotrichum, Penicillium, Aspergillus, dan Rhizomucor (Candenas et al., 2001).
) yang bersifat racun menjadi air dan oksigen. Enzim yang bekerja di luar sel disebut enzim ekstraseluler. Contoh enzim ekstraseluler adalah lipase.
menjadi lebih aktif pada bagian yang mengalami kontak langsung dengan substrat yang larut sebagian pada kondisi lingkungan yang berair. Lipase dapat mengkatalisis sintesis ester dan transesterifikasi dalam media organik yang mengandung sejumlah air (Pandey et al., 1999).
Lipase mikrobial yang telah digunakan dalam industri antara lain lipase dari Candida sp. dan
Thermomyces sp. Fungi dapat menghasilkan enzim lipase. Kelompok fungi aspergilli diketahui merupakan sumber potensial penghasil lipase mikrobial. Lipase mikrobial dapat dihasilkan dari fungi
Aspergillus carneus, Aspergillus terreus, dan Aspergillus niger (Saxena, 2005; Kaushik, 2006).
Aspergillus niger menghasilkan produk lipase ekstraseluler yang aktif pada pH asam (Mahadik et al., 2003). Lipase ekstraseluler yang telah dimurnikan bersifat khas karena bekerja secara spesifik untuk memutus ikatan pada posisi 1,3 (Mhetras, 2009). Penelitian yang dilakukan Methras and Patil (2011) menunjukkan bahwa penggunaan lipase Aspergillus niger menghasilkan kinerja proses yang tinggi, tetapi kecepatan reaksi berjalan lambat.
Lipase memiliki sifat katalitik yang luas dan umumnya bergantung pada strain
mikroorganisme penghasilnya. Lipase dalam bentuk ekstrak kasar telah sering digunakan untuk sintesis pembentukan blok kiral dan senyawa enansiomer. Sifat katalitik seperti spesifitas, enansioslektivitas, dan parameter operasional seperti termostabilitas dan pH optimum saling terkait. Sifat keterkaitan ini menentukan rentang aplikasi dari enzim dan jenis prosesnya (Pera et al., 2006).
2.5
Penggandaan Skala Hidrolisis
Penggandaan skala merupakan suatu cara untuk meningkatkan jumlah atau kapasitas dari suatu alat atau proses untuk menghasilkan sesuatu. Penggandaan skala umumnya terkait dengan proses mikrobiologi yaitu proses dengan menggunakan mikroorganisme dan produk turunannya. Fungsi penggandaan skala dalam pengembangan mikrobiologi adalah menciptakan penemuan proses baru dan memperbaiki kultur mikroorganisme , mengembangkan galur mikroorganisme terpilih, serta penyempurnaan medium dan peralatan proses yang digunakan. Penggandaan skala akan mempengaruhi perubahan faktor fisik proses. Faktor fisik yang berubah sejalan dengan berubahnya skala adalah perpindahan massa, kemampuan pencampuran, penyebaran tenaga, dan laju geser. Parameter translasi merupakan koordinat titik pusat elipsoid (x,y,z). Menurut Wang et al. (1978), beberapa parameter translasi yang umumnya diterapkan dalam penggandaan skala, antara lain :
1. Laju perpindahan oksigen volumetrik tetap (kL 2. Kecepatan impeller tetap (pND
a)
i
3. Masukkan tenaga volumetrik tetap (Pg/V) )
4. Waktu pencampuran seimbang 5. Bilangan Reynolds (NRe
6. Pengawasan umpan balik untuk menjamin besarnya faktor kunci lingkungan yang tepat ) yang sama atau faktor-faktor momentum
Tatterson (1991) menyatakan bahwa terdapat 3 komponen alat pencampuran secara konvensional, yaitu tangki (vessel), pengaduk (impeler), dan baffle. Vortex adalah cekungan permukaan media yang terbentuk pada bagian tengah tangki yang disebabkan oleh adanya gaya tangensial. Vortex menyebabkan aliran pada tangki bersifat horizontal, sehingga pencampuran tidak dapat berlangsung dengan baik. Baffle digunakan untuk mencegah terbentuknya vortex pada cairan yang memiliki kekentalan rendah. Baffle tidak dibutuhkan pada fluida yang memiliki kekekntalan tinggi, dimana vortex tidak menjadi suatu masalah (Edwards dan Baker, 1992).
Pengaduk mempunyai dua fungsi utama, yaitu untuk mengurangi ukuran gelembung-gelembung udara, sehingga luasan permukaan lebih besar untuk perpindahan oksigen dan mengurangi laju difusi, serta untuk menjaga kondisi lingkungan yang seragam pada seluruh isi tangki. Propeller, turbin, dan paddle umumnya digunakan pada pencampuran bahan yang memiliki kekentalan rendah dan beroperasi pada putaran dengan kecepatan tinggi. Ketiga jenis pengaduk tersebut baik digunakan untuk mencampur bahan yang memiliki viskositas rendah seperti cairan dengan cairan, gas dengan cairan, maupun padatan dengan cairan. Pada pencampuran bahan yang memiliki viskositas tinggi digunakan pengaduk tipe anchor, helical ribbon, dan helical screw (Edwards dan Baker, 1992).
Pola aliran pada suatu tangki berpengaduk sangat dipengaruhi oleh kecepatan pengadukan, jenis pengaduk, dan sifat reologi bahan yang diaduk (Ranade dan Joshi, 1990). Meskipun dengan fluida dan kecepatan pengadukan yang sama, penggunaan pengaduk yang berbeda akan menghasilkan pola aliran yang berbeda pula.
Informasi mengenai reologi merupakan faktor penting dalam sistem aliran laminar guna membuat perhitungan yang memadai dan proses skala besar. Pada proses pencampuran, salah satu sifat bahan yang sangat penting untuk dipertimbangkan adalah sifat reologi bahan. Reologi menurut Mackay (1988) adalah ilmu tentang sifat aliran suatu bahan. Menurut sifat reologinya, fluida dapat dibagi menjadi dua golongan besar, yaitu fluida Newtonian dan fluida non-Newtonian. Pada fluida Newtonian, nilai kekentalan adalah konstan dan tidak dipengaruhi oleh nilai laju geser, tetapi dipengaruhi oleh suhu dan tekanan. Sedangkan fluida non-Newtonian, nilai kekentalan merupakan fungsi dari laju geser.
III. METODOLOGI
3.1 Alat dan Bahan
Peralatan yang digunakan dalam proses hidrolisis minyak ikan ialah shaker waterbath, motor pengaduk 110 V, batang pengaduk dengan diameter 5,2 cm, wadah gelas berdiameter 6 cm dan 11 cm, sudip, pipet mikro, gelas piala, voltage converter dan alumunium foil. Sedangkan peralatan yang digunakan untuk analisa ialah erlenmeyer, gelas ukur, pipet tetes, penangas, alumunium foil, corong pemisah, dan buret. Pada penelitian ini juga digunakan beberapa peralatan pendukung, seperti neraca analitik, waterbath, dan Gas Chromatography Mass Spectrometry (GC-MS).
Bahan-bahan yang diperlukan dalam hidrolisis antara lain minyak ikan lemuru yang diperoleh dari daerah Muncar Banyuwangi, enzim lipase Aspergillus niger yang diperoleh dari Amano Pharmaceutical Manufacturing Co., buffer sitrat fosfat (0,1 M), aquades, pelarut organik heksana, metanol, dan gas nitrogen murni. Sedangkan bahan-bahan yang digunakan untuk analisa ialah alkohol netral, indikator phenolphtalein, KOH 0,1 N, KOH beralkohol, serta HCl 0,5 N.
3.2
Waktu Dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Februari hingga Desember 2012. Penelitian pada tahap hidrolisis dilakukan di Laboratorium Teknologi Kimia, sedangkan tahap analisa dilakukan di Laboratorium Pengawasan Mutu dan Laboratorium Dasar Ilmu Terapan milik Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor, serta Laboratorium Forensik MABES POLRI.
3.3
Metode Penelitian
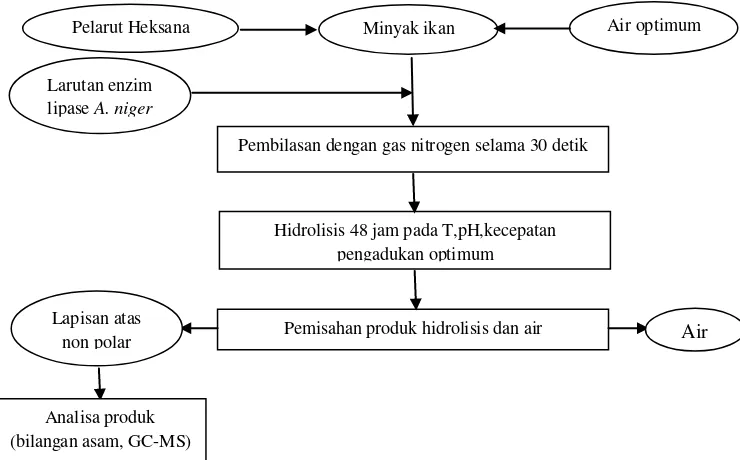
Gambar 7. Diagram alir tahapan penelitian
Tahapan persiapan media dan proses hidrolisis enzimatik minyak ikan lemuru untuk menghasilkan omega-3 dapat dilihat pada Gambar 8. Kondisi proses hidrolisis enzimatik mengacu pada penelitian terdahulu yang dilakukan Octavia (2010) yang menyatakan bahwa kondisi optimum hidrolisis enzimatik minyak ikan lemuru menggunakan enzim lipase dari Aspergillus niger adalah pada suhu 45oC dan pH buffer 5 dengan perbandingan 6 ml buffer terhadap 4 gr minyak, menggunakan minyak ikan lemuru yang ditambahkan pelarut organik heksana sebesar 1/3 volume minyak yang telah ditambahkan buffer. Minyak ditambahkan air sebesar 5% v/v minyak. Minyak ikan dihidrolisis selama 48 jam. Formulasi media dan desain penggandaan skala lebih rinci dapat dilihat pada Lampiran 2.
Gambar 8. Diagram alir hidrolisis enzimatik minyak ikan lemuru Karakterisasi minyak ikan
Mulai
Penentuan skala penggandaan hidrolisis
Penentuan pengaruh penggandaan skala terhadap bilangan asam dan tingkat hidrolisis minyak ikan
Penentuan hubungan tingkat hidrolisis dengan kandungan total
Selesai
Pelarut Heksana Minyak ikan Air optimum
Pembilasan dengan gas nitrogen selama 30 detik Larutan enzim
lipase A. niger
Hidrolisis 48 jam pada T,pH,kecepatan pengadukan optimum
Pemisahan produk hidrolisis dan air Lapisan atas
non polar Air
3.3.1
Karakterisasi Minyak Ikan
Minyak ikan yang digunakan pada penelitian ini telah mengalami proses pemurnian oleh produsen yaitu indutri pengalengan ikan lemuru dari daerah Muncar, Banyuwangi. Karakterisasi minyak ikan berupa sifat fisikokimia minyak dilakukan pada awal pelaksanaan penelitian sebagai acuan kualitas minyak ikan yang digunakan sebagai bahan baku. Sifat fisikokimia yang diamati meliputi bilangan asam, bilangan penyabunan, dan kadar asam lemak bebas (%FFA). Prosedur karakterisasi minyak ikan lemuru dapat dilihat pada Lampiran 1.
3.3.2
Penentuan Desain Penggandaan skala
Desain penggandaan skala hidrolisis enzimatik minyak ikan lemuru menggunakan lipase A. niger untuk produksi omega-3 meliputi penentuan besaran skala yang digunakan, rasio perbandingan antara diameter wadah terhadap diameter pengaduk, dan kecepatan pengadukan penggandaan skala. Besaran skala yang didesain adalah 5, 10, 20, dan 50 kali skala hidrolisis enzimatik minyak ikan lemuru terkecil. Wadah yang digunakan terdiri dari dua, yaitu wadah berukuran kecil dan wadah berukuran besar. Desain kecepatan pengadukan dirancang berdasarkan tingkat hidrolisis optimal yang dapat digandakan. Desain penggandaan skala lebih rinci dapat dilihat pada Lampiran 2.
3.3.3
Penentuan Pengaruh Ratio Dt/Di dan Kecepatan Pengadukan terhadap
Bilangan Asam
Peningkatan skala hidrolisis dengan penggunaan ratio antara diameter wadah dan diameter pengaduk (Dt/Di) dan kecepatan pengadukan mempengaruhi produk hidrolisis. Pengaruh ini dapat diketahui dengan melakukan analisa bilangan asam produk. Analisa bilangan asam produk hidrolisis dilakukan duplo. Prosedur pengujian bilangan asam dapat dilihat pada Lampiran 1.
3.3.4
Penentuan Pengaruh Ratio Dt/Di terhadap Tingkat Hidrolisis
Ratio antara diameter wadah dan diameter pengaduk (Dt/Di) dan kecepatan pengadukan mempengaruhi produk hidrolisis untuk menghasilkan omega-3 yang diinginkan. Bilangan asam produk hidrolisis digunakan untuk menghitung tingkat hidrolisis minyak ikan. Analisa tingkat hidrolisis dilakukan duplo. Prosedur perhitungan tingkat hidrolisis dapat dilihat pada Lampiran 3.
3.3.5
Penentuan Hubungan Antara Tingkat Hidrolisis Tertinggi dengan Total
Omega-3 yang Dihasilkan
IV. HASIL DAN PEMBAHASAN
4.1
Karakterisasi Minyak Ikan
[image:31.595.134.505.325.387.2]Minyak ikan yang digunakan dalam penelitian ini adalah minyak ikan hasil samping industri pengalengan ikan lemuru (Sardinella sp.) dari daerah Muncar, Banyuwangi. Minyak ikan yang digunakan telah mengalami proses pemurniaan yang dilakukan oleh pihak produsen yaitu industri pengalengan ikan itu sendiri. Karakterisasi minyak ikan dilakukan untuk mengetahui kondisi dan karakter bahan baku yang akan digunakan dalam proses hidrolisis enzimatik. Karakterisasi minyak ikan meliputi analisa terhadap bilangan asam, bilangan penyabunan, dan kadar asam lemak bebas (FFA) bahan baku. Hasil karakterisasi minyak ikan disajikan pada Tabel 2.
Tabel 2. Hasil karakterisasi sifat fisikokimia minyak ikan
Karakteristik Satuan Nilai a
Bilangan asam mg KOH/g minyak 2,718 3,26
Bilangan penyabunan mg KOH/g minyak 184,38948 204,81
Kadar asam lemak bebas (FFA) % 1,36 1,49
a
Octavia (2010)
Data pada Tabel 2 menunjukkan bahwa minyak ikan lemuru yang digunakan sebagai bahan baku dalam proses hidrolisis enzimatik dengan menggunakan katalisator berupa enzim lipase dari
pemurnian terlebih dahulu. Hal ini diperkuat dari penampakan fisik minyak ikan hasil samping pengalengan ikan lemuru yang berwarna kuning keemasan, jernih, dan berbau segar khas minyak ikan. Faktor umur minyak ikan juga berpengaruh terhadap jumlah asam lemak bebas dalam minyak ikan. Hasil pengujian bilangan asam menunjukkan bahwa minyak ikan yang digunakan masih relatif segar atau merupakan minyak hasil samping dari proses pengolahan ikan lemuru terbaru. Minyak ikan belum mengalami proses penyimpanan yang dapat menyebabkan peningkatan jumlah asam lemak bebasnya.
Bilangan penyabunan adalah jumlah miligram KOH yang diperlukan untuk menyabunkan satu gram minyak atau lemak. Tiga molekul KOH akan bereaksi dengan satu molekul minyak. Besar bilangan penyabunan tergantung dari berat molekul minyak. Minyak yang terdiri dari asam lemak berantai panjang memiliki bobot molekul lebih tinggi. Besar bilangan penyabunan dan berat molekul minyak berbanding terbalik (Ketaren, 2005). Bilangan penyabunan minyak ikan yang diujikan adalah 184,38948 mg KOH/g minyak. Bilangan penyabunan ini lebih kecil dibandingkan dengan bilangan penyabunan minyak ikan yang digunakan dalam penelitian Octavia (2010) yaitu sebesar 204,81 mg KOH/g minyak. Nilai bilangan penyabunan minyak ikan ini nantinya digunakan untuk menghitung besarnya tingkat hidrolisis minyak ikan.
Pada pengukuran bilangan asam dan bilangan penyabunan pada lampiran 1 digunakan faktor pengali sebesar 56,1 untuk KOH dan 39,9 untuk NaOH. Faktor pengali tersebut adalah besar bobot molekul larutan yang digunakan untuk titrasi dalam pengukuran bilangan asam. Pada pengujian bilangan asam dan bilangan penyabunan minyak ikan pada penelitian ini menggunakan larutan KOH, sehingga digunakan faktor pengali sebesar 56,1.
Kadar FFA (Free Fatty Acid) merupakan ukuran kualitas minyak ikan dan dinyatakan dalam % FFA atau angka asam. Angka keasaman merupakan salah satu indikator penting penentuan mutu minyak goreng. Kadar FFA minyak ikan yang diujikan adalah sebesar 1,36%. Nilai kadar minyak ikan ini lebih kecil dari kadar minyak ikan yang digunakan dalam penelitian Octavia (2010) sebesar 1,49. Hal ini menunjukkan bahwa minyak ikan yang digunakan dalam penelitian ini merupakan minyak ikan kualitas cukup baik dan proses hidrolitik yang terjadi masih relatif kecil.
4.2
Penggandaan Skala Hidrolisis Enzimatik
4.2.1
Formulasi Media dan Kondisi Hidrolisis Enzimatik
Proses hidrolisis enzimatik menggunakan lipase Aspergillus niger pada produksi omega-3 dari minyak ikan lemuru mula-mula dilakukan pada skala kecil. Proses hidrolisis enzimatik skala kecil dilakukan pada penelitian Octavia (2010), dimana hidrolisis enzimatik dilakukan dalam skala terkecil laboratorium dengan basis minyak ikan sebesar 4 gram dengan penambahan pelarut heksana, penambahan air 5% v/v minyak, dan buffer pH 5 pada suhu 45o
menghasilkan omega-3, khususnya EPA dan DHA. Shaker waterbath dioperasikan pada suhu 50oC. Penggunaan suhu tersebut didasarkan pada suhu optimum hidrolisis enzimatik yang diperoleh dari penelitian Octavia (2010) dan wadah yang digunakan pada proses hidrolisis enzimatik. Hasil penelitian Octavia (2010) menyatakan bahwa suhu optimum hidrolisis enzimatik adalah 45oC. Pada penggandaan skala hidrolisis, wadah yang digunakan adalah wadah gelas berbentuk silinder. Untuk menaikkan dan menjaga suhu minyak ikan sebagai substrat pada suhu 45oC, maka shaker waterbath
harus diset pada suhu 50oC. Panas pada air dalam shaker waterbath akan merambat secara konveksi. Panas akan tertahan akibat adanya hambatan dari bahan gelas pada wadah yang digunakan, sehingga dibutuhkan suhu lebih tinggi untuk mencapai suhu kesetimbangan guna memanaskan minyak ikan pada suhu 45oC. Perbedaan suhu bagian luar dan bagian dalam wadah gelas tidak boleh lebih dari 27oC dan pemanasan harus dilakukan secara perlahan-lahan. Hal ini dikarenakan konduktivitas panas gelas 30 kali lebih kecil dari konduktivitas panas besi (konduktivitas besi sebesar 80.4 W·m−1·K−1). Hasil pengujian menunjukkan pemanasan minyak ikan lemuru dalam wadah gelas pada suhu 50oC dapat menaikkan suhu minyak menjadi 45o
Minyak ikan dipanaskan guna memberikan kondisi optimum bagi enzim untuk bekerja. Lipase
Aspergillus niger bekerja secara optimum pada suhu 45 C.
o
Pada proses pemanasan, minyak diletakkan dalam wadah gelas bertutup. Penggunaan wadah gelas bertujuan untuk mencegah terpaparnya minyak dengan udara yang mengandung oksigen. Wadah dari bahan gelas dianggap mewakili tangki reaktor curah berbahan kaca, dimana bahan ini merupakan bahan yang sesuai untuk melakukan proses hidrolisis secara enzimatik. Pemilihan wadah berbahan gelas didasarkan pada karakteristik gelas yang menguntungkan, seperti sifat kedap air, gas, dan bau,
inert (tidak bereaksi atau bermigrasi ke dalam bahan), sesuai untuk bahan yang mengalami proses pemanasan, transparan (isi dan proses yang terjadi dapat terlihat), rigid (kaku), dan kuat. Gelas jenis
pyrex tahan terhadap suhu tinggi. Daya tahan gelas pada umumnya mencapai 1,5 x 10
C. Pemanasan minyak ikan dilakukan dengan media perantaraan air atau tanpa kontak langsung dengan sumber panas. Pemanasan menyebabkan tiga macam perubahan kimia pada minyak dan lemak, yaitu terbentuknya peroksida dalam asam lemak tidak jenuh, peroksida berdekomposisi menjadi persenyawaan karbonil, dan polimerisasi oksidasi sebagian (Ketaren, 2005). Dekomposisi minyak dapat terjadi pada proses pemanasan bahan yang terpapar udara. Reaksi yang terjadi pada permukaan minyak akan berbeda dengan reaksi pada bagian tengah minyak. Faktor-faktor yang mempengaruhi perubahan kimia pada minyak yang dipanaskan antara lain durasi waktu pemanasan, suhu, akselerator (oksigen atau hasil-hasil proses oksidasi), dan komposisi serta posisi campuran asam lemak yang terikat pada molekul trigliserida (Ketaren, 2005). Pemanasan minyak pada kondisi terbuka (terpapar udara) menyebabkan senyawa karbonil dalam minyak bertambah selama proses pemanasan. Asam lemak jenuh murni dapat terhidrogenasi dan membentuk senyawa tidak jenuh pada suhu tinggi dengan akselerator oksigen. Asam lemak jenuh yang terkonversi menjadi senyawa tidak jenuh dengan rantai pendek ikut terbuang bersama dengan hasil kondensasi.
5 kg/cm2
asam lemak dari minyak. Hal ini menyebabkan penurunan mutu minyak ikan yang akan digunakan karena minyak akan terkonversi menjadi asam lemak bebas. Pada wadah terbuka, kotoran dan debu ringan yang melayang diudara dapat masuk ke dalam wadah dan mengkontaminasi minyak. Kontaminasi ini akan berpengaruh pada kinerja enzim.
Selama proses pemanasan, pelarut organik ditambahkan ke dalam minyak. Penambahan pelarut organik dalam minyak bertujuan untuk menciptakan lingkungan hidrofobik bagi enzim dan menekan terjadinya reaksi hidrolisis oleh air. Pelarut organik yang ditambahkan adalah heksana yang bersifat non polar (hidrofobik) dengan nilai log P 3,5. Penambahan pelarut heksana ke dalam minyak ikan akan membuka lid enzim dan meningkatkan daya larut substrat menuju sisi aktif enzim, sehingga memudahkan terjadinya reaksi hidrolisis. Krienger et al. (2004) menyatakan bahwa stabilitas protein enzim akan lebih baik dan meningkat pada penggunaan pelarut organik hidrofobik dengan nilai log P antara 2 sampai 4. Pelarut heksana mudah menguap dan memiliki bau yang sangat tajam. Wadah gelas bertutup menekan proses penguapan heksana.
Secara terpisah larutan enzim disiapkan dengan cara melarutkan sejumlah enzim dalam larutan buffer. Buffer yang digunakan adalah buffer sitrat fosfat. Buffer sitrat fosfat dibuat dalam kondisi asam. Buffer ini memiliki pH 5 dengan tujuan menciptakan lingkungan yang asam bagi proses hidrolisis secara enzimatis. Penelitian yang dilakukan oleh Octavia (2010) menunjukkan bahwa lipase
Aspergillus niger memberikan hasil terbaik pada hidrolisis dengan menggunakan media pH 5. Pernyataan ini diperkuat oleh Petersen et al. (2001) yang menyatakan bahwa lipase dari Aspergillus niger akan aktif pada kondisi lingkungan yang asam dengan aktivitas optimum pada pH 4,5-6,5. Titik isoelektrik lipase Aspergillus niger berada pada pH 4,1.
Lipase Aspergillus niger yang diproduksi oleh Amano Pharmaceutical Manufacturing Co. memiliki aktivitas enzim sebesar 12.000 U, suhu proses 30-40o
Air dibutuhkan untuk mengaktifkan sisi aktif enzim yang bersifat hidrofilik. Air diperlukan untuk integritas tiga dimensi struktur molekul enzim. Setelah air ditambahkan, larutan enzim dimasukkan ke dalam wadah berisi minyak. Penelitian yang dilakukan Octavia (2010) menyatakan penambahan air minimum pada hidrolisis minyak ikan lemuru menggunakan lipase Aspergillus niger
adalah 5% v/v. Air yang ditambahkan ke dalam minyak yang diperkaya pelarut organik akan membentuk lapisan tunggal (monolayer) dan menutup permukaan enzim. Air menjaga agar lipase dapat mengaktifkan sisi katalitiknya dan memelihara struktur alaminya. Struktur alami enzim diperlukan untuk terjadinya proses migrasi asil ke arah pembentukan produk berupa omega-3. Hal ini sesuai dengan pernyataan Turner et al. (2003) bahwa kondisi lingkungan hidrofobik aktivitas katalitik enzim tertinggi diperoleh pada penggunaan air kurang dari 10% v/v larutan.
C, dan pH 4,5-6,5 seperti tertera pada label kemasan. Aktivitas enzim sebenarnya diasumsikan sama dengan aktivitas enzim pada label. Lipase Aspergillus niger berbentuk serbuk kecokelatan dalam kemasan botol gelas berwarna gelap. Tiap botol berisi 10 gram enzim dengan aktivitas 12.000 U. Lipase Aspergillus niger dilarutkan dalam buffer pH 5 dan dilakukan proses pencampuran dengan pengadukan secara manual. Enzim yang dicampurkan ke dalam buffer pada mulanya akan menggumpal dan setelah mengalami pengadukan akan menjadi larutan yang homogen. Pencampuran enzim dan buffer membutuhkan ketepatan dan waktu yang relatif lama. Ketepatan dibutuhkan untuk memastikan enzim telah larut dan homogen dengan buffer. Enzim yang tidak tercampur dengan baik akan membentuk gumpalan berukuran kecil. Hal ini akan menurunkan kinerja enzim. Waktu yang dibutuhkan untuk melarutkan enzim adalah relatif lama, khususnya untuk menjamin enzim benar-benar tercampur dan larut dalam buffer.
5% v/v minyak dan buffer pada penggandaan skala 5 kali adalah sebesar 14,5504%. Tingkat hidrolisis minyak ikan dengan penambahan 5% v/v minyak pada penggandaan skala 5 kali adalah sebesar 11,9367%. Hasil pengujian menunjukkan bahwa penambahan air sebesar 5% v/v dihitung berdasarkan volume minyak dan buffer. Penambahan air kurang dari batas minimum menyebabkan proses hidrolisis tidak berjalan secara maksimal. Hal ini dikarenakan air dalam jumlah sedikit tidak dapat menutup keseluruhan permukaan enzim dan sisi katalitik enzim tidak teraktivasi secara optimal. Pembilasan dengan gas nitrogen dilakukan pada akhir persiapan hidrolisis enzimatik. Oksigen terperangkap dan mengisi ruang dalam wadah berisi minyak ikan. Keberadaan oksigen dapat merugikan selama proses hidrolisis berlangsung. Oksigen dapat menyebabkan terjadinya oksidasi. Oksigen dapat bereaksi dengan minyak ikan dan mengubah karakteristik minyak, khususnya pada flavor minyak ikan dan produk hidrolisis. Pembilasan dilakukan dengan cara mengalirkan sejumlah gas nitrogen ke dalam media yang telah disiapkan. Nitrogen akan berpenetrasi dan mengisi ruang dalam wadah. Nitrogen tidak bereaksi dengan media, sehingga tidak menimbulkan perubahan yang tidak menguntungkan. Hal ini sesuai dengan pernyataan Jegtvig (2013) bahwa pembilasan dan pengisian gas nitrogen juga diterapkan pada proses pengemasan bahan pangan. Cara ini telah banyak dilakukan karena mampu menjaga cita rasa produk pangan yang dikemas dan produk aman untuk dikonsumsi.
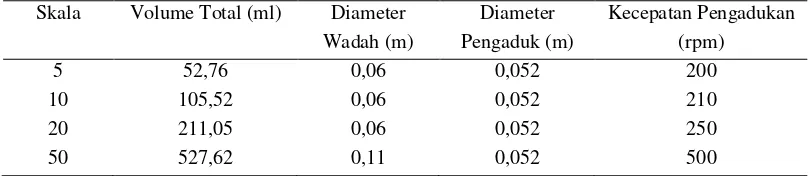
[image:35.595.116.521.467.555.2]Hidrolisis enzimatik minyak ikan untuk menghasilkan omega-3 dilakukan pada kondisi kultur curah, dimana bahan masuk pada satu tahapan dan keluar pada tahapan akhir. Oksigen dapat menyebabkan reaksi oksidasi yang tidak diinginkan pada minyak ikan. Penggandaan skala hidrolisis enzimatik minyak ikan lemuru dilakukan secara bertahap mulai dari penggandaan 5 kali hingga 50 kali. Parameter yang diamati pada penggandaan skala antara lain pengaruh rasio diameter wadah dan diameter pengaduk serta kecepatan pengadukan. Desain penggandaan skala hidrlosis enzimatik minyak ikan lemuru untuk produksi omega-3 disajikan pada Tabel 3.
Tabel 3. Desain penggandaan skala hidrolisis enzimatik
Skala Volume Total (ml) Diameter
Wadah (m)
Diameter Pengaduk (m)
Kecepatan Pengadukan (rpm)
5 52,76 0,06 0,052 200
10 105,52 0,06 0,052 210
20 211,05 0,06 0,052 250
50 527,62 0,11 0,052 500
Gambar 9. Pemisahan produk dalam corong pemisah
Proses pemisahan dalam corong pemisah menyebabkan larutan terbagi menjadi dua lapisan. Lapisan bawah berwarna kecokelatan, cair, dan keruh. Lapisan atas berwarna kekuningan, semi padat, dan mengapung. Lapisan bagian bawah terdiri dari larutan buffer, air, heksana, dan metanol. Lapisan atas terdiri atas asam lemak hasil hidrolisis dan sedikit heksana yang masih terikat. Lapisan bawah harus dipisahkan dari produk. Hasil pemisahan akan menyisakan lapisan atas yang semi padat seperti pada Gambar 10.
Gambar 10. Lapisan atas yang telah terpisah
[image:36.595.253.380.409.582.2]mencegah timbulnya api yang berdampak pada kebakaran. Produk yang telah terpisah sepenuhnya dari heksana dianalisa dengan dua uji, yaitu analisa bilangan asam dan GC-MS.
4
.2.2 Pengaruh Ratio Dt/Di dan Kecepatan Pengadukan terhadap Bilangan
Asam
[image:37.595.192.467.343.539.2]Bilangan asam merupakan analisa pada minyak untuk mengetahui jumlah asam lemak bebas dalam minyak yang telah dihidrolisis. Penggandaan skala dilakukan untuk meningkatkan produk hidrolisis yang diinginkan yaitu berupa omega-3 khususnya EPA dan DHA. Keberhasilan hidrolisis pada minyak dapat diketahui dari nilai bilangan asam. Hidrolisis yang berjalan baik akan meningkatkan jumlah asam lemak bebas dalam minyak. Hidrolisis mengubah minyak menjadi asam lemak bebas dan gliserol. Semakin tinggi nilai bilangan asam dari produk hidrolisis yang diujikan, maka semakin banyak asam lemak bebas yang terbentuk. Hal ini dapat mengindikasikan bahwa proses hidrolisis enzimatik berjalan dengan baik. Pengaruh penggandaan skala terhadap bilangan asam produk yang dihasilkan disajikan dalam Gambar 11.
Gambar 11. Kurva pengaruh ratio Dt/Di terhadap bilangan asam
Berdasarkan Gambar 11, ratio Dt/Di mempengaruhi peningkatan bilangan asam produk hidrolisis. Asam lemak bebas terbentuk dari pemotongan rantai panjang asam lemak pada posisi 1,3 untuk menghasilkan asam lemak omega-3 yang diinginkan. Data menunjukkan hidrolisis enzimatik yang dilakukan pada skala 10 kali dengan ratio Dt/Di 1,1538 meningkatkan bilangan asam produk dari 71,4921 mg KOH/g minyak menjadi 133,722 mg KOH/g minyak. Peningkatan nilai bilangan asam juga ditunjukkan pada hidrolisis skala 20 kali dengan ratio Dt/Di sebesar 1,1538 yaitu sebesar 157,2958 mg KOH/g minyak. Namun, penurunan bilangan asam terjadi pada skala hidrolisis 50 kali dengan ratio Dt/Di sebesar 2,1154 yaitu sebesar 81,3834 mg KOH/g minyak.
lipat dibandingkan dengan diameter wadah pada penggandaan skala yang lebih kecil (0,06 m). Perubahan ukuran diameter wadah tidak disertai dengan perbesaran ukuran diameter batang pengaduk. Pada penggandaan skala 5, 10 dan 20 kali berlaku persamaan (1.1) :
=
= 1,1538 (1.1)Nilai 1,1538 menunjukkan rasio diameter propeller dengan 3 pisau dan diameter wadah. Pada hidrolisis skala 50 kali, rasio diameter propeller dan diameter wadah adalah sebesar 2,1154. Hal ini menunjukkan ukuran diameter batang pengaduk yang digunakan tidak proporsional pada wadah yang lebih besar. Diameter wadah yang semakin besar tidak disertai dengan peningkatan diameter
propeller, sehingga pada saat proses pengadukan berlangsung terbentuk vortex pada cairan. Vortex
adalah cekungan pada permukaan media yang terbentuk pada bagian tengah tangki yang disebabkan oleh adanya gaya tangensial. Vortex menyebabkan aliran tangki bersifat horizontal, sehingga pencampuran tidak dapat berlangsung dengan baik. Terbentuknya vortex menyebabkan proses hidrolisis tidak dapat berjalan dengan baik. Pada skala lebih besar hidrolisis enzimatik minyak ikan lemuru dengan lipase Aspergillus niger untuk produksi omega-3 dapat dilakukan dalam reaktor kaca. Reaktor kaca dapat dilengkapi dengan baffle untuk mencegah terbentuknya vortex. Hal ini sesuai dengan pernyataan Edwards dan Baker (1992) yang menyebutkan bahwa baffle digunakan untuk mencegah terbentuknya vortex pada cairan yang memiliki kekentalan rendah.
[image:38.595.179.458.459.666.2]Hidrolisis skala 5, 10, dan 20 kali menunjukkan hasil yang berbeda meskipun menggunakan wadah dengan ukuran diameter yang sama. Hal ini dikarenakan adanya pengaruh dari kecepatan pengadukan seperti yang ditunjukkan pada Gambar 12.
Gambar 11. Kurva pengaruh kecepatan pengadukan terhadap bilangan asam
pengadukan mempengaruhi proses hidrolisis. Semakin tinggi kecepatan pengadukan media pada kondisi proporsional semakin banyak asam lemak bebas dan gliserol yang terbentuk. Hidrolisis skala 20 kali menunjukkan hasil lebih baik dibandingkan hidrolisis skala 5 dan 10 kali. Kecepatan pengadukan yang digunakan adalah 250 rpm. Perubahan kecepatan akan berlaku apabila terjadi perubahan ukuran diameter pengaduk (impeller atau propeller) mengikuti persamaan (1.2) dan persamaan (1.3).
Vtip = 2π N Di atau
(1.2)
(Ni1)3(Di1)2 = (Ni2)3(Di2)2 (1.3)
dimana,
Vtip = kecepatan propeller (rpm) N = kecepatan stirrer (rpm) Di
i = propeller
= diameter impeler (m)
1 = kondisi awal
2 = kondisi penggandaan
Pada hidrolisis skala sebesar 5, 10, dan 20 kali tidak terjadi perubahan ukuran diameter pengaduk, melainkan terjadi perubahan kecepatan pengadukan. Hal ini menunjukkan bahwa kecepatan pengadukan sebesar 250 rpm pada rasio diameter pengaduk dan diameter wadah sebesar 1,1538 merupakan kecepatan optimal hidrolisis enzimatik minyak ikan untuk produksi omega-3 dalam skala yang lebih besar.
4.2.2 Pengaruh Ratio Dt/Di terhadap Tingkat Hidrolisis
Gambar 13. Kurva pengaruh ratio Dt/Di terhadap tingkat hidrolisis
Hidrolisis skala 5 kali memiliki tingkat hidrolisis sebesar 38,0743%. Hidrolisis skala sebesar 10 kali memiliki tingkat hidrolisis lebih tinggi dibandingkan tingkat hidrolisis pada skala 5 kali yaitu sebesar 72,1104%. Hidrolisis skala 20 kali memiliki tingkat hidrolisis sebesar 85,0864%. Namun, pada hidrolisis skala 50 kali terjadi penurunan tingkat hidrolisis sebesar 43,301%. Hal ini disebabkan oleh kondisi proses yang tidak optimal terkait dengan rasio diameter pengaduk dan diameter wadah yang tidak proporsional. Pernyataan ini diperkuat dengan nilai bilangan asam produk hidrolisis pada skala 50 kali yang memiliki bilangan asam lebih kecil dari ketiga produk hidrolisis dari skala yang lebih kecil. Rendahnya tingkat hidrolisis pada hidrolisis skala 50 kali menunjukkan bahwa minyak tidak terhidrolisis secara optimal, sehingga jumlah asam lemak bebas yang terbentuk berkurang. Proses hidrolisis yang tidak berjalan optimal akan menyebabkan produksi omega-3 tidak berjalan baik, sehingga tidak dihasilkan dalam jumlah optimal dan tidak dapat mewakili produk yang ideal.
4.2.3
Hubungan Antara Tingkat Hidrolisis Tertinggi dengan Total Omega-3
yang Dihasilkan
Gambar 14. Diagram hubungan antara tingkat hidrolisis dengan total omega-3
Data menunjukkan bahwa peningkatan tingkat hidrolisis minyak ikan lemuru berbanding lurus dengan peningkatan total omega-3, namun persentase total omega-3 produk tidak sebesar tingkat hidrolisisnya. Persentase omega-3 yang dihasilkan pada hidrolisis enzimatik minyak ikan pada tingkat hidrolisis sebesar 38,0743% adalah 3,98%. Persentase total omega-3 meningkat pada tingkat hidrolisis sebesar 72,1104% adalah 4,15% dan 5,72% pada tingkat hidrolisis sebesar 85,0864. Penurunan persentase total omega-3 terjadi pada skala hidrolisis 50 kali dengan tingkat hidrolisis 43,301% yaitu sebesar 1,16%. Total omega-3 yang dihasilkan dari proses hidrolisis enzimatik minyak ikan lemuru menggunakan lipase Aspergillus niger relatif kecil. Hal ini tidak sesuai dengan pernyataan Estiasih (1996) yang menyebutkan bahwa kadar asam lemak omega-3 minyak ikan lemuru adalah 26,8%. Rendahnya total omega-3 yang dihasilkan dapat disebabkan oleh dua faktor, yaitu faktor teknis proses hidrolisis dan faktor alam yang berkaitan dengan bahan baku (ikan lemuru).
Faktor teknis proses hidrolisis berkaitan dengan kondisi proses dan instrumen yang digunakan. Pada penelitian diketahui bahwa rasio diameter pengaduk dan diameter wadah tidak proporsional. Hal ini ditunjukkan pada penurunan persentase omega-3 pada skala 20 kali ke skala 50 kali. Terbentuknya
vortex pada hidrolisis skala 50 kali menyebabkan hidrolisis dari asam lemak rantai panjang tidak optimal, sehingga omega-3 yang terbentuk tidak mencapai jumlah optimum.
rendah dari ikan yang hidup di perairan sub tropis atau dingin. Ikan lemuru yang hidup di perairan Indonesia yang tropis menyebabkan kadar omega-3 yang dikandungnya relatif rendah.
Gambar 15. Diagram hubungan antara tingkat hidrolisis dengan kadar EPA dan DHA
Pada Gambar 15, data hasil hidrolisis enzimatik minyak ikan lemuru menunjukkan bahwa kadar EPA yang dihasilkan lebih besar dari kadar DHA. Produk hidrolisis pada skala 5 kali mengandung 3,19% EPA dan 0,23% DHA. Produk hidrolisis pada skala 10 kali mengandung 3,36% EPA dan 0,32% DHA. Produk hidrolisis pada skala 20 kali mengandung 3,69% EPA dan 0,62% DHA. Peningkatan kadar EPA dan DHA sejalan dengan peningkatan skala hidrolisis. Kand