PEMANFAATAN SIRUP GLUKOSA HASIL HIDROLISIS SERAT DARI AMPAS KELAPA DALAM PEMBUATAN GULA JAWA/ GULA MERAH
DENGAN VOLUME BERVARIASI
SKRIPSI
SRI NINGSIH PARDOSI 060822007
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PEMANFAATAN SIRUP GLUKOSA HASIL HIDROLISIS SERAT DARI AMPAS KELAPA DALAM PEMBUATAN GULA JAWA/ GULA MERAH DENGAN
VOLUME BERVARIASI
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar sarjana Sains
SRI NINGSIH PARDOSI 060822007
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PEMANFAATAN SIRUP GLUKOSA HASIL
HIDROLISIS SERAT DARI AMPAS KELAPA DALAM PEMBUATAN GULA
JAWA/GULA MERAH DENGAN VOLUME BERVARIASI
Kategori : SKRIPSI
Nama : SRI NINGSIH PARDOSI
Nomor Induk Mahasiswa : 060822007
Program Studi : SARJANA ( S1 ) KIMIA
Departement : KIMIA
Fakultas : MATEMATIKA DAN ILMU
PERNYATAAN
PEMANFAATAN SIRUP GLUKOSA HASIL HIDROLISIS SERAT DARI AMPAS KELAPA DALAM PEMBUATAN GULA JAWA/ GULA MERAH
DENGAN VOLUME BERVARIASI
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Mei 2011
SRI NINGSIH PARDOSI 060822007
PENGHARGAAN
Puji dan syukur saya panjatkan kepada Tuhan Yang Maha Pengasih dan Maha Penyayang, dengan limpahan rahmad dan karunia-Nya kertas kajian ini berhasil diselesaikan.
Ucapan terima kasih saya sampaikan kepada Prof.DR.R.A.Harlinah SPW.MSc dan DR.Rumondang Bulan Nasution,MS selaku dosen pembimbing pada penyelesaian skripsi ini yang telah memberikan panduan dan penuh kepercayaan kepada saya untuk menyempurnakan kajian ini. Panduan ringkas, padat dan profesional yang telah diberikan kepada saya agar penulis dapat menyelesaikan tugas ini. Ucapan terima kasih juga ditujukan kepada Ketua dan Sekretaris Departemen DR.Rumondang Bulan Nasution,MS dan Drs.Firman Sebayang,MS, Dekan dan Pembantu Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, seluruh dosen serta staf pada Departemen Kimia FMIPA USU dan rekan – rekan mahasiswa.
Akhirnya tidak terlupakan kepada kedua orang tua saya ayahanda Alm.Marhum Pardosi,SpdI dan Ibunda Hamidah Angkat,Ama beserta keluarga dan teman – teman yang selama ini telah banyak membantu, memberi semangat dan do’a.
ABSTRAK
Telah dilakukan penelitian mengenai pengaruh polisakarida pada ampas kelapa terhadap kandungan sirup glukosa melalui proses hidrolisis mengunakan HCl 30 % pengambilan sampel dilakukan secara acak sederhana. Sampel berupa selulosa diisolasi dari ampas kelapa. Selulosa kemudian dihidrolisis dengan HCl 30 % untuk menghasilkan sirup glukosa. Kadar glukosa dianalisa dengan metode Nelson – Somogi dan dihitung dengan analisis regresi. Dari hasil penelitian diperoleh sirup glukosa dari selulosa ampas kelapa dengan kadar glukosa sebesar 12,39 %.
THE USE OF GLUCOSE SYRUP AS PRODUCT OF FIBER HIDROLIZE FROM COCONUT PULP OF PULP SUGAR/ BROWN SUGAR
PRODUCTION WITH VOLUME VARIOUS
ABSTRACT
A research on the influence of polysaccharides from coconut pulp toward the content of glucose syrup on hydrolyze with HCl 30 % has been done. Samples has got with simple random sampling. Cellulose was isolated from coconut pulp. Cellulose were hydrolyzed by HCl 30% to produce glucose syrups. The content was analyzed by Nelson – Somogyi method and calculated by regression analysis. The results of analysis shows that the content of glucose from coconut pulp cellulose were 12,39 %.
2.6.3 Kandungan nira Aren ... 14
2.6.4 Pembuatan Gula Aren/Gula Jawa ... 15
2.7. Spektrofotometer UV – Visible ... 16
2.8. Sifat – Sifat Organoleptik ... 17
BAB III BAHAN DAN METODE PENELITIAN 3.1. Alat dan Bahan ... 19 3.3.2. Isolasi Selulosa dari Ampas Kelapa ... 23
3.3.3. Analisa Kandungan Serat Kasar dari Ampas Kelapa... 22
BAB 4 HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian ... 31
4.1.1. Data Hasil Perhitungan Gula Reduksi Berdasarkan Absorbansi Glukosa Hasil Hidrolisis Ampas kelapa... 32
4.2 Pengolahan Data ... 32 4.2.1. Perhitungan Kadar Serat kasar Dari Ampas Kelapa ... 32 4.2.2. Pengolahan Data Pengukuran Absorbansi Glukosa
Hasil Hidrolisis Selulosa Ampas Kelapa ... 32 4.2.3. Perhitungan Kadar Serat Kasar Dari Ampas Kelapa ... 34 4.3. Pembahasan ... 37 BAB 5 KESIMPULAN DAN SARAN
5.1. Kesimpulan ... 38 5.2. Saran ... 38 DAFTAR PUSTAKA ... 39 LAMPIRAN
DAFTAR TABEL
Halaman Tabel.2.1. Komposisi Perasan Kelapa 7
Tabel 2.2. Perbandingan Sifat Kimia dan Produksi Nira Aren,Nira Kelapa
dan Nira Lontar 15
Tabel.3.1. Pengukuran Nilai Organoleptis Terhadap Nira Dengan
Penambahan Sirup Glukosa 25
Tabel 4.2.3.1 Working Sheet Larutan Glukosa Standar pada Berbagai Konsentrasi 34 Tabel 1. Data Absorbansi Larutan Glukosa Standart pada Berbagai
Konsentrasi pada λ= 714 nm 41 Tabel 2. Data Hasil Perhitungan Gula Reduksi Berdasarkan Absorbansi
Glukosa Hasil Hidrolisis Ampas Kelapa. 42 Tabel 3. Data Absorbansi Nira dengan Penambahan Sirup Glukosa
Pada λ= 714 nm 42
Tabel 4. Harga erf (t) atau ert (hx) dari harga T 43 Tabel 5. Data Hasil Uji Organoleptis Terhadap Rasa Gula Merah dengan
Penambahan Sirup Glukosa 44
Tabel 6. Data Hasil Uji Organoleptis Terhadap Warna Gula Merah dengan Penambahan Sirup Glukosa 45
DAFTAR GAMBAR
Gambar 2.1 : Buah Kelapa 5
Gambar 2.2 : Ampas Kelapa 7
Gambar 2.3 : Kurva Penentuan λ maksimum dari larutan glukosa 47 Gambar 2.4 : Kurva Standart Larutan Glukosa pada λ maksimum 714 nm 47
ABSTRAK
Telah dilakukan penelitian mengenai pengaruh polisakarida pada ampas kelapa terhadap kandungan sirup glukosa melalui proses hidrolisis mengunakan HCl 30 % pengambilan sampel dilakukan secara acak sederhana. Sampel berupa selulosa diisolasi dari ampas kelapa. Selulosa kemudian dihidrolisis dengan HCl 30 % untuk menghasilkan sirup glukosa. Kadar glukosa dianalisa dengan metode Nelson – Somogi dan dihitung dengan analisis regresi. Dari hasil penelitian diperoleh sirup glukosa dari selulosa ampas kelapa dengan kadar glukosa sebesar 12,39 %.
THE USE OF GLUCOSE SYRUP AS PRODUCT OF FIBER HIDROLIZE FROM COCONUT PULP OF PULP SUGAR/ BROWN SUGAR
PRODUCTION WITH VOLUME VARIOUS
ABSTRACT
A research on the influence of polysaccharides from coconut pulp toward the content of glucose syrup on hydrolyze with HCl 30 % has been done. Samples has got with simple random sampling. Cellulose was isolated from coconut pulp. Cellulose were hydrolyzed by HCl 30% to produce glucose syrups. The content was analyzed by Nelson – Somogyi method and calculated by regression analysis. The results of analysis shows that the content of glucose from coconut pulp cellulose were 12,39 %.
BAB I
PENDAHULUAN
1.1. Latar Belakang
Ampas kelapa adalah sumber selulosa, dimana bahan pangan yang sudah dimanfaatkan untuk memproduksi sirup glukosa adalah ubi kayu yang merupakan sumber amilum yang disebut dengan High Fructose Syrup (HFS) dan sudah dimanfaatkan oleh industri minuman pada tahun 1973. Maksud dari pengunaan High Fructose Syrup adalah untuk mengantikan penggunaan sakarin (biang gula) dan natrium siklamat (bibit gula) yang kualitas kemanisannya kurang serta cenderung memberikan rasa yang kurang enak apabila pemakaiannya dalam konsentrasi yang tinggi bahkan tekanan osmosinya rendah, sehingga sanggat membatasi kemungkinan pengunaan dalam industri. Karena itu pada tahun – tahun terakhir ini pemakaian sakarin dan natrium siklamat dibatasi oleh peraturan kesehatan dibanyak negara termasuk di Indonesia.
Sampah ampas kelapa memberikan dampak negatif kepada lingkungan hidup dan apabila dibiarkan akan memberikan bau busuk, karena itu kepada ibu – ibu rumah tangga dan para pengusaha restoran, kedai nasi, pabrik dodol, pabrik minyak kampong diharapkan dapat menanggulangi pencemaran lingkungan dengan membantu pemerintah dalam pengolahan ampas kelapa menjadi sirup glukosa.
(Suhardiyono,1995)
Hasil hidrolisis selulosa oleh asam kuat yang encer dapat menghasilkan sirup glukosa yang selanjutnya sirup glukosa ini dapat dimanfaatkan untuk :
1. Menaikkan kandungan glukosa dari gula kelapa (gula jawa).
2. Membantu menyediakan bahan baku bagi industri High Fructose Syrup (HFS) karena ubi kayu gini banyak dimanfaatkan manusia sebagai penganti beras lebih – lebih bila panen gabah mengalami kegagalan.
1.2 Permasalahan
Sesuai dengan uraian diatas, maka yang menjadi permasalahan pada penelitian ini adalah apakah selulosa pada ampas kelapa dapat dijadikan pemanis pada
pembuatan gula jawa/ gula merah.
1.3 Pembatasan Masalah
Mengingat begitu luasnya permasalahan dalam pemanfaatan gula jawa, maka dalam penelitian ini objek masalah dibatasi sebagai berikut :
1. Sampel diperoleh dari salah satu pajak sore di Padang Bulan 2. Varietas kelapa tidak ditentukan
3. Varietas Aren tidak ditentukan
4. Menentukan kadar glukosa dan uji Organoleptik cita rasa
1.4. Tujuan Penelitian
Adapun tujuan dilakukannya penelitian ini adalah Untuk mengetahui pengaruh penambahan sirup glukosa hasil hidrolisa ampas kelapa terhadap kemanisan pada gula jawa/gula merah.
1.5. Manfaat Penelitian
Adapun manfaat yang diperoleh dari penelitian ini adalah sebagai berikut 1. Memberikan informasi kepada masyarakat tentang kandungan ampas
kelapa yang dapat dijadikan sebagai pemanis.
1.6 Metodologi Penelitian
Penelitian yang dilakukan merupakan eksperimen yang dilakukan di laboratorium yang terdiri dari :
1. Sampel berupa ampas kelapa yang diperoleh dari pajak sore di daerah Padang Bulan.
2. Variabel – variabel yang digunakan dalam penelitian ini adalah : - Variabel Bebas : Perbandingan nira dengan sirup glukosa
( 1:1, 1:2, 1:3, 1:4 )
-Variabel terikat : kadar glukosa dan nilai organoleptik -Variabel tetap : Berat ampas kelapa dan volume nira
3. Sirup glukosa diperoleh dengan menghidrolisa ampas kelapa dengan HCl 30%. Kadar glukosanya ditentukan dengan metode Nelson Somogyi menggunakan alat Spektrofotometer pada panjang gelombang 714 nm. Sirup glukosa hasil hidrolisis digunakan untuk penambah rasa manis pada gula jawa/ gula merah.
1.7 Lokasi Penelitian
BAB II
TINJAUAN PUSTAKA
2.1. Tinjauan Umum Kelapa
Kelapa merupakan tanaman tropis yang penting bagi Negara – Negara Asia dan Pasifik. Pada tahun 1987, negara – negara Asia dan Pasifik menghasilkan 82 % dari produksi kelapa dunia, sedangkan sisanya dihasilkan oleh negara di Afrika dan Amerika Serikat.
Tanaman kelapa merupakan salah satu komoditi yang sudah dikenal di negara Indonesia. Tanaman kelapa merupakan tumbuhan tropis, tumbuh dengan baik didaerah pantai dan dataran rendah. Di indonesia kelapa merupakan sumber pencarian jutaan petani yang mampu memberikan penghidupan bagi seluruh keluarganya. Oleh karena itu tanaman kelapa ini ditanam secara besar-besaran maupun tanaman pekarangan untuk kebutuhan keluarga. ( Suhardiyono,1995)
2.1.1. Klasifikasi Kelapa
Klasifikasi dari tumbuhan kelapa yaitu : Divisio : Spermatophyta
Sub : Angiospermae
Klas : Monocotyledoneae Ordo : Spdicifloreae Famili : Palmae Genus : Cocos
Species : Cocos nucifera
Morfologi tanaman kelapa sebagai berikut : - mempunyai akar serabut
- batang tidak bercabang - daun bersirip
- bentuk daun panjang terutama pada pangkal - helai daun mempunyai tulang daun ( lidi ).
- bunga dari tanaman ini mempunyai 2 fase yaitu serbuk sari bunga betina. - Buahnya bulat
Buah kelapa yang sudah tua itu bobotnya terdiri dari 35 % sabut, 12 % tempurung, 28 % daging buah dan 26 % air.
2.1.2. Komposisi Zat Gizi Daging Kelapa
Didalam daging kelapa banyak zat – zat gizi didapatkan.dan hasil dari perasan santan. Hasil samping dari perasan santan yaitu ampas juga masih mengandung zat gizi. Senyawa – senyawa yang terdapat dalam seratus gram daging kelapa yang telah diparut adalah :
- Protein : 3.40 gr
- Lemak : 34 gr
- Karbohidrat : 14 gr
- Flour : 2.0 mg
- Fosfor : 21 mg
- Thiamin : 0.1 mg
- As.Askorbat : 2.0 mg (Suhardiyono,L. 1995)
2.1.3. Komposisi Zat Gizi dalam Santan
Hasil perasan dari parutan daging buah kelapa menghasilkan santan yang mana komposisinya adalah 56 % air, 2.8 % karbohidrat, 0.7 % protein dan lemak 35 %.
2.1.4. Komposisi Zat Gizi pada Ampas Kelapa
Ampas kelapa yang dihasilkan dari hasil perasan santan rumah tangga ( sebagai sayur ) boleh dikatakan masih mengandung lemak dan protein.
Gambar 2.2 Ampas Kelapa
Tabel 2.1. Komposisi Perasan Kelapa
Ampas yang diperas Lemak Protein
I 63.70 6.71
II 39.55 4.04
III 30.10 3.03
IV 28.24 2.94
2.1.5. Manfaat dari Ampas Kelapa
Ampas kelapa dapat juga dibuat untuk bahan dasar pembuatan tempe. Sedangkan di Filipina diolah menjadi bentuk sauce, serta di india digunakan sebagai pencampur buah – buahan tau gur yang sudah dikeringkan & pembuatan kue.
2.2. Karbohidrat
Secara kimia karbohidrat didefenisikan sebagai derivat dari polihidroksil aldehid dan polihidroksil keton ( x ). Karbohidrat dapat dibagi dalam empat golongan utama yaitu :
1. Monosakarida yaitu karbohidrat yang tidak dapat dihidrolisa menjadi bentuk yang lebih sederhana.Contoh : glukosa dan fruktosa
2. Disakarida yaitu karbohidrat yang bila dihidrolisa menghasilkan dua molekul monosakarida yang sama atau berbeda. Contoh : selobiosa, sukrosa dan maltosa.
3. Oligosakarida yaitu karbohidrat yang bila dihidrolisa menghasilkan dua Sampai enam molekul monosakarida.
4. Polisakarida yaitu karbohidrat yang bila dihidrolisa menghasilkan lebih dari enam molekul monosakarida.
Polisakarida yang penting : Pati, Glikogen, Inulin, Selulosa. ( Iswari, Yuniastuti.2006 )
2.3. Selulosa
Selulosa merupakan homopolisakarida linear tidak bercabang, terdiri dari 10.000 atau lebih unit D – glukosa yang dihubungkan oleh ikatan β-1,4 glikosida. Beberapa jenis bakteri, jamur dan beberapa invertebrate seperti termitidae ( rayap ) memiliki enzim selulosa, sehingga mereka dapat mencerna selulosa. Serabut kapas dapat dikatakan selulosa yang murni. ( Lehninger,A.L,1988).
Selulosa lebih sukar diuraikan dan mempunyai sifat – sifat sebagai berikut : memberi bentuk atau struktur pada tanaman, tidak larut dalam air dingin maupun air panas, tidak dapat dicerna oleh pencernaan manusia sehungga tidak dapat menghasilkan energi. Selulosa terdapat pada bagian – bagian yang keras dari biji
kopi atau kulit kacang dan hamper semua buah – buahan dan sayur-sayuran. ( Winarno,F.G,1995).
Selulosa merupakan komponen utama penyusun dinding sel tanaman dan hamper tidak pernah ditemui dalam keadaan murni dialam melainkan berikatan dengan lignin dan hemiselulosa membentuk lignoselulosa .
Lignin berikatan dengan hemiselulosa melalui ikatan kovalen namun ikatan yang terjadi antara selulosa dan lignin belum diketahui secara lengkap. Adanya lignin disekeliling selulosa merupakan hambatan utama dalam menghidrolisis selulosa. Selulosa terproteksi dari degradasi dengan adanya lignin. Selulosa tidak dapat dihidrolisis kecuali lignin dilarutkan dan dihilangkan. ( Lynd.L.R.2002 ).
2.3.1. Hidrolisis Selulosa
2.3.2. Hidrolisis selulosa secara kimiawi
Hidrolisis selulosa dengan asam berlangsung bertahap melalui reaksi sebagai berikut :
Selulosa selubiosa glukosa
Dalam hal ini asam ( asam sulfat, asam klorida dan asam perklorat ) menghidrolisis selulosa menjadi glukosa secara acak artinya tidak ada pola tertentu dalam pemutusan ikatan glikosida yang terdapat dalam selulosa.
Hidrolisis dalam suasana asam akhirnya menghasilkan pemecahan ikatan glikosidik, berlangsung dalam tiga tahap. Dalam tahap pertama, proton yang bertindak sebagai katalisator asam berinteraksi cepat dengan oksigen glikosida yang menghubungkan dua unit gula ( I ) membentuk asam konjugat ( II ). Langkah ini diikuti dengan pemecahan yang lambat dari ikatan C – O yang menghasilkan zat antara kation karbonium siklik ( III ). Protonasi dapat juga terjadi pada oksigen cincin ( II ), menghasilkan pembukaan cincin dan kation karbonium non siklik ( III ).tidak ada kepastian ion karbonium mana yang paling mungkin dibentuk. Mungkin kedua modifikasi protonasi terjadi dengan kemungkinan terbesar pada kation siklik. Akhirnya kation karbonium mulai mengadisi molekul air dengan cepat, membentuk hasil akhir yang stabil dan melepaskan proton ( Wijayanti,L.2005).
2.3.3. Hidrolisis selulosa secara enzimatis
Reese at al ( 1950 ) menyatakan bahwa hidrolisis selulosa diawali dengan tahap aktivasi dan diikuti serangkaian reaksi hidrolisis sebagai berikut :
Selulosa selulosa reaktif selubiosa glukosa
Aktivasi disebabkan oleh enzim non hidrolisis yang disebut C1, hidrolisis dari selulosa reaktif dilakukan oleh enzim hidrolisa Cx sedangkan mikroorganisme yang hanya menguraikan selulosa akan kekurangan enzim- enzim selobiohidrolase,
2.4 Sirup Glukosa
Sirup glukosa pertama kali digunakan sebagai pengganti gula yang dibuat dengan mereaksikan amilum dan selulosa dengan asam. Mula – mula polisakarida dihidrolisis menjadi oligosakarida,disakarida dan hasil akhirnya berupa monosakarida yaitu glukosa. Proses hidrolisis berakhir ketika semua polisakarida telah diubah menjadi glukosa cair.
Sirup glukosa merupakan suatu larutan diperoleh dari proses hidrolisis dengan bantuan katalis. Sirup glukosa adalah salah satu produk bahan pemanis makanan dan minuman yang berbentuk cairan, tidak berbau dan tidak berwarna tetapi memiliki rasa manis yang tinggi. Sirup glukosa atau gula cair mengandung D-glukosa,maltosa dan polimer D-glukosa melalui proses hidrolisis ( Cakebread.S.1975).
Perbedaan sirup glukosa dengan gula pasir atau sukrosa yaitu sukrosa merupakan gula disakarida, terdiri atas ikatan glukosa dan fruktosa, sedangkan sirup glukosa adalah monosakarida, terdiri atas satu monomer yaitu glukosa.sirup glukosa dapat dibuat dengan cara hidrolisis asam atau dengan cara enzimatis.
( htttp://www.pustakadeptan.go.id )
Bahan baku yang dapat digunakan untuk pembuatan sirup glukosa adalah tapioka, pati umbi-umbian,sagu, jagung dan serat. Industri makanan dan minuman memiliki kecenderungan untuk mengunakan sirup glukosa. Hal ini didasari oleh beberapa kelebihan sirup glukosa dibandingkan sukrosa, diantara sirup glukosa tidak mengkristal seperti halnya sukrosa jika dilakukan pemanasan pada suhu tinggi.
2.5 Metode Analisa Kuantitatif Glukosa
2.5.1. Metode Nelson – Somogyi
Metode ini dapat digunakan untuk mengukur kadar gula reduksi dengan menggunakan pereaksi tembaga arseno molibdat. Kufri mula – mula direduksi menjadi kufro dengan pemanasan larutan gula. Kufro yang terbentuk selanjutnya dilarutkan dengan arseno – molibdat menjadi molibdenum berwarna biru yang menunjukan ukuran konsentrasi gula dengan membandingkannya dengan larutan standar, konsentrasi gula dalam sampel dapat ditentukan. Reaksi warna yang terbentuk
dapat menentukan konsentrasi gula dalam sampel dengan mengukur absorbansinya. ( Sudarmadji.S.1984).
2.5.2. Metode Lane- Eynon
Penetapan gula pereduksi dengan metode ini dilakukan secara volumetrik. Biasanya digunakan untuk penentuan laktosa (anhidrat dan monohidrat) glukosa, fruktosa, maltosa (anhidrat atau monohidrat) dan lainnya. Penetapan gula pereduksi dengan metode ini didasarkan atas pengukuran volume larutan gula pereduksi standar yang dibutuhkan untuk mereduksi pereaksi tembaga basa yang diketahui volumenya. Titik akhir titrasi ditunjukan dengan metilen biru yang warnanya akan hilang karena kelebihan gula pereduksi di atas jumlah yang dibutuhkan untuk mereduksi tembaga.
2.5.3. Metode Anthrone
2.5.4. Metode Munson Walker
Penentuan gula reduksi berdasarkan atas banyaknya endapan Cu2O yang terbentuk, kemudian dengan melihat tabel Hadmond dapat diketahui jumlah gula pereduksinya. Jumlah Cu2O ditentukan secara gravimetri yaitu dengan menimbang larutan endapan Cu2O yang terbentuk.Dapat juga ditentukan secara volumetri yaitu
dengan titrasi menggunakan larutan Na-tiosulfat atau K-permanganat. ( Apriyanto.A.1989).
2.6 Tumbuhan Aren
Enau atau aren (Arenga pinnata, suku Arecaceae) adalah palma yang terpenting setelah kelapa (nyiur) karena merupakna tanaman serba guna. Tumbuhan ini dikenal dengan berbagai nama seperti nau, hanau, peluluk, biluluk, kabung,juk atau ijuk (aneka nama able di Sumatera dan Semenanjung Malaya); akol, akel, akere, inru, indu (bahasa – bahsa di Sulawesi); moka, moke, tuwa, tuwak ( di Nusa
Tenggara), dan lain – lain.
Bangsa Belanda mengenalnya sebagai arenpalm atau zuikerpalm dan bangsa Jerman menyebutnya zuckerpalme. Dalam bahasa Inggris disebut sugar palm atau gomuti palm. Hampir semua bagian atau produk tanaman ini dapat dimanfaatkan dan memiliki nilai ekonomi, yang menjadikannya populer sebagai tanaman yang serbaguna, terutama sebagai penghasil gula. Mulai dari bagian – bagian fisik pohon maupun dari hasil produksinya.
2.6.1 Fisiologi Aren
Daunnya majemuk menyirip, seperti daun kelapa, panjang hingga 5 m dengan tangkai daun hingga 1,5 m. anak daun seperti pita bergelombang, hingga 7 x 145 cm, berwarna hijau gelap di atas dan keputih – putihan oleh karena lapisan lilin di sisi bawahnya. Berumah satu, bunga – bunga jantan terpisah dari bunga – bunga betina dalam tongkol yang berbeda yang muncul di ketiak daun, panjang tongkol hingga 2,5 meter.
2.6.2 Penyadapan nira
Nira diperoleh dengan menyadap tandan bunga jantan yang dimulai mekar dan menghamburkan serbuk sari yang berwarna kuning. Tandan ini mula – mula dimemarkan dengan memukulnya selama beberapa hari, hingga keluar cairan dari dalamnya. Tandan kemudian dipotong dan di ujungnya digantungkan batang able untuk menampung cairan yang menetes.
Cairan manis yang diperoleh dinamai nira ( alias legen atau saguer ), berwarna jernih agak keruh. Nira ini tidak tahan lama, maka batang bambu yang telah berisi harus segera di ambil untuk diolah niranya; biasanya sehari dua kali pngambilan yakni pagi dan sore.
2.6.3 Kandungan nira aren
Nira dalam keadaan segar tidak berwarna, tidak berbau, harum, dan manis. Menurut Milsum dan Danner bahwa komposisi nira aren dalam 100 ml dengan berat jenis 1,0135 pada 84°C adalag sebagi berikut :
- Sukrosa 7,10 gram - Gula Invert 0,15 gram - Bukan Gula 0,29 gram - Nitrogen 0,005 gram
Berikut tabel perbandingan sifat kimia dan produksi nira aren, nira kelapa dan
2.6.4 Pembuatan Gula Aren/Gula Jawa
Nira mempunyai sifat mudah menjadi asam karena adanya proses fermentasi oleh bakteri saccaromycess s.p oleh Karena itu nira harus segera diolah setelah diambil dari pohon, paling lambat 90 menit setelah dikeluarkan dari bumbung.
Setelah kekentalan nira tersebut tercapai, kemudian bejana diturunkn dari tungku perapian dan didinginkan selama 8 – 10 menit. Kemudian menggunakan alat ciduk ( bahasa jawa: irus ), tuangkan masakan nira kental tadi kedalam cetakan berupa tempurung kelapa ( bahasa jawa: batok) atau potongan – potongan batang bambu yang berdiameter sekitar 8 cm dan ketebalannya 4 – 5 cm. penuangan masakan nira kedalam cetakan dilakukan secara berurutan sebanyak dua kali dengan perbandingan 30 % dan 70 % masing – masing untuk penuangan pertama dan kedua. Hal ini perlu dilakukan agar gula yang diperoleh itu kompak dan tidak mudah pecah jika telah dingin. Sebaiknya sebelum masakan nira dituangkan dalam cetakan, lebih dahulu alat cetakan dicelupkan dalam air sampai basah, untuk membantu pendinginan dan memudahkn mengeluarkan gula dari cetakan.
2.7. Spektrofotometer UV-Visible
Spektrometri adalah pengukuran absorbansi selektif radisi elektromagnetik yang dipakai untuk analisis kualitatif dan kuantitatif senyawa kimia. Sedangkan spektrofotometri merupakan suatu metode yang sangat dalam analisis kimia kualitatif dan kuantitatif. Banyak kelebihan yang dimilikinya, antara lain :
a. Dapat digunakan secara luas dalam pengukuran secara kualitatif dan kuantitatif untuk senyawa – senyawa organik maupun senyawa anorganik. b. Kepekaan tinggi, karena dapat mengukur dalam satuan ppm (part
permillion), bahkan ppb (part perbillion) sehingga dapat mengukur komponen trace (renik).
2.8. Sifat – Sifat Organoleptik.
Organoleptik merupakan pengujian terhadap bahan makanan berdasarkan
kesukaan dan kemauan untuk mempergunakan suatu produk.
Dalam penilaian bahan pangan sifat yang menentukan diterima atau tidak suatu
produk adalah sifat indrawinya. Penilaian indrawi ini ada enam tahap yaitu pertama
menerima bahan, mengenali bahan, mengadakan klarifikasi sifat-sifat bahan,
mengingat kembali bahan yang telah diamati, dan menguraikan kembali sifat indrawi
produk tersebut. Indra yang digunakan dalam menilai sifat indrawi suatu produk
adalah :
1. Penglihatan yang berhubungan dengan warna kilap, viskositas, ukuran dan
bentuk, volume kerapatan dan berat jenis, panjang lebar dan diameter serta
bentuk.
2. Indra peraba yang berkaitan dengan struktur, tekstur dan konsistensi. Struktur
merupakan sifat dari komponen penyusun, tekstur merupakan sensasi
tekanan yang dapat diamati dengan mulut atau perabaan dengan jari, dan
konsistensimerupakantebal,tipisdanhalus.
3. Indra pembau, pembauan juga dapat digunakan sebagai suatu indikator
terjadinya kerusakan pada produk, misalnya ada bau busuk yang
menandakan produk tersebut telah mengalami kerusakan.
4. Indra pengecap, dalam hal kepekaan rasa , maka rasa manis dapat dengan
mudah dirasakan pada ujung lidah, rasa asin pada ujung dan pinggir lidah,
rasa asam pada pinggir lidah dan rasa pahit pada bagian belakang lidah.
Penentu bahan makanan pada umumnya sangat ditentukan oleh beberapa
faktor antara lain : warna , rasa, tekstur, viskositas dan nilai gizi.
Cita rasa suatu makanan terdiri atas tiga komponen yaitu: bau, rasa dan ransangan
mulut, yang dapat diamati oleh indra pembau adalah : zat berbau berbentuk uap
sedikit larut dalam air, sedikit larut dalam lemak dan molekul-molekul bau harus
sempat menyentuh silia sel olfaktori dan diteruskan ke otak dalam bentuk impuls
Sedangkan yang mempengaruhi rasa yaitu senyawa kimia, suhu, konsentrasi
dan interaksi dengan komponen rasa yang lain. Mutu cita rasa nasi terutama sangat
ditentukan oleh kepulenan nasi tersebut, kemekaran, aroma, warna nasi dan rasa nasi.
Senyawa yang berhubungan dengan aroma bahan makanan yang di panaskan adalah
furanon, senyawa 4-hidroksi,3dimetil-3-dihidroksifuranon yang mempunyai bau
karamel. Senyawa 4-hidroksi-5-metil-3-dihidrofuranon yang mempunyai bau akar
chikori yang disangrai, senyawa 2,5-dimetil-3-dihidrofuranon yang mempunyai bau
roti yang baru selesai pengovenan, serta isomalton dan malton yang merupakan
produk karamelisasi dan pirolisin karbohidrat. Pada bahan yang mnegandung lemak
akan mengalami ketengikan akibat oksidasi, yang menyebabkan cita rasa yang
menyimpang. Bahan makanan yang mengandung minyak apabila terkena oksigen
secara langsung akan menyebabkan terjadinya reaksi oksidasi yang menghasilkan
asam lemak berantai pendek, keton, aldehid yang bersifat volatil yang menimbulkan
bau tengik.
Bahan makanan yang mengandung karbohidrat dan protein akan mengalami
pencoklatan non-enzimatis, apabila bahan tersebut dipanaskan atau sering disebut
dengan reaksi Meillard akan dapat menghasilkan bau enak maupun tidak enak. Bau
tidak enak dihasilkan oleh dehidrasi kuat yaitu furfural, dehidrofurfural dan HMF
serta hasil pemecahan yaitu piruvaldehid, diasetil.
Untuk pembentukan rasa enak adalah hasil degradasi sttrecker dari asam amino alfa
diubah menjadi aldehid dengan atom karbon yang berkurang satu.
Tekstur dan konsistensi bahan akan mempengaruhi cita rasa suatu bahan.
Perubahan tekstur dan viskositas bahan dapat mengubah rasa dan bau yang timbul,
karena dapat mempengaruhi kecepatan timbulnya rasa terhadap sel reseptor alfaktori
dan kelenjar air liur, semakin kental suatu bahan penerimaan terhadap intensitas rasa ,
bau dan rasa semakin berkurang . Kenaikan temperatur akan menaikkan ransangan
pada rasa manis tetapi akan menurunkan ransangan pada rasa asin dan pahit.
Rasa manis pada gula akan bertambah apabila konsentrasi gula semakin tinggi, tetapi
sampai pada konsentrasi tertentu rasa enak yang timbul akan berkurang, demikian
juga dengan ketiga rasa yang lain, komponen rasa akan berinteraksi dengan komponen
BAB 3
BAHAN DAN METODE PENELITIAN
3.1. Alat dan Bahan
3.1.1. Alat-Alat
- Neraca Analitik Mettler Toledo
- Indikator Universal Merck
- Spektrofotometer Genesys 20
- Inkubator Fisher
- Labu takar Pyrex
- Gelas ukur Pyrex
- Gelas beaker Pyrex
- Gelas erlenmeyer Pyrex
- Tabung reaksi Pyrex
- Hot Plate Stirer Thermolyne
- Tanur Gallenkamp
- Cawan Crusible
- Labu alas Pyrex
- Pendingin leibigh Pyrex
3.1.2. Bahan-Bahan
- C6H12O6 E. Merck
- Na2CO3 E. Merck
- KnaC4H4O6.4H2O E. Merck
- NaHCO3 E.Merck
- Na2SO4 E. Merck
- CuSO4.5H2O E. Merck
- H2SO4(p) E. Merck
- (NH4)6Mo7O24.4H2O E. Merck
- Na2HasO4.7H2O E. Merck
- Na2CO3 E. Merck
- NaOH E. Merck
- HCl (p) E. Merck
- Alkohol E. Merck
- Akuades - Nira
3.2. Pembuatan Reagen
3.2.1 Larutan Glukosa 20 mg/100 ml
Sebanyak 20 mg glukosa anhidrat dilarutkan dengan akuades dalam labu takar 100 ml sampai garis tanda dan dikocok sampai homogen.
3.2.2 Larutan Pereaksi Nelson
1. Nelson A
Sebanyak 12,5001 g Natrium Karbonat anhidrat, 12,5001 g garam Rochelle (K-Na-Tartrat), 10 g Natrium Bikarbonat, dan 100 g Natrium Sulfat anhidrat dilarutkan dalam 300 ml akuades dan diencerkan sampai 500 ml.
2. Nelson B
Sebanyak 7,5002 g CuSO4.5H2O dilarutkan dalam 50 ml akuades dan ditambahkan 1 tetes asam sulfat pekat. Pereaksi Nelson dibuat dengan cara mencampur 25 bagian Nelson A dan 1 bagian Nelson B. Pencampuran dilakukan setiap kali digunakan.
3.2.3 Larutan Arsenomolibdat
Sebanyak 25 g Ammonium Molibdat dilarutkan dalam 450 ml akuades dan ditambahkan 25 ml H2SO4. Dilarutkan pada tempat yang lain 3 g Na2HasO4.7H2O dalam 25 ml akuades kemudian dituangkan larutan ini kedalam larutan yang pertama. Disimpan dalam botol berwarna cokelat dan diinkubasi pada suhu 37oC selama 24 jam. Larutan pereaksi ini dapat digunakan setelah masa inkubasi dan berwarna kuning.
3.2.4 Pembuatan Pereaksi Benedict
(larutan I). Dilarutkan 17,3001 g CuSO4.5H2O dalam 100 ml air (dipanaskan bila perlu). Bila larutan diatas sudah dingin maka perlahan-lahan ditambahkan kedalam larutan I, kemudian diencerkan dengan akuades sampai 1 liter.
3.2.5 Pembuatan Larutan NaOH 3 %
Sebanyak 3 g NaOH dilarutkan dengan akuades dalam labu takar 100 ml sampai garis tanda lalu dikocok hingga homogen.
3.2.6 Pembuatan Larutan HCl 30%
Sebanyak 203 ml larutan HCl 37% dimasukkan kedalam labu takar 250 ml, kemudian diencerkan dengan akuades sampai garis tanda lalu dikocok sampai homogen.
3.2.7 Pembuatan Larutan H2SO4 1,25 N
Kedalam labu ukur 100 ml, dilarutkan 3,4 ml larutan H2SO(p) dan diencerkan dengan akuades sampai garis tanda.
3.2.8 Pembuatan NaOH 1,25 N
3.3 Prosedur Penelitian
3.3.1 Pengambilan Sampel
Sampel berupa ampas kelapa yang diperoleh dari suatu lokasi yaitu Pajak Sore Padang Bulan Medan.
3.3.2 Isolasi Selulosa dari Ampas Kelapa
10 g ampas kelapa di keringkan pada suhu 110 oC, ditambahakan 50 ml alkohol 96 % lalu di saring, residu ditambahakan 50 ml H2SO4 1,25 N di refluks selama 30 menit lalu disaring, residu dicuci dengan 50 ml akuades panas lalu disaring, residu ditambahkan 50 ml NaOH 1,25 N dan direfluks selama 30 menit lalu disaring. Residu dicuci gengan akuades pana, disaring kemudian diovenkan pada suhu 110 oC lalu ditimbang hingga beratnya konstan.
3.3.3. Analisa Kandungan Serat Kasar Dari Ampas Kelapa
10 g ampas kelapa yang telah dihilangkan lemaknya ditambahkan 50 ml H2SO4 1,25 N direfluks selama 30 menit dan disaring, residu dicuci dengan akuades panas lalu disaring, residu ditambah 50 ml NaOH 1,25 N dan direfluks selama 30 menit, residu dicuci dengan akuades panas, disaring kemudian dioven pada suhu 110 oC selama 1 jam kemudian di tanur pada suhu 600 oC selama 3 jam lalu ditimbang hingga beratnya konstan.
3.3.4 Hidrolisis Selulosa ampas Kelapa serta Uji Gula Reduksi
kedalam tabung reaksi kemudian ditambahkan 5 ml larutan Benedict dan dipanaskan.
3.3.5 Pengukuran Panjang Gelombang Maksimum Larutan Glukosa Standar Sebanyak 20 mg glukosa dan dilarutkan dengan akuades sampai volume 100 ml (larutan glukosa 0,2 mg/ml). Dipipet 25 ml larutan lalu diencerkan dengan akuades sampai volume 100 ml (larutan glukosa 0,05 mg/ml). Dipipet 1 ml larutan glukosa 0,05 mg/ml kedalam tabung reaksi, lalu ditambahkan 1 ml pereaksi Nelson lalu ditutup dengan kapas dan dipanaskan pada penangas air sampai mendidih selama 30 menit lalu didinginkan. Lalu ditambahkan 1 ml larutan Arsenomolibdat lalu dikocok hingga semua endapan larut. Ditambahkan 7 ml akuades lalu dikocok hingga homogen. Diukur serapan panjang gelombang pada 650–850 nm (diperoleh panjang gelombang maksimum).
3.3.6 Penyiapan Kurva Standar Glukosa
Disiapkan larutan glukosa standar dalam beberapa tabung reaksi dengan konsentrasi bertingkat dari 0,02 – 0,20 mg/ml. Ditambahkan 1 ml larutan Nelson kemudian dipanaskan hingga mendidih selama 30 menit dan didinginkan. Ditambahkan 1 ml larutan arsenomolibdat lalu dikocok. Ditambahkan 7 ml akuades lalu dikocok hingga homogen. Diukur serapannya pada panjang gelombang 714 nm. Dibuat kurva standar yang menunjukkan hubungan antara konsentrasi gula standar dan absorbansi.
3.3.7 Analisa Kandungan Glukosa Hasil Hidrolisis Sampel
3.3.8 Uji Organoleptis Terhadap Nira Dengan Penambahan Sirup Glukosa Nira dengan penambahan sirup glukosa dan harus mengalami perlakuan
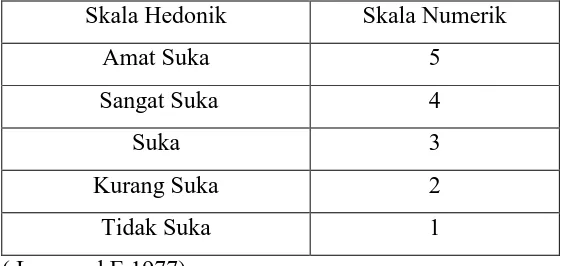
sebelum dikonsumsi yaitu penghilangan lemak, dan kemudian dilakukan pemasakan dalam larutan nira untuk memberikan rasa manis pada gula jawa. Pengukuran nilai organoleptis dari gula jawa dilakukan dengan metode kesukaan memakai angka hedonik dan numerik dengan 15 orang penelis dengan kondisi yang baik, tidak merokok dan berasal dari lingkungan yang sama. Dalam penentuan organoleptis dilakukan dengan skala yang terdapat pada tabel berikut.
Tabel.3.1.Pengukuran Nilai Organoleptis Terhadap Sirup dengan Penambahan Nira
Skala Hedonik Skala Numerik
Amat Suka 5
Sangat Suka 4
Suka 3
Kurang Suka 2
Tidak Suka 1
3.4. Bagan Penelitian
3.4.1. Isolasi Selulosa dari Ampas Kelapa
Ditambahkan 50 ml H2SO4 1,25 N 10 g Ampas Kelapa
Dikeringkan pada suhu 110 oC Ditambahkan 50 ml alkohol 96 %
Disaring
Residu
Residu
Filtrat
Dicuci dengan 50 ml akuades panas
Filtrat
Disaring
Direfluks selama 30 menit
Residu Residu Residu
Disaring
Filtrat Ditambahkan 50 ml NaOH 1,25 N
Direfluks selama 30 menit
Disaring
Filtrat Dicuci dengan akuades panas
Disaring
Residu Residu Filtrat
Dikeringkan pada suhu 110 C Ditimbang
3.4.2. Analisa Kadar Serat dari Ampas Kelapa
5,001 g ampas kelapa yang telah dihilangkan lemaknya
Ditanur pada suhu 600 C selama 3 jam Ditimbang
Hasil
Ditambahkan 50 ml H2SO4 1,25 N Direfluks selama 30 menit
Disaring
Dicuci dengan 50 ml akuades panas Disaring
Ditambahkan 50 ml NaOH 1,25 N Direfluks selama 30 menit
Disaring
Dicuci dengan akuades panas Disaring
3.4.3. Hidrolisis Selulosa serta Uji gula Reduksinya
Selulosa
Ditambahkan 5 ml akuades sambil diaduk Dipanaskan di penangas air pada suhu 72-90oC
Campuran sampel dan air
Ditambah 10 ml HCl 30% Ditutup dengan aluminium foil
Dihidrolisis di penangas air mendidih selama 2 jam
Sampel terhidrolisis
Dinetralkan dengann NaOH 3 % Disaring
Dipipet 1 ml filtrat kedalam tabung reaksi
Dipanaskan dipenangas air
Residu filtrat
Ditambahkan 5 ml larutan Benedict secara kualitatif
3.4.4. Analisa Kandungan Glukosa Hasil Hidrolisis Selulosa Ampas Kelapa
filtrat hasil hasil hidrolisis selulosa ampas kelapa
Dimasukkan kedalam labu takar 250 ml
Diencerkan dengan akuades sampai garis tanda Dipipet sebanyak 1 ml
1 ml larutan glukosa sampel
Dimasukkan kedalam tabung reaksi Ditambahkan 1 ml pereaksi Nelson Ditutup dengan kapas
Dipanaskan dipenangas air pada suhu 100oC selama 30 menit
Didinginkan dibawah air yang mengalir Larutan dengan endapan merah bata
Diaduk hingga homogen
Ditambahkan 1 ml larutan arsenomolibdat Diaduk hingga endapan larut
Larutan berwarna biru
Ditambahkan 7 ml akuades Diaduk hingga homogen
Diukur absorbansinya pada panjang gelombang 714 nm
3.4.5. Pembuatan Nira dengan Penambahan Sirup Glukosa
Nira Aren
Dipipet
Dimasukkan kedalam masing-masing tabung reaksi
Ditambahkan sirup glukosa l k l k
Diaduk Dipanaskan
Dimasukkan kedalam cetakan Didinginkan
Diulangi perlakuan yang sama dengan perbandingan nira : sirup glukosa
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
Secara umum dari pemanfaatan sirup glukosa hasil hidrolisis serat kelapa memberikan pengaruh terhadap kadar gula reduksi. Hal ini dapat dilihat pada table berikut ini :
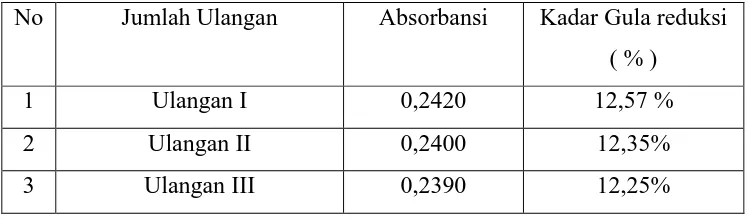
Tabel 4.1.1. Data Hasil Perhitungan Gula Reduksi Berdasarkan absorbansi Glukosa Hasil Hidrolisis Ampas kelapa.
No Jumlah Ulangan Absorbansi Kadar Gula reduksi ( % )
1 Ulangan I 0,2420 12,57 %
2 Ulangan II 0,2400 12,35%
3 Ulangan III 0,2390 12,25%
4.2. Pengolahan Data
4.2.1. Perhitungan Kadar Serat Kasar dari Ampas Kelapa
Perhitungan kadar serat kasar dapat dihitung dengan rumus sebagai berikut :
Maka Dapat Dicontohkan Kadar Serat Pada Ampas Kelapa Yakni :
4.2.2. Pengolahan Data Pengukuran Absorbansi Glukosa Hasil Hidrolisis Selulosa Ampas Kelapa
Pengolahan data pengukuran absorbansi glukosa hasil hidrolisis selulosa
ampas kelapa dilakukan secara statistik dengan metode Chauvenet Criterion Test ( CCT ) yang di ambil dari data absorbansi pada tabel 2.
Untuk melakukan Chauvenet Criterion Test perlu harga ht dan hh dapat dihitung dengan mengunakan rumus :
Maka ,
X1’ = X – X = 0,2420 – 0,2403 = 0,0017
X2’ = X – X = 0,2400 – 0,2403 = - 0,0003
X3 = X – X = 0,2390 – 0,2403 = - 0,0013
S2 = ∑ (X1 – X )2 = (0,0017 )2 + ( -0,0003 )2 + ( -0,0013 )2 n - 1 3 - 1
S2 = 2335 x 10-9
S = 0,00152
Maka Erf ht | X1’ | = 2n – 1 = 5 = 0,833 2n 6
ht | X1’| = 0,9906 ( tabel ) untuk X’ = 0,0017
Maka, ht = 0,9906 = 582,70 0,0017
Sedangkan hhitung adalah,
Hhitung = 1 = 2,7085 |S| √ 2
Karena 582,70 > 467,28 ( ht > h ) maka data signifikan dan dapat diterima dan dapat dilihat dalam tabel ( erf ). Untuk pengukuran kedua dan ketiga juga signifikan.
4.2.3. Perhitungan Kadar Glukosa Hasil Hidrolisis Selulosa Ampas Kelapa
Untuk menghitung kadar glukosa hasil hidrolisis selulosa dari ampas kelapa menggunakan HCl 30 % maka terlebih dahulu harus dicari persamaan garis regresi larutan glukosa standar dari berbagai konsentrasi.
Tabel 4.2.3.1. Working Sheet Larutan Glukosa Standar Pada Berbagai Konsentrasi
b = (∑X2) (∑Y) – ( ∑ X ) ( ∑Y ) n (∑ X2 ) - ( ∑ X )2
b = (0,1540) ( 3,8028) – ( 1.10 ) ( 0,4946 ) 10 ( 0.1540 ) – ( 1.10 )2
= 0,1257
Maka persamaan garis regresinya
Y = aX + b
Setelah diperoleh harga x kemudian disubtitusikan kedalam rumus :
Kadar gula reduksi = X . Fp x 100 % S
Dimana : X = konsentrasi glukosa dari perhitungan regresi Fp = faktor pengenceran ( mL)
Kadar gula reduksi = 0,0503 X 250 X 100 % 100
= 12,57 %
Data dari perhitungan kadar gula reduksi hasil hidrolisis selulosa diperoleh :
V = Kadar gula reduksi V1 = 12,57 %
V2 = 12,35 % V3 = 12,25 %
V = V1 + V2 + V3 3
4.3 Pembahasan
Hidrolisis selulosa dapat dilakukan oleh asam atau enzim. Jika selulosa dipanaskan dengan asam akan terurai menjadi molekul – molekul yang lebih kecil dengan tahapan yang berbeda tapi hasil akhirnya sama yaitu glukosa.
Dari hasil hidrolisis selulosa dari ampas kelapa mengunakan HCl 30 % dihasilkan sirup glukosa. Setelah diidentifikasi secara kualitatif dengan reagen benedict menunjukan hasil positif mengandung selulosa dengan terbentuknya endapan merah bata. Selanjutnya sirup glukosa dengan metode Nelson Somogyi mengunakan spektrofotometer pada panjang gelombang 714 nm.
Dari penelitian ini diperoleh kadar serat kasar ampas kelapa 22,504 % untuk 5,0001 g kering ampas kelapa. Kadar glukosa dari hasil hidrolisis selulosa dari ampas kelapa dapat menjadi salah satu alternatif yang dapat dimanfaatkan menjadi sirup glukosa.
Berdasarkan uji organoleptik yang dilakukan dapat diketahui bahwa perbandingan gula jawa dengan penambahan sirup glukosa dari ampas kelapa yang lebih dsukai adalah 1 : 3. Rata – rata panelis memberikan skor 4 untuk perbandingan tersebut.
Dari penelitian ini dapat diketahui bahwa sirup glukosa dari ampas kelapa dapat dimanfaatkan sebagai penambah rasa manis untuk gula merah/gula jawa.
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari data pada pembahasan hasil penelitian yang ber judul :Pemanfaatan sirup glukosa hasil hidrolisis serat dari ampas kelapa dalam pembuatan gula jawa / gula merah dengan volume bervariasi dapat disimpulkan bahwa serat kasar dari ampas kelapa kering dapat dimanfaatkan menjadi sirup glukosa dengan kandungan glukosanya sebesar 9,40 % dalam 10 gram ampas kelapa. Gula jawa/ gula merah yang lebih disukai adalah perbandingan 1 : 3
5.2. Saran
DAFTAR PUSTAKA
Apriyanto.A. 1989 .Analisa Pangan. Departemen Pendidikan dan Kebudayaan. Jakarta: Institut Pertanian Bogor.
Cakebread.S.H.1975. Sugar And Chocolate Confectionery. London: Oxford University.
Day.R.A., Underwood. A.L. 1999. Analisa Kimia Kuantitatif. Edisi Keempat. Jakarta: Erlangga.
Dwidjoseputro,D. 1983. Pengantar Fisiologi Tumbuhan. Jakarta: Gramedia. Dziedzic,S.Z. 1984 . Glucose Syrup, Science & Technology. New York: Elsevier Applied Science Publisher.
Fenzel,D. 1995. Kayu, Kimia, Ultrastruktur, Reaksi – Reaksi. Yogyakarta: Gadjah Mada Press.
Fogarty,W.M. 1983. Microbial Enzyme and Biotechnology. London: Applied Sciences Publishing.
Harlinah.S.P.W. 2003. Pemanfaatan Sampah Ampas Kelapa Menjadi Sirup Glukosa
Secara Hidrolisis Oleh HCl. Yogyakarta: Pusat Studi Bioteknologi Universitas Gadjah Mada.
Herlina.T. 2009. Pengaruh Lama Fermentasi dan Konsentrasi Starter Kadar Alkohol Dari Fermentasi Glukosa Hasil Hidrolisis Kulit Ubi Kayu ( manihot esculanta crant ) Dengan HCl 3 % Menggunakan Saccharomyces cerevicia. Skripsi S-1. Medan : Jurusan Kimia. FMIPA USU.
Iswari S.R,Yuniastuti.A. 2006. Biokimia . Yogyakarta : Graha Ilmu.
Larmond.E.1987.Laboratory Methods for Sensory Evaluation of Food.. Canada: Department of Agriculture.
Lynd. L.R. 2002. Microbial Cellulose Utilization Fundamental & Biotechnology. London : Applied Science Publishers.
Munandar.A.2006. Pengaruh Temperatur dan Durasi Inkubasi Kadar alkohol dari Fermentasi Glukosa Hasil Hidrolisis Pati Pulp Coklat (Theobroma cacaoL )
Dengan HCl 3 % Menggunakan Saccharomyces cerevicia. Skripsi S-1. Medan : Jurusan Kimia. FMIPA USU.
Sari.A. 2003. Pengaruh Lama Fermentasi oleh Saccharomyces cerevicia Terhadap Kadar Alkohol Hasil Hidrolisis Pati Sagu ( Metroxylon sp ) dengan HCl 3 % Skripsi S-1. Medan : Jurusan Kimia. FMIPA USU.
Sudarmadji. S. 1984. Analisa Bahan Makanan dan Pertanian. : Yogyakarta: Liberty.
Winarno. F.G. 1995. Pengantar Teknologi Pangan. Jakarta : Gramedia Pustaka Utama.
Suhardiyono,L. 1995 .Tanaman Kelapa Budidaya Dan Pemanfaatannya. Yogyakarta: Kanisius.
Wijayanti,L.2005. Pengaruh Temperatur dan Durasi Inkubasi Terhadap Kadar Alkohol dari Fermentasi Glukosa Hasil Hidrolisis Rampu Gajah ( Pennisetum pupureum) Dengan HCl 3 % Menggunakan saccharomyces cerevisiae. Skripsi S1. Jurusan Kimia. Medan: FMIPA USU
Lampiran 1
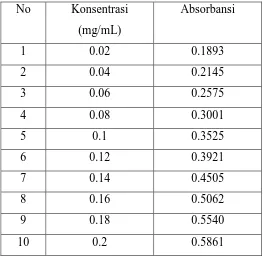
Tabel 1. Data absorbansi Larutan Glukosa standar Pada Berbagai Konsentrasi Pada λ= 714 nm
No Konsentrasi (mg/mL)
Absorbansi
1 0.02 0.1893
2 0.04 0.2145
3 0.06 0.2575
4 0.08 0.3001
5 0.1 0.3525
6 0.12 0.3921
7 0.14 0.4505
8 0.16 0.5062
9 0.18 0.5540
Tabel 2. Data Hasil Perhitungan Gula Reduksi Berdasarkan absorbansi Glukosa Hasil Hidrolisis Ampas kelapa.
No Jumlah Ulangan Absorbansi Kadar Gula reduksi ( % )
1 Ulangan I 0,2420 12,57
2 Ulangan II 0,2400 12,35
3 Ulangan III 0,2390 12,25
Tabel 3.Data Absorbansi Nira dengan penambahan Sirup Glukosa Pada λ= 714 nm
No Volume Nira : Sirup glukosa Aborbansi
1 1 : 1 0.8735
2 1 : 2 1.3975
3 1 : 3 1.4261
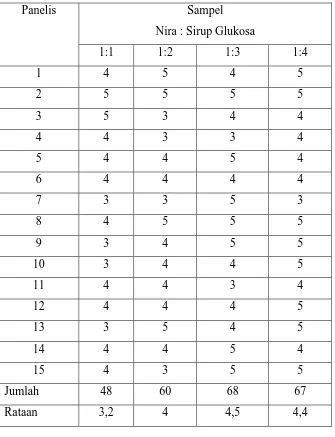
Tabel 5. Data Hasil Uji Organoleptis Terhadap Rasa Gula Merah/Gula Jawa Dengan Penambahan Sirup Glukosa
Panelis Sampel
Nira : Sirup Glukosa
1:1 1:2 1:3 1:4
1 4 5 4 5
2 5 5 5 5
3 5 3 4 4
4 4 3 3 4
5 4 4 5 4
6 4 4 4 4
7 3 3 5 3
8 4 5 5 5
9 3 4 5 5
10 3 4 4 5
11 4 4 3 4
12 4 4 4 5
13 3 5 4 5
14 4 4 5 4
15 4 3 5 5
Jumlah 48 60 68 67
Tabel 6 . Data Hasil Uji Organoleptis Terhadap Warna Gula Merah/Gula Jawa Dengan Penambahan Sirup Glukosa
Panelis Sampel
Nira : Sirup glukosa
1:1 1:2 1:3 1:4
1 4 4 4 5
2 5 5 5 5
3 5 3 4 4
4 4 3 4 4
5 4 4 5 4
6 4 4 4 4
7 3 3 5 3
8 4 5 5 5
9 3 3 5 5
10 3 3 5 5
11 4 4 3 4
12 4 4 5 5
13 3 5 4 5
14 3 4 5 4
15 3 3 5 5
Jumlah 46 57 71 67
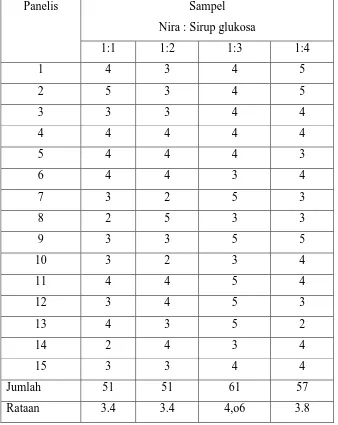
Tabel 7 . Data Hasil Uji Organoleptis Terhadap Aroma Gula Merah/Gula Jawa Dengan Penambahan Sirup Glukosa
Panelis Sampel
Nira : Sirup glukosa
1:1 1:2 1:3 1:4
1 4 3 4 5
2 5 3 4 5
3 3 3 4 4
4 4 4 4 4
5 4 4 4 3
6 4 4 3 4
7 3 2 5 3
8 2 5 3 3
9 3 3 5 5
10 3 2 3 4
11 4 4 5 4
12 3 4 5 3
13 4 3 5 2
14 2 4 3 4
15 3 3 4 4
Jumlah 51 51 61 57
Gambar 2.3 Kurva Penentuan λ Maksimum dari Larutan Glukosa (0,05 mg/mL)