PERBANYAKAN TUNAS Boesenbergia flava DENGAN PEMBERIAN BAP DAN NAA SECARA IN VITRO
SKRIPSI
Oleh :
LYLI HERAWATI SIREGAR 070307006
BDP – PEMULIAAN TANAMAN
PROGRAM STUDI AGROEKOTEKNOLOGI FAKULTAS PERTANIAN
UNIVERSITAS SUMATERA UTARA MEDAN
ABSTRAK
LYLI HERAWATI SIREGAR : Perbanyakan Tunas Boesenbergia flava dengan Pemberian BAP dan NAA Secara In Vitro, dibimbing oleh Luthfi Aziz Mahmud Siregar dan Lollie Agustina P. Putri.
Penelitian ini bertujuan untuk mengetahui pengaruh konsentrasi BAP dan NAA terhadap perbanyakan tunas Boesenbergia flava secara in vitro. Penelitian ini dilaksanakan di Laboratorium Kultur Jaringan Tanaman, Fakultas Pertanian Universitas Sumatera Utara, Medan yang dimulai pada bulan Maret sampai dengan Mei 2012. Rancangan yang digunakan adalah Rancangan Acak Lengkap (RAL) dengan dua faktor perlakuan. Faktor pertama adalah konsentrasi NAA yang terdiri dari 4 taraf yaitu 0 mg/l; 1 mg/l; 2 mg/l; 3 mg/l. Faktor kedua adalah konsentrasi BAP meliputi 0 mg/l; 1,5 mg/l; 3 mg/l; 4,5 mg/l.
Hasil penelitian menunjukkan bahwakonsentrasi NAA berpengaruh nyata terhadap panjang akar dan tinggi tanaman dan konsentrasi BAP berpengaruh nyata terhadap parameter panjang akar, tinggi tanaman tetapi tidak berpengaruh nyata terhadap jumlah akar dan jumlah daun. Demikian juga Interaksi konsentrasi NAA dan BAP berpengaruh nyata pada panjang akar dan jumlah akar namun tidak berpengaruh nyata tinggi tanaman dan jumlah daun.
ABSTRACT
LYLI HERAWATI SIREGAR : The Micropropagation of Boesenbergia flava bud by BAP and NAA for in vitro, guided by oleh Luthfi Aziz Mahmud Siregar dan Lollie Agustina P. Putri.
The research aimed to know the influence of BAP and NAA concentration on micropropagation of Boesenbergia flava bud for in vitro. The research was carried out in the Tissue Culture Laboratory, Agriculture’s facuity of Nort Sumatera University from March to May 2012. This research used Completely Randomezed Design with two treatment factors. First factor was NAA concentration consist of four level; 0 mg/l; 1 mg/l; 2 mg/l; 3 mg/l. The second factor was BAP concentration consist of four level are 0 mg/l; 1,5 mg/l; 3 mg/l; 4,5 mg/l.
The results of research showed that NAA concentration give significantly affected on long of roots and plant height and BAP concentration give significantly affected on long of roots and plant height but that was not significantly affected on roots number and leaves number. Similarly to interaction of concentration NAA dan BAP give significantly affected on long of roots and roots number butth at was not significantly affected on plant height and leaves number.
PENDAHULUAN
Latar Belakang
Boesenbergia flava merupakan tanaman yang berasal dari famili
zingiberaceae. Spesies Boesenbergia sangat langka dibandingkan dengan genera
lain. Sebagian besar, Boesenbergia ditemukan dalam area sangat lembab, area
teduh dan biasanya dekat dengan sungai atau dalam kondisi berawa, yang
keberadaannya masih susah ditemukan karena tanaman ini langka, boesenbergia
adalah genus dari tumbuh-tumbuhan rhizomatus kecil, sebagian besar tumbuh di
hutan (Sirirugsa, 1992).
Zingiberaceae merupakan tanaman herba tropis yang mempunyai 47 genus
dan 1400 spesies dan pada umumnya banyak digunakan sebagai obat-obatan,
bahan kosmetik maupun bumbu masak (Yunira dkk, 2008).
Perkembangan industri berbahan baku tanaman obat dalam 5 tahun
terakhir menunjukkan pertumbuhan yang signifikan dan omset produksinya
selama kurun waktu tersebut meningkat sebesar 2,5 – 30% /tahun. Pada tahun
2000 nilai perdagangan tanaman obat di Indonesia mencapai Rp.1,5 trilyun rupiah
setara dengan US $ 150 juta, masih jauh di bawah nilai perdagangan herbal dunia
yang mencapai US $ 20 milyar; US $ 8 milyar dikuasai oleh produk herbal dari
China (Rini, 2009).
Salah satu aspek yang terpenting dalam kultur jaringan adalah
kemampuan untuk beregenerasi dan memperbanyak tanaman (mikropropagasi).
Mikropropogasi adalah perbanyakan vegetatif tanaman dengan menggunakan
akhir ini, kendala dalam memperbanyak beberapa jenis tanaman dapat diatasi
(Wattimena dkk, 1992).
Masalah yang dihadapi dalam pengembangan tanaman penghasil obat dan
pada umumnya adalah merupakan tanaman musiman atau tahunan sehingga
membutuhkan waktu yang cukup lama untuk mendapatkan hasilnya. Berbagai
kendala dijumpai dalam perbanyakan temu-temuan antara lain : budidaya, pasca
panen, mutu dan fluktuasi harga. Di sisi lain, desakan penduduk dan
perkembangan industri yang semakin menyempitkan ketersediaan lahan-lahan
pertanian. Penggunaan teknik kultur jaringan jadi lebih menarik dari pada
menumbuhkan di lapangan yang mempunyai banyak hambatan. Perbanyakan dan
pengembangan temu-temuan dengan teknik kultur jaringan mulai dilirik untuk
mempercepat proses dalam mengatasi berbagai kendala tersebut di atas
(Kristina dkk, 2002).
Dengan teknik in vitro mampu memproduksi bibit dalam jumlah besar
dengan waktu yang relatif singkat, bebas patogen, identik dengan induknya dan
tidak dipengaruhi musim. Teknik ini memerlukan media buatan yang dibuat dari
beberapa komponen utama yaitu gula, air, unsur hara makro dan mikro, vitamin,
asam amino, serta zat pengatur tumbuh. Gula sangat diperlukan sebagai sumber
energi dalam kultur jaringan karena tanaman bersifat heterotrof (Sastra, 2005).
Perbanyakan tanaman secara in vitro bertujuan untuk memperoleh
bahan tanaman steril yang akan digunakan untuk perbanyakan bibit.
Oleh karena itu, diperlukan proses sterilisasi yang tepat untuk mematikan
mikroorganisme yang terdapat pada eksplan sehingga tidak mengganggu
(tanaman), seperti tanaman herbal atau berkayu, dan kondisi lingkungan
(Aisyah dan Dedi, 2011).
Media yang biasa adalah media Murashige & Skoog (MS). Media MS
digunakan untuk hampir semua macam tanaman, terutama tanaman herbasius.
Media ini mempunyai konsentrasi garam-garam mineral yang tinggi dan senyawa
N dalam bentuk NO3- dan NH4- (Hendaryono dan Wijayani, 1994).
Salah satu alternatif metode perbanyakan yang dapat ditempuh adalah
melalui kultur in vitro. Metode ini diharapkan mampu menghasilkan tanaman
dalam skala besar dengan waktu yang relatif cepat serta kualitas tanaman yang
dihasilkan menjadi lebih baik melalui kultur jaringan kebutuhan ketersediaan bibit
tanaman dalam jumlah yang banyak dapat terpenuhi (Gunawan, 1992).
Penelitian tentang perbanyakan Boesenbergia flava hingga saat ini masih
sangat kurang, mengingat keterbatasan informasi tentang perbanyakannya secara
in vitro pun masih sangat terbatas. Berdasarkan uraian di atas, maka dipandang
perlu untuk melakukan penelitian mengenai pengaruh pemberian NAA dan BAP
terhadap perbanyakanBoesenbergia flava secara in vitro.
Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui pengaruh NAA dan BAP serta
interaksi keduanya terhadap pertumbuhan tunas Boesenbergia flavasecara in vitro.
Hipotesis Penelitian
Ada pengaruh interaksi antara tingkat konsentrasi NAA dan BAP terhadap
Kegunaan Penelitian
Penelitian ini berguna untuk mendapatkan data penyusunan skripsi sebagai
salah satu syarat untuk mendapatkan gelar sarjana pertanian di Fakultas Pertanian,
Universitas Sumatera Utara, Medan dan diharapkan dapat pula berguna untuk
TINJAUAN PUSTAKA
Berdasarkan ZipcodeZoo.com (2012) klasifikasi tanaman
Boesenbergia flava Holttum adalah Kingdom: Plantae, Class: Magnoliopsida
Ordo: Zingiberales, Family: Zingiberaceae, Genus: Boesenbergia ,
spesies: Boesenbergia flava Holttum.
Batang yang berdaun pendek dengan masing-masing 4 daun dan pelepah
merah di pangkalnya. Helaian daun yang ke 20 dengan panjang 6 cm, agak
simetris, berbentuk bulat panjang hijau dengan tanda keperak-perakan ditengah
(dengan pelepah dan sebuah tanda di kedua sisi itu) panjang tangkai daun 2-4 cm.
Panjang ligula-lobus 1 cm, tipis, merah muda: pelepah memerah atau
belang-belang dengan warna merah hampir seluruhnya. Perbungaan seluruhnya di
sembunyikan oleh daun seperti dalam B. Pandurata dan dengan bentuk yang
mirip. Panjang bracts sekitar 5 cm dan kemerah-merah mudaan. Panjang
corolla – tube 1- 1,5 cm lebih panjang dari bracts. Panjang lobus kuning 2-2,5 cm,
lebarnya 2 cm, hampir datar kekuning-kuningan menempel di dekat pucuk dan
bercak merah di kedua sisi garis tengah menuju pangkal. Panjang serabut hampir
1-5 cm, pucat kekuning-kuningan ± sedikit merah ke merah mudaan: panjang
anther sekitar 5 mm, kantung serbuk sari agak di pucuk. Sambungan di
perpanjang menjadi 1 mm panjangnya tidak lebih lebar dari pada anther, sedikit
melipat dengan ujung yang sangat pendek (Bulletin, 1950).
Spesies ini awalnya di kenalkan oleh Ridley dari sebuah tanaman yang
di budidayakan di Penang, di bawa dari kabupaten Batang Padang (perak) gambar
yang berwarna ada di Singapura dan juga contoh keringnya di buat dari gambar
tanaman. Bunga dari Boesenbergia flava besar dan warnanya kuning dengan
tanda merah khusus (Bulletin, 1950).
Kultur Jaringan
Kultur jaringan itu sendiri dapat diartikan suatu metode untuk mengisolasi
bagian tersebut dapat memperbanyak diri dan beregenerasi menjadi tanaman
lengkap (Hartman dkk, 2002).
Berbeda dengan teknik perbanyakan vegetatif konvensional, kultur
jaringan melibatkan pemisahan komponen-komponen biologis dan tingkat
pengendalian yang tinggi dalam memacu proses regenerasi dan perkembangan
jaringan. Setiap urutan proses dapat dimanipulasi melalui seleksi bahan tanaman,
medium kultur dan faktor-faktor lingkungan, termasuk eliminasi mikroorganisme
seperti jamur dan bakteri. Semua itu dimaksudkan untuk memaksimalkan produk
akhir dalam bentuk kuantitas dan kualitas propagula berdasarkan prinsip
totipotensi sel (Zulkarnain, 2009).
Dibanding dengan perbanyakan tanaman secara konvensional,
perbanyakan tanaman secara kultur jaringan mempunyai beberapa kelebihan
sebagai berikut:
1. Untuk memperbanyak tanaman tertentu yang sulit atau sangat lambat
diperbanyak secara konvensional. Perbanyakan tanaman secara kultur
jaringan menawarkan peluang besar untuk menghasilkan jumlah bibit
tanaman yang banyak dalam waktu relatif singkat sehingga lebih ekonomis.
2. Perbanyakan tanaman secara kultur jaringan tidak memerlukan tempat yang
luas.
3. Teknik perbanyakan tanaman secara kultur jaringan dapat dilakukan
sepanjang tahun tanpa bergantung pada musim.
4. Bibit yang dihasilkan lebih sehat.
5. Memungkinkan dilakukannya manipulasi genetik.
Pada dasarnya kultur in vitro merupakan suatu proses perbanyakan sel,
jaringan, organ atau protoplasma dengan teknik steril. Keberhasilan teknologi in
vitro masih terbatas pada beberapa tanaman tertentu saja. Kultur in vitro juga
memberikan pengertian tentang studi fisiologi, biokimia, genetika pertumbuhan
dan perkembangan spesies tanaman pada tingkat molekuler (Nasir, 2000)
Eksplan
Kondisi fisiologis eksplan memiliki peranan penting bagi keberhasilan
teknik kultur jaringan. Pierik (1997) menyatakan bahwa pada umumnya
bagian-bagian vegetatif lebih siap beregenerasi daripada bagian-bagian-bagian-bagian generatif. Eksplan
mata tunas yang diperoleh dari tanaman yang sedang istirahat, lebih sulit
berpoliferasi daripada mata tunas yang diperoleh dari tanaman yang sedang aktif
tumbuh. Hal itu sama halnya dengan kasus dormansi pada eksplan biji. Kondisi
fisiologis dari suatu tanaman bervariasi secara alami, sejalan dengan pertumbuhan
tanaman yang melewati fase-fase yang berbeda dan perubahan kondisi lingkungan
(Zulkarnain, 2009).
Dalam pemilihan bagian tanaman, perlu juga dipertimbangkan tujuan dari
kulturnya. Bagian-bagian tertentu akan memberikan variasi dalam jumlah
kromosom maupun variasi dalam beberapa gen. Endosperma hanya digunakan
untuk mendapatkan kultur yang triploid. Selain bagian tanaman, genotip atau
varietas yang digunakan juga ikut menentukan keberhasilan regenerasi
(Gunawan, 1995).
Eksplan adalah bagian kecil jaringan atau organ yang di pisahkan dari
tergantung pada faktor yang meliputi genotif eksplan, umur fisiologis juga sumber
jaringan (Hughes, 1982).
Pada tanaman herba, eksplan diambil baik dari pucuk apikal maupan
lateral yang mengambil jaringan meristematik namun sering kali digunakan mata
tunas yang diharapkan akan berkembang membentuk daun dan batang sempurna.
Bagian tanaman yang digunakan sebagai eksplan adalah tunas lateral atau
terminal yang panjangnya kurang lebih 20 mm. Pengaruh dominasi apikal dapat
dihilangkan dengan menambahkan zat pengatur tumbuh (terutama sitokinin)
kedalam medium. Sebagai hasilnya adalah tunas dengan jumlah cabang yang
banyak (Wattimena, 1992).
Media Kultur
Sebelum membuat medium, maka terlebih dahulu kita harus menentukan
medium apa yang akan kita buat. Jenis medium dengan komposisi unsur kimia
yang berbeda dapat digunakan untuk media tumbuh dari jaringan tanaman yang
berbeda pula (Hendaryono dan Wijayani, 1994).
Medium yang digunakan untuk kultur in vitro tanaman dapat berupa
medium padat atau cair. Medium padat digunakan untuk menghasilkan kalus yang
selanjutnya diinduksi membentuk tanaman yang lengkap (disebut sebagai planlet),
sedangkan medium cair biasanya digunakan untuk kultur sel. Medium yang
digunakan mengandung lima komponen utama yaitu senyawa anorganik, sumber
karbon, vitamin, zat pengatur tumbuh dan suplemen organik (Yuwono, 2008).
Media yang digunakan secara luas adalah media MS yang dikembangkan
pada tahun 1962. Dari berbagai komposisi dasar ini kadang-kadang dibuat
makro yang digunakan (1/2 MS) atau menggunakan komposisi garam makro
berdasarkan MS tetapi mikro dan vitamin berdasarkan komposisi Heller. Zat
pengatur tumbuh yang akan digunakan disesuaikan dengan tujuan inisiasi kultur
(Gunawan, 1995).
Jenis dan komposisi media sangat memerlukan biaya produksi dan
keberhasilan perbanyakan tanaman secara in vitro. Teknik perbanyakan bibit
secara in vitro dapat di lakukan setiap waktu tanpa dipengaruhi oleh musim.
Walaupun demikian, biaya produksi bibit jahe dengan teknik kultur jaringan
sangat mahal, karena pada umumnya di gunakan Murashige dan skoog (MS) yang
merupakan media pertumbuhan dengan bahan pemadat agar yang diperkaya
dengan berbagai senyawa organik, vitamin dan zat pengatur tumbuh
(Sutarto dkk, 2003).
Lingkungan In Vitro
Lingkungan kultur merupakan hasil interaksi antara bahan tanaman,
wadah kultur, dan lingkungan eksternal ruang kultur, memiliki pengaruh yang
sangat besar terhadap suatu sistem kultur jaringan. Secara teoritis, semua variabel
di dalam setiap wadah kultur pada ruang kultur yang sama adalah seragam.
Sebagai konsekuensinya, hal yang sama terjadi pula di wadah-wadah kultur pada
sruang kultur yang lain. Agar pertumbuhan kultur seragam maka keseragaman
faktor lingkungan harus diupayakan, tidak hanya di dalam ruang kultur, tetapi
juga di dalam semua wadah kultur dengan cara menggunakan wadah yang
Lingkungan tumbuh yang dapat mempengaruhi regenerasi tanaman
meliputi: Temperatur, Penyinaran: panjang penyinaran, intensitas penyinaran, dan
kualitas sinar, serta ukuran wadah kultur (Gunawan, 1995).
Temperatur di dalam ruang kultur jaringan diharapkan dapat diatur.
Banyak laporan mengatakan bahwa temperatur yang baik untuk pertumbuhan
tanaman dalam in vitro antara 20-280 c yang merupakan suhu ruangan normal.
Suhu ruangan untuk negara tropis dapat diturunkan dengan pemasangan AC.
Pemakaian AC mutlak karena ruang kultur merupakan ruangan tertutup yang
sedikit sekali mempunyai aliran udara bebas (Gunawan, 1987).
Pengaruh intensitas cahaya terhadap pembentukan akar bergantung pada
cara pemberian cahaya tersebut. Protokorm Cymbidium yang berwarna hijau akan
membentuk akar dan tunas bila diberi intensitas cahaya 2200 sampai 2500 lux.
Namun, bila disimpan dalam gelap hanya membentuk tunas. Pembentukan akar
disini diduga ada kaitannya dengan metabolism nitrogen yang terjadi dengan
adanya cahaya. Untuk keperluan kultur jaringan cahaya putih dari lampu
flourscent dengan intensitas 1000 lux untuk fase inisiasi dan subkultur, sedangkan
untuk fase pengakaran dan persiapan planlet sebelum dilakukan aklimatisasi
menggunakan intensitas 3000 sampai 10000 lux. Intensitas yang lebih rendah
akan menghasilkan planlet yang mengalami etiolasi dengan daun yang berwarna
pucuk. Lama penyinaran yang dianjurkan adalah 16 jam per hari
(Wattimena dkk, 1992).
Zat Pengatur Tumbuh
Zat pengatur tumbuh memegang peranan penting dalam pertumbuhan dan
zat pengatur tumbuh antara lain jenis zat pengatur tumbuh yang akan digunakan,
konsentrasi, urutan penggunaan, dan periode masa induksi dalam kultur tertentu
(Gunawan, 1995).
Pierik (1997) mengemukakan bahwa fitohormon adalah senyawa-senyawa
yang dihasilkan oleh tanaman tingkat tinggi secara endogen. Senyawa tersebut
berperan merangsang dan meningkatkan pertumbuhan serta perkembangan sel,
jaringan dan organ tanaman menuju arah diferensiasi tertentu. Senyawa-senyawa
lain yang memiliki karakteristik yang sama dengan hormone, tetapi diproduksi
secara eksogen, dikenal sebagai zat pengatur tumbuh.
Untuk meningkatkan daya regenerasi dari eksplan tunas diperlukan
penambahan zat pengatur tumbuh dalam media tanam. Kebutuhan nutrisi dan zat
pengatur tumbuh untuk memacu proses morfogesis pada kultur in vitro akan
berbeda untuk setiap jenis tanaman dan eksplan yang digunakan ( Marlin, 2005)
Naftalen asam asetat (NAA)
Auksin adalah sekelompok senyawa yang fungsinya merangsang
pemanjangan sel-sel pucuk yang spektrum aktivitasnya menyerupai IAA
(indole-3-acetic-acid). Pierik (1997) menyatakan bahwa pada umumnya auksin
meningkatkan pemanjangan sel, pembelahan sel, dan pembentukan akar adventif.
Auksin berpengaruh pula untuk menghambat pembentukan tunas adventif dan
tunas aksilar, namun kehadirannya dalam medium kultur dibutuhkan untuk
meningkatkan embriogenesis somatik pada kultur suspensi sel. Konsentrasi auksin
yang rendah akan meningkatkan pembentukan akar adventif, sedangkan auksin
konsentrasi tinggi akan merangsang pembentukan kalus dan menekan
Pertumbuhan dari kultur jaringan atau organ dan In vitro morfogenesis
lebih dipengaruhi oleh genotipe sumber jaringan atau organ yang digunakan
dibandingkan dengan faktor lainnya. Media dan kondisi fisik lingkungan tumbuh
kultur sering kali berbeda satu genus dengan genus yang lain, atau spesies
tanaman tertentu dengan spesies lain. Tidak jarang antar varietas yang memiliki
sifat dekat namun kebutuhannya akan lingkungan dan media berbeda
(Wattimena, dkk, 1992).
Naphthalene Acetic Acid (NAA) adalah auksin sintetik yang sering
ditambahkan dalam media tanam karena mempunyai sifat lebih stabil dari pada
Indol Acetic Acid (IAA). IAA dapat mengalami degradasi yang disebabkan
adanya cahaya atau enzim oksidatif. Oleh karena sifatnya yang labil IAA jarang
digunakan dan hanya merupakan hormon alami yang ada pada jaringan
tanaman yang digunakan sebagai eksplan. Sedangkan NAA tidak mudah terurai
oleh enzim yang dikeluarkan sel atau pemanasan pada proses sterilisasi
(Wulandari dkk, 2004).
Benzil aminopurin (BAP)
Sifat paling karakteristik yang berkaitan dengan sitokinin adalah
perangsangan hormon terhadap pembelahan sel pada kultur jaringan tanaman.
Satu dari reaksi yang benar-benar dramatis terhadap sitokinin adalah
pembentukan organ-organ yang terjadi di bawah kondisi yang tepat dalam
berbagai kultur jaringan. Dengan pemprosesan sitokinin mengeluarkan
pembentukan tunas yang melimpah (Wilkins, 1989).
Sitokinin meningkatkan baik sitokineis maupun pembesaran sel, terutama
sendiri, sebab sitokinesis hanya merupakan proses pembelahan saja sitokinin
berfungsi untuk memacu pembelahan sel dan pembentukan organ, menunda
penuaan dan meningkatkan aktifitas wadah penampung hara, memacu
perkembangan pucuk dan di dukung oleh Dwidjoseputro (1980) yang menyatakan
sitokinin bukan senyawa tunggal melainkan kumpulan senyawa yang berfungsi
mirip satu dengan yang lain. Zat ini menggiatkan pembelahan sel jelas juga
pengaruhnya terhadap pertumbuhan tunas dan akar (Salisbury dan Ross, 1995).
Zat pengatur tumbuh yang diberikan harus dapat diabsorbsi dan
ditranslokasikan ke jaringan target. Hal ini tentu tergantung dari formulasi dan
konsentrasi zat pengatur tumbuh sehingga dapat dikatakan bahwa pada
konsentrasi tersebut belum dapat diabsorbsi dan ditranslokasikan oleh tanaman
untuk pertumbuhan dan perkembangan. Peningkatan konsentrasi auksin akan
menghambat inisiasi akar, pembelahan sel dan pemanjangan akar menambahkan
konsentrasi NAA yang ditingkatkan ke media pengakaran akan meningkatkan
auksin endogen sehingga terjadi akumulasi auksin. Akumulasi auksin ini akan
menghambat pemajangan akar. Konsentrasi auksin endogen yang tinggi dapat
menyebabkan pemendekan sel-sel. konsentrasi zat pengatur tumbuh untuk
pembesaran sel-sel pada batang menjadi penghambat pada pembentukan
sel-sel akar. Interaksi BAP dan NAA mempengaruhi aktivitas sel sel di batang
untuk memunculkan tunas sehingga aktivitas sel-sel di akar terhambat
(Wattimena, dkk, 1992).
Disamping merangsang pembentukan tunas adventif, sitokinin juga
merangsang multiplikasi tunas aksilar dan melawan dominasi apikal. Tunas
dikulturkan. Pengulturan dalam media yang ditambah dengan sitokinin bertujuan
untuk merangsang pecah dan tumbuhnya mata tunas samping dan mencegah
dominansi tunas apikal yang mengakibatkan terbentuknya tunas samping
(Yusnita, 2003).
Zat pengatur tumbuh pada tanaman adalah senyawa organik yang bukan
hara yang dalam jumlah sedikit dapat mendukung (promote), menghambat dan
merubah proses fisiologi tumbuhan. Auksin dan sitokinin adalah zat pengatur
tumbuh yang sering ditambahkan dalam media tanam karena mempengaruhi
pertumbuhan dan organogenesis dalam kultur jaringan dan organ. Auksin sintetik
perlu ditambahkan karena auksin yang terbentuk secara alami sering tidak
mencukupi untuk pertumbuhan jaringan eksplan. Auksin mempunyai peranan
terhadap pertumbuhan sel, dominasi apikal dan pembentukan kalus.
Kisaran konsentrasi auksin yang biasa digunakan adalah 0,01-10 ppm.
(Wulandari dkk, 2004)
BAP (6-Benzyl Amino Purine) merupakan golongan sitokinin sintetik yang
paling sering digunakan dalam perbanyakan tanaman secara kultur in vitro. Hal
ini karena BAP mempunyai efektifitas yang cukup tinggi untuk perbanyakan
tunas, mudah didapat dan relatif lebih murah dibandingkan dengan kinetin
(Kurnianingsih dkk, 2009).
Menurut Widyastuti (2004) bahwa akar yang tumbuh pada media tanpa zat
pengatur tumbuh kemungkinan diinduksi oleh auksin endogen.Rahardja (1989)
dan Cleland (1995) yang dikutip dari Kurnianingsih (2009) menyebutkan bahwa
dalam kultur jaringan auksin merupakan zat pengatur tumbuh yang dapat
merangsang pembentukan akar. Jika konsentrasi auksin dalam media kultur tinggi
maka akan menghambat pertumbuhan tunas (Kurnianingsih 2009).
Menurut Wiendi dkk (1991) menyatakan bahwa pada beberapa tanaman
membutuhkan waktu yang lama untuk beregenerasi. Kemungkinan sitokinin
endogen tidak mencukupi untuk pembentukan tunas berarti selain auksin zat
pengatur tumbuh sitokinin juga perlu ditambahkan ke dalam media. Pierik (1987)
menyatakan bahwa sitokinin berperan dalam memacu pertumbuhan dan
perkembangan tanaman khususnya tunas adventif yang di kutip dari Azriati
(2005) menyebutkan tanpa adanya penambahan sitokinin ke dalam media tanam
menyebabkan eksplan tidak mampu berorganogenesis membentuk tunas karena
belum adanya interaksi dan keseimbangan antara auksin dan sitokinin endogen
dengan auksin dan sitokinin eksogen. Menurut Evans, dkk (1986) yang dikutip
oleh Sobardini, dkk (2006) yang menyatakan bahwa tunas yang sedang
berkembang dapat memproduksi auksin dalam jumlah yang cukup untuk perakaran
BAHAN DAN METODE
Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Laboratorium Kultur Jaringan Tanaman,
Fakultas Pertanian Universitas Sumatera Utara, Medan yang dimulai pada bulan
Maret sampai dengan Mei 2012.
Bahan dan Alat Penelitian
Bahan tanaman yang digunakan dalam penelitian ini adalah planlet
Boesenbergia flava yang berasal dari PT. Tamora Stakindo dan dipelihara dalam
media MS dengan penambahan zat pangatur tumbuh NAA dan BAP. Bahan
tanaman Boesenbergia flava diperoleh dari kawasan hutan di Batang Padang,
Malaysia. Bahan untuk media meliputi larutan stok media MS, NAA, BAP,
agar-agar, NaOH 1 N, HCl, pH meter/kertas lakmus, aluminium foil dan aquades.
Bahan sterilisasi yang digunakan dalam penelitian ini adalah alkohol 96%.
Alat-alat yang digunakan adalah autoklaf, Laminar Air Flow (LAF), botol
kultur, erlenmeyer, pipet skala, gelas ukur, petridis, skalpel, gunting, bunsen,
timbangan analitik, hot plate, batang pengaduk, lemari es, kertas milimeter, pinset,
oven, dan alat-alat lainnya yang mendukung penelitian ini.
Metode Penelitian
Percobaan ini menggunakan Rancangan Acak Lengkap (RAL) Faktorial
dengan dua perlakuan, yaitu:
Faktor I : Tingkat konsentrasi Pemberian NAA dengan 4 taraf :
N1 = 1 mg/l
N2 = 2 mg/l
N3 = 3 mg/l
Faktor II : Tingkat Konsentrasi Pemberian BAP dengan 4 taraf :
B0 = 0 mg/l
B1 = 1,5 mg/l
B2 = 3 mg/l
B3 = 4,5 mg/l
Kombinasi perlakuan ada 16, yaitu:
N0B0 N1B0 N2B0 N3B0
N0B1 N1B1 N2B1 N3B1
N0B2 N1B2 N2B2 N3B2
N0B3 N1B3 N2B3 N3B3
Jumlah ulangan : 4 ulangan
Jumlah Kombinasi : 16 kombinasi
Jumlah Tanaman/botol : 1 tanaman
Jumlah sampel/botol : 1 tanaman
Jumlah seluruh botol : 64 botol kultur
Jumlah seluruh tanaman : 64 tanaman
Data hasil penelitian dianalisi dengan sidik ragam model linier sebagai
berikut:
dengan:
Yijk = Hasil pengamatan dari konsentrasi pada taraf ke-i dan konsentrasi pada
taraf ke-j dalam ulangan ke-k
µ = Efek dari nilai tengah
αi = Efek dari konsentrasi NAA pada taraf ke-i
βj = Efek konsentrasi BAP pada taraf ke-j
(αβ)ij = Interaksi antara konsentrasi NAA dan BAP pada taraf ke-i dengan
konsentrasi BAP pada taraf ke-j
εijk = Galat dan konsentrasi NAA pada taraf ke-i dengan konsentrasi BAP
pada taraf ke-j dalam ulangan ke-k
Uji lanjutan yang digunakan dalam menentukan notasi bagi perlakuan
yang berpengaruh nyata terhadap parameter yang di ambil adalah uji BNJ pada
PELAKSANAAN PENELITIAN
Pembuatan Larutan Stok
Pembuatan larutan stok bertujuan untuk memudahkan pekerjaan dalam
membuat media. Larutan stok dibuat sesuai dengan komposisi media Murashige
dan Skoog (MS) (Lampiran 3) yang diaduk dalam erlenmeyer dengan konsentrasi
yang lebih pekat. Pembuatan larutan stok bahan kimia hara makro dengan
pemekatan 20x, hara mikro dengan pemekatan 200x, larutan iron dengan
pembesaran 100x, larutan vitamin dengan pembesaran 200x. Kemudian stok
disimpan di dalam lemari es.
Sterilisasi Alat
Sterilisasi bermanfaat untuk membersihkan seluruh alat-alat yang
digunakan dalam kultur jaringan sehingga terbebas dari hal-hal yang dapat
menimbulkan kontaminasi. Alat-alat tersebut dicuci dengan deterjen, kemudian
dibilas dengan air, setelah itu dikeringkan. Kemudian alat seperti skalpel, pipa
skala, pinset dan cawan petri dibungkus dengan kertas, sedang untuk erlenmeyer
dan gelas ukur permukaannya ditutup dengan aluminium foil. Setelah itu, semua
botol kultur dan alat-alat dimasukkan ke dalam autoklaf pada tekanan 17,5 psi,
dengan suhu 1210C selama 60 menit. Kemudian alat-alat tersebut dimasukkan ke
dalam oven kecuali botol kultur.
Subkultur
Subkultur merupakan salah satu tahap dalam perbanyakan tanaman
melalui kultur jaringan. Untuk subkultur bahan tanaman yang diperoleh dari
tanaman tidak kekurangan hara. Cara kerja subkultur yaitu dengan cara planlet
dikeluarkan dari botol kultur lalu di masukkan ke dalam cawan petri, planlet di
potong-potong dengan menggunakan scalpel streril. Potongan tadi dimasukkan ke
dalam media yang baru (MS + 0,5 mg/NAA + 1 mg/BAP) kemudian dipelihara
selama 8 minggu.
Pembuatan Media
Media yang digunakan dalam penelitian ini adalah media MS dengan
menggunakan dua zat pengatur tumbuh yaitu BAP dan NAA. Untuk pembuatan
media 1 liter dilakukan dengan mengisi beker glass dengan aquades steril
sebanyak 500 ml. Kemudian ditambahkan larutan stok A (makro) sebanyak 50 ml,
stok B (mikro) 5 ml, stok C (iron) 10 ml, stok D (vitamin) 5 ml (lampiran 3).
Kemudian ditambahkan myo-inositol 0,1 gram dan sukrosa 30 gram. Setelah itu,
ditambahkan aquades sampai mendekati 2000 ml. Lalu pH-nya diukur dengan
menggunakan pH meter dan dilihat angkanya. Bila pH masih dibawah 5,7 maka
perlu ditambah NaOH 1 N, tetapi bila pH sampai mencapai 6,0 (melebihi 5,8)
maka ditambah HCl 1 N. Kemudian, ditambahkan aquades hingga volume
mencapai 2000 ml. Larutan dituangkan ke dalam 16 botol, masing-masing botol
berisi 100 ml dan sisanya disimpan dalam lemari pendingin. Setiap botol
ditambahkan zat pengatur tumbuh BAP dan NAA sesuai dengan kombinasi
perlakuan. Lalu ditambahkan agar-agar. Diaduk dengan menggunakan stirer
sampai mendidih dan agar-agarnya larut semua. Kemudian setiap media perlakuan
dituangkan ke dalam botol kultur sesuai dengan kombinasinya sehingga setiap
Media ini selanjutnya disterilkan dengan autoklaf pada suhu 121°C, tekanan 17,5
psi, selama 30 menit. Setelah itu, media diletakkan kedalam ruang kultur.
Pemotongan Eksplan
Eksplan yang digunakan adalah tunas aksilar dari planlet yang
disubkulturkan ke dua kalinya dalam media MS dengan menggunakan dua zat
pengatur tumbuh NAA dan BAP. Planlet dikeluarkan dari botol kultur dengan
menggunakan pinset setelah itu tunas-tunas aksilar dipisahkan dengan
menggunakan skalpel. Kemudian tunas-tunas yang memiliki ukuran 0,5 cm
dipotong akarnya dengan menggunakan gunting yang steril. Pemotongan
dilakukan di LAF.
Penanaman Eksplan
Penanaman eksplan dilakukan di LAF yang telah disterilkan dengan alkohol 96%. Eksplan yang telah dipotong kemudian diletakkan di petridis.
Diambil botol media lalu di dekatkan dengan api bunsen kemudian eksplan
ditanam ke dalam botol media sesuai dengan perlakuan, setiap botol media
terdapat 1 eksplan. Setelah itu botol media dikembalikan ke dalam ruang kultur.
Pemeliharaan
Botol-botol yang telah ditanami eksplan diletakkan pada rak-rak kultur di
dalam ruang kultur. Setiap hari disemprot dengan alkohol 96% agar bebas dari
organisme yang menyebabkan terjadi kontaminasi. Suhu ruangan kultur yang
Pengamatan Parameter
Persentase eksplan yang hidup (%)
Pengamatan dilakukan pada minggu ke-4 dan minggu ke-8 dengan rumus
sebagai berikut :
Persentase eksplan yang hidup = Jumlah eksplan yang hidup x 100% Jumlah eksplan seluruhnya
Persentase eksplan membentuk tunas (%)
Pengamatan eksplan membentuk tunas dilakukan pada minggu ke-4 dan
minggu ke-8 dengan rumus sebagai berikut :
Persentase eksplan membentuk tunas = Jumlah eksplan yang membentuk tunas x
Jumlah eksplan seluruhnya
Tinggi planlet (cm)
Diukur pada akhir penelitian dengan menggunakan kertas milimeter mulai
dari tempat munculnya batang (pangkal) sampai ujung daun tertinggi.
Jumlah akar (buah)
Dihitung pada akhir penelitian dengan menghitung jumlah akar yang
muncul.
Panjang akar (cm)
Di ukur pada akhir penelitian dengan menggunakan kertas milimeter mulai
dari tempat munculnya akar (pangkal) sampai ujung akar.
Jumlah daun
Dihitung pada akhir penelitian dengan menghitung jumlah daun yang
muncul.
HASIL DAN PEMBAHASAN
Hasil
Dari analisa data yang di lakukan diperoleh hasil bahwa pemberian NAA
berpengaruh nyata terhadap parameter panjang akar dan tinggi tanaman
sedangkan pemberian BAP berpengaruh nyata terhadap parameter panjang akar,
tinggi tanaman dan tidak berpengaruh nyata terhadap parameter jumlah akar dan
jumlah daun. Adapun interaksi antara NAA dan BAP berpengaruh nyata pada
parameter panjang akar dan jumlah akar namun tidak berpengaruh nyata pada
parameter tinggi tanaman dan jumlah daun.
Persentase Eksplan Yang Hidup (%)
Dari data pengamatan persentase eksplan yang hidup (Lampiran 4) rataan
persentase eksplan yang hidup dari perlakuan konsentrasi NAA dan BAP pada
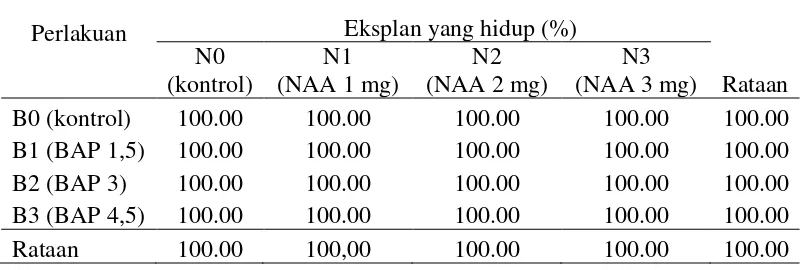
4 dan 8 minggu setelah inokulasi menunjukkan 100 % hidup (tabel 1). Persentase
eksplan yang hidup pada 8 minggu setelah inokulasi dapat dilihat pada Tabel 1.
Dari Tabel 1 di atas menunjukkan bahwa persentase eksplan yang hidup
untuk semua perlakuan konsentrasi NAA dan BAP sebesar 100%.
Persentase Eksplan Membentuk Tunas (%)
Dari pengamatan persentase eksplan membentuk tunas menunjukkan
bahwa semua perlakuan konsentrasi NAA, BAP dan interaksi antara kedua
perlakuan tidak terjadi pembentukan tunas.
Tinggi tanaman (cm)
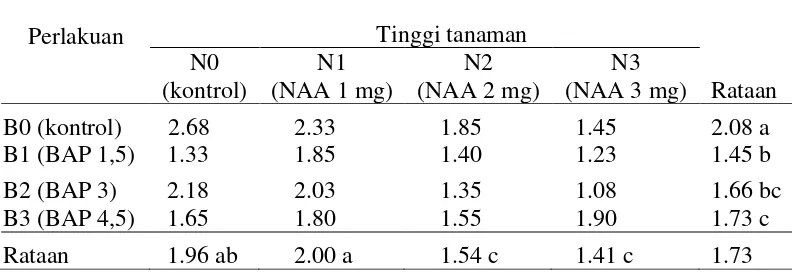
Hasil pengamatan tinggi tanaman pada akhir penelitian disajikan pada
Lampiran 6 dan sidik ragamnya disajikan pada Lampiran 8 yang menunjukan
bahwa pemberian perlakuan NAA berpengaruh nyata dan pemberian perlakuan
BAP berpengaruh nyata serta interaksi kedua perlakuan tidak berpengaruh nyata
pada parameter tinggi tanaman. menunjukkan pengaruh nyata pada uji BNJ pada taraf kepercayaan 5 %
Untuk perlakuan NAA, tinggi tanaman tertinggi terdapat pada perlakuan
berpengaruh nyata pada perlakuan yang lainnya dan paling rendah pada N3 yaitu
sebesar 1.41 cm. Tinggi tanaman tertinggi pada perlakuan BAP pada perlakuan
B0 yaitu sebesar 2.08 cm berbeda nyata dengan perlakuan yang lain dan paling
rendah pada perlakuan B1 yaitu sebesar 1.45 cm. Sedangkan kombinasi kedua
perlakuan, tinggi tanaman tertinggi pada perlakuan N0BO yaitu sebesar 2.68 cm
sedangkan paling rendah pada perlakuan N3B2 yaitu sebesar 1.08 cm. Pengaruh
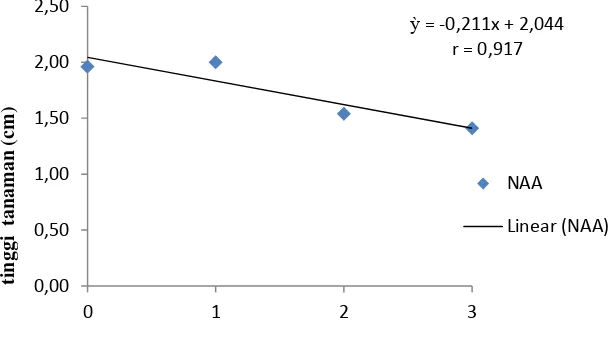
perlakuan NAA terhadap tinggi tanaman dapat dilihat pada Gambar 2.
Gambar 2. Hubungan konsentrasi NAA terhadap tinggi tanaman
Jumlah Akar (buah)
Hasil pengamatan jumlah akar pada akhir penelitian disajikan pada
Lampiran 9 dan sidik ragamnya disajikan pada lampiran 11 yang menunjukan
bahwa pemberian perlakuan NAA berpengaruh tidak nyata dan pemberian
perlakuan BAP tidak berpengaruh nyata namun interaksi kedua perlakuan
Tabel 3. Pengaruh konsentrasi NAA dan BAP terhadap jumlah akar (buah)
menunjukkan pengaruh nyata pada uji BNJ pada taraf kepercayaan 5 %
Untuk perlakuan NAA, jumlah akar tertinggi terdapat pada perlakuan N1
yaitu sebesar 5.44 cm dan paling rendah pada perlakuan N3 yaitu sebesar 2.56 cm.
Jumlah akar tertinggi pada perlakuan BAP pada perlakuan B0 yaitu sebesar 5.06
cm dan paling rendah pada perlakuan B3 yaitu sebesar 2.63 cm. Sedangkan
kombinasi kedua perlakuan, jumlah akar tertinggi pada perlakuan N1BO yaitu
sebesar 8.75 cm yang berbeda nyata dengan semua kombinasi sedangkan paling
rendah pada perlakuan N1B3 yaitu sebesar 1.00 cm.
Panjang Akar (cm)
Hasil pengamatan panjang akar pada akhir penelitian disajikan pada
Lampiran 12 dan sidik ragamnya disajikan pada lampiran 14 yang menunjukan
bahwa pemberian perlakuan NAA dan pemberian perlakuan BAP serta interaksi
kedua perlakuan berpengaruh nyata pada parameter panjang akar.
Rataan panjang akar pada pemberian konsentrasi NAA dan BAP dapat
Tabel 4. Pengaruh konsentrasi NAA dan BAP terhadap panjang akar (cm) menunjukkan pengaruh nyata pada uji BNJ pada taraf kepercayaan 5 %
Untuk perlakuan NAA, panjang akar tertinggi terdapat pada perlakuan N0
yaitu sebesar 1.61 cm dan paling rendah pada perlakuan N3 yaitu sebesar 0.39 cm.
Panjang akar tertinggi pada perlakuan BAP pada perlakuan B0 yaitu sebesar 2.15
cm dan paling rendah pada perlakuan B3 yaitu sebesar 0.56 cm Sedangkan
kombinasi kedua perlakuan, panjang akar tertinggi pada perlakuan N0BO yaitu
sebesar 4.25 cm yang berbeda nyata pada semua kombinasi sedangkan
paling rendah pada perlakuan N3B0 yaitu sebesar 0.30 cm berbeda nyata dengan
N0B0, N1B1 tetapi tidak berbeda nyata pada kombinasi yang lainnya. Pengaruh
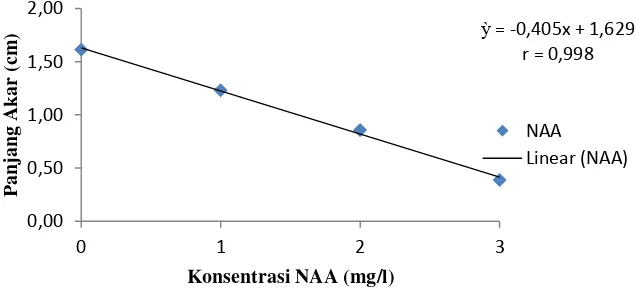
perlakuan NAA dan BAP terhadap panjang akar dapat dilihat pada gambar 3 dan
4.
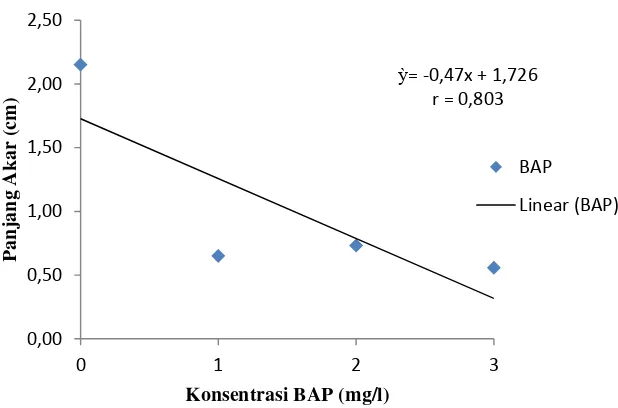
Gambar 4. Hubungan konsentrasi BAP terhadap panjang akar
Jumlah daun (helai)
Hasil pengamatan jumlah daun pada akhir penelitian disajikan pada
Lampiran 15 dan sidik ragamnya disajikan pada lampiran 17 yang menunjukan
bahwa pemberian perlakuan NAA dan pemberian perlakuan BAP serta interaksi
kedua perlakuan tidak berpengaruh nyata pada parameter jumlah daun.
Rataan jumlah daun pada pemberian konsentrasi NAA dan BAP dapat
dilihat pada Tabel 5.
Tabel 5. Pengaruh konsentrasi NAA dan BAP terhadap jumlah daun (helai)
Untuk perlakuan NAA, jumlah daun tertinggi terdapat pada perlakuan N0
yaitu sebesar 2.56 cm dan paling rendah pada perlakuan N2 dan N3 yaitu sebesar
2.00 cm. Jumlah daun tertinggi pada perlakuan BAP pada perlakuan B2 yaitu
sebesar 2.69 cm dan paling rendah pada perlakuan B1 yaitu sebesar 1.36 cm.
Sedangkan kombinasi kedua perlakuan, panjang akar tertinggi pada perlakuan
N0B2 yaitu sebesar 3.50 cm sedangkan paling rendah pada perlakuan N2B1 dan
N3B1 yaitu sebesar 1.25 cm.
Pembahasan
Pengaruh NAA terhadap perbanyakan tunas Boesenbergia flava
Dari hasil analisis data diketahui bahwa pemberian NAA berpengaruh
nyata untuk tinggi tanaman dan panjang akar. Tinggi tanaman tertinggi terdapat
pada perlakuan N1 (1 mg/l) yaitu sebesar 2.00 cm dan paling rendah pada
perlakuan N3 (3 mg/l) yaitu sebesar 1.41 cm dan panjang akar tertinggi terdapat
pada perlakuan N1 (NAA 1 mg/l) yaitu sebesar 1.61 cm dan paling rendah pada
perlakuan N3 yaitu sebesar 0.39 cm. Dari data dapat dilihat bahwa ada
kecenderungan semakin tinggi konsentrasi NAA yang diberikan maka tinggi
tanaman yang dihasilkan semakin rendah. Hal ini diduga karena proses
pemanjangan sel dan pembelahan sel pada eksplan terhambat. Zulkarnaen (2009)
menyatakan bahwa pada umumnya auksin meningkatkan pemanjangan sel,
pembelahan sel dan pembentukan akar adventif. Auksin berpengaruh pula untuk
menghambat pembentukan tunas adventif dan tunas aksilar, namun kehadirannya
dalam medium kultur dibutuhkan untuk meningkatkan embriogenesis somatik
Dari hasil analisis data diketahui bahwa pemberian NAA tidak
berpengaruh nyata terhadap jumlah akar dan jumlah daun. Hal ini diduga karena
kebutuhan auksin eksogen tidak diperlukan karena kebutuhan hormon sudah
tercukupi dari eksplan tersebut yang merupakan tunas yang sedang berkembang.
Tunas yang sedang berkembang itu dapat memproduksi auksin yang cukup untuk
memacu pertumbuhan. Hal ini sesuai dengan literatur Evans, dkk (1986) yang
dikutip oleh Dobardini, dkk (2006) yang menyatakan bahwa tunas yang sedang
berkembang dapat memproduksi auksin dalam jumlah yang cukup untuk perakaran
maka penambahan auksin eksogen tidak diperlukan. Jadi tanpa pemberian NAA pun,
eksplan dapat menginisiasi pertumbuhan akar.
Hasil pengamatan terhadap persentase eksplan membentuk tunas
menyatakan bahwa penambahan NAA dan BAP ke dalam media ternyata belum
dapat menyokong eksplan untuk membentuk tunas. Hal ini diduga karena
diperlukan waktu yang lebih lama lagi untuk proses pembentukan tunas.
Wiendi et all (1991) menyatakan bahwa pada beberapa tanaman membutuhkan
waktu yang lama untuk beregenerasi. Kemungkinan sitokinin endogen tidak
mencukupi untuk pembentukan tunas berarti selain auksin zat pengatur tumbuh
sitokinin juga perlu ditambahkan ke dalam media. Sesuai pendapat Gunawan
(1988) bahwa penambahan auksin dan sitokinin eksogen akan merubah level zat
pengatur tumbuh endogen sel. Pembentukan tunas secara in vitro baik melalui
multipikasi langsung dan tak langsung sangat tergantung pada jenis dan
konsentrasi yang tepat dari senyawa organik, inorganik dan zat pengatur tumbuh.
Eksplan yang ditanam tidak menghasilkan tunas, hanya dengan
sel, tetapi tidak terjadi perbanyakan atau multiplikasi tunas sehingga eksplan yang
ditanam hanya terlihat bertambah tinggi. Selain itu, pada perlakuan ini juga
terlihat adanya pembentukan akar. Hal ini mungkin disebabkan eksplan tunas
samping yang ditanam pada media kultur menghasilkan auksin endogen dengan
konsentrasi yang cukup tinggi sehingga pertumbuhan eksplan lebih diarahkan
pada pemanjangan sel dan pembentukan akar. Menurut Widyastuti (2004) bahwa
akar yang tumbuh pada media tanpa zat pengatur tumbuh kemungkinan diinduksi
oleh auksin endogen.Rahardja (1989) dan Cleland (1995) yang dikutip dari
Kurnianingsih (2009) menyebutkan bahwa dalam kultur jaringan auksin
merupakan zat pengatur tumbuh yang dapat menyebabkan terjadinya
pemanjangan sel pada jaringan tunas muda dan merangsang pembentukan akar.
Jika konsentrasi auksin dalam media kultur tinggi maka akan menghambat
pertumbuhan tunas.
Pengaruh BAP terhadap perbanyakan tunas Boesenbergia flava
Dari hasil analisis data diketahui bahwa pemberian BAP berpengaruh
nyata terhadap Panjang akar. Dapat dilihat pada tabel 4 panjang akar tertinggi
terdapat pada perlakuan B0 yaitu sebesar 2.15 cm dan paling rendah pada
perlakuan B3 yaitu sebesar 0.56 cm. Adanya penambahan sitokinin ke dalam
medium dapat menghambat pemanjangan dan perkembangan akar. Halperin
(1978) menyatakan bahwa adanya suplai sitokinin dalam media tanam
menyebabkan akar tidak berkambang. Disamping itu Yusnita (2003) juga
menyatakan bahwa, akar adventif belum muncul, tetapi jika tunas tersebut
dipindahkan ke media tanpa ZPT, akar akan tetap tumbuh. Sel-sel di bagian
telah mengalami perubahan yang stabil, yaitu terbentuk akar. Jika signal
lingkungan maupun harmonal tidak ada lagi, perkembangan akar tetap terjadi.
Pengaruh interaksi konsentrasi NAA dan BAP terhadap perbanyakan tunas Boesenbergia flava
Dari hasil analisis data diketahui bahwa interaksi NAA dan BAP tidak
berpengaruh nyata terhadap jumlah daun dan tinggi planlet. Hal ini diduga karena
interaksi konsentrasi NAA dan BAP yang diberikan belum mampu mencapai taraf
keseimbangan untuk pertumbuhan dan perkembangan tanaman. Wattimena, dkk
(1992) menyatakan bahwa di dalam kultur jaringan pertumbuhan dari eksplan
selalu tergantung dari interaksi antara auksin dan sitokinin.
Dari hasil analisis data diketahui bahwa interaksi NAA dan BAP
berpengaruh nyata terhadap parameter panjang akar dan jumlah akar. Kombinasi
kedua perlakuan, panjang akar tertinggi pada perlakuan N0BO yaitu sebesar 4.25
cm sedangkan paling rendah pada perlakuan N3B3 yaitu sebesar 0.30 cm. Hal ini
menunjukkan eksplan yang dikulturkan pada media tanpa penambahan BAP dan
NAA memperlihatkan pertumbuhan (pemanjangan) akar yang lebih baik
dibanding dengan kombinasi perlakuan yang lain. Hal ini membuktikan bahwa sel
akar umumnya mengandung cukup atau hampir cukup auksin untuk memanjang
secara normal. Hasil ini diperkuat oleh hasil penelitian Ammirato (1986) bahwa
beberapa sel tanaman dapat tumbuh dan berkembang dan selanjutnya beregenerasi
memjadi tanaman baru dalam media tanpa hormon tumbuh. Dengan demikian,
tanpa suplai auksin dan sitokinin secara eksogen, akar tanaman akan tetap tumbuh
KESIMPULAN
Kesimpulan
1. Perlakuan NAA berpengaruh nyata terhadap tinggi tanamn dengan hasil
yang terbaik pada konsentrasi 1 mg NAA.
2. Interaksi NAA dan BAP berpengaruh nyata terhadap jumlah akar dengan
hasil yang terbaik pada kombinasi N1B0
3. Interaksi antara NAA dan BAP belum menunjukan pengaruh yang nyata
pada jumlah daun.
4. Perlakuan BAP menunjukkan pengaruh yang nyata untuk panjang akar,
dengan hasil yang terbaik pada konsentrasi 0 mg/l (kontrol).
Saran
Perlu dilakukan penelitian lanjutan dengan konsentrasi zat pengatur
tumbuh yang lebih sesuai untuk mendapatkan hasil yang lebih baik dalam
DAFTAR PUSTAKA
Aisyah, S. dan Dedi S. 2011. Teknik Sterilisasi Rimpang Jahe Sebagai Bahan
Perbanyakan Tanaman Jahe Secara In Vitro. Buletin Teknik Pertanian Vol.
16. No 1. Halaman 34-36
Azriati Eva, Asmeliza, Nelfa Yurmita. 2005. Respon Regenerasi Eksplan Kalus Kedelai (Glycine max (L.) Merrill) Terhadap Pemberian NAA Secara in Vitro. Biologi FMIPA Universitas Negeri Padang, Padang.
Dwidjoseputro, D. 1981. Pengantar Fisiologi Tumbuhan. Penerbit PT Gramedia: Jakarta.
Evan, D. A.,W. R. Sharp, D. V. Ammirato. 1986. Handbook of Plant Cell Culture:
Techniques and Application Vol I. Macmitlan Publishing Company. New York.
Gunawan, L.W. 1995. Teknik Kultur Jaringan In Vitro dalam Hortikultura. Penebar Swadaya: Jakarta.
Hartmann, H.T., D.E. Kester, F.T. Davies and R.L. Geneve. 2002. Plant Propagation Principles and Practiese, 6th Ed. New Delhi: Prentice Hall of Insia Private Limited.
Hendaryono, D.P.S. dan A. Wijayani. 1994. Teknik Kultur Jaringan, Pengenalan dan Petunjuk Perbanyakan secara vegetatip. Jogjakarta: Kanisius.
Hughes, K. W., 1982. Ornamental Spesies in Cloning agricultur plant invitro technigues. Conger B.V.CRC Boca Raton, flodia.
Kristina. N. N, Rita N, Siti F. S dan Molide Rizal. 2002. Peluang Peningkatan Kadar Kurkumin Pada Tanaman Kunyit Dan Temulawak. Balai Penelitian Tanaman Obat dan Aromatik. Hlm 1-13.
Kurnianingsih. R, Marfuah, Ikhsan Matondang. 2009. Pengaruh Pemberian BAP (6-Benzyl Amino Purine) Pada Media Multiplikasi Tunas Anthurium hookerii Kunth. Enum. Secara In Vitro. Vis Vitalis, Vol. 02 No. 2.
Marlin. 2005. Regenerasi In Vitro Planlet Jahe Bebas Penyakit Layu Bakteri Pada Beberapa Taraf Konsentrasi 6-Benzil Amino Purine (BAP) Dan 1-Naphtalene Acetic Acid (NAA). Jurnal Ilmu-Ilmu Pertanian Indonesia. Volume 7, No 1. Hlm 8-14.
Pierik, R. I. M., 1987. In Vitro Culture of Higer Plans. Martinus Nijhoff Publishers Dordrecht, The Netherland.
Rini, P.E. 2009. Pasokan dan Permintaan Tanaman Obat Indonesia Serta Arah Penelitian dan Pengembangannya. Balai Penelitian Tanaman Obat dan Aromatik Indonesian Medicinal and Aromatic Crops Research Institute Jalan Tentara Pelajar No. 3, Bogor. Hlm 52-64
Salisbury, F.B. dan Ross, W.C., 1995. Fisiologi Tumbuhan Jilit Tiga. Penerjemah. Lukman, D. R. Dan Sumaryono. Penerbit ITB: Bandung.
Sastra. D. R., 2005. Multipikasi In Vitro Tanaman Jahe (Zingiber officinale Rosc var. amarun) Pada Berbagai Level Sukrosa Pusat Pengkajian dan Penerapan Teknologi Budidaya Pertanian, Badan Pengkajian dan Penerapan Teknologi Volume X No.1 Jurnal Agrotropika X(1): 9 –14.
Sirirugsa, P. 1992.A Revision Of The Genus Boesenbergia Kunt (Zingiberaceae) In Thailand. nat. Hist. bull. siam soc. 40: 67-90.
Steel, R.G.D dan J.H. Torrie. 1995. Prinsip dan Prosedur Statistik. Gramedia, Pustaka Utama, Jakarta.
Sutarto. I. Nana. S. Yuliasti., 2003. Penggunaan Media Alternatif Pada Kultur In Vitro Jahe (Zingiber officinale Rosc.) Varietas Gajah. Bul. Agron. (31) (1) 1-7.
Sobardini, D.,E. Suminar dan Mugayanti., 2006. Perbanyakan Cepat Tanaman Nilam (Pogostemon cablin Benth.) Secara Kultur Jaringan. Universitas Padjadjaran.
The Gardens' Bulletin Singapore 13: 113. 1950. (Gard. Bull. Singapore).
Wattimena, G.A., L.W. Gunawan, N.A. Mattjik, E. Syamsudin, N.M.A. Wiendi, A. Ernawati. 1992. Bioteknologi Tanaman. Laboratorium Kultur Jaringan Tanaman. Pusat Antar Universitas Bioteknologi IPB – Lembaga Sumberdaya Informasi IPB. Bogor.
Wiendi NMA, GA Wattimena, LW Gunawan. 1991. Bioteknologi Tanaman. Bogor: Pusat Antar Universitas (PAU) Bioteknologi. IPB.
Wilkins, M.B., 1992. Fisiologi Tanaman. Penerjemah Sutedjo M.M dan Kartasapoetra A.G. penerbit Bumi Aksara: Jakarta.
Yunira, T. Dini, R. Doppy, H. Asri, F. 2008. Zingiberaceae Primadona Baru Tanaman Hias. IPB. Bogor. 38 hlm.
Yusnita, 2003. Kultur Jaringan. Cara Memperbanyak Tanaman Secara Efisien. Agromedia Pustaka: Jakarta. 105 hlm.
Yuwono, T. 2008. Bioteknologi Pertanian. Gadjah Mada University Press: Yogyakarta. 277 hlm.
ZipcodeZoo.com. 2012. Boesenbergia flava. Diakses Pada Tanggal 12 Januari 2012.