Oleh :
! !
Skripsi
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Program Studi Kimia
Fakultas Sains dan Teknologi
DENGAN INI SAYA MENYATAKAN BAHWA SKRIPSI INI ADALAH HASIL KARYA SENDIRI YANG BELUM PERNAH DIAJUKAN SEBAGAI SKRIPSI ATAU KARYA ILMIAH PADA PERGURUAN TINGGI ATAU LEMBAGA MANAPUN
Jakarta, Agustus 2011
" Pemanfaatan Hasil Pirolisis Bulu Ayam Sebagai Adsorben Ion Na dan Fe Dalam Larutan Simulasi. Dibawah bimbingan #$ $% #&$' " $ dan ()* $+$ ' " $.
Karbon aktif pada umumnya dibuat dari kayu, batu bara, arang tempurung kelapa, bongkol jagung. Bahan alternatif yang dapat dijadikan karbon aktif adalah bulu ayam sebagai bentuk pemanfaatan limbah bulu ayam. Karbon aktif merupakan padatan amorf sebagaimana ditunjukkan hasil uji kristalin dengan XRD. Hasil rendemen karbon aktif sebesar 35%, kadar air yang didapat sebesar 0,51% dan kadar abu sebesar 4,8%. Luas permukaan karbon aktif dengan metode serapan metilen biru adalah 463,39 m2/g . Waktu kontak optimum karbon aktif dalam menyerap metilen biru adalah 30 menit. Hasil uji AAS menunjukkan besarnya adsorpsi ion Fe dengan metode kolom adalah 56,04% sementara itu ion Na tidak dapat diadsorp. Hasil uji adsorpsi ion Fe dengan metode adalah 93,59%. Pada metode pengaruh penambahan NaOH menyebabkan terjadinya endapan Fe(OH)3 dan penambahan HCl menyebabkan adsorpsi ion Fe yang berbeda@beda. Dalam penelitian ini metode adalah metode yang paling baik digunakan dalam adsorpsi ion Fe.
/
"Utilization Pirolyzed Result of Chicken Feathers for Adsorbent Na and Fe ions in the Solution Simulation. Guidanced by #$ $% #&$' " $ and ()* $+$ ' " $
Activated carbon is generally made from wood, coal, coconut shell charcoal, corn head. Alternative materials that can be used as activated carbon is chicken feathers as a form of utilization of chicken feathers waste. Activated carbon is an amorphous solid crystalline as shown by XRD test results. The results yield of activated carbon by 35%, water content obtained by 0.51% and ash content of 4.8%. The surface area of activated carbon with methylene blue adsorption method is 463.39 m2/g. The optimum contact time of activated carbon to adsorp the methylene blue is 30 minutes. AAS test results indicate the adsorption amount of Fe ions by column method is 56.04% while the Na ions can not be adsorp. Fe ion adsorption test results with method is 93.59%. In the batch method the effect of adding NaOH led to formation of precipitate Fe(OH)3 while the addition of HCl led to the adsorption of Fe ions are different. In this study the method method is best used in the adsorption of Fe ions.
Segala puji syukur penulis panjatkan kehadirat Allah SWT yang telah memberikan rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan skripsi yang berjudul Pemanfaatan Hasil Pirolisis Bulu Ayam sebagai Adsorben Ion Na dan Fe dalam Larutan Simulasi. Shalawat serta salam tidak lupa penulis limpahkan kepada Nabi Muhammad SAW, keluarga, dan para sahabatnya serta pengikutnya di akhir zaman.
Pada kesempatan ini penulis ingin mengucapkan terima kasih atas bantuan yang telah diberikan dari berbagai pihak, terutama kepada :
1. Bapak Adi Riyadhi, M.Si sebagai pembimbing I dan Ibu Yusraini DIS, M.Si sebagai Pembimbing II yang telah memberikan bimbingan serta arahan secara teknis sehingga penulis berhasil menyelesaikan skripsi ini.
2. Bapak Drs. Dede Sukandar, M.Si selaku Ketua Program Studi Kimia.
3. Bapak Dr. Syopiansyah Jaya Putra, M.Sis selaku Dekan Fakultas Sains dan Teknologi UIN Syarif Hidayatullah Jakarta.
4. Dosen@dosen Kimia yang telah banyak memberikan ilmunya.
5. Orang tua dan seluruh keluarga tercinta yang telah memberikan doa dan dukungannya baik moril maupun materiil.
6. Para wali murid yang telah membantu dana dari penelitian sampai penyelesaian skripsi ini.
7. Kiki, Udin, Ela dan Heru sebagai teman seperjuangan selama penelitian yang telah memberikan banyak bantuan, dorongan dan semangatnya.
8. Teman@Teman Kimia Angkatan 2007 yang telah membantu memberikan dorongan dan semangat.
Dengan diselesaikannya skripsi ini semoga dapat bermanfaat bagi penulis pada khususnya dan pembaca pada umumnya. Penulis meminta maaf atas segala kekurangan. Kritik dan saran selalu penulis harapkan demi sempurnanya penulisan skripsi ini.
Jakarta, Juni 2011
Hal
2.8 Spektrofotometer Serapan Atom (AAS) ... 28
3.1 Waktu dan Tempat ... 32
3.2 Bahan dan Alat ... 32
3.2.1 Bahan ... 32
3.2.2 Alat ... 32
3.3.1 Pembuatan Adsorben Karbon Aktif ... 33
3.3.2 Penentuan Kadar Air Karbon Aktif ... 33
3.3.3 Penentuan Kadar Abu Karbon Aktif ... 33
3.3.4 Analisa Kristalinitas Karbon Aktif dengan XRD ... 34
3.3.5 Penentuan Waktu Kontak Optimum ... 35
3.3.6 Penentuan Luas Permukaan ... 35
3.3.7 Proses Adsorpsi Ion Na dan Fe Menggunakan Karbon Aktif Dengan Metode Kolom ... 36
3.3.7.1 Pengaruh Massa Adsorben ... 36
3.3.7.2 Pengaruh Pengulangan ... 36
3.3.8 Proses Adsorpsi Ion Fe Menggunakan Karbon Aktif Dengan Metode ... 37
3.3.8.1 Pengaruh Massa Adsorben ... 37
3.3.8.1 Pengaruh pH ... 37
4.1 Pembuatan Adsorben Karbon Aktif... 39
4.2 Penentuan Kadar Air Karbon Aktif ... 40
4.3 Penentuan Kadar Abu Karbon Aktif... 41
4.4 Analisa Kristalinitas Karbon Aktif dengan XRD ... 42
4.5 Penentuan Waktu Kontak Optimum ... 44
4.6 Penentuan Luas Permukaan ... 46
4.7 Proses Adsorpsi Ion Na dan Fe Menggunakan Karbon Aktif dengan Metode Kolom ... 47
4.7.1 Adsorpsi Ion Na dengan Menggunakan Metode Kolom ... 47
4.7.2 Pengaruh Massa Karbon Aktif terhadap Penyerapan Ion Fe ... 51
4.7.3 Pengaruh Pengulangan terhadap Penyerapan Ion Fe ... 54
4.8 Proses Adsorpsi Ion Fe Menggunakan Karbon Aktif dengan Metode ... 55
4.8.1. Pengaruh Massa Adsorben ... 55
4.8.2. Pengaruh Penambahan HCl dan NaOH terhadap pH Larutan ... 56
4.9 Perbandingan Metode dengan Kolom terhadap Penyerapan Ion Fe ... 59
5.1 Kesimpulan ... 61
5.2 Saran ... 62
... 63
Hal
Gambar 1 : Struktur Keratin ... 8
Gambar 2 : Karbon Aktif ... 10
Gambar 3 : Skema Alat XRD ... 24
Gambar 4 : Cara Kerja Spektrofotometer UV@Visibel ... 28
Gambar 5 : Cara Kerja Spektrofotometer Serapan Atom ... 32
Gambar 6 : Kerangka Kerja Penelitian ... 38
Gambar 7 : Difraktogram Karbon Aktif yang Ditanur pada Suhu 400 oC ... 43
Gambar 8 : Difraktogram Karbon Aktif Sekam Padi yang Ditanur pada Suhu 700oC ... 44
Gambar 9 : Grafik Waktu Kontak Antara Larutan Metilen Biru dengan Karbon Aktif ... 45
Gambar 10 : Grafik Serapan Metilen Biru Sebelum dan Sesudah Ditambahkan Karbon Aktif ... 46
Gambar 11 : Grafik Pengaruh Massa Adsorben terhadap % Penyerapan Fe ... 52
Gambar 12 : Grafik Pengaruh Pengulangan terhadap Penyerapan Fe ... 54
Gambar 13 : Pengaruh Massa terhadap % Penyerapan Fe ... 56
Hal
Tabel 1 : Persyaratan Karbon Aktif ... 11
Tabel 2 : Manfat Karbon Aktif ... 13
Tabel 3 : Sifat Fisika Logam Natrium ... 20
Tabel 4 : Sifat Fisika Logam Besi ... 21
Hal
Lampiran 1 : Pembuatan Larutan Sampel ... 66
Lampiran 2 : Perhitungan Rendemen Karbon Aktif ... 67
Lampiran 3 : Perhitungan Kadar Air Karbon Aktif ... 68
Lampiran 4 : Perhitungan Kadar Abu Karbon Aktif ... 69
Lampiran 5 : Data hasil Analisis Karbon Aktif dengan XRD ... 70
Lampiran 6 : Tabel Penentuan Waktu Kontak... 71
Lampiran 7 : Tabel Penentuan Luas Permukaan ... 73
Lampiran 8 : Hasil Uji AAS untuk Adsorpsi Ion Na dan Fe ... 75
Lampiran 9 : Hasil Uji AAS untuk Adsorpsi Ion Fe ... 79
" , * 2 - +6
Pada proses pemotongan ayam dihasilkan hasil sampingan berupa bulu ayam yang biasanya dibuang begitu saja. Bulu ayam yang dibuang begitu saja lama kelamaan menumpuk dan dapat menimbulkan dampak pencemaran terhadap lingkungan. Dampak negatif yang ditimbulkan oleh industri peternakan ayam yaitu rumah potong ayam berupa terganggunya sanitasi lingkungan akibat limbah bulu ayam yang menimbulkan bau tidak sedap dan merupakan sumber penyebaran penyakit sebagai dampak penurunan kualitas udara. Selain itu limbah bulu ayam juga menimbulkan dampak penurunan kualitas tanah karena limbah bulu ayam sulit terdegradasi di lingkungan akibat adanya keratin atau berupa serat (Ketaren, 2008).
Limbah ini terus meningkat seiring dengan peningkatan populasi ayam dan kebutuhan masyarakat akan protein hewan. Jika limbah yang terus bertambah ini tidak dikelola dengan baik maka akan menimbulkan dampak pencemaran yang sangat besar terhadap lingkungan khususnya lingkungan rumah potong ayam. Berkaitan dengan hal tersebut, pemanfaatan limbah bulu ayam dengan cara pengolahan, yaitu dengan pengukusan dan penggilingan sebagai bahan pakan ayam potong, sehingga dengan termanfaatkannya limbah bulu ayam tersebut dapat diatasi limbah bulu ayam dan kekurangan bahan pakan ayam potong (Arifin, 2008). Pengolahan limbah bulu ayam untuk campuran pakan ternak dan limbah cair sebelum dibuang ke sungai dari industri potong ayam juga telah dilakukan sebelumnya (Sugita ., 2005). Pemanfaatan limbah bulu ayam sebagai adsorben ion logam berat dapat juga dijadikan alternatif untuk mengurangi pencemaran akibat menumpuknya bulu ayam.
Limbah yang mengandung logam berat perlu mendapat perhatian khusus, mengingat dalam konsentrasi tertentu dapat memberikan efek toksik (racun) yang berbahaya bagi kehidupan manusia dan ekosistem di sekitarnya. Banyak metode yang telah dikembangkan untuk menurukan kadar logam berat dari badan perairan, misalnya dengan teknik presipitasi, evaporasi, elektrokimia dan pemakaian resin (Ni’mah & Ulfin, 2007).
Karena meningkatnya kebutuhan akan air tawar, maka aliran air tanah tawar ke arah laut menurun, atau bahkan sebaliknya, air laut mengalir masuk ke dalam akuifer daratan. Kejadian ini dinamakan intrusi air laut. Pada air laut ion Cl@ dan Na+ lebih dominan, sedangkan pada air tanah ion yang dominan adalah CO32@ dan HCO3@. Karena adanya penyusupan air laut, maka komposisi air tanah akan berubah, yaitu ion Cl@ dan Na+ akan bertambah (Irham ., 2006). Kandungan Natrium yang tinggi dapat menyebabkan permeabilitas menjadi rendah. Selain itu air tanah dengan kandungan natrium dan klorida tinggi yang dijadikan air irigasi dapat menyebabkan tanaman terutama bagian daun seperti terbakar, menguning dan rontok (Ayers & Westcot, 1976). Berdasarkan Keputusan Menteri Kesehatan RI Nomor 907/MENKES/SK/VII/2002 tentang persyaratan kualitas air, kandungan natrium yang boleh dalam air minum adalah 200 ppm.
Dewasa ini telah banyak pula dikembangkan teknologi aplikasi adsorpsi, yakni menggunakan bahan biomaterial untuk menurunkan kadar logam berat dari badan air (biosorpsi), seperti penurunan kadar tembaga dengan biomassa bulu ayam (Ni’mah & Ulfin, 2007), limbah sekam padi menjadi karbon aktif sebagai adsorben (Sitohang & Dian, 2009), tempurung jarak pagar ( !" untuk adsorpsi tembaga (Wirawan, 2008), rumput laut untuk adsorpsi ion kromium (Sudiarta, 2009), adsorpsi zat warna tekstil pada limbah pabrik oleh eceng gondok (Rahmawati ., 2003), adsorpsi kadmium dengan tempurung kelapa (Gaikwad, 2004), adsorpsi natrium dengan metode pertukaran ion menggunakan eceng gondok (Kristianti, 2008), adsorpsi besi dengan karbon aktif dari bungkil jagung (Baskaran !# 2010), adsorpsi besi dari air dengan arang kayu dan pasir (Ahamad & Jawed, 2011).
pelindung pada hewan, seperti kulit rambut atau bulu. Sifat@sifat keratin yang dikaitkan dengan gugus asam amino dan hidroksil yang terikat, maka menyebabkan sifat polielektrolit kation sehingga dapat berperan sebagai penukar ion dan sebagai adsorben terhadap logam berat dalam air limbah (Lin ., 1992).
Bulu unggas, misalnya bulu ayam mengandung protein serat atau keratin yaitu: protein kasar (79,88%), lemak kasar (3,77%) dan serat kasar (0,32%) (Ketaren, 2008). Dengan demikian bulu ayam kemungkinan memiliki potensi sebagai adsorben baru yang dapat digunakan untuk mengatasi penurunan kualitas lingkungan akibat adanya ion – ion logam berat dalam limbah.
" *(3() + ) 2 &
1. Bagaimana proses pembuatan karbon aktif dari limbah bulu ayam? 2. Bagaimana terjadinya proses adsorpsi ion Na dan Fe oleh karbon aktif?
3. Bagaimana pengaruh massa adsorben terhadap kemampuan adsorpsi ion Na dan Fe oleh karbon aktif dengan metode kolom?
4. Bagaimana pengaruh variasi beberapa parameter (massa adsorben dan pH) terhadap kemampuan adsorpsi Fe oleh karbon aktif dengan Metode ?
" (5( + + 2$,$ +
1. Mengetahui proses pembuatan karbon aktif dari limbah bulu ayam.
2. Mengetahui proses adsorpsi yang terjadi pada ion Na dan Fe oleh karbon aktif.
3. Mengetahui pengaruh massa adsorben terhadap kemampuan adsorpsi ion Na dan Fe oleh karbon aktif dengan metode kolom?
4. Mengetahui kondisi optimum (massa adsorben dan pH) dari karbon aktif dalam menyerap ion Fe dengan Metode .
" +7 , + 2$,$ +
" (2( % 3 9 :
Jumlah ayam yang dipotong terus meningkat dari tahun ke tahun sehingga bulu ayam yang dihasilkan juga meningkat. Menurut Jendral Peternakan (1999), pada tahun 1999 dilaporkan bahwa populasi ayam terutama ayam pedaging di Indonesia mencapai 418.941.514 ekor dan diperkirakan jumlah bulu yang dihasilkan sejumlah 26.280 ton. Jumlah ayam yang dipotong setiap tahun semakin meningkat, dan hal ini akan menghasilkan jumlah bulu yang melimpah (Purwanti
!#2010). Hasil pemotongan ternak unggas ini dihasilkan rata@rata bobot bulu 4@9 % dari bobot hidup. Kandungan protein bulu ayam cukup tinggi, yaitu antara 80@90 %, sehingga berpotensi sebagai pakan altematif bagi industri ayam potong. Kendala utama penggunaan tepung bulu ayam sebagai pakan adalah adanya ikatan keratin dengan kandungan 85@90% dari kandungan proteinnya dengan sifat sukar larut dalam air dan sukar dicerna. Untuk memecahkan ikatan keratin tersebut guna meningkatkan kecernaan tepung bulu ayam dilakukan dengan beberapa teknik pengolahannya (Arifin, 2008).
Secara tradisional bulu ayam digunakan sebagai bahan kerajinan, peralatan rumah tangga dan bahkan bantal yang bernilai komersial rendah. Kebutuhannya tetap terbatas sementara volume limbah terus membengkak selaras dengan pertumbuhan industri peternakan nasional maupun global. Bantal dari bulu ayam sulit berkembang karena kalah mutu dari bantal bulu halus angsa. Sementara itu volume limbah bulu ayam global terus membengkak selaras dengan pertumbuhan pesat industri peternakan ayam dunia. Keadaan ini telah menggugah para ilmuwan mencari cara agar lebih banyak lagi bulu ayam yang bisa dijadikan produk komersial (Anoninm, 2008).
lebih kecil sehingga lebih banyak partikel@partikel mini, spora, debu, bahan@bahan $ yang terperangkap di saringan. Karakteristik tersebut membuka peluang kertas dari bulu ayam digunakan sebagai filter % (Barone & Schmidt, 2005).
" * ,$+ :
Keratin adalah suatu kelompok protein yang sangat khusus memproduksi sel epitel tertentu dari hewan bertulang belakang dan lapisan tanduk kulit luar serta epidermal tambahan seperti rambut, kuku dan bulu ayam. Sedangkan keratinase adalah spesifik protease hidrolisis keratin yang terdapat pada bulu ayam, wool dan rambut. Keratin serupa dengan komponen protein lainnya, secara umum dan tidak tampak jelas perbedaan substratnya. Keratin dapat didegradasi
oleh mikroba % (Lin ., 1992).
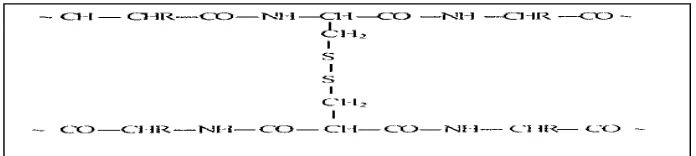
Keratin atau serat terdiri dari ikatan sistin disulfida, ikatan hidrogen, dan interaksi hidrofobik molekul protein (Lin ., 1992). Ikatan sistin disulfida atau ikatan silang terbentuk antara antara asam amino sistin yang mengandung gugus @SH. Jika dua unit sistin berikatan, maka terbentuklah sebuah jembatan disulfida @S@S@ melalui oksidasi@oksidasi gugus –SH. Protein serat terbentuk dari molekul yang rapat dan teratur berupa ikatan silang antara rantai@rantai asam amino yang berdekatan sehingga molekul air sukar menerobos struktur ini, oleh karena itu protein serat tidak larut di dalam air (hidrofobik). Logam berat dapat merusak ikatan disulfida karena aktivitasnya yang tinggi dan kemampuannya untuk menarik sulfur sehingga mengakibatkan denaturasi protein. Pembentukan ikatan silang sistin disulfida atau ikatan komplek peptida terjadi karena proses hidrolisis yang tidak sempurna, hal ini dapat diatasi dengan melakukan hidrolisis ulang melalui fermentasi (Ketaren, 2008). Selain itu ikatan keratin dapat diputuskan dengan bantuan@bantuan enzim proteolitik. Secara jelas komponen@komponen keratin dapat dilihat pada struktur kimia keratin berikut ini :
" *41+ -,$7 9 :
Arang merupakan suatu padatan berpori yang mengandung 85@95% karbon, dihasilkan dari bahan@bahan yang mengandung karbon dengan pemanasan pada suhu tinggi. Ketika pemanasan berlangsung, diusahakan agar tidak terjadi kebocoran udara didalam ruangan pemanasan sehingga bahan yang mengandung karbon tersebut hanya terkarbonisasi dan tidak teroksidasi. Arang selain digunakan sebagai bahan bakar, juga dapat digunakan sebagai adsorben (penyerap). Daya serap ditentukan oleh luas permukaan partikel dan kemampuan ini dapat menjadi lebih tinggi jika terhadap arang tersebut dilakukan aktivasi dengan aktifator bahan@bahan kimia ataupun dengan pemanasan pada temperatur tinggi. Dengan demikian, arang akan mengalami perubahan sifat@sifat fisika dan kimia. Arang yang demikian disebut sebagai arang aktif.
Arang aktif merupakan senyawa karbon amorf, yang dapat dihasilkan dari bahan@bahan yang mengandung karbon atau dari arang yang diperlakukan dengan cara khusus untuk mendapatkan permukaan yang lebih luas. Luas permukaan arang aktif berkisar antara 300@3500 m2/gram dan ini berhubungan dengan struktur pori internal yang menyebabkan arang aktif mempunyai sifat sebagai adsorben. Arang aktif dapat mengadsorpsi gas dan senyawa@senyawa kimia tertentu atau sifat adsorpsinya selektif, tergantung pada besar atau volume pori@pori dan luas permukaan. Daya serap arang aktif sangat besar, yaitu 25@1000% terhadap berat arang aktif (Sembiring & Sinaga, 2003).
Gambar 2 Karbon Aktif
Karbon aktif mengandung elemen@elemen yang terikat secara kimia, seperti oksigen dan hidrogen. Elemen@elemen ini dapat berasal dari bahan baku yang tertinggal akibat tidak sempurnanya proses karbonisasi, atau pula dapat terikat secara kimia pada proses aktivasi. Demikian pula adanya kandungan abu yang bukan bagian organik dari produk. Untuk tiap@tiap jenis karbon aktif kandungan abu dan komposisinya ada bermacam@macam. Adsorpsi elektrolit dan non elektrolit dari larutan dari karbon aktif, juga dipengaruhi oleh adanya sejumlah kecil abu. Adanya oksigen dan hidrogen mempunyai pengaruh besar pada sifat@sifat karbon aktif. Elemen@ elemen ini berkombinasi dengan atom@atom karbon membentuk gugus@gugus fungsional tertentu.
Pengujian mutu arang aktif sangat diperlukan untuk mengetahui kemampuan arang aktif agar dapat berfungsi sebagaimana mestinya. Pengujian mutu arang aktif meliputi: penentuan bagian yang hilang pada pemanasan 950 oC, penentuan kadar air, penentuan kadar abu dan daya serap terhadap larutan I2.
Menurut SNI, karbon aktif yang baik mempunyai persyaratan yang tercantum pada tabel berikut ini :
Tabel 1 Persyaratan Karbon Aktif (SNI 06@3730@95)
+$) *)% * , +
Bagian yang hilang pada pemanasan 950 oC Maksimum 15%
Kadar air Maksimum 15%
Kadar abu Maksimum 10%
Bagian yang tidak diperarang Tidak nyata
Daya serap terhadap larutan I2 Maksimum 20%
& Shawabkah, 2009). Jadi kecepatan adsorpsi yang menggunakan & (PAC) lebih besar dari pada $ (GAC). Luas permukaan total mempengaruhi kapasitas adsorpsi total sehingga meningkatkan efektivitas karbon aktif dalam menyisihkan senyawa organik dalam air buangan.
Struktur pori adalah faktor utama dalam proses adsorpsi. Distribusi ukuran pori menentukan distribusi molekul yang masuk dalam partikel karbon untuk diadsorp. Molekul yang berukuran besar dapat menutup jalan masuk ke dalam mikropori sehingga membuat area permukaan yang tersedia untuk mengadsorpsi menjadi sia@sia. Karena bentuk molekul yang tidak beraturan dan pergerakan molekul yang konstan, pada umumnya molekul yang lebih kecil menembus kapiler yang ukurannya lebih kecil juga.
Karbon aktif sering digunakan untuk mengurangi kontaminan organik dan partikel kimia organik, tetapi karbon aktif juga efektif untuk mengurangi kontaminan inorganik seperti radon@ 222, merkuri, dan logam beracun lainnya. Karbon aktif terdiri dari berbagai mineral yang dibedakan berdasarkan kemampuan adsorpsi (daya serap) dan karakteristiknya. Sumber bahan baku dan proses yang berbeda akan menghasilkan kualitas karbon aktif yang berbeda. Sumber bahan baku karbon aktif berasal dari kayu, batu bara, arang tempurung kelapa, dan bongkol jagung.
Karbon aktif dapat digunakan sebagai bahan pemucat, adsorpsi gas, adsorpsi logam, menghilangkan polutan mikro misalnya zat organik, detergen, bau, senyawa phenol dan lain sebagainya. Pada pori@pori arang aktif ini terjadi proses adsorpsi, yaitu proses penyerapan zat@zat yang akan dihilangkan oleh permukaan karbon aktif. Apabila seluruh permukaan karbon aktif sudah jenuh, atau sudah tidak mampu lagi menyerap maka kualitas air yang disaring sudah tidak baik lagi, sehingga karbon aktif harus diganti dengan karbon aktif yang baru.
Tabel 2 Manfaat Karbon Aktif (Sembiring & Sinaga, 2003)
1 -)(# , ( (5( + 3 - $ +
1 Industri obat dan makanan Menyaring dan menghilangkan warna, bau, rasa yang tidak enak pada makanan
2 Minumam ringan, minuman keras
Menghilangkan warna, bau pada arak/minumam keras dan minumam ringan
3 Kimia perminyakan Penyulingan bahan mentah, zat perantara 4 Pembersih air Menyaring atau menghilangkan bau, warna, zat
pencemar dalam air, sebagai pelindung dan penukaran resin dalam alat atau penyulingan air 5 Pembersih air buangan Mengatur dan membersihkan air buangan dan
pencemar, warna, bau, dan logam berat
8 Pemurnian gas Menghilangkan sulfur, gas beracun dan bau busuk asap 9 Katalisator Reaksi katalisator pengangkut vinil klorida, vinil asetat 10 Pengolahan pupuk Pemurnian, penghilangan bau
Sifat karbon aktif yang paling penting adalah daya serap. Dalam hal ini, ada beberapa faktor yang mempengaruhi daya serap dari karbon aktif, yaitu :
1. Sifat Adsorben
Karbon aktif yang merupakan adsorben adalah suatu padatan berpori, yang sebagian besar terdiri dari unsur karbon bebas dan masing@ masing berikatan secara kovalen. Dengan demikian, permukaan karbon aktif bersifat non polar. Selain komposisi dan polaritas, struktur pori juga merupakan faktor yang penting diperhatikan. Struktur pori berhubungan dengan luas permukaan, semakin kecil pori@ pori karbon aktif, mengakibatkan luas permukaan semakin besar. Dengan demikian kecepatan adsorpsi bertambah. Untuk meningkatkan kecepatan adsorpsi, dianjurkan agar menggunakan karbon aktif yang telah dihaluskan. Jumlah atau dosis karbon aktif yang digunakan, juga diperhatikan.
2. Sifat Adsorpsi
Banyak senyawa yang dapat diadsorpsi oleh karbon aktif, tetapi kemampuannya untuk mengadsorpsi berbeda untuk masing@ masing senyawa. Adsorpsi akan bertambah besar sesuai dengan bertambahnya ukuran molekul adsorpsi dari sturktur yang sama, seperti dalam deret homolog. Adsorpsi juga dipengaruhi oleh gugus fungsi,posisi gugus fungsi, ikatan rangkap, struktur rantai dari senyawa yang akan diadsorp.
Dalam pemakaian karbon aktif dianjurkan untuk menyelidiki temperatur pada saat berlangsungnya proses. Karena tidak ada peraturan umum yang biasanya diberikan mengenai temperatur yang digunakan dalam adsorpsi. Faktor yang mempengaruhi temperatur proses adsoprsi adalah viskositas dan stabilitas termal senyawa serapan. Jika pemanasan tidak mempengaruhi sifat@sifat senyawa yang akan diadsorp, seperti terjadi perubahan warna maupun dekomposisi, maka perlakuan dilakukan pada titik didihnya. Untuk senyawa volatil, adsorpsi dilakukan pada temperatur kamar atau bila memungkinkan pada temperatur yang lebih kecil. 4. Derajat Keasaman (pH)
Untuk asam@asam organik adsorpsi akan meningkat bila pH diturunkan, yaitu dengan penambahan asam@asam mineral. Hal ini disebabkan karena kemampuan asam mineral untuk mengurangi ionisasi asam organik tersebut. Sebaliknya bila pH asam organik dinaikkan yaitu dengan menambahkan alkali, adsorpsi akan berkurang sebagai akibat terbentuknya garam. 5. Waktu Kontak
Bila karbon aktif ditambahkan dalam suatu cairan, dibutuhkan waktu untuk mencapai kesetimbangan. Waktu yang dibutuhkan berbanding terbalik dengan jumlah yang digunakan. Waktu yang dibutuhkan ditentukan oleh dosis karbon aktif, pengadukan juga mempengaruhi waktu kontak. Pengadukan dimaksudkan untuk memberi kesempatan pada partikel karbon aktif untuk bersinggungan dengan senyawa yang akan diadsorp. Untuk larutan yang mempunyai viskositas tinggi, dibutuhkan waktu kontak yang lebih lama.
Struktur pori adalah faktor utama dalam proses adsorpsi. Distribusi ukuran pori menentukan distribusi molekul yang masuk dalam partikel karbon untuk diadsorp. Molekul yang berukuran besar dapat menutup jalan masuk ke dalam mikropori sehingga membuat area permukaan yang tersedia untuk mengadsorp menjadi sia@sia. Karena bentuk molekul yang tidak beraturan dan pergerakan molekul yang konstan, pada umumnya molekul yang lebih besar dapat menembus kapiler yang ukurannya lebih kecil juga.
" #)1*8)$
dan zat yang diserap sehingga tidak mungkin terjadi proses yang bolak@balik (Al@Qoddah & Shawabkah, 2009).
Adsorpsi adalah proses dimana substansi molekul meninggalkan larutan dan bergabung pada permukaan zat padat oleh ikatan fisika dan kimia. Substansi molekul atau bahan yang diserap disebut adsorbat, dan zat padat penyerapnya disebut adsorben. Proses adsorpsi biasanya dengan menggunakan karbon aktif yang digunakan untuk menyisihkan senyawa@senyawa aromatik dan senyawa organik terlarut (Al@Degs !# 2009).
Proses adsorpsi dapat digambarkan sebagai proses dimana molekul meninggalkan larutan dan menempel pada permukaan zat akibat ikatan kimia dan fisika. Adsorpsi dapat dikelompokkan menjadi dua yaitu adsorpsi fisika dan adsorpsi kimia .
Adsorpsi fisika yaitu berhubungan dengan gaya ' ( dan merupakan proses bolak@balik. Apabila gaya tarik menarik antara zat terlarut dengan adsorben lebih besar dari pada gaya tari menarik antara zat terlarut dengan pelarutnya maka zat terlarut akan diadsorpsi pada permukaaan adsorben. Ikatan tersebut sangat lemah, sehiggga mudah untuk diputuskan apabila konsentrasi zat terlarut yang teradsorpsi diubah. Jadi proses ini berlangsung bolak@balik.
Adsoprsi kimia yaitu reaksi yang terjadi antara zat padat dan zat terlarut yang teradsorpsi. Molekul@molekul yang teradsorpsi pada permukaan adsorben bereaksi secara kimia. Hal ini disebabkan pada adsorpsi kimia terjadi pemutusan dan pembentukan ikatan. Dalam proses adsorpsi kimia, ikatan antara zat terlarut yang teradsorpsi dan adsorben sangat kuat, sehingga sulit untuk dilepaskan dan proses hampir tidak mungkin untuk bolak@balik.
Proses adsorpsi dapat terjadi karena adanya gaya tarik atom atau molekul pada permukaan padatan yang tidak seimbang. Adanya gaya ini, padatan cenderung menarik molekul@ molekul lain yang bersentuhan dengan permukaan padatan, baik fasa gas atau fasa larutan ke dalam permukaannya. Akibatnya, konsentrasi molekul pada permukaan menjadi lebih besar daripada dalam fasa gas atau zat terlarut dalam larutan. Adsorpsi dapat terjadi pada antarfasa padat@cair, padat@gas, atau gas@cair (Haryani ., 2007).
Bahan yang digunakan untuk menyerap mempunyai kemampuan berbeda@beda, tergantung dari bahan asal dan juga metode aktivasi yang digunakan.
2. Ukuran butir
Semakin kecil ukuran butir, maka semakin besar permukaan sehingga dapat menyerap kontaminan makin banyak. Secara umum kecepatan adsorpsi ditujukan oleh kecepatan difusi zat terlarut ke dalam pori@pori partikel adsorben. Ukuran partikel yang baik untuk proses penyerapan antara @100 / +200 mesh.
3. Derajat Keasaman (pH Larutan)
Pada pH rendah, ion H+ akan berkompetisi dengan kontaminan yang akan diserap, sehingga efisiensi penyerapan turun. Proses penyerapan akan berjalan baik bila pH larutan tinggi. Derajat keasaman mempengaruhi adsorpsi karena pH menentukan tingkat ionisasi larutan, pH yang baik berkisar antara 8@9. Senyawa asam organik dapat diadsorpsi pada pH rendah dan sebaliknya basa organik dapat diadsorpsi pada pH tinggi.
4. Waktu serap
Waktu serap yang lama akan memungkinkan proses difusi dan penempelan molekul zat terlarut yang terserap berlangsung dengan baik.
5. Konsentrasi
Pada konsentrasi larutan rendah, jumlah bahan diserap sedikit, sedangkan pada konsentrasi tinggi jumlah bahan yang diserap semakin banyak. Hal ini disebabkan karena kemungkinan frekuensi tumbukan antara partikel semakin besar.
"; 16 3
litium sebagai logam dengan massa jenis paling kecil sampai osmium yaitu logam dengan massa jenis paling besar.
Dari semua golongan logam dapat dibedakan menjadi lima bagian yaitu :
(1). Logam berat adalah apabila berat jenisnya lebih besar dari 5 kg/dm3, terletak di sudut kanan bawah sistem periodik, mempunyai afinitas yang tinggi terhadap unsur S dan biasanya bernomor atom 22 sampai 92 dari perioda 4 sampai 7. Berdasarkan sifat kimia dan fisikanya, maka tingkat atau daya racun logam berat terhadap hewan air dapat diurutkan (dari tinggi ke rendah) sebagai berikut merkuri (Hg), kadmium (Cd), seng (Zn), timbal (Pb), krom (Cr), nikel (Ni), dan kobalt (Co) (Sutamihardja ., 1982). Menurut Darmono (1995) daftar urutan toksisitas logam paling tinggi ke paling rendah terhadap manusia yang mengkomsumsi ikan adalah sebagai berikut Hg2+ > Cd2+ > Ag2+ > Ni2+ > Pb2+ > As2+ > Cr2+ > Sn2+ > Zn2+. Sedangkan menurut Kementrian Negara Kependudukan dan Lingkungan Hidup (1990) sifat toksisitas logam berat dapat dikelompokan ke dalam 3 kelompok, yaitu : (a) Bersifat toksik tinggi yang terdiri dari atas unsur@unsur Hg, Cd, Pb, Cu, dan Zn, (b) Bersifat toksik sedang terdiri dari unsur@unsur Cr, Ni, dan Co, dan (c) Bersifat tosik rendah terdiri atas unsur Mn dan Fe.
(2). Logam ringan adalah apabila berat jenisnya lebih kecil dari 5 kg/dm3. Misalnya : aluminium, magnesium, natrium, titanium, dan lain@lain.
(3). Logam mulia adalah logam yang dalam keadaan tunggal sudah dapat dipakai sebagai bahan teknik, artinya dalam keadaan murni tanpa dicampur dengan bahan logam lain sudah dapat diproses menjadi barang jadi atau setengah jadi, dengan sifat@sifat yang baik sesuai dengan yang diinginkan. Pada umumnya bahan logam belum memiliki sifat@sifat yang baik apabila tidak dicampur dengan bahan lainnya dan tidak memenuhi syarat sebagai bahan teknik, kecuali logam mulia tersebut. Diantara logam mulia yang kita kenal adalah emas, perak dan platina.
(4). Logam refraktori yaitu logam tahan api. Misalnya : wolfram, molebdenum, dan titanium. (5). Logam radioaktif adalah bahan yang menunjukkan gejala radioaktif karena radionuklida. Radioaktif adalah radiasi elektromagnetik dan penyebaran partikel pada saat terjadi perubahan spontan suatu inti atom atau disebabkan pembelahan inti secara spontan. Diantara logam radioaktif yang kita kenal adalah uranium, radium dan plutonium.
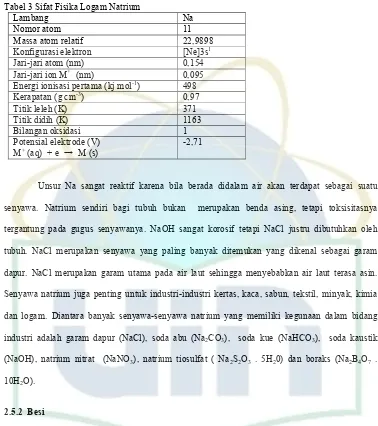
Natrium merupakan unsur terbanyak ke empat di bumi, terkandung sebanyak 2.6% di kerak bumi. Sifat fisika dari natrium besi terdapat dalam tabel 3 sebagai berikut:
Tabel 3 Sifat Fisika Logam Natrium
Lambang Na senyawa. Natrium sendiri bagi tubuh bukan merupakan benda asing, tetapi toksisitasnya tergantung pada gugus senyawanya. NaOH sangat korosif tetapi NaCl justru dibutuhkan oleh tubuh. NaCl merupakan senyawa yang paling banyak ditemukan yang dikenal sebagai garam dapur. NaCl merupakan garam utama pada air laut sehingga menyebabkan air laut terasa asin. Senyawa natrium juga penting untuk industri@industri kertas, kaca, sabun, tekstil, minyak, kimia dan logam. Diantara banyak senyawa@senyawa natrium yang memiliki kegunaan dalam bidang industri adalah garam dapur (NaCl), soda abu (Na2CO3), soda kue (NaHCO3), soda kaustik (NaOH), natrium nitrat (NaNO3), natrium tiosulfat ( Na2S2O3 . 5H20) dan boraks (Na2B4O7 . 10H2O).
";" )$
Tabel 4 Sifat Fisika Logam Besi
Lambang Fe
Nomor atom 26
Massa atom relatif 55,847
Konfigurasi elektron [Ar]3d64s2
Jari@jari atom (nm) 0,116
Jari@jari ion M3+ (nm) 0,064
Energi ionisasi pertama (kj mol@1) 768
Kerapatan (g cm@1) 7,87
Di alam, besi berikatan dengan mineral lain yaitu oksigen dan sulfur. Sumber utama besi adalah hematit (Fe2O3) terdiri dari 69,94% Fe dan 30,06% O2, magnetit (Fe3O4) terdiri dari 72,4% Fe dan 27,6% O2, limonit (FeO(OH) terdiri dari 62,9% Fe, 27% O2 dan H2O 10,01% , ilmenit(FeTiO3) terdiri dari 36,8% Fe, 31,6% O2 dan 31,6% Ti, dan Siderit (FeCO3) terdiri dari 48,2% Fe dan 51,8% CO2 .
Besi merupakan logam berat yang secara alamiah berada di lingkungan akibat adanya pelapukan dari batuan. Pada umumnya besi yang terdapat dalam air dapat bersifat terlarut sebagai Fe (II) (ferro) atau Fe (III) (ferri) yang tersuspensi sebagai butir koloidal (diameter < 1 Rm) atau lebih besar seperti Fe2O3 , FeO, Fe(OH)3 yang tergabung dengan zat organik atau zat padat organik seperti tanah liat. Pada air permukaan jarang ditemui kadar besi lebih dari 1 mg/L, tetapi di dalam air kadar Fe dapat jauh lebih tinggi. Besi di dalam air dengan kadar tinggi dapat dirasakan dan dapat menodai kain atau perkakas rumah tangga. Besi di dalam air juga dapat menyebabkan air berwarna agak kuning, baunya amis, menimbulkan karat besi pada sisi pipa atau bak, serta menimbulkan bakteri yang tahan terhadap adanya kandungan besi dalam air (Hasanah, 2006). Menurut Standar Nasional Indonesia (SNI) untuk syarat air minum kandungan besi hanya berkisar antara 0,3 – 1 ppm.
oksigen udara dari paru@paru ke jaringan tubuh. Walaupun besi sangat diperlukan dalam tubuh tetapi penumpukan dalam jumlah yang berlebihan berakibat tidak baik bagi kesehatan.
"! < 9 :
Difraksi sinar@X ( /XRD) merupakan salah satu metode karakterisasi material yang sudah ada sejak lama dan masih digunakan hingga sekarang. Teknik ini digunakan untuk mengidentifikasi fasa kristalin dalam material dengan cara menentukan parameter struktur kisi serta untuk mendapatkan ukuran partikel .
Sinar X adalah gelombang elektromagnetik yang dihasilkan dari penembakan logam dengan elektron berenergi tingggi. Elektron itu mengalami perlambatan saat masuk ke dalam logam dan menyebabkan elektron pada kulit logam tersebut terpental membentuk kekosongan. Elektron dengan energi tinggi yang lebih tinggi masuk ke tempat kosong dengan memancarkan kelebihan energinya sebagai foton sinar@ X. Adapun radiasi elektromagnetik sinar@X berada pada panjang gelombang 0,5@2,5 Ao dan energi +107 eV. Dasar metode ini adalah adanya kekhasan jarak antar bidang kristal (d) pada setiap kristal yang berbeda .
Spektroskopi XRD digunakan untuk mengidentifikasi fasa kristalin dalam material dengan cara menentukan parameter struktur kisi serta untuk mendapatkan ukuran partikel. Dasar dari penggunaan XRD untuk mempelajari kisi kristal adalah berdasarkan persamaan Bragg :
dengan :
λ = panjang gelombang sinar@X yang digunakan d = jarak antara dua bidang kisi
θ = sudut antara sinar datang dengan bidang normal n = bilangan bulat yang disebut sebagai orde pembiasan
Metode analisis dengan XRD pada umumnya menggunakan susunan alat yang terdiri atas :
a. Tabung sinar@X, merupakan bagian instrumen XRD yang berupa filamen tungsten (W) sebagai sumber elektron dan anoda berupa ion logam target.
b. Goniometer, merupakan bagian instrumen XRD yang masih satu unit dengan tempat sampel dan detektor dimana goniometer akan bergerak memutar selama alat beroperasi.
c. Tempat sampel, berupa lempeng ion logam/plat kaca cekung dengan lubang ditengah untuk mengisikan sampel serbuk. Dalam operasi alat, sampel akan berputar bersama goniometer dan membentuk sudut terhadap sinar@X yang datang.
d. Detektor, berisi gas yang sensitif terhadap sinar@X, katoda dan anoda. Sinar@X yang terdifraksi oleh sampel akan mengenai atom@atom gas sehingga atom@atom gas tersebut akan terionisasi dan membentuk elektron dan kation, selanjutnya elektron tersebut akan menuju katoda dan kation akan menuju anoda akibatnya dihasilkan suatu arus listrik.
e. Difraktometer, merupakan bagian alat yang terdiri atas dan . Arus listrik yang dihasilkan dari proses sebelumnya akan diubah menjadi pulsa yang dapat dihitung oleh dan . bertugas mendeteksi sudut difraksi, sedangkan bertugas mendeteksi intensitas.
f. Rekorder, merupakan bagian instrumen difraksi sinar@X yang digunakan untuk menampilkan keluaran berupa pola difraksi yang bentuknya tertentu.
Gambar 3 berikut ini menunjukkan cara kerja dari XRD :
Gambar 3 Skema alat XRD
tersebut . Sinar@X yang dibiaskan oleh cuplikan dipusatkan pada celah penerima dan jatuh pada detektor yang sekaligus mengubahnya menjadi bentuk cahaya tampak (foton), kemudian diterjemahkan sebagai sebuah puncak difraksi. Makin banyak bidang kristal yang terdapat dalam sampel, makin kuat intensitas pembiasan yang dihasilkannya. Tiap puncak yang muncul pada pola XRD mewakili satu bidang kristal yang memiliki orientasi tertentu dalam sumbu tiga dimensi dan grafik puncak difraksi yang didapat kemudian dianalisis, terdiri atas mineral liat apa saja dan komposisi utamanya. Puncak@puncak yang didapatkan dari data pengukuran ini kemudian dicocokkan dengan standar XRD untuk hampir semua jenis material. Keuntungan utama penggunaan sinar@X dalam karakterisasi material adalah kemampuan penetrasinya, sebab sinar@X memiliki energi sangat tinggi akibat panjang gelombangnya yang pendek .
Beberapa informasi yang dapat diperoleh dari XRD adalah sebagai berikut:
a. Posisi puncak difraksi memberikan gambaran tentang parameter kisi, jarak antar bidang, struktur kristal dan orientasi dari sel satuan.
b. Intensitas relatif puncak difraksi memberikan gambaran tentang posisi atom dalam sel satuan. c. Bentuk puncak difraksi memberikan gambaran tentang ukuran kristalit dan
ketidaksempurnaan kisi. " 8 -,*171,13 , * = $)$4 2
Spektrofotometer UV@visibel (sinar tampak) adalah analisa kuantitatif dan kualitatif spesies kimia dengan pengukuran absorbansi atau transmittansi dalam spektroskopi . Spektrofotometer UV@Visibel menggunakan cahaya tampak dalam rentang ultraviolet (UV) dan infrared (IR). Sifat optik Spektrofotometer UV@Visibel digunakan untuk mengetahui tingkat absorpsi dan dispersi bahan. Spektrofotometer UV@Visibel mempunyai rentang panjang gelombang 10@6 – 10@7 nm dengan peristiwa absorpsi yang mengakibatkan adanya transisi elektron. Spektrum absorpsi dari UV@Visibel berkisar antara 200 nm sampai 800 nm dan dinyatakan dalam spektrum elektron. Spektrum ultraviolet (UV) berada pada daerah ultraviolet pada panjang gelombang 200 – 400 nm sedangkan spektrum visibel berada pada daerah sinar tampak pada panjang gelombang 400 – 800 nm. Terdapat dua jenis Spektrofotometer UV@Visibel yaitu $
Spektrofotometer UV@Visibel terdiri atas : 1. Sumber Radiasi (Cahaya)
Sumber cahaya yang digunakan adalah sebuah lampu pijar dengan kawat rambut terbuat dari wolfram. Wolfram dapat merupakan sumber cahaya yang dapat menyediakan seluruh spektrum tampak dan ultra@ungu dekat sehingga didapat spektrum pada daerah 200 nm – 800 nm.
2. Monokromator
Monokromator adalah suatu alat optik yang digunakan untuk memunculkan suatu berkas radiasi dari suatu sumber secara berkesinambungan, dimana berkas yang ditampilkan mempunyai spektral yang tinggi dengan panjang gelombang yang akan diteliti. Komponen dari monokromator yang utama adalah suatu sistem celah dan suatu unsur dispersif. Radiasi dari sumber difokuskan masuk ke celah, kemudian disejajarkan oleh sebuah lensa atau cermin sehingga suatu berkas sejajar jatuh ke unsur pendispersi, yang berupa prisma atau suatu kisi difraksi. Dengan memutar suatu prisma atau kisi tersebut secara mekanis, macam@macam tampilan spektrum yang dihasilkan oleh unsur pendispersi dipusatkan pada celah keluar kemudian diteruskan ke sampel.
3. Tempat Sampel (Kuvet)
Kuvet adalah wadah gelas yang terbuat dari kaca atau silika yang dibuat sedemikian rupa dengan jarak yang dilalui berkas sinar adalah 1 cm. Sel sampel berisi larutan yang akan diuji yang biasanya berupa larutan yang sangat encer.
4. Detektor dan Komputer
Detektor mengubah sinar yang masuk menjadi arus listrik. Arus lebih tinggi jika sinarnya lebih tinggi. Untuk tiap panjang gelombang sinar yang melewati spektrofotometer, intensitas yang melewati sel sampel dihitung. Biasanya disimbolkan I0 untuk intensitas yang masuk dan I untuk intensitas yang keluar. Jika I lebih kecil dari I0, berarti sampel menyerap sejumlah sinar. Kemudian suatu persamaan matematika sederhana dikerjakan oleh komputer untuk mengubahnya menjadi apa yang dinamakan absorbansi yang disimbolkan A. Persamaan matematika tersebut yaitu :
dengan :
A = Absorbansi
I0 = intensitas yang masuk
I = intensitas yang keluar
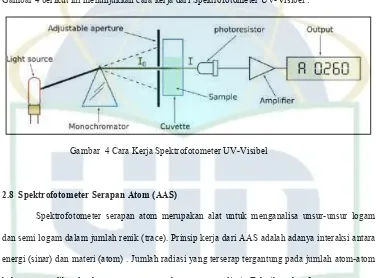
Secara umum cara kerja Spektrofotometer UV@Visibel adalah sinar dari sumber radiasi diteruskan menuju monokromator. Cahaya dari monokromator diarahkan terpisah melalui blangko dan sampel dengan sebuah cermin berotasi. Kedua cahaya lalu bergantian berubah arah karena pemantulan dari cermin yang berotasi secara kontinyu. Detektor menerima cahaya dari blangko dan sampel secara bergantian secara berulang – ulang. Sinyal listrik dari detektor diproses, diubah ke digital dan dibandingkan antara sampel dan blangko. Perhitungan dilakukan dengan komputer yang sudah terprogram.
Gambar 4 berikut ini menunjukkan cara kerja dari Spektrofotometer UV@Visibel :
Gambar 4 Cara Kerja Spektrofotometer UV@Visibel
"> 8 -,*171,13 , * * 8 + ,13 9 :
AAS adalah suatu alat yang digunakan pada metode analisis untuk penentuan unsur@unsur logam dan metalloid yang pengukurannya berdasarkan penyerapan cahaya dengan panjang gelombang tertentu oleh atom logam dalam keadaan bebas. Metode ini sangat tepat untuk analisis zat pada konsentrasi rendah. Memang selain dengan metode serapan atom, unsur@unsur dengan energi eksitasi rendah dapat juga dianalisis dengan fotometri nyala, akan tetapi fotometri nyala tidak cocok untuk unsur@unsur dengan energi eksitasi tinggi. Fotometri nyala memiliki range ukur optimum pada panjang gelombang 400@800 nm, sedangkan AAS memiliki range ukur optimum pada panjang gelombang 200@300 nm.
Untuk analisis kualitatif, metode fotometri nyala lebih disukai dari AAS, karena AAS memerlukan lampu katoda spesifik ( & ). Kemonokromatisan dalam AAS merupakan syarat utama. Suatu perubahan temperatur nyala akan mengganggu proses eksitasi sehingga analisis dari fotometri nyala berfilter terganggu juga. Dapat dikatakan bahwa metode fotometri nyala dan AAS merupakan komplementer satu sama lainnya. Metode AAS berprinsip pada absorbsi cahaya oleh atom, atom@atom menyerap cahaya tersebut pada panjang gelombang tertentu, tergantung pada sifat unsurnya. Unsur Natrium menyerap cahaya pada panjang gelombang 589 nm dan Fe menyerap pada panjang gelombang 248 nm.
Spektrofotometer serapan atom terdiri atas : 1. Sumber Radiasi
Suatu sumber radiasi yang digunakan harus memancarkan spektrum atom dari unsur yang ditentukan. Spektrum atom yang dipancarkan harus terdiri dari garis tajam yang mempunyai setengah lebar yang sama dengan garis serapan yang dibutuhkan oleh atom@atom dalam contoh. Sumber radiasi yang lazim dipakai adalah lampu katoda berongga ( & % ). Untuk penetapan apa saja yang diminta, lampu katoda berongga yang digunakan mempunyai sebuah katoda pemancar yang terbuat dari unsur yang sama yang akan dipelajari dalam nyala ini.
2. Nyala
2000 oK. Konsentrasi atom@atom dalam bentuk gas dalam nyala, baik dalam keadaan dasar maupun keadaan tereksitasi, dipengaruhi oleh komposisi nyala.
Komposisi nyala asitilen@udara sangat baik digunakan untuk lebih dari tiga puluh unsur sedangkan komposisi nyala propana@udara disukai untuk logam yang mudah diubah menjadi uap atomik. Untuk logam seperti aluminium (Al) dan titanium (Ti) yang membentuk oksida refraktori temperatur tinggi dari nyala asitilen@NO sangat perlu, dan sensitiitas dijumpai bila nyala kaya akan asitilen.
3. Sistem Pembakar@Pengabut (Nebulizer)
Tujuan sistem pembakar@pengabut adalah untuk mengubah larutan uji menjadi atom@atom dalam bentuk gas. Fungsi pengabut adalah menghasilkan kabut atau aerosol larutan uji. Larutan yang akan dikabutkan ditarik ke dalam pipa kapiler oleh aksi semprotan udara yang ditiupkan melalui ujung kapiler, diperlukan aliran gas bertekanan tinggi untuk menghasilkan aerosol yang halus.
4. Monokromator
Dalam spektrofotometer serapan atom fungsi dari monokromator adalah untuk memisahkan garis resonansi dari semua garis yang tidak diserap yang dipancarkan oleh sumber radiasi. Dalam kebanyakan instrumen komersial digunakan kisi difraksi karena sebaran yang dilakukan oleh kisi seragam daripada yang dilakukan oleh prisma dan akibatnya instrumen kisi dapat memelihara daya pisah yang lebih tinggi sepanjang jangka panjang gelombang yang lebih besar.
5. Detektor
Detektor pada spektrofotometer serapan atom berfungsi mengubah intensitas radiasi yang datang menjadi arus listrik. Pada spektrofotometer serapan atom yang umum dipakai sebagai detektor adalah tabung penggandaan foton (PMT = ) * ".
6. Sistem Pembacaan
Hasil dari sistem pembacaan dapat berupa angka atau berupa kurva dari suatu rekorder yang menggambarkan absorbansi atau intensitas emisi.
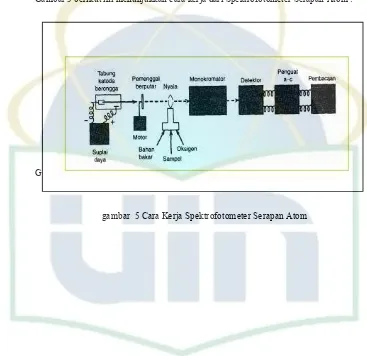
di dalam atomizer dengan nyala api yang dihasilkan dari pembakaran bahan bakar dengan oksigen. Monokromator akan mengisolasi salah satu garis resonansi yang sesuai dengan sampel dari beberapa garis resonansi yang berasal dari sumber sinar. Energi sinar dari monokromator akan diubah menjadi energi listrik dalam detektor. Energi listrik dari detektor inilah yang akan menggerakkan jarum dan mengeluarkan grafik. Sistem pembacaan akan menampilkan data yang dapat dibaca dari grafik.
Gambar 5 berikut ini menunjukkan cara kerja dari Spektrofotometer Serapan Atom :
G
" ? -,( # + 38 ,
Penelitian ini dilakukan di laboratorium Kimia, Pusat Laboratorium Terpadu Universitas Islam Negeri Syarif Hidayatullah mulai bulan Maret @ Mei 2011.
" & + # + 2 , " " & +
Bahan yang digunakan dalam penelitian ini antara lain limbah bulu ayam pedaging ( ), larutan metilen biru (C16H18ClN3S.3H2O) , akuades, NaOH 1 M, HCl 1 M, larutan standar Fe 100 ppm (dari padatan (NH4)2Fe(SO4)2.6H2O), larutan standar Na 100 ppm dari padatan NaCl.
" " 2 ,
Alat yang digunakan dalam penelitian ini adalah neraca analitik, seperangkat alat@alat gelas, cawan porselen dan tutupnya, spatula, tanur, desikator, magnetik, magnetik , lumpang, kertas saring ( % no. 1, pengayak (ukuran 50 mesh), spektrofotometer UV@Vis
$ %, (XRD), spektrofotometer serapan atom (AAS).
" / * *5
" " 34( , + #)1*4 + *41+ -,$7
" " + +,( + # * $* *41+ -,$7
Sebanyak 1 gram karbon aktif ditempatkan dalam cawan porselin yang telah diketahui bobot keringnya. Cawan yang berisi sampel dikeringkan dalam oven pada suhu 105 oC selama 3 jam sampai bobotnya konstan dan didinginkan di dalam desikator sekitar 15 menit lalu ditimbang. Pengeringan dan penimbangan diulangi setiap 1 jam sampai diperoleh bobot konstan. Perhitungan kadar air menggunakan persamaan :
dengan :
a = bobot sampel sebelum pemanasan (g) b = bobot sampel setelah pemanasan (g)
" " + +,( + # * 4( *41+ -,$7
Sebanyak 1 gram karbon aktif ditempatkan dalam cawan porselin yang telah dikeringkan dalam oven dan diketahui bobot keringnya. Cawan yang berisi sampel dipanaskan dalam tanur pada suhu 750 oC selama 6 jam. Setelah itu didinginkan di dalam desikator sekitar 30 menit lalu ditimbang. Pemanasan dan penimbangan diulangi setiap 1 jam sampai diperoleh bobot konstan. Perhitungan kadar abu menggunakan persamaan :
dengan :
a = bobot awal sampel (g) b = bobot sisa sampel (g)
" " + 2$) *$), 2$+$, ) *41+ -,$7 # +6 + <
Penentuan kristalinitas karbon aktif dengan pemanasan 400 oC dilakukan dengan menggunakan instrumen difraksi sinar@X (XRD). Karakterisasi ini dilakukan dengan cara sebagai berikut : sampel diletakkan dalam sampel holder, kemudian disinari dengan sinar@X. Jarak antara bidang@bidang mineral dalam sampel ditetapkan dari difraktogram masing@masing sampel berdasarkan hukum Bragg :
Kadar Abu (%) = x 100%
Kadar Air (%) =
x 100%
dengan :
λ = panjang gelombang sinar@X yang digunakan d = jarak antara dua bidang kisi
θ = sudut antara sinar datang dengan bidang normal n = bilangan bulat yang disebut sebagai orde pembiasan
Metode pengukuran sudut 2θ dari difraktogram sinar@X berdasarkan pada pengukuran sudut yang telah direkam pada setiap difraktogram, dan dihitung secara proposional setelah sudut 2θ diketahui.
" "; + +,( + ? -,( 1+, - 8,$3(3
Untuk menentukan waktu kontak optimum maka adsorben (0,1 gram) ditambahkan ke dalam larutan metilen biru 10 ppm (20 mL) diaduk dengan stirrer dengan waktu kontak yang divariasi 5, 10, 15, 20, 25, 30, 35, dan 40 menit. Larutan hasil pengadukan disaring dan filtrat yang di peroleh diukur absorbansinya dengan UV@Vis pada panjang gelombang 665 nm untuk mendapatkan persentase penyerapan maksimum dengan membandingkan absorbansi sebelum ditambahkan adsorben (Ni’mah & Ulfin, 2007).
" "! + +,( + ( ) *3(- +
Luas permukaan adsorben ditentukan menggunakan uji serapan metilen biru (MB), (Santamarina ., 2002). 0,1 gram adsorben ditambahkan pada 20 mL larutan MB 2 ppm dan suspensi diaduk dengan stirrer sesuai waktu kontak optimum. Larutan dibiarkan selama 24 jam untuk mencapai kesetimbangan. Larutan disaring kemudian dianalisis dengan spektrofotometer UV@visibel pada panjang gelombang 665 nm untuk menentukan jumlah MB diserap. Percobaan diulang dengan penambahan adsorben pada larutan MB dengan konsentrasi yang lebih tinggi (4@ 10 ppm) dilakukan secara berurutan dan dengan langkah@langkah seperti sebelumnya. Grafik dari konsentrasi MB yang ditambahkan dengan jumlah MB diserap digunakan untuk mengidentifikasi titik optimum dimana terjadi penyerapan secara maksimum.
Luas permukaan spesifik dihitung dari jumlah MB diserap pada titik optimum sebagai berikut (Santamarina ., 2002) :
dengan :
mMB = jumlah MB yang diserap pada titik penyerapan maksimum ms = massa adsorben (gram) diatasnya ditambahkan karbon aktif dengan variasi massa 3, 6, 9, 12 dan 15 gram. Larutan Na 100 ppm sebanyak 50 ml dialirkan pada kolom dengan laju alir 3 ml/menit. Efluen ditampung pada gelas beker 50 mL dan dianalisis dengan menggunakan spektrofotometer serapan atom untuk mengetahui seberapa besar penyerapannya. Perlakuan yang sama dilakukan untuk larutan Fe 100 ppm. Persentase logam yang teradsorpsi dihitung dengan rumus sebagai berikut :
dengan :
C0 = konsentrasi awal logam (ppm)
C = konsentrasi logam setelah diadsorpsi (ppm) " " " +6 *(& +6(2 +6 +
Kolom yang telah dipakai sebelumnya digunakan kembali untuk mengetahui pengaruh penyerapan larutan Na 100 ppm sebanyak 50 ml dengan laju alir 3 ml/menit. Perlakuan yang sama dilakukan juga untuk larutan Fe 100 ppm. Efluen dianalisis dengan menggunakan spektrofotometer serapan atom untuk mengetahui seberapa besar penyerapannya.
" "> *1) ) #)1*8)$ 1+ +66(+ - + *41+ -,$7 # +6 + ,1# " ">" +6 *(& )) #)1*4 +
Karbon aktif dengan massa yang berbeda (0,2 ; 0,4 ; 0,6 ; 0,8 dan 1,0 gram) dicampurkan dengan 20 mL larutan Fe 100 ppm kemudian diaduk dengan % $ menggunakan waktu kontak optimum. Setelah itu campuran disaring dengan kertas saring ( % no 1. Filtrat yang dihasilkan dianalisis dengan menggunakan spektrofotometer serapan atom untuk mengetahui
seberapa besar penyerapan adsorben. Persen logam yang teradsorpsi dihitung dengan rumus sebagai berikut :
dengan :
C0 = konsentrasi awal logam (ppm)
C = konsentrasi logam setelah diadsorpsi (ppm)
" ">" +6 *(& 8
Sebanyak 20 mL larutan Fe 100 ppm diatur pHnya menjadi 1,2,3,4,5,6,7 dan 8 dengan penambahan HCl 1 M atau NaOH 1 M kemudian diaduk pada temperatur ruang dengan menggunakan waktu kontak optimum. Setelah itu campuran disaring dengan kertas saring ( % no. 1. Filtrat yang dihasilkan dianalisis dengan mengggunakan spektrofotometer serapan atom untuk mengetahui konsentrasi masing@masing ion logam yang tersisa dalam larutan.
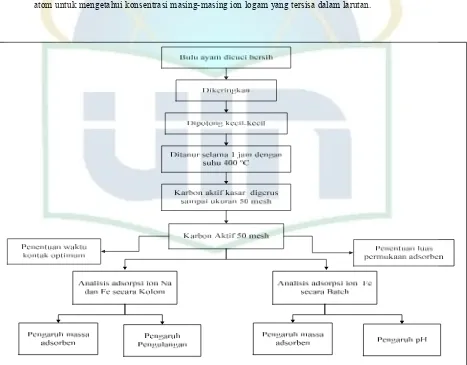
Gambar 6 Bagan Alir Kerja Penelitian
" 34( , + #)1*4 + *41+ -,$7
Limbah bulu ayam merupakan bahan yang utama dalam penelitian ini. Sebelum dijadikan karbon aktif, limbah bulu ayam dicuci bersih dengan deterjen untuk menghilangkan baunya. Pengeringan dengan sinar matahari bertujuan untuk menghilangkan kadar air setelah pencucian. Bulu ayam yang telah kering dipotong@potong kecil dengan tujuan untuk menyempurnakan dan meratakan proses pirolisis (Pujiarti & Sutapa, 2005). Pemanasan dengan suhu 400 oC menyebabkan semua senyawa organik yang terdapat pada limbah bulu ayam terdegradasi karena proses pirolisis menjadi karbon aktif.
Pada penelitian ini karbon aktif yang didapat dari pembakaran 2 gram bulu ayam adalah 0,7 gram. Dengan demikian rendemen yang didapat sebesar 35% (lampiran 1). Rendemen karbon aktif dari kayu Mahoni 54,12% (Pujiarti & Sutapa, 2005), rendemen karbon aktif dari tongkol jagung 70,5% (Suryani, 2009). Dari perbandingan dengan penelitian yang lain ternyata rendemen karbon aktif yang didapatkan pada penelitian ini jauh lebih kecil. Penetapan rendemen ini bertujuan untuk mengetahui jumlah karbon aktif yang didapat setelah proses karbonisasi. Rendahnya rendemen karbon aktif yang didapat disebabkan oleh pengaruh suhu pemanasan sehingga banyak senyawa yang mudah menguap ( % ) terlepas (Pujiarti & Sutapa, 2005).
50 mesh dengan tujuan agar luas permukaan karbon aktif yang didapat seragam sehingga siap digunakan sebagai adsorben.
" + +,( + # * $* *41+ -,$7
Penetapan kadar air bertujuan untuk mengetahui sifat higroskopis arang aktif (Pujiarti & Sutapa, 2005). Metode yang digunakan pada penentuan kadar air karbon aktif adalah metode gravimetri yakni analisis kimia berdasarkan penimbangan perbedaan bobot antara karbon aktif sebelum diuapkan kandungan airnya dengan sesudah dilakukan penguapan karbon aktif. Gravimetri penguapan adalah gravimetri dimana komponen yang tidak diinginkan (air) diubah menjadi uap. Kadar air diasumsikan bahwa hanya air yang merupakan senyawa volatil, karena dimungkinkan masih adanya air yang terjebak dalam rongga dan menutupi pori karbon aktif. Semakin rendah kadar air menunjukkan sedikitnya air yang tertinggal dan menutupi pori karbon aktif.
Kadar air karbon aktif yang dihasilkan pada penelitian ini adalah 0,51%. Penelitian lain yaitu kadar air karbon aktif dari tongkol jagung 4,4% (Suryani, 2010), kadar air karbon aktif dari kayu Mahoni 3,32% (Pujiarti & Sutapa, 2005), kadar air karbon aktif dari kulit singkong 2,18% (Ikawati & Melati, 2008). Kadar air yang didapat pada penelitian ini jauh lebih kecil dari penelitian karbon aktif jenis bahan lainnya. Kadar air yang dihasilkan dari penelitian ini memenuhi standar kualitas karbon aktif berdasar SNI 06@3730@95, yaitu maksimal 15% untuk arang aktif bentuk serbuk. Secara keseluruhan kadar air hasil penelitian ini relatif kecil, hal ini menunjukkan bahwa kandungan air yang terikat pada bulu ayam telah hilang pada saat dikarbonisasi dengan suhu 400 oC (Pujiarti & Sutapa, 2005).
" + +,( + # * 4( *41+ -,$7
bahan alam sebagai bahan dasar pembuatan karbon aktif tidak hanya mengandung senyawa karbon tetapi juga mengandung beberapa mineral, dimana sebagian dari mineral ini telah hilang pada saat karbonisasi dan aktivasi, sebagian lagi diperkirakan masih tertinggal dalam karbon aktif.
Kandungan abu sangat berpengaruh pada kualitas karbon aktif. Keberadaan abu yang berlebihan dapat menyebabkan terjadinya penyumbatan pori@pori sehingga luas pemukaan karbon aktif menjadi berkurang. Kadar abu karbon aktif yang dihasilkan pada penelitian ini adalah 4,8%. Jika dibandingkan penelitian kadar abu karbon aktif dari bahan lain yaitu dari kayu Mahoni 3% (Pujiarti & Sutapa, 2005), kulit singkong 3,8% (Ikawati & Melati, 2008), tongkol jagung 4,4% (Suryani, 2010) didapat bahwa kadar abu dari penelitian ini lebih besar. Kadar abu yang dihasilkan dari penelitian ini memenuhi standar kualitas karbon aktif berdasar SNI 06@3730@95, yaitu maksimal 10% untuk arang aktif bentuk serbuk. Rendahnya kadar abu kemungkinan disebabkan pemanasan yang terlalu lama yaitu selama 6 jam dengan suhu 750 oC menjadikan karbon aktif yang terbentuk berubah menjadi abu (Pujiarti & Sutapa, 2005).
" + 2$) *$), 2$+$, ) *41+ -,$7 # +6 + <
Karakteristik karbon aktif dilakukan dengan metode difraksi sinar@X untuk mengetahui tingkat kristalinitas karbon aktif. Karakterisasi dengan difraksi sinar@X dapat memberikan informasi struktur dalam karbon aktif. Karbon aktif yang diabukan pada suhu 400 oC berdasarkan hasil analisa XRD menunjukkan pola difraksi dengan kristalinitas yang rendah dan cenderung amorf.
Hal ini terlihat dari bentuk puncak atau peak yang tidak tajam dan melebar, ditunjukkan pada gambar 7 sebagai berikut:
Gambar 7 menunjukkan adanya tiga puncak yang tidak terlalu tajam yaitu pada 2θ = 25,43 dengan intensitas 100%, 2θ = 22,24 dengan intensitas 32% dan 2θ = 28,68 dengan intensitas 20%. Peak yang tidak terlalu tajam dan adanya hump (gundukan) menunjukkan bahwa karbon aktif yang didapat berbentuk amorf. Pada penelitian lain yaitu hasil uji kristalinitas dengan XRD pada karbon aktif sekam padi didapatkan difraktokram yang hampir sama dengan hasil pada penelitian ini. Karbon sekam padi yang ditanur pada suhu 700 oC memiliki intensitas maksimum pada 2θ = 20,04 – 25,30 (d = 4,42@3,51) dengan puncak yang melebar dan cenderung amorf (Umah ., 2010).
Hasil difraktogram karbon aktif sekam padi yang ditanur pada suhu 700 oC dapat dilihat pada gambar 8 berikut ini :
Gambar 8 Difraktogram Karbon Aktif Sekam Padi yang Ditanur pada 700 oC
"; + +,( + ? -,( 1+, - 8,$3(3
yang digunakan pada analisa optimasi waktu kontak ini adalah 10 ppm dengan berat karbon aktif yang digunakan adalah 0,1 gram.
Dari data tersebut dapat dibuat hubungan antara waktu kontak dengan persentase metilen biru terserap yang ditunjukkan pada Gambar 9 berikut ini :
Gambar 9 Grafik Waktu Kontak Antara Larutan Metilen Biru dengan Karbon Aktif
Gambar 9 menunjukkan bahwa semakin lama waktu kontak maka persentase metilen biru yang terserap semakin besar. Penyerapan metilen biru berdasarkan grafik di atas mengalami peningkatan yang konstan. Penyerapan optimum terjadi pada menit ke@30 dengan % metilen biru yang terserap sebanyak 87,46. Setelah menit ke@30 penyerapan cenderung menurun. Hal ini terjadi karena pada awal penyerapan, waktu kontak karbon aktif dan metilen biru belum mencukupi sehingga proses penyerapan berlangsung tidak maksimal. Tetapi pada menit ke@30 penyerapan antara karbon aktif dan metilen biru terjadi secara maksimal sehingga penyerapan yang dihasilkan tinggi. Pada menit di atas 30 menit terjadi penurunan penyerapan. Karena pengaruh pengadukan yang terlalu lama menyebabkan metilen biru yang terserap dalam keadaan ini akan terlepas kembali dan akibatnya penyerapan pada waktu kontak diatas 30 menit menjadi turun.
"! + +,( + ( ) *3(- + *41+ -,$7
Luas permukaan suatu karbon aktif adalah perbandingan antara luas permukaan dengan massanya. Tingkat adsorpsi yang tinggi oleh karbon aktif dengan ukuran yang partikel yang lebih kecil dikaitkan dengan tersedianya luas permukaan yang lebih besar pada karbon aktif. Dengan memecah partikel yang lebih besar cenderung dapat membuka celah kecil dan saluran pada permukaan partikel dari materi sehingga akses penyerapan lebih banyak untuk proses difusi yang lebih baik karena ukuran partikel lebih kecil (Onwu & Ogah, 2010).
Luas permukaan spesifik dihitung berdasarkan jumlah metilen biru yang diserap dengan penambahan karbon aktif pada konsentrasi metilen biru yang berbeda@beda. Jumlah penyerapan metilen biru yang tertinggi digunakan untuk menentukan luas permukaan karbon aktif.
Perbandingan jumlah adsorbansi metilen biru sebelum dan sesudah ditambahkan karbon aktif dapat dilihat berdasarkan grafik berikut ini :
Gambar 10 Grafik Serapan Metilen Biru Sebelum dan Sesudah Ditambahkan Karbon Aktif
Berdasarkan Gambar 10 dapat diketahui bahwa jumlah penyerapan yang maksimum sebesar 95,65% yaitu pada konsentarsi 2 ppm dimana jumlah metilen biru yang terserap adalah 0,01894. Berdasarkan perhitungan diketahui bahwa luas permukaan yang didapat adalah 463,39 m2/g (lampiran 7). Secara umum luas permukaan yang dihasilkan memenuhi kriteria yang disyaratakan bagi karbon aktif yang berkualitas (300@3500 m2/g).
" *1) ) #)1*8)$ 1+ # + +66(+ - + *41+ -,$7 # +6 +
,1# 1213
" " #)1*8)$ 1+ # +6 + +66(+ - + ,1# 1213
permukaan air laut. Dengan demikian terjadilah keadaan keseimbangan antar air tawar dan air laut dengan laju resapan dari aliran air tanah ke laut. Pengambilan air tanah melalui sumur@sumur akan mengakibatkan lengkung penurunan muka air tanah ( ), makin besar laju pengambilan air tanah, makin curam lengkung permukaan air tanah yang terjadi di sekitar sumur sampai tercapai keseimbangan baru jika terjadi pengisian dari daerah resapan. Keseimbangan baru ini dapat terjadi hanya jika laju pengambilan air tanah lebih kecil dari pengisian oleh air hujan pada daerah resapan. Tetapi kalau laju pengambilan air tanah dari sejumlah sumur jauh lebih besar dari pengisiannya maka lengkung@lengkung penurunan muka air tanah antara sumur satu dengan lainnya akan menyebabkan terjadinya penurunan muka air tanah secara permanen. Pada daerah pantai terjadinya penurunan air tanah dapat mengakibatkan terjadinya intrusi air asin (Ayers & Westcot, 1976). Meskipun natrium tidak tidak membahayakan bagi tubuh karena bukan merupakan logam berat, akan tetapi tingginya kandungan natrium berakibat pada sumber air yang berada di sekitar air laut terasa asin.
Salah satu upaya untuk mengurangi kandungan natrium adalah dengan melakukan adsorpsi menggunakan karbon aktif dari limbah bulu ayam yang dilakukan pada penelitian ini. Dari hasil penelitian dengan larutan simulasi didapatkan bahwa ion natrium tidak dapat diserap oleh karbon aktif dari bulu ayam (tabel 5). Hal ini disebabkan karena ukuran ion natrium lebih besar dari ukuran pori@pori karbon aktif. Ukuran ion dari Na+ adalah 0,095 nm sedangkan ukuran pori@pori karbon aktif pada penelitian ini diasumsikan lebih kecil dari 0,095 nm dan digolongkan sebagai karbon aktif mikropori. Pori@pori pada karbon aktif dapat dikelompokkan menjadi 3 golongan yaitu makropori (diameter > 50 nm), mesopori (diameter 2 – 50 nm) dan mikropori (diameter < 2nm) (Danarto & Samun, 2008). Ukuran ion natrium yang lebih besar dari ukuran pori@pori karbon aktif diasumsikan tidak dapat menembus pori@pori karbon aktif dan akibatnya ion natrium tidak dapat terserap oleh karbon aktif. Asumsi lain adalah sifat dari natrium itu sendiri dimana natrium merupakan unsur yang mempunyai sifat elastis karena susunan atom@atomnya yang renggang meskipun ukuran ionnya besar menyebabkan ion natrium dalam larutannya mempunyai kelarutan yang besar dan akibatnya susah untuk diadsorpsi.
pertukaran kation dilakukan pada sebuah kolom dimana kolom dipacking dengan 1 gram biomassa daun eceng gondok yang terimmobilisasi pada matriks polisilikat sampai homogen. Pelapisan glass wool di bawah dan di atas adsorben adalah untuk menahan biomassa agar tidak lolos dari kolom, yang dapat menimbulkan penyumbatan pada aliran kolom. Di samping itu agar permukaan adsorben tidak terganggu ketika ditambahkan pelarut atau sampel. Kolom yang sudah siap, kemudian dialiri dengan HCl sampai bersifat asam (dicek dengan kertas lakmus biru menjadi merah). Tujuannya adalah proses aktivasi, yaitu suatu proses untuk menaikkan kapasitas pertukaran ion.
Pengaktifan disini bertujuan untuk menghilangkan kation@kation lain yang kemungkinan masih terikat pada adsorben ketika proses preparasi kolom dilakukan, sehingga semua gugus kation menjadi seragam karena telah ditukar dengan H+. Proses penentuan kapasitas pertukaran ion dilakukan yaitu dengan cara, kolom yang netral berisi adsorben tersebut dialiri NaCl jenuh. Effluen yang keluar dari kolom lama kelamaan bersifat asam (dicek dengan kertas lakmus biru menjadi merah). Pertukaran kation dari ion Na+ ini diduga terjadi pertukaran dengan ion H+ yang berasal dari gugus aktif karboksilat (HCOO@) yang ada di dalam biomassa daun eceng gondok. Terbukti pada saat proses pertukaran ion yang dilakukan, ketika kolom netral yang berisi adsorben dialiri dengan NaCl jenuh, effluen yang keluar lama kelamaan bersifat asam. Hal tersebut menunjukkan bahwa ion Na+ benar@benar tertukar dengan ion H+. Pertukaran ion dapat terjadi karena biomassa sebagai fase diam mempunyai struktur molekuler yang terbuka dan permiabel (dapat ditembusi), sehingga ion@ion dalam larutan NaCl sebagai fase gerak dapat bergerak keluar masuk. Biomassa enceng gondok ini mengandung ion@ion aktif atau ion@ion lawan yang akan ditukarkan secara reversibel dengan ion Na+ yang mengelilinginya.
Gugus aktif pada biomassa yang mengandung ion H+ ini dibuat berkontak dengan larutan NaCl yang mengandung ion Na+. Kation Na+ ini akan berdifusi ke dalam gugus aktif pada struktur biomassa, dan kation H+ berdifusi keluar sampai tercapai kesetimbangan sesuai dengan reaksi berikut ini:
COO2@H+ + Na+(larutan) COO2@Na+ + H+(larutan)