PENGARUH TIPE KATALIS KOH DAN CaO PADA PEMBUATAN BIODIESEL TURUNAN MINYAK KACANG TANAH MELALUI
TRANSESTERIFIKASI DENGAN LAMA REAKSI 3 JAM PADA SUHU 65 OC MENGGUNAKAN ETER
SEBAGAI COSOLVENT
TESIS
Oleh
SABAR SILAEN 087026033/FIS
PROGRAM PASCASARJANA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PENGARUH TIPE KATALIS KOH DAN CaO PADA PEMBUATAN BIODIESEL TURUNAN MINYAK KACANG TANAH MELALUI
TRANSESTERIFIKASI DENGAN LAMA REAKSI 3 JAM PADA SUHU 65 OC MENGGUNAKAN ETER
SEBAGAI COSOLVENT
TESIS
Untuk memperoleh gelar Magister Sains dalam Program Studi Magister Fisika pada Sekolah Pascasarjana Universitas Sumatera Utara
Oleh
SABAR SILAEN 087026033/FIS
PROGRAM PASCASARJANA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN
2010
PENGESAHAN TESIS
Judul Tesis : PENGARUH TIPE KATALIS KOH DAN CAO
PADA PEMBUATAN BIODIESEL TURUNAN MINYAK KACANG TANAH MELALUI TRANSESTERIFIKASI DENGAN LAMA
REAKSI 3 JAM PADA SUHU 65 oC
MENGGUNAKAN ETER SEBAGAI COSOLVENT
Nama Mahasiswa : Sabar Silaen Nomor Induk Mahasiswa : 087026033 Program Studi : Magister Fisika
Fakultas : Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
Menyetujui Komisi Pembimbing
DR. Marhaposan Situmorang Drs. Nimpan Bangun, M.Sc Ketua Anggota
Ketua Program Studi, Dekan,
Prof. Drs. Eddy Marlianto, M.Sc., Ph.D Prof. Drs. Eddy Marlianto, M.Sc., Ph.D NIP. 195503171986011001 NIP. 195503171986011001
PERNYATAAN ORISINALITAS
PENGARUH TIPE KATALIS KOH DAN CaO PADA PEMBUATAN BIODIESEL TURUNAN MINYAK KACANG TANAH MELALUI
TRANSESTERIFIKASI DENGAN LAMA REAKSI 3 JAM PADA SUHU 65 oC MENGGUNAKAN ETER
SEBAGAI COSOLVENT
T E S I S
Dengan ini saya nyatakan bahwa saya mengakui semua karya tesis ini adalah hasil karya saya sendiri kecuali kutipan dan ringkasan yang tiap satunya telah dijelaskan sumbernya dengan benar.
Medan, Juni 2010
SABAR SILAEN
PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Sebagai sivitas akademika Universitas Sumatera Utara, saya yang bertanda tangan di bawah ini:
N a m a : Sabar Silaen N I M : 087026033 Program Studi : Magister Fisika Jenis Karya Ilmiah : Tesis
Demi pengembangan ilmu pengetahuan, menyetujui untuk memberikan kepada Universitas Sumatera Utara Hak Bebas Royalti Non-Eksklusif (Non-Excluxive Royalty Free Right) atas Tesis saya yang berjudul :
PENGARUH TIPE KATALIS KOH DAN CaO PADA PEMBUATAN BIODIESEL TURUNAN MINYAK KACANG TANAH MELALUI TRANSESTERIFIKASI DENGAN LAMA
REAKSI 3 JAM PADA SUHU 65 oC MENGGUNAKAN ETER
SEBAGAI COSOLVENT
Beserta perangkat yang ada (jika diperlukan). Dengan Hak Bebas Royalti Non-Eksklusif ini, Universitas Sumatera Utara berhak menyimpan, mengalih media, memformat, mengelola dalam bentuk data-base, merawat dan mempublikasikan tesis saya tanpa meminta izin dari saya selama tetap mencantumkan nama saya sebagai penulis dan sebagai pemegang dan atau sebagai pemilik hak cipta.
Demikian pernyataan ini dibuat dengan sebenarnya.
Medan, Juni 2010
Telah diuji pada
Tanggal : 14 Juni 2010
PANITIA PENGUJI TESIS
Ketua : Dr. Marhaposan Situmorang
Anggota : 1. Drs. Nimpan Bangun, M.Sc
2. Prof. Dr. Eddy Marlianto, M.Sc, Ph.D
3. Prof. Dr. Timbangen S., M.Sc
4. Dr. Anwar Dharma Sembiring, MS
RIWAYAT HIDUP
DATA PRIBADI
Nama lengkap berikut gelar : Sabar Silaen, S.Pd.
Tempat dan TanggalLahir : Balige, 21 September 1965
Alamat Rumah : Jl. Pendidikan Gg. Gesba Mariendal - I
Telepon/ HP : 08126313124
Instansi Tempat Kerja : SMA Negeri 5 Medan
Alamat Kantor : Jl. Pelajar No. 17 Medan
Telepon : (061) 7360664
DATA PENDIDIKAN
SD : SD Swasta Mandala Medan Tamat : 1977
SMP : SMP Negeri 7 Medan Tamat : 1981
SMA : SMA Negeri 5 Medan Tamat : 1984
Diploma III : FMIPA USU Medan Tamat : 1988
Strata-1 : FPMIPA IKIP Negeri Medan Tamat : 2007
Strata-1 : FKIP Univ. Terbuka Tamat : 2007
Strata-2 : PSMF PPs FMIPA USU Medan Tamat : 2010
KATA PENGANTAR
Puji syukur penulis panjatkan kehadirat Tuhan Yang Maha Esa karena hanya kasih karuniaNya penulis dapat menyelesaikan penelitian dan penyusunan tesis.
Kami ucapkan terima kasih sebesar-besarnya kepada Pemerintah Republik Indonesia c.q Pemerintah Provinsi Sumatera Utara yang telah memberikan bantuan dana sehingga kami dapat melaksanakan Program Magister Sains pada Program Studi Magister Ilmu Fisika Program Pascasarjana FMIPA Universitas Sumatera Utara.
Dengan selesainya tesis ini, perkenankanlah kami mengucapkan terima kasih yang sebesar-besarnya kepada:
Rektor Universitas Sumatera Utara, Prof. Dr. dr. Syahrial Pasaribu, DTM & H, M.Sc (CTM), SPA (K) atas kesempatan yang diberikan kepada kami untuk mengikuti dan menyelesaikan pendidikan Program Magister Sains.
Dekan Fakultas MIPA Universitas Sumatera Utara Prof. Drs. Eddy Marlianto, M.Sc., Ph.D atas kesempatan menjadi mahasiswa Program Magister Sains pada Program Pascasarjana FMIPA Universitas Sumatera Utara.
Ketua Program Studi Magister Fisika, Prof. Drs. Eddy Marlianto, M.Sc., Ph.D. Sekretaris Program Studi Magister Fisika Drs Nasir Saleh, M.Eng, Sc., beserta seluruh Staf Pengajar pada Program Studi Magister Fisika Program Pascasarjana FMIPA Universitas Sumatera Utara.
Terima kasih yang tak terhingga dan penghargaan setinggi-tingginya kami ucapkan kepada Dr. Marhaposan Situmorang selaku pembimbing Utama yang dengan penuh perhatian dan telah memberikan dorongan, bimbingan dan arahan, demikian juga kepada Bapak Drs. Nimpan Bangun, M.Sc selaku pembimbing lapangan yang dengan penuh kesabaran menuntun dan membimbing kami hingga selesainya penelitian ini.
Kepala SMA Negeri 5 Medan, Drs. Salmi Effendi, M.Pd., yang telah memberi izin belajar di program Pascasarjana tanpa meninggalkan tugas.
Pak Uda Hasiolan Silaen, S.H., Edward Silaen, S.T., dan Kakek Parsaoran Silaen yang memberikan bantuan kesempatan dan moril selama mengikuti perkuliahan.
Mahasiswa pascasarjana Henri Jannu, Juniar limbong, Januaris Pane, Jamson Siboro, dan Juaksa Manurung, atas saran-saran, kerjasama selama perkuliahan dan menyelesaikan penelitian.
Rekan-rekan sejawat Dra. Tiamar Hutapea, Drs. Salon Sinaga, M.Si., Tiorinse Sinaga, S.Pd., M.Si, Drs. Ajis Pakpahan, M.si, dan Farawiati Andrianti, S.Pd, M.Si atas dorongan semangat yang diberikan.
Kepada Ibunda Hermina Br. Sianipar, mertua H. Simanungkalit, D. Br. Napitupulu serta isteri tercinta Magdalena Simanungkalit serta anak-anakku terkasih William Fransisco, Kelvin E. Andreas dan Christine Monica atas segala pengorbanan kalian baik berupa moril dan materil.
Medan, Juni 2010 Penulis
PENGARUH TIPE KATALIS KOH DAN CaO PADA PEMBUATAN BIODIESEL MINYAK KACANG TANAH MELALUI
TRANSESTERIFIKASI DENGAN LAMA REAKSI 3 JAM PADA SUHU 65 oC MENGGUNAKAN
ETER SEBAGAI COSOLVENT
ABSTRAK
Biodiesel sebagai energi alternatif telah banyak dilaporkan dan emisi gas CO2
lebih kecil dari solar. Katalis yang sudah umum adalah KOH dan NaOH, pemakaian minyak kacang tanah sebagai bahan bakar dan katalis Cao belum banyak dilaporkan. Karena itu dalam penelitian ini dilakukan transesterifikasi minyak kacang tanah menggunakan katalis KOH dan CaO memakai eter sebagai cosolvent. Metode transesterifikasi katalis KOH dan CaO dengan lama reaksi 3 jam pada suhu 65 oC. Hasil campuran reaksi dipisahkan dengan mengekstraksi dalam heksan, fraksi heksan dicuci dengan larutan HCl4-n dibilas dengan aquades
kemudian fase atas dikeringkan dengan Na2SO4. Fraksi fase diperoleh setelah
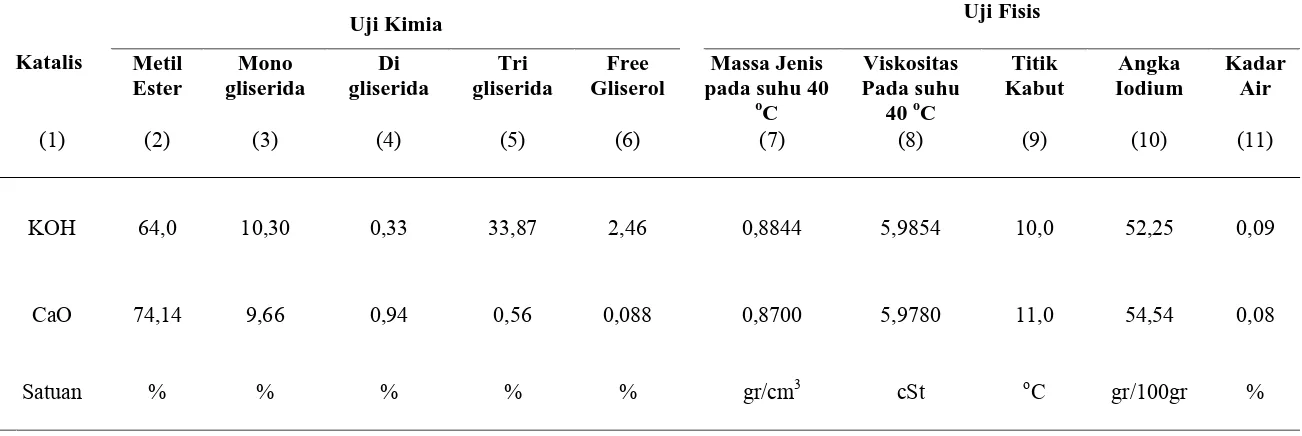
menguapkan heksan tersebut dan kadarnya diukur dengan gascromatografiuntuk mendapatkan komposisi kimia. konversi minyak kacang tanah dengan katalis KOH adalah 60,53% sedangkan katalis CaO 58,10%. Biodiesel yang diperoleh dengan katalis KOH mengandung 10,31% monogliserida, 0,33% digliserida, 33,87% trigliserida, 2,46% free gliserol. Biodiesel yang diperoleh dengan katalis CaO mengandung 9,66% monogliserida, 0,94% digliserida, 0,56% trigliserida, 0,088 free gliserol. Sifat fisis dari biodiesel yang diperoleh dengan menggunakan katalis KOH kadar airnya 0,09%, angka iodium 52,25 gr/100 gr, titik kabut 10,0
o
C, viskositas 5,9854 cSt, massa jenis 0,8844 g/cm3. Biodiesel yang diperoleh dengan menggunakan katalis CaO kadar airnya 0,08%, angka iodium 55,54 gr/100 gr, titik kabut 11,0 oC, viskositas 5,9780 cSt, massa jenis 0,8700 g/cm3.
Kata kunci :Minyak Kacang Tanah, Trigliserida, Katalis, Gliserol, Cosolvent, Transesterifikasi, biodiesel, kadar air, massa jenis, viskositas,
EFFECT OF CATALYST TYPE ON KOH AND CaO peanut oil biodiesel transesterification BY REACTION WITH OLD
3 HOURS IN USING TEMPERATURE 65 oC
ETHERS AS COSOLVENT
ABSTRACT
Biodiesel as an alternative energy has been widely reported and less CO2
emissions than diesel. Which is a common catalyst is KOH and NaOH, using peanut oil as fuel and catalyst Cao has not been widely reported. Therefore, this study of peanut oil transesterification using KOH and CaO catalyst using ether as a cosolvent. Transesterification method of KOH and CaO catalyst with reaction time 3 hours at a temperature of 65 oC. Results are separated by extracting the reaction mixture in hexane, the hexane fraction was washed with HCl4-n solution
rinsed with distilled water and then dried with Na2SO4 phase above. Phase
fraction was obtained after evaporating hexane and its purity was measured by gascromatografi to obtain the chemical composition. conversion of peanut oil with KOH catalyst was 60.53% while 58.10% CaO catalyst. Biodiesel is obtained by KOH catalyst containing monogliceride 10.31%, 0.33% diglycerides, triglycerides, 33.87%, 2.46% free glycerol. Biodiesel is obtained by CaO catalyst containing 9.66% monogliceride, 0.94% diglycerides, triglycerides 0.56%, 0.088 free glycerol. The physical properties of biodiesel obtained by using the catalyst KOH water level is 0.09%, iodine number 52.25 gr/100 gr, cloud point 10.0 oC, cSt viscosity of 5.9854, density 0.8844 g/cm3. Biodiesel is obtained by using CaO catalyst water content of 0.08%, iodine number 55.54 gr/100 gr, cloud point 11.0
o
C, cSt viscosity of 5.9780, density 0.8700 g/cm3.
Keywords: Peanut Oil, Triglycerides, Catalyst, Glycerol, Cosolvent,
Transesterification, biodiesel, water content, density, viscosity, cloud point and iodine number.
DAFTAR ISI
Halaman
KATA PENGANTAR i
ABSTRAK iii
ABSTRACT iv
DAFTAR ISI v
DAFTAR TABEL viii
DAFTAR GAMBAR ix
DAFTAR LAMPIRAN x
BAB I PENDAHULUAN 1
1.1 Latar Belakang 1
1.2 Batasan Masalah 3
1.3 Perumusan Masalah 3
1.4 Tujuan Penelitian 4
1.5 Hipotesis 4
1.6 Manfaat Penelitian 5
BAB II TINJAUAN PUSTAKA 6
2.1 Biodiesel 6
2.2 Bahan Baku Biodiesel 7
2.3 Proses Produksi Biodiesel Turunan Minyak Kacang Tanah 9
2.4 Standar Biodiesel di Indonesia 11
2.5 Katalis 12
2.5.1 Katalis Homogen 12
2.5.2 Katalis Heterogen 13
2.5.3 Bio Katalis (Enzim) 14
2.5.4 Auto Katalis 14
2.5.4.1 Katalis Sebagai Perantara 16
2.6 Alkohol 17
2.7 Reaksi Transesterifikasi 18
2.8 Sifat-sifat Penting dari Biodiesel 20
2.8.1 Massa Jenis (Densitas) 20
2.8.2 Viskositas 21
2.8.3 Titik Kabut 22
2.8.4 Angka Iodium 24
2.8.5 Kadar Air 24
BAB III METODE PENELITIAN 26
3.1 Tempat dan Waktu Penelitian 26
3.2 Bagan Penelitian 26
3.2.1 Pembuatan Minyak Kacang 26
3.2.2 Pembuatan FAME 27
3.2.3 Uji Karakteristik FAME 28
3.3 Pembuatan Minyak Kacang Tanah 28
3.3.1 Alat dan Bahan 28
3.3.2 Prosedur Kerja 29
3.4 Proses Pembuatan Biodiesel dengan Menggunakan
Katalis KOH dan Cosolvent Eter 30
3.4.1 Alat dan Bahan 30
3.4.2 Prosedur Kerja 30
3.5 Proses Pembuatan Biodiesel dengan Menggunakan
Katalis CaO dan Cosolvent Eter 32
3.5.1 Alat dan Bahan 32
3.5.2 Prosedur Kerja 33
3.6 Pengujian Massa Jenis (Densitas) 34
3.6.1 Alat dan Bahan 34
3.6.2 Prosedur Kerja 34
3.7 Pengujian Viskositas 37
3.7.1 Alat dan Bahan 37
3.8 Pengujian Titik Kabut 38
3.8.1 Alat dan Bahan 38
3.8.2 Prosedur Kerja 38
3.9 Pengujian Angka Iodium 38
3.9.1 Alat dan Bahan 38
3.9.2 Prosedur Kerja 39
3.10 Pengujian Kadar Air 40
3.10.1 Prinsip Kerja 40
3.10.2 Alat dan Bahan 40
3.10.3 Prosedur Kerja 40
3.10.4 Perhitungan 40
BAB IV HASIL DAN PEMBAHASAN 42
4.1 Pembuatan Minyak Kacang Tanah 42
4.2 Pembuatan Biodiesel 42
4.3 Uji Kimia 49
4.4 Uji Fisis 49
4.4.1 Uji Massa Jenis (Densitas) 51
4.4.2 Uji Viskositas 51
4.4.3 Uji Titik Kabut 52
4.4.4 Uji Angka Iodium 52
4.4.5 Uji Kadar Air 53
BAB V KESIMPULAN DAN SARAN 54
5.1 Kesimpulan 54
5.2 Saran 54
DAFTAR PUSTAKA 55
DAFTAR TABEL
Nomor Tabel
Judul Halaman
2.1 Jenis Tanaman Bahan Baku Biodiesel 7
2.2 Jenis Asam Lemak yang Terkandung dalam
Minyak Kacang Tanah
9
2.3 Persyaratan Kualitas Biodiesel
Menurut SNI – 04 – 7182 - 2006
11
4.1 Hasil Uji GC Analisa Komposisi FFA
Minyak Kacang Tanah
43
4.2 FAME Kasar Hasil Transesterifikasi 44
4.3 Jenis dan Komposisi Asam Lemak pada Kacang Tanah 45
4.4 Kandungan Asam Lemak Minyak Kacang dalam
Hitungan 100 gram
46
4.5 Data Hasil Reaksi Transesterifikasi 884,0 gr
Minyak Kacang dengan Katalis KOH dan CaO
Lama Reaksi 3 Jam pada Suhu 65 oC
49
4.6 Hasil Uji Kimia dan Uji Fisis Biodiesel Turunan Minyak
Kacang Tanah
DAFTAR GAMBAR
Nomor Gambar
Judul Halaman
2.1 Proses Pembuatan Biodiesel Turunan
Minyak Kacang Tanah
10
2.2 Reaksi Transesterifikasi dengan Katalis Homogen 12
2.3 Reaksi Transesterifikasi dengan Katalis Heterogen 13
2.4 Perubahan Energi Aktivasi Setelah Menggunakan
Katalis
15
3.1 Bagan Pembuatan Minyak Kacang Tanah 26
3.2 Bagan Pembuatan FAME 27
DAFTAR LAMPIRAN
Lampiran
Huruf
Judul Halaman
A Uji Kimia Minyak Kacang Tanah L – 1
B Proses Pembuatan Biodiesel L – 2
C Uji Kimia Biodiesel Turunan Minyak Kacang Tanah L – 12
D Standar Solar L – 16
PENGARUH TIPE KATALIS KOH DAN CaO PADA PEMBUATAN BIODIESEL MINYAK KACANG TANAH MELALUI
TRANSESTERIFIKASI DENGAN LAMA REAKSI 3 JAM PADA SUHU 65 oC MENGGUNAKAN
ETER SEBAGAI COSOLVENT
ABSTRAK
Biodiesel sebagai energi alternatif telah banyak dilaporkan dan emisi gas CO2
lebih kecil dari solar. Katalis yang sudah umum adalah KOH dan NaOH, pemakaian minyak kacang tanah sebagai bahan bakar dan katalis Cao belum banyak dilaporkan. Karena itu dalam penelitian ini dilakukan transesterifikasi minyak kacang tanah menggunakan katalis KOH dan CaO memakai eter sebagai cosolvent. Metode transesterifikasi katalis KOH dan CaO dengan lama reaksi 3 jam pada suhu 65 oC. Hasil campuran reaksi dipisahkan dengan mengekstraksi dalam heksan, fraksi heksan dicuci dengan larutan HCl4-n dibilas dengan aquades
kemudian fase atas dikeringkan dengan Na2SO4. Fraksi fase diperoleh setelah
menguapkan heksan tersebut dan kadarnya diukur dengan gascromatografiuntuk mendapatkan komposisi kimia. konversi minyak kacang tanah dengan katalis KOH adalah 60,53% sedangkan katalis CaO 58,10%. Biodiesel yang diperoleh dengan katalis KOH mengandung 10,31% monogliserida, 0,33% digliserida, 33,87% trigliserida, 2,46% free gliserol. Biodiesel yang diperoleh dengan katalis CaO mengandung 9,66% monogliserida, 0,94% digliserida, 0,56% trigliserida, 0,088 free gliserol. Sifat fisis dari biodiesel yang diperoleh dengan menggunakan katalis KOH kadar airnya 0,09%, angka iodium 52,25 gr/100 gr, titik kabut 10,0
o
C, viskositas 5,9854 cSt, massa jenis 0,8844 g/cm3. Biodiesel yang diperoleh dengan menggunakan katalis CaO kadar airnya 0,08%, angka iodium 55,54 gr/100 gr, titik kabut 11,0 oC, viskositas 5,9780 cSt, massa jenis 0,8700 g/cm3.
Kata kunci :Minyak Kacang Tanah, Trigliserida, Katalis, Gliserol, Cosolvent, Transesterifikasi, biodiesel, kadar air, massa jenis, viskositas,
EFFECT OF CATALYST TYPE ON KOH AND CaO peanut oil biodiesel transesterification BY REACTION WITH OLD
3 HOURS IN USING TEMPERATURE 65 oC
ETHERS AS COSOLVENT
ABSTRACT
Biodiesel as an alternative energy has been widely reported and less CO2
emissions than diesel. Which is a common catalyst is KOH and NaOH, using peanut oil as fuel and catalyst Cao has not been widely reported. Therefore, this study of peanut oil transesterification using KOH and CaO catalyst using ether as a cosolvent. Transesterification method of KOH and CaO catalyst with reaction time 3 hours at a temperature of 65 oC. Results are separated by extracting the reaction mixture in hexane, the hexane fraction was washed with HCl4-n solution
rinsed with distilled water and then dried with Na2SO4 phase above. Phase
fraction was obtained after evaporating hexane and its purity was measured by gascromatografi to obtain the chemical composition. conversion of peanut oil with KOH catalyst was 60.53% while 58.10% CaO catalyst. Biodiesel is obtained by KOH catalyst containing monogliceride 10.31%, 0.33% diglycerides, triglycerides, 33.87%, 2.46% free glycerol. Biodiesel is obtained by CaO catalyst containing 9.66% monogliceride, 0.94% diglycerides, triglycerides 0.56%, 0.088 free glycerol. The physical properties of biodiesel obtained by using the catalyst KOH water level is 0.09%, iodine number 52.25 gr/100 gr, cloud point 10.0 oC, cSt viscosity of 5.9854, density 0.8844 g/cm3. Biodiesel is obtained by using CaO catalyst water content of 0.08%, iodine number 55.54 gr/100 gr, cloud point 11.0
o
C, cSt viscosity of 5.9780, density 0.8700 g/cm3.
Keywords: Peanut Oil, Triglycerides, Catalyst, Glycerol, Cosolvent,
Transesterification, biodiesel, water content, density, viscosity, cloud point and iodine number.
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Meningkatnya populasi manusia di bumi mengakibatkan kebutuhan akan
energi semakin meningkat pula. Bahan bakar minyak bumi adalah salah satu
sumber energi utama yang banyak digunakan berbagai negara di dunia pada saat
ini. Kebutuhan bahan bakar ini selalu meningkat, seiring dengan penggunaannya
di bidang industri maupun transportasi. Setiap hari jutaan barrel minyak mentah
bernilai jutaan dolar dieksplotasi tanpa memikirkan bahwa minyak tersebut
merupakan hasil dari proses evolusi alam yang berlangsung selama ribuan bahkan
jutaan tahun yang lalu dan tidak bisa diperbaharui (unrenewable), sehingga untuk
memperoleh bahan bakar minyak bumi dalam waktu yang singkat tidak mungkin.
Besarnya kebutuhan akan minyak bumi yang tidak diimbangi ketersediaan
kuantitasnya membuat harga minyak sangat mahal. Dengan demikian manusia
mulai mencari sumber-sumber energi alternatif yang ketersediaan kuantitasnya
tidak terbatas (dapat diperbaharui) dan ramah lingkungan.
Dua buah laporan terbaru dari Congressional Research Services (CRS) pada tahun
1985 dan 2003 kepada Komisi Energi di Konggres Amerika Serikat, menyebutkan
bahwa jika tingkat penggunaan bahan bakar fosil masih terus seperti sekarang
(tanpa peningkatan dalam efisiensi produksi, penemuan cadangan baru, dan
peralihan ke sumber-sumber energi alternatif terbarukan), cadangan sumber energi
bahan bakar fosil dunia khususnya minyak bumi, diperkirakan hanya akan cukup
untuk 10-15 tahun lagi (Alam Syah, A. N., 2006)
Beberapa upaya penelitian telah dilakukan untuk memperoleh pengganti energy
fosil (minyak bumi), energi yang terbarukan, ramah lingkungan, yang
ketersediaannya dapat diperoleh dalam yang singkat seperti energi matahari,
bersumber dari tenaga matahari, angin dan arus laut mengalami kesulitan dalam
hal penampungan (storage) khususnya untuk benda bergerak. Salah satu
diantaranya adalah pemanfaatan minyak nabati untuk menggantikan bahan bakar
minyak, baik berupa bio-ethanol sebagai pengganti premium maupun biodiesel
sebagai pengganti minyak solar.
Saat ini dunia banyak mengkaji tentang sumber energi yang terbaharui yaitu
lemak atau minyak nabati ataupun hewani . Bahan ini ditransformasikan menjadi
alkil metil ester asam lemak atau yang disebut juga FAME (Fatty Acids Methyl
Ester) menggunakan katalis NaOH dan KOH. Secara umum telah banyak dikaji
metode pembuatan metil ester asam lemak dari kelapa sawit dengan proses
transesterifikasi dengan katalis NaOH dan KOH. Penggunaan katalis ini
mempunyai kekurangan seperti sifat korosif yang tinggi dan katalis ini tidak
mungkin digunakan kembali sehingga dalam proses pembuatan metil ester ini
NaOH dibuang dalam bentuk larutan (Bangun, N., 2009).
Proses produksi biodiesel (BIOX) dikembangkan oleh Profesor David Boocock
dari Universitas Toronto, reaksi transesterifikasi dalam cosolvent dapat terjadi
hasil yang tinggi. Cosolvent yang dapat dipakai seperti tetrahidrofuran (THF)
suatu eter siklik (Demirbas, A., 2009). Metode transesterifikasi dengan katalis
dapat dilakukan dengan basa, asam dan enzim, katalis basa digunakan CaO dan
MgO.
Sebagaimana basa alkali dengan metanol membentuk metoksida secara insitu,
maka sifat ini juga dapat terjadi pada golongan II A. Misalnya MgO dan CaO
dapat juga menghasilkan Mg(OCH3)2 dan Ca(OCH3)2. Pemakaian oksida ini
sebagai katalis memberi keuntungan dimana MgO dan CaO memiliki kelarutan
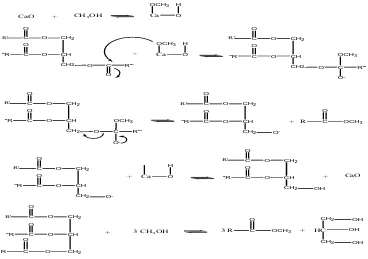
Jika dipakai CaO sebagai katalis maka akan terbentuk reaksi:
CaO + CH3OH Ca O
OCH3 H
Tanpa menghasilkan air. Keuntungan ini mendorong peneliti untuk menggunakan
oksida golongan II A sebagai katalis dalam reaksi transesterifikasi.
Penggunaan CaO sebagai katalis telah banyak dilaporkan. Suppes telah
menggunakan CaO sebagai katalis heterogen dalam reaksi alkoholisis untuk
menghasilkan monogliserida pada temperatur 200–220 oC dengan lama reaksi
1–4 jam (Suppes, G. J., 2001).
Zhu meneliti reaksi transesterifikasi minyak curcas jatropha menggunakan CaO
sebagai katalis. Tapi, katalis tersebut harus diperlakukan dalam larutan amonium
karbonat dan terkalsinasi pada temperatur tinggi menghasilkan yield metil ester
93%. Penggunaan CaO sebagai katalis basa padat mempunyai banyak
keuntungan, seperti tingginya aktivitas, kondisi reaksi yang ringan, masa hidup
katalis yang panjang dan biaya katalis yang rendah.
1.2 BATASAN MASALAH
Dalam penelitian, peneliti membatasi masalah yakni: proses pembuatan
biodiesel turunan minyak kacang tanah menggunakan katalis KOH, CaO dan
cosolvent eter dengan lamanya reaksi 3 jam pada suhu 65 oC.
1.3 PERUMUSAN MASALAH
Dengan semakin terbatasnya cadangan minyak bumi (minyak fosil),
sementara kebutuhan akan minyak bumi semakin meningkat yang diakibatkan
semakin bertambahnya jumlah konsumen (industri, transportasi dan kegiatan
manusia) dan juga karena dampak negatif penggunaan bahan bakar fosil maka
diatas dengan cara menemukan sember energi alternatif (biodiesel sebagai
pengganti bahan bakar solar) yang dapat diperbaharui dan ramah lingkungan.
Bahan baku biodiesel yang digunakan dalam penelitian ini adalah minyak kacang
tanah, dan diantara jenis-jenis katalis yang digunakan adalah katalis KOH dan
CaO. Dari uraian diatas maka perumusan masalah adalah:
1. Apakah CaO dapat digunakan sebagai katalis dalam reaksi
transesterifikasi untuk menghasilkan biodiesel turunan minyak kacang
tanah?
2. Apakah penggunaan katalis KOH dan CaO akan menghasilkan jumlah
dan sifat fisis biodiesel turunan minyak kacang tanah yang berbeda?
3. Apakah sifat kimia biodiesel turunan minyak kacang tanah yang
dihasilkan melalui proses transesterifikasi dengan menggunakan katalis
KOH dan CaO adalah berbeda?
1.4 TUJUAN PENELITIAN
1. Untuk mendapatkan katalis yang lebih baik.
2. Untuk memanfaatkan katalis yang mudah diperoleh dan dapat
digunakan kembali.
3. Untuk mengetahui perbedaan jumlah dan sifat fisis biodiesel turunan
minyak kacang tanah dengan menggunakan katalis KOH dan CaO.
1.5 HIPOTESIS
Sistem katalis KOH tidak dapat diperoleh kembali sedangkan sistem
katalis CaO dapat diperoleh kembali setelah reaksi transeseterifikasi dan
menghasilkan jumlah dan sifat fisis biodiesel turunan minyak kacang tanah yang
1.6 MANFAAT PENELITIAN
1. Untuk memberikan informasi kepada masyarakat yang melakukan
penelitian tentang biodiesel bahwa CaO dapat digunakan sebagai
katalis.
2. Memberikan informasi kepada masyarakat bahwa minyak kacang tanah
dapat digunakan sebagai sumber bahan bakar alternatif untuk mengatasi
kelangkaan bahan bakar minyak bumi (minyak Solar) dimasa yang
akan datang.
3. Sebagai suatu usaha untuk memberdayakan kacang tanah sebagai bahan
BAB II
TINJAUAN PUSTAKA
2.1 BIODIESEL
Biodiesel merupakan bahan bakar yang diperoleh dari proses esterifikasi
atau transesterifikasi asam lemak dengan alkohol dan bantuan katalis. Asam
lemak tersebut berasal dari tumbuh-tumbuhan ataupun dari hewan yang
viskositasnya hampir sama dengan solar. Biodiesel dapat diperoleh melalui suatu
proses yang disebut reaksi esterifikasi asam lemak bebas atau reaksi
transesterifikasi trigliserida dengan metanol dan dari reaksi ini akan dihasilkan
metil ester/etil ester asam lemak dan gliserida.
Katalis
Trigliserida + Metanol /Eter Metil ester/Etil ester + Gliserol
Kadar polusi yang ditimbulkannya rendah dibandingkan solar, emisi gas buang
lokal lebih aman. Emisi langsung kendaraan diesel dengan bahan bakar biodiesel
lebih tidak beracun dibandingkan dengan bahan bakar solar. Efek pengurangan
karbon monoksida yang sangat beracun, efek pengurangan emisi hidrokarbon tak
terbakar (unburn hydrocarbon) adalah keuntungan pemakaian biodiesel secara
langsung karena membantu pengurangan efek pemanasan global yang sangat
berbahaya bagi kehidupan manusia.
Biodiesel memiliki efek pelumasan yang sangat tinggi, sehingga membuat mesin
diesel lebih awet. Biodiesel juga memiliki angka setana relatif tinggi, mengurangi
ketukan pada mesin sehingga mesin bekerja lebih mulus. Biodiesel juga memiliki
flash point yang lebih tinggi dibandingkan dengan solar, tidak menimbulkan bau
yang berbahaya sehingga lebih mudah dan aman untuk ditangani. Keunggulan
biodiesel lainya seperti dapat diperbaharui, biodegradabel (dapat terurai oleh
mikroorganisme), tidak mengandung sulfur dan benzene yang mempunyai sifat
karsinogen. Dapat dengan mudah dicampur dengan solar dalam berbagai
komposisi dan tidak memerlukan modifikasi mesin apapun. Mengurangi asap
5%–10% volum biodiesel kedalam solar, memberikan nilai tambah pada sektor
agribisnis mendorong penggunaan biodiesel mulai mendapat perhatian dunia
sebagai alternatif bahan bakar pengganti solar.
2.2 BAHAN BAKU BIODIESEL
Indonesia sebagai daerah tropis yang subur diberkahi oleh Tuhan Yang
Maha Esa dengan berbagai keanekaragaman hayati, tabel 2.1 daftar beberapa
jenis tanaman yang dapat di kembangkan sebagai bahan baku untuk menghasilkan
energi alternatif (biodiesel). Salah satu diantaranya adalah kacang tanah untuk
menggantikan bahan bakar minyak bumi sebagai pengganti minyak solar.
Tabel 2.1 Jenis Tanaman Bahan Baku Biodiesel
Sumber:Eka Tjipta Foundatiaon, 2008
No Nama Lokal Nama Latin Sumber Minyak
Isi % Berat Kering
1 Jarak Pagar Jatropha Curcas Inti biji 40-60
2 Jarak Kaliki Riccinus Communis Biji 45-50
3 Kacang Suuk Arachis Hypogea Biji 35-55
4 Kapok/ Randu Ceiba Pantandra Biji 24-40
5 Karet Hevea Brasiliensis Biji 40-50
6 Kecipir Psophocarpus Tetrag Biji 15-20
7 Kelapa Cocos Nucifera Inti biji 60-70
8 Kelor Moringa Oleifera Biji 30-49
9 Kacang tanah Aleurites Moluccana Inti biji 57-69
10 Kusambi Sleichera Trijuga Sabut 55-70
11 Nimba Azadiruchta Indica Inti biji 40-50
12 Saga Utan Adenanthera Pavonina Inti biji 14-28
13 Sawit Elais Suincencis Sabut dan biji 45-70 + 46-54 14 Nyamplung Callophyllum
Lanceatum
Inti biji 40-73
15 Randu Alas Bombax Malabaricum Biji 18-26
16 Sirsak Annona Muricata Inti biji 20-30
17 Srikaya Annona Squosa Biji 15-20
18 Sawit Elais Guineensis Pulp+Kernel 45-70+46-54
Minyak nabati mengandung 90-98% trigliserida dan sejumlah kecil mono dan
digliserida. Trigliserida adalah ester dari tiga asam lemak rantai panjang yang
lima jenis asam lemak yaitu: asam stearat, asam palmitat, asam oleat, asam
linoleat dan asam linolenat. Asam stearat dan asam palmitat termasuk jenis asam
lemak jenuh, asam oleat, asam linoleat, asam linolenat termasuk asam lemak tak
jenuh, jika asam lemak terlepas dari trigliseridanya maka akan menjadi lemak
asam bebas (free fatty acids = FFA). Minyak nabati sebagai bahan baku
pembuatan biodiesel dapat dikelompokkan menjadi tiga jenis berdasarkan
kandungan FFA (Kinast, J. A., 2003) yakni Refined Oil, minyak nabati dengan
kandungan FFA kurang dari 1,5%, minyak nabati dengan kandungan FFA rendah
kurang dari 4%, minyak nabati dengan kandungan FFA tinggi lebih dari 20%.
Berdasarkan kandungan FFA dalam minyak nabati maka proses pembuatan
biodiesel dapat dibedakan atas dua bagian yaitu:
1. Transesterifikasi dengan menggunakan katalis basa untuk refined Oil
atau minyak nabati dengan kandungan FFA rendah.
2. Esterifikasi dengan katalis asam untuk minyak nabati dengan
kandungan FFA yang tinggi di lanjutkan dengan transesterifikasi
dengan katalis basa.
Dari hasil uji Gascromatografi (GC) terhadap minyak kacang tanah yang
digunakan sebagai bahan baku untuk menghasilkan biodiesel diperoleh
kandungan asam lemak bebas (FFA) 0,58 lebih kecil dari 1,5%, berdasarkan
kandungan FFA maka untuk memperoleh biodiesel turunan minyak kacang tanah
dapat dilakukan dengan proses transesterifikasi dengan katalis basa.
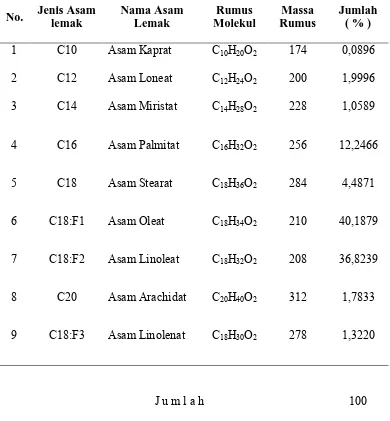
Minyak kacang tanah mengandung asam lemak jenuh dengan komposisi sebagai berikut tabel dibawah ini.
Tabel 2.2 Jenis Asam Lemak Yang Terkandung Dalam Minyak Kacang Tanah
Nama asam Struktur %
Proses produksi biodiesel dari bahan baku minyak nabati berkadar FFA
yang rendah dengan metode transesterifikasi terdiri dari:
1. Pencampuran katalis dan metanol pada konsentrasi katalis antara
0,5-1 wt% dan 10-20 wt% metanol terhadap massa minyak nabati.
2. Pencampuran katalis dan metanol dengan minyak pada temperatur
55-65 oC dengan kecepatan pengadukan yang konstan.
3. Setelah reaksi berhenti, campuran didiamkan sehingga terjadi
pemisahan metil ester dengan gliserol.
4. Pencucian metil ester dengan menggunakan air hangat untuk
memisahkan zat-zat pengotor seperti sisa metanol, sisa katalis,
gliserol, dan sabun, kemudian dilanjutkan dengan drying untuk
menguapkan air yang terkandung dalam biodiesel (Hambali, E., 2008).
Minyak kacang tanah sebelum dimasukkan kedalam reaktor terlebih dahulu
tersebut adalah biodiesel yang masih memerlukan prosses pencucian dan
pemurnian sehingga diperoleh biodiesel yang memenuhi syarat sebagai bahan
bakar. Proses pembuatan biodiesel turunan minyak kacang tanah dapat dilihat
pada diagram berikut ini:
Biji
kacang tanah
Ekstraksi kacang
tanah
Rotavapour hasil ekstraksi
Minyak kacang tanah
Titrasi/GC
Katalis
KOH/CaO
Gambar 2.1 Proses Pembuatan Biodiesel Turunan Minyak Kacang Tanah
Gliserol Biodiesel Pemurnian
biodiesel
FAME
Cosolvent Eter
Reaktor
Pencucian
2.4 STANDART BIODIESEL DI INDONESIA
Biodiesel yang dihasilkan diuji apakah memenuhi standart (Kualitas) yang
sudah dibakukan dalam SNI -04-7182-2006, yang telah disahkan dan diterbitkan
oleh Badan Standarisasi Nasional (BSN) tanggal 22 Pebruari 2006 berlaku di
Indonesia seperti tabel dibawah ini:
Tabel 2.3Persyaratan Kualitas Biodiesel Menurut SNI-04-7182-2006
Parameter dan satuannya
Batas nilai Metode uji Metode
setara
Massa jenis pada 40 oC, kg/m3 850 – 890 ASTM D 1298 ISO 3675
Viskositas kinematik pada 40
o
C, mm2/s (cSt)
2,3 – 6,0 ASTM D 445 ISO 3104
Angka setana min. 51 ASTMD 613 ISO 5165
Titik nyala (mangkok tertutup),
o - dalam contoh asli
- dalam 10% ampas distilasi
Maks. 0,05 (maks 0,03)
ASTM D 4530 ISO 10370
Air dan sedimen, %-vol. maks. 0,05 ASTM D 2709 -
Temperatur distilasi 90%, oC maks. 360 ASTM D 1160 -
Abu tersulfatkan, %-berat maks. 0,02 ASTM D 874 ISO 3987
Belerang, ppm-b (mg/kg) maks. 100 ASTM D 5453 Pr EN ISO
20884
Fosfor, ppm-b (mg/kg) maks. 10 AOCS Ca 12-55 FBI-A05-03
Angka asam, mg-KOH/g maks. 0,8 AOCS Cd 3-63 FBI-A01-03
Gliserol bebas, %-berat maks. 0,02 AOCS Ca 14-56 FBI-A02-03
Gliserol total, %-berat maks. 0,24 AOCS Ca 14-56 FBI-A02-03
Kadar ester alkil, %-berat Min. 96,5 Dihitung *) FBI-A03-03
Angka iodium, g-I
2/(100 g) maks. 115 AOCS Cd 1-25 FBI-A04-03
Uji Halphen Negative AOCS Cb 1-25 FBI-A06-03
2.5 KATALIS
Katalis adalah suatu zat yang mempercepat suatu laju reaksi dan
menurunkan energi aktivasi, namun zat tersebut tidak habis bereaksi. Ketika
reaksi selesai, kita akan mendapatkan massa katalis yang sama seperti pada awal
kita tambahkan. Zat yang menghambat berlangsungnya reaksi disebut inhibitor.
Dalam suatu reaksi kimia, katalis tidak ikut bereaksi secara tetap sehingga
dianggap tidak ikut bereaksi. Secara umum, katalis yang digunakan dalam reaksi
kimia ada tiga jenis, yaitu katalis homogen, katalis heterogen, biokatalis(Enzim),
dan Autokatalis.
2.5.1 Katalis Homogen
Adalah katalis yang wujudnya sama dengan wujud reaktannya. Dalam
reaksi kimia, katalis homogen berfungsi sebagai zat perantara (fasilitator).
Beberapa jenis katalis homogen yang telah digunakan antara lain NaOH, KOH,
ZA, ZA kering, ZKOH, dan Z-KOH kering terjadi reaksi dibawah ini:
R-COOH + NaOH RCOONa + H2O
Gambar 2.2 Reaksi Transesterifikasi Dengan Katalis Homogen
Penggunaan katalis ini mempunyai kekurangan seperti sifat korosif yang tinggi
dan katalis ini tidak mungkin digunakan kembali sehingga dalam proses
pembuatan metil ester ini NaOH dibuang dalam bentuk larutan dan mengganggu
2.5.2 Katalis Heterogen
Adalah katalis yang wujudnya berbeda dengan wujud reaktannya. Reaksi
zat-zat yang melibatkan katalis jenis ini, berlangsung pada permukaan katalis
tersebut. Reaksi fase gas dan fase cair dikatalisa oleh katalis heterogen biasanya
lebih mungkin terjadi di permukaan katalis dari pada di fase gas atau fase cair.
Untuk alasan ini maka kadangkala katalis heterogen disebut katalis kontak.
Beberapa jenis katalis heterogen yang telah dilaporkan antara lain CaO, MgO.
Proses katalis heterogen sedikitnya dapat melalui 4 tahap yakni:
1. Difusi produk dari permukaan katalis
2. Reaksi reaktan yang diserap
3. Aktivasi penyerapan reaktan
4. Adsorpsi reaktan pada permukaan katalis
Reaksi transesterifikasi dengan menggunakan katalis heterogen (CaO) seperti
dibawah ini:
2.5.3 Biokatalis (Enzim)
Adalah katalis yang memiliki keunggulan sifat (aktivitas tinggi,
selektivitas dan spesifitas) sehingga dapat dapat membantu proses–proses kimia
kompleks pada kondisi lunak dan ramah lingkungan. Kelemahannya antara lain
sangat mahal, sering tidak stabil, mudah terhambat, tidak dapat diperoleh kembali
setelah dipakai. Salah satu Biokatalis yang telah dilaporkan penggunaanya
adalah Enzim lipase (Triacylglycerol Acllydrolases).
Enzim lipase atau enzim pemecah lemak dipakai dalam reaksi pembuatan
biodiesel. Enzim itu dapat mengatalisis, menghidrolisis, serta menyintesis bentuk
ester dari gliserol dan asam lemak rantai panjang seperti halnya minyak goreng
dan jelantah. Berbeda dengan katalis soda api yang masih menghasilkan limbah,
katalis enzim tidak menghasilkan limbah. Pasalnya, dengan menggunakan enzim
lipase, asam lemak bebas akan larut dan menjadi biodiesel. “Yang diperlukan
hanya menyaring kotoran-kotoran berupa kerak yang sering ada, khususnya pada
minyak jelantah”, (Luthfi, 2009). Untuk membuat biodiesel dengan katalis enzim
lipase, hal yang harus dilakukan pertama kali adalah menyiapkan enzim lipase ke
dalam sebuah penampang berupa membrane tertentu. Dengan menggunakan dua
filter lipase sebagai katalisnya. Filter pertama digunakan untuk menyaring 60
persen kotoran, dan sisa kotoran yang sebanyak 40 persen disaring oleh filter
kedua. Alhasil, total kotoran yang berhasil disaring mencapai 100 persen “Enzim
ditempelkan pada filter”. Ketika minyak lewat, berarti telah menjadi biodiesel.
Sekarang ini harga enzim masih berkisar satu juta hingga tiga juta rupiah per
kilogram. Untuk filter berukuran satu meter persegi, dibutuhkan tiga gram enzim .
2.5.4 Autokatalis.
Adalah zat hasil reaksi yang berfungsi sebagai katalis. Artinya, produk
reaksi yang terbentuk akan mempercepat reaksi kimia. Reaksi antara kalium
berupa senyawa mangan sulfat (MnSO4). Semakin lama, laju reaksinya akan
semakin cepat karena MnSO4 yang terbentuk berfungsi sebagai katalis.
2KMnO4(aq) + 5H2C2O4(aq) + 3H2SO4(aq) 2MnSO4(aq) + 10CO2(g) + K2SO4(aq) + 8H2O(l)
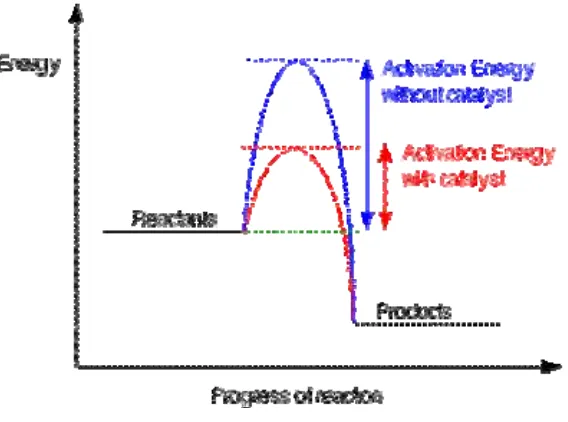
Untuk meningkatkan laju reaksi kita perlu untuk meningkatkan jumlah
tumbukan-tumbukan yang menghasilkan reaksi. Salah satu cara yang efektif adalah dengan
menurunkan energi aktivasi. Penambahan katalis dapat menurunkan energi
aktivasi. Suatu reaksi eksoterm AB(g) + C(g) --> AC(g) + B(g). Reaksi ini
berlangsung lambat, karena energi aktivasinya (Ea) lebih besar dibanding energi
molekulnya. Hanya sebagian kecil molekul yang mencapai Ea.
Gambar 2.4 Perubahan Energi Aktivasi Setelah Menggunakan Katalis
Berdasarkan diagram di atas, Ea' dengan katalis lebih rendah. Katalis itu berupa
zat yang dicampurkan dengan reaktan. Jika reaksi di atas tanpa katalis, AB dan C
bertumbukan sampai mencapai Ea yang relatif tinggi. Karena umumnya energi
molekulnya rendah, jadi tumbukan yang terjadi tidak efektif. Ea sangat sulit
dicapai. Untuk itu maka ditambahkan zat yang bertindak sebagai katalis.
Ternyata pada saat katalis dicampurkan reaksi makin cepat. Jelas bahwa katalis itu
sifatnya dengan AB. Maka seperti robot AB tertarik ke katalis membentuk KAB.
KAB tergolong kompleks teraktivasi yang merupakan tahap reaksi hipotesis;
KAB kemudian terurai menjadi KA dan B. Setelah itu terjadi tahap reaksi
berikutnya, yaitu C ditarik oleh KA menjadi KAC yang kemudian langsung K
lepas dan terbentuklah AC.
Mekanisme reaksi di atas adalah:
K + AB --> KAB --> KA + B (lambat)
KA + C --> KAC --> K + AC (cepat)
K+AB+C-->K+AC+B
Jadi katalis ikut ambil bagian dalam reaksi, memberi jalan baru melalui
mekanisme reaksi baru yang energi aktivasinya lebih rendah, kemudian terbentuk
kembali dalam keadaan yang sama. Katalis dapat berfungsi sebagai zat perantara
maupun sebagai zat pengikat.
2.5.4.1 Katalis sebagai zat parantara
Perhatikan contoh berikut ini:
Reaksi tanpa katalis: A+B ---> AB (lambat)
Reaksi dengan katalis: A+B ---> AB (cepat)
Mekanisme reaksi dapat dijelaskan sebagai berikut:
B + K ---> BK
BK+A ---> A-B-K
A-B-K ---> A-B +K
Dengan terikatnya zat B pada katalis, senyawa B-K yang terbentuk menjadi lebih
reaktif ketika bereaksi dengan A sehingga terbentuk senyawa AB-K. Pada tahap
berikutnya, dihasilkan senyawa AB dan katalis K diperoleh kembali dalam
jumlah yang sama seperti semula. Jadi, katalis ikut bereaksi, namun pada akhir
2.5.4.2 Katalis sebagai zat pengikat
Katalis yang berfungsi sebagai zat pengikat, yaitu logam-logam seperti Pt,
Cr, dan Ni. Permukaan logam-logam ini memiliki kemampuan mengikat zat yang
akan bereaksi sehingga terbentuk spesi yang reaktif. Logam-logam ini
mempercepat reaksi-reaksi gas dengan cara membentuk ikatan lemah antara gas
dan atom-atom logam pada permukaan, proses ini disebut adsorpsi. Gas-gas yang
terikat pada permukaan logam lebih mudah bereaksi dibandingkan jika gas-gas
tersebut berada di udara. Setelah terjadi reaksi, produk hasil reaksi melepaskan
ikatannya dengan permukaan logam, proses ini disebut dengan desorpsi.
Katalis hanya mempengaruhi laju mencapaian kesetimbangan, tidak berpengaruh
dalam hasil reaksi dan konsentrasi atau massa zat setelah reaksi. Jumlah katalis
setelah reaksi berlangsung akan sama dengan jumlah katalis sebelum terjadinya
reaksi.
2.6 ALKOHOL
Kekentalan minyak nabati dapat dikurangi dengan memotong cabang
rantai carbon dengan proses transesterifikasi dengan menggunakan alkohol rantai
pendek. Alkohol yang biasa digunakan adalah metanol dan etanol. Metanol
merupakan jenis alkohol yang paling disukai dalam pembuatan biodiesel karena
metanol (CH3OH) mempunyai keuntungan lebih mudah bereaksi atau lebih stabil
dibandingkan dengan etanol (C2H5OH) karena metanol memiliki satu ikatan
karbon sedangkan etanol memiliki dua ikatan karbon, sehingga lebih mudah
memperoleh pemisahan gliserol dibanding dengan etanol, untuk mendapatkan
hasil biodiesl yang sama penggunaan etanol 1,4 kali lebih banyak dibanding
dengan metanol. Kerugiannya metanol merupakan zat beracun dan berbahaya bagi
kulit, mata, paru-paru dan pencernaan dan dapat merusak plastik dan karet terbuat
dari batu bara. Metanol berwarna bening seperti air, mudah menguap, mudah
terbakar dan mudah bercampur dengan air. Etanol lebih aman, tidak beracun dan
terbuat dari hasil pertanian, etanol memiliki sifat yang sama dengan metanol yaitu
bercampur dengan air. Pemisahan gliserin dengan menggunakan etanol lebih sulit
dari metanol dan jika tidak berhati-hati akan berakhir dengan emulsi. Metanol dan
etanol yang dapat digunakan hanya yang murni 99%. Metanol memiliki massa
jenis 0,7915 g/m3 dan titik didih 65 oC, sedangkan etanol memiliki massa jenis
0,79 g/m3 dan titik didih 79 oC.
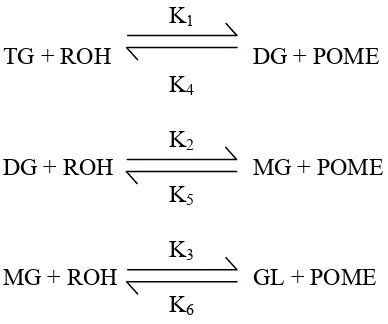
2.7 REAKSI TRANSESTERIFIKASI
Transeseterifikasi adalah proses yang mereaksikan trigliserida dalam
minyak nabati atau lemak hewani dengan alkohol rantai pendek hingga
menghasilkan metal ester asam lemak (Fatty Acids Methyl Esters = FAME) atau
biodiesel dan gliserol sebagai produk samping. Reaksi transesterifikasi
diperlihatkan pada gambar 2.1, proses ini akan dapat berlangsung dengan
mengunakan katalis alkali/basa pada tekanan 1 atmosfer temperatur 65 oC dengan
menggunakan Alkohol, katalis yang biasa digunakan adalah Kalium Hidroksida
atau Natrium Hidroksida. Proses transesterifikasi meliputi: Katalis basa (KOH)
dicampur dengan alkohol (metanol) dan minyak nabati dengan perbandingan
katalis basa 1% dari minyak nabati sedangkan perbandingan molar antara metanol
dengan minyak nabati adalah 1:6 dengan kadar asam lemak bebas (FFA) di bawah
1% untuk mengasilkan rendemen yang maksimum (Darnoko, D., 2000).
Fartor-faktor yang mempengaruhi reaksi transesterifikasi:
1. Pengaruh air dan kandungan asam lemak bebas
Minyak nabati yang akan ditransesterifikasi harus bebas air, karena air
akan bereaksi dengan katalis sehingga jumlah katalis akan berkurang,
dan harus memiliki angka asam lemak bebas < 1.
2. Perbandingan molar alkohol dengan minyak nabati
Secara stoikiometri jumlah alkohol yang dibutuhkan untuk reaksi 3 mol
mol gliserol. Semakin banyak jumlah alkohol yang digunakan maka
konversi ester yang dihasilkan akan bertambah banyak dan pada rasio
molar 1:6 setelah 1 jam konversi yang dihasilkan 98-99%, sedangkan
pada rasio molar 1:3 adalah 74-89%. Maka rasio molar yang terbaik
adalah 1:6 karena dapat menghasilkan rendemen yang optimum.
3. Katalis
Katalis berfungsi untuk mempercepat reaksi dan menurunkan energi
aktiviasi sehingga reaksi dapat berlangsung pada suhu kamar sedangkan
tanpa katalis reaksi dapat berlangsung pada suhu 250 oC, katalis yang
biasa digunakan dalam reaksi transesterifikasi adalah katalis basa
seperti Kalium Hodroksida dan Natrium Hidroksida. Reaksi
transesterifikasi dengan katalis basa akan menghasilkan konversi
minyak nabati menjadi ester yang optimum (94-99%) dengan jumlah
katalis 0,5–1,5% wt minyak nabati. Jumlah katalis KOH yang efektif
untuk menghasilkan konversi yang optimum pada reaksi
transesterifikasi adalah 1% wt minyak nabati (Darnoko, D., 2000).
4. Suhu
Suhu mempengaruhi kecepatan reaksi transesterifikasi dalam
pembentukan biodiesel. Pada umumnya reaksi transesterifikasi
dilakukan pada suhu 60–65 oC pada tekanan atmosfer. Kecepatan
reaksi akan meningkat sejalan dengan kenaikan temperatur yang berarti
semakin banyak energi yang dapat digunakan reaksi untuk mencapai
energi aktivasi sehingga akan menyebabkan semakin banyak tumbukan
5. Lama Reaksi
Semakin lama waktu reaksi semakin banyak eter yang dihasilkan
karena situasi ini akan memberikan kesempatan terhadap
molekul-molekul reaktan untuk semakin lama bertumbukan.
6. Pengadukan
Pengadukan dilakukan dengan tujuan untuk menghasilkan campuran
yang homogen antara gliserida dan alkohol pada saat terjadi reaksi
transesterifikasi.
2.8 SIFAT – SIFAT PENTING DARI BIODIESEL
2.8.1 Massa Jenis ( Densitas )
Kerapatan suatu fluida (ρ) dapat didefinisikan sebagai massa persatuan
volume.
v
m
=
ρ
(2.1)Dengan: ρ = rapat massa (kg/m3)
m = massa (kg)
v = volume (m3)
Yang mempengaruhi densitas adalah faktor gliserol yang terdapat dalam metil
ester (FAME). Semakin besar kadar densitas menunjukkan bahwa proses
pencucian dan pemurnian kurang sempurna dilakukan. Densitas dari suatu FAME
sebanding dengan viskositas, artinya semakin besar densitasnya semakin besar
2.8.2 Viskositas
Viskositas (kekentalan) merupakan sifat intrinsik fluida yang menunjukkan
resistensi fluida terhadap aliran. Hubungan antara tegangan geser dinding dengan
viskositas untuk fluida Newton bisa dilihat pada persamaan berikut ini:
(
)
y oW
=
∂
u
/
∂
y
=τ
(2.2)Dengan: µ = kekentalan dinamik (Poise)
τ = tegangan geser fluida (Newton/m 2 )
∂u = kecepatan relatif kedua permukaan (m/s)
∂y = tebal lapisan filem fluida (m)
Sedangkan hubungan antara tegangan geser dinding dengan penurunan tekanan
(pressure drop) adalah sebagai berikut:
(2.3) Dengan: D = diameter pipa (m)
∆p = penurunan tekanan (Pa)
L = panjang pipa yang ditinjau (m)
Dari Persamaan diatas dapat dilihat bahwa viskositas fluida berpengaruh langsung
terhadap besarnya penurunan tekanan yang dialami oleh fluida tersebut.
Penurunan tekanan (pressure drop) fluida berkaitan dengan energi pengaliran
fluida sebagai berikut:
(2.4)
Dengan: P = daya (Watt)
Q = debit fluida (m3/s)
Persamaan–persamaan diatas menunjukkan bahwa fluida dengan viskositas tinggi
lebih sulit untuk dialirkan dibandingkan dengan fluida dengan viskositas rendah.
akan mengalir dengan kecepatan lebih rendah. Gesekan yang terjadi didalam
bagian cairan yang berpindah dari suatu bahan ke bahan lain mempengaruhi
pengontrolan bahan bakar dengan injeksi ke ruang pembakaran, Akibatnya
terbentuk endapan pada mesin (Knothe, G., 2005).
Kecepatan alir bahan bakar melalui injektor akan mempengaruhi derajat atomisasi
bahan bakar di dalam ruang bakar. Viskositas bahan bakar juga berpengaruh
secara langsung terhadap kemampuan bahan bakar tersebut bercampur dengan
udara. Visikositas yang tinggi cenderung menjadi masalah dari bahan bakar, dan
ini menjadi salah satu faktor yang menentukan dalam produksi dan pemakaian
biodiesel. Tingginya harga viskositas SVO (straight vegetable oil) atau refined
fatty oil yang mendasari perlu dilakukannya proses kimia, transesterifikasi, untuk
menurunkan harga viskositas minyak tumbuhan sehingga mendekati viskositas
solar.
Dengan demikian, viskositas bahan bakar yang tinggi, seperti yang terdapat pada
SVO, tidak diharapkan pada bahan bakar mesin diesel. Oleh karena itulah
penggunaan SVO secara langsung pada mesin diesel menuntut digunakannya
mekanisme pemanas bahan bakar sebelum memasuki sistem pompa dan injeksi
bahan bakar. Untuk menjamin bahan bakar dapat bercampur baik dengan udara
dan selanjutnya siap terbakar, maka diperlukan proses atomisasi yang baik pula.
2.8.3 Titik Kabut
Suhu yang dingin menyebabkan titik-titik kristal seperti lilin yang
ukurannya sangat kecil tidak dapat dilihat mata. Penurunan temperatur yang lebih
jauh akan membentuk kristal. Temperatur pada saat terjadi kristal yang dapat
dilihat dengan mata disebut titik kabut (cloud point). Meski bahan bakar masih
bisa mengalir pada titik ini, keberadaan kristal di dalam bahan bakar bisa
mempengaruhi kelancaran aliran bahan bakar di dalam filter, pompa, dan injektor.
Sedangkan pour point adalah temperatur terendah yang masih memungkinkan
mengalir karena terbentuknya kristal/gel yang menyumbat aliran bahan bakar.
Pada umumnya permasalahan pada aliran bahan bakar terjadi pada temperatur
diantara cloud dan pour point; pada saat keberadaan kristal mulai mengganggu
proses filtrasi bahan bakar. Dilihat dari definisinya, cloud point terjadi pada
temperatur yang lebih tinggi dibandingkan dengan pour point. Pembentukan
kristal umumnya akan membentuk suspensi agak berkabut, temperatur dibawah
cloud point terbentuk kristal lebih besar.
Pada umumnya, cloud dan pour point biodiesel lebih tinggi dibandingkan dengan
solar. Hal ini bisa menimbulkan masalah pada penggunaan biodiesel, terutama, di
negara-negara yang mengalami musim dingin. Untuk mengatasi hal ini, biasanya
ditambahkan aditif tertentu pada biodiesel untuk mencegah aglomerasi
kristal-kristal yang terbentuk dalam biodiesel pada temperatur rendah. Selain
menggunakan aditif, bisa juga dilakukan pencampuran antara biodiesel dan solar.
Pencampuran (blending) antara biodiesel dan solar terbukti dapat menurunkan
cloud dan pour point bahan bakar.
Teknik lain yang bisa digunakan untuk menurunkan cloud dan pour point bahan
bakar adalah dengan melakukan “winterization” (Knothe,G., 2005). Pada metode
ini, dilakukan pendinginan pada bahan bakar hingga terbentuk kristal-kristal yang
selanjutnya disaring dan dipisahkan dari bahan bakar. Proses kristalisasi parsial ini
terjadi karena asam lemak tak jenuh memiliki titik beku yang lebih rendah
dibandingkan dengan asam lemak jenuh. Maka proses winterization sejatinya
merupakan proses pengurangan asam lemak jenuh pada biodiesel. Di sisi lain,
asam lemak jenuh berkaitan dengan angka setana. Maka proses winterization bisa
menurunkan angka setana bahan bakar.
Namun demikian, karakteristik biodiesel pada temperatur rendah ini tidak terlalu
menjadi masalah untuk negara dengan temperatur tinggi sepanjang tahun, seperti
2.8.4 Angka Iodium
Asam lemak yang tidak jenuh dalam minyak, mampu menyerap sejumlah
iod dan membentuk senyawa yang jenuh. Besarnya jumlah iod yang diserap
menunjukkan banyaknya ikatan rangkap atau ikatan tak jenuh (Ketaren, S., 2006).
Angka iodium pada biodiesel menunjukkan tingkat ketidakjenuhan senyawa
penyusun biodiesel. Naiknya ketidakjenuhan metil ester dapat meningkatkan
emisi gas NOX , sehingga makin tnggi angka iod makin tinggi gas NOX yang
dihasilkan.
Di satu sisi, keberadaan senyawa lemak tak jenuh meningkatkan performansi
biodiesel (angka setana) pada temperatur rendah, karena senyawa ini memiliki
titik leleh (melting point) yang lebih rendah (Knothe, G., 2005) sehingga
berkorelasi pada cloud dan pour point yang juga rendah. Namun di sisi lain,
banyaknya senyawa lemak tak jenuh di dalam biodiesel memudahkan senyawa
tersebut bereaksi dengan oksigen di atmosfer dan.bisa terpolimerisasi membentuk
material serupa plastik. Oleh karena itu, terdapat batasan maksimal harga angka
iod yang diperbolehkan untuk biodiesel, yakni 115 berdasarkan kualitas biodiesel
menurut SNI-04-7182-2006. Di samping itu, konsentrasi asam linolenic dan asam
yang memiliki 4 ikatan ganda masing-masing tidak boleh melebihi 12 dan 1%.
Sebuah penelitian yang dilakukan di Mercedez-Benz menunjukkan bahwa
biodiesel dengan angka iodine lebih dari 115 tidak bisa digunakan pada kendaraan
diesel karena menyebabkan deposit karbon yang berlebihan. Meski demikian,
terdapat studi lain yang menghasilkan kesimpulan bahwa angka iodine tidak
berkorelasi secara signifikan terhadap kebersihan dan pembentukan deposit di
dalam ruang bakar.
2.8.5 Kadar Air
Kadar air menunjukkkan persentase air yang terkandung dalam bahan
bakar. Schindlbauer (1998) menyebutkan bahwa fattty Acid Methyl Esters
terlarut sempurna dengan biodiesel. Pada temperatur yang sangat dingin, air yang
terkandung dalam bahan bakar membentuk kristal dan menyumbat aliran bahan
bakar dan bersifat korosif. Kadar air tinggi yang terdapat pada biodiesel diduga
bahwa reaksi transesterifikasi dan proses pencucian masih belum sempurna. Pada
saat penyimpanan akan menimbulkan reaksi balik kekiri atau dengan kata lain
BAB III
METODE PENELITIAN METODE PENELITIAN
3.1 TEMPAT DAN WAKTU PENELITIAN 3.1 TEMPAT DAN WAKTU PENELITIAN
a. Penelitian dilakukan di Laboratorium Kimia Anorganik USU,
Laboratorium Perusahaan Swasta dan Laboratorium PPKS Medan.
a. Penelitian dilakukan di Laboratorium Kimia Anorganik USU,
Laboratorium Perusahaan Swasta dan Laboratorium PPKS Medan.
b. Penelitian ini dilaksanakan dari bulan Januari sampai Mei 2010. b. Penelitian ini dilaksanakan dari bulan Januari sampai Mei 2010.
3.2 BAGAN PENELITIAN 3.2 BAGAN PENELITIAN
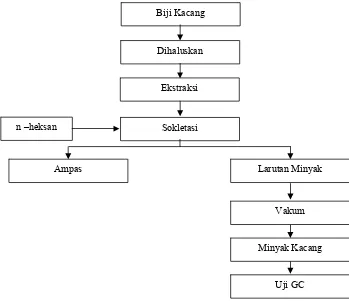
3.2.1 Pembuatan Minyak Kacang 3.2.1 Pembuatan Minyak Kacang
Untuk mendapatkan minyak kacang tanah dari biji kacang tanah dilakukan
seperti bagan dibawah ini:
Untuk mendapatkan minyak kacang tanah dari biji kacang tanah dilakukan
seperti bagan dibawah ini:
Ampas Larutan Minyak
Vakum
Minyak Kacang
Uji GC Biji Kacang
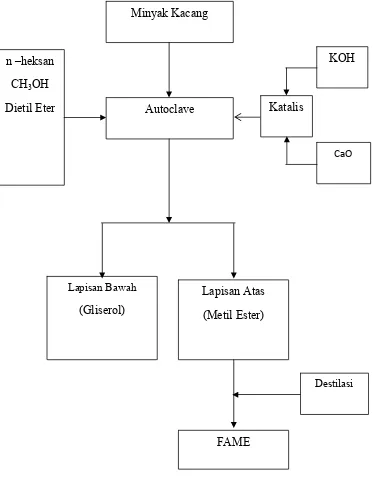
3.2.2 Pembuatan FAME
Minyak kacang tanah yang diperoleh, kemudian dilakukan transesterifikasi
untuk mendapatkan FAME seperti bagan dibawah ini:
udian dilakukan transesterifikasi
untuk mendapatkan FAME seperti bagan dibawah ini:
Minyak Kacang
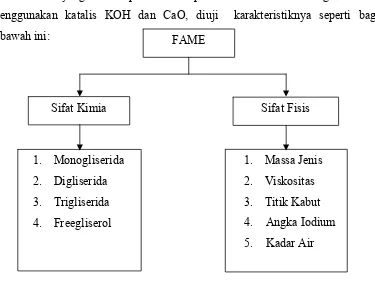
3.2.3 Uji Karakteristik FAME
FAME yang telah diperoleh dari proses transesterifikasi trigliserida dgn
menggunakan katalis KOH dan CaO, diuji karakteristiknya seperti bagan
dibawah ini:
Sifat Kimia Sifat Fisis
1. Monogliserida
2. Digliserida
3. Trigliserida
4. Freegliserol
1. Massa Jenis
2. Viskositas
3. Titik Kabut
4. Angka Iodium
5. Kadar Air FAME
3.3PEMBUATAN MINYAK KACANG TANAH
3.3.1 Alat dan Bahan
a. Alat yang dibutuhkan:
- Blender - Termometer
- Soxhlet apparatus - Alat Rotavapour
- Tungku pemanas - Corong
- Statif - Neraca
- Gelas labu - Gelas ukur
b. Bahan yang diperlukan:
- Kacang tanah (Aleurites moluccana) sebagai bahan baku dari
biodiesel
- n-Heksan
- Kertas saring
3.3.2 Prosedur Kerja:
a. Kacang tanah yang telah kering di giling hingga halus dengan
menggunakan blender.
b. Kacang yang telah halus dibungkus dengan kertas saring lalu
dimasukkan kedalam alat sokletasi.
c. Isi gelas labu dengan n-heksan ± 250 ml, letakkan diatas pemanas
d. Hubungkan alat pemanas dengan sumber arus listrik, biarkan ±3
jam, atau tetesan n-heksan dan minyak tidak lagi keruh (dari soklet
ke gelas labu).
e. Putuskan hubungan listrik alat pemanas dengan sumber arus listrik,
Biarkan hingga dingin.
f. Tuang campuran minyak dan n-heksan kedalam wadah lain.
g. Ulangi cara diatas dengan sampel yang lain.
h. Setelah diperoleh 8 liter lalu di rotavapour, Untuk memisahkan
minyak kacang tanah dari n-heksan (lampiran B gambar 2).
i. Minyak kacang tanah yang diperoleh kemudian di uji GC untuk
mengetahui kandungan asam lemak bebas (FFA).
3.4 PROSES PEMBUATAN BIODIESEL DENGAN MENGGUNAKAN
KATALIS KOH DAN COSOLVENT ETER
3.4.1 Alat dan Bahan
a. Alat yang dibutuhkan:
- Labu leher tiga - Corong
- Gelas Ukur - Neraca
- Pompa Vakum - Hotplate Stirer
- Reaktor - Autoclave
- Corong Pemisah - Termometer
b. Bahan yang diperlukan:
- Minyak kacang tanah - Kertas Saring
- KOH - Kertas Lakmus
- Metanol - Eter
- HCl4 - n-heksan
- Na2SO4 - Aquades
3.4.2 Prosedur Kerja
a. Menentukan jumlah Metanol, katalis KOH dan Eter
Dalam reaksi transesterifikasi untuk mendapatkan jumlah biodiesel
yang maksimal perbandingan molar metanol terhadap minyak
nabati 1:12 dan konsentrasi katalis 0,5%-1,5% wt, massa minyak
kacang tanah ditimbang dengan neraca sebanyak 884,0 gr (1 mol),
massa metanol 384,0 gr (12 mol), Jumlah katalis 1,5% wt = 13,2
gr, dan eter sebanyak 200 ml.
b. Mencampurkan katalis KOH dengan Metanol
Katalis KOH dalam bentuk padat dilarutkan kedalam metanol, lalu
diaduk selama lebih kurang 15 menit dengan tujuan agar KOH dan
Metanol membetuk potassium methoxide (K2OCH3) kemudian
dimasukkan kedalam Autoclave.
c. Mencampur minyak kacang tanah, potassium methoxide dan eter
Minyak kacang tanah, potasuim methoxide, eter dimasukkan
kedalam autoclave, lalu reaktor dipanaskan didalam oilbath pada
suhu 65 oC dan campuran diaduk dengan menggunakan Hotplate
Stirer dengan kecepatan pengadukan 2700 rpm selama 3 jam
(lampiran B gambar 3).
d. Hasil transesterifikasi dimasukkan kedalam labu leher tiga,
kemudian didiamkan terlihat ada 3 lapisan yang terbentuk
(lampiran B gambar 4). Lapisan atas merupakan metil ester, lapisan
bawah merupakan gliserol dan kotoran.
e. Proses pencucian
• Campuran dikeluarkan dari Autoclave dimasukkan kedalam labu leher tiga, pH-nya diukur dengan menggunakan kertas
diturunkan dengan menggunakan cairan HCL4–normal
sebanyak 67 ml hingga pH campuran = 7 (lampiran B
gambar 5).
• Jika pH campuran telah diperoleh 7, Campuran dimasukkan kedalam corong pisah ditambahkan aquades untuk proses
pencucian.
• Pada saat proses pencucian didalam corong pisah, Campuran diaduk kemudian didiamkan hingga terjadi pemisahan antara
biodiesel dengan gliserol, lapisan atas biodesel, lapisan bawah
gliserol bercampur air (lampiran B gambar 6).
f. Proses pemisahan biodiesel dengan gliserol
• Kedalam corong pisah ditambahkan lagi n-hexana dengan tujuan agar zat-zat yang terlarut dan gliserol berpisah secara
sempurna dengan biodesel.
• Gliserol dikeluarkan dari corong pisah
• Biodiesel dimasukkan kedalam gelas ukur lalu kedalamnya dimasukkan Na2SO4 dengan tujuan untuk mengikat air yang
terdapat didalam biodesel, didiamkan selama 24 jam hingga
terbentuk serbuk putih didasar tabung reaksi (lampiran B
gambar 7).
• Serbuk Na2SO4 dipisahkan dari biodesel dengan menggunakan
kertas saring.
g. Proses pemurnian biodesel
Untuk memurnikan biodiesel dari n-hexana, metanol dan eter,
biodiesel didestilasi atau divakum selama 5 jam (lampiran B
h. Diperoleh biodiesel (FAME), hasil transesterifikasi minyak kacang
tanah dengan katalis KOH, lama reaksi 3 jam (lampiran B
gambar 9).
3.5 PROSES PEMBUATAN BIODIESEL DENGAN MENGGUNAKAN
KATALIS CaO DAN COSOLVENT ETER
b. Bahan yang diperlukan
- Minyak kacang tanah - Kertas Saring
3.5.2 Prosedur Kerja
a. Menentukan jumlah metanol, katalis CaO dan eter. CaO yang akan
digunakan sebagai katalis terlebih dahulu dikalsinasi pada suhu 600
o
C selama 2 jam, sehingga ketika katalis CaO dilarutkan di dalam
metanol akan terjadi reaksi:
CaO + CH3OH Ca(OCH3) + H2O
(Tobing, M., 2009)
1:12 dan konsentrasi katalis 8% wt, massa minyak kacang tanah
ditimbang dengan neraca sebanyak 884,0 gr (1 mol), massa
metanol 384,0 gr (12 mol), Jumlah katalis 8% wt = 70,72 gr,
dan eter sebanyak 200,0 ml.
• Kemudian autoclave dipanaskan didalam oilbath pada suhu tetap 65 oC dan diaduk dengan menggunakan Hotplate Stirer
selama 3 jam.
b. Proses pencucian
• Campuran dikeluarkan dari autoclave dimasukkan kedalam gelas ukur.
• Kemudian katalis CaO disaring dengan kertas saring, Untuk memisahkan metil ester dari Katalis CaO (lampiran B
gambar 10).
• Setelah katalis CaO disaring, pH campuran diukur dengan menggunakan kertas lakmus didapat pH = 11 (campuran
bersifat basa).
• Sifat basa ini diturunkan dengan menggunakan cairan HCL4
-normal hingga diperoleh pH campuran = 7.
c. Proses Pemisahan biodiesel dengan gliserol
• Kedalam corong pisah ditambahkan lagi n-Hexana dengan tujuan agar zat-zat yang terlarut dan gliserol berpisah secara
sempurna dengan biodesel (lampiran B gambar 11).
• Biodiesel dimasukkan kedalam gelas ukur lalu kedalamnya dimasukkan Na2SO4 dengan tujuan untuk mengikat air yang
terdapat didalam biodesel lalu didiamkan selama 24 jam hingga
terbentuk serbuk putih didasar tabung reaksi.
• Serbuk Na2SO4 dipisahkan dari biodesel dengan menggunakan
kertas saring (lampiran B gambar 12).
Untuk memurnikan biodiesel dari n-hexana, metanol dan eter ,
biodiesel didestilasi atau divakum selama 5 jam.
f. Diperoleh biodiesel (FAME), hasil transesterifikasi minyak kacang
tanah menggunakan katalis CaO, lama reaksi 3 jam (lampiran B
gambar 13).
3.6 PENGUJIAN MASSA JENIS (DENSITY)
Tujuan pengujian adalah untuk mengetahui massa jenis dari biodiesel
turunan kacang tanah.
3.6.1 Alat dan Bahan
- Piknometer - n-hexane
- Beaker glass - Water bath
- Asam kromat - Petroleum eter
- Alkohol - Kain lap
3.6.2 Prosedur Kerja
I. STANDARISASI
1. Cuci piknometer (kapasitas 50 ml) dengan asam kromat.
Bersihkan dan biarkan beberapa jam. Kosongkan piknometer dan
timbang, lalu bilas dengan aquades (lampiran B gambar 14).
2. Isi dengan aquades yang baru mendidih hingga penuh,
didinginkan sampai suhu 20 oC dan tempatkan pada waterbath
pada suhu 30 oC. Tunggu atau biarkan selama 30 menit. Setelah
30 menit atur posisi aquades pada tanda batas dan tutup.
3. Keluarkan dari waterbath, lap hingga kering dengan tissu dan
timbang (A).
4. Kosongkan piknometer, bilas beberapa kali dengan alkohol
kemudian petroleum eter, biarkan kering sempurna (sampai hilang
5. Hitung massa aquades pada suhu 30 oC (X) = (A - B) sebanyak 3
kali.
II. Densitas pada 30/30 oC
1. Isi piknometer yang telah kering dengan sampel hingga penuh
(yang telah di cairkan).
2. Tempatkan pada waterbath selama 30 menit pada suhu 30 oC.
3. Atur volume biodiesel sampai tanda batas dan tutup.
4. Angkat dari waterbath, lap dengan tissu dan keringkan.
Selanjutnya timbang (C) (lampiran B gambar 15).
5. Timbang massa piknometer kosong. Seperti halnya pada bagian I
(D). Massa jenis pada 30/30 oC (Apparent) dihitung berdasarkan
(C - D) / X, lakukan pengulangan sampai 3 kali.
III. Densitas pada 40/30 oC
1. Cara kerjanya hampir sama dengan cara kerja pada 30/30 oC,
Hanya setting suhu waterbath pada suhu 40 oC, Biarkan selama 30
menit dan dinginkan pada temperatur kamar.
2. Bersihkan botol sampai kering dengan lap atau tissue dan timbang
(lampiran B gambar 16).
3. Massa jenis sampel ditentukan pada suhu tertentu, maka massa
jenis pada 30/30 oC dihitung sebagai berikut:
G = G’ + 0,00064 ( T – 30 oC ) (3.1)
Dimana: G = Massa jenis pada 30/30 oC
G’ = Massa jenis pada T/30 oC
T = Suhu dimana massa jenis ditentukan pada 0,00064
adalah koreksi rata-rata untuk 1 oC