PERANCANGAN PROSES PRODUKSI SURFAKTAN NON IONIK
ALKIL POLIGLIKOSIDA (APG) BERBASIS PATI SAGU DAN
DODEKANOL SERTA KARAKTERISASINYA
PADA FORMULASI HERBISIDA
MOCHAMAD NOERDIN N.K.
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN SEKOLAH PASCASARJANA
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa Tesis Perancangan Proses Produksi Surfaktan Non Ionik Alkil Poliglikosida (APG) Berbasis Pati Sagu dan Dodekanol serta Karakterisasinya pada Formulasi Herbisida adalah karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir Tesis ini.
Bogor, Agustus 2008
ABSTRACT
MOCHAMAD NOERDIN N.K. Process Design of Non Ionic Alkyl Polyglicosides (APG) Surfactant Production from Sago Starch and Dodekanol and Its Characteristics on Herbicide Formulation. Under direction of ANI SURYANI and DADANG.
Alkyl poliglycosides (APG) are non ionic surfactant which is commonly used in some products like herbicides, personal care products, cosmetics and textile bleachings. APG is new generation of surfactant that is environmental friendly. Raw materials of APG are fatty alcohol from palm oil or palm kernel oil and carbohydrates like the strach, that make APG as biodegradable surfactant. The aim of research was to obtain non ionic surfactant alkyl polyglycosides (APG) based on sago starch and fatty alcohol C12 (dodekanol). This research is modification of production process of APG two steps method from Wuest, et al. (1992), in order to obtain optimum condition temperature of butanolysis and mol ratio of sago starch-dodecanol to emulsion stability (water : xylene), characterisisation of APG, herbicide formulation and its hebicide formulation effectiveness. Result of response surface, showed that emulsion stability (water:xylene) added APG (%) was 72.58% at temperature of butanolysis 147.8oC and at ratio of sago starch-dodekanol 1:3.27 (w/w). Result of validation showed that emulsion stability (water : xylene) with addtion of APG was 72.3%. Equation model of optimum condition was Y= 64.29 + 35.53X1 – 29.82X12 –
9.63x2 – 23.09X22 -20.56X1X2 which similar with experimental datas. APG at 1 % (w/v)
was able to decrease surface tension 23.375 dyne/cm and interfacial tension between water : xylene at APG concentration of 0.4% (w/v) was 8.17 dyne/cm. Value of HLB was 8.8 so that the catogorize of this surfactant emulsion of oil in water (O/W) and wetting agent. APG pH in optimum process condition was 7.15. Application of herbicide formulation (glyphosate and APG surfactant) that was stored five weeks at temperature of 150C, room temperatur (26-290C) and 400C showed high effectiveness. The storeage temperature was not significantly different on herbicide efectiveness.
RINGKASAN
MOCHAMAD NOERDIN N.K. Perancangan Proses Produksi Surfaktan Non Ionik Alkil Poliglikosida (APG) Berbasis Pati Sagu dan Dodekanol serta Karakterisasinya Pada Formulasi Herbisida. Di bimbing oleh ANI SURYANI dan DADANG
Surfaktan (surface active agent) merupakan senyawa aktif penurun tegangan permukaan yang pada umumnya diproduksi dari minyak bumi (petrokimia) dan minyak-lemak (oleokimia). Penggunaan oleokimia sebagai bahan baku surfaktan perlu pengembangan lebih lanjut karena beberapa kelebihan oleokimia jika dibandingkan petrokomia, diantaranya mudah terurai secara biologis dan dapat diperbaharui.
Alkil Poliglikosida (APG) merupakan surfaktan non ionik yang dapat digunakan pada formulasi beberapa produk seperti formulasi herbisida, produk-produk perawatan tubuh, produk kosmetik, dan pemucatan kain tekstil. Bahan baku APG adalah alkohol lemak dari oleokimia minyak kelapa atau minyak inti sawit dan karbohidrat dari sumber pati seperti kentang, jagung, dan sagu.
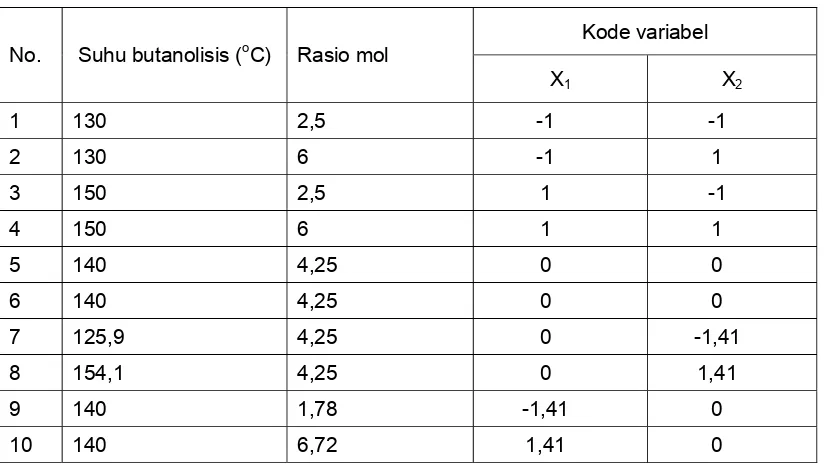
Penelitian ini bertujuan untuk memperoleh surfaktan non ionik APG yang berbasis pada pati sagu dan alkohol lemak C 12 (dodekanol). Penelitian ini mengkaji rancang proses produksi APG metode dua tahap, optimasi suhu proses butanolisis dan rasio mol pati sagu-dodekanol terhadap nilai kestabilan emulsi air:xilena, karakterisasi APG dan hasil formulasi dan efektivitas herbisidanya. Rancang proses produksi APG dilakukan dengan memodifikasi proses produksi dua tahap Wuest, et al. (1992) dengan merubah sumber patinya dari kentang menjadi pati sagu dan netralisasi mengganti MgO dengan NaOH, serta penggunaan 2 buah reaktor menjadi 1 buah reaktor. Rancangan percobaan yang digunakan untuk optimasi menggunakan metode permukaan respon dengan faktor rasio mol pati sagu – dodekanol = 1 : 2,5 sampai dengan 1 : 6 dan suhu proses butanolisis dari suhu 1300C sampai 1500C.
Rancangan percobaan optimasi sintesis APG menggunakan metode permukaan respon (Response Surface Method) dan penelitian menggunakan rancangan komposit terpusat. Faktor yang dianalisis ada dua yaitu suhu proses butanolisis (X1) dengan
rentang antara 130 – 150 °C dan rasio mol pati : alkohol lemak (X2) dengan rentang
antara 1:2,5 – 1:6. Sedangkan rancangan percobaan pada aplikasi formulasi herbisida hasil penyimpan adalah rancangan acak lengkap faktorial dengan 3 faktor dan dua kali ulangan. Faktor yang dikaji adalah variasi suhu penyimpanan yaitu suhu 15oC, suhu ruang (26-290C), dan suhu 40oC , variasi konsentrasi glifosat yaitu konsentrasi 16%, 24%
dan 48%, variasi konsentrasi surfaktan APG terdiri dari 4%, 6%, 8% dan 10%. Untuk pengujian efektivitas dengan skoring menggunakan statistik non parametrik uji Kruskal Wallis.
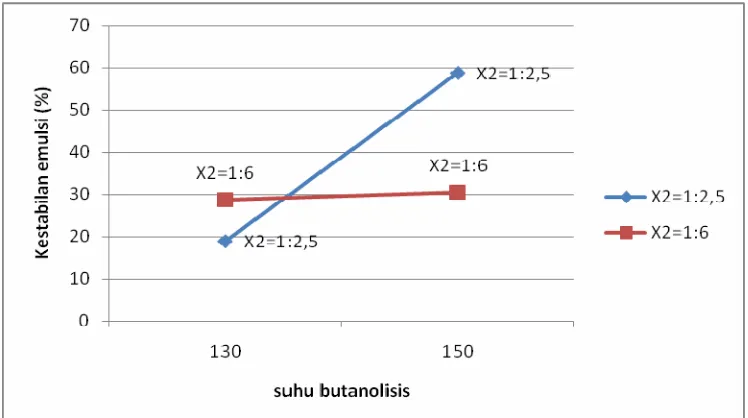
Hasil penelitian menunjukkan bahwa suhu butanolisis memiliki pengaruh 2,76 % dengan selang kepercayaan 97,53 %. Suhu butanolisis berpengaruh positif terhadap nilai kestabilan emulsi air : xilene dengan penambahan surfaktan APG. Sedangkan faktor rasio mol pati sagu dengan alkohol lemak memberikan pengaruh negatif dengan selang kepercayaan 60,44 %. Hasil analisis terhadap permukaan respon kestabilan emulsi APG dari suhu proses butanolisis (X1) dan rasio mol pati sagu-dodekanol (X2) menunjukkan
model yang berbentuk optimum dengan persamaan Y= 64,29 + 35,53X1 – 29,82X12 -
9,63x2 – 23,09X22 -20,56X1X2
Hasil analisis statistik dari model tersebut menunjukkan nilai kestabilan emulsi air:xilena dengan penambahan APG (%) yaitu 72,58% pada suhu butanolisis 147,8oC
dan pada rasio mol pati sagu-dodekanol 1:3,27 (b/b). Hasil validasi dengan melakukan percobaan dititik tersebut menunjukkan nilai kestabilan emulsi air:xilena dengan penambahan APG yang dihasilkan sebesar 72,3%.
komersial 21,36 dyne/cm dan APG hasil validasi 23,375 dyne/cm. Nilai tegangan antarmuka antara air dan xilene pada konsentrasi 0.4% (b/v) APG komersial 7,96 dyne/cm dan APG hasil validasi 8.17 dyne/cm. Nilai HLB yang diperoleh APG komersial 13,4 dan APG hasil validasi 8,8. Menurut Griffin, APG yang dihasilkan termasuk kategori surfaktan jenis minyak dalam air (O/W) dan bahan pembasah. Pengukuran pH penting dilakukan mengingat APG merupakan suatu asetal yang akan stabil pada kondisi netral dan lebih baik lagi pada kondisi basa. Pengukuran dilakukan dengan pengenceran sebesar 10% (b/v) dikarenakan APG berbentuk pasta. Dari hasil pengukuran pH APG komersial sebesar 7,55 dan APG hasil validasi kondisi optimum sebesar 7,15.
Karakterisasi formulasi herbisida antara lain warna formulasi herbisida adalah coklat keruh, derajat keasaman (pH) sekitar basa (6,7) nilai tegangan permukaan formulasi herbisida berkisar antara 27,69 - 29,25 dyne/cm.
Penyimpanan 5 minggu pada suhu 150C menyebabkan formulasi herbisida membeku, pada suhu ruang kestabilan formulasi berubah sampai minggu kedua dan minggu selanjutnya tidak berubah. Sedangkan penyimpanan pada suhu 400C, kestabilan
emulsi formulasi herbisida konstan.
Pengamatan aplikasi formulasi herbisida hasil penyimpanan 5 minggu dengan suhu 150C, suhu ruang (26-290C) dan 400C antara lain persentase penutupan gulma dan efektivitas herbisida. Semakin tinggi konsentrasi glifosat maka persentase penutupan gulma akan semakin rendah dan dengan konsentrasi APG 6 % atau 8 % sudah cukup meningkatkan efektivitas herbisidanya terutama pada 2 MSA. Berdasarkan uji Kruskal Wallis, hanya konsentrasi glifosat yang signifikan yaitu konsentrasi 48 % sedangkan konsentrasi APG tidak berpengaruh nyata
©. Hak Cipta milik IPB, tahun 2008
Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumber.
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian,, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar IPB.
PERANCANGAN PROSES PRODUKSI SURFAKTAN NON IONIK
ALKIL POLIGLIKOSIDA (APG) BERBASIS PATI SAGU DAN
DODEKANOL SERTA KARAKTERISASINYA
PADA FORMULASI HERBISIDA
MOCHAMAD NOERDIN N.K.
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains Pada
Departemen Teknologi Industri Pertanian
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN SEKOLAH PASCASARJANA
Judul Tesis : Perancangan Proses Produksi Surfaktan Non Ionik Alkil Poliglikosida (APG) Berbasis Pati Sagu dan Dodekanol serta Karakterisasinya pada Formulasi Herbisida
Nama : Mochamad Noerdin N K
NIM : F351060091
Disetujui Komisi Pembimbing
Dr. Ir. Ani Suryani, DEA Ketua
Dr. Ir. Dadang, MSc. Anggota
Diketahui
Ketua Program Studi Teknologi Industri Pertanian
Dr. Ir. Irawadi Jamaran
Dekan Sekolah Pascasarjana
Prof. Dr. Ir. Khairil A. Notodiputro, MS.
PRAKATA
Puji syukur kehadirat Allah SWT atas limpahan rahmat dan hidayahNYA sehingga penulis dapat menyelesaikan karya ilmiah ini dengan judul Perancangan Proses Produksi Surfaktan Non Ionik Alkil Poliglikosida (APG) Berbasis Pati Sagu dan Dodekanol serta Karakterisasinya pada Formulasi Herbisida. Penelitian dilaksanakan dari bulan November 2007 hingga bulan Juni 2008. Karya ilmiah ini disusun guna memenuhi salah satu syarat untuk memperoleh gelar Magister Sains pada Program Studi Teknologi Industri Pertanian (TIP), Sekolah Pasca Sarjana, Institut Pertanian Bogor.
Terima kasih dan penghargaan yang sebesar-besarnya penulis sampaikan kepada Ibu Dr. Ir. Ani Suryani, DEA dan Dr. Ir. Dadang, MSc selaku pembimbing, atas segala arahan dan bimbingan selama penelitian serta kepercayaan dan kesabaran dalam membimbing sampai terselesaikannya tesis ini. Ucapan terima kasih disampaikan kepada Kepala Balai Besar Industri Agro (BBIA) Bogor, yang memberikan kesempatan belajar di IPB dengan biaya dari Anggaran DIPA 2006 Departemen Perindustrian. Terima kasih pula disampaikan kepada Bapak Dr. Ir. Irawadi Jamaran selaku Ketua Program Studi Pasca Sarjana TIP, para staf pengajar TIP dan teman-teman TIP angkatan 2006 atas bantuan dan dukungan selama studi.
Semasa studi banyak orang yang membantu saya namun tidak ada yang melebihi bantuan isteri, anak, orang tua, kakak-kakak dan adik-adik tercinta yang dengan sabar memberikan semangat serta mendoakan keberhasilan studi ini. Terima kasih kepada bapak dan ibu di Laboratorium TIP dan Balai Besar Industri Agro serta semua pihak yang tidak dapat disebutkan satu persatu yang telah berperan dalam proses penulisan karya ilmiah ini.
Penulis menyadari bahwa karya ilmiah ini masih jauh dari sempurna oleh karena itu kritik dan saran membangun sangat penulis harapkan. Semoga karya ilmiah ini dapat bermanfaat.
Bogor, Agustus 2008
RIWAYAT HIDUP
Penulis dilahirkan di Bandung Jawa Barat tanggal 8 Juli 1963 sebagai anak pertama dari enam bersaudara. Ayah bernama Nana Kurniadji dan ibu Imas Maspupah. Pendidikan sarjana ditempuh di program studi Teknologi Hasil Pertanian Fakultas Pertanian Universitas Padjadjaran Bandung, dan lulus pada tahun 1988.
Penulis pernah bekerja pada Silvonsult Wanayasa di Bogor selama dua tahun, sejak tahun 1992 bekerja sebagai pegawai negeri sipil di Balai Besar Industri Agro (BBIA) Departemen Perindustrian Bogor. Selama bekerja sebagai peneliti di BBIA, penulis berkesempatan untuk mendapatkan pendidikan non gelar di dalam dan luar negeri. Dalam bidang lingkungan, tahun 1995 penulis mendapat beasiswa dari Carl Duisberg Gesselschaft (CDG) untuk pelatihan penanganan limbah cair di Bremen Universitat Jermanselama 13 bulan.
PERANCANGAN PROSES PRODUKSI SURFAKTAN NON IONIK
ALKIL POLIGLIKOSIDA (APG) BERBASIS PATI SAGU DAN
DODEKANOL SERTA KARAKTERISASINYA
PADA FORMULASI HERBISIDA
MOCHAMAD NOERDIN N.K.
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN SEKOLAH PASCASARJANA
PERNYATAAN MENGENAI TESIS DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa Tesis Perancangan Proses Produksi Surfaktan Non Ionik Alkil Poliglikosida (APG) Berbasis Pati Sagu dan Dodekanol serta Karakterisasinya pada Formulasi Herbisida adalah karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir Tesis ini.
Bogor, Agustus 2008
ABSTRACT
MOCHAMAD NOERDIN N.K. Process Design of Non Ionic Alkyl Polyglicosides (APG) Surfactant Production from Sago Starch and Dodekanol and Its Characteristics on Herbicide Formulation. Under direction of ANI SURYANI and DADANG.
Alkyl poliglycosides (APG) are non ionic surfactant which is commonly used in some products like herbicides, personal care products, cosmetics and textile bleachings. APG is new generation of surfactant that is environmental friendly. Raw materials of APG are fatty alcohol from palm oil or palm kernel oil and carbohydrates like the strach, that make APG as biodegradable surfactant. The aim of research was to obtain non ionic surfactant alkyl polyglycosides (APG) based on sago starch and fatty alcohol C12 (dodekanol). This research is modification of production process of APG two steps method from Wuest, et al. (1992), in order to obtain optimum condition temperature of butanolysis and mol ratio of sago starch-dodecanol to emulsion stability (water : xylene), characterisisation of APG, herbicide formulation and its hebicide formulation effectiveness. Result of response surface, showed that emulsion stability (water:xylene) added APG (%) was 72.58% at temperature of butanolysis 147.8oC and at ratio of sago starch-dodekanol 1:3.27 (w/w). Result of validation showed that emulsion stability (water : xylene) with addtion of APG was 72.3%. Equation model of optimum condition was Y= 64.29 + 35.53X1 – 29.82X12 –
9.63x2 – 23.09X22 -20.56X1X2 which similar with experimental datas. APG at 1 % (w/v)
was able to decrease surface tension 23.375 dyne/cm and interfacial tension between water : xylene at APG concentration of 0.4% (w/v) was 8.17 dyne/cm. Value of HLB was 8.8 so that the catogorize of this surfactant emulsion of oil in water (O/W) and wetting agent. APG pH in optimum process condition was 7.15. Application of herbicide formulation (glyphosate and APG surfactant) that was stored five weeks at temperature of 150C, room temperatur (26-290C) and 400C showed high effectiveness. The storeage temperature was not significantly different on herbicide efectiveness.
RINGKASAN
MOCHAMAD NOERDIN N.K. Perancangan Proses Produksi Surfaktan Non Ionik Alkil Poliglikosida (APG) Berbasis Pati Sagu dan Dodekanol serta Karakterisasinya Pada Formulasi Herbisida. Di bimbing oleh ANI SURYANI dan DADANG
Surfaktan (surface active agent) merupakan senyawa aktif penurun tegangan permukaan yang pada umumnya diproduksi dari minyak bumi (petrokimia) dan minyak-lemak (oleokimia). Penggunaan oleokimia sebagai bahan baku surfaktan perlu pengembangan lebih lanjut karena beberapa kelebihan oleokimia jika dibandingkan petrokomia, diantaranya mudah terurai secara biologis dan dapat diperbaharui.
Alkil Poliglikosida (APG) merupakan surfaktan non ionik yang dapat digunakan pada formulasi beberapa produk seperti formulasi herbisida, produk-produk perawatan tubuh, produk kosmetik, dan pemucatan kain tekstil. Bahan baku APG adalah alkohol lemak dari oleokimia minyak kelapa atau minyak inti sawit dan karbohidrat dari sumber pati seperti kentang, jagung, dan sagu.
Penelitian ini bertujuan untuk memperoleh surfaktan non ionik APG yang berbasis pada pati sagu dan alkohol lemak C 12 (dodekanol). Penelitian ini mengkaji rancang proses produksi APG metode dua tahap, optimasi suhu proses butanolisis dan rasio mol pati sagu-dodekanol terhadap nilai kestabilan emulsi air:xilena, karakterisasi APG dan hasil formulasi dan efektivitas herbisidanya. Rancang proses produksi APG dilakukan dengan memodifikasi proses produksi dua tahap Wuest, et al. (1992) dengan merubah sumber patinya dari kentang menjadi pati sagu dan netralisasi mengganti MgO dengan NaOH, serta penggunaan 2 buah reaktor menjadi 1 buah reaktor. Rancangan percobaan yang digunakan untuk optimasi menggunakan metode permukaan respon dengan faktor rasio mol pati sagu – dodekanol = 1 : 2,5 sampai dengan 1 : 6 dan suhu proses butanolisis dari suhu 1300C sampai 1500C.
Rancangan percobaan optimasi sintesis APG menggunakan metode permukaan respon (Response Surface Method) dan penelitian menggunakan rancangan komposit terpusat. Faktor yang dianalisis ada dua yaitu suhu proses butanolisis (X1) dengan
rentang antara 130 – 150 °C dan rasio mol pati : alkohol lemak (X2) dengan rentang
antara 1:2,5 – 1:6. Sedangkan rancangan percobaan pada aplikasi formulasi herbisida hasil penyimpan adalah rancangan acak lengkap faktorial dengan 3 faktor dan dua kali ulangan. Faktor yang dikaji adalah variasi suhu penyimpanan yaitu suhu 15oC, suhu ruang (26-290C), dan suhu 40oC , variasi konsentrasi glifosat yaitu konsentrasi 16%, 24%
dan 48%, variasi konsentrasi surfaktan APG terdiri dari 4%, 6%, 8% dan 10%. Untuk pengujian efektivitas dengan skoring menggunakan statistik non parametrik uji Kruskal Wallis.
Hasil penelitian menunjukkan bahwa suhu butanolisis memiliki pengaruh 2,76 % dengan selang kepercayaan 97,53 %. Suhu butanolisis berpengaruh positif terhadap nilai kestabilan emulsi air : xilene dengan penambahan surfaktan APG. Sedangkan faktor rasio mol pati sagu dengan alkohol lemak memberikan pengaruh negatif dengan selang kepercayaan 60,44 %. Hasil analisis terhadap permukaan respon kestabilan emulsi APG dari suhu proses butanolisis (X1) dan rasio mol pati sagu-dodekanol (X2) menunjukkan
model yang berbentuk optimum dengan persamaan Y= 64,29 + 35,53X1 – 29,82X12 -
9,63x2 – 23,09X22 -20,56X1X2
Hasil analisis statistik dari model tersebut menunjukkan nilai kestabilan emulsi air:xilena dengan penambahan APG (%) yaitu 72,58% pada suhu butanolisis 147,8oC
dan pada rasio mol pati sagu-dodekanol 1:3,27 (b/b). Hasil validasi dengan melakukan percobaan dititik tersebut menunjukkan nilai kestabilan emulsi air:xilena dengan penambahan APG yang dihasilkan sebesar 72,3%.
komersial 21,36 dyne/cm dan APG hasil validasi 23,375 dyne/cm. Nilai tegangan antarmuka antara air dan xilene pada konsentrasi 0.4% (b/v) APG komersial 7,96 dyne/cm dan APG hasil validasi 8.17 dyne/cm. Nilai HLB yang diperoleh APG komersial 13,4 dan APG hasil validasi 8,8. Menurut Griffin, APG yang dihasilkan termasuk kategori surfaktan jenis minyak dalam air (O/W) dan bahan pembasah. Pengukuran pH penting dilakukan mengingat APG merupakan suatu asetal yang akan stabil pada kondisi netral dan lebih baik lagi pada kondisi basa. Pengukuran dilakukan dengan pengenceran sebesar 10% (b/v) dikarenakan APG berbentuk pasta. Dari hasil pengukuran pH APG komersial sebesar 7,55 dan APG hasil validasi kondisi optimum sebesar 7,15.
Karakterisasi formulasi herbisida antara lain warna formulasi herbisida adalah coklat keruh, derajat keasaman (pH) sekitar basa (6,7) nilai tegangan permukaan formulasi herbisida berkisar antara 27,69 - 29,25 dyne/cm.
Penyimpanan 5 minggu pada suhu 150C menyebabkan formulasi herbisida membeku, pada suhu ruang kestabilan formulasi berubah sampai minggu kedua dan minggu selanjutnya tidak berubah. Sedangkan penyimpanan pada suhu 400C, kestabilan
emulsi formulasi herbisida konstan.
Pengamatan aplikasi formulasi herbisida hasil penyimpanan 5 minggu dengan suhu 150C, suhu ruang (26-290C) dan 400C antara lain persentase penutupan gulma dan efektivitas herbisida. Semakin tinggi konsentrasi glifosat maka persentase penutupan gulma akan semakin rendah dan dengan konsentrasi APG 6 % atau 8 % sudah cukup meningkatkan efektivitas herbisidanya terutama pada 2 MSA. Berdasarkan uji Kruskal Wallis, hanya konsentrasi glifosat yang signifikan yaitu konsentrasi 48 % sedangkan konsentrasi APG tidak berpengaruh nyata
©. Hak Cipta milik IPB, tahun 2008
Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumber.
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian,, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah.
b. Pengutipan tidak merugikan kepentingan yang wajar IPB.
PERANCANGAN PROSES PRODUKSI SURFAKTAN NON IONIK
ALKIL POLIGLIKOSIDA (APG) BERBASIS PATI SAGU DAN
DODEKANOL SERTA KARAKTERISASINYA
PADA FORMULASI HERBISIDA
MOCHAMAD NOERDIN N.K.
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains Pada
Departemen Teknologi Industri Pertanian
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN SEKOLAH PASCASARJANA
Judul Tesis : Perancangan Proses Produksi Surfaktan Non Ionik Alkil Poliglikosida (APG) Berbasis Pati Sagu dan Dodekanol serta Karakterisasinya pada Formulasi Herbisida
Nama : Mochamad Noerdin N K
NIM : F351060091
Disetujui Komisi Pembimbing
Dr. Ir. Ani Suryani, DEA Ketua
Dr. Ir. Dadang, MSc. Anggota
Diketahui
Ketua Program Studi Teknologi Industri Pertanian
Dr. Ir. Irawadi Jamaran
Dekan Sekolah Pascasarjana
Prof. Dr. Ir. Khairil A. Notodiputro, MS.
PRAKATA
Puji syukur kehadirat Allah SWT atas limpahan rahmat dan hidayahNYA sehingga penulis dapat menyelesaikan karya ilmiah ini dengan judul Perancangan Proses Produksi Surfaktan Non Ionik Alkil Poliglikosida (APG) Berbasis Pati Sagu dan Dodekanol serta Karakterisasinya pada Formulasi Herbisida. Penelitian dilaksanakan dari bulan November 2007 hingga bulan Juni 2008. Karya ilmiah ini disusun guna memenuhi salah satu syarat untuk memperoleh gelar Magister Sains pada Program Studi Teknologi Industri Pertanian (TIP), Sekolah Pasca Sarjana, Institut Pertanian Bogor.
Terima kasih dan penghargaan yang sebesar-besarnya penulis sampaikan kepada Ibu Dr. Ir. Ani Suryani, DEA dan Dr. Ir. Dadang, MSc selaku pembimbing, atas segala arahan dan bimbingan selama penelitian serta kepercayaan dan kesabaran dalam membimbing sampai terselesaikannya tesis ini. Ucapan terima kasih disampaikan kepada Kepala Balai Besar Industri Agro (BBIA) Bogor, yang memberikan kesempatan belajar di IPB dengan biaya dari Anggaran DIPA 2006 Departemen Perindustrian. Terima kasih pula disampaikan kepada Bapak Dr. Ir. Irawadi Jamaran selaku Ketua Program Studi Pasca Sarjana TIP, para staf pengajar TIP dan teman-teman TIP angkatan 2006 atas bantuan dan dukungan selama studi.
Semasa studi banyak orang yang membantu saya namun tidak ada yang melebihi bantuan isteri, anak, orang tua, kakak-kakak dan adik-adik tercinta yang dengan sabar memberikan semangat serta mendoakan keberhasilan studi ini. Terima kasih kepada bapak dan ibu di Laboratorium TIP dan Balai Besar Industri Agro serta semua pihak yang tidak dapat disebutkan satu persatu yang telah berperan dalam proses penulisan karya ilmiah ini.
Penulis menyadari bahwa karya ilmiah ini masih jauh dari sempurna oleh karena itu kritik dan saran membangun sangat penulis harapkan. Semoga karya ilmiah ini dapat bermanfaat.
Bogor, Agustus 2008
RIWAYAT HIDUP
Penulis dilahirkan di Bandung Jawa Barat tanggal 8 Juli 1963 sebagai anak pertama dari enam bersaudara. Ayah bernama Nana Kurniadji dan ibu Imas Maspupah. Pendidikan sarjana ditempuh di program studi Teknologi Hasil Pertanian Fakultas Pertanian Universitas Padjadjaran Bandung, dan lulus pada tahun 1988.
Penulis pernah bekerja pada Silvonsult Wanayasa di Bogor selama dua tahun, sejak tahun 1992 bekerja sebagai pegawai negeri sipil di Balai Besar Industri Agro (BBIA) Departemen Perindustrian Bogor. Selama bekerja sebagai peneliti di BBIA, penulis berkesempatan untuk mendapatkan pendidikan non gelar di dalam dan luar negeri. Dalam bidang lingkungan, tahun 1995 penulis mendapat beasiswa dari Carl Duisberg Gesselschaft (CDG) untuk pelatihan penanganan limbah cair di Bremen Universitat Jermanselama 13 bulan.
DAFTAR ISI
Halaman
DAFTAR TABEL... xii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPI RAN... . xvi
PENDAHULUAN ... 1
Latar Belakang ... 1
Perumusan Masalah ... 2
Tujuan Penelitian ... 2
Ruang Lingkup ... 3
Hipotesis ... 3
TI NJAUAN PUSTAKA ... 4
Kelapa... 4
Alkohol Lemak ... 7
Pati Sagu... 11
Surfaktan ... 12
Alkil Poliglikosida (APG) ... 17
Herbisida ... 23
METODE PENELI TI AN ... 26
Kerangka Pemikiran ... 26
Tempat dan Waktu Penelitian ... 26
Alat dan Bahan ... 26
Tahapan Penelitian ... 27
Rancangan Percobaan... 30
HASI L DAN PEMBAHASAN ... 32
Perancangan Proses Produksi APG ... 34
Proses Produksi APG dengan Dua Tahap ... 35
Optimasi Proses Produksi APG ... 38
Karakterisasi APG... 43
Karakterisasi Formulasi Herbisida... 57
SI MPULAN DAN SARAN ... 79
DAFTAR PUSTAKA ... 86
DAFTAR TABEL
Halaman 1 Peta potensi kelapa dunia... 4 2 Produktivitas kelapa Indonesia dan negara-negara lain ... 5 3 Komposisi asam-asam lemak minyak kelapa dan minyak nabati lain (%). 6 4 Reaksi kimia alkohol lemak dan hasilnya... 9 5 Karakteristik alkohol lemak dengan berbagai panjang rantai ... 10 6 Komposisi kandungan pati sagu dan beberapa sumber pati lainnya per
100 g ... 12 7 Kandungan amilosa dan amilopektin berbagai jenis pati ... 12 8 Nilai HLB dan aplikasinya berdasarkan konsep Grifin ... 17 9 Desain percobaan untuk optimasi sintesis APG ... 31 10 Koefisien parameter dan nilai signifikansi pengaruh faktor suhu butanolisis dan rasio mol pati sagu dengan lemak alkohol dengan respon uji kestabilan emulsi air : xilena dengan penambahan surfaktan APG ... 39 11 Nilai uji perbandingan tegangan permukaan air akibat pengaruh penambahan APG pada berbagai konsentrasi ... 44 12 Nilai uji perbandingan tegangan antar muka air : xilena ... 45 13 Nilai KL dan Γ∞ untuk tegangan peremukaan hasil optimasi metode
Nedler-Mead ... 47 14 Perbandingan tegangan permukaan (γ) APG komersial dan APG yang
dihasilkan dengan model... 48 15 Nilai KL dan Γ∞ untuk tegangan antarmuka hasil optimasi metode
Nedler-Mead ... 49 16 Perbandingan tegangan antar muka APG komersial dan APG yang
dihasilkan dengan model... 50 17 Penentuan kurva standar HLB ... 52 18 Nilai HLB APG ... 52 19 Pita serapan spektrofotometer FTIR APG hasil sintesa dan komersial
(cm-1) ... 55 20 Komposisi formulasi herbisida ... 58 21 Derajat keasaman (pH) formulasi herbisida... 60
22 Kestabilan formulasi herbisida (%) perminggu selama penyimpanan lima
minggu pada suhu 150C, 26-290C, dan 400C ... 61
23 Persentase penutupan gulma pada aplikasi formulasi herbisida hasil penyimpanan 5 minggu pada suhu 150C, suhu ruang (26-290C) dan 400C 66 24 Persentase penutupan gulma dari aplikasi formulasi herbisida hasil
penyimpanan lima minggu pada suhu 150C, suhu ruang (26-290C), dan
400C ... 70 25 Efektivitas formulasi herbisida hasil penyimpanan lima minggu pada suhu
150C, 26-290C, dan 400C ... 73
DAFTAR GAMBAR
Halaman
1 Proses pembuat an alkohol lemak ... 8
2 Micelles dan pembentukannya ... 14 3 Proses sint esis APG... 18
4 Proses reaksi dan st rukt ur al kyl pol ygl ycoside (APG). . . 19
5 Sint esis Fischer secara langsung . . . 19
6 Sint esis Fischer met ode dua t ahap . . . 20
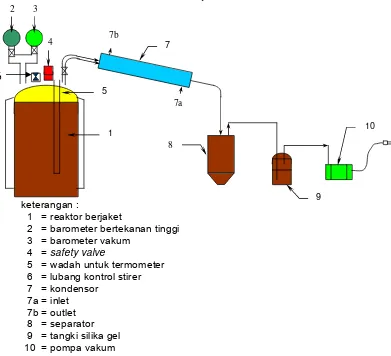
7 Tutup reaktor dengan barometer tekanan tinggi dan vakum ... 27
8 Met ode sint esis APG dua t ahap . . . 29
9 Reakt orberj aket dan t hermoset . . . 34
10 Rangkaian peralatan proses produksi APG ... 34 11 Hasil akhir proses butanolisis... 35 12 Hasil akhir proses transasetalisasi... 36 13 Hasil akhir destilasi ... 37 14 Hasil akhir pemucatan ... 38 15 Grafik pola interaksi faktor suhu butanolisis terhadap faktor rasio mol pati
sagu-dodekanol... 40 16 Grafik pola interaksi faktor rasio mol pati sagu–dodecanol terhadap
faktor suhu butanolisis ... 40 17 Permukaan respon nilai kestabilan emulsi air:xilena dengan penambahan
APG... 42 18 Kontur permukaan respon nilai kestabilan emulsi air:xilena dengan
penambahan APG... 42 19 Grafik tegangan permukaan air akibat pengaruh penambahan APG pada
berbagai konsentrasi. ... 44 20 Grafik tegangan antarmuka air : xilena akibat pengaruh penambahan
APG pada berbagai konsentrasi. ... 46 21 Tegangan permukaan APG komersial dan model ... 48 22 Tegangan permukaan APG hasil penelitian dan model... 49 23 Tegangan antar muka APG komersial dan model ... 50 24 Tegangan antar muka APG yang dihasilkan dan model... 50 25 Kurva standar HLB... 52
26 Hasil analisa FTIR APG komersial sebagai standar ... 54 27 Hasil analisa FTIR APG pada kondisi optimum ... 54 28 Neraca massa proses produksi APG dua tahap ... 56 29 Formulasi herbisida berbahan aktif glifosat dengan APG dan formulasi
pembanding ... 59 30 Histogram kestabilan emulsi formulasi herbisida setelah satu minggu pada
suhu 15oC, suhu ruang (26-29oC) dan 40oC ... 62 31 Histogram kestabilan emulsi formulasi herbisida setelah dua/tiga/empat/
lima minggu pada suhu 15oC, suhu ruang (26-29oC) dan 40oC ... 63 32 Histogram persentase penutupan gulma 1 MSA hasil penyimpanan ....lima
minggu pada suhu 15oC, suhu ruang (26-29oC) dan 40oC ... 67
33 Histogram persentase penutupan gulma 2 MSA hasil penyimpanan ....lima
minggu pada suhu 15oC, suhu ruang (26-29oC) dan 40oC ... 68 34 Histogram bobot kering gulma 1 MSA hasil penyimpanan lima minggu
pada suhu 15oC, suhu ruang (26-29oC) dan 40oC ... 71 35 Histogram bobot kering gulma 2 MSA hasil penyimpanan lima minggu
pada suhu 15oC, suhu ruang (26-29oC) dan 40oC ... 71 36 Foto lahan percobaan awal penelitian (0 MSA) untuk aplikasi formulasi
herbisida dengan konsentrasi glifosat 48 % dan konsentrasi APG 8 % pada
suhu 400C (a),suhu 150C (b), dan suhu ruang (26-290C) (c) ... 75
37 Foto lahan percobaan awal penelitian (4 HSA) untuk aplikasi formulasi herbisida dengan konsentrasi glifosat 48 % dan konsentrasi APG 8 % pada
suhu 400C (a),suhu 150C (b), dan suhu ruang (26-290C) (c) ... 76 38 Foto lahan percobaan awal penelitian (7 HSA) untuk aplikasi formulasi
herbisida dengan konsentrasi glifosat 48 % dan konsentrasi APG 8 % pada
suhu 400C (a),suhu 150C (b), dan suhu ruang (26-290C) (c) ... 77 39 Foto lahan percobaan awal penelitian (14 HSA) untuk aplikasi formulasi
herbisida dengan konsentrasi glifosat 48 % dan konsentrasi APG 8 % pada
suhu 400C (a),suhu 150C (b), dan suhu ruang (26-290C) (c) ... 78
DAFTAR LAMPIRAN
Halaman 1 Proses produksi alkil poliglikosida dengan dua tahap... 84 2 Metode analisa APG ... 85 3 Data proses produksi APG... 88 4 Data analisa pengujian APG ... 91 5 Pengolahan data suhu butanolisis dan rasio mol pati sagu-alkohol lemak
terhadap nilai kestabilan emulsi pada sintesa APG dua tahap ... 92 6 Aplikasi formulasi herbisida... 94 7 Analisis statistik kestabilan formulasi herbisida (%)... 95
8 Analisis statistik persentase penutupan gulma ... 101 9 Analisis statistik bobot kering gulma ... 104 10 Analisis statistik efektivitas herbisida hasil penyimpanan ... 108
Latar Belakang
Surfaktan merupakan senyawa aktif penurun tegangan permukaan yang dapat
diproduksi secara sintesis kimiawi ataupun biokimiawi. Surfaktan memiliki gugus
hidrofobik dan hidrofilik dalam satu molekul. Pembentukan film pada antar muka fasa menurunkan energi antar muka. Surfaktan dimanfaatkan sebagai bahan penggumpal,
pembasah, pembusaan, emulsifier oleh industri farmasi, industri kosmetika, industri
kimia, industri pertanian, industri pangan.
Bahan baku surfaktan dapat terbuat dari sumber nabati yang bersifat dapat
diperbaharui dan mudah terurai, tidak menggangu aktivitas enzim, proses produksi lebih bersih sehingga sejalan dengan isu lingkungan (Suryani et al., 2002).
Industri surfaktan di Indonesia masih terbatas, padahal surfaktan dibutuhkan
dalam jumlah besar. Kebutuhan surfaktan Indonesia pada tahun 2006 adalah 95.000
ton, sekitar 45.000 ton, masih diimpor (Wuryaningsih, 2007) dan diperkirakan jumlah
impor tersebut setiap tahunnya terus bertambah sejalan dengan tumbuhnya industri
kosmetik, industri makanan, industri minuman, industri farmasi, industri tekstil dan
industri penyamakan kulit (Sofiyaningsih dan Nurcahyani, 2006).
Indonesia merupakan negara yang berbasis pertanian sehingga mempunyai
potensi bahan nabati yang berlimpah, misalnya kelapa sebagai bahan baku alkohol
lemak. Selain itu, potensi pati-patian di Indonesia cukup besar.
Salah satu surfaktan yang dapat diproduksi dari bahan nabati adalah Alkil
poliglikosida (APG) dan surfaktan ini telah diklasifikasikan di Jerman sebagai surfaktan
kelas I yang ramah lingkungan (Hill et al., 1996), sehingga potensi pengembangan dan produksi APG masih sangat besar mengingat potensi pasar yang cukup besar pada
berbagai industri, seperti industri herbisida, personal care, kosmetik dan industri tekstil. Surfaktan APG ini tidak berbahaya untuk mata, kulit dan membran lendir, mengurangi
efek iritan serta dapat terurai baik secara aerob maupun anaerob.
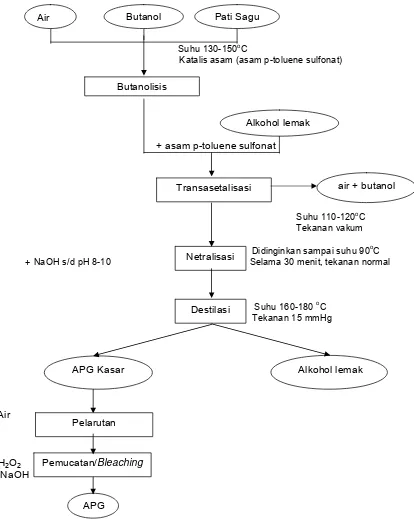
Menurut Hall et al. (2000), surfaktan APG dapat diproduksi secara langsung (asetalisasi) dan secara tidak langsung melalui dua tahap yaitu butanolisis dan
transasetalisasi dan selanjutnya melalui tahapan netralisasi, distilasi, pelarutan dan
pemucatan.
Dalam formulasi herbisida, surfaktan dapat meningkatkan penetrasi bahan aktif
herbisida kedalam tanaman (Van Valkenburg, 1990). Formulasi glifosat
Herbisida umumnya dikirim ke berbagai daerah dengan suhu yang
berbeda-beda, mulai dari daerah dingin sampai daerah panas, bahkan ada yang disimpan dalam
ruangan yang beratap seng yang suhunya dapat mencapai 400C.
Salah satu penilaian pengguna herbisida antara lain kestabilan formulasi
herbisida. Menurut Suryani et al. (2001), usaha untuk mempertahankan stabilitas emulsi antara lain dengan penyimpanan pada suhu yang tepat, terlindung dari sinar matahari,
dan terhindar dari guncangan.
Perumusan Masalah
Beberapa permasalahan pada penelitian ini antara lain :
• Bagaimana modifikasi rancangan proses produksi APG dua tahap menggunakan pati sagu pada proses butanolisis dan transasetalisasi terhadap APG yang
dihasilkan?
• Bagaimana kondisi suhu butanolisis dan rasio mol pati sagu dengan alkohol lemak yang optimum pada proses produksi APG ?
• Bagaimana karakteristik APG yang diperoleh pada kondisi proses produksi optimum ?
• Bagaimana karakteristik formulasi herbisida dari bahan aktif glifosat dengan APG yang dihasilkan ?
• Bagaimana pengaruh penyimpanan pada suhu yang berbeda formulasi herbisida dari bahan aktif glifosat dengan surfaktan APG terhadap efektivitas pengendalian
gulma ?
Tujuan Penelitian :
o Memperoleh modifikasi rancangan proses produksi surfaktan alkil poliglikosida
(APG) berbasis alkohol lemak dari kelapa dan pati sagu khususnya proses dua
tahap (butanolisis dan transasetalisasi)
o Mendapatkan informasi karakteristik APG yang dihasilkan pada kondisi optimum
proses produksinya.
o Mendapatkan karakteristik (fisik-kimia, efektivitas, dan daya tahan simpan pada suhu
yang berbeda) formulasi herbisida terbaik dengan menggunakan APG yang
Ruang Lingkup
Penelitian pendahuluan meliputi penentuan rancangan proses produksi APG
untuk reaksi dua tahap terutama pada reaksi butanolisis dan transasetalisasi.
Penelitian utama meliputi :
• Penentuan kondisi optimum proses produksi APG dua tahap (butanolisis dan transasetalisasi) dengan perlakuan suhu butanolisis dan rasio mol pati sagu dengan
lauril alkohol.
• Karakterisasi APG yang dihasilkan meliputi, kemampuan menstabilkan emulsi, kemampuan menurunkan tegangan permukaan dan tegangan antar muka,
mengontrol jenis formasi emulsi dengan menentukan nilai Hidrofil Lipofil Balance dari
APG, dan mengetahui struktur gugus fungsi APG dengan menggunakan FTIR. • Formulasi herbisida menggunakan bahan aktif glifosat dengan surfaktan APG yang
dihasilkan dan uji efektivitas herbisida hasil penyimpanan dengan suhu yang
berbeda .
Hipotesis
• Suhu butanolisis dan rasio mol pati sagu dengan alkohol lemak didugaberpengaruh terhadap produksi surfaktan APG yang dihasilkan.
• Konsentrasi bahan aktif glifosat dan penggunaan surfaktan APG diduga
berpengaruh terhadap karakteristik formulasi herbisida.
• Penyimpanan formulasi herbisida pada suhu yang berbeda diduga berpengaruh
terhadap efektivitas pengendalian gulma.
TINJAUAN PUSTAKA
Kelapa
Luas areal dan produksi kelapa Indonesia merupakan yang terbesar di dunia.
Pada tahun 2006 Indonesia memiliki luas areal pertanaman kelapa 3,818 juta Ha (32,37
%) disusul berturut-turut oleh Filipina 3,243 juta hektar (27,50%), India 1,935 juta
hektar (16,41 %), Srilangka 0,395 juta hektar (3,35 %), dan Thailand 0,226 juta hektar
(1,91 %) (APCC, 2007). Potensi kelapa dunia dapat dilihat pada Tabel 1 sedangkan
potensi kelapa Indonesia disajikan pada Tabel 2.
Tabel 1 Peta potensi kelapa dunia
Tahun
2002 2003 2004 2005 2006 No. Negara
1000 ha
1. Indonesia 3.885 3.911 3.870 3.894 3.818
2. Filipina 3.182 3.217 3.259 3.243 3.243
3. India 1.892 1.919 1.899 1.935 1.935
4. Sri Lanka 442 442 395 395 395
5. Thailand 327 328 343 344 226
6. Tanzania 310 310 310 310 313
7. Papua New Guinea 260 260 260 260 260
8. Brazil 263 271 275 281 280
9. Mexico 171` 148 148 150 12
10. Vietnam 165 136 133 132 133
159 131 131 130 115
70 70 70 70 78
Sumber : APCC (2007)
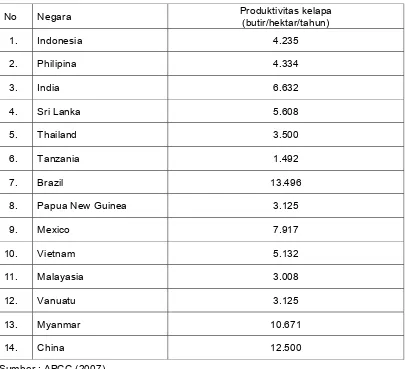
Dari Tabel 2 dapat dilihat bahwa produktivitas kelapa Indonesia 4.235 butir
kelapa per hektar per tahun masih rendah dibanding negara-negara penghasil kelapa
lainnya misalnya Philipina, India, Sri Lanka, Brazil, Mexico, Vietnam, Myanmar dan Cina.
produktivitas tertinggi yaitu masing-masing 13.496, 12.500, 10.671 dan 7.917 butir
kelapa per hektar per tahun.
Bagi masyarakat Indonesia, kelapa merupakan bagian dari kehidupannya karena
semua bagian tanaman dapat dimanfaatkan untuk memenuhi kebutuhan ekonomi,
sosial dan budaya. Di samping itu, arti penting kelapa bagi masyarakat juga tercermin
dari luasnya areal perkebunan rakyat yang mencapai 98% (sejak tahun 2004) dan
[image:31.612.112.517.221.590.2]melibatkan lebih dari tiga juta rumah tangga petani.
Tabel 2 Produktivitas kelapa Indonesia dan negara-negara lain
No Negara Produktivitas kelapa
(butir/hektar/tahun)
1. Indonesia 4.235
2. Philipina 4.334
3. India 6.632
4. Sri Lanka 5.608
5. Thailand 3.500
6. Tanzania 1.492
7. Brazil 13.496
8. Papua New Guinea 3.125
9. Mexico 7.917
10. Vietnam 5.132
11. Malayasia 3.008
12. Vanuatu 3.125
13. Myanmar 10.671
14. China 12.500
Sumber : APCC (2007)
Kelapa biasa disebut sebagai pohon kehidupan (tree of life) dan pohon surga (A heavenly tree) karena semua bagian tanaman ini dapat digunakan untuk kehidupan. Pada umumnya, produk kelapa di Indonesia dipasarkan dalam bentuk primer sehingga
nilai ekonominya sangat rentan terhadap fluktuasi musim yang menyebabkan nilai jual
rendah dan menimbulkan kerugian di pihak petani. Namun demikian, penerimaan dari
pengelolaan dan efisiensi pengolahan serta pengolahan lebih lanjut untuk meningkatkan
nilai tambah dari komoditi ini.
Komposisi kimia minyak kelapa berbeda dengan komposisi kimia sumber minyak
lainnya. Keunikan minyak kelapa, yaitu kaya akan kandungan asam-asam lemak jenuh
berantai pendek dan berantai menengah. Minyak biji sawit atau palm kernel oil (PKO) merupakan minyak yang komposisi kimiawinya mirip dengan minyak kelapa Sebagai
perbandingan komposisi asam-asam lemak berbagai sumber minyak nabati dapat
dilihat pada Tabel 3.
Tabel 3 Komposisi asam-asam lemak minyak kelapa dan minyak nabati lain (%)
Sumber minyak
Kelapa Biji sawit Sawit Jagung Kedelai
Jenuh :
C6:0 kaproat 0,50 0,30 - - -
C8:0 kaprilat 8,00 3,90 - - -
C10:0 kaprat 7,00 4,00 - - -
C12:0 laurat 48,00 49,60 0,30 - -
C14:0 miristat 17,00 16,00 1,10 - 0,10
C16:0 palmitat 9,00 8,00 45,20 11,50 10,50
C18:0 stearat 2,00 2,40 4,70 2,20 3,20
C20:0 arahidat 0,10 0,10 0,20 0,20 0,20
Tidak jenuh :
C16:1 palmitoleat 0,10 - - - -
C18:1 oleat 6,00 13,70 38,80 26,60 22,30
C18:2 linoleat 2,30 2,00 9,40 58,70 54,50
C18:3 linolenat - - 0,30 0,80 8,30
C20:4 arahidonat - - - - 0,90
Total 100,00 100,00 100,00 100,00 100,00
Persen tidak jenuh 8,40 15,70 48,50 86,10 86,00
Alkohol Lemak(Fatty Alcohol)
Alkohol lemak merupakan turunan dari minyak nabati seperti minyak kelapa
maupun minyak kelapa sawit yang lebih dikenal sebagai Alkohol lemak alami sedangkan turunan dari petrokimia (parafin dan etilen) dikenal sebagai Alkohol lemak
sintetik(Hall et al., 2000).
Alkohol lemak termasuk salah satu jenis bahan oleokimia dasar yang merupakan
alkohol alifatik rantai panjang. dengan panjang rantai antara C6 sampai C22. Sebagian besar merupakan rantai lurus dan monohidrat serta dapat diserap atau mempunyai satu
atau lebih ikatan ganda. Alkohol dengan panjang atom karbon lurus di atas C22 lebih
dikenal dengan Wax Alkohol. Karakter Alkohol lemak (primer atau sekunder) linier atau
bercabang, jenuh atau tidak jenuh ditentukan oleh proses pabrik dan bahan baku yang
digunakan (Presents, 2000).
Alkohol lemak utamanya digunakan sebagai bahan intermediates, di Eropa Barat hanya 5% yang digunakan secara langsung dan kira-kira 95 % dimanfaatkan dalam
bentuk turunannya. Pemanfaatan Alkohol lemak untuk pembuatan surfaktan kira-kira
sebesar 70-75% (Presents, 2000)
Menurut Suryani et al. (2001), Alkohol lemak diturunkan dari asam lemak dan metil ester melalui reaksi hidrogenasi. Reaksi ini dapat dilakukan dengan dua cara, yaitu : • Minyak nabati ditransesterifikasi menjadi metil ester, lalu dihidrogenasi menjadi
Alkohol lemak.
• Minyak nabati dihidrolisis menjadi asam lemak, lalu dihidrogenasi menjadi Alkohol lemak
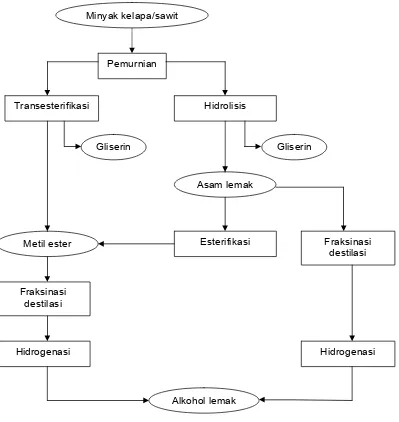
Untuk menghasilkan Alkohol lemak terlebih dahulu dilakukan transesterifikasi
yang merupakan proses paling efektif untuk transformasi molekul trigliserida menjadi
molekul ester asam lemak. Transesterifikasi melalui reaksi antara alkohol dan molekul
trigliserida dengan adanya katalis asam atau basa (Gambar 1). Sedangkan reaksi kimia
Alkohol lemak dan hasilnya dapat dilihat pada Tabel 4.
Alkohol mampu mengadisi ikatan C=O (Aldehid/ keton), gugus OR akan melekat
pada karbon dan proton akan melekat pada oksigen. Aldehid dapat bereaksi dengan
alkohol membentuk hemiasetal. Sedangkan Keton dapat bereaksi dengan alkohol
membentuk hemiketal. Mekanisme pembentukan hemiasetal/hemiketal melibatkan tiga
langkah. Pertama oksigen karbonil (C=O) diprotonasi oleh katalis asam, kemudian
oksigen alkohol menyatu dengan karbon karbonil, dan proton dilepaskan dari oksigen
Gambar 1 Proses pembuatan Alkohol lemak (Present, 2000)
Dengan kehadiran alkohol berlebih, hemiasetal/hemiketal bereaksi lebih lanjut
membentuk asetal/ketal. Gugus hidroksil (OH) dari hemiasetal digantikan oleh gugus
alkoksil (OR). Reaksi pembentukan asetal terjadi karena salah satu dari kedua oksigen
hemiasetal dapat diprotonasi. Bila oksigen hidroksil diprotonasi, lepasnya air
menghasilkan karbokation resonansi. Reaksi karbokation ini bereaksi dengan alkohol
yang biasa sebagai pelarut dan berada dalam keadaaan berlebih menghasilkan asetal
(sesudah proton lepas).
.
Minyak kelapa/sawit
Pemurnian
Transesterifikasi Hidrolisis
Gliserin
Asam lemak
Esterifikasi Fraksinasi
destilasi Gliserin
Metil ester
Fraksinasi destilasi
Hidrogenasi Hidrogenasi
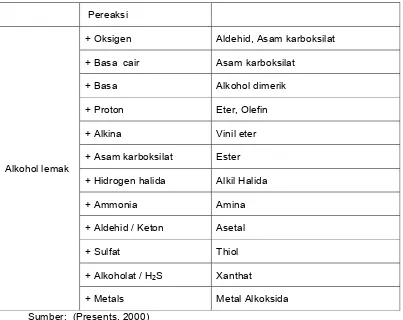
Tabel 4 Reaksi kimia alkohol lemak dan hasilnya
Pereaksi
+ Oksigen Aldehid, Asam karboksilat
+ Basa cair Asam karboksilat
+ Basa Alkohol dimerik
+ Proton Eter, Olefin
+ Alkina Vinil eter
+ Asam karboksilat Ester
+ Hidrogen halida Alkil Halida
+ Ammonia Amina
+ Aldehid / Keton Asetal
+ Sulfat Thiol
+ Alkoholat / H2S Xanthat
Alkohol lemak
+ Metals Metal Alkoksida
Sumber: (Presents, 2000)
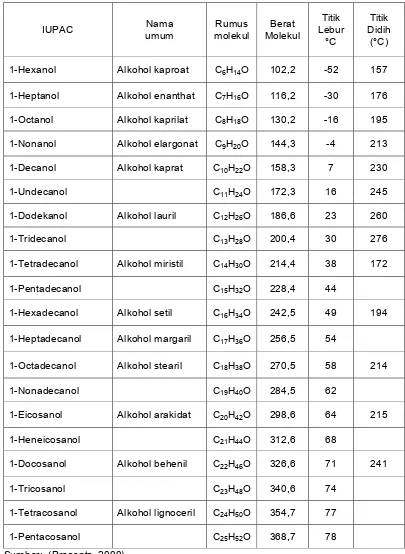
Pada Tabel 5 dapat dilihat beberapa karakteristik Alkohol lemak dengan
berbagai panjang rantai.
Alkohol lemak C12 lebih dikenal dengan nama alkohol lauril (dodekanol/ dodecyl
alcohol) dengan rumus bangun C12H26O, bobot molekul 186,6, densitas 0,8309 dan titik
Tabel 5 Karakteristik Alkohol lemak dengan bebagai panjang rantai
IUPAC Nama
umum
Rumus molekul
Berat Molekul
Titik Lebur °C
Titik Didih
(°C)
1-Hexanol Alkohol kaproat C6H14O 102,2 -52 157
1-Heptanol Alkohol enanthat C7H16O 116,2 -30 176
1-Octanol Alkohol kaprilat C8H18O 130,2 -16 195
1-Nonanol Alkohol elargonat C9H20O 144,3 -4 213
1-Decanol Alkohol kaprat C10H22O 158,3 7 230
1-Undecanol C11H24O 172,3 16 245
1-Dodekanol Alkohol lauril C12H26O 186,6 23 260
1-Tridecanol C13H28O 200,4 30 276
1-Tetradecanol Alkohol miristil C14H30O 214,4 38 172
1-Pentadecanol C15H32O 228,4 44
1-Hexadecanol Alkohol setil C16H34O 242,5 49 194
1-Heptadecanol Alkohol margaril C17H36O 256,5 54
1-Octadecanol Alkohol stearil C18H38O 270,5 58 214
1-Nonadecanol C19H40O 284,5 62
1-Eicosanol Alkohol arakidat C20H42O 298,6 64 215
1-Heneicosanol C21H44O 312,6 68
1-Docosanol Alkohol behenil C22H46O 326,6 71 241
1-Tricosanol C23H48O 340,6 74
1-Tetracosanol Alkohol lignoceril C24H50O 354,7 77
1-Pentacosanol C25H52O 368,7 78
Pati Sagu
Sagu (Metroxylon sagu Rottb.) merupakan tanaman penghasil pati yang sangat
potensial di masa yang akan datang. Tanaman sagu banyak tumbuh secara alami di
Papua dan Maluku yang dimanfaatkan oleh sebagian besar penduduk sebagai makanan
sehari-hari. Pati sagu, selain sebagai bahan pangan juga banyak digunakan sebagai
bahan baku pada industri kosmetik, makanan, kertas, dan plastik (Limbongan, 2007)
Potensi sagu yang masih dapat digarap di Indonesia sangat tinggi, karena masih
terdapat hutan sagu seluas 1,25 juta ha di Papua dan Maluku, serta 148 ribu ha lahan
sagu semibudidaya di Kepulauan Riau, Mentawai, Sumatera, kalimantan, Sulawesi,
Maluku, dan Papua. Lahan sagu ini merupakan lahan terluas di dunia (Humas, 2006)
Tepung sagu merupakan hasil ekstraksi inti batang sagu (Metroxylon sp.) yang juga hampir seluruh bagiannya mengandung pati. Kandungan pati sagu sekitar 84 %
sehingga sagu mampu menghasilkan pati kering hingga 25 ton per ha.
Indonesia termasuk satu dari dua negara yang memiliki areal sagu terbesar di
dunia selain Papua Nugini. Areal sagu seluas ini belum di eksploitasi secara maksimal
sebagai penghasil tepung sagu untuk bahan kebutuhan lokal (pangan) maupun untuk
komoditi ekspor. Sangat rendahnya pemanfaatan areal sagu yang hanya sekitar 0,1%
dari total areal sagu nasional disebabkan oleh kurangnya minat masyarakat dalam
mengelola sagu, rendahnya kemampuan dalam mengolah tepung sagu menjadi
bentuk-bentuk produk lanjutannya, kondisi geografis dimana habitat tanaman sagu umumnya
berada pada daerah marginal/rawa-rawa yang sukar dijangkau, serta adanya
kecenderungan masyarakat menilai bahwa pangan sagu adalah tidak superior seperti
halnya beras dan beberapa komoditas karbohidrat lainnya.
Menurut Samad (2002), sagu Indonesia memiliki kadar pati yang lebih baik
dibanding Malaysia. Bahkan, beberapa varietas sagu asal Kendari (Sulawesi Tenggara)
dan Bukit Tinggi (Sumatera Barat) mampu memproduksi pati lebih dari 300 kilogram per
pohon. Produksi sagu saat ini mencapai 200 ribu ton per tahun, Usia tanaman sagu ini
sekitar 7-10 tahun untuk bisa dipanen. Namun baru 56% saja yang dimanfaatkan
dengan baik.
Sagu mempunyai keunggulan antara lain dapat disimpan lebih lama, dapat
dipanen dan diolah tanpa mengenal musim, dan jarang terkena hama penyakit (Bujang
dan Ahmad, 2000). Komposisi kandungan pati sagu dan beberapa sumber pati lainnya
Tabel 6 Komposisi kandungan pati sagu dan beberapa sumber pati lainnya per 100 g
Komponen Sagu Jagung Tapioka
Kalori (cal) 357,0 349,0 98,0
Protein (g) 1,4 9,1 0,7
Lemak (g) 0,2 4,2 0,1
Karbohidrat (g) 85,9 71,7 23,7
Air (g) 15,0 14,0 19,0
Fe (g) 1,4 2,8 0,6
Sumber : www. pustaka bogor.net 2007
Granula pati dapat menyerap air dan mengembang. Pengembangan granula
pati bersifat bolak balik sebelum mencapai suhu tertentu. Proses dimana granula pati
bersifat tidak kembali ke bentuk awal disebut gelatinisasi. Suhu dimana larutan pati
bersifat tidak kembali ke bentuk awal disebut suhu gelatinisasi. Suhu gelatinisasi pati
berbedabeda tergantung jenis pati. Kisaran suhu gelatinisasi pati sagu adalah 72
-74oC. Kandungan amilosa dan amilopektin dari setiap jenis pati dapat dilihat pada Tabel
7.
Tabel 7 Kandungan amilosa dan amilopektin berbagai jenis pati
Sumber Pati Amilosa (%) Amilopektin (%)
Sagu 27 73
Jagung 28 72
Beras 17 83
Kentang 21 79
Gandum 28 72
Ubikayu 17 83
Sumber : Swinkel dalam Herliana (2005).
Surfaktan
Surfaktan merupakan senyawa aktif penurun tegangan permukaan (surface active agent) yang mempunyai struktur bipolar. Bagian kepala bersifat hidrofilik dan bagian ekor bersifat hidrofobik sehingga menyebabkan surfaktan cenderung berada
seperti minyak dan air. Kegunaan surfaktan antara lain untuk menurunkan tegangan
permukaan, tegangan antarmuka, meningkatkan kestabilan partikel yang terdispersi dan
mengontrol jenis formasi emulsi, misalnya oil in water (O/W) atau water in oil (W/O) (Rieger,1985).
Secara umum surfaktan dapat diklasifikasikan kedalam empat kelompok, yaitu
kelompok anionik, nonionik, kationik dan amfoterik. Klasifikasi tersebut berdasarkan
keberadaan gugus hidrofilik yang bersifat menarik air. Gugus hidrofilik yang bermuatan
negatif disebut anionik, yang bermuatan positif disebut kationik, yang tidak bermuatan
disebut nonionik, dan yang bermuatan positif dan negatif disebut amfoterik (Metheson,
1996). Sedangkan Swern (1997) membagi surfaktan menjadi empat kelompok sebagai
berikut:
• Surfaktan kationik, merupakan surfaktan yang bagian pangkalnya berupa gugus hidrofilik dengan ion bermuatan positif (kation). Umumnya merupakan garam-garam
amonium kuarterner atau amina.
• Surfaktan anionik, merupakan surfaktan yang gugus hidrofobiknya dengan ion bermuatan negatif (anion). Umumnya berupa garam natrium, akan terionisasi
menghasilkan Na+ dan ion surfaktan yang bermuatan negatif.
• Surfaktan nonionik, merupakan surfaktan yang tidak berdisosiasi dalam air, kelarutannya diperoleh dari sisi polarnya. Surfaktan jenis ini tidak membawa muatan
elektron, tetapi mengandung hetero atom yang menyebabkan terjadinya momen
dipol.
• Surfaktan amfoterik, mengandung gugus yang bersifat anionik dan kationik seperti pada asam amino. Sifat surfaktan ini tergantung pada kondisi media dan nilai pH.
Menurut Sadi (1994), Surfaktan pada umumnya dapat disintesis dari minyak
nabati melalui senyawa antara metil ester dan alkohol lemak. Proses-proses yang
diterapkan untuk menghasilkan surfaktan diantaranya, yaitu asetilasi, etoksilasi,
esterifikasi, sulfonasi, sulfatasi, amidasi, sukrolisis, dan saponifikasi. Jenis surfaktan
yang dipilih pada proses pembuatan suatu produk tergantung pada kinerja dan
karektiristik surfaktan tersebut serta karakteristik produk akhir yang diinginkan.
Flider (2001) menyatakan bahwa surfaktan berbasis bahan alami dapat dibagi
menjadi empat kelompok yaitu :
• Berbasis minyak-lemak seperti monogliserida, digliserida, dan poligliserol ester. • Berbasis karbohidrat seperti alkyl poliglikosida, dan n-metil glukamida.
• Ekstrak bahan alami seperti lesitin dan saponin.
Menurut Porter (1991), sifat hidrofilik surfaktan nonionik terjadi karena adanya
kelompok yang dapat larut dalam air yang tidak berionisasi, yaitu kelompok hidroksil
(R-OH) dan kelompok eter (R-O-R’). Daya kelarutan dalam air kelompok hidroksil dan eter
lebih rendah dibandingkan dengan kelarutan kelompok sulfat atau sulfonat.
Micelle
Pada konsentrasi rendah, molekul surfaktan dalam larutan teradsorpsi pada
permukaan udara atau air. Jika ditambahkan konsentrasi surfaktan, maka surfaktan
akan teradsorpsi pada permukaan hingga mencapai kejenuhan dan tegangan
permukaan menjadi konstan. Jika surfaktan terus ditambahkan ke dalam larutan
tersebut, maka molekul surfaktan berada dalam larutan namun bagian hidrofobik dari
surfaktan tetap menolak air sehingga molekul-molekul surfaktan membentuk bulatan
yang dikenal micelles (Gambar 2.a) dan pembentukan micelles dapat dilihat pada Gambar 2.b.
Gambar 2a. Micelles Gambar 2b. Pembentukan micelles
Gambar 2 Micelles dan pembentukannya
Pembasah
Jika setetes air dijatuhkan di atas suatu permukaan maka tetesan air tersebut
dapat saja menyebar pada permukaan (membasahi) atau membentuk suatu tetesan
stabil di atas permukaan tersebut (tidak membasahi). Penurunan tegangan permukaan
pada air oleh surfaktan dapat membuat sebuah larutan sukar basah menjadi larutan
mudah basah. Semakin pendek rantai hidrokarbon pada struktur kimia suatu surfaktan
semakin baik daya basahnya. Karakteristik daya basah yang optimum dimiliki surfaktan
dengan rantai sekitar C12 (Porter, 1991).
Keterangan :
Micelles surfaktan
Molekul air
Pembentukan buih
Kebanyakan surfaktan dalam larutan dapat membentuk buih, baik diinginkan
maupun tidak diinginkan dalam penggunaannya. Buih cair adalah sistem koloid dengan
fase terdispersi gas dan medium pendispersi zat cair. Kestabilan buih diperoleh dari
adanya zat pembuih (surfaktan). Zat pembuih ini teradsorpsi ke daerah antar - fase dan
mengikat gelembung -gelembung gas sehingga diperoleh suatu kestabilan.
Struktur buih cair tidak ditentukan oleh komposisi kimia atau ukuran buih
rata-rata, melainkan kandungan zat cairnya. Jika fraksi zat cair lebih dari 5%, maka
gelembung gas akan mempunyai bentuk hampir seperti bola. Sebaliknya, jika kurang
dari 5% maka bentuk gelembung gas adalah polihedral.
Struktur buih cair dapat berubah jika diberi gaya dari luar. Apabila aya tersebut
kecil, maka struktur buih akan kembali ke bentuk awal setelah gaya tersebut ditiadakan.
Namun, jika gaya yang diberikan cukup besar, maka akan terjadi deformasi.
Pengujian surfaktan meliputi kemampuan untuk menstabilkan emulsi,
kemampuan untuk menurunkan tegangan permukaan dan tegangan antar muka,
mengontrol jenis formasi emulsi dengan hidrophilic lipophilic balance, dan penentuan gugus fungsi dengan FTIR (Fourier Transform Infra RedSpectroscopy).
Kestabilan Emulsi
Emulsi yang stabil mengacu pada proses pemisahan yang berjalan lambat
sedemikian rupa sehingga proses itu tidak teramati pada selang waktu tertentu yang
diinginkan (Kamel, 1991).
Semakin tinggi viskositas dari suatu sistem emulsi, semakin rendah laju rata-rata
pengendapan yang terjadi, sehingga mengakibatkan kestabilan semakin tinggi (Suryani
et al., 2000). Viskositas berkaitan erat dengan tahanan yang dialami molekul untuk mengalir pada sistem cairan. Ada beberapa faktor yang mempengaruhi sifat alir suatu
emulsi, diantaranya untuk ukuran partikel dan distribusi ukuran partikel. Emulsi dengan
globula berukuran halus lebih tinggi viskositasnya dibandingkan dengan emulsi yang
globulanya tidak seragam (Muchtadi, 1990).
Tegangan Permukaan
Prinsip dasar tentang kestabilan emulsi adalah kesetimbangan antara gaya
tarik-menarik dan gaya tolak menolak yang terjadi antar partikel dalam suatu sistem emulsi.
Apabila gaya ini dapat dipertahankan tetap seimbang atau terkontrol, maka
partikel-partikel dalam sistem emulsi dapat dipertahankan agar tidak bergabung (Suryani et al.
Tegangan permukaan dirumuskan sebagai energi yang harus digunakan untuk
memperbesar permukaan suatu cairan sebesar 1 cm2. Tegangan permukaan
disebabkan oleh adanya gaya tarik menarik dari molekul cairan. Tegangan permukaan
diukur menggunakan Tensiometer du Nouy dan dinyatakan dalam dyne per centimeter (dyne/cm) atau miliNewton per meter (mN/m).
Pada cairan, terdapat molekul-molekul yang tersebar di bawah permukaan dan
pada permukaan cairan. Molekul-molekul ini saling tarik menarik. Gaya tarik-menarik
molekul-molekul di bawah permukaan cairan adalah sama pada semua arahnya.
Molekul-molekul di atas permukaan cairan tersebut kemudian mendapatkan gaya tarik
dari molekul-molekul di bawahnya yang mencoba untuk menariknya kembali ke tubuh
cairan, sehingga menyebabkan cairan mengambil bentuk yang memungkinkan luas
permukaan menjadi sekecil mungkin. Bentuk tersebut adalah bentuk bola (sphere). Besarnya energi yang mengendalikan bentuk cairan tersebut dinamakan tegangan
permukaan. Semakin besar ikatan antar molekul-molekul dalam cairan maka semakin
besar tegangan permukaan (Bodner dan Pardue, 1989).
Air merupakan cairan yang umumnya digunakan untuk membersihkan sesuatu
yang memiliki tegangan permukaan. Setiap molekul dalam struktur molekul air,
dikelilingi dan ditarik oleh molekul air yang lainnya. Tegangan permukaan tersebut pada
saat molekul air yang terdapat pada permukaan air ditarik ke tubuh air. Tegangan ini
mengakibatkan air membentuk butiran-butiran pada permukaan gelas atau kain yang
lambat laun akan membasahi bagian permukaan dan menghambat proses
pembersihan.
Tegangan antarmuka
Tegangan antarmuka adalah gaya per satuan panjang yang terjadi pada
antarmuka antara dua fase cair yang tidak dapat tercampur. Tegangan antarmuka
sebanding dengan tegangan permukaan, akan tetapi nilai tegangan antarmuka akan
selalu lebih kecil daripada tegangan permukaan pada konsentrasi yang sama
(Moecthar, 1989).
Hydrophilic Lipophilic Balance (HLB)
Menurut Suryani et al. (2000), HLB adalah ukuran empiris untuk mengetahui hubungan antara gugus hidrofilik dan hidrofobik pada suatu surfaktan. Sistem HLB
digunakan untuk mengidentifikasi emulsifikasi minyak dan air oleh surfaktan. Terdapat
dua tipe emulsi, yaitu :
a. Water-in-oil (w/o), artinya air terdispersi di dalam minyak.
b. Oil-in-water (o/w), artinya minyak terdispersi di dalam air
Memerlukan surfaktan dengan nilai HLB tinggi.
Makin tinggi nilai HLB, maka surfaktan makin bersifat larut air, makin rendah nilai
HLB, surfaktan makin bersifat larut minyak. Nilai HLB dan aplikasinya berdasarkan
konsep Grifin disajikan pada tabel dibawah ini.
Tabel 8 Nilai HLB dan aplikasinya berdasarkan konsep Grifin
Nilai HLB Aplikasi
3 – 6 Pengemulsi W/O
7 – 9 Wetting agent
8 – 14 Pengemulsi O/W
9 – 13 Detergen
10 -13 Solubilizer
12 -14 Dispersant
Sumber : Holmberg et al. (2003)
Fourier Transform Infra RedSpectroscopy (FTIR)
Fourier Transform Infra Red Spectroscopy merupakan pencirian unsur dan gugus fungsi dalam suatu polimer. Analisis ini diperlukan karena dalam suatu polimer
terkandung aneka unsur kimia baik logam maupun bukan logam. Spektrum inframerah
dari senyawa organik mempunyai sifat fisik yang khas. Energi radiasi inframerah akan
diabsorpsi oleh senyawa organik sehingga molekulnya akan mengalami rotasi atau
vibrasi. Setiap ikatan kimia yang berbeda seperti C-C, C=C, C=O, O-H dan sebagainya
mempunyai frekuensi vibrasi yang berbeda sehingga kemungkinan dua senyawa
berbeda akan mempunyai absorpsi yang sama adalah kecil sekali (Randall et al., dalam Indrawanto, 2007).
Alkil poliglikosida (APG)
APG pertama kali dikenal sekitar tahun 1983 oleh Emil fischer (Margaretha,
1999). APG merupakan surfaktan yang ramah lingkungan karena disintesis dengan
bahan baku yang berbasis pati (kentang, sagu, tapioka dan lain-lain) dengan alkohol
lemak berbasis minyak nabati (kelapa, sawit, biji kapok dan biji karet).
Proses produksi APG dapat dilakukan melalui dua metode, yaitu pertama
berbasis bahan baku pati dan alkohol lemak sedang kedua berbasis dekstrose dan
alkohol lemak. Diagram proses pembuatan APG disajikan pada Gambar 3.
Pada diagram proses Gambar 3 tersebut dapat dilihat perbedaan proses sintesis
dan transasetalisasi, sedang metode kedua hanya melalui proses asetalisasi yang
selanjutnya dari masing-masing metode masuk ke proses netralisasi, distilasi, pelarutan,
dan pemucatan.
APG mempunyai dua struktur kimia. Rantai hidrokarbon yang bersifat hidrofobik
(lipofilik) dan hidrofilik. Sifat rantai yang hidrofobik disebabkan oleh rantai hidrokarbon
tersebut tersusun dari alkohol lemak yang berasal dari minyak sawit atau minyak kelapa.
Sedangkan, bagian molekul yang bersifat hidrofilik dari APG tersusun dari molekul
glukosa/pati. Gambar proses reaksi dan struktrur APG disajikan pada Gambar 3.
Gambar 3 Proses sintesis APG
Proses produksi APG melalui proses asetalisasi dilakukan dengan
mencampurkan alkohol lemak dan glukosa dengan perbandingan 2:1 sampai dengan
perbandingan 10:1 dengan katalis asam p-toluena sulfonat. Kondisi reaksi diatur pada suhu 100-120°C selama 3-4 jam pada tekanan 15-25 mmHg. Setelah itu, campuran
bahan dilakukan netralisasi sampai pH 8-10 dengan menggunakan NaOH 50 % pada
suhu 80°C. Setelah tahap tersebut akan terbentuk APG kasar yang masih bercampur
dengan residu (air + alkohol lemak ) yang tidak bereaksi sehingga dilakukan pemisahan
dengan menggunakan distilasi vakum untuk mengeluarkan residu. Pemisahan alkohol
Pati atau sirup dekstrosa
Butanolisis
Transasetalisasi
Butanol
Alkohol lemak
Butanol/ Air
Netralisasi
Destilasi
Pelarutan
Pemucatan
Alkil poliglikosida
Asetalisasi Alkohol lemak
Glukosa anhidrat atau glukosa monohidrat (dekstrosa)
Air
Alkohol lemak
lemak dilakukan pada suhu 160-200°C dan tekanan 15 mmHg. Tahap akhir adalah
pemucatan untuk memperoleh APG murni pada suhu 50-100°C kurang lebih selama 2
jam (Indrawanto, 2007).
Gambar 4. Proses reaksi dan struktur alkyl polyglycoside (APG) Gambar 4 Proses reaksi dan struktur APG
Menurut Wuest et al. (1992), sintesis surfaktan APG dapat dengan reaksi 2 tahap dari pati atau hasil degradasi pati seperti poliglukosa atau sirup glukosa, tahap
pertama direaksikan dengan alkohol rantai pendek, terutama butanol, dan tahap kedua
transasetalisasi direaksikan dengan rantai lebih panjang C 8-22 terutama C 12-18 dari
alkohol lemak bahan baku alami. Reaksi butanolisis dilakukan pada temperatur diatas
125oC dan dengan tekanan 4-10 bar dalam zone reaksi tertutup. Reaksi transasetalisasi
dilaksanakan pada temperatur 115-118 oC pada kondisi vakum dengan rasio mol pati
dengan alkohol rantai panjang adalah 1: 1,5 sampai 1: 7, 1:2,5 sampai 1:7, dan 1:3
sampai 1: 5.sedangkan rasio mol sakarida : air = 1:5 sampai 1:12, 1:6 sampai 1:12, 1:6
sampai 1:9, 1:6 sampai 1:8. Pada Gambar 5 dapat dilihat proses reaksi sintesa APG
satu tahap dan Gambar 6 sintesis APG dengan dua tahap.
Gambar 6 Proses sintesis APG dua tahap
Tahapan proses sintesa APG dengan dua tahap meliputi tahap dasar sebagai
berikut:
Reaksibutanolisis
Reaksi butanolisis merupakan reaksi antara sumber pati dengan menggunakan
katalis asam dengan butanol untuk membentuk produk butil glikosida.
Pemilihan katalis pada proses sintesa APG juga sangat menentukan
keberhasilan terbentuknya ikatan asetal serta memperpendek proses sintesa
berlangsung. Katalis-katalis asam yang dapat digunakan pada tahapan proses
asetalisasi meliputi:
• Asam anorganik: asam fosfat, asam sulfat, asam klorida, dll.
• Asam organik: asam triflouroasetat, asam p-toluen sulfonat, asam sulfosuksinat, asam kumena sulfonat, asam lemak tersulfonasi, ester asam lemak tersulfonasi , dll. • Asam dari surfaktan: asam alkil benzena sulfonat, alkohol lemak sulfat, alkoksilat
alkohol lemak sulfat, alkil sulfonat rantai lurus, alkil ester dari asam sulfosuccinat,
alkil naphthalena sulfonat dll.
Dari katalis tersebut diatas dipilih katalis organik asam p-toluena sulfonat, karena
katalis cenderung bersifat organik dan dapat terurai serta berupa asam lemah. Jika
menggunakan asam kuat, kemungkinan asam akan bereaksi dengan menghidrolisa
glukosa. Penggunaan asam lemah juga akan memudahkan dalam proses netralisasi.
Selain itu asam p-toluena sulfonat juga bersifat tidak korosif terhadap pipa besi ataupun
stainless steel (Hill et al., 1996)
Gibson et al. (2001) menentukan katalis asam yang digunakan dalam proses asetalisasi/transasetalisasi menggunakan perhitungan sebagai berikut :
• Katalis pertama kira-kira 0,7-1,4% dari berat pati
• Katalis yang digunakan pada tahapan proses asetalisasi adalah penjumlahan dari katalis pertama dan katalis kedua.
Reaksi Transasetalisasi
Produk akhir proses butanolisis (butil glikosida) direaksikan dengan alkohol
rantai panjang (C8-C22) dengan katalisator asam yang jumlahnya 25-50% dari berat
katalis pertama membentuk alkil poliglikosida, sedangkan butanol dan air pada suhu proses ini (1200C) akan teruapkan dan ditampung dalam separator.
Alkil poliglikosida (APG) merupakan suatu asetal yang diperoleh dari pati
(glukosa) dan alkohol rantai panjang (C8-C22), sehingga proses pengikatan glukosa
siklik terhadap alkohol sering disebut reaksi asetalisasi (wuest et al, 1992). Salah satu proses asetalisasi bisa melalui glikosidasi (pembentukan ikatan glikosida) glukosa
dengan menggunakan alkohol berlebih sehingga proses asetalisasi pada sintesa APG
sering pula disebut glycosidation.
McCurry et al, (1996) menyatakan bahwa alkohol lemak rantai panjang yang diperkenankan dalam sintesa APG adalah mulai rantai C8-C22, tetapi menurut Hill et al. (1996) rantai panjang alkohol lemak yang dapat digunakan C8–C18 lebih dianjurkan.
Alkohol lemak memiliki gugus hidroksil (OH) yang sifat kelarutannya sangat
dipengaruhi oleh ikatan hidrogen yang berikatan dengan atom karbon. Dengan
bertambah panjangnya rantai karbon, maka pengaruh gugus hidroksil yang bersifat
polar menurun dan sifat non polar akan semakin tinggi. Alkohol lemak pada APG
diperlukan untuk memperoleh gugus alkil rantai panjang sebagai bagian yang bersifat
hidrofobik. Pemilihan alkohol lemak yang tepat juga akan berpengaruh pada suhu
transasetalisasi berlangsung sebab semakin panjang rantai maka titik didih alkohol
lemak semakin tinggi.
Netralisasi
Tahapan netralisasi ini bertujuan untuk menghentikan proses asetalisasi/
transasetalisasi dengan menambahkan basa hingga tercapai suasana basa yaitu pH
sekita