UJI AKTIVITAS ANTIINFLAMASI EKSTRAK DAUN
KELOR (Moringa oleifera Lam.) DENGAN METODE
STABILISASI MEMBRAN SEL DARAH MERAH SECARA
IN VITRO
SKRIPSI
LUTFIANA
NIM : 109102000053
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
UJI AKTIVITAS ANTIINFLAMASI EKSTRAK DAUN
KELOR (Moringa oleifera Lam.) DENGAN METODE
STABILISASI MEMBRAN SEL DARAH MERAH SECARA
IN VITRO
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
LUTFIANA
NIM : 109102000053
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
Nama : Lutfiana Program Studi : Farmasi
Judul : Uji Aktivitas Antiinflamasi pada Daun Kelor (Moringa oleifera L.) dengan Metode Stabilisasi Membran Sel Darah Merah.
Kelor (Moringa oleifera L.) merupakan tanaman yang banyak digunakan dalam pengobatan tradisional. Analisis fitokimia ekstrak tanaman kelor mengungkapkan adanya kandungan senyawa flavonoid dan senyawa polifenol lain yang diketahui memiliki aktivitas antiinflamasi. Penelitian ini bertujuan untuk mengetahui aktivitas antiinflamasi dari ekstrak etanol 70%, fraksi n-heksan, fraksi etil asetat dan fraksi etanol 50% dari daun kelor menggunakan metode stabilisasi membran sel darah merah. Penghambatan lisis sel darah merah akibat induksi larutan hipotonis digunakan sebagai ukuran aktivitas antiinflamasi. Aktivitas antiinflamasi dari ekstrak dan fraksi daun kelor tersebut kemudian dibandingkan dengan standar natriun diklofenak. Hasil uji aktivitas antiinflamasi menggunakan metode stabilisasi membran sel darah manusia berdasarkan perhitungan % stabilitas menunjukkan bahwa fraksi yang mempunyai aktivitas tertinggi adalah fraksi etil asetat. Kemudian fraksi etil asetat tersebut dibuat beberapa seri konsentrasi (50 ppm, 100 ppm, 200 ppm, 400 ppm dan 800 ppm dan 1000 ppm) dan dibandingkan dengan kontrol positif berupa Na diklofenak pada konsentrasi yang sama. Diperoleh perlindungan paling efektif dari semua konsentrasi padakonsentrasi 1000 ppm yaitu sebesar 90,575%, sehingga dengan demikian konsentrasi tersebut dikatakan yang paling tinggi/efektif memberikan perlindungan membran sel darah merah yang diinduksi larutan hipotonik. Semakin tinggi konsentrasi stabilisasi yang digunakan maka kemampuan dalam menstabilkan membran sel darah merah yang induksi larutan hipotonik akan semakin meningkat, sehingga dengan demikian aktivitas menstabilkan membran sel darah merah dapat dikaitkan dengan konsentrasi. Hasil ini ditunjang dengan uji statistik ANOVA, yang menyatakan bahwa (P≤0,05) yang artinya terdapat perbedaan yang nyata pada setiap konsentrasi dengan perlakuan.
Program Study : Pharmachy
Tittle :Evaluation of Anti-inflammatory Activity of Leaf Extracts of Moringa oleifera L. By Human Red Blood Cell Membrane Stabilisation
Method.
Moringa oleifera L. is widely used in traditional medicine. Pytochemical analysis of M.oleifera plant extracts revealed the presence of various biochemical compounds such as flavonoid anh other poly phenol group which heve remarkable as antiinflamatory. So this study aimed at evaluating in the in vitro anti-inflammatory activity of the ethanol70% extract, n-hexane, ethyl acetate and ethanol 50% fraction from the leaves of M. oleifera by red blood cell membrane stabilization method. The Inhibition of hypotonicity induced Red Blood Cell (RBC) membrane lysis was taken as a measure of the anti inflammatory activity. The potency of the extract was compared with standard diclofenac sodium. Among the three fractions tested, ethyl acetate fraction provided highest stabilization. Then ethyl acetate fraction was made a series of concentrations (50 ppm, 100 ppm, 200 ppm, 400 ppm, 800 ppm and 1000 ppm) and compared with the positive control of diclofenac sodium at the same concentration. The maximum membrane stabilization of ethyl acetat fraction was found to be 90.575% at dose of 1000 ppm ,thus the concentration is in the most high / effective protection of red blood cell membranes induced hypotonic solution. The higher the concentration stabilization used the ability to stabilize the membranes of red blood cells induced hypotonic solution will increase, thus stabilizing the activity of red blood cell membranes can be attributed to the concentration. This result is supported by statistical ANOVA, which states that (P≤ 0.05) which means that there are significant differences in any concentration with treatment.
Bismillahirrahmaanirrahiim. Alhamdulillah, puji syukur penulis panjatkan
kepada Allah SWT atas segala berkat dan rahmat-Nya, yang telah diberikan kepada
penulis sehingga penulis dapat menyelesaikan skripsi ini. Shalawat dan salam selalu
tercurah limpahkan kepada Rosulullah SAW, sosok yang selama ini penulis teladani.
Skripsi dengan judul “Uji Aktivitas Antiinflamasi pada Daun Kelor (Moringa oleifera L.) dengan Metode Stabilisasi Membran Sel Darah Merah” ini diajukan untuk
memenuhi tugas akhir sebagai salah satu syarat untuk memperoleh gelar Sarjana
Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan
Universitas Islam Negeri Syarif Hidayatullah Jakarta.
Dalam penyusunan skripsi ini, penulis dibantu oleh berbagai pihak. Oleh karena itu pada
kesempatan ini, penulis mengucapkan banyak terima kasih yang sedalam-dalamnya
kepada :
1. Prof. Dr. H. Chairul,Apt sebagai Pembimbing I dan Eka Putri, M.Si, Apt sebagai
Pembimbing II yang telah meluangkan waktu, pikiran dan tenaganya serta
memberikan nasehat, arahan dan ilmu terbaik yang mereka miliki.
2. Departemen Agama RI yang telah membiayai penulis selama menjalani
pendidikan di jenjang S1 Farmasi UIN Syarif Hidayatullah ini..
3. Prof. Dr. (hc) dr. M. K. Tadjudin, Sp.And, selaku Dekan Fakultas Kedokteran
dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
4. Drs. Umar Mansyur, M.Sc., Apt selaku Ketua Program Studi Farmasi Fakultas
Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah
Jakarta.
5. Ibu/Bapak Dosen dan Staff Akademika Program Studi Farmasi Fakultas
Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah
terhingga yang tak akan pernah mampu penulis membalas semua itu. Adik-adik
penulis, Nadia Soba dan Muhammad Akbar yang sangat penulis cintai.
7. Laboran yang telah membantu keseharian penulis selama penelitian di
laboraturium, teh Ana, teh Lina, ka Lisna dan ka Liken.
8. Teman-teman farmasi angkatan 2009 khususnya teman-teman Edta-C. Terima
kasih atas kesempatan mengenal kalian semua.
9. Teman-teman penelitian di LIPI Cibinong, Leliana Nurul Wachidah, Nurul
Fithriyah dan Muhammad Arif yang telah berjuang bersama.
10.Teman-teman CSSMoRA 2009, PIM Lovers, Butet, Nuyung, Leli, Omi, Dhea,
Dhila, Wali, Lulu, Ziza, Cime, Dyah, Ainul, Nurul, Cucut, Neneng, Cucut, Zaky,
Ferry, terima kasih telah menjadi keluarga kedua bagi penulis. Serta semua pihak
yang telah membantu penulis selama ini yang tidak bisa disebutkan satu per satu.
Penulis sadar bahwa dalam penulisan skripsi ini masih jauh dari sempurna,
Kritik dan saran pembaca diharapkan penulis guna perbaikan dimasa mendatang. Akhir
kata, penulis berharap mudah-mudahan skripsi ini berguna bagi kita semua, Amin.
Jakarta, 20 September 2013
Halaman
HALAMAN JUDUL ……… ii
HALAMAN PERNYATAAN ORISINALITAS ……….. iii
HALAMAN PERSETUJUAN PEMBIMBING ………... iv
ABSTRAK ……… v
ABSTRACT ………. vi
KATA PENGANTAR ………. vii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ……… ix
2.2.2. Mekanisme inflamasi ………. 16
2.2.3. Penyebab Inflamasi ……… 18
2.2.4. Tipe inflamasi ………... 19
2.2.5. Mediator inflamasi ……… 20
2.4. Obat Antiinflamasi ……….. 23
2.4.1. Obat antiinflamasi Steroid ………. 23
2.4.2. Obat antiinflamasi Non steroid ……….. 24
2.5. Uji Aktivitas Antiinflamasi ……… 25
2.5.1. Metode stabilisasi membran sel darah merah manusia 25
2.6. Spektrofotometer UV-VIS………... 26
3.4.3. Fraksinasi bertingkat denan metode partisi cair-cair …… 31
3.4.5 Uji aktivitas anti inflamasi metode stabilisasi membran eritrosit 32 3.4.4. Skrining fitokimia ……….…... 35
4.1.5. Hasil Uji Aktivitas Antiinflamasi ……… 39
4.1.4. Hasil Skirining Fitokimia ……… 44
Halaman Tabel 1. Kandungan Kimia Daun Kelor (Moringa oleifera L.) ……….... 8
Tabel 2. Hasil Rendemen Ekstrak dan Fraksi Daun Kelor ……… 38
Tabel 3. Stabilisasi Membran Eritrosit dari Ekstrak Uji dan Kontrol
Positif pada Konsentrasi 1000 ppm ……….. 39
Tabel 4. Stabilisasi Fraksi Etil Asetat Daun Kelor terhadap Membran
Eritrosit Akibat Induksi Larutan Hipotonik dengan Beberapa
Variasi Konsentrasi ………... 41
Tabel 5. Hubungan antara % Stabilitas dan Log Konsentrasi
untuk Menentukan Nilai IC50 dengan Metode Analisis Probit 43
Halaman
Gambar 1. Akar, Daun dan Pohon Kelor ………..…. 6
Gambar 2. Struktur Kimia Golongan Flavonoid ……… 13
Gambar 3. Struktur Kimia dari Beberapa Steroid Sapogenin ……… 14
Gambar 4. Skema Mekanisme Radang ……….. 18
Gambar 5. Mediator Inlamasi ………. 21
Gambar 6. Asam Arakhidonat dan Mediator Peradangan ………. 23
Gambar 7. Mekanisme Kerja Obat Antiinflamasi Steroid & Nonsteroid terhadap Prostaglandin ……….. 24
Gambar 8. Skema Spektrofotometer UV-VIS ……….… 27
Gambar 9. Serbuk Daun Kelor (Moringa oleifera L.) ……… 37
Gambar 10. Ekstrak Etanol 70%, Fraksi n-heksan, Etil Asetat dan Etanol 50% 38 Gambar 11. Stabilisasi Membran Eritrosit dari Ekstrak Uji dan Kontrol Positif Terhadap Induksi Larutan Hipotonik ………. 40
Gambar 12.Kurva Stabilisasi Kerusakan Membran Eritrosit Akibat Induksi Larutan Hipotonik dengan Beberapa Variasi Konsentrasi 42
Gambar 13.Kurva antara Probit dan Log Konsentrasi Fraksi Etil Asetat Daun Kelor pada Berbagai Varian Konsentrasi …………... 44
Gambar 14.Reaksi Pembentukan Garam Flavilium ... 48
Halaman
Lampiran 1. Hasil Determinasi Tanaman ……….... 61
Lampiran 2. Alur Penelitian ……….... 62
Lampiran 3. Skema Pengujian Fitokimia ... 63
Lampiran 4. Pembuatan Larutan Ekstrak Uji ……….... 64
Lampiran 5. Pembuatan Larutan Na Diklofenak ………... 65
Lampiran 6. Hasil Rendemen Ekstrak Etanol 96% dan masing-masing Fraksi Daun Kelor ……….. 66
Lampiran 7. Penentuan Stabilisasi Membran Eritosit terhadap Ekstrak Etanol 70%, Fraksi n-heksan, Etil Asetat dan Fraksi Etanol 50% Daun Kelor (Moringa oleifera L.) pada konsentrasi 1000 ppm .... 67
Lampiran 8. Penentuan Stabilisasi Membran Eritosit terhadap Fraksi Etil Asetat Daun Kelor (Moringa oleifera L.) ………. 68
Lampiran 9. Penentuan Stabilisasi Membran Eritosit terhadap Kontrol Positif (Na Diklofenak) ………. 70
Lampiran 10. Hasil Uji Statistik Persen Stabilitas Ekstrak Etanol 70%, Fraksi n-heksan, Fraksi Etil Asetat, Fraksi Etanol 50% dan Na diklofenak pada Konsentrasi 1000 ppm………... 72
Lampiran 11. Hasil Uji Statistika Persen Stabilitas Fraksi Etil Asetat dan Na Diklofenak pada Konsentrasi 50, 100, 200, 400 dan 800 ppm 78
Lampiran 12. Perhitungan Nilai IC50 Fraksi Etil Asetat dan Na Diklofenak dengan Metode Analisa Probit ... 86
Lampiran 13 Foto-foto Alat Penelitian dan Proses Uji Aktivitas ……… 89
Lampiran 14. Gambar Penapisan Fitoimia ... 91
1.1Latar Belakang
Indonesia dikenal sebagai salah satu negara yang memiliki keanekaragaman
hayati terbesar (mega biodiversitas) di dunia setelah Brasil. Tercatat di hutan tropis
Indonesia ditemukan kurang lebih 30.000 dari 40.000 jenis tumbuhan di dunia
(Wulandari, 2001). Sekitar 9.600 jenis telah diketahui berkhasiat obat. Dari jumlah
tersebut tercatat 283 jenis merupakan tumbuhan obat penting bagi industri obat
tradisional. Dewasa ini penelitian dan pengembangan tumbuhan obat baik di dalam
maupun di luar negeri berkembang dengan pesat, terutama dalam bidang khasiat
farmakologisnya salah satunya sebagai antiinflamasi (Kusuma et al., 2005).
Peradangan (inflamasi) adalah respon protektif normal untuk cedera jaringan
dan melibatkan berbagai proses fisiologis di dalam tubuh seperti aktivasi enzim,
pelepasan mediator, diapedesis atau pergerakan sel darah putih melalui kapiler ke
daerah peradangan, migrasi sel, kerusakan dan perbaikan jaringan (Kumar et al.,
2012). Inflamasi adalah proses yang kompleks, yang sering dikaitkan dengan rasa
sakit dan melibatkan kejadian seperti peningkatan permeabilitas pembuluh darah,
peningkatan denaturasi protein dan perubahan membran (Leelaprakash & Mohan,
2011). Faktor yang dapat menyebabkan cedera pada jaringan, yang kemudian diikuti
oleh inflamasi adalah patogen, iritan kimia (asam dan basa kuat,fenol, racun) dan
iritan fisika (trauma,benda asing ,dingin, arus listrik, radiasi). Inflamasi adalah upaya
perlindungan tubuh untuk menghilangkan rangsangan merugikan serta memulai
proses penyembuhan untuk jaringan. Namun, jika peradangan (inflamasi) tidak
diobati menyebabkan timbulnya penyakit seperti rinitis vasomotor, rematoid artritis
dan aterosklerosis (R Ilakkiya et al., 2013).
Pada umumnya pengobatan yang dipakai untuk mengatasi terjadinya
(OAINS) dan steroid yang berguna untuk mengurangi pembengkakan dan rasa sakit
peradangan. Tetapi obat-obatan ini membawa risiko toksisitas gastrointestinal,
toksisitas jantung dan lainnya untuk penggunaan yang berkepanjangan. Untuk alasan
ini, ada kebutuhan untuk memiliki obat antiinflamasi dengan efek samping yang lebih
ringan saat digunakan untuk penyakit inflamasi kronis. Oleh karena itu, tumbuhan
lebih banyak dipilih sebagai obat alternatif dan alami untuk pengobatan berbagai
penyakit, tetapi masih kurangnya bukti ilmiah untuk khasiat tersebut (Madhavi et al.,
2012).
Salah satu tanaman yang sering digunakan dalam pengobatan adalah Moringa
oleifera Lam. (Syn. Moringa pterygosperma Gaertn.) atau pohon kelor. Khasiatnya
sebagai obat telah lama dikenal dalam sistem obat tradisional. Beberapa bagian
berbeda dari digunakan dalam pengobatan tradisional untuk berbagai penyakit seperti
rematik, kelumpuhan dan epilepsi.Selain itu ekstrak daun, biji, dan akar dari pohon
kelor telah dipelajari secara ekstensif untuk berbagai potensi penggunaan termasuk
antiinflamasi, antitumor, antihepatotoksik dan analgesik (Sashidhara et al., 2009).
Kandungan fitokimia dalam daun kelor yaitu tanin, steroid dan triterpenoid,
flavanoid, saponin, antraquinon, dan alkaloid. Flavonoid inilah yang mempengaruhi
berbagai macam aktivitas biologi atau farmakologi, diantaranya antioksidan,
antitumor, antiangiogenik, antiinflamasi, antialergik dan antiviral (Kasolo et al.,
2010).
Pada penelitian terdahulu ekstrak etanol daun kelor (M. oleifera) telah
dilaporkan memiliki aktivitas antiinflamasi pada dosis 500mg/ kgBB tikus putih
jantan dengan metode induksi karagenan (Singh et al., 2012), oleh karena itu perlu
dilakukan penelitian lanjutan yang akan memperkuat potensi dari tumbuhan tersebut
sebagai sumber senyawa antiinflamasi dengan menguji aktivitas stabilisasi atau
1.2Rumusan Masalah
Berdasarkan latar belakang diatas, maka dirumuskan masalah penelitian
sebagai berikut:
Apakah ekstrak daun kelor memiliki aktivitas anti-inflamasi secara in-vitro ditinjau
dari kemampuannya untuk menstabilisasi membran sel darah merah?
1.3Tujuan Penelitian
Tujuan dari penelitian ini adalah:
Mengetahui aktivitas ekstrak daun kelor (Moringa oleifera L.) terhadap stabilisasi
membran sel darah merah.
1.4 Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini adalah:
1. Sebagai pengetahuan dasar bagi peneliti lanjutan tentang aktivitas antiinflamasi
yang terdapat pada daun kelor.
2. Sebagai informasi ilmiah dasar pada bidang kimia bahan alam dan bidang
farmasi dalam upaya pengembangan senyawa aktif antiinflamasi pada tanaman
kelor.
3. Untuk memberikan latar belakang ilmiah (scientivic background) dari khasiat
BAB 2
TINJAUAN PUSTAKA
2.1 KELOR (Moringa oleifera L.) 2.1.1 Klasifikasi (USDA, 2013 )
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh)
Super Divisi : Spermatophyta (Menghasilkan biji)
Divisi : Magnoliophyta (Tumbuhan berbunga)
Kelas : Magnoliopsida (berkeping dua / dikotil)
Sub Kelas : Dilleniidae
Ordo : Capparales
Famili : Moringaceae
Genus : Moringa
Spesies : Moringa oleifera Lam
2.1.2 Sinonim
Anoma moringa (L.) Lour., Guilandina moringa L.,
Hyperanthera decandra Willd., Hyperanthera moringa (L.) Vahl,
Hyperanthera pterygosperma Oken, Moringa edulis Medic.,
Moringa erecta Salisb., Moringa moringa (L.) Small, Moringa
myrepsica Thell., Moringa nux-eben Desf., Moringa octogona
Stokes, Moringa oleifera Lour., Moringa parvifora Noronha,
Moringa polygona DC., Moringa pterygosperma Gaertn., Moringa
zeylanica Pers., Copaiba langsdorfi (Desf.) Kuntze, Copaifera nitida
2.1.3 Nama Daerah
Tanaman kelor memiliki banyak sebutan, diantaranya imaran,
kelintang (Jawa), murong (Sumatera), wona marungga, kelohe,
parangge, kewona (Nusa tenggara), rowe, kelo, wori (Sulawesi),
kanele, oewa herelo (Maluku). Diluar negeri dikenal dengan nama
drumstick tree, horseradish tree (Inggris), nugge (Kannada), la ken
(Cina), mungna, saijna, shajna (Hindi) (DepKes RI,1989 & Rollof,
2009).
2.1.4 Deskripsi
Kelor (Moringa oleifera L.) tumbuh dalam bentuk pohon,
berumur panjang (perenial) dengan tinggi 7 - 12 m. Batang berkayu
(lignosus), tegak, berwarna putih kotor, kulit tipis, permukaan kasar.
Percabangan simpodial, arah cabang tegak atau miring, cenderung
tumbuh lurus dan memanjang. Daun majemuk, bertangkai panjang,
tersusun berseling (alternate), beranak daun gasal (imparipinnatus),
helai daun saat muda berwarna hijau muda, setelah dewasa hijau tua,
bentuk helai daun bulat telur, panjang 1 - 2 cm, lebar 1 - 2 cm, tipis
lemas, ujung dan pangkal tumpul (obtusus), tepi rata, susunan
pertulangan menyirip (pinnate), permukaan atas dan bawah halus.
Bunga muncul di ketiak daun (axillaris), bertangkai panjang, kelopak
berwarna putih agak krem, menebar aroma khas. Buah kelor
berbentuk panjang bersegi tiga, panjang 20 - 60 cm, buah muda
berwarna hijau setelah tua menjadi cokelat, bentuk biji bulat
berwarna coklat kehitaman, berbuah setelah berumur 12 - 18 bulan.
Akar tunggang, berwarna putih, membesar seperti lobak.
Perbanyakan bisa secara generatif (biji) maupun vegetatif (stek
batang). Tumbuh di dataran rendah maupun dataran tinggi sampai di
Gambar 1. Akar, Daun dan Pohon Kelor [Navie, 2010]
2.1.5 Penyebaran
Asal tepat spesies ini tidak diketahui secara pasti karena telah
dibudidayakan secara luas sejak zaman dahulu. Tumbuhan ini
dimanfaatkan oleh Roma, Yunani dan Mesir kuno dan kini banyak
dibudidayakan di seluruh daerah tropis dan subtropis di dunia (Fahey,
2005).
Namun, M. oleifera dianggap tumbuhan asli untuk sub-wilayah
Himalaya India Utara. Hal ini juga umum ditemukan di seluruh
bagian lain di India serta di dataran Punjab, Sind, Baluchistan, dan di
daerah North West Frontier Province Pakistan, meskipun populasi
ini mungkin dihasilkan dari budidaya awal. Beberapa penulis juga
menganggapnya sebagai bagian asli dari Asia Barat (yaitu Oman,
Qatar, Arab Saudi, Uni Emirat Arab dan Yaman) dan bahkan Afrika
Utara. Moringa oleifera L. juga banyak naturalisasi di daerah tropis
lainnya di dunia. Telah dilaporkan di sebagian besar selatan dan
timur Asia termasuk Afganistan, Israel, Iran, Nepal, Banglades, Cina,
Taiwan, Sri Lanka, Myanmar, Malaysia, Filipina, Thailand, Vietnam,
Indonesia dan Papua New Guinea. Tumbuhan ini juga banyak
naturalisasi di sub-Sahara Afrika, termasuk di Zimbabwe,
Burkina Faso, Kamerun, Chad, Gambia, Ghana, Guinea, Kenya,
Liberia, Mali, Mauritania, Nigeria, Sierra Leone, Sudan, Ethiopia,
Somalia, Zaire, Togo, Uganda dan Senegal. Di Amerika tropis, kelor
dinaturalisasi di wilayah selatan-timur Amerika Serikat (yaitu
Florida), Karibia (yaitu Kuba, Haiti, Republik Dominika, Bahama,
Jamaika, Puerto Rico dan Kepulauan Virgin), Meksiko, Amerika
Tengah (yaitu Belize, Kosta Rika, El Salvador, Guatemala,
Honduras, Nikaragua dan Panama) dan Amerika Selatan (yaitu
Colombia, Guyana, Venezuela,Brazil dan Paraguay). Kelor juga
dinaturalisasi di pulau-pulau Pasifik, termasuk Kiribati, Guam,
Kepulauan Marshall, Kepulauan Mariana Utara, Kepulauan Solomon
dan Amerika Federasi Mikronesia (Navie & Steve, 2010).
2.1.6 Kandungan Kimia
Daun kelor kaya asam askorbat, asam amino, sterol, glukosida
isoquarsetin, karoten, ramentin, kaemperol dan kaemferitin. Hasil
analisis nutrien juga melaporkan adanya kandungan senyawa-senywa
berikut: 6,7 mg protein, 1,7 mg lemak (ekstrak eter), 13,4 mg
karbohidrat, 0,9 mg serat dan 2,3% bahan mineral: 440 mg kalsium,
70 mg fosfor, dan besi 7,0 mg/100 g daun. Daun kelor juga
mengandung 11.300 IU karoten (prekursor vitamin A), vitamin B,
220 mg vitamin C dan 7,4 mg tokoferol /100g daun. Daun kelor juga
mengandung substansi estrogenik dan esterase pektin. Asam amino
esensial yang terdapat dalam protein daun adalah (/16g daun): 6,0 mg
arginin, 2,0 mg metionin, 4,9 mg treonin, 9,3 mg leusin, 6,3 mg
Tabel 1. Kandungan kimia yang diisolasi dari Moringa oleifera L.
Bagian Kandungan Kimia
Akar 4-(α-L-rhamnopiranoksiloksi)-benzilglukosinolat dan benzilglukosinolat
Batang 4-hidroksimellein, vanillin, β-sitosteron, asam oktacosanik dan β-sitosterol
Kulit kayu 4-(α-L-rhamnopiranosiloksi)-benzilglukosinolat
Eksudat gum L-arabinosa, D-galaktosa,asam D-glukuronat, L-rhamnosa, D-mannosa, D-xylosa dan leukoantosianin
Daun Glikosida niazirin, niazirinin dan three mustard oil glycosides, 4-[4’-O-asetil- α -L-rhamnosiloksi) benzil] isothiosianat, niaziminin A dan B
Bunga yang matang D-mannosa, D-glukosa, protein, asam askorbat, polisakarida
Keseluruhan biji Nitril, isotiosianat, tiokarbanat, 0-[2’-hidroksi-3’-(2’’ -hepteniloksi)]-propilundekanoat, 0-etil-4-[( α
-1-ramnosiloksi)-benzil] karbamat, metil-p-hidroksibenzoat dan β-sitosterol
Biji yang tua Crude protein, Crude fat, karbohidrat, metionin, sistein,
4-(α-L-ramnopiranosiloksi)-benzilglukosinolat,
benzilglukosinolat, moringin, mono-palmitat and di-oleic trigliserida
Minyak biji Vitamin A, beta karoten, prekursor Vitamin A
Sumber : [Singh et al., 2012]
2.1.7 Khasiat
Selain digunakan untuk bahan makanan, daun kelor telah
dilaporkan menjadi sumber yang kaya akan makronutrien maupun
mikronutrien yang juga mengandung β-karoten, protein, vitamin C,
Buah dan daun telah digunakan untuk mengatasi malnutrisi, terutama
di kalangan bayi dan ibu menyusui untuk meningkatkan produksi
susu dan juga mengatur ketidakseimbangan hormon tiroid (Luqman
et al., 2012).
Sejumlah khasiat obat dihubungkan dengan berbagai bagian
dari M.oleifera telah diakui oleh sistem pengobatan Ayurveda dan
Unani. penerapan tanaman ini telah ditemukan secara luas dalam
pengobatan penyakit kardiovaskular antara lain dalam akar, daun,
gum, bunga, dan infus biji mengandung glikosida nitril, mustard oil,
dan glikosida tiokarbamat sebagai kandungan kimia yang dianggap
bertanggung jawab untuk aktivitas diuretik, menurunkan kolesterol,
antiulser, hepatoprotektif, dan sebagai pelindung kardiovaskular.
Tanaman ini juga memiliki aktivitas antimikroba karena mengandung
pterigospermin sebagai komponen utama. Ekstrak daun segar
diketahui menghambat pertumbuhan patogen pada manusia
(Staphylococcus aureus dan Pseudomonas aeruginosa). Kandungan
kimia dari berbagai bagian pohon seperti; niazimin, niaiminin,
berbagai karbamat dan tiokarbamat telah menunjukkan aktivitas
antitumor in vitro. Bagian bunga menunjukkan aktivitas
hepatoprotektif yang efektif. Karena adanya efek kuarsetin. Biji dapat
digunakan sebagai biosorben untuk menghilangkan kadmium dari
medium cair dan merupakan salah satu koagulan alami. Kelor juga
dianggap sebagai antipiretik, dan dilaporkan menunjukkan aktivitas
antimikroba (Luqman et al., 2012).
Materia medika Indonesia menjelaskan penggunaan akar kelor
(M.oleifera) dalam pengobatan sejumlah penyakit, termasuk asma,
asam urat, sakit pinggang, rematik, pembesaran limpa atau hati,
radang internal yang terdapat dalam inflamasi dan adanya batu pada
sebagai diuretik dan aktivitas antiinflamasi akut (Sashidhara et al.,
2009)
Semua bagian dari pohon dianggap berkhasiat obat dan
digunakan dalam pengobatan asites, rematik, dan gigitan hewan
berbisa serta sebagai stimulan jantung dan peredaran darah. Daun
kelor kaya Vit. A dan C dan dianggap berguna untuk sariawan dan
kataral, mereka juga digunakan sebagai emetik. Sebuah pasta dari
daun digunakan secara eksternal untuk luka. Bunga digunakan
sebagai tonik dan anti diuretik. Biji kelor sebagai antipiretik. Minyak
biji digunakan sebagai antiinflamasi dalam rematik dan asam urat.
Bunga-bunga, daun, dan akar yang digunakan dalam obat tradisional
untuk tumor serta biji untuk tumor abdominal. Rebusan akar
digunakan di Nikaragua untuk mengobati edema (pembengkakan).
Sari dari akar diterapkan secara eksternal sebagai obat gosok. Daun
juga bisa digunakan untuk sakit kepala, dan dikatakan memiliki sifat
pencahar alami. Kulit, daun dan akar yang pedas dan berbau tajam,
dan diambil untuk meningkatkan proses pencernaan. Minyak agak
berbahaya jika diminum, namun dapat diterapkan secara eksternal
untuk penyakit kulit. Kulit kayu dianggap sebagai antiskorbut, dan
mengeluarkan gum kemerahan dengan sifat seperti tragakan dan
kadang-kadang digunakan untuk diare. Akar yang pahit, sebagai
tonik bagi tubuh dan paru-paru, dan juga berguna sebagai pemicu
menstruasi (emmenagogue) dan ekspektoran (Kumar et al., 2012).
2.2. EKSTRAKSI DAN FRAKSINASI 2.2.1. Ekstraksi
Ekstraksi merupakan suatu cara untuk mengambil atau menarik
yang sesuai. Ekstraksi yang benar dan tepat tergantung dari jenis
senyawa, tekstur dan kandungan air bahan tumbuhan yang akan
diekstraksi. Dalam mengekstraksi suatu tumbuhan sebaiknya
menggunakan jaringan tumbuhan yang masih segar, namun
kadang-kadang tumbuhan yang akan dianalisis tidak tersedia di tempat
sehingga untuk itu jaringan tumbuhan yang akan diekstraksi dapat
dikeringkan terlebih dahulu (Kristanti, 2008).
Ektraksi serbuk kering jaringan tumbuhan dapat dilakukan
secara maserasi, perkolasi, refluks atau sokhletasi dengan
menggunakan pelarut yang tingkat kepolarannya berbeda-beda. Teknik
ekstraksi yang akan digunakan dalam penelitian ini adalah teknik
maserasi (Kristanti et al., 2008).
Maserasi adalah proses perendaman sampel untuk menarik
komponen yang kita inginkan, dengan kondisi dingin diskontinyu.
Keuntungan dari maserasi adalah lebih praktis, pelarut yang digunakan
lebih sedikit dibandingkan perkolasi dan tidak memerlukan
pemanasan, sedangkan kekurangannya adalah waktu yang dibutuhkan
lebih lama. Filtrat yang diperoleh dari proses tersebut diuapkan dengan
alat penguap putar vakum (vacuum rotary evaporator) hingga
menghasilkan ekstrak pekat (Kristanti et al., 2008).
2.2.2. Fraksinasi (Partisi Cair-Cair)
Fraksinasi merupakan prosedur pemisahan yang bertujuan
untuk memisahkan golongan utama kandungan yang satu dari
kandungan yang lain. Senyawa yang bersifat polar akan masuk ke
pelarut polar dan senyawa non polar akan masuk ke pelarut non polar.
Bila kita menelaah profil fitokimia lengkap dari suatu jenis tumbuhan,
memisahkan golongan utama kandungan yang satu dari golongan
utama yang lainnya (Harborne, 1987).
2.3. Skrining Fitokimia
Metode identifikasi dilakukan berdasarkan metode penapisan fitokimia
(phytochemical screening). Penapisan fitokimia dilakukan untuk mengetahui
kandungan metabolit sekunder yang terkandung disimplisia tersebut.
Pengujian ini merupakan pengujian pendahuluan yang biasa dilakukan
sebelum dilakukan pengujian-pengujian lanjutan. Adanya pengetahuan
mengenai kandungan senyawa metabolit sekunder yang terkandung di dalam
suatu ekstrak, akan memudahkan dalam identifikasi kemungkinan aktivitas
dari ekstrak tumbuhan yang digunakan, seperti flavonoid, alkaloid, saponin,
tanin, dan antrakuinon (Putra, 2007).
2.3.1 Alkaloid
Alkaloid secara umum mengandung paling sedikit satu buah
atom nitrogen yang bersifat basa dan merupakan bagian dari cincin
heterosiklik (Putra, 2007). Banyak tumbuhan yang digunakan untuk
pengobatan yang setelah diisolasi berupa senyawa nitrogen
heterosiklik (Fessenden, 1982b). Senyawa alkaloid merupakan
senyawa organik terbanyak ditemukan di alam. Hampir seluruh
alkaloid berasal dari tumbuhan dan tersebar luas dalam berbagai jenis
tumbuhan (Putra, 2007).
Ada sekitar 5500 macam alkaloid yang telah diketahui.
Alkaloid merupakan golongan metabolit sekunder yang terbesar.
Alkaloid bersifat racun bagi manusia namun banyak yang mempunyai
kegiatan fisiologi menonjol sehingga digunakan secara luas dalam
bidang pengobatan. Uji organoleptik sering dilakukan untuk menguji
adanya kandungan alkaloid dalam daun atau buah segar yang dideteksi
2.3.2 Flavonoid
Senyawa flavonoid adalah suatu kelompok senyawa fenol
terbesar yang ditemukan di alam. Senyawa-senyawa ini merupakan zat
warna merah, ungu, dan biru dan kuning yang ditemukan dalam
tumbuhan. (Lenny, 2006).
Dalam tumbuhan flavonoid terikat pada gula sebagai glikosida
dan aglikon flavonoid yang mungkin terdapat dalam satu tumbuhan
dalam bentuk kombinasi glikosida (Harbone, 1987). Aglikon
flavonoid (yaitu flavonoid tanpa gula terikat) terdapat dalam berbagai
bentuk struktur (Markham, 1988).
Flavonoid merupakan salah satu dari sekian banyak senyawa
metabolit sekunder yang dihasilkan oleh suatu tanaman, yang bisa
dijumpai pada bagian daun, akar, kayu, kulit, tepung sari, bunga dan
biji. Secara kimia, flavonoid mengandung cincin aromatik tersusun
dari 15 atom karbon dengan inti dasar tersusun dalam konjugasi
C6-C3-C6 (dua inti aromatik terhubung dengan 3 atom karbon yang
merupakan rantai alifatik) (Lenny, 2006), seperti ditunjukkan pada
Gambar 2.
Gambar 2 : Struktur Umum Flavonoid
2.3.3 Saponin
Saponin mula-mula diberi nama demikian karena sifatnya yang
menyerupai sabun yaitu ketika menimbulkan busa bila dikocok dalam
air. Senyawa saponin merupakan senyawa golongan glikosida yang
apabila dihidrolisis secara sempurna akan didapatkan gula dan satu
ini secara sederhana dapat dilakukan dengan pengocokan, busa stabil
setinggi satu sampai sepuluh sentimeter dalam sepuluh menit
menandakan hasil positif dari senyawa saponin (Harborne, 1987).
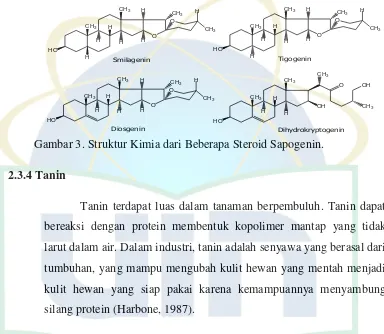
Gambar 3. Struktur Kimia dari Beberapa Steroid Sapogenin.
2.3.4 Tanin
Tanin terdapat luas dalam tanaman berpembuluh. Tanin dapat
bereaksi dengan protein membentuk kopolimer mantap yang tidak
larut dalam air. Dalam industri, tanin adalah senyawa yang berasal dari
tumbuhan, yang mampu mengubah kulit hewan yang mentah menjadi
kulit hewan yang siap pakai karena kemampuannya menyambung
silang protein (Harbone, 1987).
Tanin merupakan senyawa polifenol yang berarti termasuk
dalam senyawa fenolik. Terdapat 2 jenis utama tanin yaitu, tanin
terkondensasi yang tersebar pada paku-pakuan, angiosperma, dan
gymnospermai. Dan tanin terhidrolisis yang terdapat pada tumbuhan
berkeping dua (Harbone, 1987).
2.3.5. Antrakuinon
Antrakuinon merupakan golongan kuinon (3 cincin benzena
berdampingan) yang terbanyak tersebar di alam. Beberapa antrakuinon
tumbuhan tinggi dihidroksilasi pada atom C-1 dan antrakuinon
terhidroksilasi jarang terdapat dalam tumbuhan secara bebas tetapi
sebagai glikosida. Dalam banyak kasus tampaknya aglikon dari
glikosidanya berbentuk antrakuinon tereduksi dikenal sebagai antron
(Guevara & Recio, 1985).
Turunan antrakuinon biasanya merupakan senyawa berwarna
merah jingga yang larut dalam air panas dan alkohol encer,
memberikan warna yang spesifik dengan basa (LOH) seperti, merah,
violet dan hijau. Secara spektrofotometri antrakuinon memberikan pita
resapan yang berbeda dengan senyawa kuinon lainnya, dimana
memberikan 4 atau 5 pita resapannya pada daerah UV dan sinar
tampak (Guevara & Recio, 1985).
2.4 INFLAMASI 2.4.1 Definisi
Inflamasi adalah reaksi jaringan tubuh tehadap luka, seperti
trauma fisik, benda asing, zat kimia, pembedahan, radiasi, atau arus
listrik. Tujuan akhir dari respon inflamasi adalah menarik protein
plasma dan fagosit ke tempat yang mengalami cedera atau terinvasi agar
keduanya dapat mengisolasi, menghancurkan, atau menginaktifkan
antigen yang masuk, membersihkan debris dan mempersiapkan jaringan
untuk proses penyembuhan (Robbins, 2007).
Gejala-gejala klinis dari inflamasi adalah rubor (kemerahan),
kalor (panas), tumor (pembengkakan), dolor (nyeri) dan functio laesa
(kehilangan fungsi). Kemerahan dan rasa panas disebabkan oleh dilatasi
pembuluh darah arteriol dengan demikian darah lebih banyak mengalir
kedalam mikrosirkulasi lokal. Kalor atau panas terjadi bersamaan
sekelilingnya sebab darah disalurkan lebih banyak ke daerah tersebut
dibandingkan dengan daerah tubuh normal lainnya. Tumor atau
pembengkakan disebabkan oleh air, protein dan zat-zat lain dari darah
bergerak ke jaringan yang mengalami inflamasi. Rasa sakit terjadi
karena ujung sel saraf terstimulasi oleh kerusakan langsung jaringan
(terjadi perubahan pH dan konsentrasi lokal ion-ion tertentu) dan
beberapa mediator inflamasi untuk menghasilkan sensasi rasa sakit. Di
samping itu, peningkatan tekanan di jaringan yang disebabkan oleh
udem dan akumulasi nanah, juga dapat menyebabkan rasa sakit.
Terbatasnya pergerakan oleh karena udem, rasa sakit dan destruksi
jaringan menyebabkan gangguan fungsi (Price & Lorraine, 2006).
2.3.2. Mekanisme Inflamasi Akut
Terdapat dua stadium pada reaksi inflamasi akut, yaitu vaskular
dan selular. Stadium vaskular pada respon inflamasi dimulai segera
setelah jaringan mengalami cedera. Arteriol di daerah tersebut
berdilatasi, sehingga terjadi peningkatan aliran darah ke tempat cedera.
Hal ini menyebabkan timbulnya gejala rubor (kemerahan) dan kalor
(panas). Vasodilatasi ini terutama akibat pelepasan bahan kimia dari
degranulasi sel mast dan pelepasan mediator-mediator kimia lain selama
inflamasi. Peningkatan aliran darah lokal tersebut menyebabkan lebih
banyak leukosit fagositik dan protein plasma yang tiba di tempat cedera.
Pada waktu yang bersamaan, histamin dan mediator kimia yang
dibebaskan selama inflamasi menyebabkan membesarnya pori-pori
kapiler (ruang antar sel endotel), sehingga permeabilitas kapiler
meningkat. Protein plasma yang dalam keadaan normal tidak dapat
keluar dari pembuluh darah dapat lolos ke ruang interstisium.
Peningkatan tekanan osmotik koloid di ruang interstisium yang
disebabkan oleh kebocoran protein plasma dan peningkatan tekanan
udem lokal yang disebut juga turgor (pembengkakan) (Corwin &
Elizabeth, 2008).
Stadium selular dimulai setelah peningkatan aliran darah ke
bagian yang mengalami cedera. Leukosit dan trombosit tertarik ke
daerah tersebut karena bahan kimia yang dilepaskan oleh sel yang
cedera, sel mast dan produksi sitokin. Penarikan leukosit yang meliputi
nuetrofil dan monosit ke daerah cedera disebut kemotaksis. Satu jam
setelah cedera, daerah yang cedera sudah dipadati oleh leukosit yang
keluar dari pembuluh darah. Neutrofil adalah sel yang pertama kali tiba
kemudian diikuti oleh monosit yang dapat membesar dan berubah
menjadi makrofag dalam periode delapan sampai dua belas jam
berikutnya. Emigrasi leukosit dari darah ke jaringan melibatkan proses
marginasi, diapedesis dan gerakan amuboid. Marginasi adalah
melekatnya leukosit darah, terutama neutrofil dan monosit ke bagian
dalam lapisan endotel kapiler pada jaringan yang cedera. Leukosit
segera keluar dari darah ke dalam jaringan dengan berprilaku seperti
amuba dan menyelinap melalui pori-pori kapiler yang disebut
diapadesis. Gerakan leukosit ini juga dibantu oleh adanya kemokin,
yaitu suatu mediator kimiawi yang bersifat kemotaksis yang dapat
menarik leukosit ke daerah inflamasi. Neutrofil dan makrofag
membersihkan daerah yang meradang dari zat toksik dan debris jaringan
dengan cara fagositosis. Setelah sel-sel fagositik memasukkan benda
sasaran, terjadi fusi lisosom dengan membran yang membungkus benda
tersebut dan lisosom mengeluarkan enzim hidrolitiknya ke dalam
vesikel dalam membrane tersebut, sehingga benda yang terperangkap
dapat diuraikan. Trombosit yang masuk ke daerah cedera merangsang
pembekuan untuk mengisolasi infeksi dan mengontrol pendarahan.
Sel-sel yang tertarik ke daerah cedera akhirnya akan berperan melakukan
Gambar 4. Skema Mekanisme Radang (Pringgoutomo, 2002).
2.3.3. Penyebab Inflamasi
Inflamasi disebabkan oleh beberapa faktor, yaitu :
1) Mikroorganisme (infeksi bakteri, virus, jamur, protozoa dan ragi)
2) Iritan kimia (asam dan basa kuat, fenol, racun)
3) Iritan fisika (trauma, benda asing, dingin, arus listrik, radiasi)
4) Jaringan nekrosis
5) Semua jenis reaksi imunologis : hipersensitifitas, kompleks imun,
autoimun (Rubbin, 1988). Statis
Stimulasi Saraf Mediator
Luka (jejas)
Dilatasi pembuluh
↑ permeabilitas
eksudasi ekstraseluler (leukosit&fibrinogen)
Koloid osmotik diluar pembuluh darah
Retardasi marginisasi
Trombosis
Emigrasi leukosit
Enzim proteolitik
Kemotaksis
2.3.4. Tipe Inflamasi
Secara umum inflamasi dibagi menjadi:
1) Inflamasi akut, yaitu inlamasi dengan durasi relatif lebih singkat
bertahan untuk beberapa jam atau satu sampai dua hari.
Karakteristik utamanya berupa adanya cairan eksudat dari protein
plasma (udem) dan migrasi dari leukosit, terutama neutrofil.
2) Inflamasi kronis, yaitu inflamasi dengan durasi lebih lama. Secara
histologi dihubungkan dengan adanya limfosit dan makrofag, serta
poliferasi pembuluh darah dan jaringan ikat (Pringgoutomo, 2002).
Berdasarkan pada karakteristik utama inflamasi kronik dan akut, dapat
dibedakan menurut jenis eksudat dan variabel morfologi :
1) Inflamasi serosa, yaitu inflamasi yang ditandai dengan
melimpahnya cairan encer, tergantung dari daerah luka dapat
berasal dari serum darah atau sekresi sel mesotel yang terhubung
dengan peritoneum, pleura dan perikardium.
Contoh : luka bakar dan efusi pleura
2) Inflamasi kataral, yaitu inflamasi permukaan ditandai dengan
meningkatnya sekresi mukus, pada mukosa terutama pada saluran
pernafasan. Inflamasi ini terlihat pada penyakit flu dan berbagai
bentuk kolitis.
3) Inflamasi fibrinosa, yaitu inflamasi yang menghasilkan eksudat
protein plasma dalam jumlah besar, termasuk fibrinogen dan
endapan fibrin. Karakteristik utama, respon inflamasi melibatkan
rongga-rongga tubuh seperti pleura, perikardium dan peritoneum.
Contoh : pneumonia, karditis rheumatika.
4) Inlamasi supuratif / purulenta, yaitu inflamasi yang ditandai oleh adanya produksi nanah dalam jumlah besar atau eksudat purulen,
biasanya terjadi pada infeksi bakteri piogenik.
5) Ulser, yaitu defek lokal pada permukaan organ atau jaringan, yang
dihasilkan oleh terkelupasnya jaringan nekrotik terinflamasi
(Robbins et al., 2007).
2.3.5. Mediator Inflamasi
Sejak penemuan Lewis mengenai histamin, banyak penelitian
lain yang dilakukan terhadap zat-zat yang berperan dalam proses
inflamasi. Mediator inlamasi dapat berasal dari plasma, sel atau
jaringan yang rusak. Mediator inflamasi dibagi dalam beberapa
kelompok :
1) Vasoaktif amin : histamin dan serotonin
2) Konstituen lisosomal : protease
3) Metabolit asam arakidonat
a. Melalui sikolooksigenase : prostaglandin, endoperoksida,
tromboksan A2
b. Melalui lipooksigenase : leukotrin, 5-HPETE, 5-HETE
4) Platelet activating factor (PAF)
5) Sitokin dan radikal bebas derivat oksigen
6) Plasma protease
- Sistem kinin : bradikinin dan kalikrein - Sistem komplemen : C3a, C5a, C5b-C9
Gambar 5. Mediator Inlamasi (Cotran, 1992)
Beberapa mediator inlamasi yang penting :
1) Histamin dan serotonin
Berperan pada pertengahan fase aktif dalam peningkatan
permeabilitas pembuluh darah. Pada manusia, histamin disimpan
dan tersedia dalam jumlah besar pada granul sel mast dan basofil
serta platelet. Golongan amin menyebabkan vasodilatasi dan
meningkatkan permeabilitas venula. Histamin bekerja pada
mikrosirkulasi terutama melalui reseptor jenis H1 dengan durasi
selama 60 menit.
Banyak faktor yang menyebabkan pelepasan amin dari sel mast,
antara lain :
a) Faktor fisik (trauma atau dingin)
b) Reaksi imunologis melalui mekanisme yang melibatkan
ikatan pada permukaan sel mast dengan IgE.
c) C3a dan C5a, yaitu fragmen dari komplemen yang
menginduksi peningkatan permeabilitas pembuluh
darah
d) Histamine-releasing factors dari neutrofil, monosit dan
platelet
-Radikal bebas derivat oksigen
e) Interleukin-1
2) C3a dan C5a
Disebut juga sebagai anafilatoksin, komplemen-komplemen yang
meningkatkan permeabilitas pembuluh darah. C3a dapat secara
langsung mengalami cleaving oleh plasmin, bakterial protease dan
enzim C3-cleaving yang tersebar di berbagai jaringan. C5a
merupakan zat kemotaksis tinggi terhadap netrofil, eosinofil,
basofil dan monosit yang dilepaskan oleh aktivasi komplemen
melalui tripsin, bakteri protease dan enzim pada netrofil serta
makrofag.
3) Bradikinin
Zat yang sangat poten meningkatkan permeabilitas pembuluh
darah, juga menyebabkan kontraksi otot polos, dilatasi pembuluh
darah dan rasa sakit ketika diinjeksikan pada kulit. Bradikinin
bukan merupakan zat kemotaksis, diaktivasi oleh faktor XII sistem
pembekuan darah intrinsik, melalui kontak permukaaan bahan
aktif seperti kolagen, membran basal dan endokrin.
4) Prostaglandin
Merupakan suatu zat autokoid, dibentuk dengan cepat dan bekerja
secara lokal, hilang secara spontan atau melalui proses enzimatis.
Prostaglandin berasal dari biosintesis asam arakidonat jalur
siklooksigenase membentuk prostaglandin endoperoksida PGG2
selanjutnya diubah secara enzimatis menjadi PGH2. Dari PGH2
diubah lagi secara enzimatis menjadi :
a) Tromboksan A2 (TXA2)
Ditemukan pada platelet dan sel lainnya, memiliki masa
hidup yang singkat (waktu paruh dalam detik), poten sebagai
penghambat agregator platelet dan konstriktor pembuluh
b) Prostasilkin (PGI2)
Ditemukan pada dinding pembuluh darah, poten sebagai
penghambat agregasi platelet dan vasodilator.
c) PGE2, PGF2 dan PGD2
Memiliki kerja yang bervariasi terhadap permeabiltas
pembuluh darah.
Gambar 6. Metabolisme Asam Arakhidonat dan Mediator Peradangan
[Price & Lorraine, 2006].
2.4. OBAT ANTIINFLAMASI
2.4.1. Obat antiinflamasi steroid
Kortikosteroid disintesis secara alami di korteks adrenal dan
merupakan hasil biosintesis dari kolesterol, dengan contoh
hidrokortison dan kortison, yang banyak digunakan untuk pengobatan
Bentuk-bentuk semi sintesis dari hormon ini lebih banyak digunakan
antara lain deksametason dan prednison. Mekanisme kerja
antiinflamasi steroid adalah menghambat pelepasan prostaglandin dari
membran sel dengan cara membatasi ketersediaan substrat asam
arakidonat.
Antiinflamasi ini juga mengurangi ketersediaan substrat untuk
enzim lain yang memetabolisir asam arakidonat seperti lipoksigenase
yang tidak terhambat oleh aspirin dan obat jenis lainnya. (Gilman et
al., 1985).
2.4.2. Obat Antiinflammasi Non-steroid
Obat-obat yang termasuk golongan ini adalah asam salisilat,
indometasin, asam mefenamat, fenilbutason dan diklofenak.
Mekanisme kerja obat ini adalah menahan migrasi dari
mediator-mediator inflamasi, menghambat pembentukan mediator-mediator inflamasi dan
mengurangi aktivitas protease inflamasi. Obat-obat tersebut juga
diyakini menghambat fosfolirasi oksidatif yang meniadakan energi
metabolisme yang diperlukan oleh jaringan inflamasi. (Gilman et al.,
1985).
2.5. UJI AKTIVITAS ANTIINFLAMASI
Terdapat berbagai metode yang digunakan dalam studi obat,
kandungan kimia dan preparasi herbal untuk menunjukkan adanya aktivitas
atau potensi anti-inflamasi. Tekhnik- tekhnik tersebut termasuk pelepasan
fosforilasi oksidatif (ATP biogenesis terkait dengan respirasi), penghambatan
denaturasi protein, stabilisasi membran eritrosit, stabilisasi membran
lisosomal, tes fibrinolitik dan agregasi trombosit (Oyedapo et al., 2010).
2.5.1. Metode Stabilisasi Membran Sel Darah Merah Manusia
Membran sel darah merah manusia atau eritrosit adalah analog
dengan membran lisosomal dan stabilisasi nya menunjukkan bahwa
ekstrak dapat juga menstabilkan membran lisosomal. Stabilisasi
membran lisosomal penting dalam membatasi respon inflamasi dengan
menghambat pelepasan konstituen lisosomal dari neutrofil aktif seperti
enzim bakterisida dan protease, yang menyebabkan peradangan dan
kerusakan jaringan lebih lanjut atas extra cellular release (Kumar et al.,
2012). Enzim lisosomal dilepaskan selama peradangan yang akan
menghasilkan berbagai gangguan yang mengarah ke cedera jaringan
dengan merusak makromolekul dan peroksidasi lipid membran yang
dianggap bertanggung jawab untuk kondisi patologis tertentu seperti
serangan jantung, syok septik dan rheumatoid arthritis dll. Kegiatan
enzim ekstra selular ini dikatakan berhubungan dengan peradangan akut
atau kronis (Chippada et al., 2011).
Luka pada membran lisosom biasanya memicu pelepasan
fosfolipase A2 yang menjadi perantara hidrolisis fosfolipid untuk
menghasilkan mediator inflamasi. Stabilisasi membran sel-sel ini
menghambat lisis sel dan pelepasan isi sitoplasma yang akhirnya
membatasi kerusakan jaringan dan memperburuk respon inflamasi. Oleh
membran harus memberikan perlindungan yang signifikan dari
membran sel terhadap pelepasan zat merugikan.(Karunanithi et al.,
2012).
Eritrosit telah digunakan sebagai sistem model untuk beberapa
studi interaksi obat dengan membran. Obat seperti anestesi, tranquilizer
dan antiinflamasi steroid menstabilkan membran eritrosit terhadap
induksi hipotonik pemicu hemolisis sehingga dapat mencegah pelepasan
hemoglobin. Aktivitas menstabilkan membran sel darah merah yang
diperlihatkan oleh beberapa obat, berfungsi sebagai metode in vitro
untuk menilai aktivitas antiinflamasi dari berbagai senyawa (Awe et al.,
2009).
Sebuah penjelasan yang mungkin bisa dihubungkan dengan
kaitan membran eritrosit dengan perubahan muatan permukaan sel yang
mungkin telah mencegah interaksi fisik dengan agen agregasi atau
mendorong penyebaran dengan adanya gaya tolakan menolak seperti
yang terlibat dalam hemolisis sel darah merah (Oyedapo et al., 2010).
2.6. SPEKTROFOTOMETER UV-VIS
Spektrofotometer telah digunakan pada 35 tahun terakhir dan menjadi yang paling instrumen analitis yang cukup penting di laboratorium kimia
modern (Greenlief, 2004). Spektrofotometri serap merupakan pengukuran
interaksi antara radiasi elektromagnetik panjang gelombang tertentu yang
sempit dan mendekati monokromatik, dengan molekul atau atom dari suatu
zat kimia (Sastroamidjojo, 1985). Metode pengukuran dengan
spektrofotometri ini mudah dilakukan, murah, terandalkan dan memberikan
presisi yang baik untuk melakukan pengukuran kuantitatif obat-obatan dan
Spektrum absorpsi daerah ini adalah sekitar 220 nm sampai 800 nm dan
dinyatakan sebagai spektrum elektron. Suatu spektrum ultraviolet meliputi
daerah bagian ultraviolet (190-380 nm), spektrum Visible bagian sinar tampak
(380-780 nm).
Pengukuran dengan alat spektrofotometer UV-Vis didasarkan pada
hubungan antara berkas radiasi elektromagnetik yang ditransmisikan
(diteruskan) atau yang diabsorpsi dengan tebalnya cuplikan dengan
konsentrasi dari komponen penyerap (Sastroamidjojo, 1985). Hubungan
antara intensitas, tebal medium dan konsentrasi zat digambarkan dengan
persamaan yang sesuai dengan Hukum Lambert-Beers, yakni :
Keterangan :
A : Serapan
a : Daya serap
b : Tebal kuvet
c : Konsentrasi larutan
Instrument dari spektrofotometer UV-Vis ini dapat diuraikan sebagai berikut:
Gambar 8. Skema Spektrofotometer UV-VIS
1. Suatu sumber cahaya polikromatis di daerah panjang gelombang yang di
kehendaki.
2. Suatu monokromator merupakan sebuah alat untuk menguraikan berkas
radiasi dari sumber yang polikromatis menjadi sinar yang monokhromatis
(panjang gelombang tunggal). A = a . b . c
Monokromator Kuvet Detektor Amplifier
Rekorder Sumber
3. Kuvet merupakan suatu wadah untuk menempatkan sampel
4. Detektor, berupa transduser berfungsi untuk menangkap cahaya yang
diteruskan dari sampel dan mengubahnya menjadi arus listrik.
5. Amplifier (pengganda) dan rangkaian yang berkaitan yang membuat arus
listrik itu memadai untuk dibaca. Berguna untuk menangkap isyarat arus
listrik yang masuk (imput) dari rangkaian detektor dan melalui beberapa
proses elektronik tertentu kemudian menghasilkan suatu arus listrik keluar
(output) yang beberapa kali lebih besar dari imput.
6. Rekorder merupakan sistem baca yang menagkap besarnya arus listrik
3.1. Tempat dan Waktu Penelitian
Penelitian dilaksanakan mulai bulan Februari-Juli 2013 di
Laboratorium Produk Alam, Bidang Botani dan Mikrobiologi Pusat Penelitian
Biologi, Lembaga Ilmu Pengetahuan Indonesia (LIPI) yang berada di Jalan
Raya Jakarta–Bogor Km 46, Cibinong serta di Laboratorium Pharmacy
Medicinal Chemistry (PMC) dan Pharmacy Sterile Technology (PST), FKIK
UIN Syarif Hidayatullah Jakarta, Ciputat.
3.2. Bahan
3.2.1 Bahan Uji
Bahan uji yang digunakan adalah daun kelor (Moringa oleifera
L.)dikumpulkan dari kota Cilegon, Banten pada bulan Januari-Februari
2013. Tanaman sebelumnya dideterminasi di Herbarium Bogoriense,
Pusat Penelitian Biologi LIPI, Bogor, Jawa Barat.
3.2.2 Bahan Kimia
Bahan-bahan yang digunakan dalam penelitian ini adalah
dekstrosa, Na sitrat, asam sitrat, NaCl, dapar fosfat pH 7,4 (0,15 M), Na
diklofenak, DMSO (Dimethyl Sulfoxide), serbuk magnesium, HCl Pekat,
amil alkohol, HCl (2N), FeCl3 (1%), kloroform, NH4OH, H2SO4 (1M),
pereaksi Mayer, pereaksi Dragendorff, pereaksi Lieberman-Bourchard,
3.3. Alat
Alat-alat yang digunakan dalam penelitian ini adalah timbangan
bahan, labu erlenmeyer, labu ukur, corong pisah, corong, alat destilasi,
perkolator, grinder, botol kaca, botol vial, batang pengaduk, spatula, pipet
tetes besar, pipet volume 5 & 10 ml, mikropipet (Effendorf Reference)
200µL, Autoclave, oven, centrifuge (Hettich EBA 85), rotary evaporator
(Eyela N-1000), ultrasonic cleaner (WT-600-40), water bath (Eyela
SB-1000).
3.4. Prosedur Kerja
3.4.1 Penyiapan Simplisia
Penyiapan simplisia daun kelor dilakukan sortasi kering, kemudian
dicuci dengan air mengalir, lalu di lanjutkan dengan sortasi basah untuk
membersihkannya dari kotoran. Selanjutnya daun kelor dikering-anginkan
sampai didapat sampel kering, kemudian dibubukkan dengan menggunakan
grinder dan siap digunakan untuk pekerjaan selanjutnya.
3.4.2.Ekstraksi
3. 4.2.1 Maserasi dengan Pelarut Etanol 70%
Serbuk daun kelor sebanyak 700 gr dimasukkan ke dalam alat
perkolator, dimana bagian bawah alat ini telah dialasi dengan kapas.
Kemudian dimasukkan pelarut etanol 70% untuk kali pertama
menggunakan etanol panas (70OC) guna mematikan aktivitas enzim
tanaman yang akan mengganggu proses berikutnya (Harbone,1987).
Selanjutnya proses maserasi dilakukan berulangkali hingga pelarut
mendekati tidak berwarna.
Total hasil maserasi yang keluar digabung dan selanjutnya
dikentalkan menggunakan vacuum rotary evaporator pada suhu 50oC,
dan dihasilkan residu berupa ekstrak padat. Ekstrak yang diperoleh
kemudian dihitung dengan membandingkan berat awal simplisia dan
berat akhir ekstrak yang dihasilkan, dengan rumus:
Berat ekstrak yang diperoleh
Rendemen ekstrak total = x 100% Berat simplisia awal
3.4.3. Fraksinasi Bertingkat dengan Metode Partisi Cair-cair
a. Fraksi n-Heksan
150 mg ekstrak etanol yang didapat dari hasil maserasi dilarutkan
dalam etanol 50% secukupnya lalu dimasukkan kedalam corong pisah.
Selanjutnya dipartisi dengan menambahkan n-heksan, dikocok dalam
corong pemisah dan didiamkan hingga terdapat dua lapisan (lapisan
etanol 50% di bagian bawah dan lapisan n-heksan di bagian atas). Kedua
lapisan yang terbentuk kemudian dipisahkan. Lapisan n-heksan (atas)
dikumpulkan, sedangkan lapisan etanol 50% (bawah) ditambahkan
n-heksan dan dipartisi kembali sampai lapisan n-n-heksan mendekati tidak
berwarna. Total lapisan n-heksan dipekatkan dengan vacuum rotary
evaporator kemudian ditimbang untuk diperoleh fraksi n-heksan.
b. Fraksi Etil Asetat
Lapisan etanol 50% yang telah dipisahkan dari fraksi n-heksan
dimasukan kembali ke corong pemisah. Selanjutnya dilakukan pemisahan
fraksi etil asetat dengan menambahkan sejumlah volume tertentu etil
asetat kedalam corong pisah kemudian dikocok dan didiamkan hingga
terdapat dua lapisan (lapisan etanol 50% di bagian bawah dan lapisan etil
asetat di bagian atas). Kedua lapisan yang terbentuk kemudian
dipisahkan. Lapisan etil asetat (atas) dikumpulkan, sedangkan lapisan
etanol 50% (bawah) ditambahkan etil asetat dan dipartisi kembali sampai
didapat selama fraksinasi digabungkan menjadi satu dan dipekatkan
dengan vacuum rotary evaporator kemudian ditimbang untuk diperoleh
fraksi etil asetat
c. Fraksi Etanol 50%
Lapisan etanol 50% yang telah dipisahkan dari fraksi etil asetat
dipekatkan dengan vacuum rotary evaporator kemudian dipekatkan
dengan penanggas air. Ekstrak yang didapatkan kemudian ditimbang
untuk mendapatkan fraksi etanol 50%.
3.4.5. Uji Aktivitas Antiinflamasi Metode Stabilisasi Membran Eritrosit 3.4.5.1 Pembuatan Larutan yang dibutuhkan
a. Pembuatan Larutan Alsever Steril
2 g dekstrosa, 0,8 g natrium sitrat, 0,05 g asam sitrat dan 0,42 g NaCl
dilarutkan dalam aquades sampai 100 mL pada suhu ruang. Kemudian
disterilisasi menggunakan autoklaf pada suhu 115oC selama 30 menit
(Kumar et al., 2012).
b. Pembuatan dapar fosfat pH 7,4 (0,15 M)
Sebanyak 2,671 g dinatrium hidrogen fosfat (Na2HPO4. 2H2O) dilarutkan
dalam aquades sampai 100 ml (0,15 M). 2,070 g natrium dihidrogen fosfat
(NaH2PO4 . H2O) dilarutkan dalam aquades sampai 100 mL (0,15 M).
Kemudian 81 mL larutan Na2HPO4. 2H2O (0,15 M) dicampurkan dengan
19 mL larutan NaH2PO4 . H2O (0,15 M) pada suhu ruang (Ruzin, 1999).
Kemudian disterilisasi dengan autoklaf pada suhu 115oC.
c. Pembuatan isosalin
0,85 gram NaCl dilarutkan dalam dapar fosfat pH 7,4 (0,15 M) sampai
volume 100 mL pada suhu ruang (Oyedapo et al., 2010). Kemudian
d. Pembuatan Hiposalin
0,25 gram NaCl dilarutkan dalam dapar fosfat pH.7,4 (0,15 M) sampai
volume 100 mL pada suhu ruang (Oyedapo et al., 2010). Kemudian
disterilisasi dengan autoklaf pada suhu 115oC.
e. Penyiapan konsentrasi ekstrak dan Na diklofenak
50 mg ekstrak dari setiap fraksi dilarutkan dalam isosalin sampai 50 mL
(1000 ppm) pada suhu ruang. Begitu juga dengan Na diklofenak, sebanyak
50 mg Na diklofenak dilarutkan dalam 50 mL isosalin (1000 ppm) pada
suhu ruang. Kemudian kedua larutan tersebut diencerkan menjadi beberapa
seri konsentrasi (50, 100, 200, 400 dan 800 ppm).
3.4.5.2 Pembuatan suspensi sel darah merah
Metode ini dijelaskan oleh Gandhisan, 1991 dalam Kumar et al., 2012
dan dimodifikasi dengan metode Sadique et al., 1989 dalam Oyedapo et al.,
2010. Darah diambil dari sukarelawan sehat sebanyak 10 mL lalu
dimasukkan kedalam tabung centrifuge yang telah berisi larutan alsever
steril sebanyak 10 mL. Campuran darah dan larutan alsever steril tersebut
kemudian disentrifugasi pada 3000 rpm selama 10 menit pada suhu 27oC.
Supernatan yang terbentuk dipisahkan menggunakan pipet steril. Endapan
sel-sel darah yang tersisa kemudian dicuci dengan larutan isosalin dan
disentrifugasi kembali. Proses tersebut diulang 4 kali sampai isosalin jernih.
Volume sel darah diukur dan diresuspensi dengan isosalin sehingga
didapatkan suspensi sel darah merah dengan konsentrasi 10% v/v. Suspensi
sel darah tersebut disimpan pada suhu 4oC jika belum digunakan (Oyedapo
et al., 2010)
3.4.5.3 Pengujian Aktivitas Ekstrak Terhadap Stabilisasi Membran Eritrosit. Untuk menentukan aktivitas ekstrak terhadap stabilisasi membran
a. Pembuatan Larutan uji
Larutan uji (4,5 mL) terdiri dari 1 mL dapar fosfat pH 7,4 (0,15 M), 2
mL hiposalin, 0,5 mL suspensi sel darah merah dan 1 mL larutan sampel.
b. Pembuatan Larutan Kontrol Positif
Larutan kontrol positif terdiri dari 1mL dapar fosfat pH 7,4 (0,15 M),
2 mL hiposalin, 0,5 mL suspensi sel darah merah dan 1 mL larutan Na
diklofenak.
c. Pembuatan Larutan Kontrol Larutan Uji
Larutan kontrol larutan uji terdiri dari 1 mL dapar fosfat pH 7,4 (0,15
M), 2 mL hiposalin, 0,5 mL larutan isosalin sebagai pengganti suspensi sel
darah merah dan 1 mL larutan sampel.
d. Pembuatan Larutan Kontrol Negatif
Larutan kontrol negatif terdiri dari 1 mL dapar fosfat pH 7,4 (0,15 M),
2 mL hiposalin, 0,5 mL suspensi sel darah merah dan 1 mL larutan isosalin
sebagai pengganti larutan sampel.
Setiap larutan di atas kemudian diinkubasi pada 37ºC selama 30 menit
dan disentrifugasi pada 3000 rpm selama 20 menit. Cairan supernantan yang
didapat diambil dan kandungan hemoglobinnya diperhitungkan dengan
menggunakan spektrofotometer UV pada panjang gelombang 560 nm.
Persen stabilitas membran sel darah merah dapat dihitung dengan rumus,
sebagai berikut:
% Stabilitas =
3.4.6. Analisis Data
Data yang diperoleh dianalisis dengan uji Kolmogorov-Smirnov untuk
melihat distribusi data dan dianalisis dengan uji Levene untuk melihat
homogenitas data. Jika data terdistribusi normal dan homogenitas maka
dilanjutkan dengan uji Analisis of Varians (ANOVA) satu arah dengan
taraf kepercayaaan 95% sehingga dapat diketahui apakah perbedaan yang
diperoleh bermakna atau tidak. Jika terdapat perbedaan bermakna,
dilanjutkan dengan uji Beda Nyata Terkecil (BNT) dengan metode LSD
(Santoso, 2008).
3.4.7. Skrining Fitokimia
Skrining fitokimia meliputi flavonoid, saponin, tanin, alkaloid dan
antrakuinon (Guevara & Recio, 1985) dilakukan terhadap fraksi etil asetat
daun kelor.
3.4.7.1 Alkaloid
Fraksi Etil asetat sebanyak 10 mg ditimbang, lalu ditambahkan
10 mL kloroform diaduk rata. Campuran disaring kedalam tabung
reaksi. Kemudian ditambahkan 0,5 mL H2SO4 1 M dan dikocok
baik-baik, dibiarkan beberapa saat. Lapisan atas yang jernih dipipet kedalam
2 tabung reaksi kecil. Salah satunya diberikan pereaksi Dragendorff dan
tabung lainnya pereaksi Mayer 2-3 tetes. Reaksi positif apabila
menunjukkan endapan kuning jingga (orange) dengan pereaksi
Drogendorff dan endapan putih dengan pereaksi Mayer (Guevara &
Recio, 1985).
3.4.7.2 Flavonoid
Metode Wilstatter Cyanidin
Fraksi etil asetat sebanyak 10 mg ditimbang. Setelah itu
tabung reaksi lain. Campuran ditambahkan 0,5 mL HCl pekat, 3-4 butir
Mg dan ditambahkan 1 mL amil alkohol. Kocok kuat-kuat dan biarkan
beberapa saat kemudian amati perubahan warna pada masing-masing
lapisan pelarut. Apabila terjadi pembentukan atau perubahan warna
menunjukkan reaksi positif terhadap flavonoida (Guevara & Recio,
1985).
3.4.7.3 Saponin Uji Forth
Fraksi etil asetat sebanyak 10 mg ditimbang, lalu ditambahkan
10 mL air panas. Selanjutnya dikocok kuat selama 10 detik, akan
terbentuk buih yang mantap setinggi 1-10 cm selama 10 menit.
Kemudian ditambahkan 1 tetes HCl 2 N dan diamati (Guevara & Recio,
1985).
3.4.7.4 Tanin
Metode Feri Klorida
Fraksi etil asetat sebanyak 10 mg ditimbang, kemudian
ditambahkan 20 mL air panas dan 5 tetes larutan NaCl 10%. Campuran
dibagi menjadi 2 tabung reaksi, salah satunya sebagai kontrol negatif
dan yang lainnya ditambahkan larutan FeCl3 1% sebanyak 3 tetes.
Perubahan warna diamati, dimana tanin terhidrolisa memberikan warna
biru atau biru-hitam, sedangkan tanin terkondensasi memberikan warna
biru-hijau dan dibandingkan dengan kontrol (Guevara & Recio, 1985).
3.4.7.5 Antrakuinon Metode Borntrager’s
Masing-masing ekstrak sebanyak 10 mg ditimbang, lalu
salah satunya sebagai kontrol negatif dan yang lainnya ditambahkan 5
mL amoniak 25%. Apabila terjadi warna merah muda seulas pada
lapisan larutan amonia menunjukkan positif adanya senyawa
4.1. Hasil
4.1.1. Hasil Determinasi
Untuk memastikan kebenaran simplisia yang digunakan dalam
penelitian ini, maka dilakukan determinasi di Herbarium Bogoriense,
Pusat Penelitian Biologi LIPI, Bogor, Jawa Barat. Hasil determinasi
menunjukkan bahwa sampel merupakan spesies Moringa oleifera L..
Sertifikat hasil determinasi dapat dilihat pada Lampiran 1.
4.1.2. Pembuatan Serbuk Simplisia
Daun kelor segar yang digunakan sebanyak 1,5 kg, setelah melalui
serangkaian proses pembuatan simplisia seperti pengeringan, penyerbukan
dan pengayakan diperoleh serbuk daun kelor sebanyak 800 gram. Serbuk
simplisia yang dihasilkan halus dan berwarna hijau. Gambar serbuk simplisia
dapat dilihat pada Gambar 9 .

![Gambar 1. Akar, Daun dan Pohon Kelor [Navie, 2010]](https://thumb-ap.123doks.com/thumbv2/123dok/776859.461107/21.612.139.527.119.686/gambar-akar-daun-dan-pohon-kelor-navie.webp)




![Gambar 6. Metabolisme Asam Arakhidonat dan Mediator Peradangan [Price & Lorraine, 2006]](https://thumb-ap.123doks.com/thumbv2/123dok/776859.461107/38.612.137.575.82.516/gambar-metabolisme-asam-arakhidonat-mediator-peradangan-price-lorraine.webp)

