EFEKTIVITAS NANOKITOSAN SEBAGAI ALTERNATIF
ZAT ANTIBAKTERI ALAMI DALAM PEMBERSIH TANGAN
DONA FRADILLA BAHRI
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul “Efektivitas Nanokitosan sebagai Alternatif Zat Antibakteri Alami dalam Pembersih Tangan” adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, September 2015
ABSTRAK
DONA FRADILLA BAHRI. Efektivitas Nanokitosan sebagai Alternatif Zat Antibakteri Alami dalam Pembersih Tangan. Dibimbing oleh PIPIH SUPTIJAH dan SAFRINA DYAH HARDININGTYAS.
Kitosan dapat dimanfaatkan dalam berbagai bidang industri modern, misalnya farmasi, biokimia, kosmetika, industri pangan, dan industri tekstil. Perkembangan modifikasi fisik dari kitosan mengarah kepada bentuk nanopartikel, yang biasa disebut sebagai nanokitosan. Nanokitosan merupakan bagian dari teknologi nano karena memiliki sifat lebih reaktif dan memiliki ukuran lebih kecil. Tujuan penelitian ini adalah untuk mengkarakterisasi kitosan dan nanokitosan yang akan digunakan sebagai pembersih tangan dan memberikan pilihan alternatif sebagai antibakteri dengan bahan yang lebih aman. Pengujian yang dilakukan meliputi karakterisasi mutu kitosan, FTIR, PSA, SEM, dan analisis efektivitas pembersih tangan. Kitosan yang digunakan telah sesuai dengan SNI 7949: 2013 mengenai syarat dan mutu pengolahan kitosan. Derajat deasetilasi pada kitosan uji sebesar 85,94%. Distribusi ukuran nanokitosan berdasarkan intensitas, angka, dan volume didapatkan rata-rata ukuran partikel 140,94 nm dengan polydispersi intensity (PDI) sebesar 0,5830. Nanokitosan yang dihasilkan dilakukan analisis efektivitas pembersih tangan. Konsentrasi nanokitosan yang digunakan yaitu 1000, 1500, dan 2000 ppm, serta dibandingkan dengan pembersih tangan komersial. Hasil yang diperoleh menunjukkan bahwa semakin tinggi konsentrasi nanokitosan yang digunakan, maka total koloni bakteri akan semakin berkurang. Konsentrasi nanokitosan 2000 ppm menurunkan total koloni bakteri dari 35,33±4,51 CFU (sebelum) menjadi 2,33±0,58 CFU (setelah) yang tidak berbeda nyata dengan pembersih tangan komersial 2,00±0,00 CFU (setelah).
Kata kunci: antibakteri, efektivitas, kebersihan, nanokitosan, pembersih tangan
ABSTRACT
DONA FRADILLA BAHRI. Effectiveness Nanokitosan as Alternative Antibacterial Natural Substances in Handsanitizer. Supervised by PIPIH SUPTIJAHAND SAFRINA DYAH HARDININGTYAS.
was qualified to the standar of chitosan (SNI 7949: 2013). Degree of deacetylation on chitosan of 85.94%. Distribution of nanochitosan size based on intensity, volume number, and obtanined an average particle size 140.94 nm with polydispersi intensity (PDI) of 0.5830. Futhermore, nanochitosan was tested for the effectiveness handsanitizer. The formulation of nanochitosan used at 1000, 1500, and 2000 ppm. The results showed that the higher concentration of nanochitosan had a lower number of total colony of bacteria. The concentration of nanochitosan 2000 ppm reduce number colony of bacteria from 35.33±4.51 CFU (before) into 2.33±0.58 CFU (after) that comparable with commercial handsanitizer 2.00±0.00 CFU (after).
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
EFEKTIVITAS NANOKITOSAN SEBAGAI ALTERNATIF
ZAT ANTIBAKTERI ALAMI DALAM PEMBERSIH TANGAN
DONA FRADILLA BAHRI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Teknologi Hasil Perairan
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas karunia-Nya sehingga dapat menyelesaikan skripsi yang berjudul “Efektivitas Nanokitosan sebagai Alternatif Zat Antibakteri Alami dalam Pembersih Tangan”. Penulis mengucapkan terima kasih kepada:
1 Dr Dra Pipih Suptijah MBA selaku dosen pembimbing yang selalu memberikan ilmu, bimbingan, dan nasihat.
2 Safrina Dyah Hardiningtyas SPi MSi selaku dosen pembimbing yang selalu memberikan ilmu, bimbingan, dan nasihat.
3 Dr rer nat Asadatun Abdullah SPi MSi MSm selaku dosen penguji yang memberikan saran dan masukkannya.
4 Dr Desniar SPi MSi selaku perwakilan ketua program studi yang memberikan saran dan masukkannya.
5 Prof Dr Ir Joko Santoso MSi selaku Ketua Departemen Teknologi Hasil Perairan yang telah memberikan arahan dan ilmu yang bermanfaat.
6 Ema Masruroh SSi, Zacky Arivaie AMd (Laboratorium THP IPB), yang telah membantu penulis selama penelitian di laboratorium.
7 Kedua orang tua dan keluarga yang senantiasa membimbing penulis, menuntun dalam doa, kasih sayang, semangat, dan dukungan.
8 Keluarga besar Teknologi Hasil Perairan Institut Pertanian Bogor serta Pascasarjana yang telah memberi semangat dan banyak membantu.
9 Semua pihak yang telah membantu baik secara langsung maupun tidak langsung hingga terselesaikannya skripsi ini.
Penulis mengharapkan kritik dan saran untuk penyempurnaan karya ini dan karya yang akan datang. Semoga karya ilmiah ini dapat bermanfaat.
Bogor, September 2015
DAFTAR ISI
Karakterisasi Nanokitosan ... 11
Efektivitas Pembersih Tangan ... 13
KESIMPULAN DAN SARAN ... 16
5 Total koloni bakteri pada pra-perlakuan dan perlakuan nanokitosan ... 14
6 Presentase efektivitas pembersih tangan ... 14
DAFTAR TABEL
1 Karakteristik kitosan uji dan Standar Nasional Indonesia ... 102
DAFTAR LAMPIRAN
1 Tahap hand disinfection sesuai dengan EN1500 ... 23
2 Hasil analisis spectra inframerah dari kitosan ... 23
3 Proses pembuatan nanokitosan ... 24
4 Hasil pembersih tangan yang dihasilkan ... 24
5 Hasil analisis efektivitas ... 25
6 Grafik hasil analisis Particle Size Analyze (PSA) ... 25
PENDAHULUAN
Latar Belakang
Tangan merupakan salah satu bagian tubuh yang memiliki fungsi vital bagi manusia, salah satunya adalah untuk berinteraksi dengan lingkungannya. Mulai dari jam pertama setelah dilahirkan, interaksi makro dan mikroorganisme dimulai dengan masuknya mikroba pada permukaan kulit, gastrointertinal, pernafasan, dan saluran urogenital. Salah satu interaksi tersebut adalah menyebabkan terjadinya kolonisasi bakteri pada permukaan tangan (Hogenova et al. 2004).
Kebersihan kulit, khususnya pada tangan merupakan salah satu langkah penting dalam upaya mengurangi dan mencegah penyebaran agen infeksi (Badar et al. 2014). Pencucian tangan merupakan salah satu cara yang sering dilakukan dan dapat mereduksi jumlah bakteri yaitu Escherichia coli, Staphylococcus marcescens, Staphylococcus aureus, dan Pseudomonas aeruginosa (Kampf dan Kramer 2004). Perkembangan kebersihan tangan telah menuntut suatu cara yang tepat dan efektif akan ketergantungan terhadap keberadaan air dan sabun. Dalam kondisi tertentu, sulit mencari air dan sarana tempat mencuci tangan yang memadai. Hal tersebut telah memberikan dampak yang tinggi terhadap produksi pembersih tangan (handsanitizer) di pasaran.
Cairan pembersih tangan komersial umumnya menggunakan alkohol sebagai bahan aktif antibakterinya. Cimiotti et al. (2003) mengungkapkan bahwa alkohol dapat menyebabkan kasus allergic contact dermatitis terjadi ketika kulit terpapar etil alkohol. Kandungan lain yang terdapat pada pembersih tangan yaitu triklosan. Triklosan bersifat photoallergic contact dermatitis (PACD) atau dapat menimbulkan reaksi alergi ketika kulit yang diberi triklosan terpapar sinar matahari. Photoallergic contact dermatitis (PACD) akan menimbulkan ruam, umumnya pada bagian wajah, leher, dan punggung tangan (APUA 2011). Berdasarkan latar belakang tersebut, maka diperlukan suatu zat antibakteri baru yang lebih aman untuk mengatasi kasus alergi tersebut, yaitu dengan menggunakan kitosan.
Kitosan merupakan polisakarida alami yang diperoleh dari kitin melalui proses deasetilasi (Sano et al. 2003). Kitosan banyak digunakan pada berbagai bidang yaitu pengolahan air limbah, anti tumor (Chaiyakosa et al. 2007) dan sebagai antibakteri (Fernandes et al. 2006). Produk kitosan pada umumnya dimanfaatkan dengan melakukan modifikasi kitosan fisik. Modifikasi gelasi fisik pada kitosan mencakup perubahan ukuran partikel menjadi lebih kecil untuk pemanfaatan yang lebih luas dan perkembangan modifikasi fisik mengarah ke bentuk nanopartikel. Menurut Suwarda dan Maarif (2012) nanopartikel merupakan suatu partikel yang memiliki ukuran sekitar 10-1000 nm (1 nm = 10-9 meter).
Qi et al. (2004) mengungkapkan bahwa nanokitosan mempunyai keunggulan dibandingkan dengan material sejenis dalam ukuran besar (kitosan) karena ukuran nanopartikel memiliki ukuran partikel yang lebih kecil. Hal ini membuat nanopartikel bersifat lebih reaktif.
Pemanfaatan nanokitosan sebagai antibakteri lebih aman karena nanokitosan memiliki LC50 sebesar 464,13 ppm dan digolongkan sebagai toksik
2
dalam cairan pembersih tangan dinilai aman sehingga perlu dilakukan pengembangan lebih lanjut. Tuntutan pola hidup yang semakin praktis juga menjadi salah satu alasan pengembangan nanokitosan sebagai alternatif dalam pembersih tangan.
Perumusan Masalah
Penyebaran agen penyebab penyakit sering terjadi melalui tangan. Menjaga kebersihan tangan diharapkan mampu menghambat penyebaran tersebut. Penggunaan air dan sabun dinilai tidak praktis lagi. Penggunaan pembersih tangan dengan kandungan desinfektan alkohol dapat menimbulkan iritasi kulit yang terpapar dan infeksi saluran pencernaan apabila digunakan dalam jangka panjang (Zaragoza et al. 1999). Penggunaan nanokitosan sebagai antibakteri pada pembersih tangan belum pernah digunakan sebelumnya. Penelitian ini diharapkan dapat menghasilkan pembersih tangan dengan efektivitas penurunan total koloni bakteri yang baik pada tangan.
Tujuan Penelitian
Tujuan umum penelitian ini adalah memanfaatkan kitosan menjadi nanokitosan sebagai antibakteri pada pembersih tangan. Tujuan khusus penelitian ini meliputi:
1. Mengkarakterisasi kitosan dan nanokitosan.
2. Menguji efektivitas nanokitosan sebagai antibakteri pada pembersih tangan.
Manfaat Penelitian
Manfaat dari penelitian ini yaitu adanya pilihan alternatif sebagai zat antibakteri pada pembersih tangan yang aman dan praktis serta memperkaya khasanah informasi bagi dunia farmasi mengenai manfaat nanokitosan.
Ruang Lingkup Penelitian
METODE PENELITIAN
Waktu dan Tempat
Penelitian dilaksanakan pada bulan Februari hingga Juli 2015. Pembuatan larutan nanokitosan dilakukan di Laboratorium Kitin dan Kitosan Hasil Perairan. Pengujian efektivitas pembersih tangan dilakukan di Laboratorium Mikrobiologi Hasil Perairan, Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Pengujian analisis proksimat kitosan di Pusat Antar Universitas, Institut Pertanian Bogor. Analisis derajat deasetilasi kitosan dengan menggunakan Fourier Transform Infra Red (FTIR) di Laboratorium Biofarmaka, Institut Pertanian Bogor. Analisis ukuran partikel dengan Particle Size Analyzer (PSA) di Laboratorium Analisa Bahan, Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Pengujian analisis morfologi nanokitosan dengan Scanning Electron Microscopy (SEM) di Laboratorium Nanoteknologi, Balai Besar Penelitian dan Pengembangan Pascaapanen.
Bahan Penelitian
Bahan-bahan yang digunakan antara lain kitosan serpihan berbahan dasar cangkang udang yang diproduksi oleh PT Biotech Surindo, asam asetat (Merck), alkohol, akuades, air steril, tripolifosfat (Bratachem), surfaktan (tween 80) (Bratachem), dan media Nutrient Agar (Merck).
Peralatan Penelitian
Alat-alat yang digunakan untuk pembuatan nanokitosan yaitu timbangan digital (Genetic OM Type 58), magnetic stirrer (Yamato MD-41), inkubator (Yamato IS900), autoklaf (Yamato SM-52), micropipette, ruang laminar, spray drying (Labconco), Particle Size Analyzer (PSA) (DelsaTM Nano, Cordoun), Fourier Transform Infra Red (FTIR) (Bruker Tensor Tipe MBQ00, ABB Group), Scanning Electron Microscopy (SEM) (ZEIIS EVOIMA10).
Prosedur Penelitian
4
nanokitosan meliputi parameter analisis Particle Size Analyze (PSA) dan analisis Scanning Electron Microscopy (SEM). Tahap ketiga meliputi pengujian efektivitas pembersih tangan mengacu Babeluk et al. (2014). Prosedur penelitian secara umum disajikan pada Gambar 1.
Gambar 1 Diagram alir penelitian
5
Pembuatan Larutan Nanokitosan
Komposisi dasar larutan mengacu Suptijah et al. (2011) yang meliputi pelarutan kitosan dengan asam asetat, pembuatan gel kitosan, emulsifikasi dengan menggunakan tween 80 (polioksietilen 20 sorbitan monooleat) dan stabilisasi dengan tripolifosfat (TPP) dengan komposisi kitosan 1,5 gram.
Pembuatan larutan stok nanokitosan dengan konsentrasi 2500 ppm diawali dengan melarutkan kitosan 1,5 gram kitosan dalam 50 mL asam asetat 1% menggunakan magnetic stirrer pada suhu ruang (25 oC) selama 1 jam. Tahap
selanjutnya sizing kitosan, diawali dengan penambahan akuades hingga 500 mL menggunakan magnetic stirrer pada suhu ruang (25 oC) selama 2 jam. Tahap emulsifikasi larutan kitosan dengan tween 80 (poliosietilen 20 sorbitan monooleat) 0,1% diawali dengan penyemprotan 4 spray tween 80 (poliosietilen 20 sorbitan monooleat) 0,1% selama 30 menit. Tahap stabilisasi larutan kitosan dengan penambahan tripolifosfat (TPP) 0,1% dilakukan dengan penambahan 100 mL tripolifosfat (TPP) 0,1 % kedalam larutan kitosan dengan pipet tetes secara perlahan-lahan. Pengadukan terus dilakukan selama 1 jam agar proses ikatan silang berlangsung berlangsung sempurna dan partikel yang dihasilkan tetap stabil.
Karakterisasi uji larutan nanokitosan meliputi parameter analisis Particle Size Analyze (PSA) dan analisis Scanning Electron Microscopy (SEM). Analisis selanjutnya yaitu pengujian efektivitas pembersih tangan dengan konsentrasi 1000, 1500, 2000 ppm, dan pembersih tangan komersial.
Pengujian Efektivitas Pembersih Tangan (modifikasi Babeluk et al. 2014) Pengujian efektivitas pembersih tangan mengacu Babeluk et al. (2014). Modifikasi dari Babeluk et al. (2014) yaitu pada jumlah probandus yang digunakan.
Pengujian efektivitas pembersih tangan menggunakan probandus sebanyak 12 orang. Probandus tersebut kemudian dibagi menjadi empat kelompok.
Tahapan pengujian efektivitas pembersih tangan terdiri dari 2 tahapan yaitu pra-perlakuan dan penerapan konsentrasi nanokitosan dengan 1000 ppm, 1500 ppm, dan 2000 ppm sebagai pembersih tangan, serta pembersih tangan komersial yang berbasis alkohol.
1 Pra-perlakuan, yaitu pencucian tangan menggunakan air steril kepada seluruh probandus dengan menerapkan prosedur hand disinfection EN1500 (Lampiran 1).
2 Penerapan perlakuan dibagi menjadi empat kelompok yaitu: a Nanokitosan 1000 ppm (n=3)
b Nanokitosan 1500 ppm (n=3) c Nanokitosan 2000 ppm (n=3)
d Pembersih tangan komersial berbasis alkohol 70% (n=3)
6
penyemprotan telapak tangan probandus dengan penerapan masing-masing perlakuan sebanyak 3 spray, kemudian dilakukan penempelan tiga ujung jari tangan kanan pada cawan petri yang telah berisi media Nutrient Agar (NA).
Cawan hasil penempelan tiga ujung jari tersebut selanjutnya diinkubasi dalam inkubator selama 24 jam pada suhu 37 oC. Tahap selanjutnya yaitu
pengamatan dan perhitungan jumlah koloni bakteri yang terdapat dalam cawan. Presentase efektivitas merupakan penurunan jumlah total koloni bakteri dari pembersih tangan dihitung dari hasil yang telah didapatkan pada pengujian efektivitas pembersih tangan. Presentase efektivitas pembersih tangan diperoleh dengan rumus:
Efektivitas Pembersih Tangan % = B – AA x 100%
Keterangan:
A = jumlah koloni bakteri sebelum diberikan perlakuan pembersih tangan B = jumlah koloni bakteri setelah diberikan perlakuan pembersih tangan
Prosedur Analisis
Analisis Derajat Deasetilasi
Pengukuran dengan menggunakan Spektroskopi IR Fourier Transform Infra Red (FTIR) dioperasikan menurut ASTM E1252 (2013). Sampel kitosan diletakkan pada IR card. Spektrum gelombang inframerah ditembakkan melalui sampel yang diletakkan di antara elektroda spektrofotometer dan diteruskan melalui komputer. Data yang didapatkan berupa persentase nilai transmitansi, dengan pengukuran spektrum pada rentang bilangan gelombang 4000-400 cm-1. Selanjutnya nilai
transmitan pada spektra hasil pengukuran dicocokkan dengan data pada tabel acuan dari OchemOnline (2013) serta menggunakan perangkat lunak IR Pal 2.0.
Nilai transmitan yang diperoleh dapat digunakan untuk analisis kuantitatif yaitu derajat deasetilasi dari kitosan. Perhitungan persentase derajat deasetilasi mengacu pada Khan et al. (2002). Pengukuran derajat deasetilasi berdasarkan kurva yang tergambar oleh spektrofotometer. Puncak tertinggi (Po) dan puncak terendah
(P) dicatat dan diukur dengan garis dasar yang dipilih. Absorbansi dihitung dengan rumus:
A = Log PoP Keterangan:
Po = Jarak antara garis dasar dengan garis singgung antara dua puncak
tertinggi dengan panjang gelombang 1655 cm-1 atau 3450 cm-1
P = Jarak antara garis dasar dengan lembah terendah dengan panjang gelombang 1655 cm-1 atau 3450 cm-1
Perbandingan absorbansi pada 1655 cm-1 dengan absorbansi atau 3450 cm-1
7
N deasetilasi % = − [�� ] � , � Keterangan:
A1655 = Absorbansi pada panjang gelombang 1655 cm-1
A3450 = Absorbansi pada panjang gelombang 3450 cm-1 1,33 = Konstanta untuk derajat deasetilasi yang sempurna
Analisis Kadar Air (AOAC 2005)
Cawan porselen dikeringkan dahulu dalam oven pada suhu 105 oC selama 60 menit. Cawan porselen yang sudah kering dimasukkan dalam desikator selama 15 menit dan ditimbang hingga menunjukkan berat yang konstan. Selanjutnya sampel sebanyak 2 gram ditimbang dan dimasukkan ke cawan lalu dikeringkan dalam oven pada suhu 105 oC selama 3 jam. cawan beserta isinya kemudian didinginkan dalam desikator selama 30 menit dan ditimbang hingga diperoleh berat yang konstan. Kadar air dihitung dengan rumus:
Kadar air (%) = B–CB–A x 100% Keterangan:
A = berat cawan kosong (g)
B = berat cawan + sampel awal (g) C = berat cawan + sampel kering (g)
Analisis Kadar Abu (AOAC 2005)
Cawan porselen dikeringkan dahulu dalam oven pada suhu 105 oC selama 60 menit. Cawan porselen yang sudah kering dimasukkan dalam desikator selama 15 menit dan ditimbang hingga menunjukkan berat yang konstan. Selanjutnya sampel sebanyak 3 gram ditimbang dan dimasukkan ke cawan porselen lalu dibakar di atas kompor listrik hingga tidak berasap. Setelah itu dimasukkan ke dalam tanur pengabuan dengan suhu 600 oC selama 6 jam. cawan porselen yang berisi sampel hasil pengabuan dimasukkan ke dalam desikator selama 30 menit kemudian ditimbang hingga diperoleh berat yang konstan. Kadar abu dihitung dengan rumus:
Kadar abu (%) = C–AB–A x 100% Keterangan :
A = berat cawan kosong (g)
B = berat cawan + sampel awal (g) C = berat cawan + sampel kering (g)
Analisis Kadar Nitrogen (AOAC 2005)
Tahap yang dilakukan dalam analisis protein terdiri dari tiga tahap yaitu destruksi, destilasi, dan titrasi. Pengukuran kadar nitrogen dilakukan dengan metode mikro kjedahl. Penimbangan dan pemasukkan 0,25 gram kitosan kedalam labu kjedahl 100 mL, kemudian penambahan satu butir kjedahl dan 3 mL H2S04
8
dilakukan proses destilasi dengan suhu destilator 100 oC. Hasil destilasi ditampung
dalam erlenmeyer 125 mL yang berisi campuran 10 mL asam borat (H3BO3) 2%
dan 2 tetes indikator bromcherosol green-methyl red yang berwarna merah muda. Setelah volume destilat mencapai 40 mL dan berwarna hijau kebiruan, maka proses destilasi dihentikan. Pentitrasian destilat dengan HCl 0,1 N sampai terjadi perubahan warna merah muda. Pembacaan dan pencatatan volume titran. Penganalisisan larutan blanko seperti contoh. Kadar nitrogen dihitung dengan rumus sebagai berikut:
Nitrogen (%) = (S–B) x N HCl x 14,007 x FPW x 100%
Keterangan:
S = Volume titran sampel (mL) B = Volume titran blanko (mL)
N HCl = Normalitas HCl standar yang digunakan (mgrek/mL) 14,007 = Berat ekuivalen atom nitrogen (mg/mgrek)
FP = Faktor pengenceran W = Bobot sampel kering (mg)
Analisis Partikel dengan Particle Size Analyzer (PSA)
Analisis partikel menggunakan Particle Size Analyzer (PSA) dioperasikan menurut ASTM D422-63 (2007) mengacu ISO-13320 (2009). Satu mL larutan diletakkan pada media yang ditembakkan laser inframerah, sehingga menghasilkan difraksi partikel dengan prinsip transmitansi cahaya. Hasil yang didapat adalah nilai ukuran dan sebaran indeks partikel pada larutan.
Analisis Morfologi dengan Scanning Electron Microscopy (SEM)
Morfologi kenampakan dilakukan dengan menggunakan Scanning Electron Microscope (SEM) yang dioperasikan menurut SEMO (Robbins 2013). Analisis SEM menggunakan larutan stok nanokitosan yang kemudian dilakuran pengeringan dengan menggunakan spray drying, sehingga didapatkan serbuk nanokitosan. Serbuk nanokitosan kemudian dilapisi dengan serbuk emas hingga konduktif elektron. Kenampakan nanokitosan akan ditangkap melalui elektron emas oleh Scanning Electron Microscope (SEM) dan ditampilkan pada komputer. Pengukuran dilakukan dengan perbesaran 1000x dan 2000x untuk kenampakan permukaan dari nanokitosan.
Analisis Data
Rancangan Percobaan (Steel dan Torrie 1993)
9
Yijk= μ+αi+ j+δijk+ωk+αωkj+ jk
Keterangan:
Yijk = Nilai pengamatan pada perlakuan konsentrasi nanokitosan ke-i, ulangan
ke-j, dan waktu ke-k μ = Nilai rataan umum populasi
αi = Pengaruh perlakuan nanokitosan taraf ke-i j = Nilai respon terhadap kelompok ke-1
δijk = Komponen acak perlakuan
ωk = Pengaruh kelompok dalam pengamatan ke-k
αωkj = Pengaruh interaksi kelompok dengan perlakuan nanokitosan jk = Komponen acak kelompok pengamatan
Hipotesis yang diuji yaitu:
Ho = Perlakuan konsentrasi pembersih tangan berbasis nanokitosan tidak
memberikan pengaruh terhadap penurunan total koloni bakteri pada ujung jari.
H1 = Perlakuan konsentrasi pembersih tangan berbasis nanokitosan
memberikan pengaruh terhadap penurunan total koloni bakteri pada ujung jari.
Data yang diperoleh dianalisis sidik ragam (ANOVA), jika hasilnya berbeda nyata pada selang kepercayaan 95% maka dilakukan uji lanjut dengan menggunakan uji Duncan, rumus uji Duncan yaitu:
= ∑ ; � ; √�
Keterangan:
Rp = Nilai kritikal untuk perlakuan yang dibandingkan p = Perlakuan
10
(NH2) pada rantai molekul kitosan sehingga kitosan semakin reaktif. Hasil
karakteristik kitosan uji dan Standar Nasional Indonesia 7949: 2013 dapat dilihat pada Tabel 1.
Tabel 1 Karakteristik kitosan uji dan Standar Nasional Indonesia 7949: 2013
Sifat Parameter uji
Kitosan uji SNI 7949:2013*
Bentuk partikel Serpihan Serpihan sampai serbuk
Kadar air (%) 9,65% Maks 12%
Kadar abu (%) 0,87% Maks 5%
Kadar nitrogen (%) 4,03% Maks 5%
Derajat deasetilasi 85,94% Min 75%
Sumber: *Badan Standardisasi Nasional (2013)
Hasil analisis proksimat kitosan menunjukkan bahwa nilai kadar air kitosan yang digunakan dalam penelitian memiliki nilai yang lebih kecil jika dibandingkan dengan SNI 7949: 2013 (Tabel 1). Nilai kadar air dari kitosan sebesar 9,65%. Suptijah et al. (2011) menyatakan bahwa kadar air rendah karena cara pengeringan yang baik. Kumar (2004) mengemukakan bahwa kadar air dipengaruhi oleh beberapa faktor diantaranya disebabkan waktu penyimpanan dari kitosan serta lingkungan yang lembab. Faktor lingkungan yang lembab merupakan faktor yang memberikan pengaruh besar terhadap nilai kandungan air dalam kitosan. Kitosan juga memiliki sifat yang mudah menyerap air, sehingga apabila kitosan terlalu lama dalam penyimpanan dan berapa pada kondisi lingkungan lembab maka jumlah kadar air kitosan semakin meningkat.
Kadar abu merupakan parameter untuk mengetahui mineral yang terkandung pada kitosan. Kadar abu dari kitosan sebesar 0,87%. Angka dan Suhartono (2000) menyatakan bahwa kadar abu yang rendah menunjukkan kadar mineral yang rendah. Suptijah et al. (2011) menambahkan bahwa faktor yang memiliki pengaruh terhadap kandungan mineral kitosan adalah kualitas air yang digunakan ketika proses penetralan kitosan serta efektivitas proses demineralisasi yang dilakukan. Angka dan Suhartono (2000) proses pencucian yang baik dan diperolehnya pH netral juga berpengaruh terhadap kadar abu.
Kadar nitrogen kitosan uji yang dihasilkan telah memenuhi standar mutu dan pengolahan kitosan menurut Standar Nasional Indonesia 7949: 2013 (Tabel 1). Kadar nitrogen dari kitosan sebesar 4,03%. Kim dan Cho (2005) menyatakan bahwa kadar nitrogen menentukan sifat kitosan yang berinteraksi dengan gugus amina (NH2). Keberadaan NH2 menyebabkan kitosan memiliki reaktivitas yang tinggi,
sehingga kitosan mampu mengikat air dan larut dalam asam asetat.
Analisis Fourier Transform Infrared (FTIR) adalah salah satu analisis yang digunakan untuk mengidentifikasi gugus fungsi dalam suatu bahan. Bilangan gelombang yang digunakan untuk senyawa organik maupun senyawa polimer yaitu 400-4000 cm-1 (Shalini dan Prema 2012). Analisis FTIR pada kitosan yang digunakan meliputi struktur gugus fungsi dari kitosan (Lampiran 2a). Hasil analisis Fourier Transform Infrared (FTIR) pada kitosan dapat dilihat pada Gambar 2.
11
semakin tinggi tingkat kemurniaannya yang berarti kitin atau kitosan sudah murni dari pengotornya yaitu protein, mineral, dan pigmen, serta gugus asetil pada kitosan yang disertai kelarutannya yang sempurna dalam asam asetat 1% (Suptijah 2006).
Gambar 2 Spektrum FTIR kitosan
Derajat deasetilasi menentukan banyaknya gugus asetil yang hilang selama proses deasetilasi. Derajat deasetilasi yang tinggi menunjukkan kemurnian kitosan yang dihasilkan. Derajat deasetilasi pada kitosan sebesar 85,94% (Lampiran 2b). Agustini dan Sedjati (2007) menjelaskan bahwa semakin tinggi derajat deasetilasi kitosan maka semakin banyak gugus amina pada rantai molekul kitosan, sehingga kitosan semakin reaktif karena banyaknya gugus amina yang menggantikan gugus asetil.
Karakteristik Nanokitosan
Morfologi nanokitosan ditunjukkan menggunakan analisis Scanning Electron Microscope (SEM). Mohanraj dan Chen (2006) menjelaskan bahwa nanopartikel didefinisikan sebagai penyebaran partikel atau partikel padat dengan kisaran ukuran 10-1000 nm. Hasil analisis SEM dapat dilihat pada Gambar 3.
a b
Gambar 3 Morfologi nanokitosan perbesaran (a) 1000x (b) 5000x
12
bahwa morfologi kitosan pada perbesaran 1500x dan 5000x memiliki morfologi berupa serpihan yang berpori. Suptijah et al. (2011) menambahkan bahwa penambahan tween 80 pada larutan kitosan bertujuan untuk menstabilkan partikel-partikel kitosan satu sama dengan yang lain yang sudah menjadi emulsi homogen (misel), sehingga proses pemecahan partikel akan semakin efektif. Partikel yang telah terpecah akan kembali terstabilkan dalam larutan emulsi, sehingga mencegah terjadinya aglomerelasi. Penambahan TPP sebagai zat penstabil dan pengikat silang yang akan memperkuat matriks nanokitosan. Semakin banyak ikatan silang yang terbentuk antara kitosan dan TPP, maka kekuatan mekanik matriks kitosan akan meningkat sehingga partikel kitosan menjadi semakin kuat dan lebih stabil.
Pembuatan nanopartikel dipengaruhi oleh beberapa faktor, antara lain komposisi material dan metode yang digunakan. Material yang digunakan pada pembuatan nanokitosan yaitu kitosan, tween 80, dan tripolifosfat (TPP). Metode pembuatan nanopartikel merupakan salah satu faktor lain yang menentukan selain komposisi material. Banyak metode yang dikembangkan untuk menghasilkan nanopartikel. Metode yang didapat silang emulsi (emulsion cross-linking) presipitasi (Tiyaboonchai 2003), metode homogenizer, dan metode ultrasonikator (Suptijah et al. 2011).
Pembuatan nanokitosan menggunakan metode gelasi ionik dan pengecilan ukuran (sizing) dengan magnetic stirrer dipilih karena prosesnya yang sederhana serta dapat menghasilkan partikel nanokitosan yang memiliki ukuran lebih seragam dan berbentuk bulat. Menurut Agnihorti et al. (2004) prinsip pembentukan partikel pada metode gelasi ionik adalah terjadinya interaksi ionik antara gugus amina (NH2) pada kitosan yang bermuatan positif dengan polianion yang bermuatan
negatif membentuk struktur network inter dan intramolekul tiga dimensi. Menurut Katas dan Alpar (2006) penggunaan tripolifosfat sebagai polianion untuk crosslinker dengan kitosan melalui interaksi elektrostatik, dan surfaktan (tween 80) sebagai pengemulsi, karena bersifat tidak toksik. BPOM (2013) menjelaskan bahwa penggunaan TPP dan tween 80 diperbolehkan sebagai bahan tambahan pangan dengan batas maksimum 70 mg/kg berat badan.
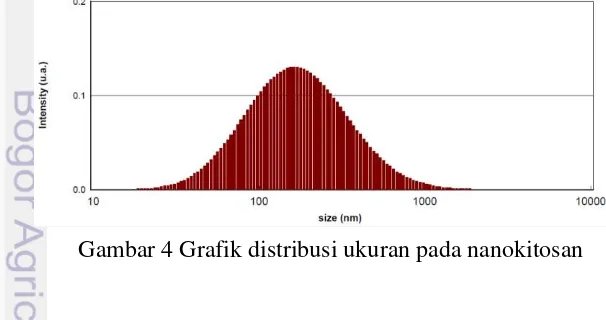
Pengujian Particle Size Analyze (PSA) dilakukan untuk melihat ukuran partikel nanokitosan. Nanokitosan dibuat dengan menggunakan prinsip gelasi ionik. Metode gelasi ionik menggunakan alat magnetic stirrer. Rachmania (2011) mengungkapkan bahwa pengecilan ukuran dengan magnetic stirrer dengan kecepatan tinggi akan menyamaratakan energi yang diterima oleh partikel di seluruh bagian sisi larutan sehingga ukuran partikel semakin homogen. Berikut hasil analisis Particle Size Analyze (PSA) dapat dilihat pada Gambar 4.
13
Nanokitosan yang dihasilkan mempunyai dispersi ukuran sebesar 29,27 nm (Gambar 4). Distribusi ukuran nanokitosan berdasarkan intensitas, angka, dan volume (Lampiran 6a) didapatkan rata-rata ukuran partikel 140,94 nm dengan polydispersi intensity (PDI) sebesar 0,5830. Mohanraj dan Chen (2006) mengemukakan bahwa nanopartikel merupakan partikel dengan kisaran ukuran 10-1000 nm. Metode gelasi ionik digunakan bertujuan untuk menghasilkan nanokitosan yang memiliki stabilitas yang baik, berukuran partikel terkecil dan meningkatkan skala produksi.
Chang dan Overby (2011) mengemukakan berdasarkan teori kinetik bahwa molekul dapat bertumbukan satu dengan lainnya, sehingga reaksi kimia berlangsung sebagai akibat dari kinetika kimia, laju reaksi akan berbanding lurus dengan banyaknya tumbukan molekul perdetik atau berbanding lurus dengan frekuensi tumbukan molekul. Suptijah et al. (2011) menjelaskan bahwa semakin cepat putaran maka dapat memperbesar intensitas sentuhan molekul pelarut dengan kitosan, sehingga semakin besar intensitas kecepatan putaran dari magnetic stirrer maka partikel yang dihasilkan semakin kecil. Yongmei dan Yumin (2003) menambahkan bahwa pembentukan nanopartikel hanya terjadi pada konsentrasi kitosan dan TPP tertentu. Yongmei dan Yumin (2003) berhasil membuat nanokitosan berukuran 20-200 nm dengan menggunakan konsentrasi kitosan 1,5 mg/mL dan konsentrasi TPP 0,7 mg/mL. Silva et al. (2006) menjelaskan bahwa penambahan tween 80 ke dalam larutan kitosan dapat menurunkan diameter partikel berturut-turut dari 198 nm menjadi 181,3 nm dan dari 132,6 nm menjadi 24,9 nm. Selain itu, Honary et al. (2011) menjelaskan bahwa aktivitas antibakteri dari nanokitosan juga ditentukan oleh ukuran partikelnya. Partikel yang lebih kecil menunjukkan aktivitas antibakteri yang lebih besar dibandingkan dengan ukuran partikel yang lebih besar.
Pengujian fisik terhadap nanokitosan sebagai pembersih tangan dan pembersih tangan komersial yaitu pengujian pH. Hasil pengukuran pH tersebut dapat dilihat pada Tabel 2.
Tabel 2 Pengukuran pH pada nanokitosan
Perlakuan pH
Nanokitosan 1000 ppm 5,35±1,51
Nanokitosan 1500 ppm 5,44±1,48
Nanokitosan 2000 ppm 6,11±1,31
Pembersih tangan komersial 6,11±1,20
Hasil pengujian pH pada konsentrasi nanokitosan 1000 ppm dan nanokitosan 1500 ppm yaitu 5,35±1,51 dan 5,44±1,48. Sedangkan, pada nanokitosan 2000 ppm dan pembersih tangan komersial yaitu 6,11±1,31 dan 6,11±1,20. Nilai pH suatu antiseptik harus sesuai dengan pH kulit yaitu 4,5-6,5 karena apabila pH tidak sesuai maka akan menimbulkan iritasi pada kulit yang terpapar (Titaley et al. 2014).
Efektivitas Pembersih Tangan
14
Pengujian efektivitas pembersih tangan dilakukan dengan menggunakan metode swab untuk melihat jumlah total koloni bakteri yang terdapat pada tangan. Pengujian terdiri dari 2 tahapan yaitu pra-perlakuan dan perlakuan konsentrasi nanokitosan 1000 ppm, nanokitosan 1500 ppm, nanokitosan 2000 ppm, dan pembersih tangan komersial. Hasil total koloni bakteri pada pra-perlakuan dan perlakuan nanokitosan tersebut dapat dilihat pada Gambar 5.
Gambar 5 Total koloni bakteri pada pra-perlakuan dan perlakuan nanokitosan Keterangan: sebelum ( ), setelah ( )
Total koloni bakteri pada pra-perlakuan dan perlakuan nanokitosan tersebut (Gambar 5) menunjukkan penurunan angka koloni bakteri yang signifikan seiring peningkatan konsentrasi nanokitosan. Konsentrasi nanokitosan 2000 ppm menurunkan angka koloni bakteri dari 35,33±4,51 CFU (sebelum) menjadi 2,33±0,58 CFU (setelah). Penurunan total koloni bakteri ini diduga disebabkan oleh sifat antibakteri yang terdapat pada nanokitosan.
Total koloni bakteri pada ujung jari mengalami penurunan seiring dengan peningkatan konsentrasi nanokitosan. Hal ini menunjukkan adanya sifat antibakteri yang terdapat dalam nanokitosan. Abdou et al. (2012) mengemukakan bahwa peningkatan konsentrasi dapat mengakumulasi gugus reaktif nanokitosan yaitu gugus amina (NH2), sehingga mempunyai efektivitas lebih besar untuk merusak
dinding sel bakteri. Zhang et al. (2010) menambahkan bahwa aktivitas antibakteri dapat meningkat seiring dengan konsentrasi yang lebih tinggi dan ukuran partikel yang lebih kecil. Presentase efektivitas pembersih tangan dapat dilihat pada Gambar 6.
Gambar 6 Presentase efektivitas pembersih tangan 70,79±0,91a
nanokitosan 1000 nanokitosan 1500 nanokitosan 2000 pembersih tangan komersial
15
Presentase efektivitas nanokitosan dengan analisis ragam (Lampiran 7b) menunjukkan bahwa perlakuan konsentrasi pembersih tangan berbasis nanokitosan memberikan pengaruh terhadap penurunan total koloni bakteri pada ujung jari. Hasil uji lanjut Duncan (Lampiran 7c) menunjukkan konsentrasi nanokitosan 1000 ppm memberikan hasil yang berbeda nyata terhadap konsentrasi nanokitosan 1500 ppm dan nanokitosan 2000 ppm, sedangkan nanokitosan 2000 ppm memberikan hasil yang tidak berbeda nyata terhadap pembersih tangan komersial (Lampiran 7c). Presentase efektivitas jumlah penurunan total koloni bakteri pada nanokitosan yang semakin meningkat ini diduga akibat adanya gugus-gugus amina dari nanokitosan yang reaktif sehingga dapat mengakibatkan lisis pada sel bakteri. Rafaat et al. (2008) menjelaskan bahwa kitosan dapat mengakibatkan lisis pada bakteri Gram negatif maupun bakteri Gram positif melalui interaksi elektrostatik.
Target kerja dari antibakteri terhadap suatu bakteri diantaranya yaitu pada dinding sel, perubahan permeabilitas sel, pada molekul protein dan asam nukleat, enzim, dan DNA dan RNA (Pelczar dan Chan 2006). Kelebihan nanokitosan sebagai antibakteri karena mempunyai efektivitas terhadap bakteri Gram positif dan bakteri Gram negatif, serta residunya pada produk akhir tidak membahayakan kesehatan manusia (Du et al. 2009). Nanokitosan bersifat lebih reaktif terhadap sel bakteri dibandingkan kitosan, karena nanokitosan mudah teradsopsi kedalam sel bakteri dalam waktu yang lebih cepat (Qi et al. 2004).
Kitosan memiliki tiga jenis grup reaktif fungsional yaitu grup amino, grup hidroksil primer, dan hidroksil sekunder (Xia 2003). Jenis interaksi antara kitosan yang bermuatan postif dan membran sel bakteri yang bermuatan negatif. Jenis interaksi ini karena adanya interaksi elektrostatik antara grup positif NH3+ kitosan
dan grup negatif sel bakteri, mekanisme interaksi elektrostatik ini dibagi menjadi dua yaitu, pertama mempengaruhi permeabilitas membran, sehingga terjadi ketidakseimbangan tekanan internal osmotik dari sel bakteri dan menghambat pertumbuhan dari bakteri, kedua yaitu dengan hidrolisis dari peptidoglikan pada dinding sel bakteri, sehingga terjadi kebocoran komponen intraseluler seperti ion kalium dan ion dengan berat molekul rendah (protein, asam nukleat, glukosa, dan laktat dehidrogenase) (Tsai dan Su 1999). Penelitian Rafaat et al. (2008) menunjukkan secara visual bahwa kitosan dapat mengakibatkan lisis pada bakteri Gram negatif maupun bakteri Gram positif. Selain itu, mekanisme yang didasarkan pada interaksi elektrostatik dipengaruhi oleh banyaknya ion amina kation, semakin banyak ion kation yang terkandung dalam kitosan tersebut maka akan menghasilkan aktivitas antibakteri yang lebih tinggi.
Thatte (2004) menyatakan bahwa aktivitas antibakteri kitosan dipengaruhi oleh beberapa faktor, yaitu sumber kitosan, unit monomer yang menyusun kitosan, derajat deasetilasi, pH, bobot molekul kitosan, dan kondisi lingkungan (kadar air, nutrisi yang tersedia bagi mikroba). Solval et al. (2014) menambahkan bahwa nanokitosan memiliki efektivitas antibakteri yang lebih tinggi daripada kitosan karena antara nanokitosan memiliki luas permukaan yang lebih besar, sehingga interaksi antara gugus amina (NH2) lebih besar dengan membran sel bakteri.
16
mengungkapkan bahwa aktivitas antibakteri berbeda antara bakteri Gram positif dan bakteri Gram negatif yang diakibatkan oleh perbedaan karakteristik permukaan sel bakteri. Staphylococcus aureus merupakan jenis bakteri Gram positif. Struktur dinding sel bakteri Gram positif lebih sederhana dibandingkan dinding sel bakteri Gram negatif. Bakteri Gram positif tidak memiliki membran luar sehingga memudahkan senyawa antibakteri menemukan sasaran untuk bekerja (Coyle 2005). No et al. (2002) menambahkan bahwa kitosan menunjukkan efek antibakteri yang besar pada bakteri Gram positif dibandingkan Gram negatif.
KESIMPULAN DAN SARAN
Kesimpulan
Kitosan yang digunakan dalam penelitian ini telah memenuhi standar mutu SNI 7949: 2013. Morfologi nanokitosan memiliki bentuk partikel berupa bulatan, dengan ukuran sebesar 140,94 nm dan PDI sebesar 0,5830. Efektivitas nanokitosan sebagai alternatif zat antibakteri alami dalam pembersih tangan dilakukan pada konsentrasi nanokitosan 1000 ppm hingga 2000 ppm, dengan konsentrasi terbaik diperoleh pada nanokitosan 2000 ppm, dengan presentase efektivitas penurunan total koloni bakteri sebesar 93,44±0,55% dan tidak berbeda nyata terhadap pembersih tangan komersial yaitu sebesar 94,39±0,69%.
Saran
Untuk melengkapi penelitian ini, diperlukan penelitian pula mengenai efektivitas antibakteri dari nanokitosan sebagai pembersih tangan dengan menggunakan keseluruhan telapak tangan, serta penelitian lanjutan mengenai variasi formulasi dari sediaan pembersih tangan tersebut dengan penambahan pelembab dan esens.
DAFTAR PUSTAKA
Abdou ES, Osheba AS, Sorour MA. 2012. Effect of chitosan and chitosan-nanoparticles as active coating on microbiologycal characteristics of fish fingers. Journal of Applied Science and Technology. 2:158-163.
Agnihotri SA, Mallikarjuna NN, Aminabhavi TM. 2004. Recent advances on chitosan-based micro and nanoparticles in drug delivery. Journal of Controlled Release. 100: 5-28.
17
Angka SL, Suhartono MT. 2000. Bioteknologi Hasil Laut: Pemanfaatan Limbah Hasil Laut. Bogor (ID): Pusat Kajian Sumberdaya Pesisir dan Lautan. [AOAC] Association of Official Analytical Chemist. 2005. Washington (US): The
Association of Official Analytical Chemist, Inc.
[APUA] Alliance for the Prudent Use of Antibiotics. 2011. Triclosan. www.apua.org, dapat diakses di www.tufts.edu/med/apua [3 Mei 2015]. [ASTM] American Standard Testing and Material. 2013. ASTM E1252: Standard
Practice for General Techiques for Obtaining Infrared Spectra for Qualitative Analysis. Pennsylvania (US): American Society for Testing Material.
Babeluk R, Jutz S, Mertlitz S, Matlasek J, Klaus C. 2014. Hand hygiene-evaluation of three disinfectant handsanitizer in a community setting. A Public Health Setting: Hand Rubs in Compatison. 9(11): 1-7.
Badar EGB, Arances ZG, Cayumo JP, Cirunay IMA, Cirunay LMD, Lumano MV, Tan NRB. 2014. The antibacterial effectiveness of select commercial handsanitizers against Escherichia coli and Staphylococcus aureus. Journal Advancing Medical Technology Research. 2: 106-130.
Balicka-Ramisz A, Wojtasz-Pajak, Pilarczyka B, Ramisz A, Laurans L. 2005. Antibacterial and antifungal activity of chitosan. ISAH. 2: 406-408.
[BPOM] Badan Pengawas Obat dan Makanan. 2013. Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor 16 Tahun 2013 Tentang Batas Maksimum Penggunaan Bahan Tambahan Pangan Garam Pengemulsi. Jakarta (ID): Badan Pengawas Obat dan Makanan.
Chaiyakosa S, Charernjirtragul W, Umsakul K, Vuddhakul V. 2007. Comparing the efficiency of chitosan with the chlorine for reducing Vibrio parahaemolyticus in shrimp. Journal of Food Control. 61: 199-207.
Chang R dan Overby J. 2011. General Chemistry: The Essential Concepts Sixth Edition 7. New York (US): McGraw-Hill Professional Publishing.
Chung Y, Su Y, Chen C, Jia G, Wang H, Wu JCG, Lin J. 2004. Relationship between antibacterial activity of chitosan and surface characteristics of cell wall. Acta Pharmacol Sin. 25(7): 932-936.
Cimiotti JP, Marmur ES, Nedin M, Hamlin CP, Larson EL. 2003. Adverse reaction associated with an alcohol-based han antiseptic among nurses in a neonatal intensive care unit. American Journal of Infection Control. 31(1): 43-48.
Coyle MB. 2005. Manual of Antimicrobial Susceptibility Testing. Seattle (US): American Society for Microbiology.
Du WL, Niu SS, Xu YL, Xu ZR, Fan CL. 2009. Antibacterial activity of chitosan tripolyphosphate nanoparticles loaded with various metal ions. Carbohydrate Polymers. 75: 385-389.
18
Hogenova HT, Stepankova R, Hudcovic T, Tuckova L, Cukrowska B, Zadnikova RL, Kozakova H, Rossmann P, Bartova J, Sokol D, Funda DP, Brovska D, Rehakova Z, Sinkora J, Hofman J, Dratich P, Kokesova A. 2004. Commensal bacteria (normal microflora), mucosal immunity and chronic inflammatory and autoimmune diseases. Immunology Letters. 93(2004): 97-107.
Honary S, Ghajar K, Khazaeli P, Shalchian P. 2011. Preparation, characterization, and antibacterial of silver-chitosan nanocomposites using different molecular weight grades of chitosan. Tropical Journal of Pharmaceutical Research 10(1): 69-74.
Islam MM, Masum S, Mahbub KR, Haque MZ. 2011. Antibacterial activity of crab-chitosan agains Staphylococcus aureus and Escherichia coli. Journal of Advanced Research. 2(4): 63-66.
[ISO] International Organization for Standardization. 2009. ISO 13320: 2009 Particle Size Analysis-Laser Difraction Methode. London (EN): International Organization for Standardization.
Kampf G, Kramer A. 2004. Epidermiologic background of hand hygiene and evaluation of the most important agent for scrubs and rubs. Clinical Microbiology 17(4): 863-893.
Katas H, Alpar HO. 2006. Development and characterisation of chitosan nanoparticles for siRNA delivery. Journal of Controlled Release. 11(2006): 216-225.
Khan TA, Peh KK, Chang HS. 2002. Reposting degree of deacetylation values of chitosan: the influence of analytical methods. Journal of Pharmacy and Pharmaceutical Science. 5(3): 205-2012.
Kim TY, Cho SY. 2005. Adopsi equilibria of reactive dye onto highly polyaminatid porous chitosan bead. Journal Chemistry English. 22(5): 691-696.
Kumar MNV, Muzzarelli RRA, Sahiwa H, Domb AJ. 2004. Chitosan chemistry and pharmaceutical perspectives. Chemical Reviews. 104: 6017-6084.
Kurniawati N. 2014. Enkapsulasi nanokitosan pada ekstrak daun tapak dara (Catharanthus roseus) sebagai antihiperglikemia [skripsi]. Bogor (ID): Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Mohanraj UJ, Chen Y. 2006. Nanoparticle- A Review. Tropical Journal of Pharmaceutical Research. 5(1): 561-573.
No HK, Park NY, Lee SH, Meyers SP. 2002. Antibacterial activity of chitosan and chitosan oligomers with different molecular weight. International Journal of Food Microbiology. 74(2002): 65-72.
OchemOnline. 2013. Infrared spectroscopy absorption table. Dapat diakses di http://ochemonline.com/ [12 Juni 2015].
Pelczar MJ, Chan ECS. 2006. Dasar-Dasar Mikrobiologi Edisi 2. Jakarta (ID): Universitas Indonesia Press.
19
Raafat D, Bargen KV, Haas A, Sahl HG. 2008. Insights into the mode of action of chitosan as an antibacterial compound. Journal Applied and Environmental Mocrobiology. 74(23): 3764-3773.
Rachmania D. 2011. Karakteristik nanokitosan cangkang udang vananmei (Litopenaes vannamei) dengan metode gelasi ionik [skripsi]. Bogor (ID): Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Reddish GF. 1961. Antiseptics, Desinfectants, Fungicides, and Chemical and Physical Sterilization, Reddish GF, editor, Philadelphia (US): Lea and Febinger.
Robbins R. 2013. Scanning Electron Microscope Operation. Dallas (US): The University of Texas.
Sano H, Shibasaki K, Matsukobo T, Takaesu Y. 2003. Effect of chitosan rinsing on reduction of dental plaque formation. Bull Tokyo Dent. Coll. 44(1): 9-16.
Shalini S, Prema S. 2012. Phytochemical screening and antimicrobial activity of plant extracts for disease management. International Journal of Current Science. 209-218.
Solval SS, Santos MI, Coutinho OP, Mano JF, Reis RL. 2005. Physical properties and biocompatibility of chitosan/sury blendet membran. Journal of Material Science. 16: 575-579.
[SNI] Standar Nasional Indonesia. 7949-2013. Kitosan, syarat mutu dan pengolahan. Jakarta (ID): Badan Standardisasi Nasional.
Solval KA, Rodezno LAE, Moncada M, Bankston D, Sthaviel S. 2014. Evaluation of chitosan nanoparticles as a glazing material for cryogenically frozen shrimp. Journal Food Science and Technology. 57: 172-180.
Steel RGD, Torrie JH. 1993. Prinsip dan Prosedur Statistika: Suatu Pendekatan Biometrik. Terjemahan: Bambang Sumantri. Jakarta (ID): Gramedia Utama. Suptijah P. 2006. Deskripsi karakteristik fungsional dan aplikasi kitin kitosan.
Prosiding Seminar Nasional Kitin Kitosan: 14-24.
Suptijah P, Jacoeb MA, Rachamania D. 2011. Karakterisasi nanokitosan cangkang udang vannamei (Litopenaus vannamei) dengan metode gelasi ionik. Jurnal Pengolahan Hasil Perikanan Indonesia. 17(2): 78-84.
Suwarda R, Maarif MS. 2012. Pengembangan inovasi terknologi nanopartikel berbasis pati untuk menciptakan produk yang berdaya saing. Jurnal Teknik Industri. 2(1): 109-122.
Thatte MR. 2004. Synthesis and antibacterial assessment of water soluble hydrophobic chitosan derivatives bearing quaternary ammonium functionality [disertasi]. Los Angeles (US): Lousiana State University and Agricultural and Mechanical Collage.
20
Tiyaboonchai W. 2003. Chitosan nanoparticles: a promising system for drug delivery. Naresua University Journal. 11(3): 51-66.
Tsai GJ, Su WH. 1999. Antibacterial activity of shrimp chitosan against Echerichia coli. Journal of Food Protection. 62(3): 239-243.
Xia WS. 2003. Physiological activities of chitosan and its application in functional food. Journal of Chinese Institute of Food Science and Technology. 3: 77-81.
Yongmei X, Yumin D. 2003. Effect of melecular structure of chitosan on protein delivery properties of chitosan nanoparticles. Journal of Pharmaceutics. 250: 215-226.
Zaragoza M, Salles M, Gomez J, Bayas JM, Trilla A. Handwashing with soap or alcoholic solutions? A randomized clinical trial of its effectiveness. American Journal of Infection Control. 27(3): 258-261.
21
23
Lampiran 1 Tahap hand disinfection sesuai dengan EN1500
Lampiran 2 Hasil analisis spektra inframerah dari kitosan
Lampiran 2a Analisis dan interpretasi spektra inframerah dari kitosan
Lampiran 2b Hasil perhitungan derajat deasetilasi kitosan Bilangan
gelombang (cm-1)*
Bilangan
gelombang (cm-1)
Chitosan
%T Struktur weak/ medium/
strong Gugus
1650-1580 1580 12,334 N-H bending strong amine
3500-3400 3350 1,413 N-H stretching medium secondary amine
1085-1050 1074 11,482 C-O stretching strong primary alcohol
3550-3200 3431-3429 1,001 C-O stretching strong alcohol
1450-1375 1375 13,186 C-H bending strong alkane
3200-2700 2920 4,919 O-H stretching weak alcohol
P
P
P
24
� = � ���
= log 0,13 – log 0,82
= - 0,1801
� = � ���
= log 0,28 – log 0,73
= - 0,9602
% DD = − [�1 ,
� , × , ] × %
= − [− ,
− , × , ] × %
= − [ , ×
, ] × %
= , %
Lampiran 3 Proses pembuatan nanokitosan dengan menggunakan magnetic stirrer
25
Lampiran 5 Hasil analisis efektivitas perlakuan terbaik Ua
Lampiran 6 Grafik hasil analisis Particle Size Analyze (PSA)
Lampiran 6a Rata-rata ukuran nanokitosan berdasarkan intensitas, angka, dan volume
Lampiran 6b Rata-rata ukuran nanokitosan berdasarkan volume
26
Lampiran 6d Rata-rata ukuran nanokitosan berdasarkan angka
Lampiran 7 Analisis statistik presentase efektivitas pembersih tangan nanokitosan
Lampiran 7a Analisis homogenitas
Levene Statistic df1 df2 Sig.
0,211 3 6 0,451a
a nilai Sig. lebih besar dari 0,05, maka data efektivitas pembersih tangan mempunyai varian yang sama
Lampiran 7b Analisis ragam Sumber
Variasi
Rerata Kuadrat
Simpangan df MS Fhit Ftabel
Kelompok 1,435466667 2 0,717733333 0,992075194 5,143253
Konsentrasi 1089,455825 3 363,1519417 501,9608482 4,757063
Galat 4,3408 6 0,723466667
Total 1095,232092 11
Lampiran 7c Uji lanjut Duncan
Perlakuan N Galat untuk α = 0,05
1 2 3
Nanokitosan 1000 ppm 3 70,7900
Nanokitosan 1500 ppm 3 83,3200
Nanokitosan 2000 ppm 3 93,4400
Pembersih tangan komersial 3 94,3867
RIWAYAT HIDUP
Penulis dilahirkan di Banyuwangi pada tanggal 29 Juli 1993. Penulis merupakan putri pertama pasangan Saiful Bahri dan Holifah. Tahun 2011 penulis lulus dari SMA Negeri 5 Kota Tangerang dan pada tahun yang sama penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Ujian Talenta Mandiri (UTM) masuk IPB dan diterima di Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan.
Selama mengikuti perkuliahan, penulis menjadi asisten praktikum Pengantar Desain Alat Uji Praktis dan Metode Deteksi Mutu Bahan Baku Hasil Perairan 2014/2015, asisten praktikum Teknologi Pengolahan Kitin dan Kitosan 2015/2016. Penulis juga aktif sebagai pengurus Himpunan Mahasiswa Teknologi Hasil Perairan (HIMASILKAN) 2013/2014 dan 2014/2015, serta dalam berbagai kepanitian.