MUTU NATA DE MADOE HASIL FERMENTASI
ACETOBACTER XYLINUM PADA MEDIA
BERBAHAN DASAR MADU AFKIR
SKRIPSI
REGINA MORINA SIMANGUNSONG
DEPARTEMEN ILMU PRODUKSI DAN TEKNOLOGI PETERNAKAN FAKULTAS PETERNAKAN
i
RINGKASAN
Regina Morina Simangunsong D14080290. 2012. Mutu Nata de Madoe Hasil Fermentasi Acetobacter xylinum pada Media Berbahan Dasar Madu Afkir.
Skripsi. Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan, Institut Pertanian Bogor.
Pembimbing Utama : Ir. B. N. Polii, S.U.
Pembimbing Aggota : Ir. Hotnida C. H. Siregar, M. Si.
Madu adalah salah satu jenis pangan yang sangat lengkap kandungan nutrisinya dan kini telah diketahui tidak kurang dari 181 macam zat atau senyawa dalam madu. Madu memiliki sifat higroskopis yang tinggi, yaitu sangat mudah menyerap air dari lingkungan sekitar apabila terjadi kontak langsung dengan udara sehingga memicu peningkatan kadar air madu. Semakin tinggi kadar air dapat mempercepat kerusakan madu sebab memicu pertumbuhan khamir dalam madu.
Suatu kasus menarik di penjual yaitu ditemukan sejumlah besar madu hutan afkir yang disimpan di dalam jeriken. Madu hutan afkir ini adalah madu yang tidak laku di pasaran yang ditarik kembali kemudian sebagian dikirim ke peternak untuk dijadikan pakan lebah dan sebagian disimpan di dalam gudang. Karakteristik madu hutan afkir ini adalah adanya perubahan warna yang semakin gelap, aroma yang kurang sedap, rasa yang menjadi asam dan sedikit pahit, kadar air yang sangat tinggi tetapi kadar gula dari madu hutan afkir ini cukup tinggi (72%). Oleh sebab, itu madu hutan afkir ini dapat menggantikan air kelapa dalam pembuatan nata serta tidak perlu penambahan sukrosa sebagai sumber karbohidrat.
Pembuatan nata de madoe merupakan suatu diversifikasi produk yang menunjukkan bahwa madu hutan afkir yang hendak dijadikan pakan lebah dapat dimanfaatkan sebagai bahan pangan dengan cara fermentasi oleh bakteri nata yaitu Acetobacter xylinum. Pengolahan madu hutan afkir menjadi nata de madoe diharapkan dapat memberikan pilihan pada konsumen dalam pemenuhan kebutuhan pangan fungsional bagi tubuhnya.
Pembuatan nata de madoe tidak dapat dihasilkan dari madu saja tapi harus dibantu dengan penambahan nutrisi lain seperti air kelapa sebagai media tumbuh alami Acetobakter xylinum dan whey. Hal ini disebabkan adanya zat anti mikroba yang menghambat pertumbuhan bakteri pembentuk nata.
Penelitian ini dilaksanakan pada bulan Januari sampai Juni 2012 di Laboratorium Fakultas Peternakan Institut Pertanian Bogor. Tujuan dari penelitian ini adalah mencari cara pemanfaatan madu hutan afkir untuk mendapatkan produk nata dengan kualitas fisik dan kimia yang memenuhi persyaratan serta diterima oleh panelis.
ii kekenyalan dan warna nata), karakteristik kimia (kadar air, kadar abu, kadar serat kasar, kadar protein, kadar lemak dan kadar serat makanan) dan tingkat kesukaan (warna, aroma, rasa, kekenyalan dan kesan secara keseluruhan). Rancangan percobaan yang digunakan adalah rancangan acak lengkap pola searah (4x1) dengan 3 kali ulangan. Perlakuan yang digunakan adalah media fermentasi (madu hutan afkir, madu hutan afkir whey, madu hutan afkir air kelapa dan madu hutan afkir whey air kelapa). Pada penilaian sensori sebelum disajikan nata direndam terlebih dahulu dengan larutan madu dengan kadar gula 15% dan 20%.
Perbedaan media fermentasi berpengaruh sangat nyata (P<0,01) terhadap rendemen, ketebalan, kekenyalan dan warna nata. Mutu kimia nata terbaik yaitu nata de madoe pada media madu afkir air kelapa adalah sebagai berikut : kadar air 96,4%, kadar abu 0,18%, kadar serat kasar 0,4%, kadar lemak 1,56%, kadar protein 0,9% dan kadar serat makanan 0,11%. Uji hedonik menunjukkan bahwa nata de madoe direndam dengan larutan madu kadar gula 15% lebih disukai dibandingkan dengan nata de madoe direndam dengan larutan madu kadar gula 20% tetapi dari semua sampel yang disajikan panelis lebih menyukai nata de coco komersil dengan kadar gula 15%.
Madu hutan afkir dapat dimanfaatkan sebagai bahan baku pembuatan nata dengan bantuan nutrisi tambahan berupa air kelapa dan whey. Nata terbaik dihasilkan dari media fermentasi madu hutan afkir ditambah air kelapa dengan nilai serat makanan sebesar 0,11% memenuhi standar nata dalam kemasan yaitu maksimal 4,5%. Panelis menyukai produk nata de madoe yang direndam larutan madu dengan kadar gula 15%.
iii
ABSTRACT
The Quality of Nata de Madoe from Kinds of Fermentation Medium Based Rejected Honey
Simangunsong, R. M., B. N. Polii and H. C. H. Siregar
Nata is a jelly formed fermented food product from Acetobacter xylinum. Nata has properties such as low calorie, able to facilitate healthy digestion, and consisted of 98% water content. Nata generaly made from water coconut, but in this research nata made from other material that had high sugar content such as honey and so it called nata de madoe. Honey contain essential elements for the body and easily fermented so that reducing honey shelf life. Founded an interesting case in public there are a large amount of honey was returned from the market. This rejected honey content glucose 72%, that can be replaced coconut water as material for nata without the addition of sucrose, but to fulfill nitrogen needed, ammonium sulfate was added. Observing parameters are the physical characteristic and chemical characteristics and test sensory. The variance analyze showed that different fermentation medium influenced significally (P<0,01) to rendemen, thickness, hardness and colour of nata. The best appearance from different media is media rejected honey with coconut water, result analysis proksimat are 96,4 water content, 0,18 ash content, 0,4% crude fiber, 1,56 fat, 0,9% protein and 0,11% dietary fiber. Sensory test showed that nata de madoe soak in 15% honey solution was more preferred than in 20% honey solution but less than commercial nata de coco in 15% sugar solution.
iv
MUTU NATA DE MADOE HASIL FERMENTASI
ACETOBACTER XYLINUM PADA MEDIA
BERBAHAN DASAR MADU AFKIR
REGINA MORINA SIMANGUNSONG D14080290
Skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Peternakan pada
Fakultas Peternakan Institut Peternakan Bogor
DEPARTEMEN ILMU PRODUKSI DAN TEKNOLOGI PETERNAKAN FAKULTAS PETERNAKAN
v
Judul : Mutu Nata de Madoe Hasil Fermentasi Acetobacter xylinum pada Media Berbahan Dasar Madu Afkir
Nama : Regina Morina Simangunsong NRP : D14080290
Menyetujui,
Pembimbing Utama, Pembimbing Anggota,
( Ir. B. N. Polii, SU) ( Ir. Hotnida C. H. Siregar, M.Si.) NIP : 19480402 198003 2 001 NIP : 19620617 199003 2 001
Mengetahui, Ketua Departermen
Ilmu Produksi dan Teknologi Peternakan
( Prof. Dr. Ir. Cece Sumantri, M.Agr.Sc) NIP : 19591212 198603 1 004
vi
RIWAYAT HIDUP
Penulis dilahirkan pada tanggal 17 September 1989 di Pematang Siantar.
Penulis adalah anak keempat dari enam bersaudara dari pasangan Mangatur
Simangunsong dan Riama Tambunan.
Penulis menyelesaikan pendidikan kanak-kanak di TK Santa Theresia Balige
pada tahun 1994, pendidikan dasar di SD Katolik Sanfrancesco Balige lulus pada
tahun 2001, pendidikan menengah pertama di SLTP Budhi Dharma Balige lulus pada
tahun 2004, pendidikan menengah atas di SMA Santo Thomas 2 Medan lulus pada
tahun 2007. Penulis diterima sebagai mahasiswa pada Program Studi Teknologi
Produksi Peternakan, Departemen Ilmu Produksi dan Teknologi Peternakan, Institut
Pertanian Bogor pada tahun 2008 melalui jalur SNMPTN.
Selama mengikuti perkuliahan di IPB, Penulis aktif di beberapa kegiatan
kemahasiswaan yaitu Persekutuan Mahasiswa Kristen (2008-2012), Komisi Literatur
(2011), Persekutuan Okumene Protestan dan Katolik (POPK) pada tahun
2009-2011, Himpunan Mahasiswa Produksi Peternakan (HIMAPROTER) pada tahun
2009-2011 sebagai anggota divisi keprofesian unggas, Gerakan Mahasiswa Kristen
Indonesia (2011-2012), Ikatan Anak Siantar dan Sekitarnya (IKANMASS)
2008-2012. Penulis mengikuti program BEST (Building Entrepreneur Student Training)
Fakultas Peternakan. Penulis aktif dibidang olah raga menjadi tim basket putri
Fakutas Peternakan menjadi pemenang juara II basket putri tahun 2009, juara II
basket putri tahun 2010 dan juara I basket putri tahun 2012 tingkat Fakultas
Peternakan, Institut Pertanian Bogor. Penulis juga penerima dana penelitian untuk
progran kreatifitas mahasiswa (PKM-P) Whey Kefir. Penulis juga menjadi asisten
vii
KATA PENGANTAR
Puji syukur Penulis panjatkan ke hadirat Tuhan Yesus Kristus atas segala
berkat dan karunia-Nya yang tiada pernah berkesudahaan sehingga Penulis dapat
menyelesaikan skripsi yang berjudul “Mutu Nata de Madoe Hasil Fermentasi Acetobacter xylinum pada Media Berbahan Dasar Madu Afkir”, yang merupakan
salah satu syarat kelulusan untuk memperoleh gelar Sarjana Peternakan di
Departemen Ilmu Produksi dan Teknologi Peternakan, Fakultas Peternakan, Institut
Pertanian Bogor.
Madu hutan afkir selama ini hanya dipergunakan untuk formulasi pakan
lebah. Setelah diteliti ternyata madu hutan afkir memiliki kandungan nutrisi yang
cukup tinggi untuk dijadikan suatu produk bahan makanan seperti cuka madu dan
tidak menutup kemungkinan menjadi produk nata karena memiliki kandungan gula
cukup tinggi. Gula pada pembentukan nata diubah oleh Acetobacter xylinum
menjadi selulosa ekstraseluler. Hasil uji trial and error menunjukkan bahwa
pembuatan nata dari madu hutan afkir kurang bagus hasilnya sehingga diteliti
beberapa media fermentasi yang dapat menghasilkan nata yang mutunya lebih baik
dengan penambahan amonium sulfat sebagai nutrisi tambahan untuk pertumbuhan
Acetobacter xylinum.
Penelitian ini dilaksanakan pada bulan Januari sampai Juni 2012 di Fakultas
Peternakan, Institut Pertanian Bogor. Skripsi ini membahas tentang karakteristik
fisik, kimia dan tingkat kesukaan nata de madoe yang berasal dari media fermentasi
yang berbeda yaitu madu hutan afkir, madu hutan afkir ditambah whey, madu hutan
afkir ditambah air kelapa dan madu hutan afkir ditambah whey dan air kelapa serta
madu segar sebagai kontrol.
Penulis menyadari bahwa penulisan skripsi ini terdapat banyak kekurangan
dan masih jauh dari sempurna. Penulis berharap skripsi ini dapat memberikan
manfaat bagi masyarakat luas, khususnya bagi dunia peternakan serta pembaca pada
umumnya.
Bogor, September 2012
viii
Starter Nata (Acetobacter xylinum)……….. 9
Amonium Sulfat.………. 12
Sifat Kimia Madu Hutan Afkir………. 18
Kadar Gula………. 18
ix
Kadar air……… 18
Kadar abu………... 19
Kadar Hidroksimetilfurfural (HMF)……….. 19
Kemurnian dan Viabilitas Starter A.xylinum……….... 20
Pengenceran Madu Afkir………... 21
Kemurnian dan Viabilitas starter A. xylinum………... 33
x
KESIMPULAN DAN SARAN……….. 52
Kesimpulan………. 52
Saran………... 52
UCAPAN TERIMAKASIH……….. 53
DAFTAR PUSTAKA……… 54
xi
DAFTAR TABEL
1. Komposisi Kimia Madu………... 4
2. Standar Nasional Mutu Madu Indonesia……….. 5
3. Kondisi Optimum untuk Memproduksi Nata pada Media Air Kelapa…. 6 4. Standar Mutu Produk Nata Dalam Kemasan……… 7
5. Komposisi Whey dan Air Kelapa………. 9
6. Kategori Warna Menurut Kisaran Nilai °Hue……….. 15
7. Sifat Kimia Madu Hutan Afkir yang Digunakan………. 32
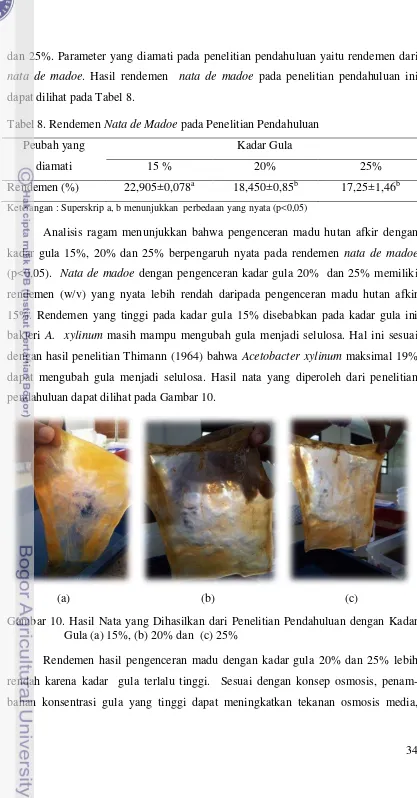
8. Rendemen Nata de Madoe pada Penelitian Pendahuluan……… 34
9. Nilai pH Media Fermentasi yang Digunakan………... 36
10. Karakteristik Fisik Nata de Madoe………... 36
11. Karakteristik Kimia Nata de Madoe………. 42
12. Uji Hedonik Nata de Madoe Terhadap Warna, Aroma, Rasa, Kekenyalan dan Kesan Secara Keseluruhan……… 48
xii
DAFTAR GAMBAR
1. Mekanisme Pembentukan Selulosa oleh Acetobacter xylinum………… 11
2. Ikatan β (1-4) antar Unit Glukosa pada Selulosa………. 14
3. Acetobacter xylinum yang Digores pada Media MRSA………... 20
4. Proses Pembuatan Nata de Madoe pada Penelitian Pendahuluan……… 22
5. Bagan Penelitian………...……….... 23
6. Penetrometer ………..………... 25
7. Chromameter Minolta CR-310……….... 26
8. Nata yang Terkontaminasi Khamir………...……… 31
9. Morfologi Acetobacter xylinum……… 33
10. Hasil Nata yang Dihasilkan dari Penelitian Pendahuluan dengan Kadar Gula (a) 15%, (b) 20% dan (c) 25%... 34
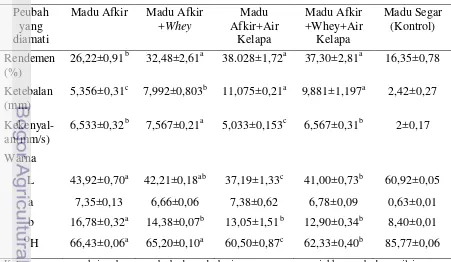
11. Nilai Rataan Rendemen dari Kelima Media Fermentasi………….……. 37
12. Nilai Rataan Ketebalan Nata dari Kelima Media Fermentasi……….…. 38
13. Nilai Rataan Kekenyalan Nata dari Kelima Media Fermentasi………... 39
14. Warna Nata yang Dihasilkan dari Media Fermentasi (a) Madu Hutan Afkir, (b) Madu Hutan Afkir Whey, (c) Madu Hutan Afkir Air Kelapa, (d) Madu Hutan Afkir Whey Air Kelapa dan (e) Madu Segar... 41
15. Kadar Air Nata de Madoe………. 43
16. Kadar Abu Nata de Madoe………... 44
17. Kadar Serat Kasar Nata de Madoe………... 45
18. Warna Sampel (a) Nata de Madoe dan (b) Nata de Coco Komersil…… 48
xiii
DAFTAR LAMPIRAN
1. Hasil Analisis Ragam Rendemen Penelitian Pendahuluan………. 60
2. Hasil Analisis Ragam Rendemen Penelitian Lanjutan Nata de Madoe... 60
3. Hasil Analisis Ragam Ketebalan Nata de Madoe... 60
4. Hasil Analisis Ragam Kekenyalan Nata de Madoe………... 61
5. Hasil Analisis Nilai Lightness Nata de Madoe……… 61
6. Hasil Analisis Ragam Nilai a Nata de Madoe……….. 62
7. Hasil Analisis Ragam Nilai b Nata de Madoe………. 62
8. Hasil Analisis Ragam Nilai ºHUE Nata de Madoe……….. 62
9. Hasil Analisis Ragam Warna pada Uji Hedonik Nata………. 63
10. Hasil Analisis Ragam Aroma pada Uji Hedonik Nata………. 63
11. Hasil Analisis Ragam Rasa pada Uji Hedonik Nata………... 63
12. Hasil Analisis Ragam Kekenyalan pada Uji Hedonik Nata………. 63
13. Hasil Analisis Ragam Kesan Secara Keseluruhan pada Uji Hedonik Nata……….. 64
14. Hasil Uji Analisis Proksimat Nata de Madoe Hedonik……… 64
15. Form Uji ………..……… 65
1
PENDAHULUAN
Latar Belakang
Madu telah dikenal dan dikonsumsi manusia sejak berabad tahun yang lalu.
Manusia menyadari bahwa mengkonsumsi madu dapat menjaga kondisi tubuh agar
tetap sehat karena madu merupakan salah satu jenis pangan yang memiliki nutrisi
yang sangat lengkap dan telah diketahui 181 macam zat atau senyawa yang
terkandung di dalamnya.
Madu memiliki komponen nutrisi yang sangat lengkap, sebagian besar terdiri
atas gula dan enzim kompleks yang memungkinkan terjadi beberapa reaksi
biokimia. Reaksi ini dapat mempengaruhi kualitas madu sehingga terjadi perubahan
komposisi, rasa, aroma, viskositas dan warna.
Madu juga memiliki sifat higroskopis yang tinggi yaitu sangat mudah
menyerap air dari lingkungan sekitar apabila terjadi kontak langsung dengan udara
sehingga memicu peningkatan kadar air madu. Kadar air yang tinggi dapat memicu
pertumbuhan khamir seperti Zygosaccharomyces dalam madu sehingga mempercepat
kerusakan madu .
Ditemukan suatu kasus menarik di tingkat penjual madu yaitu terdapat
sejumlah besar madu hutan afkir yang tidak laku lagi di jual. Madu afkir tersebut
tidak banyak dimanfaatkan. Sebagian dari madu tersebut ada yang dikembalikan ke
peternak untuk diformulasikan lagi sebagai pakan lebah dan sisanya hanya dibiarkan
tersimpan di jeriken dan di tumpuk di gudang. Karakteristik madu hutan afkir adalah
warna yang semakin gelap, aroma kurang sedap, rasanya asam, sedikit pahit, kadar
gulanya tinggi lebih dari 70% dan kadar air lebih dari 29%. Kadar gula madu hutan
afkir cukup tinggi sehingga memungkinkan untuk dimanfaatkan sebagai sumber
karbon bagi Acetobacter xylinum.
Madu hutan afkir banyak yang tidak dimanfaatkan, sehingga perlu dicarikan
solusi untuk meningkatkan nilai tambahnya. Salah satu upaya cara pemanfaatan
madu hutan afkir adalah pembuatan nata de madoe melalui proses fermentasi gula
menjadi selulosa dengan bantuan A. xylinum dengan penambahan amonium sulfat
sebagai sumber nitrogen.
Nata merupakan produk makanan hasil fermentasi yang kaya akan serat,
2 fermentasinya. Selulosa yang dibentuk oleh bakteri A. xylinum mengandung air
sekitar 98%, kadar serat kasar sekitar 2,5%. Kandungan seratnya yang tinggi
menyebabkan nata sangat membantu dalam proses fisiologis tubuh, yaitu untuk
memperlancar pencernaan. Nata juga tergolong makanan rendah kalori dan tidak
mengandung kolesterol sehingga aman dikonsumsi oleh penderita diabetes.
Nata pada mulanya dibuat dari air kelapa dan dikenal dengan nama nata de
coco. Perkembangan industri yang semakin pesat menghasilkan produk nata yang
bervariasi. Nata tidak lagi hanya berbahan dasar air kelapa tetapi dapat dibuat dari
bahan lain seperti sari buah yang cukup mengandung gula seperti nenas dengan nama
nata de pina, tomat dengan nata de tomato, coklat dengan nata de cacao, whey
dengan nata de whey dan madu dengan nata de madoe. Prinsip proses pengolahan
semua nata tersebut sama yaitu memanfaatkan A. xylinum dalam proses
fermentasinya hanya saja media fermentasinya yang berbeda.
Beberapa percobaan sebelumnya diketahui bahwa pertumbuhan A. xylinum
pada madu hutan afkir kurang bagus sehingga perlu dicari solusi memperbaiki
kualitas nata yang dihasilkan antara lain dengan diberikan campuran air kelapa dan
whey sebagai sumber nutrisi tambahan. Air kelapa merupakan media fermentasi
alami A. xylinum sedangkan whey merupakan produk peternakan hasil ikutan olahan
keju yang masih mempunyai kandungan nutrisi cukup banyak. Whey telah diteliti
sebelumnya dapat menghasilkan nata dengan kualitas baik sehingga hal ini dapat
membantu pertumbuhan A. xylinum dalam pembuatan nata de madoe. Pembuatan
nata de madoe diharapkan dapat menambah peluang pengembangan industri rumah
tangga.
Tujuan
Penelitian ini bertujuan mencari cara pemanfaatan madu hutan afkir untuk
pembentukan produk nata dengan mutu fisik dan kimia yang memenuhi persyaratan
3
TINJAUAN PUSTAKA
Madu
Madu adalah zat pemanis alami yang diproduski oleh lebah madu dari nektar
tanaman atau sekresi bagian lain dari tanaman atau ekresi dari insekta pengisap
tanaman, yang dikumpulkan, diubah dan dikombinasikan dengan zat tertentu dari
lebah kemudian ditempatkan, dikeringkan, lalu disimpan dalam sarang hingga
matang (Codex, 1989). Standar Nasional Indonesia (2004) mendefinisikan madu
adalah cairan alami yang umumnya mempunyai rasa manis yang dihasilkan oleh
lebah madu dari sari bunga tanaman (floral nektar) atau bagian lain dari tanaman
(ekstra floral nektar) atau eksresi serangga.
Lebah memproduksi madu dengan bahan nektar yang merupakan cairan
mengandung gula yang disekresikan oleh kelenjar nektari tanaman. Selain nektar,
lebah madu juga menggunakan nambur madu (honeydew) sebagai bahan baku madu.
Nambur madu merupakan ekskreta serangga yang mengisap cairan floem
(Sihombing, 2005).
Madu biasanya digolongkan berdasarkan sumber nektarnya. Madu
monoflora digolongkan sebagai madu yang bersumber dari nektar yang didominasi
oleh satu jenis tanaman (bunga) seperti madu randu, madu karet, madu lengkeng dan
madu kaliandra. Apabila sumber nektar dari berbagai jenis tanaman, maka madu
yang dihasilkan digolongkan sebagai madu multiflora, misalnya madu Nusantara,
madu Kalimantan dan madu Sumba. Perbedaan sumber nektar merupakan salah satu
faktor yang mempengaruhi karakteristik madu (Sihombing, 2005)
Madu memiliki sifat higroskopis yang tinggi, yaitu sangat mudah menyerap
air dari lingkungan sekitar apabila terjadi kontak langsung dengan udara sehingga
memicu peningkatan kadar air madu. Kadar air yang semakin tinggi dapat
mempercepat pertumbuhan khamir dalam madu. Secara alami madu mengandung
khamir yang bersifat osmofilik yang dapat tumbuh pada medium dengan aktivitas air
rendah, yaitu 0,62-0,65 (Fardiaz, 1992). Semakin banyak madu menyerap air maka
kualitas mutunya semakin rendah sehingga dapat dikategorikan sebagai madu afkir.
Zat yang terkandung dalam madu sangat kompleks dan kini telah diketahui
tidak kurang dari 181 macam zat atau senyawa dalam madu. Komposisi madu
4 faktor-faktor eksternal seperti cuaca dan iklim (Sihombing, 2005). Komposisi kimia
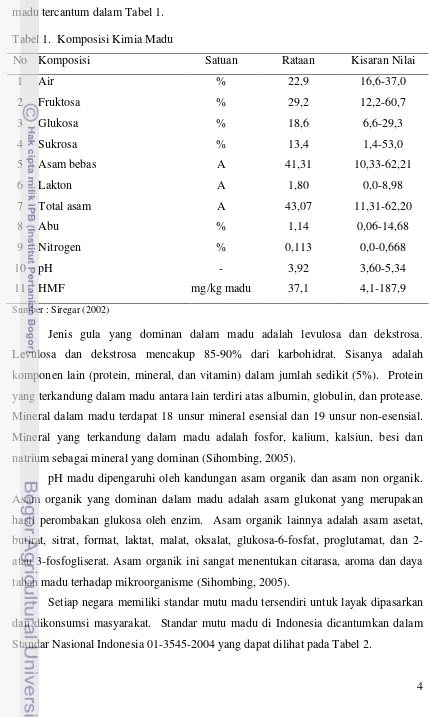
madu tercantum dalam Tabel 1.
Tabel 1. Komposisi Kimia Madu
No Komposisi Satuan Rataan Kisaran Nilai
1 Air % 22,9 16,6-37,0
2 Fruktosa % 29,2 12,2-60,7
3 Glukosa % 18,6 6,6-29,3
4 Sukrosa % 13,4 1,4-53,0
5 Asam bebas A 41,31 10,33-62,21
6 Lakton A 1,80 0,0-8,98
7 Total asam A 43,07 11,31-62,20
8 Abu % 1,14 0,06-14,68
9 Nitrogen % 0,113 0,0-0,668
10 pH - 3,92 3,60-5,34
11 HMF mg/kg madu 37,1 4,1-187,9
Sumber : Siregar (2002)
Jenis gula yang dominan dalam madu adalah levulosa dan dekstrosa.
Levulosa dan dekstrosa mencakup 85-90% dari karbohidrat. Sisanya adalah
komponen lain (protein, mineral, dan vitamin) dalam jumlah sedikit (5%). Protein
yang terkandung dalam madu antara lain terdiri atas albumin, globulin, dan protease.
Mineral dalam madu terdapat 18 unsur mineral esensial dan 19 unsur non-esensial.
Mineral yang terkandung dalam madu adalah fosfor, kalium, kalsiun, besi dan
natrium sebagai mineral yang dominan (Sihombing, 2005).
pH madu dipengaruhi oleh kandungan asam organik dan asam non organik.
Asam organik yang dominan dalam madu adalah asam glukonat yang merupakan
hasil perombakan glukosa oleh enzim. Asam organik lainnya adalah asam asetat,
butirat, sitrat, format, laktat, malat, oksalat, glukosa-6-fosfat, proglutamat, dan 2-
atau 3-fosfogliserat. Asam organik ini sangat menentukan citarasa, aroma dan daya
tahan madu terhadap mikroorganisme (Sihombing, 2005).
Setiap negara memiliki standar mutu madu tersendiri untuk layak dipasarkan
dan dikonsumsi masyarakat. Standar mutu madu di Indonesia dicantumkan dalam
5 Tabel 2. Standar Nasional Mutu Madu Indonesia
No Jenis Uji Satuan Persyaratan
1 Aktivitas enzim diastase Diastase Number Maksimal 3
2 Hidroksimetilfurfural (HMF) mg/kg Maksimal 50
3 Air % Maksimal 22
4 Gula Pereduksi % b/b Maksimal 65
5 Sukrosa % b/b Maksimal 5
6 Keasaman ml NaOH 1 N/kg Maksimal 50
7 Padatan yang tak larut air % b/b Maksimal 0,5
8 Abu % b/b Maksimal 0,5
Sumber : SNI 01-3545-2004
Kadar HMF di Indonesia maksimal 50% tetapi sering ditemui madu dengan
kadar HMF diatas standar. Hal ini disebabkan kadar air madu di Indonesia cukup
tinggi sehingga diperlukan perlakuan untuk mengurangi kadar air madu tersebut
dengan pemanasan. Pemanasan madu di masyarakat banyak yang tidak terkontrol
sehingga memicu peningkatan kadar HMF yang berakibat penurunan kualitas madu
dan tidak sesuai dengan standar yang telah ditetapkan.
Nata
Istilah nata diduga berasal dari bahasa Spanyol yaitu nadir yang berarti
berenang, Nata juga berasal dari bahasa Latin yaitu nature, yang berarti
terapung-apung. Nata merupakan produk fermentasi dihasilkan oleh bakteri Acetobacter
xylinum pada substrat yang mengandung gula. Gula dimanfaatkan untuk aktivitas
metabolisme dan membentuk polisakarida yang dikenal dengan extracellular
sellulosa berbentuk gel (Setiani, 2007). Hidayat et al. (2006) menyatakan bahwa
nata adalah suatu zat yang menyerupai gel, tidak larut dalam air dan terbentuk pada
permukaan media fermentasi air kelapa dan beberapa sari buah masam. Sedangkan
menurut Alaban (1961) nata adalah selulosa bakteri dengan tekstur agak kenyal padat
dan mempunyai konsistensi yang tegas dan kokoh, hasil sintesa gula oleh A. xylinum
dan berwarna putih dan transparan.
Nata dapat dibuat dari air kelapa, nenas, whey susu, whey tahu, tomat, lidah
buaya, rumput laut, ubi, dll. Nama dagang nata mengacu pada bahan baku yang
6 fermentasinya, seperti nata de coco untuk produk dari air kelapa, nata de pina dari
limbah nenas, nata de soya dari limbah tahu dan dari limbah keju dikenal dengan
nama nata de whey, nata de aloe dari lidah buaya, nata de tomato dari tomat, nata de
gracillaria dari bahan dasar rumput laut (Suryani et al., 2007).
Keberhasilan pembentukan nata dipengaruhi dari faktor intrinsik dan
ekstrinsik. Faktor intrisik berupa kemampuan hidup (viabilitas) A. xylinum dalam
mengubah glukosa menjadi selulosa, pH, sumber nitrogen dan sumber karbon
(Pambayun, 2006). Faktor ekstrinsik berupa kondisi fermentasi (suhu dan
kelembapan) suhu optimum A.xylinum 28 °C, lama fermentasi, ketinggian media
dalam wadah, luas permukaan wadah, ukuran wadah dan kebersihan lingkungan
fermentasi. Semakin tinggi media dan semakin lama waktu inkubasi akan
menghasilkan nata yang tebal (Darmajana, 2004). Kondisi optimum untuk
memproduksi nata dari air kelapa tercantum pada Tabel 3.
Tabel 3. Kondisi Optimum untuk Memproduksi Nata pada Media Air Kelapa
Parameter Alaban (1961) Lapuz et al. (1967)
Sumber karbon Sukrosa (5-8%) Glukosa dan sukrosa (5%)
Sumber nitrogen Nitrogen organik Amonium fosfat
Keasaman (pH) 4 – 5 5,0 – 5,5
Suhu 28 – 32OC 28OC
Asam cuka glacial 2 – 4% -
Starter 10 – 20% -
Lama inkubasi 15 hari 15 hari
Menurut Moat dan Foster (1988), pembentukan selulosa oleh A. xylinum
memerlukan gula sebagai unsur utama, protein dan lemak sebagai senyawa
perantara, serta mineral sebagai penstimulasi dalam pembentukan selulosa.
Nata tergolong sebagai sumber makanan rendah energi untuk keperluan diet
karena nilai gizi produk ini sangat rendah. Selain itu nata juga mengandung serat
yang sangat dibutuhkan oleh tubuh dalam proses fisiologis sehingga dapat
memperlancar pencernaan. Nata mengandung kalori yang rendah sehingga aman
7 Badan Standarisasi Nasional 01-4317-1996 menetapkan kriteria-kriteria mutu
yang harus dipenuhi dalam produksi nata dalam kemasan sebagaimana disajikan
pada Tabel 4.
Tabel 4. Standar Mutu Produk Nata dalam Kemasan
No Komponen Satuan Persyaratan
1 Keadaan
- Bau - Normal
- Rasa - Normal
- Warna - Normal
2 Bobot tuntas % Min.50
3 Jumlah gula (dihitung sebagai sukrosa) % Min. 15
4 Serat makanan % Maks. 4,5
5 Pewarna tambahan Sesuai SNI 01-0222-1995
6 Pengawet Sesuai SNI 01-0222-1995
Sumber : SNI 01-4317-1996
Nata dipercaya dapat mencegah tubuh dari serangan kanker kolon karena erat
kaitannya dengan sifat kimianya yaitu makanan berserat tinggi dan rendah kalori
serta ampuh melangsingakan tubuh. Konsumsi serat yang teratur dan seimbang
setiap hari di kolon akan difermentasi oleh bakteri kolon yang baik menjadi asam
lemak rantai pendek yang berfungsi sebagai anti kanker, asam lemak ini akan
mengikat asam empedu yang bersifat karsiogenik dan selanjutnya asam ini akan
dibuang bersamaan dengan feses (Metcalfe, 1994).
Panen nata dilakukan setelah 14 hari fermentasi. Hasbullah (2001)
menyatakan bahwa nata akan mengalami kerusakan oleh mikroba pencemar jika
fermentasi tetap dilanjutkan setelah batas akhir waktu optimum pertumbuhan nata.
Bahan Pembuatan Nata Media
Madu afkir. Madu afkir adalah madu yang telah menurun kualitasnya baik dari segi fisik dan kimia. Penurunan kualitas madu disebabkan adanya rekasi
biokimia oleh mikroorganisme pada madu seperti Zygosaccharomyces dan
penyimpanan madu yang sangat lama dengan kondisi suhu penyimpanan yang tidak
8 meningkat (Damanhuri, 2005). Winarno (1982) menyatakan bahwa kadar HMF
dapat menjadi indikator kerusakan madu oleh pemanasan yang berlebihan atau
karena pemalsuan dengan gula invert. Semakin lama penyimpanan madu semakin
tinggi kadar HMF madu tetapi kenaikan kadar HMF tergantung pada suhu
penyimpanan.
Air Kelapa. Air kelapa adalah bagian dari buah kelapa yang dihasilkan dari endosperma cair. Air kelapa yag berupa cairan jernih mengisi kurang lebih tiga per
empat bagian rongga sebelah dalam buah kelapa (Freemond dan Ziller, 1996).
Jumlah air kelapa yang terkandung di dalam satu buah kelapa tua sekitar 300 ml
yang dipengaruhi oleh ukuran kelapa, varietas, kematangan dan kesegaran kelapa
(Tenda, 1992).
Air kelapa matang mempunyai nilai pH 4,88 ± 0,05 dengan Aw 0,995 ±
0,003 (Walter et al., 2009). Nilai pH akan menurun selama penyimpanan.
Berdasarkan penelitian Mashudi (1993), penundaan penggunaan air kelapa
berpengaruh terhadap mutu nata de coco yang dihasilkan. Penundaan pemakaian air
kelapa lebih dari sembilan hari sudah tidak dapat menghasilkan nata sedangkan bila
kurang dari sembilan hari masih memungkinkan menghasilkan nata tetapi sudah
berkurang kualitasnya dibandingkan air kelapa segar. Hal ini diduga karena air yang
telah ditunda terlalu lama komposisinya sudah banyak berkurang akibat telah
mengalami fermentasi yang mengkontaminasi air kelapa. Selain itu air kelapa yang
penggunaannya ditunda lama, pHnya akan semakin turun sehingga berada diluar
selang yang memungkinkan A. xylinum untuk dapat hidup.
Whey. Whey merupakan produk samping pembuatan keju yang masih
mengandung komponen nutrisi berupa protein, laktosa dan mineral (Scott, 1986).
Whey memiliki warna kuning kehijauan yang berasal dari riboflavin yakni pigmen
yang larut dalam air yang terdapat dalam susu. Komposisi utama whey berupa
laktosa (4-7%) dan protein (0,6-1,0%). Komposisi lainnya seperti, -laktalbumin, β
-laktoglobulin dan mineral (Marshall, 2004).
Media pembuatan nata tidak hanya dari air kelapa, whey sebagai hasil ikutan
pengolahan keju juga dapat menghasilkan nata apabila difermentasikan dengan A.
9 dengan starter A. xylinum dapat menghasilkan nata de whey. Perbandingan
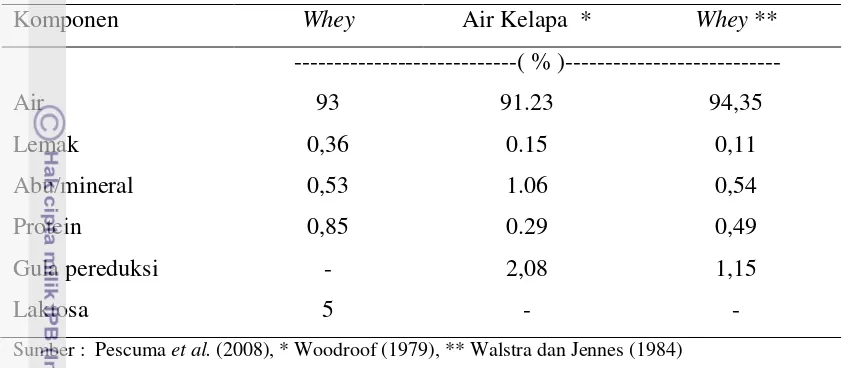
komposisi antara whey dan air kelapa dapat dilihat pada Tabel 5.
Tabel 5. Komposisi Whey dan Air Kelapa
Komponen Whey Air Kelapa * Whey **
---( % )---
Air 93 91.23 94,35
Lemak 0,36 0.15 0,11
Abu/mineral 0,53 1.06 0,54
Protein 0,85 0.29 0,49
Gula pereduksi - 2,08 1,15
Laktosa 5 - -
Sumber : Pescuma et al. (2008), * Woodroof (1979), ** Walstra dan Jennes (1984)
Whey dapat digolongkan menjadi beberapa jenis asam atau enzim yang
digunakan dalam pembuatan keju. Whey manis diperoleh dari metode koagulasi
yang menggunakan enzim sedangkan whey asam diperoleh dari metode koagulasi
yang menggunakan asam
Starter Nata (Acetobacter xylinum)
Starter merupakan syarat terpenting pada proses fermentasi. Demikian pula
dengan pembuatan nata de madoe, penggunaan starter merupakan syarat mutlak.
Starter adalah kultur mikroba yang diinokulasikan ke dalam medium fermentasi
dengan kriteria sehat dan aktif, sifat yang sesuai, digunakan dalam jumlah rendah
dibandingkan jumlah medium fermentasi dan bebas kontaminasi. Pembuatan nata de
madoe menggunakan starter A. xylinum.
Bakteri A. xylinum termasuk golongan acetobacter yang mempunyai ciri-ciri
antara lain Gram negatif, berbentuk batang pada media asam, berbentuk kapsul pada
media basa, panjang 2-10µm, lebar 0,5-1,0µm, obligat aerobik, nonmotil.
Acetobacter xylinum tidak berspora, membentuk asam dari glukosa, mampu
mengoksidasi asam asetat, dapat membentuk rantai ataupun tunggal, membentuk
lendir yang menyelubungi sel dan tumbuh pada permukaan medium (Lapuz et al.,
1967). Acetobacter xylinum tidak mampu mencairkan gelatin, tidak memproduksi
10 suhu kematian (thermal death point) (Dewan Ilmu Pengetahuan, Teknologi dan
Industri Sumatera Barat, 2002).
Acetobacter xylinium memiliki ciri-ciri yang hampir sama dengan spesies
lain, seperti: A. aceti, A. orleanensis dan A. liquefaciens. Acetobacter xylinum
memiliki kelebihan dari spesies acetobacter lainnya yaitu jika ditumbuhkan pada
media yang mengandung gula maka bakteri ini akan memecah gula untuk mensintesa
suatu polisakarida yang dikenal dengan selulosa ekstraseluler (Brown, 1996).
Thimann (1964) menyatakan bahwa A. xylinum jika ditumbuhkan pada
media yang mengandung gula, dapat mengubah sampai 19% gula menjadi selulosa.
A. xylinum mampu mensintesis selulosa dari gula yang tersedia dalam media dan
dapat membentuk suatu lapisan yang mengambang di permukaan substrat.
Acetobacter xylinum dapat membentuk suatu lapisan yang mencapai beberapa
sentimeter pada permukaan substrat cair tempat hidupnya, bakteri itu sendiri
terperangkap di dalam massa fibril yang dibuatnya.
Selulosa yang dihasilkan A. xylinum berbeda dengan selulosa yang dihasilkan
tumbuhan. Selulosa dari A. xylinum merupakan selulosa murni tanpa ada campuran
hemiselulosa, pektin dan lignin (Backdahl et al., 2006). Selulosa pada tumbuhan
merupakan sintesis selulosa dengan glukosa-diphospat sedangkan selulosa yang
dibentuk oleh A. xylinum merupakan sintesis selulosa dengan urasil diphospat.
Pembentukan selulosa oleh A. xylinum memerlukan gula sebagai unsur
utama, protein dan lemak sebagai senyawa perantara, serta mineral sebagai
penstimulasi dalam pembentukan selulosa (Moat dan Foster, 1988). Keshk dan
Someshima (2006) menyatakan selulosa yang dihasilkan oleh A. xylinum mempunyai
kapasitas penyerapan air yang tinggi.
Selulosa yang dihasilkan A. xylinum dibentuk dari glukosa menjadi glukosa
6-fosfat (Glu6P) dengan bantuan enzim glukokinase, Glu6P diubah menjadi
glukosa-1-phospat (Glu1P) dengan enzim fosfoglukomutase, selanjutnya dengan
bantuan enzim uridil transferas diubah menjadi uridin-5 diphospat glukosa
(UDP-5Glu) sehingga terbentuklah selulosa dengan bantuan enzim sintetase selulosa dalam
11 Mekanisme pembentukan selulosa yang dihasilkan A. xylinum dapat dilihat
pada Gambar 1.
Glukosa ATP
Glu-6P ADP
(fosfoglukomutase)
Glu-1P UTP
UDP-5Glu P
Senyawa perantara (rantai lipid dan rantai protein)
Selulosa
(β-1, 4-D-Glu)n
Gambar 1. Mekanisme Pembentukan Selulosa oleh Acetobacter xylinum (Moat dan Foster, 1998)
Kondisi optimum untuk memproduksi nata pada media air kelapa
membutuhkan starter A. xylinum sebanyak 10-20% (Alaban, 1961). Isti (2005)
menyatakan bahwa kondisi optimum untuk memproduksi nata rumput laut.
membutuhkan starter A. xylinum sebanyak 10%.
Nilai pH medium pertumbuhan A. xylinum merupakan salah satu faktor
penting yang mempengaruhi pertumbuhan dan pembentukan produk. Nilai pH
optimum untuk pertumbuhan A. xylinum adalah 5,4-6,3 (Pambayun, 2006). Hasil
penelitian Embuscado et al. (1994) menemukan bahwa hasil selulosa tertinggi
diperoleh pada pH 4,5 sedangkan menurut Masaoka et al. (1993) pH optimum untuk
produksi selulosa adalah 4,0-6,0.
Jumlah populasi starter A. xylinum juga menetukan kualitas nata yang
dihasilkan. Jumlah bakteri yang dibutuhkan dalam pembuatan produk fermentasi
yaitu 1,0 x 108 cfu/ml (Makinen dan Bigret, 1998). Saxenaa (2001) menyatakan
bahwa starter dengan jumlah koloni 5,5 x 105 cfu/ml telah cukup untuk
menumbuhkan nata dengan ketebalan 0,8 cm.
Pertumbuhan A. xylinum diawali dengan timbulnya kekeruhan setelah
fermentasi 24 jam pada suhu kamar. Di permukaan medium akan terbentuk suatu
12 bertahap dan lapisannya akan lebih kompak. Apabila lapisan diganggu dengan
guncangan maka lapisan akan terlepas dari dinding wadah fermentasi dan akan
tenggelam, kemudian akan terbentuk lapisan baru pada permukaan media.
Amonium Sulfat
Amonium sulfat merupakan pupuk buatan berbentuk kristal dengan rumus
kimia (NH4)2SO4 yang mengandung unsur hara nitrogen dan belerang, yang juga
disebut sebagai pupuk Zwavelzuur Ammoniak (ZA). Indrarti dan Rahmi (2008)
menyatakan bahwa amonium sulfat adalah sumber nutrisi yang diperlukan bakteri
dalam proses fermentasi untuk membentuk selulosa.
Amonium sulfat bersifat tidak higroskopis dan baru akan menyerap air bila
kelembapan nisbi mencapai 80% pada suhu 30 °C. Amonium sulfat sangat
membantu pertumbuhan A. xylinum pada proses pembuatan nata. Kandungan
nitrogen dalam SNI 02-1760.2005 minimal 20,8%. Kandungan Nitrogen yang tinggi
dapat dimanfaatkan A. xylinum untuk bertahan hidup dan mampu merombak gula
menjadi selulosa lebih banyak. Menurut Wijaningsih (1999), ammonium sulfat
sebagai sumber nitrogen akan dipecah menjadi komponen yang lebih sederhana dan
melalui transformasi aktif komponen ini akan masuk ke dalam sel untuk selanjutnya
digunakan sebagai bahan dasar untuk biosintesis protein, sehinggga pertumbuhan
dan perkembangan A. xylinum dapat dipercepat.
Penambahan amonium sulfat juga meningkatkan jumlah polisakarida yang
terbentuk, merangsang aktivitas bakteri dalam mensintesis bioselulosa (selulosa yang
dihasilkan dari bakteri), meningkatkan rendemen bioselulosa serta meningkatkan
kekuatan tarik dan modulus elastisitas bioselulosa. Semakin meningkatnya kerapatan
dari serat-serat selulosa dapat meningkatkan interaksi fibril selulosa yang terbentuk
sehingga menghasilkan ikatan hidrogen intra dan interfibrilar yang kuat dan akan
memberikan peningkatan sifat mekaniknya. Penambahan ammonium sulfat ini harus
terkontrol karena apabila penggunaan amonium sulfat yang berlebihan akan
menurunkan pH secara drastis sehingga menyebabkan kondisi fermentasi menjadi
terlalu asam dan rendemen nata yang dihasilkan juga menurun (Rosario, 1978).
Berbagai penelitian menyatakan bahwa persentase kadar penambahan
amonium sulfat sebesar 0,5%. Berdasarkan hasil penelitian Setiani (2007)
13 gracilaria sp (nata rumput laut) tertinggi, dengan rendemen 43,80% dan ketebalan
1,97cm. Indrarti dan Rahmi (2008) juga menyatakan dalam penelitiannya
menggunakan amonium sulfat 0,5% untuk pertumbuhan dan sifat mekanik
bioselulosa dengan medium kulit pisang, ketebalan bioselulosa yang diperoleh
sebesar 2,2 cm dan rendemen bioselulosa sebesar 57,15%. Ketebalan nata tertinggi
dihasilkan oleh nata dengan penambahan ammonium sulfat 0,45%-0,5% (Jaganath et
al., 2008).
Nata dengan amonium sulfat sebagai sumber nitrogen sebenarnya tidak
terlalu membahayakan karena ketika sudah menjadi nata, amonium sulfat tidak lagi
berbentuk amonium sulfat. Unsur nitrogen yang terdapat pada amonium sulfat telah
difermentasi oleh A. xylinum (Kholifa, 2010).
Serat Makanan
Serat kasar berbeda dengan serat makanan. Serat kasar adalah komponen
sisa hasil hidrolisis suatu bahan pangan dengan asam kuat selanjutnya dihidrolisis
dengan basa kuat sehingga terjadi kehilangan selulosa sekitar 50% dan hemiselulosa
85%. Sementara itu serat makanan adalah bahan makanan yang meliputi semua jenis
polisakarida dan lignin serta beberapa jenis oligosakarida yang tahan terhadap yang
enzim pencernaan manusia dan mampu mempengaruhi satu atau lebih fungsi tubuh
sehingga dapat memberikan manfaat bagi kesehatan (Diplock et al., 1999).
Polisakarida terdiri atas polisakarida yang dapat dicerna dan tidak dapat
dicerna. Polisakarida yang dapat dicerna biasanya terdapat pada pati dan beberapa
jenis glikogen dalam daging. Polisakarida yang tidak dapat dicerna pada umumnya
berupa pembentuk tekstur dalam bahan pangan, khususnya pangan nabati (Winarno,
2008). Beberapa contoh polisakarida yang tidak dapat dicerna antara lain selulosa,
hemiselulosa dan inulin.
Selulosa merupakan polimer rantai lurus dari glukosa dengan ikatan β (1-4) yang tidak dapat terhidrolisis oleh enzim amilase. Meskipun selulosa bersifat
resistan terhadap pencernaan manusi, bakteri yang terdapat pada usus besar mampu
memetabolisme serat dan menghasilkan asam lemak rantai pendek (asam asetat,
14 Gambar 2. Ikatan β (1-4) antar Unit Glukosa pada Selulosa (Jalili et al., 2001)
Serat makanan tidak dapat dicerna oleh enzim manusia, tetapi sebagian
komponen serat larut air dapat difermentasi oleh bakteri usus menghasilkan produk
yang dapat diserap dan dimetabolis menjadi energi (Bender, 2003). Serat makanan
tidak tercerna dapat memperbesar volume feses dan menimbulkan efek laksatif serta
mempercepat pembuangan feses sehingga mengurangi resiko pembentukan kanker
kolon.
Sistem Notasi Warna
Sistem notasi warna adalah suatu cara sistematik dan objektif untuk
menyatakan atau mendeskripsikan suatu jenis warna. Sistem notasi warna ini
dinyatakan dalam notasi (simbol) huruf atau angka. Banyak sistem notasi warna
yang telah dikembangkan diantaranya, yaitu sistem notasi International Commision
on Illumination (I.C.I), sistem notasi Munsel dan sistem notasi Hunter (Andarwulan,
2011).
Sistem notasi I.C.I didasarkan pada prinsip bahwa semua jenis warna dapat
dibentuk dari tiga warna dasar, yaitu merah (λ = 720 nm), hijau (λ = 520 nm) dan biru (λ = 380 nm). Sistem notasi Munsel pengukuran warna didasarkan pada pengamatan warna secara subjektif, dimana notasi warna didasarkan pada tiga atribut
subjektif warna, yaitu warna kromatik (hue), kecerahan (value) dan intensitas warna
(chroma atau saturation). Warna kromatik meliputi warna monokromatik yang terdiri
dari warna pelangi dan warna campurannya, seperti warna ungu-merah, ungu-biru,
hijau mudah, biru muda dan lain-lain. Kecerahan (value) menyatakan warna
akromatik yang berkisar dari warna hitam pekat sampai putih bersih. Nilai intensitas
warna (chroma) berkisar dari nilai tidak berwarna sampai warna penuh (Andarwulan,
15 Sistem notasi Hunter dikembangkan oleh Hunter pada tahun 1952. Sistem
notasi warna Hunter dicirikan dengan tiga parameter warna, yaitu warna kromatik
(hue) yang ditulis dengan notasi a, intensitas warna dengan notasi b dan kecerahan
dengan notasi L. Notasi L menyatakan parameter kecerahan (lightness) dari hitam (0)
sampai putih (100). Nilai L menyatakan cahaya pantul yang menghasilkan warna
akromatik puith, abu-abu dan hitam (Andarwulan, 2011). Notasi a menyatakan warna
kromatik campuran merah-hijau dengan nilai +a (positif) dari 0 sampai +100 untuk
warna merah, nilai –a (negatif) dari 0 sampai -80 untuk warna hijau. Notasi b
menyatakan warna warna kromatik campuran biru-kuning dengan nilai +b (positif)
dari 0 dampai +70 untuk warna kuning dan nilai –b (negatif) dari 0 sampai -80 untuk
warna biru. Berdasarkan nilai a dan b dapat dihitung derajat Hue dengan rumus
sebagai berikut :
°Hue = tan -1
Kategori Warna Menurut Kisaran Nilai °Hue dapat dilihat pada Tabel 6.
Tabel 6. Kategori Warna Menurut Kisaran Nilai °Hue
Warna Kisaran nilai °Hue
Merah-ungu 342 – 18
Merah 18 – 54
Kuning – merah 54 – 90
Kuning 90 – 126
Kuning – hijau 126 – 162
Hijau 162 – 198
Hijau – biru 198 – 234
Biru 234 – 270
Biru – ungu 270 – 306
Ungu 306 – 342
Sumber : Hutching (1999)
Pengukuran warna dengan sistem notasi warna Hunter dilakukan secara
objektif menggunakan kolorimeter fotoelektrik yang disebut dengan kolorimeter
Hunter. Pengukuran warna dengan sistem ini mempunyai beberapa keuntungan,
16 mudah, notasinya dapat diterjemahkan atau dikonversikan dengan sistem notasi lain,
seperti I.C.I dan alat pengukur warna relatif sederhana sehingga harganya relatif
rendah.
Penilaian Sensori
Cara penilaian suatu bahan pangan dibagi menjadi dua cara yaitu secara
objektif dan subjektif. Pengujian objektif merupakan suatu pengujian menggunakan
alat atau instrument dan faktor manusia dapat diabaikan, sehingga pengukurannya
lebih objektif. Pengujian secara subjektif (uji organoleptik) adalah pengujian dengan
bantuan panca indera manusia untuk menilai karakteristik mutu yang bertujuan
mengetahui sifat-sifat cita rasa makanan serta daya terima terhadap masyarakat.
Pengujian secara subjektif dapat dilakukan dengan menggunakan uji hedonik
(kesukaan) dan uji mutu hedonik (Damayanthi dan Mudjajanto, 1998).
Warna. Warna faktor utama yang sangat menentukan penilaian bahan pangan sebelum faktor-faktor lain dipertimbangkan secara visual. Penerimaan warna
suatu bahan berbeda-beda tergantung dari faktor alam, geografis dan aspek sosial
masyarakat penerima. Warna dapat digunakan sebagai indikator kesegaran atau
kematangan (Winarno, 2008). Warna dapat berasal dari pigmen alami bahan pangan
itu sendiri, reaksi Maillard, reaksi karamelisasi, reaksi senyawa organik dengan udara
dan penambahan zat warna, baik alami maupun sintetik.
Rasa. Tekstur dan konsistensi suatu bahan pangan akan mempengaruhi cita rasa yang timbul. Perubahan tekstur dan konsistensi bahan dapat mengubah rasa dan
bau yang timbul karena dapat mempengaruhi kecepatan timbulnya rangsangan
terhadap olfaktori dan kelenjar air liur. Gerakan lidah akan mempercepat timbulnya
respon terhadap rasa. Rasa dipengaruhi oleh beberapa faktor, yaitu senyawa kimia,
suhu, konsentrasi dan interakasi dengan komponen rasa lain (Winarno, 2008).
Aroma. Indera pembau berfungsi untuk menilai aroma suatu produk atau komoditi baik berupa pangan maupun nonpangan. Kepekaan pembauan lebih tinggi
dari pencicipan. Aroma atau bau dapat dikenali apabila berbetuk uap dan
molekul-molekul baunya menyentuh silia sel olfaktori dan diteruskan ke otak dalam bentuk
impuls listrik oleh ujung-ujung syaraf olfaktori sehingga bau dapat dideteksi
17
MATERI DAN METODE
Lokasi dan Waktu
Penelitian ini dilaksanakan dari bulan Januari sampai dengan Juni 2012, di
Laboratorium Teknologi Hasil Ternak, Fakultas Peternakan Institut Pertanian Bogor,
Laboratorium Research, Fakultas Peternakan Institut Pertanian Bogor. Analisis
proksimat dilaksanakan di Laboratorium Ilmu dan Teknologi Pakan Fakultas
Peternakan Institut Pertanian Bogor dan analisis serat makanan dilaksanakan di Balai
Besar Industri Agro.
Materi
Bahan yang digunakan untuk pembuatan nata de madoe adalah madu hutan
afkir, madu segar, whey, air kelapa, starter A. xylinum diperoleh dari pabrik nata de
coco Ciampea, amonium sulfat, akuades, H2SO4, NaOH, HCl, MRSA, NaCl
NaHSO3, Zn(CH3COO)).2H2O dan K4Fe(CN)6.3H2O
Peralatan yang digunakan dibagi atas dua bagian, yaitu: peralatan dalam
proses pengolahan (loyang plastik segi empat, kain saring, aluminium foil, plastik
wrap, gelas ukur, laminar air flow, stirrer, mikropipet, timbangan, hotplate,
pengaduk, termometer dan panci) dan peralatan untuk pengujian analisis (pH meter,
hand refractometer, gelas ukur, jangka sorong, penetrometer, chromameter, tabung
reaksi, cawan porselin, cawan aluminium, labu Kjedhal, labu Erlemeyer, vortex dan
spektrofotometer ). Peralatan untuk uji organoleptik adalah form uji hedonik, gelas
dan sendok.
Prosedur
Penelitian Pendahuluan
Penelitian pendahuluan dilakukan untuk mengetahui sifat kimia dari madu
afkir, memeriksa kemurnian dan viabilitas starter A. xylinum dan menentukan
konsentrasi gula yang tepat dengan cara pengenceran sebagai media untuk
pembuatan nata de madoe. Hasil terbaik dari penelitian pendahuluan ini akan
digunakan dalam penelitian lanjutan. Sifat kimia madu hutan afkir yaitu kadar gula,
18
Sifat Kimia Madu Hutan Afkir
Kadar gula madu afkir (Badan standardisasi nasional, 2006). Kadar gula madu afkir diukur dengan menggunakan hand refractometer. Air diteteskan satu
tetes di atas prisma refraktometer untuk menentukan titik nol atau digunakan sebagai
koreksi. Madu hutan afkir diteteskan di permukaan prisma hand refraktrometer.
Jangan sampai terbentuk gelembung. Prisma ditutup kemudian hasilnya dilihat di
hand refractrometer.
Nilai pH (Badan standardisasi nasional, 1992). Sampel madu hutan afkir sebanyak 10 ml disiapkan dalam wadah. pH meter dikalibrasi dengan larutan buffer
pH 4 dan 7. Elektroda dibilas dengan akuades dan dilap dengan tisu, selanjutnya
dicelupkan ke dalam sampel madu hutan afkir. Nilai pH ditentukan setelah pH meter
menunjukkan angka yang stabil.
Kadar air (Association of official analytical chemist, 1999). Kadar air merupakan jumlah air yang terkandung di dalam satu satuan nata de madoe yang
dinyatakan dalam persen. Analisis kadar air pada prinsipnya menguapkan air yang
terkandung dalam bahan dengan cara pengeringan oven pada suhu 105 °C sampai
diperoleh berat yang tetap. Prosedur kerja analisis kadar air sebagai berikut: cawan
aluminium dikeringkan dengan oven pada suhu 105 °C selama satu jam. Cawan
didinginkan di desikator dan ditimbang. Nata de madoe dihancurkan dan diambil
sampel lima gram dan ditempatkan pada cawan. Cawan yang berisi sampel nata
dimasukkan ke oven bersuhu 105 OC selama tiga jam. Cawan didinginkan di
desikator lalu ditimbang. Kadar air dihitung dengan rumus :
Kadar air = x 100%
Keterangan :
a = berat sampel (g)
b = berat sampel kering + cawan (g)
19
Kadar Abu (Association of official analytical chemist, 1999). Kadar abu merupakan jumlah residu anorganik yang terkandung dalam satu satuan berat nata.
Kadar abu nata de madoe diperoleh dengan cara sebagai berikut: cawan porselen
dibakar dalam tanur kemudian didinginkan dalam deksikator dan ditimbang. Nata
dihaluskan kemudian ditimbang tiga gram dan diletakkan dalam cawan porselen
tersebut. Cawan dibakar di kasa pembakar Bunsen sampai tidak berasap lagi,
kemudian dimasukkan ke dalam tanur dengan suhu 550 oC. Pengabuan dilakukan
sampai berat cawan konstan selama ± 12 jam. Cawan didinginkan di desikator
selama 30 menit lalu ditimbang. Kadar abu dapat dihitung dengan rumus:
Kadar abu = x 100%
Keterangan :
W = bobot contoh sebelum diabukan (g)
W1 = bobot contoh + cawan sesudah diabukan (g)
W2 = bobot cawan (g)
Kadar Hidroksimetilfurfural (Badan standardisasi nasional, 2004). Kadar Hidroksimetil-furfural (HMF) diukur dengan alat spektrofotometer dengan panjang
gelombang 284 nm dan 336 nm. Tahap pertama, larutan Carez I (15 g ferosianida
K4Fe(CN)6.3H2O dilarutkan dengan akuades dan diencerkan sampai 100 ml) dan
laruran Carez II (30g seng asetat Zn(CH3COO)).2H2O dilarutkan dengan akuades
dan diencerkan sampai 100 ml) dipersiapkan.
Sebanyak lima gram sampel madu ditimbang dalam labu ukur 50 ml,
kemudian ditambahkan akuades sampai larutan dalam labu ukur mencapai kurang
lebih 25 ml. Sebanyak 0,5 ml Larutan Carez I ditambahkan ke dalam labu ukur
kemudian diaduk. Tahap selanjutnya larutan Carez II ditambahkan ke dalam labu
ukur kemudian diaduk kembali. Volume campuran ditepatkan hingga tanda tera
dengan akuades, kemudian disaring dengan kertas saring abu.
Filtrat hasil penyaringan dipipet lima ml ke dalam dua tabung reaksi
berukuran 18 x 150 ml. Tabung pertama ditambahkan lima ml akuades, sedangkan
tabung kedua (pembanding) ditambahkan lima ml NaHSO3 0,2%. Campuran diaduk
rata dengan menggunakan vortex. Tahap berikutnya sampel diukur absorbannya
dengan menggunakan spektrofotometer pada panjang gelombang 284 nm dan 336
20 diencerkan dengan akuades dan larutan standar NaHSO3 0,1%. Perhitungan kadar
HMF dirumuskan sebagai berikut :
Kadar HMF = (A284 –A336) x 14,97 x 5 / berat sampel
Keterangan :
A284 = absorbansi pada 284 nm
A336 = absorbansi pada 336 nm
14,97 = faktor koreksi
Kemurnian dan Viabilitas Starter Acetobacter xylinum (modifikasi Agustrianingsih, 2007)
Pemeriksaan kemurnian dilakukan melalui pemeriksaan mikroskopis dengan
bantuan pewarnaan Gram untuk pengamatan morfologi starter yang digunakan.
Pemeriksaan kemurnian starter bertujuan untuk menghindari kontaminasi yang
berasal dari lingkungan. Pemeriksaan kemurnian starter A. xylinum, terlebih dahulu
ditumbuhkan pada media de-Man Rogosa Sharp Agar (MRSA) kemudian diinkubasi
pada suhu 37 °C selama 24-48 jam (Gambar 3). Object glass terlebih dahulu
difiksasi di atas Bunsen, kemudian isolat A. xylinum diambil dari media MRSA
dengan menggunakan ose steril diletakkan pada Object glass lalu dihomogenkan
dengan akuades satu tetes, selanjutnya difiksasi di atas api atau di udara sampai
kering. Zat warna pertama yang diberikan adalalah Gentiant violet yang ditambah
dengan zat warna Lugol masing-masing selama satu menit lalu dicuci dengan air
mengalir. Setelah itu diberikan Aseton alkohol selama 20 detik dan segera dicuci
dengan air mengalir. Zat warna terakhir yakni Safranin yang diberikan selama satu
menit, kemudian dicuci dengan air mengalir dan dikeringkan di udara. Selanjutnya di
amati di bawah mikroskop dengan perbesaran 1000 kali dan menggunakan minyak
emersi.
21 Pemeriksaan viabilitas starter dilakukan dengan cara menghitung jumlah
populasi starter kerja yang akan digunakan dalam penelitian dengan metode spread
plate. Pengenceran tujuh kali dilakukan untuk setiap satu ml sampel starter A.
xylinum. Perhitungan cawan dimulai dari pengenceran ke tiga sampai pengenceran
ke tujuh. Satu ml dari setiap pengenceran dipipet dan dituangkan ke cawan petri yang
telah disterilkan secara duplo. Lima belas ml MRSA dituangkan ke cawan petri,
dihomogenkan dengan gerakan angka delapan dan dibiarkan selama 15 menit sampai
media mengeras. Cawan petri kemudian dibalikkan dan diinkubasi pada suhu 37 °C
selama 24-48 jam. Populasi starter harus memenuhi syarat minimal jumlah bakteri
dalam pembuatan produk fermentasi, yaitu 1,0 x 108 cfu/ml (Makinen dan Bigret,
1998).
Pengenceran Madu Afkir (Chemistry, 2011)
Pengenceran dilakukan untuk memperoleh kadar gula terbaik yang mendukung
pertumbuhan Acetobacter xylinum. Perhitungan pengenceran kadar gula total 15%,
20% dan 25% diperoleh dengan rumus:
V1 x M1 = V2 x M2
Keterangan :
V1 = volume madu afkir (ml)
M1 = kadar gula yang diketahui (72%)
V2 = volume pengencer (100ml)
M2 = kadar gula (15%, 20%, 25%)
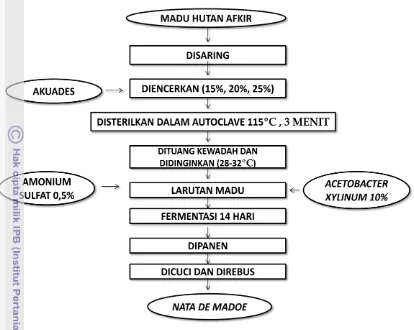
Pembuatan nata de madoe dilakukan sesuai Gambar 4. Proses pembuatan nata
de madoe pada penelitian pendahuluan ini diawali dengan penyaringan madu hutan
afkir. Madu diencerkan dengan akuades hingga kadar gula sebesar 15%, 20% dan
25% kemudian diautoclave pada suhu 115 °C selama tiga menit. Madu yang telah
disterilkan dituang ke wadah fermentasi yang juga telah disterilkan dan didinginkan
pada suhu berkisar 28-32 °C. Starter A. xylinum diinokulasi sebanyak 10% dan
ditambahkan amonium sulfat 0,5%. Larutan madu hutan afkir difermentasi selama
14 hari kemudian nata de madoe dipanen dan dihitung persentase rendemennya
dengan cara berikut:
Rendemen =
22 Gambar 4. Proses Pembuatan Nata de Madoe pada Penelitian Pendahuluan
Hasil nata terbaik diperoleh dari nilai rendemen tertingi. Hasil rendemen nata
yang terbaik dari ketiga pengenceran digunakan sebagai bahan untuk penelitian
lanjutan.
Penelitian Utama
Pembuatan nata de madoe menggunakan pengenceran yang terbaik dari
penelitian pendahuluan. Proses pembuatan nata de madoe pada penelitian utama
hampir sama dengan penelitian pendahuluan. Namun media fermentasi yang
digunakan berbeda, yaitu: madu hutan afkir, madu hutan afkir ditambah whey, madu
hutan afkir ditambah air kelapa, madu hutan afkir ditambah whey dan air kelapa dan
madu segar sebagai kontrol.
Ratio perbandingan media fermentasi diperoleh dari hasil try and error
sebelum penelitian lanjutan ini, yakni: madu hutan afkir ditambah whey (2:1) v/v ,
madu afkir ditambah air kelapa (2:1) v/v dan madu hutan afkir ditambah whey dan
23 Gambar 5. Bagan Penelitian
Nata yang dipanen kemudian dicuci dengan air tiga kali kemudian di rebus
selama 30 menit dan didiamkan satu malam kemudian dicuci kembali dan direbus
selama 15 menit tanpa menggunakan penutup agar aroma asam dari nata terlepas ke
udara bebas. Nata de madoe yang dihasilkan diuji sifat fisik, sifat kimia dan tingkat
kesukaannya. Nata de madoe yang diuji tingkat kesukaanya terlebih dahulu
direndam pada larutan madu berkadar gula 15% dan 20% sehingga nata yang diuji
tidak terasa hambar.
Rancangan dan Analisis Data
Rancangan percobaan yang digunakan adalah rancangan acak lengkap
(RAL) dengan tiga kali pengulangan. Perlakuan yang diberikan adalah media
fermentasi yang berbeda yaitu madu hutan afkir, madu hutan afkir ditambah whey,
madu hutan afkir ditambah air kelapa dan madu hutan afkir ditambah whey dan air
kelapa terhadap rendemen nata de madoe. Media fermentasi madu segar dijadikan
24 Model matematikanya menurut Steel dan Torrie (1995) adalah sebagai
berikut:
Yij= µ + αi+ εij
Keterangan :
Yij = Nilai Pengamatan rendemen nata de madoe dengan media fermentasi ke-i pada ulangan ke-j
µ = Nilai rataan dari rendemen nata de madoe
αi = Pengaruh media fermentasi pada taraf ke-i
εij = Pengaruh galat percobaan dengan media fermentasi pada taraf ke-i dan
ulangan ke-j. i = 1, 2, 3, 4 j = 1, 2, 3
Data sifat fisik dianalisis dengan analisis keragaman dan perlakuan yang
berpengaruh nyata dilanjutkan dengan uji Tukey untuk melihat perbedaan di antara
perlakuan.
Analisis nonparametrik dilakukan terhadap hasil uji sensori dengan
menggunakan adalah Kruskal Wallis (Steel dan Torrie, 1995).
H =
Ri = jumlah rangking dalam perlakuan ke-i T = jumlah pengamatan seri dalam ulangan H = statistik Kruskal-Wallis
H’ = H terkoreksi
Apabila hasil analisis Kruskal Wallis berpengaruh nyata dilakukan uji
perbandingan (Multiple Comparison) untuk melihat perbedaan di antara perlakuan,
yaitu dengan rumus (Steel dan Torrie, 1995) :
Ri – Rj > < Z /2p
Keterangan :
Ri = Rata-rata nilai rangking perlakuan ke-i Rj = Rata-rata nilai rangking perlakuan ke-j k = jumlah perlakuan
25
Peubah yang Diamati
Peubah yang diamati meliputi : (a) karakteristik fisik yaitu rendemen,
ketebalan, kekenyalan dan warna, (b) karakteristik kimia meliputi kadar air, kadar
abu, serat kasar, protein kasar, lemak kasar, dan serat pangan, (c) tingkat kesukaan.
Karakteristik Fisik
Rendemen (Association of official analytical chemist, 1999). Rendemen nata adalah berat nata yang dihasilkan dari tiap satuan volume media fermentasi yang
digunakan, dinyatakan dalam persen. Rendemen nata ditentukan dengan metode
gravimetri dan dinyatakan dalam berat per volume (w/v). Rendemen nata dihitung
dengan rumus:
Rendemen =
x 100%
Ketebalan ( Modifikasi dari Yoneda, 2003). Ketebalan adalah rataan tebal nata yang diperoleh dari hasil perubahan glukosa menjadi selulosa oleh A. xylinum.
Ketebalan nata diukur pada lima tempat yang berbeda yaitu pada masing-masing
ujung segiempat dan bagian tengahnya.dengan menggunakan jangka sorong digital
ditusukkan pada permukaan hingga mencapai dasar nata. Angka yang ditunjukkan
oleh jangka sorong menunjukkan tebal nata. Ketebalan dihitung dengan rumus
sebagai beikut :
Ketebalan =
Keterangan : t (1-5) = tebal
Kekenyalan ( Modifikasi dari Yoneda, 2003). Kekenyalan adalah daya tahan nata untuk pecah akibat gaya tekan. Kekenyalan nata diukur dengan menggunakan
Penetrometer (Gambar 6). Sampel dipotong kotak dengan ukuran 8x8 cm.
Pengukuran kekenyalan dilakukan dengan menusukkan jarum penetrometer ke nata.
26 Kekenyalan nata diperoleh dari rata-rata penusukan pada lima tempat yang
berbeda. Angka yang ditunjukkan oleh jarum Penetrometer menunjukkan
kekenyalan nata. Satuan pengukuran dinyatakan dalam mm/detik dari berat yang
diberikan. Kekenyalan dihitung dengan rumus sebagai beikut :
Kekenyalan =
Keterangan :
k (1-5) = kekenyalan nata
Warna (Hutching, 1999). Warna adalah kesan yang diperoleh mata dari cahaya yang dipantulkan oleh nata. Analisis warna dilakukan dengan menggunakan
sistem notasi warna Hunter dengan alat Chromameter Minolta CR-310 (Gambar 7).
Chromameter dikalibrasi terlebih dahulu mengunakan pelat standar warna
putih (L=97,15; a=5,35; b=3,37) kemudian dilanjutkan dengan pengukuran warna
sampel. Sistem warna yang digunakan adalah sistem L, a, b.
Gambar 7. Chromameter Minolta CR-310
Sampel diletakkan pada tempat yang tersedia, kemudian ditekan tombol start
maka akan diperoleh nilai L, a dan b dari sampel. Hasil pengukuran dikonversi ke
dalam sistem Hunter dengan notasi L menyatakan parameter kecerahan dari hitam
(0) sampai putih (100). Notasi a menyatakan warna kromatik campuran merah-hijau
dengan nilai +a (positif) dari 0 sampai +100 untuk warna merah, nilai –a (negatif)
dari 0 sampai -80 untuk warna hijau. Notasi b menyatakan warna kromatik
campuran biru-kuning dengan nilai +b (positif) dari 0 dampai +70 untuk warna
kuning dan nilai –b (negatif) dari 0 sampai -80 untuk warna biru. Berdasarkan nilai a
dan b dapat dihitung derajat Hue dengan rumus sebagai berikut :
°Hue = tan -1
Selanjutnya warna produk ditetapkan berdasarkan °Hue yang diperoleh,
27
Karakteristik Kimia
Karakteristik kimia meliputi kadar air, kadar abu, kadar serat kasar, kadar
protein, kadar lemak dan kadar serat pangan. Karakteristik kimia dilakukan secara
komposit di Laboratorium Ilmu dan Teknologi Pangan serta Balai Besar Industri
Agro dan dianalisis secara deskriptif. Prinsip kerja kadar air dan kadar abu sama
halnya dengan metode kadar air dan kadar abu pada penelitian pendahuluan.
Kadar Serat Kasar (Association of official analytical chemist, 1999). Serat kasar merupakan residu dari bahan makanan atau pertanian setelah diperlakukan
dengan asam dan alkali mendidih, dan terdiri dari selulosa dengan sedikit lignin dan
pentosan (Apriyantono et al., 1989). Kadar serat kasar diperoleh dengan cara sebagai
berikut : sampel ditimbang sebanyak 3-5 gram dimasukkan ke labu Erlenmyer 500
ml kemudian ditambahkan H2SO4 25 % sebanyak 50 ml dan didihkan selama 30
menit. Campuran tersebut ditambahkan 50 ml larutan NaOH 3,25% kemudian
didihkan 30 menit. Campuran disaring dengan corong Buchner yang berisi kertas
saring yang telah dikeringkan dan telah diketahui bobotnya. Endapan pada kertas
saring dicuci dengan H2SO4 1,25%, air panas dan etanol 96%, selanjutnya ditimbang
dan dikeringkan pada suhu 105 oC. Endapan dan kertas saring yang telah kering
didinginkan dalam desikator selama 30 menit, selanjutnya ditimbang. Kadar serat
kasar dapat dihitung dengan rumus :
Kadar serat kasar =
x 100% Keterangan :
W = Bobot sampel (g)
W1 = Bobot endapan pada kertas saring (g)
W2 = Bobot abu (g)
Kadar Protein (Association of official analytical chemist, 1999). Protein merupakan molekul polipeptida berukuran besar yang disusun oleh lebih dari 100
buah asam amino yang berikatan satu sama lain secara kovalen dan dalam urutan
yang khas yang disebut ikatan peptida. Penetapan protein pada prinsipnya didasarkan
oksidasi bahan berkarbon dan konversi nitrogen menjadi amonia. Kadar protein
diperoleh dengan cara sebagai berikut : Sampel nata de madoe dihaluskan dan
diambil sampel lima gram. Sampel dimasukkan ke labu Kjehdal dan ditambahkan