LAMPIRAN
Lampiran 1. Dokumentasi tahap penelitian
a. Uji media padat hari 1 b. Uji media padat hari ke 2
c. Uji media padat hari ke 3 d. Uji media padat ke 4
e. Uji media padat hari ke 5
a b
a b
a b
a b
a
f. Uji media cair tanpa fungi pelarut fosfat
g. Uji media cair dengan fungi pelarut fosfat
h. Analisis P-larutan
keterangan : a. zona bening
.Lampiran 2. Prosedur peremajaan pada isolat fungi pelarut fosfat
Bahan : Isolat fungi pelarut fosfat, akuades, agar-agar, NaOH 0,1%, HCl
0,1%, alkohol 96%, kapas, aluminium foil, plastik, wrap, label, kertas, dan tisu.
Media yang digunakan adalah media Pikovskaya (glukosa 10g ; Ca3(PO4)2 5 g ;
(NH4)2SO4 0,5 g ; KCl 0,2 g; MgSO4.7H2O 0,1 g; MnSO4 0,002 g; FeSO4
1. Media Pikovskaya dituang 5ml ke dalam tabung reaksi, lalu di tutup rapat
untuk menghindari kontaminasi.
0,002
g; ekstrak khamir 0,5 g; agar 20 g; akuades).
Alat : Erlemeyer, tabung reaksi, autoklaf, kompor gas, pipet tetes, pipet
skala, jarum ose, timbangan, sprayer, bunsen, oven, laminar air flow, inkubator,
korek api, batang pengaduk.
Cara kerja:
2. Selanjutnya tabung reaksi yang berisi media pikovskaya di autoklaf
dengan suhu 121o
3. Tabung reaksi yang berisi media pikovskaya steril dimiringkan ± 35 C selama 30 menit.
o
4. Diambil isolat yang akan diremajakan sebanyak 1 jarum ose dan
digoreskan secara zig zag di seluruh permukaan media biakan steril
kemudian di tutup rapat.
dan
dibiarkan hingga mengeras.
5. Tiap kultur diulang sebanyak 3 ulangan.
6. Isolat yang telah diremajakan di pindahkan ke dalam inkubator dan
diinkubasi selama tiga hari.
7. Setelah tiga hari dilihat pertumbuhan isolat yang baik untuk digunakan
6A4 U2 0,5 0,6 1,3 1,3 1,6 1,2 1,7 2,1 1,2 2,4 3,2 1,3 3,4 4,3 1,3 1,27 U3 0,6 0,0 0,0 1,8 2,0 1,1 2,4 2,7 1,1 2,9 3,4 1,2 3,4 4,1 1,2 0,92 U1 1,1 0,0 0,0 1,7 1,9 1,1 2,2 2,5 1,1 2,8 3,2 1,1 3,4 4,0 1,2 0,91 7A1 U2 1,1 0,0 0,0 1,5 0,0 0,0 1,9 0,0 0,0 2,5 0,0 0,0 2,9 0,0 0,0 0,00 U3 1,2 0,0 0,0 2,0 2,1 1,1 2,5 2,7 1,1 3,2 3,6 1,1 4,8 5,4 1,1 0,88 U1 1,1 1,2 1,1 1,9 2,9 1,5 2,0 3,3 1,7 2,7 4,2 1,6 3,5 5,5 1,6 1,48 7A2 U2 0,9 1,0 1,1 1,4 1,9 1,4 1,8 2,9 1,6 2,7 4,0 1,5 3,3 4,70 14,2 3,97 U3 0,9 1,0 1,1 1,2 1,7 1,4 1,4 2,1 1,5 2,2 3,2 1,5 4,2 6,3 1,5 1,40 U1 1,1 1,2 1,1 2,0 2,3 1,2 2,7 3,2 1,2 3,5 4,2 1,2 4,8 5,8 1,2 1,16m 7A3 U2 1,1 1,2 1,1 2,1 2,7 1,3 2,6 3,3 1,3 3,1 3,9 1,3 3,5 4,5 1,3 1,24
8A4 U2 0,7 0,0 0,0 1,1 1,4 1,3 1,7 2,1 1,2 3,5 4,1 1,2 5,5 6,2 1,1 0,96 U3 0,7 0,8 1,1 1,3 1,5 1,2 2,1 2,5 1,2 2,9 3,6 1,2 3,5 4,5 1,3 1,20 U1 1,2 0,0 0,0 1,5 0,0 0.0 2,0 0,0 0,0 3,1 0,0 0,0 5,8 0,0 0,0 0,0 9A1 U2 0,9 0,0 0,0 1,5 1,6 1,1 1,7 1,8 1,1 2,8 3,0 1,1 5,0 5,4 1,1 0,86
Keterangan :
Isolat 1-11 : isolat fungi yang digunakan (Aspergillus sp)
1: JF12 7 : JS6
2 : JF4 8 : JS10)
3 : JF1 9 : JV9
4. JNV3 10 : JNV7
5. JS8 11 : JNV4
6: JS4
A1- A4 : Sumber posfat
A1 : FePO4 A3 : batuan fosfat
A2 : AlPO4 A4 : Ca3PO4
42 JS4.Fe.III 0,865 16,80 1,86
43 JS4.Al.I 1,261 25,80 2,58
44 JS4.Al.II 1,790 37,82 2,52
45 JS4.Al.III 1,588 33,23 2,66
46 JS4.RP.I 1,535 32,02 3,16
47 JS4.RP.II 1,039 20,75 2,19
48 JS4.RP.III 2,740 59,41 3,89
49 JS6.Ca.I 3,200 69,86 4,00
50 JS6.Ca.II 3,170 69,18 3,19
51 JS6.Ca.III 3,760 82,59 4,97
52 JS6.Fe.I 2,436 52,50 2,22
53 JS6.Fe.II 2,198 47,09 2,25
54 JS6.Fe.III 1,992 42,41 2,24
55 JS6.Al.I 2,750 59,64 2,73
56 JS6.Al.II 2,141 45,80 2,75
57 JS6.Al.III 2,196 47,05 2,73
58 JS6.RP.I 0,085 -0,93 3,22
59 JS6.RP.II 2,750 59,64 3,14
60 JS6.RP.III 2,320 49,86 2,50
Keterangan :
JF4 : fungi pelarut fosfat yang berasal dari gambut fibrik
Lampiran 4. Tabel anova P-tersedia
SK db JK KT F.hitung F. tabel
Isolat 4 2143,75 535,93 *7,83 2,61
Sumber P 3 2566,42 855,47 *12,51 2,84
Interaksi 12 5422,2435 451,85 *6,60 2,00
Galat 40 2734,56 68,36
Total 59 12866,90
DAFTAR PUSTAKA
Brady, N. C, dan R.R. Well, 2002. Element of The Nature and Properties of Soil. Prentice Hall Uppersadle River, New Jersey.
Cunningham, JE., dan C. Kuiack. 1992. Production of citric and oxalic acid and solubilization of calsium phosphate by Penicillium bilail. Appl. Environ. Microbial. 58:1451-1458.
Clark B. 2001. Soils, water, and watersheds. In: Fire Effects Guide. National Interagency Fire Center. USA.
Elfiati, D. 2005. Peranan Mikroba Pelarut Fosfat Terhadap Pertumbuhan Tanaman. Jurusan Kehutanan. Fakultas Pertanian. Universitas Sumatera Utara. E-USU Repository © 2005 Universitas Sumatera Utara.
El-Azouni, I. M. 2008. Effect of Phosphate Solubilizing Fungi on Growth and Nutrien Uptake of Soybean (Glycine max L.) Plants. Journal of Applied Science Research. INSInet Publications, 4(6):592-598.
Fankem H, Nwaga D, Deubel A, Dieng L, Merbach W, dan Etoa FX. 2006. Occurrence and Functioning of Phosphate Solubilizing Microorganisms from Oil Palm Tree (Elaeisguineensis) Rhizosphere in Cameroon. African Journal of Biotechnology. 5 (24) : 2450 - 2460.
Foth, D.H. 1994. Dasar-dasar Ilmu Tanah. Universitas Gadjah Mada. Yogyakarta.
Gandjar, L., Syamsuridzal, W, dan Oetari, A. 2006. Mikologi Dasar dan Terapan. Yayasan Obor Indonesia. Jakarta.
Gaur, A.C., R.S. Mathur, dan K.V. Sadasivam. 1990. Effect of organic materials and phosphate-dissolving culture on the yield of wheat and greengram. Indian. J. Argon. 25: 501-503.
Goenadi, D.H, dan Saraswati, R. 1994. Kemampuan Melarutkan Fosfat dari Beberapa Isolat Fungi Pelarut Fosfat. Menara Perkebunan 61 (3): 61-66.
Ginting, R. Badia, R. Saraswati dan E.F. Husen. 2006. Pupuk Organik Dan Pupuk Hayati. Balai Besar Penelitian dan Pengembangan Sumberdaya Lahan Pertanian. Bogor.
Hanafiah, K.A. 2009. Dasar-Dasar Ilmu Tanah. Raja Grafindo Persada. Jakarta. 360 halaman.
Havlin, J.L.,J.D. Beaton, S.L. Tisdale, dan W.L. Nelson. 1999. Soil Fertility and
Fertilizer. An Introduction to Nutrient Management. Sixth ed. Pretice
Hall, New Jersey.
Jang J., dan S. Suh. 2002. Aplication of va Mychorrhizae and Phosphate
Solubilizer as Biofertilizers in Korea. National Institute of Agricultural
Science and Technology RDA, pp. 1-7.
Kasno, A., S. Rochayati, dan Bambang H.P. 2009. Fosfat Alam: Pemanfaatan Fosfat Alam yang Digunakan Langsung Sebagai Pupuk Sumber P. Balai Penelitian Tanah Badan Penelitian dan Pengembangan Pertanian, Departemen Pertanian. Bogor.
Khan, A.A., G. Jilani, M. S. Akhtar., S. M. S. Naqvi., dan M. Rasheed. 2009.
Phosphorus Solubilizing Bacteria: Occurrence, Mechanisms and their Role in Crop Production. Agriculture University, Rawalpindi, Pakistan.
Published in J. agric. Biol. sci. 1 (1):48-58.
Lestari, Y, dan Saraswati, R. 1997. Aktivitas Enzim Fosfatase Jamur Pelarut Fosfat Pada Tanah Podzolik Merah Kuning. Banjarmasin
Maryanti, D. 2006. Isolasi dan uji kemampuan bakteri pelarut fosfat dari rhizosfir
tanaman pangan dan semak. [Skripsi]. Padang. Fakultas Pertanian
Universitas Andalas. 84 halaman.
Mulyani. S. E. 2013. Eksplorasi dan Potensi Jamur Pelarut Fosfat Pada Ekosistem Lahan Gambut yang Bervegetasi dan Tidak Bervegetasi. [Skripsi]. USU. Medan
Nautiyal, S.C. 1999. An efficient microbiological growth medium for screening
phosphate solubilizing microorganisms. FEMS Lett. 170:265 – 270.
Noor. M. 2001. Pertanian Lahan Gambut: Potensi dan Kendala. Penerbit Kanisius, Jakarta.
Novizan. 2002. Petunjuk Pemupukan yang Efektif. Agromedia Pustaka, Jakarta.
Nurtjahyani, S. P. 2011 Peran Mikroorganisme dalam Perkembangan Mikrobiologi Pangan.
Prasad, R., dan Power JF. 1997. Soil Fertility Management for Sustaniable Agriculturew: New York: CRC Lesi Publisher.
Rao, N.S,S. 1994. Mikroorganisme Tanah dan Pertumbuhan Tanaman, Edisi Kedua. Universitas Indonesia, Jakarta.
Reddy, M. S., S Kumar dan K. Babita. 2002. Biosolubilization of Poorly Soluble Rock Phosphat by Aspergillus tubingensis and Aspergillus niger. Bioresour. Technol,. 84: 187-189
Rodriguez, H dan Fraga, R. 2000. Phosphate solubilizing bacteria and their role in plant growth promotion. Departement of Microbiology, Cuban Research Institute On Sugarcane By-Products (ICIDCA), P.O.Box 4026, CP 11000, Havana, Cuba. http://www.molecular-plant-biotechnology.
Rosmarkam, A., dan Yuwono, N.W. 2002. Ilmu Kesuburan Tanah. Kanisius, Yogyakarta.
Setiawati, T. C. 2005. Efektifitas Mikroba Pelarut P dalam Meningkatkan Ketersediaan P dan Pertumbuhan Tembakau Besuki Na-Oogst (Nicotiana tabacum L.). Tesis. Program Pascasarjana. IPB. Bogor.
Sitanggang, M. H. P. 2013. Eksplorasi dan Potensi Jamur Pelarut Fosfat pada Ekosistem Lahan Gambut Fibrik dan Hemik. [Skripsi]. USU. Medan
Suhendra, T. 2013. Eksplorasi dan Potensi Jamur Pelarut Fosfat Asal Ekosistem Lahan Gambut Desa Bukkas Malombu Kecamatan Angkola Kabupaten Tapanuli Selatan. USU. Medan.
Suriadikarta, R.D.M dan Simanungkalit, D.A. 2006. Pupuk Organik dan Pupuk Hayati, Balai Besar Litbang Sumberdaya Lahan Pertanian dan Pengembangan Pertanian Bogor.
Sutedjo, M. M. 1996. Mikrobiologi Tanah. Rineka Cipta. Jakarta
Tisdale, S.L, W.L. Nelson, dan J.D. Beaton. 1990. Soil Fertility and Fertilizer. 4th ed. McMillan Publishing Company. New York.
Whitelaw. 2000. Growth promotion of plants inoculated with phosphate
solubilizing fungi. Adv. Agron. 69 : 99-151.
Widjajanti, E. 1991. Peningkatan Kelarutan P Sumber Fosfat Sukar Larut Dengan Menggunakan Bakteri Pelarut P. UNPAD. Bandung.
BAHAN DAN METODE
Waktu dan tempat penelitian
Penelitian dilakukan pada bulan Mei sampai dengan Agustus 2016. Uji
kemampuan fungi pelarut fosfat dilaksanakan di Laboratorium Biologi Tanah
Program Studi Agroekoteknologi Fakultas Pertanian, Universitas Sumatera Utara.
Bahan dan Alat
Bahan yang di gunakan adalah isolat yang diisolasi dari tanah gambut dari
Desa Nagasaribu Kecamatan Lintong Nihuta Kabupaten Humbanghas oleh
Mulyani (2013) dengan kode isolat JNV3, JNV4, JNV7, dan JV9 dari genus
Aspergillus dari tanah bervegetasi dan non vegetasi, tanah gambut dari Dusun
XVI Pasar Banjar, Kecamatan Simpang Empat, Tanjung Balai oleh Sitanggang
(2013), dengan kode isolat JF1, JF4, JF10 dan JF12, dari genus Aspergillus yang
berasal dari gambut fibrik dan dari Desa Bukkas Malombu Kecamatan Angkola
Kabupaten Tapanuli Selatan oleh Suhendra (2013) dengan kode isolat JS4, JS6,
JS8, dan JS10 dari genus Aspergillus yang berasal dari rhizosfer sawit, akuades,
agar-agar, NaOH 0,1%, HCl 0,1%, alkohol 96%, kapas, aluminium foil, plastik,
wrap,label, kertas, dan tisu. Media yang digunakan adalah media Pikovskaya
(glukosa 10g ; Ca3(PO4)2 5 g ; (NH4)2SO4 0,5 g ; KCl 0,2 g; MgSO4.7H2O 0,1 g;
MnSO4 0,002 g; FeSO4 0,002 g; ekstrak khamir 0,5 g; agar 20 g; akuades) dengan
sumber P yang berbeda, yaitu Ca3PO4, AlPo4, FePO4
Alat yang digunakan adalah petridish 10 cm, Erlenmeyer 1000 ml, 500 ml,
dan 250 ml, autoklaf, kompor gas, pipet tetes, pipet skala, tabung reaksi, jarum
inkubator, korek api, sentrifus, pH meter, kamera digital, batang pengaduk, baki,
serbet, alat tulis, alat dokumentasi, maskers, sarung tangan, dan baju laboratorium.
Prosedur Penelitian
a. Uji potensi pada media padat
Fungi pelarut fosfat yang telah disimpan di laboratorium selama tiga tahun
terlebih dahulu di remajakan (lampiran), kemudian diuji kemampuannya
melarutkan fosfat dalam cawan petri berisi media Pikovskaya padat steril. Bahan
yang digunakan dalam pembuatan media uji ini sama dengan bahan media
Pikovskaya pada tahap isolasi (glukosa 10g ; Ca3(PO4)2 5 g ; (NH4)2SO4 0,5 g ;
KCl 0,2 g; MgSO4.7H2O 0,1 g; MnSO4 0,002 g; FeSO4 0,002 g; ekstrak khamir
0,5 g; agar 20 g; akuades), namun Ca3(PO4)2 pada media isolasi diganti dengan
AlPO4, FePO4, dan batuan fosfat (rock phosphate) dengan dosis 5 g/L media.
Media Pikovskaya padat steril dituang secukupnya sampai menutupi
permukaan cawan petri dan dibiarkan mengeras. Selanjutnya biakan murni
ditumbuhkan pada media uji. Tiap kultur diulang sebanyak 3 kali untuk
mendapatkan rataan hasil yang valid. Inkubasi dilaksanakan selama lima hari.
Selama masa pengujian diamati ukuran zona bening dan koloni yang tumbuh pada
media.
Parameter uji potensi pada media padat adalah fungi pelarut fosfat yang
membentuk holozone paling cepat dengan diameter paling besar secara kuantitatif
di sekitar koloni menunjukkan besar kecilnya potensi fungi pelarut fosfat dalam
Dihitung potensi fungi dengan menggunakan nilai indeks pelarutan yaitu:
Indeks pelarutan =
b. Uji potensi pada media cair
Diameter zona bening
Diameter koloni
Fungi pelarut fosfat yang terpilih (nilai indeks pelarutan lebih besar daripada
satu) selanjutnya diuji kemampuannya melarutkan fosfat pada media Pikovskaya
cair. Sebanyak 50 ml media Pikovskaya cair ditempatkan dalam Erlenmeyer 250
ml dan sebanyak 1 jarum ose fungi pelarut fosfat diinokulasikan pada media cair
tersebut, selanjutnya diinkubasi selama 14 hari pada suhu kamar. Setelah proses
inkubasi selesai, kultur disentrifugasi dengan kecepatan 8000 rpm selama 10
menit sampai terjadi pemisahan filtrat dengan fungi sehingga terbentuk endapan.
Diambil filtrat jernih menggunakan pipet dan dijaga agar endapan tidak terikut.
Filtrat jernih ditentukan kadar P-tersedianya dengan metode kolorimetri dan
dihitung dengan Bray-II. Fungi yang paling besar meningkatkan P terlarut secara
kuantitatif pada media merupakan fungi yang efektif dan potensial. Setelah itu pH
medium diukur dengan pH meter untuk mengetahui pengaruh pelarutan fosfat
oleh fungi terhadap pH media.
Uji potensi pada media cair menggunakan Rancangan Acak Lengkap Faktorial
dengan dua faktor perlakuan dan tiga kali ulangan. Masing-masing faktor tersebut
adalah :
1. Faktor pertama adalah isolat fungi pelarut fosfat
F1 : Aspergillus sp. (JF4)
F2 : Aspergillus sp. ( JNV3)
F4 : Aspergillus sp. (JS4)
F5 : Aspergillus sp. (JS6)
2. Faktor kedua adalah sumber P
P1 = Ca3PO4
P2 = AlPO4
P3 = FePO4
P4 = Batuan fosfat (rock phosphate)
Dengan demikian diperoleh 60 jumlah unit percobaan (5 x 4 x 3).
Model linear yang digunakan :
Yij(k) = µ + αi + βj + αβ + €ijk
Keterangan :
Yij(k) = pengamatan pada perlakuan isolat ke–i, pada sumber fosfat ke-j, dan
interaksi isolat ke-i dan sumber fosfat ke-j
µ = rataan umum
αi = pengaruh perlakuan isolat ke-i
βj = pengaruh perlakuan berbagai sumber fosfat ke-j
(αβ)ij = pengaruh interaksi perlakuan isolat ke-i dan berbagai sumber fosfat ke-j
€ijk = pengaruh galat dari perlakuan isolat ke-i, berbagai sumber ke-j, dan
interaksi isolat ke-i dan berbagai sumber fosfat ke-j.
Untuk mengetahui pengaruh dari setiap perlakuan maka akan dilakukan
analisis sidik ragam (Anova). Apabila F-hitung nyata atau sangat nyata maka
dilanjutkan dengan uji lanjutan berdasarkan uji jarak Duncan (Duncan Multiple
HASIL DAN PEMBAHASAN
Kemampuan Fungi Pelarut Fosfat dalam media pikovskaya padat
Sebanyak 11 isolat Fungi pelarut fosfat yang merupakan koleksi
laboratorium yang telah disimpan selama tiga tahun diuji kemampuannya dalam
melarutkan P-terikat dalam media Pikovskaya padat. Pengujian dilakukan dengan
menggunakan sumber P yang berbeda yaitu Ca3PO4, AlPO4, FePO4
Sumber Fosfat
dan batuan
fosfat. Kemampuan fungi dalam melarutkan fosfat dapat dilihat dari terbentuknya
zona bening di sekitar koloni. Daerah bening ini terbentuk karena adanya
pelarutan fosfat dari sumber fosfat sukar larut yang ada dalam media oleh
asam-asam organik yang dihasilkan koloni fungi. Kemampuan melarutkan fosfat
ditunjukkan oleh nilai indeks pelarutan, yaitu nisbah antara diameter holozone
(diameter zona bening) dengan diameter koloni (Tabel 1).
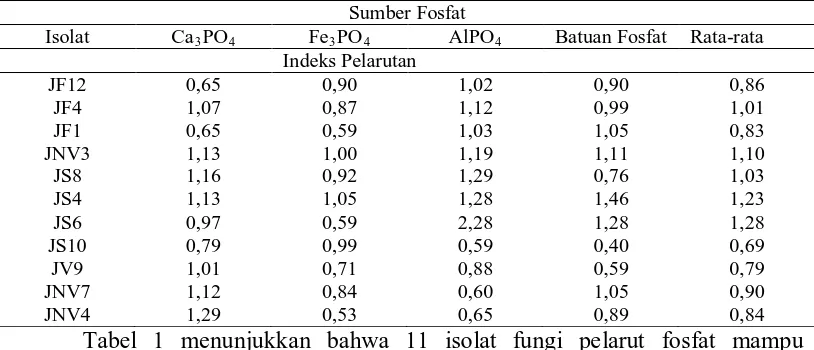
Table 1. Nilai indeks pelarutan fosfat pada media padat dengan berbagai sumber P
Isolat Ca3PO4 Fe3PO4 AlPO4 Batuan Fosfat Rata-rata
Tabel 1 menunjukkan bahwa 11 isolat fungi pelarut fosfat mampu
melarutkan fosfat meskipun dengan indeks pelarutan yang bervariasi pada setiap
sumber P (Ca3PO4, FePO4, AlPO4 dan batuan fosfat). Fungi pelarut fosfat yang
mampu melarutkan fosfat dari sumber Ca3PO4 adalah JNV4 dengan indeks
sumber Fe3PO4 yang paling besar adalah JS4 dengan indeks pelarutan sebesar
1,05. Fungi pelarut fosfat yang mampu melarutkan fosfat dari sumber AlPO4 yang
paling besar adalah JS6 dengan indeks pelarutan sebesar 2,28, sedangkan fungi
pelarut Fosfat yang mampu melarutkan fosfat dari sumber batuan fosfat yang
paling besar adalah JS4 dengan indeks pelarutan sebesar 1,46.
Kemampuan setiap isolat dalam melarutkan P sangat berbeda-beda. Isolat
JS6 mempunyai nilai indeks terbesar melarutkan P dari sumber AlPO4 belum
tentu mempunyai nilai indeks pelarutan terbesar dari sumber Ca3PO4, Fe3PO4,
maupun batuan fosfat. Hal ini sesuai dengan pernyataan Elfiati (2005) yang
menyatakan bahwa setiap fungi memiliki kemampuan yang berbeda-beda dalam
melarutkan ikatan fosfat Ca3(PO4)2, AlPO4, FePO4 dan RP. Isolat FPF yang
mampu mereduksi senyawa fosfat mungkin terkait erat dengan kemampuannya
dalam menghasilkan asam organik, karena menurut Ginting et al., (2006) asam
organik yang dilepaskan oleh isolat FPF mampu mengikat PO4.
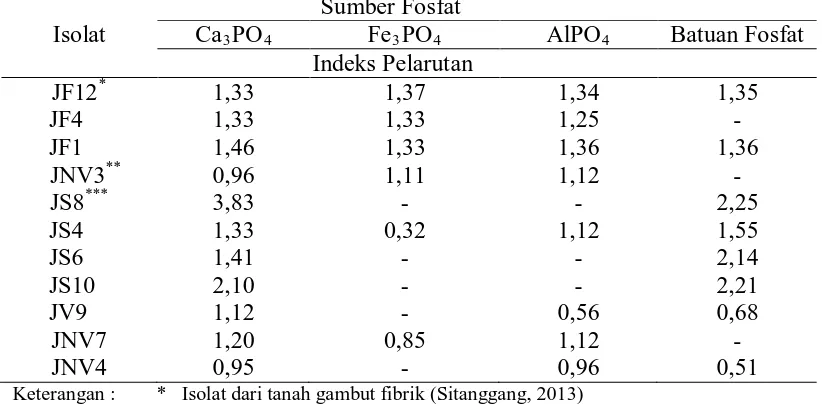
Tabel 2. Nilai indeks pelarutan fosfat dengan berbagai sumber P tahun 2013 Sumber Fosfat
Keterangan : * Isolat dari tanah gambut fibrik (Sitanggang, 2013)
Pada Tabel 1 dapat dilihat bahwa 11 isolat mampu melarutkan P dari
berbagai sumber, sedangkan pada Tabel 2 terdapat isolat yang tidak mampu dalam
melarutkan P dari berbagai sumber. Adanya perubahan kemampuan isolat tersebut
diduga karena fungi mempunyai pertumbuhan yang berbeda-beda. Hal ini sesuai
dengan pernyataan Gaur et al., (1990) menyatakan bahwa fungi yang dapat
menyesuaikan diri dengan kondisi di sekitarnya akan mudah tumbuh dan cepat
berkembang biak, dan jumlahnya akan lebih banyak. Fungi yang pertumbuhannya
lambat membutuhkan waktu inkubasi yang lama untuk berkembang biak.
Efektifitas pelarutan fosfat sangat dipengaruhi oleh pH, suhu, aerasi, dan waktu
inkubasi.
Tabel 2 menunjukkan bahwa indeks pelarutan terbesar pada tahun 2013
adalah isolat JS8 yaitu 3,83 dari sumber Ca3PO4, tetapi tidak mampu melarutkan
P pada sumber media AlPO4, FePO4. Sedangkan nilai indeks pelarutan terkecil
ditunjukkan oleh isolat JNV4 sebesar 0,51 yang berasal dari sumber batuan fosfat
dan mampu melarutkan P pada media Ca3PO4 dan AlPO4.
Berdasarkan Tabel 1 dan Tabel 2, hasil pengukuran indeks pelarutan pada
tahun 2013 lebih besar dibandingkan dengan hasil pengukuran indeks pelarutan
pada tahun 2016. Hal ini dapat dilihat dari nilai rata-rata indeks pelarutan yang
dihasilkan dari pengukuran tersebut. Penurunan nilai indeks pelarutan disebabkan
karena kemungkinan jumlah populasi yang tidak seragam pada saat inokulasi,
konsentrasi fosfat yang tidak larut dalam air, ketebalan agar yang tidak seragam,
dan kecepatan pertumbuhan isolat yang berbeda. Hal ini sesuai dengan
pernyataan Geonadi dan Saraswati (1994), variasi indeks pelarutan fosfat
1. Konsentrasi fosfat tidak larut dalam air, untuk menuang medium ini ke
dalam cawan petri perlu digoyang-goyang terlebih dahulu. Ada
kemungkinan bahwa konsentrasi sumber fosfatnya tidak seragam,
sehingga zona jernihnya juga berpengaruh.
2. Ketebalan agar juga mempengaruhi zona bening yang terbentuk. Agar
yang lebih tebal tentunya lebih sulit untuk dilarutkan dari pada agar yang
tipis.
3. Kecepatan pertumbuhan mikroba. Ada mikroba yang tumbuh dengan
cepat dan ada mikroba yang tumbuh lambat.
Menurut Maryanti (2006) Pelarutan unsur Ca yang mengikat P pada media
Pikovskaya dapat dilihat dari lebar zona bening yang terbentuk di sekeliling
koloni. Semakin besar zona bening maka semakin besar kemampuannya dalam
melarutkan fosfat. Pertambahan lebar zona bening yang lebih tinggi oleh suatu
isolat terhadap isolat lainnya menunjukkan bahwa isolat fungi ini mempunyai sifat
yang lebih unggul. Pertambahan zona bening tentunya diikuti juga oleh
pertambahan diameter koloni fungi. Oleh sebab itu perlu dilakukan pengujian
lebih lanjut untuk mengetahui kemampuan isolat fungi pelarut fosfat dalam
melarutkan fosfat pada media Pikovskaya cair.
Kemampuan Fungi Pelarut Fosfat dalam media pikovskaya cair
Aktifitas masing-masing isolat fungi pelarut fosfat yang tumbuh pada
media padat berbeda dengan aktifitas pada media cair. Pengujian pada media
padat digunakan untuk mengetahui secara kuantitatif besar kecilnya kemampuan
isolat dalam melarutkan fosfat yaitu melalui terbentuknya zona bening disekitar
kualitatif dapat dianggap sebagai tanda kemampuan fungi pelarut fosfat
melarutkan fosfat dalam media tumbuh semakin besar. Pada umumnya semakin
besar nilai perbandingan antara garis tengah zona bening dengan garis tengah
koloni, menunjukkan kemampuan fungi pelarut fosfat dalam melarutkan fosfat
secara kualitatif semakin besar, walaupun hal ini belum cukup untuk
menggambarkan kemampuan fungi pelarut fosfat dalam pelarutan fosfat yang
sebenarnya.
Dari Tabel 1 isolat yang diuji kemampuannya pada media padat tidak
semuanya diuji pada media cair. Hasil uji potensi pada media padat hanya didapat
lima isolat yang mempunyai nilai indeks pelarutan yang mempunyai nilai indeks
pelarut paling besar. Nilai indeks pelarutan paling besar dapat dilihat dari rata-rata
nilai indeks pelarutan dari setiap isolat pada berbagai sumber P dengan nilai
indeks pelarutannya lebih besar dari satu cm (>1). Kelima isolat yang mempunyai
nilai indeks terbesar yaitu JF4, JNV3, JS8, JS4, dan JS6. Kelima isolat ini diuji di
media cair dengan sumber fosfat dari Ca3PO4, AlPO4, FePO4
dan batuan fosfat.
Menurut Geonadi dan Saraswati (1994) kemampuan melarutkan fosfat diukur
berdasarkan peningkatan kadar P terlarut dibandingkan kontrol.
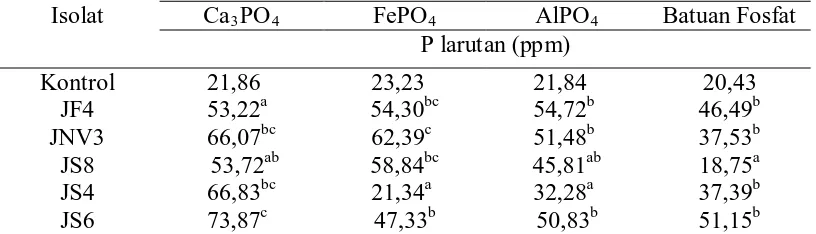
Tabel 3. Hasil Pengukuran P tersedia yang dilarutkan fungi pelarut fosfat Sumber Fosfat
Berdasarkan hasil pengujian yang disajikan pada Tabel 3 terlihat bahwa
kemampuan fungi pelarut fosfat dari sumber P yang berbeda sangat bervariasi.
Jumlah P yang dapat dilarutkan dari sumber Ca3(PO4)2 lebih tinggi dibandingkan
dengan sumber AlPO4, FePO4 dan batuan fosfat. Menurut Noor (2001) hal ini
disebabkan karena sumber AlPO4, FePO4, dan batuan fosfat lebih sukar larut atau
memerlukan waktu yang cukup lama untuk melarutkannya dibandingkan dengan
sumber Ca3(PO4)2 dan berkaitan erat dengan kemampuan fungi pelarut fosfat
dalam menghasilkan asam organik yang berbobot molekul rendah karena jumlah
asam organik yang diekskresikan oleh fungi pelarut fosfat berbeda-beda, asam
organik ini berperan membentuk khelat organik yang stabil sehingga dapat
membebaskan ion fosfat dari bentuk tidak tersedia menjadi bentuk yang tersedia
(Widjajanti, 1991).
Kemampuan Fungi pelarut fosfat dalam melarutkan fosfat pada uji media
cair berbeda-beda. Pada kontrol ditemukan P terlarut meskipun tidak diberi
inokulum fungi pelarut fosfat. Besar P pada kontrol Ca3PO4 sebesar 21,86 ppm,
pada FePO4 sebesar 23,23 ppm, sedangkan pada media AlPO4
Kemampuan isolat dalam pelarutan fosfat dari keempat sumber media
kemudian dibandingkan dengan besar kontrol dari keempat media. Isolat yang
paling besar dalam melarutkan P dari sumber fosfat Ca
sebesar 21,84 ppm
dan pada media batuan fosfat sebesar 20,43 ppm. Pelarutan fosfat yang terjadi
pada kontrol ini kemungkinan disebabkan karena adanya pemanasan saat
sterilisasi media.
3PO4 yaitu JS6 dengan P tersedia sebesar 73,87 ppm, artinya isolat JS6 memiliki kemampuan
terikat menjadi bentuk tersedia dibandingkan dengan kontrol yang tanpa
inokulasi. Sedangkan yang terkecil dari sunber Ca3PO4 adalah isolat JF4 dengan P
tersedia sebesar 53,22 ppm. Hasil uji lanjut isolat dari sumber Ca3PO4
menunjukkan isolat JS6 tidak berbeda nyata dengan isolat JS4 dan isolat JNV3
tetapi berbeda nyata dengan isolat lainnya.
Kemampuan isolat yang paling besar dalam membebaskan fosfat dari
sumber FePO4 adalah JNV3 yaitu sebesar 62,39 ppm, artinya isolat JNV3
memiliki kemampuan melarutkan fosfat 2,68 kali lebih tinggi dalam
membebaskan fosfat dibandingkan dengan kontrol tanpa inokulasi, sedangkan
isolat terkecil dari sumber FePO4 adalah JS4 dengan P tersedia sebesar 21,34
ppm. hasil uji lanjut menunjukkan isolat JNV3 tidak berbeda nyata dengan isolat
JF4 dan isolat JS8 tetapi berbeda nyata dengan isolat lainnya.
Kemampuan isolat yang paling besar dalam melarutkan P dari sumber
AlPO4 adalah JF4 dengan P tersedia sebesar 54,72 ppm, artinya isolat JF4
memiliki kemampuan membebaskan fosfat 2,50 kali lebih tinggi dalam
membebaskan fosfat dibandingkan kontrol tanpa inokulasi dan terendah
membebaskan fosfat dari sumber AlPO4 adalah isolat JS4 yaitu sebesar 32,28
ppm. Hasil uji lanjut pada sumber AlPO4
Kemampuan isolat yang mampu melarutkan P dari sumber batuan fosfat
adalah JS6 dengan P tersedia sebesar 51,15 ppm artinya isolat JS6 memiliki
kemampuan membebaskan fosfat 2,50 kali lebih tinggi dibandingkan kontrol
tanpa inokulasi dan terendah membebaskan fosfat dari sumber batuan fosfat menunjukkan isolat JF4 tidak berbeda
adalah JS8 yaitu sebesar 18,75 ppm. Hasil uji lanjut pada sumber batuan fosfat
menunjukkan isolat JS8 berbeda nyata dengan isolat lainnya.
Aktivitas masing-masing isolat Fungi pelarut fosfat dalam melarutkan P
yang tumbuh pada medium padat berbeda dengan aktivitas pada medium cair.
Kemampuan fungi pada medium cair dapat dipengaruhi oleh aerasi dan lamanya
waktu inkubasi. Menurut Fankem et al. (2006), aktivitas fungi dalam melarutkan
P pada media padat dan cair tidak mutlak sama. Kriteria zona bening tidak cukup
untuk menentukan kemampuan mikroba dalam melarutkan P. Jumlah mikroba
yang banyak juga belum tentu memiliki kemampuan yang tinggi dalam
melarutkan P.
Semua isolat (JF4, JNV3, JS8, JS4, JS6) mampu melarutkan P dari sumber
Ca, Al, Fe dan batuan fosfat dikarenakan Aspergillus sp. mampu menghasilkan
asam organik. Hal ini didukung oleh pernyataan Khan et al. (2009) yang
menyatakan bahwa Aspergillus sp. telah diketahui mampu menghasilkan asam
organik berupa asam oksalat, asam sitrat asam glukonat, dan asam suksinat.
Asam-asam organik seperti asam sitrat, asam suksinat, dan asam oksalat dapat
menggantikan kedudukan anion P, dan mengelat kation-kation seperti Ca, Al, dan
Fe membentuk senyawa kompleks.
Dari Tabel 3 dapat dilihat bahwa urutan kemampuan pelarutan media
fosfat yang terbesar terdapat pada media Ca3PO4,diikuti oleh media AlPO4 dan
FePO4. Hal ini sesuai dengan pernyataan Premono (1994) yang menyatakan
bahwa asam organik yang mampu membentuk komplek yang lebih mantap
sehingga akan melepas P yang lebih besar. Urutan kemudahan fosfat terlepas
mengikuti urutan Ca3[(PO)4]2 > AlPO4 > FePO4
.
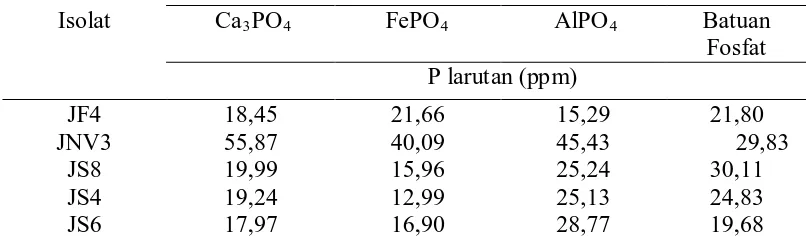
Tabel 4. Hasil pengukuran P-tersedia tahun 2013
Sumber Fosfat
Pada Tabel 4 dapat dilihat bahwa isolat yang terbesar dalam melarutkan P
dari media Ca3PO4 adalah JNV3 sebesar 55,87 ppm. Isolat yang mampu
melarutkan P terbesar pada sumber FePO4 adalah JNV3 40,09 ppm. Isolat yang
mampu melarutkan P terbesar pada sumber AlPO4 adalah JNV3 sebesar 45,43
ppm. Isolat yang mampu melarutkan P terbesar pada sumber batuan fosfat adalah
JS8 sebesar 30,11 ppm.
Berdasarkan Tabel 3 dan Tabel 4 hasil pengukuran P terlarut pada tahun
2016 lebih besar dibandingkan dengan pengukuran P terlarut pada tahun 2013.
Hal ini dapat dilihat dari nilai pengukuran P terlarut. Peningkatan nilai P terlarut
menunjukkan bahwa isolat yang disimpan selama tiga tahun masih berpotensi
dalam melarutkan P.
Selain mengukur kadar P-tersedia, pada uji media cair dilakukan
pengukuran pH media sebelum dilakukan inokulasi dan diukur kembali pH media
setelah dilakukan inokulasi fungi pelarut fosfat selama 14 hari untuk mengetahui
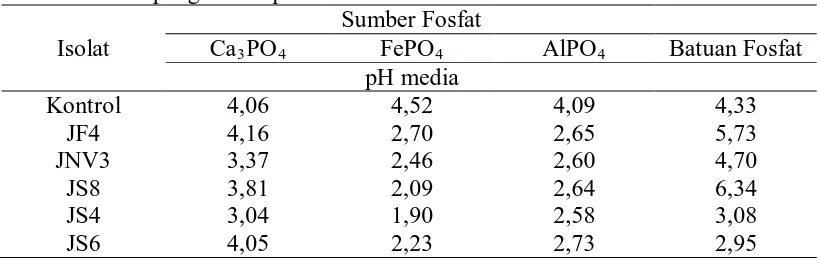
Tabel 5. Hasil pengukuran pH media
Perubahan pH yang terjadi dapat dilihat setelah dilakukannya inkubasi
selama 14 hari. pH sebelum dilakukan pemberian isolat adalah pH netral (6,92)
dan terjadi penurunan pH dimana kisaran pH setelah inkubasi adalah 1,90-6,34.
Penurunan pH terjadi karena pada saat fungi pelarut fosfat melarutkan fosfat,
fungi pelarut fosfat mengeluarkan sejumlah asam-asam organik yang dapat
mempengaruhi terhadap perubahan pH dari netral menjadi masam. Hal ini sesuai
dengan pernyataan Setiawati (2005) yang menyatakan bahwa penurunan pH ini
diduga akibat pembebasan sejumlah asam-asam organik oleh fungi pelarut fosfat
sebagai hasil metabolismenya akibat banyaknya asam organik yang diekskresikan
membuat pH menjadi turun. Hal ini merupakan bentuk adaptasi fungi pelarut
fosfat terhadap media yang mengandung P terikat yang lebih tinggi dari P
terlarut. Fosfat merupakan sumber energi primer bagi oksidasi fungi pelarut
fosfat. Jika fungi pelarut fosfat mati maka P-organik yang terdapat dalam jaringan
mikroba akan lepas kembali dalam bentuk P-anorganik. Fungi pelarut fosfat
mengeluarkan berbagai macam asam organik seperti asam formiat, asetat,
propionat, laktat, glikolat, fumarat, dan suksinat. Asam-asam organik ini dapat
membentuk khelat (kompleks stabil) dengan kation Al, Fe atau Ca yang mengikat
Penurunan pH media menandakan bahwa terjadi pelarutan P oleh fungi
pelarut fosfat, dimana fungi pelarut fosfat mengeluarkan asam-asam organik
sehingga pH media menjadi semakin masam. Menurut Jang dan Suh (2002),
terdapat korelasi negatif antara pH dengan pelarutan P, dimana penurunan pH
sejalan dengan penaikan pelarutan P. Hubungan antara pH dengan P terlarut
dimana pelarutan P tergantung dari banyaknya dan jenis asam organik yang
dikeluarkan oleh isolat tersebut yang ditandai dengan penurunan pH.
Asam-asam organik melarutkan P pada media dan dalam tanah melalui
mekanisme antara lain: kompetisi anion ortofosfat pada tapak jerapan, perubahan
pH media, pengikatan logam membentuk logam organik dan khelat oleh ligan
organik. Terdapatnya asam-asam organik ini dalam tanah sangat penting artinya
dalam mengurangi ikatan P oleh unsur penjerapannya dan mengurangi daya racun
logam seperti aluminium pada tanah masam. Menurut Premono (1994), kecepatan
pelarutan P dari mineral P oleh asam organik ditentukan oleh: (1) kecepatan difusi
asam organik dari larutan tanah, (2) waktu kontak antara asam organik dan
permukaan mineral, (3) tingkat dissosiasi asam organik, (4) tipe dan letak gugus
KESIMPULAN DAN SARAN
Kesimpulan
Fungi pelarut fosfat yang disimpan selama tiga tahun di Laboratorium
masih mempunyai potensi dalam melarutkan fosfat. Fungi pelarut fosfat yang
paling baik dalam melarutkan P dari sumber Ca3PO4 adalah JS4, fungi pelarut
fosfat yang paling baik dalam melarutkan P dari sumber FePO4 adalah JNV3,
fungi pelarut fosfat yang paling baik dalam melarutkan P dari sumber AlPO4
adalah JF4 dan fungi pelarut fosfat yang paling baik dalam melarutkan P dari
sumber batuan fosfat adalah JS6.
Saran
Perlu dilakukan perhitungan jumlah koloni fungi pelarut fosfat sebelum
TINJAUAN PUSTAKA
Unsur Hara Fosfor (P)
Unsur fosfat (P) adalah unsur esensial kedua setelah N yang berperan
penting dalam fotosintesis dan perkembangan akar. Ketersediaan fosfat
dalam tanah jarang yang melebihi 0,01% dari total P. Sebagian besar bentuk
fosfat terikat oleh koloid tanah sehingga tidak tersedia bagi tanaman. Fosfat
tersebut tidak dapat dimanfaatkan semaksimal mungkin oleh tanaman, karena
fosfat dalam bentuk P-terikat di dalam tanah. Pada tanah-tanah masam, fosfat
akan bersenyawa dalam bentuk-bentuk Al-P, Fe-P, dan occluded-P, sedangkan
pada tanah-tanah alkali, fosfat akan bersenyawa dengan kalsium (Ca) sebagai
Ca-P membentuk senyawa kompleks yang sukar larut
(Suriadikarta dan Simanungkalit, 2006).
Unsur P terdapat pada seluruh sel hidup tanaman. Beberapa fungsi
phosphor adalah membentuk asam nukleat (RNA dan DNA), menyimpan serta
memindahkan energi ATP dan ADP, merangsang pembelahan sel dan membantu
proses asimilasi dan respirasi (Novizan, 2002).
Fosfat di dalam tanah terdapat dalam bentuk fosfat anorganik dan fosfat
organik. Bentuk anorganiknya berupa senyawa-senya-wa Ca-fosfat, Fe-fosfat dan
Al-fosfat. Fosfor organik mengandung senyawa-senyawa yang berasal dari
tanaman dan mikroba dan tersusun dari asam nukleat, fosfolipid dan fitin. Materi
organik yang berasal dari sampah tanaman mati dan membusuk kaya akan
sumber-sumber fosfor organik. Beberapa faktor yang mempengaruhi kelarutan
alam khususnya adanya substitusi karbonat terhadap P pada apatit, derajat
percampuran antara fosfat alam dan tanah serta tingkat penggunaan fosfat alam
pada tanah (Sutedjo, 1996).
Tanaman menyerap P dalam bentuk ion ortofosfat (H2PO4-) dan ion
ortofosfat sekunder (HPO42-). Unsur P masih dapat diserap dalam bentuk lain,
yaitu bentuk pirofosfat dan metafosfat, dan kemungkinan unsur P diserap dalam
bentuk senyawa organik yang larut dalam air, misalnya asam nukleat dan fitin. P
yang diserap tanaman dalam bentuk ion anorganik cepat berubah menjadi
senyawa P organik yang mudah bergerak antarjaringan tanaman. Kadar optimal P
dalam tanaman pada saat pertumbuhan vegetative adalah 0,3–0,5% dari berat
kering tanaman (Rosmarkam dan Yuwono, 2002).
Tanah dengan bahan organik yang tinggi, khususnya fraksi aktif dan bahan
organik secara relatif mengikat fosfat dalam tingkat yang rendah. Derajat pengikat
P tinggi terjadi pada pH yang sangat rendah dan sangat tinggi. Sebagaimanapun
pH meningkat dari bawah 5-6, Fe dan Al-P menjadi suatu yang lebih terlarut juga
pada titik pH> 8 dan diatas 6 senyawa Ca-P kelarutannya tinggi. Bahan organik
secara umum memiliki kapasitas yang rendah dalam mengikat ion fosfat
( Brady dan Well, 2002).
Kadar P pada tanah gambut beragam. Sebagian dalam bentuk organik
sehingga memerlukan proses mineralisasi untuk dapat digunakan tanaman.
Keberadaan P pada tanah gambut diketahui mudah hilang atau rendah disebabkan
oleh pencucian. Mekanisme ini di gambarkan oleh kapasitas tukar anion tanah
yang rendah. Namun kadar P relatif tinggi pada lapisan atas dibandingkan lapisan
R
2R R4R R 4R
Fosfat alam memiliki sifat tidak larut dalam air tetapi larut dalam kondisi
asam. Faktor yang memengaruhi kelarutan fosfat alam adalah sifat fisik, kimia
fosfat alam, tanah, dan tanaman. Sifat tanah yang menentukan kelarutan fosfat
alam adalah pH tanah. Fosfat alam lebih mudah larut pada tanah yang memiliki
pH rendah, oleh sebab itu fosfat alam tidak sesuai diaplikasikan pada tanah yang
bereaksi netral hingga alkalis. Kadar Ca yang tinggi menghambat kelarutan fosfat
alam, sedangkan tanah yang memiliki kadar Ca dan P yang rendah seperti tanah
ultisol atau oksisol akan mendorong kelarutan fosfat alam sehingga aplikasi fosfat
alam menjadi efektif meningkatkan ketersediaan Ca dan P pada tanaman. Tingkat
kelarutan fosfat alam dapat diketahui melalui pelarutan asam sitrat 2%, amonium
sitrat pH 7, asam format 2%, indeks kelarutan sitrat absolut dalam asam
sitrat terhadap kadar P2O5
Sifat P dalam tanah tidak mobil karena tingkat ketersediaannya dalam
tanah dipengaruhi oleh: reaksi tanah (pH), kadar Al dan Fe oksida, kadar Ca,
kadar bahan organik, tekstur dan pengelolaan lahan. Fosfat tanah dapat dalam
bentuk P larutan, P labil, P difiksasi oleh Al, Fe atau Ca, dan P organik. Fosfat
dalam larutan dapat berbentuk H PO ־ atau HPO
pada mineral apatit (Hartatik, 2011).
Ketersediaan Fosfat dalam Tanah
42־
Ketersediaan fosfor tanah untuk tanaman sangat dipengaruhi oleh sifat dan
ciri tanah itu sendiri. Ada beberapa faktor yang turut mempengaruhi ketersediaan , tergantung dari kemasaman
larutan (pH). Fosfat tidak tersedia difiksasi oleh Fe dan Al oksida pada tanah
masam, difiksasi Ca pada tanah basa. Bentuk-bentuk tersebut saling terjadi.
keseimbangan, artinya apabila bentuk P tidak tersedia dalam jumlah sedikit akan
P tanah, yaitu tipe liat, pH tanah, waktu reaksi, temperatur, dan bahan organik
tanah (Foth, 1994).
Ketersediaan P di kebanyakan tanah maksimum pada rentan pH 6,0.
Fiksasi P terjadi pada tanah-tanah masam dan kapuran atau bereaksi alkalin. Pada
tanah masam (pH rendah), fosfat larut akan bereaksi dengan Fe atau Al larut dan
oksida-oksida hidrusnya, membentuk senyawa sebagai Fe- atau Al-fosfat yang
relatif kurang larut, sehingga tidak dapat di serap oleh tanaman. Sebaliknya pada
tanah-tanah alkalin (pH tinggi) ion Ca dan senyawa karbonatnya akan
mengendap dengan P larut sebagai mineral Ca-P. Fosforus paling banyak tersedia
pada rentan pH antara 5,5 dan 6,5 (Prasad dan Power, 1997).
Kelarutan senyawa fosfor anorganik secara langsung mempengaruhi
ketersediaan P untuk pertumbuhan tanaman. Kelarutan P dipengaruhi oleh pH
tanah, yaitu pada pH 6-7 untuk tanaman. Jika pH dibawah 6, maka fosfor akan
terikat oleh Fe dan Al. Ketersediaan fosfor umumnya rendah pada tanah asam dan
basa. Pada tanah dengan pH diatas 7, maka fosfor akan diikat oleh Mg dan Ca
(Rosmarkan dan Yuwono, 2000).
Beberapa factor yang mempengaruhi kelarutan fosfat antara lain
konsentrasi H, Ca dan P di dalam larutan, komposisi fosfat alamnya khususnya
adanya subtitusi karbonat terhadap P pada apatit, derajat percampuran antara
fosfat alam dan tanah serta tingkat penggunaan fosfat alam pada tanah. Kelarutan
fosfat alam dalam larutan tanah akan lebih baik jika pH tanah, ca dapat
dipertukarkan dan konsentrasi P di dalam larutan tanah rendah. Pada tanah
masam yang banyak memerlukan P penggunaan fosfat alam dinilai lebih efektif
alam lebih reaktif dan lebih murah dibandingkan menggunakan super fosfat
(Chien, 1990 dalam Kasno et al., 2009).
Secara umum faktor-faktor yang memprngaruhi serapan P dalam tanah
ialah: 1)sifat dan jumlah komponen-komponen dalam tanah yang terdiri atas
hidrus oksidasi logam dari besi dan aluminium, tipe liat, kadar liat, koloid-koloid
amorf, dan kalsium karbonat, 2) pH, 3) kation, 4) anion, 5) kejenuhan kompleks
jerapan, 6) bahan organic, 7) suhu, dan 8) waktu reaksi ( Tisdale et al., 1990).
Mikroba pelarut fosfat
Mikroba pelarut fosfat hidup di sekitar perakaran tanaman, mulai
permukaan tanah sampai kedalaman 25cm. Keberadaannya berkaitan dengan
jumlah bahan organik yang akan mempengaruhi populasi serta aktivitasnya dalam
tanah. Mikroba yang hidup dekat daerah perakaran secara fisiologis lebih aktif
dibanding mikroba yang hidup jauh dari daerah perakaran. Keberadaan mikroba
pelarut fosfat beragam dari satu tempat ke tempat lainnya karena perbedaan sifat
biologis mikroba itu sendiri. Terdapat mikroba yang hidup pada kondisi masam
dan ada pula yang hidup pada kondisi netral dan basa, ada yang hipofilik,
mesofilik dan termofilik ada yang hidup aerob maupun anaerob dan beberapa sifat
lain yang bervariasi. Masing-masing mikroorganisme memiliki sifat-sifat khusus
dan kondisi lingkungan optimal yang berbeda-beda yang mempengaruhi
efektivitasnya melarutkan fosfat (Ginting et al., 2006).
Mikroba tanah yang berperan dalam penyediaan unsur hara adalah mikroba
pelarut unsur fosfat (P) dan kalium (K). Kandungan P yang cukup tinggi (jenuh) pada
tanah, sedikit sekali yang dapat digunakan oleh tanaman karena terikat pada mineral
liat dan menyediakannya bagi tanaman. Banyak sekali mikroba yang mampu
melarutkan P, antara lain: Aspergillus sp, Penicillium sp, Pseudomonas sp dan
Bacillus megatherium. Mikroba yang berkemampuan tinggi dalam melarutkan P (Nurtjahyani, 2011).
Mikroba pelarut fosfat berperanan dalam melarutkan fosfat yang terikat
oleh asam organik dan menjaga unsur P yang terlarut tidak hilang dan terikat oleh
asam organik tanah sehingga dapat tersedia bagi tanaman. Mikroba pelarut fosfat
fungi menghasilkan asam organik monokarboksilat seperti asam asetat, asam
formiat, monokarboksil hidroksil seperti asam laktat, asam monokarboksil
ketogluconat (asam oksalat, suksinat dan dikarboksilat hiroksilat sperti asam
malat untuk melarutkan P (Khan et al., 2009). Selain itu fosfat juga dapat
dilarutkan oleh enzim yang dihasilkan mikroba. Lebih lanjut disebutkan bahwa
spesies fungi seperti Aspergillus, dan Penicillium serta bakteri seperti Bacillus,
Rhizobium, Burkholderia, Achromobacter, Agrobacterium, Micro-coccus, Aerobacter, Flavobacterium dan Erwinia berkemampuan sebagai pelarut fosfat.
Mikroba pelarut fosfat bersifat menguntungkan karena mengeluarkan
berbagai macam asam-asam organik seperti asam format, asetat, propionate,
laktat,glikolat, fumarat dan asam suksinat. Asam-asam organik ini membentuk
khelat (komplek stabil) dengan kation Al, Fe atau Ca yang mengikat P, sehingga
ion H2PO4
Fungi terbagi menjadi tiga kelompok, yaitu mold, yeast dan mushroom.
Fungi berperan dalam transformasi unsur pokok di dalam tanah dan pembentukan menjadi bebas dari ikatannya dan tersedia bagi tanaman
(Rodriquezz dan Fraga, 2000).
pada bahan organik tanah. Jumlah fungi di dalam tanah bervariasi sekitar 106
individu per gram tanah, tergantung pada kondisi tanah. Faktor yang penting
berhubungan dengan aktivitas fungi adalah ketersediaan makanan
(Brady dan Well, 2002).
Kemampuan fungi pelarut fosfat mampu meningkatkan ketersediaan P
sebesar 26-40% serta dapat di jumpai pada berbagai habitat dan kondisi yang
berbeda dan tahan terhadap kondisi kelembaban dan suhu yang rendah. Pada pH
5−5.5 umumnya di jumpai dominasi fungi, kemasaman (pH) daerah rizosfer
sebagian dikontrol oleh sumber hara nitrogen bagi tanaman. Dekomposisi bahan
organik oleh mikroba cenderung meningkatkan kemasaman tanah akibat asam
organik yang dihasilkan (Clark, 2001).
Gaur et al., (1990) menyatakan bahwa fungi yang dapat menyesuaikan diri
dengan kondisi di sekitarnya akan mudah tumbuh dan cepat berkembang biak, dan
jumlahnya akan lebih banyak. Fungi yang pertumbuhannya lambat membutuhkan
waktu inkubasi yang lama untuk berkembang biak. Efektifitas pelarutan fosfat
sangat dipengaruhi oleh pH, suhu, aerasi, materi organik, dan waktu inkubasi.
Fungi pelarut P mampu meningkatkan kadar fosfat terlarut sebesar
24-47% ditanah masam. Jenis jamur yang paling banyak diteliti adalah Aspergillus sp
dan Penicillum sp. Kelompok Penicillum sp mampu melarutkan 26-40% Ca3PO4.
Asam sitrat yang di hasilkan oleh Aspergillus berperan dalam pelarutan Ca-P
(Lestari dan Saraswati, 1997). Peningkatan konsentrasi P tanaman dipengaruhi
oleh fungi pelarut fosfat dalam menghasilkan substrat sebagai sumber nutrisi,
sedangkan P yang terfiksasi dalam mineral tanah dapat dilepaskan sehingga
Diantara fungi penghuni rizosfer, Aspergillus sp. dan Penicillium sp.
merupakan fungi yang umum ditemukan dan telah diketahui memiliki
kemampuan melarutkan P, sehingga kedua jenis cendawan ini berpotensi untuk
dikembangkan sebagai pupuk hayati yang dapat meningkatkan produktifitas
pertanian. Pelarutan P oleh cendawan dilakukan melalui produksi asam organik.
Salah satu spesies Penicillium, yaitu P. bilaii berperan dalam aktivitas pelarutan P
terikat melalui produksi asam sitrat dan asam oksalat. Selain melarutkan P, A.
niger dan Penicillium sp. merupakan jenis cendawan yang ditemukan sebagai
endosimbion pada Ficus bengalensis. Kolonisasi cendawan ini ditemukan di
berbagai organ dengan frekuensi yang berbeda. Mikrob endosimbion adalah
mikrob yang hidup di dalam jaringan tanaman dan mampu membentuk koloni di
dalam jaringan. Mikroba yang dapat meningkatkan ketersediaan hara bagi
tanaman akan lebih efektif jika berada di dalam jaringan tanaman, sebab unsur
hara yang tersedia dapat langsung ditransportasikan ke tanaman
(Cunningham dan Kuiack 1992)
Reddy et al., (2002) menemukan bahwa semua isolat Aspergillus yang
diisolasi dari tanah-tanah yang mengandung rizosfer mempunyai kemampuan
untuk melarutkan semua bentuk batuan fosfat alam. Ini adalah laporan pertama
mengenai pelarutan batuan fosfat dengan Aspergillus dan menunjukkan bahwa
fungi dapat berpotensi sebagai pelarut fosfat yang sangan baik ketika
diinokulasikan ke dalam tanah dimana batuan fosfat digunakan sebagai pupuk P.
Aspergillus mampu meningkatkan ketersediaan P pada tanah sebesar 25% dan
Pada umumnya pertumbuhan fungi dipengaruhi oleh
(Gandjar et al., 2006):
1. Substrat
Substrat merupakan sumber nutrien utama bagi fungi. Nutrien-nutrien baru dapat
dimanfaatkan sesudah fungi mengekskresi enzim-enzim ekstraselular yang dapat
mengurai senyawa kompleks dari substrat tersebut menjadi
senyawa-senyawa yang lebih sederhana.
2. Kelembapan
Faktor ini sangat penting untuk pertumbuhan fungi. Pada umumnya fungi seperti
Aspergillus, Penicillium, Fusarium, dan banyak hyphomycetes lainnya dapat
hidup pada kelembapan nisbi yang lebih rendah, yaitu 80%.
3. Suhu
Berdasarkan suhu kisaran lingkungan yang baik untuk pertumbuhan, fungi dapat
dikelompokkan sebagai fungi psikofril adalah fungi yang dengan kemampuan
untuk tumbuh pada atau dibawah 0-300C. Hanya sebagian kecil spesies fungi yang
psikofril. Fungi mesofil adalah fungi yang tumbuh pada suhu 25-370C, dan
termofil yang mampu tumbuh pada kisaran suhu 40-740C. Fungi dapat tumbuh
baik pada suhu ruangan (22-250C).
4. Derajat keasaman lingkungan
pH substrat sangat penting untuk pertumbuhan fungi, karena enzim-enzim tertentu
hanya akan mengurai suatu substrat sesuai dengan aktivitasnya pada pH tertentu.
Mekanisme pelarutan fosfat
Ketersediaan P-organik bagi tanaman dipengaruhi antara lain oleh
aktivitas mikroba. Namun seringkali hasil mineralisasi oleh mikroba, langsung
bersenyawa dengan bagian-bagian anorganik dalam tanah untuk membentuk
senyawa yang relatif sukar larut. Enzim fosfatase berperan utama dalam
melepaskan P dari ikatan Porganik. Enzim ini banyak dihasilkan oleh mikroba
tanah, terutama yang bersifat heterotrof. Aktivitas fosfatase dalam tanah
meningkat dengan meningkatnya C-organik, tetapi juga dipengaruhi oleh pH,
kelembapan, temperatur, dan faktor lainnya. Dalam kebanyakan tanah, total
P-organik sangat berkorelasi dengan C-organik tanah, sehingga mineralisasi P
meningkat dengan meningkatnya total C-organik. Semakin tinggi C-organik dan
semakin tinggi P-organik, maka semakin meningkat immobilisasi P. P-anorganik
dapat diimmobilisasi menjadi P-organik oleh mikroba (Havlin et al,. 1999).
Pelarutan fosfat secara biologis terjadi karena mikroorganisme tersebut
menghasilkan enzim antara lain enzim fosfat dan enzim fitase. Fosfatase
merupakan enzim yang akan dihasilkan apabila ketersediaan fosfat rendah.
Fosfatase diekskresikan oleh akar tanaman dan mikroorganisme, dan di dalam
tanah yang lebih dominan adalah fosfatase yang dihasilkan oleh mikroorganisme
(Joner, et al., 2000 dalam Suriadikarta dan Simanungkalit, 2006). Pada proses
mineralisasi bahan organik, senyawa fosfat organik diuraikan menjadi bentuk
fosfat anorganik yang tersedia bagi tanaman dengan bantuan enzim fosfatase
(Suriadikarta dan Simanungkalit, 2006).
Mikroba pelarut fosfat mensekresikan sejumlah asam organik seperti
yang mampu membentuk khelat dengan kation-kation seperti Al dan Fe pada
Ultisol sehingga berpengaruh terhadap pelarutan fosfat yang efektif sehingga P
menjadi tersedia dan dapat diserap oleh tanaman (Rao, 1994).
Mikroorganisme tanah berperan penting dalam dinamika dan
ketersediaan P dalam tanah. Komunitas mikroba mempengaruhi kesuburan tanah
melalui proses dekomposisi, mineralisasi, dan penyimpanan/melepaskan nutrisi.
Mikroorganisme mampu meningkatkan ketersediaan P untuk tanaman melalui
mineralisasi P organik di tanah dan membantu melarutkan fosfat. Fungi pelarut
fosfat (FPF) hanya sekitar 0,1–0,5%. Pelarut fosfat yang unggul dari kelompok
fungi adalah Penicillium dan Aspergillus (Whitelaw, 2000).
Cendawan seperti A. niger dan Penicillium sp. telah diketahui
menghasilkan asam-asam organik. Keduanya telah diketahui mampu
menghasilkan asam organik berupa asam oksalat, asam sitrat asam glukonat, dan
asam suksinat. Asam-asam organik seperti asam sitrat, asam suksinat, dan asam
oksalat dapat menggantikan kedudukan anion P, dan mengelat kation-kation
seperti Ca, Al, dan Fe membentuk senyawa kompleks. Keberadaan Al dapat
membuat mobilisasi P di jaringan akar terhambat (Khan et al., 2009)
Mikroba pelarut fosfat juga memiliki kemampuan dalam mensekresikan
enzim fosfatase yang berperan dalam proses hidrolisasi P organik manjadi P
anorganik (Whitelaw, 2000). Beberapa kelompok fungi juga berperan aktif dalam
melarutkan fosfat dalam tanah antara lain Aspergillus sp. dan Penicillium sp.
mampu melarutkan Al-P dan Fe-P. Penicillium sp. mampu melarutkan 40%
Mikroorganisme yang termasuk dalam kelompok jamur antara lain:
Aspergillus sp, Penicillium sp, Zerowilia lipolitika, Pseudomonas sp. Hasil
penelitian menyebutkan bahwa fungi mampu melarutkan P dalam bentuk AlPO4
pada tanah antara 12-162 ppm di medium Pikovskaya yang mengandung sumber
P AIPO4 yang relatif lebih sukar larut sebesar 27-47% (Yuliana, 2010)
Mikroba pelarut fosfat berperanan dalam melarutkan fosfat yang terikat
oleh asam organik dan menjaga unsur P yang terlarut tidak hilang dan terikat oleh
asam organik tanah sehingga dapat tersedia bagi tanaman. Fungi pelarut fosfat
menghasilkan asam organik monokarboksilat seperti asam asetat, asam formiat,
monokarboksil hidroksil seperti asam laktat, asam monokarboksil ketogluconat
(asam oksalat, suksinat dan dikarboksilat hiroksilat sperti asam malat untuk
melarutkan P. Lebih lanjut disebutkan bahwa spesies fungi seperti Aspergillus,
dan Penicillium (Lestari dan Saraswati, 1997).
Secara garis besar, mekanisme mikroba pelarut fosfat dalam mereduksi
fosfat melalui dua tahapan yaitu secara kimiawi dan secara biologis.
1. Mekanisme pelarutan fosfat secara kimia dimulai saat MPF mengekresikan
sejumlah asam organik berbobot molekul rendah hasil metabolismenya ke dalam
tanah. Asam-asam organik tersebut dapat membentuk kompleks stabil dengan
kation-kation pengikat P di dalam tanah seperti Al dan Fe yang merupakan
pengikat P pada tanah masam. Setiap MPF memiliki kemampuan yang berbeda
secara genetik dalam mengekskresikan jenis dan jumlah asam organik. Efektivitas
asam-asam organik yang dihasilkan tergantung pada kondisi lingkungan mikro di
2. Reduksi fosfat secara biologis terjadi karena mikroorganisme tersebut
menghasilkan enzim antara lain enzim fosfatase. Fosfatase merupakan enzim yang
akan dihasilkan apabila ketersediaan fosfat rendah, apabila ketersediaan fosfat
tinggi maka enzim fosfatase kurang berguna atau produksi mikroba untuk
menghasilkan fosfat tidak efektif (Ginting et al., 2006)
Asam-asam organik melarutkan P pada media dan dalam tanah melalui
mekanisme antara lain: kompetisi anion ortofosfat pada tapak jerapan, perubahan
pH media, pengikatan logam membentuk logam organik dan khelat oleh ligan
organik. Terdapatnya asam-asam organik ini dalam tanah sangat penting artinya
dalam mengurangi ikatan P oleh unsur penjerapannya dan mengurangi daya racun
logam seperti aluminium pada tanah masam. Kecepatan pelarut P dari mineral P
oleh asam organik ditentukan oleh: (1) kecepatan difusi asam organik dari larutan
tanah, (2) waktu kontak antara asam organik dan permukaan mineral, (3) tingkat
dissosiasi asam organik, (4) tipe dan letak gugus fungsi asam organik, (5) affinitas
kimia agen pengkhelat terhadap logam dan (6) kadar asam organik dalam larutan
tanah Urutan kemampuan asam organik dalam melarutkan fosfat adalah asam
sitrat > asam oksalat = asam tartarat = asam malat > asam laktat = asam fumarat =
asam asetat. Asam organik yang mampu membentuk komplek yang lebih mantap
dengan kation logam lebih efektif dalam melepas Al dan Fe mineral tanah
sehingga akan melepas P yang lebih besar. Urutan kemudahan fosfat terlepas
mengikuti ukuran Ca
PENDAHULUAN
Latar Belakang
Ketersediaan P dalam tanah pada umumnya rendah. Hal ini disebabkan P
terikat menjadi Fe-fosfat dan Al-fosfat pada tanah masam atau Ca3 (PO4
Sitanggang(2013), Mulyani (2013) dan Suhendra (2013) berhasil
mengisolasi dan menguji fungi pelarut fosfat dari tanah gambut. Fungi kemudian )2 pada
tanah basa. Tanaman tidak dapat menyerap P dalam bentuk terikat dan harus
diubah menjadi bentuk yang tersedia bagi tanaman. Mikroba tanah berperan
dalam beberapa aktivitas dalam tanah seperti pelarutan P terikat oleh sekresi asam,
dan mineralisasi komponen fosfat organik dengan mengubahnya menjadi
bentuk anorganik (Cunningham dan Kuiack, 1992).
Pemberian pupuk fosfat ke dalam tanah sebagian besar tidak tersedia
dalam tanaman, hanya 10% sampai 20% yang mampu diserap atau dimanfaatkan
oleh tanaman. Alternatif lain untuk mengatasi ketersediaan fosfat bagi tanaman
adalah dengan pemberian pupuk hayati yang berisi mikroba tanah. Mikroba
tertentu yang hidup bebas memiliki kemampuan dalam melarutkan fosfat tanah
yang terikat dan fosfat dari pupuk kimia yang terakumulasi, sehingga dapat
dimanfaatkan oleh tanaman (Hasanudin, 2009).
Mikroba pelarut P merupakan salah satu jenis pupuk hayati yang dapat
mengefisiensikan penggunaan pupuk P anorganik, sehingga dapat mengatasi
rendahnya P-tersedia tanah dan meningkatkan konsentrasi P pada tanaman.
Diketahui bahwa Aspergillus sp dan Penicillium sp merupakan spesies jamur yang
menunjukkan bahwa Aspergillus mampu melarutkan fosfat. Kemudian isolat hasil
isolasi fungi pelarut fosfat (FPF) disimpan sebagai koleksi di laboratorium biologi
tanah selama tiga tahun. Hal ini yang menjadi dasar penelitian ini dilakukan yaitu
untuk menguji kembali kemampuan fungi pelarut fosfat dalam melarutkan P
setelah disimpan selama kurun waktu tiga tahun di laboratorium. Penelitian ini
menggunakan empat sumber P yang berbeda yaitu Ca3PO4, AlPO4, FePO4 dan
batuan posfat.
Tujuan Penelitian
Tujuan penelitian adalah untuk menguji kembali kemampuan fungi pelarut
fosfat asal gambut yang di simpan selama tiga tahun di Laboratorium Biologi
Tanah Fakultas Pertanian Sumatera Utara dalam melarutkan P dari berbagai
sumber.
Kegunaan Penelitian
Penelitian diharapkan dapat memberikan informasi tentang kemampuan
fungi pelarut fosfat dalam melarutkan P yang potensial setelah disimpan dalam
kurun waktu tiga tahun.
Hipotesis
Fungi pelarut fosfat yang diisolasi dari tanah gambut diduga masih
memiliki potensi dalam melarutkan P dari berbagai sumber, meskipun telah
ABSTRAK
SUGIARTI SIPAHUTAR: Kemampuan Fungi Pelarut Fosfat Asal Gambut Dalam Melarutkan P dari Berbagai Sumber Setelah Tiga Tahun. Dibawah bimbingan DENI ELFIATI dan DELVIAN.
Ketersediaan P dalam tanah pada umumnya rendah sehingga sebagian besar tidak dapat dimanfaatkan oleh tanaman. Untuk mengatasi ketersediaan fosfat di tanah maka dilakukan pemberian pupuk hayati berupa mikroba pelarut fosfat dan Aspergillus sp diketahui mampu melarutkan fosfat. Penelitian ini dilakukan untuk menguji kemampuan fungi pelarut fosfat yang disimpan selama tiga tahun di Laboratorium. Isolat yang di gunakan adalah hasil isolasi dari tanah gambut yang berasal dari tiga tempat yang berbeda yaitu dari Desa Nagasaribu Kecamatan Lintong Nihuta Kabupaten Humbanghas, tanah gambut dari Dusun XVI Pasar Banjar, Kecamatan Simpang Empat, Tanjung Balai, dan dari Desa Bukkas Malombu Kecamatan Angkola Kabupaten Tapanuli Selatan. Uji potensi fungi pelarut fosfat dilakukan di Laboratorium Biologi Tanah Program Studi Agroekotegnologi Fakultas Pertanian Universitas Sumatera Utara. Pengujian menggunakan media pikovskaya dengan sumber fosfat Ca3PO4, FePO4, AlPO4 dan batuan fosfat. Kemampuan fungi pelarut fosfat secara kuantitatif didasarkan pada nilai indeks pelarutan, sedangakan secara kualitatif didasarkan pada pengukuran potensi fungi pelarut fosfat dalam melarutkan P dengan metode kolorimetri dan Bray II. Hasil penelitian menunjukkan bahwa fungi pelarut fosfat masih berpotensi dalam melarutkan P meskipun adanya penyimpanan selama tiga tahun. Hasil pengukuran kadar fosfat tersedia paling besar dari media Ca3PO4 adalah JS4 sebesar 66,83 ppm, kadar fosfat tersedia paling besar dari media FePO4 adalah JNV3 sebesar 62,39 ppm, kadar fosfat tersedia paling besar dari media AlPO4 adalah JF4 sebesar 54,72 ppm dan kadar fosfat tersedia paling besar dari media batuan fosfat adalah JS6 sebesar 51, 15 ppm.
ABSTRACT
SUGIARTI SIPAHUTAR. The Ability of Phosphate Solubilizing Fungi From Peatlands For Phosphate Dissolving From Various Sources After Three Years Stored. Under academic supervision by DENI ELFIATI and DELVIAN.
Generally, availability of phosphate in the soil is low so most of the phosphate can not be used by plants. To cope the availability of phosphate biological fertilizer made in the form of soil microbial and Aspergillus sp known to be capable of dissolving phosphate. The aim of this research is to test the ability of phosphate solubilizing fungi after three years stored at the Laboratory. Used isolates were isolated from three different peatland, Desa Nagasaribu Kecamatan Lintong Nihuta Kabupaten Humbanghas, peatland of Dusun XVI Pasar Banjar, Kecamatan Simpang Empat, Tanjung Balai, and Desa Bukkas Malombu Kecamatan Angkola Kabupaten Tapanuli Selatan. Potential of phosphate solubilizing fungi was conducted at the Laboratory of Soil Biology, Agroecotechnology, Faculty of Agriculture, University of North Sumatera. Calibration are using pikovskaya media the source phosphate from Ca3PO4,
FePO4, AlPO4 and rock phosphate. The ability of phosphate solubilizing fungi
quantitatively based on the index value of dissolution, while the qualitative is based on measuring the potential of phosphate solubilizing fungi for phosphate dissolving by colorimetric methods and Bray II. Result of this research showed that phosphate solubilizing fungi still potential for phosphate dissolving although after three years stored. The measurement results of most phosphate levels provided of Ca3PO4 media is JS4 amounted to 66.83 ppm, most of phosphate
levels are available of FePO4 media is JNV3 amounted to 62.39 ppm, most of
phosphate levels are available of AlPO4 media is JF4 amounted to 54.72 ppm and
most of phosphate levels provided of rocks phosphate is JS6 amounted to 51, 15 ppm.
ABSTRAK
SUGIARTI SIPAHUTAR: Kemampuan Fungi Pelarut Fosfat Asal Gambut Dalam Melarutkan P dari Berbagai Sumber Setelah Tiga Tahun. Dibawah bimbingan DENI ELFIATI dan DELVIAN.
Ketersediaan P dalam tanah pada umumnya rendah sehingga sebagian besar tidak dapat dimanfaatkan oleh tanaman. Untuk mengatasi ketersediaan fosfat di tanah maka dilakukan pemberian pupuk hayati berupa mikroba pelarut fosfat dan Aspergillus sp diketahui mampu melarutkan fosfat. Penelitian ini dilakukan untuk menguji kemampuan fungi pelarut fosfat yang disimpan selama tiga tahun di Laboratorium. Isolat yang di gunakan adalah hasil isolasi dari tanah gambut yang berasal dari tiga tempat yang berbeda yaitu dari Desa Nagasaribu Kecamatan Lintong Nihuta Kabupaten Humbanghas, tanah gambut dari Dusun XVI Pasar Banjar, Kecamatan Simpang Empat, Tanjung Balai, dan dari Desa Bukkas Malombu Kecamatan Angkola Kabupaten Tapanuli Selatan. Uji potensi fungi pelarut fosfat dilakukan di Laboratorium Biologi Tanah Program Studi Agroekotegnologi Fakultas Pertanian Universitas Sumatera Utara. Pengujian menggunakan media pikovskaya dengan sumber fosfat Ca3PO4, FePO4, AlPO4 dan batuan fosfat. Kemampuan fungi pelarut fosfat secara kuantitatif didasarkan pada nilai indeks pelarutan, sedangakan secara kualitatif didasarkan pada pengukuran potensi fungi pelarut fosfat dalam melarutkan P dengan metode kolorimetri dan Bray II. Hasil penelitian menunjukkan bahwa fungi pelarut fosfat masih berpotensi dalam melarutkan P meskipun adanya penyimpanan selama tiga tahun. Hasil pengukuran kadar fosfat tersedia paling besar dari media Ca3PO4 adalah JS4 sebesar 66,83 ppm, kadar fosfat tersedia paling besar dari media FePO4 adalah JNV3 sebesar 62,39 ppm, kadar fosfat tersedia paling besar dari media AlPO4 adalah JF4 sebesar 54,72 ppm dan kadar fosfat tersedia paling besar dari media batuan fosfat adalah JS6 sebesar 51, 15 ppm.
ABSTRACT
SUGIARTI SIPAHUTAR. The Ability of Phosphate Solubilizing Fungi From Peatlands For Phosphate Dissolving From Various Sources After Three Years Stored. Under academic supervision by DENI ELFIATI and DELVIAN.
Generally, availability of phosphate in the soil is low so most of the phosphate can not be used by plants. To cope the availability of phosphate biological fertilizer made in the form of soil microbial and Aspergillus sp known to be capable of dissolving phosphate. The aim of this research is to test the ability of phosphate solubilizing fungi after three years stored at the Laboratory. Used isolates were isolated from three different peatland, Desa Nagasaribu Kecamatan Lintong Nihuta Kabupaten Humbanghas, peatland of Dusun XVI Pasar Banjar, Kecamatan Simpang Empat, Tanjung Balai, and Desa Bukkas Malombu Kecamatan Angkola Kabupaten Tapanuli Selatan. Potential of phosphate solubilizing fungi was conducted at the Laboratory of Soil Biology, Agroecotechnology, Faculty of Agriculture, University of North Sumatera. Calibration are using pikovskaya media the source phosphate from Ca3PO4,
FePO4, AlPO4 and rock phosphate. The ability of phosphate solubilizing fungi
quantitatively based on the index value of dissolution, while the qualitative is based on measuring the potential of phosphate solubilizing fungi for phosphate dissolving by colorimetric methods and Bray II. Result of this research showed that phosphate solubilizing fungi still potential for phosphate dissolving although after three years stored. The measurement results of most phosphate levels provided of Ca3PO4 media is JS4 amounted to 66.83 ppm, most of phosphate
levels are available of FePO4 media is JNV3 amounted to 62.39 ppm, most of
phosphate levels are available of AlPO4 media is JF4 amounted to 54.72 ppm and
most of phosphate levels provided of rocks phosphate is JS6 amounted to 51, 15 ppm.
RIWAYAT HIDUP
Sugiarti Sipahutar dilahirkan di Hutaraja pada tanggal 15 Mei 1994, anak
kedua dari enam bersaudara dari pasangan Bapak Apet Sipahutar dan Ibu
Megawati Sinaga.
Pada tahun 2006 penulis menyelesaikan pendidikan Sekolah Dasar di SD
Negeri 173144 Silangkitang, pada tahun 2009 menyelesaikan pendidikan di SMP
St. Maria Tarutung, dan pada tahun 2012 menyelesaikan pendidikan di SMA
Negeri 4 Medan. Pada tahun 2012 penulis terdaftar sebagai mahasiswa
Universitas Sumatera Utara, Fakultas Kehutanan, Program Studi Kehutanan,
Minat Budidaya Kehutanan melalui jalur Ujian Masuk Bersama (UMB).
Selama mengikuri perkuliahan, penulis aktif sebagai anggota Rain Forest.
Pada tahun 2014 penulis melaksanakan Praktik Pengenalan Ekosistem Hutan
(P2EH) di hutan mangrove Pulau Sembilan, Kecamatan Pangkalan Susu, pada
tahun 2015 penulis menjadi asisten praktikum Hidrologi Hutan. Penulis juga
melaksanakan Praktik Kerja lapangan (PKL) di Taman Nasional Gunung Merapi
(TNGM) Yogyakarta pada 27 Januari sampai dengan 29 Februari 2016.
Kemudian pada bulan Mei sampai dengan Agustus penulis melakukan penelitian
yang berjudul “ Kemampuan Fungi Pelarut Fosfat Asal Gambut Dalam
Melarutkan P Dari Berbagai Sumber” di bawah bimbingan Dr. Deni Elfiati,
KATA PENGANTAR
Puji dan syukur penulis ucapkan kehadirat Tuhan Yang Maha Esa, karena
rahmat dan karuniaNya penulis dapat menyelesaikan penelitian yang berjudul
“Kemampuan Fungi Pelarut Fosfat Asal Gambut dalam Melarutkan P dari
Berbagai Sumber Setelah Tiga Tahun” ini dengan baik.
Dalam kesempatan ini penulis ingin mengucapkan terima kasih kepada:
1. Kedua orangtua tercinta, Ayahanda Apet Sipahutar dan Ibunda Megawati
Sinaga yang telah memberi dukungan doa,materi dan semangat kepada penulis
dalam menyelesaikan penelitian ini. Serta kepada kakak dan adik tercinta
(Berlian Sipahutar, Herna Sipahutar, Boy Sipahutar, Bangkit Sipahutar dan
Joylin Sipahutar) atas dukungan moril yang diberikan.
2. Ibu Dr. Deni Elfiati, S.P., M.P., selaku dosen penasehat akademik dan dosen
pembimbing yang telah membimbing penulis selama masa perkuliahaan
hingga penyelesaian skripsi. Bapak Dr. Delvian, S.P., M.P. selaku komisi
pembimbing yang telah banyak mengarahkan dan memberikan saran kepada
penulis dalam menyelesaikan penelitian ini.
3. Bapak Dr. Muhdi, S.Hut., M.Si., dan Bapak Dr. Rudi hartono, S.Hut., M.Si
dalam kesediaan menguji, membimbing dan memberikan saran kepada penulis
dalam penyelesaian skripsi ini.
4. Sahabat-sahabatku Monika P Malau, Amalia Nadhila Sembiring, Ervi Utari
Ginting, Pradipta Wijaya, Marnida Uli Lubis, serfi sipahutar, Champion
Marpaung, dan Bimbo yang telah banyak memberikan dukungan moril kepada
5. Program Studi Kehutanan dan Laboratorium Biologi Tanah Fakultas
Pertanian yang telah membantu dalam penyediaan fasilitas yang mendukung
jalannya penelitian.
6. Teman-teman di Program Studi Kehutanan terkhusus stambuk 2012 atas
kebersamaannya selama perkuliaahan dan yang memberikan semangat kepada
penulis.
Penulis masih mengharapkan kritik, saran dan masukan dari pembaca
demi kelancaran penelitian ini. Semoga penelitian ini akan memberikan manfaat
dan menyumbangkan kemajuan bagi ilmu pengetahuan, khususnya di bidang
kehutanan. Akhir kata penulis mengucapkan terima kasih.
Medan, Februari 2017