MEMPELAJARI PERUBANAN AKTIVITAS
AWTIOKSIDAM
DAN LEMAK SELAMA FERMENTASI
DAGING BlJl PICUNG
( Pangiom edule Reinw.)Oleh
ETI
ROMLAHF 24. 0592
1 9 9 2
FAKULTAS TEKNOLOGI PERTANIAN WSTITUT PERTANIAN BOGOR
Eti Romlah. F 24.0592. Mempelajari perubahan aktivitas antioksidan dan leniak selaina fermentasi daging biji picung (Potigi~rt?~ cc[~l/e Reinw.). Di bawah birnbingnn Dedi Fardiaz.
RINGKASAN
Antinksidan merupakan senyawa yang dapat ~ n e n c e ~ a h oksidasi. khususnya oksidasi lemak. Menurut penelitian Meiriyanto (1988) daging biji p i c ~ ~ n g segar dan yang terfer~nentasi mempunyai aktivitas antioksidan yang
berbeda, dimana aktivitas antioksidan daging biji picung terfermentasi lebih
tinggi dibandingkan aktivitas antioksidan daging biji picung segar.
Tujuii~l penelitian ini untuk inempelajari prrubahan aktivitas antioksiclan d a n lelnilk selama fermentasi daging biji picung.
Fermentasi daging biji picung dilakukan dengan tahap-tahap perebusan
daging biji picung segar, penirisan, pemberian abu dapur dan fermentasi biji
picung. Lama perebusan yang dilakukan ada dua taraf yaitu perebusan selama 80
lnenit dan 40 menit. Fermentasi daging biji picung dilakukan di dapur dan di 1;lboratorium dengan Suhu perebusan 99OC. Waktu fermentasi daging hiji picutng
i
rnasing-masing 0, 7, 14, 21, 28, 35, dan 42 hari.
Warna daging biji picung hasil fermentasi b e w e r n a coklat kehitalnan.
senlakin lama fermentasi warnanya semakin gelap. Dernikian juga ekstrak metanol yang dihasilkan beiwarna coklat kehitaman, semakin lama fel-rnentasi
wtrrnanya scmakin gelap. Semakin lama fermenrasi kadar air daging biji pic~lng
srmaltin I-endah. I<adai- air daging biji picung hasil fermrntasi di dajxtr dengan lama perehusan*kO menit denyan lama fermentasi no1 hari sarnpai 42 hari masing- inasing 55.11%: 71.62%, 57.45%, 51.41%. 60.13%,55.75%, dan 41.74%. I<adar
air daging hiji picung yang direbus selama SO menit. difermentasi di laboratorium p t ~ d ; ~ hari ke no1 sampai hari 42 masing-masing 5S.72%, 61.49%> 56.29%. 57.35%.
menit, ciifermentasi d:cpur. fel-tnentasi s e l a ~ n a no1 hi~ri sampai 42 I masing- masing nilainya 60.56%. 73.04Yo. 59.31'%, 53.70%. 01.13%. 51.63%. dan 38.00%.
Kadar air ciilging biji picung yang direbus selama 40 menit difermentasi tli
l a b o r a t o r i t ~ ~ n dengan lama fel-mentasi no1 hari sampai 42 hari masing-masing nilainya 56.09%;;, 54.25%: 65.78%> 61.77%. 58.29%,42.79%, dan 62.64% pada hari ke 42. Kadar air dipengaruhi secara nyata oleh lamanya prrebusan dan lamanya fermentasi, tetapi tidak dipengaruhi secara nyata oleh tempat fermentasi.
Faktor protektif selama fermentasi daging biji picung mengal>ilni
peningkatan. Untuk perebusan selilma 80 menit dan tempat fermentasi di dapur
dengt~n lama fermentasi no1 hari si~rnpai 42 hari masing-masing adalah 1.57. 1.99:
1.85. I . 1.75. 3.17. dan 2.92. Faktor protektifdaging biji picung dengan lamil p e r e h u s ; ~ ~ ~ 80 inenit. tempat fermentasi di laboratorium untuk masing-masing lama fe1.1nenrasi no1 hari sampai 42 hari adalah 1.75, 1.34, 2.51. 2.62. 1.85, 1.26
dan 2.88. Faktor prorektif daging biji picung yang dit'ermentasi selama no1 hac-i
s;~mpai 42 hari pada perebusan selama 40 menit dengan tempat fermentilsi di
~I:IPLII- clan di lal>oratorium masing-masing 1.36. 1.68. 1.84. 2.09. 1.30 1.77. 1.94
i
dan 1 . 0 1.51. 1.25. 1.63, 1.90, 3.06, 1.66. Faktor protektif dipengaruhi st-cara nyata oleh lalnanya perebusan, tempat fermentasi dan lamanya fermentasi.
Kadar lemak daging biji picung dipengaruhi secara nyata oleh lama
perebus:ln. tempat dan lama fermentasi. Nilai kadar lemak daging biji picung
direbus selicrna SO menit difermentasi di dapur, direbus selama 80 menit
clifel-lnelitasi di lahoratoriurn. direh~ls sflama 40 menit difermentilsi di d a p i ~ r . dan
clirebus s e l a ~ n a 40 rnenit clifet-nlentasi di labol-atorium herticrut-turut aclalah
47.71%. 44.94C~;. -3.?.lOC,k. 53.23%. 42.00%. 38.78%. 2S.55%, d i ~ n 44.66%, 40.')6%, 3 5 51.41%. 37.81%. 34.63%. 28.69% dan 44.85%: 36.75%. 44.03%, 49.65%. 41.07C;;. 25.SS5;. 47.70C;; sertil 44.-35%. 44.84%> 35.01%. 55.56%, 27.17%:
e
Faktol- [,I-otektif ekstrak metitnol dagi~ig hiji picung yang clifel-tiientasi cli diipur lebili tinggi dibiinding ysng difertnent:~si cli lal~o~.;~toric~m. ~1etiiiki;tn J L I ~
faktor l?~-otektif ekstl-;ik metanol daging biji picung 1i:lsil fel-mentasi deng;in l i i ~ i i ; ~
1xrebils;in $0 nirnit lrllili tinggi clihaliding lania pert.h~~s:rn 10 ~ n e n i t . K ~ c I ~ I -
leln;~lc ~ 1 1 1 t l 1 k s c i i i ~ ~ i i prrl;iku;ln dari 1ii11-i kc nol si~mpai Iitiri ke 14 ~ i i r n ~ : ~ I ; i ~ i i i
INSTITUT PERTANIAN BOGOR
FAKULTAS TEKNOLOGI PERTANIAN
MEMPELAJARI PERUBAMAN AKTIVITAS ANTIOKSIDAN
DAN LEMAK SELAMA FERMENTASI
DAGING BIJI PICUNG (~rcl~~ilon
ed~rle Reinw.)SKRIPSI
s e b i ~ g ~ i salah satu s p r a t u n r u k memperoleh gelai
SARJANA TEKNOLOGI PERTANTAN
pada Jurusan Teknologi Pangan dan Gizi
Fakultzts teknologi Pertanian
Institut Pel-tanian Bogor
OIeh
ETI ROMLAH
KATA PENGANTAR
Puji syukur penulis panjatkan ke hadirat Tuhan Yang
Mahaesa yang telah memberikan rahmat dan anugerahNya
sehingga skripsi ini dapat tersusun.
Skripsi ini disusun sebagai salah satu syarat untuk
memperoleh gelar Sarjana Teknologi Pertanian pada Jurusan
Teknologi Pangan dan Gizi, Institut Pertanian Bogor.
Pada kesempatan ini penulis mengucapkan banyak
terimakasih kepada:
1. Bapak Dr. Ir. Dedi Fardiaz, MSc. selaku dosen pembim-
pembimbing yang telah memberikan bimbingan selama
penelitian sampai tersusunnya skripsi ini.
2. Ibu Dr. Ni Luh Puspitasari, MSc. dan Ir. Nuri Andarwu-
lan yang telah turut menguji skripsi ini.
3. Bapak clan Mamah yang selalu berdoa untuk kemajuan putri-
putrinya.
4. Ceu Enung dan Bang Cius yang telah memberikan bantuan
serta dorongan moril sehingga penulis dapat menyele-
saikan skripsi ini.
4. Ibu Ing Mokoginta, ibu Effionora yang telah banyak
memberikan bimbingan, dorongan dan bantuan selama
penelitian ini.
5. Bapak Hasan Basri, Syarifah dan ~ i e s t a yang telah ba-
nyak memberikan bantuan selama penelitian ini.
penulis menyadari bahwa tulisan ini masih jauh dari
sempurna, oleh karena itu kritik dan saran yang membangun
dari pembaca sangat penulis harapkan guna penyempurnaan
selanjutnya.
Akhirnya penulis mengharapkan semoga skripsi ini
dapat bermanfaat bagi yang memerlukannya.
DAFTAR IS1
Halaman
KATA PENGANTAR
...
iDAFTAR IS1
...
iii...
DAFTAR GAMBARv
DAFTAR LAMPIRAN...
viiI
.
PENDAHULUAN...
1I1
.
TINJAUAN PUSTAKA...
3A
.
BOTANI PICUNG...
3B
.
KOMPOSISI DAN DAYA GUNA PICUNG...
6C
.
OKSIDASI...
10D
.
ANTIOKSIDAN...
14E
.
FERMENTASI...
18I11
.
BAHAN DAN METODE PENELITIAN...
21A
.
BAHAN DAN ALAT...
211
.
Bahan...
i 21 2.
Alat...
21B
.
METODE PENELITIAN...
221
.
Perlakuan Fermentasi...
222
.
Kadar Air (A.O.A.C., 1971)...
263
.
Kadar Lemak (Fardiaz et al.. 1986)..
2 7 4.
Pemisahan Asam Lemak Bebas...
(Fardiaz et al.. 1986) 28 5.
Esterifikasi Asam Lemak Bebas (Fardiaz et al.. 1986)...
286
.
Analisis Asam Lemak Bebas denganHalaman
7
.
Ekstraksi Antioksidan dengan Metanol(Hammerschmidt. 1 9 7 8 )
...
2 98
.
Pengukuran Aktivitas ~ n t i o k s i d a n(Taylor dan Richardson. 1 9 8 0 )
...
3 0C
.
MODEL RANCANGAN PERCOBAAN...
3 2A
.
FERMENTASI DAGING BIJI PICUNG( P a n q i u m edule Reiwn.)
...
36B
.
KADAR AIR...
37C
.
EKSTRAKSI ANTIOKSIDAN DAN PENGAMATANAKTIVITASNYA
...
4 0...
D
.
LEMAK DAN ASAM LEMAK 48V
.
KESIMPULAN DAN SARAN...
5 5..
A
.
KESIMPULAN...
5 5B
.
SARAN...
5 6LAMPIRAN
...
G0DAFTAR GAMBAR
Halaman
Gambar 1.
Gambar 2.
Gambar 3.
Gambar 4.
Gambar 5.
Gambar 6.
Gambar 7.
Gambar 8. Gambar 9. Gambar 10. Gambar 11. Gambar 12. Gambar 13. Gambar 14. Gambar 15. Gambar 16.
Daun picung
...
5Buah picung
...
6Struktur kimia asam hidnokarpat (A),
asam khaulmograt (B) dan asam gorlat
. . . .
(C) (Hilditch dan Williams, 1964) 9
Skema umum oksidasi lemak (Nawar,
1985)
...
12Rumus struktur paradifenol dan ortodi-
fen01 (Winarno et al., 1980)
...
15~ e a k s i antioksidan dengan gugus fenol
dan amina aromatik dengan radikal pe-
roksida (Ranney, 1979)
...
16Reaksi antara radikal antioksidan
dengan radikal peroksida (Ranney,
1979)
...
17Reaksi ion logam yang terlibat dalam
proses oksidasi (Ranney, 1979)
. . .
18Diagram alir perlakuan fermentasi da-
ging biji picung
...
2 3Drum dan gas burner zepplin untuk
perebusan daging biji picung segar
..
24Penirisan dan pendinginan daging biji
picung yang telah direbus
...
25Abu dapur (A) dan biji picung siap di-
...
fermentasi 25
Fermentasi daging biji picung
. . .
2 6Diagram alir metode ekstraksi daging biji picung yang larut dalam metanol
(modifikasi metode Hammerschmidt, 1978) 3 2
Oksigenmeter
...
3 4Halaman
Gambar 17
Gambar 18.
Gambar 19.
Gambar 2 0.
Gambar 21.
Gambar 22.
Gambar 23.
Gambar 24.
Gambar 25.
Gambar 26.
Gambar 27
Daging biji picnug hasil fermentasi 0,
14, 28 dan 4 2 hari yang telah dikering
bekukan (menurut arah jarum jam)
...
37Grafik hubungan antara kadar air dengan
lamanya fermentasi daging biji picung 3 9
Pembentukan malonaldehid dari hasil ok- sidasi asam lemak tidak jenuh (Nawar,
1985)
...
43Pengukuran faktor protektif
...
44Reaksi asam linoleat dengan BHT (Nawar,
1985)
...
45Hubungan nilai faktor protektif dengan lamanya fermentasi
. . .
47Hubungan kadar lemak dengan lamanya
...
fermentasi 49
Distribusi asam lemak bebas dari daging biji picung hasil fermentasi di dapur
dan lama perebusan 80 menit
...
53Distribusi asam lemak bebas dari daging biji picung hasil fermentasi di dapur
dan lama perebusan 40 menit
...
53Distribusi asam lemak bebas dari daging biji picung hasil fermentasi di lab dan
lama perebusan 80 menit
...
54Distribusi asam lemak bebas dari daging biji picung hasil fermentasi di lab dan
DAFTAR LAMPIRAN
Halaman
Lampiran 1.
Lampiran 2a.
Lampiran 2 b .
Lampiran 2c.
Lampiran 2d.
Lampiran 2e.
Lampiran 3a.
Lampiran 3b.
Lampiran 3c.
Lampiran 3d.
Lampiran 3e.
Lampiran 4a.
Lampiran 4 b .
Lampiran 4 c .
Lampiran 4d.
Rekapitulasi data analisis fermentasi
daging biji picung
...
6 1Daftar sidik ragam pengukuran kadar
air
...
62Uji BNJ interaksi AxB pada pengukuran
kadar air
...
62Uji BNJ interaksi AxC pada pengukuran
kadar air
...
6 3Uji BNJ interaksi BxC pada pengukuran
kadar air
...
6 3Uji BNJ interaksi AxBxC pada penguku-
ran kadar air
...
64Daftar sidik ragam pengukuran faktor
protektif
...
65Uji BNJ interaksi AxB pada pengukuran
faktor protektif
...
65Uji BNJ interaksi AxC pada pengukuran
faktor protektif
...
6 6Uji BNJ interaksi BxC pada pengukuran
faktor protektif
...
66Uji BNJ interaksi AxBxC pada penguku-
ran faktor protektif
...
6 7Daftar sidik ragam pengukuran kadar
lemak
...
68Uji BNJ interaksi AxB pada pengukuran
kadar lemak
...
6 8Uji BNJ interaksi AxC pada pengukuran
kadar lemak
...
69Uji BNJ interaksi BxC pada pengukuran
Halaman
Lampiran 4e. Uji BNJ interaksi A x B x C pada penguku-
ran kadar lemak
...
7 0Lampiran 5. Hasil analisis aktivitas antioksidan
dengan menggunakan alat oksigen meter 71
Lampiran 6a. Distribusi asam lemak bebas hasil
analisis dengan alat kromatografi gas 72
Lampiran Gb. Kromatogram asam lemak standar I
....
- 1 3-
Lampiran Gc. Kromatogram asam lemak standar I1
...
7 4Lampiran Gd. Kromatogram asam lemak standar I11
..
7 5I. PENDAHULUAN
Antioksidan merupakan senyawa yang dapat mencegah
oksidasi lemak. Antioksidan dewasa ini telah banyak
digunakan untuk berbagai jenis makanan yang mengandung
lemak, baik antioksidan alami maupun buatan. Menurut
Ketaren (1986) antioksidan untuk bahan pangan harus
memenuhi persyaratan tertentu yaitu: (1) tidak beracun dan
tidak mempunyai efek fisiologis, (2) tidak menimbulkan
flavor yang tidak enak, rasa dan warna pada minyak atau
bahan pangan, (3) larut sempurna dalam minyak atau lemak,
(4) efektif dalam jumlah yang relatif kecil (menurut Food
& Drug Administration dosis yang diizinkan adalah 0.01 -
0.1%), dan (5) tidak mahal serta selalu tersedia.
Antioksidan yang sering dipergunakan dalam bahan
pangan umumnya berasal dari alam (natural antioksidan),
misalnya dsam sitrat, askorbat, tartarat, dan malat serta
lesitin. Perhatian kepada antioksidan alami semakin
meningkat dikarenakan berbagai alasan, antara lain: (1)
bahan alami diduga lebih aman daripada bahan sintetik, (2)
untuk menghindari bahan sintetik yang belum terjamin
keamanannya
,
(3) untuk menurunkan biaya, (4) untukmendapatkan sifat karakteristik yang sesuai dengan
keinginan (Dugan, 1980).
Banyak antioksidan alami yang telah ditemukan dari
bahwa ekstrak metanol panas dari Spanish peanut mempunyai
aktivitas antioksidan karena mengandung dihidroquersetin
(taxifolin). Houlihan et al. (1964) berhasil mengisolasi
dan mengidentifikasi senyawa antioksidan dalam daun
Rosmarinus officinalis L. sebagai rosmaridifenol yang
merupakan diterpendifenol. Pada pengujian memakai lemak
babi ternyata rosmaridifenol tersebut aktivitasnya lebih
besar daripada BHA (butylated hydroxyanisole). Satu tahun
kemudian Houlihan et al. berhasil mengisolasi dan
mengidentifikasi senyawa antioksidan lain dari daun
Rosmarinus officinalis L. sebagai rosmariquinon
(C19H2202). Taga et al. (1978) melaporkan bahwa ekstrak
metanol dari Chia seeds mempunyai potensi antioksidan.
Menurut penelitian Meiriyanto (1988) komponen yang
terdapat dalam biji picung (Pangium edule Reiwn.) sebelum
dan sesudah fermentasi memiliki sifat aktivitas
I
antioksidan sehingga dapat mencegah oksidasi bahan pangan.
Panghegar (1990) mengisolasi komponen antioksidan alami
dari daging biji picung, dan Adidjaja (1991) menganalisis
aktivitas antioksidan alami dari daginq biji picung pada
minyak kelapa. Penelitian ini dimaksudkan untuk
mengetahui perubahan antioksidan dan komponen lemak pada
11. TINJAUAN PUSTAKA
A . B O T A N I P I C U I j G ( P a n g i u m e d u l e R e i n w . )
Nama P a n g i u m j e l a s b e r a s a l d a r i b a h a s a ' i e l a y u
P a n g i ; s e d a n g e d u l e b e r a s a l d a r i k a t a l a t i n e d e r e y a n g
b e r a r t i c a k a n d a n e d u l e b e r a r t i d a p a t d i m a k a n
( S u g i a n t o , 1 9 8 4 ) .
P i c u n g ( P a n q i u m e d u l e R e i n w . ) m e m p u n y a i nama
d a e r a h , s e p e r t i B a t a k : P a n g i ( D a i r i ) , H a p e s o n g ( T o b a ) -
I n d o n e s i a : K a p a y a n g , P a n g i ( M e l a y u ) , P u c u n g ( J a k a r t a ) -
M i n a n q k a b a u : K a p a y a n g , K a p e n c u e n g , K a p e c o n g , S i m a u n y -
L,avpunq: Kayu t u b a h b u a h - S u n d a : P a c u n y , P i c u n g - J a v a :
Pakem t u ) , P u c u n g - M a d u r a : P a k e m - B a l i : P a n g i -
Sumbawa: K a l o w a - B u g i s : P a n g i - T a n i m b a r : N a g a f u ( H e y n e ,
1 9 8 7 ) .
P i c u n g ( P a n g i u m e d u l e R e i w n . ) t e r m a s u k d a l a m j e n i s
t a n a m a n D i c o t y l e d o n a e ( t a n a m a n b e r k e p i n g d u a ) d a r i
d i v i s i S p e r m a t o p h y t a d e n g a n s u b d i v i s i A n g i o s p e r m a e
( t u n b u h a n b e r b i j i t e r t u t u p ) d e n g a n o r d o P a r i e n t a l i s ,
f a m i l i F l a c o u r t i a c e a e , g e n u s P a n g i u m d a n s p e c i e s P a n g i -
urn e d u l e R e i n w . ( B a c k e r d a n B r i n k
,
1 9 6 3 ) .M e n u r u t K o o r d e r s d a n V a l e t o n y a n g d i k u t i p o l e h
I l e y n e (19;-) p o h o n p i c u n y t i n g g i n y a s a m p a i 4 0 a d a n h e s a r b a t a n c j n y a ( d e n ~ ~ a n b a n i r - b a n i r ) 2 . 5 0 m, t e i - s e b a r
d i s e l u r u h T J u s a n t a r a . P o h o n i n i t e r d a p a t t u m b u h l i a r
l a u t - c l i J a w a B a r a t b i a s a n y a h a n y a t u m b u h t e r p e n c a r -
d i t a n a m t e r u t a m a d i d a e r a h - d a e r a h b u k i t r e n d a h .
M e n u r u t M a n g o n t a n e t a l . ( 1 9 2 5 ) t a n a m a n p i c u n g d a p a t t u m b u h p a d a b e r b a g a i k o n d i s i t a n a h , b a i k d i d a e r a h
p i n g g i r a n s u n g a i , d a e r a h h u t a n j a t i , t a n a h y a n g k e r i n g
maupun t e r g e n a n g a i r , t a n a h b e r l e m p u n g d a n k a d a n y -
kaclang p d d a t a n a h y a n y b e r b a t u , d e n g a n 3 0 0 - 1 0 0 0 m d i .
a t a s p e r n u k a a n l a u t . Tanaman i n i d a p a t m e n j a d i b e s a r
d e n g a n d i a m e t e r b a t a n g d a p a t m e n c a p a i 2 . 5 m d a n t i n g g i m e n c a p a i 4 0 n .
D i b a g i a n p u n c a k p o h o n p i c u n g b a n y a k t e r d a p a t c a b a n g , d a n c a b a n g y a n g m a s i h mudah b e r b u l u . X u l i t
k a y u b e r w a r n a c o k l a t k e m e r a h a n a t a u a b u - a b u k e c o k l a t a n ,
l i c i n d a n k a d a n g - k a d a n g k a s a r d e n g a n b a n y a k c e l a h y a n g
m e n g e r a s ( K e n g , 1 9 6 9 )
.
M a n g o n t a n e t a l . ( 1 9 8 5 ) m e l a p o r k a n bahwa d a u n
p i c u n g t e r k u n p u l p a d a u j u n g r a n t i n g , b e r t a n g k a i p a n j a n g
pacla p o h o n n u d a h e r l e k u k t i g a , p a d a p o h o n t u a b u l a t
t e l u r l e h a r d e n g a n p a n g k a l y a n g t e r p a n c u n g a t a u b c r h e n -
t u k j a n t u n g , m e r u n c i n y , m e n g k i l a t d a n b e r w a r n a h i j a u
t u a , t u l a n g d a u n p a d a s i s i bawah m e n o n j o l . Daun p i c u n g
d a p a t d i l i h a t p a d a Gambar 1.
M e n u r u t B u r k i l ( 1 9 3 5 ) p o h o n p i c u n g s e j a k b e r u m u r
1 5 t a h u n b e r k x ~ a h t e r u s m e n e r u s s e p a n j a n g m u s i m . Buah
a g a k t i d a k s i v e t r i s , b e r h e n t u k b u l a t t e l u r d e g a n k e d u a
Gambar 1. Daun picung
Ukuran buah picung bervariasi dengan panjang 17-30 c m
dan lebar 7-10 cm atau lebih. Kulit buah berwarna
coklat kemerahan dengan permukaannya kasar dimana
terdapat ientisel. Tangkai buah berukuran panjang 8-15
cm denqan diameter 7-12 mm. Sugianto (1984) mengatakan
di dalam buah picung apabila sudah masak panjangnya
dapat mencapai 25 cm terdapat kira-kira 20 biji yang
. .
Gambar 2. Buah picung
B. KOMPOSISI DAN DAYA GUNA PICUNG
Picung pada umumnya dikonsumsi dalam bentuk hasil
fermentasi, yang disebut kluwak. Komposisi kluwak,
dapat dilihat pada Tabel 1.
Tabel 1. Komposisi gizi Kluwak setiap loog*)
Komponen Jumlah
Kalori (xal) 273.0
Protein (9) 10.0
Lemak (9) 24.0
Karbohidrat (g) 13.5
Kalsium (mg) 40.0
~ o s f or (m9) 100.0
Besi (mg) 2 . 0
Vit A (SI) 0.0
Vit C (mg) 30.0
Vit B1 (mg) 0.15
Air (9) 51.0
Bdd ( % ) 80.0
* ) Daftar Komposisi Bahan Makanan, Dir. Gizi
Menurut Sugianto (1984) baik daun, biji maupun bagian-bagian lainnya dari tanaman picung beracun. Hal
ini disebabkan oleh senyawa glikosida yang ada di
dalamnya, yaitu.ginokardin (C13HlgOgN). Karena penga-
ruh enzim ginokardase, maka senyawa tersebut mengalami
hidrolisis, dengan membebaskan HCN, seperti reaksi
berikut ini:
C H 0 N
+
H20-
C6H804+
CfHk206+
HCNgEok&Zin keton g u osa
Ginokardin glukosida dan enzim ginokardase seka-
rang masing-masing dikenal dengan nama sianogenik
glukosida dan enzim glukosidase (Muchtadi, 1989).
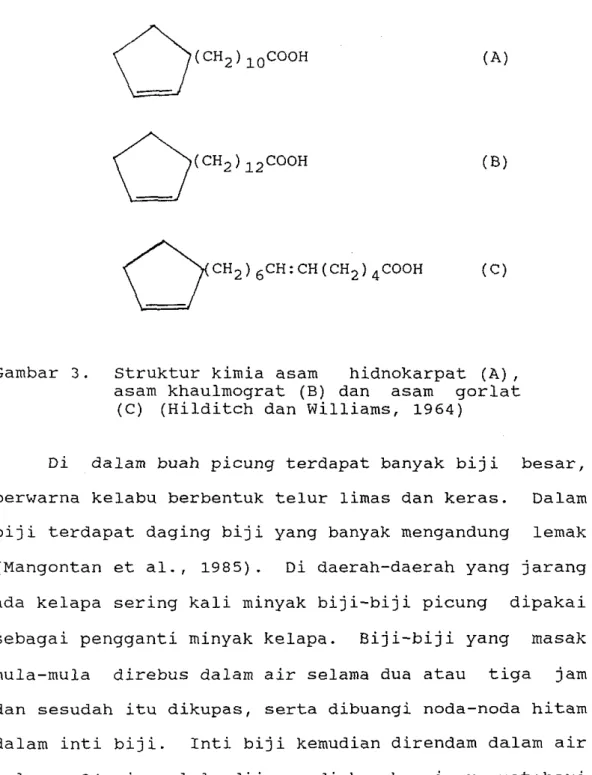
Menurut Hilditch dan Williams (1964) lemak biji
picung apabila diasamkan akan menghasilkan lemak siklik
yang tidak jenuh yaitu asam hidnokarpat (C16H2802) dan
asam khaulmograt (C18H3202), atau asam Z-siklopentena-
1-undekanoat dan asam 2-siklopentena-1-tridekanoat.
Asam gorlat (C18H3002) yang jumlahnya lebih sedikit
daripada kedua asam lemak di atas dalam kondisi
tertentu menyertai kedua asam lemak lainnya. Struktur
kimia asam hidnokarpat, asam gorlat dan asam
khaulmograt dapat dilihat pada Gambar 3. Asam lemak
siklik ini mempunyai sifat anti bakteri dengan keis-
timewaan mampu mengobati lepra, kudis dan beberapa
Menurut Rumphius yang dikutip oleh Heyne (1987)
kulit kayu pohon ini yang diramas-ramas dan ditaburkan
di perairan akan mematikan ikan, oleh sebab itu dipakai
sebagai tuba ikan. Demikian juga daunnya dapat dipakai
dengan cara yang sama untuk menangkap udang tanpa
membahayakan kesehatan, kemudian udang tersebut dapat
dimakan. Jika sepotong daging yang terdapat ulat di
dalamnya itu konon dibungkus dalam daun ini maka ulat-
ulat itu akan keluar dan mati.
Menurut Vorderman yang dikutip oleh Heyne (1987)
di Banten biji picung yang dicincang halus dan dijemur
selama 2-3 hari dipakai untuk mengawetkan ikan. Ikan
laut yang baru ditangkap yang berukuran sedang, diber-
sihkan perutnya di pantai oleh para pembeli dan setelah
itu rongga badannya diisi dengan cincangan tadi. Pada
dasar keranjang angkutan ikan dihamp.arkan selapis
cincangan biji picung dan di atasnya diatur selapis
ikan; lapisan ikan ini ditutupi dengan selapis cin-
cangan biji picung, di atasnya dipasang lagi selapis
ikan dan seterusnya sampai keranjang terisi penuh.
Untuk pengangkutan berjarak jauh maka para penjualnya
kadang-kadang menggunakan satu bagian qaram dan tiga
bagian picung, akan tetapi kadang-kadang hanya memakai
Gambar 3. Struktur kimia asam hidnokarpat (A), asam khaulmograt (B) dan asam gorlat
(C) (Hilditch dan Williams, 1964)
Di dalam buah picung terdapat banyak biji besar,
berwarna kelabu berbentuk telur limas dan keras. Dalam
biji terdapat daging biji yang banyak mengandung lemak
(Mangontan et al., 1985). Di daerah-daerah yang jarang
ada kelapa sering kali minyak biji-biji picung dipakai
sebagai pengganti minyak kelapa. Biji-biji yang masak
mula-mula direbus dalam air selama dua atau tiga jam
dan sesudah itu dikupas, serta dibuangi noda-noda hitam
dalam inti biji. Inti biji kemudian direndam dalam air
selama 24 jam, lalu dijemur di bawah sinar matahari
sehingga minyaknya keluar jika dipijit dan akhirnya
dikempang. Jika minyak tidak disimpan dalam botol yang
terisi penuh niscaya akan cepat menjadi tengik. Untuk
dipanaskan dan dikerinqkan terlebih dahulu serta
selanjutnya dijaqa agar minyaknya itu janqan sampai
banyak terguncang dan dipanaskan dua hari sekali
(Heyne, 1987).
Menurut Vorderman yang dikutip oleh Heyne (1987)
juqa menqemukakan bermacam cara untuk dapat memakan
bijinya. Biji tadi dengan sendirinya harus dibebaskan
dari sianida yanq beracun. Cara yanq dilakukan adalah
sebagai berikut: buahnya yang masak dan jatuh dengan
sendirinya disimpan selama 10-14 hari sehinqqa buahnya
menjadi busuk. Kemudian bi j i-bi j inya dipisahkan,
dicuci dan direbus cukup lama. Setelah dingin biji-
biji ini diselaputi abu dan ditumpuk dalam lubang luar
rumah, lubang tadi ditutupi dengan daun pisanq dan
ditimbuni tanah. Biji-biji itu dibiarkan terkubur
selama 40 hari, sesudah itu digali keluar dan setelah
dicuci bersih dibawa ke pasar untuk dijual sebaqai
kluwak. Isinya berwarna coklat berlemak dan licin,
rasanya tidak enak, akan tetapi untuk pindanq dan
samba1 sebagai lauk nasi, kluwak sangat digemari.
C. OKSIDASI
Kerusakan oksidatif pada bahan makanan yanq menqan-
dung lemak merupakan masalah yanq pentinq karena dapat
bahkan produk teroksidasi dapat beracun. Sebaliknya,
oksidasi lemak pada batas tertentu kadang-kadang di-
inginkan, seperti pada keju khusus dan aroma pada
makanan yang digoreng (Nawar, 1985). Kerusakan lemak
yang utama adalah timbulnya bau dan rasa tengik yang
disebut proses ketengikan. Hal ini disebabkan
oleh autooksidasi radikal asam lemak tidak jenuh
dalam lemak (Winarno, 1988).
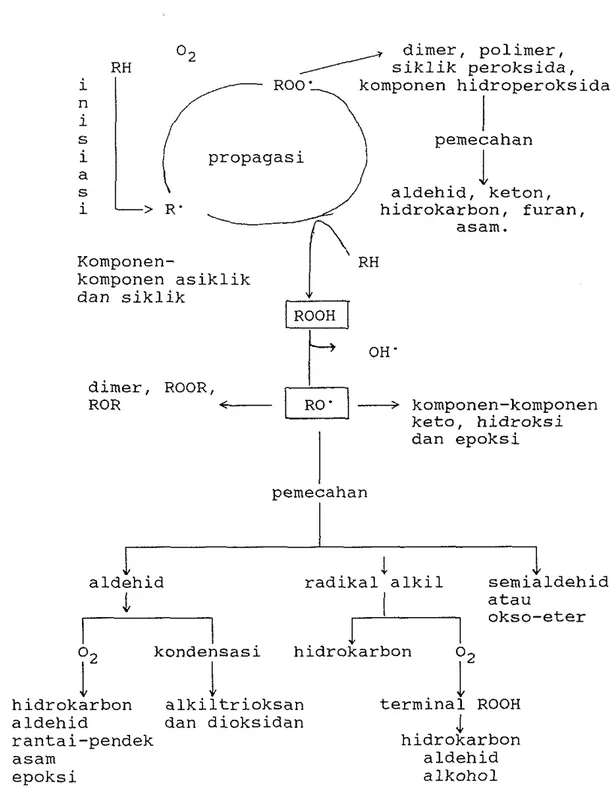
Menurut Nawar (1985) mekanisme oksidasi pada lemak
terdiri dari tiga tahap yaitu inisiasi (pembentukan
peroksida), propagasi (dekomposisi peroksida) dan
terminasi (penghentian reaksi). Skema umum oksidasi
lemak secara jelas dapat dilihat pada Gambar 4. Menurut
teori yang sampai kini masih dianut orang, sebuah atom
hidrogen yang terikat pada suatu atom karbon yang
letaknya di sebelah atom karbon lain yang mempunyai
ikatan rangkap dapat disingkirkan oleh sudtu kuantum
energi sehingga membentuk radikal bebas. Kemudian
radikal ini dengan O 2 membentuk peroksida aktif
yany dapat membentuk hidroperoksida yang bersifat
sangat tidak stabil dan mudah pecah menjadi senyawa
dengan rantai karbon yang lebih pendek oleh energi yang
lebih tinggi, energi panas, katalis logam, atau enzim.
Senyawa-senyawa dengan'rantai karbon yang lebih pendek
O 2 dimer, polimer,
RH
/
siklik peroksida,komponen hidroperok&ida
i
I
s pemecahan
s aldehid, keton,
1
i hidrokarbon, furan,
asam.
Komponen-
komponen asiklik dan siklik
[ROOHI
I
t-'
OHdimer
,
ROOR,ROR +
&]
---+
komponen-komponen keto, hidroksiI
dan epoksipemecahan
I
1
aldehid radikal alkil
1
semialdehidJ
.
4
atauI---!
11
okso-eterO2 kondensasi hidrokarbon
I
I
i2
4, .L
hidrokarbon alkiltrioksan terminal ROOH 4,
aldehid dan dioksidan
rantai-pendek hidrokarbon
.1
asam aldehid
epoks i alkohol
yang bersifat folatil dan menimbulkan bau tengik pada
lemak (Winarno et al., 1988). Menurut Labuza (1971)
yang dikutip oleh Ragnarsson et al. (1977) reaksi
oksidasi yang terjadi pada lemak tidak jenuh dapat
menyebabkan hilangnya asam lemak esensial, pemecahan
beberapa vitamin dan pigmen, dan dapat pula menurunkan
nilai biologis protein.
Adanya panas dapat merangsang atau menstimulir
reaksi oksidasi. Semakin tinggi suhu kecepatan oksida-
si akan semakin bertambah. Sinar juga dapat memperce-
pat oksidasi, sinar ultra violet lebih aktif dalam
mempercepat oksidasi daripada sinar-sinar tampak
(visible light) karena sinar ultra violet mempunyai
panjang gelombang yang lebih kecil sehingga energinya
lebih besar (Winarno et al., 1980).
Menurut Stuckey (1977) jalannya autooksidasi lemak
dan hasil produk akhirnya tergantung pada besarnya
tingkat kondisi yang sedang berlangsung seperti
temperatur, katalis, jenis asam lemak, distribusi dan
bentuk geometri ikatan rangkap dan jumlah oksigen
tersedia. Dan Winarno et al. (1980) mengatakan kece-
patan oksidasi lemak tergantung dari jenis asam
lemaknya, adanya antioksidan, adanya prooksidan
(katalis) dan faktor-faktor lainnya. Beberapa Zat
kimia seperti ozon, peroksida, serta logam-logam
dapat mempercepat oksidasi lemak. Beberapa enzim
tertentu, misalnya lipoksidase juga dapat bertindak
sebagai katalis dalam reaksi oksidasi lemak.
D. ANTIOKSIDAN
Kata antioksidan digunakan pada semua senyawa
yang dapat mencegah reaksi oksidasi tanpa memperhatikan
mekanismenya. Lebih jauh lagi, terminologi antioksidan
pangan sering digunakan untuk menunjukkan komponen yang
dapat mengganggu rantai reaksi radikal bebas yang
terlibat dalam reaksi oksidasi lemak (Lindsay, 1985)
dalam tulisan ini yang dimaksud antioksidan adalah zat
yang dapat memperlambat atau mencegah reaksi autooksi-
dasi pada lemak. Winarno et al. (1980) mengatakan
antioksidan adalah senyawa yang biasanya mengandung
orto atau para difenol, seperti terlihat pada Gambar 5.
Menurut Winarno (1988) antioksidanqdibagi menjadi
antioksidan primer dan antioksidan sekunder. Antioksi-
dan primer adalah suatu zat yang dapat menghentikan
reaksi berantai pembentukan radikal yang melepaskan
radikal hidrogen, seperti tokoferol, lesitin, fosfati-
da, sesamol, gosipol, asam askorbat, BHT, PG dan NDGA.
Antioksidan sekunder adalah suatu zat yang dapat mence-
gah kerja prooksidan sehingga dapat digolongkan sebagai
para difenol orto difenol
Gambar 5. Rumus struktur paradifenol dan
ortodifenol (Winarno et al., 1980)
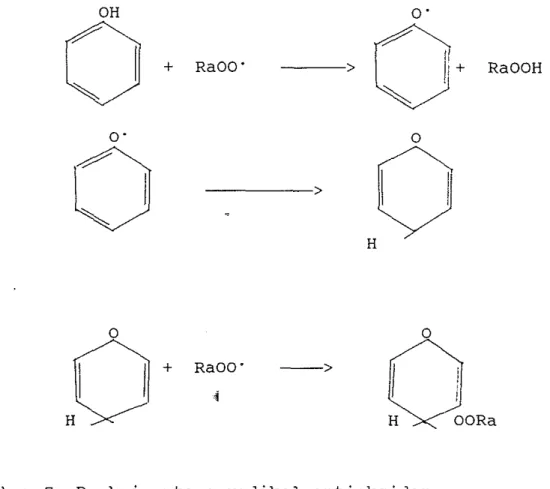
Adapun Ranney (1979) mengklasifikasikan antioksi-
dan atas tiga bagian berdasarkan prinsip kerjanya dalam
mencegah terjadinya proses oksidasi, pertama adalah
antioksidan yang mempunyai gugus fen01 dan amina aroma-
tik sebagai contoh adalah BHT, BHA, metilen bisfenol
dan difenilamin, yang bekerja dengan cara berinteraksi
dengan radikal bebas yang terdapat dalam sistem yang
membentuk produk substrat non radikal dan suatu radikal
fenoksi atau fenimino melalui pemberian atom hidrogen
yang dimiliki antioksidan terhadap radikal substrat
seperti yang terlihat pada Gambar 6.
Jika radikal antioksidan yang dihasilkan cukup
stabil atau secara sterik dicegah dari reaksi
berikutnya, maka radikal antioksidan tersebut tidak
akan bekerja sebagai suatu initiator dari reaksi
berikutnya. Pada kenyataannya adalah mungkin bereaksi
dengan reaksi bebas kedua dalam sistem sehingga
bereaksi dengan reaksi rantai dua radikal seperti yang
Gambar 6. Reaksi antioksidan dengan gugus fen01 dan amina aromatik dengan radikal
peroksida (Ranmy, 1979)
Kedua adalah antioksidan yang berfungsi dengan
cara yang sama untuk menghilangkan molekul-molekul
hidroperoksida dari sistem. Caranya adalah melalui
suatu mekanisme yang tidak melibatkan radikal-radikal
bebas. Molekul-molekul hidroperoksida RaOOH diikat
oleh antioksidan melalui ikatan hidrogen dan susunan
sterik sehingga terjadi suatu migrasi ikatan untuk
menghasilkan suatu alkohol dari suatu bentuk teroksida-
si dari tio eter. Contoh jelas dari antioksidan ini
adalah dilauril tiodipropionat (DLTDP). Molekul ini
mengandung atom sulfur peroksidasi yang mampu bereaksi
dengan molekul hidroperoksida berikutnya. Model kerja
ini menempatkan grup hidroksil ke dalam sistim atau
substrat. Juga dikenal fenomena sinergis, yaitu
radikal bebas dan lainnya merupakan pengurai hidroper-
oksida digunakan secara kombinasi, maka pengaruh kese-
luruhan melebihi penggunaan masing-masing secara terpi-
sah.
Gambar 7 . Reaksi antara radikal antioksidan
dengan radikal peroksida (Ranney, 1 9 7 9 )
Ketiga adalah antioksidan yang dapat menginaktiva-
si logam yang dapat mencegah terjadinya oksidasi.
Inisiasi oksidasi bisa dihasilkan oleh reaksi pertu-
karan elektron antara substrat dan ion logam bervalensi
banyak. Pada Gambar 8 ion logam direduksi dan
18
dapat dioksidasi kembali oleh oksigen dari udara atau
melalui mekanisme lain untuk menghasilkan katalis
oksidasi.
oksidasi
M(n-l)+ > Mn+
Gambar 8. Reaksi ion logam yang terlibat dalam
proses oksidasi (Ranney, 1979)
Antioksidan yang umum digunakan langsung pada
makanan adalah grup fenol kecuali etoksikuin yang
merupakan seriamine. Metode analisa untuk menentukan
adanya antioksidan pada makanan pada dasarnya :
1. Separasi fenol denqan cara ekstraksi, destilasi,
presipitasi atau kromatografi.
2. Pengukuran kuantitatif dengan kolorimeter, UV, infra
merah atau teknik yang lainnya (Stuckey, 1977)
Ditinjau dari segi biokimia, fermentasi merupakan
aktivitas mikroorganisme untuk memperoleh energi yang
diperlukan untuk metabolisme dan pertumbuhannya melalui
pemecahan atau katabolisme terhadap senyawa-senyawa
organik secara anaerobik. Untuk memperoleh energi
penerima elektron. Dari segi mikrobiologi industri,
fermentasi adalah proses untuk menghasilkan berbagai
produk dengan perantara atau dengan melibatkan
mikroorganisme (Rachman, 1989). Buckle et al,. (1978)
menambahkan bahwa fermentasi adalah perubahan kimia
balam bahan pangan yang disebabkan oleh enzim. Enzim
yang berperan dapat dihasilkan oleh mikroorganisme atau
telah ada dalam bahan pangan
Menurut Pratt (1972) ekstrak air panas dari
konsentrat protein kedelai, tepung kedelai yang
dihilangkan lemaknya, dan kacang kedelai segar maupun
kering cukup besar aktivitas antioksidannya. Gyorgy et
al., (1964) telah mengisolasi dan mengidentifikasi tiga
antioksidan alami yang terkandung di dalam kedelai
terfermentasi (tempe), yaitu 6,7,4'-trihidroksi iso-
lavon (faktor-Z), 7,4-dihidroksi isoflavon (daidzein)
,
3
dan 5,7,4'-trihidroksiisoflavon (genestein). Menurut
Hammerschmidt dan Pratt (1978) terdapat senyawa
flavonoid yang tidak lazim yaitu 6,7,4'-trihidroksi
isof lavon yang dapat diisolasi dari kedelai
terfermentasi (tempe)
,
dan memiliki aktivitasantioksidan. Daidzein dan genestein terdapat secara
alami pada kedelai mentah, sedangkan faktor-2 belum
dapat diisolasi pada kedelai mentah (Pratt dan Birac,
1979). Keadaan tersebut dapat disimpulkan bahwa
sebelum proses fermentasi (Gyorgy et al., 1984).
Dalam proses pembuatan daging bi j i picung
terfermentasi mula-mula biji picung segar direbus, lalu
dibungkus dengan abu sisa pembakaran kayu kemudian
dipendam selama 40 hari agar terjadi fermentasi
(Burkill, 1935) Menurut Meiriyanto (1988) aktivitas
antioksidan dari daging biji picung fermentasi memper-
lihatkan peningkatan aktivitas antioksidan dari mulai
hari k e no1 sampai ka 40 hari fermentasi. Berdasarkan
proses pembuatan yang melalui tahap perebusan, maka
dapat diduga bahwa senyawa antioksidan alami yang
111. BAHAN D A N METODE PENELITIAN
A. BAHAN DAN ALAT
1. Bahan
Bahan yang digunakan dalam penelitian ini
adalah biji picung (Pangium edule Reinw.) segar
yang diperoleh dari daerah Ciampea, Bogor. BHT
(Eastman Chemical Product Inc., Kingsport,
TENNESE), Petroleum eter p.a., Dietil eter p.a.,
(MERCK, Darmstadt) diperoleh dari laboratorium
kimia PAU Pangan dan Gizi. BF3-Metanol, Etanol,
NaC1, Na2C03, H2SOq diperoleh dari laboratorium
Kimia Pangan Teknologi Pangan Dan Gizi, Darmaga,
Bogor. Asam linolenat dari Cica Kamto Chemical Co.
Inc., Tokyo Japan. n-heptadekanoat diperoleh dari
Nacalai Tesque. Inc., Kyoto Japan.
2. Alat
Peralatan yang digunakan dalam penelitian ini
adalah: warning blender, freeze Drier (NEOCOOL-
Yamato, Tokyo, JAPAN, kromatografi gas (Shimadzu
GC-9Am), biological oxygen monitor YSI model 53
(Yellow Spring Instrument Co., Inc., Ohio, USA),
thermostat model CB - 500 ts. (Riko-Kagaku Sangyo
polyrecorder EPR - 111A, Tokyo, JAPAN), soxhlet,
kertas saring Whatman No.42, neraca analitis, dan
alat-alat gelas untuk keperluan analisis.
B. METODE PENELITIAN
Dalam penelitian ini dilakukan perlakuan fermentasi
daging biji picung, pengamatan dan analisis sebagai
berikut :
1. Perlakuan fermentasi
Percobaan yang dilakukan untuk mempelajari
fermentasi biji picung adalah mengkombinasikan
faktor tempat fermentasi, waktu perebusan dan
lamanya fermentasi secara faktorial. Lama
perebusan terdiri atas dua taraf yaitu 80 menit
(Ao) dan 40 menit (Al), tempat fermentasi terdiri
atas dua taraf yaitu di'dapur asal (Bo) dan di
laboratorium (Bl), lamanya fermentasi terdiri dari
7 taraf yaitu masing-masing 0, 7 , 14, 21, 28, 35
dan 42 hari (Co, C1, C2, C3, C4, C5 dan CG) dengan
suhu perebusan tetap. ~ i a g r a m alir perlakuan
Biji picung
I
6 perebusan
80 menit dan 10 menit
I
penirisan
1
penaburan abu dapur
I
j.
fermentasi
di dapur dan di laboratoriun I
.I
pengambilan contoh
masing-masing dengan lama fermentasi
0, 7, 14, 21, 28, 3 5 dan 42 hari
I
i.
analisis kadar air
I
1
pengering bekuan
I
I
6 .
analisis leblh lanjut
P
Gambar 9. Diagram alir perlakukan fermentasi daging
biji picung
Pada penelitian ini perebusan biji picung
dilakukan di dalam drum besar yang telah dipotong
setengah tingginya. Untuk merebus seribu biji
picung diperlukan air i 3 0 liter, dan suhu air
selama perebusan 9 g 0 c . Sumber panas untuk
perebusan ini berasal dari api kompor uap minyak
tanah yang dikenal dengan sebutan g a s burner
zepplin (Gambar 10). Setelah perebusan selesai (80
d i n g i n d e n g a n s e n d i r i n y a (Gambar 1 1 ) . S e t e l a h d i n g i n b a r u b i j i p i c u n g t e r s e b u t d i t a b u r i d e n g a n
a b u d a p u r (Gambar 1 2 d a n 1 3 ) . C o n t o h yang d i a m b i l m a s i n g - m a s i n g 2 5 b i j i , d i u k u r k a d a r a i r n y a d a n s i s a n y a d i k e r i n g b e k u k a n u n t u k d i a n a l i s i s l e b i h
l a n j u t .
Gambar 11. P e n i r i s a n d a n p e n d i n g i n a n d a g i n g b i j i p i c u n g y a n g t e l a h d i r e b u s
-
Gambar 1 3 . F e r m e n t a s i d a g i n g b i j i p i c u n g
2 . K a d a r a i r (A.O.A.C., 1 9 7 1 )
K a d a r a i r c o n t o h d i t e n t u k a n s e b a g a i b e r i k u t ,
c o n t o h d i t i m b a n g s e b a n y a k 2 gram d a n d i k e r i n g k a n d a l a m o v e n p a d a s u h u I O S ~ C , p e n g e r i n g a n d i l a k u l c a n
s a m p a i b e r a t n y a k o n s t a n .
IZadar a i r c o n t o h d a p a t d i h i t u n g d e n g a n
menggunakan rumus :
k a d a r a i r = a-b x 100%
C
a = b e r a t wadah d a n b a h a n n u l a - m u l a
b= b e r a t wadah d a n b a h a n s e t e l a h k e r i n g
Tiga gram sampel ditimbang langsung dalam
saringan timbel lalu dilipat diletakkan dalam alat
ekstraksi soxhlet yang kering, dilakukan reflux
selama 5 jam. Lemak yang diperoleh dipanaskan
dalam oven pada suhu 1 0 5 ~ ~ sampai berat konstan.
Kadar lemak contoh dapat dihitung dengan
menggunakan rumus:
kadar lemak = berat lemak x 100%
berat sampel
4. Pemisahan Asam Lemak Bebas (Fardiaz et al., 1986)
Minyak diekstrak dengan dietil eter,kemudian
asam lemak bebas dipisahkan dengan metode Mattick
dan Lee (1959).
Ke dalam satu gram contoh minyak di dalam
corong pemisah ditambahkan berturut-turut 8 4mg n-
heptadekanoat, 35 ml campuran dietil eter dan
petroleum eter (1:1), 6.5 ml etanol dan 12.5 mg
Na2C03 1%. Air dipisahkan dari lapisan eter.
Lapisan eter tersebut diekstraksi kembali masing-
masing dengan:
(1) 1.5 ml etanol 95%
+
7.5 ml Na2C03 1%(2) 1.5 ml etanol 95% + 5 ml Na2COj 1%
(3) 6.5 ml air destilata.
pemisah baru, ditambahkan 1.5 ml H2S04 10% dan
diekstrak dengan 12.5 ml campuran pelarut dietil
eter:petroleum eter (1:l). Lapisan eter dipisahkan
k e dalam botol kecil bertutup dengan volume 5 ml
dengan melewati kertas saring Whatman no.1 yang
berisi beberapa gram Na2S04 anhidrat. Pelaruf
diuapkan dengan cara melewatkan gas N2 k e dalan
botol, dan ekstraksi dengan 12.5 ml campuran
petroleum eter dan dietil eter (1:l) dilakukan tiga
kali dengan pelarut segar.
5. Esterifikasi Asam Lemak Bebas (Fardiaz et al., 1986)
Sebelum dianalisa dengan kromatografi gas,
asam-asam lemak bebas diesterifikasi dengan tujuan
supaya asam lemak tersebut mudah diuapkan. Asam
lemak bebas yang diperoleh ditimbang sebanyak 5-15
mg di dalam vial, ditambah BF3-metanol sebanyak 0.S
ml dan dipanaskan pada suhu 65-70°c selama satu
jam. Kemudian k e dalam vial tersebut ditambahkan
larutan NaCl jenuh sebanyak 0.4 ml dan diaduk
merata. Sesaat sebelum diinjeksikan k e dalam
kromatografi gas, k e dalam vial ditambahkan 0.4 ml
petroleum eter. Lapisan atas dari larutan ini
diambil sebanyak 5-10 p 1 untuk diinjeksikan k e
6 . Analisis Asam Lemak Bebas dengan Kromatografi Gas
(Fardiaz et al., 1986)
Analisis asam lemak bebas dilakukan dengan
menggunakan alat kromatografi gas model Shimadzu
GC-9Am. Jenis kolom yang digunakan adalah SP233O
(10% phenyl, 90% cyanopropyl) dengan dimensi kolom
250
x
0.5 x 0.3 cm. Ukuran injektor yang digunakan5 p 1 dan suhu injektor 2 3 0 ~ ~ . Gas karier adalah
nitrogen dengan "flow rate" 20 mllmenit, tekanan
gas H2 dan O2 masing-masing dipasang pada tekanan
0.6 kg/cm2 dan 0.2 kg/cm2. Suhu kolom 1 5 0 - 1 8 0 ~ ~
(15 menit), 1 8 0 - 2 1 0 ~ ~ (24 menit) dan terakhir
2 3 0 ~ ~ . Detektor yang digunakan adalah jenis FID
(Flame Ionization Detector).
7. Ekstraksi Antioksidan dengan Metanol (Hammerschmidt,
Untuk menentukan aktivitas antioksidan,
percobaan diawali dengan prosedur ekstraksi dari
komponen daging biji picung (Panqium edule Reinw.)
yang larut dalam metanol. Prosedur ekstraksi
menggunakan metode Hammerschmidt (1978) dengan
sedikit modifikasi seperti Gambar 14. Hasil
ekstraksi kemudian diukur aktivitas antioksidannya
penambahan 125 ml metanol
I
penghancuran
(2 menit)
I
J.pengocokan semalam
pemanasan
(5 menit)
I
.L
penyaringan dengan Whatman no.42 pencucian residu dengan 25 ml metanol
panas
I
4.
ekstrak (150 ml)
Gambar 14. Diagram alir metode ekstraksi daging biji picung yang larut dalam metanol (modifikasi me- tode Hammerschmidt, 1978)
1
8. Pengukuran Aktivitas Antioksidan (Taylor dan
Richardson, 1980)
Aktivitas antioksidan ditentukan dengan
menggunakan oksigenmeter (metode aktivitas
oksigen)
.
Sampel sebanyak 0.2 ml dilarutkan dalam5 ml air jenuh oksigen dan ditambah asam linolenat
sebanyak 53 mg (36 mM). Untuk kontrol dipergunakan
asam linolenat 36 mM dilarutkan dalam 5.2 ml air
jenuh oksigen, dan sebagai pembanding dipergunakan
jenuh oksigen juga dengan penambahan asam linolenat
sebanyak 53 mg.
Air jenuh oksigen diperoleh dengan cara
memberikan udara k e dalam air suling dengan bantuan
pompa udara (aspirator) selama 1.5 jam. dapun
cara kerja analisis aktivitas antioksidan dengan
menqgunakan oksigenmeter adalah sebagai berikut:
(1) menghubungkan alat ke arus listrik,' (2)
menghidupkan sirkulator (penangas air dengan
temperatur konstan 3g0c)
,
(3) menghidupkanoksigenmeter, (4) memutar tombol k e ampermeter, (5)
memasukkan 5 ml air jenuh oksigen dengan pengaduk
magnet ke dalam tabung contoh, (6) membiarkan
selama tiga menit sampai temperatur seimbang, (7)
memasukkan sensor k e dalam tabung contoh, mengelu-
arkan seluruh udara melalui lubang kecil (dibantu
dengan sedikit memutar batang sensor), batas
larutan plunger berada di tengah over flow groove
(8) menyalakan pengaduk magnetik, (9) menempatkan
skala pada 0% dengan mengatur tombol amper nol,
(10) menempatkan perekam pada skala nol, (11)
memutar tombol selektor k e posisi air, dan
menempatkan skala pada loo%, (12) menempatkan
perekam ke skala maksimum dengan menggunakan
recorder adjust, (13) memperhatikan . kestabilan
bebas gangguan (noise), (14) memasukkan kontrol/
sampel/pembanding (total volume 5.2 ml) dan
pengaduk magnetik k e dalam tabung contoh, (15)
memasukkan sensor ke dalam tabung contoh, dan (16)
membiarkan selama 90 menit, dan laju penangkapan
oksigen tercatat oleh perekan. Oksigen meter
ditunjukkan pada Gambar 15, sedangkan sensor dan
ruang contoh diperlihatkan pada Gambar 16.
Hasil analisis aktivitas antioksidan dengan
mengyunakan oksigenmeter dinyatakan sebagai faktor
protektif, yaitu perbandingan lamanya waktu (menit)
oksidasi yang terjadi pada emulsi dengan penambahan
antioksidan dengan lamanya waktu (menit) oksidasi
yang terjadi pada kontrol.
C . MODEL RANCANGAN PERCOBAAN
Model rancangan percobaan yang digunakan adalahl
rancangan faktorial di dalam rancangan acak lengkap.
Modelnya adalah:
Y . . = p + A . + 6 . + Ck + ( A S ) . . + (AC)ik + ( 6 C ) j k + ( A S C ) i j k + L , ( i j k )
Ijkt 1 1 I J
dengan
'ijkl = peubah respon karena pengaruh bersama
taraf ke-i faktor A , taraf ke-j faktor
B, taraf ke-k faktor C yang terdapat
= pengaruh rata-rata yang sebenarnya
= pengaruh tambahan dari taraf ke-i fak-
tor A
= pengaruh tambahan dari taraf ke-j fak-
tor B
= pengaruh tambahan dari taraf ke-k fak-
tor C
= pengaruh tambahan dari interaksi anta-
ra taraf ke-i faktor A dan taraf ke-j
f aktor B
= penqaruh tambahan dari interaksi anta-
ra taraf ke-i faktor A dan taraf ke-k
f aktor C
= pengaruh tambahan dari interaksi anta-
ra taraf ke-j faktor B dan taraf ke-k
f aktor C
= pengaruh tambahan dari interaksi anta-
ra taraf ke-i faktor A , taraf ke-j
faktor B dan taraf ke-k faktor C
= pengaruh tambahan dari satuan percoba-
an ke-1 dalam kombinasi perlakuan
RUBBER
PROBE CLAMP
HOLD DOWN RING
SHOULDER SCREW
BATH COVER
OVERFLOW GROOVE
;i
ACCES SLUT
MAGNETIC S T I R R E R
IV. HASIL DAN PEMBAHASAN
A. FERMENTASI DAGING BIJI PICUNG (Panqium edule Reiwn.)
Menurut Sugianto (1984) daging biji picung dapat
dimakan, asal dibebaskan dahulu HCN-nya. Caranya ialah
dengan merebus dahulu biji buah picung yang sudah masak
(sebaiknya buah yang telah jatuh dari pohon dengan
sendirinya). Biji-biji tersebut kemudian ditanam dalam
tanah, kira-kira 40 hari lamanya.
Selama perebusan suhu tidak boleh turun, sehingga
besarnya api harus diperhatikan, dan air pada awal
perebusan harus cukup karena bila kekurangan air,
sewaktu perebusan berjalan tidak boleh ditambah air
dingin. Kalau ha1 ini dilakukan biasanya daging biji
picung hasil fermentasi masih terasa pahit, yang
i menandakan HCN belum semuanya dibebaskan.
Abu dapur ialah abu yang dihasilkan dari pembakaran
kayu bakar. ~iasanya abu ini merupakan limbah rumah
tangga yang memasak makanannya menggunakan tungku kayu
bakar. Abu ini berguna untuk melindungi biji picung
selama fermentasi dari fluktuasi kelembaban udara
karena abu dapur bersifat higroskopis.
Warna daging biji picung hasil fermentasi 0, 7,
14, 21, 28, 35 dan 42 hari semakin lama semakin coklat
tua (Gambar 17). Hasil analisa kadar air, kadar lemak
d i f e r m e n t a s i s e l a m a 0, 7 , 1 4 , 2 1 , 28, 35 dan 42 h a r i d i s a j i k a n pada Lampiran 1.
Gambar 1 7 . Daging b i j i p i c u n g h a s i l f e r m e n t a s i 0 , 1 4 , 28 dan 42 h a r i y a n g t e l a h d i k e r i n g bekukan
( m e n u r u t a r a h jarum jam)
B . KADAR A I R
H a s i l a n a l i s i s k a d a r a i r d a r i d a g i n g b i j i p i c u n g
dengan p e r e b u s a n selama 80 m e n i t dan t e m p a t f e r m e n t a s i
d i d a p u r pada h a r i k e no1 s e b e s a r 55.11%, s e d a n g k a n
pada h a r i k e 4 2 b e r u b a h m e n j a d i 4 1 . 7 4 % . Demikian j u g a
u n t u k d a g i n g b i j i p i c u n g yang d i r e b u s s e l a m a 8 0
m e n i t , d i f e r m e n t a s i d i l a b o r a t o r i u m pada h a r i k e no1
3 9 . 0 8 % . Kadar air daging biji picung yang direbus
selama 4 0 menit dan fermentasi dilakukan di dapur pada
hari ke no1 sebesar 6 0 . 5 6 % turun menjadi 3 8 . 6 6 % pada
fermentasi hari ke 42. Kadar air daging biji picung
yang direbus selama 40 menit dan fermentasi dilakukan
di laboratorium ternyata mengalami peningkatan dari
5 6 . 0 9 % pada hari ke no1 menjadi 62.64% pada hari ke 42.
Hasil percobaan Buchner menunjukkan bahwa
fermentasi akan terjadi apabila terdapat aktivitas
enzim (Rachman, 1 9 8 9 ) . Buckle et al. (1978) mengatakan
berkurangnya reaksi enzimatis disebabkan oleh
berkurangnya gerakan dari substrat untuk meresap ke
bagian aktif dari enzim. Walaupun bagian aktif dari
enzim tetap berfungsi sekalipun nilai a, sangat rendah,
substrat dan bahan pereaksi lainnya seperti air, harus
cukup mampu bergerak untuk mencapai bagian tersebut.
Winarno (1988) menyatakan kadar air semakin tinggi
mengakibatkan aktivitas enzim akan semakin tinggi.
Dari pengamatan kadar air dan perhitungan statis-
tika dengan uji-F pada tingkat kepercayaan 9 9 % ,
diperoleh bahwa kadar air dipenqaruhi oleh lama
perebusan dan lamanya fermentasi, tetapi tidak
dipengaruhi oleh tempat fermentasi. Diduga faktor
lingkungan tempat fermentasi tidak banyak berpengaruh
hampir sama dan selama fermentasi biji picung ditutup
oleh abu dapur. Baik perebusan selama 80 menit maupun
40 menit mempunyai kadar air semakin rendah bila
fermentasi semakin lama (Gambar 18).
Penurunan kadar air ini diduga disebabkan oleh
penguapan yang terjadi selama fermentasi. Penquapan
ini terjadi melalui kulit biji picung bagian bawah yanq
kerapatannya lebih rendah dibandinqkan bagian kulit
lainnya.
A 1 : u a k t u peretusan 80 m e n i t A2 : v a k t u perebusan 40 m n i t
61 : tempat fermentasi d i d a p r
i
I 02 : tempat fermentasi d i Laboratoriun0
0 7 14 21 2 8 36 4 2
lama fermentas1 (harl)
- A181 + A 1 2 A ,4251 ,4252
!
Gambar l a . Grafik hubungan antara kadar air dengan
C. EKSTRAKSI ANTIOKSIDAN DAN PENGAMATAN AKTIVITASNYA
Masing-masing daging biji picung terfermentasi
yang telah dikering-bekukan (sebanyak 20 gram)
diekstrak dalam metanol (150 ml) sehingga didapatkan
13.3% b.k (w/v). Ekstraksi ini bertujuan untuk
melarutkan komponen antioksidan yang larut dalam
metanol. Meiriyanto (1988) telah berhasil membuat
ekstrak aaging biji picung yang mempunyai aktivitas
antioksidan menggunakan pelarut metanol. Demikian juga
Panghegar (1990) telah berhasil mengisolasi antioksidan
dari ekstrak metanol daging biji picung, serta Adidjaja
(1991) berhasil membuat kristal antioksidan dari ekstrak metanol daging biji picung.
Chang et al. (1977) telah mencoba berbagai pelarut
untuk mengisolasi antioksidan dari rosemary dan sage.
Ekstraksi dengan pelarut polar metanol mendapatkan
hasil komponen antioksidan murni tertinggi.
Hammerschmidt dan Pratt (1978) mengekstrak antioksidan
fenolik dari kedelai kering menggunakan metanol.
~ e m i k i a n juga Taga et al. (1984) melakukan ekstraksi
komponen antioksidan fenolik dari Salvia bispanica L.
dengan metanol.
Ekstrak yang dihasilkan dari daging biji picung
terfermentasi memiliki warna kuning kecoklatan.
Semakin lama fermentasi dllakukan warna ekstrak semakin
dengan metode penurunan intensitas warna 13-karoten,
warna ini perlu dihilangkan karena mengganggu
pengukuran intensitas warna 8-karoten. Penghilangan
warna dapat dilakukan dengan menggunakan karbon aktif.
Dalam penelitian ini tidak dilakukan penghilangan warna
karena metode yang digunakan untuk mengukur aktivitas
antioksidan adalah metode aktivitas oksigen (oksigen-
meter). Dengan metode ini warna tidak mempengaruhi
hasil analisis.
Pada prinsipnya analisis aktivitas antioksidan
dengan menggunakan metode aktivitas oksigen didasarkan
atas reaksi reduksi oksidasi dalam emulsi asam linoleat
dengan air jenuh oksigen pada suhu 3g0c. Penambahan
antioksidan k e dalam emulsi mengakibatkan waktu yang
dibutuhkan untuk menangkap oksigen yang terlarut
dibandingkan dengan emulsi tanpa penambahan antioksidan
1
lebih lama (Taylor dan Richardson, 1980). Laju
penangkapan oksigen oleh sensor (probe) berbanding
lurus dengan arus yang dihasilkan. Reaksi yang terjadi
adalah sebagai berikut:
O2
+
2H20 4- 4e--40H- (katoda)4Ag
+
4C1-'
4AgC1+
4e- (anoda)Oksigen dapat bereaksi dengan katoda karena ada
arus yang mengalir melalui sensor, yang sebanding
dari teflon dan silikon yang permeabel terhadap
oksigen. Pada saat oksigen diserap oleh katoda,
tekanan oksigen pada membran adalah nol. Dengan
demikian terjadi gaya yang menyebabkan oksigen
berdifusi melalui membran, besarnya setara dengan
tekanan absolut dari oksigen di luar membran. Jika
tekanan oksigen meningkat oksigen akan banyak berdifusi
melalui membran sehingga arus yang mengalir melalui
sensor semakin besar. Demikian sebaliknya tekanan
oksigen yang rendah akan menghasilkan arus yang kecil.
Difusi yang terjadi pada membran setara dengan tekanan
dan arus pada sensor, sehingga terdapat hubungan yang
linear antara tekanan oksigen di luar membran dengan
arus pada sensor.
Oksigen dapat mengoksidasi asam lemak tidak jenuh
membentuk malonaldehid sebagai indikasi adanya oksidasi
3
lipid (Gambar 19). Adanya antioksidan akan menghambat
oksidasi asam lemak tidak jenuh. Antioksidan dari
daging biji picung diduga menghambat oksidasi linolenat
dengan cara memberikan atom hidrogen pada radikal
peroksida asam lemak. Hal ini disebabkan zat aktif
antioksidan dari daging biji picunq diduga mempunyai
+
o2
dan kemudian RHI OOH
1
Gambar 19. Pembentukan malonaldehid dari hasil oksidasi asam lemak tidak jenuh (Nawar, 1965)
Pola penurunan kadar kejenuhan pada kontrol
terlihat sangat cepat (Gambar 20). Oksigen banyak
digunakan untuk mengoksidasi asam linoienat sehingga
kadar kejenuhan oksigen berkurang sangat cepat. Hal
ini menunjukkan terjadi reaksi oksidasi dan reduksi
qntara asam linolenat dan oksigen. Asam linolenat
berperan sebagai reduktor sedangkan oksigen yang
terlarut dalam air berfungsi sebagai oksidator. Reaksi
berjalan dengan cepat karena tidak ada senyawa yang
dapat menghambat atau melindungi oksidasi asam linolenat
oleh oksigen.
Taylor dan Richardson (1980) mengatakan bahwa
aktivitas antioksidan dapat dinyatakan dengan faktor
protektif yang merupakan perbandingan antara waktu
oksidasi pada emulsi yang ditambah antioksidan (menit)
(menit). Faktor protektif dalam percobaan ini dihituny
berdasarkan penurunan kejenuhan oksigen pada saat
mencapai 50%. Faktor protektif kemudian dihitung
sebagai perbandingan antara waktu (menit) yang
dibutuhkan untuk oksidasi emulsi yang ditambahkan
antioksidan dengan emulsi tanpa antioksidan (kontrol)
pada saat kejenuhan oksigen mencapai 50%. Adanya
aktivitas antioksidan ditunjukkan denqan nilai
protektif yang lebih besar daripada satu. Makin kuat
aktivitas antioksidan nilai faktor protektif yany
dimilikinya juga semakin besar.
P E R S E H R B J E N U H A H
Keterangan:
FPA = faktor protektif antioksidan A
Emulsi asam linolenat dalam air jenuh oksigen
dengan penambahan BHT (0.4% v/v) menghasilkan grafik
yang landai. Adanya BHT dapat menghentikan reaksi
berantai oksidasi asam linolenat oleh oksigen pada
tahap terminasi. BHT akan menyumbangkan hidrogen dan
bereaksi dengan radikal ROO' membentuk produk yang
stabil (Gambar 21). Dengan demikian kadar kejenuhan
oksigen dapat dipertahankan karena oksigen terlarut
tidak digunakan untuk mengoksidasi asam linolenat.
Gambar 21. Reaksi asam linoleat dengan BHT (Nawar, 1985)
00'
I
+
[1H3 (CH2) 4 ~ ~ = ~ k( c H ~ ) ~ ~7 ~= ~~ ~~m-e ~ ~-OCH3 BHT
peroksida dari
Hasil analisis aktivitas antioksidan alami daging
biji picung hasil fermentasi dengan menggunakan oksi-
yenmeter dapat dilihat pada Lampiran 5. Kurva untuk
kontrol yang merupakan emulsi asam linolenat dalam air
jenuh oksigen terlihat lebih curam dibandingkan dengan
kurva yang lainnya (contoh dan standar). Hal ini
menunjukkan bahwa dalam sistem emulsi tersebut terjadi
proses oksidasi reduksi yang lebih cepat dibandingkan
dengan sistem emulsi yang ditambah BHT atau ekstrak
metanol daging biji picung. Pada kontrol, oksigen yang
terdapat dalam emulsi lebih banyak digunakan untuk
mengoksidasi asam linolenat, sehingga persentase
.kejenuhan oksigen berkurang sangat cepat. Dalam emulsi
ini, asan linolenat berperan sebagai reduktor sedangkan
oksigen sebagai oksidator.
Penambahan ekstrak metanol daging biji picung
terfermentasi 0 sampai 42 hari dapat mengurangi
penurunan oksigen terlarut. Hal yang sama terjadi pada
penambahan antioksidan sintetis BHT. Hal ini
menunjukkan ekstrak daging biji picung terfermentasi
mempunyai aktivitas antioksidan.
Lampiran 3a sampai 3c dan Gambar 22 menunjukkan
terjadinya peningkatan nilai faktor protektif bila
waktu fermentasi makin lama untuk semua perlakuan.
Nilai faktor protektif ini sangat nyata dipengaruhi
fermentasi juga oleh interaksi faktor yang berpengaruh
tersebut.
A 2 : vaktu perebusan 40 menit
81 : tenpat fermentasi d i daplr
62 : tempat fermentasi di labarrrtoriun
Gambar 22. Hubungan nilai faktor protektif dengan lama- nya fermentasi
Faktor protektifi selama fermentasi daging biji
picung dari perlakuan perebusan selama 80 menit dan
tempat fermentasi di dapur pada hari k e no1 dan hari k e
42 masing masing 1.57, 2.92, demikian juga nilai faktor
protektif daging biji picung dengan perebusan selama 80
menit difermentasi di laboratorium, lama perebusan 40
menit difermentasi di dapur dan di laboratorium dari
hari k e no1 clan hari k e 42 masing-masing berturut-turut
1.75, 2.88, 1.36, 1.94, 1.50, dan 1.66, menunjukkan
lamanya fermentasi daging biji picung. Hal ini sesuai
dengan hasil penelitian Meiriyanto (1388).
Terjadinya peningkatan aktivitas antioksidan
selama fermentasi -daging biji picung diduga sama
seperti pembentukan antioksidan pada tempe. Penelitian
Pandoe (1984) menyatakan tempe sangat tahan terhadap
pembentukan peroksida, sehingga tidak mudah menjadi
tengik. Keadaan ini menunjukkan adanya antioksidan
alami yang dikandung tempe. Menurut Hammerschmidt dan
Pratt (1978) terdapat senyawa flavonoid yang tidak
lazim yaitu 6,7,4'-trihidroksi isoflavon (faktor-2),
yang dapat diisolasi dari kedelai terfermentasi
(tempe), dan memiliki antivitas antioksidan. Daidzein
(7,4'-dihidroksi) isoflavon dan gonestein (5,7,4'-
trihidroksi) terdapat secara alami pada kedelai mentah
dan ditemukan dalam tempe. Sedangkan faktor-2 belum
dapat diisolasi pada kedelai mentah. Oleh
Hammerschmidt dan Pratt (1978) disimpulkan bahwa
senyawa faktor-2 tidak aktif sebelum proses fermentasi.
D. LEMAK DAN ASAM LEMAK
Dalam sistem biologis, termasuk di dalamnya
makanan, molekul lemak seringkali berada dalam
keteraturan yang tinggi, dan secara relatif terbatas
dalam ha1 jarak antar molekul dan gerakannya, dan
sekitarnya seperti protein, karbohidrat, air, enzim,
garam, vitamin dan pro atau antioksidan. Komposisi
lemak, derajat keteraturan molekulnya dan hubungan
dengan komponen bukan lemak sangat beragam tergantung
pada spesies tumbuhan dan hewan serta letak lemak dalam
bagian tubuh organisme (Nawar, 1985)
Kadar lemak pada hari ke no1 untuk perlakuan
perebusan 80 menit fermentasi dilakukan di dapur,
perebusan 80 menit fermentasi di lakukan di
laboratorium, perebusan 40 menit fermentasi di dapur,
dan perebusan selama 40 menit fermentasi di
laboratorium masing-masing 47.71%, 44.66%, 44.85% dan
44.35%. Sedangkan pada hari k e 42 berturut-turut kadar
lemaknya 28.55%, 28.69%, 42.70%, dan 42.35%.
A2 : waktu prebusan 40 menit
81 : t m p a t f e m n t a s i di daplr
1
/
82 : t m t fermentasi di LvboratoriunI
0 1 I
0 7 14 21 28 36 4 2
lama ferrnentsal (harl)
Dari hasil analisis sidik ragam dan interaksinya
dengan tingkat kepercayaan 99%, kadar lemak dipengaruhi
oleh lama perebusan, tempat fermentasi dan lamanya
fermentasi. Gambar 23 menunjukkan hubungan kadar lemak
dengan lamanya fermentasi. Fermentasi daging bi ji
picung pada hari ke 21 untuk semua perlakuan memiliki
kadar lemak yang meningkat, ha1 ini diduga karena
komponen yang semula tidak larut dalam petroleum eter
mengalami pernutusan ikatan sehingga dapat larut dalam
petroleum eter. Setelah hari 2 1 komponen yang larut
dalam petroleum eter diduga mengalami degradasi menjadi
komponen yang lebih sederhana dan tidak larut dalan
petroleum eter.
Menurut Pratt (1980) banyak minyak nabati yang
dilindungi secara alami oleh antioksidan (polifenol).
Antioksidan tersebut menghasilkan suatu efek protek