DAFTAR ISI LEMBAR PERSETUJUAN LEMBAR PENGESAIIAI\ LEMBAR PERNYATAAN ABSTRAK ABSTRACT
KATA PENGANTAR DAFTAR ISI
DAT'TAR TABEL DAFTAR GAMBAR DAFTARLAMPIRAI\
...1
. . .. ... .11
BAB
I
PENDAIIULUAN1.1
Latar Belakangl-2
Perumusan Masalah1.3
Tujuan Penelitian.1.4
Manfaat Penelitian1.5
Batasan penelitianBAB
II
TINJAUAI.I PUSTAKA2.1
SibutraminHidroklorida.2.2
Jamu2.3
Kromatografi CairKinerja Tinegr (KCKT).2.3.1
Pendahuluan2.3.2
Sistem Instumen KCKT2.3.3
Teknik Pemisahan Dalam KCKT2.3.4
Validasi Metode Analisis... Teknik Sampling.KerangkaTeori.
BAB UI METODOLOGI PENELITIAFI
3.1
Waktu dan Tempat penelitian ... ...3.2
Bahan dan Alat3.2.1
Bahan3.2.2
AIat...3.3
MetodePenelitian3.3.1
Pemilihan Sampel...3.3.2. Ptepmasi
Sampel...
...:...;...3.3.2
ValidasiMetode
...:...3.3.3
Penetapan Kadar Sibuhamin HCI dalam Sampel...BAB IV
BAB V
HASIT DAN PEMBAHASAN
4.1.1 Hasil Uji Efesiensi (o1orr...
4.1.2 Hasil Uii Perolehan kembati (UPK)...
4.1.3 Hasil Penetapan Kurva Kalibrasi...
4.1.4 Hasil Anatisa Kadar Sibutramin HCI Dalam Sampel...
4.2
Pembahasan...DAFTAR PUSrAKA....re.r*--ri*,or...,,..{o...r..r.,,
tAMPI.RAN
31 31
32
32
34 35
44 48
DAFTAR TABEL
[image:10.612.16.570.2.817.2] [image:10.612.18.559.21.812.2]Halaman Tabol.
I
Laporm efck samping sibutramin HCI di Australia (BPOM, 2006)...11 Tabel.2
Jamu yang Mengnndrrng Bahan Kimia Obat(Yuliarti,2008)...
...12l
TaM. 3 Uji Efisionsi koloru pada sibutramin
HC1...
...31 Tabel.4
Uji UPK / Rcoovery Sibutramin [ICl dengnn alatKCKT.
...32 Tabel. 5 [Iasilhrvakalibrasi SibutraminHC1...
...32DAFTAR GAMBAR
Stuktur Kimia Sibutramin HCI
Sistem Instrumen KCKT
Kurva Kalibrasi Larutan Standar sibutramin HCI Instrumen KCKT...
Blanko
Blanko
*
sampel baku banding sibutramin HCl... Hasil analisa jamu kode HS....Hasil analisa jamu kode SR.... Hasil analisa jamu kode JT...
Hasil analisa jamu kode LD.... Hasil analisa jamu kode LX.... Hasil analisa jamu kode SL....
Instrumen KCKT... pH meter
Jamu antiobesitas (HS). Jamu antiobesitas (SL)
Jamu antiobesitas (LD).
Jarnu antiobesitas (SR) Jamu antiobesitas (JT)... Jamu antiobesitas (LX)
Baku pembanding Sibutramin HCI
[image:11.588.85.547.65.747.2] [image:11.588.71.540.70.816.2]Halaman Gambar 1.
Gambar 2.
Gambar 3.
Gambar 4.
Gambar 5.
Gambar 6.
Gambar 7.
Gambar 8.
Gambar 9.
Gambar 10.
Gambar 11.
Gambar 12.
Gambar 13.
Gambar 14.
Gambar 15.
Gambar 16.
Gambar 17.
Gambar 18.
Gambar 19.
Gambar 20.
Gambar 21.
DATTARIAMPIf,AN
Lampira.n. t Sertifikasi Fenguiian
Sibutramin.
...r 48Lampiran.2Hasill(urvaKalibrasiSibutramin}lCl...
Latnpiran. 3 hlasil Uli Perolehan
Kembali...
... 50Lampiran,4 HasilUji ldentifikasisibutramin HCI pada
Sampe1...
52Lampiran. 5 Gambar
alat-a1ct...
... 59Lampirran. 6 Gambar Sanrpet Jamu Antiobesitas yang di
ufi...
...'... 61tampiran. 7 Tabel Komposki Kandungan SampelJamu Antiobesitas yang di uji... 62
{1
"
1
BAB I
PENDAHULUAN
1.1. Latar Belakang
Indonesia merupakan salah satu negara dengan kekayaan hayati
terbesar di dunia yang memiliki lebih dari 30.000 spesies tanaman tingkat
tinggi. Hingga saat ini, tercatat 7000 spesies tanaman telah diketahui
khasiatnya namun kurang dari 300 tanaman yang digunakan sebagai bahan
baku industri farmasi secara regular. Sekitar 1000 jenis tanaman telah
diindentifkasi dari aspek botani sistematik tumbuhan yang baik. WHO pada
tahun 2008 mencatat bahwa 68% penduduk dunia masih menggantungkan
sistem pengobatan tradisional yang mayoritas melibatkan tumbuhan untuk
penyembuhan penyakit dan lebih dari 80% penduduk dunia menggunakan
obat herbal untuk mendukung kesehatan mereka. Fakta-fakta tersebut
menunjukkan bahwa tumbuhan obat memiliki arti penting yakni secara
mendasar mendukung kehidupan maupun potensi perdagangan (Saefudin,
2011 ).
Sesuai dengan peraturan perundang-undangan yang berlaku, obat
tradisional dilarang menggunakan bahan kimia hasil isolasi atau sintetik
berkhasiat obat. Namun pada kenyataannya, di pasaran masih juga beredar
2
Sejalan dengan perkembangan obat tradisional inimenjadikan
persaingan yang semakin ketat dan cenderung membuat industri jamu
menghalalkan segala cara untuk dapat bertahan hidup, pencampuran jamu
dengan bahan – bahan kimia berbahaya sering dilakukan untuk menjadikan
jamu tersebut semakin berkhasiat secara instan ( Hermanto, 2007).
Vepriati (2008) berpendapat bahwa pencampuran jamu dengan
bahan kimia obat berbahaya apalagi kebanyakan bahan kimia obat yang
ditambahkan tergolong obat keras yang dalam pemakaian harus dengan
resep dokter, karena disamping mempunyai efek terapi juga mempunyai
efek samping dan kontra indikasi. Lebih bahaya lagi bahan kimia obat yang
di tambahkan biasanya tanpa dosis yang jelas, dan biasanya obat tradisional
dikonsumsi secara rutin yang menjadi adat kebiasaan dan dalam jangka
panjang.
Beberapa penelitian telah dilakukan dan ditemukan jamu-jamu yang
didalamnya mengandung BKO, salah satu jenis jamu yang mungkin
ditambahkan obat didalamnya adalah jamu antiobesitas. Mengingat
tingginya minat masyarakat Indonesiakhususnya kaum wanita untuk
melangsingkan tubuhnya, jamu yang dapat memberikan efek penurunan
berat badan dengan cepat kemungkinan besar akan banyak di konsumsi oleh
masyarakat. Bahan kimia obat yang dicampurkan ke dalam obat tradisional
ini kebanyakan masuk ke dalam kategori obat keras dengan dosis yang jauh
daripada dosis yang dianjurkan. Sehingga jika masyarakat mengkonsumsi
3
hati.Keberadaan obat ini selain menyalahi peraturan pemerintah, juga dapat
membahayakan kesehatan konsumen itu sendiri(Kurniadi, 1999).
Sibutramin Hidroklorida adalah obat penurun berat badan, golongan
obat keras yang hanya dapat diperoleh dan hanya dapat digunakan
berdasarkan resep dokter. Obat keras ini merupakan senyawa kimia turunan
siklobutan yang bekerja dengan cara menghambat ambilan (reuptake)
norepinefrin, serotonin, dan dopamin. Dengan pengawasan dokter,
sibutramin HCl digunakan sebagai terapi tambahandalam program
penurunan berat badan pada nutritional obesity patients dengan indeks
massa tubuh (Body Mass Index, BMI) lebih dari atau sama dengan 30
kg/m2, atau pada nutritional excess weight patients dengan indeks massa
tubuh lebih dari atau sama dengan 27 kg/m2, yang memiliki faktor risiko
yang terkait dengan obesitas seperti diabetes tipe 2 atau dislipidemia.
Namun kenyataannya, obat ini banyak ditemukan dijual bebas di pasaran
(BPOM, 2006)
Berdasarkan struktur Sibutramin HCl yang mempunyai gugus
kromofor maka analisa senyawa ini dapat dilakukan dengan
menggunakan kromatografi cair kinerja tinggi (KCKT) menggunakan
detektor UV-VIS.
Berdasarkan hal tersebut, maka peneliti ingin mengetahui apakah
Sibutramin HCl digunakan sebagai bahan tambahan pada jamu tradisional
yang beredar di masyarakat dengan menggunakan metode KCKT. Penelitian
ini diharapkan memberikan informasi kepada masyarakat agar lebih
4
1.2. Perumusan Masalah
Apakah jamu tradisional Antiobesitas yang beredar di masyarakat
teridentifikasiadanya senyawa kimia Sibutramin HClyang terkandung dalam
sampel, dengan menggunakan metode KCKT ?
1.3. Tujuan Penelitian
Penelitian ini bertujuan untuk mengidentifikasi kandungan sibutramin
HClpada beberapa jamu tradisional Antiobesitas yang beredar di masyarakat
dengan menggunakan metodeKCKT.
1.4. Manfaat Penelitian
1. Hasil penelitian ini diharapkan dapatmemberikan informasi kepada
masyarakat tentang bahaya dari sibutramin HCljika mengkonsumsi jamu
tradisional yang mengandung sibutramin HCl.
2. Sebagai masukan bagi dinas kesehatan, Badan Pengawas Obat dan
Makanan tentang kandungan sibutramin HCl pada jamu tradisional yang
beredar di masyarakat.
1.5. Batasan Penelitian
Penelitian ini dilakukan terhadap 6 jamu tradisional antiobesitas yang
diperoleh dari wilayah Ciputat – Tangerang Selatan dengan metode
Investigasi Sampling, di dasarkan atas peminatan masyarakat yang cukup
5
BAB II
A. TINJAUAN PUSTAKA
2.1. Sibutramin Hidroklorida
Sibutramin HClmerupakan salah satu obat antiobesitas yang
berkhasiat sebagai anoreksansia. Dimana anoreksansia merupakan zat-zat
berdaya menekan nafsu makan dan digunakan untuk menunjang diet pada
penanganan obesitas. Obesitas didefinisikan sebagai terdapatnya lemak
tubuh dalam jumlah abnormal, yang mengakibatkan kegemukan dan
overwight pada keadaan tinggi badan dan jumlah otot tertentu. Obesitas
merupakanpencetus faktor resiko untuk diabetes dan dapat meningkatkan
resiko akan timbulny, hernia, varices,dan artrose pada lutut dan kaki. (Tjah,
2007)
Dalam usaha mencari anoreksansia baru yang efektif dan aman, telah
dilakukan kajian dengan hormon kenyang. Tetapi karena orang obese
kurang atau tidak peka untuk leptin, maka hormon ini tidak menghasilkan
efek baik. (Tjah, 2007).
Dewasa ini tersedia tiga obat baru yang berfungsi sebagai antiobesitas,
yaitu sibutramin HCl, rimonabant dan ekstrak kaktus Hoodia, di samping
obat-obatyang sudah ada (amfepramon dan orlistat).(Tjah, 2007),
Mekanisme kerjanya berlainan, yaitu :
a. Menekan nafsu makan dan rasa lapar : amfepramon, sibutramin HCl,
rimonabant dan hoodia. Menghambat re-uptake serotonin, yang di
6
Rimonabant memblok reseptor reseptor cannabinoid yang apabila
diduduki endocannabinoid menimbulkan rasa lapar. Hoodia
mengandung zat aktif yang bersaing dengan glukosauntuk reseptor
yang sama, sehingga hipotalamus “dikelabui” dan tidak memicu
isyarat lapar.
b. Menghambat penyerapan lemak : orlistat. Lemak baru dapat
diabsorpsi seusai dirombak oleh lipase menjadi asam lemak bebas
dan gliseol. Orlistat merintangi lipase, sehingga sebagian lemak
tidak diserap usus.
c. Meningkatkan pengeluaran energi : sibutramin HCl, mungkin
dengan jalan aktivitas adrenergis perifer. Setelah penggunaan enam
bulan, dapat dicapai penurunan bobot badan rata-rata 11 kg (Tjah,
2007).
Sibutramin HClmerupakan golongan obat keras yang digunakan
dalam pengobatan obesitas, dimana obat ini hanya dapat diperoleh dan
digunakan berdasarkan resep dokter. Namun kenyataannya, obat ini banyak
ditemukan dijual bebas di pasaran (BPOM, 2006).
Sibutramin HCl (derivat siklobutan) adalah suatu serotonin – NA
re-uptakebloker, yang berperan pada terjadinya perasaan kenyang sesudah
makan. Di samping itu juga dapat meningkatkan penggunaan energi akibat
kerja adrenergis perifer. Tanpa diet penurunan hanya 1 % , terapi sebaiknya
7
kg. Digunakan pada penderita obese dengan BMI > 30kg/m2 atau di atas 27
dengan resiko diabetes, dislipidemia, dan hipertensi (Tjah, 2007).
Mekanisme dari sibutramin HCladalah menghambat reuptake
noradrenaline dan serotonin oleh sel saraf setelah kedua neurotransmiter ini
menyampaikan pesan diantara sel saraf yang ada di otak. dihambatnya
reuptake membuat kedua neurotransmitter ini bebas menjelajah di otak. saat
itulah keduanya menghasilkan perasaan penuh (kenyang) pada pasien
sehingga mengurangi keinginan untuk makan (Tjah, 2007).
Efek samping yang dapat timbul dari penggunaan sibutramin HCl
meliputi peningkatan denyut jantung, palpitasi (jantung berdebar),
peningkatan tekanan darah, sakit kepala, kegelisahan, kehilangan nafsu
makan, konstipasi, mulut kering, gangguan pada alat perasa, vasodilatasi,
insomnia, pusing, paraaesthesia, berkeringat dan lain-lain ( BPOM,
2006).Penggunaan sibutramin HCl dalam dosis tinggi berisiko
meningkatkan tekanan darah dan denyut jantung serta menyebabkan
penggunanya sulit tidur sehingga senyawa kimia itu tidak boleh dikonsumsi
secara sembarangan oleh orang yang mempunyai riwayat penyakit arteri
koroner, gagal jantung kongestif, aritmia dan stroke.
Interaksi sibutramin HCl, jikadigunakan bersamaan dengan
obat-obat yang mekanisme kerjanya menghambat oksidasi monoamine (MAOIs,
seperti selegiline), sibutramin HCl secara klinis akan menghasilkan interaksi
yang bermakna karena meningkatkan resiko serotonin syndrome
.
Selain itu,8
CYP3A4 seperti ketokonazol dan eritromisin dapat meningkatkan kadar
sibutramin HCl dalam plasma (Tjah, 2007).
Dosis sibutramin HCl yaitu oral 1 dd 10 mg, setelah 4 minggu bila
berat badan menurun < 2 kg, dapat dinaikkan sampai 15 mg, maks. Selama
1 tahun (Tjay, 2007).
Obat ini merupakan obat keras yang salah satunya kontraindikasi
dengan penyakit kardiovaskuler. Sedangkan orang yang mengalami
kelebihan berat badan (obesitas) memiliki resiko yang sangat besar untuk
menderita penyakit kardiovaskuler. Oleh karena itu sangat perlu dilakukan
konsultasi mengenai riwayat penyakit pasien dengan Dokter sebelum
memilih menggunakan sibutramin HCl (BPOM, 2006)
Sibutramin HCl menghasilkan 2 metabolit aktif yang mekanisme
kerjanya sama dengan senyawa induknya yaitu sibutramin HCl. Hal ini
dapat meningkatkan toksisitas dari obat tersebut jika dosis, frekuensi dan
lama pemberian tidak dikontrol (BPOM, 2006).
Sibutramin HClmerupakan obat golongan anoreksansia yang
berdaya menekan nafsu makan secara efektif selama 4 sampai 6 minggu
namun setelah digunakan 3 sampai 6 bulan efeknya akan sangat berkurang
akibat terjadinya toleransi. Jika terjadi toleransi, maka ketika dilakukan
peningkatan dosis (menjadi 15 mg , maksimal selama 1 tahun) perlu
pengawasan ketat dari dokter untuk menghindari efek samping obat (Tjah,
9
Resiko lain mengkonsumsi obat-obat antiobesitastanpa pengawasan
dokter adalah membuat tubuh lemas dan sistem kekebalan tubuh menurun
karena jarang makan (tetapi tidak merasa lapar), jantung berdebar-debar,
dehidrasi, sulit tidur, diare, penurunan tekanan darah, nyeri kepala, dan gula
darah menurun drastis. Namun, resiko yang timbul pada setiap orang tidak
sama, karena itu konsumsi obat-obat antiobesitas harus di bawah
10
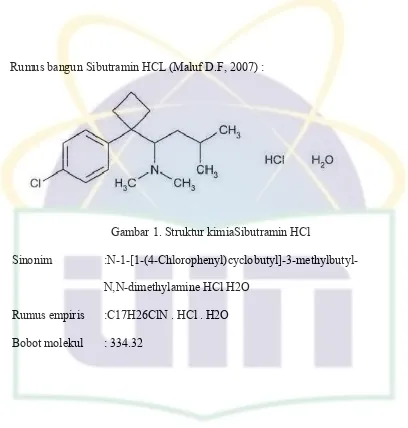
[image:22.595.130.538.67.495.2]Rumus bangun Sibutramin HCL (Maluf D.F, 2007) :
Gambar 1. Struktur kimiaSibutramin HCl
Sinonim
:N-1-[1-(4-Chlorophenyl)cyclobutyl]-3-methylbutyl-N,N-dimethylamine HCl H2O
Rumus empiris :C17H26ClN . HCl . H2O
11
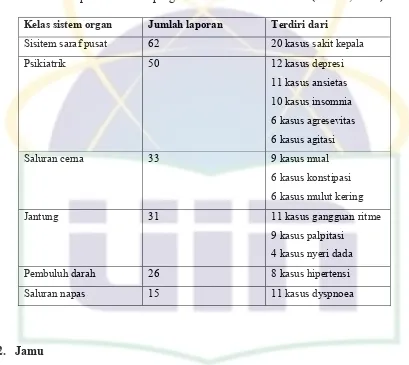
Tabel. 1 Laporan efek samping sibutramin HCldi Australia (BPOM, 2006)
Kelas sistem organ Jumlah laporan Terdiri dari
Sisitem saraf pusat 62 20 kasus sakit kepala
Psikiatrik 50 12 kasus depresi
11 kasus ansietas 10 kasus insomnia
6 kasus agresevitas 6 kasus agitasi
Saluran cerna 33 9 kasus mual
6 kasus konstipasi 6 kasus mulut kering
Jantung 31 11 kasus gangguan ritme
9 kasus palpitasi 4 kasus nyeri dada
Pembuluh darah 26 8 kasus hipertensi
Saluran napas 15 11 kasus dyspnoea
2.2. Jamu
Jamu adalah obat tradisional Indonesia. Obat tradisional didefinisikan
sebagai bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan
hewan atau mineral, bahan sarian (galenik), atau campuran bahan tersebut,
yang secara turun temurun telah digunakan untuk pengobatan berdasarkan
pengalaman (Sutrisno, 1986).
Peraturan Kepala Badan POM RI Nomor: HK.00.05.41.1384 tahun
2005 tentang Kriteria dan Tata Laksana Pendaftaran Obat Tradisional, Obat
12
boleh mengandung bahan kimia sintetik atau hasil isolasi yang berkhasiat
obat (Sutrisno, 1986).
Mutu jamu ditentukan oleh beberapa persyaratan pokok yang meliputi
komposisi yang benar, tidak mengalami perubahan fisika kimia dan tidak
tercemar bahan asing. Hal ini berarti secara kualitatif dan kuantitatif jamu
tersebut diolah dari simplisia sebagaimana tertera pada pendaftaran jamu.
Selain itu dalam ramuan jamu tidak diperbolehkan memasukkan zat
berkhasiat lain (Sutrisno, 1986).
Beberapa jenis jamu dinilai berbahaya karena didalamnya terkandung
BKO. Menurut temuan Badan POM RI, obat tradisional yang sering
dicemari BKO umumnya adalah obat tradisional yang digunakan pada
[image:24.595.137.531.186.675.2]penyakit-panyakit tertentu seperti pada tabel berikut ini (Yuliarti,2008):
Tabel. 2Jamu yang Mengandung Bahan Kimia Obat(Yuliarti,2008)
Kegunaan Obat Tadisional
BKO yang sering Ditambahkan
Pegal
Linu/Encok/Re matik
Fenilbutazon,metampiron,diklofenaksodium,piroksika m,parasetamol, prednison, atau deksametason.
13
2.3. Kromatografi Cair Kinerja Tinggi (KCKT)
2.3.1. Pendahaluan
Pada tahun 1902 Mikhael Tswett menemukan metode untuk
memisahkan pigmen daun dengan menggunakan berbagai macam
adsorben, yang kemudian pigmen daun akan tertahan di berbagai macam
adsorben yang digunakan dan membentuk pita-pita warna. Ini yang
menjadi awal mula kata kromatografi yang berasal dari bahasa yunani
“chromate” yang berarti warna dan “graph” yang berarti merekam.
Kromatografi sendiri dapat di definisikan sebagai pemisahan campuran
dengan distribusi antara dua atau lebih fase yang tidak bercampur.
Sejumlah fase tidak bercampur tersebut dapat berupa fase cair,
gas-padat, cair-cair, cair-gas-padat, gas-cair-gas-padat, dan cair-cair-padat (Rohman,
2009).
Perkembangan kromatografi dimulai pada tahun 1930-an dengan di
temukanya kromatografi lapis tipis (KLT), tahun 1940 mulai di
kembangkan kromatografi gas dan kromatografi kertas, baru pada tahun
1960an perkembangan kromatografi cair mulai di perhatikan dengan di
temukanya KCKT (Rohman, 2009).
KCKT merupakan tehnik kromtografi yang komplementer. Dalam
pengaplikasianya alat kromatografi ini dapat di kendalikan dengan
komputer disertaisoftware yang canggih dan berkemampuan untuk
memisahkan sampai 100 komponen dalam campuran yang kompleks
14
Kegunaan umum KCKT adalah untuk pemisahan senyawa organik,
anorganik, maupun senyawa biologis, analisis ketidakmurnian
(impurities), analisis senyawa non volatile baik dalam jumlah kecil,
dalam jumlah banyak dan dalam skala proses industri. KCKT merupakan
metode tidak destruktif dan dapat digunakan baik untuk analisis
kuantitatif maupun kualitatif (Gandjar & Rohman, 2007).
KCKT memiliki banyak kelebihan dibanding metode analisis
lainnya. Kelebihan tersebut diantaranya adalah
a. Waktu analisis relatif cepat.
b. Daya pisahnya cukup baik.
c. Peka.
d. Pemilihan kolom dan eluen sangat bervariasi.
e. Kolom dapat dipakai kembali.
f. Dapat digunakan untuk molekul besar dan kecil
Dapat menghitung sampel dengan kadar yang sangat rendah
(Gandjar & Rohman, 2007).
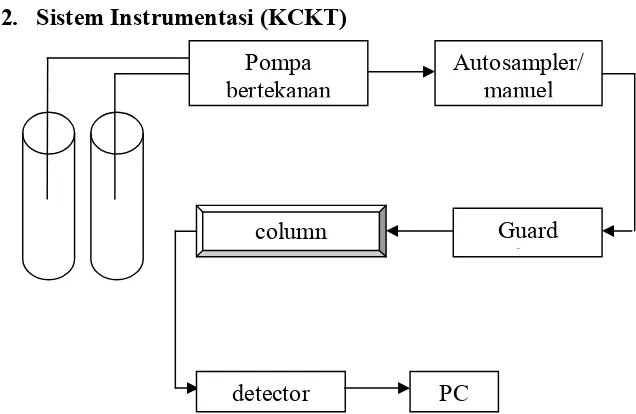
[image:26.595.166.484.525.732.2]2.3.2. Sistem Instrumentasi (KCKT)
Gambar 2. Sistem Instrumentasi KCKT(Gandjar & Rohman, 2007). Pompa
bertekanan
Autosampler/ manuel
Guard column column
15 a. Wadah Pelarut
Tempat penyimpanan pelarut untuk KCKT dengan jumlah
yang cukup untuk pengoprasian sistem KCKT. Wadah pelarut dapat
dilangkapi pengawasan secara online dan filter untuk melindungi
pelarut dari pengaruh lingkungan
b. Pompa
Berfungsi untuk menjaga aliran fase gerak ke sistem secara
konstan dan terus menerus. Sebagian besar pompa modern
memungkinkan pengaturan pencampuran berbagai macam pelarut dari
wadah pelarut yang berbeda
c. Injektor
Berfungsi untuk menginjeksikan analit agar bercampur
kedalam aliran fase gerak sebelum memasuki kolom. Sebagian
injektor modern sudah dilengkapi dengan autosamplerdimana
memungkinkan menginjeksikan sampel dengan volume yang berbeda
dari vial yang berbeda
d. Kolom
Kolom berfungsi untuk memisahkan masing-masing
komponen. Kolom yang mempunyai rantai alkil pendek umumnya
kurang stabil pada fase gerak yang sangat asam (pH < 2). Sedangkan
16
umumnya lebih stabil, namun komponen kolom ini akan tetap rusak
apabila digunakan pada pH yang sangat rendah atau sangat tinggi,
sehingga pH kondisi analisis yang digunakan sebaiknya berada pada
rentang pH 2,00-8,00, kolom yang sering digunakan adalah bahan
silika.
Selain pH, suhu yang tinggi (>400C) juga dapat merusak kolom
yang berbahan silika. Perubahan suhu kolom dapat mengubah waktu
retensi secara bermakna sehingga dapat menyulitkan analisis kualitatif
dan mempengaruhi presisi analisis kunatitatif. Analisa pada suhu yang
lebih tinggi dapat menguntungkan karena dapat mempercepat analisis,
viskositas fasegerak berkurang, transfer massa bertambah dan kelarutan
sampel dapat bertambah sehingga dapat menghasilkan resolusi yang baik
(Gandjar & Rohman, 2007).
e. Detektor
Adalah alat yang berfungsi untuk menentukan secara spesifik
karakteristik dari analit yang telah di pisahkan di dalam kolom.
Sebagian besar detektor yang digunakan dalam KCKT adalah detektor
UV-VIS, dimana detektor UV-VIS memungkinkan untuk secara terus
menerus memonitor absorbansi dari sampel dalam rentang panjang
gelombang UV-VIS. Kemunculan analit dalam detektor apabila analit
menyerap/mengabsorbansi sinar UV-VIS lebih banyak dari pada
17 f. Analisis Data dan kontrol Sistem
Adalah bagian dari KCKT yang berbasis komputer dimana semua
parameter instrument dalam KCKT (komposisi pembawa, campuran dari
beberapa pelarut, temperatur, urutan injeksi, dll) merupakan bagian untuk
mendapatkan dan mengolah data yang di dapat dari detektor (Gandjar &
Rohman, 2007).
2.3.3. Teknik Pemisahan Dalam KCKT
Sistem isokratik yaitu suatu teknik pemisahan dimana selama
proses analisis berlangsung, fese gerak atau komposisi fase gerak tidak
berubah yang berarti polaritasnya juga tetap.
Sedangkan sistem gradien adalah suatu teknik pemisahan dimana
selama analisis berlangsung komposisi fase gerak berubah secara
periodik. Teknik ini dilakukan dengan tujuan memisahkan campuran
dengan polaritas yang sangat beragam (Gandjar & Rohman, 2007).
2.3.4. Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter-parameter tertentu, berdasarkan percobaan laboratorium. Untuk
membuktikan bahwa parameter tersebut memenuhi persyaratan untuk
penggunaanya. Tujuan utama validitas adalah untuk menjamin metode
analisis yang digunakan mampu memberikan hasil yang cermat dan handal
serta dapat dipercaya (Rohman, 2009).
Beberapa parameter yang harus di uji dalam validasi metode
analisis, antara lain : selektivitas (spesifikasitas), kecermatan (akurasi),
18
detection = LOD) dan batas kuantitas (Limit of Quantitation = LOQ),
ketangguhan metode (ruggedness), dan kekuatan (robustness)(Rohman,
2009).
a. Selektivitas (spesifisitas)
Selektivitas atau spesifisitas adalah suatu metode kemampuan
yang hanya mengukur zat tertentu saja secara cermat dan seksama
dengan adanya komponen lain yang mungkin ada dalam matriks
sampel.
b. Kecermatan (akurasi)
Kecermatan adalah ukuran yang menunjukan derajat
kedekatan hasil analisis dengan kadar sebenarnya . kecermatan
dinyatakan sebagai persen perolehan kembali (recovery) analit
yang ditambahkan. Persen perolehan kembali dinyatakan sebagai
rasio antara hasil kadar yang diperoleh dengan kadar yang
sebenarnya. Syarat akurasi yang baik ; 98 – 102 %, untuk saampel
hayati (biologis atau nabati) : ± 10%
% perolehan kembali = Kadar hasil analisis x 100%
Kadar sesungguhya
c. Keseksamaan (presisi)
Presisi adalah ukuran yang menunjukan derajat kesesuaian
hasil uji individual, diukur melalui penyebaran hasil individual dari
rata-rata jika prosedur ditetapkan secara berulang pada
19
sebagai simpangan baku atau simpangan baku relatif (koefisien
variasi). Kriteria seksama diberikan jika metode memberikan
simpangan baku relatif atau koefisien variasi 2% atau kurang. Dari
penelitian dijumpai bahwa koefisien relatif meningkat dengan
menurunnya kadar analit yang dianalsis.
Perhitungan rumus koefisien variasi :
_
X = ∑ N
Presisi = simpangan baku/ simpangan devisiasi (SD)
= ( ) ½
Presisi = Koefisien variasi (KV) atau simpangan baku relatif (RSD)
= 100%
d. Liniearitas
Liniearitas adalah kemampuan metode analisis yang
memberikan respon yang secara langsung atau dengan bantuan
transformasi matematik yang baik, proporsional terhadap
konsentrasi analit dalam sampel. Rentang metode adalah
pernyataan batas terendah dan tertinggi analit yang sudah
ditunjukkan dapat ditetapkan dengan kecermatan, keseksamaan,
20
e. Batas deteksi dan batas kuantitas.
Batas deteksi adalah jumlah terkecil analit dalam
sampel yang dapat dideteksi yang masih memberikan respon
signifikan dibandingkan dengan blanko. Batas deteksi merupakan
parameter uji batas. Batas kuantitasi merupakan parameter pada
analisis renik dan diartikan sebagai kuantitas terkecil analit dalam
sampel yang masih dapat memenuhi kriteria cermat dan seksama.
Pada analisa instrumen batas deteksi dapat dihitung
dengan mengukur respon blanko beberapa kali lalu dihitung
simpangan baku respon blanko dan formula di bawah ini dapat
digunakan untuk perhitungan.
=
Q = LOD (batas deteksi) atau LOQ (batas kuantitasi)
K = 3 (untuk batas deteksi) atau 10 (untuk batas kuantitasi)
Sb = simpangan baku respon analitik dari blanko
SI = arah garis linier (kepekaan arah dari kurva antara respon
terhadap konsentrasi, atau sama dengan slope (b pada persamaan
garis y = a + bX)
Batas deteksi dan kuantitasi dapat dihitung secara statistik
melalui garis regresi linier dari kurva kalibrasi. Nilai
pengukurannya akan sama dengan nilai b pada persamaan garis
linier y = a + bX sedangkan simpangan baku blanko sama dengan
21
= ( ) dan = ( )
f. Ketangguhan metode (ruggedness)
Ketangguhan metode adalah derajat ketertiruan hasil uji yang
diperoleh dari hasil analisis sampel yang sama dalam berbagai kondisi uji
normal, seperti laboratorium, analisis, instrumen, bahan pereaksi, suhu,
hari yang berbeda, dan lain-lain. Ketangguhan biasanya dinyatakan
sebagai tidak adanya pengaruh perbedaan operasi atau lingkungan kerja
pada hasil uji. Ketangguhan metode merupakan ukuran ketertiruan pada
kondisi operasi normal antara lab dan antar analis (Rohman, 2009).
2.4 TEKNIK SAMPLING
Sampel adalah bagian dari populasi yang menjadi objek penelitian
(sampel sendiri sacara harfiah berarti contoh). Alasan perlunya
pengambilan sampel adalah sebagai berikut : keterbatasan waktu, tenaga
dan biaya; lebih cepat dan lebih mudah; memberi informasi yang lebih
banyak dan dalam; dapat ditangani lebih teliti (Nasution R, 2003).
Populasi penelitian terdiri dari populasi sampling dan populasi sasaran.
Populasi sampling adalah keseluruhan objek yang diteliti, sedangkan
populasi sasaran adalah populasi yang benar-benar dijadikan sumber data.
Pemilihan teknik pengambilan sampel merupakan upaya penelitian
22
menggambarkan populasinya. Teknik pengambilan sampel tersebut dibagi
atas kelompok besar, yaitu (Nasution R, 2003) :
1. Sampel acak atau random sampling / Probability Sampling : pada
pengambilan sampel secara random, setiap unit populasinya
mempunyai kesempatan yang sama untuk diambil sebagai sampel.
Keuntungan pengambilan sampel dengan Probability Sampling adalah
sebagai berikut :
a. Derajat kepercayaan terhadap sampel dapat ditentukan
b. Beda penaksiran parameter populasi dengan statistik sampel, dapat
diperkirakan.
c. Besar sample yang akan diambil dapat dihitung secara statistik.
Ada 5 cara pengambilan sampel yang termasuk secara random, yaitu
sebagai berikut :
a. Sampel random sederhana (simple Random sampling) :
Proses pengambilan sampel dilakukan dengan memberi
kesempatan yang sama pada setiap anggota populasi untuk menjadi
anggota sampel.
Keuntungan; proedur mudah dan sederhana
Kerugian; membutuhkan daftar seluruh anggota populasi, biaya
transportasi besar.
b. Sampel Random Sistematik ( systematic Random sampling )
Proses, pengambilan sampel, setiap urutan dari titik awal yang
23
Keuntungan; perencanaan dan penggunaannya mudah, sampel
tersebar di daerah populasi.
Kerugian; membutuhkan daftar populasi.
c. Sampel Random Berstrata ( Stratified Random Sampling)
Populasi dibagi strata-strata, (sub populasi), kemudian
pengambilan sampel dilakukan dalam setiap strata baik secara
simple random sampling, maupun secara systematik random
sampling.
Keuntungan; taksiran mengenai karakteristik populasi lebih
tepat.
Kerugian ; daftar populasi secara strata diperlukan.
d. Sampel random berkelompok ( Cluster Sampling)
Pengambilan sampel dilakukan terhadap sampling unit, dimana
sampling unitnya terdiri dari satu kelompok (cluster). Tiap
item (individu) didalam kelompok yang terpilih akan diambil
sebagai sampel.
Keuntungan; tidak memerlukan daftar populasi
Kerugian; prosedur sulit
e. Sample Bertingkat ( Multi sample sampling)
Proses pengambilan sample dilakukan bertingkat, baik
bertingkat 2 atau lebih.
Keuntungan; biaya transportasi kurang
Kerugian; prosedur sulit, prosedur pengambilan sampel
24
2. Non probability sample ( Selected Sample)
Pemilihan sampel tidak secara random. Cara ini dipergunakan : bila
biaya sangat sedikit, hasil yang diminta segera, tidak memerlukan
ketepatan yang tinggi.
Ada 3 cara yang dikenal :
a. Pusposive Sampling : sampel dilakukan hanya atas dasar
pertimbangan penelitiannya saja yang mnganggap unsur-unsur
yang dikehendaki telah ada dalam anggota sampel yang di ambil.
b. Accidental Sampling : sampel diambil atas dasar seandainya saja,
tanpa direncanakan terlebih dahulu. Juga jumlah sampel yang
dikehendaki tidak berdasarkan pertimbangan yang dapat
dipertanggungjawabkan, asal memenuhi keprluan saja.
Kesimpulan yang diperoleh bersifat kasar dan sementara saja.
c. Quota sampling : pengambilan sampel hanya berdasarkan
pertimbangan peneliti saja, hanya disini besar dan kriteria sampel
telah ditentukan lebih dulu. Cara ini dipergunakan kalau
penelitian akan dilakukan.
3. Investigasi Sampel :
Pemilihan sampel diambil secara acak dan dilihat dari nomor
registrasi yang berbeda untuk setiap sampel serta peminatan
25
2.5KERANGKA TEORI
Jamu Tradisional Antiobesitas
Peraturan Kepala Badan POM RI Nomor:
HK.00.05.41.1384 tahun 2005 tentang Kriteria dan Tata Laksana Pendaftaran Obat Tradisional, bahwa obat tradisional tidak boleh mengandung bahan kimia sintetik atau hasil isolasi yang berkhasiat obat.
Mekanisme, dosis, dan efek samping Sibutramin HCl
.
DOSIS : 10 mg - 15 mg per hari MEKANISME : secara
selektif menghambat re-uptake (penyerapan) noradrenalin, serotonin dan dopamine.
Serotonin adalah suatu neurotrasmitter di otak yang memberikan sinyal kenyang pada otak.
EFEK SAMPING : peningkatan denyut jantung, palpitasi (jantung berdebar), peningkatan tekanan darah, sakit kepala, kegelisahan, kehilangan nafsu makan,
konstipasi, mulut kering, gangguan pada alat perasa, vasodilatasi, insomnia, pusing, paraaesthesia, berkeringat dan lain-lain Metode KCKT Sistematika random sampling Standar sibutramin Validasi Preparasi sampel Penetapan kadar kesimpulan
26
BAB III
METODOLOGI PENELITIAN
3.1. Tempat dan Waktu Penelitian
Penelitian dilaksanakan mulai bulan November 2011 sampai bulan
Februari 2012 di Laboratorium Farmasi Fakultas Kedokteran dan Ilmu
Kesehatan UIN Syarif Hidayatullah Jakarta.
3.2. Bahan dan Alat
3.2.1. Bahan
a. Bahan uji
Bahan yang digunakan dalam penelitian ini adalah jamu
tradisional antiobesitas yang diperoleh dari 3toko jamu terbesar
yang berada diwilayah pasar Ciputat-Tangerang Selatan sehingga
diperoleh 6 sampel jamu.
b. Bahan kimia
Bahan-bahan kimia yang digunakan terdiri dari: metanol
grade HPLC (Merck), ammonium hidroksida (Merck), asam
format (Sigma), aquadestilasi dan bahan baku pembanding
Sibutramin HCl yang di dapat dari BPOM RI.
3.2.2. Alat
Alat-alat yang digunakan dalam penelitian ini terdiri dari:
27
x 150 mm), syiringe 5 mL, filter fase gerak 0.5µm (whatmann) dan
filter sampel 0.45 µm (nylon), Neraca anaitik (AND) ( max 220 g; min
1 mg; e=1 mg d =0,01/0,1 mg), strirer (Nouva,thermolyne), pH meter
(Horiba) , alat sentrifugasi(Eppendrorf), dan alat-alat gelas.
3.3. Metode Penelitian
3.3.1. Pemilihan Sampel
Pengambilan Sampel ini adalah jamu tradisional antiobesitas
yang diperoleh dari 3toko jamu terbesar yang berada diwilayah Pasar
Ciputat-Tangerang Selatan. Teknik pengambilan sample yang
dilakukan adalah dengan menggunakan metode sampling investigasi,
didasarkan pada peminatan masyarakat yang cukup tinggi terhadap
produk tersebut.
3.3.2. Preparasi Sampel
a. Pembuatan larutan standar sibutramin HCl
Sebanyak 50,0 mg standar sibutramin HCl ditimbang, dan
dimasukan kedalam labu ukur 100,0 mL, dilarutkan dengan fase gerak
yang digunakan sampai tanda batas, di kocok hingga homogen (500
µg/mL). Setelah itu dibuat larutan sibutramin HCl dengan konsentrasi
50,60,70,80, dan 90 µg/mL.
b. Pembuatan fase gerak
Sebanyak 700 mL metanol dan 300 mL buffer (asam format
0.05%, pH adj 3.5 dengan ammonia), dimasukkan kedalam labu ukur
1000 mL. Dikocok hingga homogen dengan menggunakan incubator
28
3.3.3. Validasi Metode
a. Pembuatan kondisi analisis optimum
Kondisi analisis yang digunakan pada saat percobaan, yaitu fase gerak
(metanol:buffer) dengan perbandingan (70:30); (60:40); (50:50);
(45:65), Volume injeksi 10 µL;20 µL; 40 µL dan 50 µL, panjang
gelombang 225 nm dan 254 nm.
b. Uji Kesesuaian Sistem
Larutan standar sibutramin HCl dengan konsentrasi 40 µg/mL
disuntikkan ke dalam KCKT, lalu di hitung jumlah teoritical plate dan
efesiensi kolom.
c. Pembutan kurva kalibrasi
Larutan standar 50;60;70;80;dan90 µg/mL masing-masing
diinjekkan sebanyak 10 µL kedalam KCKT pada kondisi terpilih.
Luas puncak yang diperoleh dicatat, dan dibuat kurva antara luas
puncak dengan konsentrasi larutan.
d. Pengujian batas deteksi dan batas kuantitasi
Batas deteksi dan batas kuantitasi dihitung secara statistik
melalui garis regresi linier dari kurva kalibrasi.
e. Uji keterulangan (presisi)
Larutan standar 50; dan 70 µg/mL disuntikkan sebanyak 10 µL
kedalam KCKT pada kondisi terpilih, diulang sebanyak 5 kali,
29 f. Uji perolehan kembali (akurasi)
Sebanyak 5 mg standar sibutramin HCl ditimbang, dan
ditambahkan sampel jamu antiobesitas dari tanaman jati belanda
(Guazumae Folium) sebanyak 1 gram. Kemudian dilarutkan dalam 100
mL metanol,dikocok dengan stirrerselama 30 menit kemudian saring
dengan penyaring whatmann, ambil filtrat kemudian di oven pada suhu
400C hingga metanol menguap kemudian di larutkan dengan fase gerak
sebanyak 2 mL dan di sentifugasi pada kecepatan 5000 RPM selama 15
menit, saring dengan penyaring nylon 0,45 µm, dimasukkan kedalam
vial2 mL. Sampel disuntikkan sebanyak 10 µL kedalam KCKT.
Perlakuan yang sama dilakukan terhadap sampel tanpa standar
sibutramin HCl. Kemudian di catat luas puncaknya. Dari data tersebut
yaitu sampel dengan sibutramin HCl dan sampel tanpa sibutramin HCl
ditentukan persen perolehan kembali(% UPK).
3.3.4. Penetapan kadar sibutramin HCl dalam Sampel
Sampel jamu antiobesitas ditimbang sebanyak 1 gram,
kemudian dilarutkan dalam 100 mL metanol, dikocok dengan stirer
selama 30 menit kemudian saring dengan penyaring whatmann, ambil
filtrat kemudian di oven pada suhu 400C hingga metanol menguap
kemudian di larutkan dengan fase gerak sebanyak 2 mL dan di
sentifugasi pada kecepatan 5000 RPM selama 15 menit, saring dengan
30
disuntikkan sebanyak 10 µL kedalam KCKT. Percobaan di ulang
sebanyak 3 kali. Kadar sibutramin HCl di hitung dengan menggunakan
31
BAB IV
HASIL DAN PEMBAHASAN
4.1 HASIL
4.1.1 Hasil Uji Efisiensi Kolom
Jumlah teoritical plate yang diperoleh 2798, efesiensi kolom yang
[image:43.595.114.549.65.502.2]diperoleh 0,0053 cm dan persen area yang diperoleh 100%.
Tabel 3. Uji efisiensi kolom pada sibutramin HCl
No Rt Peak name Height Area Rel.Area Amount Plates HETP
% Ppm (USP)
1. 4.47 sibutramin 39,644 10,179 100 40 2798 0,0053
Spesifikasi Kolom : Acclaim ® C-18; 3 µm; 4.6 x 150 mm
Detektor : UV-VIS, λ = 225 nm
Fase gerak : Metanol-Buffer (asam format 0.05%, pH adj 3.5
dengan ammonia) (70:30)
Laju alir : 1,0 mL/menit
Volume injeksi : 10 µL
32
4.1.2 Hasil Uji Perolehan Kembali (UPK) / Recovery Kadar Sibutramin
[image:44.595.119.536.87.454.2]HCl dengan Alat KCKT
Tabel 4. Uji UPK / Recovery Sibutramin HCl dengan alat KCKT
No
Kadar
Sibutramin HCl
40 50 70
1 10,3047 9,6093 14,0015
2 10,1778 9,5556 14,2255
3 10,1777 9,6093 14,3416
4 10,3048 9,5699 14,0096
5 10,1778 9,5618 14,3681
rata-rata 10,2286 9,57956 14,1893
SD 0,38% 0,27% 1,24%
UPK 101,57% 99,42% 100,75%
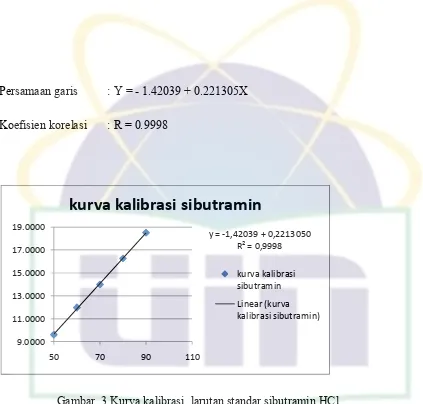
4.1.3 Hasil Penetapan Kurva Kalibrasi
Hasil linieritas diperoleh dengan membuat kurva kalibrasi. Kurva
kalibrasi dibuat dari larutan standar konsentrasi 50; 60; 70; 80; dan 90
µg/mL.
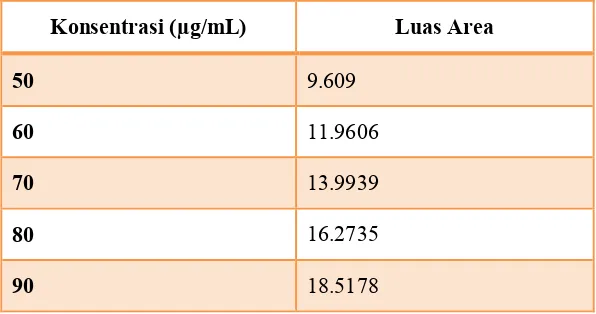
Tabel. 5 Hasil kurva kalibrasi Sibutramin HCl
Konsentrasi (µg/mL) Luas Area
50 9.609
60 11.9606
70 13.9939
80 16.2735
[image:44.595.163.461.586.743.2]33
Persamaan garis : Y = - 1.42039 + 0.221305X
[image:45.595.114.537.68.472.2]Koefisien korelasi : R = 0.9998
Gambar. 3 Kurva kalibrasi larutan standar sibutramin HCl
y = -1,42039 + 0,2213050 R² = 0,9998
9.0000 11.0000 13.0000 15.0000 17.0000 19.0000
50 70 90 110
kurva kalibrasi sibutramin
34
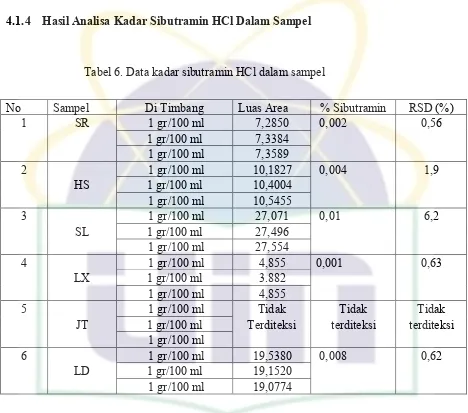
[image:46.595.107.575.71.484.2]4.1.4 Hasil Analisa Kadar Sibutramin HCl Dalam Sampel
Tabel 6. Data kadar sibutramin HCl dalam sampel
No Sampel Di Timbang Luas Area % Sibutramin RSD (%)
1 SR 1 gr/100 ml 7,2850 0,002 0,56
1 gr/100 ml 7,3384
1 gr/100 ml 7,3589
2 1 gr/100 ml 10,1827 0,004 1,9
HS 1 gr/100 ml 10,4004
1 gr/100 ml 10,5455
3 1 gr/100 ml 27,071 0,01 6,2
SL 1 gr/100 ml 27,496
1 gr/100 ml 27,554
4 1 gr/100 ml 4,855 0,001 0,63
LX 1 gr/100 ml 3.882
1 gr/100 ml 4,855
5 1 gr/100 ml Tidak Tidak Tidak
JT 1 gr/100 ml Terditeksi terditeksi terditeksi 1 gr/100 ml
6 1 gr/100 ml 19,5380 0,008 0,62
LD 1 gr/100 ml 19,1520
1 gr/100 ml 19,0774
Dari tabel di atas dapat dilihat bahwa kadar sibutramin HCl tertinggi
terdapat pada jamu dengan kode SL dengan kandungan sibutramin HCl sebesar
0,01% dan pada jamu dengan kode JT tidak teridentifikasi adanya kandungan
35
4.2 PEMBAHASAN
Berdasarkan hasil analisis yang dilakukan terhadap 6 jenis jamu
tradisional antiobesitas yang beredar di kota Ciputat-Tangerang Selatan,
terdapat 5 jenis jamu yang teridentifikasi adanya sibutramin HCl. Penelitian
dilakukan karena mengingat banyaknya jamu tradisional antiobesitas yang
ditarik dari peredaran karena mengandung bahan kimia obat (BKO), dimana
salah satunya adalah sibutramin HCl. Menurut Peringatan Badan POM RI
No. KH.00.01.43.2773/2008 tentang obat tradisional mengandung BKO,
sibutramin HCl tidak boleh terdapat dalam jamu tradisional antiobesitas.
Kesalahan fatal yang dilakukan oleh produsen jamu adalah menggunakan
sibutramin HCl sebagai bahan campuran dalam pembuatan jamu tradisional
antiobesitas. Sibutramin HCl secara sengaja ditambahkan ke dalam jamu
tradisional untuk menjadikan jamu tersebut semakin berkhasiat secara instan.
Analisis sibutramin HCl dalam jamu antiobesitas ini di awali dengan
pemilihan sampel, teknik sampel yang di gunakan pada penelitian ini adalah
dengan teknik investigasi sample, sampel ini di ambil dari tiga toko jamu
terbesar yang berada di pasar Ciputat-Tangerang Selatan dan sampel yang
dicari yaitu jamu antiobesitas dengan minat masyarakat paling tinggi
diperoleh 6 jamu antiobesitas.
Pada penelitian ini untuk mengidentifikasi senyawa sibutramin HCl pada
jamu antiobesitas saya menggunakan alat HPLC dengan tujuan mendapatkan
pemisahan senyawa yang baik dan proses analisis barlangsung dalam waktu
36
perhatikan kualitas dari kromatogramnya. Parameter-parameter yang dapat
digunakan untuk mengetahui kualitas suatu kromatogram, yaitu : waktu
tambat, faktor kapasitas, jarak setara plat teori, resolusi dan faktor simetri.
Dimulai dari uji kesesuaian sistem, Pada pengujian ini dilakukan
menggunakan sampel dengan standar 40 ppm, dimana pada sampel ini
terdapat tiga macam puncak, dua buah puncak yang berukuran besar adalah
puncak-puncak yang dihasilkan oleh analit yang tertahan pada fasa diamnya
pada sistem kesetimbangan distribusi yang tegas (dinamis). Di samping itu
terdapat puncak kecil yang dihasilkan oleh analit yang tidak tertahan oleh fasa
diam, namun bersama fasa gerak keluardari kolom dengan kecepatan yang
sama dengan kecepatan fasa geraknya.Selang waktu yang diperlukan oleh
analit mulai saat injeksi sampai keluar dari kolom dan sinyalnya secara
maksimal ditangkap oleh detektor disebut sebagai waktu tambat atau waktu
retensi (retention time / tR). Sedangkan waktu tambat analit yang tidak
tertahan pada fase diam atau sering disebut sebagai waktu tambat pelarut
pengembang dinyatakan to. Dan pada sampel ini menunjukan tR pada (4.47 ).
Parameter lain yang digunakan untuk mengetahui efisiensi suatu kolom
kromatografi adalah Jumlah plat teori (N) dimana banyaknya distribusi
keseimbangan dinamis yang terjadi didalam suatu kolom. Pada sampel ini
menunjukan Jumlah teoritical plate yang diperoleh 2798karena syarat
teoritical plate yang baik yaitu lebih besar dari 2500 (Harmita, 2006) maka
nilai yang diperoleh ini menunjukan hasil yang baik, untuk nilai rata-rata
efesiensi kolomnya yaitu 0,00571 maka kolom dikatakan baik dan efisien
37
adalah 100 % maka hal ini menunjukkan bahwa sistem analisis beroperasi
secara benar dan sesuai untuk uji identifikasi sibutramin HCl.Dalam proses
pemisahan menghasilkan harga N yang besar. Dan pada umumnya efisiensi
kolom HPLC meningkat dengan semakin kecilnya ukuran partikel yang ada
didalam kolom serta Makin besar harga N/L atau makin kecil harga H maka
makin efisien kolom yang dipakai untuk pemisahan.
Pemilihan instrumentasi HPLC yang digunakan juga sangat mendukung
hasil kualitas kromatogram yang baik, injektor yang digunakan adalah sistem
injektor otomatis (autoinjektor) mempunyai cara kerja yang lebih baik dan
Keuntungan sistem ini adalah volume yang diinjeksikan tidak akan berkurang
selama proses injeksi dan mampu memisahkan sampel-sampel dalam jumlah
yang banyak dan dalam waktu yang singkat. Selanjutnya pemilihan Kolom
pada HPLC merupakan bagian yang sangat penting, sebab pemisahan
komponen-komponen sampel yang akan terjadi didalam kolom. Kolom yang
digunakan Kolom fasa terbalik(Reversed Phase Column)karena fasa diamnya
bersifat non polar yaitu menggunakan silika gel jenis kolom Acclaim ® C-18;
3 µm; 4.6 x 150 mm, sedangkan fasa geraknya bersifat polar yaitu
menggunakan metanol dan buffer asam format 0,05% pH 3,5 dengan
penambahan ammonia, pemilihan fase gerak ini didasari dari penelitian yang
pernah dilakukan sebelumnya (L.ding, 2003). Pada teknik pemisahan dalam
HPLC menggunakan Sistem isokratik karena selama proses analisis
berlangsung, fese gerak atau komposisi fase gerak tidak berubah yang berarti
38
Untuk membuktikan bahwa parameter yang digunakan dapat
memenuhi persyaratan maka dilakukan uji validasi. Menurut USP metode
validasi ini bertujuan untuk menjamin metode analisis yang digunakan
mampu memberikan hasil yang cermat dan handal serta dapat dipercaya.
Parameter yang digunakan dalam uji ini meliputi uji presisi, serta uji
linieritas.
Penelitian dilanjutkan dengan menguji perolehan kembali (UPK),
UPK adalah ukuran yang menunjukan derajat kedekatan hasil analisis dengan
kadar sebenarnya . UPK dinyatakan sebagai persen perolehan kembali
(recovery) analit yang ditambahkan. Persen perolehan kembali dinyatakan
sebagai rasio antara hasil kadar yang diperoleh dengan kadar yang
sebenarnya. Syarat akurasi yang baik ; 99 – 101 % (Lakshmana Rao et al,
2011) dimana sampel jamu antiobesitas di tambahkan dengan standar baku
sibutramin HCl kemudian dilarutkan dalam metanol, dikocok dengan stirrer
selama 30 menit kemudian di saring dan di uapkan dalam oven pada suhu
400C hingga metanol menguap, hal ini bertujuan untuk memisahkan
sibutramin HCl dengan komponen – komponen lain yang terdapat pada jamu
antiobesitas. Kemudian di larutkan dengan fase gerak dan di sentifugasi pada
kecepatan 5000 RPM selama 15 menit, saring dengan penyaring nylon 0,45
µm, dimasukkan kedalam vial 2 mL. Sampel disuntikkan sebanyak 10 µL
kedalam KCKT. Perlakuan yang sama dilakukan terhadap sampel tanpa
standar sibutramin HCl. Kemudian di catat arenya. Hasil data UPK yang di
dapat adalah 101.09 %. Hal ini menunjukan nilai UPK yang baik karena
39
Penentuan parameter validasi dilanjutkan dengan uji linieritas.
Linieritas merupakan kemampuan suatu metode untuk memperoleh
hasil-hasil uji secara langsung proporsional dengan konsentrasi analit pada kisaran
yang diberikan. Dari percobaan dengan lima seri konsentrasi standar, yaitu
50; 60; 70; 80; dan 90 µg/mL. Mula-mula dibuat larutan induk 500 µg/mL
pada labu ukur 100 mL, kemudian dilakukan pengenceran hingga mendapat 5
seri konsentrasi standar. Dari hasil analisis deret standar tersebut didapat area
kromatogram yang berbeda-beda. Nilai dari luas area diplotkan kedalam
sumbu-Y, sedangkan deret standar diplotkan ke dalam sumbu-X, sehingga
terciptalah kurva kalibrasi dengan persamaan garis Y= - 1,42039 +
0,221305X. dari persamaan tersebut didapat nilai intersep yang dilambangkan
dengan a= 1,42039 yang berarti kurva tersebut memotong sumbuY di titik
-1,42039. Sedangkan nilai b= 0,221305. Nilai b merepresentatifkan nilai slope
atau kemiringan dari kurva tersebut. Sedangkan untuk nilai r = 0,99998. Nilai
r merupakan koefisien korelasi. Syarat diterimanya koefisien korelasi adalah
jika r ≥ 0,999 (Lakshmana Rao et al, 2011). Jika ditinjau hasil nilai r pada
percobaan ini yaitu 0,99998, maka hal ini menunjukkan bahwa nilai koefisien
korelasi lebih besar dari 0,999 sehingga kurva kalibrasi sibutramin HCl
memberikan nilai linieritas yang baik, dan penetapan kadar dengan kurva
kalibrasi terjamin kebenarannya.
Hasil uji dari parameter validasi metode analisis yang dilakukan dapat
memenuhi syarat yang ditetapkan. Hal ini menunjukan bahwa metode analisa
sibutramin HCl pada jamu antiobesitas dengan meggunakan metode KCKT
40
Dari hasil penetapan kadar sibutramin HCl tersebut, didapat nilai area
sibutramin HCl pada masing-masing sampel. Nilai dari masing-masing area
tersebut disubtitusikan sebagai nilai Y ke dalam persamaan garis kurva
kalibrasi Y= - 1,42039 + 0,221305X, sehingga didapatlah nilai X sebagai
konsentrasi dari sibutramin HCl. Dari hasil pemeriksaan kadar sibutramin
HCl pada jamu tradisional antiobesitas yang memiliki kadar sibutramin HCl
terendah sampai tertinggi yaitu jamu dengan nomor kode LX (1,07 mg/g), SR
(2,7 mg/g), HS (4,07 mg/g), LD (8,05 mg/g), SL (11,7 mg/g).
Berdasarkan hasil analisis yang dilakukan, diperoleh kadar sibutramin
HCl dalam jamu tradisional antiobesitas yang beredar di kota Ciputat masih
dalam rentang syarat dosis yang di perbolehkan. Dosis sibutramin HCl dalam
bentuk obat antiobesitas maksimal 15 mg. Namun walaupun demikian
sibutramin HCl mutlak tidak di perbolehkan terdapat dalam jamu tradisional
antiobesitas sesuai dengan Badan POM RI No. KH.00.01.43.2773/2008
tentang obat tradisional mengandung BKO (BPOM, 2006).
Penggunaan Sibutramin HCl yang tidak di bawah pengawasandokter dan
penggunaan yang tidak tepat, dapat meningkatkan tekanandarah dan denyut
jantung serta sulit tidur(BPOM, 2006).Mengingat efek samping dari
mengkonsumsi sibutramin HCl dalam dosis yang berlebih dan dalam jangka
waktu panjang, maka perlindungan terhadap masyarpakat harus lebih
diperhatikan. Tindakan tegas harus diambil bagi industri yang memproduksi
jamu tradisional antiobesitas serta pengawasan yang terus menerus harus
41
danMakanan untuk tetap secara konsisten mencari dan menemukan produk
42
BAB V
KESIMPULAN
5.1 Kesimpulan
Berdasarkan hasil analisa sibutramin HCl yang dilakukan pada 6
sampel jamu tradisional antiobesitas yang beredar di kota
Ciputat-Tangerang Selatan, maka dapat disimpulkan:
1) kondisi optimasi analisis pada KCKT yang digunakan yaitu dengan
detektor UV-VIS, λ = 225 nm; kolom C-18; 3 µm (4.6 x 150 mm); fase
gerak metanol-buffer (asam format 0.05% dengan penambahan ammonia
sampai pH 3.5) (70:30); laju alir 1,0 mL/menit; volume injeksi 10 µL;
dan model elusi isokratik. Hasil uji (LOD) sibutramin HCladalah 0,32
µg/mL, sedangkan LOQ adalah 1,08 µg/mL, hasil uji presisi sibutramin
HCl pada konsentrasi 50 didapat RSD = 0,27% dan pada konsentrasi 70
µg/mL didapat RSD = 1,24%, dan hasil uji (UPK) adalah 101.09 %.Hasil
uji parameter validasi metode analisis yang dilakukan dapat memenuhi
syarat yang ditetapkan.
2) Dari 6 sampel jamu antiobesitas yang di analisa, terdapat 5 sampel yang
positif mengandung sibutramin HCl.Kadar yang diperiksa bervariasi yaitu
jamu dengan kode LX (1,07 mg/g), SR (2,7 mg/g), HS (4,07 mg/g), LD
(8,05 mg/g), SL (11,7 mg/g).
43
Bagi peneliti selanjutnya perlu dilakukan uji identifikasi sibutramin HCl
pada jamu antiobesitas lain yang beredar di masyarakat dengan
menggunakan metode analisis yang berbeda atau dengan metode KCKT
44
DAFTAR PUSTAKA
A.P. Suthar et al. 2009. A Validated Specific Reverse Phase Liquid
Chromatographic Method for the estimation of Sibutramine
Hydrochloride Monohydrate in bulk drug and capsule dosage forms.
Int.J. ChemTech Res.Vol.1, No.4, pp 793-801.
Anonim, 1997, FDA Talk Paper, FDA Approves Sibutramine To Treat
Obesity, http://fdahomepage.html, diakses tanggal 15 Maret 2009.
Anonim, 2006, Drug Information Handbook, 14th Edition, 1444-1446, Lexi
Comp, Ohio, diakses tanggal 15 November 2011.
Anonim, 2007, Efek Samping Meridia, dan Interaksi Obat".RxList.com, 05
November 2011
Anonim, 2008, Sibutramine Turunkan Berat Badan,
http://princessraia.blogspot.com, diakses tanggal 15 Maret 2009
Anonim, 2008, Tanggung Jawab Badan Pengawas Obat dan Makanan
Terhadap Konsumen Obat Tradisional Yang Mengandung Bahan
Kimia Obat ( BKO ), http://pustaka.net, diakses tanggal 15 Maret
2009.
Anonim, 2009, Meridia, http://rxlist.com, diakses tanggal 15 November
2011.
Anonim, 2011,
http://www.chemnet.com/cas/my/106650-56-0/Sibutramine.html, diakses tanggal 30 Desember 2011.
Badan Pengawas Obat dan Makanan Republik Indonesia. Peringatan
Kepada Masyarakat Nomor KH.00.01.1.034 Tanggal 20 Agustus 2005
45
Bahan Kimia Obat Keras Sibutramin HCl. www.pom.go.id. 15
November 2011, pukul 14.45.
Badan Pengawas Obat dan Makanan Republik Indonesia. Info POM. Vol. 7,
No. 4, Juli 2006.www.pom.go.id. 10 November 2011, pukul 16.45.
Badan Pengawas Obat dan Makanan Republik Indonesia. Peringatan Nomor
: KH.00.01.1.43.2397. Tanggal : 4 Juni 2009. TentangObat
Tradisional Dan Suplemen MakananMengandung Bahan Kimia Obat.
www.pom.go.id. 14 Oktober 2011, pukul 14.05.
Badan Pengawas Obat dan Makanan Republik Indonesia. Peringatan Nomor
: HM.03.03.1.43.08.10.8013Jakarta, 13 Agustus 2010. Tentang Obat
tradisional mengandung bahan kimia obat. . www.pom.go.id. 15
November 2011, pukul 14.45.
Gandjar, I. G dan Abdul Rohman. 2007. Kimia Farmasi Analisis. Pustaka
Relajar. Yogyakarta
Hermanto dan subroto, 2007. Pilih Jamu dan Herbal Tanpa Efek Samping,
Penerbit PT Elex Media Komputindo, Jakarta.
Jeanette Woolard, Terence Bennett, William R. Dunn, David J. Heal, Susan
Aspley, and Sheila M. Gardiner. 2003. Acute Cardiovascular Effects
of Sibutramine in Conscious Rats. JPET 308:1102–1110, 2004. Vol.
308, No. 3. USA.
Kurniadi M, Kawira JA, Detri S. Identifikasi Obat Antiinflamasi Non
Steroid dalam Jamu Pegal Linu Secara Kromatografi Lapis Tipis.
46
Obat Bahan Alami II. Depok: Jurusan Farmasi FMIPA UI, 1999:
341-355.
Lakshmana Rao et al. 2011. A Stability Indicating HPLC Method for the
Determination of Sibutramine Hydrochloride in Bulk and Commercial
Formulations. IJRPC.
L. Ding et al, 2003. Simultaneous determination of sibutramine and its
N-desmethyl metabolites in human plasma by liquid chromatography–
electrospray ionization–mass spectrometry Method and clinical
applications.Analytica Chimica Acta 492 (2003) 241–248.
M.J. Bogusz et al. 2005. Application of LC–ESI–MS–MS for detection of
synthetic adulterants in herbal remedies. Journal of Pharmaceutical
and Biomedical Analysis 41 (2006) 554–564.
Maluf D.F., Farago P.V., Barreira S.M.W., Pedroso C.F. & Pontarolo R.
2007. Validation of an Analytical Method for Determination of
Sibutramine Hydrochloride Monohydrate in Capsules by Uv-Vis
Spectrophotometry. Lat. Am. J. Pharm. 26 (6): 909-12.
Mayasari B, Eka. 2009. Analisa Metampiron Pada Jamu Tradisional yang
Beredar di Kota Medan Tahun 2009, Skripsi. Fakultas Kesehatan
Masyarakat Universitas Sumatra Utara, Medan.
Nasution R. 2003. Teknik Sampling. FKM Universitas Sumatra Utara.
Oktora, Lusia, 2006.Pemanfaatan Obat Tradisional dengan Pertimbangan
Manfaat dan Keamanannya, Majalah ilmu Kefarmasian, Vol III, No
47
Rohman, Abdul. 2009. Kromatografi Untuk Analisis Obat. Edisi pertama.
Graha Ilmu : Yogyakarta.
Saefudin, Aziz; Rahayu; Viesa; Teruna; Hilwan Yuda. 2011. Standarisasi
Bahan Obat Alam. Edisi pertama. Yogyakarta: Graha Ilmu.
Sofian Kanan, Imad A. Abu-Yousef, Conjeevaram Gunasekar, Naser Abdo
and Srinivasan Narasimhan.Detection and Quantification of Synthetic
Drugs in HerbalSlimming Formula. European Journal of Scientific
Research ISSN 1450-216X Vol.34 No.3 (2009), pp.348-357.
http://www.eurojournals.com/ejsr.htm.
Subagja. 2009. Optimasi Metode Analisis Katekin dan Epikatekin dalam Biji
Kakao Serta Produk Olahannya Secara Kromatografi Cair
Spektrometri massa, Skripsi. Prodi Farmasi Fakultas Matematika dan
Ilmu Pengetahuan Alam Program Pasca Sarjana Universitas
Indonesia, Depok.
Sutrisno B, 1986. Analisis Jamu. Edisi pertama. Jakarta : Fakultas Farmasi
Universitas Pancasila.
Tjay, Tan Hoan, dan Kirana Rahardja, 2007. Obat-Obat Penting, Edisi
Keenam, 497-499, Elex Media Computindo, Jakarta.
Vepriati, Neti, 2008. Awas, Obat Tradisional Mengandung Bahan Kimia
Obat. http://dinkeskabkulonprogo.org/. Diakses tanggal 20 Oktober
2011
Yuliarti, Nurheti, 2008.Tips Cerdas mengkonsumsi Jamu, Penerbit Banyu
59
[image:71.595.115.560.67.487.2]Lampiran 5. Gambar alat-alat
'l:i Lampiran i. Sertifikat pengujian Sibutramin HCI
F."r:[un
.
I Serbuk hablur warna putihldentifikasi :
spektrofotometri lnframerah :.Dispersi lebih kurang 2 mg zat dalam lebih kurang
200 mg kaliLim hromio, rnenunlukkan spoktrum inframorah seperil yans reic6niu";d.6-;fi;;
ie,s"y &vv ,,,r
,,Kffitrr-"-s
: B ercak p"di ilffi;dd;;iili[^
;, ;a;lfo,i"iarn ukuran densa q bercak
-_-BADAN POM RI
.,rffiA
No, Kontrol 110395 Tujuan ponggunaan :
Beku Pombandlns srbufram,n Hidroktorrda no. kinrror 11039s dapat drgunakan sebi q 'lam ldentlllkasl-mensgunakan
rputitrorotomutJiiijirJ,riur"r, o.r''ri,i,,i.iJjili"ffi"i|,:i
ffiT:il:'*: ffiltJi::**" kromatosralicalr kinerJa tlneei;;;il;';;eiapan raoar secJiu'xirli"togr.r carr ktnerja
!.U6ulrh . ,rrr .
'Qambar 3- l(omatograrp KCKT penetapan kadar siburramin Hidroklorida I 5,8170.(n'= { Sb = 0,i0%)
gica+ {LnelglfEg! : Memenuhi kriteria. Jumlah area.sernua Kromatogram larutan uji adalah 0,0Zyo.
dengap kromatogram
5ffin":!!!:,*,,!:1,,,:]n-=6)c',H,6ClN.HCldihitungterhadapzatyangtelah
fl
f *:mI",.yffi
F;,1"!"n,i1v;'ilJJ;ri',"i:H"#ffi"JlKesimpuran
i
surtoiii mi,o-xiiii"il:'flffi1i'1?frB8'x3iiidinyarakan Ep*K\trarmakope tndonesia
"uru.i denoln ddngan tujuan p.ngg.1n"rnnyu,i;;;;;"""",,^...,.
:sebagal Baku
: Dalam wadah lertutup baik, terlindung dari cahaya.
Qbaf dan Makanan Nasional Laboratorium Bahan Baku pembanding
2 001
EADAN
. J!. perieioko:, P.ENGAWAS Negc.o No. A3, Jokorlc OB.A; ?u;flt lO5rO I)AN ,",0. ,r*rO)j,i"r.'MTlKAN .Gambar 1. Spektrum
infram erah Sibutramin HC!
altlSES!'S$rdti!ffi A gt lq
l.!l91l tain setain puilcafffi;paG
sepeni yang lercantum dalam gambar
2.
48
Lampiran 2. Hasil kurva kalibrasi sibutranrin IICI
<1 - SIBUTRAMIN6#1
<2 - SIBUTRAMINo#1
std 90ppm
std 90ppm UV-VIS_UV_VIS_
iiv--yi$-- UV_VIS-ii.ir--viq..
UV VIS
1 1 I 1 .t 1 -:.13 - $iiiiji'R,,\!',4iN$
S?
stcf 5$pp*r-':.3 - SIBUTRAMINO #3 [modified by Administratcr]
" 3 - #i'3Li'l'"*.Afulii\ii #"1 .,i';i.3 ii'iii:;i::i;
::6 - SIBUTRAMINo #5
VltlL:225
Sampel NO
simpel
name Ret Time
IruN
sibutramiri
rlv
vls I
Area mAU*min sibutramin
UV
\rIS
I
Lleight mAU sibutramin
uvwsl
Amount ppm sibutraminuv
\.Is
1I std 90pom 4-440 18.7080 67-79 '90.9866
2 std 80ppm 4.450 t6.2208 57-53 78,8901
3 std 70ppm 4.473 13.9657 49.72 70.8612
4 std 60pom 4.487 I 1.8312 40.28 60,0309
5 std 60porn 4.473 9.6093 34,11 48.1573
average : 4,465 14,0670 49.886 69,9052
Lampiran 3. Hasil Uji Perolehan Kembali
[image:74.600.76.552.67.615.2]1-0.383 I
\,-z_3.2!33.577
_e_s.0j0Gambar 5. Blanko
)
50 Ret.Time
min
Height
mAU
mAt!'minArea1 2 q 4 5 6 7
I
I
0.38
n.a.1.74
n.a.1.87
n.a.2.02
n.a.2.37
n.a.2.66
n.a.3.29
n.a..3.68
n-a.5.01
n.a.0.592
1.6230.09't
82.3&0.359
0.980.119
0.320.238
0.650.197
0.140.767
2.100.829
2.272.898
7.93n.a
BMBn.a.
BMn.a
Rdn.a.
Rdn.a.
Rdn.a.
Rdn.a.
Mn.a.
Mn.a.
M2.227 50.521 4.383 1.006 q.e23 2.09s 3.095 2.681 3.291
Ret.Zeit min
Height
Width
Type
Resol1 2 3 4. 5 o 7 B 9 10 11 12
0.643 n.a.
1.CI87 n.a.
1.72O n.a.
2.460 n.a.
2.530 n.a.
2.720 n.a.
3-177 n.a.
3,330 n.a.
3-737 n.a.
4.317 sibutramin 5.500 n.a.
6.517 n.a.
1.237
0.6320.004
n.a.15.838
0.8883.924
1.3590.090
n.a.0.277
n.a.0.014
n.a.0.025
n.a.0.206
n.a.45.030
0.3010.849
s.2300.675
0.739 [image:75.612.75.571.51.621.2]BM MB BM M Rd Rd Rd Rd Rd M M MB 17 n.a. 79 n.a. n.a. n.a. n.a n.a. n.a. n.a. n-4. n.ar n.a. n.a. n.a. n.a. n.a. n.a. n.a. 0.74 n.a. n.a. n.a, n.a. Il.?. n.a n.a. n.a. 1.66 n.a. n.a. n.a. n-4. 3358 n.a. 998
)
Gambar 6. Blanko
*
sampel baku banding sibutramin HCISample
Sample NameNo'
1
UPK jr2
UPKit3
UPKAverage: Rel.Std.Dev:
Ret.Time
Area
Height
erno@
rnin
mAU*min
mAU (usP)sibutram in s ibutramin si butramin sib utram in sibutram ir sibutram UV-VIS-1 UV-VIS_I UV-VI.S-1 UV-VIS-1 UV.-VIS 1 UV VIS 1
4.317 9.7785
45.03
50.0618
M
32914.313 9.7314
44.88.
49.8207
M
33081.310 9.7894
44.82
50.1175
M
32ss4.313 9.7664
44.91
50.0000-
32ss0.a77
%
0.3't60/o0.241%
0.316 % 0.258Gambar.
4
Kromatogram SamPel HSLampiran 4. Hasil Uji Identifikasi Jamu
9 - 4.130
10-sibutramin-4.477
No Rt Nama peak Luas area
1 4.23 n.a; 1.939
2 1.76 n.a. 10.113
3 2.O2 n.a. 13.770
4 2.21 n.a. 0.465
5 2.39 n.a. 0.394
6 2.63 n.a. 0.234
7 3.09 n.a. 1.481
8 3.67 n.a. 0.323
9 4.13 n.a- 12.746
10 4.48 sibutramin 10.4004
11 5.83 n,a. 0.