LAMPIRAN A
DATA HASIL PERCOBAAN
L-A.1 DATA HASIL PENCUCIAN ADSORBEN PASIR PUTIH Berikut merupakan hasil pencucian adsorben pasir putih L-A.1.1 Data pencucian adsorben pasir putih
Tabel L-A.1. Data pencucian adsorben pasir putih
L-A.2 DATA PENGERINGAN ADSORBEN PASIR PUTIH Berikut merupakan hasil pengeringan adsorben pasir putih L-A.2 Data pengeringan adsorben pasir putih
L.A.3 DATA HASIL REMOVAL EFISIENSI DENGAN VARIASI KONSENTRASI SURFAKTAN
Tabel L-A.3 Data hasil removal efisiensi dengan berbagai variasi konsentrasi surfaktan dan kecepatan pengadukan shaker
Konsentrasi
L.A.4 DATA PENENTUAN KINETIKA DESORPSI PADA KONSENTRASI SURFAKTAN (SDS) 2 CMC 100 RPM
LAMPIRAN B
Maka, dilarutkan 0,593 g Cd(CH3COO)2.2H2O dengan aquadest hingga volume
larutan mencapai 5 liter.
B.2 Perhitungan Kapasitas Adsorpsi
Untuk pH 4,5 dan konsentrasi larutan 50 ppm (Konsentrasi Cd aktual, C0 =
qt = 37,7817 mg/kg
Kapasitas Cd(II) teradsorpsi di pasir = qt = 37,7817 mg/kg
Maka, Kapasitas Cd(II) teradsorpsi di pasir pada setiap 13 gram sampel(q13) =
= 0,4911 mg
Kapasitas adsorpsi residual, dengan vr = 70ml dan massa sampel 13 gram:
qr =
=
= 0,2034mg
Kapasitas adsorpsi total pasir kontaminasi dengan pengeringan menggunakan oven:
+
= 0,4911 mg+0,2034mg = 0,6945
B.3 Perhitungan pore volume pada kolom remediasi Kalibrasi volume kolom
1. Kolom diisi setinggi batas kawat dan diukur volumenya sebagai, Vb = 1 ml
vo vi
2. Kolom diisi dengan 13 gr pasir, kemudian ditambahkan aquadest sebanyak 10 ml sampai semua pasir terbasahi.
3. Effluent ditampung dan diukur volumenya sebagai, Ve = 3 ml. Maka didapat volume pada setiap pori pasir( volume pore pasir = Vop)
4. Pore volune pasir dihitung dengan rumus : Vop = Ve- Vk = 3 ml – 1 ml = 2ml
Maka 1 cmc SDS adalah sebesar : 2,364 gr/L Jika 0,5 x cmc = 0,5 x 2,364= 1,182 gr/L 2x cmc = 2 x 2,364 = 4,728 gr/ L
B.5 Perhitungan persen removal efisiensi – remediasi Removel Efisiensi pada 2 CMC 100 RPM
Konsentrasi aktual hasil analisa AAS Cd(II) yang berhasil ter-remove atau terlepas = 0,1535 ppm ( 0,1535 mg/L) dengan volume sampel yang ditampung = 50 ml maka dapat dihitung kapasitas desorpsi Cd dengan persamaan sebagai berikut :
qr = 0,06953 mg
maka, persen removal efisiensi :
LAMPIRAN C
DOKUMENTASI PERCOBAAN
C.1 Hasil Pencucian Adsorben Pasir Putih
Gambar C.1 Pencucian Pasir Putih yang Akan Digunakan Sebagai Adsorben
C.2 Hasil Kontaminasi Ion Logam Cd (II)
(a) (b)
Gambar C.2 Kontaminasi Adsorben Pasir Putih dengan ion logam Cd(II) a) Foto Kontaminasi Adsorben sebelum dikeringkan
C.3 Foto Shaking Sampel Saat Penentuan Persen Removal Efisiensi
Gambar C.3 Foto Shaking Sampel saat Penentuan Persen Removal Efisiensi
C.4 Foto Shaking Sampel Saat Penentuan Kinetika Desorpsi
C.5 Botol Sampel Untuk Diuji Di Alat AAS
DAFTAR PUSTAKA
[1] Endang Rochyatun, Lestari Dan Abdul Rozak. 2004. “Kondisi Perairan Muara Sungai Digul Dan Perairan Laut Arafura dilihat dari Kandungan Logam Berat. Bidang Dinamika Laut, Pusat Penelitian Oseanografi Lipi.
[2] Festri Istarani dan Ellina S. Pandebesie. 2014. Studi Dampak Arsen (As) dan Kadmium (Cd) terhadap Penurunan Kualitas Lingkungan. Jurusan Teknik Lingkungan, Fakultas Teknik Sipil dan Perencanaan, Institut Teknologi Sepuluh Nopember (ITS) : Surabaya.
[3] Anhua Long. 2013.” Surfactant flushing remediation of toluene contaminated soil: Optimization with response surface methodology and surfactant recovery by selective oxidation with sulfate radicals”. Separation and Purification Technology. Department of Environmental Engineering, Hubei
Biomass-Resource Chemistry and Environmental Biotechnology Key Laboratory, Wuhan University, China.
[4] J.D. Rouse. 1993. “Minimizing surfactant losses using twinhead anionic surfactants in subsurface remediation”, Environ. Sci. Technol 27 (1993).
[5] D.H. Lee. 2002. “Surfactant recycling by solvent extraction in surfactant-aided remediation”. Purif. Techno 27 (2002)
[6] Suiling Wang dan Catherine N. Mulligan. 2009. “Rhamnolipid biosurfactant -enhanced soil flushing for the removal of arsenic and heavy metals from mine tailings”. Process Biochemistry. Department of Building, Civil and Environmental Engineering, Concordia University, Canada.
[7] Shai Arnon. 2006. “Evaluation of soil flushing potential for clean-up of desert soil contaminated by industrial wastewater”. Chemosphere 62. Department of Environmental Hydrology and Microbiology, Zuckerberg Institute for Water Research, Israel.
[8] Bode Haryanto, dan Chien-Hsiang Chang. 2014. “Foam-enhanced removal of adsorbed metal ions from packed sands with biosurfactant solution flushing”. Journal of the Taiwan Institute of Chemical Engineers. Department of Chemical
Engineering, National Cheng Kung University, Taiwan.
[10] Paul B Tchounwou. Clement G Yedjou. Anita K Patlolla. “Heavy Metals Toxicity and the Environment”. http://www.ncbi.nlm.nih.gov. Diakses pada 12 Desember 2015
[11] G. Ziemacki. G Vivino. F. Merli. “Heavy Metals Sources and Environmental Presence”. Laboratorio di Igiene Ambientale, Institu Superio Di Sanita, Rome, Italy. Vol 25 N.3. 1989.
[12] Agency for toxic substance and diseases registry (ATSR). “Toxicological Profile For Cadmium”. 2008. http://www.atsdr.cdc.gov. Diakses pada 12 Desember 2015
[13]IARC Monograph. “Cadmium and Cadmium Compounds”. https://monographs.iarc.fr. Diakses pada 12 Desember 2015.
[14] Raymond A. Wuana and Felix E. Okieimen. 2011. “Heavy Metals in Contaminated Soils: A Review of Sources, Chemistry, Risks and Best Available Strategies for Remediation”. ISRN Ecology. Analytical Environmental Chemistry Research Group, Department of Chemistry, Benue State University, Nigeria.
[15] Okeola F.O. And Odebunmi E.O. 2010. Freundlich and Langmuir Isotherms Parameters for Adsorption of Methylene Blue by Activated Carbon Derived from Agrowastes. Chemistry Department University of Ilorin Ilorin,nigeria Advances in Natural and Applied Sciences, 4(3): 281-288, 2010.
[16] A. Dabrowski. 2001. “Adsorption from theory to practice”. Faculty of Chemistry, M.Curie-Skłodowska University, Lublin, Poland.
[17] Paul A. Webb. 2003. “Introduction to Chemical Adsorption Analytical Techniques and their Applications to Catalysis”. Micro. meritics Instrument Corp, Norcross, Georgia.
[18] Ferdinan delesev ginting, 2008. “Pengujian Alat Pendingin Sistem Adsorpsi Dua Adsorber dengan Menggunakan Metanol 1000 ml Sebagai Refrigen”. Fakultas Teknik. Program Teknik Mesin. Universitas Indonesia, Depok.
[20] D.M. Hamby. “Site Remediation Techniques Supporting Environmental Restoration Activities: A Review”. Department of Environmental and Industrial Health School of Public Health University of Michigan Ann Arbor, MI 48109-2029 U.S.A.
[21] Amruthur Ramamurthy dan Hesham Schalchian. 2013. “Surfactant Assisted Removal Of Cu(II), Cd(II) And Pb(II) From Contaminated Soils”. Environment Protection Engineering. Vol. 39 2013. No. 3.
[22] Ikha Novita Ma’wa Sukriya. 2011. “Formulasi Surfaktan untuk Screening Awal Chemical Flooding Pada EOR (Enhanced Oil Recovery)”. Skripsi. Fakultas Teknik Program Ekstensi Teknik Kimia.
[23] Trievita Anna Furi, Pamilia Coniwanti. 2012 “Pengaruh Perbedaan Ukuran Partikel Dari Ampas Tebu Dan Konsentrasi Natrium Bisulfit (Nahso3) Pada Proses Pembuatan Surfaktan”. Jurusan Teknik Kimia Fakultas Teknik Universitas Sriwijaya. Jurnal Teknik Kimia No. 4, Vol. 18, Desember 2012. [24] Yolan Nursintia Dewi. 2015. “Optimasi Formulasi Basis Sediaan Emulgel
dengan Variasi Konsentrasi Surfaktan. Prosiding Penelitian Sivitas Akademika Unisba (Kesehatan dan Farmasi). ISSN 2460-64672.
[25] Jojor Rohana Oppusunggu. 2015. “Pengaruh Jenis Pelarut Dan Temperatur Reaksi Pada Sintesis Surfaktan Dari Asam Oleat dan N-Metil Glukamina Dengan Katalis Kimia”. Jurnal Teknik Kimia USU, Article in Press (2015). [26] Jean-Louis Salager. 2002. “ Surfactants Types And Uses” Laboratory Of
Formulation, Interfaces Rheology And Processes. Universidad De Los Andes Facultad De Ingenieria Escuela De Ingenieria Quimica.
[27] Sri Wahyu Murni, Sri Wahyuni Santi R, IGS Budiaman, Ika Perwitasari dan Abdul Aji Kresna Tri Anggara. 2013. “Pembuatan Surfaktan Berbahan Dasar Jerami Padi”. Program Studi Teknik Kimia, FTI, UPN ”Veteran” Yogyakarta. Vol 11 No 1, Juni 2013.
[29] Venkatesh Chaturvedi, Ashok Kumar. 2010. “Toxicity Of Sodium Dodecyl Sulfate In Fishes And Animals. A Review”. International Journal of Applied Biology and Pharmaceutical Technology. School of Biotechnology, Banaras Hindu University, Varanasi.
[30] Sanjay Kumar, Thejasenuo Julia Kirha and Tsipila Thonger. 2014. “Toxicological Effects Of Sodium Dodecyl Sulfate”. Journal of Chemical and Pharmaceutical Research, 2014, 6(5):1488-1492.
[31] Agus M.Hani. 2012. “Pengeringan Lapisan Tipis Kentang ( Solanum Tuberosum. L) Varietas Granola”. Skripsi Hasil Penelitian Program Studi Keteknikan Pertanian Jurusan Teknologi Pertanian Fakultas Pertanian Universitas Hasanuddin.
[32] Douglas A. Skoog, F James Holler, Timothy A. Nieman. 1998. “Principles of Instrumental Analysis” . Fifth Edition.
[33] Bode Haryanto, Jo-Shu Chang , Chien-Hsiang Chang. 2011. “An Investigation On The Removal Efficiency For Metal Ions From Porous Sand-Packed Columns By A Biosurfactant With The Foam-Enhanced Flushing Technique”. The 2nd Annual Indonesian Scholars Conference in Taiwan. Vol 1 /No 1/2011. [34] Suiling Wang, Catherine N. Mulligan. 2004. An Evaluation Of Surfactant Foam Technology In Remediation Of Contaminated Soil. Department of Building, Civil and Environmental Engineering, Concordia University. Chemosphere 57 (2004) 1079–1089.
BAB III
METODOLOGI PENELITIAN
3.1 Lokasi Dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Proses Industri Kimia dan Laboratorium Operasi Teknik Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan. Penelitian ini dilakukan selama lebih kurang 3 bulan.
3.2 Bahan
Pada penelitian ini bahan yang digunakan antara lain: 1. Sodium Dodecyl Sulfate (SDS)
2. Pasir putih terkontaminasi ion logam Cd 3. Aquades (H2O)
4. Natrium Hidroksida (NaOH) 5. Asam Klorida (HCl)
6. Kadmium Asetat Dihidrat (Cd(CH3COO)2.2H2O)
3.3 Peralatan
Peralatan yang digunakan dalam penelitian ini adalah propeler, kontainer plastik, shaker, saringan mesh 20 , pH meter, gelas ukur, beaker glass 1 Liter, corong, erlenmeyer, neraca analitik, cawan, termometer, pipet tetes, cutter dan Atomic Adsorption Spectroscopy (AAS) yang berfungsi untuk mengukur kandungan
logam, Peristaltic pump, kolom pencuci, statif dan klem.
3.4 Prosedur Penelitian
3.4.1 Prosedur Preparasi Pasir (Adsorben) a. Pencucian Adsorben Pasir
1. Pasir putih diperoleh dari Pantai Wisata di Kecamatan Pantai Cermin, Kabupaten Serdang Berdagai, Sumatera Utara, Indonesia.
Gambar 3.1 Flowchart Persiapan Adsorben Pasir Putih
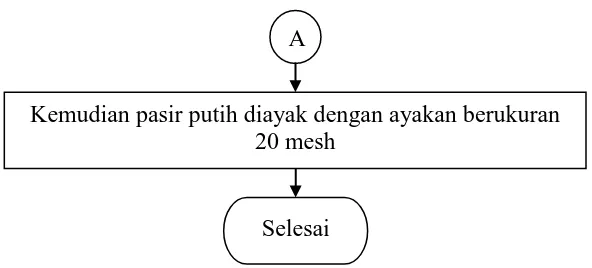
b. Pengeringan Adsorben Pasir
1. Oven dinyalakan dan ditunggu hingga mencapai suhu 55oC [8]. 2. Pasir putih yang telah dicuci kemudian di ratakan diatas tray oven. 3. Ditimbang sejumlah pasir putih yang dialasi aluminium foil, dicatat
massanya lalu diletakkan diatas tray oven.
4. Setiap 10 menit pengeringan, pasir putih yang dialasi aluminium foil ditimbang sampai massanya konstan.
5. Kemudian pasir putih diayak dengan ayakan berukuran 20 mesh. Selesai
Mulai
Setiap 1000 gr pasir putih dicuci dengan 1,2 L air deionisasi sebanyak 3-4 kali sampai pH air pencuci konstan sambil diaduk dengan propeler
Pasir putih diperoleh dari Pantai Wisata di Kecamatan Pantai Cermin, Kabupaten Serdang Berdagai, Sumatera Utara, Indonesia
Setiap 10 menit pengeringan, pasir putih yang dialasi aluminium foil ditimbang sampai massanya konstan
Mulai
Oven dinyalakan dan ditunggu hingga mencapai suhu 55°C
Pasir putih yang telah dicuci kemudian di ratakan diatas tray oven
Gambar 3.2 Flowchart Pengeringan Adsorben Pasir Putih
3.4.2 Prosedur Pembuatan Larutan
Larutan yang perlu disediakan yaitu larutan asam serta larutan basa yaitu larutan 0,1 M HCl dan 0,1 M NaOH, pelarut logam yang pH-nya 4,5 sebanyak 5 L dan larutan logam Cd2+ dengan konsentrasi 50 ppm dari senyawa Cd(CH3COO)2.2H2O.
a. Pembuatan Larutan Pengontrol pH : HCl 0,1 M (1 L) 1. Larutan HCl 37% dipipet sebanyak 8,36 mL.
2. Larutan dimasukkan ke dalam beaker glass 1000 mL. 3. Larutan diencerkan dengan aquadest sampai batas 1000 mL.
Gambar 3.3 Flowchart Pembuatan Larutan HCl 0,1 M
b. Pembuatan Larutan Pengontrol pH: NaOH 0,1 M (1 L) 1. Padatan NaOH ditimbang sebanyak 4gr
2. Padatan NaOH dimasukkan ke dalam beaker glass 1000 mL A
Selesai
Kemudian pasir putih diayak dengan ayakan berukuran 20 mesh
Mulai
Larutan HCl 37% dipipet sebanyak 8,36 mL
Selesai
Larutan dimasukkan ke dalam beaker glass 1000 mL
3. Padatan NaOH diencerkan dengan aquadest sampai batas 1000 mL
Gambar 3.4 Flowchart Pembuatan Larutan NaOH 0,1 M
c. Pembuatan Larutan Pelarut dengan pH 4,5
1. Aquadest sebanyak 5 L dimasukkan ke dalam botol steril.
2. Kemudian ke dalam aquadest ditambahkan HCl dan NaOH hingga pH larutan 4,5.
Gambar 3.5 Flowchart Pembuatan Larutan Pelarut Mulai
Padatan NaOH ditimbang sebanyak 4gr
Selesai
Padatan NaOH dimasukkan ke dalam beaker glass 1000 mL
Padatan NaOH diencerkan dengan aquadest sampai batas 1000 mL
Mulai
Aquadest sebanyak 5 L dimasukkan ke dalam botol steril
Selesai
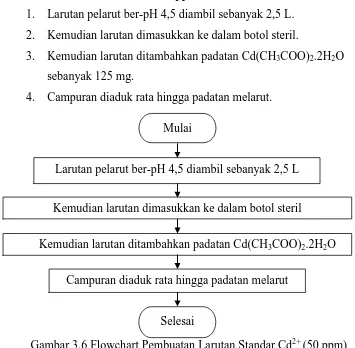
d. Pembuatan Larutan Cd2+ 50 ppm
1. Larutan pelarut ber-pH 4,5 diambil sebanyak 2,5 L. 2. Kemudian larutan dimasukkan ke dalam botol steril.
3. Kemudian larutan ditambahkan padatan Cd(CH3COO)2.2H2O
sebanyak 125 mg.
4. Campuran diaduk rata hingga padatan melarut.
Gambar 3.6 Flowchart Pembuatan Larutan Standar Cd2+ (50 ppm)
3.4.3 Mengukur Pengaruh Konsentrasi Ion Logam Terhadap Kemampuan Adsorpsi
1. Larutan Cd2+ 50 ppm sebanyak 100 ml diambil dari botol 2,5 L lalu dimasukkan kedalam tiap 10 erlenmeyer.
2. Kemudian 100 gram adsorben pasir putih dengan ukuran adsorben tertentu ditambahkan larutan kedalam masing-masing 10 erlenmeyer. 3. Kemudian campuran diaduk dengan shaker dengan kecepatan
pengadukan 100 rpm pada suhu kamar selama 2 jam.
4. Kemudian didiamkan tanpa pengadukan 24 jam untuk mencapai kesetimbangan adsorpsi Cd(CH3COO)2.2H2O terhadap pasir.
5. Seluruh pasir dan larutan diakumulasikan 1000 gram 1000 L untuk menyeragamkan konsentrasi Cd di larutan.
Mulai
Selesai
Campuran diaduk rata hingga padatan melarut Larutan pelarut ber-pH 4,5 diambil sebanyak 2,5 L
Kemudian larutan ditambahkan padatan Cd(CH3COO)2.2H2O
6. Lalu 50 mL sampel diambil untuk dianalisis.
7. Konsentrasi ion Cd2+ pada larutan setelah adsorpsi dianalisis dengan Atomic Adsorption Spectroscopy (AAS).
8. Diambil cairan 900 ml. 9. Lalu nilai qt dihitung
(3.1) [6]
Mulai
Larutan Cd2+ 50 ppm sebanyak 100 gram diambil dari botol 2,5 L lalu dimasukkan kedalam tiap 10 erlenmeyer
Kemudian campuran diaduk dengan shaker dengan kecepatan pengadukan 100 rpm pada suhu kamar selama 24 jam
Kemudian 100 gram 100 ml adsorben pasir putih dengan ukuran adsorben tertentu ditambahkan larutan ke dalam masing-masing
10 erlenmeyer
Kemudian didiamkan tanpa pengadukan 24 jam untuk mencapai kesetimbangan adsorpsi Cd(CH3COO)2.2H2Oterhadap pasir.
Konsentrasi ion Cd2+ setelah adsorpsi dianalisa dengan Atomic Adsorption Spectroscopy (AAS)
Lalu nilai qt dihitung
Lalu 2 mL sampel diambil untuk dianalisis
Kemudian diakumulasikan adsorben 1000 gram 1000 L pengadukan 24 jam untuk mencapai kesetimbangan adsorpsi
Diambil cairan 900 ml
Tidak
Gambar 3.7 Flowchart Mengukur Pengaruh Konsentrasi Ion Logam Terhadap Kemampuan Adsorpsi
Apakah ada variasi konsentrasi ion logam
lainnya?
Selesai
A B
A
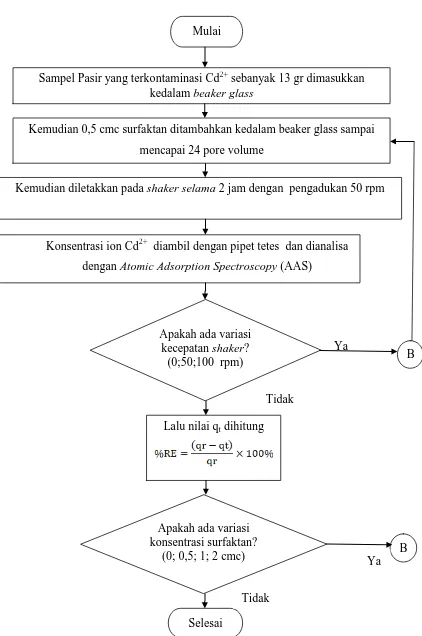
3.4.4 Mengukur Removal Efficiency terhadap Variasi Konsentrasi SDS dan Pengadukan pada Batch System
1. Sampel pasir yang terkontaminasi Cd2+ sebanyak 13 gr [2] dimasukkan kedalam beaker glass.
2. Kemudian 0,5 cmc SDS [2] ditambahkan kedalam beaker glass hingga mencapai 24 pore volume.
3. Kemudian diletakkan pada shaker selama 2 jam dengan laju variasi shaking 50 dan 100 rpm dan tanpa pengadukan (0 rpm).
4. Konsentrasi ion Cd2+ diambil dengan pipet tetes, dan dianalisa dengan Atomic Adsorption Spectroscopy (AAS).
5. Lalu nilai REdihitung
(3.2)
[6]
Gambar 3.8 Flowchart Mengukur removal eficiency terhadap Variasi Konsentrasi SDS dan Pengadukan pada Batch System
Apakah ada variasi kecepatan shaker? (0;50;100 rpm)
Mulai
Sampel Pasir yang terkontaminasi Cd2+ sebanyak 13 gr dimasukkan kedalam beaker glass
Kemudian diletakkan pada shaker selama 2 jam dengan pengadukan 50 rpm Kemudian 0,5 cmc surfaktan ditambahkan kedalam beaker glass sampai
mencapai 24 pore volume
Konsentrasi ion Cd2+ diambil dengan pipet tetes dan dianalisa dengan Atomic Adsorption Spectroscopy (AAS)
B
Selesai
Lalu nilai qt dihitung
Apakah ada variasi konsentrasi surfaktan?
(0; 0,5; 1; 2 cmc) B
Ya
Tidak
Tidak
3.4.5 Mengukur Kinetika Pencucian Pasir terhadap Logam Cd2+ pada Batch
System
1. Sampel pasir yang terkontaminasi Cd2+ sebanyak 13 gr [2] dimasukkan kedalam beaker glass.
2. Kemudian 2 cmc SDS [2] ditambahkan kedalam beaker glass hingga mencapai 24 pore volume.
3. Kemudian diletakkan pada shaker dengan variasi waktu 5;10;20;40;60 dan 180 menit dengan pengadukan shaking 100 rpm.
4. Konsentrasi ion Cd2+ diambil dengan pipet tetes dan dianalisa dengan Atomic Adsorption Spectroscopy (AAS).
5. Lalu nilai REdihitung.
[6]
Gambar 3.9 Flowchart Mengukur Kinetika Pencucian Pasir terhadap Logam Cd2+ pada Batch System
Mulai
Sampel pasir yang terkontaminasi Cd2+ sebanyak 13 gr dimasukkan kedalam beaker glass.
Kemudian diletakkan pada shaker dengan variasi waktu 5;10;20;40;60 menit dengan pengadukan shaking 100 rpm.
Konsentrasi ion Cd2+ pada eluent setelah adsorpsi dianalisa dengan Atomic Adsorption Spectroscopy (AAS).
Selesai
Lalu nilai RE dihitung
3.5 Rangkaian Peralatan Percobaan Remediasi Pasir Terkontaminasi pada
Batch System
BAB IV
HASIL DAN PEMBAHASAN
4.1 Pretreatment Adsorben Pasir Putih
Penelitian ini menggunakan, pasir putih sebagai penjerap (adsorben) yang diperoleh dari pantai wisata di Kecamatan Pantai Cermin, Kabupaten Serdang Bedagai. Pasir putih terlebih dahulu dikeringkan di bawah sinar matahari dan setelah kering, pasir diayak dengan ukuran (mesh) 40 mesh. Lalu, pasir putih dicuci dengan aquadest dan dibilas sampai bersih. Tujuan dari proses pencucian yang dilakukan pada adsorben pasir putih adalah untuk menghilangkan mineral-mineral garam serta kotoran yang masih melekat pada pasir putih tersebut. Indikator pencucian diperoleh apabila pH air cucian sama dengan pH aquadest sebelum digunakan untuk mencuci.
Gambar 4.1 Pencucian Adsorben Pasir Putih
Gambar 4.1 menunjukkan kondisi konstan pH terhadap banyaknya pencucian. Dari proses pencucian diperoleh bahwa untuk dapat menghilangkan kandungan mineral-mineral garam dan kotoran-kotaran yang ada pada pasir putih dibutuhkan 7 kali pencucian sampai pH pencucian menjadi konstan. Dari grafik
diketahui bahwa pada pencucian ke 4 dan seterusnya pH air cucian konstan, yaitu 6,9
Gambar 4.2 Pengeringan Adsorben Pasir Putih
Setelah proses pencucian selesai, pasir putih yang telah dipisahkan menurut ukurannya dikeringkan di dalam oven dengan kondisi operasi pada suhu 60oC. Pengeringan merupakan cara untuk menghilangkan sebagian besar air dari suatu bahan dengan bantuan energi panas dari sumber alam (sinar matahari) atau buatan (alat pengering) [31]. Dari proses pengeringan diperoleh hasil untuk sampel dengan ukuran 40 mesh yang membutuhkan waktu pengeringan selama 4 jam.
4.2 Penentuan Kapasitas Adsorpsi.
Ukuran adsorben yang ada pada penelitian ini adalah 40 mesh. Proses adsorpsi berlangsung selama 2 jam pengadukan dan didiamkan selama 24 jam pada sistem batch. Tujuan penentuan kapasitas adsorpsi untuk mengetahui besarnya penjerapan ion logam Cd2+ atau ada tidaknya penyerapan ion logam Cd2+ di adsorben pasir putih dengan ukuran 40 mesh.
Perhitungan kapasitas adsorpsi pada pasir terkontaminasi yang telah dikeringkan menggunakan oven, telah terlampir pada bab 3 persamaan 3.1
adsorpsi yaitu sebesar 0,694602 pada setiap 13 gram sampelnya serta persentase adsorpsi 23,36%.
Pasir di Indonesia memiliki luas permukaan yang cukup besar. Hal ini dapat dilihat dari hasil analisa penentuan besarnya luas permukaan pasir putih yang dilakukan di Laboratorium Analisa Instrumental, PT. Indonesia Asahan Aluminium (PT. INALUM), diperoleh bahwa luas permukaan spesifik dari adsorben pasir putih adalah sebesar 0,622 m2/gram. Berbeda dengan hasil luas permukaan spesifik pasir di Taiwan yang diperoleh Haryanto (2015), sebesar 0,17 m2/gram. Namun, hasil luas permukaan spesifik pasir di Netherland yang diperoleh Noordman (2002), sebesar 0,74 m2/gram berbeda pula dengan Taiwan dan Indonesia. Luas permukaan pasir di Netherland lebih besar dibandingkan Taiwan dan Indonesia.
Tabel 4.1 Konfirmasi Data Analisa BET Pasir Indonesia
Pasir Analisa AAS (ppm) Analisa BET (m2/gr)
Sebelum Terkontaminasi 0 0,6220
Setelah Terkontaminasi 37,718 0,368
Tabel 4.1 menunjukkan adanya Cd (II) yang teradsorpsi dengan didukung oleh konfirmasi analisa BET (Brunaeur Emmet Teller). Dimana terjadi perubahan luas permukaan antara pasir sebelum terkontaminasi Cd (II) dan sesudah terkontaminasi Cd (II).
Keberadaan atau adsorpsi Cd (II) pada pasir juga dikonfirmasi dengan data analisa FTIR (Fourier Transform Infrared) :
(b)
Gambar 4.3 (a) konfirmasi analisa FTIR pasir sebelum terkontaminasi (b) konfirmasi analisa FTIR pasir sesudah terkontaminasi
4.3 Penentuan Removal Efisiensi Cd2+ dengan Variasi Konsentrasi Surfaktan (SDS)
Data Removal Efisiensi pada variasi konsentrasi Variasi Konsentrasi Surfaktan (SDS) dapat dilihat pada Tabel A.4 (Lampiran A) dan pada Gambar 4.6.
Gambar 4.6 Nilai Removal Efisiensi dengan Variasi Konsentrasi Surfaktan (SDS) dan variasi kecepatan pengadukan shaker
Gambar 4.6 dan 4.7 Nilai Removal Efisiensi dengan Variasi Konsentrasi Surfaktan (SDS) dan variasi kecepatan rotasi. Pada konsentrasi larutan Cd2+ 50 ppm pada saat, t0 = 0 menit dan ts = 2 jam hingga t = 24 jam memiliki Kapasitas Cd(II)
teradsorpsi di pasir = qt = 37,7817 mg/kg. Untuk Kapasitas Cd(II) teradsorpsi di
pasir pada setiap 13 gram sampel (q13) = 0,4911 mg. Kapasitas Cd(II) teradsorpsi
residu pada setiap 13 gr sampel = 0,2034 mg. Maka, Kapasitas adsorpsi total pasir kontaminasi dengan pengeringan menggunakan oven:
+
= (0,4911 mg + 0,2034 mg) kg-1 = 0,6945 mg kg-1
Berikut merupakan tabel hasil data Removal Efisiensi dengan Variasi Kecepatan Rotasi dan Variasi Surfaktan
Tabel 4.2 Hasil Data Removal Efisiensi Kecepatan Pengadukan
Konsentrasi removal efisiensi terbesar terdapat pada saaat konsentrasi SDS 2 CMC dan kecepatan pengadukan 100 rpm, yaitu sebesar: 1,3906 ppm. Untuk persentase removal efisiensinya sebesar 10,01005%. Sedangkan removal efisiensi yang terkecil adalah 0,481 ppm dengan removal efisiensinya 3,462414%.
Menurut Haryanto, Chang dan Hsiang Chang, 2011 [33] kecepatan shaking berbanding lurus dengan hasil removal efisiensi. Semakin besar kecepatan shaking maka removal efisiensi logam juga semakin besar. Permukaan pasir
memiliki pecahan pada permukaan dan porosnya terluarnya. Dengan dilakukannya shaking, surfaktan dapat meresap ion logam Cd2+ lebih jauh sehingga removal efisiensi lebih besar.
surfaktan meningkatkan solubilisasi dari komponen organik hidrofobik dengan meningkatkan kelarutan kontaminan melalui solubilisasi micelle. Hal ini dikarenakan bahwa dibawah nilai CMC, sifat fisika-kimia surfaktan anionik seperti sodium dodecyl sulfate (SDS) (sifat konduktif, daya elektromotif) mengalami gaya elektrolit yang kuat. Diatas nilai CMC sifat-sifat ini menurun secara drastic [35].
Oleh karena itu, surfaktan pada konsentrasi rendah terutama menumpuk di padat-cair atau cairan-cairan antarmuka dalam bentuk monomer. Dengan konsentrasi meningkat, molekul surfaktan secara bertahap menggantikan pelarut antarmuka seperti air, sehingga menghasilkan kepolaran fasa cair yang lebih rendah dan menurunkan tegangan permukaan [36].
4.4 Penentuan Kinetika Desorpsi pada Konsentrasi Surfaktan (SDS) 2 CMC 100 Rpm
Gambar 4.7 Grafik Kinetik Desorpsi pada 2 CMC 100 Rpm
Pada gambar 4.7 dilihat bahwa pada 5 menit pertama sampai 20 menit mengalami kenaikan removal efisiensi hingga akhirnya konstan setelah menit ke 40 hingga menit ke 180.
hanya dalam zona permukaan pasir, namun juga masuk kedalam pori-pori pasir, inilah yang membuat adanya peningkatan drastis removal efisiensi pada menit 5-40. Setelah itu nilai removal akan konstan dikarenakan ion kadmium sudah habis teradsorpsi ke dalam pasir saat mencapai keadaan setimbang [37].
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Adapun kesimpulan yang dapat diperoleh antara lain sebagai berikut : 1. Pada proses pencucian adsorben pasir putih dibutuhkan 3 kali pencucian
hingga pH konstan sedangkan batang jagung bentuk serbuk 50 mesh dan 70 mesh membutuhkan 4 kali pencucian.
2. Pada proses pengeringan dibutuhkan waktu 4 jam.
3. Pada penentuan removal efisiensi dengan variasi konsentrasi surfaktan (SDS), hasil removal efisiensi terbesar yaitu 1,3906 ppm dengan persen removal 10,01005% pada konsentrasi 2 CMC dengan pengadukan shaker 100 Rpm dan removal efisiensi terkecil dengan konsentrasi 0 CMC dengan pengadukan 0 Rpm dengan persen removal 3,462414 %.
4. Nilai removal efisiensi mulai konstan pada menit ke-60 hingga 180 pada penentuan konetika desorpsi 2 CMC 100 Rpm.
5.2 SARAN
Adapun saran yang perlu dilakukan penelitian lanjutan seperti:
1. Penelitian lebih lanjut dengan menggunakan dua jenis pasir yang berbeda sebagai adsorbennya, contohnya pasir hitam dan pasir putih.
2. Mekanisme pengadukan pada proses adsorpsi menggunakan alat stirrer. 3. Digunakan alat atau media pengering pasir yang berbeda, misalnya
dengan menghantarkan gas N2.
BAB II
TINJAUAN PUSTAKA
2.1 Karakteristik Logam Berat
Logam berat merujuk pada elemen metal yang memiliki massa jenis tinggi dan beracun bahkan pada konsentrasi rendah. Logam berat adalah istilah umum, yang mengacu pada kelompok logam dan metalloid dengan massa jenis atom lebih besar dari 4 g/cm3 atau 5x lebih besar dibandingkan air. Bagaimanapun, logam berat tidak terlalu berpengaruh pada massa jenis namun pada sifat kimia nya. Logam berat mencakupi timbal (Pb), kadmium (Cd), seng (Zn), merkuri (Hg), arsenik (As), perak (Ag), kromium, Cr), tembaga (Cu), besi (Fe), dan senyawa kelompok platinum [9].
Meskipun logam berat merupakan senyawa alami yang ditemukan di seluruh
kerak bumi, pencemaran lingkungan lebih berpotensi disebabkan dari hasil paparan
aktivitas antropogenik seperti operasi pertambangan dan peleburan, produksi industri
dan penggunaan, dan penggunaan domestik dari logam. Pencemaran lingkungan juga
dapat terjadi melalui korosi logam, deposisi atmosfer, erosi tanah, ion logam dan
pencucian logam berat, sedimen suspensi ulang dan penguapan logam dari sumber
air. Fenomena alam seperti pelapukan dan letusan gunung berapi juga berkontribusi
terhadap polusi logam berat [10].
Dalam sistem biologis, logam berat telah dilaporkan mempengaruhi organel sel
dan komponen seperti membran sel, mitokondria, lisosom, retikulum endoplasma,
inti, dan beberapa enzim yang terlibat dalam metabolisme, detoksifikasi, dan
memperbaiki kerusakan. Ion logam yang berinteraksi dengan komponen sel seperti
protein DNA dan nuklir, menyebabkan kerusakan DNA dan perubahan konformasi
yang dapat menyebabkan modulasi siklus sel, karsinogenesis atau apoptosis.
Beberapa penelitian telah menunjukkan bahwa spesies oksigen reaktif (ROS)
produksi dan stres oksidatif memainkan peran kunci dalam toksisitas dan
karsinogenisitas dari logam seperti arsenik, kadmium, kromium, timbal, dan merkuri.
Logam ini merupakan racun sistemik yang dikenal untuk menginduksi kerusakan
multiorgan, bahkan pada tingkat yang lebih rendah dari paparan. Menurut Badan
Penelitian Kanker (IARC), logam ini juga diklasifikasikan sebagai "dikenal" atau
"kemungkinan" karsinogen manusia berdasarkan studi epidemiologi dan
eksperimental yang menunjukkan hubungan antara paparan dan kejadian kanker pada
manusia dan hewan [10].
Kadmium memiliki no atom 48, berat atom 112,4, massa jenis 8,65 g/cm3, titik lebur 320,09oC, dan titik didih 765oC [12]. Kadmium merupakan bahan beracun yang menyebabkan keracunan kronik pada manusia, maka tingkat maksimum yang diperbolehkan di perairan adalah 0,01 mg/L (PP No 82 Th 2001 Tentang Kualitas Air). Kadmium (Cd) adalah logam berat yang secara normal terdapat pada tanah dan air dalam kadar rendah. Kadmium berasal dari beberapa sumber yaitu sumber alami, pertambangan dan industri. Gunung berapi merupakan sumber kadmium terbesar secara alami. Dari pertambangan, kadmium tidak ditambang secara tersendiri, tetapi merupakan bahan ikutan dari pengolahan tambang dan produksi timah hitam (Pb), Seng (Zn), Kuprum (Cu), batu bara dan minyak (Melalui interaksi dengan rantai makanan akhirnya kadmium yang telah mencemari lingkungan perairan akan sampai pada manusia) [13].
Penggunaan yang paling signifikan dari Cd yaitu dalam baterai Ni / Cd, sebagai sumber daya yang dapat diisi ulang atau sekunder menunjukkan output yang tinggi, dan pertahanan yang tinggi terhadap tegangan fisik dan elektrik. Pelapis kadmium memberikan pertahanan korosi yang bagus untuk kapal dan kendaraan lainnya, khususnya di lingkungan tekanan tinggi seperti laut dan luar angkasa. Kegunaan lain dari kadmium adalah sebagai pigmen (memberi zat warna), stabilisator untuk polyvinyl chloride (PVC), dalam paduan dan senyawa elektronik. Kadmium juga
sebagai hasilnya konsentrasi permukaan air cenderung meningkat karena pH air menurun [14].
Kadmium dalam tubuh diketahui mempengaruhi beberapa enzim. Hal ini diyakini bahwa kerusakan ginjal yang menghasilkan proteinuria adalah hasil dari Cd yang dapat mempengaruhi enzim untuk reabsorpsi protein dalam tubulus ginjal. Kadmium juga mengurangi aktivitas delta-aminolevulinic acid synthetase, arylsulfatase, alcohol dehydrogenase, and lipoamide dehydrogenase, dan
meningkatkan aktivitas delta - aminolevulinat asam dehidratase, dehidrogenase piruvat, dan piruvat dekarboksilase. Kejadian keracuran kadmium paling mengejutkan dan dipublikasikan dihasilkan dari asupan makanan kadmium oleh orang-orang di Lembah Sungai Jintsu , dekat Fuchu, Jepang. Para korban menderita penyakit itai itai , yang berarti “aduh,aduh” dalam bahasa Jepang. Gejala nya yaitu sakitnya osteomalacia ( penyakit tulang ) yang dikombinasikan dengan kerusakan ginjal. Racun kadmium di Lembah Sungai Jintsu disebabkan beras irigasi yang terkontaminasi dari tambang hulu sungai yang memproduksi Pb, Zn, dan Cd. Ancaman utama bagi kesehatan manusia adalah akumulasi kronis pada ginjal yang menyebabkan disfungsi ginjal. Namun, produk makanan dan merokok merupakan
penyebab utama masuknya Cd ke dalam tubuh [14].
2.3 Adsorpsi
Adsorpsi adalah suatu proses yang terjadi ketika suatu fluida (cairan maupun gas)
terikat pada suatu padatan dan akhirnya membentuk suatu film (lapisan tipis) pada
permukaan padatan tersebut. Adsorpsi dideskripsikan sebagai proses pemisahan yang
efektif untuk menghilangkan effluent secara domestik atau industri [15].
Mekanisme penjerapan dapat dibedakan menjadi dua, yaitu adsorpsi secara fisika (fisisorpsi) dan secara kimia (kemisorpsi). Bertentangan dengan fisisorpsi, kemisorpsi hanya terjadi sebagai monolayer. Adsorpsi fisik dapat dibandingkan
untuk proses kondensasi serap tersebut. Sebagai aturan, fisisorpsi adalah proses
reversibel yang terjadi pada suhu yang lebih rendah atau dekat dengan temperatur
kritis dari substansi yang terserap [16].
fisisorpsi bersifat eksotermis dan besarnya energi yang dilepaskan – 40 kJ/mol. Kemisorpsi merupakan peristiwa terjadinya pertukaran elektron serta pembentukan ikatan kimia antara molekul gas reaktan dengan permukaan katalis dan bersifat eksotermis. Besarnya energi yang dilepaskan pada peristiwa kemisorpsi adalah – 400 kJ/mol [17].
2.4 Faktor-faktor yang Mempengaruhi Adsorpsi
Secara umum, faktor-faktor yang mempengaruhi dari proses adsorpsi adalah sebagai berikut:
a. Luas permukaan
Semakin luas permukaan adsorben, maka makin banyak zat yang teradsorpsi. Luas permukaan adsorben ditentukan oleh ukuran partikel dan jumlah dari adsorben.
b. Jenis adsorbat
Peningkatan polarisabilitas adsorbat akan meningkatkan kemampuan adsorpsi molekul yang mempunyai polarisabilitas yang tinggi (polar) memiliki kemampuan tarik-menarik terhadap molekul lain dibandingkan molekul yang tidak dapat membentuk dipol (non polar). Peningkatan berat molekul adsorbat dapat meningkatkan kemampuan adsorpsi. Adsorbat dengan rantai yang bercabang biasanya lebih mudah diadsorp dibandingkan rantai yang lurus. c. Struktur molekul adsorbat
Hidroksil dan amino mengakibatkan mengurangi kemampuan penyisihan sedangkan nitrogen meningkatkan kemampuan penyisihan.
d. Konsentrasi adsorbat
Semakin besar konsentrasi adsorbat dalam larutan maka semakin banyak jumlah substansi yang terkumpul pada permukaan adsorben.
e. Temperatur
Pemanasan atau pengaktifan adsorben akan meningkatkan daya serap adsorben terhadap adsorbat menyebabkan pori-pori adsorben lebih terbuka. Pemanasan yang terlalu tinggi menyebabkan rusaknya adsorben sehingga kemampuan penyerapannya menurun.
2.5 Remediasi Logam Berat pada Pasir terkontaminasi Remediasi dapat dilakukan, antara lain melalui :
i. Penggalian/pengeluaran (ex-situ), in situ (pengolahan di tempat), pencucian/leaching/pembilasan dengan zat kimia
ii. Immobilisasi kimia/ metode stabilisasi untuk mengurangi kelarutan logam berat dengan menambahkan zat tidak beracun kedalam media pasir
iii. Elektrokinetik (ektromigrasi)
iv. Menutup permukaan media yang terkontaminasi dengan pasir yang bersih v. Metode pengenceran (mencampurkan pasir yang tercemar dengan
meletakkan pasir yang bersih di bawah dan atas pasir yang tercemar untuk mengurangi konsentrasi kontaminan)
vi. Fitoremediasi dengan menggunakan tumbuhan seperti tanaman berkayu [19]
Pencucian pasir dengan penambahan surfaktan merujuk pada pengolahan kontaminan pasir dengan larutan surfaktan. Pencucian pasir, di sisi lain, mengacu pada proses sederhana (proses in situ).
Larutan pencuci untuk remediasi pasir bisa berupa air, larutan asam, chelating atau complexing agent, basic solutions (larutan yang memiliki pH>7), cosolvent, atau
surfaktan. Air akan mengekstraksi hidrofilik dan konstituen air. Tidak seperti pelarut yang melarutkan kontaminan dan menempatkan kontaminan dalam larutan, surfaktan merupakan senyawa yang mengurangi ketegangan permukaan antara cairan atau antara cair dan padatan. Surfaktan dapat berpengaruh karena strukturnya : salah satu ujung molekul surfaktan mudah larut dalam air dan molekul lainnya tidak mulah larut. Surfaktan dapat melepaskan kontaminan dari pasir. Surfaktan ditambahkan ke dalam air yang akan digunakan untuk pencucian pasir. Air dengan penambahan surfaktan dapat meningkatkan kemampuan detergen dalam larutan air dan efisiensi dengan senyawa organik yang dibawa dalam larutan air. Pengolahan ini akan lebih efektif jika banyak luas permukaan dari partikel pasir yang terolah [20].
Pada konsentrasi tinggi, surfaktan meningkatkan terlarutnya komponen organik
hidrofobik dengan meningkatkan kelarutan kontaminan melalui misel solubilisasi.
kontaminan campuran (organik dan logam berat) dalam pasir telah berhasil
dilakukan. [21]
Pencucian pasir sering digunakan dalam remediasi disebabkan oleh :
(i) dapat seluruhnya melepas kontaminan, oleh sebab itu menentukan pembersihan yang cepat dari media yang terkontaminasi
(ii) memenuhi spesifik kriteria
(iii) dapat menjadi metode yang paling efektif dan dapat mendaur ulang bahan/energi [21].
Teknik pencucian dapat dicapai dengan sangat baik dengan menggunakan agen yang bisa meningkatkan batas desorpsi antara pasir- logam. Sebuah teknik remediasi yang efektif untuk situasi tersebut adalah metode pencucian larutan surfaktan. Beberapa kelebihan dan keuntungan mengenai pencucian tanpa busa (tanpa foam), misalnya, gradien tekanan yang diperlukan relatif rendah dan tidak merusak struktur tanah dan membutuhkan lebih sedikit energi untuk mencapai remediasi. Namun, remediasi dengan surfaktan membutuhkan konsumsi besar surfaktan dengan efisiensi penyisihan rendah [8].
2.6 Surfaktan
Surfaktan merupakan suatu molekul yang sekaligus memiliki gugus hidrofilik dan gugus lipofilik sehingga dapat mempersatukan campuran yang terdiri dari air dan minyak. Surfaktan adalah bahan aktif permukaan. Aktifitas surfaktan diperoleh karena sifat ganda dari molekulnya. Molekul surfaktan memiliki bagian polar yang suka akan air (hidrofilik) dan bagian non polar yang suka akan minyak/lemak (lipofilik). Bagian polar molekul surfaktan dapat bermuatan positif, negatif atau netral. Sifat rangkap ini yang menyebabkan surfaktan dapat diadsorbsi pada antar muka udara-air, minyak-air dan zat padat-air, membentuk lapisan tunggal dimana gugus hidrofilik berada pada fase air dan rantai hidrokarbon ke udara, dalam kontak dengan zat padat ataupun terendam dalam fase minyak. Umumnya bagian non polar (lipofilik) adalah merupakan rantai alkil yang panjang, sementara bagian yang polar (hidrofilik) mengandung gugus hidroksil [22]
surfaktan rata-rata 3 persen per-tahun. Penggunaan surfaktan sangat bervariasi, seperti bahan deterjen, kosmetik, farmasi, makanan, tekstil, plastik dan lain lain. Beberapa produk pangan seperti margarin, es krim, dan lain-lain menggunakan surfaktan sebagai satu bahannya. Syarat agar surfaktan dapat digunakan untuk produk pangan yaitu bahwa surfaktan tersebut mempunyai nilai Hydrophyle Lypophyle Balance (HLB) antara 2-16, tidak beracun, serta tidak menimbulkan
iritasi. Penggunaan surfaktan terbagi atas tiga golongan, yaitu sebagai bahan pembasah (wetting agent), bahan pengemulsi (emulsifying agent) dan bahan pelarut (solubilizing agent). Penggunaan surfaktan ini bertujuan untuk meningkatkan kestabilan emulsi dengan cara menurunkan tegangan antarmuka, antara fasa minyak dan fasa air. Surfaktan dipergunakan baik berbentuk emulsi minyak dalam air maupun berbentuk emulsi air dalam minyak [23].
Emulsi didefinisikan sebagai suatu sistem yang terdiri dari dua fasa cairan yang tidak saling melarut, dimana salah satu cairan terdispersi dalam bentuk globula-globula cairan lainnya. Cairan yang terpecah menjadi globula-globula-globula-globula dinamakan fase terdispersi, sedangkan cairan yang mengelilingi globula-globula dinamakan fase kontinu atau medium dispersi. Berdasarkan jenisnya emulsi dibedakan menjadi dua yaitu:
1) Emulsi minyak dalam air (O/W), adalah emulsi dimana bahan pengemulsinya mudah larut dalam air sehingga air dikatakan sebagai fase eksternal.
2) Emulsi air dalam minyak (W/O), adalah emulsi dimana bahan pengemulsinya mudah larut dalam minyak [23].
Penambahan surfaktan dalam larutan akan menyebabkan turunnya tegangan permukaan larutan. Setelah mencapai konsentrasi tertentu, tegangan permukaan akan konstan walaupun konsentrasi surfaktan ditingkatkan. Bila surfaktan ditambahkan melebihi konsentrasi ini maka surfaktan mengagregasi membentuk misel. Konsentrasi terbentuknya misel ini disebut Critical Micelle Concentration (CMC). Tegangan permukaan akan menurun hingga CMC tercapai. Setelah CMC tercapai, tegangan permukaan akan konstan yang menunjukkan bahwa antar muka menjadi jenuh dan terbentuk misel yang berada dalam keseimbangan dinamis dengan monomernya [25].
Klasifikasi surfaktan berdasarkan muatannya dibagi menjadi empat golongan yaitu:
1) Surfaktan anionik yaitu surfaktan yang bagian alkilnya terikat pada suatu anion. Contohnya adalah garam alkana sulfonat, garam olefin sulfonat, garam sulfonat asam lemak rantai panjang.
2) Surfaktan kationik yaitu surfaktan yang bagian alkilnya terikat pada suatu kation. Contohnya garam alkil trimethil ammonium, garam dialkil-dimethil ammonium dan garam alkil dimethil benzil ammonium.
3) Surfaktan nonionik yaitu surfaktan yang bagian alkilnya tidak bermuatan. Contohnya ester gliserin asam lemak, ester sorbitan asam lemak, ester sukrosa asam lemak, polietilena alkil amina, glukamina, alkil poliglukosida, mono alkanol amina, dialkanol amina dan alkil amina oksida.
4) Surfaktan amfoter yaitu surfaktan yang bagian alkilnya mempunyai muatan positif dan negatif. Contohnya surfaktan yang mengandung asam amino, betain, fosfobetain.
[26]
Masalah inilah yang menyebabkan banyak pihak mencari alternatif surfaktan yang mudah terdegradasi dan berasal dari bahan baku yang dapat diperbaharui [27].
2.7. Sodium Dodechyl Sulfate (SDS)
Sodium dodecyl sulfat (SDS) tergolong surfaktan anionik yang relatif murah
dan digunakan secara luas pada produk sampo, deterjen dan pasta gigi. SDS juga
digunakan dalam pengolahan mineral untuk flotasi komponen tertentu dan digunakan
untuk denaturasi protein dalam aplikasi laboratorium [28].
Dalam industri SDS digunakan sebagai agen pelunakan produk kulit seperti tas, sepatu, ikat pinggang, agen pembersih wol, dalam industri kertas sebagai penetran,
flocculating agent, de-inking agent, dalam konstruksi bangunan sebagai aditif beton,
perangkat pemadam kebakaran, minyak pelumas mesin, pembersih lantai, dan sabun
cuci mobil, dll [29].
Sodium lauril sulfat (SLS), natrium lauril sulfat atau natrium dodesil sulfat (SDS atau Nads) (C12H25SO4Na) adalah surfaktan anionik yang digunakan di banyak
pembersihan dan kebersihan produk. Molekul ini memiliki ekor 12 atom karbon, yang melekat pada kelompok sulfat, memberikan sifat molekul amfifilik diperlukan dari deterjen [30].
SLS adalah surfaktan yang sangat efektif dan digunakan dalam setiap tugas yang memerlukan penghilangan noda berminyak dan residu. Misalnya, ditemukan dalam konsentrasi yang lebih tinggi dengan produk industri termasuk minyak pelumas mesin, pembersih lantai, dan sabun cuci mobil. Hal ini digunakan dalam konsentrasi yang lebih rendah dengan pasta gigi, shampoo, dan busa cukur. Ini merupakan komponen penting dalam formulasi bubble bath untuk efek penebalan dan kemampuannya untuk membuat busa [30].
2.7.1 Sifat Fisika Dan Kimia SDS
Sifat fisika dan kimia dari SDS dapat dilihat dari data dibawah ini:
a) Tampilan : padat
b) Warna : putih
c) pH : 7,2
e) Titik nyala : 180 °C
f) f) Mudah terbakar (padat, gas) : bahan atau campuran adalah padat mudah terbakar dengan kategori 1.
g) Berat jenis relatif : 0,370 g/cm3 h) Kelarutan dalam air : larut [29].
2.8 Rangkaian Peralatan Percobaan Remediasi Pasir Terkontaminasi pada
Batch System
Keterangan Gambar:
BAB I
PENDAHULUAN
1.1 Latar Belakang
Secara alamiah unsur atau senyawa logam berat terdapat dalam sedimen, air atau organisme laut namun kadarnya sangat rendah. Pada kondisi ini unsur atau senyawa logam berat tidak bersifat racun, sifat racun logam berat yang berbahaya akan timbul bila kadarnya meningkat [1]. Terlepasnya kontaminan ke lingkungan tidak dapat dihindari, hal ini merupakan proses karena adanya pabrik-pabrik serta akibat dari proses penanganan limbah dan pembuangan sampah akhir. Setelah terlepas ke lingkungan, kontaminan akan bereaksi secara cepat, sulit terdekomposisi oleh makhluk hidup dan kadang juga sangat lambat terserap oleh makhluk hidup dan terakumulasi di dalamnya [2].
Di antara semua teknologi remediasi untuk mengurangi hidrofobik pasir yang terkontaminasi organik, pencucian adalah cara yang efektif dan ekonomis. Metode ini merupakan proses in situ, di mana cairan pencucian diterapkan ke permukaan media yang terkontaminasi atau diinjeksikan ke dalam zona terkontaminasi jenuh. Teknik ini memindahkan polutan dengan menggunakan media air, uap, dll dan mengekstraknya keluar dari tanah. Untuk teknik ini, matriks pasir harus dapat terserap (berpori) dan polutan harus bersentuhan langsung dengan media yang digunakan [3]
Penggunaan surfaktan untuk meningkatkan pengurangan dari kontaminan pasir telah secara luas dipelajari dalam beberapa tahun terakhir. Surfaktan anionik biasanya dipilih untuk pencucian kontaminan karena kadarnya yang lebih rendah terhadap adsorpsi di pasir dibandingkan dengan kationik dan nonionik [4]. Selain itu, natrium dodesil sulfat (SDS, CH3(CH2) 11SO4Na), sebuah anion surfaktan dengan
konsentrasi misel kritis (CMC) dari 8 mM, dapat diuraikan oleh bakteri dan mudah terurai oleh tanah atau air [5].
bisa digunakan sebagai ekstraktan untuk mentransfer ion logam dari larutan encer menjadi fasa organik. Mekanisme yang memungkinkan untuk ekstraksi dari logam berat oleh surfaktan yaitu pertukaran ion, pengendapan, dan pengikatan ion. Polimer atau busa bisa ditambahkan untuk mengontrol gerakan dari kontaminan [6].
Pencucian pasir in situ bisa terbatas berdasarkan beberapa alasan, khususnya : 1. Media pasir telah terkontaminasi dalam jangka waktu yang lama dan
menunjukkan pola dua fase desorpsi dengan tahap awal cepat (menit-jam) dan selanjutnya fase lambat (hari-tahun).
2. Sifat heterogen pasir yang menyiratkan bahwa daerah dengan konduktivitas hidrolik rendah mungkin ada, dimana kontaminan harus berdifusi selama periode waktu yang panjang ke lapisan pencuci yang lebih efektif.
Beberapa Penelitian Remediasi Pasir Terkontaminasi Dengan Surfaktan yang telah dilakukan disajikan pada tabel 1.1 :
Tabel 1.1 Penelitian Terdahulu Remediasi Pasir Terkontaminasi dengan Surfaktan
Hasil beberapa penelitian terdahulu yang telah dilakukan maka dapat disimpulkan bahwa logam berat dari pasir terkontaminasi berhasil terdesorpsi dengan peningkatan surfaktan pada batch system. Dalam studi ini penulis meninjau pengaruh variasi pengadukan shaker, konsentrasi surfaktan (SDS), terhadap kemampuan mencuci / remediasi pasir terkontaminasi pada batch system
1.2 Perumusan Masalah
Dalam penelitian ini yang menjadi permasalahan adalah:
1. Bagaimana pengaruh variasi laju pengadukan shaking terhadap pencucian remediasi pasir terkontaminasi.
2. Bagaimana pengaruh konsentrasi SDS terhadap logam berat yang dihilangkan dari remediasi pasir terkontaminasi.
1.3 Tujuan Penelitian Penelitian ini bertujuan:
1. Mempelajari pengaruh variasi laju pengadukan shaking terhadap pencucian/remediasi pasir terkontaminasi.
2. Mempelajari pengaruh konsentrasi SDS terhadap logam berat yang didesorpsi dari remediasi pasir terkontaminasi.
1.4 Manfaat Penelitian
Adapun Manfaat dari penelitian ini adalah
1. Mengetahui kemampuan pasir dalam mengadsorpsi logam Cd2+ pada kasus studi ini.
2. Mengetahui kemampuan surfaktan dalam mendesorpsi logam Cd2+ kontaminan.
3. Memberikan informasi mengenai teknologi remediasi dengan surfaktan pada batch system.
1.5 Ruang Lingkup Penelitian
Adapun ruang lingkup dari penelitian ini adalah :
1. Penelitian ini dilakukan di Laboratorium Proses Industri Kimia dan Laboratorium Operasi Teknik Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan.
Bahan baku utama yang digunakan adalah pasir putih yang diperoleh dari Pantai Wisata di Kecamatan Pantai Cermin, Kabupaten Serdang Berdagai, Sumatera Utara dan Larutan ion logam Cd2+ (kadmium) yang diperoleh dari Pembuatan Larutan Cd2+ dari padatan Cd(CH3COO)2.2H2O. Peralatan yang
digunakan dalam penelitian ini adalah propeller, kontainer plastik, shaker, saringan mesh 20, pH meter, gelas ukur, beaker glass 1 Liter, corong, erlenmeyer, neraca analitik, cawan, termometer, pipet tetes, cutter, statif dan
klem.
3. Variabel – variabel pada penelitian ini adalah sebagai berikut : A. Variabel tetap untuk kontaminasi pasir :
a) Ukuran mesh pasir : 20 mesh b) Berat pasir : 100 gram
c) pH : 4,5 [8]
d) Kecepatan pengadukan : 100 rpm [8] e) Lama pengadukan : 2 jam [8] f) Konsentrasi Larutan : 50 ppm
g) Suhu : 25 °C (298 K)
h) Volume larutan : 100 mL [8]
B. Variabel tetap untuk pencucian pasir: a) Ukuran beaker glass : 1000 ml b) Berat pasir : 13 gram
1) Variabel berubah : Konsentrasi SDS dan Variasi Pengadukan Shaker a) Konsentrasi SDS : 0; 0,5; 1; 2 cmc
b) Variasi Pengadukan Shaker : 0;50; 100 rpm
4. Analisa yang dilakukan :
a. Analisa Atomic Adsorption Spectroscopy (AAS) b. Analisa pH dengan menggunakan pH meter
ABSTRAK
Penelitian ini bertujuan untuk mengetahui kemampuan desorpsi dan interaksi antara pasir putih yang terkontaminasi ion logam (Cd2+) 50 ppm dengan variasi konsentrasi SDS dan variasi kecepatan rotasi shaker pada larutan SDS dengan pH 7. Konsentrasi SDS yang digunakan adalah 0; 0,5; 1 dan 2 CMC. Variasi kecepatan rotasi shaker yang digunakan adalah 0; 50 dan 100 Rpm. Penelitian ini terbagi menjadi 2 tahap, yaitu perlakuan awal dengan melakukan kontaminasi pasir yang diawali dengan pencucian dan pengeringan hingga kondisi seragam. Kemudian dilanjutkan dengan pengukuran potensi kapasitas adsorpsi dengan sistem batch adsorption. Tahap kedua dilakukan tahap remediasi atau pencucian dengan SDS untuk meninjau kemampuan desorpsi dan interaksi antara SDS dan pasir putih yang terkontaminasi (Cd2+). Pengaruh konsentrasi SDS dalan me-remove atau mencuci ion logam Cd2+ terjadi peningkatan yang signifikan, disebabkan oleh adanya gaya mekanis rotasi shaker. Hasil removal terbesar terdapat pada saat konsentrasi SDS 2 CMC dengan kecepatan rotasi sebesar 100 Rpm, yaitu 10,01005% dan hasil removal terkecil berada pada konsentrasi 0 CMC dengan kecepatan rotasi 0 Rpm sebesar 3,462414%.
ABSTRAK
REMEDIASI PASIR TERKONTAMINASI DENGAN METODE
BATCH SYSTEM DENGAN PENINGKATAN
SURFAKTAN BERBAHAN BAKU SODIUM DODECYL
SULFATE
(SDS)
SKRIPSI
Oleh
AULIA CHAIRUNNISA
110405133
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Esa atas limpahan rahmat dan karunia-Nya sehingga skripsi ini dapat diselesaikan. Tulisan ini merupakan skripsi dengan judul “Remediasi Pasir Terkontaminasi Dengan Metode Batch System dengan Peningkatan Surfaktan Berbahan Baku Sodium Dodecyl Sulfate (SDS)”, berdasarkan hasil penelitian yang penulis lakukan di
Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini merupakan salah satu syarat untuk mendapatkan gelar sarjana teknik.
Hasil penelitian ini bermanfaat untuk mengetahui kemampuan SDS berinteraksi dan me-remove ion logam berat yang dapat diaplikasikan untuk mengatasi permasalahan mengenai pencemaran logam berat yang sering terdapat pada sedimentasi bebatuan dan badan air.
Dalam kesempatan ini penulis ingin mengucapkan terima kasih kepada :
1. Dosen pembimbing penelitian ini, Bapak Bode Haryanto, S.T, M.T, Ph.D. 2. Dosen penguji penelitian, Bapak Prof. Dr. Ir. M. Turmuzi, MS dan Bapak
Ir. Bambang Trisakti, MT.
3. Kordinator penelitian, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Ibu Ir. Renita Manurung, M.T.
4. Ketua Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera. Utara, Bapak Dr. Eng. Ir. Irvan, M.Si
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna oleh karena itu penulis mengharapkan saran dan masukan demi kesempurnaan skripsi ini. Semoga skripsi ini memberikan manfaat bagi pengembangan ilmu pengetahuan.
Medan, Agustus 2016
DEDIKASI
RIWAYAT HIDUP PENULIS
Nama : Aulia Chairunnisa NIM : 110405133
Tempat/tgl lahir : Lhokseumawe / 09 April 1993
Nama orang tua : Hari Waluyo Ginting dan Meirna Rollina Alamat orang tua :
Taman Setiabudi Indah II blok IV/52
Asal Sekolah :
TK 3 Taman Siswa Arun tahun 1998-1999 SD 1 Taman Siswa Arun tahun 1999-2004 SMP Yayasan Pendidikan Arun tahun 2004-2008 SMA Yayasan Pendidikan Arun tahun 2008-2011 Pengalaman Organisasi :
Anggota HIMATEK periode 2013 – 2014
Artikel yang telah dipublikasikan dalam jurnal :
ABSTRAK
Penelitian ini bertujuan untuk mengetahui kemampuan desorpsi dan interaksi antara pasir putih yang terkontaminasi ion logam (Cd2+) 50 ppm dengan variasi konsentrasi SDS dan variasi kecepatan rotasi shaker pada larutan SDS dengan pH 7. Konsentrasi SDS yang digunakan adalah 0; 0,5; 1 dan 2 CMC. Variasi kecepatan rotasi shaker yang digunakan adalah 0; 50 dan 100 Rpm. Penelitian ini terbagi menjadi 2 tahap, yaitu perlakuan awal dengan melakukan kontaminasi pasir yang diawali dengan pencucian dan pengeringan hingga kondisi seragam. Kemudian dilanjutkan dengan pengukuran potensi kapasitas adsorpsi dengan sistem batch adsorption. Tahap kedua dilakukan tahap remediasi atau pencucian dengan SDS untuk meninjau kemampuan desorpsi dan interaksi antara SDS dan pasir putih yang terkontaminasi (Cd2+). Pengaruh konsentrasi SDS dalan me-remove atau mencuci ion logam Cd2+ terjadi peningkatan yang signifikan, disebabkan oleh adanya gaya mekanis rotasi shaker. Hasil removal terbesar terdapat pada saat konsentrasi SDS 2 CMC dengan kecepatan rotasi sebesar 100 Rpm, yaitu 10,01005% dan hasil removal terkecil berada pada konsentrasi 0 CMC dengan kecepatan rotasi 0 Rpm sebesar 3,462414%.
ABSTRAK
DAFTAR ISI
1.5 Ruang Lingkup Penelitian 5
BAB II TINJAUAN PUSTAKA 6
2.1 Karakteristik Logam Berat 6
2.2 Logam Kadmium (Cd) 7
2.3 Adsorpsi 9
2.4 Faktor-faktor yang Mempengaruhi Adsorpsi 12 2.5 Remediasi Logam Berat pada Pasir Terkontaminasi 10
2.6 Surfaktan 11
2.7 2.8
Sodium Dodecyl Sulfate (SDS)
Rangkaian Peralatan Percobaan Remediasi Pasir Terkontaminasi pada Batch System
14
BAB III METODOLOGI PENELITIAN 16
3.1 Lokasi dan Waktu Penelitian 16
3.2 Bahan dan Peralatan 16
3.3 Rancangan Percobaan 16
3.4 Prosedur Penelitan 16
3.5 Rangkaian Peralatan Percobaan Remediasi Pasir
Terkontaminasi pada Batch System 28
BAB IV HASIL DAN PEMBAHASAN 29
4.1 Pre-Treatment Awal pada Adsorben Pasir Putih 29
4.2 Penentuan Kapasitas Adsorpsi 30
4.3 Penentuan Removal Efisiensi Cd(II) dengan Variasi
Konsentrasi Surfaktan 33
4.4 Penentuan Kapasitas Adsorpsi 36
BAB V KESIMPULAN DAN SARAN 38
5.1 Kesimpulan 38
5.2 Saran 38
DAFTAR PUSTAKA 39
LAMPIRAN A 43
LAMPIRAN B 45
DAFTAR GAMBAR
Halaman Gambar 2.1 Rangkaian Peralatan Percobaan Remediasi Sistem
Batch 15
Gambar 3.1 Flowchart Persiapan Adsorben Pasir Putih 21 Gambar 3.2 Flowchart Pengeringan Adsorben Pasir Putih 21 Gambar 3.3 Flowchart Pembuatan Larutan HCL 0,1 M 22 Gambar 3.4 Flowchart Pembuatan Larutan NaOH 0,1 M 22 Gambar 3.5 Flowchart Pembuatan Larutan Pelarut dengan pH 4,5 23 Gambar 3.6 Flowchart Pembuatan Larutan Standar Cd2+ 50 ppm 23 Gambar 3.7 Flowchart Mengukur Pengaruh Ukuran Adsorben
terhadap Kemampuan Adsorpsi 24
Gambar 3.8 Flowchart Mengukur Removal Efisiensi terhadap
Variasi Konsentrasi SDS 25
Gambar 3.9 Flowchart Mengukur Kinetika Pencucian Pasir
terhadap Logam Cd2+ pada Batch System 27
Gambar 4.1 Pencucian Adsorben Pasir Putih 29
Gambar 4.2 Pengeringan Adsorben Pasir Putih 30
Gambar 4.3 (a) Konfirmasi Analisa FTIR pasir sebelum
Terkontaminasi 31
Gambar 4.3 (b) Konfirmasi Analisa FTIR pasir setelah
Terkontaminasi 31
Gambar 4.4 Nilai Removal Efisiensi dengan Variasi Konsentrasi
Surfaktan (SDS) dan Variasi Kecepatan rotasi (shaker) 33 Gambar 4.5 Grafik Kinetika Desorpsi pada 2 CMC 100 Rpm 36 Gambar L-C.1 Pencucian Pasir Putih yang Akan digunakan Sebagai
Adsorben 49
Gambar L-C.2 Kontaminasi Adsorben Pasir Putih dengan Ion Logam
Cd(II) 49
Gambar L-C.4 Foto Shaking Sampel saat Penentuan Persen Kinetika
Desorpsi 50
DAFTAR TABEL
Halaman Tabel 1.1 Data Beberapa Hasil Penelitian yang Memanfaatkan
Pasir sebagai Adsorben 3
Tabel 4.1 Data Hasil Removal Efisiensi 34
Tabel L-A.1 Data Proses Pencucian Adsorben Pasir Putih 43 Tabel L-A.2 Data Proses Pengeringan Pasir Putih 43 Tabel L-A.3
Tabel L-A.4
Data Hasil Removal Efisiensi dengan Berbagai Variasi Konsentrasi Surfaktan dan Kecepatan Pengadukan Shaker
Data Hasil Penentuan Kinetika Desorpsi Pada Konsentrasi Surfaktan (SDS) 2 CMC 100 Rpm
44
DAFTAR LAMPIRAN
LAMPIRAN A DATA HASIL PERCOBAAN Halaman
LA.1 Data Hasil Pencucian Adsorben Pasir Putih 43 LA.2 Data Hasil Pengeringan Adsorben Pasir
Putih 43 Pada Konsentrasi Surfaktan (SDS) 2 CMC 100 Rpm
44
44
LAMPIRAN B CONTOH HASIL PERHITUNGAN 45
LB.1 Pembuatan Larutan 45
LB.2 LAMPIRAN C FOTO HASIL PENELITIAN
LC.1 Pencucian Pasir Putih yang Akan
Digunakan Sebagai Adorben 49
LC.2 Kontaminasi Adsorben Pasir Putih dengan
Ion Logam Cd(II) 45
LC.3 Foto Shaking Sampel dan Penentuan
Persen Removal Efisiensi 50
LC.4 Foto Shaking Sampel dan Penentuan Persen Kinetika Desorpsi
DAFTAR SINGKATAN
AAS Atomic Adsorption Spectroscopy BET Brunaeur Emmet Teller
FTIR Fourier Transform Infrared RPM
PPM CMC
Rotation per minute
Part per Million
DAFTAR SIMBOL
Simbol Keterangan Dimensi
Cd Kadmium
Ni Nikel
CdS CdO
Kadmium Sulfida Kadmium Oksida
% Persen
HCl Asam klorida
NaOH Natrium Hidroksida
H2O
Cd(CH3COO)2.2H2O
Air
Kadmium Asetat Dihidrat
H+ Ion hidrogen
m Berat adsorben g
V Volume larutan logam yang
digunakan ml