MODIFIKASI ASILASI DAN SUKSINILASI PATI
TAPIOKA SEBAGAI BAHAN ENKAPSULASI
KOMPONEN FLAVOR
RINI HUSTIANY
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
MODIFIKASI ASILASI DAN SUKSINILASI PATI
TAPIOKA SEBAGAI BAHAN ENKAPSULASI
KOMPONEN FLAVOR
RINI HUSTIANY
Disertasi
sebagai salah satu syarat untuk memperoleh gelar Doktor
pada
Departemen Ilmu dan Teknologi Pangan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
sebagai Bahan Enkapsulasi Komponen Flavor
Nama
: RINI HUSTIANY
NRP
: F 226010031
Disetujui,
Komisi Pembimbing
Prof.Dr.Ir. Dedi Fardiaz, MSc
Ketua
Dr.Ir. Anton Apriyantono, MS
Dr.Ir. Nuri Andarwulan
Anggota
Anggota
Diketahui,
Ketua Program Studi
Dekan Sekolah Pascasarjana
Ilmu Pangan
Prof.Dr.Ir. Betty Sri Laksmi Jenie, MS
Dr.Ir. Khairil Anwar Notodiputro, MS
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa disertasi yang berjudul Modifikasi Asilasi dan Suksinilasi Pati Tapioka sebagai Bahan Enkapsulasi Komponen Flavor adalah benar merupakan hasil karya saya sendiri dan belum pernah diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka pada disertasi ini.
Bogor, Agustus 2006
@ Hal cipta milik Institut Pertanian Bogor, tahun 2006 Hak cipta dilindungi
Dilarang mengutip dan memperbanyak tanpa izin tertulis dari Institut Pertanian Bogor, sebagian atau seluruhnya dalam bentuk apapun,
encapsulant of flavor compound. Be guidance Dedi Fardiaz, Anton Apriyantono, and Nuri Andarwulan.
ABSTRACT
Modified starch is one of common ingredients used in food processing among other for coating and flavor encapsulation. This component can be made by modifying the structure of native starch either through chemical or enzymatic reaction. The encapsulation method by spray drying seems to be useful to solve these problems for flavor compounds which its high volatility. It was very important problems for applications and shelf life. This research was aimed to chemically modify tapioca starch into a modified starch with improved coating characteristic. The modified starches used to encapsulate flavor compounds. Encapsulated of flavor compound investigated its stability during storage at 45oC with Avrami equation and through accelerated test with Arrhenius equation and linear equation. The tapioca starch was first hydrolyzed to a hydrolyzate with dextrose equivalent of 9.1. Both tapioca starch and hydrolyzate were further acylated with stearic acid and propionic acid and succinylated with succinic acid. The concentrations of acids used for acylation and succinylation were 2.44, 4.76, and 9.09 %. The seven of flavor compounds, i.e α-pinene, ethyl butanoate, myrcene, ethyl crotonate, limonene, linalool, and α-terpineol encapsulated with tapioca starch and hydrolyzate stearic 9.09%, propionic 9.09% and succinic 4.76% by spray drying at flavor compounds/modified starch ratio 20:80 and 30:70. The encapsulated of flavor compounds with starch hydrolyzate stearic 9.09% and propionic 9.09% at flavor compounds/modified starch ratio 20:80 stored in bottle at 45oC for 9 weeks to investigated its stability during storage with Avrami equation and through accelerated test with Arrhenius equation and linear equation at 30oC, 37.5oC, and 45oC for 9 weeks. The modified starches were analyzed for their yield and moisture content, the degree of substitution, functional groups, crystalline structure, polarization, gelatinization properties and viscosity. Encapsulated of flavor compounds were analyzed for the yield, moisture content, water activity, shape of structure with scanning electron microscope and retention flavor with chromatography gas. The storage of encapsulated of flavor compounds were analyzed for water activity, retention flavor with chromatography gas. The moisture content of the modified starches was 1.52-3.32% and the yield was 87.45-95.43%. The hydroxyl group substitution into acyl and succinyl groups was low, i.e 0.03-0.04 and 0.05-0.08 respectively. The results showed that methyl, methylene and CO carbonyl groups were formed in the modified starches. The crystalline structure of the modified starches was broken. This revealed that the peak 22.62o was widen and the doublet were disappearing on peak 16.85o and 17.99o. Birefringence of the acylated and succinylated starch changed significantly and disappeared in the case of acylated and succinylated hydrolizate. The initial and optimum gelatinization temperature of acylated and succinylated starch were 57.6 -64.2oC
and 68.62-92.4oC respectively, and the maximum viscosity was 14-714
hydrolyzat were (25.85-35.59%), (3.41-4.80%) and (0.472-0.559), respectively, while with the acylated and succinylated starch were (18.93-19.46%), (4.76-5.10%) and (0.566-0.586), respectively. The surfaces of particles encapsulated starches were rough, hallow in the middle, with a concave radius of curvature. The flavor compounds entrapped within the wall encapsulants. Retention flavor compounds on different encapsulants were α−pinene (4.87-45.45%), ethyl butanoate (2.17-17.7%), myrcene (5.94-77.35%), ethyl crotonate (5.23-35.76%), limonene (6.19-81.03%), linalool (16.78-100%), and α-terpineol (58.67-100%). The stability of retention of flavor compounds during storage were decrease. After collaps, retention of flavor compounds were stable and finally retention of flavor compounds were decrease again. The stability of retention of flavor compounds were analyzed with Avrami equation at 45oC, Arrhenius equation and linear
equation. The fastest of retention of encapsulated flavor compounds decrease were ethyl butanoate, followed ethyl crotonate, myrcene, limonene, α-pinene, linalool, and α-terpineol, respectively with Avrami equation. The effect of temperature, the fastest of retention of encapsulated flavor compounds in hydrolysate stearic decrease were linalool followed α-terpineol, myrcene, limonene and α-pinene. And the fastest of retention of encapsulated flavor compounds in hydrolysate propionic decrease were α-pinene followed myrcene, linalool, α-terpineol, and limonene. Based on our finding it is suggested that acylation (9.09%) and succinylation (4.76%) of tapioca starch can be used to modify the starch into a product with better coating characteristic. The flavor compounds recommended to encapsulated with hydrolyzate stearic 9.09% and propionic 9.09% at flavor compounds/modified starch ratio 20:80. The best of stability of retention of flavor compounds were encapsulated with hydrolyzate stearic.
Key words: modified starch, acylation, succinylation, flavor, ancapsulation,
enkapsulasi komponen flavor. Dibawah bimbingan Dedi Fardiaz, Anton Apriyantono dan Nuri Andarwulan.
RINGKASAN
Pati termodifikasi adalah salah satu ingeredien pangan yang umum digunakan sebagai penyalut pada proses enkapsulasi flavor. Pati termodifikasi ini dapat dihasilkan dengan memodifikasi struktur pati melalui reaksi kimia atau enzimatik. Produk pati termodifikasi dapat dijadikan matrikspada proses enkapsulasi komponen-komponen flavor yang bersifat sangat volatil dengan
spray drying untuk memecahkan permasalahan selama proses aplikasi dan
penyimpanan. Penelitian ini bertujuan untuk memodifikasi pati tapioka menjadi pati termodifikasi yang dapat digunakan sebagai enkapsulan. Pati termodifikasi ini digunakan untuk mengenkapsulasi tujuh komponen flavor. Komponen flavor terenkapsulasi dilihat stabilitasnya selama penyimpanan pada suhu 45oC dan
melalui uji akselerasi dengan persamaan Arrhenius dan persamaan linear. Metode yang digunakan adalah pertama kali dilakukan hidrolisis pati tapioka menjadi hidrolisat pati tapioka dengan dextrose equivalent 9,1. Pati tapioka dan hidrolisat pati tapioka diasilasi dengan asam stearat dan asam propionat dan disuksinilasi dengan asam suksinat. Konsentrasi digunakan untuk asilasi dan suksinilasi adalah 2,44, 4,76, dan 9,09%. Tujuh komponen flavor, yaitu ethyl
butanoate, ethyl crotonate, α-pinene, myrcene, limonene, linalool, dan α-terpineol
dienkapsulasi dengan pati stearat 9,09%, pati propionat 9,09% dan pati suksinat 4,76%, serta hidrolisat pati stearat 9,09%, hidrolisat pati propionat 9,09% dan hidrolisat pati suksinat 4,76% dengan pengering semprot pada nisbah antara komponen flavor/pati termodifikasi 20:80 dan 30:70. Komponen flavor terenkapsulasi dengan hidrolisat pati stearat 9,09% dan hidrolisat pati propionat 9,09% pada nisbah antara komponen flavor dan pati termodifikasi 20:80 disimpan didalam botol dan suhu 45oC selama 9 minggu untuk dilihat pola stabilitas dan stabilitasnya selama penyimpanan. Untuk melihat pengaruh suhu terhadap laju penurunan stabilitas retensi komponen flavor terenkapsulasi, komponen flavor terenkapsulasi disimpan dalam botol pada 30oC, 37,5oC, dan
45oC selama 9 minggu. Pati termodifikasi dianalisis berupa rendemen, kadar air,
derajat substitusi, gugus fungsional, struktur kristal, polarisasi, tingkat gelatinisasi dan viskositas. Pati terenkapsulasi dengan komponen flavor dianalisis berupa rendemen, kadar air, aktivitas air, bentuk struktur dengan scanning electrone
microscope dan retensi flavor dengan kromatografi gas. Stabilitas komponen
flavor terenkapsulasi selama penyimpanan dianalisis aktivitas air dan retensi flavor dengan kromatografi gas untuk menentukan pola stabilitas dan laju penurunan stabilitas retensi komponen flavor selama penyimpanan dengan data empirik dan persamaan Avrami, serta persamaan Arrhenius dan persamaan linear. Kandungan air pati termodifikasi adalah 1,52-3,32% dan rendemennya adalah 87,45-95,443%. Substitusi gugus hidroksil dengan gugus asil dan suksinil adalah rendah, yaitu masing-masing 0,03-0,04 dan 0,05-0,08. Buktinya adalah terbentuknya gugus metil, metilen dan CO karbonil pada pati termodifikasi. Struktur kristal pati termodifikasi rusak. Hal ini ditunjukkan dengan peak 22,62o hasil difraksi sinar x yang melebar dan doublet pada peak 16,85o dan 17.99o
viskositas maksimum adalah 14-714 Brabender Unit. Tidak ada suhu awal dan suhu optimal gelatinisasi serta tidak ada viskositas maksimum yang ditemukan pada hidrolisat pati terasilasi dan tersuksinilasi. Rendemen, kadar air dan aktivitas air pati terenkapsulasi dengan hirolisat pati terasilasi dan tersuksinilasi masing -masing adalah 25,85-35,59%, 3,42-4,80% dan 0,47-0,56, sedangkan dengan pati terasilasi dan tersuksinilasi masing-masing adalah 18,93-19,46%, 4,76-5,20% dan 0,57-0,59. Permukaan partikel pati terenkapsulasi adalah kasar, berlubang pada bagian tengahnya dengan bentuk seperti cekungan. Komponen-komponen flavor berada pada dinding enkapsulan. Retensi flavor pada berbagai matriksadalah α-pinene (4,87-45,45%), ethyl butanoate (2,17-17,7%), myrcene
(5,94-77,35%), ethyl crotonate (5,23-35,76%), limonene (6,19-81,03%), linalool
(16,78-100%), and α-terpineol (58,67-100%). Pola stabilitas retensi komponen flavor adalah menurun sampai titik collaps, kemudian stabil dan setelah itu menurun lagi secara tajam. Stabilitas retensi terendah berdasarkan persamaan Avrami dan data empirik pada suhu 45oC adalah ethyl butanoate diikuti dengan
ethyl crotonate, myrcene, limonene, α-pinene, linalool dan α-terpineol. Adanya
pengaruh suhu, stabilitas retensi komponen flavor terenkapsulasi dalam hidrolisat pati stearat yang paling cepat turun adalah linalool diikuti dengan α-terpineol,
myrcene, limonene, dan α-pinene. Adapun stabilitas retensi komponen flavor
terenkapsulasi dalam hidrolisat pati propionat yang paling cepat turun adalah α
-pinene diikuti dengan myrcene, linalool, α-terpineol, dan limonene. Berdasarkan
hal diatas, kesimpulan dari penelitian ini adalah asilasi (9,09%) dan suksinilasi (4,76%) pati tapioka dapat digunakan sebagai pati termodifikasi dengan karakteristik yang baik untuk pengenkapsulasi. Hidrolisat pati stearat 9,09% dan hidrolisat pati propionat 9,09% pada nisbah antara komponen flavor dan pati termodifikasi 20:80 direkomendasikan untuk mengenkapsulasi komponen-komponen flavor. Selain itu juga direkomendasikan untuk mengenkapsulasi komponen-komponen flavor yang bersifat hidrofobik, seperti α-pinene, myrcene,
dan limonene dengan hidrolisat pati stearat. Adapun komponen flavor yang
kurang bersifat hidrofobik, seperti linalool dan α-terpineol, direkomendasikan untuk dienkapsulasi dengan hidrolisat pati propionat. Stabilitas retensi komponen flavor terbaik apabila dienkapsulasi dengan hidrolisat pati stearat.
Puji syukur ke-hadirat Allah Subhana wa Ta’ala kami panjatkan atas rahmat
dan ridho -Nya sehingga penulis diberikan kesempatan untuk mengikuti Program
Doktor di Program Studi Ilmu Pangan, Sekolah Pascasarjana, Institut Pertanian
Bogor. Akhirnya penulis dapat menyelesaikan disertasi yang berjudul “Modifikasi
Asilasi dan Suksinilasi Pati Tapioka sebagai Bahan Enkapsulasi Komponen Flavor”.
Dengan selesainya disertasi ini penulis menyampaikan ucapan terima kasih dan
penghargaan yang setinggi-tingginya kepada :
1. Prof.Dr.Ir. Dedi Fardiaz, MSc yang telah memberikan bimbingan dan perhatian
di tengah kesibukan beliau yang padat.
2. Dr.Ir. Anton Apriyantono, MS yang banyak memberikan pembelajaran, falsafah
keilmuan dan ilmuwan, idealisme, pemecahan masalah kehidupan dan
perhatian. Kami yakin, walaupun Bapak jauh, Bapak pasti masih ingat kepada
kami.
3. Dr.Ir. Nuri Andarwulan yang telah memberikan bimbingan dan perhatian
ditengah kesibukan beliau, yang baru belakangan penulis rasakan. Ada
pepatah yang mengatakan “kala u tidak kenal maka tak sayang”
4. Dr.Purwiyatno Hariyadi, MSc sebagai penguji luar komisi pada ujian Preliminary
dan ujian tertutup. Saran Bapak sangat berharga bagi ketajaman pemahaman
penulis.
5. Prof. Dr. Ir. Djoko Said Damardjati dan Prof. Dr. Ir. Djumali Mangunwidjaja, DEA
yang bertindak sebagai penguji pada ujian terbuka. Saran dan pertanyaan
Bapak sangat membantu bagi ketajaman analisis penulis.
6. Dr. Ir. Khairil Anwar Notodiputro, MS selaku Dekan Sekolah Pasca Sarjana
Institut Pertanian Bogor dan pimpinan sidang pada ujian terbuka
7. Prof. Betty Sri Laksmi Jenie, MS sebagai ketua program studi Ilmu Pangan
yang banyak memberikan masukan kepada penulis, baik sebagai dosen
maupun sebagai ibu.
8. Dr. Ir. Ratih Dewanti-Hariyadi, MSc yang bersedia menjadi wakil dari Program
Studi Ilmu Pangan sekaligus menjadi pimpinan sidang ujian tertutup.
9. Prof. Ir. Rasmadi, MS dan Prof.Dr.Ir. Hakimah Halim, MSc selaku Rektor dan
Dekan Fakultas Pertanian Universitas Lambung Mangkurat yang telah
memberikan kesempatan dan perhatian kepada penulis untuk melanjutkan S3
Muda tahun anggaran 2006, Pemda Kalimantan Selatan dan Yayasan
Supersemar yang telah memberikan bantuannya berupa anggaran penelitian,
sehingga penulis dapat menyelesaian penelitian ini
12. PT Firmenich Indonesia melalui bapak Yonogowasakti, PT Mane Indonesia
melalui Ib u Eni dan Ibu Trisna, serta National Starch Indonesia sehingga
penulis mendapatkan bahan-bahan penelitian dengan mudah
13. Ibu Siti Nurjanah yang penulis tidak kenal secara fisik, hanya dunia maya yang
mengenalkan penulis dengan ibu. Ibu banyak membantu penulis, sehingga
penulis dimudahkan untuk mencari literatur yang up to date dan sesuai dengan perkembangan jaman.
14. Teman-teman serta teknisi-teknisi yang tidak bisa penulis sebutkan satu
persatu yang telah banyak membantu penulis dalam penyelesaian penelitian
ini.
15. Secara hormat pada orang tua penulis, yaitu Bapak M. Husni (alm) dan Ibu
Djurniah. Kasih sayang orang tua tanpa batas dan tanpa pamrih. Tanpa mereka
penulis tidak ada apa-apanya
16. Akhirnya buat suamiku dan anakku tersayang adalah ucapan terima kasih yang
tak bisa dilukiskan dengan kata -kata.
Tak lupa penulis baik secara pribadi maupun beserta keluarga mohon maaf
apabila selama penyelesaian pendidikan banyak melakukan kekhilafan. Semoga
Allah SWT selalu melimpahkan rahmat dan hidayahNya kepada semua pihak yang
telah membantu dalam pelaksanaan pendidikan, penelitian dan penulisan disertasi.
Semoga karya kecil ini bermanfaat.
Bogor, Agustus 2006
Penulis dilahirkan di Banjarmasin pada tanggal 24 Mei 1971 dari Bapak
bernama M. Husni (alm) dan Ibu bernama Djurniah, diberi nama Rini Hustiany.
Penulis adalah anak pertama dari tiga bersaudara. Masa kecil penulis berada di
suatu daerah di aliran sungai Barito, yaitu kota Marabahan. Dari kota inilah, penulis
mulai mengenal apa itu “ilmu pengetahuan” dan bersekolah SD di kota ini sampai
kelas empat. Kepindahan orang tua bekerja, penulis melanjutkan sekolah SD di
Banjarmasin, SMPN 9 Banjarmasin dan SMAN 1 Banjarmasin. Pada tahun 1990
penulis mendapat undangan dari Institut Pertanian Bogor untuk melanjutkan S1
melalui jalur USMI dan menjadi mahasiswa IPB angkatan 27. Tahun pertama
adalah Tingkat Persiapan Bersama (TPB), kemudian pada tahun 1991 penulis
diterima di Jurusan Teknologi Industri Pertanian, Fakultas Teknologi Pertanian.
Bulan Desember 1994 penulis ujian dengan judul penelitian “Ekstraksi dan
Karakterisasi Minyak Atsiri serta Oleoresin Daging Buah Pala (Myristica fragrans, Houtt)” dan diwisuda pada bulan Januari 1995. Desember 1995, penulis diterima
sebagai staf pengajar pada Fakultas Pertanian Universitas Lambung Mangkurat
sampai sekarang. Pada tahun 1997, penulis mendapat beasiswa BPPS untuk
melanjutkan S2 di Program Studi Ilmu Pangan, Institut Pertanian Bogor dan
diwisuda pada Januari 2001 dengan judul penelitian ”Identifikasi dan Karakterisasi
Komponen Off Odor Pada Daging Itik”. September 2001, penulis mendapatkan beasiswa lagi untuk melanjutkan S3 di Program Studi Ilmu Pangan, Institut
Halaman
DAFTAR ISI... xii
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xvi
DAFTAR DATA PELENGKAP... xix
PENDAHULUAN... 1
Latar Belakang ... 1
Tujuan Penelitian... 5
Hipotesis Penelitian ... 5
Manfaat Penelitian ... 6
Tahapan Peneltian... 6
TINJAUAN PUSTAKA... 9
Tapioka ... 9
Pati ... 10
Struktur Pati... 11
Struktur Kristal Pati ... 14
Granula Pati ... 16
Gelatinisasi ... 18
Sifat Fisik Struktur Pati ... 19
Modifikasi Pati ... 20
Enkapsulasi ... 22
Enkapsulasi dengan Pengering Semprot ... 24
Jenis-Jenis Matriks Pembawa ... 26
Flavor... 27
Stabilitas Flavor Terenkapsulasi ... 30
Metode Penentuan Stabilitas Flavor Terenkapsulasi ... 33
DAFTAR PUSTAKA... 35
MODIFIKASI ASILASI DAN SUKSINILASI PATI TAPIOKA... 41
Abstract ... 41
Pendahuluan... 41
Bahan dan Metode... 42
Hasil dan Pembahasan... 47
Simpulan ... 66
Ucapan Terima Kasih... 66
Daftar Pustaka ... 66
ENKAPSULASI KOMPONEN FLAVOR DENGAN PATI TAPIOKA TERMODIFIKASI... 70
Abstract ... 70
Pendahuluan... 70
Bahan dan Metode... 72
Hasil dan Pembahasan... 75
Daftar Pustaka ... 92
STABILIT AS RETENSI KOMPONEN FLAVOR TERENKAPSULASI DENGAN PATI TAPIOKA TERMODIFIKASI ... 95
Abstract ... 95
Pendahuluan... 95
Bahan dan Metode... 98
Hasil dan Pembahasan... 103
Simpulan ... 120
Daftar Pustaka ... 120
PEMBAHASAN UMUM... 123
SIMPULAN DAN SARAN UMUM... 127
Simpulan ... 127
Saran ... 128
Halaman Tinjauan Pustaka
1. Berbagai tipe pati tapioka termodifkasi berserta sifat dan
aplikasinya dalam bidang pangan... 10
2. Sifat-sifat beberapa granula pati ... 10
3. Sifat-sifat bahan pengenkapsulasi... 27
4. Sifat-sifat fisik dari beberapa flavor bua h-buahan... 28
Modifikasi Asilasi dan Suksinilasi Pati Tapioka 1. Nilai DE, kadar air dan rendemen pati tapioka termodifikasi ... 48
2. Identifikasi gugus CO karbonil pada pati tapioka termodifikasi ... 55
3. Tingkat gelatinisasi dan viskositas pati termodifikasi ... 65
Enkapsulasi Komponen Flavor dengan Pati Tapioka Termodifikasi 1. Rendemen, kadar air dan aw produk flavor terenkapsulasi pada nisbah 30:70 ... 75
2. Rendemen, kadar air dan aw produk flavor terenkapsulasi pada nisbah 30:70 dan 20:80 ... 79
3. Pengaruh jenis komponen flavor terhadap retensi produk flavor terenkapsulasi dengan hidrolisat pati stearat pada nisbah 20:80 beserta sifat-sifat masing-masing komponen flavor ... 84
4. Pengaruh nisbah antara komponen flavor dengan pati termodifikasi terhadap retensi produk flavor terenkapsulasi dengan hidrolisat pati stearat ... 86
5. Pengaruh jenis matriks terhadap retensi produk flavor terenkapsulasi... 88
6. Ukuran partikel komponen flavor yang dienkapsulasi dengan berbagai matriks... 89
7. Karakteristik pati komersial... 91
stearat selama penyimpanan pada suhu 45 C, aw 0,36 – 0,52 yang
dinyatakan sebagai persen perbandingan dengan retensi hari ke-0... 108
3. Retensi komponen flavor terenkapsulasi dengan hidrolisat pati propionat selama penyimpanan pada suhu 45oC, aw 0,35 – 0,51
yang dinyatakan sebagai persen perbandingan dengan retensi hari
ke-0... 108
4. Titik uap pada berbagai tekanan atmosfir dan titik didih
komponen-komponen flavor ... 109
5. Parameter n persamaan Avrami pada retensi komponen flavor terenkapsulasi selama penyimpanan suhu 45oC, aw 0,35 – 0,52
yang dinyatakan sebagai persen perbandingan dengan rete nsi hari
ke-0... 111
6. Parameter n persamaan Avrami pada retensi komponen flavor terenkapsulasi selama penyimpanan suhu 45oC, a
w 0,35 – 0,52
yang dinyatakan sebagai persen perbandingan dengan retensi hari
ke-0 setelah minggu ke-4 atau ke-5 ... 112
7. Hubungan anta ra lama penyimpanan dan retensi komponen flavor terenkapsulasi yang dinyatakan sebagai persen perbandingan
dengan retensi hari ke-0 pada aw 0,35 – 0,641 pada ordo 1 ... 114
8. Hubungan antara 1/T dan ln k untuk komponen flavor
terenkapsulasi dalam hidrolisat pati stearat pada ordo 1 ... 115
9. Hubungan antara 1/T dan ln k untuk komponen flavor
terenkapsulasi dalam hidrolisat pati propionat pada ordo 1 ... 116
10. Hubungan antara T(oC) dan ln k untuk komponen flavor
terenkapsulasi dalam hidrolisat pati stearat pada ordo 1 ... 118
11. Hubungan antara T (oC) dan ln k untuk komponen flavor
terenkapsulasi dalam hidrolisat pati propionat pada ordo 1 ... 118
12. Ukuran partikel komponen flavor yang dienkapsulasi dengan
Halaman Tinjauan Pustaka
1. Struktur molekul amilosa ... 11
2. Struktur molekul amilopektin ... 12
3. Struktur granula pati ... 13
4. Kelompok struktur amilopektin pada lapisan semikristal ... 14
5. Struktur granula pati ... 14
6. Difraksi sinar x pati ... 15
7. Pembetukan sulur ganda pada proses retrogradasi amilosa ... 16
8. Berbagai bentuk dan ukuran granula pati ... 17
9. Proses kelarutan granula pati ... 18
10. Hubungan antara viskositas dan lama pemanasan dan pendinginan pada granula pati ... 19
11. Perubahan sifat fisik bahan pangan... 20
12. Reaksi asilasi dan suksinilasi... 23
13. Alat pengering semprot... 26
14. Biosintesis komponen flavor buah-buahan... 29
15. Struktur kimia komponen flavor ... 29
16. Proses hidrasi awal, collaps, dan full collaps pada produk flavor terenkapsulasi... 32
Modifikasi Asilasi dan Suksinilasi Pati Tapioka 1. Derajat substitusi pati termodifikasi ... 49
2. Proses asilasi dan suksinilasi ... 51
3. Dugaan struktur kimia pati tapioka termodifikasi... 52
4. Spektrum infra merah (IR) ... 54
6. Pola difraksi sinar x pati tapioka dan pati tapioka termodifikasi ... 58
7. Pola difraksi sinar x pati tapioka terasilasi dan tersuksinilasi ... 59
8. Pola difraksi sinar x hidrolisat pati tapioka terasilasi dan
tersuksinilasi ... 60
9. Sifat mikroskopik granula pati ... 62
Enkapsulasi Komponen Flavor dengan Pati Tapioka Termodifikasi
1. Bentuk partikel produk flavor terenkapsulasi dengan pati terasilasi
atau tersuksinilasi di bawah scanning electron microscope... 77
2. Retensi produk flavor terenkapsulasi dengan pati terasilasi atau
tersuksinilasi ... 78
3. Bentuk partikel di bawah scanning electron microscope. A, pati tapioka; B, hidrolisat pati terasilasi atau tersuksinilasi yang telah
dihomogenisasi dan di pengering semprot ... 80
4. Bentuk partikel produk flavor terenkapsulasi dengan hidrolisat pati terasilasi dan tersuksinilasi menggunakan scanning electron
microscope... 81
5. Ilustrasi model enkapsulasi dengan pati termodifikasi yang di
pengering semprot ... 82
6. Profil kromatogram komponen flavor terenkapsulasi pati tapioka
termodifikasi... 83
7. Ikatan hidrogen antara α-terpineol dengan hidrolisat pati stearat ... 85
8. Ikatan hidrogen antara matriks yang mengandung sisi suksinat
dengan α-terpineol ... 90
9. Ikatan hidrogen antara matriks yang mengandung sisi propionat
dengan α-terpineol... 90
10. Perbandingan retensi komponen flavor terenkapsulasi antara hidrolisat pati terasilasi atau tersuksinilasi dengan pati komersial
(K4484 dan Flomax-8) pada nisbah 20:80 ... 91
Stabilitas Retensi Komponen Flavor Terenkapsulasi dengan Pati Tapioka Termodfikasi
1. Pola stabilitas retensi komponen-komponen flavor terenkapsulasi dengan hidrolisat pati stearat selama penyimpanan pada suhu 45oC dan aw 0,36-0,52 yang dinyatakan sebagai persen perbandingan
dengan hidrolisat pati propionat selama penyimpanan pada suhu 45oC dan aw 0,35-0,51 yang dinyatakan sebagai persen
perbandingan dengan retensi hari ke-0 ... 105
3. Hubungan antara retensi komponen flavor terenkapsulasi dalam hidrolisat pati stearat dengan waktu menggunakan persamaan
Avrami ... 111
4. Hubungan antara retensi α-pinene terenkapsulasi dalam hidrolisat
pati stearat dengan waktu menggunakan persamaan Avrami ... 112
5. Hubungan antara retensi α-pinene terenkapsulasi dalam hidrolisat pati stearat yang dinyatakan sebagai persen perbandingan dengan
retensi hari ke-0 dengan lama penyimpanan... 114
6. Hubungan antara retensi α-pinene terenkapsulasi dalam hidrolisat pati propionat yang dinyatakan sebagai persen perbandingan
dengan retensi hari ke-0 dengan lama penyimpanan... 115
7. Hubungan antata ln k dan 1/T pada α-pinene terenkapsulasi dalam
hidrolisat pati stearat pada ordo 1 ... 115
8. Hubungan antata ln k dan T(oC) pada α-pinene terenkapsulasi
dalam hidrolisat pati stearat pada ordo 1 dengan persamaan linear ... 117
9. Stabilitas retensi komponen-komponen flavor terenkapsulasi dengan hidrolisat pati stearat dan hidrolisat pati propionat selama penyimpanan pada suhu 45oC dan a
w 0,36-0,52 yang dinyatakan
Halaman
1. Perhitungan aktivitas enzim α-amilase dengan standar maltosa... 130
2. Spektrum infra merah (IR) dari pati tapioka termodifikasi ... 134
3. Nilai faktor respon (RF) dan waktu retensi (RT) masing -masing komponen flavor... 152
4. Karakteristik pati komersial Flo-Max 8 dan K4484 ... 153
5. Aktivitas air produk flavor terenkapsulasi selama penyimpanan... 155
Latar Belakang
Modifikasi tapioka sudah banyak dilakukan dengan berbagai macam cara,
seperti asilasi tapioka dan pregelatinisasinya dengan asam stearat untuk matriks
flavor (Varavinit et al. 2001), asilasi tapioka dengan asam propionat dicampur
dengan poliester poliuretan untuk dijadikan film (Santayonan dan
Wootthikanokkhan, 2003), hidrolisis dengan HCl untuk memperoleh tingkat kristal
yang tinggi (Atichokudomchai et al. 2001; Atichokudomchai et al. 2002), hidrolisis dengan HCl dan reaksi sila ng dengan natrium trimetafosfat untuk
pembuatan tablet (Atichokudomchai dan Varavinit, 2003); reaksi silang dengan fosfor oksiklorida (Khatijah, 2000), dekstrin (seperti K4484 adalah dekstrin
tapioka) dan pati termodifikasi (seperti flomax 8 adalah pati tapioka termodifikasi)
untuk dijadikan matriks (National Starch, 2005).
Pati-pati termodifikasi untuk matriks biasanya dalam bentuk pati oktenil
suksinat (Krishnan et al. 2005; Shaikh et al. 2005), pati suksinat (Jeon et al.
2003; Mongenot et al. 2000), pati pregelatinisasi (Ongen et al. 2002), pati dan pati pregelatinisasi stearat (Varavinit et al. 2001), maltodekstrin/pati oktenil
suksinat (Mongenot et al. 2000), maltodekstrin (Krishnan et al. 2005; Che Man et
al. 1999;Bhandari et al. 1992), dan siklodekstrin (Jeon et al. 2003; Bhandari et al. 1999). Dengan demikian untuk matriks biasanya digunakan pati termodifikasi
dengan asilasi atau suksinilasi, dan pati terhidrolisis. Proses asilasi atau
suksinilasi biasanya dilakukan pada media air, seperti NaOH (Lawal, 2004;
Miladinov dan Hanna, 2000; Jarowenko, 1989) atau dalam media nir-air, seperti
piridin (Lawal 2004; Santayonan dan Wootthikanokkhan, 2003) dan etanol
(Varavinit et al. 2001). Proses tersebut dapat dilakukan pada pati (Miladinov dan Hanna, 2000; Varavinit et al. 2001; Santayonan dan Wootthikanokkhan, 2003)
atau pati pregelatinisasi (Varavinit et al. 2001). Adapun proses hidrolisis yang banyak dilakukan adalah menggunakan asam, seperti HCl (Atichokudomchai dan
Varavinit, 2003) dan enzim (Kukman et al. 1998).
Produk -produk pangan yang biasa dilakukan enkapsulasi diantaranya
adalah flavor (Jeon et al. 2003; Varavinit et al. 2001; Mongenot et al. 2000; Gunning et al. 1999; Che Man et al. 1999; Bhandari et al. 1992), lemak/minyak
al.2004; Chan dan Zhang, 2005), vitamin (Redmond et al. 2003), mineral (Bebe
et al. 1999), pemanis dan warna.
Proses enkapsulasi dilakukan untuk memecahkan berbagai
permasalahan yang akan muncul pada waktu aplikasi dan penyimpanan, seperti
komponen-komponen flavor yang mempunyai volatilitas yang tinggi. Apabila
komponen flavor dienkapsulasi dengan suatu matriks, maka dapat melindungi
komponen flavor dari reaksi degradatif, mencegah kehilangan komponen flavor
dan meningkatkan stabilitas komponen flavor, serta menekan kerugian selama
penyimpanan dan pendistribusian.
Matriks yang biasa digunakan pada proses enkapsulasi komponen flavor
adalah maltodekstrin (Krishnan et al. 2005; Soottitantawat et al. 2005a; Che Man
et al. 1999; Bhandari et al. 1992), siklodekstrin (Yuliani et al. 2006; Jeon et al.
2003; Goubet et al. 2001; Bhandari et al. 1999), pati termodifikasi (Krishnan et
al. 2005; Shaikh et al. 2005; Soottitantawat et al. 2005a; Soottitantawat et al.
2005b; Jeon et al. 2003; Varavinit et al. 2001; Mongenot et al. 2000), dan gum arab (Yoshii et al. 2001; Kim dan Morr, 1996; Rosenberg et al. 1990).
Proses enkapsulasi dilakukan dengan berbagai teknik enkapsulasi
diantaranya adalah pengering semprot, spray chilling, ekstrusi, fluidized bed,
ekstrusi sentrifugal, koaservasi dan kompleksasi inklusi. Pengering semprot
paling umum digunakan untuk proses enkapsulasi komponen flavor
(Soottitantawat at al. 2005a dan 2005b; Krishnan et al. 2005; Shaikh et al. 2005; Kim dan Morr, 1996; Bhandari et al. 1992). Keuntungan dari metode pengering
semprot adalah melindungi reaksi degradatif dan mencegah kehilangan
komponen flavor selama penyimpanan. Ditambah lagi bahwa keuntungan utama
dari metode pengering semprot adalah melindungi komponen flavor dan
mengontrol pelepasan komponen flavor selama penyimpanan.
Komponen-komponen flavor seperti ethyl butanoate, ethyl crotonate, α
-pinene, myrcene, limonene, linalool dan α-terpineol adalah komponen-komponen
yang mudah menguap. Pencegahan kehilangan komponen flavor karena
menguap dengan enkapsulasi sudah banyak dilakukan, diantaranya adalah oleh
Rosenberg et al. (1990), Whorton (1995), Whorton dan Reineccius (1995),
Rosenberg et al. (1990) dan Yoshii et al. (2001) mengenkapsulasi ethyl
butanoate dengan gum arab menggunakan pengering semprot dan Yoshii et al.
(2001) mengenkapsulasi ethyl butanoate dengan maltodekstrin menggunakan
pengering semprot. Myrcene, α-pinene, limonene, dan linalool dienkapsulasi
dengan gum arab menggunakan pengering semprot (Bertolini et al. 2001).
Limonene dienkapsulasi dengan campuran gum arab dan maltodekstrin,
campuran HICAP 100 dengan maltodekstrin, HICAP 100 menggunakan
pengering semprot (Soottitantawat et al. 2004).
Kestabilan komponen flavor terenkapsulasi selama penyimpanan dan
distribusi dipengaruhi beberapa faktor, diantaranya adalah aw (Whorton dan
Reineccius, 1995; Soottitantawat et al. 2004; Soottitantawat et al. 2005b),
kelembaban relatif (Rosenberg et al. 1990; Yoshii et al. 2001; Soottitantawat et
al. 2004; Soottitantawat et al. 2005b), suhu transisi gelas (Whorton, 1995; Soottitantawat et al. 2004), komposisi dinding matriks (Soottitantawat et al. 2004;
Soottitantawat et al. 2005b); dan jenis komponen flavor (Rosenberg et al. 1990; Whorton dan Reineccius, 1995; Bertolini et al. 2001; Yoshii et al. 2001;
Soottitantawat et al. 2004; Soottitantawat et al. 2005b).
Whorton dan Reineccius (1995) menyatakan bahwa dengan nilai aw yang
semakin meningkat sampai pada suatu titik collaps, semakin meningkat pula pelepasan flavor terenkapsulasi di dalam maltodekstrin dengan berbagai nilai
dextrose equivalent (DE). Aldehida (C3 - C11) yang dicampur dengan minyak
sayur dan dienkapsulasi dengan maltodekstrin akan lepas pada aw > 0,44. Begitu
pula pada l-Menthol terenkapsulasi dengan HICAP 100 (pati jagung waxy oktenil suksinat anhidrat yang dicampur dengan sirup jagung DE 32-37) dan gum arab
akan lepas pada aw > 0,5 (Soottitantawat et al. 2005b). D-limonene juga semakin
meningkat pelepasannya dari matriks dengan meningkatnya aw pada daerah aw
rendah (0,1 – 0,5), kemudian menurun pada aw sekitar 0,7 – 0,8 dan meningkat
lagi pada aw yang lebih tinggi (Soottitantawat et al. 2004). Senada dengan
pengaruh aw (aw=RH/100) terhadap stabilitas retensi flavor terenkapsulasi,
kelembaban relatif (RH) yang semakin meningkat juga meningkatkan pelepasan
flavor (Soottitantawat et al. 2004; Soottitantawat et al. 2005b).
Suhu juga berpengaruh terhadap stabilitas retensi flavor terenkapsulasi.
Soottitantawat et al. (2004) menggambarkan bahwa pada suhu T – Tg (T adalah
flavor terenkapsulasi meningkat. Pada suhu T – Tg yang mendekati no l,
pelepasan flavor terenkapsulasi menurun.
Selain itu, matriks enkapsulasi juga berpengaruh terhadap stabilitas
retensi flavor. Soottitantawat et al. (2005b) menggambarkan bahwa pelepasan
l-menthol terenkapsulasi dengan gum arab dan HICAP 100 akan semakin
meningkat dengan semakin meningkatnya RH. Adapun pelepasan l-menthol
terenkapsulasi dengan CAPSUL (pati jagung waxy oktenil suksinat anhidrat)
adalah stabil dengan semakin meningkatnya RH.
Begitupula dengan Soottitantawat et al. (2004) yang menggambarkan
bahwa D-limonene terenkapsulasi dalam HICAP 100 dicampur dengan maltodekstrin DE 20 lebih cepat lepas dari matriks dibandingkan dengan
D-limonene terenkapsulasi dalam maltodekstrin DE 20 dicampur dengan gum arab
atau HICAP 100 saja. D-limonene paling lambat lepasnya dari matriks apabila
D-limonene terenkapsulasi dalam SSPS (soybean soluble polysaccharide)
dicampur dengan maltodekstrin DE 20.
Penurunan stabilitas retensi komponen flavor pada matriks padat atau
flavor terenkapsulasi disebabkan adanya perubaha n struktur matriks
terenkapsulasi dari fase glassy ke fase rubbery (Whorton, 1995; Soottitantawat et
al. 2004; Soottitantawat et al. 2005b). Fase rubbery menjadikan mobilitas molekuler dan volume bebas dari struktur matriks terenkapsulasi menjadi
meningkat. Kondisi ini semakin meningkat dengan meningkatnya suhu (Whorton,
1995). Stabilitas retensi flavor akan semakin menurun. Pada saat bersamaan
matriks terenkapsulasi menjadi collaps, partikel-partikel terenkapsulasi saling berdekatan dan bersatu serta menurunkan daerah permukaan matriks untuk
melepaskan flavor (Soottitantawat et al. 2004). Whorton dan Reineccius (1995) mengistilahkannya sebagai “reenkapsulasi” flavor.
Stabilitas retensi komponen flavor terenkapsulasi dapat ditentukan
dengan melihat pola stabilitas secara empiris maupun dengan menggunakan
persamaan Avrami pada suhu 50oC (Yoshii et al. 2001; Soottitantawat et al.
2004) dan suhu 43oC (Soottitantawat et al. 2005). Selain itu, stabilitas retensi
komponen flavor terenkapsulasi juga dapat ditentukan dengan uji akselerasi
dengan mempercepat suatu peubah penyimpanan, semisal suhu. Persamaan
yang biasa digunakan dengan suhu sebagai faktor akselerasinya adalah
Tujuan Penelitian
Tujuan dari penelitian ini adalah :
1. Di Indonesia, sebagian besar pati termodifikasi diperoleh dari impor. Dengan
begitu, dilakukan modifikasi pati tapioka dengan cara melakukan asilasi dan
suksinilasi menggunakan asam stearat, asam propionat dan asam suksinat
pada pati yang telah dihidrolisis dan yang belum dihidrolisis, sehingga
diperoleh pati termodifikasi yang dapat digunakan untuk berbagai tujuan
proses, seperti enkapsulasi.
2. Pati tapioka termodifikasi yang mempunyai sifat-sifat terbaik sebagai matriks
digunakan untuk mengenkapsulasi tujuh komponen flavor yang dijadikan
sebagai model, yaitu ethyl butanoate, ethyl crotonate, α-pinene, myrcene,
limonene, linalool, dan α-terpineol, dengan pengering semprot.
3. Pengaruh berbagai bahan matriks diteliti pada bentuk partikel pati
terenkapsulasi dan retensi komponen flavor terenkapsulasi.
4. Mengetahui stabilitas retensi komponen flavor terenkapsulasi pati tapioka
termodifikasi disimpan pada suhu 45oC berdasarkan pola stabilitas secara empiris dan dengan persamaan Avrami.
5. Mengetahui stabilitas komponen flavor terenkapsulasi dengan pati tapioka
termodifikasi selama penyimpanan pada suhu 30oC, 37,5oC dan 45oC dengan persamaan Arrhenius dan persamaan linear.
Hipotesis Penelitian
Hipotesis dari penelitian ini adalah :
1. Pati tapioka termodifikasi yang dihasilkan dengan cara dihidrolisis dan
dilanjutkan dengan proses asilasi dan suksinilasi mempunyai sifat-sifat
sebagai matriks.
2. Semakin besar sifat hidrofobik gugus yang disubstitusikan, maka semakin
besar pula interaksinya terhadap komponen flavor.
3. Semakin tinggi derajat substitusi gugus asil atau suksinil, maka semakin
Manfaat Penelitian
Manfaat dari penelitian ini adalah :
1. Menghasilkan pati tapioka termodifikasi yang mempunyai sifat-sifat sebagai matriks. Dengan begitu dapat membantu penganekaragaman pemanfaatan
tapioka, mengurangi impor pati-pati termodifikasi, dan yang tidak kalah pentingnya adalah membantu meningkatkan pendapatan industri kecil dan
mikro tapioka dan para petani singkong.
2. Memberikan informasi kepada pelaku industri pangan umumnya dan industri
flavor pada khususnya tentang dihasilkannya pati tapioka termodifikasi yang dapat dijadikan sebagai matriks flavor yang tidak kalah bersaingnya dengan
pati komersial.
3. Memberikan informasi kepada pelaku industri pangan umumnya dan industri
flavor pada khususnya tentang stabilitas retensi komponen flavor yang dienkapsulasi dengan pati tapioka termodifikasi selama penyimpanan pada
suhu 45oC dan dengan uji akselerasi pada suhu 30oC, 37,5oC dan 45oC menggunakan persamaan Arrhenius dan persamaan linear.
Tahapan Penelitian
Penelitian ini terdiri dari beberapa tahapan penelitian yang disajikan
dalam bentuk beberapa artikel tulisan yang sudah dipublikasikan dan yang akan
dipublikasikan. Tahapan penelitian tersebut adalah :
1. Modifikasi Asilasi dan Suksinilasi Pati Tapioka
Pada tahapan ini dilakukan modifikasi pati tapioka dengan asilasi
menggunakan asam stearat dan asam propionat dan suksinilasi dengan
menggunakan asam suksinat. Asilasi dan suksinilasi dilakukan pada tiga
konsentrasi, yaitu 2,44%, 4,76%, dan 9,09% pada hidrolisat pati DE 9,1 dan
pati tapioka. Pati termodifikasi yang dihasilkan adalah pati stearat, pati
propionat, pati suksinat, hidrolisat pati stearat, hidrolisat pati propionat dan
hidrolisat pati suksinat dengan konsentrasi 2,44%, 4,76%, dan 9,09%. Pati
termodifikasi yang dihasilkan bersifat derajat substitusi rendah, yaitu kurang
dari 0,5, terbentuknya ikatan ester, bagian kristal menurun, dan viskositas
rendah. Pati termodifikasi yang direkomendasikan untuk bahan enkapsulasi
propionat dengan konsentrasi 9,09%, serta pati suksinat dan hidrolisat pati
suksinat dengan konsentrasi 4,76%.
2. Enkapsulasi Komponen Flavor dengan Pati Tapioka Termodifikasi
Pati tapioka termodifikasi yang direkomendasikan pada tahap pertama
digunakan untuk mengenkapsulasi tujuh komponen flavor yang digunakan
sebagai model, yaitu ethyl butanoate, ethyl crotonate, α-pinene, myrcene,
limonene, linalool, dan α-terpineol, dengan pengering semprot. Nisbah antara
komponen flavor dan pati termodifikasi adalah 30:70 dan 20:80. Partikel
produk flavor terenkapsulasi yang dihasilkan berbentuk agak bulat dengan
permukaan yang tidak mulus, kasar dan ada cekungan-cekungan. Retensi
komponen flavor terenkapsulasi yang terendah adalah ethyl butanoate diikuti dengan ethyl crotonate, α-pinene, myrcene, limonene, linalool, dan α
-terpineol. Komponen flavor terenkapsulasi dengan hidrolisat pati stearat dan
hidrolisat pati propionat dengan nisbah 20:80 menghasilkan retensi yang lebih
tinggi dibandingkan dengan pati termodifikasi lainnya dan direkomendasikan
untuk diketehui stabilitas retensinya selama penyimpanan.
3. Stabilitas Retensi Komponen Flavor Terenkapsulasi dengan Pati Tapioka Termodifikasi
Pati tapioka termodifikasi dan nisbah antara komponen flavor dengan pati
termodifikasi yang direkomendasikan pada tahap kedua digunakan untuk
mengenkapsulasi tujuh komponen flavor yang digunakan sebagai model, yaitu
ethyl butanoate, ethyl crotonate, α-pinene, myrcene, limonene, linalool, dan α
-terpineol, dengan pengering semprot. Produk flavor terenkapsulasi disimpan
pada suhu 45oC selama 9 minggu untuk mengetahui pola penurunan stabilitas
retensi komponen flavor dan laju penurunan stabilitas retensi komponen flavor
terenkapsulasi berdasarkan data empiris dan persamaan Avrami. Selain itu,
stabilitas retensi komponen flavor terenkapsulasi dengan pati tapioka
termodifikasi ditentukan berdasarkan uji akselerasi dengan suhu sebagai
faktor akselerasinya. Caranya, produk flavor terenkapsulasi disimpan pada
suhu 30oC, 37,5oC dan 45oC selama 9 minggu untuk mengetahui laju
penurunan stabilitas retensi komponen flavor terenkapsulasi berdasarkan
persamaan Arrhenius dan persamaan linear. Hasil yang diperoleh adalah
aktivitas air produk flavor terenkapsulasi selama penyimpanan berkisar antara
sampai suatu titik collaps selama 4 sampai 5 minggu, kemudian stabil selama
3 minggu, setelah itu terus menurun. Penurunan stabilitas retensi komponen
flavor mengikuti mekanisme difusi dan termasuk reaksi ordo 1 berdasarkan
persamaan Avrami. Berdasarkan data empiris dan persamaan Avrami,
komponen flavor yang stabilitas retensinya terendah pada penyimpanan suhu
45oC adalah ethyl butanoate diikuti dengan ethyl crotonate, myrcene,
limonene, α-pinene, linalool dan α-terpineol. Laju penurunan stabilitas retensi
ethyl butanoate dan ethyl crotonate hanya berdasarkan data empiris tetapi
tidak bisa ditentukan berdasarkan persamaan Avrami. Ethyl butanoate dan
ethyl crotonate juga tidak dapat ditentukan stabilitas retensinya selama
penyimpanan dengan uji akselerasi menggunakan persamaan Arrhenius dan
persamaan linear. Dengan adanya pengaruh suhu selama penyimpanan
(30oC, 37,5oC dan 45oC), berdasarkan uji akselerasi menggunakan persamaan Arrhenius dan persamaan linear, komponen flavor terenkapsulasi
dalam hidrolisat pati stearat yang stabilitasnya terendah adalah linalool diikuti dengan α-terpineol, myrcene, limonene, dan α-pinene. Adapun komponen
flavor terenkapsulasi dalam hidrolisat pati propionat, komponen flavor yang
stabilitasnya terendah adalah α-pinene diikuti dengan myrcene, linalool, α
-terpineol dan limonene. Stabilitas retensi komponen flavor terenkapsulasi
Tapioka
Tapioka adalah pati yang banyak dihasilkan di Brazil, Thailand, Malaysia,
Indonesia, dan Nigeria. Tapioka berasal dari umbi singkong (Manihot esculenta) yang diambil patinya melalui proses penggilingan umbi singkong, dekantasi,
pemisahan ampas dengan konsentrat, pengendapan, dan pengeringan (Dziedzic
dan Kearsley, 1995).
Komponen utama dari tapioka adalah pati, yaitu 73,3 – 84,9%, yang terdiri
dari amilosa sebanyak 17% dan amilopektin 83%. Selain itu, tapioka juga
mengandung lemak sebesar 0,08-1,54%, protein (0,03-0,60%), abu
(0,02-0,33%), dan sedikit fosfor (0,8 -4,0% x 102) (Rickard et al. 1991).
Granula pati tapioka berbentuk semi bulat sampai bulat dengan salah satu dari bagian ujungnya mengerucut dengan ukuran 5-35 µm. Suhu gelatinisasi
berkisar antara 52-64oC, kristalinitas 38%, kekuatan pembengkakan sebesar 42 dan kelarutan 31%. Kekuatan pembengkakan dan kelarutan tapioka lebih kecil
dari pati kentang, tetapi lebih besar dari pati jagung (Rickard et al. 1991).
Suhu gelatinisasi pati tapioka berada di antara pati jagung waxy dan pati jagung reguler. Viskositasnya lebih rendah dibandingkan dengan pati jagung
waxy. Apabila dilakukan pendinginan, larutan pati mengalami retrogradasi untuk menghasilkan suatu gel yang halus. Larutan pati tapioka lebih jernih
dibandingkan pati-pati native yang lainnya (National Starch and Chemical Company, 1995).
Pati tapioka dapat digunakan pada industri pangan dan industri
non-pangan. Pada industri non-pangan, tapioka digunakan pada industri kertas, tekstil, kayu lapis, farmasi dan komestik, sedangkan pada industri pangan dapat
digunakan pada industri bakery, konfeksionari, es krim, saus dan mi instan. Pati tapioka digunakan sebagian besar dalam bentuk pati modifikasinya
atau turunannya. Pati tapioka native terbatas penggunaannya pada produk
bakery saja. Adapun apabila pati tapioka sudah dimodifikasi, maka dapat
Tabel 1. Berbagai tipe pati tapioka termodifkasi berserta sifat dan aplikasinya dalam bidang pangan1
Tipe Pati Sifat Aplikasi
Pati Pre-Gelatinisasi Larut dalam air dingin Sup instan, puding instan
Bahan Pengisi Saus, campuran bakery, makanan beku
Pati Hidrolisis Asam Viskositas rendah, retrogradasi Gum, permen, formulasi pangan tinggi, gel kuat cair
Dekstrin Bahan pengikat, pembungkus Konfeksionari, baking
Enkapsulasi Perisa, rempah dan minyak Pati Teroksidasi Stabiliser, perekat, penggel Formulasi pangan, gum,
agen penjernih konfeksionari
Pati Eter Stabiliser Sup, puding, makanan beku Pati Ester Stabiliser, bahan pengisi Permen, emulsi
penjernih
Pati reaksi silang Bahan pengisi, stabiliser, Pengisi pie, roti, makanan beku, pembentuk tekstur bakery, puding, makanan instan,
sup, salad dressing, saus
1
Anonim (2003)
Pati
Pati adalah karbohidrat utama yang diisolasi dari umbi tumbuhan dan
endosperma biji-bijian yang ditemukan dalam bentuk granula. Pati yang berasal
dari biji-bijian, dapat berasal dari serealia, seperti gandum, jagung, oats, beras
dan sorghum, sedangkan dari kacang-kacangan, seperti pea. Adapun dari umbi,
seperti kentang dan singkong (Belitz dan Grosch, 1999). Sifat-sifat granula pati
ini dapat dilihat pada Tabel 2.
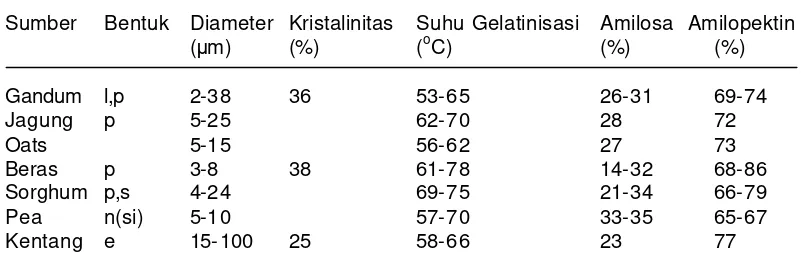
Tabel 2. Sifat-sifat beberapa granula pati1
Sumber Bentuk Diameter Kristalinitas Suhu Gelatinisasi Amilosa Amilopektin
(µm) (%) (oC) (%) (%)
Gandum l,p 2-38 36 53-65 26-31 69-74
Jagung p 5-25 62-70 28 72
Oats 5-15 56-62 27 73
Beras p 3-8 38 61-78 14-32 68-86
Sorghum p,s 4-24 69-75 21-34 66-79
Pea n(si) 5-10 57-70 33-35 65-67
Kentang e 15-100 25 58-66 23 77
Keterangan : l= lentikular, p= polihedral, s= bola, o= oval, n= ginjal , e= elips, si= sederhana
1Belitz dan Grosch (1999)
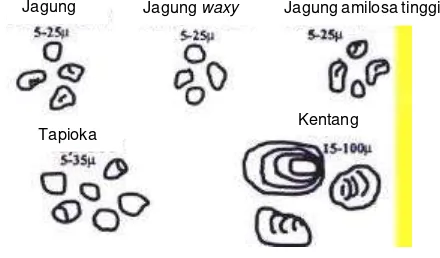
Selain itu ada pati yang mengandung 99% amilopektin, yang disebut
[image:30.595.111.514.508.643.2]disebut dengan pati amilosa tinggi (Dziedzic dan Kearsley, 1995). Pati waxy,
misalnya pati waxy jagung mempunyai sifat tidak menggel dan gelnya bersih, sedangkan pati amilosa tinggi membentuk gel yang kaku dan keruh (Schwenk,
2001).
Struktur Pati
Pati adalah karbohidrat yang merupakan polimer glukosa yang terdiri dari
amilosa dan amilopektin. Amilosa merupakan bagian polimer linear dengan
ikatan α-(1-->4) unit glukosa (Gambar 1). Derajat polimerisasi dari amilosa
berkisar antara 500-6000 unit glukosa, tergantung dari sumbernya. Adapun
amilopektin merupakan polimer α-(1-->4) unit glukosa dengan rantai samping α
-(1-->6) unit glukosa (Gambar 2). Ikatan α-(1-->6) unit glukosa ini jumlahnya
sangat sedikit dalam suatu molekul pati, berkisar antara 4-5%. Akan tetapi jumlah
molekul dengan rantai cabang, yaitu amilopektin, adalah amat sangat banyak
dengan derajat polimerisasi (DP) berkisar antara 105 sampai 3x106 unit glukosa (Jacobs dan Delcour, 1998).
Gambar 2. Struktur molekul amilopektin (Chaplin, 2002)
Amilosa merupakan bagian rantai lurus yang dapat memutar dan
membentuk daerah sulur ganda sebagaimana yang terlihat pada Gambar 1.
Pada permukaan luar amilosa sulur tunggal terdapat hidrogen yang berikatan
dengan atom O-2 dan O-6. Rantai lurus amilosa yang membentuk sulur ganda
kristal ini tahan terhadap amilase. Ikatan hidrogen inter- dan intra- sulur
mengakibatkan terbentuknya struktur hidrofobik dengan kelarutan yang rendah.
Oleh karena itu, sulur tunggal amilosa mirip dengan siklodekstrin yang bersifat
hidrofobik pada permukaan dalamnya (Chaplin, 2002).
Pada struktur granula pati, amilosa dan amilopektin ini tersusun dalam
suatu cincin-cincin. Jumlah cincin dalam suatu granula kurang lebih berjumlah
16, ada yang merupakan cincin lapisan amorf dan cincin yang merupakan
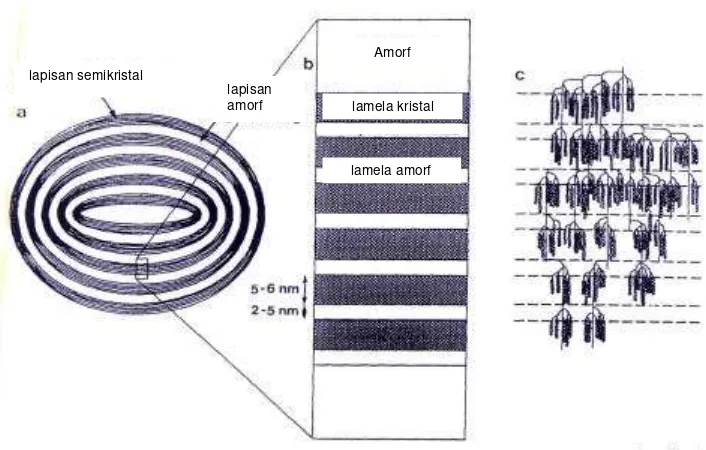
lapisan semikristal (Gambar 3a).
Semikristal merupakan lapisan cincin yang terdiri dari lamela kristal (5-6
nm) dan lamela amorf (2-5 nm). Kedua lamela ini tersusun secara bergantian
pada lapisan semikristal (Gambar 3b). Bagian lamela kristal merupakan sulur
ganda amilopektin dan rantai paralel glukan (Oates, 1997) dengan titik
percabangan amilopektin terletak pada daerah lamela amorf (Gambar 3c). Oleh
karena itu, lokasi amilosa dalam suatu granula pati tidak diketahui secara pasti
Gambar 3. Struktur granula pati (a) granula pati terdiri dari lapisan amorf dan semikristal; (b) lapisan semikristal yang terdiri dari lamela kristal dan lamela amorf; (c) kelompok struktur amilopektin pada lapisan semikristal (Jenkins et al. (1994) didalam Jacobs dan Delcour, 1998)
Amilosa merupakan fraksi gerak, artinya dalam granula pati letaknya tidak
pada satu tempat, tergantung dari jenis pati. Secara umum amilosa terletak
diantara molekul-molekul amilopektin dan secara acak berada selang seling
diantara daerah amorf dan kristal (Oates, 1997).
Dalam satu molekul amilopektin terdapat beberapa kelompok dan cabang
yang diberi nama rantai A, B dan C (Gambar 4). Rantai A adalah rantai yang
terluar yang melingkupi rantai B. Rantai A ini tidak bercabang dapat diserang
molekul dengan rantai tunggal. Rantai B melingkupi rantai B yang lainnya atau
rantai C. Rantai B ini bercabang dan dihubungkan oleh dua atau lebih rantai yang
lain. Pada setiap molekul amilopektin terdapat satu rantai C yang mengandung
satu gula pereduksi pada ujung rantainya. Rantai B yang banyak membuat
struktur granula menjadi kaku (Peat et al. (1952) di dalam Donald et al. 2003;
Oates, 1997).
Amilopektin ketika dipanaskan di dalam air membentuk suatu lapisan
yang transparan, larutan dengan viskositas yang tinggi dan berbentuk
lapisan-lapisan seperti untaian tali. Tidak cenderung terjadi retrogradasi dan tidak
membentuk gel, kecuali pada konsentrasi yang tinggi (Belitz dan Grosch, 1999).
lapisan semikristal
lapisan amorf
Amorf
lamela kristal
Gambar 4. Kelompok struktur amilopektin pada lapisan semikristal (Donald et al.
2003)
Selain itu didalam pati juga ditemukan komponen lain dalam jumlah yang
sedikit, yaitu lipida (sekitar 1%), protein, fosfor dan mineral-mineral (Jacobs dan
Delcour, 1998). Bagian lipida ada yang berikatan dengan amilosa dan ada yang
bebas (Gambar 5) (Belitz dan Grosch, 1999).
Gambar 5. Struktur granula pati. Sulur ganda amilopektin , sulur gandacampuran amilosa dan amilopektin ,V sulur
amilosa yang berikatan dengan lemak , lemak bebas amilosa bebas (Belitz dan Grosch, 1999)
Struktur Kristal Pati
Bagian kristal adalah bagian dari suatu materi dengan atom-atom atau
unit-unit selnya disusun dalam bentuk tiga dimensi yang tetap, pada suatu
daerah yang panjang dan massanya utuh. Polimer yang dapat membentuk kristal
adalah polimer bercabang yang mempunyai daerah linear dengan rantai panjang
dan bersulur, seperti amilopektin pada granula pati (Aguilera dan Stanley, 1999).
Granula pati native mengandung bagian kristal berkisar antara 15 sampai 45%. Bentuk -bentuk kristal pada granula pati bermacam-macam tergantung
ujung gula pereduksi rantai C
ikatan-α-1,6 ujung gula non pereduksi
rantai B
rantai B rantai B
rantai A
pada jenis patinya, yaitu tipe A, B, C dan V. Kristal A adalah kristal yang bagian
pusat monoklinik selnya mengandung 12 residu glukosa dan dua rantai pada
bagian sebelah kirinya mengandung 4 molekul air diantara rantai sulurnya.
Bentuk kristal A digambarkan seperti ortorombik. Kristal B adalah kristal
berbentuk heksagonal yang mengandung 12 residu glukosa dan 36 molekul air.
Setengah dari jumlah molekul air tersebut berikatan dengan sulur ganda dan
setengah yang lainnya berada pada pusat 6 lipatan sumbu. Adapun kristal C
adalah kristal antra bentuk A dan B (Oates, 1997). Selain itu juga ada bentuk
kristal V yang terjadi pada granula pati yang dapat mengembang (Belitz dan
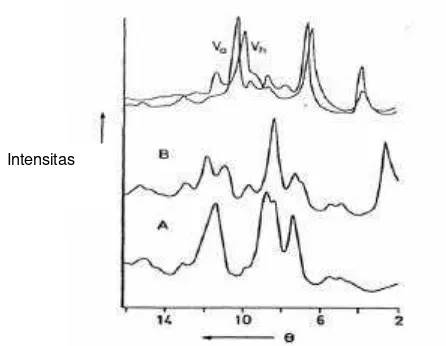
Grosch, 1999). Bentuk -bentuk kristal A, B dan V dapat ditentukan berdasarkan
[image:35.595.178.401.307.480.2]difraksi sinar x pati (Gambar 6).
Gambar 6. Difraksi sinar x pati: A: kristal A, B: kristal B, V; kristal V (Belitz dan Grosch, 1999)
Bagian amilosa juga dapat membentuk kristal. Pembentukan kristal pada
amilosa, yang sering disebut proses retrogradasi, terjadi setelah proses
pemanasan dan pendinginan pati. Granula pati yang membengkak kemudian
disimpan, maka dapat melepaskan amilosa. Amilosa ini diduga membentuk suatu
sulur ganda dengan rantai panjang atau membentuk suatu rantai sulur ganda
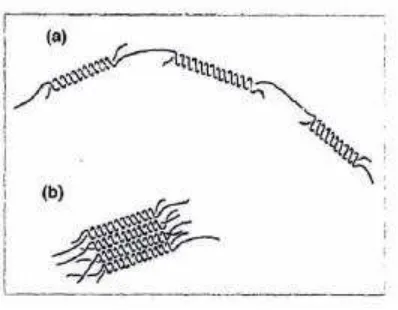
dengan cara menyamping (lateral) (Gambar 7) (Morris, 1990). Proses
retrogradasi ini juga dapat terjadi pada pati yang dihidrolisis. Sewaktu proses
hidrolisis, granula pati tergelatinisasi dan melepaskan amilosa. Amilosa yang
terlepas ini membentuk sulur ganda dan membentuk kristal (Atichokudomchai et
al. 2004). Kondisi seperti ini juga terjadi pada amilopektin, sehingga terjadi rekristalisasi pada amilopektin (Morris, 1990). Pati-pati yang telah terhidrolisis
dan granula patinya tergelatinisasi, mengakibatkan amilopektinnya keluar dan
[image:36.595.216.415.140.295.2]mengalami rekristalisasi (Atichokudomchai et al. 2004).
Gambar 7. Pembetukan sulur ganda pada proses retrogradasi amilosa (a) pembentukan sulur dengan rantai memanjang; (b) pembentukan sulur secara lateral (Morris, 1990)
Apabila dilakukan modifikasi pada pati, seperti modifikasi pati tapioka
dengan dihidrolisis menggunakan asam dan dilakukan reaksi silang dengan
natrium trimetafosfat, pola difraksi sinar x pati tapioka termodifikasi tidak terjadi
perbedaan yang besar dengan pati native. Perbedaannya terletak pada saat pati tapioka dihidrolisis dengan asam selama 192 jam, pola difraksi sinar x-nya lebih
melebar (Atichokudomchai dan Varavinit, 2003).
Granula Pati
Granula pati mengandung lapisan kristal dan amorf. Kedua lapisan ini
terletak selang seling dalam granula yang disebut leukoplas. Lapisan ini mulai
dibentuk dari lapisan yang paling dalam atau inti granula pati yang disebut
dengan hilum (McWilliams, 2001). Hilum sebagian besar mengandung ujung gula
pereduksi molekul pati. Adapun ujung gula non pereduksi berada pada
permukaan granula (Oates, 1997; Elliasson dan Gudmundsson, 1996).
Apabila granula pati berada di bawah filter polarisasi, maka tampak suatu
pola birefringence, yaitu refraksi cahaya pada dua daerah yang berbeda. Pola
birefringence ini memperlihatkan suatu persilangan yang berbentuk V dengan
titik persilangannya hilum, yang disebut dengan Maltese cross. Maltese cross
memisahkan antara bagian kristal dan amorf dengan sama panjang (McWilliams,
Pola birefringence yang unik pada granula pati ini hanya terdapat pada
pati mentah. Ketika pati dipanaskan dengan air, daerah kristal yang bertanggung
jawab terhadap refraksi cahaya alami terjadi perubahan. Akhirnya pola Maltese
cross tidak sama panjang atau menghilang (McWilliams, 2001).
Bentuk dan ukuran granula pati berbeda-beda tergantung dari sumber
tanamannya. Granula pati beras adalah kecil (3-8 µm), berbentuk poligonal dan
cenderung terjadi agregasi atau bergumpal-gumpal. Granula pati jagung agak
lebih besar (sekitar 15 µm), berbentuk bulat kearah poligonal. Granula tapioka
berukuran lebih besar (sekitar 20 µm), berbentuk agak bulat dan pada sala h
bagian bagian ujungnya berbentuk kerucut. Granula pati gandum cenderung
berkelompok dengan berbagai ukuran. Ukuran normalnya adalah 18 µm, granula
yang lebih besar berukuran rata-rata 24 µm, dan granula yang lebih kecil
berukuran 7 – 8 µm. Bentuk granula pati gandum adalah bulat sampai lonjong.
Pati kentang berbentuk oval dan sangat besar, berukuran rata-rata 30 – 50 µm
[image:37.595.226.446.417.546.2](Deis, 1998). Bentuk dan ukuran beberapa granula pati dapat dilihat pada
Gambar 8.
Gambar 8. Berbagai bentuk dan ukuran granula pati (Schwenk, 2001)
Distribusi ukuran granula pati berpengaruh terhadap kekuatan
pembengkakan pati. Ukuran granula pati yang kecil, maka kekuatan
pembengkakannya juga kecil. Sebaliknya dengan ukuran granula yang besar,
maka kekuatan pembengkakannya juga besar. Oleh karena itu, untuk
meningkatkan kekuatan pembengkakannya, maka ukuran granula lebih besar
(Chaplin, 2002).
Bentuk dan ukuran granula pati yang dimodifikasi, seperti pati beras
terasetilasi pada media air, yaitu NaOH, terjadi perubahan. Pati beras native Jagung Jagung waxy
Tapioka Kentang
berbentuk poligonal pada tepi-tepinya dan membentuk kelompok-kelompok
dengan ukuran 4,46 sampai 7,2 µm. Apabila dilakukan modifikasi menjadi pati
beras terasetilasi bentuk pati beras berubah menjadi kehilangan bentuk poligonal
pada tepi-tepinya dan permukaannya menjadi kasar serta cenderung untuk
membentuk gumpalan dengan ukuran granula 3,9 sampai 6,5 µm (Gonzales dan
Perez, 2002).
Gelatinisasi
Amilosa dan amilopektin pada granula pati dihubungkan dengan ikatan
hidrogen. Apabila granula pati dipanaskan di dalam air, maka energi panas ini
menyebabkan ikatan hidrogen pada granula pati pecah dan air masuk ke dalam
granula. Dengan adanya molekul air yang berdifusi ke dalam granula pati,
molekul air membentuk ikatan hidrogen dengan amilosa dan amilopektin
(McWilliams, 2001). Proses pertama yang terjadi adalah melelehnya bagian
kristal dan membentuk suatu jaringan. Semakin tinggi energi panas, jaringan
kristal yang meleleh akan menjadi rusak dan melarutkan bagian amilosa dan
amilopektin. Kelarutan amilosa pada bagian kristal mengakibatkan bagian amorf
menjadi rusak tidak stabil (Belitz dan Grosch, 1999). Akibatnya ikatan hidrogen
diantara amilosa dan amilopektin menjadi rusak.
Kondisi di atas menyebabkan molekul air yang terus menerus masuk ke
dalam granula pati membuat ikatan hidrogen dengan amilosa maupun
amilopektin pada bagian amorf maupun kristal. Granula pati menjadi
membengkak dan sejalan dengan itu meningkat pula ukuran granulanya sampai
batas tertentu sebelum granulanya pecah. Inilah yang disebut gelatinisasi. Pada
waktu granula pati pecah, bagian amilosa dan amilopektin berdifusi keluar
granula (Gambar 9) (McWilliams, 2001; Fleche, 1985).
Pembengkakan Viskositas Maksimum Difusi
Amilosa H2O
[image:38.595.115.530.613.689.2]Amilopektin
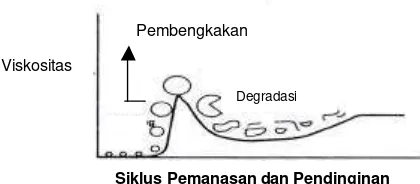
Proses gelatinisasi granula pati juga berhubungan dengan viskositas.
Schwenk (2001) menggambarkan bahwa pati pada awalnya mempunyai
viskositas 0 Brabander Unit sebelum dilakukan pemanasan. Setelah dilakukan
pemanasan, granula pati sedikit demi sedikit mengalami pembengkakan sampai
titik tertentu. Semakin besar pembengkakan granula pati, semakin besar pula
viskositas pati. Setelah pembengkakan maksimum, pati mengalami degradasi.
[image:39.595.176.386.265.357.2]Sejalan dengan proses degradasi, viskositas pati juga semakin menurun
(Gambar 10).
Gambar 10. Hubungan antara viskositas dan lama pemanasan dan pendinginan pada granula pati (Schwenk, 2001)
Sifat Fisik Srtuktur Pati
Sifat fisik bahan pangan berpengaruh terhadap sifat-sifat bahan pangan
selama pengolahan, penyimpanan dan pemakaian (Ross dan Karel, 1991).
Secara mendasar, bentuk fisik bahan pangan ada tiga, yaitu padat, cair dan gas.
Sifat fisik bahan pangan dapat berubah dari satu fase ke fase yang lain dengan
adanya perubahan tekanan atau suhu, yang disebut dengan fase transisi.
Transisi dari padatan menjadi cair atau dari cair menjadi gas adalah transisi orde
pertama (first-order transitions). Contohnya adalah gelatinisasi pati dan denaturasi protein (Aguilera dan Stanley, 1999).
Adapun transisi orde kedua (second-order transitions) adalah transisi gelas. Hal ini terjadi dengan adanya perubahan pada padatan amorf dengan
adanya perubahan suhu, sehingga terjadi perubahan dari padatan glassy
berubah menjadi cairan kental (Roos, 1995; Roos et al. 1996).
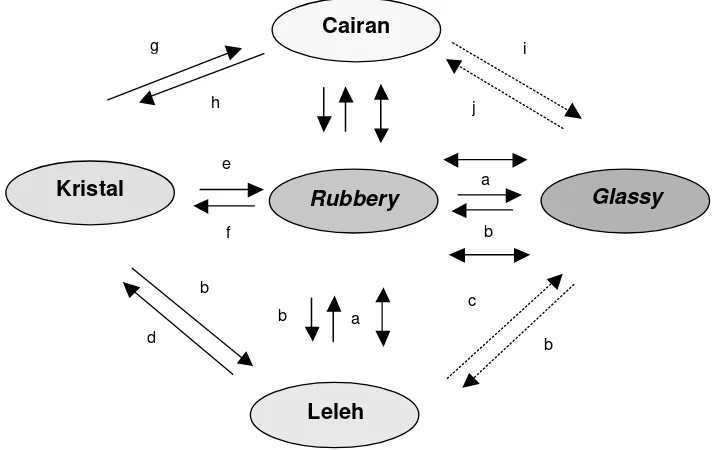
Perubahan pada padatan amorf dapat dilihat pada Gambar 11. Pada
gambar tersebut dapat dilihat bahwa terjadi perubahan sifat padatan amorf, dari
padatan glassy menjadi seperti cairan rubbery. Diantara kedua fase ini terdapat daerah transisi gelas dan merupakan fase amorf (Roos et al., 1996).
Pembengkakan
Degradasi
Viskositas
Suhu yang terletak pada daerah transisi gelas (Tg) merupakan faktor yang
paling penting untuk mengontrol sifat-sifak fisik, mekanis, (Roos et al., 1996) dan fisiko-kimia (Roos dan Karel, 1991) dari suatu polimer yang amorf. Apabila suatu
bahan yang amorf terletak di atas suhu transisi gelas (Tg), maka akan terjadi
kerusakan sifat fisiko-kimia, mobilitas molekular meningkat dan volume yang
dibebaskan juga meningkat (Roos dan Karel, 1991).
[image:40.595.137.496.212.437.2]Keterangan : a, pendinginan; b, pemanasan; c, pendinginan cepat; d, pendinginan lambat; e, tekanan; f, kristalisasi; g, solubilisasi; h, superjenuh; i, dehidrasi; j, plastilisasi
Gambar 11. Perubahan sifat fisik bahan pangan (Roos dan Karel, 1991)
Gelas yang amorf merupakan bahan yang dapat membungkus komponen
flavor pada proses enkapsulasi, mencegah oksidasi dan menurunkan kecepatan
retensi komponen flavor selama penyimpanan. Kecepatan mobilitas retensi
komponen flavor meningkat apabila proses enkapsulasi dan penyimpanan flavor
terenkapsulasi di atas Tg (Roos dan Karel, 1991). Karena pada suhu di atas Tg,
maka terjadi perubahan struktur bagian amorf.
Modifikasi Pati
Modifikasi pati dilakukan untuk melakukan perubahan sifat kimia dan atau
fisik dari pati native. Modifikasi pati dapat dilakukan dengan cara pemotongan
struktur molekul, penyusunan kembali struktur molekul, oksidasi atau dengan
cara melakukan substitusi gugus kimia pada molekul pati (Wurzburg, 1989). Ada
Leleh
a
b c
b b
d
Rubbery Glassy
Kristal a
b e
f
Cairan
g
h
i
beberapa cara untuk memodifikasi pati, diantaranya adalah hidrolisis dengan
enzim, dan substitusi kimiawi secara asilasi dan suksinilasi.
Modifikasi pati dengan metode hidrolisis dapat dilakukan dengan
menggunakan asam (Oviedo dan Camargo, 1998; Atichokudomchai dan
Varavinit, 2003) atau enzim (Kukman et al. 1998). Hidrolisis pati dengan enzim
ada beberapa langkah, yaitu likuefaksi, sakarifikasi, dan isomerisasi. Langkah
yang pertama adalah likuefaksi dengan 30 - 40% suspensi padatan untuk
menghasilkan maltodekstrin dengan menggunakan enzim α-amilase. Setelah
lekuefaksi dilakukan sakarifikasi menggunakan enzim glukoamilase atau
pullulanase untuk menghasilkan sirup glukosa atau sirup maltosa. Hasil
sakarifikasi dilakukan isomerisasi dengan enzim glukosa isomerase untuk
menghasilkan sirup fruktosa (Olsen, 1995).
Hidrolisis dengan enzim menghasilkan suatu daerah fungsional yang luas,
tergantung dengan enzim yang digunakan. Komposisi ini dapat ditentukan
dengan pengukuran ekivalen dekstrosa (DE). Nilai DE sama dengan 100 adalah
murni dekstrosa (glukosa) (Murphy, 2000), nilai DE sama dengan 50 adalah
maltosa (Wuzburg, 1989) dan nilai DE sama dengan 0 adalah pati native
(Murphy, 2000). Apabila dalam satu molekul hirolisat amilosa dan amilopektin
mengandung 100 unit anhidroglukosa dan terdapat 1 gugus gula pereduksi,
maka nilai DE-nya adalah 1 (Wuzburg, 1989). Hidrolisat dengan DE di bawah 20
adalah maltodekstrin, sedangkan DE diantara 20 dan 100 adalah sirup glukosa
(Murphy, 2000).
Produk dengan DE sedang atau lebih rendah lebih efisien digunakan
untuk enkapsulasi flavor dengan pengering semprot. Hal ini kemungkinannya
disebabkan adanya keseimbangan panjangnya polimer, yang menolong untuk
menangkap komponen flavor pada permukaan droplet yang diinginkan (Kenyon,
1995). Nilai DE yang biasa digunakan untuk enkapsulasi flavor adalah 8-9,5
(Matsutani Chemical Industry, 1999).
Enzim yang digunakan untuk menghasilkan dekstrin atau maltodekstrin
adalah berasal α-amilase yang berifat endo-amilase yang dapat menghidrolisis
ikatan α-(1--->4) secara acak, seperti α-amilase yang berasal dari bakteri.
Hidrolisis ini mengakibatkan menurunnya viskositas pati dan meningkatkan nilai
DE.
Sementara itu, modifikasi pati dengan asilasi adalah proses asilasi pati
rantai yang lebih panjang lagi, seperti asam propionat (Santayonan dan
Wootthikanokkhan, 2003), asam heptanoat dan asam palmitat (Miladinov dan
Hanna, 2000), serta asam stearat (Varavinit et al. 2001). Adapun modifikasi
suksinilasi adalah proses suksinilasi pati dengan asam suksinat atau alkenil
suksinat (Trubiano, 1989), seperti asam oktenil suksinat (Shogren et al. 2000).
Reaksi asilasi pada suhu ruang menghasilkan fraksi air (Jarowenko,
1989; Santayonan dan Wootthikanokkhan, 2003) (Gambar 12A), sedangkan
reaksi suksinilasi dengan menggunakan asam suksinat bereaksi dengan media
yang digunakan dan menghasilkan fraksi air (Trubiano, 1989) (Gambar 12B).
Derajat substitusi pati terasilasi atau pati tersuksinilasi pada media air, seperti
NaOH (Lawal, 2004; Miladinov dan Hanna, 2000; Shogren, 2000) atau media
semiair, seperti etanol 95% (Varavinit et al.