KOMBINASI BIOAKTIVATOR DAN KANGKUNG AIR (
Ipomoea
aquatica
Forsk.) DALAM SISTEM RESIRKULASI BUDIDAYA
LOBSTER AIR TAWAR (
Cherax quadricarinatus
)
NUNUH SULAEMAN
DEPARTEMEN MANAJEMEN SUMBER DAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa skripsi berjudul Kombinasi Bioaktivator dan Kangkung Air (Ipomoea aquatica Forsk.) dalam Sistem Resirkulasi Budidaya Lobster Air Tawar (Cherax quadricarinatus) adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
ABSTRAK
NUNUH SULAEMAN. Kombinasi Bioaktivator dan Kangkung Air (Ipomoea aquatica Forsk.) dalam Sistem Resirkulasi Budidaya Lobster Air Tawar (Cherax quadricarinatus). Dibimbing oleh HEFNI EFFENDI.
Akuaponik merupakan kombinasi sistem akuakultur dan tanaman air dengan menggunakan sistem resirkulasi. Penelitian ini bertujuan untuk mengurangi limbah budidaya lobster air tawar dan menentukan korelasi antara pertumbuhan kangkung air, bakteri, kualitas air, dan pertumbuhan lobster air tawar. Hasil penelitian menunjukkan adanya korelasi negatif antara bakteri dengan konsentrasi amonia (r=0,641) (p<0,05) dan berkorelasi positif dengan pertumbuhan lobster air tawar (r=0,725) (p<0,01). Kangkung air berkorelasi negatif dengan konsentrasi amonia (r=0,595) (p<0,05) dan konsentrasi ortofosfat (r=0,780) (p<0,01). Hasil kombinasi bioaktivator dan kangkung air menunjukkan penurunan konsentrasi amonia sebesar 81%, nitrat 33%, dan penurunan konsentrasi ortofosfat sebesar 89%. Nilai suhu, pH, dan oksigen terlarut dalam media budidaya cukup baik untuk mendukung pertumbuhan lobster air tawar.
Kata kunci: resirkulasi, kangkung air, korelasi, kualitas air, lobster air tawar
ABSTRACT
NUNUH SULAEMAN. Combination of Bioactivator and Water Spinach (Ipomoea aquatica Forsk.) in Recirculation Culture System of Freshwater Crayfish (Cherax quadricarinatus). Supervised by HEFNI EFFENDI.
Aquaponic system is a combination of aquaculture and hydroponic cultivation in recirculation system. The purpose of the study was to reduce wastewater of freshwater crayfish culture and to determine correlation between bacteria, water spinach, water quality, and crayfish growth. Negative correlation occurred between bacteria and amonia (r=0,641) (p<0,05) and positive correlation of bacteria and freshwater crayfish (0,725) (p<0,01). Water spinach negatively correlated with amonia (r=0,595) (p<0,05) and orthophosphate (r=0,780) (p<0,01). Combination of bacteria and water spinach resulted in amonia reduction up to 81%, nitrate 33%, and orthophosphate 89%. Temperature, pH, and dissolved oxygen in aquaculture media was suitable for freshwater crayfish growth.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan
pada
Departemen Manajemen Sumber Daya Perairan
KOMBINASI BIOAKTIVATOR DAN KANGKUNG AIR (
Ipomoea
aquatica
Forsk.) DALAM SISTEM RESIRKULASI BUDIDAYA
LOBSTER AIR TAWAR (
Cherax quadricarinatus
)
NUNUH SULAEMAN
DEPARTEMEN MANAJEMEN SUMBER DAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Juli 2013 ini ialah pengolahan limbah, dengan judul Kombinasi Bioaktivator dan Kangkung Air (Ipomoea aquatica Forsk.) dalam Sistem Resirkulasi Budidaya Lobster Air Tawar (Cherax quadricarinatus).
Penulis mengucapkan terima kasih yang sebesar-besarnya kepada semua pihak yang telah membantu dalam penulisan skripsi ini. Ungkapan terima kasih Penulis sampaikan kepada:
1. Institut Pertanian Bogor yang telah memberikan kesempatan studi kepada Penulis.
2. Penelitian yang pembiayaannya bersumber dari BOPTN melalui Pusat Penelitian Lingkungan Hidup (PPLH) IPB yang diketuai oleh Dr Ir Hefni Effendi, MPhil.
3. Beasiswa BIDIK MISI yang telah membantu keuangan Penulis untuk menyelesaikan studi.
4. Dr Ir Hefni Effendi, MPhil sebagai ketua komisi pembimbing yang telah memberi arahan dan masukan dalam penulisan karya ilmiah ini.
5. Dr Ir Niken Tunjung Murti Pratiwi, MSi selaku pembimbing akademik yang telah memberikan motivasi selama perkuliahan.
6. Dr Ir Sigid Hariyadi, MSc selaku penguji tamu dan Ali Mashar, SPi, Msi selaku komisi pendidikan Departemen Manajemen Sumber Daya Perairan atas saran dan masukan yang sangat berarti.
7. Keluarga Penulis, Ibu (Neni), bapak (alm.Abdul Rojak), kakak, dan adik beserta keluarga besar yang telah memberikan banyak motivasi, do’a, dan dukungan kepada Penulis baik moril maupun materil.
8. Teman seperjuangan penelitian: Dwi, Bani, Mas Bagus, Mas Derry, Pak Hendrik, Pak Nata, Pak Jantan, Pak Deni, Mba Keke, dan semua yang telah membantu.
9. Teman-teman seperjuangan: Lulu, Wahyu, Serli, Nina, Noor, Tiwi, Aji, Yuyun, Kak Nia, Kak Bani, dan semua teman MSP angkatan 47 atas semangat, dukungan, dan doanya.
Demikian skripsi ini disusun, semoga bermanfaat.
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 2
Manfaat Penelitian 2
METODE 3
Waktu dan Lokasi Penelitian 3
Perancangan Pelaksanaan Penelitian 3
Analisis Data 5
HASIL DAN PEMBAHASAN 8
Hasil 8
Pembahasan 14
KESIMPULAN DAN SARAN 18
Kesimpulan 18
Saran 18
DAFTAR PUSTAKA 18
LAMPIRAN 22
DAFTAR TABEL
1 Parameter analisis kualitas air 5
2 Nilai kelimpahan total bakteri 12
3 Perbandingan nilai pertumbuhan lobster: GR, SGR, dan SR 13
DAFTAR GAMBAR
1 Skema perumusan masalah penggunaan kombinasi bioaktivator dan kangkung air (I. aquatica Forsk.) dalam sistem resirkulasi
budidaya lobster air tawar 2
2 Sketsa desain akuarium sistem resirkulasi dan desain akuarium
resirkulasi penelitian 4
3 Pengukuran panjang lobster air tawar dan kangkung air 5
4 Hasil pengamatan suhu 9
5 Hasil pengamatan pH 9
6 Hasil pengamatan oksigen terlarut 10
7 Hasil pengamatan amonia 10
8 Hasil pengamatan nitrat 11
9 Hasil pengamatan ortofosfat 11
10 Persentase perubahan konsentrasi limbah pada perlakuan berbeda 12
11 Panjang rata-rata losbter air tawar 13
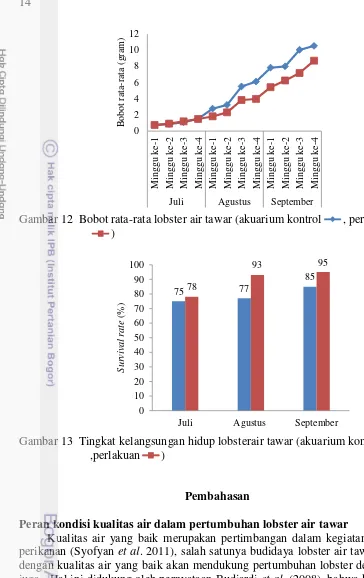
12 Bobot rata-rata lobster air tawar 14
13 Tingkat kelangsungan hidup losbter air tawar 14
DAFTAR LAMPIRAN
1 Persentase perubahan konsentrasi limbah pada akuarium kontrol 22 2 Persentase perubahan konsentrasi limbah pada akuarium
perlakuan 22
3 Data suhu, pH, dan DO pada akuarium kontrol 23 4 Data suhu, pH, dan DO pada akuarium perlakuan 23 5 Data jumlah, panjang dan bobot lobster pada akuarium kontrol 24 6 Data jumlah, panjang dan bobot lobster, kangkung air, dan bakteri
akuarium perlakuan 24
7 Contoh perhitungan % perubahan kualitas air, parameter
pertumbuhan lobster, dan kangkung air 24
8 Uji normalitas panjang-bobot rata-rata lobster air tawar pada
akuarium kontrol 25
10 Uji normalitas kualitas air dan panjang-bobot rata-rata pada
akuarium perlakuan 25
11 Uji normalitas SR pada akuarium perlakuan 26
12 Hasil uji Pearson Coefficient Correlation akuarium kontrol,
pengaruh kualitas air terhadap pertumbuhan lobster air tawar 26 13 Hasil uji Pearson Coefficient Correlation akuarium kontrol,
pengaruh kualitas air terhadap SR lobster air tawar 27 14 Hasil uji Pearson Coefficient Correlation akuarium perlakuan,
pengaruh kualitas air terhadap pertumbuhan lobster air tawar 28 15 Hasil uji Pearson Coefficient Correlation akuarium perlakuan,
pengaruh kualitas air terhadap SR lobster air tawar 29 16 Hasil uji Pearson Coefficient Correlation akuarium perlakuan,
pengaruh bakteri terhadap kualitas air limbah 29 17 Hasil uji Pearson Coefficient Correlation akuarium perlakuan,
pengaruh bakteri terhadap pertumbuhan lobster air tawar 30 18 Hasil uji Pearson Coefficient Correlation akuarium perlakuan,
pengaruh kangkung air terhadap kualitas air limbah 31
PENDAHULUAN
Latar Belakang
Lobster air tawar capit merah atau Cherax quadricarinatus merupakan komoditas budidaya air tawar yang saat ini cukup diminati masyarakat. Menurut Sukmajaya dan Suharjo (2003), kelebihan lobster dari jenis ini jika dibandingkan dengan lobster air tawar lainnya adalah tidak mudah terserang penyakit, pemakan tumbuhan sekaligus hewan (omnivora), memiliki pertumbuhan relatif cepat, dan memiliki fekunditas yang tinggi. Selain itu, menurut Budiardi et al. (2008), lobster jenis ini mudah dibudidayakan, sehingga memiliki peluang untuk dikembangkan dalam kegiatan budidaya perikanan.
Air dari suatu kegiatan budidaya perikanan akan menghasilkan limbah yang berasal dari feses dan sisa pakan yang tidak termakan (Chung et al. 2002). Limbah budidaya tersebut mengandung bahan organik yang menjadi suatu cemaran terhadap kualitas air dalam media budidaya. Jika air dalam media budidaya tidak mengalami pergantian, maka limbah akan terakumulasi dan kualitas air akan semakin menurun, sehingga berpengaruh pada kelangsungan hidup organisme yang dibudidayakan (Klinger dan Naylor 2012). Keberadaan bahan organik yang tidak didekomposisi dengan sempurna dapat menghasilkan amonia dan sulfida, serta dapat menurunkan kadar oksigen terlarut di dalam media air budidaya. Hal ini dapat menghambat pertumbuhan biota yang dipelihara (Tumembouw 2011). Kualitas air yang memenuhi syarat bagi pertumbuhan biota akuatik yang dipelihara sangat penting dan harus dipertimbangkan. Oleh karena itu, perlu didapatkan teknologi yang dapat menciptakan ketersediaan air yang memenuhi syarat untuk kelangsungan hidup biota air tersebut. Teknologi yang mungkin dilakukan, yaitu bioremediasi melalui akuaponik.
2
Perumusan Masalah
Kegiatan budidaya perikanan akan menghasilkan limbah organik yang dapat menurunkan kualitas air media budidaya dan dapat menghambat pertumbuhan biota yang dipelihara. Suatu upaya untuk mengurangi kandungan bahan organik tersebut, metode biologi menjadi salah satu pilihan yang paling baik. Pengolahan air limbah dengan metode biologi (bioremediasi) berupa proses pengolahan dengan memanfaatkan kombinasi antara aktivitas mikroorganisme berupa bakteri dan kangkung air (Ipomoea aquatica Forsk.) sebagai agen pengolah limbah. Bakteri akan merombak bahan organik menjadi bahan anorganik yang terlarut dalam air, juga memanfaatkannya untuk membangun biomassa. Selanjutnya, bahan anorganik tersebut dimanfaatkan oleh kangkung air untuk membangun biomassa.
v
Gambar 1 Skema perumusan masalah penggunaan kombinasi bioaktivator dan kangkung air (I. aquatica Forsk.) dalam sistem resirkulasi budidaya lobster air tawar
Tujuan Penelitian
Penelitian ini bertujuan untuk mengurangi dan memanfaatkan limbah sisa pakan dan feses budidaya lobster air tawar secara bioremediasi menggunakan bioaktivator (bakteri) dan kangkung air (Ipomoea aquatica Forsk.), serta menentukan korelasi atau pengaruh keduanya terhadap kualitas air dan pertumbuhan lobster air tawar.
Manfaat Penelitian
Manfaat penelitian ini adalah sebagai alternatif teknologi sederhana dalam pengolahan limbah budidaya perikanan melalui bioremediasi oleh bioaktivator berupa bakteri dan kangkung air (Ipomoea aquatica Forsk.).
3
METODE
Waktu dan Lokasi Penelitian
Penelitian dilaksanakan selama tiga bulan, yaitu bulan Juli-September 2013 yang bertempat di Laboratorium Lingkungan, Pusat Penelitian Lingkungan Hidup, Institut Pertanian Bogor (PPLH IPB). Analisis Fisika-Kimia dan Biologi dilakukan di Laboratorium Lingkungan, Pusat Penelitian Lingkungan Hidup, Institut Pertanian Bogor. Metode penelitian yang digunakan adalah percobaan laboratorium.
Perancangan Pelaksanaan Penelitian
Penelitian terdiri dari dua perlakuan, yaitu perlakuan (1) kontrol (pemeliharaan lobster air tawar tanpa bakteri dan kangkung air) dan perlakuan (2) dengan menggunakan kombinasi bakteri dan kangkung air. Alat yang digunakan pada penelitian ini adalah akuarium dengan sistem resirkulasi terdiri dari akuarium tanpa sekat berukuran 80 x 40 x 40 cm3 dengan volume total air sebanyak 96 liter dan debit air 0,0267 Liter/detik, serta drum yang dibagi menjadi dua potongan bagian, dan serangkaian perlengkapan untuk resirkulasi. Bahan yang digunakan berupa lobster air tawar jenis Red claw (Cherax quadricarinatus) berumur 2 bulan yang berasal dari kolam budidaya diploma IPB, diaklimatisasi selama 1 hari 1 malam. Sebanyak 60 ekor dimasukkan pada tiap akuarium untuk perlakuan 1 dan 2 dengan ukuran panjang sekitar 4-5 cm.
Kangkung air (I. aquatica Forsk.) yang digunakan dalam penelitian ini berasal dari kolam perkebunan di belakang kampus IPB. Sebanyak 5 rumpun kangkung air ditanam sejajar pada talang menggunakan bantuan styrofoam agar daun kangkung air tidak terendam (hanya akar yang berada di air). Bakteri cair komersial bermerk Microplus dicampur dengan air dengan perbandingan 1:10 (Aerobacter sp., Nitrobacter sp., Nitrosomonas sp., Lactobacillus sp., Saccharomyces sp.). Sebanyak 1 L bakteri cair dicampurkan dengan 10 L air. Hasil campuran tersebut kemudian ditambahkan ke dalam drum (tandon) media budidaya masing-masing sebanyak 5,5 L pada akuarium kontrol dan perlakuan. Penambahan bakteri ke dalam media budidaya dilakukan pada bulan September, yaitu pada bulan ke-3 penelitian.
4
(a)
(b)
Gambar 2 Sketsa desain akuarium sistem resirkulasi (a) dan desain akuarium resirkulasi penelitian (b)
Pengambilan contoh
Pengambilan contoh air dilakukan seminggu sekali pada akuarium dan talang, serta pengambilan lobster air tawar dan kangkung air. Contoh air diambil dengan menggunakan botol sampel dan dibawa ke laboratorium untuk dianalisis. Pengukuran sampel lobster air tawar sebanyak 30 ekor pada akuarium kontrol dan 30 ekor pada akuarium perlakuan. Panjang total lobster air tawar diukur dengan penggaris dan berat lobster air tawar ditimbang dengan timbangan digital bermerek Quattro Type. Pengukuran kangkung air sebanyak 1 tangkai batang dan daun pada masing-masing rumpunnya. Kemudian dilakukan pengukuran panjang batang dan panjang daun menggunakan penggaris.
Analisis kualitas air di laboratorium
Analisis kualitas air dilakukan dengan prosedur APHA (2012). Parameter yang diukur adalah suhu, pH, oksigen terlarut (Dissolved Oxygen), amonia, nitrat, dan ortofosfat. Parameter kualitas air yang dianalisis disajikan pada Tabel 1.
5 Purnomo et al. (2013), dan Sutiknowati (2013). Pengukuran pertumbuhan kangkung air (cm/minggu) dan lobster air tawar (cm/minggu dan gram/minggu) juga dilakukan. Cara pengukuran panjang daun dan batang kangkung air serta lobster air tawar disajikan pada Gambar 3.
Tabel 1 Parameter kualitas air yang dianalisis
Parameter Satuan Metode Alat Fisika
Suhu 0C Pemuaian Termometer
Kimia
pH - Elektroda pH meter
DO mg/L Probe Elektroda DO meter
Amonia mg/L Phenate Spektrofotometer
Nitrat mg/L Reduksi kadmium Spektrofotometer
Ortofosfat mg/L Stanous klorida Spektrofotometer
Gambar 3 Pengukuran panjang lobster air tawar dan kangkung air
Analisis Data
Persentase perubahan konsentrasi limbah
Parameter kualitas air dianalisis berdasarkan perubahan konsentrasi awal pengamatan hingga akhir pengamatan dengan melihat persentase perubahan konsentrasinya. Persentase ini menjelaskan tingkat penurunan limbah yang dapat diserap oleh kangkung air dan didekomposisi oleh bioaktivator (bakteri) (Faturochman 2012). Menurut Ulfah (2009), persentase perubahan tersebut dapat dihitung menggunakan rumus sebagai berikut.
% perubahan = x 100% Keterangan:
a : Nilai parameter tertentu kualitas air pada saat awal (sebelum diolah) untuk masing-masing akuarium
6
Pertumbuhan bobot harian lobster air tawar (growth rate)
Growth rate (GR) merupakan pertambahan nilai bobot per hari dinyatakan dalam satuan gram/hari. Nilai tersebut dihitung menggunakan rumus berikut (Karplus et al. 2001 dan Manor et al. 2002).
GR = - 0 Keterangan:
GR : Pertumbuhan bobot harian (gram/hari) Wt : Bobot rata-rata akhir pemeliharaan (gram) W0 : Bobot rata-rata awal pemeliharaan (gram) t : Waktu pemeliharaan (hari)
Laju pertumbuhan sesaat lobster air tawar (specific growth rate)
Specific growth rate (SGR) merupakan nilai pertumbuhan dalam waktu (hari). Laju pertumbuhan sesaat menggambarkan persentase berat rata-rata individu per hari (Ernawati dan Wahyuni 2008). Nilai tersebut dihitung menggunakan rumus berikut (Canto et al. 2002; Manor et al. 2002; Webster et al. 2004; Barki et al. 2006; Leon et al. 2014).
SGR = - 0 X 100% Keterangan:
SGR : Laju pertumbuhan sesaat (%/hari)
Wt : Bobot rata-rata akhir pemeliharaan (gram) W0 : Bobot rata-rata awal pemeliharaan (gram) t : Waktu pemeliharaan (hari)
Pertumbuhan panjang mutlak lobster air tawar
Panjang total lobster air tawar dimulai dari ujung rostrum hingga ujung telson. Menurut Effendie (1979), pertumbuhan panjang mutlak dapat dihitung menggunakan rumus berikut.
Pm = Lt-L0 Keterangan :
Pm : Pertumbuhan panjang mutlak (cm)
Lt : Rata-rata panjang individu pada hari ke-t (cm) L0 : Rata-rata panjang individu pada hari ke-0 (cm)
Tingkat kelangsungan hidup (survival rate) lobster air tawar
7
SR = x 100% Keterangan:
SR : Survival rate (%)
N0 : Jumlah lobster pada awal pengamatan (ekor) Nt : Jumlah lobster pada akhir pengamatan (ekor)
Rasio konversi pakan (feed conversion ratio/ FCR)
Rasio konversi pakan adalah suatu nilai efisiensi penggunaan pakan, semakin rendah nilai FCR maka semakin sedikit pakan yang dibutuhkan untuk menghasilkan satu unit berat badan atau daging ikan (Buwono 2000). Nilai FCR tersebut dapat dihitung menggunakan rumus berikut (Heinsbroek 1989 in Ernawati dan Wahyuni 2008; Leon et al. 2014). Pemberian pakan lobster air tawar selama penelitian dilakukan sebanyak 3 kali, yaitu pagi, siang, dan sore hari dengan dosis pakan sebesar 10% dari bobot rata-rata lobster air tawar.
FCR=F/(Wt-W0) FCR : Rasio konversi pakan
F : Jumlah pakan yang diberikan (gram) Wt : Bobot rata-rata akhir pemeliharaan (gram) W0 : Bobot rata-rata awal pemeliharaan (gram)
Pertumbuhan kangkung air
Pengamatan pertumbuhan kangkung air dilakukan dengan cara mengukur pertumbuhan panjang daun dan panjang batang kangkung air. Laju pertumbuhan panjang dihitung dengan menggunakan rumus berikut (Huisman 1987).
[√
]
100%Keterangan :
: Laju pertumbuhan panjang harian (%) : Panjang rata-rata pada hari ke-t (cm) : Panjang rata-rata pada hari ke-0 (cm) t : Waktu pemeliharaan (hari)
Uji korelasi Pearson Coefficient Correlation
Ada dua jenis uji korelasi, yaitu Pearson Coefficient Correlation dan Rank Spearman Correlation (Rahayu 2005; Priyatno 2013; Sujarweni 2014). Uji statistik korelasi ini dilakukan dengan menggunakan aplikasi SPSS 20.00 untuk menentukan korelasi objek (parameter) pengamatan dalam penelitian. Ketentuan untuk memilih uji Pearson Coefficient Correlation dan Rank Spearman adalah sebagai berikut.
8
2. Rank Spearman Correlation, jika hasil uji normalitas menunjukkan nilai signifikan <0,05 (data tidak berdistribusi normal).
Hasil uji normalitas data penelitian diperoleh nilai signifikan >0,05, sehingga dilakukan uji korelasi Pearson Coefficient Correlation (Lampiran 8-11). Uji korelasi ini dimaksudkan untuk menentukan korelasi atau hubungan antara dua variabel, yaitu variabel terikat (dependen) dan bebas (independen). Sifat nilai koefisien korelasi terdiri dari dua sifat, yaitu positif (+) dan negatif (-). Korelasi positif berarti bahwa jika variabel independen dinaikkan, maka variabel dependen akan mengalami kenaikan, begitu sebaliknya. Korelasi negatif berarti bahwa jika variabel independen dinaikkan, maka variabel dependen akan mengalami penurunan, begitu sebaliknya (Priyatno 2013 dan Sujarweni 2014).
Menurut Sujarweni (2014), tingkat signifikan digunakan untuk menyatakan apakah dua variabel memiliki hubungan atau tidak, dengan syarat sebagai berikut. 1. Jika nilai signifikan >0,05 maka H0 diterima yang artinya tidak
terdapat hubungan.
2. Jika nilai signifikan <0,05 maka H0 ditolak yang artinya terdapat hubungan.
HASIL DAN PEMBAHASAN
Hasil
Parameter hasil pengamatan penelitian meliputi nilai kualitas air dan pertumbuhan lobster air tawar. Parameter nilai kualitas air yaitu, suhu, pH, oksigen terlarut, amonia, amonium, nitrat, ortofosfat, persentase perubahan, dan kelimpahan total bakteri. Parameter pertumbuhan lobster air tawar yaitu, panjang rata-rata, bobot rata-rata, dan tingkat kelangsungan hidup lobster air tawar.
Suhu
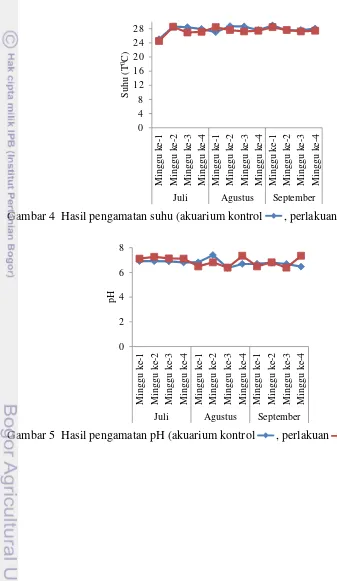
Suhu suatu perairan dapat dipengaruhi oleh waktu dalam hari, sirkulasi udara, dan aliran serta kedalaman badan air (Effendi 2003). Hasil pengamatan nilai suhu pada akuarium kontrol dan akuarium perlakuan selama penelitian mengalami fluktuasi. Kisaran suhu pada akuarium kontrol antara 25-28 0C, sedangkan pada akuarium perlakuan berkisar antara 24-27 0C. Hasil pengamatan suhu selama penelitian disajikan pada Gambar 4.
Nilai pH
9 Dissolved oxygen (oksigen terlarut)
Fluktuasi konsentrasi oksigen terlarut terjadi pada akuarium kontrol dan pada akuarium perlakuan. Kisaran oksigen terlarut akuarium perlakuan adalah 5,78-7,67 mg/L, sedangkan pada akuarium kontrol berkisar antara 5,18-7,77 mg/L. Hasil pengamatan konsentrasi oksigen terlarut selama penelitian disajikan pada Gambar 6.
Gambar 4 Hasil pengamatan suhu (akuarium kontrol , perlakuan )
10
Gambar 6 Hasil pengamatan oksigen terlarut (akuarium kontrol , perlakuan )
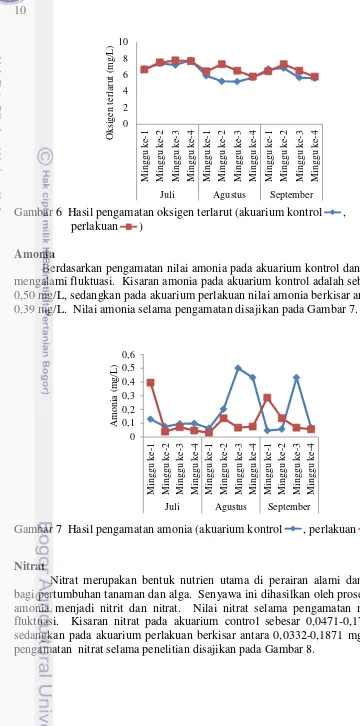
Amonia
Berdasarkan pengamatan nilai amonia pada akuarium kontrol dan perlakuan mengalami fluktuasi. Kisaran amonia pada akuarium kontrol adalah sebesar 0,05-0,50 mg/L, sedangkan pada akuarium perlakuan nilai amonia berkisar antara 0,03-0,39 mg/L. Nilai amonia selama pengamatan disajikan pada Gambar 7.
Gambar 7 Hasil pengamatan amonia (akuarium kontrol , perlakuan )
Nitrat
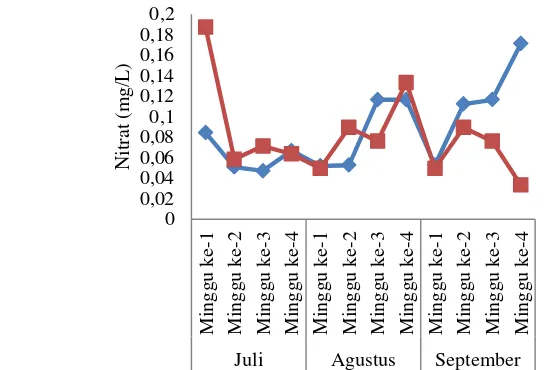
Nitrat merupakan bentuk nutrien utama di perairan alami dan berperan bagi pertumbuhan tanaman dan alga. Senyawa ini dihasilkan oleh proses oksidasi amonia menjadi nitrit dan nitrat. Nilai nitrat selama pengamatan mengalami fluktuasi. Kisaran nitrat pada akuarium control sebesar 0,0471-0,1713 mg/L, sedangkan pada akuarium perlakuan berkisar antara 0,0332-0,1871 mg/L. Hasil pengamatan nitrat selama penelitian disajikan pada Gambar 8.
11
Gambar 8 Hasil pengamatan nitrat (akuarium kontrol , perlakuan )
Ortofosfat
Hasil pengamatan nilai ortofosfat menunjukkan fluktuasi selama penelitian, baik pada akuarium kontrol maupun pada akuarium perlakuan. Kisaran ortofosfat pada akuarium kontrol sebesar 0,0421-1,4019 mg/L, sedangkan pada akuarium perlakuan berkisar antara 0,0571-0,9540 mg/L. Hasil pengamatan ortofosfat selama penelitian disajikan pada Gambar 9.
Gambar 9 Hasil pengamatan ortofosfat (akuarium kontrol , perlakuan )
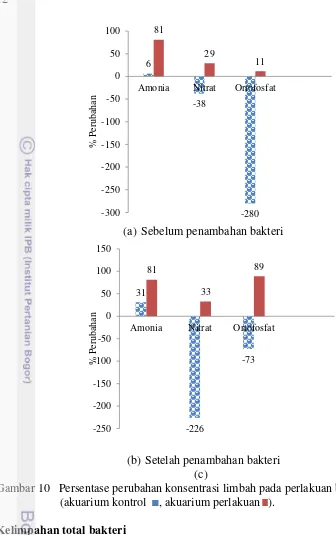
Persentase perubahan konsentrasi limbah
12
(a) Sebelum penambahan bakteri
(b) Setelah penambahan bakteri (c)
Gambar 10 Persentase perubahan konsentrasi limbah pada perlakuan berbeda (akuarium kontrol , akuarium perlakuan ).
Kelimpahan total bakteri
Berdasarkan pengamatan nilai kelimpahan total bakteri mengalami penurunan. Kelimpahan total bakteri disajikan pada Tabel 2.
Tabel 2 Nilai kelimpahan total bakteri
Bulan Minggu Total bakteri (Cfu/mL)
13
Panjang dan bobot rata-rata lobster air tawar
Parameter pertumbuhan lobster air tawar dapat dilihat melalui pertambahan panjang dan bobotnya. Nilai pertumbuhan lobster air tawar disajikan pada Tabel 3. Kisaran panjang lobster air tawar pada akuarium kontrol sebesar 3,10-7,84 cm, sedangkan pada akuarium perlakuan berkisar 3,10-7,37 cm. Kisaran bobot lobster air tawar pada akuarium kontrol sebesar 0,76-10,52 gram, sedangkan pada akuarium perlakuan berkisar 0,75-8,70 gram. Pertambahan panjang dan bobot rata-rata lobster selama pengamatan disajikan pada Gambar 11 dan 12.
Tingkat kelangsungan hidup lobster air tawar (survival rate)
Tingkat kelangsungan hidup merupakan nilai perbandingan antara jumlah ikan yang hidup pada akhir pemeliharaan dengan jumlah ikan pada awal pemeliharaan (Goddard 1996). Kisaran SR pada akuarium kontrol sebesar 75-78%, sedangkan pada akuarium perlakuan berkisar 78-95%. Nilai tingkat kelangsungan hidup lobster air tawar selama penelitian disajikan pada Gambar 13. Tabel 3 Perbandingan nilai pertumbuhan lobster: GR (g/hari), SGR (%/hari), dan
SR (%)
14
Gambar 12 Bobot rata-rata lobster air tawar (akuarium kontrol , perlakuan )
Gambar 13 Tingkat kelangsungan hidup lobsterair tawar (akuarium kontrol ,perlakuan )
Pembahasan
Peran kondisi kualitas air dalam pertumbuhan lobster air tawar
Kualitas air yang baik merupakan pertimbangan dalam kegiatan budidaya perikanan (Syofyan et al. 2011), salah satunya budidaya lobster air tawar, karena dengan kualitas air yang baik akan mendukung pertumbuhan lobster dengan baik juga. Hal ini didukung oleh pernyataan Budiardi et al. (2008), bahwa kualitas air merupakan salah faktor dalam menentukan keberhasilan dalam suatu kegiatan budidaya. Salah satu langkah untuk memperbaiki kualitas air adalah dengan bioremediasi, yaitu pengolahan air limbah dengan menggunakan tumbuhan air atau dengan memanfaatkan aktivitas mikroorganisme (Akpor dan Muchie 2010; Dhall et al. 2011; Lopes et al. 2011; Vharsa et al. 2011).
Berdasarkan hasil pengamatan, nilai kisaran suhu disajikan pada Gambar 4. Rata-rata suhu pada akuarium kontrol dan akuarium perlakuan masing-masing
15 sebesar 27,8 0C dan 27,4 0C. Secara umum kondisi suhu pada semua perlakuan sangat mendukung untuk pertumbuhan lobster air tawar. Hal ini sesuai dengan pernyataan Rouse (1977) dan Rouse et al. (1988), bahwa lobster air tawar mengalami pertumbuhan terbaiknya pada kisaran suhu 24-29 0C. Guerrero et al. (2013) mengatakan bahwa lobster air tawar tumbuh baik pada kisaran suhu 23 0 C-28 0C. Selanjutnya, hal ini diperkuat oleh Boyd (1990) yang mengatakan bahwa kisaran suhu yang baik bagi ikan di daerah tropis adalah 25-32 0C.
Berdasarkan pengamatan penelitian, nilai pH pada akuarium kontrol dan perlakuan berada pada kondisi yang mendukung bagi pertumbuhan lobster air tawar (Gambar 5). Sesuai dengan pernyataan Sukmajaya dan Suharjo (2003), bahwa pH untuk pertumbuhan lobster air tawar adalah berkisar antara 6,5-9,0. Nilai pH kurang dari 5,0 sangat buruk bagi kehidupan udang, karena dapat menyebabkan kematian dan pH di atas 9,0 dapat menurunkan nafsu makan (Iskandar 2003).
Hasil pengamatan nilai oksigen terlarut pada akuarium kontrol dan perlakuan dalam kondisi yang baik bagi kehidupan lobster air tawar (Gambar 6). Nilai rata-rata oksigen terlarut pada akuarium kontrol dan akuarium perlakuan masing-masing sebesar 6,32 mg/L dan 6,80 mg/L. Hasil ini menunjukkan bahwa secara keseluruhan dari semua perlakuan pemeliharaan lobster air tawar memiliki konsentrasi oksigen terlarut yang layak dan mendukung untuk kehidupan lobster air tawar. Konsentrasi oksigen terlarut yang baik untuk mendukung pertumbuhan lobster air tawar adalah lebih dari 5 mg/L (Budiardi et al. 2008 dan Rakocy 1997). Oksigen terlarut sangat dibutuhkan oleh semua organisme untuk respirasi, proses metabolisme atau pertukaran zat yang kemudian menghasilkan energi untuk pertumbuhan dan pembiakan (Salmin 2005), sehingga keberadaa oksigen terlarut dalam suatu perairan sangat mutlak dibutuhkan bagi kehidupan suatu organisme.
Hasil uji Pearson Coefficient Correlation menunjukkan adanya hubungan positif antara oksigen terlarut dengan pertumbuhan lobster air tawar, baik pada akuarium kontrol maupun perlakuan (p<0,01) (Lampiran 12 dan Lampiran 14). Nilai koefisien korelasi antara oksigen terlarut dengan panjang lobster pada akuarium kontrol sebesar 0,679 (hubungan kuat), sedangkan nilai koefisien korelasi pada akuarium perlakuan adalah sebesar 0,673 (memiliki hubungan kuat) (Lampiran 19). Hal ini menjelaskan bahwa dengan meningkatnya konsentrasi oksigen terlarut akan meningkatkan pertambahan panjang lobster air tawar.
Berdasarkan hasil pengamatan, rata-rata nilai amonia pada akuarium kontrol sebesar 0,1828 mg/L dan pada akuarium perlakuan sebesar 0,0962 mg/L. Secara umum, dari semua perlakuan pemeliharaan menjelaskan bahwa kandungan amonia masih layak untuk kehidupan lobster air tawar (Gambar 7). Hal ini sesuai dengan pernyataan Setiawan (2006) in Tumembouw (2011), bahwa kadar maksimum amonia dalam media budidaya lobster tidak boleh lebih dari 1,2 mg/L. Sumber amonia di perairan adalah pemecahan nitrogen organik (protein dan urea) dan nitrogen anorganik yang terdapat dalam tanah dan air, yang berasal dari dekomposisi bahan organik (tumbuhan air dan biota akuatik yang telah mati) oleh mikroba dan jamur atau lebih dikenal dengan sebutan amonifikasi (Effendi 2003; Cao et al. 2007; Tyson et al. 2008).
16
Nilai koefisien korelasi antara amonia dengan panjang lobster air tawar pada akuarium kontrol sebesar 0,603 (hubungan kuat) dan pada akuarium perlakuan sebesar 0,613 (hubungan kuat) (Lampiran 19). Hal ini menjelaskan bahwa dengan meningkatnya kadar amonia dalam media budidaya akan menghambat pertumbuhan lobster air tawar. Budiardi et al. (2008) menyebutkan bahwa dalam kegiatan budidaya secara intensif, amonia seringkali menjadi faktor pembatas, karena merupakan zat beracun dan nilainya bergantung pada kepadatan ikan serta proses pengelolaan air media budidaya. Organisme akuatik tidak dapat menoleransi kadar amonia yang terlalu tinggi, karena dapat mengganggu proses pengikatan oksigen oleh darah dan pada akhirnya dapat menyebabkan sufokasi.
Berdasarkan hasil pengamatan pertumbuhan lobster, nilai rata-rata panjang dan bobot mengalami peningkatan (Gambar 11 dan 12). Pertumbuhan lobster air tawar pada akuarium kontrol lebih besar jika dibandingkan pada akuarium perlakuan. Hal ini diduga karena lebih sedikitnya jumlah lobster air tawar pada akuarium kontrol jika dibandingkan pada akuarium perlakuan (nilai SR lebih kecil) (Gambar 13), sehingga ketersediaan pakan pada akuarium kontrol lebih besar. Tabel 2 menjelaskan perbandingan nilai pertumbuhan lobster air tawar pada beberapa penelitian yang telah dilakukan. Nilai GR pada akuarium kontrol sebesar 0,11 g/hari dan pada akuarium perlakuan sebesar 0,09 g/hari. Nilai SGR pada akuarium kontrol dan pada akuarium perlakuan berturut-turut sebesar 2,36%/hari dan 0,03%/hari. Nilai pertumbuhan panjang mutlak pada akuarium kontrol dan perlakuan sebesar 4,74 cm dan 4,27 cm.
Nilai FCR pada akuarium kontrol dan akuarium perlakuan masing-masing sebesar 4,18 dan 3,86. Hal ini menjelaskan bahwa untuk memproduksi satu unit (kg) larva atau daging lobster dibutuhkan 4,18 kg pakan untuk akuarium kontrol dan 3,86 kg pakan untuk akuarium perlakuan. Efisiensi penggunaan pakan pada akuarium perlakuan lebih tinggi jika dibandingkan pada akuarium kontrol, karena FCR pada akuarium perlakuan lebih kecil.
Pengamatan tingkat kelangsungan hidup lobster air tawar pada akuarium kontrol berkisar 75-78%, sedangkan pada akuarium perlakuan berkisar 78-95% (Gambar 13). Uji Pearson Coefficient Correlation menunjukkan bahwa tidak ada korelasi yang signifikan antara tingkat kelangsungan hidup lobster air tawar dengan kondisi kualitas air, kecuali oksigen terlarut pada akuarium kontrol (Lampiran 13). Hal ini menjelaskan bahwa kondisi kualitas air tidak terlalu berpengaruh terhadap tingkat kelangsungan hidup lobster air tawar yang dipelihara. Pernyataan ini didukung oleh Budiardi et al. (2008) yang mengatakan bahwa kondisi kualitas air dalam media budidaya tidak menjadi faktor pembatas terhadap kelangsungan hidup lobster air tawar. Kematian yang terjadi pada saat pemeliharaan disebabkan oleh sifat kanibalisme lobster itu sendiri.
Peran bakteri dan kangkung ai (Ipomoea aquatica Forsk.) terhadap perbaikan kualitas air limbah budidaya
17 Berdasarkan hasil percobaan dengan menggunakan kombinasi bakteri dan kangkung air (Ipomoea aquatica Forsk.) memberikan pengaruh terhadap perbaikan kualitas air. Pada akuarium perlakuan, sebelum dan setelah penambahan bakteri konsentrasi amonia dapat diturunkan sebesar 81%, sedangkan konsentrasi amonia pada akuarium kontrol berturut-turut sebesar 6% dan 31% (Gambar 10a dan 10b). Hasil uji Pearson Coefficient Correlation menunjukkan adanya korelasi negatif antara kelimpahan bakteri dengan amonia (Lampiran 16). Nilai koefisien korelasi tersebut sebesar 0,641 (hubungan kuat) (Lampiran 19). Hal ini menjelaskan bahwa sebesar 41,08% penurunan konsentrasi amonia dipengaruhi oleh keberadaan bakteri (p<0,05) (Lampiran 16).
Nilai koefisien korelasi antara kelimpahan bakteri dengan panjang dan bobot rata-rata lobster air tawar adalah sama, yaitu sebesar 0,725 (hubungan sangat kuat). Hal ini menjelaskan bahwa sebesar 52,56% pertambahan panjang dan bobot rata-rata lobster air tawar dipengaruhi oleh keberadaan bakteri (p<0,01) (Lampiran 17). Secara tidak langsung, hal ini memberikan penjelasan bahwa adanya bakteri dapat menjadikan kualitas air lebih baik, sehingga memberikan pengaruh yang baik juga terhadap kehidupan dan pertumbuhan lobster air tawar.
Hasil pengamatan menunjukkan adanya korelasi negatif antara kangkung air (I. aquatica Forsk.) dengan konsentrasi amonia (Lampiran 18). Nilai koefisien korelasi tersebut sebesar 0,595 (hubungan kuat). Hal ini menjelaskan bahwa sebesar 35,40% penurunan konsentrasi amonia dipengaruhi oleh kangkung air (p<0,05) (Lampiran 18). Hal ini berarti kangkung air memiliki kemampuan untuk menyerap amonia dengan baik, diduga bahwa amonia diserap oleh kangkung air setelah diubah menjadi amonium (amonifikasi). Proses ini berlangsung oleh bakteri yang berperan dalam proses amonifikasi tersebut. Pernyataan ini diperkuat oleh Syafaat (2000) in Ika dan Rifa’i (2012) yang menyebu kan bahwa salah satu tanaman yang dapat menurunkan konsentrasi amonia hingga 80% adalah kangkung air. Selanjutnya, Ulfah (2009) juga mengatakan bahwa akar kangkung air merupakan tempat hidup mikroorganisme yang membantu proses purifikasi air serta mampu menyerap unsur hara hasil dekomposisi bahan organik oleh bakteri yang diubah menjadi bobot kangkung air melalui proses fotosintesis. Pemanfaatan unsur hara ini dapat diinterpretasikan melalui adanya peningkatan panjang batang dan daun kangkung air.
18
KESIMPULAN DAN SARAN
Kesimpulan
Penggunaan kombinasi bioaktivator dan kangkung air berhasil menurunkan konsentrasi amonia sebesar 81%, konsentrasi nitrat sebesar 33%, dan konsentrasi ortofosfat sebesar 89%. Terdapat korelasi negatif antara jumlah bakteri dengan konsentrasi amonia dan korelasi positif antara bakteri dengan pertambahan panjang dan bobot lobster air tawar. Pertumbuhan kangkung air berkorelasi negatif dengan konsentrasi amonia dan ortofosfat media air budidaya.
Saran
Aplikasi bioremediasi melalui akuaponik dapat diterapkan pada media budidaya dengan kualitas air yang tidak memenuhi syarat baku mutu budidaya perikanan, sehingga akan dapat dilihat persentase perubahan konsentrasi limbah yang lebih tepat, karena pada penelitian ini kualitas air berada pada kondisi yang baik.
DAFTAR PUSTAKA
Afrianto E, Liviawaty E. 1988. Metode Budidaya Ikan. Yogyakarta (ID): Kanisius. Akbar RA. 2003. Efisiensi nitrifikasi dalam sistem biofilter submerged bed,
trickling filter, dan fluidized bed [skripsi]. Bandung (ID): Institut Teknologi Bandung.
Akpor OB, Muchie M. 2010. Bioremediation of polluted wastewater influent: phosphorus and nitrogent removal. Scientific Research and Essays. 5(21): 3222-3230.
[APHA, AWWA, WEF] American Public Health Association, American Water Works Association, Water Environment Federation. 2012. Standard Methods for the Examination of Water and Wastewater. Washington(US): The Association Official Analytical Chemist, Inc.
Arthana IW. 2006. Studi kualitas air di Danau Beratan, Buyan, dan Tamblingan di Bedugul, Bali. Journal of Ecotrophic.I(2): 34-38.
Barki A, Karplus I, Manor R, Parnes S, Aflalo ED, Sagi A. 2006. Growth of Redclaw Crayfish (Cherax quadricarinatus) in three dimensional compartments system: Does a neighbor matter? Aquaculture. 252: 348-355. Boyd CE. 1990. Water Quality Management In Pond Fish Culture. International
center for aquaculture agricultural experiment station. Alabama (US): Auburn Univ.
19 resirkulasi dengan kepadatan yang berbeda. Jurnal Akuakultur Indonesia. 7(2): 109-114.
Buwono. 2000. Kebutuhan Asam Amino Esensial dalam Ransum Ikan. Yogyakarta (ID): Kanisius.
Canto AR. Arredondo Figueroa JL, Ponce Palafox JT, Rouse DB. 2002. Growth characteristics of the Australian Redclaw Crayfish, Cherax quadricarinatus, cultured in an indoor recirculating system. Journal of Applied Aquaculture. 12(3): 59-64.
Cao L, Wang W, Yang, Y, Yang, C, Yuan Z, Xiong S, Diana J. 2007. Environmental impact of aquaculture and counter measures to aquaculture pollution in China. Environmental Science Pollution Resources. 14(7): 452– 462.
Chung IK., Kang YH, Yarish C, Kraemer GP, Lee JA. 2002. Application of seaweed cultivation to the bioremediation of nutrient rich effluent. Algae. 17(3): 1-10.
Dhall P, Kumar R, Kumar A. 2011. Biodegradation of sewage wastewater using autochthonous bacteria. The Scientific World Journal. 2012: 1-8.
Effendi H. 2003. Telaah Kualitas Air: bagi Pengelolaan Sumber Daya dan Lingkungan Perairan. Yogyakarta (ID): Kanisius.
Effendie MI. 1979. Metode Biologi Perikanan. Bogor (ID): Yayasan Dewi Sri. Ernawati, Wahyuni R. 2008. Pengaruh pemberian pakan daphnia terhadap
kelulushidupan dan pertumbuhan larva lobster air tawar (Cherax quadricarinatus). Jurnal Akuakultur Indonesia. 7(2). 7-13.
Faturochman I. 2012. Aplikasi tumbuhan air Mayaca fluviatilis dengan sistem kanal dalam bioremediasi limbah organik dari Waduk Cirata [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Goddard S. 1996. Feed Management in Intensive Aquaculture. New York (US): Chapman and Hall.
Guerrero MG, Sandoval PH, Rojas JO, Jacinto EC. 2013. Effect of temperature on weight increase, survival, and thermal preference of jouvenile Redclaw Crayfish Cherax quadricarinatus. Hidrobiological. 23(1): 73-81.
Huisman EA.. 1987. The Principles of Fish Culture Production. Department of Aquaculture. Netherland (NL): Wageningen University.
Ika RP, Rifa’i M. 2012. Pemanfaa an pho ovol aik pada sis em o omasi akuaponik berbasis mikrokontroler atmega 8535. Jurnal Teknik Elektronika. 10(02): 22-32.
Irianto A. 2008. Statistik Konsep Dasar dan Aplikasinya. Jakarta (ID): Kencana. Iskandar. 2003. Budidaya Lobster Air Tawar. Jakarta (ID): Penebar Swadaya. Karplus I, Zoran M, Milstein A, Harpaz S, Eran Y, Joseph D, Sagi A. 1998.
Culture of the Australian Redclaw Crayfish (Cherax quadricarinatus) in Israel III. survival in earthen ponds under ambient winter temperatures. Aquaculture. 166: 259-267.
Karplus I, Harpaz S, Hulata G, Segev R, Barki A. 2001. Culture of the Australia Redclaw Crayfish (Cherax quadricarinatus) in Israel IV. Crayfish incorporation into intensive tilapia production units. The Israeli Jounal of Aquaculture-Bamidgeh. 53(1): 23-33.
20
Leon DC, Dimitrov IR, Hernandez RC, Quevedo AM, Victoria LO, Paramo JS, Villarreal H. 2014. Growth, metabolic, and physiological response of jouvenile Cherax quadricarinatus feed different available nutrition substrates. Journal Aquaculture Research and Development. 5(2): 1-7. Lopes RB, Olinda RA, Souza BAI, Cyrino JEP, Dias CTS, Queiroz JF, Tavares
LHS. 2011. Efficiency of bioaugmentation in the removal of organic matter in aquaculture systems. Brazilian Journal of Biology. 71(2): 409-419. Liu L, Hu Z, Dai X, Avnimelech Y. 2014. Effect of addition of maize starch on
the yield, water quality and formation of bioflocs in an integrated shrimp culture system. Aquaculture. 418-419: 79-86.
Manor R, Segev R, Leibovitz MP, Aflalo ED, Sagi A. 2002. Intensification of Redclaw Crayfish Cherax quadricarinatus culture II. growout in a separate cell system. Aquaculture Engineering. 26: 263-276.
Priyatno D. 2013. Analisis, Korelasi, Regresi, dan Multivariate dengan SPSS. Yogyakarta (ID). Gava Media.
Purnomo PD. 2012. Pengaruh penambahan karbohidrat pada media pemeliharaan terhadap produksi budidaya intensif nila (Oreochromis niloticus). Journal of Aquatic Management and Technology. 1(1): 161-179.
Purnomo WP, Nitisuparjo M, Purwandari Y. 2013. Hubungan antara total bakteri dengan bahan organik, NO3, dan H2S pada lokasi sekitar eceng gondok dan perairan terbuka di Rawa Pening. Journal of Management of Aquatic
Rakocy JE, Masser MP, Losordo TM. 2006. Recirculating aquaculture tank production systems: Aquaponics—integrating fish and plant culture.SRAC (Southern Regional Aquaculture Centre) Publication. 454: 1-16.
Roosta HR. 2014. Effect of foliar spray of K on mint, radish, parsley and coriander plants in quaponic system. Journal of Plants Nutrition. 37: 2236-2254.
Rouse DB. 1977. Production of Australian Redclaw Crayfish. USA (US): Auburn University.
Rouse DB, Kahn BM. 1998. Production of Australian Redclaw Cherax quadricarinatus in polyculture with nile tilapia Oreochromis niloticus. Journal of the World Aquaculture Society. 29(3): 340-344.
Sagi A, Milstein A, Eran Y, Joseph D, Khalaila I, Abdu U, Harpaz S, Karplus I. 1997. Culture of the Australian Redclaw Crayfish (Cherax quadricarinatus ) in Israel, second growout season of overwintered populations. The Israeli Journal of Aquaculture-Bamidgeh. 49(4): 222-229. Salmin. 2005. Oksigen terlarut (DO) dan kebutuhan oksigen biologi (BOD)
sebagai salah satu indikator untuk menentukan kualitas perairan. Jurnal Oseana. 30(3): 21-26.
Sujarweni VW. 2014. SPSS untuk Penelitian. Yogyakarta (ID). Pustaka Baru Press.
21 Sutiknowati LI. 2013. Mikroba parameter kualitas perairan Pulau Pari untuk upaya pembesaran biota budidaya. Jurnal Ilmu dan Teknologi Kelautan Tropis. 5(1): 204-218.
Syofyan I, Usman, Nasution P. 2011. Studi kualitas air untuk kesehatan ikan dalam budidaya perikanan pada aliran Sungai Kampar Kiri. Jurnal Perikanan dan Kelautan. 16(1): 64-70.
Tyson RV, Simonne EH, Treadwell DD. 2008. Reconciling pH for ammonia biofiltration and cucumber yield in a recirculating aquaponic system with perlite biofilters. Hort Science. 43(3): 719-724.
Tumembouw SS. 2011. Kualitas air pada kolom lobster air tawar (Cherax quadricarinatus) di BBAT Talelu. Jurnal Perikanan dan Kelautan Tropis. 7(3): 128-131.
Varsha YM, Deepthi NCH, Chenna S. 2011. An emphasis on xenobiotic degradation in environmental clean up. Journal Bioremediation and Biodegradation. ISSN: 2155-6199.
Ulfah WN. 2009. Pengolahan air limbah kantin secara biologi: suatu kajian terhadap efektivitas penggunaan Bacillus sp. dan kangkung air (Ipomea aquatica) [skripsi]. Bogor (ID): Institut Pertanian Bogor.
22
LAMPIRAN
Lampiran 1 Persentase perubahan konsentrasi limbah pada akuarium kontrol Bulan Minggu Ammonia (mg/L) Nitrat (mg/L) Ortofosfat (mg/L) Sulfida (mg/L)
Juli
tanda (-) %perubahan: menunjukkan peningkatan nilai limbah
Lampiran 2 Persentase perubahan konsentrasi limbah pada akuarium perlakuan
Bulan Minggu Ammonia
23 Lampiran 3 Data suhu, pH, dan oksigen terlarut pada akuarium kontrol
Bulan Minggu Suhu
Lampiran 4 Data suhu, pH, dan oksigen terlarut pada akuarium perlakuan
24
Lampiran 5 Data jumlah, panjang dan bobot lobster pada akuarium kontrol
Bulan Minggu Jumlah
25
Laju pertumbuhan rata-rata panjang harian daun kangkung air ( ) = [√
̅ ] x 100%
*. This is a lower bound of the true significance.
Lampiran 9 Uji normalitas SR lobster air tawar pada akuarium kontrol Tests of Normality
Kolmogorov-Smirnova Shapiro-Wilk
Statistic df Sig. Statistic df Sig.
*. This is a lower bound of the true significance.
a
26
Lampiran 11 Uji normalitas SR pada akuarium perlakuan Tests of Normality
Kolmogorov-Smirnova Shapiro-Wilk
Statistic df Sig. Statistic df Sig.
SR 0,257 12 0,057 0,842 12 0,059
a
. Lilliefors Significance Correction
Lampiran 12 Hasil uji Pearson Coefficient Correlation akuarium kontrol, pengaruh kualitas air terhadap pertumbuhan lobster air tawar
Correlation
Correlation 0,069 -0,329
27 Lampiran 13 Hasil uji Pearson Coefficient Correlation akuarium kontrol,
pengaruh kualitas air terhadap SR lobster air tawar Correlation
Suhu pH DO Amonia SR
Suhu
Pearson
Correlation 1 -0,040 -0,068 0,069 -0,323
Sig. (2-tailed) 0,902 0,833 0,831 0,306
N 12 12 12 12 12
pH
Pearson
Correlation -0,040 1 0,174 -0,329 0,410
Sig. (2-tailed) 0,902 0,590 0,296 0,186
N 12 12 12 12 12
DO
Pearson
Correlation -0,068 0,174 1 -0,619 0,650*
Sig. (2-tailed) 0,833 0,59 0,032 0,022
N 12 12 12 12 12
Amonia
Pearson
Correlation 0,069 -0,329 -0,619 1 -0,336
Sig. (2-tailed) 0,831 0,296 0,032 0,285
N 12 12 12 12 12
SR
Pearson
Correlation -0,323 0,410 0,650* -0,336 1
Sig. (2-tailed) 0,306 0,186 0,022 0,285
N 12 12 12 12 12
28
Lampiran 14 Hasil uji Pearson Coefficient Correlation akuarium perlakuan, pengaruh kualitas air terhadap pertumbuhan lobster air tawar
Correlation
Suhu pH DO Amonia L-bar W-bar
Suhu
Pearson
Correlation 1 -0,249 0,003 -0,573 0,298 0,217
Sig. (2-tailed) 0,436 0,993 0,052 0,346 0,498
N 12 12 12 12 12 12
pH
Pearson
Correlation -0,249 1 0,091 -0,057 -0,307 -0,201
Sig. (2-tailed) 0,436 0,778 0,861 0,332 0,530
N 12 12 12 12 12 12
DO
Pearson
Correlation 0,003 0,091 1 -0,094 0,673** 0,671**
Sig. (2-tailed) 0,993 0,778 0,772 0,005 0,002
N 12 12 12 12 12 12
Amonia
Pearson
Correlation -0,573 -0,057 -0,094 1 -0,613 -0,107
Sig. (2-tailed) 0,052 0,861 0,772 0,027 0,74
N 12 12 12 12 12 12
L-bar
Pearson
Correlation 0,298 -0,307 0,673** -0,613* 1 0,977**
Sig. (2-tailed) 0,346 0,332 0,005 0,027 0
N 12 12 12 12 12 12
W-bar
Pearson
Correlation 0,217 -0,201 0,671** -0,107 0,977** 1
Sig. (2-tailed) 0,498 0,530 0,002 0,74 0
N 12 12 12 12 12 12
29 Lampiran 15 Hasil uji Pearson Coefficient Correlation akuarium perlakuan,
pengaruh kualitas air terhadap SR lobster air tawar Correlation
Lampiran 16 Hasil uji Pearson Coefficient Correlation akuarium perlakuan, pengaruh bakteri terhadap kualitas air limbah
30
Lampiran 17 Hasil uji Pearson Coefficient Correlation akuarium perlakuan, pengaruh bakteri terhadap pertumbuhan lobster air tawar
Correlation
Amonia Nitrat L-bar W-bar Bakteri
Amonia
Pearson
Correlation 1 0,619 0,298 0,217 -0,641*
Sig. (2-tailed) 0,032 0,346 0,498 0,021
N 12 12 12 12 12
Nitrat
Pearson
Correlation 0,619 1 -0,307 -0,201 0,026
Sig. (2-tailed) 0,032 0,332 0,530 0,937
N 12 12 12 12 12
L-bar
Pearson
Correlation 0,298 -0,307 1 1,000 0,725**
Sig. (2-tailed) 0,346 0,332 0 0,008
N 12 12 12 12 12
W-bar
Pearson
Correlation 0,217 -0,201 1,000** 1 0,725**
Sig. (2-tailed) 0,498 0,530 0 0,008
N 12 12 12 12 12
Bakteri
Pearson
Correlation -0,641* 0,026 0,725** 0,725** 1
Sig. (2-tailed) 0,021 0,937 0,008 0,008
N 12 12 12 12 12
31 Lampiran 18 Hasil uji Pearson Coefficient Correlation akuarium perlakuan,
pengaruh kangkung air terhadap kualitas air limbah Correlation
Lampiran 19 Interpretasi nilai koefisien korelasi
Interval koefisien Tingkat hubungan
32
RIWAYAT HIDUP
Penulis dilahirkan di Bogor pada tanggal 23 April 1880. Anak ke-4 dari 5 bersaudara dari pasangan ibu Neni dan bapak Abdul Razak (alm). Penulis menempuh pendidikan formal di MI YAPEMAS (1998), SMP TAMAN ISLAM (2004), SMA ISLAM PAMBUDI LUHUR (2007). Pada tahun 2010 penulis lulus dari SMA ISLAM PAMBUDILUHUR dan pada tahun yang sama Penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB di Departemen Manajemen Sumberdaya Perairan, Fakultas Perikanan dan Ilmu Kelautan.