PENGARUH HYDRAULIC RETENTON TIME (HRT) DAN
RECYCLE SLUDGE PADA PROSES ASIDOGENESIS
LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS)
MENGGUNAKAN TEMPERATUR 45 °C
SKRIPSI
Oleh
YOLA MELIDA
110405016
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGARUH HYDRAULIC RETENTON TIME (HRT) DAN
RECYCLE SLUDGE PADA PROSES ASIDOGENESIS
LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS)
MENGGUNAKAN TEMPERATUR 45 °C
SKRIPSI
Oleh
YOLA MELIDA
110405016
SKRIPSI INI DIAJUKAN UNTUK MELENGKAPI SEBAGIAN
PERSYARATAN MENJADI SARJANA TEKNIK
DEPARTEMEN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
i
PERNYATAAN KEASLIAN SKRIPSI
Saya menyatakan dengan sesungguhnya bahwa skripsi dengan judul:
PENGARUH
HYDRAULIC RETENTON TIME
(HRT) DAN
RECYCLE
SLUDGE
PADA PROSES ASIDOGENESIS
LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS)
MENGGUNAKAN TEMPERATUR 45 °C
Dibuat untuk melengkapi sebagian persyaratan menjadi Sarjana Teknik pada Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini adalah hasil karya saya kecuali kutipan-kutipan yang telah saya sebutkan sumbernya.
Demikian pernyataan ini diperbuat, apabila dikemudian hari terbukti bahwa karya ini bukan karya saya atau merupakan hasil jiplakan maka saya bersedia menerima sanksi sesuai dengan aturan yang berlaku.
Medan, Oktober 2015
iv
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Allah SWT atas limpahan rahmat dan karunia-Nya sehingga skripsi ini dapat diselesaikan. Tulisan ini merupakan skripsi dengan judul “Pengaruh Hydraulic Retenton Time (HRT) Dan Recycle Sludge
Pada Proses Asidogenesis Limbah Cair Pabrik Kelapa Sawit (LCPKS) Menggunakan Temperatur 45 °C”, berdasarkan hasil penelitian yang penulis lakukan di Departemen Teknik Kimia Fakultas Teknik Universitas Sumatera Utara. Skripsi ini merupakan salah satu syarat untuk mendapatkan gelar sarjana teknik.
Hasil penelitian ini:
1. Memberikan informasi mengenai proses loading up dan variasi recycle sludge dalam proses digestasi anaerobik tahapan asidogenesis menggunakan temperatur 45 oC.
2. Memberikan sumbangan ilmu pengetahuan mengenai pengolahan limbah cair pabrik kelapa sawit.
Selama melakukan penelitian sampai penulisan skripsi ini, penulis banyak mendapat bantuan dari berbagai pihak, untuk itu penulis mengucapkan terimakasih dan penghargaan yang sebesar-besarnya kepada:
1. Dr. Eng. Ir. Irvan, M.Si. sebagai Ketua Departmen Teknik Kimia dan sebagai Dosen Pembimbing yang telah banyak memberikan arahan dan bantuan dalam pelaksanaan sidang.
2. Ibu Ir. Renita Manurung, M.T selaku Koordinator Penelitian Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara.
3. Prof. Dr. Ir. Rosdanelli Hasibuan, MT dan Dr. Ir. Fatimah, MT selaku Dosen Penguji yang telah memberikan saran dan masukan untuk kesempurnaan skripsi ini.
v
5. Kedua orang tua tercinta yang telah memberikan semangat, dorongan baik secara material maupun secara spiritual kepada penulis.
6. Rekan penelitian Intan Afrilia yang telah sabar dan membantu Penulis bekerja sama dalam menyelesaikan penelitian.
7. Rekan-rekan LPPM yaitu Bg Zoeliadi, Bg Dedy Anwar, Aidil Saputra, Ramlan, M. Darul Nafis, Rio Agung Prakoso, Ekuino Simanungkalit, Tri Putra Pasaribu, Khairul Fahmi, Endah Hutabarat, Christianto Sitio dan Muksalmina.
8. Teman-teman angkatan 2011 yang telah menemani Penulis dalam menempuh jalan menuju skripsi terutama, Ayu, Tika, Dania, Kherly, Piti, Yani dan Amin.
9. Teman-teman LETHGEN dan KAMMI TEKNIK yang selalu memberikan motivasi dan doa kepada penulis.
10. Seluruh Dosen/Staf Pengajar dan Pegawai Administrasi Departemen Teknik Kimia yang telah memberikan banyak ilmu yang berharga dan bantuan kepada penulis selama menjalankan perkuliahan.
11. Semua orang yang telah membantu penulis hingga penyusunan skripsi ini, yang tidak dapat ditulis namanya satu per satu.
Penulis menyadari bahwa laporan hasil penelitian ini masih jauh dari sempurna, oleh karena itu penulis mengharapkan saran dan masukan demi kesempurnaan skripsi ini. Semoga skripsi ini memberikan manfaat bagi pengembangan ilmu pengetahuan.
Medan, Oktober 2015
vi
DEDIKASI
Skripsi ini saya persembahkan untuk : Bapak & Ibu tercinta
Bapak Donni Hendri dan Ibu Erlinda
Orang tua dengan seluruh perhatian, nasehat dan kasih sayang yang telah membesarkan dan mendidikku
hingga seperti saat ini.
Serta Kakak & Adik tersayang Ruri Soraya dan Ahmad Gani
Terima kasih atas pengorbanan, cinta kasih sayang dan do’a yang tak pernah putus selalu kalian
vii
RIWAYAT HIDUP PENULIS
Nama : Yola Melida
NIM : 110405016
Tempat, tanggal lahir : Duri / 16 Mei 1993 Nama Orang Tua : Donni Hendri dan Erlinda Alamat Orang Tua:
Jalan Gajah Mada Pelita III No. 96 Sebanga, Kelurahan Titian Antui, Kecamatan Pinggir, Kota Duri, Riau.
Asal Sekolah:
SD Negeri 04 Talang Mandi Duri tahun 1999–2005
SMP S IT Mutiara Duri tahun 2005–2008
SMA Negeri Plus Prop.Riau tahun 2008–2011 Beasiswa yang pernah diperoleh:
1. Peningkatan Prestasi Akademik (PPA) tahun 2012–2013 2. Beasiswa Kabupaten Bengkalis tahun 2011–2012
Pengalaman Organisasi/Kerja:
1. Kesatuan Aksi Mahasiswa Muslim Indonesia (KAMMI) Teknik USU periode 2014/2015 sebagai Sekretaris Umum
2. Himpunan Mahasiswa Teknik Kimia (HIMATEK) FT USU periode 2014/2015 sebagai anggota Sosial dan Rohani
3. Covalen Study Group (CSG) periode 2013/2014 sebagai Ketua Keputrian 4. Anggota English Club FT USU tahun 2012-2013
5. Anggota USU Youth Rural Envoy tahun 2014
viii
ABSTRAK
Asidogenesis merupakan proses yang kompleks dimana mikroba anaerob bersama-sama mengurai senyawa organik menjadi asam organik molekul rendah berupa Volatile Fatty Acid (VFA) yang terdiri dari asam asetat, asam propionat dan asam butirat. Penelitian ini bertujuan untuk mendapatkan pengaruh variasi HRT dan
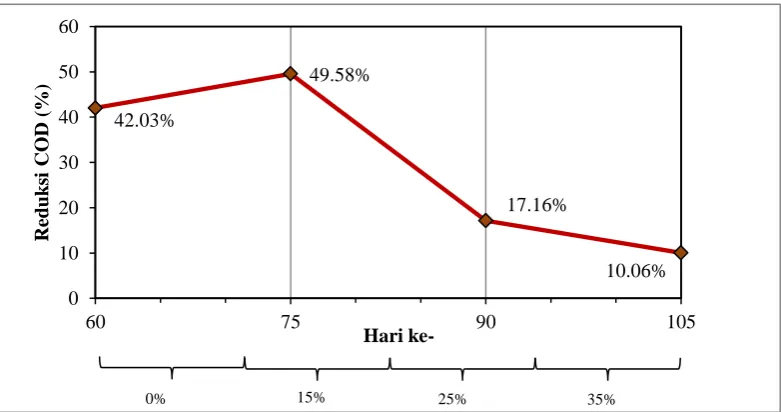
recycle sludge serta mendapatkan rasio recycle sludge terbaik pada proses asidognesis Limbah Cair Pabrik Kelapa Sawit (LCPKS) pada temperatur 45 oC. Fermentor yang digunakan yaitu CSTR dan laju pengadukan fermentor 150 rpm. Proses loading up dilakukan dengan variasi HRT yang dimulai dari HRT 20, 15, 10 dan 4 dengan pH 6 kemudian dilanjutkan dengan variasi recycle sludge yaitu pada 0, 15, 25, dan 35% dengan pH 6 dan HRT 4. Analisis yang dilakukan yaitu analisis TS, VS, TSS, VSS, COD dan VFA. Kondisi terbaik pada variasi recycle sludge dengan HRT 4 dicapai pada rasio recycle sludge 15% dengan konsentrasi VSS 9.467 mg/L dan reduksi VS tertinggi sebesar 27% serta memiliki reduksi COD tertinggi sebesar 49,58%.
ix
ABSTRACT
Acidogenesis is a complex process in which microbes decompose anaerobically together organic compounds into low molecular organic acids such as Volatile Fatty Acid (VFA) consisting of acetic acid, propionic acid and butyric acid. This study aims to get the effect of variations in HRT and recycle sludge and to obtain the best sludge recycle ratio on Palm Oil Mill Effluent (POME) acidogenesis process at a temperature of 45 oC. Fermenter used is CSTR fermentor and agitation rate of 150 rpm. Up the loading process is done by varying the starting HRT 20, 15, 10 and 4 to pH 6 and then proceed with the variation of the recycle sludge that is at 0, 15, 25, and 35% with a pH of 6 and HRT 4. Analysis conducted the analysis TS, VS, TSS, VSS, COD and VFA. The best conditions in the variation of the recycle sludge with HRT 4 achieved in the sludge recycle ratio of 15% with a VSS concentration of 9.467 mg / L and the highest VS reduction of 27% and has the highest COD reduction of 49.58%.
x
DAFTAR ISI
Halaman
PERNYATAAN KEASLIAN SKRIPSI i
PENGESAHAN ii
PRAKATA iii
DEDIKASI v
DAFTAR RIWAYAT HIDUP vi
ABSTRAK vii
ABSTRACT DAFTAR ISI
DAFTAR GAMBAR DAFTAR TABEL DAFTAR LAMPIRAN DAFTAR SINGKATAN
viii ix xii xiv xv xvii BAB I PENDAHULUAN
1.1 LATAR BELAKANG 1.2 PERUMUSAN MASALAH 1.3 TUJUAN PENELITIAN 1.4 MANFAAT PENELITIAN
1.5 RUANG LINGKUP PENELITIAN
1 1 4 4 4 5 BAB II TINJAUAN PUSTAKA
2.1 LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS) 2.2 BIOGAS
2.3 PROSES PEMBUATAN BIOGAS 2.3.1 Hidrolisis
2.3.2 Asidogenesis 2.3.3 Asetogenesis 2.3.4 Metanogenesis
2.4 PEMILIHAN PROSES DIGESTASI ANAEROBIK DUA TAHAP
7 7 9 11 12 13 13 14
xi 2.4.1 Parameter Digestasi Anaerobik
2.4.1.1 Temperatur 2.4.1.2 Nilai pH 2.4.1.3 Nutrisi
2.4.1.4 Kecepatan Pengadukan
2.4.1.5 Hydraulic Retention Time (HRT) 2.4.1.6 Alkalinitas
2.7 ANALISA EKONOMI
16 16 17 17 18 18 19 19 BAB III METODOLOGI PENELITIAN
3.1 LOKASI PENELITIAN 3.2 BAHAN DAN PERALATAN
3.2.1 Bahan-Bahan 3.2.2 Peralatan
3.2.2.1 Peralatan Utama 3.2.2.2 Peralatan Analisa
3.3 TAHAPAN PENELITIAN
3.3.1 Analisa Bahan Baku Limbah Cair Pabrik Kelapa Sawit (LCPKS)
3.3.1.1 Analisis pH
3.3.1.2 Analisi M-Alkalinity 3.3.1.3 Analisis Total Solids (TS) 3.3.1.4 Analisis Volatile Solids (VS)
3.3.1.5 Analisis Total Suspended Solids (TSS) 3.3.1.6 Analisis Volatile Suspended Solids (VSS) 3.3.1.7 Analisis Chemical Oxygen Demand (COD)
3.3.2 Loading Up dan Operasi Target 3.3.3 Recycle
3.3.4 Pengujian Sampel (Sampling) 3.4 JADWAL PENELITIAN
22 22 22 22 22 22 23 24 24 24 24 24 25 26 26 27 28 28 29 30 BAB IV PEMBAHASAN
4.1 KARAKTERISTIK LIMBAH CAIR PABRIK KELAPA SAWIT 4.2 HASIL PENELITIAN VARIASI HRT (PROSES LOADING UP)
xii
4.2.1 Pengaruh HRT terhadap Profil pH dan Alkalinitas 4.2.2 Pengaruh HRT terhadap Profil Pertumbuhan Mikroba 4.2.3 Pengaruh HRT terhadap Reduksi Chemical Oxygen
Demand (COD)
4.2.4 Pengaruh HRT terhadap Pembentukan Volatile Fatty Acid
(VFA)
4.2.5 Pengaruh HRT terhadap Rasio VFA/Alkalinitas 4.3 HASIL PENELITIAN VARIASI RECYCLE SLUDGE
4.3.1 Pengaruh recycle sludge terhadap Profil pH dan Alkalinitas
4.3.2 Pengaruh recycle sludge terhadap Profil Pertumbuhan Mikroba
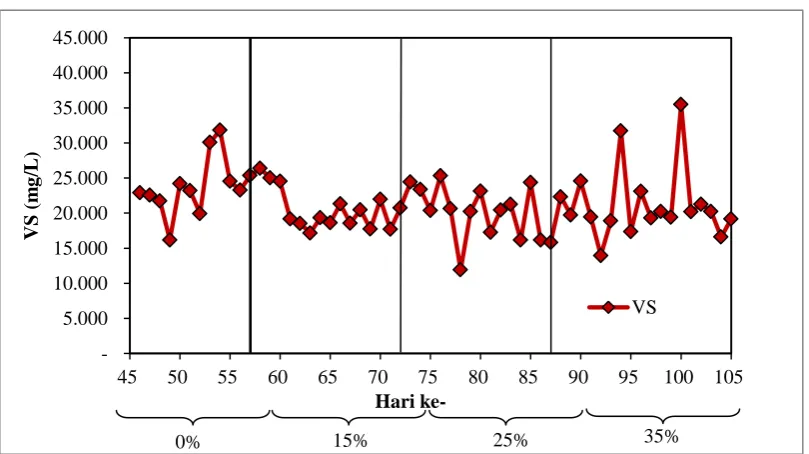
4.3.3 Pengaruh recycle sludge terhadap Volatile SolidS (VS) 4.3.4 Pengaruh recycle sludge terhadap Reduksi Chemical
Oxygen Demand (COD)
32 33 35
36
37 38 38
40
42 44
BAB V KESIMPULAN DAN SARAN 46
xiii
DAFTAR GAMBAR
Halaman Gambar 2.1 Diagram alir sederhana proses produksi minyak sawit
mentah termasuk limbah cair pabrik kelapa sawit (LCPKS)
Gambar 2.2 Tahapan proses fermentasi metana Gambar 2.3 Proses Digestasi Anaerobik Dua Tahap Gambar 2.4 Konversi Total VFA menjadi Biogas Gambar 3.1 Rangkaian Peralatan
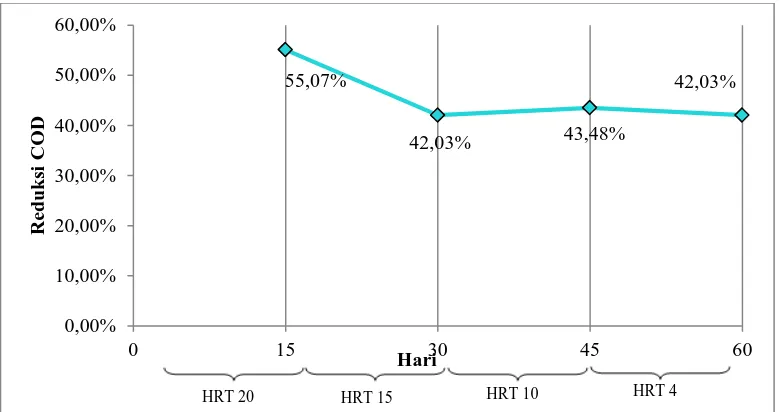
Gambar 4.1 Pengaruh HRT terhadap Profil pH dan Alkalinitas Gambar 4.2 Pengaruh HRT terhadap Profil Pertumbuhan Mikroba Gambar 4.3 Pengaruh HRT terhadap Reduksi Chemical Oxygen
Demand (COD)
Gambar 4.4 Pengaruh HRT terhadap Pembentukan Volatile Fatty Acid (VFA)
Gambar 4.5 Pengaruh HRT terhadap Rasio VFA/Alkalinitas Gambar 4.6 Pengaruh Recycle Sludge terhadap Alkalinitas
Gambar 4.7 Pengaruh Recycle Sludge terhadap Rata-Rata Alkalinitas
Gambar 4.8 Pengaruh Recycle Sludge terhadap Konsentrasi VSS pada Operasi Target
Gambar 4.9 Pengaruh Recycle Sludge terhadap Rata-Rata VSS Gambar 4.10 Pengaruh Recycle Sludge terhadap Reduksi Volatile
Solid (VS) pada Operasi Target
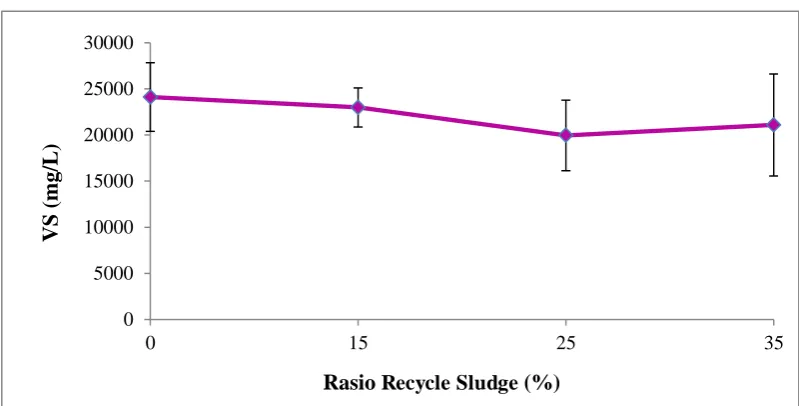
Gambar 4.11 Pengaruh Recycle Sludge terhadap Rata-Rata Volatile Solid (VS)
Gambar 4.12 Pengaruh Recycle Sludge terhadap Reduksi Chemical Oxygen Demand (COD)
Gambar A.1 Rangkaian Peralatan
Gambar A.2 Flowchart Prosedur Analisis pH
7
12 15 20 21 33 34 35
36
37 39 39
41
41 42
43
44
xiv
Gambar A.3 Flowchart Prosedur Analisis M-Alkalinity
Gambar A.4 Flowchart Prosedur Analisis Total Solids (TS) Gambar A.5 Flowchart Prosedur Analisis Volatile Solids (VS) Gambar A.6 Flowchart Prosedur Analisis Total Suspended Solids
(TSS)
Gambar A.7 Flowchart Prosedur Analisis Volaite Suspended Solids
(VSS)
Gambar A.8 Flowchart Prosedur Analisis Chemical Oxygen Demand
(COD)
Gambar A.9 Flowchart Prosedur Analisis Loading Up dan Operasi Target
Gambar A.10 Flowchart Prosedur Recycle
Gambar D.1 Tangki Umpan Gambar D.2 Fermentor
Gambar D.3 Botol Keluaran Fermentor (Discharge) Gambar D.4 Botol Penampung Biogas (Gas Collector) Gambar D.5 Gas Meter
Gambar D.6 Rangkaian Peralatan
Gambar D.7 Peralatan Analisis M-Alkalinity
Gambar D.8 Detecting Tube Hasil Analisis Gas H2S dan CO2
Gambar D.9 Peralatan Analisis Padatan Tersuspensi
Gambar D.10 Peralatan Analisis Chemical Oxygen Demand (COD) Gambar D.11 Timbangan Analitik
Gambar D.12 Desikator Gambar D.13 Oven Gambar D.14 Furnace
57 58 59 60
61
62
63
xv
DAFTAR TABEL
Halaman
Tabel 1.1 Potensi Sumber Daya Energi Baru Terbarukan Tabel 1.2 Rangkuman Hasil Penelitian Terdahulu
Tabel 2.1 Karakteristik Limbah Cair Pabrik Kelapa Sawit (LCPKS) Tabel 2.2 Baku Mutu Limbah Cair untuk Industri Minyak Sawit Tabel 2.3 Karakteristik Biogas
Tabel 2.4 Perbandingan Nilai Kalori dan Kesetaraan Biogas dengan Sumber Energi Lain
Tabel 2.5 Kebutuhan Nutrisi Mikroba
Tabel 2.6 Volume Pembentukan Biogas dari Jumlah VFA yang Terbentuk
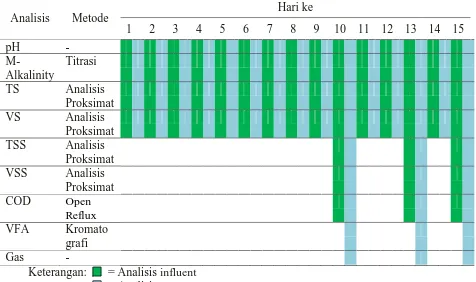
Tabel 3.1 Jadwal Analisis Influent dan Effluent
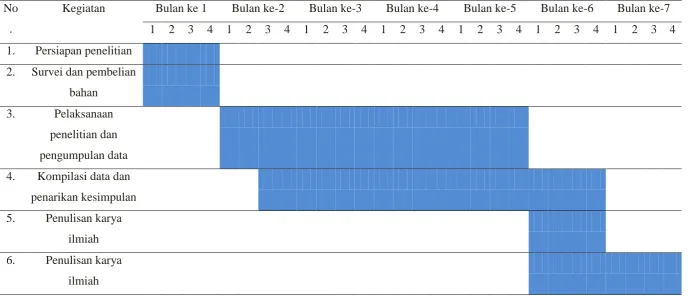
Tabel 3.2 Jenis Kegiatan dan Jadwal Pelaksanaan Penelitian Tabel 4.1 Karakteristik LCPKS dari PKS Adolina PTPN IV
Tabel B.1 Hasil Analisis Karakteristik LCPKS dari PTPN IV PKS Adolina
Tabel B.2 Data Hasil Analisa pH, Alkalinitas, TS, VS, TSS dan VSS pada Variasi Hydraulic Retention Time (HRT)
Tabel B.3 Data Hasil Analisis Chemical Oxygen Demand (COD) pada Variasi Hydraulic Retention Time (HRT)
Tabel B.4 Data Hasil Analisis Pembentukan Volatile Fatty Acid
(VFA) pada Variasi Hydraulic Retention Time (HRT) Tabel B.5 D Data Hasil Analisa pH, Alkalinitas, TS, VS, TSS dan
VSS pada Variasi Recycle Sludge
Tabel B.6 Data Hasil Analisis Chemical Oxygen Demand (COD) pada Variasi Recycle Sludge
2 3 8 9 10 10
18 20
29 30 31 65
65
67
67
67
xvi
DAFTAR LAMPIRAN
Halaman LAMPIRAN A METODOLOGI PENELITIAN
A.1 LOKASI PENELITIAN A.2 BAHAN DAN PERALATAN
A.2.1 Bahan-Bahan A.2.2 Peralatan
A.3 FLOWCHART PROSEDUR PENELITIAN A.3.1 Flowchart Prosedur Analisis pH
A.3.2 Flowchart Prosedur Analisis M-Alkalinity
A.3.3 Flowchart Prosedur Analisis Total Solids (TS) A.3.4 Flowchart Prosedur Analisis Volatile Solids (VS)
A.3.5 Flowchart Prosedur Analisis Total Suspended Solids
(TSS)
A.3.6 Flowchart Prosedur Analisis Volaite Suspended Solids
(VSS)
A.3.7 Flowchart Prosedur Analisis Chemical Oxygen Demand
(COD)
A.3.8 Flowchart Prosedur Analisis Loading Up dan Operasi Target
A.3.9 Flowchart Prosedur Recycle
53 53 53 53 53 56 56 57 58 59
60
61
62
63 64 LAMPIRAN B DATA HASIL ANALISIS
B.1 KARAKTERISTIK LIMBAH CAIR PABRIK KELAPA SAWIT
B.2 DATA HASIL PENELITIAN
B.2.1 Data Hasil Penelitian pada Variasi Hydraulic Retention Time (HRT)
B.2.2 Data Hasil Penelitian pada Variasi Recycle Sludge
65
65 65
65 67 LAMPIRAN C CONTOH PERHITUNGAN
C.1 PERHITUNGAN REDUKSI COD C.2 PERHITUNGAN STANDAR DEVIASI
xvii
LAMPIRAN D DOKUMENTASI 71
LAMPIRAN E HASIL UJI LABORATORIUM
E.1 HASIL UJI LABORATORIUM UNTUK ANALISIS LEMAK DALAM LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS) E.2 HASIL UJI LABORATORIUM UNTUK ANALISIS PROTEIN DALAM LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS) E.3 HASIL UJI LABORATORIUM UNTUK ANALISIS
KARBOHIDRAT DALAM LIMBAH CAIR PABRIK
KELAPA SAWIT (LCPKS)
E.4 HASIL UJI LABORATORIUM UNTUK ANALISIS
VOLATILE FATTY ACID (VFA)
76
76
77
77
xviii
DAFTAR SINGKATAN
BOD COD CPO CSTR HRT LCPKS MLSS OLR PKS POME SBR SCABR TBS TCOD TKS TN TS TSS UASB VFA VS VSS
Biological Oxygen Demand Chemical Oxygen Demand Crude Palm Oil
Continous Stirred Tank Reactor Hydraulic Retention Time
Limbah CairPabrik Kelapa Sawit
Mix Liquor Suspended Solid Organic Loading Rate
Pabrik Kelapa Sawit
Palm Oil Mill Effluent Sequencing Batch Reactor
Suspended Closed Anaerobic Bioreactor
Tandan Buah segar
Total Chemical Oxygen Demand
Tandan Kosong Sawit Total Nitrogen
Total Solids
Total Suspended Solids
Upflow Anaerobic Sludge Bed Volatile Fatty Acid
Volatile Solids
viii
ABSTRAK
Asidogenesis merupakan proses yang kompleks dimana mikroba anaerob bersama-sama mengurai senyawa organik menjadi asam organik molekul rendah berupa Volatile Fatty Acid (VFA) yang terdiri dari asam asetat, asam propionat dan asam butirat. Penelitian ini bertujuan untuk mendapatkan pengaruh variasi HRT dan
recycle sludge serta mendapatkan rasio recycle sludge terbaik pada proses asidognesis Limbah Cair Pabrik Kelapa Sawit (LCPKS) pada temperatur 45 oC. Fermentor yang digunakan yaitu CSTR dan laju pengadukan fermentor 150 rpm. Proses loading up dilakukan dengan variasi HRT yang dimulai dari HRT 20, 15, 10 dan 4 dengan pH 6 kemudian dilanjutkan dengan variasi recycle sludge yaitu pada 0, 15, 25, dan 35% dengan pH 6 dan HRT 4. Analisis yang dilakukan yaitu analisis TS, VS, TSS, VSS, COD dan VFA. Kondisi terbaik pada variasi recycle sludge dengan HRT 4 dicapai pada rasio recycle sludge 15% dengan konsentrasi VSS 9.467 mg/L dan reduksi VS tertinggi sebesar 27% serta memiliki reduksi COD tertinggi sebesar 49,58%.
ix
ABSTRACT
Acidogenesis is a complex process in which microbes decompose anaerobically together organic compounds into low molecular organic acids such as Volatile Fatty Acid (VFA) consisting of acetic acid, propionic acid and butyric acid. This study aims to get the effect of variations in HRT and recycle sludge and to obtain the best sludge recycle ratio on Palm Oil Mill Effluent (POME) acidogenesis process at a temperature of 45 oC. Fermenter used is CSTR fermentor and agitation rate of 150 rpm. Up the loading process is done by varying the starting HRT 20, 15, 10 and 4 to pH 6 and then proceed with the variation of the recycle sludge that is at 0, 15, 25, and 35% with a pH of 6 and HRT 4. Analysis conducted the analysis TS, VS, TSS, VSS, COD and VFA. The best conditions in the variation of the recycle sludge with HRT 4 achieved in the sludge recycle ratio of 15% with a VSS concentration of 9.467 mg / L and the highest VS reduction of 27% and has the highest COD reduction of 49.58%.
1
BAB I
PENDAHULUAN
1.1 LATAR BELAKANG
Saat ini Indonesia merupakan produsen minyak sawit pertama dunia. Namun demikian, industri pengolahan kelapa sawit menyebabkan permasalahan lingkungan yang perlu mendapat perhatian, antara lain adalah mesokarp, serat, tempurung, tandan kosong kelapa sawit, dan palm oil mill effluent atau limbah cair pabrik kelapa sawit (LCPKS) [1]. LCPKS merupakan limbah cair yang dibuang dari pabrik kelapa sawit sebagai cairan coklat kental pada suhu antara 80 oC dan 90 oC dengan pH antara 4 dan 5. Ini merupakan kombinasi dari air limbah yang dihasilkan dan dibuang dari sterilisasi kondensat (36% dari total LCPKS), air limbah klarifikasi (60% dari total LCPKS) dan air limbah hidrosiklon (hampir 4% dari total LCPKS) [2].
Namun, di sisi lain kandungan organik pada LCPKS sangat tinggi dengan kandungan BOD sebesar 25.000 – 65.714 dan COD sebesar 44.300 – 102.696, sehingga membuat LCPKS menjadi sumber yang baik untuk menghasilkan gas metana melalui proses anaerobik. Selain itu, LCPKS juga mengandung konstituen biodegradable
dengan rasio BOD / COD sebesar 0,5 dan ini berarti bahwa LCPKS dapat diurai dengan mudah menggunakan cara biologis [3]. Perhatian pada menipisnya bahan bakar fosil telah menyebabkan peningkatan kegiatan penelitian pada pengembangan energi terbarukan seperti produksi biogas. LCPKS sebagai limbah dengan kandungan karbon organik tinggi menjadi sumber yang menjanjikan untuk produksi biogas dan berpotensi menaikkan sektor energi terbarukan [4].
2
Indonesia memiliki potensi sumber daya energi baru terbarukan yang sangat beragam selain sumber energi fosil, seperti yang terlampir pada Tabel 1.1 berikut.
Tabel 1.1 Potensi Sumber Daya Energi Baru Terbarukan [5]
No Energi Baru Terbarukan Sumber Daya
1 Tenaga Air 75.091 MW
2 Panas Bumi 29.164 MW
3 Mini/Mikro Hydro 769,69 MW
4 Biomasa 49.810 MW
5 Tenaga Surya 4,80 kWh/m2/day
6 Tenaga Angin 3 – 6 m/s
7 Bahan Bakar Nabati 161,5 juta SBM
8 Biogas 2,3 juta SBM
9 Sampah Kota 1.872 MW
10 Uranium 3.000 MW
Biogas adalah campuran beberapa gas yang merupakan hasil fermentasi dari bahan organik dalam kondisi anaerobik, yang terdiri dari campuran metana (50-75%), CO2 (25-45%), dan sejumlah kecil H2, N2, dan H2S [1]. Salah satu faktor yang penting
yang harus diperhatikan dalam proses fermentasi untuk menghasilkan biogas pada digester anaerob adalah temperatur yang digunakan untuk memanaskan digester [6].
Proses fermentasi anaerobik adalah proses yang kompleks yang mengalami empat fase: hidrolisis, asidogenesis - fase pengasaman, asetogenesis, metanogenesis. Terlibat dalam konversi biokimia dari H2 dan CO2 menjadi metana dan asetat menjadi
metana dan CO2 [7]. Dalam setiap langkah dari proses, produksi gas dan laju
dekomposisi bahan organik dipengaruhi oleh faktor-faktor seperti suhu, pH, waktu retensi hidrolik (HRT) dan konsentrasi substrat [8].
Untuk meningkatkan laju dekomposisi COD, salah satu caranya yaitu dengan melakukan recycle sludge atau pengembalian lumpur dari digester ke reaktor. Selain itu,
recycle sludge juga digunakan untuk mendapatkan kembali mikroba pengurai yang sudah familiar dengan kondisi reaktor. Berdasarkan penelitian Sulaiman (2009) proses
3
rate) 6,0 kg COD m3/hari di mana konsentrasi VFA dalam digester menunjukkan peningkatan [9].
Hasil keluaran tahap asidogenesis adalah asam-asam lemak volatil seperti asam asetat, asam propionat dan asam butirat. Penelitian sebelumnya menunjukkan bahwa proses metanogenesis dipengaruhi oleh propionat ketika konsentrasi propionat sebanyak 1500-2220 mg/L. Degradasi propionat menjadi asetat dianggap sebagai salah satu langkah laju pembatas dalam sistem pencernaan anaerobik. Selanjutnya konsentrasi propionat yang tinggi (> 3000 mg/L) dapat menghentikan proses fermentasi [10]. Oleh sebab itu penelitian ini penting dilakukan untuk melihat pengaruh rasio recycle sludge
terhadap proses asidognesis LCPKS.
Berikut ini beberapa penelitian terdahuluyang telah dilakukan untuk menguraikan LCPKS pada proses asidogesis diantaranya ditunjukkan oleh Tabel 1.2 berikut ini:
Tabel 1.2 Rangkuman Hasil Penelitian Terdahulu
Peneliti (Tahun) Metode Penelitian Hasil Penelitian
Bambang Trisakti, Veronica Manalu, Irvan, Taslim, Muhammad Turmuzi (2015) [11]
Menggunakan reaktor Continous Stirred Tank Reactor dengan volume 2 liter untuk menguraikan POME variasi HRT menggunakan HRT 6,7; 5 dan 4 hari dengan laju pengadukan 50 rpm, pH 6 dan temperatur ruangan, sedangkan variasi pH menggunakan pH 5; 5,5; 6, dengan laju pengadukan 100-110 rpm pada temperatur 55°C
Hasil terbaik didapatkan pada HRT 4 dengan konsentrasi mikroba 20.62 mg VSS/L dan pengurangan COD sebesar 15.7%. Konsentrasi VFA maksimum (5.622,72 mg/L) pada HRT 4 hari dan pH 6.
Maneerat Khemkhao, Boonyarit Nuntakumjorn, Somkiet Techkarnjanaruk, Chantaraporn Phalakornkule (2012) [12]
Menggunakan reaktor Upflow Anaerobic Sludge Bed (UASB) dengan volume 5,3 liter untuk menguraikan POME dengan OLR antara 2.2 dan 9.5 g COD/L.hari. Dioperasikan pada suhu 37oC, 42oC, 47oC, 52oC dan 57oC dengan HRT 2 sebanyak 123 hari.
Penurunan COD efisiensi berkisar antara 76 dan 86%. Total VFA tertinggi diperoleh pada hari ke 94 dengan suhu 57 oC sebanyak 4.400 mg CH3COOH/L. Suhu
termofilik 57 oC ditemukan lebih cocok untuk diversifikasi hidrolitik dan asidogenik.
Tjandra Setiadi, Husaini and Asis Djajadiningrat. (1996) [13]
Menggunakan Anaerobic Baffled reactor dengan volume 5 liter untuk penguraian POME pada suhu 35oC. Dioperasikan pada HRT 4 selama 80
Efisiensi penurunan COD tertinggi pada rasio recycle 25% yaitu 84.6%. untuk rasio recycle
4
hari dengan variasi recycle 5, 10, 15, 20 dan 25%.
penanganan pH agar tidak ebih besar dari 6.8.
Yi Jing Chan, Mei Fong Chong, Chung Lim Law (2015) [14]
Menggunakan Sequencing Batch Reactor (SBR) dengan volume 2 liter untuk menguraikan POME pada suhu 50oC. waktu operasi divariasikan dengan MLSS 18.000, 21.000, 24.000, 27.000 dan 30.000 mg/L serta OLR 1.5, 2.5 dan 3.5 dan COD/L.day. HRT 4 hari.
Efisiensi penurunan COD, BOD dan TSS optimal hingga 86%, 87% dan 89% pada konsentrasi MLSS 27.000 mg/L dan OLR 2.5 g COD/L.day
1.2 PERUMUSAN MASALAH
Berdasarkan hasil penelitian terdahulu dapat dilihat bahwa proses asidogenesis dapat dilangsungkan pada keadaan mesofilik [13] dan termofilik [12], namun juga dapat dilakukan pada temperatur intermediet 45oC [15]. Menurut penelitian Bambang Trisakti [11] HRT terbaik untuk proses ini adalah 4 hari pada temperatur 55 oC . Sedangkan menurut Tjandra Setiadi [13] rasio recycle slugde terbaik untuk proses digestasi anaerobik cenderung meningkat dengan meningkatnya rasio recycle (25%) pada temperatur 35oC.
Oleh karena itu perlu dikaji pengaruh variasi HRT dan pengaruh variasi rasio
recycle sludge terhadap proses asidogenesis LCPKS pada temperatur 45°C.
1.3 TUJUAN PENELITIAN
Adapun yang menjadi tujuan dari penelitian ini adalah:
1. Mendapatkan pengaruh variasi HRT dan mendapatkan HRT target untuk proses asidognesis LCPKS pada temperatur 45 oC.
2. Mendapatkan pengaruh recycle sludge dan rasio recycle sludge terbaik pada proses asidognesis LCPKS pada temperatur 45 oC.
1.4 MANFAAT PENELITIAN
Manfaat dari penelitian ini antara lain yaitu :
5
2. Memberikan informasi mengenai pengaruh recycle sludge dan rasio recycle sludge terbaik pada proses asidognesis LCPKS pada temperatur 45 oC.
3. Memberikan informasi bagi peneliti yang ingin melakukan penelitian sejenis atau yang berhubungan.
1.5 RUANG LINGKUP PENELITIAN
Penelitian dilakukan dengan proses asidogenesis digestasi anaerobik menggunakan digester jenis Continous Stirred Tank Reactor (CSTR) recycle sludge dan tanpa recycle sludge dengan volume umpan 2 liter. Adapun variabel-variabel dari penelitian ini adalah sebagai berikut:
1. Variabel konstan:
a. Starter yang digunakan berasal dari hasil olahan penelitian sebelumnya yaitu
proses digestasi anaerobik tahapan asidogenesis, dimana starter yang
digunakan paling awal berasal dari kolam pengasaman Pabrik Kelapa Sawit
Torgamba PTPN III.
b. Jenis bahan baku atau umpan yang digunakan : Limbah cair kelapa sawit dari Pabrik Kelapa Sawit Adolina PTPN IV.
c. Kecepatan pengadukan tangki umpan : 250 rpm. d. Kecepatan pengadukan fermentor : 150 rpm. e. Temperatur fermentor 45oC.
f. pH : 6
2. Variabel divariasikan:
a. HRT dari fermentor yaitu : 20; 15; 10 dan 4 hari
b. Perlakuan non-recyclesludge dan recycle sludge pada effluent dari fermentor : 0%, 15%, 25% dan 35% .
Analisis yang akan dilakukan di dalam penelitian ini meliputi analisis pada bahan baku yang digunakan yaitu LCPKS dengan influent limbah dan effluent limbah. Adapun analisis cairan ini terdiri dari :
1. Pengontrolan pH
6
3. Analisis kadar total solid (TS) (Metode Analisis Proksimat) 4. Analisis volatile solid (VS) (Metode Analisis Proksimat)
5. Analisis kadar total suspended solid (TSS) (Metode Analisis Proksimat) 6. Analisis volatile suspended solid (VSS) (Metode Analisis Proksimat) 7. Analisis COD (Chemical Oxygen Demand) (Metode Open Reflux) 8. Analisis volatile fatty acid (VFA) (Metode Kromatografi)
Adapun analisis gas dilakukan jika pada penelitian ada terbentuk gas yaitu gas CO2, H2S dan CH4.
7
BAB II
TINJAUAN PUSTAKA
2.1 LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS)
Indonesia memproduksi minyak sawit mentah (CPO) sebesar hampir 33 juta metrik ton sawit di 2014/2015 karena tambahan 300.000 hektar perkebunan pindah ke buah usia bantalan. Total luas panen kelapa sawit Indonesia diperkirakan akan mencapai 8,4 juta hektar di tahun ini [16].
Proses untuk mengekstrak minyak sawit membutuhkan sejumlah besar air untuk uap sterilisasi tandan buah sawit dan mengklarifikasi minyak yang diekstraksi. Pabrik-pabrik kelapa sawit juga memerlukan sejumlah besar air untuk operasi dan debit dalam jumlah besar air limbah atau limbah cair pabrik kelapa sawit (LCPKS). Gambar 2.1 berikut merupakan diagram alir proses ekstraksi minyak sawit pada industri kelapa sawit, dilengkapi dengan limbah yang dihasilkan beserta sumber limbahnya.
8
Dalam satu ton buah kelapa sawit sekitar 0,87 m3 LCPKS dihasilkan atau 3,7 ton limbah per ton minyak yang dihasilkan. Pabrik kelapa sawit juga menghasilkan sejumlah besar limbah padatan seperti tandan kosong buah (TKS) (23%), serat mesocarp (12%) dan shell (5%) untuk setiap ton tandan buah segar (TBS) yang diproses [18].
LCPKS berwarna kecoklatan, berbentuk bubur, kental, asam dan mengandung minyak dan lemak yang tinggi. Karakteristik LCPKS dan TKS yang ditunjukkan pada Tabel 2.1 berikut.
Tabel 2.1 Karakteristik Limbah Cair Pabrik Kelapa Sawit
Parameter Satuan Nilai Referensi
Ph – 4 – 5 [19]
Suhu °C 47 [20]
Biochemical Oxygen Demand (BOD) mg/l 25.000 – 65.714 [19]
Chemical Oxygen Demand (COD) mg/l 44.300 – 102.696 [19]
Soluble Chemical Oxygen Demand
(SCOD)
mg/l 22.000 – 32.400 [21]
Total Chemical Oxygen Demand
(TCOD)
mg/l 54.100 – 94.300 [21]
Total Solids (TS) mg/l 40,500 – 72,058 [19]
Total Suspended Solids (TSS) mg/l 16,000 – 32,000 [21]
Volatile Solids (VS) mg/l 34,000 – 49,300 [19]
Volatile Suspended Solids (VSS) mg/l 15,200 – 30,600 [21]
Minyak dan Lemak mg/l 4.000 – 9.341 [19]
Total nitrogen (TN) mg/l 750 – 770 [19]
Ammoniacal nitrogen(NH3–N) mg/l 35 – 103 [19]
Total P mg/l 628 – 2,370 [22]
Total K mg/l 260 – 400 [23]
Total Ca mg/l 1.000 – 2.000 [23]
Total Mg mg/l 250 – 350 [23]
Volatile Fatty Acid / VFA (CH3COOH) mg/l 3540 [20]
Limbah LCPKS ini, jika tidak dibuang dengan benar, akan memiliki dampak negatif yang besar terhadap lingkungan sekitar. Beberapa peneliti menyoroti bahwa membuang LCPKS tanpa pengolahan yang memadai di kolam terbuka menyebabkan degradasi lingkungan dan emisi gas rumah kaca yang tinggi [17].
9
Tabel 2.2 Baku Mutu Limbah Cair untuk Industri Minyak Sawit [24]
Parameter Kadar Maksimum
(mg/l)
Beban Pencemaran Maksimum (kg/ton)
BOD5 250 1,5
COD 500 3,0
TSS 300 1,8
Minyak dan Lemak 30 0,18
Amonia Total (sebagai NH3-N) 20 0,12
pH 6,0 – 9,0
Debit Limbah Maksimum 6 m3 ton bahan baku
Perhatian pada menipisnya bahan bakar fosil telah menyebabkan peningkatan kegiatan penelitian pada pengembangan energi terbarukan seperti produksi biogas dari limbah untuk pembangkit listrik yang berkelanjutan. LCPKS menjadi limbah dengan kandungan karbon organik yang tinggi telah menjadi sumber yang menjanjikan untuk produksi biogas dan berpotensi menaikkan sektor energi terbarukan .
2.2 BIOGAS
Biogas adalah gas digester yang timbul dari aktivitas bakteri anaerob metanogen yang menguraikan bahan organik [25]. Biogas yang diperoleh dapat digunakan dalam berbagai bidang ekonomi, terutama dalam proses teknologi dan untuk tujuan rekayasa listrik, termasuk yang berikut :
1. Produksi energi panas di boiler gas dan produksi energi panas dan listrik dalam satuan terkait - (dari 1 m3 biogas - dalam produksi terkait energi 2.1 kWh energi listrik dan 2,9 kWh panas diperoleh);
2. Produksi energi listrik di percikan - pengapian atau turbin mesin;
3. Menggunakan gas yang diperoleh sebagai bahan bakar dalam mesin motor-mobil; 4. Menggunakan gas yang diperoleh dalam berbagai proses teknologi, misalnya dalam
produksi methanol [7].
10
Tabel 2.3 Karakteristik Biogas
Parameter Komposisi Referensi
Metana (CH4) 50 – 60% [26]
Karbon dioksida (CO2) 38 – 48% [26]
Nitrogen (N2) 0,4 – 1,2% [27]
Oksigen (O2) 0 – 0,4% [27]
Hidrogen Sulfida (H2S) 0,02 – 0,4% [27]
Kandungan Energi 6,0 – 6,5 kWh/m3 [28]
Kesetaraan Bahan Bakar
0,60 – 0,65 liter minyak/m3 udara [28]
Batas Ledakan 6 – 12% biogas di udara [28]
Temperatur Nyala 650 – 750 °C [28]
Tekanan Kritis 75 – 89 bar [28]
Temperatur Kritis –82,5 °C [28]
Densitas Normal 1,2 kg/m3 [28]
Massa Molar 16,043 kg/kmol-1 [28]
Kandungan energi biogas tergantung langsung pada isi metana. Semakin tinggi kandungan zat mudah terurai seperti lemak dan pati yang akan difermentasi, substrat yang lebih tinggi akan menjadi output gas. Sebuah meter kubik gas metana memiliki kandungan energi hampir sepuluh jam kilowatt (9,97 kWh). Jika kandungan metana akan berjumlah 60% kandungan energi total dari satu meter kubik biogas sekitar enam kWh, nilai kalor akan sesuai kira-kira 0,6 liter bahan bakar minyak [25].
Efisiensi rata-rata pencernaan metana mencapai sekitar 0,24 m3 metana dari 1 kg bahan organik kering. 1 m3 biogas dari 26 MJ nilai kalori dapat menggantikan 0,77 m3 gas alam dari nilai kalori 33,5 MJ, 1,1 kg batubara keras nilai kalori 23,4 MJ atau 2 kg kayu bakar dari 13,3 MJ nilai kalori [7]. Tabel 2.4 berikut merupakan perbandingan nilai kalori dan kesetaraan biogas dengan sumber energi lain.
Tabel 2.4 Perbandingan Nilai Kalori dan Kesetaraan Biogas dengan Sumber Energi Lain [7],[18].
No Bahan Bakar Nilai Kalori (kJ) Nilai Kesetaraan
1 Biogas 15000 1 m3
2 Gas alam 33500 0.77 m3
3 Batubara 23400 1.1 kg
4 Minyak tanah 8000 0.62 liter
11
bakteri metana
hidrolisis
fosforilas i
β-oksidasi
bakteri metana
bakteri metana
hidrolisis deaminasi bakteri metana
2.3 PROSES PEMBUATAN BIOGAS
Proses pencernaan anaerobik terdiri dari hidrolisis, asidogenesis, asetogenesis, dan tahap metanogenesis, dan setiap tahap merupakan fungsi dari kondisi metabolik dari berbagai mikroorganisme [29]. Langkah-langkah degradasi individu dilakukan oleh berbagai mikroorganisme, yang memiliki kebutuhan yang berbeda pada lingkungan. Mikroorganisme hidrolisis dan fermentasi seperti Clostridia, dan Bifidobacteria
bertanggung jawab untuk awal serangan terhadap polimer dan monomer dan menghasilkan terutama asetat, hidrogen dan volatile lemak asam seperti propionat dan butirat dalam jumlah yang bervariasi [30].
Proses fermentasi memerlukan waktu 7 sampai 10 hari untuk menghasilkan biogas dengan suhu optimum 35 oC dan pH optimum pada range 6,4 – 7,9 [31]. Pada akhir rantai degradasi, dua kelompok bakteri metanogen menghasilkan metana dari asetat atau hidrogen dan karbon dioksida. Bakteri ini adalah jenis anaerob yang memerlukan potensial redoks yang lebih rendah untuk pertumbuhannya daripada kebanyakan bakteri anaerobik lainnya. Hanya sedikit spesies yang mampu mendegradasi asetat ke CH4 dan CO2, misalnya, Methanosarcina barkeri, Metanonococcus mazei, dan
Methanotrix soehngenii, sedangkan semua bakteri metanogen dapat menggunakan hidrogen untuk membentuk metana [30].
Reaksi pembentukan metana dari bahan – bahan organik yang dapat terdegradasi dengan bantuan enzim maupun bakteri dapat dilihat sebagai berikut [31]:
polisakarida glukosa asam asetat CH4+CO2+H2 (2.1)
gliserol asam asetat CH4+CO2+H2 (2.2)
lemak asam lemak asam asetat CH4+CO2+H2 (2.3)
protein asam amin asam asetat CH4+CO2+H2 (2.4)
12
[image:33.612.147.505.133.423.2]Empat tahapan proses digestasi anaerobik yaitu hidrolisis, asidogenesis, asetogenesis dan metanogenesis dapat dilihat pada gambar 2.2 berikut.
Gambar 2.2 Tahapan proses fermentasi metana [7].
2.3.1 Hidrolisis
Degradasi bahan organik diawali dengan tahapan penguraian secara enzimatik
bahan organik dengan berat molekul besar (berantai panjang) sebagai sumber energi
bagi sel dan sumber karbon. Sejumlah a-glycosidic carbohydrates, seperti zat tepung,
sukrosa, glikogen dan amilase terhidrolisis oleh enzim amilase yang dihasilkan oleh
mikroorganisme. Enzim ini merusak polisakarida dengan memutus ikatan rantai
glycosidic menjadi disakarida yang kemudian oleh enzim glikosidase diuraikan menjadi
monosakarida. Sedangkan protein akan di hidrolisis oleh enzim protease dan peptidase,
kedua enzim ini sebagian bersumber dari dinding sel mikroorganisme dan sebagian lagi
terdapat bebas dalam reaktor [32].
Polimers, proteins, carbohydrates, lipids
Acetic acid
HYDROLYSIS
Monomeres, oligomeres, aminoacids, sugars, long-chain fatty acids
Fatty acids (propionic, butylic, valeric and others), alcohols ACIDOGENESIS
ACETOGENESIS
H2
METHANOGENESIS
13
selulosa air glukosa
Reaksi hidrolisis dapat dilihat seperti dibawah ini [31]: (C6H10O5)n (s) + n H2O(l) n C6H12O6 (2.5)
2.3.2 Asidogenesis
Asam amino, gula dan asam lemak yang dihasilkan proses hidrolisis selanjutnya difermentasi menjadi asam lemak volatile (asam asetat, asam propionat, asam butirat). Konsentrasi total asam volatil terbentuk dapat meningkat dengan adanya kenaikan nilai pembebanan organik dan keberadaan toksik [33].
Asidogenesis mungkin dua-arah karena efek dari berbagai populasi mikroorganisme. Proses ini dapat dibagi menjadi dua jenis: Hidrogenasi dan dehidrogenasi. Jalur dasar transformasi melewati asetat, CO2 dan H2, sedangkan produk
asidogenesis lainnya memainkan peran signifikan. Produk baru tidak boleh digunakan secara langsung oleh bakteri metanogen dan harus diubah oleh bakteri wajib memproduksi hidrogen dalam proses yang disebut asetogenesis. Diantara produk dari asidogenesis, amonia dan hidrogen sulfida yang memberikan bau yang tidak menyenangkan. Bakteri asam anaerob fakultatif yang digunakan sebagai berikut:
Pseudomonas, Bacillus, Clostridium, Micrococcus atau Flavobacterium [7]. Reaksi asidogenesis dapat di lihat di bawah ini [34]:
C6H12O6 CH3CH2CH2COOH + 2 CO2 + 2 H2 (2.6)
Glukosa asam butirat
C6H12O6 + 2 H2 CH3CH2COOH + 2 H2O (2.7)
Glukosa asam propionat
2.3.3 Asetogenesis
Tahap berikutnya asetogenesis, permintaan biologis oksigen (BOD) dan kebutuhan oksigen kimia (COD) berkurang melalui jalur ini. Asetogenesis terjadi melalui fermentasi karbohidrat, di mana asetat merupakan produk utama, dan proses metabolisme lainnya. Hasilnya adalah kombinasi dari asetat, CO2, dan H2. Peran
14
Asam lemak rantai panjang, terbentuk dari hidrolisis lipid, yang teroksidasi menjadi asetat atau propionat dan gas hidrogen terbentuk. Dalam kondisi standar, dengan adanya hidrogen dalam larutan dapat menghambat oksidasi.
Reaksi penting lainnya dalam tahap asetogenesis melibatkan konversi glukosa (2.8), etanol (2.9) dan bikarbonat (2.10) menjadi asetat, yaitu :
C6H12O6 + 2H2O ↔ 2CH3COOH + 2 CO2 + 4H2 (2.8)
CH3CH2OH + 2H2O ↔ CH3COO- + 2H2 +H+ (2.9)
2HCO3- + 4H2+ H+ ↔ CH3COO- + 4H2O (2.10)
Transisi dari substrat bahan organik menjadi asam organik dalam tahap pembentukan asam menyebabkan pH sistem drop. Hal ini menguntungkan bagi bakteri
acidogenic dan acetagenic yang lebih memilih lingkungan yang sedikit asam, dengan pH 4,5-5,5, dan kurang sensitif terhadap perubahan dalam aliran umpan yang masuk, tetapi bermasalah bagi bakteri yang terlibat dalam tahap berikutnya metanogenesis [35].
2.3.4 Metanogenesis
Proses ini sangat penting dalam digester anaerob. Selama proses metanogenesis karbondioksida direduksi menjadi metana dan air, asetat dikonversi menjadi metana dan karbondioksida. Bakteri penghasil metana antara lain Methanococcus, Methanobacteria, dan Methanosarcina. Kebanyakan bakteri metanogen bersifat mesofilik dengan kisaran suhu optimum 20oC - 40oC, namun bakteri metanogen juga dapat ditemui pada suhu termofilik. Bakteri ini akan membentuk gas CH4 dan CO2 dari gas H2, CO2 dan asam
asetat yang dihasilkan pada tahap pengasaman [36]. CH3COOH → CH4 + CO2 (2.11)
(methane)
2 H2 + CO2→ CH4 + 2 H2O (2.12)
(methane)
2.4 PEMILIHAN PROSES DIGESTASI ANAEROBIK DUA TAHAP
Proses dekomposisi bahan organik dengan sistem anaerobik akan dihasilkan
biogas yang dapat dimanfaatkan sebagai sumber energi substitusi (bukan sumber energi
15
itu sendiri. Pada sistem anaerobik ini terdapat dua kelompok besar mikroorganisme yang
bekerja yaitu bakteri pembentuk asam dan bakteri pembentuk metan. Kedua bakteri ini
memiliki kemampuan duplikasi yang sangat berbeda dan sangat kontradiksi. Dengan
menggunakan sistem anaerobik, permasalahan ini dapat diatasi karena sistem ini
mempunyai kemampuan penyangga pH (buffer) terhadap tingkat keasaman dengan
adanya alkalinitas sebagai reaksi adanya komponen bikarbonat dan hidroksida dalam
reaktor [32].
Pembentukan biogas lebih besar pada proses fermentasi 2 tahap disebabkan
karena adanya proses hidrolisa terlebih dahulu yang merupakan proses degradasi
senyawa kompleks yaitu polisakarida menjadi senyawa yang lebih sederhana yaitu
disakarida dan monosakarida sehingga akan mempermudah proses pembentukan asam
oleh bakteri asetogenik dan juga proses pembentukan metan oleh bakteri metanogenesis.
Proses tersebut tidak akan dijumpai pada fermentasi 1 tahap, sehingga akan terjadi
pembentukan asam yang terlalu cepat. Pembentukan asam yang terlalu cepat ini
menyebabkan banyaknya bakteri metanogenesis yang mati karena tidak tahan dengan
suasana asam [36]. Proses digestasi anaerobik dua tahap dapat digambarkan sebagai
[image:36.612.189.463.451.658.2]berikut:
16
Pengembangan reaktor tingkat tinggi didasarkan pada imobilisasi dari biomassa dalam sistem pengolahan air limbah yang meningkatkan tingkat degradasi sistem pengolahan anaerobik dengan mengurangi waktu retensi. Kelemahan dari sistem ini adalah bahwa sistem biasanya cocok untuk aliran air limbah encer, yang mengandung sekitar 3% total suspensi padatan dengan ukuran partikel kurang dari 0,75 mm. Ini berarti bahwa substrat dengan kandungan padatan tinggi harus dilarutkan sebelum dapat diperkenalkan ke sistem tingkat tinggi ini. Oleh karena itu, sistem dua fasa yang diperlukan dalam rangka untuk mencapai pencernaan yang cepat dan operasi lebih stabil dan kapasitas beban organik yang lebih tinggi. Namun, hanya ada pemeriksaan yang sangat sedikit pada penerapan substrat dengan kandungan total padatan yang tinggi dalam proses dua tahap [22].
2.4.1 Parameter Digestasi Anaerobik
Keberhasilan dari proses digestasi anaerobik tergantung dari beberapa parameter. Pertumbuhan dan aktivitas mikroorganisme anaerobik sangat dipengaruhi oleh kondisi lingkungan seperti :
a) Temperatur b) Nilai pH c) Nutrisi
d) Kecepatan pengadukan
e) Hydraulic Retention Time (HRT) f) Alkalinitas
2.4.1.1 Temperatur
17
drastis dari tingkat konversi dan dengan demikian diharapkan produksi biogas dapat terbentuk.
Jika tingkat aliran tinggi yang digunakan dan substrat yang digunakan adalah
biowastes, maka proses termofilik akan menjadi keuntungan. Proses termofilik mencapai kecepatan dekomposisi lebih tinggi, produksi gas lebih tinggi dan lebih stabil untuk sejumlah beban. Operasi mesofilik dan operasi termofilik berbeda dalam hal adaptasi bakteri untuk suhu lingkungan dan tidak boleh cepat berubah [25].
2.4.1.2 Nilai pH
Pada pH dikendalikan, biogas yang terbentuk adalah lebih besar daripada pH yang tidak terkendali. Pengaruh perubahan pH sangat sensitif terhadap proses fermentasi yang dilakukan oleh aktivitas bakteri. Oleh karena itu, kontrol pH adalah parameter penting untuk aplikasi produksi biogas. Penurunan pH disebabkan oleh bakteri asidogenesis yang menghasilkan asetat, gas hidrogen, karbon dioksida, dan beberapa lainnya VFA seperti asam propionat dan butirat. Nilai pH yang rendah menghambat aktivitas mikroorganisme yang terlibat dalam produksi biogas terutama bakteri metanogen.
Kondisi pH rendah disebabkan oleh dua sumber keasaman (H2CO3 dan VFA),
yang dihasilkan oleh aktivitas bakteri. Asam ini diperlukan alkalinitas untuk netralisasi sehingga aktivitas bakteri tidak terganggu dengan penurunan pH. Natrium karbonat (Na2CO3) dapat meningkatkan alkalinitas atau penyangga kapasitas fermentasi untuk
mengontrol pH substrat. Hubungan yang sempurna antara tahap asidogenesis dan metanogenesis adalah saat pH tetap pada 7,0 dan tidak ada peningkatan drastis dalam keasaman atau alkalinitas [37].
2.4.1.3 Nutrisi
18
mikronutrien yang cukup dan tersedia populasi bakteri yang diperlukan untuk fermentasi anaerobik [25]. Tabel 2.5 berikut merupakan kebutuhan nutrisi mikroba dalam fermentasi.
Tabel 2.5 Kebutuhan Nutrisi Mikroba [38].
Bahan Jumlah Kebutuhan
(mg/gr asetat)
NH4-N 3.3
PO4-P 0.1
S 0.33
Ca 0.13
Mg 0.018
Fe 0.023
Ni 0.004
Co 0.003
Zn 0.02
2.4.1.4 Kecepatan pengadukan
Kecepatan upflow yang lebih tinggi berpengaruh terhadap pengadukan dalam reaktor sehingga mikroorganisme dan substrat dapat bercampur dengan lebih baik dan memudahkan mikroorganisme dalam mendegradasi zat organik. Kecepatan upflow yang tinggi memberikan kontak yang baik antara substrat dan biomassa yang menyebabkan peningkatan efisiensi penyisihan dalam reaktor. Menurunkan kecepatan upflow dapat mengurangi pencampuran dalam reaktor dan karenanya yang mengganggu kontak antara substrat dan biomassa [39].
2.4.1.5 Hydraulic Retention Time (HRT)
Kebanyakan sistem anaerob dirancang untuk mempertahankan limbah agar tetap jumlahnya setiap harinya. Jumlah hari bahan tetap dalam tangki disebut Hydraulic Retention Time (HRT). HRT sama dengan volume tangki dibagi dengan aliran harian
(HRT = V / Q). HRT penting karena menetapkan jumlah waktu yang tersedia untuk pertumbuhan bakteri dan konversi berikutnya dari bahan organik ke gas [40].
19
yang mudah untuk mengontrol, tetapi juga waktu makro-konseptual untuk bahan organik untuk tinggal di reaktor. Dalam rekayasa bio-reaksi, kebalikan dari HRT didefinisikan sebagai tingkat pengenceran, yang jika lebih besar dari laju pertumbuhan sel-sel mikroba dalam reaktor, mikroba akan dicuci, dan sebaliknya mikroba akan terakumulasi dalam reaktor. Salah satu dari situasi ini dapat mengakibatkan kerusakan biologis dalam reaktor [41].
2.4.1.6 Alkalinitas
Alkalinitas dalam air limbah dapat dihasilkan dari keberadaan senyawa hidroksida dan karbonat dari kalsium, magnesium, natrium, kalium atau ammonia memegang peranan penting dalam proses pengkontrolan pH. Tingginya nilai alkalinitas cairan dalam sistem digestasi anaerobik diperlukan untuk meningkatkan kemampuan netralisasi terhadap asam lemak volatil yang dihasilkan untuk mencegah terjadinya penurunan pH drastis yang dapat bersifat menghambat aktivitas metanogen. Jika alkalinitas tidak tersedia cukup dalam substrat, maka dapat dilakukan pengurangan laju pembebanan organik atau penambahan bahan kimia. Penambahan senyawa kimia seperti Ca(OH)2 dan Na2CO3 dapat dilakukan untuk meningkatkan nilai pH dan alkalinitas
larutan perlu dilakukan pada substrat dengan kadar alkalinitas di bawah 1000 mg/L CaCO3. Peningkatan nilai alkalinitas akan menghasilkan peningkatan laju metanogenesis
yang selanjutnya berakibat pada perbaikan dalam reduksi COD [42].
2.5 ANALISA EKONOMI
20
Tabel 2.6 Volume Biogas dari Jumlah VFA yang Terbentuk
Pada penelitian ini, total pembentukan VFA diperoleh pada variasi HRT 4 hari (tanpa Recycle Sludge) dengan jumlah 14.984,32 mg/L. Melalui Tabel 2.6 dapat digambarkan grafik linear seperti ditunjukkan pada Gambar 2.4 berikut.
Gambar 2.4 Konversi Total VFA menjadi Biogas [57, 58, 59]
Gambar 2.4 menunjukkan grafik linearisasi pembentukkan biogas dari VFA dengan persamaan garis lurus: y = 0,0009 x + 0,1043 dengan y merupakan produksi biogas dan x merupakan VFA yang terbentuk. Berdasarkan persamaan tersebut maka jumlah biogas yang dapat dihasilkan dari total VFA tertinggi pada penelitian ini adalah:
y = 0,0009 x + 0,1043
= (0,0009) (14.984,32) + 0,1043 = 13,59 liter biogas/liter LCPKS hari = 13,59 m3 biogas/m3 LCPKS hari
y = 0,0009x + 0,104 0
2 4 6 8
0 1000 2000 3000 4000 5000 6000 7000 8000
P
ro
du
k
si
B
io
g
a
s
(lite
r/lit
er
·ha
ri)
Total VFA (mg/l)
Produksi Biogas
Linear (Produksi Biogas)
Peneliti Total VFA (mg/L) Volume Biogas (L/L·hari)
Ivet Ferrer et al [57] 1.270 0,87
Setiadi et al [13] 19.800 19,8
21
Ekivalensi 1 m3 biogas terhadap solar adalah sebesar 0,62 liter [7]. Sehingga
=
×
= 8,43 liter solar/m3 LCPKS
Harga solar industri adalah Rp 8.200/liter [56], sehingga untuk biogas yang dihasilkan pada proses satu tahap diperoleh keuntungan sebesar:
Harga biogas yang dihasilkan =
×
= Rp. 69.126/m3 LCPKS
Jika LCPKS yang diolah sebesar 450 m3/ hari, maka keuntungan yang akan diperoleh perhari adalah:
Keuntungan yang diperoleh =
×
22
BAB III
METODOLOGI PENELITIAN
3.1 LOKASI PENELITIAN
Penelitian ini dilakukan di Laboratorium Ekologi, Departemen Teknik
Kimia, Fakultas Teknik, Universitas Sumatera Utara (USU), Medan.
3.2 BAHAN DAN PERALATAN 3.2.1 Bahan-bahan
1. Starter dari penelitian sebelumnya 2. Sampel LCPKS dari fat pit PKS Adolina 3. Asam klorida (HCl) 0,1 N
4. Aquadest (H2O)
5. Natrium Bikarbonat (NaHCO3)
3.2.2 Peralatan
3.2.2.1 Peralatan Utama
1. Fermentor tangki berpengaduk/jar fermentor (EYELA model No: MBF 300ME)
2. Pompa sludge/slurry pump (HEISHIN, model No.:3NY06F) 3. Gas meter (SHINAGAWA, model No.:W-NK-0.5B)
4. Tangki umpan (service tank) 5. Pengaduk
6. Sensor temperatur 7. pH elektroda
8. Timer (OMRON, model No.:H5F) 9. Botol penampungan keluaran fermentor
10.Gascollector
23 3.2.2.2 Peralatan Analisis
1. Buret 25 ml
2. Timbangan analitik 3. Oven
4. Desikator 5. Pipet volumetrik 6. Karet penghisap 7. Pengaduk magnetic
8. Furnace
1. Pengaduk (mixer) 2. Tangki Umpan 3. Pompa Sludge 4. Jar Fermentor
5. Tombol pompa air jaket 6. Tombol penghidup fermentor 7. Pengatur kecepatan pengaduk 8. Pengatur suhu air jaket
1 0
2 4
3 1
11
7 5
3
10
8 6
4 2
3 alarm
heating 13
12
14
9
9. Wadah keluaran fermentor
10. Gas Meter
11. Gas Collector
12. pH elektroda 13. Penyerap H2S 14. Sampling injector
24
3.3 TAHAPAN PENELITIAN
3.3.1 Analisis Bahan Baku Limbah Cair Pabrik Kelapa Sawit
3.3.1.1 Analisis pH
Adapun prosedur analisis pH adalah :
1) Kalibrasi pH meter dilakukan ke dalam pH 4 dan pH 7.
2) Bagian elektroda dari pH meter dicuci dengan aquadest.
3) Elektoda dimasukkan ke dalam sampel yang akan diukur pH-nya.
4) Nilai bacaan pH meter ditunggu sampai konstan lalu dicatat nilai
bacaannya.
3.3.1.2 Analisis M-Alkalinity
Adapun prosedur analisis M-alkalinity adalah :
1) Sampel dimasukkan sebanyak 5 ml ke dalam beaker glass lalu
ditambahkan dengan aquadest hingga volume larutan 80 ml.
2) Beaker glass diletakkan di atas magnetic stirrer, dan diletakkan pH
elektroda di dalam beaker gelas, kemudian stirrer dihidupkan dan
kecepatan diatur sedemikian rupa hingga sampel tercampur sempurna
dengan aquadest.
3) Campuran dititrasi dengan larutan HCl 0,1 N hingga pH mencapai 4,8 ±
0,02.
4) Analisis M-Alkalinity dilakukan untuk LCPKS dan limbah fermentasi pada
Jar fermentor.
5) M-Alkalinity dapat dihitung berdasarkan rumus sebagai berikut:
M-Alkalinity =
Sampel Vol
5 x 1000 x M x terpakai yang
Vol.HCl HCl
3.3.1.3Analisis Total Solids (TS)
Adapun prosedur analisis TS adalah :
1) Cawan penguap kosong yang telah dibersihkan, dipanaskan pada 105oC di
dalam oven selama 1 jam. Apabila akan dilanjutkan untuk analisis zat
tersuspensi organik, cawan dipanaskan pada 550oC, selama 1 jam.
2) Cawan didinginkan selama 15 menit di dalam desikator, lalu ditimbang.
25
3) Sampel dikocok merata, lalu dituangkan ke dalam cawan. Volume sampel
diatur sehingga berat residu antara 25-250 mg.
4) Cawan berisi sampel dimasukkan ke dalam oven, suhu 98oC untuk
mencegah percikan akibat didihan air di dalam cawan. Namun bila volum
sampel kecil dan dinding cawan cukup tinggi maka langkah ini tidak perlu.
5) Pengeringan diteruskan di dalam oven dengan suhu 103-105oC selama 1
jam.
6) Cawan yang berisi residu zat padat tersebut didinginkan di dalam desikator
sebelum ditimbang.
7) Langkah 5 dan 6 diulang sampai didapat berat yang konstan atau
berkurang berat lebih kecil 4% berat semula atau 0,5 mg, biasanya
pemanasan 1-2 jam sudah cukup. Penimbangan harus dikerjakan dengan
cepat untuk mengurangi galat.
8) Kandungan TS dapat dihitung berdasarkan rumus sebagai berikut:
mL sampel, volume
1000 B) -(A tal/L
padatan to
mg
Keterangan: A = berat residu kering + cawan porselen, mg
B = berat cawan porselen, mg
3.3.1.4Analisis Volatile Solids (VS)
Adapun prosedur analisis VS adalah :
1) Cawan penguap setelah dari TS dipanaskan dengan menggunakan muffle
furnace pada suhu 550oC selama 1 jam.
2) Setelah itu cawan penguap didinginkan di dalam desikator hingga
mencapai suhu kamar.
3) Berat cawan penguap ditimbang.
4) Kandungan VS dapat dihitung berdasarkan rumus sebagai berikut:
mL sampel, volume
1000 B) -(A latil/L
padatan vo
mg
Keterangan: A = berat residu+cawan porselen sebelum pembakaran, mg
B = berat residu + cawan porselen setelah pembakaran, mg (3.2)
26
3.3.1.5Analisis Total Suspended Solids (TSS)
Adapun prosedur analisis TSS adalah :
1) Berat kertas saring kering yang digunakan ditimbang.
2) Kertas saring dibasahi dengan sedikit air suling.
3) Sampel diaduk dengan magnetic stirrer untuk memperoleh sampel yang
lebih homogen.
4) Sampel dipipetkan ke penyaringan dengan volume tertentu pada waktu
contoh diaduk dengan magnetic stirer.
5) Kertas saring dicuci atau disaring dengan 3 x 10 ml aquadest.
6) Kertas saring dipindahkan secara hati-hati dari peralatan penyaring ke
wadah timbang dengan aluminium sebagai penyangga.
7) Dikeringkan di dalam oven setidaknya selama 1 jam pada suhu 103ºC
sampai dengan 105ºC, didinginkan dalam desikator untuk
menyeimbangkan suhu dan massanya.
8) Tahapan pengeringan, pendinginan dalam desikator, dan penimbangan
diulangi sampai diperoleh berat konstan atau sampai perubahan berat lebih
kecil dari 4% terhadap penimbangan sebelumnya atau 0,5 mg.
9) Kandungan TSS dapat dihitung berdasarkan rumus sebagai berikut:
mL sampel, volume
1000 B) -(A total/L
rsuspensi padatan te
mg
Keterangan: A = berat kertas saring + berat residu, mg
B = berat kertas saring, mg
3.3.1.6Analisis Volatile Suspended Solids (VSS)
Adapun prosedur analisis VSS adalah :
1) Sampel residu hasil analisa TSS dibakar mengunakan api bunsen di dalam
cawan porselen yang telah dikering dan diketahui beratnya.
2) Setelah terbakar sempurna atau bebas asap, selanjutnya sampel diabukan
di dalam furnace pada suhu 550oC selama 1 jam.
3) Setelah 1 jam, furnace dimatikan dan sampel diambil setelah suhu furnace
sekitar 100oC dan disimpan di dalam desikator selama 15 menit lalu
ditimbang.
4) Kandungan VSS dapat dihitung berdasarkan rumus sebagai berikut:
27
mL sampel, volume
1000 B) -(A volatil/L
rsuspensi padatan te
mg
Keterangan: A = berat residu + cawan porselen sebelum pembakaran, mg
B = berat residu + cawan porselen setelah pembakaran, mg
3.3.1.7Analisis Chemical Oxygen Demand (COD)
Analisis ini dilakukan di luar Departemen Teknik Kimia, Fakultas Teknik,
Universitas Sumatera Utara yaitu di Balai Teknik Kesehatan Lingkungan dan
Pengendalian Penyakit (BTKLPP) Kelas 1 Medan dengan Metode Open Reflux.
Adapun prosedur analisis COD adalah :
1) Dimasukkan 10 ml contoh uji ke dalam erlenmeyer 250 ml.
2) Ditambahkan 0,2 g serbuk raksa (II) sulfat (HgSO4) dan beberapa batu didih.
3) Ditambahkan 5 ml larutan kalium dikromat, (K2Cr2O7) 0,25 N.
4) Ditambahkan 15 ml pereaksi asam sulfat (H2SO4) – perak sulfat (Ag2SO4)
perlahan-lahan sambil didinginkan dalam air pendingin.
5) Dihubungkan dengan pendingin Liebig dan dididihkan di atas hot plate
selama 2 jam.
6) Didinginkan dan dicuci bagian dalam dari pendingin dengan air suling hingga volume contoh uji menjadi lebih kurang 70 ml.
7) Didinginkan sampai temperatur kamar, ditambahkan indikator ferroin 2 sampai dengan 3 tetes, dititrasi dengan larutan ferro ammonium sulfat atau FAS 0,1 N sampai warna merah kecoklatan, dicatat kebutuhan larutan FAS. 8) Langkah 1 sampai dengan 7 dilakukan terhadap air suling sebagai blanko.
Kebutuhan larutan FAS dicatat. Analisis blanko ini sekaligus melakukan pembakuan larutan FAS dan dilakukan setiap penentuan COD.
9) Kandungan COD dapat dihitung berdasarkan rumus sebagai berikut:
sampel ml
N)8000 )(
B A ( O mg/l 2
Keterangan: A = ml FAS untuk titrasi blanko B = ml FAS untuk titrasi sampel N = Normalitas FAS
8000 = berat miliekivalen oksigen 1000 ml/l
(3.5)
28
3.3.2 Loading Up dan Operasi Target
Adapun prosedur loading up dan operasi target adalah:
1) Starter asidogenesis sebanyak 2 L dimasukkan ke dalam fermentor.
2) Bahan baku LCPKS dimasukkan ke dalam tangki umpan.
3) Kecepatan di dalam tangki umpan LCPKS segar diatur hingga kecepatan
150 rpm agar larutan LCPKS akan tercampur dengan baik.
4) Bahan baku LCPKS dialirkan dari tangki umpan ke dalam fermentor.
5) Suhu di dalam fermentor selama proses loading up dan operasi target
dijaga pada suhu 45 oC dengan kecepatan pengadukan pada 250 rpm.
6) HRT awal dimulai dengan HRT 20 hari karena untuk adaptasi hidrolitik bakteri dengan umpan dimasukkan secara bertahap yaitu 2 kali sehari. 7) Setelah 15 hari, percobaan dilanjutkan untuk HRT 15, 10, dan 4.
Dilakukan analisis untuk tiap HRT.
8) pH di dalam fermentor di atur 6 dengan penambahan NaHCO3 hingga pH
yang dinginkan tercapai.
9) Dilakukan analisis untuk setiap run.
3.3.3 Prosedur Recycle
1) Keluaran fermentor (discharge) dipindahkan ke dalam gelas ukur 1000 ml.
2) Keluaran fermentor (discharge) dibiarkan selama 6 jam hingga terjadi
sedimentasi.
3) Bagian yang jernih dipisahkan dengan bagian yang mengendap.
4) Lumpur bagian bawah diambil sesuai variasi sebesar 0%, 15%, 25%
Prosedur dan 35% lalu dikembalikan ke dalam tangki umpan.
3.3.4 Pengujian Sampel (Sampling)
Adapun prosedur yang dilakukan untuk pengujian sampel adalah sama
seperti prosedur yang dilakukan untuk analisis bahan baku, ditambah dengan
analisis VFA, sedangkan analisis gas dilakukan jika pada penelitian ada terbentuk
29
Tabel 3.1 Jadwal Analisis Influent dan Effluent
Analisis Metode Hari ke
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
pH -
M-Alkalinity
Titrasi
TS Analisis
Proksimat
VS Analisis
Proksimat
TSS Analisis
Proksimat
VSS Analisis
Proksimat
COD Open
Reflux
VFA Kromato
grafi
Gas -
Keterangan: = Analisis influent
30
3.4 Jadwal Penelitian
[image:51.842.83.775.175.471.2]Pelaksanaan penelitian direncanakan selama 7 (tujuh) bulan. Jenis kegiatan dan jadual pelaksanaannya dapat dilihat pada Tabel 3.2.
Tabel 3.2 Jenis Kegiatan dan Jadwal Pelaksanaan Penelitian
No
.
Kegiatan Bulan ke 1 Bulan ke-2 Bulan ke-3 Bulan ke-4 Bulan ke-5 Bulan ke-6 Bulan ke-7
1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4
1. Persiapan penelitian
2. Survei dan pembelian
bahan
3. Pelaksanaan
penelitian dan
pengumpulan data
4. Kompilasi data dan
penarikan kesimpulan
5. Penulisan karya
ilmiah
6. Penulisan karya
31
BAB IV
HASIL DAN PEMBAHASAN
4.1 KARAKTERISASI LIMBAH CAIR PABRIK KELAPA SAWIT (LCPKS)
Bahan baku LCPKS yang digunakan dalam penelitian ini berasal dari PKS Adolina PTPN IV. Adapun hasil analisa karakteristik dari bahan baku yang digunakan dapat dilihat pada Tabel 4.1.
Tabel 4.1 Karakteristik LCPKS dari PKS Adolina PTPN IV
No. Parameter Satuan Hasil Uji Metode Uji
1. pH - 3,5 - 4,7 APHA 4500-H
2. Chemical Oxygen Demand (COD)
mg/L 41.818 SNI
3. Total Solid (TS) mg/L 16.040-61.000 APHA 2540B 4. Volatile Solid (VS) mg/L 16.060-52.360 APHA 2540E 5.
6.
Total Suspended Solid (TSS)
Total Suspended Solid (TSS)
mg/L mg/L 2.920-24.700 1.920-25.800 APHA 2540D APHA 2540E 7. 8. 9. 10.
Volatile fatty acids
-Asam asetat -Asam propionat -Asam butirat Lemak Protein Karbohidrat mg/L % % % 1.508,987 560,0297 1.088,613 31,8 0,14 1,99 APHA 2540E Ekstraksi Sokletasi Kjeldah Lane Eynon * Laporan hasil uji laboratorium terlampir
LCPKS merupakan cairan kecoklatan yang kental, koloid dan mengandung padatan tersuspensi. Meskipun LCPKS tidak beracun, tetapi LCPKS memiliki efek buruk terhadap lingkungan. Hal ini dapat dilihat pada Tabel 4.1 dimana pH limbah sangat asam sebesar 3,5-4,7. Sementara menurut Kementerian Lingkungan Hidup dalam Keputusan Menteri Negara Lingkungan Hidup Nomor: KEP 51-/MENLH/10/1995, syarat limbah yang dapat dibuang ke lingkungan yaitu sebesar 6-9 [24].
32
dimana seharusnya yang dizinkan hanya bernilai sebesar 500 mg/L. Tingginya nilai COD ini menunjukkan tingginya kandungan bahan organik yang ada dalam LCPKS sehingga dapat dimanfaatkan sebagai bahan baku pembuatan VFA.
Pada Tabel 4.1 juga dapat dilihat kandungan lemak, protein, dan karbohidrat dari LCPKS yaitu sebesar 31,8%, 0,14% dan 1,99%. Senyawa-senyawa organik inilah yang nantinya akan diolah pada proses asidogenesis menjadi asam-asam lemak rantai pendek yang terkandung didalam VFA.
4.2 HASIL PENELITIAN VARIASI HRT (PROSES LOADING UP) Loading up merupakan langkah penting untuk kelancaran proses digestasi anaerobik. Proses loading up dilakukan dengan memvariasikan HRT yang dimulai dari HRT 20 hari, 15 hari, 10 hari, dan 4 hari. Proses ini dilakukan agar mikroba pada starter dapat beradaptasi. Starter berasal dari kolam pengasaman PTPN III PKS Torgamba. Selama proses loading up, fermentor dioperasikan pada kondisi temperatur 45 oC, pengadukan fermentor sebesar 150 rpm dan pH dijaga konstan pada 6 (±0,2) dengan penambahan natrium bikarbonat (NaHCO3). Analisis pH,
alkalinitas, TS, VS, TSS, VSS, COD serta VFA dilakukan untuk melihat metabolisme dan pertumbuhan mikroba selama proses loading up.
4.2.1 Pengaruh HRT terhadap Profil pH dan Alkalinitas
Sebagai produk dari asidogeneis, VFA bisa bisa berdifusi ke dalam sel bakteri anaerob dan mengionisasi untuk mengurangi pH. Hal ini umumnya diakui sebagai penghambat asidogenesis [43]. Alkalinitas memungkinkan netralisasi VFA yang menyebabkan penurunan pH, sehingga proses asidogenesis dapat berjalan dengan baik [44]. Menurut penelitian Rafael Borja et al [45] pH antara 5,2-5,8 menunjukkan peningkatan produksi asam yang baik saat proses asidogenesis. Oleh sebab itu, pada proses loading up perlu dilakukan pengontrolan pH (6±0,2) agar proses asidogenesis yang diharapkan dapat tercapai. pH LCPKS dijaga stabil dengan dengan penambahan NaHCO3. Pengaruh
33
0 1 2 3 4 5 6 7
0 500 1000 1500 2000 2500 3000 3500 4000 4500
0 5 10 15 20 25 30 35 40 45 50 55 60
pH
Alk
a
lin
it
a
s
(m
g
/L
)
Hari ke-
Alkalinitas pH
[image:54.595.107.516.89.325.2]HRT 20 HRT 15 HRT 10 HRT 4
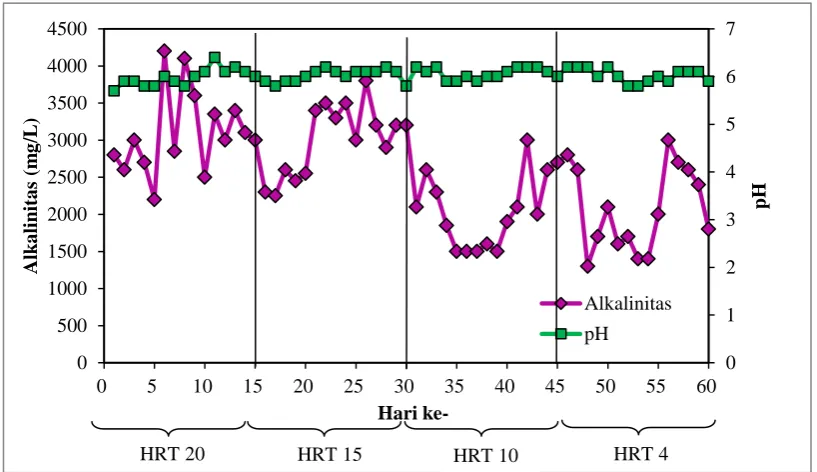
Gambar 4.1 Pengaruh HRT terhadap Profil pH dan Alkalinitas
Pada Gambar 4.1, menunjukkan grafik pH yang relatif konstan diantara 5,8-6,2. Fluktuasi pH disebabkan oleh penambahan umpan segar yang memiliki pH berbeda-beda, sehingga untuk menjaga pH fermentor tetap berada antara 5,8-6,2 dilakukan penambahan NaHCO3.
Nilai alkalinitas yang diperoleh pada HRT 20 hingga HRT 4 berfluktuasi antara 1.300 – 4.200 mg/L. Nilai Alkalinitas yang diperoleh masih dalam rentang yang diizinkan yaitu 2000-4000 mg/L untuk kondisi fermentor yang stabil [46]. Penelitian Kameswari et al [29] memberikan nilai alkalinitas 2000 – 3.500 mg/L yang menunjukkan mikroba beradaptasi dengan baik.
Pada proses loading up penurunan HRT tidak memberikan dampak yang signifikan pada perubahan alkalinitas. Grafik alkalinitas berfluktuasi pada kisaran pH dan alkalinitas asidognesis.
4.2.2 Pengaruh HRT Terhadap Pertumbuhan Mikroba
Proses digestasi dipengaruhi oleh pH, suhu, alkalinitas dan HRT. Kandungan biomassa dipantau dengan mengukur profil VSS effluent fermentor.
![Gambar 2.2 Tahapan proses fermentasi metana [7].](https://thumb-ap.123doks.com/thumbv2/123dok/534966.62064/33.612.147.505.133.423/gambar-tahapan-proses-fermentasi-metana.webp)
![Gambar 2.3 Proses Digestasi Anaerobik Dua Tahap [22]](https://thumb-ap.123doks.com/thumbv2/123dok/534966.62064/36.612.189.463.451.658/gambar-proses-digestasi-anaerobik-dua-tahap.webp)