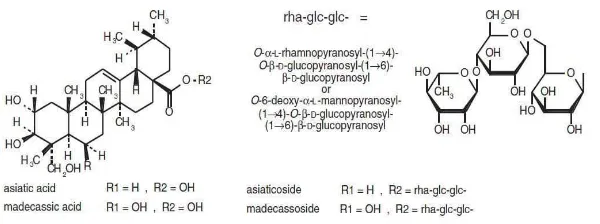EFEKTIVITAS PEMBERIAN EKSTRAK ETHANOL 70 % DAUN KECOMBRANG (Etlingera elatior) TERHADAP LARVA INSTAR III
Aedes aegypti SEBAGAI BIOLARVASIDA POTENSIAL
Oleh : Sulaiman 0918011022
Skripsi
Sebagai Salah Satu Syarat untuk Mencapai Gelar SARJANA KEDOKTERAN
pada
Fakultas Kedokteran Universitas Lampung
FAKULTAS KEDOKTERAN UNIVERSITAS LAMPUNG
ABSTRAK
Efektivitas Pemberian Ekstrak Ethanol 70 % Daun Kecombrang (Etlingera elatior) Terhadap Larva Instar III Aedes aegypti sebagai Biolarvasida Potensial
Oleh
Sulaiman
Penyakit demam berdarah dengue merupakan salah satu masalah kesehatan masyarakat di negara – negara yang memilki iklim tropis, termasuk Indonesia. Penyakit DBD mempunyai perjalanan klinis yang sangat cepat dan sering menyebabkan kematian akibat penanganan yang terlambat. Upaya pengendalian dan pemberantasan terhadap vektor penyakit DBD telah banyak dilakukan. Penggunaan insektisida buatan sebagai larvasida merupakan cara yang paling umum digunakan oleh masyarakat untuk mengendalikan pertumbuhan vektor tersebut. Namun, penggunaan insektisida buatan dapat menimbulkan bahaya bagi kesehatan maupun lingkungan. Bahaya penggunaan insektisida buatan tersebut dapat diminimalisir dengan menggunakan insektisida alami, salah satunya tanaman Kecombrang (Etlingera elatior) . Tanaman Kecombrang memiliki kandungan senyawa aktif yaitu saponin dan flavonoid yang memiliki potensi sebagai larvasida.
Dibagi menjadi 6 kelompok uji yaitu ; 1. kelompok 1 ( kontrel negatif ) 0 % 2. kelompok 2 dengan konsentrasi 0,25 % 3. kelompok 3 dengan konsentrasi 0,5 % 4. kelompok 4 dengan konsentrasi 0,75 % 5. kelompok 5 dengan konsentrasi 1 % 6. kelompok 6 ( kontrol positif ) abate 1 %
Jumlah sampel yang digunakan pada penelitian ini adalah 480 larva. Masing-masing kelompok berisi 20 larva dalam 200 ml larutan yang berisi ekstrak ethanol daun Kecombrang. Pengulangan dilakukan 4 kali dan diberi makanan ikan selama penelitian. Uji yang digunakan adalah uji Kruskal- wallis (p < 0,05), uji Post-hoc Man Whitney (p < 0,05) dan uji Probit untuk mencari nilai LC50 dan LT50.
Hasil penelitian menunjukkan bahwa rata-rata jumlah larva yang mati sebesar 72,50 % pada konsentrasi 0,25 %; 80,00 % pada kosentrasi 0,5 %; 93,50 % pada konsentrasi 0,75 % dan 100 % pada konsentrasi 1 %. Berdasarkan hasil tersebut konsentrasi yang paling efektif yaitu konsentrasi 1 % karena daya bunuhnya lebih cepat dan jumlah kematiannya sama dengan abate 1 %. Nilai LC50 adalah 4,38 % di menit ke-20; 1,64 % menit ke-40; 1,04 % menit ke60; 0,82 % menit ke-120; 0,67 % menit ke-240; 0,56 % menit ke-480; 0,47 % di menit ke-1440; 0,27 % di menit ke-2880 dan 0,15 % pada menit ke-4320 . Nilai LT50 adalah 290,2 menit pada konsentrasi 0,75 % dan 148,2 menit pada konsentrasi 1 %.
i
4. Kandungan kimia dalam tanaman kecombrang ... 21
ii
F. Definisi Operasional variabel ... 35
G. Prosedur Penelitian ... 36
1. Tahap Persiapan ... 36
a. Sterilisasi alat ... 36
b. Persiapan sampel ... 37
c. Persiapan ekstrak daun kecombrang ... 37
I. PENDAHULUAN
A. Latar Belakang
Sejak tahun 1968 hingga tahun 2009, World Health Organization (WHO) mencatat negara Indonesia sebagai negara dengan kasus DBD tertinggi di Asia Tenggara. Di Indonesia, kasus DBD pertama kali ditemukan di kota Surabaya pada tahun 1968, sebanyak 58 orang terinfeksi dan 24 orang meninggal dunia. Sejak saat itu, penyakit ini menyebar luas ke seluruh Indonesia. Sampai akhir tahun 2008 juga belum ditemukan obat yang secara efektif dapa tmengobati penyakit DBD (Depkes RI, 2010). Berdasarkan data Dinas Kesehatan kota Bandar Lampung Januari hingga 14 Februari 2012, ditemukan 440 kasus Demam Berdarah Dengue di puskesmas dan rumah sakit kota Bandar Lampung dengan korban meninggal dunia sebanyak empat orang (Tribun Lampung, 2012).
Pemberantasan larva merupakan salah satu pengendalian vektor Aedes aegypti yang diterapkan hampir diseluruh dunia. Penggunaan insektisida sebagai larvasida merupakan cara yang paling umum digunakan oleh masyarakat untuk mengendalikan pertumbuhan vektor tersebut. Insektisida yang sering digunakan di Indonesia adalah Abate. Penggunaan abate di Indonesia sudah ada sejak tahun 1976. Empat tahun kemudian yakni tahun 1980, temephos 1% (abate) ditetapkan sebagai bagian dari program pemberantasan massal Aedes aegypti di Indonesia (Daniel, 2008).
Penggunaan insektisida kimiawi yang berulang akan menimbulkan dampak kontaminasi residu pestisida dalam air, terutama air minum. Selain itu, Biaya yang tinggi dari penggunaan pestisida kimiawi dan munculnya resistensi dari berbagai macam spesies nyamuk yang menjadi vektor penyakit menjadi perhatian penting yang harus dicermati (Ndione RD, 2007). Laporan resistensi larva Aedes aegypti terhadap Temephos sudah ditemukan di beberapa negara seperti Brazil, Bolivia, Argentina, Kuba, French Polynesia, Karibia, dan Thailand.Selain itu juga telah dilaporkan resistensi larva Aedes aegypti terhadap temephos di Surabaya (Raharjo B, 2006).
aktivitas makan dan peneluran, pengatur pertumbuhan dan perkembangan serangga, kematian/mortalitas, dan sebagainya; serta memenuhi syarat-syarat untuk digunakan dalam pengendalian vektor, seperti efektif, efisien, dan aman (Dadang dan Prijono, 2008).
Indonesia merupakan Negara tropis yang memiliki banyak jenis tumbuhan yang memiliki potensi sebagai insektisida alami. Menurut Arnason et al. (1993) dalam Syahputra (2001), famili tumbuhan yang dianggap sebagai sumber potensial insektisida nabati adalah Meliaceae, Annonaceae, Asteraceae, Piperaceae, dan Rutaceae. Namun hal ini tidak menutup kemungkinan untuk ditemukannya famili tumbuhan yang baru. Salah satu tanaman yang dianggap memiliki potensi insektisida adalah Kecombrang (Etlingera elatior). Kecombrang mengandung senyawa flavonoid dan saponin. Selain itu, kecombrang juga mengandung polifenol dan minyak atrisi (Sitanggang dkk, 2008).
Penelitian yang dilakukan oleh Novitha tahun 2012 mengenai efek ekstrak Batang Kecombrang sebagai larvasida menunjukan bahwa terdapat efek ekstrak batang Kecombrang (Etlingera elatior) sebagai larvasida terhadap larva Aedes aegypti instar III. Berdasarkan penelitian tersebut diketahui bahwa kematian larva dimulai dari menit ke-40 pada konsentrasi 0,75% dengan rerata kematian larva sebesar 6,25%. Kematian larva uji pada konsentrasi 0,75% terus berlanjut hingga mencapai 100% pada menit ke-2880 dengan nilai LT50 259,06 menit dan LC50 0,569%. Pada konsentrasi 1% kematian larva dimulai pada menit ke-20 dengan persentase rerata kematian larva uji sebesar 2,5%. Kematian larva uji terus berlanjut hingga mencapai 100% pada konsentrasi 1% di menit ke-240 dengan nilai LT50 158,34 menit dan LC50 0,634%.
B. Rumusan masalah
Deman berdarah dengue ( DBD) atau Dengue Hemorrhagic Fever (DHF) adalah penyakit virus yang ditularkan melalui Nyamuk Aedes aegypti sangat berbahaya karena dapat menyebabkan penderita meninggal dalam waktu sangat singkat. Nyamuk Aedes aegypti mempunyai siklus hidup mulai dari telur, larva, pupa, dan dewasa. Salah satu pencegahan penyebaran DBD dapat dilakukan dengan memberantas vektor penyebabnya atau memutuskan siklus hidupnya dengan larvasida.
sehingga dinding traktus digestivus pada larva menjadi korosif dan menyebabkan kematian pada larva.
Berdasarkan latar belakang di atas, peneliti dapat merumuskan masalah sebagai berikut :
Apakah ada efek ekstrak ethanol 70% daun kecombrang (Etlingera elatior) sebagai biolarvasida Aedes aegypti instar III.
C. Tujuan penelitian
1. Tujuan umum
Untuk mengetahui efektifitas ekstrak ethanol 70% daun kecombrang (Etlingera elatior) sebagai biolarvasida Aedes aegypti Instar III.
2. Tujuan khusus
a. Mengetahui konsentrasi yang paling efektif dari ekstak ethanol 70% daun kecombrang (Etlingera elatior ) sebagai biolarvasida Aedes aegypti instar III.
b. Mengetahui Lethal Time 50 % (LT50) ekstrak daun Kecombrang (Etlingera elatior) sebagai biolarvasida terhadap larva Aedes aegypti instar III.
D. Manfaat penelitian
Dari penelitian yang dilakukan diharapkan penelitian ini dapat bermanfaat bagi :
1. Peneliti
Dapat meningkatkan pengetahuan tentang efektifitas ektrak ethanol 70% daun kecombrang (Etlingera elatior) sebagai biolarvasida Aedes aegypti instar III.
2. Institusi pendidikan
Dapat menambah wawasan dan sebagai sumber informasi ilmiah untuk pembaca dan untuk penelitian selanjutnya.
3. Masyarakat
E. Kerangka Penelitian
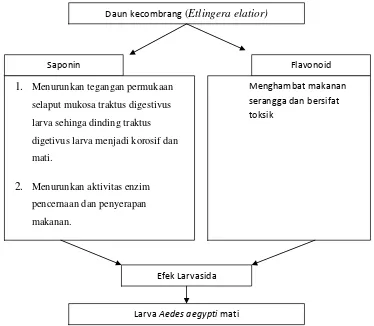
1. Kerangka teori
Gambar 1. Kerangka teori
(Etlingera elatior)
1. Menurunkan tegangan permukaan selaput mukosa traktus digestivus
larva sehinga dinding traktus
digetivus larva menjadi korosif dan
mati.
2. Menurunkan aktivitas enzim pencernaan dan penyerapan
makanan
!
"! #
$
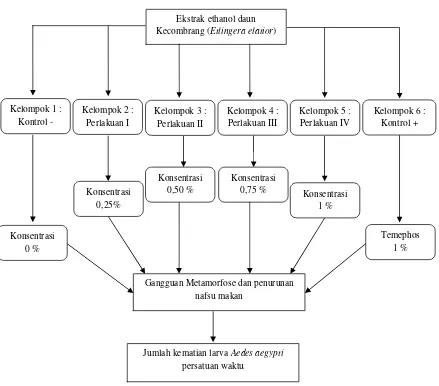
2. Kerangka konsep
Gambar 2. Kerangka konsep
F. Hipotesis
Hipotesis dalam penelitian ini adalah ekstrak ethanol 70% daun kecombrang (Etlingera elatior) efektif sebagai Biolarvasida Aedes aegypti instar III.
Gangguan Metamorfose dan penurunan nafsu makan
II. TINJAUAN PUSTAKA
A. Nyamuk Aedes aegypti
1. Taksonomi Aedes aegypti
Urutan klasifikasi dari nyamuk Aedes aegypti adalah sebagai berikut:
Kingdom : Animalia
Phylum : Arthropoda
Subphylum : Uniramia
Kelas : Insekta
Ordo : Diptera
Subordo : Nematosera
Familia : Culicidae
Sub family : Culicinae
Tribus : Culicini
Genus : Aedes
Spesies : Aedes aegypti
2. Morfologi Aedes aegypti
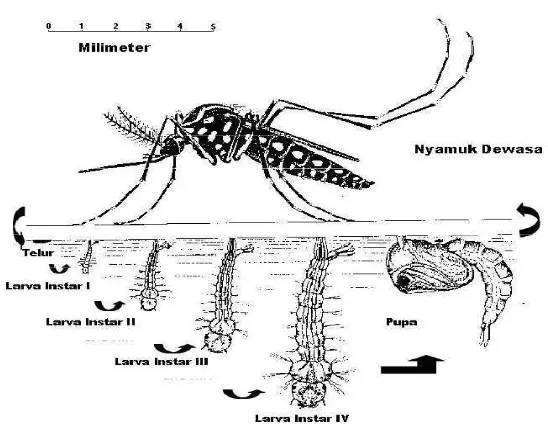
Aedes aegypti mengalami metamorfosis sempurna, yaitu mengalami
perubahan bentuk morfologi selama hidupnya dari stadium telur berubah
menjadi stadium larva kemudian menjadi stadium pupa dan menjadi
stadium dewasa.
Gambar 3. Daur HidupAedes aegypti
(sumber : Aminah, NS. dkk, 2001)
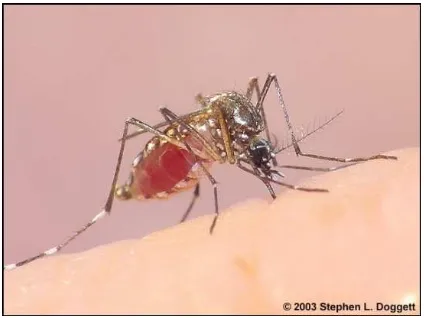
Aedes aegypti dewasa berukuran lebih kecil jika dibandingkan dengan
ukuran nyamuk rumah (Culex quinquefasciatus), mempunyai warna dasar
yang hitam dengan bintik putih pada bagian badannya terutama pada
a. Stadium telur Aedes aegypti
Seekor nyamuk betina rata-rata dapat menghasilkan 100 butir telur
setiap kali bertelur dan akan menetas menjadi larva dalam waktu 2 hari
dalam keadaan telur terendam air. Telur Aedes aegypti berwarna hitam,
berbentuk ovale, kulit tampak garis-garis yang menyerupai sarang
lebah, panjang 0,80mm, berat 0,0010-0,015 mg. Telur Aedes aegypti
dapat bertahan dalam waktu yang lama pada keadaan kering. Hal
tersebut dapat membantu kelangsungan hidup spesies selama kondisi
iklim yang tidak memungkinkan (Depkes RI, 2007).
Pada umumnya nyamuk Aedes aegypti akan meletakan telurnya pada
suhu sekitar 20° sampai 30°C. Pada suhu 30°C, telur akan menetas
setelah 1 sampai 3 hari dan pada suhu 16°C akan menetas dalam waktu
7 hari. Telur nyamuk Aedes aegypti sangat tahan terhadap kekeringan
(Sudarmaja JM dan Mardihusodo, 2009).
Pada kondisi normal, telur Aedes aegypti yang direndam di dalam air
akan menetas sebanyak 80% pada hari pertama dan 95% pada hari
kedua. Berdasarkan jenis kelaminnya, nyamuk jantan akan menetas
lebih cepat dibanding nyamuk betina, serta lebih cepat menjadi dewasa.
Faktor-faktor yang mempengaruhi daya tetas telur adalah suhu, pH air
perindukkan, cahaya, serta kelembaban disamping fertilitas telur itu
Gambar 4. Telur Aedes aegypti ( Sumber : entnemdept.ufl.edu )
b. Stadium Larva Aedes aegypti
Larva nyamuk Aedes aegypti selama perkembangannya mengalami 4
kali pergantian kulit larva instar I memiliki panjang 1-2 mm, tubuh
transparan, siphon masih transparan, tumbuh menjadi larva instar II
dalam 1 hari. Larva intar II memiliki panjang 2,5 – 3,9 mm, siphon
agak kecoklatan, tumbuh menjadi larva instar III selama 1-2 hari. Larva
instar III berukuran panjang 4-5 mm, siphon sudah berwarna coklat,
tumbuh menjadi larva instar IV selama 2 hari. Larva instar IV
berukuran 5-7 mmm sudah terlihat sepasang mata dan sepasang antena,
tumbuh menjadi pupa dalam 2-3 hari. Umur rata-rata pertumbuhan
larva hingga pupa berkisar 5-8 hari. Posisi istirahat pada larva ini
adalah membentuk sudut 450 terhadap bidang permukaan air
Gambar 5. Larva Aedes aegypti
(Sumber : Dept. Entomology ICPMR 2002)
c. Stadium Pupa Aedes aegypti
Pada stadium pupa tubuh terdiri dari dua bagian, yaitu cephalothorax
yang lebih besar dan abdomen. Bentuk tubuh membengkok. Pupa tidak
memerlukan makan dan akan berubah menjadi dewasa dalam 2 hari.
Dalam pertumbuhannya terjadi proses pembentukan sayap, kaki dan
alat kelamin (Depkes RI, 2007).
Gambar 6. Pupa Aedes aegypti
d. Nyamuk dewasa Aedes aegypti
Tubuh nyamuk dewasa terdiri dari 3 bagian, yatu kepala (caput), dada
(thorax) dan perut (abdomen). Badan nyamuk berwarna hitam dan
memiliki bercak dan garis-garis putih dan tampak sangat jelas pada
bagian kaki dari nyamuk Aedes aegypti. tubuh nyamuk dewasa
memiliki panjang 5 mm. Pada bagian kepala terpasang sepasang mata
majemuk, sepasang antena dan sepasang palpi, antena berfungsi sebagai
organ peraba dan pembau. Pada nyamuk betina, antena berbulu pendek
dan jarang (tipe pilose). Sedangkan pada nyamuk jantan, antena berbulu
panjang dan lebat (tipe plumose). Thorax terdiri dari 3 ruas, yaitu
prothorax, mesotorax, dan methatorax. Pada bagian thorax terdapat 3
pasang kaki dan pada ruas ke 2 (mesothorax) terdapat sepasang sayap.
Abdomen terdiri dari 8 ruas dengan bercak putih keperakan pada
masing-masing ruas. Pada ujung atau ruas terakhir terdapat alat
kopulasi berupa cerci pada nyamuk betina dan hypogeum pada nyamuk
jantan (Depkes RI, 2007).
Nyamuk jantan dan betina dewasa perbandingan 1:1, nyamuk jantan
keluar terlebih dahulu dari kepompong, baru disusul nyamuk betina,
dan nyamuk jantan tersebut akan tetap tinggal di dekat sarang, sampai
nyamuk betina keluar dari kepompong, setelah jenis betina keluar,
maka nyamuk jantan akan langsung mengawini betina sebelum mencari
Pada nyamuk betina, bagian mulutnya mempunyai probosis panjang
untuk menembus kulit dan penghisap darah. Sedangkan pada nyamuk
jantan, probosisnya berfungsi sebagai pengisap sari bunga atau
tumbuhan yang mengandung gula. Nyamuk Aedes aegypti betina
umumnya lebih suka menghisap darah manusia karena memerlukan
protein yang terkandung dalam darah untuk pembentukan telur agar
dapat menetas jika dibuahi oleh nyamuk jantan. Setelah dibuahi
nyamuk betina akan mencari tempat hinggap di tempat tempat yang
agak gelap dan lembab sambil menunggu pembentukan telurnya,
setelah menetas telurnya diletakkan pada tempat yang lembab dan
basah seperti di dinding bak mandi, kelambu, dan kaleng-kaleng bekas
yang digenangi air (Hoedojo R dan Zulhasril, 2008).
Gambar 7. Aedes aegypti dewasa
Tempat pembangkitan tersebut berupa :
1) Tempat penampungan air (TPA) yaitu tempat menampung air guna
keperluan sehari-hari seperti drum, tempayan, bak mandi, bak WC
dan ember.
2) Bukan tempat penampungan air (non TPA) yaitu tempat-tempat
yang biasa digunakan untuk menampung air tetapi bukan untuk
keperluan sehari-hari seperti tempat minum hewan piaraan, kaleng
bekas, ban bekas, botol, pecahan gelas, vas bunga dan perangkap
semut.
3) Tempat penampungan air alami (TPA alami) seperti lubang pohon,
lubang batu, pelepah daun, tempurung kelapa, kulit kerang, pangkal
pohon pisang dan potongan bambu.
3. Pengendalian vektor
Pengendalian nyamuk dapat dibagi menjadi tiga yaitu :
1. Pengendalian secara mekanik
Cara ini dapat dilakukan dengan mengubur kaleng-kaleng bekas atau
tempat-tempat sejenis yang dapat menampung air hujan dan
membersihkan lingkungan yang berpotensial dijadikan sebagai sarang
nyamuk Aedes aegypti misalnya got dan potongan bambu.
Pengendalian mekanis lain yang dapat dilakukan adalah pemasangan
kelambu dan pemasangan perangkap nyamuk baik menggunakan
2. Pengendalian secara biologis
Intervensi yang didasarkan pada pengenalan organisme pemangsa,
parasit, pesaing untuk menurunkan jumlah Aedes aegypti.
Pengendalian ini biasa dilakukan dengan memelihara ikan yang
relative kuat dan tahan, misalnya ikan mujaer di bak atau tempat
penampungan air lainnya sehingga sebagai predator bagi jentik dan
pupa.
3. Pengendalian secara kimia
Penggunaan insektisida secara sembarangan untuk pencegahan dan
pengontrolan infeksi dengue harus dihindari. Selama periode sedikit
atau tidak ada aktifitas virus dengue, tindakan reduksi sumber secara
rutin yang diuraikan dalam bagian metode pelaksana lingkungan dapat
dipadukan dengan penggunaan larvasida dalam wadah yang tidak
dapat dibuang di tutup, diisi atau ditangani dengan cara lain. Untuk
pengendalian emergensi menekan epidemik virus dengue atau untuk
mencegah ancaman wabah, suatu program penghancuran yang tepat
B.Kecombrang (Etlingera elatior)
1. Klasifikasi
Urutan Klasifikasi tanaman Kecombrang (Etlingera elatior) adalah
sebagai berikut :
Kingdom : Plantae
Subkingdom : Tracheobionta
Super Divisi : Spermatophyta
Divisi : Magnoliophyta
Kelas : Liliopsida
Sub Kelas : Commelinidae
Ordo : Zingiberales
Famili : Zingiberaceae
Genus : Etlingera
Spesies : Etlingera elatior
2. Morfologi kecombrang (Etlingera elatior)
Kecombrang termasuk dalam famili Zingiberaceae. Tanaman
kecombrang (Etlingera elatior) merupakan tanaman tahunan yang
berbentuk semak dengan tinggi 1-3 m. Tanaman ini mempunyai batang
semu, tegak, berpelepah, membentuk rimpang, dan berwarna hijau.
Daunnya tunggal, lanset, ujung dan pangkal runcing tetapi rata,
panjang daun sekitar 20-30 cm dan lebar 5-15 cm, pertulangan daun
menyirip, dan berwarna hijau. Bunga kecombrang merupakan bunga
majemuk yang berbentuk bongkol dengan panjang tangkai 40-80 cm.
Panjang benang sari ± 7,5 cm dan berwarna kuning. Putiknya kecil dan
putih. Mahkota bunganya bertaju, berbulu jarang dan warnanya merah
jambu. Biji kecombrang berbentuk kotak atau bulat telur dengan warna
putih atau merah jambu. Buahnya kecil dan berwarna coklat. Daunnya
berbentuk serabut dan berwarna kuning gelap (DepKes, 2005).
Gambar 8. Tumbuhan Kecombrang (Etlingera elatior)
3. Manfaat Kecombrang
Menurut Hasbah dkk. (2005) tanaman kecombrang dapat dipakai
untuk mengobati penyakit-penyakit yang tergolong berat yaitu kanker
dan tumor. Bunga dari tanaman ini bisa digunakan sebagai bahan
kosmetik alami dimana bunganya dipakai untuk campuran cairan
pencuci rambut dan daun serta rimpangnya dipakai untuk bahan
campuran bedak oleh penduduk lokal (Chan dkk, 2007).
Di Malaysia, bunga kecombrang direbus. Air rebusannya dijadikan
untuk obat sakit telinga. Sedangkan daun kecombrang digunakan
untuk pencuci luka. Selain bunganya, daun muda kecombrang juga
berkhasiat menghilangkan bau badan. Juga berkhasiat memperbanyak
air susu ibu. Honje, nama lain kecombrang, dapat dimanfaatkan
sebagai sabun dengan dua cara yaitu mengosokkan langsung batang
pohon honje ke tubuh dan wajah atau dengan mememarkan pelepah
batang daun honje hingga keluar busa yang harum yang dapat
langsung digunakan sebagai sabun. Tumbuhan ini juga dapat
digunakan sebagai obat untuk penyakit yang berhubungan dengan
kulit, termasuk campak. Bunga pokok ini yang berwarna merah muda
banyak digunakan sebagai gubahan hiasan manakala tunas bunga ini
dijadikan bahan memasak dalam masakan Melayu seperti laksa.
Tumbuhan ini mengandung banyak bahan antioksidan yang amat baik
4. Kandungan kimia dalam tanaman kecombrang
Kandungan bahan aktif yang terdapat dalam tanaman adalah saponin,
flavonoid, polifenol dan minyak atsiri (Warta, 2008).
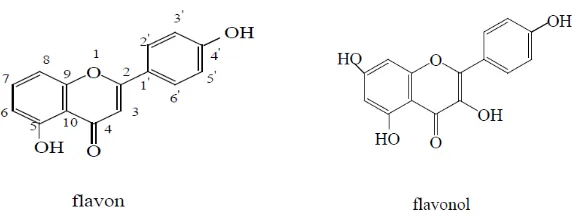
1. Flavonoid
Flavonoid merupakan senyawa metabolit sekunder yang terdapat
pada tanaman hijau, kecuali alga. Flavonoid merupakan termasuk
senyawa fenolik alam yang potensial sebagai antioksidan dan
mempunyai bioaktifitas sebagai obat.
Beberapa fungsi flavonoid bagi tumbuhan adalah pengaturan
tumbuh, pengaturan fotosintesis, kerja antimikroba dan antivirus,
fitoaleksin merupakan komponen abnormal yang hanya dibentuk
sebagai tanggapan terhadap infeksi atau luka dan kemudian
menghambat fungus menyerangnya, mengimbas gen pembintilan
dalam bakteria bintil nitrogen (Yunilda D, 2011).
Flavonoid dapat dikelompokkan berdasarkan rantai C3 yaitu :
a. Katekin dan proantosianidin
Katekin dan proantosianidin adalah dua golongan senyawa
yang mempunyai banyak kesamaan, terdapat pada tumbuhan
kayu. Katekin ditemukan dalam paku-pakuan dan dua spesies
Equisetum. Tiga jenis katekin yaitu katekin (+) dan katekin (-)
hidrogen-2 dan hidrogen-3 nya trans. Beberapa katekin terdapat
sebagai ester asam galat. Proantosianidin adalah senyawa yang
b. Flavanon dan flavanonol
Berwarna kuning sedikit karena kosentrasinya rendah.
Flavanon sering terjadi sebagai aglikon tetapi beberapa
glikosidanya dikenal sebagai hesperidin dan naragin dari kulit
jeruk. Flavononol merupakan flavonoid yang paling kurang
dikenal, senyawa ini stabil dalam asam klorida panas tetapi
terurai oleh basa hangat menjadi kalkon. Menurut Dinata
(2009). Flavonoid merupakan senyawa pertahanan tumbuhan
yang dapat bersifat menghambat makan serangga dan juga
bersifat toksik.
Gambar 9. Rumus bangun flafon dan flavonol (sumber: http//: repository.usu.ac.id)
2. Saponin
Saponin merupakan senyawa glikosida triterpenoida atau glikosida
Steroida yang merupakan senyawa aktif permukaan dan bersifat
seperti sabun serta dapat dideteksi berdasarkan kemampuannya
membentuk busa dan menghemolisa sel darah merah
( Harborne JB, 1996 ). Keberadaan saponin sangat dapat ditandai
dikocok menimbulkan buih yang stabil. Saponin merupakan
senyawa berasa pahit menusuk dan dapat menyebabkan bersin dan
bersifat racun bagi hewan berdarah dingin, banyak di antaranya
digunakan sebagai racun ikan (Gunawan D dan Mulyani S, 2004).
Menurut Nio (1989). Sifat-sifat saponin adalah sebagai berikut :
1. Mempunyai rasa pahit.
2. Dalam larutan air membentuk busa yang stabil.
3. Menghemolisa eritrosit.
4. Merupakan racun kuat untuk ikan dan amfibi.
5. Membentuk persenyawaan dengan kolesterol dan
hidroksisteroid lainnya.
6. Sulit untuk dimurnikan dan diidentifikasi.
7. Berat molekul relatif tinggi, dan analisis hanya menghasilkan
formula empiris yang mendekati.
Berdasarkan struktur aglikonnya, saponin dibedakan menjadi dua
tipe, yaitu tipe steroida dan tipe triterpenoida.
a. Steroida
Saponin steroida terdapat pada tumbuhan monokotil maupun
dikotil, contohnya diosgenin yang terdapat pada Dioscorea
hispida dan hecogenin yang terdapat pada Agave americana
b. Triterenoida
Saponin triterpenoida banyak terdapat pada tumbuhan dikotil
seperti: gipsogenin terdapat pada Gypsophylla sp. dan asam
glisiretat terdapat pada Glycyrrhiza glabra (Gunawan dan
Mulyani, 2004).
Saponin memiliki aksi sebagai insektida dan larvasida. Saponin
dapat menurunkan tegangan permukaan selaput mukosa traktus
digestivus larva sehinga dinding traktus digetivus larva menjadi
korosif (Aminah dkk, 2001). Saponin yang terdapat dalam
makanan yang dikonsumsi serangga dapat menurunkan aktivitas
enzim pencernaan dan penyerapan makanan (Dinata A, 2009).
Gambar 10. Rumus Bangun Saponin
( sumber: http//: repository.usu.ac.id )
3. Minyak atrisi
Minyak atsiri merupakan salah satu senyawa metabolit sekunder
yang mudah menguap (volatil) dan bukan merupakan senyawa
berasal dari golongan terpenoid (Guenther E, 2006). Minyak atsiri
terdiri dari campuran zat yang mudah menguap dengan komposisi
dan titik didih yang berbeda beda. Minyak atsiri yang mudah
menguap terdapat dalam kelenjar minyak khusus didalam kantung
minyak atau di dalam ruang antar sel dalam jaringan tanaman.
Minyak atrisi umumnya terdiri dari berbagai campuran
persenyawaan kimia yang terbentuk dari unsur carbon
( C ), Hidrogen ( H ), Oksigen ( O ) dan beberapa senyawa kimia
yang mengandung unsur Nitrogen ( N ) dan Belerang ( S )
(Guenther E, 2006).
C.Ekstrak
Bioaktifitas tanaman sangat dipengaruhi oleh kandungan senyawa kimia
yang terdapat didalamnya. Sedangkan untuk mendapatkan senyawa kimia
yang bersifat aktif tersebut dipengaruhi oleh metode pemisahan meliputi
cara ekstraksi dan pelarut yang digunakan. Perbedaan kandungan senyawa
kimia yang ada menunjukkan perbedaan aktifitas farmakologis dari
tanaman yang bersangkutan (Halimah, 2010).
Tujuan ekstraksi adalah untuk menarik dan memisahkan senyawa yang
mempunyai kelarutan berbeda–beda dalam berbagai pelarut komponen
kimia yang terdapat dalam bahan alam baik dari tumbuhan, hewan, dan
biota laut dengan menggunakan pelarut organik tertentu. Proses ekstraksi
sel dan masuk ke dalam rongga sel secara osmosis yang mengandung zat
aktif Zat aktif akan larut dalam pelarut organik dan karena adanya
perbedaan konsentrasi antara di dalam dan di luar sel, mengakibatkan
terjadinya difusi pelarut organik yang mengandung zat aktif keluar sel.
Proses ini berlangsung terus menerus sampai terjadi keseimbangan
konsentrasi zat aktif di dalam dan di luar sel (Dirjen POM, 2000 dan
Harborne 1987). Metode ekstraksi menggunakan pelarut dapat dilakukan
secara dingin yaitu maserasi dan perkolasi, dan secara panas yaitu refluks,
soxhlet, digesti, infus, dan dekok (Dirjen POM, 2000).
Metode maserasi merupakan cara penyarian yang sederhana. Maserasi
dilakukan dengan cara merendam serbuk simplisia dalam cairan penyari.
Cairan penyari akan menembus dinding sel dan masuk ke dalam rongga
sel yang mengandung zat aktif, zat aktif akan larut dan karena adanya
perbedaan konsentrasi antara larutan zat aktif di dalam sel dengan yang
diluar sel, maka larutan yang terpekat di desak keluar. Peristiwa tersebut
berulang sehingga terjadi keseimbangan konsentrasi antara larutan diluar
sel dan didalam sel. Maserasi digunakan untuk penyarian simplisia yang
mengandung zat aktif yang mudah larut dalam cairan penyari, tidak
mengandung zat yang mudah mengembang dalam cairan penyari, tidak
mengandung benzoin, stiraks dan lain-lain. Keuntungan cara penyarian
dengan maserasi adalah cara pengerjaan dan peralatan yang digunakan
Cairan penyari yang digunakan dapat berupa air, ethanol, air-ethanol atau
pelarut lain. Bila cairan penyari digunakan air maka untuk mencegah
timbulnya kapang, dapat ditambahkan bahan pengawet, yang diberikan
pada awal penyarian. Maserasi pada umumnya dilakukan dengan cara
memasukkan 10 bagian simplisia dengan derajat halus yang cocok
kedalam sebuah bejana, ditambahkan dengan 75 bagian penyari, dan
ditutup, serta dibiarkan selama 5 hari, terlindung dari cahaya sambil
sekali-kali diaduk. Setelah 5 hari sari diserkai, ampas diperas. Ampas
ditambah cairan penyari secukupnya kemudian diaduk dan diserkai,
sehingga diperoleh seluruh sari sebanyak 100 bagian. Bejana kemudian
ditutup dan dibiarkan ditempat sejuk, terlindung dari cahaya, selama 2
hari. Kemudian endapan dipisahkan (Dirjen POM, 2000).
Pada penyarian dengan cara maserasi, perlu dilakukan pengadukan.
Pengadukan diperlukan untuk meratakan konsentrasi larutan di luar butir
serbuk simplisia, sehingga dengan pengadukan tersebut tetap terjaga
adanya derajat perbedaan konsentrasi yang sekecil-kecilnya antara larutan
di dalam sel dengan larutan di luar sel. Hasil penyarian dengan cara
maserasi perlu dibiarkan selama waktu tertentu. Waktu tersebut diperlukan
untuk mengendapkan zat-zat yang tidak diperlukan tetapi ikut terlarut
Adapun metode ekstraksi yang dapat digunakan selain maserasi adalah:
1) Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
sempurna (exhaustive extraction) yang umumnya dilakukan pada
temperatur ruangan. Proses terdiri dari tahapan pengembangan bahan,
tahap maserasi antara, tahap perkolasi sebenarnya (penetapan atau
penampungan ekstrak) yang jumlahnya 1–5 bahan.
2) Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya,
selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan
dengan adanya pendingin balik. Umumnya dilakukan pengulangan
proses pada residu pertama sampai 3–5 kali sehingga dapat termasuk
proses ekstraksi sempurna.
3) Soxhlet
Soxhlet adalah ekstraksi menggunakan pelarut yang selalu baru yang
umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi
kontinyu dengan jumlah pelarut relatif konstan dengan adanya
pendingin balik.
4) Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinyu) pada
temperatur yang lebih tinggi dari temperatur ruangan (kamar), yaitu
5) Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas air
(bejana infus tercelup dalam penangas air mendidih, temperatur terukur
96–980C) selama waktu tertentu 15–20 menit.
6) Dekok
Dekok adalah infus pada waktu yang lebih lama (>300C) dan
III. METODE PENELITIAN
A. Rancangan Penelitian
Penelitian ini menggunakan metode eksperimental laboratorium
dengan Rancangan Acak Lengkap (RAL) atau completely randomized
design yang terdiri dari 4 perlakuan dan 2 kontrol, yaitu positif dan
negatif dengan pengulangan sebanyak 4 kali. Rancangan Acak
Lengkap merupakan jenis rancangan percobaan yang paling sederhana.
Metode ini dipilih karena satuan percobaan yang digunakan bersifat
homogen atau tidak ada faktor lain yang mempengaruhi respon di luar
faktor yang diteliti.
B. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan di Laboratorium Parasitologi Fakultas
Kedokteran Univeritas Lampung, prosedur uji efektivitas larvasida di
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas
Lampung, proses ekstraksi daun kecombrang (Etlingera elatior).
C. Populasi dan Sampel
1. Populasi
Populasi yang digunakan dalam penelitian ini adalah larva instar
III Aedes aegypti yang diperoleh dari dari Loka Litbang P2B2
Ciamis dalam bentuk kering dengan media kertas saring. Untuk
memudahkan dalam penentuan sampel maka dipakai kriteria
inklusi dan ekslusi sebagai berikut :
a. Kriteria Inklusi
1) Larva Aedes aegypti yang telah mencapai instar III
2) Larva bergerak aktif
b. Kriteria Eksklusi
1) Larva Aedes aegypti instar I dan II
2) Larva yang sudah mati sebelum pengujian
3) Larva yang telah berubah menjadi pupa atau nyamuk
dewasa
4) Bukan larva bebas
2. Sampel
Menurut Wulandari et al (2006) larva pada tahap instar III dipakai
sebagai bahan penelitian karena tahap ini dianggap cukup mewakili
kondisi larva. Ukuran larva instar III tidak terlalu kecil sehingga
mudah untuk diamati dan larva ini merupakan bentuk yang aktif
mencari makan. Menurut acuan WHO tahun 2005 besar sampel
instar III untuk masing-masing perlakuan dengan pengulangan
sebanyak 4 kali untuk setiap perlakuan. Pada penelitian ini, besar
sampel adalah 20 ekor larva dengan 4 kali pengulangan sehingga
pada penelitian ini diperlukan total sampel sebanyak 480 larva.
Adapun rincian sampel yang digunakan adalah sebagai berikut :
Perlakuan Jumlah larva (ekor) x jumlah
pengulangan Total (ekor)
Kontrol (-) : 0% 20 larva x 4 80 larva
Perlakuan I : 0,25% 20 larva x 4 80 larva
Perlakuan II : 0,50%
20 larva x 4 80 larva
Perlakuan III : 0,75%
20 larva x 4 80 larva
Perlakuan IV : 1% 20 larva x 4 80 larva
Kontrol (+) : Temephos 1% abate 20 larva x 4 80 larva
Jumlah total larva yang
dipakai dalam penelitian 480 larva
D. Alat dan Bahan
1. Alat
Adapun Alat-alat yang digunakan dalam penelitian ini adalah
sebagai beriku :
a. Alat Untuk Preparasi Bahan Uji
1. Nampan plastik dengan ukuran 30 x 15 cm
2. Kain kasa
3. Gelas plastik
4. Sangkar nyamuk berukuran 40 x 40 x 40 cm
b. Alat Untuk Pembuatan Larutan Uji
1. Neraca analitik ( timbangan )
2. Blender
3. Toples
4. Baskom
5. Saringan
c. Alat Untuk Uji Efektifitas
1. Pipet larva
2. Pipet tetes
3. Daun pengaduk
4. Gelas ukur 250 ml
5. Kontainer atau gelas plastik
2. Bahan
Adapun Bahan yang digunakan pada penelitian ini adalah sebagai
berikut :
a. Daun kecombrang (Etlingera elatior)
b. Larva Aedes aegypti instar III
c. larutan ethanol 70 %
d. Temephos 1% (abate)
e. aquadest
f. Fish food untuk makanan larva
E. Identifikasi Variabel
1. Identifikasi Variabel
Variabel pada penelitian ini terdiri atas :
a. Variabel Bebas
Variabel bebas atau independent variable penelitian ini adalah
berbagai konsentrasi ekstrak daun Kecombrang (Etlingera
elatior) dengan lima level konsentrasi yaitu 0%, 0,25%, 0,5%,
0,75% dan 1% dan larva Aedes aegypti instar III.
b. Variabel Terikat
Variabel terikat atau dependent variable penelitian ini adalah
level konsentrasi yang paling efektif untuk kematian larva
Aedes aegypti instar III.
F. Definisi Operasional Variabel
Untuk memudahkan pelaksanaan penelitian dan agar penelitian tidak
menjadi terlalu luas maka dibuat definisi operasional sebagai berikut :
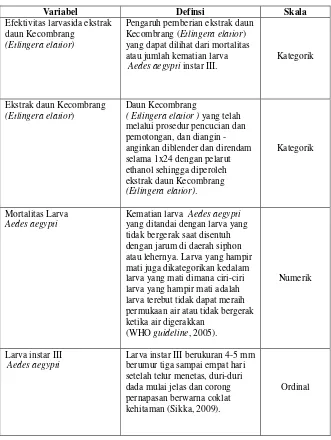
Tabel 2. Definisi Operasional
Variabel Definsi Skala
Efektivitas larvasida ekstrak daun Kecombrang
(Etlingera elatior)
Pengaruh pemberian ekstrak daun Kecombrang (Etlingera elatior) yang dapat dilihat dari mortalitas atau jumlah kematian larva
Aedes aegypti instar III.
Kategorik
Ekstrak daun Kecombrang
(Etlingera elatior)
Daun Kecombrang
( Etlingera elatior ) yang telah melalui prosedur pencucian dan
Kematian larva Aedes aegypti
yang ditandai dengan larva yang tidak bergerak saat disentuh dengan jarum di daerah siphon atau lehernya. Larva yang hampir mati juga dikategorikan kedalam larva yang mati dimana ciri-ciri larva yang hampir mati adalah larva terebut tidak dapat meraih permukaan air atau tidak bergerak ketika air digerakkan
(WHO guideline, 2005).
Numerik
Larva instar III
Aedes aegypti
Larva instar III berukuran 4-5 mm berumur tiga sampai empat hari setelah telur menetas, duri-duri dada mulai jelas dan corong pernapasan berwarna coklat kehitaman (Sikka, 2009).
Berbagai konsentrasi ekstak 0% yang kemudian akan dicari dosis subletalnya yaitu LC50 yang akan ditentukan dengan analisis
kematian pada 50 % hewan uji. Numerik
Lethal Time 50 ( LT50 ) Merupakan panjang waktu saat 50 % hewan uji sudah mati dan 50 %
hewan uji lainnya masih hidup. Numerik
Konsentrasi efektif Konsentrasi ekstrak daun Kecombrang ( Etlingeraelatior ) yang paling banyak membunuh larva Aedes aegypti instar III.
Kategorik
G. Prosedur Penelitian
Prosedur penenilian ini terdiri dari tiga tahap, yakni tahap persiapan,
tahap pelaksanaan dan tahap analisis data.
1. Tahap Persiapan
a. Sterilisasi alat
Alat dan bahan yang akan digunakan terlebih dahulu disiapkan,
kemudian dibersihkan. Bahan-bahan yang akan digunakan
ditimbang dengan neraca analitik terlebih dahulu sesuai dengan
kebutuhan. Setelah itu, alat dan bahan disterilisasi dengan
autoklaf selama 15 menit pada suhu 1210C dengan tekanan
b. Persiapan Sampel
Sampel yang digunakan dalam penelitian ini adalah telur
nyamuk Aedes aegypti yang diperoleh dari Ruang Insektarium
Loka Penelitian dan Pengembangan Pemberantasan Penyakit
Bersumber Binatang Ciamis, Pangandaran, Jawa Barat. Telur
kemudian diletakkan di dalam nampan plastik yang berukuran
30 x 15 cm berisi air bersih ± 1000 cc untuk pemeliharaan larva
agar tidak mati. Telur akan menetas menjadi larva dalam waktu
1-2 hari. Kemudian telur yang sudah menetas menjadi larva
dipisahkan dengan menggunakan kasa untuk pengkolonisasian
dan diberi fish food sebagai makanan larva. Dalam waktu
kurang lebih 4 hari, larva akan mencapai instar III. Setelah usia
larva mencapai instar III larva dipindahan dengan
menggunakan pipet larva ke dalam gelas plastik yang berisi
ekstrak daun Kecombrang (Etlingera elatior).
c. Persiapan ekstrak daun Kecombrang
Daun Kecombrang (Etlingera elatior) ini didapat dari
lingkungan sekitar tempat tinggal peneliti. Daun kecombrang
sebelumnya diidentifikasi terlebih dahulu di Laboratorium
Kimia FMIPA Universitas Lampung. Dan ditimbang sebanyak
20gr kemudian dicuci menggunakan air sampai bersih. Daun
yang sudah bersih, dicacah terlebih dahulu kemudian
dihaluskan menggunakan blender kering tanpa menggunakan
dikeringkan. Pengeringan tidak boleh dilakukan langsung
dibawah terik matahari karena akan menghilangkan senyawa
kimia yang terkandung didalam daun kecombrang. Daun
kecombrang diekstraksi menggunakan metode meserasi dan
menggunakan pelarut alkohol (etanol 70%).
Metode Maserasi adalah proses pengekstraksian simplisia
dengan menggunakan pelarut dengan beberapa kali
pengocokan atau pengadukan pada temperatur ruangan
(kamar). Secara teknologi termasuk ekstraksi dengan prinsip
metode pencapaian konsentrasi pada keseimbangan. Maserasi
kinetik berarti dilakukan pengadukan yang kontinu
(terus-menerus). Remaserasi berarti dilakukan pengulangan
penambah pelarut setelah dilakukan penyaringan maserat
pertama, dan seterusnya (dirjen POM depkes RI, 2000).
Potongan halus daun Kecombrang direndam selama 24 jam ke
dalam ethanol 70 % sebanyak 25 ml. Setelah direndam
selanjutnya bahan tersebut disaring sehingga diperoleh hasil
akhirnya berupa ekstrak Kecombrang dengan konsentrasi
Untuk membuat berbagai konsentrasi yang diperlukan dapat
digunakan digunakan rumus V M = V M .
Keterangan :
V = Volume larutan yang akan diencerkan (ml)
M = Konsentrasi ekstrak daun Kecombrang yang tersedia (%)
V = Volume larutan (air + ekstrak) yang diinginkan (ml)
M = Konsentrasi ekstrak daun Kecombrang yang akan dibuat
(%)
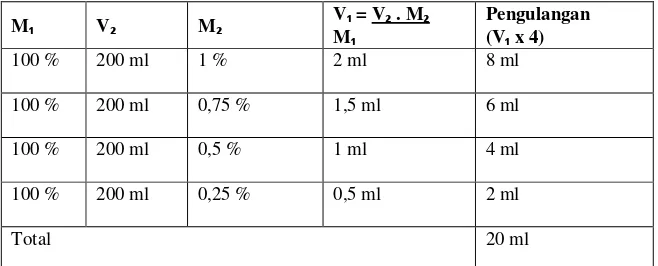
Tabel 3. Jumlah Ekstrak Daun Kecombrang yang Dibutuhkan
M V M V = V . M
M
Pengulangan (V x 4)
100 % 200 ml 1 % 2 ml 8 ml
100 % 200 ml 0,75 % 1,5 ml 6 ml
100 % 200 ml 0,5 % 1 ml 4 ml
100 % 200 ml 0,25 % 0,5 ml 2 ml
Total 20 ml
2. Tahap Pelaksanaan
1) Pembagian kelompok
Penelitian ini dibagi menjadi 6 ( enam ) kelompok yang terdiri
dari 4 perlakuan dan 2 kontrol dengan berbagai konsentrasi
a) Kelompok 1
Kontrol negatif (-) : Ekstrak ethanol daun kecombrang
dengan level konsentrasi 0 %
b) Kelompok 2
Perlakuan I : Ekstrak ethanol daun kecombrang dengan
level konsentrasi 0,25 %
c) Kelompok 3
Perlakuan II : Ekstrak ethanol daun kecombrang dengan
level konsentrasi 0,50 %
d) Kelompok 4
Perlakuan III : Ekstrak ethanol daun kecombrang dengan
level konsentrasi 0,75 %
e) Kelompok 5
Perlakuan IV : Ekstrak ethanol daun kecombrang dengan
level konsentrasi 1 %
f) Kelompok 6
Kontrol positif (+) : Ekstrak ethanol daun kecombrang
dengan penambahan temephos 1% (abate)
2) Uji Efektivitas
Uji efektifitas ini dilakukan untuk menentukan nilai LC50
(Lethal Consentration 50), LT50 (Lethal Time 50) dan level
konsentrasi yang paling efektif sebagai larvasida larva Aedes
aegypti. Ekstrak daun Kecombrang (Etlingera elatior) dengan
plastik. Larva diletakkan ke dalam gelas plastik yang berisi
berbagai konsetrasi daun Kecombrang (Etlingera elatior)
dengan menggunakan pipet larva. Perlakuan menggunakan
ekstrak daun Kecombrang (Etlingera elatior) hanya diberikan
pada kelompok eksperimen sebanyak 200 ml ekstrak daun
Kecombrang (Etlingera elatior) pada tiap ulangan, sedangkan
pada kelompok kontrol diberikan perlakuan mengunakan air
galon dengan volume 200 ml pada tiap ulangan.
Masing-masing perlakuan berisi 20 larva Aedes aegypti instar III
dengan jumlah pengulangan sebanyak 4 kali. Jumlah sampel
dan pengulangan berdasarkan kriteria WHO tahun 2005.
Pengukuran pada kelompok-kelompok sampel dilakukan dalam
24 jam dan pembagian pencatatan waktu selama perlakuan
yaitu dengan interval waktu 10, 20, 40, 60, 120, 240, 480,
1440, 2880, dan pengukuran berakhir pada menit ke 4320
dengan cara menghitung jumlah larva yang mati.
3) Menentukan Nilai LC50 dan LT50
Kelompok perlakuan terdiri dari 1 kontrol negatif, 4 level
konsentrasi ekstrak daun Kecombrang dan 1 kontrol positif.
Tiap kelompok perlakuan dilakukan pengulangan sebanyak 4
kali dan diamati pada menit ke-20, 40, 60, 120, 240, 480, 1440,
2880, dan 4320. Pengamatan dilakukan dengan menghitung
jumlah larva yang mati kemudian dihitung presentase rata-rata
rata-rata kematian masing-masing kelompok perlakuan pada
tiap masing-masing waktu pengamatan dianalisis dengan
menggunakan analisis Probit hingga diperoleh nilai LC50 dan
LT50.
4) Alur Penelitian
Untuk memperjelas proses penelitian, maka dibutuhkan
diagram alur penelitian sebagai berikut :
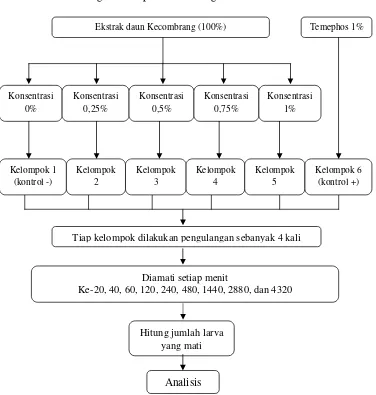
Gambar 11. Diagram Alir Uji Efek Ekstrak Daun Kecombrang (Etlingera elatior) sebagai Larvasida
Tiap kelompok dilakukan pengulangan sebanyak 4 kali
3. Tahap Analisis Data
1. ANOVA satu arah
Uji varian satu arah digunakan untuk mengetahui ada tidaknya
perbedaan rata-rata kematian nyamuk Aedes aegypti pada
berbagai kelompok konsentrasi ekstrak daun kecombrang
(Etlingera elatior). Untuk mengetahui adanya perbedaan antara
perlakuan yang diberikan maka digunakan analisis ANOVA
satu arah, tetapi bila sebaran data tidak normal atau varians
data tidak sama dapat dilakukan uji alternatif yaitu uji
Kruskal-Wallis. Uji ini bertujuan untuk mengetahui paling tidak
terdapat perbedaan antara dua kelompok perlakuan. Apabila
pada uji tersebut didapatkan hasil yang signifikan (bermakna)
yaitu p value < 0,05 maka dilakukan analisis post-hoc untuk
mengetahui kelompok perlakuan yang bermakna. Uji post-hoc
untuk ANOVA satu arah adalah Bonferroni sedangkan untuk
uji Kruskal-Wallis adalah Mann Whitney.
2. Uji Probit.
Untuk menilai toksisitas suatu insektisida dapat menggunakan
suatu metode pengujian dengan menggunakan analisis probit.
Lethal consentration merupakan suatu ukuran untuk mengukur
daya racun dari jenis pestisida. Pada uji efektifitas ditunjukan
LC50 yang berarti berapa ppm atau persen konsentrasi yang
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan hasil penelitian yang telah dilakukan, maka dapat ambil beberapa kesimpulan yaitu :
1. Ekstrak daun Kecombrang (Etlingera elatior) mempunyai efek sebagai larvasida terhadap larva Aedes aegypti instar III.
2. Level Konsentrasi yang efektif dalam membunuh larva Aedes aegypti instar III adalah konsentrasi 1%.
3. Nilai LC50 ekstrak daun Kecombrang (Etlingera elatior) sebagai larvasida terhadap larva Aedes aegypti instar III adalah 0,82%pada menit 120; 0,67% pada menit 240; 0,56% pada menit ke-480; 0,47% pada menit ke-1440; 0,27%pada menit ke-2880,dan 0,15% pada menit ke-4320.
B. Saran
Dari hasil penelitian yang diperoleh, peneliti menyarankan agar : 1. Dilakukan penelitian lebih lanjut mengenai biolarvasida dengan
metode Fraksi n-heksana daun kecombrang yang berfungsi sebagai larvasida alami sebagai pengganti larvasida sintetik.
2. Dilakukan penelitian lebih banyak lagi mengenai Manfaat dan fungsi tanaman kecombrang.
3. Ekstrak daun kecombrang diteliti sebagai larvasida pada spesies larva nyamuk lainnya yang berpotensi sebagai vektor penyakit. 4. Penelitian dengan menggunakan pelarut lain untuk mendapatkan
DAFTAR PUSTAKA
AgoesR, 2005. Entomologimedik.Fakultaskedokteranunpad. Jatinangor.Halaman 343
Chan dkk, 2007. Antioxidant and antibacterial activity of leavesof Etlingera species (Zingiberaceae) in Peninsular Malaysia. Food Chemistry 104: pp.1586–1593.
Dadang dan Prijono, 2008. Insektisida Nabati: Prinsip, Pemanfaatan, dan Pengembangan. Departemen Proteksi Tanaman. Institut PertanianBogor, Bogor.
Daniel, 2008. Ketika Larva dan Nyamuk Dewasa Sudah Kebal Terhadap Insektisida. FARMACIA. Vol.7 No.7.
Depkes RI. 2000. Parameter standar umum ekstrak tumbuhan obat. Dirjen pom. Jakarta. Halaman 13-38.
Depkes RI, 2007. Inside ( inspirasi dan ide) litbangkes p2b2 vol ii : aedes aegypti vampir mini yang mematikan. Badan penelitian dan pengembangan kesehatan depkes RI. Jakarta.
DepKes, 2005. Nicolaia Speciosa Horan. http://iptek.apjii.or.id/ artikel
/ttg_tanaman_ obat/DepKes/buku1/1-205.pdf. diakses tanggal 16 september 2012.
Dinata A, 2009. Mengatasi dbd dengan kulit jengkol. Www. Miqraindonesia. Blogspot.com. Diakses tanggal 16 september 2012.
Djakaria S, 2004. Pendahuluanentomologi.Parasitologikedokteranedisi ke-3.Fakultaskedokteranuniversitasindonesia. Jakarta. Halaman 343.
Guenther E, 2006. The Essential Oil. Vol I. Robert W. Kringer, Article Publishing Co., Inc. Huntington, New York.
Gunawan D dan Mulyani S, 2004. Ilmu obat alam (farmakognosi). Jilid pertama. Penebar swadaya. Jakarta.
Halimah, 2010. Uji Fiokimia dan Uji Toksisitas ekstrak tanaman Anting-Anting (acalypha indica Linn) terhadap larva udang (Artemia salina
Leach).Skripsi.Jurusan Kimia Fakultas Sains dan Teknologi. Universitas IslamNegeri Maulana Malik Ibrahim, Malang.
Harborne JB, 1996. Metode Fitokimia: Penuntun Cara Modern Menganalisis Tumbuhan. Institut Teksnologi Bandung. Bandung.
Hoedojo R dan Zulhasril, 2008. Buku ajar parasitologi kedokteran edisi keempat. Jakarta: balai penerbit fakultas kedokteran universitas indonesia.
Nio OK, 1989. Zat-zat Toksik yang secara alamiah ada pada bahan makanan Nabati. http:/www.kable.co.id/files/cdk/files/58 10 zat zat toksik
alamiah.pdf/58_10_zat-zattoksikalamiah.html. diakses tanggal 13 september 2012.
Raharjo B, 2006. Uji Kerentanan (Susceptibility test) Aedes aegypti (Linnaeus) dari Surabaya, Palembang dan Beberapa Wilayah di Bandung terhadap Larvasida Temephos (Abate 1 SG).Skripsi. Sekolah Ilmu dan Teknologi HayatiITB,Bandung.
Sitanggang dkk, 2008. Uji toksisitas daun murbei dan bunga kecombrang sebagai minuman alternatif bagi penderita diabetes melitus.pkmp. Institut Pertanian Bogor, Bogor.
Soedarto, 1992. Atlas Entomologi Kedokteran. EGC. Jakarta.
Sudarmaja IM dan Mardihusodo SJ, 2009. Pemilihan tempat bertelur nyamuk Aedes aegypti pada air limbah rumah tangga di laboratorium. Vol. 10 ( 4): 205-207.
Sukandar dkk, 2011.Karakterisasi senyawa antibakteri ekstrak air daun kecombrang (etlingera elatior). Valensi vol. 2 (3), Halaman 414-419. TjitrosoepomoG, 2005. Taksonomitumbuhanobat-obatan. Yogyakarta: Gadjah
Mada University Press. Halaman 447.
Tribun lampung. 2012. 440 kasus dbd ditemukan di bandar
World Health Organization. 2005. Guidelines for laboratory and field testing of mosquito larvicides. Who/cds/whopes/gcdpp/2005.13.
Wulandari, D. N., H. Soetjipto., dan S. P. Hastuti. 2006. Skrining Fitokimia dan Efek Larvasida Ekstrak Biji Kecubung Wulung (Datura metel L.) terhadap Larva Instar III dan IV Aedes aegypti. Berkala Ilmiah Biologi, Vol. 5(2); 101-107