PENETAPAN KADAR KALSIUM DAN FOSFOR DALAM
BUAH NAGA DAGING MERAH (Hylocereus costaricensis) DAN
BUAH NAGA DAGING PUTIH (Hylocereus undatus)
SKRIPSI
OLEH:
CHRISTINA DEBORA TAMBUNAN NIM 091501089
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENETAPAN KADAR KALSIUM DAN FOSFOR DALAM
BUAH NAGA DAGING MERAH (Hylocereus costaricensis) DAN
BUAH NAGA DAGING PUTIH (Hylocereus undatus)
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara OLEH:
CHRISTINA DEBORA TAMBUNAN NIM 091501089
PROGRAM STUDI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PENETAPAN KADAR KALSIUM DAN FOSFOR DALAM
BUAH NAGA DAGING MERAH (Hylocereus costaricensis) DAN
BUAH NAGA DAGING PUTIH (Hylocereus undatus)
OLEH:
CHRISTINA DEBORA TAMBUNAN NIM 091501089
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 20 Desember 2013
Pembimbing I, Panitia Penguji,
Dra. Siti Nurbaya, M.Si., Apt. Drs. Chairul Azhar Dalimunthe, M.Sc., Apt NIP 195008261974122001 NIP 194907061980021001
Pembimbing II, Dra. Siti Nurbaya, M.Si., Apt.
NIP 195008261974122001
Dr. Muchlisyam, M.Si., Apt. Dra. Sudarmi, M.Si., Apt. NIP 195006221980021001 NIP 195409101983032001
Drs. Maralaut Batubara, M.Phill., Apt. NIP 195101311976031003
Medan, Desember 2013 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
KATA PENGANTAR
Puji dan syukur kepada Tuhan Yesus Kristus, karena limpahan rahmat
kasih dan karuniaNya, sehingga penulis dapat menyelesaikan skripsi ini yang
berjudul ”Penetapan Kadar Kalsium dan Fosfor dalam Buah Naga Daging Merah
(Hylocereus costaricensis) dan Buah Naga Daging Putih (Hylocereus undatus)”.
Skripsi ini diajukan sebagai salah satu syarat untuk memperoleh gelar sarjana
farmasi pada Fakultas Farmasi Universitas Sumatera Utara.
Pada kesempatan ini penulis ingin mempersembahkan rasa terima kasih
yang tak terhingga kepada Ayahanda A. Tambunan dan Ibunda Sornia R.P.
Marbun atas doa dan pengorbanannya dengan tulus dan ikhlas,
Penulis juga menyampaikan ucapan terimakasih kepada Bapak Prof. Dr.
Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas
Sumatera Utara yang telah memberikan fasilitas selama masa pendidikan. Ibu
Dra. Siti Nurbaya, M.Si., Apt., dan Bapak Dr. Muchlisyam, M.Si., Apt., selaku
pembimbing yang telah membimbing dengan sangat baik, memberikan petunjuk,
perhatian, saran, dan motivasi selama penelitian hingga selesainya skripsi ini. Ibu
Dra. Juanita Tanuwijaya, M.Si., Apt., selaku penasehat akademis yang telah
memberikan bimbingan kepada penulis selama masa perkuliahan. Bapak Drs.
Chairul Azhar Dalimunthe, M.Sc., Apt., Ibu Dra. Sudarmi, M.Si., Apt., dan Bapak
Drs. Maralaut Batubara, M.Phill., Apt., yang telah memberikan saran dan
bimbingan sehingga penyusunan skripsi ini menjadi lebih baik. Bapak dan Ibu staf
pengajar Fakultas Farmasi Universitas Sumatera Utara yang telah mendidik
Kepala Laboratorium Penelitian Fakultas Farmasi USU dan Ibu Dra. Masfria,
M.Si., Apt., selaku Kepala Laboratorium Kimia Farmasi Kualitatif Fakultas
Farmasi USU yang telah memberikan izin dan fasilitas untuk penulis sehingga
dapat mengerjakan dan menyelesaikan penelitian.
Penulis juga mempersembahkan rasa terima kasih untuk adik-adikku
tersayang Risnawati Tambunan, Zosen Christison Tambunan, Jhon Klismen
Tambunan, Juwita Indah Permata Sari Tambunan, Serti Julini Sesar
Tambunan.dan teman-teman STF 2009 yang selalu setia memberi doa, dorongan
dan semangat. Serta seluruh pihak yang telah ikut membantu penulis namun tidak
tercantum namanya.
Penulis menyadari bahwa skripsi ini masih banyak kekurangannya, oleh
karena itu sangat diharapkan kritik dan saran yang bersifat membangun dari
semua pihak guna perbaikan skripsi ini. Akhir kata penulis berharap semoga
skripsi ini bermanfaat bagi ilmu pengetahuan khususnya bidang farmasi.
Medan,
Penulis,
Christina Debora Tambunan
PENETAPAN KADAR KALSIUM DAN FOSFOR DALAM BUAH NAGA DAGING MERAH (Hylocereus costaricensis) DAN BUAH NAGA DAGING
PUTIH (Hylocereus undatus) ABSTRAK
Buah naga pada umumnya sering dikonsumsi oleh masyarakat dalam bentuk buah segar. Buah naga banyak mengandung mineral diantaranya kalsium dan fosfor. Kedua mineral ini merupakan mineral yang sangat dibutuhkan oleh tubuh. Oleh karena itu, perlu dilakukan penelitian tentang kadar kalsium dan fosfor pada buah naga. Tujuan penelitian ini adalah untuk menentukan kadar kalsium dan fosfor pada buah naga daging merah (Hylocereus costaricensis) dan buah naga daging putih (Hylocereus undatus).
Penelitian yang dilakukan adalah analisis kualitatif dan analisis kuantitatif. Analisis kualitatif dilakukan dengan uji nyala kawat Ni/Cr dan pereaksi H2SO4
untuk kalsium, serta dengan pereaksi ammonium molibdat untuk fosfor. Sedangkan analisis kuantitatif dilakukan secara spektrofotometri serapan atom pada panjang gelombang 422,7 nm untuk kalsium dan secara spektrofotometri sinar tampak pada panjang gelombang 711 nm untuk fosfor.
Hasil penetapan kadar kalsium untuk buah naga daging merah adalah 7,7212 ± 0,0581 mg/100 g dan untuk buah naga daging putih adalah 3,3884 ± 0,0435 mg/100 g. Hasil penetapan kadar fosfor untuk buah naga daging merah adalah 32,5206 ± 0,4119 mg/100 g, dan untuk buah naga daging putih adalah 36,5592 ± 0,5146 mg/100 g. Hasil uji validasi metode yang dilakukan memberikan akurasi dan presisi yang memenuhi syarat yaitu 107,22% recovery dengan RSD 2,79%, batas deteksi (LOD) 0,2694 µg/ml dan batas kuantitasi (LOQ) 0,8979 µg/ml untuk kalsium. Sedangkan untuk fosfor, hasil uji validasi metode yang dilakukan memberikan akurasi dan presisi yang memenuhi syarat yaitu 102,09% recovery dengan RSD 5,57%, batas deteksi (LOD) 0,2405 µg/ml dan batas kuantitasi (LOQ) 0,8017 µg/ml.
Berdasarkan hasil penelitian tersebut dapat disimpulkan bahwa kadar kalsium pada buah naga daging merah (Hylocereus costaricensis) lebih tinggi dari kadar kalsium pada buah naga daging putih (Hylocereus undatus) dan kadar fosfor pada buah naga daging merah (Hylocereus costaricensis) lebih rendah dari kadar fosfor pada buah naga daging putih (Hylocereus undatus).
ASSAY OF CALCIUM AND PHOSPHORUS CONTENT IN RED DRAGON FRUIT (Hylocereus costaricensis) AND WHITE DRAGON
FRUIT (Hylocereus undatus) ABSTRACT
Dragon fruit is often consumed by the general public in the form of fresh fruit. Dragon fruit contains many minerals such as calcium and phosphorus. Both of these minerals are needed by the body. Therefore, it is necessary to do research on calcium and phosphorus levels on dragon fruit. The purpose of this study is to determine the levels of calcium and phosphorus in the red flesh dragon fruit (Hylocereus costaricensis) and white flesh dragon fruit (Hylocereus undatus).
Research is qualitative analysis and quantitative analysis. Qualitative analysis performed by flame test wire Ni/Cr and H2SO4 reagent for calcium, as
well as with ammonium molybdate reagent for phosphorus. Quantitative analysis performed atomic absorption spectrophotometry at a wavelength of 422,7 nm for calcium and visible spectrophotometry at a wavelength of 711 nm for phosphorus.
The result of calcium assay for red flesh dragon fruit is 7,7212 ± 0,0581 mg/100 g and for white flesh dragon fruit is 3,3884 ± 0,0435 mg/100 g. The result of phosphorus assay for red flesh dragon fruit is 32,5206 ± 0,4119 mg/100 g, and for white flesh dragon fruit is 36,5592 ± 0,5146 mg/100 g. Results of the validation test method conducted to provide accuracy and precision are eligible 107,22% recovery with RSD 2,79%, the limit of detection ( LOD ) 0,2694 µg/ml and the limit of quantitation ( LOQ ) 0,8979 µg/ml for calcium. While for phosphorus, the results of the validation test method conducted to provide accuracy and precision are eligible 102,09% recovery with RSD 5,57%, the limit of detection ( LOD ) 0,2405 µg/ml and the limit of quantitation ( LOQ ) 0,8017 µg/ml.
Based on these results can be concluded that the level of calcium in the red flesh dragon fruit (Hylocereus costaricensis) is higher than the level of calcium in the white flesh dragon fruit (Hylocereus undatus) and phosphorus levels in the red flesh dragon fruit (Hylocereus costaricensis) is lower than the levels of phosphorus in white flesh dragon fruit (Hylocereus undatus).
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Uraian Tumbuhan ... 5
2.1.1 Buah Naga ... 5
2.1.2 Kandungan Gizi ... 7
2.2. Mineral ... 7
2.2.2 Fosfor ... 9
2.3 Spektrofotometri Serapan Atom ... 10
2.3.1 Instrumen Spektrofotometri Serapan Atom ... 11
2.3.2 Gangguan-Gangguan pada Spektrofotometri Serapan Atom ... 13
2.4 Spektrofotometri Sinar Tampak dan Sinar Ultraviolet ... 14
2.5 Validasi Metode Analisis ... 16
BAB III METODE PENELITIAN ... 18
3.1 Tempat dan Waktu Penelitian ... 18
3.2 Bahan-bahan ... 18
3.2.1 Sampel ... 18
3.2.2 Pereaksi ... 18
3.3 Alat-alat ... 18
3.4 Identifikasi Sampel ... 19
3.5 Pembuatan Pereaksi ... 19
3.5.1 Larutan HNO3 (1:1) ... 19
3.5.2 Larutan H2SO4 1N ... 19
3.5.3 Larutan HNO3 5N ... 19
3.5.4 Larutan H2SO4 5N ... 19
3.5.5 Larutan Ammonium molibdat 4% b/v ... 20
3.5.6 Larutan Asam Askorbat 0,1 N ... 20
3.5.7 Larutan Kalium antimonil tartrat 0,274% b/v ... 20
3.5.8 Larutan Pengembang Warna Fosfor ... 20
3.6 Prosedur Penelitian ... 20
3.6.2 Penyiapan Sampel ... 21
3.6.3 Proses Destruksi Kering ... 21
3.6.4 Pembuatan Larutan Sampel ... 22
3.6.5 Analisis Kualitatif ... 22
3.6.6 Analisis Kuantitatif ... 23
3.6.7 Analisis Data Secara Statistik ... 27
3.6.8 Validasi Metode Analisis ... 29
BAB IV HASIL DAN PEMBAHASAN ... 32
4.1 Analisis Kualitatif Kalsium dan Fosfor pada Sampel ... 32
4.2 Analisis Kuantitatif Kalsium dan Fosfor pada Sampel ... 33
4.2.1 Analisis Kuantitatif Kalsium... ... 33
4.2.2 Analisis Kuantitatif Fosfor ... 34
4.2.3 Pengujian Beda Nilai Rata-Rata Antar Sampel ... 37
4.2.4 Validasi Metode Analisis ... 38
BAB V KESIMPULAN DAN SARAN ... 40
5.1 Kesimpulan ... 40
5.2 Saran ... 40
DAFTAR PUSTAKA ... 41
DAFTAR TABEL
Halaman
Tabel 1 Hasil Analisis Kualitatif Kalsium dan Fosfor pada Sampel.... ... 32
Tabel 2 Hasil Analisis Kuantitatif Kalsium pada Sampel ... ... 34
Tabel 3 Hasil Analisis Kuantitatif Fosfor pada Sampel ... ... 37
Tabel 4 Hasil Uji Beda Nilai Rata-Rata Kalsium dan Fosfor antar
Sampel ... ... 37
Tabel 5 Persen Uji Perolehan Kembali (recovery) Kalsium dan Fosfor
DAFTAR GAMBAR
Halaman
Gambar 1 Kurva Kalibrasi Larutan Baku Kalsium ... 33
Gambar 2 Kurva Serapan Senyawa Fosfor pada Konsentrasi 6 µg/ml 35
Gambar 3 Absorbansi Panjang Gelombang Maksimum Larutan
Standar Fosfor pada Konsentrasi 6 µg/ml ... 35
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Gambar Sampel ... 43
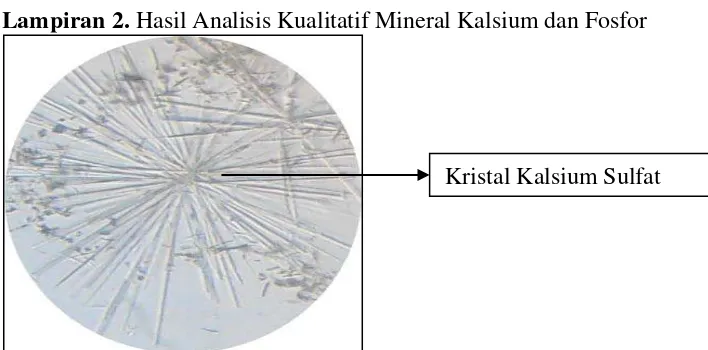
Lampiran 2. Hasil Analisis Kualitatif Mineral Kalsium dan Fosfor ... 44
Lampiran 3. Bagan Alir Proses Destruksi Kering ... 46
Lampiran 4. Bagan Alir Proses Pembuatan Larutan Sampel ... 47
Lampiran 5. Data penentuan Waktu Kerja Senyawa Fosfor Kompleks pada Panjang Gelombang 711 nm ... 48
Lampiran 6. Data Kalibrasi Kalsium dengan Spektrofotometer Serapan Atom, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) ... 50
Lampiran 7. Data Kalibrasi Fosfor dengan Spektrofotometer Sinar Tampak, Perhitungan Persamaan Garis Regresi dan Koefisien Korelasi (r) ... 52
Lampiran 8. Hasil Analisis Kadar Kalsium dan Fosfor dalam Sampel ... ... 54
Lampiran 9. Contoh Perhitungan Kadar Kalsium dan Fosfor dalam Sampel ... 56
Lampiran 10. Perhitungan Statistik Kadar Kalsium dalam Sampel ... 58
Lampiran 11. Perhitungan Statistik Kadar Fosfor dalam Sampel ... 61
Lampiran 12. Pengujian Beda Nilai Rata-rata Kadar Kalsium pada Sampel ... 64
Lampiran 13. Pengujian Beda Nilai Rata-rata Kadar Fosfor pada Sampel ... 66
Lampiran 14. Perhitungan Batas Deteksi dan Batas Kuantitasi ... 68
Lampiran 16. Contoh Perhitungan Uji Perolehan Kembali Kadar
Kalsium dan Fosfor pada Sampel ... . 71
Lampiran 17. Perhitungan Simpangan Baku Relatif (RSD) Kadar Kalsium dan Fosfor pada Sampel ... ... 73
Lampiran 18. Hasil Identifikasi Sampel ... 75
Lampiran 19. Tabel Distribusi T ... 77
PENETAPAN KADAR KALSIUM DAN FOSFOR DALAM BUAH NAGA DAGING MERAH (Hylocereus costaricensis) DAN BUAH NAGA DAGING
PUTIH (Hylocereus undatus) ABSTRAK
Buah naga pada umumnya sering dikonsumsi oleh masyarakat dalam bentuk buah segar. Buah naga banyak mengandung mineral diantaranya kalsium dan fosfor. Kedua mineral ini merupakan mineral yang sangat dibutuhkan oleh tubuh. Oleh karena itu, perlu dilakukan penelitian tentang kadar kalsium dan fosfor pada buah naga. Tujuan penelitian ini adalah untuk menentukan kadar kalsium dan fosfor pada buah naga daging merah (Hylocereus costaricensis) dan buah naga daging putih (Hylocereus undatus).
Penelitian yang dilakukan adalah analisis kualitatif dan analisis kuantitatif. Analisis kualitatif dilakukan dengan uji nyala kawat Ni/Cr dan pereaksi H2SO4
untuk kalsium, serta dengan pereaksi ammonium molibdat untuk fosfor. Sedangkan analisis kuantitatif dilakukan secara spektrofotometri serapan atom pada panjang gelombang 422,7 nm untuk kalsium dan secara spektrofotometri sinar tampak pada panjang gelombang 711 nm untuk fosfor.
Hasil penetapan kadar kalsium untuk buah naga daging merah adalah 7,7212 ± 0,0581 mg/100 g dan untuk buah naga daging putih adalah 3,3884 ± 0,0435 mg/100 g. Hasil penetapan kadar fosfor untuk buah naga daging merah adalah 32,5206 ± 0,4119 mg/100 g, dan untuk buah naga daging putih adalah 36,5592 ± 0,5146 mg/100 g. Hasil uji validasi metode yang dilakukan memberikan akurasi dan presisi yang memenuhi syarat yaitu 107,22% recovery dengan RSD 2,79%, batas deteksi (LOD) 0,2694 µg/ml dan batas kuantitasi (LOQ) 0,8979 µg/ml untuk kalsium. Sedangkan untuk fosfor, hasil uji validasi metode yang dilakukan memberikan akurasi dan presisi yang memenuhi syarat yaitu 102,09% recovery dengan RSD 5,57%, batas deteksi (LOD) 0,2405 µg/ml dan batas kuantitasi (LOQ) 0,8017 µg/ml.
Berdasarkan hasil penelitian tersebut dapat disimpulkan bahwa kadar kalsium pada buah naga daging merah (Hylocereus costaricensis) lebih tinggi dari kadar kalsium pada buah naga daging putih (Hylocereus undatus) dan kadar fosfor pada buah naga daging merah (Hylocereus costaricensis) lebih rendah dari kadar fosfor pada buah naga daging putih (Hylocereus undatus).
ASSAY OF CALCIUM AND PHOSPHORUS CONTENT IN RED DRAGON FRUIT (Hylocereus costaricensis) AND WHITE DRAGON
FRUIT (Hylocereus undatus) ABSTRACT
Dragon fruit is often consumed by the general public in the form of fresh fruit. Dragon fruit contains many minerals such as calcium and phosphorus. Both of these minerals are needed by the body. Therefore, it is necessary to do research on calcium and phosphorus levels on dragon fruit. The purpose of this study is to determine the levels of calcium and phosphorus in the red flesh dragon fruit (Hylocereus costaricensis) and white flesh dragon fruit (Hylocereus undatus).
Research is qualitative analysis and quantitative analysis. Qualitative analysis performed by flame test wire Ni/Cr and H2SO4 reagent for calcium, as
well as with ammonium molybdate reagent for phosphorus. Quantitative analysis performed atomic absorption spectrophotometry at a wavelength of 422,7 nm for calcium and visible spectrophotometry at a wavelength of 711 nm for phosphorus.
The result of calcium assay for red flesh dragon fruit is 7,7212 ± 0,0581 mg/100 g and for white flesh dragon fruit is 3,3884 ± 0,0435 mg/100 g. The result of phosphorus assay for red flesh dragon fruit is 32,5206 ± 0,4119 mg/100 g, and for white flesh dragon fruit is 36,5592 ± 0,5146 mg/100 g. Results of the validation test method conducted to provide accuracy and precision are eligible 107,22% recovery with RSD 2,79%, the limit of detection ( LOD ) 0,2694 µg/ml and the limit of quantitation ( LOQ ) 0,8979 µg/ml for calcium. While for phosphorus, the results of the validation test method conducted to provide accuracy and precision are eligible 102,09% recovery with RSD 5,57%, the limit of detection ( LOD ) 0,2405 µg/ml and the limit of quantitation ( LOQ ) 0,8017 µg/ml.
Based on these results can be concluded that the level of calcium in the red flesh dragon fruit (Hylocereus costaricensis) is higher than the level of calcium in the white flesh dragon fruit (Hylocereus undatus) and phosphorus levels in the red flesh dragon fruit (Hylocereus costaricensis) is lower than the levels of phosphorus in white flesh dragon fruit (Hylocereus undatus).
BAB I PENDAHULUAN
1.1Latar Belakang
Tanaman buah naga merupakan salah satu tanaman yang telah
dibudidayakan di pulau Jawa seperti di Jember, Malang, Pasuruan dan daerah
lainnya. Bentuk buahnya unik dan menarik, kulitnya merah dan bersisik hijau
mirip sisik naga sehingga dinamakan buah naga atau dragon fruit. Jenis buah naga
ada empat, yaitu Hylocereus undatus (buah naga kulit merah daging putih),
Hylocereus costaricensis (buah naga kulit merah daging super merah), Hylocereus
polyrhizus (buah naga kulit merah daging merah), Selenicereus megalanthus
(buah naga kulit kuning daging putih) (Cahyono, 2009). Namun buah naga yang
beredar di pasaran Kota Medan adalah buah naga daging merah dan buah naga
daging putih.
Laboratorium Taiwan Food Industry Develop and Research Authoritis
menyebutkan bahwa kandungan gizi per 100 gram buah naga merah adalah air
82,5-83 g, protein 0,159-0,229 g, lemak 0,21-0,61 g, serat kasar 0,7-0,9 g, karoten
0,005-0,012 g, kalsium 6,3-8,8 mg, fosfor 30,2-36,1 mg, besi 0,55-0,65 mg,
vitamin B1 0,28-0,043 g, vitamin B2 0,043-0,045 g, vitamin B3 0,297-0,43 g dan
vitamin C 8-9 mg. Sedangkan kandungan gizi per 100 gram buah naga putih
adalah air 89,4 g, protein 0,5 g, lemak 0,1 g, serat kasar 0,3 g, kalsium 6 mg,
fosfor 19 mg, besi 0,4 mg, vitamin B3 0,2 mg dan vitamin C 25 mg (Gunasena
disebabkan karena perbedaan varietas dan pengaruh lingkungan tempat tumbuh
(Harris dan Karmas, 1989).
Kalsium adalah mineral yang paling banyak ditemukan dalam tubuh.
Kalsium merupakan mineral yang penting dalam pembentukan tulang dan gigi.
Selain itu, kalsium merupakan komponen penting untuk kehidupan sel dan
jaringan. Kalsium juga penting dalam aktivitas beberapa sistem enzim dan juga
terlibat dalam sistem koagulasi darah (Darmono, 1995). Fosfor merupakan
mineral terbanyak kedua di dalam tubuh. Kurang lebih 85% fosfor di dalam tubuh
terdapat sebagai garam kalsium fosfat, bagian dari kristal hidroksiapatit di dalam
tulang dan gigi (Almatsier, 2004). Selain untuk pertumbuhan tulang dan gigi,
fosfor juga berperan dalam metabolisme karbohidrat, lemak dan protein. Sebagai
fosfolipid, fosfor merupakan komponen esensial bagi banyak sel dan merupakan
alat transpor asam lemak. Fosfor berperan pula dalam mempertahankan
keseimbangan asam-basa (Pudjiadi, 2000).
Metode penetapan kadar kalsium di dalam literatur antara lain
kompleksometri (Rivai, 1995), gravimetri, permanganometri, dan
spektrofotometri serapan atom (Gandjar dan Rohman, 2007). Penetapan kadar
fosfor dapat dilakukan secara spektrofotometri sinar tampak (Lim, 1991).
Adapun alasan untuk meneliti kalsium pada buah naga daging merah dan
daging putih dengan metode spektrofotometri serapan atom adalah karena
analisisnya yang cepat, dapat mengukur kadar logam dalam jumlah kecil dan
spesifik untuk setiap logam tanpa dilakukan pemisahan (Khopkar, 1990).
Sedangkan untuk meneliti fosfor pada buah naga daging merah dan buah naga
lebih sederhana dan lebih sensitif (Lim, 1991) serta merujuk dari penelitian
sebelumnya mengenai penetapan kadar fosfor (Hadiyanto, 2009).
Berdasarkan uraian di atas, maka peneliti ingin mengetahui kadar kalsium
secara spektrofotometri serapan atom dan fosfor secara spektrofotometri sinar
tampak pada buah naga daging merah (Hylocereus costaricensis) dan buah naga
daging putih (Hylocereus undatus).
1.2Perumusan Masalah
1. Berapakah kadar kalsium dan fosfor pada buah naga daging merah
(Hylocereus costaricensis) dan buah naga daging putih (Hylocereus
undatus).
2. Apakah terdapat perbedaan kadar kalsium dan fosfor pada buah naga
daging merah (Hylocereus costaricensis) dan buah naga daging putih
(Hylocereus undatus).
1.3Hipotesis
1. Buah naga daging merah (Hylocereus costaricensis) dan buah naga
daging putih (Hylocereus undatus) mengandung kalsium dan fosfor dalam
jumlah tertentu.
2. Terdapat perbedaan kadar kalsium dan fosfor pada buah naga daging
merah (Hylocereus costaricensis) dan buah naga daging putih (Hylocereus
1.4Tujuan Penelitian
1. Untuk mengetahui kadar kalsium dan fosfor yang terdapat pada buah naga
daging merah (Hylocereus costaricensis) dan buah naga daging putih
(Hylocereus undatus).
2. Untuk mengetahui perbedaan kadar kalsium dan fosfor yang terdapat pada
buah naga daging merah (Hylocereus costaricensis) dan buah naga daging
putih (Hylocereus undatus).
1.5Manfaat Penelitian
Untuk mengetahui kadar kalsium dan fosfor pada buah naga daging merah
(Hylocereus costaricensis) dan buah naga daging putih (Hylocereus undatus) agar
dapat dimanfaatkan sebagai salah satu buah yang dapat dipilih untuk asupan
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan 2.1.1 Buah Naga
Dalam dunia taksonomi, buah naga masuk dalam Family Cactaceae.
Berikut adalah klasifikasi ilmiah dari buah naga (Idawati, 2012):
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledonae
Ordo : Cactales
Famili : Cactaceae
Subfamily : Hylocereanea
Genus : Hylocereus
Species : - Hylocereus costaricensis
- Hylocereus undatus
- Hylocereus polyrhizus
Buah naga adalah buah sejenis pohon kaktus. Buah naga berasal dari Meksiko,
Amerika Selatan dan juga Amerika Tengah namun saat ini buah naga sudah
ditanam secara komersial di Vietnam, Taiwan, Malaysia, Australia, dan Indonesia.
Nama asing dari buah naga adalah “Dragon Fruit”, dalam bahasa latin buah naga
dikenal dengan “Phitahaya”. Isi buah naga berwarna putih, merah, atau ungu
dengan taburan biji-biji berwarna hitam yang boleh dimakan (Idawati, 2012).
Tanaman buah naga merupakan salah satu tanaman yang telah
dibudidayakan di pulau Jawa seperti di Jember, Malang, Pasuruan dan daerah
lainnya. Bentuk buahnya unik dan menarik, kulitnya merah dan bersisik hijau
mirip sisik naga sehingga dinamakan buah naga atau dragon fruit. Jenis buah naga
ada empat, yaitu Hylocereus undatus (buah naga kulit merah daging putih),
Hylocereus costaricensis (buah naga kulit merah daging super merah), Hylocereus
polyrhizus (buah naga kulit merah daging merah), Selenicereus megalanthus
(buah naga kulit kuning daging putih) (Cahyono, 2009).
Berdasarkan klasifikasi buah naga dalam ilmu taksonomi, maka secara
morfologis bisa digambarkan bahwa tanaman buah naga merupakan tumbuhan
tidak lengkap sebab tidak memiliki daun seperti tumbuhan lainnya. Meskipun
demikian, tanaman buah naga juga memiliki akar, batang, cabang, biji, dan juga
bunga. Buah naga atau dragon fruit merupakan buah yang eksotik, rasanya asam
manis menyegarkan dan memiliki beragam manfaat untuk kesehatan (Idawati,
2012).
2.1.1.1 Buah Naga Daging Merah
Buah naga daging merah memiliki kulit berwarna merah yang cerah dan
berwarna merah. Tak hanya unik, rasa daging buahnya juga cukup nikmat. Di
antara jenis buah naga lainnya, varian dengan daging merah ini banyak digemari
karena memiliki karakteristik rasa manis melebihi rasa asamnya. Buah naga
daging merah atau dalam dunia biologi dikenal dengan istilah Hylocereus
costaricensis ini tergolong cukup popular di Indonesia (Idawati, 2012).
2.1.1.2 Buah Naga Daging Putih
Varietas buah naga putih (Hylocereus undatus) merupakan jenis buah naga
yang ditemukan pertama kali. Adapun ciri-ciri buah naga daging putih kurang
lebih sama dengan jenis buah naga lainnya. Satu-satunya perbedaan yang menjadi
dasar pengelompokkan varietas ini adalah pada daging buahnya. Buah naga
daging putih memiliki kulit buah berwarna merah cerah lengkap dengan sisiknya
namun memiliki daging buah yag berwarna putih dan dipenuhi dengan bebijian
berwarna hitam. Buah naga daging putih memiliki karakteristik rasa manis yang
tidak dominan melainkan seimbang dengan rasa asamnya (Idawati, 2012).
2.1.2 Kandungan Gizi
Dalam 100 g buah naga merah , kandungan airnya cukup tinggi yaitu
82,5-83 g, serat 0,7-0,9 g, betakaroten 0,005-0,012 g, kalsium 6,3-8,8 mg, zat besi
0,55-0,65 mg, fosfor 30,2-36,1 mg, protein 0,16-0,23 g, lemak 0,21-0,61 g, beragam
vitamin seperti B1 sebanyak 0,28-0,30 mg, vitamin B2 0,043-0,045 mg, vitamin C
8-9 mg dan kandungan niasin sebanyak 1,297-1,300 mg. Sedangkan dalam 100 g
buah naga putih mengandung air 89,4 g, serat 0,3 g, kalsium 6 mg, zat besi 0,4
mg, fosfor 19 mg, protein 0,5 g, lemak 0,1 g, niasin 0,2 mg dan vitamin C 25 mg
2.2 Mineral
Mineral merupakan unsur esensial bagi fungsi normal sebagian enzim dan
sangat penting dalam pengendalian komposisi cairan tubuh. Selain itu, mineral
juga berperan dalam proses pertumbuhan (Pudjiadi, 2000). Namun tubuh tidak
mampu mensintesis mineral sehingga unsur-unsur ini harus disediakan lewat
makanan. Mineral digolongkan ke dalam mineral makro dan mineral mikro.
Mineral makro adalah mineral yang dibutuhkan tubuh dalam jumlah lebih dari
100 mg sehari, sedangkan mineral mikro dibutuhkan kurang dari 100 mg sehari.
Yang termasuk mineral makro antara lain: natrium, klorida, kalium, kalsium,
fosfor, dan magnesium, sedangkan yang termasuk mineral mikro antara lain: besi,
mangan dan tembaga (Almatsier, 2004). Peran mineral dalam tubuh kita berkaitan
satu sama lainnya, dan kekurangan atau kelebihan salah satu mineral akan
berpengaruh terhadap kerja mineral lainnya (Pudjiadi, 2000).
2.2.1 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh,
yaitu 1,5 – 2% dari berat badan orang dewasa atau kurang lebih sebanyak 1 kg.
Dari jumlah ini, 99% berada didalam jaringan keras, yaitu tulang dan gigi
terutama dalam bentuk hidroksiapatit selebihnya kalsium tersebar luas di dalam
tubuh. Absorpsi kalsium terutama terjadi di bagian atas usus halus yaitu
duodenum. Peningkatan kebutuhan akan kalsium terjadi pada masa pertumbuhan,
kehamilan, dan menyusui (Almatsier, 2004).
Mineral kalsium dibutuhkan untuk perkembangan tulang. Jumlah yang
dianjurkan per hari untuk bayi sebesar 300-400 mg, anak-anak 500 mg, remaja
Kalsium mempunyai berbagai fungsi dalam tubuh antara lain untuk
pertumbuhan tulang dan gigi, mengatur pembentukan darah, sebagai katalisator
reaksi-reaksi biologik dan berperan dalam kontraksi otot (Almatsier, 2004).
Konsumsi kalsium tidak boleh melebihi 2500 mg sehari. Kelebihan
kalsium dapat menimbulkan gangguan ginjal. Disamping itu, dapat menyebabkan
konstipasi (susah buang air besar). Kekurangan kalsium pada masa pertumbuhan
dapat menyebabkan gangguan pertumbuhan. Tulang kurang kuat, mudah bengkok
dan rapuh. Semua orang dewasa, terutama sesudah usia 50 tahun akan mengalami
resorpsi kalsium dari tulangnya. Tulang menjadi rapuh dan mudah patah. Ini yang
dinamakan osteoporosis. Kadar kalsium dalam darah yang sangat rendah dapat
menyebabkan tetani atau kejang. Kepekaan serabut saraf dan pusat saraf terhadap
rangsangan meningkat, sehingga terjadi kejang otot (Almatsier, 2004).
2.2.2 Fosfor
Fosfor merupakan mineral kedua terbanyak di dalam tubuh, yaitu 1% dari
berat badan. Kurang lebih 85% fosfor di dalam tubuh terdapat sebagai garam
kalsium fosfat di dalam tulang dan gigi yang tidak dapat larut. Fosfor di dalam
tulang berada dalam perbandingan 1 : 2 dengan kalsium. Fosfor selebihnya
terdapat di dalam semua sel tubuh, separuhnya di dalam otot dan di dalam cairan
ekstraseluler. Sebagai fosfolipid, fosfor merupakan komponen struktural dinding
sel. Sebagai fosfat organik, fosfor memegang peranan penting dalam reaksi yang
berkaitan dengan penyimpanan atau pelepasan energi dalam bentuk Adenin
Trifosfat (ATP) (Almatsier, 2004).
Jumlah kebutuhan fosfor yang dianjurkan per hari untuk bayi sebesar
dan ibu hamil serta menyusui sebesar kebutuhan untuk dewasa ditambah 200 mg
(Almatsier, 2004).
Selain untuk pertumbuhan tulang dan gigi, fosfor mempunyai peranan
dalam metabolisme karbohidrat, lemak, dan protein, sebagai fosfolipid, fosfor
merupakan komponen esensial bagi banyak sel dan merupakan alat transport asam
lemak. Fosfor berperan pula dalam mempertahankan keseimbangan asam-basa
(Pudjiadi, 2000).
Pada umumnya bahan makanan yang mengandung banyak kalsium
merupakan juga sumber fosfor, seperti susu, keju, daging, ikan, telur, dan saleria.
Biasanya kira-kira 70% dari fosfor yang berada dalam makanan dapat diserap oleh
tubuh. Penyerapan akan lebih baik bila fosfor dan kalsium dimakan dalam jumlah
yang sama (Poedjiadi, 2000).
Kelebihan fosfor karena makanan jarang terjadi. Bila kadar fosfor darah
terlalu tinggi, ion fosfat akan mengikat kalsium sehingga dapat menimbulkan
kejang. Kekurangan fosfor karena makan juga jarang terjadi. Kekurangan fosfor
bisa terjadi bila menggunakan obat antasida untuk menetralkan asam lambung
seperti aluminium hidroksida. Aluminium hidroksida mengikat fosfor sehingga
tidak dapat diabsorpsi. Kekurangan fosfor juga dapat terjadi pada penderita yang
kehilangan banyak cairan melalui urin. Kekurangan fosfor menyebabkan rasa
2.3 Spektrofotometri Serapan Atom
Spektrofotometri serapan atom didasarkan pada penyerapan energi sinar
oleh atom-atom netral, dan sinar yang diserap biasanya sinar tampak atau sinar
ultraviolet (Gandjar dan Rohman, 2007).
Spektrofotometri serapan atom digunakan untuk analisis kuantitatif
unsur-unsur mineral dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace).
Cara analisis ini memberikan kadar total unsur mineral dalam suatu sampel dan
tidak tergantung pada bentuk molekul mineral dalam sampel tersebut. Cara ini
cocok untuk analisis sekelumit mineral karena mempunyai kepekaan yang tinggi
(batas deteksi kurang dari 1 ppm) dan pelaksanaannya relatif cepat dan sederhana
(Gandjar dan Rohman, 2007).
Metode spektrofotometri serapan atom berprinsip pada absorpsi cahaya
oleh atom. Atom-atom menyerap cahaya pada panjang gelombang tertentu,
tergantung pada sifat unsurnya. Cahaya pada panjang gelombang ini mempunyai
cukup energi untuk mengubah tingkat elektronik suatu atom. Transisi elektronik
suatu unsur bersifat spesifik. Dengan absorpsi energi, berarti memperoleh lebih
banyak energi, suatu atom pada keadaan dasar dinaikkan tingkat energinya ke
tingkat eksitasi (Khopkar, 1990).
2.3.1 Instrumen Spektrofotometer Serapan atom
Bagian instrumentasi spektrofotometer serapan atom adalah sebagai berikut:
a. Sumber Radiasi
Sumber radiasi yang digunakan adalah lampu katoda berongga (hollow
suatu katoda dan anoda. Katoda berbentuk silinder berongga yang dilapisi dengan
mineral tertentu (Gandjar dan Rohman, 2007).
b. Tempat Sampel
Dalam analisis dengan spektrofotometer serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan
azas. Ada berbagai macam alat yang digunakan untuk mengubah sampel menjadi
uap atom-atomnya, yaitu:
- Dengan nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi
bentuk uap atomnya dan untuk proses atomisasi. Suhu yang dapat dicapai oleh
nyala tergantung pada gas yang digunakan, misalnya untuk gas asetilen-udara
suhunya sebesar 2200°C. Sumber nyala asetilen-udara ini merupakan sumber
nyala yang paling banyak digunakan. Pada sumber nyala ini asetilen sebagai
bahan pembakar, sedangkan udara sebagai bahan pengoksidasi (Gandjar dan
Rohman, 2007).
- Tanpa nyala (Flameless)
Pengatoman dilakukan dalam tungku dari grafit. Sejumlah sampel diambil
sedikit (hanya beberapa µL), lalu diletakkan dalam tabung grafit, kemudian
tabung tersebut dipanaskan dengan sistem elektris dengan cara melewatkan arus
listrik pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis berubah
menjadi atom-atom netral dan pada fraksi atom ini dilewatkan suatu sinar yang
berasal dari lampu katoda berongga sehingga terjadilah proses penyerapan energi
c. Monokromator
Monokromator merupakan alat untuk memisahkan dan memilih spektrum
sesuai dengan panjang gelombang yang digunakan dalam analisis dari sekian
banyak spektrum yang dihasilkan lampu katoda berongga (Gandjar dan Rohman,
2007).
d. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui
tempat pengatoman (Gandjar dan Rohman, 2007).
e. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva yang
menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman, 2007).
2.3.2Gangguan-gangguan pada Spektrofotometri Serapan Atom
Gangguan-gangguan (interference) pada Spektrofotometri Serapan Atom
adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang
dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan
konsentrasinya dalam sampel (Gandjar dan Rohman, 2007).
Gangguan-gangguan yang terjadi dalam Spektrofotometri Serapan Atom
antara lain:
- Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi
banyaknya sampel yang mencapai nyala.
- Gangguan kimia yang dapat mempengaruhi jumlah/banyaknya atom yang
- Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi atom yang
dianalisis; yakni absorbansi oleh molekul-molekul yang tidak terdisosiasi di
dalam nyala (Gandjar dan Rohman, 2013).
2.4 Spektrofotometri Sinar Tampak dan Sinar Ultraviolet
Spektrofotometri serapan merupakan pengukuran suatu interaksi antara
radiasi elektromagnetik dan molekul atau atom dari suatu zat kimia. Teknik yang
sering digunakan dalam analisis farmasi meliputi spektroskopi serapan ultraviolet,
sinar tampak, infra merah, dan serapan atom (Ditjen POM, 1995). Keuntungan
utama dari metode spektrofotometri yaitu dapat menetapkan kadar suatu zat yang
sangat kecil (Bassett, dkk, 1994).
Spektrofotometer Ultraviolet dan Visibel adalah pengukuran panjang
gelombang dan intensitas sinar ultraviolet dan cahaya tampak yang diabsorbsi
oleh sampel. Sinar ultraviolet dan cahaya tampak memiliki energi yang cukup
untuk mempromosikan elektron pada kulit terluar ke tingkat energi yang lebih
tinggi. Spektrofotometer Ultraviolet dan Visibel biasanya digunakan untuk
molekul dan ion organik atau kompleks di dalam larutan. Spektrum Ultraviolet
dan Visibel sangat berguna untuk pengukuran secara kuantitatif. Konsentrasi dari
analit di dalam larutan bisa ditentukan dengan mengukur absorbansi pada panjang
gelombang tertentu dengan menggunakan hukum Lambert-Beer. Sinar ultraviolet
berada pada panjang gelombang 400-800 nm (Dachriyanus, 2004).
Panjang gelombang cahaya UV atau cahaya tampak bergantung pada
mudahnya promosi elektron. Molekul-molekul yang memerlukan lebih banyak
energi untuk promosi elektron, akan menyerap pada panjang gelombang yang
pada panjang gelombang yang lebih panjang. Senyawa yang menyerap cahaya
dalam daerah tampak mempunyai elektron yang lebih mudah dipromosikan
daripada senyawa yang menyerap pada panjang gelombang UV yang lebih pendek
(Gandjar dan Rohman, 2007).
Metode spektrofotometri langsung seperti analisis ultraviolet banyak
digunakan di dalam analisis tetapi biasannya kurang selektif. Selektivitas atau
kekhasan dapat ditingkatkan melalui pemisahan atau dengan mereaksikan gugus
fungsional yang sesuai. Misalnya dengan menambahkan reagensia tertentu
sehingga dihasilkan warna yang kemudian diukur pada daerah visibel (Gandjar
dan Rohman, 2007).
Warna sinar tampak dapat dihubungkan dengan panjang gelombangnya.
Sinar putih mengandung radiasi pada semua panjang gelombang di daerah sinar
tampak. Sinar pada panjang gelombang tunggal (radiasi monokromatik) dapat
dipilih dari sinar putih. Spektrofotometer yang sesuai untuk pengukuran di daerah
spektrum ultraviolet dan sinar tampak terdiri atas suatu sistem optik dengan
kemampuan menghasilkan sinar monokromatis dalam jangkauan panjang
gelombang 200-800 nm (Gandjar dan Rohman, 2007).
Alat spektrofotometri pada dasarnya terdiri atas sumber sinar,
monokromator, tempat sel untuk zat yang diperiksa, detektor, penguat arus, dan
alat ukur atau pencatat. Spektrofotometer dapat bekerja secara otomatik ataupun
tidak, dan dapat mempunyai sistem sinar tunggal dan ganda (Ditjen POM, 1979).
Sebagai sumber cahaya biasanya digunakan lampu hidrogen atau
cahaya tampak. Panjang gelombang dari sumber cahaya akan dibagi oleh
pemisahan atau monokromator (Dachriyanus, 2004).
2.5 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap
parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan
bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita,
2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi
metode analisis adalah sebagai berikut:
a. Kecermatan
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil
analisis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai
persen perolehan kembali (recovery) analit yang ditambahkan. Kecermatan
ditentukan dengan dua cara, yaitu: metode simulasi (Spiked-placebo recovery) dan
metode penambahan baku (standart addition method).
Metode simulasi (Spiked-placebo recovery) merupakan metode yang
dilakukan dengan cara menambahkan sejumlah analit bahan murni ke dalam suatu
bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan
hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar yang
sebenarnya) (Harmita, 2004).
Metode penambahan baku (standard addition method) merupakan metode
yang dilakukan dengan cara menambahkan sejumlah analit dengan konsentrasi
divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa
penambahan sejumlah analit. Persen perolehan kembali ditentukan dengan
menentukan berapa persen analit yang ditambahkan ke dalam sampel dapat
ditemukan kembali (Harmita, 2004).
b. Keseksamaan (presisi)
Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat
kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Keseksamaan atau presisi diukur sebagai
simpangan baku atau simpangan baku relatif (koefisien variasi). (Harmita, 2004).
c. Batas deteksi (Limit of detection) dan batas kuantitasi (Limit of
quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
BAB III
METODE PENELITIAN 3.1 Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Farmasi Kualitatif
Fakultas Farmasi Universitas Sumatera Utara dan di Laboratorium Penelitian
Fakultas Farmasi Universitas Sumatera Utara pada bulan April 2013 – Juni 2013.
3.2 Bahan-bahan 3.2.1 Sampel
Sampel yang digunakan dalam penelitian ini adalah buah naga daging
merah (Hylocereus costaricensis) dan buah naga daging putih (Hylocereus
undatus) yang diperoleh dari Berastagi Supermarket, Jalan Jenderal Gatot
Subroto.
3.2.2 Pereaksi
Pereaksi yang digunakan dalam penelitian ini adalah bahan yang
berkualitas pro analis dari E. Merck yaitu asam nitrat pekat 65% b/v, ammonium
molibdat, asam sulfat 96% v/v, asam askorbat, larutan baku kalsium 1000 µg/ml,
kalium dihidrogen fosfat, kalium antimonil tartrat, kecuali aquabides dari
Laboratorium Penelitian Fakultas Farmasi USU.
3.3 Alat-alat
Alat-alat yang digunakan adalah Spektrofotometer Serapan Atom Hitachi
neraca analitik, tanur, oven, hot plate, blender, krus porselen, kertas saring
Whatman No. 42, dan alat-alat gelas (Pyrex).
3.4 Identifikasi Sampel
Identifikasi buah naga dilakukan di Laboratorium Taksonomi Tumbuhan
Departemen Biologi Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara. Hasil identifikasi dapat dilihat pada Lampiran 18,
halaman 75-76.
3.5 Pembuatan Pereaksi 3.5.1 Larutan HNO3 (1:1) v/v
Larutan HNO3 65% b/v sebanyak 500 ml diencerkan dengan aquabides
hingga 500 ml (Helrich, 1990).
3.5.2 Larutan H2SO4 1 N
Sebanyak 3 ml larutan H2SO4 96% v/v diencerkan dengan aquabides
hingga 100 ml (Ditjen POM, 1979).
3.5.3 Larutan HNO3 5 N
Larutan HNO3 65% b/v sebanyak 172 ml diencerkan dengan aquabides
hingga 500 ml (Ditjen POM, 1979).
3.5.4 Larutan H2SO4 5 N
Dipipet 70 ml H2SO4 96% v/v, dimasukkan perlahan-lahan melalui
dinding ke dalam labu tentukur 500 ml yang telah berisi aquabides setengahnya.
Dicukupkan volumenya dengan aquabides hingga garis tanda (Lancashire, 2006).
Ditimbang secara seksama 20 g ammonium molibdat. Dilarutkan ke dalam
labu tentukur 500 ml dengan aquabides dan dicukupkan volumenya dengan
aquabides hingga garis tanda (Lancashire, 2006).
3.5.6 Larutan Asam Askorbat 0,1 N
Ditimbang secara seksama 0,88 g asam askorbat dan dilarutkan dalam labu
tentukur 50 ml dengan aquabides dan dicukupkan volumenya dengan aquabides
hingga garis tanda (Lancashire, 2006).
3.5.7 Larutan Kalium Antimonil Tartrat 0,274% b/v
Ditimbang secara seksama 0,274 g kalium antimonil tartrat, dilarutkan
dalam labu tentukur 100 ml dengan aquabides dan dicukupkan volumenya dengan
aquabides hingga garis tanda (Lancashire, 2006).
3.5.8 Larutan Pengembang Warna Fosfor
Dicampur 500 ml asam sulfat 5 N, 150 ml ammonium molibdat 4% b/v,
300 ml asam askorbat 0,1 N dan 50 ml kalium antimonil tartrat 0,274% b/v
(Lancashire, 2006).
3.6 ProsedurPenelitian 3.6.1 Pengambilan Sampel
Metode pengambilan sampel dilakukan dengan cara sampling purposif,
yaitu sampel ditentukan atas dasar pertimbangan bahwa semua sampel
Sampel diperoleh dari Berastagi Supermarket, Jalan Jenderal Gatot
Subroto, Medan, yaitu buah naga daging merah (Hylocereus costaricensis) dan
buah naga daging putih (Hylocereus undatus).
3.6.2 Penyiapan Sampel
Buah naga daging merah (Hylocereus costaricensis)dan buah naga daging
putih (Hylocereus undatus) masing-masing ditimbang sebanyak + 0,7 kg dengan
neraca kasar. Kemudian dibersihkan dengan air mengalir, dicuci bersih dan
ditiriskan. Selanjutnya dikeringkan dengan menggunakan tisu. Kemudian buah
naga dikupas kulitnya, setelah itu daging buahnya dipotong kecil-kecil sebesar
satu ruas jari tangan. Lalu dihaluskan dengan menggunakan blender tanpa
penambahan aqua. Sampel yang telah dihaluskan ditimbang secara seksama
dengan neraca analitik masing-masing sebanyak 30 gram ke dalam krus porselen
yang sebelumnya sudah ditara dengan neraca.
3.6.3 Proses Destruksi Kering
Sampel yang telah dimasukkan ke dalam krus porselen dipanaskan di atas
hot plate sampai kering dan mengarang. Diabukan di tanur dengan temperatur
awal 100oC dan perlahan-lahan temperatur dinaikkan menjadi 500oC dengan
interval 25oC setiap 5 menit. Pengabuan dilakukan selama 36 jam dan dibiarkan
hingga dingin dalam desikator. Abu ditambahkan 5 ml HNO3 (1:1), kemudian
diuapkan pada hot plate sampai kering, kemudian dimasukkan kembali ke dalam
tanur dengan temperatur awal 100oC dan perlahan – lahan temperatur dinaikkan
hingga suhu 500oC dengan interval 25oC. Pengabuan dilakukan selama + 1 jam
dalam desikator (Helrich, 1990). Bagan alir proses destruksi kering pada sampel
dapat dilihat pada Lampiran 3, halaman 46.
3.6.4 Pembuatan Larutan Sampel
Sampel hasil destruksi (berasal dari 30 gram sampel) yang telah dingin
dilarutkan dalam 5 ml HNO3 (1:1) di dalam krus porselen, lalu dimasukkan ke
dalam labu tentukur 50 ml menggunakan corong gelas. Sisa pada krus porselen
dibilas tiga kali dengan aquabides dan hasil pembilasan dimasukkan ke dalam
labu tentukur. Dicukupkan volumenya dengan aquabides hingga garis tanda
(Helrich, 1990). Larutan dalam labu tentukur disaring dengan kertas saring
Whatman No. 42 dan 5 ml filtrat pertama dibuang untuk menjenuhkan kertas
saring kemudian filtrat selanjutnya ditampung dalam botol. Filtrat ini digunakan
sebagai larutan sampel untuk analisis kualitatif dan kuantitatif kalsium dan fosfor.
Bagan alir pembuatan larutan sampel dapat dilihat pada Lampiran 4, halaman 47.
3.6.5 Analisis Kualitatif
3.6.5.1 Analisis Kualitatif Kalsium 3.6.5.1.1 Uji Nyala Ni/Cr
Kawat Ni/Cr dibersihkan dengan kawat ke dalam tabung yang berisi HCl
pekat lalu dipijar pada api bunsen sampai tidak memberikan warna khusus pada
nyala bunsen. Kemudian kawat dibasahi dengan HCl pekat lalu dicelupkan ke
dalam sampel lalu dipijar pada api bunsen, diamati warna yang terjadi pada nyala
bunsen. Jika terdapat kalsium akan terbentuk warna merah bata pada nyala bunsen
(Vogel,1979).
Larutan sampel sebanyak 1-2 tetes diteteskan pada object glass kemudian
ditetesi dengan larutan asam sulfat 1 N lalu diamati di bawah mikroskop. Jika
terdapat kalsium akan terlihat kristal berbentuk jarum (Vogel, 1979).
3.6.5.2 Analisis Kualitatif Fosfor
Analisis kualitatif fosfor dapat dilakukan dengan pereaksi ammonium
molibdat. Analisis kualitatif dilakukan pada larutan sampel dengan cara:
a. Ke dalam tabung reaksi dimasukkan 2 ml larutan sampel, ditambah
pereaksi ammonium molibdat 4% b/v sebanyak 2 ml, dikocok dan
didiamkan, maka akan terbentuk endapan kuning (Vogel, 1979).
b. Ke dalam tabung reaksi dimasukkan 2 ml larutan sampel, ditambah
pereaksi barium klorida 4% b/v sebanyak 1 ml, maka akan terbentuk
endapan putih (Vogel, 1979).
3.6.6 Analisis Kuantitatif
3.6.6.1 Analisis Kuantitatif Kalsium
3.6.6.1.1 Pembuatan Kurva Kalibrasi Kalsium
Larutan baku kalsium (konsentrasi 1000 µg/ml) dipipet sebanyak 1,0 ml,
dimasukkan ke dalam labu tentukur 100 ml dan dicukupkan hingga garis tanda
dengan aquabides (konsentrasi 10 µg/ml). Larutan untuk kurva kalibrasi kalsium
dibuat dengan memipet (2,5; 5; 7,5; 10; dan 12,5) ml dari larutan baku 10 µg/ml,
masing-masing dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan
volumenya masing-masing hingga garis tanda dengan aquabides (larutan ini
mengandung (1,0; 2,0; 3,0; 4,0 dan 5,0) µg/ml) dan diukur absorbansinya
menggunakan spektrofotometer serapan atom pada panjang gelombang 422,7 nm
3.6.6.1.2 Penetapan Kadar Kalsium dalam Sampel
Larutan sampel hasil destruksi yang berasal dari buah naga daging merah
(Hylocereus costaricensis) dipipet sebanyak 1,0 ml dimasukkan ke dalam labu
tentukur 25 ml dan dicukupkan dengan aquabides sampai garis tanda (Faktor
pengenceran = 25/1 = 25 kali). Sedangkan larutan sampel hasil destruksi yang
berasal dari buah naga daging putih (Hylocereus undatus) dipipet sebanyak 2,0 ml
dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan dengan aquabides
sampai garis tanda (Faktor pengenceran = 25/2 = 12,5 kali). Lalu diukur
absorbansinya dengan menggunakan spektrofotometer serapan atom pada panjang
gelombang 422,7 nm dengan nyala udara-asetilen. Nilai absorbansi yang
diperoleh harus berada dalam rentang kurva kalibrasi larutan baku kalsium
sehingga konsentrasi kalsium dapat dihitung dengan menggunakan persamaan
garis regresinya.
Konsentrasi kalsium dalam sampel ditentukan berdasarkan persamaan
garis regresi dari kurva kalibrasi. Kadar kalsium dalam sampel dapat dihitung
dengan cara sebagai berikut:
Kadar logam (µg/g)= ������������ µ�
��������� (��)�����������������
����������� (�)
3.6.6.2 Analisis Kuantitatif Fosfor
3.6.6.2.1 Pembuatan Larutan Induk Baku KH2PO4 (LIB I)
Ditimbang secara seksama 0,0439 g KH2PO4 yang telah dikeringkan di
dalam oven dengan suhu 105oC, kemudian dimasukkan ke dalam labu tentukur
100 ml, ditambahkan 5 ml larutan HNO3 5 N, dikocok hingga larut, dicukupkan
3.6.6.2.2 Penentuan Waktu Kerja
Dari LIB I dipipet 3,0 ml, dimasukkan ke dalam labu tentukur 50 ml,
dicukupkan volume dengan aquabides hingga garis tanda (konsentrasi 6 µg/ml).
Dipipet 1,0 ml larutan tersebut, ditambahkan 5,0 ml aquabides dan 1,0 ml larutan
pengembang warna fosfor, dikocok kemudian diukur absorbansinya menggunakan
spektrofotometer UV-Visible pada panjang gelombang 711 nm mulai menit ke-1
hingga menit ke-74 dengan interval waktu 1 menit (Sitompul, 2009).
3.6.6.2.3 Pembuatan Kurva Serapan Larutan KH2PO4
Dari LIB I dipipet 3,0 ml, dimasukkan ke dalam labu tentukur 50 ml,
dicukupkan volume dengan aquabides hingga garis tanda (konsentrasi 6 µg/ml).
Dipipet 1,0 ml larutan tersebut, ditambahkan 5,0 ml aquabides dan 1,0 ml larutan
pengembang warna fosfor, dikocok lalu didiamkan, kemudian diukur
absorbansinya menggunakan spektrofotometer UV-Visible pada panjang
gelombang 400-800 nm pada menit ke-31 (Sitompul, 2009).
3.6.6.2.4 Pembuatan Kurva Kalibrasi Larutan Baku Fosfor
Larutan untuk kurva kalibrasi kalsium dibuat dengan memipet (0,5; 1,0;
1,5; 2,0; dan 2,5) ml dari LIB 1 (konsentrasi 100 µg/ml), masing-masing
dimasukkan ke dalam labu tentukur 25 ml dan dicukupkan volumenya
masing-masing dengan aquabides hingga garis tanda (konsentrasi 2; 4; 6; 8; dan 10
µg/ml). Dipipet 1,0 ml dari masing-masing larutan tersebut, ditambahkan 5,0 ml
aquabides dan 1,0 ml larutan pengembang warna, dikocok dan didiamkan selama
30 menit kemudian diukur menggunakan spektrofotometer UV-Visible pada
panjang gelombang 711 nm pada menit ke-31 dengan spektrofotometer sinar
3.6.6.2.5 Penetapan Kadar Fosfor dalam Sampel
Larutan sampel hasil destruksi yang berasal dari buah naga daging merah
(Hylocereus costaricensis) dan buah naga daging putih (Hylocereus undatus)
masing-masing dipipet 0,5 ml, dimasukkan ke dalam labu tentukur 25 ml, dan
dicukupkan dengan aquabides hingga garis tanda (Faktor pengenceran = 25/0,5 =
50 kali). Dari masing-masing larutan tersebut dipipet 1,0 ml kemudian
ditambahkan 5,0 ml aquabides dan 1,0 ml larutan pengembang warna fosfor,
dikocok dan didiamkan selama 30 menit. Diukur absorbansinya menggunakan
spektrofotometer UV-Visible pada panjang gelombang 711 nm dengan
spektrofotometer sinar tampak pada menit ke-31. Nilai serapan yang diperoleh
harus berada didalam rentang nilai kurva kalibrasi larutan baku, dengan demikian
konsentrasi fosfor dapat dihitung berdasarkan persamaan garis regresi linier dari
kurva kalibrasi.
Kadar fosfor dapat dihitung dengan rumus:
Kadar logam (µg/g)= ������������ µ�
��������� (��)�����������������
����������� (�)
Menurut Walpole (1995), kadar fosfor sebenarnya dalam sampel dapat
dihitung dengan rumus:
µ = x ± ((t(α/2, dk) x SD/ √n)
Keterangan: x : kadar rata-rata sampel SD : Standar Deviasi
dk : derajat kebebasan ( dk = n-1) α : tingkat kepercayaan
n : jumlah pengulangan
Menurut Sudjana (2005), kadar kalsium dan fosfor yang diperoleh dari
hasil pengukuran masing-masing larutan sampel dianalisis untuk mengetahui data
ditolak atau diterima menggunakan uji distribusi t dengan rumus:
t hitung =
n SD
X Xi
/
−
Data diterima jika –t hitung < t hitung < t tabel. Tabel distribusi t dapat dilihat
pada Lampiran 19, halaman 77.
Untuk mencari standar deviasi (SD) digunakan rumus:
SD =
(
)
1 -n
X
-Xi 2
∑
Keterangan : Xi = Kadar sampel
X = Kadar rata-rata sampel n = jumlah pengulangan
dan untuk menentukan kadar mineral di dalam sampel dengan interval
kepercayaan 99%, α = 1%, dk = n-1, dapat digunakan rumus:
Kadar Mineral : µ = X ± ((tα/2, dk) x SD / √n ) Keterangan :
−
X = Kadar rata-rata sampel SD = Standar Deviasi
dk = Derajat kebebasan (dk = n-1) α = taraf kepercayaan
n = jumlah pengulangan
3.6.7.2 Pengujian Beda Nilai Rata-Rata Antar Sampel
Menurut Sudjana (2005), sampel yang dibandingkan adalah independen
dan jumlah pengamatan masing-masing lebih kecil dari 30 dan variansi (σ) tidak
diketahui sehingga dilakukan uji F untuk mengetahui apakah variansi kedua
Fo = 2 2 2 1 S S
Keterangan : Fo = Beda nilai yang dihitung
S1 = Standar deviasi terbesar
S2 = Standar deviasi terkecil
Apabila dari hasilnya diperoleh Fo tidak melewati nilai kritis F maka
dilanjutkan uji dengan distribusi t dengan rumus:
2 1 2 1 0 1 1 ) ( n n S X X t + − = Sp 2 ) 1 ( ) 1 ( 2 1 2 2 2 2 1 1 − + − + − = n n S n S n Keterangan :
X1 = kadar rata-rata sampel 1
X2 = kadar rata-rata sampel 2
Sp = Simpangan baku
n 1 = Jumlah pengulangan sampel 1
n 2 = Jumlah pengulangan sampel 2
Jika Fo melewati nilai kritis F, dilanjutkan uji dengan distribusi t dengan rumus
2 2 2 1 2 1 2 1 0 ) ( n S n S Sp X X t + − =
Keterangan : X1 = Kadar rata-rata sampel 1
X2 = Kadar rata-rata sampel 2
n1 = Jumlah pengulangan sampel 1
n2 = Jumlah pengulangan sampel 2
S1 = Standar deviasi sampel 1
S2 = Standar deviasi sampel 2
Kedua sampel dinyatakan berbeda apabila to yang diperoleh melewati nilai
kritis t, dan sebaliknya.
3.6.8.1 Kecermatan
Kecermatan atau akurasi adalah ukuran yang menunjukkan deraajat
kedekatan hasil analisis dengan kadar analit yang sebenarnya. Kecermatan
dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan.
Uji perolehan kembali atau recovery dilakukan dengan metode penambahan
larutan baku (standard addition method). Dalam metode ini, kadar kalsium dan
fosfor dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan
kadar kalsium dan fosfor dalam sampel setelah penambahan larutan standar
dengan konsentrasi tertentu (Harmita, 2004).
Daging buah naga merah (Hylocereus costaricensis) yang telah dihaluskan
ditimbang seksama sebanyak 30 gram, lalu ditambahkan 2,3 ml larutan baku
kalsium (konsentrasi 1000 µg/ml) dan 10,0 ml larutan KH2PO4 (konsentrasi 100
µg/ml). Perlakuan tersebut dilakukan sebanyak 6 kali pengulangan. Kemudian
dilanjutkan dengan prosedur destruksi kering seperti yang telah dilakukan
sebelumnya. Pengukuran uji perolehan kembali dilakukan sama dengan prosedur
penetapan kadar dalam sampel.
Menurut Harmita (2004), persen perolehan kembali (uji recovery) dapat
dihitung dengan rumus di bawah ini (Harmita, 2004):
% recovery = 100%
A * C
C C
× − A
F
Keterangan: CF = Kadar setelah penambahan larutan baku
CA = Kadar sebelum penambahan larutan baku
C*A = Kadar larutan baku yang ditambahkan
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau
koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan
derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara
berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang
memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan
(Harmita, 2004).
Menurut Harmita (2004), simpangan baku relatif dapat dihitung dengan
rumus di bawah ini:
RSD = ×100%
X SD
Keterangan : −
X = Kadar rata-rata sampel SD = Standar Deviasi
RSD = Relative Standard Deviation
3.6.8.3 Penentuan Batas Deteksi (Limit of Detection) dan Batas Kuantitasi (Limit of Quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Sedangkan batas kuantitasi
merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi
kriteria cermat dan seksama (Harmita, 2004).
Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat
dihitung dengan rumus sebagai berikut:
Simpangan Baku ( X
SY ) =
(
)
2
2
− −
∑
n Yi Y
Batas deteksi (LOD) =
slope X SY x 3
Batas kuantitasi (LOQ) =
BAB IV
HASIL DAN PEMBAHASAN
4.1 Analisis Kualitatif Kalsium dan Fosfor pada Sampel
Analisis kualitatif dilakukan untuk mengetahui ada atau tidaknya kalsium
[image:47.596.109.519.433.634.2]dan fosfor dalam sampel. Data dapat dilihat pada Tabel 1 di bawah ini.
Tabel 1. Hasil Analisis Kualitatif Kalsium dan Fosfor pada Sampel No.
Mineral yang dianalisis
Pereaksi Hasil Reaksi Keterangan
1. Kalsium
Reaksi Nyala menggunakan kawat
Nikel-Krom
Warna nyala
Merah Bata +
H2SO4 1N Kristal jarum +
2. Fosfor
Ammonium molibdat 4% b/v
Larutan berwarna
kuning +
Barium Klorida (BaCl2)
4% b/v
Larutan dengan
endapan putih +
Pada Tabel 1 dapat dilihat hasil pengujian kualitatif bahwa sampel positif
mengandung kalsium karena menghasilkan kristal jarum dengan penambahan
asam sulfat encer serta memberikan warna nyala merah bata saat dibakar
larutan berwarna kuning dengan penambahan larutan ammonium molibdat 4% b/v
dan endapan putih dengan penambahan barium klorida 4% b/v (Vogel, 1990).
Gambar kristal dan hasil reaksi dapat dilihat pada Lampiran 2, halaman 44-45.
Hasil absorbansi dengan spektrofotometer serapan atom menunjukkan
adanya absorbansi pada panjang gelombang kalsium yaitu 422,7 nm, ini sesuai
dengan uji kualitatif kalsium dengan menggunakan kawat Ni/Cr yang
menghasilkan warna nyala merah bata seperti dilihat pada warna nyala merah bata
pada spektrofotometri serapan atom pada panjang gelombang 422,7 nm. Hasil
absorbansi dengan spektrofotometri sinar tampak menunjukkan adanya absorbansi
kompleks fosfor pada panjang gelombang 711 nm, hal ini juga sesuai dengan
reaksi warna pada fosfor dan membuktikan bahwa sampel mengandung kalsium
dan fosfor.
4.2 Analisis Kuantitatif Kalsium dan Fosfor pada Sampel 4.2.1 Analisis Kuantitatif Kalsium
4.2.1.1 Kurva Kalibrasi Kalsium
Kurva kalibrasi kalsium diperoleh dengan cara mengukur absorbansi dari
larutan standar kalsium pada panjang gelombang 422,7 nm. Dari pengukuran
kurva kalibrasi untuk kalsium diperoleh persamaan garis regresi yaitu Y =
0,03253X + 0,00365. Data dan perhitungan persamaan regresi kurva kalibrasi
dapat dilihat pada Lampiran 6, halaman 50-51.
Gambar 1. Kurva Kalibrasi Kalsium
Berdasarkan kurva di atas diperoleh hubungan yang linear antara konsentrasi
dengan absorbansi, dimana koefisien korelasi (r) untuk kalsium sebesar 0,9991.
Nilai r ≥ 0,995 menunjukkan adanya korelasi linier hubungan antara X dan Y
(Watson, 2005).
4.2.1.2 Penetapan Kadar Kalsium dalam Sampel
Penetapan kadar kalsium dilakukan secara spektrofotometri serapan atom
pada panjang gelombang 422,7 nm. Konsentrasi kalsium pada sampel ditentukan
berdasarkan persamaan garis regresi kurva kalibrasi larutan baku kalsium. Faktor
pengenceran untuk penetapan kadar kalsium pada buah naga daging merah
(Hylocereus costaricensis) adalah sebesar 25 kali dan faktor pengenceran pada
buah naga daging putih (Hylocereus undatus) adalah sebesar 12,5 kali. Data dan
contoh perhitungan dapat dilihat pada Lampiran 8 dan Lampiran 9, halaman 54
dan 56.
Selanjutnya dilakukan perhitungan statistik terhadap hasil analisis
menggunakan uji T dengan taraf kepercayaan 99% (Perhitungan statistik dapat
Tabel 2. Hasil Analisis Kuantitatif Kalsium pada Sampel
No. Sampel Buah Naga Kadar (mg/100 g)
1 Buah Naga Daging Merah 7,7212 ± 0,0581
2 Buah Naga Daging Putih 3,3884 ± 0,0435
4.2.2 Analisis Kuantitatif Fosfor
4.2.2.1 Penentuan Panjang Gelombang Absorbsi Maksimum Senyawa Kompleks Fosfor Molibdat
Kurva penentuan panjang gelombang absorbsi maksimum senyawa
[image:50.596.160.461.296.475.2]kompleks fosfor molibdat dapat dilihat pada Gambar 2.
Gambar 2. Kurva Serapan Senyawa Kompleks Fosfor Molibdat pada Konsentrasi 6 µg/ml.
Gambar 3. Absorbansi Panjang Gelombang Maksimum Larutan Standar Fosfor Pada Konsentrasi 6 µg/ml
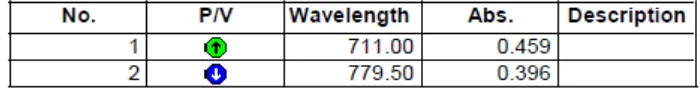
4.2.2.2 Penentuan Waktu Kerja Kompleks Fosfor Molibdat pada Panjang Gelombang Maksimum 711 nm
Untuk menentukan waktu kerja senyawa kompleks fosfor molibdat,
digunakan larutan baku KH2PO4 dengan konsentrasi 6 µg/ml dan diukur
[image:50.596.142.492.532.576.2]ke-74. Dari penentuan waktu kerja kompleks fosfor molibdat didapatkan waktu kerja
yang stabil selama 12 menit pada menit ke-30 sampai menit ke-41. (data dapat
dilihat pada Lampiran 5, halaman 48-49).
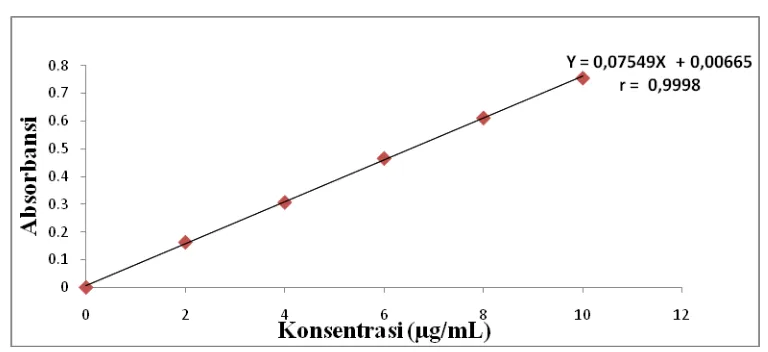
4.2.2.3 Kurva Kalibrasi Fosfor
Kurva kalibrasi fosfor diperoleh dengan cara mengukur absorbansi dari
larutan baku KH2PO4 pada panjang gelombang 711 nm. Dari pengukuran kurva
kalibrasi untuk fosfor diperoleh persamaan garis regresi yaitu Y = 0,07549X +
0,00665. Data dan hasil perhitungan persamaan garis regresi kurva kalibrasi fosfor
dapat dilihat pada Lampiran 7, halaman 52-53.
[image:51.596.120.504.353.529.2]Kurva kalibrasi larutan baku KH2PO4 dapat dilihat pada Gambar 4.
Gambar 4. Kurva Kalibrasi Fosfor
Berdasarkan kurva di atas diperoleh hubungan yang linear antara konsentrasi
dengan absorbansi, yaitu koefisien korelasi (r) untuk fosfor sebesar 0,9998. Nilai r
≥ 0,995 menunjukkan adanya korelasi linier hubungan antara X dan Y (Watson,
2005).
4.2.2.4 Penetapan Kadar Fosfor dalam Sampel
Penetapan kadar fosfor dilakukan secara spektrofotometri sinar tampak.
ammonium molibdat yang berasal dari campuran larutan pengembang warna yang
terdiri dari asam sulfat, ammonium molibdat, asam askorbat dan kalium antimonil
tartrat membentuk senyawa kompleks fosfomolibdat. Senyawa kompleks
fosfomolibdat membentuk senyawa yang berwarna biru yang stabil selama 12
menit yang diukur pada menit ke-31 dan diukur pada λ = 711 nm. Konsentrasi
fosfor pada sampel ditentukan berdasarkan persamaan regresi kurva kalibrasi
larutan baku KH2PO4. Faktor pengenceran untuk penetapan kadar fosfor pada
buah naga daging merah (Hylocereus costaricensis) dan buah naga putih
(Hylocereus undatus) adalah sebesar 50 kali. Data dan contoh perhitungan dapat
dilihat pada Lampiran 8 dan Lampiran 9, halaman 54-57.
Kemudian dilakukan perhitungan statistik terhadap hasil analisis
menggunakan uji distribusi t dengan taraf kepercayaan 99% (Perhitungan dapat
dilihat pada Lampiran 11, halaman 61-63). Hasil analisis kuantitatif fosfor dan
pada sampel dapat dilihat pada Tabel 3.
Table 3. Hasil Analisis Kuantitatif Fosfor pada Sampel
No. Sampel Buah Naga Kadar (mg/100 g)
1 Buah Naga Daging Merah 32,5206 ± 0,4119
2 Buah Naga Daging Putih 36,5592 ± 0,5146
4.2.3 Pengujian Beda Nilai Rata-Rata Antar Sampel
Data yang didapat kemudian diuji kembali secara statistik untuk
mengetahui beda nilai kadar rata-rata mineral antar kedua sampel (Perhitungan
dapat dilihat pada Lampiran 12 dan Lampiran 13, halaman 64-67). Hasil
perhitungan uji statistik dapat dilihat pada Tabel 4.
Tabel 4. Hasil Uji Beda nilai rata-rata kadar kalsium dan fosfor antar sampel
BNP
2. Fosfor BNM -24,7160 -3,1693 Beda
BBNP Keterangan :
BNM : Buah Naga Daging Merah (Hylocereus costaricensis) BNP : Buah Naga Daging Putih (Hylocereus undatus)
Berdasarkan Tabel 2 dan 3 dapat diketahui bahwa kadar kalsium dalam
buah naga daging merah (Hylocereus costaricensis) lebih besar dibandingkan
kadar kalsium di dalam buah naga daging putih (Hylocereus undatus) sedangkan
kadar fosfor lebih kecil dalam buah naga daging merah (Hylocereus costaricensis)
daripada kadar fosfor dalam buah naga daging putih (Hylocereus undatus). Hal ini
menunjukkan bahwa jenis buah naga yang berbeda mengandung kalsium dan
fosfor dengan kadar yang berbeda pula. Perbedaan ini dapat disebabkan oleh
varietas tumbuhan dimana varietas berpengaruh terhadap kemampuan
metabolisme senyawa di dalam tumbuhan yang dikendalikan oleh faktor genetik.
Selain faktor genetik, kemampuan metabolisme senyawa juga dapat dipengaruhi
oleh faktor lingkungan (cahaya, panas, air, susunan dan tanah) (Harris dan
Karmas, 1989).
4.2.4 Validasi Metode Analisis 4.2.4.1 Kecermatan (Akurasi)
Hasil uji perolehan kembali (recovery) kadar kalsium dan fosfor setelah
penambahan masing-masing larutan baku kalsium dan fosfor dalam sampel dapat
dilihat pada Lampiran 15, halaman 70. Perhitungan persen recovery kalsium dan
fosfor dalam sampel dapat dilihat pada Lampiran 16, halaman 71-72. Persen
recovery kalsium dan fosfor dalam sampel dapat dilihat pada Tabel 5.
[image:53.596.112.515.85.139.2]