POTENSI SENYAWA
β
-KARIOFILENA DAN ISOEUGENOL
DARI MINYAK ATSIRI CENGKIH (Syzygium aromaticum)
SEBAGAI PELANGSING AROMATERAPI SECARA IN VIVO
FAHMI HASIM
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul Potensi Senyawa β -Kariofilena dan Isoeugenol dari Minyak Atsiri Cengkih (Syzygium aromaticum) sebagai Pelangsing Aromaterapi secara In Vivo adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, November 2015
Fahmi Hasim
RINGKASAN
FAHMI HASIM. Potensi Senyawa β-Kariofilena dan Isoeugenol dari Minyak Atsiri Cengkih (Syzygium aromaticum) sebagai Pelangsing Aromaterapi secara In Vivo. Dibimbing oleh IRMANIDA BATUBARA dan IRMA HERAWATI SUPARTO.
Aromaterapi didefinisikan sebagai suatu metode terapi alternatif menggunakan bahan mudah menguap yang berasal dari tanaman, seperti minyak atsiri dan senyawa aromatik lainnya. Aromaterapi dapat menjadi solusi untuk menggantikan obat sintetik dalam mengatasi masalah obesitas. Kondisi obesitas perlu ditangani karena dapat menyebabkan beberapa penyakit degeneratif, seperti hiperkolesterol, aterosklerosis, diabetes, tekanan darah tinggi, dan penyakit jantung koroner. Salah satu tanaman herbal Indonesia yang mengandung minyak atsiri ialah cengkih (Syzygium aromaticum). Cengkih mengandung minyak atsiri yang terdiri atas eugenol dan β-kariofilena, serta senyawa lain yang biasa digunakan sebagai bahan baku parfum. Tujuan penelitian ini adalah mengisolasi β-kariofilena dan mendapatkan isoeugenol melalui reaksi isomerisasi eugenol dari minyak atsiri daun cengkih, serta menganalisis potensinya sebagai pelangsing aromaterapi secara in vivo.
Minyak cengkih diekstraksi menggunakan larutan alkalin hingga diperoleh eugenol dan ekstrak nonpolar. Persen perolehan kembali eugenol dan rendemen ekstrak nonpolar yang diperoleh sebesar 83% dan 15%. Hasil analisis kromatografi gas-spektrometri massa menunjukkan bahwa isolat eugenol mengandung eugenol dengan kadar 85%. Sementara itu, senyawa dominan pada ekstrak nonpolar adalah
β-kariofilena sebesar 35%. Isolasi β-kariofilena menggunakan kromatografi lapis tipis preparatif (KLTP) menghasilkan 6 spot terpisah. Spot dengan nilai Rf 0.95 dikoleksi karena memiliki nilai Rf yang sama dengan Rfstandar β-kariofilena, yakni 0.95. Persen perolehan kembali yang diperoleh sebesar 96% dengan kadar 83%. Sementara itu, produk isomerisasi yang diperoleh masih berupa campuran antara eugenol, cis-isoeugenol, dan trans-isoeugenol dengan waktu retensi 10.62 menit dengan persen area sebesar 96%.
Hasil uji in vivo menunjukkan bahwa inhalasi isoeugenol dengan kadar 1% selama 5 minggu berpotensi sebagai pelangsing aromaterapi dengan cara menurunkan bobot deposit lemak tikus. Uji profil lipid menunjukkan terjadinya penurunan kadar trigliserida pada kelompok minyak cengkih dan berbeda nyata (p < 0.05) dibandingkan dengan kontrol negatif. Selain itu, kelompok yang diinhalasikan minyak cengkih juga memperlihatkan kecenderungan penurunan bobot badan yang didukung oleh peningkatan termogenesis pada jaringan adiposa cokelat melalui aktivitas saraf simpatetik.
Kata kunci: isoeugenol, minyak atsiri, minyak cengkih, pelangsing aromaterapi,
SUMMARY
FAHMI HASIM. The Potency of β-Caryophyllene and Isoeugenol of Essential Oil of Clove (Syzygium aromaticum) as Slimming Aromatheraphy by In Vivo Assay. Supervised by IRMANIDA BATUBARA and IRMA HERAWATI SUPARTO.
Aromatherapy can be defined as an alternative therapy method using volatile materials derived from plants, such as essential oil and other aromatic compounds. Aromatherapy can be one solutions replacing the synthetic drugs to overcome the obesity. Efforts to overcome obesity is necessary because it can cause many degenerative diseases, such as hypercholesterolemia, atherosclerosis, diabetes, high blood pressure and coronary heart disease. One of Indonesian herbal plants containing essential oil is clove (Syzygium aromaticum). Clove contain essential oil which consists of eugenol and β-caryophyllene and other compounds which used make perfume. The objectives of this research are to isolate β-caryophyllene, to obtain isoeugenol through isomerization reaction of eugenol of essential oil of
clove’s leaves, and to analyze its potency as slimming aromatheraphy by in vivo
assay.
Clove oil was extracted using alkaline solution until eugenol and nonpolar extract were gained. Percent recovery of eugenol and the yield of nonpolar extract were 83% and 15%, respectively. Analysis of gas chromatography-mass spectrometry showed that eugenol isolate contained eugenol with the concentration of 85%, while the nonpolar extract contained 35% of β-caryophyllene.Isolation of
β-caryophyllene using thin layer chromatography (PTLC) resulted in 6 separated-spot. The spot that has similar Rf value with β-caryophyllene standard was collected and it was at 0.95. Percent recovery obtained was 96% and containing concentration compound as 83%. Meanwhile, the isomerization products was obtained as mixture of eugenol, cis-isoeugenol and trans-isoeugenol with a retention time of 10.62 minutes and percent of area of 96%.
The results of in vivo assays showed that inhalation of isoeugenol with concentration of 1% for five weeks had a potential for slimming aromatherapy by decreasing body fat tissues of rats. Blood lipid profile showed a decrease of triglyceride concentration in the clove oil group and significantly different (p < 0.05) compared to our negative control. In addition, there was a trend of decreasing body weight for clove oil that was supported by the increase in thermogenesis of their brown adipose tissues through the activity of sympathetic nerve.
© Hak Cipta Milik IPB, Tahun 2015
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
pada
Program Studi Kimia
POTENSI SENYAWA
β
-KARIOFILENA DAN ISOEUGENOL
DARI MINYAK ATSIRI CENGKIH (Syzygium aromaticum)
SEBAGAI PELANGSING AROMATERAPI SECARA IN VIVO
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2015
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian ini ialah pelangsing aromaterapi, dengan judul Potensi Senyawa β-Kariofilena dan Isoeugenol dari Minyak Atsiri Cengkih (Syzygium aromaticum) sebagai Pelangsing Aromaterapi secara In Vivo.
Penulis mengucapkan terima kasih kepada Dr Irmanida Batubara, MSi selaku pembimbing pertama dan Dr dr Irma H Suparto, MS selaku pembimbing kedua yang senantiasa memberikan arahan, dorongan semangat, dan doa kepada penulis selama melaksanakan penelitian ini. Terima kasih juga penulis ucapkan kepada ayah, ibu, dan seluruh keluarga atas doa dan kasih sayangnya. Ucapan terima kasih juga penulis ucapkan kepada Baiq Amelia Riyandari dan Rizki Damayanti yang turut membantu selama penelitian berlangsung. Penulis juga mengucapkan terima kasih kepada staf Kependidikan Laboratorium Kimia Analitik, yaitu Bapak Eman, Ibu Nunung, Bapak Dede, dan Bapak Kosasih, serta pihak di Pusat Studi Biofarmaka Lembaga Penelitian dan Pengabdian kepada Masyarakat Institut Pertanian Bogor khususnya di unit kandang hewan percobaan (UKHP), yaitu drh Aidell dan Bapak Mulyadi. Penelitian ini merupakan bagian dari Penelitian Kerja Sama Luar Negeri dan Publikasi Internasional yang didanai oleh Direktorat Jenderal Pendidikan Tinggi dengan nomor kontrak 083/SP2H/PL/Dit.Lit abmas/II/2015 dan 489/IT3.11/LT/2015.
Semoga karya ilmiah ini bermanfaat.
Bogor, November 2015
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
1 PENDAHULUAN 1
Latar Belakang 1
Tujuan Penelitian 2
Hipotesis 2
Waktu dan Lokasi Penelitian 2
Ruang Lingkup Penelitian 3
2 METODE 3
Alat dan Bahan 3
Isolasi Eugenol 4
Penentuan Eluen Terbaik 4
Isolasi β-Kariofilena dengan KLTP 4
Reaksi Isomerisasi Eugenol menjadi Isoeugenol 5
Identifikasi Senyawa dengan GC-MS 5
Uji In Vivo pada Tikus Putih Jantan Galur Sprague-Dawley 5
Penentuan Bobot Deposit Lemak pada Hewan Uji 6
Uji Aktivitas Saraf Simpatetik 6
Analisis Profil Lipid 7
Uji Statistik 8
3 HASIL DAN PEMBAHASAN 8
Isolasi Eugenol dan Ekstrak Nonpolar 8
Penentuan Eluen Terbaik dengan Kromatografi Lapis Tipis 10
Isolasi β-Kariofilena dengan KLTP 11
Reaksi Isomerisasi Eugenol menjadi Isoeugenol 13 Bobot Badan, Pakan, Feses dan Urin, serta Lemak Tubuh Terhadap Efek
Inhalasi 14
Analisis Profil Lipid 18
4 SIMPULAN DAN SARAN 20
Simpulan 20
Saran 21
DAFTAR PUSTAKA 21
LAMPIRAN 25
DAFTAR TABEL
1 Komposisi senyawa di dalam minyak cengkih, eugenol, ekstrak
nonpolar, dan β-kariofilena 10
2 Posisi sinyal-sinyal 1H-NMR isoeugenol dalam pelarut CD3OD 14 3 Rerata bobot badan tikus pada akhir masa adaptasi dan masa perlakuan 15 4 Rerata konsumsi pakan dan ekskresi feses dan urin pada akhir masa
adaptasi dan masa perlakuan 16
5 Rerata kadar kolesterol total pada akhir masa adaptasi dan perlakuan 19
6 Rerata kadar HDL-c pada akhir masa perlakuan 19
7 Rerata kadar trigliserida pada akhir masa adaptasi dan perlakuan 20
DAFTAR GAMBAR
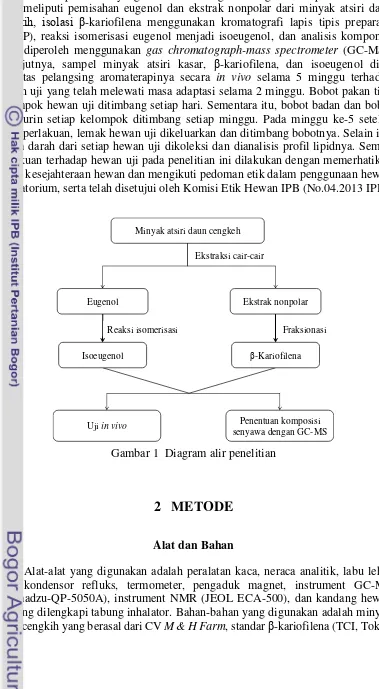
1 Diagram alir penelitian 3
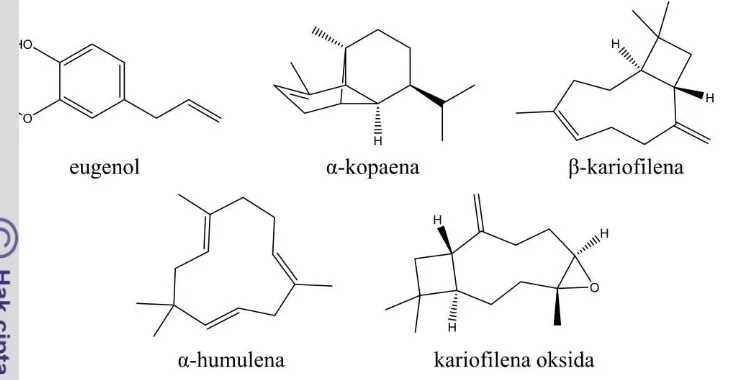
2 Beberapa senyawa yang terkandung di dalam minyak daun cengkih 9
3 Mekanisme reaksi isolasi eugenol 9
4 Sampel, (i) minyak atsiri daun cengkih, (ii) isolat eugenol, dan (iii)
ekstrak nonpolar 10
5 Kromatogram lapis tipis ekstrak nonpolar dengan eluen campuran n
-heksana dan etil asetat 11
6 Hasil pemisahan β-kariofilena dengan KLTP pada ʎ = 254 nm 12
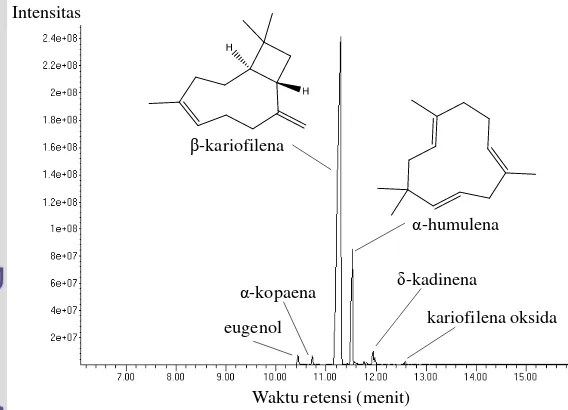
7 Kromatogram GC-MS isolat β-kariofilena 12
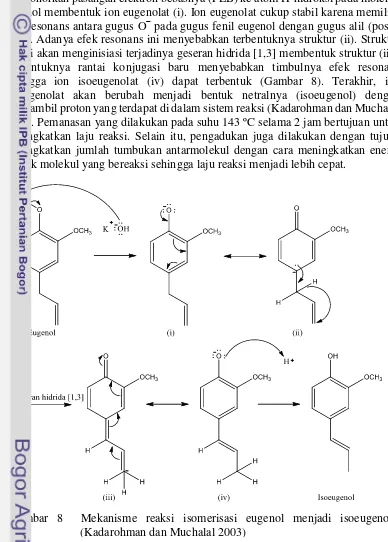
8 Mekanisme reaksi isomerisasi eugenol menjadi isoeugenol 13 9 Persen rerata perubahan bobot badan tikus setiap minggu selama masa
perlakuan 15
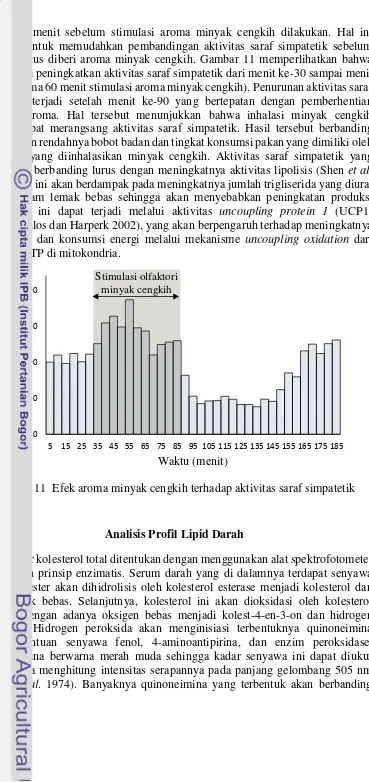
10 Persentase deposit lemak/bobot badan pada akhir perlakuan 17 11 Efek aroma minyak cengkih terhadap aktivitas saraf simpatetik 18
DAFTAR LAMPIRAN
1 Komposisi pakan yang diberikan kepada hewan uji 25
2 Kelompok perlakuan pada hewan uji 26
3 Penentuan bobot jenis minyak cengkih 27
4 Persen perolehan kembali isolat eugenol 27
5 Kromatogram GC-MS, (a) minyak atsiri daun cengkih, (b) isolat
eugenol, dan (c) ekstrak nonpolar 28
6 Rendemen pemisahan ekastrak nonpolar 29
1
PENDAHULUAN
Latar Belakang
Salah satu masalah kesehatan global yang paling serius dan telah mencapai status epidemik ialah obesitas. Pada tahun 2008, WHO (2014) melaporkan bahwa lebih dari 200 miliar pria dan 300 miliar wanita menderita obesitas. Kegemukan dan obesitas akan meningkatkan risiko kematian dan terkena berbagai penyakit. Sekitar 3.4 juta orang dewasa meninggal setiap tahun akibat menderita obesitas, sedangkan sisanya mengalami berbagai penyakit, di antaranya 44% menderita diabetes, 23% mengalami penyakit jantung iskemik, dan 7-41% mengalami kanker (WHO 2014). Giannessi et al. (2008) menyatakan bahwa penyakit degeneratif yang dapat ditimbulkan oleh obesitas, antara lain hiperkolesterol, penyempitan pembuluh darah, diabetes, tekanan darah tinggi, dan penyakit jantung koroner.
Berbagai cara telah dikembangkan untuk mengatasi masalah obesitas, salah satunya dengan menggunakan obat pelangsing, seperti sibutarmin dan orlistat. Sibutarmin merupakan obat antiobesitas yang bekerja dengan cara menekan nafsu makan dan meningkatkan aktivitas termogenesis. Hal ini dilakukan dengan cara menghambat penggunaan kembali norepinefrina dan serotonin di dalam sistem saraf pusat (Li dan Cheung 2009). Sementara itu, orlistat juga merupakan obat antiobesitas yang bekerja dengan cara menghambat aktivitas enzim lipase dalam menghidrolisis lemak (Lewis dan Liu 2012). Kedua jenis obat tersebut tergolong dalam obat sintetik dengan beberapa efek samping. Li dan Cheung (2011) melaporkan bahwa sibutarmin dapat meningkatkan risiko terkena penyakit kardiovaskular. Sementara itu, orlistat juga diketahui dapat menyebabkan diare, dispepsia, flatulens, dan perut kembung (Snow et al. 2005). Oleh karena itu, pengembangan metode terapi antiobesitas yang tidak menggunakan obat sintetik menjadi ranah penelitian yang menarik untuk dikaji lebih lanjut, seperti metode aromaterapi.
Aromaterapi didefinisikan sebagai suatu metode terapi alternatif menggunakan bahan mudah menguap yang berasal dari tanaman, seperti minyak atsiri dan senyawa aromatik lainnya (Shah et al. 2011). Mekanisme aromaterapi dalam menurunkan bobot badan telah dilaporkan berkaitan dalam memengaruhi sistem saraf simpatetik yang berada di hipotalamus (Shimazu 1981; Diego et al. 1998). Sebelumnya, kajian mengenai minyak atsiri dalam memengaruhi bobot badan telah beberapa kali dilakukan. Minyak atsiri jeruk dilaporkan dapat menstimulasi saraf simpatetik dan mengendalikan jaringan adiposa putih dan cokelat (Niijima dan Nagai 2003; Shen et al. 2005a). Selain itu, minyak jeruk juga teramati dapat menghambat saraf parasimpatetik lambung, meningkatkan lipolisis, dan suhu tubuh, serta menekan nafsu makan hewan uji sehingga berdampak pada menurunnya bobot badan (Shen et al. 2005a; Farouk et al. 2012). Hasil sebaliknya diperoleh dari minyak lavender (Shen et al. 2005b) dan minyak lempuyang gajah (Batubara et al. 2013) yang dapat menaikkan bobot badan hewan uji dengan cara menekan aktivitas saraf simpatetik dan menekan aktivitas lipolisis.
2
(Aisha et al. 2012), antibakteri (Saeed et al. 2013), dan antioksidan (Ivanovica et al. 2013). Minyak cengkih mengandung komponen utama berupa eugenol dan β -kariofilena (Jirovetz et al. 2006). Eugenol merupakan bahan utama yang biasa digunakan untuk memeroleh isoeugenol. Isoeugeol diketahui berpotensi sebagai antiinflamasi (Li et al. 2006), antioksidan (Kadoma et al. 2007; Bortolomeazzi et al. 2010; Findik et al. 2011), dan antiarthritis (Kaur dan Sultana 2012). Selain itu, isoeugenol juga merupakan senyawa alami yang biasa digunakan sebagai bahan baku parfum. Akunna et al. (2011) melaporkan bahwa aroma dari parfum dapat menurunkan bobot badan. Sementara itu, β-kariofilena memiliki potensi sebagai antiinflamasi (Fernandes et al. 2007) dan antibakteri (Huang et al. 2011).
Hasim (2014) melaporkan bahwa hasil uji aktivitas pelangsing aromaterapi secara in vivo dari minyak cengkih dan ekstrak nonpolarnya menunjukkan kecenderungan respons penurunan bobot badan yang lebih rendah dibandingkan dengan kontrol negatif, sedangkan inhalasi eugenol memperlihatkan hasil yang sebaliknya. Hasil ini mengindikasikan bahwa senyawa β-kariofilena yang terdapat di dalam minyak cengkih dan ekstrak nonpolarlah yang berpotensi sebagai pelangsing aromaterapi atau bisa juga campuran dari beberapa senyawa, yakni eugenol, β-kariofilena, α-humulena, dan kariofilena oksida pada minyak cengkih yang memiliki aktivitas sinergis dalam menurunkan bobot badan. Potensi β -kariofilena dan isoeugenol sebagai pelangsing aromaterapi belum pernah dilaporkan. Berkaitan dengan hal tersebut maka penelitian ini bertujuan memisahkan β-kariofilena yang terkandung dalam minyak atsiri daun cengkih, mengubah eugenol menjadi isoeugenol, serta menganalisis potensi dari minyak cengkih, β-kariofilena, dan isoeugenol sebagai pelangsing aromaterapi secara in vivo.
Tujuan Penelitian
Penelitian bertujuan mengisolasi β-kariofilena dan mendapatkan isoeugenol melalui reaksi isomerisasi eugenol dari minyak atsiri daun cengkih, serta menganalisis potensi dari minyak cengkih, β-kariofilena, dan isoeugenol sebagai pelangsing aromaterapi secara in vivo.
Hipotesis
Hipotesis penelitian ini adalah β-kariofilena dari minyak atsiri daun cengkih dan senyawa turunan eugenol, yakni isoeugenol memiliki aktivitas sebagai pelangsing aromaterapi.
Waktu dan Lokasi Penelitian
3
Ruang Lingkup Penelitian
Metode penelitian yang dilakukan mengikuti diagram alir pada Gambar 1 yang meliputi pemisahan eugenol dan ekstrak nonpolar dari minyak atsiri daun
cengkih, isolasi β-kariofilena menggunakan kromatografi lapis tipis preparatif (KLTP), reaksi isomerisasi eugenol menjadi isoeugenol, dan analisis komponen yang diperoleh menggunakan gas chromatograph-mass spectrometer (GC-MS). Selanjutnya, sampel minyak atsiri kasar, β-kariofilena, dan isoeugenol diuji aktivitas pelangsing aromaterapinya secara in vivo selama 5 minggu terhadap hewan uji yang telah melewati masa adaptasi selama 2 minggu. Bobot pakan tiap kelompok hewan uji ditimbang setiap hari. Sementara itu, bobot badan dan bobot feses-urin setiap kelompok ditimbang setiap minggu. Pada minggu ke-5 setelah masa perlakuan, lemak hewan uji dikeluarkan dan ditimbang bobotnya. Selain itu, serum darah dari setiap hewan uji dikoleksi dan dianalisis profil lipidnya. Semua perlakuan terhadap hewan uji pada penelitian ini dilakukan dengan memerhatikan aspek kesejahteraan hewan dan mengikuti pedoman etik dalam penggunaan hewan laboratorium, serta telah disetujui oleh Komisi Etik Hewan IPB (No.04.2013 IPB).
2
METODE
Alat dan Bahan
Alat-alat yang digunakan adalah peralatan kaca, neraca analitik, labu leher dua, kondensor refluks, termometer, pengaduk magnet, instrument GC-MS (Shimadzu-QP-5050A), instrument NMR (JEOL ECA-500), dan kandang hewan uji yang dilengkapi tabung inhalator. Bahan-bahan yang digunakan adalah minyak atsiri cengkih yang berasal dari CV M & H Farm, standar β-kariofilena (TCI, Tokyo,
Gambar 1 Diagram alir penelitian
Minyak atsiri daun cengkeh
Eugenol
Ekstraksi cair-cair
Ekstrak nonpolar
Uji in vivo Penentuan komposisi
senyawa dengan GC-MS
Isoeugenol β-Kariofilena
4
Jepang), standar isoeugenol (NT, Kyoto, Jepang), pelat aluminium jenis silika gel G60F254 dari Merck, KLTP, propiltiourasil (PTU), dan pereaksi profil lipid dari Biolabo Reagent. Hewan uji berupa tikus putih jantan galur Sprague Dawley
diperoleh dari Pusat Studi Biofarmaka IPB yang diberi pakan standar atau pakan tinggi kolesterol (Lampiran 1).
Isolasi Eugenol (Fitri dan Kawira 2006)
Sebelumnya, minyak cengkih yang diperoleh dianalisis sifat fisiknya berupa penentuan bobot jenis. Selanjutnya, minyak cengkih ditambahkan larutan NaOH 4% dengan nisbah 1:5 dan dikocok dengan kecepatan 100 rpm selama 3 jam kemudian didiamkan selama 19 jam. Selanjutnya, campuran dipisahkan dengan corong pisah sehingga diperoleh lapisan eugenol yang larut dalam NaOH dan ekstrak nonpolar. Kemudian, lapisan eugenol dipindahkan ke dalam corong pisah dan diekstraksi dengan n-heksana teknis 3 kali dengan nisbah volume fase air dan
n-heksana sebesar 1:1, 1:1/2, dan 1:1/2. Lapisan eugenol yang tidak larut dalam n -heksana dipisahkan, kemudian ditambahkan HCl 3% dengan nisbah 1:2, lalu didiamkan selama 24 jam. Selanjutnya, lapisan eugenol dipisahkan dengan corong pisah dan dicuci dengan akuades, lalu ditambahkan Na2SO4 anhidrat dan disaring.
Penentuan Eluen Terbaik (Sanchez-Munoz et al. 2012)
Pelat kromatografi lapis tipis (KLT) yang digunakan adalah pelat aluminium jenis silika gel G60F254 dari Merck dengan ukuran lebar 1 cm dan panjang 10 cm. Ekstrak nonpolar yang diperoleh dari hasil pemisahan ditotolkan pada pelat KLT sebanyak 20 kali totolan. Setelah kering, langsung dielusi dalam bejana kromatografi yang telah dijenuhkan oleh uap eluen pengembang. Proses elusi dilakukan menggunakan eluen campuran n-heksana dan etil asetat dengan variasi konsentrasi. Konsentrasi n-heksana dan etil asetat awal yang digunakan ialah 9:1 yang mengacu pada penelitian yang telah dilaporkan oleh Fernandes et al. (2007) dan Sanchez-Munoz et al. (2012) mengenai pemisahan β-kariofilena. Selanjutnya, variasi konsentrasi sebesar 6:1, 3:1, 19:1, dan 39:1 digunakan sebagai pembanding. Spot yang dihasilkan dari proses elusi masing-masing eluen diamati di bawah lampu UV pada panjang gelombang 254 dan 366 nm. Selain itu, spot yang dihasilkan juga direaksikan dengan pereaksi semprot anisaldehida-H2SO4. Eluen yang menghasilkan spot terpisah dan terbanyak dipilih sebagai eluen terbaik.
Isolasi β-Kariofilena dengan KLTP
5
Reaksi Isomerisasi Eugenol menjadi Isoeugenol (Salmoria et al. 1997)
Reaksi isomerisasi dilakukan dengan menggunakan labu leher dua yang dilengkapi dengan kondensor refluks, termometer, dan pengaduk magnet. Sebanyak 30 mL larutan KOH 4 M dalam n-butanol ditambahkan 4 g eugenol hasil pemisahan, kemudian campuran tersebut diaduk dan dipanaskan pada suhu 143 oC selama 2 jam. Setelah waktu reaksi tercapai, larutan didiamkan hingga suhunya turun, lalu dipekatkan dan disimpan di dalam refrigerator. Produk isomerisasi diuji kualitatif menggunakan KLT dan profil kromatografinya dibandingkan dengan standar isoeugenol. Setelah diperoleh profil kromatografi yang sesuai dengan profil kromatografi dari standar isoeugenol, kemudian produk isoeugenol dikarakterisasi lebih lanjut menggunakan instrumen GC-MS dan 1H-NMR (JEOL ECA-500, pelarut CD3OD).
Identifikasi Senyawa dengan GC-MS
β-Kariofilena hasil isolasi dan isoeugenol hasil reaksi isomerisasi dianalisis menggunakan GC-MS (Shimadzu-QP-5050A). Kolom: HP-5 MS, 60 m x 250 µm diameter internal x 0.25 μm ketebalan film. Suhu terprogram: dari 70 °C sampai 290 °C (selama 40 menit) dengan kenaikan suhu sebesar 15 °C/menit. Suhu injektor dan lubang injektor sama, yaitu 290 °C. Suhu detektor: 250 °C. Mode injeksi: split (50:1). Tekanan inlet: 18.03 psi. Gas pembawa berupa helium dengan laju alir 1 mL/menit. Spektrometer massa (SM) yang digunakan ialah energi ionisasi 70 eV, dengan mode ionisasinya adalah ionisasi tumbukan elektron. Suhu SM: 250 °C, suhu kuadrupol SM: 150 °C, dan suhu antarmuka: 290 °C. Area deteksinya ialah 40800 m/z. Setiap puncak yang muncul dalam kromatogram ion total diidentifikasi dengan menganalisis hasil spektrum massa yang terdapat pada library index MS.
Uji In Vivo pada Tikus Putih Jantan Galur Sprague-Dawley (Modifikasi Batubara et al. 2013)
a. Masa Adaptasi
6
b. Masa Perlakuan Aromaterapi
Uji inhalasi minyak cengkih, β-kariofilena, dan isoeugenol secara in vivo
yang dilakukan pada penelitian ini didasarkan pada metode Batubara et al. (2013). Standar β-kariofilena (TCI, Tokyo, Jepang) dan standar isoeugenol (NT, Kyoto, Jepang) digunakan pada uji inhalasi ini untuk memastikan bahwa hewan uji hanya menerima efek dari aroma molekul tersebut dan meminimalisir adanya efek dari senyawa lain. Tikus-tikus tersebut dikelompokkan menjadi 4 kelompok, yaitu kelompok I, II, III, dan IV (Lampiran 2). Masing-masing kelompok tersebut terdiri atas 6 ekor tikus. Selama masa perlakuan, semua kelompok tikus tetap diberikan pakan tinggi kolesterol dengan dosis 25 g/ekor/hari dan diberi air mineral secara ad libitum, akan tetapi pada tiap kelompok diberikan perlakuan yang berbeda. Kelompok I dijadikan kontrol negatif tanpa perlakuan inhalasi, kelompok II diinhalasi minyak cengkih, kelompok III diinhalasi standar β-kariofilena, dan kelompok IV diinhalasi standar isoeugenol. Perlakuan yang berbeda ini dilakukan selama 5 minggu. Bobot badan setiap tikus dari semua kelompok ditimbang setiap satu minggu sekali. Sisa bobot pakan yang dikonsumsi ditimbang setiap hari. Bobot feses dan urin ditimbang setiap minggu.
Penentuan Bobot Deposit Lemak pada Hewan Uji (Batubara et al. 2013)
Pada minggu ke-5 setelah masa perlakuan, setiap tikus dari setiap kelompok perlakuan, yaitu kelompok I-IV dipuasakan selama 12 jam. Tikus disedasi (pembiusan) dengan cara menyuntikkan ketamin (80 mg/kg bobot badan) dan xilazin (10 mg/kg bobot badan). Setelah tikus tidak sadarkan diri kemudian darah diambil sebanyak-banyaknya dari jantung (exsanguinous). Lemak pada bagian perut kanan dan kiri, serta sekitar testis kanan dan kiri dikumpulkan. Selanjutnya, bobot deposit lemak tersebut ditimbang.
Uji Aktivitas Saraf Simpatetik (Batubara et al. 2013)
Tikus putih jantan galur Wistar, berumur ±12 minggu dengan bobot badan 260−280 g digunakan setelah diadaptasi terhadap lingkungan selama 1 minggu. Sebelum dibedah, tikus dibius terlebih dahulu dengan uretan (1 g uretan/1 kg bobot badan). Irisan kecil dibuat di atas tulang belikat untuk memisahkan jaringan adiposa cokelat dari otot. Salah satu cabang saraf itu dibedah dan diisolasi. Saraf terisolasi ditempatkan pada sepasang elektroda kawat perak. Sinyal asli yang dihasilkan oleh elektroda, diperkuat dan disaring menggunakan Bioelectric Amplified ER-1. Sinyal yang telah diperkuat kemudian dikonversi menjadi sinyal digital oleh Power Lab
7
Analisis Profil Lipid (Biolabo 2011)
Profil lipid dari serum darah setiap tikus pada penelitian ini dianalisis sesuai dengan protokol kerja dari perusahaan Biolabo SA dengan mengunakan 1/5 dari resep. Pengujian ini dilakukan pada plat dengan 96 sumur. Analisis profil lipid dilakukan pada masa adaptasi sebagai baseline diambil dari vena ekor dan akhir masa perlakuan melalui jantung. Profil lipid yang diukur antara lain kadar kolesterol total, HDL-c, dan trigliserida. Selanjutnya, sampel darah tersebut disentrifugasi pada kecepatan 3500 rpm selama 15 menit kemudian bagian cairan jernih yang merupakan serum darah diambil dan disimpan pada suhu 4 oC untuk dianalisis pada tahap selanjutnya.
a. Pengukuran Kadar Kolesterol Total
Serum darah dipipet sebanyak 2 μL dan dimasukkan ke dalam sumur. Setelah itu, sebanyak 200 μL larutan pereaksi kolesterol dipipet ke dalam sumur yang sama. Campuran tersebut didiamkan selama 10 menit pada suhu ruang, kemudian serapannya diukur pada panjang gelombang 505 nm terhadap blangko. Pada blangko digunakan air bebas ion sebagai pengganti serum darah. Sementara itu pada pengukuran serapan standar, serum darah diganti dengan standar kolesterol. Kadar kolesterol total dihitung dengan persamaan berikut:
� = � � � × � � �� � �
Keterangan :
C : Kadar kolesterol (mg/dL) A : Serapan
Cstandar : Kadar kolesterol standar (200 mg/dL)
b. Pengukuran Kadar HDL-c
Sebanyak 500 μL serum darah dipipet ke dalam tabung sentrifuga, lalu ditambahkan 50 μL larutan pengendap dan didiamkan selama 10 menit pada suhu ruang. Setelah itu, campuran disentrifugasi pada kecepatan 4000 rpm selama 15 menit. Larutan supernatan yang terbentuk, diambil sebanyak 5 μL dan dimasukkan ke dalam sumur. Setelah itu, sebanyak 200 μL larutan pereaksi kolesterol dipipet ke dalam sumur yang sama. Campuran tersebut didiamkan selama 10 menit pada suhu ruang, kemudian serapannya diukur pada panjang gelombang 505 nm terhadap blangko. Pada blangko digunakan air bebas ion sebagai pengganti cairan supernatan. Sementara itu pada pengukuran serapan standar, cairan supernatan diganti dengan standar kolesterol. Kadar HDL-c dihitung dengan persamaan berikut:
� = � � � × � � �� � �
Keterangan :
8
Cstandar : Kadar kolesterol standar (175 mg/dL)
c. Pengukuran Kadar Trigliserida
Serum darah dipipet sebanyak 2 μL dan dimasukkan ke dalam sumur. Setelah itu, sebanyak 200 μL larutan pereaksi trigliserida dipipet ke dalam sumur yang sama. Campuran tersebut didiamkan selama 10 menit pada suhu ruang, kemudian serapannya diukur pada panjang gelombang 505 nm terhadap blangko. Pada blangko digunakan air bebas ion sebagai pengganti serum darah. Sementara itu pada pengukuran serapan standar, serum darah diganti dengan standar trigliserida. Kadar trigliserida dihitung dengan persamaan berikut:
� = � � � × � � �� � �
Keterangan :
C : Kadar trigliserida (mg/dL) A : Serapan
Cstandar : Kadar trigliserida standar (200 mg/dL)
Uji Statistik (Batubara et al. 2013)
Data bobot badan, bobot deposit lemak, dan profil lipid hewan uji yang diperoleh dianalisis dengan metode rancangan acak kelompok lengkap (RAKL) dan ANOVA (Analysis of Variance) pada taraf kepercayaan 95% (taraf α 0.05) dilanjutkan dengan Duncan’s multiple range test menggunakan SPSS 20.
3
HASIL DAN PEMBAHASAN
Isolasi Eugenol dan Ekstrak Nonpolar
Minyak atsiri cengkih komersial yang digunakan pada penelitian ini berwarna kuning dengan bobot jenis pada suhu 20 °C sebesar 1.0312 g/mL (Lampiran 3). Hasil ini sesuai dengan persyaratan mutu BSN (2006) mengenai minyak daun cengkih, yakni berwarna kuning-cokelat tua dan memiliki bobot jenis pada suhu 20 °C sebesar 1.02501.0490 g/mL. Eugenol merupakan komponen terbesar yang terdapat di dalam minyak daun cengkih (Jirovetz et al. 2006; Jayanudin 2011; Arifin
9 dan α-humulena (3.63%). Beberapa struktur senyawa yang terdapat di dalam minyak daun cengkih disajikan pada Gambar 2.
Metode ekstraksi dengan basa NaOH 4% digunakan untuk mengisolasi eugenol yang terdapat di dalam minyak cengkih. Metode ini memanfaatkan sifat asam lemah yang dimiliki oleh gugus fenol (pKa = 10.3) yang terdapat pada eugenol sehingga gugus OH pada fenol ini akan bereaksi dengan basa membentuk Na-eugenolat yang larut dalam NaOH 4%. Sementara itu lapisan non-fenol, yakni berupa komponen yang bersifat nonpolar tidak akan larut dalam NaOH 4% sehingga dapat dipisahkan menggunakan corong pisah. Reaksi ini bersifat eksoterm. Pengadukan dengan kecepatan 100 rpm bertujuan mempercepat laju reaksi yang terjadi akibat peningkatan energi kinetik molekul dan jumah tumbukan antarmolekul. Selanjutnya, lapisan fenol yang di dalamnya terdapat Na-eugenolat diekstraksi cair-cair dengan n-heksana dengan tujuan menghilangkan komponen-komponen lain yang bersifat nonpolar yang mungkin terbawa saat pemisahan berlangsung. Lapisan fenol tersebut kemudian direaksikan dengan HCl 3% dengan maksud untuk menetralkan garam berupa Na-eugenolat ke bentuk awalnya. Dua lapisan yang terbentuk, yakni lapisan fenol dan lapisan NaCl kemudian dipisahkan menggunakan corong pisah. Lapisan fenol yang di dalamnya terdapat eugenol dicuci dengan akuades untuk menghilangkan sisa asam yang ada dan ditambahkan Na2SO4 anhidrat untuk menjerap sisa air yang terdapat di lapisan tersebut. Mekanisme reaksi isolasi eugenol ditunjukkan pada Gambar 3.
Gambar 3 Mekanisme reaksi isolasi eugenol
10
Isolasi eugenol ini menghasilkan persen perolehan kembali sebesar 82.62% (b/b) (Lampiran 4), dengan kadar 84.82%. Hasil ini menunjukkan bahwa telah terjadi peningkatan kadar eugenol sebesar 44.84%. Kadar eugenol yang diperoleh sedikit lebih tinggi dibandingkan dengan yang dilaporkan oleh Arifin et al. (2015), yakni sebesar 83.23%. Pada kromatogram isolat eugenol (Lampiran 5) juga tidak menunjukkan lagi adanya senyawa β-kariofilena, α-humulena, dan kariofilena oksida yang awalnya teridentifikasi pada minyak atsiri daun cengkih. Hasil isolasi eugenol ini dapat dilihat pada Gambar 4. Selanjutnya, isolat eugenol ini akan digunakan sebagai bahan baku untuk memperoleh isoeugenol.
Sementara itu, ekstrak nonpolar yang merupakan hasil samping dari reaksi isolasi eugenol juga dikoleksi dan dianalisis menggunakan instrumen GC-MS. Rendemen ekstrak nonpolar yang diperoleh sebesar 15.03% (Lampiran 6). Hasil analisis GC-MS ini menunjukkan telah terjadi peningkatan konsentrasi senyawa yang bersifat nonpolar, seperti α-kopaena, β-kariofilena, α-humulena, dan kariofilena oksida (Tabel 1). Pada ekstrak nonpolar ini, eugenol masih dapat ditemukan akan tetapi konsentrasinya sudah menurun drastis menjadi 12.20%
Penentuan Eluen Terbaik dengan Kromatografi Lapis Tipis
Penentuan eluen terbaik dilakukan dengan membuat variasi konsentrasi menggunakan eluen campuran berupa n-heksana dan etil asetat. Hal tersebut mengacu pada penelitian yang telah dilaporkan oleh Fernandes et al. (2007) dan Gambar 4 Sampel, (i) minyak atsiri daun cengkih, (ii) isolat eugenol, dan (iii)
ekstrak nonpolar
i ii iii
Tabel 1 Komposisi senyawa di dalam minyak cengkih, isolat eugenol, ekstrak nonpolar, dan isolat β-kariofilena
Golongan Nama Fenilpropanoid Eugenol 58.56 84.82 12.20 0.98
11 Sanchez-Munoz et al. (2012) mengenai pemisahan β-kariofilena yang berhasil dilakukan dengan menggunakan eluen campuran n-heksana dan etil asetat dengan perbandingan 9:1. Ketika digunakan eluen campuran dengan perbandingan 9:1, terbentuk 4 spot dengan spot berwarna ungu yang diduga merupakan senyawa β -kariofilena (Stahl 1969) terletak sangat berdekatan dengan spot berwarna biru (Gambar 5i). Selain itu, profil kromatografi yang terbentuk juga kurang baik karena adanya spot yang berekor. Oleh karena itu, konsentrasi dari eluen campuran ini divariasikan hingga diperoleh pola pemisahan yang lebih baik.
Berdasarkan profil kromatografi yang terbentuk, ketika konsentrasi etil asetat ditingkatkan dari 10.00% (Gambar 5i) menjadi 14.29% (Gambar 5ii) dan 25.00% (Gambar 5iii) terjadi penumpukan spot di bagian atas KLT. Hal ini disebabkan oleh kemiripan sifat kepolaran senyawa-senyawa yang terdapat di dalam ekstrak nonpolar dengan kepolaran dari etil asetat. Selanjutnya, penurunan konsentrasi etil asetat dilakukan, yakni menjadi 5.00% (Gambar 5iv) dan 2.50% (Gambar 5v). Hasilnya menunjukkan pola pemisahan yang lebih baik dibandingkan dengan eluen 9:1. Eluen dengan perbandingan 19:1 dan 39:1 ini masing-masing menghasilkan 6 dan 5 spot terpisah. Skoog et al. (2004) menyatakan bahwa eluen yang dapat menghasilkan jumlah spot terbanyak dan terpisah disebut eluen terbaik sehingga eluen dengan perbandingan 19:1 dipilih sebagai eluen terbaik dan akan digunakan untuk memisahkan β-kariofilena.
Isolasi β-Kariofilena dengan KLTP
Isolasi β-kariofilena dilakukan dengan menggunakan KLT preparatif. Eluen yang digunakan merupakan eluen terbaik, yakni campuran n-heksana dan etil asetat dengan perbandingan 19:1. Isolasi ini menghasilkan 6 spot terpisah. Spot dengan nilai Rf 0.95 dikoleksi karena memiliki nilai Rf yang sama dengan Rf standar β -kariofilena, yakni 0.95. Spot dengan nilai Rf 0.95 yang diduga merupakan β -Gambar 5 Kromatogram lapis tipis ekstrak nonpolar dengan eluen campuran n -heksana dan etil asetat dengan perbandingan (kiri ke kanan), (i) 9:1, (ii) 6:1, (iii) 3:1, (iv) 19:1, dan (v) 39:1, dideteksi dengan pereaksi semprot anisaldehida-H2SO4
12
kariofilena (Gambar 6i) diidentifikasi secara kualitatif menggunakan KLT, serta dibandingkan dengan pola KLT dari standar β-kariofilena. Hasil identifikasi menggunakan KLT menunjukkan bahwa isolat β-kariofilena dan standar β -kariofilena masing-masing menghasilkan spot tunggal dengan nilai Rf yang sama, yakni 0.95 (Gambar 6ii dan 6iii). Selain itu, keduanya juga menghasilkan spot dengan warna yang sama, yakni ungu ketika disemprot dengan pereaksi anisaldehida-H2SO4. Hal ini mengindikasikan bahwa pemisahan β-kariofilena dari ekstrak nonpolar telah berhasil dilakukan yang selanjutnya akan dikonfirmasi lebih lanjut menggunakan instrumen GC-MS. Persen perolehan kembali isolat β -kariofilena yang didapatkan sebesar 96.09% (Lampiran 7).
Berdasarkan kromatogram GC-MS pada Gambar 7, kadar β-kariofilena yang semula hanya 35.10% telah jauh meningkat menjadi 82.56%, akan tetapi masih
ditemukan senyawa α-humulena (12.12%) pada hasil isolasi ini (Tabel 1). Kedua
Gambar 7 Kromatogram GC-MS isolat β-kariofilena
eugenol β-kariofilena
α-humulena
kariofilena oksida
α-kopaena δ-kadinena
Intensitas
Waktu retensi (menit)
Gambar 6 Hasil pemisahan β-kariofilena dengan KLTP pada ʎ = 254 nm (i), isolat
β-kariofilena (ii), dan standar β-kariofilena (iii) dengan pereaksi semprot anisaldehida-H2SO4
Spot dugaan
β-kariofilena
13 senyawa ini merupakan senyawa isomer sehingga memiliki sifat kepolaran yang
tidak jauh berbeda. Hal ini menyebabkan β-kariofilena tidak dapat terpisah dengan
baik dari α-humulena pada proses KLTP.
Reaksi Isomerisasi Eugenol menjadi Isoeugenol
Reaksi isomerisasi eugenol menjadi isoeugenol dilakukan dalam sistem homogen dengan katalis KOH. KOH merupakan basa Lewis sehingga dapat mendonorkan pasangan elektron bebasnya (PEB) ke atom H-hidroksi pada molekul eugenol membentuk ion eugenolat (i). Ion eugenolat cukup stabil karena memiliki efek resonans antara gugus O− pada gugus fenil eugenol dengan gugus alil (posisi
para). Adanya efek resonans ini menyebabkan terbentuknya struktur (ii). Struktur (ii) ini akan menginisiasi terjadinya geseran hidrida [1,3] membentuk struktur (iii). Terbentuknya rantai konjugasi baru menyebabkan timbulnya efek resonans sehingga ion isoeugenolat (iv) dapat terbentuk (Gambar 8). Terakhir, ion isoeugenolat akan berubah menjadi bentuk netralnya (isoeugenol) dengan mengambil proton yang terdapat di dalam sistem reaksi (Kadarohman dan Muchalal 2003). Pemanasan yang dilakukan pada suhu 143 ºC selama 2 jam bertujuan untuk meningkatkan laju reaksi. Selain itu, pengadukan juga dilakukan dengan tujuan meningkatkan jumlah tumbukan antarmolekul dengan cara meningkatkan energi kinetik molekul yang bereaksi sehingga laju reaksi menjadi lebih cepat.
14
Kromatogram produk isomerisasi memiliki kadar yang cukup tinggi, yakni 96.16% (Lampiran 8), akan tetapi hasil identifikasi berdasarkan library index MS menunjukkan bahwa puncak tersebut memiliki persen kemiripan yang sama antara eugenol dan isoeugenol. Berdasarkan analisis waktu retensi (WR), WR produk isomerisasi (10.62 menit) berada di antara WR standar eugenol (10.43 menit) dan WR standar isoeugenol (10.96 menit). Oleh karena itu, produk isoeugenol dikarakterisasi lebih lanjut menggunakan 1H-NMR (Tabel 2). Hasil analisis menunjukkan 5 sinyal proton menyerupai spektrum isoeugenol seperti yang dilaporkan oleh Salmoria et al. (1997). Geseran kimia pada 6.68-6.73 ppm menunjukkan keberadaan gugus benzena. Sinyal benzena tersebut cenderung berada di medan atas karena adanya pengaruh sumbangan elektron dari gugus hidroksil dan metoksi. Proton vinilik memberikan sinyal di daerah 6.60 ppm (C1’) dan 5.91-5.94 ppm (C2’) dengan pola pembelahan doublet dan multiplet yang merupakan ciri khas dari isoeugenol. Pada daerah 3.80-3.82 ppm terdapat sinyal dengan integrasi 3 dengan pola pembelahan singlet yang berasal dari 3 proton ekuivalen pada gugus metoksi, akan tetapi terdapat 2 sinyal pada geseran kimia ini. Hal tersebut menunjukkan bahwa bahan baku eugenol masih terdapat di dalam produk hasil isomerisasi. Selain itu, isoeugenol juga masih berupa campuran antara bentuk cis-isoeugenol dan trans-isoeugenol. Hasil ini mendukung data sebelumnya, yakni WR dari produk isomerisasi yang berada di antara WR standar eugenol dan WR standar isoeugenol.
Bobot Badan, Pakan, Feses dan Urin, serta Lemak Tubuh Terhadap Efek Inhalasi
Minyak cengkih, β-kariofilena, dan isoeugenol dianalisis sebagai pelangsing aromaterapi pada tikus jantan dewasa galur Sprague-Dawley dengan mengamati perubahan bobot badan selama 5 minggu masa perlakuan inhalasi. Perlakuan inhalasi sampel yang menyebabkan penurunan bobot badan tertinggi akan dianalisis lebih lanjut dengan uji aktivitas saraf simpatetik. Sebelum diberi perlakuan inhalasi, hewan uji diadaptasikan selama 2 minggu. Masa adaptasi ini berfungsi untuk
Tabel 2 Posisi sinyal-sinyal 1H-NMR isoeugenol dalam pelarut CD3OD
15 menyesuaikan kondisi fisiologis, nutrisi, dan lingkungan dari hewan uji. Pada minggu pertama masa adaptasi, semua kelompok tikus diberi pakan standar dan pada minggu ke-2 masa adaptasi, semua kelompok tikus diberi pakan tinggi kolesterol (TK). Pakan TK yang diberikan mengandung propiltiourasil (PTU). Tikus merupakan hewan uji yang memiliki kecepatan metabolisme tubuh yang tinggi sehingga sulit untuk mengalami obesitas. PTU merupakan salah satu senyawa yang dapat bertindak sebagai zat antitiroid sehingga dengan penambahan zat ini diharapkan dapat menghambat proses penggabungan yodium pada residu tirosil dari tiroglobulin dan juga menghambat penggabungan residu dari yodotirosil untuk membentuk yodotironin. Hal ini akan berdampak pada menurunan katabolisme kolesterol LDL dengan cara menurunkan sintesis dan ekspresi reseptor kolesterol LDL di hati sehingga akan menyebabkan terjadinya peningkatan konsentrasi kolesterol, fosfolipid, dan trigliserida darah (Noorrafiqi et al. 2013).
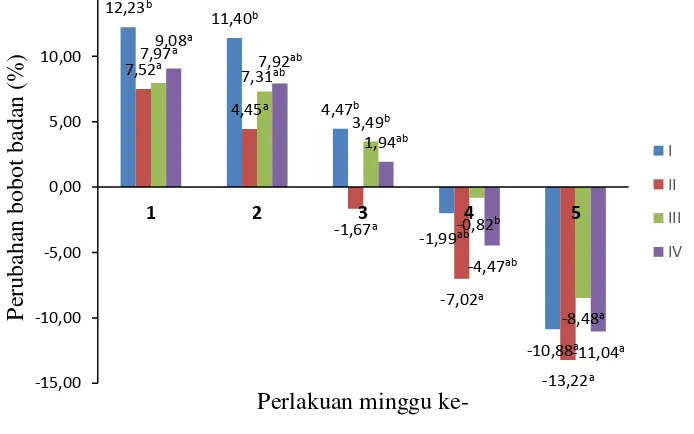
Hasil analisis varians (ANOVA) menunjukkan bahwa bobot badan setiap kelompok tidak berbeda nyata (p > 0.05) pada akhir masa adaptasi (Tabel 3). Tahap perlakuan sampel dilakukan selama 5 minggu berupa inhalasi minyak cengkih, β -kariofilena, dan isoeugenol dengan kadar 1%. Gambar 9 memperihatkan persen perubahan bobot badan tikus setiap minggu selama 5 minggu perlakuan inhalasi.
Gambar 9 Persen rerata perubahan bobot badan tikus setiap minggu selama masa perlakuan, kelompok I (pakan TK), kelompok II (TK + minyak cengkih), kelompok III (TK + β-kariofilena), dan kelompok IV (TK + isoeugenol) Tabel 3 Rerata bobot badan tikus pada akhir masa adaptasi dan masa perlakuan
Kelompok Masa adaptasi (g) Masa perlakuan (g) (I) Tinggi kolesterol (TK) 282 ± 14a 252 ± 25a (II) TK + minyak cengkih 275 ± 18a 238 ± 13a (III) TK + β-kariofilena 283 ± 18a 260 ± 36a
(IV) TK + isoeugenol 282 ± 13a 252 ± 29a
16
Pada minggu pertama perlakuan inhalasi, kelompok I yang merupakan kontrol negatif mengalami peningkatan bobot badan tertinggi (12.23%) dan berbeda nyata pada tingkat kepercayaan 95% dibandingkan dengan kelompok II-IV yang diberi peralakuan inhalasi, serta kelompok II yang diinhalasi minyak cengkih menunjukkan peningkatan bobot badan terendah, yakni 7.52%. Selama 5 minggu masa perlakuan, inhalasi minyak cengkih dan isoeugenol menghasilkan persentase perubahan bobot badan yang lebih rendah dibandingkan dengan kontrol negatif. Persentase perubahan bobot badan kelompok yang diinhalasikan minyak cengkih berbeda nyata pada tingkat kepercayaan 95% dibandingkan dengan kontrol negatif hanya sampai minggu ke-3 dari 5 minggu masa perlakuan. Sementara itu, persentase perubahan bobot badan kelompok yang diinhalasi isoeugenol tidak berbeda nyata dibandingkan dengan kontrol negatif, walaupun kelompok ini memiliki persentase perubahan bobot badan yang lebih rendah. Inhalasi β -kariofilena memiliki persentase perubahan bobot badan yang lebih rendah dibandingkan dengan kontrol negatif hanya sampai minggu ketiga. Hasil yang telah dipaparkan di atas berdampak pada bobot badan kelompok perlakuan inhalasi di akhir masa perlakuan (minggu ke-5) yang tidak berbeda nyata pada tingkat kepercayaan 95% dibandingkan dengan kontrol negatif, walaupun kelompok yang diinhalasikan minyak cengkih memiliki bobot badan terendah dibandingkan dengan kelompok lainnya.
Penurunan bobot badan yang ikut dialami oleh kelompok kontrol negatif diduga menjadi salah satu faktor yang menyebabkan bobot badan tidak berbeda nyata pada akhir masa perlakuan (Tabel 3). Penurunan ini disebabkan oleh tingkat konsumsi pakan kelompok kontrol negatif yang menurun sejak minggu ke-2 masa perlakuan. Penelitian sebelumnya melaporkan bahwa tikus galur Wistar
(Hardiningsih dan Nurhidayat 2006) dan tikus galur Sprague-Dawley (Reman 2013) memiliki tingkat konsumsi pakan kolesterol yang lebih rendah dibandingkan dengan pakan standar. Beberapa faktor yang memengaruhi tingkat konsumsi pakan pada hewan uji ialah jenis pakan, lingkungan sekitar, dan hewan itu sendiri (Parakkasi 1999). Walau demikian, kelompok yang diinhalasikan minyak cengkih memiliki tingkat konsumsi pakan terendah dibandingkan dengan kelompok lainnya selama masa perlakuan, yakni 14 g/tikus/hari (Tabel 4). Salah satu faktor inilah yang menyebabkan tikus yang diinhalasikan minyak cengkih memiliki rerata bobot badan terendah dibandingkan dengan kelompok lainnya. Tingkat konsumsi pakan yang cukup rendah menyebabkan jumlah feses dan urin yang diekskresikan kelompok II menjadi yang terendah, yakni 51 g/tikus/minggu.
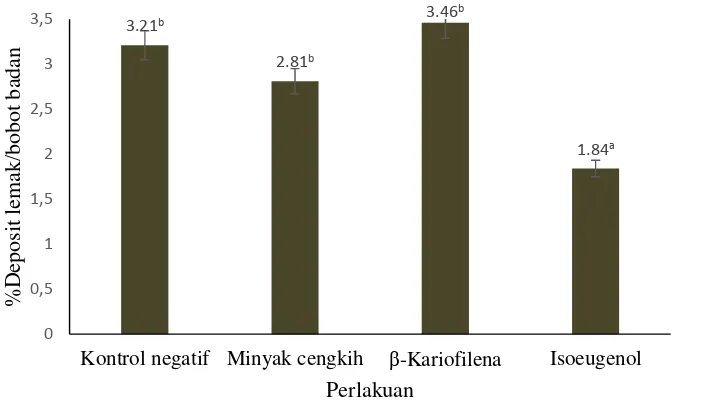
17 Potensi pelangsing aromaterapi juga dapat dilihat dari persentase bobot deposit lemak per bobot badan dari hewan uji setelah masa perlakuan inhalasi. Gambar 10 menunjukkan bahwa kelompok yang diinhalasikan minyak cengkih memiliki persentase bobot deposit lemak yang lebih rendah dibandingkan dengan kontrol negatif. Sebaliknya, inhalasi β-kariofilena menghasilkan persentase bobot deposit lemak yang lebih tinggi. Hasil ini berbanding lurus dengan bobot badan yang dimiliki oleh ketiga kelompok tersebut, akan tetapi hasil ini tidak berbeda nyata (p > 0.05). Hasil yang menarik dihasilkan oleh kelompok yang diinhalasikan isoeugenol. Kelompok ini memiliki persentase bobot deposit lemak terendah, yakni 1.8% dan berbeda nyata dibandingkan dengan kontrol negatif (p < 0.05).
Suatu senyawa atau campuran senyawa dapat dikatakan berpotensi sebagai obat pelangsing jika obat tersebut dapat menstimulasi pembakaran lemak, menghalangi absorpsi lemak, dan mengurangi nafsu makan (Birari dan Bhutani 2007). Berdasarkan data penelitian yang diperoleh, campuran senyawa di dalam minyak cengkih dan isoeugenol menunjukkan potensi sebagai pelangsing aromaterapi. Inhalasi minyak cengkih terindikasi dapat menurunkan nafsu makan sehingga berdampak pada menurunnya bobot badan dan bobot deposit lemak. Sementara itu, inhalasi isoeugenol tidak dapat menurunkan nafsu makan dan bobot badan, akan tetapi inhalasi isoeugenol ini dapat menurunkan bobot deposit lemak dan berbeda nyata dibandingkan dengan kontrol negatif (p < 0.05).
Mekanisme pelangsing aromaterapi telah dilaporkan berkaitan erat dengan efek aroma terhadap aktivitas saraf simpatetik. Aroma dari suatu senyawa aktif yang dapat menyebabkan aktivitas saraf simpatetik meningkat akan berdampak pada menurunnya nafsu makan dan bobot badan (Shen et al. 2005a). Sebaliknya, suatu aroma yang dapat menyebabkan aktivitas saraf simpatetik menurun akan berdampak pada meningkatnya nafsu makan dan bobot badan (Shen et al. 2005b; Batubara et al. 2013).
Berdasarkan kajian literatur tersebut, maka aroma minyak cengkih diduga dapat meningkatkan aktivitas saraf simpatetik. Hal tersebut dicoba untuk dibuktikan dengan cara menguji efek aroma minyak cengkih dengan kadar 1% terhadap aktivitas saraf simpatetik. Aktivitas saraf simpatetik harus dijaga konstan
Gambar 10 Persentase deposit lemak/bobot badan pada akhir perlakuan
3.21b
Kontrol negatif Minyak cengkih β-Kariofilena Isoeugenol
18
selama 30 menit sebelum stimulasi aroma minyak cengkih dilakukan. Hal ini bertujuan untuk memudahkan pembandingan aktivitas saraf simpatetik sebelum dan saat tikus diberi aroma minyak cengkih. Gambar 11 memperlihatkan bahwa telah terjadi peningkatkan aktivitas saraf simpatetik dari menit ke-30 sampai menit ke-90 (selama 60 menit stimulasi aroma minyak cengkih). Penurunan aktivitas saraf simpatetik terjadi setelah menit ke-90 yang bertepatan dengan pemberhentian stimulasi aroma. Hal tersebut menunjukkan bahwa inhalasi minyak cengkih terbukti dapat merangsang aktivitas saraf simpatetik. Hasil tersebut berbanding lurus dengan rendahnya bobot badan dan tingkat konsumsi pakan yang dimiliki oleh kelompok yang diinhalasikan minyak cengkih. Aktivitas saraf simpatetik yang tinggi akan berbanding lurus dengan meningkatnya aktivitas lipolisis (Shen et al.
2005a). Hal ini akan berdampak pada meningkatnya jumlah trigliserida yang diurai menjadi asam lemak bebas sehingga akan menyebabkan peningkatan produksi panas. Hal ini dapat terjadi melalui aktivitas uncoupling protein 1 (UCP1) (Argyropoulos dan Harperk 2002), yang akan berpengaruh terhadap meningkatnya suhu badan dan konsumsi energi melalui mekanisme uncoupling oxidation dari produksi ATP di mitokondria.
Analisis Profil Lipid Darah
Kadar kolesterol total ditentukan dengan menggunakan alat spektrofotometer berdasarkan prinsip enzimatis. Serum darah yang di dalamnya terdapat senyawa kolesterol ester akan dihidrolisis oleh kolesterol esterase menjadi kolesterol dan asam lemak bebas. Selanjutnya, kolesterol ini akan dioksidasi oleh kolesterol oksidase dengan adanya oksigen bebas menjadi kolest-4-en-3-on dan hidrogen peroksida. Hidrogen peroksida akan menginisiasi terbentuknya quinoneimina dengan bantuan senyawa fenol, 4-aminoantipirina, dan enzim peroksidase. Quinoneimina berwarna merah muda sehingga kadar senyawa ini dapat diukur dengan cara menghitung intensitas serapannya pada panjang gelombang 505 nm (Allain et al. 1974). Banyaknya quinoneimina yang terbentuk akan berbanding
19 lurus dengan banyaknya kolesterol ester sehingga semakin tinggi nilai absorbans yang diperoleh menandakan tingginya kadar kolesterol total di dalam darah.
Kadar kolesterol total antar kelompok menunjukkan hasil yang tidak berbeda nyata (p > 0.05) pada akhir masa adaptasi dan akhir masa perlakuan (Tabel 5). Pada akhir masa adaptasi, kadar kolesterol total dari kelompok I dan II telah melebihi ambang batas normal (<200 mg/dL) (NCEP 2001), sedangkan pada akhir masa perlakuan tercatat bahwa kadar kolesterol pada semua kelompok berada pada rentang normal. Kadar kolesterol total terendah dan tertinggi masing-masing dihasilkan oleh kelompok yang diinhalasikan minyak cengkih dan isoeugenol. Kelompok yang diinhalasikan minyak cengkih mengalami penurunan kadar kolesterol total hingga 44.28%, sedangkan kelompok yang diinhalasikan isoeugenol hanya mengalami penurunan sebesar 13.56%. Hasil tersebut menunjukkan bahwa inhalasi minyak cengkih dapat menurunkan kadar kolesterol total di dalam darah.
Sementara itu, analisis kadar HDL-c menunjukkan hasil yang kontradiktif. Setiap kelompok yang diberi perlakuan inhalasi memiliki kadar HDL- c <40 mg/dL (Tabel 6). Nilai ini tergolong dalam katagori rendah (NCEP 2001). Sebaliknya, kelompok kontrol negatif memiliki kadar HDL-c >60 mg/dL yang tergolong dalam katagori tinggi (NCEP 2001) dan berbeda nyata (p < 0.05) dibandingkan dengan kelompok lainnya. Rendahnya kadar HDL-c ini dapat meningkatkan resiko terkena penyakit jantung koroner.
Prinsip penentuan kadar trigliserida secara enzimatis dilakukan dengan cara mereaksikan trigliserida yang terdapat di dalam serum darah dengan lipase sehingga terbentuk gliserol dan asam lemak bebas melalui reaksi hidrolisis. Selanjutnya, gliserol dikonversi menjadi gliserol-3-fosfat oleh gliserol kinase. Gliserol-3-fosfat ini terbentuk melalui proses fosfolirasi, yakni proses transfer gugus fosfat dari ATP ke gliserol dengan bantuan gliserol kinase. Berikutnya, gliserol-3-fosfat oksidase akan mengoksidasi gliserol-3-fosfat menjadi dihidroksiaseton fosfat dan hidrogen peroksida. Seperti halnya prinsip penentuan
Tabel 5 Rerata kadar kolesterol total pada akhir masa adaptasi dan perlakuan Kelompok Kadar kolesterol total (mg/dL)
Setelah adaptasi Setelah perlakuan (I) Tinggi kolesterol (TK) 203.509 ± 50.537a 138.844 ± 45.152a (II) TK + minyak cengkih 222.428 ± 33.326a 123.940 ± 23.557a (III) TK + β-kariofilena 185.396 ± 27.789a 147.526 ± 8.520a (IV) TK + isoeugenol 179.611 ± 33.025a 155.257 ± 17.597a
Angka yang diikuti oleh huruf superscripts yang sama tidak berbeda nyata pada taraf uji (P > 0.05) (Duncan’s multiple range test)
Tabel 6 Rerata kadar HDL-c pada akhir masa perlakuan
Kelompok Kadar HDL-c (mg/dL)
(I) Tinggi kolesterol (TK) 68.428 ± 24.148b (II) TK + minyak cengkih 19.752 ± 2.892a (III) TK + β-kariofilena 11.851 ± 2.093a (IV) TK + isoeugenol 11.595 ± 2.182a
20
kolesterol total, hidrogen peroksida ini akan bereaksi dengan klorofenol dan 4-aminoantipirina yang dikatalisi oleh peroksidase membentuk quinoneimina yang berwarna merah muda (Fossati dan Prencipe 1982). Intensitas serapan dari senyawa ini dapat diukur pada panjang gelombang 505 nm. Intensitas senyawa ini akan proporsional dengan jumlah trigliserida di dalam sampel serum darah.
Pada akhir masa adaptasi, kadar trigliserida pada setiap kelompok perlakuan tidak berbeda nyata (p > 0.05). Kelompok II memiliki kadar trigliserida tertinggi, yakni 110.543 mg/dL (Tabel 7). Analisis kadar trigliserida pada akhir perlakuan menunjukkan bahwa kelompok yang diinhalasikan minyak cengkih memiliki kadar terendah (31.892 mg/dL) dan berbeda nyata (p < 0.05) jika dibandingkan dengan kontrol negatif yang menghasilkan kadar trigliserida tertinggi (52.860 mg/dL). NCEP (2001) menyatakan bahwa kadar trigliserida yang normal ialah <150 mg/dL sehingga setiap kelompok masih memiliki kadar trigliserida yang normal. Penurunan kadar trigliserida pada kelompok yang diinhalasikan minyak cengkih ini mencapai 71.15%, jika dibandingkan dengan kadar sebelum perlakuan inhalasi diberikan. Sementara itu, inhalasi isoeugenol menyebabkan terjadinya penurunan kadar trigliserida sebesar 55.49%. Berdasarkan data yang telah dijabarkan tersebut, inhalasi minyak cengkih berpotensi sebagai penurun kadar trigliserida di dalam darah.
4
SIMPULAN DAN SARAN
Simpulan
Isolasi β-kariofilena dari ekstrak nonpolar menghasilkan persen perolehan kembali sebesar 96% dengan kadar 83%. Berdasarkan kromatogram GC dan spektrum NMR yang diperoleh, produk isomerisasi ini masih berupa campuran antara eugenol, cis-isoeugenol, dan trans-isoeugenol. Inhalasi minyak cengkih dan isoeugenol dengan kadar 1% menunjukkan potensi sebagai pelangsing aromaterapi. Aroma minyak cengkih dapat merangsang aktivitas saraf simpatetik sehingga berdampak terhadap penurunan nafsu makan dan bobot badan sebesar 13%. Sementara itu, inhalasi isoeugenol dapat merangsang pembakaran lemak di dalam tubuh. Inhalasi minyak cengkih juga dapat menurunkan kadar trigliserida di dalam darah.
Tabel 7 Rerata kadar trigliserida pada akhir masa adaptasi dan perlakuan
Kelompok Kadar trigliserida (mg/dL)
21
Saran
Penelitian lebih lanjut perlu dilakukan untuk menganalisis efek dari aroma isoeugenol terhadap aktivitas saraf simpatetik dan suhu di jaringan adiposa cokelat. Uji kadar minyak atsiri yang terdapat di ruang inhalasi juga perlu dilakukan sehingga dapat diketahui kadar minyak atsiri yang benar-benar dihirup oleh hewan uji. Selain itu, pengukuran parameter antropometri, seperti panjang lingkar perut dan dada, panjang tubuh, indeks massa tubuh, indeks Lee, dan laju spesifik dari peningkatan massa tubuh perlu dilakukan untuk memudahkan identifikasi terjadinya obesitas pada tikus.
DAFTAR PUSTAKA
Aisha AF, Abu-Salah KM, Alrokayan SA, Siddiqui MJ, Ismail Z, Majid AM. 2012.
Syzygium aromaticum extracts as good source of betulinic acid and potential anti-breast cancer. Braz J Pharmacogn. 22(2):335-343.doi:10.1590/S0102-695X2011005000185.
Akunna GG, Saalu LC, Ogunmodede OS, Ogunlade B, Adefolaju GA, Bello AJ. 2011. The effects of two Nigerian made parfumes on the liver of adult Wistar rat.
J Med Sci. 11(5):220-225.doi:10.3923/jms.2011.220-225.
Allain CC, Poon LS, Chan CSG, Richmond W, Fu PC. 1974. Enzymatic determination of total serum cholesterol. Clin Chem [Internet]. [diunduh 2015 Jun 7]; 20(4):470-475. Tersedia pada: http//clinchem.org/content/20/4/470.full.p df.
Argyropoulos G, Harperk ME. 2002. Uncoupling proteins and thermoregulation. J Appl Physiol. 92(5):2187-2198.doi:10.1152/japplphysiol.00994.2001.
Arifin B, Tang DF, Achmadi SS. 2015. Transformation of eugenol and safrole into hydroxychavicol. Indones J Chem [Internet]. [diunduh 2015 Jun 7]; 15(1):77-85. Tersedia pada: http//pdm-mipa.ugm.ac.id/ojs/indx.php/ijc/article/viewFile/941/ 1037.
Batubara I, Suparto IH, Sadiah S, Matsuoka R, Mitsunaga T. 2013. Effect of
Zingiber zerumbet essential oils and zerumbone inhalation on body weight of
Sprague Dawley rat. Pak J Biol Sci. 16(19):1028-1033.doi:10.3923/pjbs.2013.1 028.1033.
Biolabo. 2011. Reagent for Quantitative Determination of Total Cholesterol, Triglcerides, and HDL-c in Human Serum or Plasma . [Internet] [diunduh 2014 Des 12]. Tersedia pada: http//biolabo.fr/biolabo/pdfs/noticesE/biochimieE. Birari RB, Bhutani KK. 2007. Pancreatic lipase inhibitors from natural
sources:unexplored potential. Drug Discov Today. 12:379-389.doi:10.1016/j.dru dis.2007.07.024.
Bortolomeazzi R, Verardo G, Liessi A, Callea A. 2010. Formation of dehydrodiisoeugenol and dehydrodieugenol from the reaction of isoeugenol and eugenol with DPPH radical and their role in the radical scavenging activity. Food Chem. 118:256-265.doi:10.1016/j.foodchem.2009.04.115.
22
Diego MA, Jones NA, Field T, Hernandez-Reif M, Schanberg S, Kuhn C, Mcadam V, Galamaga R, Galamaga M. 1998. Aromatherapy positively affects mood, eeg patterns of alertness, and math computations. Inter J Neurosci. 96:211-224.doi:10.3109/00207459808986469.
Farouk H, El-Sayeh BA, Mahmoud SS, Sharaf OA. 2012. Effect of olfactory stimulation with grapefruit oil and sibutramine in obese rats. J Pak Med Stud [Internet]. [diunduh 2014 Des 12]; 2(1):3-10. Tersedia pada: http//jpmsonlin e.com/wp-content/uploads/2011/12/JPMS-VOL2-ISSUE1-PAGES3-10-OA1.p df.
Fernandes ES, Passos GF, Medeiros R, da Cunha FM, Ferreira J, Campos MM, Pianowski LF, Calixto JB. 2007. Anti-inflammatory effects of compounds alpha-humuleneand (−)-trans-caryophyllene isolated from the essential oil of Cordia verbenacea. Eur J Pharmacol. 569:228–236.doi:10.1016/j.ejphar.2007.04.059. Findik E, Ceylan M, Elmasta M. 2011. Isoeugenol-based novel potent antioxidants:
synthesis and reactivity. Eur J Med Chem. 46:4618-4624.doi:10.1016/j.ejmech.2 011.07.041.
Fitri N, Kawira JA. 2006. Perbandingan variable pada isolasi dan pemurnian eugenol dari minyak daun cengkeh. Media Litbang Kesehatan [Internet]. [diunduh 2013 Sep 12]; 16(2):16-21. Tersedia pada: http//ejournal.litbang.depk es.go.id/index.php /MPK/article/viewFile/895/824.
Fossati P, Prencipe L. 1982. Serum triglycerides determined colorimetrically with an enzyme that produces hydrogen peroxide. Clin Chem [Internet]. [diunduh 2015 Jun 7]; 28(10):2077-2080. Tersedia pada: http//clinchem.org/content/28/10 /2077.full.pdf.
Giannessi J, Alviar B, Agusta A. 2008. Variously Substituted Derivatives of Guanidine, and their Use as Medicines with Anti-diabetes and/or Anti-obesity Activity. United States Patents No. 7368605. [Internet] [diacu 2013 Mei 10]. Tersedia pada: http//uspto.gov.
Hardiningsih R, Nurhidayat N. 2006. Pengaruh pemberian pakan hiperkolesterolemia terhadap bobot badan tikus putih wistar yang diberi bakteri asam laktat. Biodivers [Internet]. [diunduh 2014 Mei 15]; 7(2):127-130. Tersedia pada: http//biodiversitas.mipa.uns.ac.id/D/D0702/D070207.pdf.
Hasim A. 2014. Pemisahan eugenol dari minyak atsiri daun cengkih (Syzygium aromaticum) sebagai pelangsing aromaterapi secara in vivo [skripsi]. Bogor (ID): Institut Pertanian Bogor.
Hau J, Hoosier GL. 2003. Handbook of Laboratory Animal Science. Ed ke-2. New York (US): CRC Press LLC.
Huang M, Sanchez-Moreiras AM, Abel C, Sohrabi R, Lee S, Gershenzon J, Tholl D. 2011. The major volatile organic compound emitted from Arabidopsis thaliana flowers, the sesquiterpene (E)-β-caryophyllene, is a defense against a bacterial pathogen. New Phytol. 193:997-1008.doi:10.1111/j.1469-8137.2011.0 4001.x.
23 Jayanudin. 2011. Komposisi kimia minyak atsiri daun cengkeh dari proses penyulingan uap. J Tek Kim Indones [Internet]. [diunduh 2013 Jun 10]; 10(1):37-42. Tersedia pada: http//jtki.aptekindo.org/index.php/jtki/article/view/7/5. Jirovetz L, Buchbauer G, Stoilova I, Stoyanova A, Krastanov A, Schmidt E. 2006.
Chemical composition and antioxidant properties of clove leaf essential oil. J Agric Food Chem. 54(17):6303-6307.doi:10.1021/jf060608c.
Kadarohman A, Muchalal M. 2003. Mekanisme Reaksi Isomerisasi Eugenol
.
[Internet] [diunduh 2015 Jun 15]. Tersedia pada: http//file.upi.edu/Direktori/FP MIPA/JUR._PEND._KIMIA/196305091987031-R._ASEP_KADAROHMAN/ Mekanisme_Reaksi_Isomerisasi_Euegenol.pdf.Kadoma Y, Atsumi T, Okada N, Ishihara M, Yokoe I, Fujisawa S. 2007. Radical-scavenging activity of natural methoxyphenols vs synthetic ones using the induction period method. Molecules. 12(2):130-138.doi:10.3390/12020130. Kaur G, Sultana S. 2012. Evaluation of antiarthritic activity of isoeugenol in
adjuvant induced arthritis in murine model. Food Chem Toxicol. 50:2689-2695.doi: 10.1016/j.fct.2012.05.016.
Lewis DR, Liu DJ. 2012. Direct measurement of lipase inhibition by orlistat using a dissolution linked in vitro assay. Clinic Pharmacol Biopharm. 1(3):1-3.doi:10.4172/2167-065X.100010.
Li MF, Cheung BMY. 2009. Pharmacotherapy for obesity. Br J Clin Pharmacol. 68(6):804-810.doi:10.1111/j.1365-2125.2009.03453.x.
Li MF, Cheung BMY. 2011. Rise and fall of anti-obesity drugs. World J Diabetes. 2(2):19-23.doi:10.4239/wjd.v2.i2.19.
Li W, Tsubouchi R, Qiao S, Haneda M, Murakami K, Yoshino M. 2006. Inhibitory action of eugenol compounds on the production of nitric oxide in RAW264.7 macrophages. Biomed Res. 27(2):69-74.doi:10.2220/biomedres.2 7.69.
[NCEP] National Cholesterol Education Program. 2001. Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults. JAMA. 285(19): 2486-2497.doi:10.1001/jama.285.19.2486.
Niijima A, Nagai K. 2003. Effect of olfactory stimulation with flavor of grapefruit oil and lemon oil on the activity of sympathetic branch in the white adipose tissue of the epididymis. Exp Biol Med [Internet]. [diunduh 2014 Des 12]; 228:1190-1192. Tersedia pada: http//sayshabeauty.com/EffectofOlfactoryStimulationwith GrapefruitOil_FINAL.pdf.
Noorrafiqi MI, Yasmina A, Hendriyono FX. 2013. Efek jus buah karamunting (Melastoma malabathricum L.) terhadap kadar trigiserida serum darah tikus putih yang diinduksi propiltiourasil. Berkala Kedokteran [Internet]. [diunduh 2013 Des 12]; 9(2):219-227. Tersedia pada: http//ejournal.unlam.ac.id/index.ph p/bk/article/viewFile/681/637.
Parakkasi A. 1999. Ilmu Makanan Ternak Ruminansia. Jakarta (ID): Universitas Indonesia.
Pinto E, Silva LV, Cavaleiro C, Salgueiro L. 2009. Antifungal activity of the clove essential oil from Syzygium aromaticum on Candida, Aspergillus and
dermatophyte species. J Med Microbiol. 58(11):1454-1462.doi:10.1099/jmm.0. 010538-0.
24
Saeed M, Nadeem M, Khan MR, Shabbir MA, Shehzad A, Amir RM. 2013. Antimicrobial activity of Syzygium aromaticum extracts against food spoilage bacteria. Afr J Microbiol Res. 7(41):4848-4856.doi:10.5897/AJMR2013.5946. Salmoria GV, Dall'Oglio EL, Zucco C. 1997 Isomerization of Safrole and Eugenol
Under Microwave Irradiation. Synth Commun. 27(24):4335-4340 doi:10.1080/0 0397919708005058.
Sanchez-Munoz BA, Aguilar MI, King-Diaz B, Rivero JF, Lotina-Hennsen B. 2012.
The sesquiterpenes β-caryophyllene and caryophyllene oxide isolated from
senecio salignus act as phytogrowth and photosynthesis inhibitors. Molecules. 17(2):1437-1447.doi:10.3390/molecules17021437.
Shah YR, Sen DJ, Patel RN, Patel JS, Patel AD, Prajapati PM. 2011. Aromatherapy: the doctor of natural harmony of body and mind. Int J Drug Dev Res[Internet].
[diunduh 2014 Des 12]; 3(1):286-294. Tersedia pada: http//ijddr.in/old/Dacumen ts/IJDDR%20JAN-MARCH%202011%20ISSUE%20PDF/NO.%2032,%20VO L.3,%20ISSUE%201,%202011.pdf.
Shen J, Niijima A, Tanida M, Horii Y, Maeda K, Nagai K. 2005a. Olfactory stimulation with scent of grapefruit oil affects autonomic nerves, lipolysis and appetite in rats. Neurosci Lett. 380(3):289-294.doi:10.1016/j.neulet.2005.01.05 8.
Shen J, Niijima A, Tanida M, Horii Y, Maeda K, Nagai K. 2005b. Olfactory stimulation with scent of lavender oil affects autonomic nerves, lipolysis and appetite in rats. Neuroscience Letters 383:188-193.doi:10.1016/j.neulet.2005.0 4.010.
Shimazu T. 1981. Central nervous system regulation of liver and adipose tissue metabolism. Diabetol. 20(3):343-356.doi:10.1007/BF00254502.
Skoog DA, West DM, Holler FJ, Crouch SR. 2004. Fundamental of Analytical Chemistry. Ed ke-8. Belmont (US): Thomson Learning.
Snow V, Barry P, Fitterman N, Qaseem A, Weiss K. 2005. Pharmacologic and surgical management of obesity in primary care: a clinical practice guideline from the american college of physicians. Ann Intern Med. 142(7):525-531.doi:10.7326/0003-4819-142-7-200504050-00011.
Stahl E. 1969. Thin Layer Chromatography. Edisi ke-2. Berlin (DE): Springer-verlag.
25 Lampiran 1 Komposisi pakan yang diberikan kepada hewan uji
Pakan standar di Pusat Studi Biofarmaka
Komposisi Kadar (%)
Air Maks 13.00
Protein 19.00-21.00
Lemak Min 5.00
Serat Maks 5.00
Abu Maks 7.00
Kalsium Min 0.90
Fosforus Min 0.60
Pakan tinggi kolesterol
Komposisi Kadar (%)
PTU 0.10
Kuning telur 12.50
Minyak kelapa barco 5.00
26
27 Lampiran 3 Penentuan bobot jenis minyak cengkih
Ulangan Bobot (g) Bobot jenis (g
M adalah massa piknometer kosong (g)
M1 adalah massa piknometer berisi air pada 20 °C (g) M2 adalah massa piknometer berisi sampel pada 20 °C (g) Da adalah bobot jenis air pada suhu 20 °C (g/mL)
Lampiran 4 Persen perolehan kembali isolat eugenol
Ulangan
Bobot eugenol dalam minyak cengkih g
= Bobot minyak cengkih × % area eugenol dalam minyak cengkih = . g × . % = . g
Bobot eugenol dalam isolat eugenol g
= Bobot isolat eugenol × % area eugenol dalam isolat eugenol = . g × . % = . g
Perolehan kembali isolat eugenol % = Ca ˳ ×Ca %
= . g
. g × %
28
29 Lampiran 6 Rendemen pemisahan ekastrak nonpolar
Ulangan Minyak cengkih
Rendemen % =Bobot ekstrak nonpolarBobot minyak cengkih × %
= .. g g × %
= . %
Lampiran 7 Persen perolehan kembali isolat β-kariofilena
Ulangan
Bobot kariofilena dalam ekstrak nonpolar g
= Bobot ekstrak nonpolar × % area kariofilena dalam ekstrak nonpolar = . g × . %
= . g
Bobot kariofilena dalam isolat kariofilena g
= Bobot isolat kariofilena × % area kariofilena dalam isolat kariofilena = . g × . %
= . g
Perolehan kembali isolat kariofilena % = Ca ˳ ×Ca %
= .. g × g %
30
Lampiran 8 Kromatogram GC (a) dan spektrum 1H-NMR (b) produk isomerisasi
Geseran kimia (ppm)
Intensitas
Intensitas
Waktu retensi (menit)
(a)
31