PENENTUAN KADAR Ag, Cu DAN Fe DIDALAM BATUAN
MINERAL YANG BERASAL DARI DUSUN JAMBU
DOLOK KABUPATEN TOBA SAMOSIR
SKRIPSI
BELLA KRESENSIA TAMBUNAN
080802048
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN
ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
PERSETUJUAN
Judul : PENENTUAN KADAR Ag, Cu, dan Fe di DALAM BATUAN MINERAL YANG BERASAL DARI DUSUN JAMBU DOLOK KABUPATEN TOBA SAMOSIR
Kategori : SKRIPSI
Nama : BELLA KRESENSIA TAMBUNAN
NIM : 080802048
Program Studi : SARJANA ( S1 ) KIMIA Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di, Medan, Juni 2013
Komisi Pembimbing
Dosen Pembimbing II Dosen Pembimbing I
Dr.Hamonangan Nainggolan,MSc Jamahir Gultom, Ph.D NIP 19562406198301002 NIP195209251977031001
Diketahui / disetujui oleh
Departemen Kimia FMIPA USU
Ketua
PERNYATAAN
PENENTUAN KADAR Ag, Cu DAN Fe DIDALAM BATUAN MINERAL YANG BERASAL DARI DUSUN JAMBU DOLOK
KABUPATEN TOBA SAMOSIR
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa
kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Juni 2013
BELLA KRESENSIA TAMBUNAN
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Yuhan Yesus Kristus untuk setiap kasih
karuniaNya, kesetiaan, dan kebaikanNya setiap saat dalam penyelesaian penelitian
dan penyusunan skripsi ini.
Saya juga mengucapkan terimakasih yang terdalam kepada bapak tersayang
Selamat Tambunan dan mama terkasih Martha Sidabutar untuk cinta kasih,
dukungan doa dan pengorbanan yang diberikan kepada penulis. Terima kasih juga
untuk Bang Ferdinan, Rumi, Agung, Paulina, Mickhael, dan Benedik untuk
semangat dan harapannya kepada penulis.
Dengan kerendahan hati, penulis mengucapkan terima kasih banyak kepada
Bapak jamahir Gultom,Ph.D selaku dosen pembimbing I dan Bapak
Dr.Hamonangan Nainggolan,MSc selaku dosen pembimbing II yang telah
memberikan bimbingan, waktu, saran, dan menolong penulis dan kepada Kepala
Laboratorium Kimia Analitik Bapak Prof. Harlem Marpaung yang telah
memberikan saran-saran kepada penulis. Ucapan terima kasih juga ditujukan
kepada Ketua dan Sekretaris Departemen Kimia FMIPA USU, Ibu Dr. Rumondang
Bulan Nst, MS dan bapak Dr. Albert Pasaribu, M.Sc, Dekan dan pembantu Dekan
FMIPA USU Medan. Kepada seluruh asisten dan Laboran Kimia Analitik FMIPA
USU Kak Tiwi, Bang Ferry, Bang Grand, Kak Sari, Kak Vaskah, Indah, Destaria,
Emilia, Juliana, Reh Malem, dan Royman atas bantuan dan semangatnya selama
ini. Terimakasih juga untuk Bang Jhan untuk semangat, doa dan perhatiannya. Dan
terima kasih juga untuk teman-teman satu stambuk khususnya Fasma, Cristiana,
ABSTRAK
Telah dilakukan penelitian tentang penentuan kadar Ag, Cu dan Fe pada batuan
mineral dari Dusun jambu Dolok Kabupaten Toba Samosir. Pengambilan sampel
dilakukan dengan metode acak. Sampel didestruksi dengan mengabukan sampel
pada suhu 900oC. Penentuan konsentrasi logam Ag, Cu dan Fe dilakukan dengan
menggunakan metode destruksi basah. Pelarut yang digunakan untuk Ag dan Cu
adalah HNO3(p) dan pelarut yang digunakan untuk Fe adalah HNO3(p) dan HCl(p)
dan hasil preparasi sampel ditentukan kadarnya dengan Spektrofotometer Serapan
Atom. Dari analisis yang telah dilakukan diperoleh kadar perak, tembaga, dan besi
DETERMINATION OF CONTENT Ag, Cu and Fe IN THE ROCKS MINERAL ORIGINATING FROM DUSUN JAMBU DOLOK
KABUPATEN TOBA SAMOSIR
ABSTRACT
The determination of content Ag, Cu and Fe in the rocks mineral that taken using
randomly method from Jambu Dolok Kabupaten Toba Samosir has been
conducted. The samples has been carried out by ashing on 900oC. The
concentration of Ag, Cu and Fe was determined using wet digestion method by
using HNO3(p) for Ag and Cu and HNO3(p) and HCl(p) for determining Fe. The
concentration was analyzed using Atomic Absorption Spechtrophotometer. It was
found the content of Ag, Cu and Fe sequentially 2,1590 mg/Kg, 21.311 mg/Kg dan
DAFTAR ISI 1.1.Latar Belakang 1 1.2.Permasalahan 2 1.3.Pembatasan Masalah 2 1.4.Tujuan Penelitian 2
1.5.Manfaat Penelitian 3 1.6.Lokasi Penelitian 3
BAB 3 METODOLOGI PENELITIAN
3.3.2.1. Penyediaan Larutan Sampel untuk Penentuan Ag dan Cu 23
3.3.2.2. Penyediaan Larutan Sampel untuk Penentuan Fe 24
3.3.3.Pembuatan Kurva Kalibrasi Larutan Standar Ag 24
3.3.4.Pembuatan Kurva Kalibrasi Larutan Standar Cu 24
3.3.5.Pembuatan Kurva Kalibrasi Larutan Standar Fe 25
3.3.6.Penentuan Kadar Ag pada sampel dengan menggunakan Spektrofotometer Serapan Atom 25
3.3.7.Penentuan Kadar Cu pada sampel dengan menggunakan Spektrofotometer Serapan Atom 25
3.3.8.Penentuan Kadar Fe pada sampel dengan menggunakan Spektrofotometer Serapan Atom 25
3.4.6.Penentuan Kadar Ag dengan Menggunakan Spektrofotometer Serapan Atom 30
3.4.8.Penentuan Kadar Fe dengan Menggunakan
Spektrofotometer Serapan Atom 30
BAB 4 HASIL DAN PEMBAHASAN
4.1.Hasil dan pengolahan Data 31
4.1.1.Logam Perak 31
4.1.2.Pengolahan Data Logam Perak (Ag) 32
4.1.2.1. Penurunan Persamaan Garis Regresi dengan
Metode Least Square 32
4.1.2.2. Koefisien Korelasi 34
4.1.2.3. Penentuan Kadar Logam Perak (Ag) Dari Sampel
Batuan Mineral Dari Dusun Jambu Dolok
Kabupaten Toba Samosir 34
4.1.2.4. Perhitungan Kadar Logam Perak (Ag) dalam mg/Kg 35
4.1.3.Logam Tembaga 36
4.1.4.Pengolahan Data Logam Tembaga (Cu) 37
4.1.4.1. Penurunan Persamaan Garis Regresi dengan
Metode Least Square 37
4.1.4.2. Koefisien Korelasi 39
4.1.4.3. Penentuan Kadar Logam Tembaga (Cu)
Dari Sampel Batuan Mineral Dari Dusun Jambu Dolok
Kabupaten Toba Samosir 40
4.1.4.4. Perhitungan Kadar Logam Tembaga (Cu)
dalam mg/Kg 40
4.1.5.Logam Besi 41
4.1.6.Pengolahan Data Logam Besi (Fe) 42
4.1.6.1. Penurunan Persamaan Garis Regresi dengan
Metode Least Square 42
4.1.6.2. Koefisien Korelasi 44
4.1.6.3. Penentuan Kadar Logam Besi (Fe) Dari Sampel
Batuan Mineral Dari Dusun Jambu Dolok
Kabupaten Toba Samosir 45
4.2. Pembahasan 46
BAB 5 KESIMPULAN DAN SARAN
5.1.Kesimpulan 49
5.2.Saran 49
DAFTAR GAMBAR
Halaman
Gambar 2.1 Diagram Balok Peralatan Spektrofotometer
Serapan Atom 14
Gambar 4.1 Kurva Kalibrasi Larutan Standar Perak (Ag) 32
Gambar 4.2 Kurva Kalibrasi Larutan Standar Tembaga (Cu) 37
DAFTAR TABEL
Halaman
Tabel 4.1 Kondisi alat SSA Merek Hitachi Z-2000 pada
pengukuran konsentrasi logam Perak (Ag) 31
Tabel 4.2 Data Absorbansi Larutan Standar Perak (Ag) 31
Tabel 4.3 Penurunan Persamaan Garis Regresi untuk Penentuan Konsentrasi
Logam Perak (Ag) Berdasarkan Pengukuran Absorbansi Larutan
Standar Perak (Ag) 33
Tabel 4.4 Kondisi alat SSA Merek Hitachi Z-2000 pada pengukuran
konsentrasi logam Tembaga (Cu) 36
Tabel 4.5 Data Absorbansi Larutan Standar Tembaga (Cu) 36
Tabel 4.6 Penurunan Persamaan Garis Regresi untuk Penentuan Konsentrasi
Logam Tembaga (Cu) Berdasarkan Pengukuran Absorbansi Larutan
Standar Tembaga (Cu) 38
Tabel 4.7 Kondisi alat SSA Merek Hitachi Z-2000 pada pengukuran
konsentrasi logam Besi (Fe) 41
Tabel 4.8 Data Absorbansi Larutan Standar Besi (Fe) 41
Tabel 4.9 Penurunan Persamaan Garis Regresi untuk Penentuan Konsentrasi
Logam Besi (Fe) Berdasarkan Pengukuran Absorbansi
ABSTRAK
Telah dilakukan penelitian tentang penentuan kadar Ag, Cu dan Fe pada batuan
mineral dari Dusun jambu Dolok Kabupaten Toba Samosir. Pengambilan sampel
dilakukan dengan metode acak. Sampel didestruksi dengan mengabukan sampel
pada suhu 900oC. Penentuan konsentrasi logam Ag, Cu dan Fe dilakukan dengan
menggunakan metode destruksi basah. Pelarut yang digunakan untuk Ag dan Cu
adalah HNO3(p) dan pelarut yang digunakan untuk Fe adalah HNO3(p) dan HCl(p)
dan hasil preparasi sampel ditentukan kadarnya dengan Spektrofotometer Serapan
Atom. Dari analisis yang telah dilakukan diperoleh kadar perak, tembaga, dan besi
DETERMINATION OF CONTENT Ag, Cu and Fe IN THE ROCKS MINERAL ORIGINATING FROM DUSUN JAMBU DOLOK
KABUPATEN TOBA SAMOSIR
ABSTRACT
The determination of content Ag, Cu and Fe in the rocks mineral that taken using
randomly method from Jambu Dolok Kabupaten Toba Samosir has been
conducted. The samples has been carried out by ashing on 900oC. The
concentration of Ag, Cu and Fe was determined using wet digestion method by
using HNO3(p) for Ag and Cu and HNO3(p) and HCl(p) for determining Fe. The
concentration was analyzed using Atomic Absorption Spechtrophotometer. It was
found the content of Ag, Cu and Fe sequentially 2,1590 mg/Kg, 21.311 mg/Kg dan
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Desa Meranti Utara Kecamatan Pintu Pohan Meranti Kabupaten Toba Samosir
berada pada ketinggian 700-1500 meter di atas permukaan laut. Di desa ini terdapat
sebuah dusun yang disebut dengan Dusun Jambu Dolok yang berada di atas bukit
di wilayah Bukit Barisan. Dusun Jambu Dolok di dalam Peta Kabupaten Toba
Samosir termasuk daerah Hutan Suaka Alam dengan kondisi alam sebagian besar
ditutupi oleh semak dan batu-batuan. Dusun ini terletak sejauh ±20 km ke arah
Kabupaten Asahan.
Suatu hal yang sangat menarik perhatian di daerah ini adalah bahwa
mayoritas batu-batuan yang ada pada lapisan permukaan berwarna kuning emas,
mengkilap dan bercampur dengan warna kecoklatan. Informasi lisan yang
diperoleh penulis dari Dinas Perindustrian dan Perdagangan Kabupaten Toba
Samosir menyatakan bahwa belum pernah ada penelitian dan inventarisasi terhadap
kandungan mineral didalam batu-batuan yang ada di Dusun jambu Dolok
Kecamatan Pintu Pohan Meranti. Informasi lisan yang sama juga diberikan oleh
Dinas Pertambangan dan Energi Propinsi Sumatera utara.
Perak, tembaga dan besi merupakan logam yang mempunyai nilai ekonomis
yang tinggi karena sangat dibutuhkan dalam kehidupan sehari-hari. Logam-logam
ini mempunyai konduktivitas panas yang sangat tinggi dan konduktivitas listrik
yang sangat baik. Perak dan tembaga digunakan dalam pembuatan peralatan
elektronik, perhiasan dan seni bahkan juga di dalam pembuatan uang logam.
Logam besi banyak digunakan dalam pembuatan bahan bangunan, peralatan rumah
Berdasarkan warna yang ditampilkan oleh batu-batuan yang terdapat di
Dusun Jambu Dolok Kabupaten Toba Samosir, penulis menduga adanya
kandungan Perak, Tembaga dan Besi di dalam batu-batuan tersebut. Oleh karena
itu, penulis merasa tertarik untuk menentukan kandungan Perak, Tembaga dan Besi
yang ada didalam batu-batuan tersebut dengan judul “Penentuan Kandungan Ag,
Cu, Dan Fe didalam Batuan Mineral Yang Berasal Dari Dusun Jambu Dolok
Kabupaten Toba Samosir.”
1.2. Permasalahan
1. Apakah batuan mineral yang terdapat di Dusun Jambu Dolok mengandung
Ag, Cu dan Fe?
2. Berapakah kandungan Ag, Cu dan Fe didalam batuan mineral tersebut?
1.3. Pembatasan Masalah
1. Batuan mineral yang dijadikan sampel didalam penelitian ini diambil
secara acak dari Desa Jambu Dolok.
2. Penentuan kandungan Ag, Cu dan Fe dilakukan dengan menggunakan
Spektrofotometer Serapan Atom.
1.4. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui kandungan Ag, Cu dan Fe didalam
batuan mineral yang berasal dari Dusun jambu Dolok Kabupaten Toba
1.5. Manfaat Penelitian
Penelitian ini diharapkan memberikan informasi ilmiah yang bermanfaat bagi
masyarakat di Dusun Jambu Dolok dan Pemerintah kabupaten Toba Samosir
sebagai salah satu upaya inventarisasi Sumber Daya Alam yang ada di Dusun
jambu Dolok, khususnya mengenai kandungan mineral.
1.6. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik FMIPA USU dan di
Laboratorium Penelitian Fakultas Farmasi USU Medan.
1.7. Metodologi Penelitian
1. Penelitian ini merupakan eksperimen laboratorium dan bersifat purposif.
2. Sampel batuan mineral diambil secara acak dari daerah hutan suaka alam di
Dusun Jambu Dolok Kabupaten Toba Samosir.
3. Untuk penentuan Ag dan Cu sampel terlebih dahulu didestruksi dengan
HNO3(p) dan untuk penentuan Fe sampel didestruksi dengan HNO3(p) dan
HCl(p).
4. Kandungan Ag, Cu dan Fe di dalam sampel ditentukan dengan
menggunakan SSA dengan panjang gelombang untuk Ag = 328,1 nm; Cu =
BAB 2
TINJAUAN PUSTAKA
2.1.Batuan
Batu merupakan suatu zat yang padat, keras, dan tahan lama. Karakteristik dari
beberapa jenis batu bervariasi bergantung kepada kondisi dan cara
pembentukannya. Kadang-kadang , kondisi geologi seperti menciptakan suatu batu
bermassa besar dari mineral yang tunggal. Lebih sering beberapa mineral
terkristalisasi serempak dan berbagai proporsi.
Batuan terdiri dari tiga jenis menurut cara pembentukannya, yaitu: batuan
beku, batuan sedimen, dan malihan. Kebanyakan dari batuan beku diproses melalui
pendinginan selama awal kehidupan bumi, massa mineral yang mencair disebut
magma yang pada dasarnya merupakan larutan dari mineral-mineral lain dalam
silika yang mencair. Terakhir kalinya batuan beku dibentuk melalui pendinginan
melalui aliran lahar gunung api yang aktif.
Batuan sedimen mempunyai asal yang sangat berbeda. Misalnya batu pasir
terbentuk ketika pasir halus bersama dengan penyemenan zat-zat seperti liat dan
batu kapur terlarut, didepositkan oleh air. Dibawah tekanan lapisan pasir tersemen
dan membentuk batuan yang sangat keras.
Batuan malihan diproses melalui penerapan pemanasan, tekanan ekstrim,
atau keduanya batuan beku dan batuan sedimen. Jika merupakan suatu batuan
sedimen seperti batu kapur, harus mengalami kontak dengan massa batuan beku
panas yang besar dibawah tekanan yang cukup untuk mencegah dekomposisi dari
kalsium karbonat, akan terekristalisasi, mendapatkan struktur yang baru dan
dipanaskan secara instens dapat mengalami perubahan bentuk dibawah tekanan
yang cukup (Markham E, 1955).
Dari sejarah pembentukan Bumi, diperoleh gambaran bahwa pada awalnya
seluruh bagian luar dari Bumi ini terdiri dari batuan beku. Dengan perjalanan
waktu serta perubahan keadaan, maka terjadilah perubahan-perubahan yang disertai
dengan pembentukan kelompok-kelompok batuan yang lainnya. Proses perubahan
dari satu kelompok batuan ke kelompok lainnya, merupakan suatu siklus yang
dinamakan daur batuan.
Dalam daur tersebut, batuan beku terbentuk sebagai akibat dari pendinginan
dan pembekuan magma. Pendinginan magma yang berupa lelehan silikat, akan
diikuti oleh proses penghabluran yang dapat berlangsung dibawah atau diatas
permukaan Bumi melalui erupsi gunung berapi. Kelompok batuan beku tersebut,
apabila kemudian tersingkap dipermukaan, maka ia akan bersentuhan dengan
atmosfir dan hidrosfir, yang menyebabkan berlangsungnya proses pelapukan.
Melalui proses ini batuan akan mengalami penghancuran. Selanjutnya, batuan yang
telah dihancurkan ini akan dipindahkan/digerakkan dari tempatnya terkumpul oleh
gaya berat, air yang mengalir di atas dan di bawah permukaan, angin yang bertiup,
gelombang dipantai dan gletser di pegunungan-pegunungan yang tinggi. Media
pengangkut tersebut juga dikenal sebagai alat pengikis, yang dalam bekerjanya
berupaya untuk meratakan permukaan Bumi. Bahan-bahan yang diangkutnya baik
itu berupa fragmen-fragmen atau bahan yang larut, kemudian akan diendapkan di
tempat-tempat tertentu sebagai sedimen.
Proses berikutnya adalah terjadinya ubahan dari sedimen yang bersifat
lepas, menjadi batuan yang keras, melalui pembebanan dan perekatan oleh
senyawa mineral dalam larutan, dan kemudian disebut batuan sedimen. Apabila
terhadap batuan sedimen ini terjadi peningkatan tekanan dan suhu sebagai akibat
dari penimbunan dan atau terlibat dalam proses pembentukan pegunungan, maka
lingkungan yang baru, dan terbentuk batuan malihan atau batuan metamorfis.
2.2.Mineral
Batuan tersusun atas campuran mineral-mineral. Kebanyakan mineral terbentuk
ketika magma (lelehan batuan yang mengandung banyak gas) panas mendorong ke
atas dari bawah kerak bumi, mendingin dan memadat. Kondisi-kondisi di tempat
magma mendingin menentukan jenis mineral yang terbentuk. Bentuk-bentuk
geometris yang disebut kristal terbentuk ketika mineral mendingin secara lambat.
Mineral dibagi dalam kelompok-kelompok menurut unsur-unsur yang
menyusunnya. Mineral-mineral yang tersusun dari satu unsur saja disebut
unsur-unsur asli. Contoh: Silikat yang mengandung silika (silika yang bergabung dengan
oksigen), merupakan kelompok terbesar yang jumlahnya mencapai 92% dari
meneral-mineral yang ada di kerak bumi, Karbonat merupakan mineral yang
mengandung unsur-unsur yang tergabung dengan karbon dan oksigen. Mineral ini
merupakan mineral yang paling banyak ditemukan setelah silikat. Halida
merupakan sekelompok mineral yang mengandung unsur-unsur halogen. Sulfida
merupakan sekelompok mineral yang mengandung unsur-unsur yang tergabung
dengan sulfur. Posfat merupakan mineral yang terbentuk ketika fosfor bereaksi
dengan oksigen dan unsur-unsur lain. Oksida merupakan unsur-unsur yang
bergabung dengan oksigen dalam kerak bumi.
Mineral yang terbentuk akan ditentukan oleh elemen-elemen yang tersedia
dan melalui berbagai jenis temperatur dan tekanan yang berbeda yang merata
selama waktu kristal terjadi. Misalnya, jika logam seperti Cu, Zn, Pb, dan Fe
terdapat bersama sulfur, sulfida-sulfida dari elemen ini akan terbentuk seperti FeS2,
CuFeS2, PbS, dan ZnS. Di sisi lain, jika metal seperti Cu, Pb, Zn, dan Fe terdapat
bersama dengan karbon dan oksigen, kemudian karbonat kemungkinan akan
Mineral sebagai pembangun batu merupakan padatan anorganik dengan
suatu struktur dalam yang spesifik dan komposisi kimia yang berbeda. Dapat
terbentuk pada berbagai kondisi, seperti:
1. Selama pendinginan material yang mendingin (baja, dari lahar, batuan
beku)
2. Selama penguapan cairan (garam, gula, yang cenderung menguap)
3. Pendinginan cairan (larutan jenuh)
4. Pada suhu dan tekanan yang tinggi kristal yang baru mungkin
bertumbuh dalam material padat (berlian dari batu arang, metamorfosis)
Mineral dapat diklasifikasikan ke dalam beberapa golongan berdasarkan
pada komposisi kimianya, yaitu:
1. Elemen (karbon/berlian, sulfur, seng, emas, perak, tembaga, besi, dll)
2. Halida (unsur dan halogen seperti klorin, bromin, iodin, misalnya
natrium klorida)
3. Oksida (unsur dan oksigen seperti hematit/ besi oksida)
4. Sulfida (unsur dan sulfur seperti pyrit/ besi sulfur dan galena/ timah
sulfur)
5. Unsur dan ion kompleks (ion tidak hanya yang bermuatan tunggal),
umumnya seperti:
a. Karbonat (CO32-), kalsit
b. Sulfat (SO42-), gips dan2kulit telur
Kelimpahan mineral pada lapisan bumi ditunjukkan dalam tabel berikut:
2.3.Perak
Perak seringkali terdapat bersama dengan emas, tetapi sekitar 70 persen biasanya
berikatan dalam deposit logam dasar sulfida dari plumbum, tembaga, atau seng
dan terkandung sebagai biproduk; oleh karena itu, angka produksi perak dikontrol
melalui produksi dari logam yang berikatan. Bijih-bijih mineral yang terutama dari
perak adalah sebagai berikut:
Mineral Komposisi Persen Ag
Perak murni Ag 100,0
Acanthite Ag2S 87,1
Cerargyrite AgCl 75,3
Proustite Ag3AsS3 65,4
Perak yang berwarna dasar putih keperakan ini membedakannya mudah
dari logam-logam lain yang mirip. Perak yang murni ditemukan dalam
deposit-deposit hidrotermal sulfida utama berikatan dengan bermacam sulfida dari perak
dan timbel, dan dalam beberapa bijih deposit dalam daerah teroksidasi, berikatan
dengan calcite, barite, dan kwarsa. Perak juga berikatan dengan uranit pada tempat
tertentu. Beberapa perak sangat sering tersedia bersama dengan emas murni.
Platina menyerupai perak tetapi sedikit lebih keras. Bismut murni juga kelihatan
seperti perak, tetapi bismut berwarna pucat kemerahan pada permukaan yang sejuk.
Kegunaan utama perak untuk waktu yang lama adalah pembuatan uang
logam; tetapi sekarang kegunaan yang paling banyak digunakan dalam pelapisan
film fotografi (perak bromida dan perak iodida). Kegunaan yang lain adalah untuk
peralatan perak, peralatan listrik dan elektronik (tombol, penunjuk, dalam
komputer dan tabulator),pelapisan dengan perak, berbagai macam campuran pada
perhiasan dan seni, sebagaimana juga dalam industri kimia. Penggunaannya dalam
perhiasan dan seni berdasar kenyataan bahwa perak adalah yang paling bersinar
dari semua logam. Dalam bentuk koloidal, perak digunakan untuk obat-obatan
tertentu, juga digunakan dalam pengawetan makanan, minuman, dan pengobatan
gigi. Campuran perak umumnya adalah bersifat keras dan liat. Perak murni
tersusun dari 92,5 persen perak dan 7,5 persen logam lain, biasanya tembaga. Emas
kuning adalah 53 persen emas, 25 persen perak, dan 22 persen tembaga.
Perak dapat ditempa dan mempunyai konduktivitas panas yang sangat
tinggi dan konduktivitas listrik yang baik. Lebih keras dari emas tetapi lebih
lembek dari tembaga. Logam yang berkilau ini meleleh pada 960oC (1761oF) dan
dapat lebih mudah dikerjakan dan dibentuk. Perak tidak berubah karena
kelembapan, kekeringan, atau keadaan basa, tetapi sangat cepat pudar dalam udara
2.4.Tembaga
Tembaga terdapat sedikit berlimpah dalam deposit sulfida, dalam daerah
pemotongan batuan malihan, dan juga tembaga murni pada lahar. Deposit yang
banyak juga terdapat sebagai sedimen kaya tembaga. Bijih mineral dari logam
merah oranye ini terjadi dalam berbagai jenis deposit di bawah ini:
Mineral Komposisi Persen Cu
Kalkopirit CuFeS2 34,5
Bornit Cu5FeS4 63,3
Kalkosit Cu2S 79,8
Enargit Cu3AsS4 48,3
Tetrahedrit Cu12Sb4S13 52,1
Malasit Cu2CO3(OH)2 57,3
Ekstraksi dan pemurnian tembaga merupakan proses yang relatif sederhana
dan memperlihatkan beberapa sifat-sifat kimia yang penting. Bijih karbonat
tembaga CuCO3 dapat direduksi dengan karbon menghasilkan Cu. Bijih sulfida
sebagian dioksidasi dan kemudian dileburkan untuk memberikan produk yang lebih
murni (Mahan B, 1966).
Tembaga merupakan salah satu dari banyak logam penting dalam industri.
Khususnya pada industri elektronik, yang menggunakan sekitar 60 persen logam.
Logam ini mempunyai titik lebur pada 1083oC (1981oF). Tembaga merupakan
konduktor panas yang baik dan dapat digunakan dalam perkakas memasak,
pemanas, dan pendingin. Tembaga sangat mudah ditempa, dapat dipukul, dapat
dicap, dapat dipintal ke dalam berbagai macam bentuk, dapat digulung dalam
bentuk lembaran. Logam ini dapat ditarik menjadi kawat yang lebih tipis dari
sehelai rambut. Tembaga mempunyai warna merah tembaga, elastis, dan
merupakan logam yang berkilau. Tembaga juga tahan terhadap korosi, dan dapat
Logam ini dapat digunakan dalam banyak produk, sebagai contoh
sebagaimana tembaga yang murni dalam kabel dan peralatan elektronik karena
konduktivitasnya yang sangat baik. Tembaga juga digunakan sebagai pembangkit,
mesin, lokomotif listrik, bola lampu, telegrap, pendingin udara dan kapal.
Campuran tembaga baik dengan seng dalam kuningan dan dengan nikel,
aluminium, dan logam lain dalam bermacam-macam campuran lain. Area
penggunaannya termasuk dalam industri elektronik, otomobil, konstruksi, amunisi,
dan mata uang.
2.5.Besi
Besi merupakan logam yang paling penting dalam peradaban modern karena
merupakan dasar dari industri baja, tetapi rangkaian dari logam lain dimanfaatkan
dalam pembuatan berbagai macam campuran logam dengan besi di dalam berbagai
macam aspek dari industri baja. Hal ini disebut sebagai logam campuran besi
(ferroalloy metals).Ketika ditambahkan pada pembuatan baja dalam jumlah yang
sedikit, sifat kekerasan, kekuatan, daya tahan, kelunakan, kelunakan dan daya tahan
terhadap korosi umumnya bertambah baik.
Besi merupakan logam berwarna putih keperakan dan dapat dibentuk dan
elastis. Besi merupakan logam yang sangat reaktif, bereaksi dengan oksigen
membentuk karat. Logam ini melebur pada 1540oC.
Bijih mineral besi terdapat dalam beberapa jenis utama:
Mineral Komposisi Persen Fe
Magnetit Fe3O4 72,4
Hematit Fe2O3 70,0
Limonit FeO(OH).nH2O 59,0-63,0
Siderit FeCO3 48,2
Besi terdapat sekitar lima persen dari batuan beku pada kerak bumi.
Kemungkinan merupakan unsur yang paling melimpah di planet bumi karena inti
bumi terdiri dari hampir seluruhnya besi dan nikel. Pada kondisi bebas, besi
ditemukan hanya dalam meteorit yang bercampur dengan nikel. Senyawanya
melimpah di alam. Sulfida (pirit) FeS2 merupakan mineral yang sangat umum
tetapi tidak digunakan sebagai bijih besi karena sulitnya menghilangkan sulfur
secara sempurna. Bijih besi yang paling penting adalah hematit Fe2O3; tetapi besi
juga dilebur dari oksida hidrat 2 Fe2O3.3H2O, dari magnetit Fe3O4 (mengandung
kandungan besi yang lebih tinggi dibandingkan bijih lainnya) dan karbonatnya
siderit FeCO3 bijih besi utama Inggris (Scarlett, 1956).
Dalam deposit besi dengan kondisi oksidasi siderite dan besi silikat
menghasilkan limonite berlimpah. Deposit hematit dan magnetit sangat lambat
teroksidasi akhirnya membentuk limonit. Oksidasi di bawah kondisi tropikal
menghasilkan hematit dari ferrosilikat dalam batu. Deposit sulfida pyrit, pyrrhotite
dan marcasite adalah mineral-mineral besi yang dasar. Pyrite merupakan mineral
keras yang terbentuk dalam semua deposit dan segala temperatur bahkan secara
lokal pada permukaan di bawah kondisi reduksi dan dapat dihasilkan dalam larutan
alkalin.
Marcasite terbentuk hanya dalam larutan yang asam, tetapi dapat
mengkristal bersama-sama dengan pyrit. Diatas 450oC akan berubah menjadi pyrit.
Marcasite adalah mineral yang relatif tidak stabil terbentuk terutama dekat ke
permukaan dan lebih mudah teroksidasi dibandingkan pyrit dalam reaksi yang
sama. Pyrrhotite (Fe7S8) dianggap sebagai suatu larutan padat dari sulfur dalam
FeS. Mudah dihancurkan dengan melarutkan dengan H2SO4 dengan perkemabngan
H2S dimana deposit tembaga mungkin mengendapkan tembaga sulfida dan
mencegah pengembangan dari daerah chalcocite. Jugamudah diserang dengan
2.6.Spektrofotometri Serapan Atom
Suatu spektrum merupakan hasil yang diperoleh bila suatu berkas energi radiasi
dibagi-bagi kedalam panjang-panjang gelombang komponennya. Jika radiasi yang
terbagi-bagi (terdispersikan) itu berasal dari atom tereksitasi, spektrum itu disebut
spektrum atom. Bila radiasi elektromagnetik kontinu misalnya cahaya putih
dilewatkan suatu zat, panjang gelombang tertentu dari radiasi itu mungkin akan
diserap. Panjang-panjang gelombang ini karakteristik dari zat-zat yang
mengabsorpsi (menyerap) radiasi dan pola-pola garis gelap ini disebut spektrum
absorpsi. Bila dingin, suatu zat akan mengabsorpsi radiasi pada panjang-panjang
gelombang yang sama dengan panjang-panjang gelombang emisinya bila zat itu
tereksitasi (Keenan, 1980).
Perubahan dari elemen-elemen logam suatu sampel dari larutan menjadi
uap terdisosiasi dapat dicapai dengan energi panas, baik dengan suatu nyala atau
tanur listrik. Pengendalian yang cermat dari temperatur dibutuhkan untuk konversi
optimum ke uap atom. Temperatur yang terlalu tinggi tidak baik karena fraksi atom
menjadi terionisasi dan ion-ion tidak mengabsorpsi pada panjang gelombang yang
sama sebagaimana atom-atom yang netral (Ewing, 1960).
Pada spektrofotometri serapan atom, atom pada keadaan dasar
mengabsorpsi energi cahaya dari panjang gelombang yang spesifik karena
memasuki keadaan tereksitasi. Sebagaimana jumlah atom pada garis cahaya
meningkat, jumlah cahaya yang disbsorpsi juga meningkat. Dengan mengukur
jumlah cahaya yang diabsorpsi, penentuan kuantitatif dari analit dapat dilakukan.
Penggunaan sumber cahaya yang khusus dan pemilihan panjang gelombang secara
hati-hati mengizinkan penentuan khusus dari elemen-elemen tunggal.
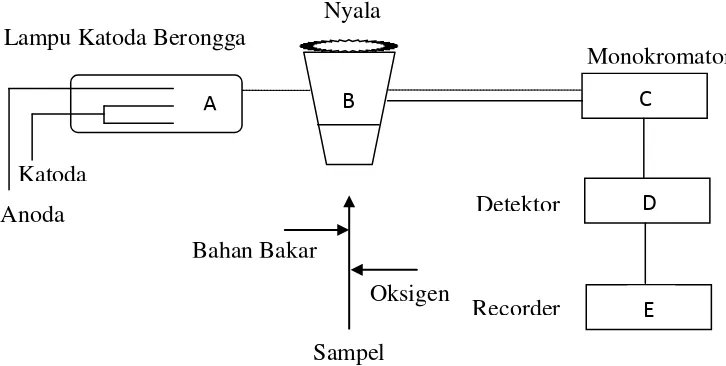
Terdapat 5 dasar dalam instrumen spektroskopi serapan atom:
1. Sumber cahaya yang mengemisikan spektrum dari elemen yang sesuai
2. Sel absorpsi dimana atom-atom dari sampel diproduksi
5. Rekorder untuk menunjukkan pembacaan setelah proses instrumen selesai
(PelkinElmer, 1996).
Gambar 2.1 Diagram Balok Peralatan Spektrofotometer Serapan Atom dengan
Nyala (Clark, D.V., 1979)
Atomisasi dapat dilakukan baik dengan nyala maupun dengan tungku.
Untuk mengubah unsur metalik menjadi uap atau hasil disosiasi diperlukan energi
panas. Temperatur harus benar-benar terkendali dengan sangat hati-hati agar proses
atomisasinya sempurna. Ionisasi harus dihindarkan dan ini dapat terjadi bila
temperatur terlalu tinggi. Suatu tipe atomiser nyala, bahan bakar dan gas oksidator
dimasukkan ke dalam gas pencampur kemudian dilewatkan menuju pembakar.
Sampel dihisap masuk ke kamar pencampur. Nyala akan dihasilkan. Pada proses
atomisasi tanpa nyala, sampel diletakkan pada batang grafit yang porosnya
horizontal atau pada logam tantalum yang berbentuk pita. Pada tungku grafit
temperatur dapat dikendalikan secara elektris. Biasanya temperatur dinaikkan
secara bertahap untuk menguapkan dan sekaligus mendisosiasi senyawa yang
dianalisis (Khopkar, 1984).
Pada spektrofotometri serapan atom sampel diaspirasikan ke dalam nyala
dimana temperaturnya adalah 2000-3000 K. Sampel diatomisasikan (dipecah
Sumber radiasi di dalam peralatan ini adalah lampu katoda berongga.
Lampu katoda berongga diisi dengan Ne atau Ar pada tekanan 130-170 Pa. Ketika
tegangan yang sangat tinggi digunakan di antara katoda dan anoda, gas pengisi
menjadi terionisasi dan ion-ion positif dipercepat menuju katoda. Kemudian
menumbuk katoda dengan energi yang cukup untuk memercikkan atom-atom
logam dari katoda ke fase gas. Kebanyakan atom-atom yang terpercik berada pada
keadaan eksitasi, mengemisikan foton dan kemudian kembali kekeadaan dasar.
Radiasi atom ini persis sama dengan frekuensi sebagaimana yang akan diabsorpsi
oleh atom-atom analit.
2.7. Metode Analisis dengan Menggunakan SSA
1. Metode Kurva Standar
Metode Kurva Standar menggunakan jumlah unsur yang diinginkan dalam
larutan dengan suatu komposisi yang sama dengan yang tidak diketahui. Kurva
Standar kemudian digunakan untuk menemukan konsentrasi yang tidak
diketahui dari absorbansinya. Medium dimana analit terkandung disebut
matriks. Sangat penting bahwa komposisi standar harus sedekat mungkin
dengan yang konsentrasi sampelyang tidak diketahui karena larutan yang
berbeda mempunyai jenis pengganggu yang mempengaruhi sinyal.
2. Metode Standar Addisi
Pada metode standar adisi, ditambahkan larutan standar yang telah diketahui
konsentrasinya dalam volume tertentu dan peningkatan sinyal absorbansi
diukur. Masing-masing larutan diencerkan sampai volume total yang sama dan
harus mempunyai komposisi akhir yang sama (kecuali untuk konsentrasi
analit). Jika konsentrasi yang mau dicari adalah [X] da konsentrasi standar
yang ditambahkan [S], maka dapat dikatakan bahwa:
[�]
Dimana AX adalah absorbansi analit yang dicari dan AS+X adalah absorbansi
dari analit yang dicari ditambah standar.
3. Metode Internal Standar
Pada internal standar, sejumlah unsur yang tidak ada dalam analit ditambahkan
ke dalam sampel. Dalam menggunakan internal standar, campuran yang telah
diketahui dari sampel dan analit digunakan untuk membuat kurva kalibrasi.
Jika sejumlah standar ditambahkan ke sampel yang tidak diketahui, kurva
kalibrasi dapat digunakan untuk menentukan konsentrasi yang tidak diketahui
(D. Harris, 1982).
Suatu garis yang cocok di dalam spektrum emisi dari sumbernya dipilih
untuk dianalisa. Garis ini, yang disebut garis resonansi menunjukkan suatu
perpindahan dari keadaan dasar ke keadaan tereksitasi dan dengan demikian
menunjukkan frekuensi yang tepat bagi absorpsi oleh atom-atom di dalam nyala
yang ada pada keadaan dasar. Garis-garis emisi dari katoda cekung sangat tajam,
pada umumnya lebih sempit daripada garis-garis absorpsi di dalam nyala sehingga
dengan demikian cukup sesuai untuk percobaaan absorpsi atomik. Yang hanya
diperlukan oleh monokromator adalah bahwa garis-garis lain di dalam spektrum
dari sumber yang timbul dari katoda logam dan dari gas inert tidak dipancarkan ke
detektor (Underwood, 1980).
2.8. Cara Kerja spektrofotometer serapan atom
Radiasi dihasilkan oleh lampu katoda berongga dimana katoda dibuat dari logam
yang sesuai dengan yang akan dianalisa. Permukaan dibombardir dengan elektron
menyebabkan eksitasi dari atom yang dipilih dan menyebabkan emisi dari radiasi
Temperatur yang tinggi dari nyala menyebabkan:
• Pelarut diuapkan
• Molekul dan ion yang terdapat di larutan dipisahkan menjadi atom-atom
untuk menghasilkan uap atom.
• Sebagian kecil dari atom-atom tereksitasi, elektron naik ke tingkat energi
yang lebih tinggi. Hal ini bahkan memberikan suatu warna pada nyala
sesuai dengan energi emisi pada saat elektron tereksitasi kembali ke
keadaan dasar.
Atomisasi analit di dalam Spektrofotometer Serapan Atom dapat dituliskan sebagai
berikut:
penguapan
M+ X- M+ X- MX
Larutan uap padatan
M(gas) + X(gas) MX
Gas
Penyerapan energi radiasi (SSA)
hV
M*(gas)
Larutan analit kemudian diubah menjadi kabut dengan melewatkannya melalui
nebuliser. Larutan bercampur dengan gas pembakar dan udara bergerak pada sudut
yang tepat ke alirannya yang memecah menjadi tetesan halus. Sisa kabut dari
Cahaya yang ditransmisikan, berkurang intensitasnya masuk melalui suatu
monokromator yang memilih panjang gelombang untuk pengukuran dan kemudian
masuk ke detektor. Detektor merespon dengan memproduksi suatu sinyal yang
sesuai dengan intensitas cahaya yang mengenainya. Hal ini sesuai dengan intensitas
cahaya yang tidak terserap oleh atom yang sebanding dengan konsentrasi analit.
Sinyal diperkuat dan diproses untuk menghasilkan pembacaan langsung dari
BAB 3
METODOLOGI PENELITIAN
3.1.Alat – Alat
− Spektrofotometer Serapan Atom Hitachi Z-2000 − Neraca analitik Mettler PM 400
− Oven Fisher
− Termometer Fisher
− Tanur listrik Fisher
− Peralatan gelas Pyrex
− Cawan crusibel
− Kertas saring whatman no 42 − Botol akuades
− Hot plate − Desikator
− Alu dan lumpang − Spatula
3.2.Bahan – Bahan
− Akuades
− Indikator universal
3.3.Prosedur
3.3.1. Penyediaan Reagen
3.3.1.1. Pembuatan Larutan Standar Ag
a. Larutan Blanko
Sebanyak 50 mL akuades ditambahkan dengan 5 mL HNO3 pekat kemudian
dipanaskan sampai setengah volume awal kemudian disaring ke dalam labu takar
50 mL dan diencerkan sampai garis tanda dan dihomogenkan.
b. Larutan Standar Ag 1000 mg/L
Sebanyak 1,575 gram AgNO3 dilarutkan ke dalam akuades dan ditambahkan
dengan 1,5 mL HNO3(p) kemudian diencerkan dalam labu ukur 1000 mL sampai
garis tanda dan dihomogenkan.
c. Larutan standar Ag 100 mg/L
Dipipet sebanyak 10 mL larutan induk Ag 1000 mg/L dan dimasukkan ke dalam
labu ukur 100 mL, diencerkan dengan akuades hingga garis tanda dan
d. Larutan standar Ag 10 mg/L
Dipipet sebanyak 10 mL larutan induk Ag 100 mg/L dan dimasukkan ke dalam
labu ukur 100 mL, diencerkan dengan akuades hingga garis tanda dan
dihomogenkan.
e. Larutan seri standar Ag 0,05; 0,10; 0,50; 1,00; 2,00; 3,00; 4,00; 5,00 mg/L
Dipipet masing-masing sebanyak 0,25; 0,5; 2,5; 5; 10; 15; 20 dan 25 mL larutan
standar Ag 10 mg/L dan dimasukkan ke dalam labu ukur 50 mL, diencerkan
dengan akuades sampai garis tanda dan dihomogenkan.
3.3.1.2. Pembuatan Larutan Standar Cu
a. Larutan Blanko
Sebanyak 50 mL akuades ditambahkan dengan 5 mL HNO3 pekat kemudian
dipanaskan sampai setengah volume awal kemudian disaring ke dalam labu takar
50 mL dan diencerkan sampai garis tanda dan dihomogenkan.
b. Larutan Standar Cu 1000 mg/L
Sebanyak 3,929 gram CuSO4.5H2O dilarutkan ke dalam akuades kemudian
c. Larutan standar Cu 100 mg/L
Dipipet sebanyak 10 mL larutan induk Cu 1000 mg/L dan dimasukkan ke dalam
labu ukur 100 mL, diencerkan dengan akuades hingga garis tanda dan
dihomogenkan.
d. Larutan standar Cu 10 mg/L
Dipipet sebanyak 10 mL larutan induk Cu 100 mg/L dan dimasukkan ke dalam
labu ukur 100 mL, diencerkan dengan akuades hingga garis tanda dan
dihomogenkan.
e. Larutan seri standar Cu 0,5; 1,0; 1,5; 2,0; 2,5; 3,0 mg/L
Dipipet masing-masing sebanyak 2,5; 5; 7,5; 10 dan 12,5 mL larutan standar Cu 10
mg/L dan dimasukkan ke dalam labu ukur 50 mL, diencerkan dengan akuades
sampai garis tanda dan dihomogenkan.
3.3.1.3. Pembuatan Larutan Standar Fe
a. Larutan Blanko
Sebanyak 50 mL akuades ditambahkan dengan 2 mL HNO3 pekat dan ditambahkan
6 mL HCl pekat kemudian dipanaskan sampai setengah volume awal kemudian
disaring ke dalam labu takar 50 mL dan diencerkan sampai garis tanda dan
b. Larutan Standar Fe 1000 mg/L
Sebanyak 4,321 gram Fe(NO3)3 dilarutkan ke dalam akuades kemudian diencerkan
dalam labu ukur 1000 mL sampai garis tanda dan dihomogenkan.
c. Larutan standar Fe 100 mg/L
Dipipet sebanyak 10 mL larutan induk Fe 1000 mg/L dan dimasukkan ke dalam
labu ukur 100 mL, diencerkan dengan akuades hingga garis tanda dan
dihomogenkan.
d. Larutan standar Fe 10 mg/L
Dipipet sebanyak 10 mL larutan induk Fe 100 mg/L dan dimasukkan ke dalam labu
ukur 100 mL, diencerkan dengan akuades hingga garis tanda dan dihomogenkan.
e. Larutan seri standar Fe 0,5; 1,0; 1,5; 2,0; 2,5; 3,0 mg/L
Dipipet masing-masing sebanyak 2,5; 5; 7,5; 10 dan 12,5 mL larutan standar Fe 10
mg/L dan dimasukkan ke dalam labu ukur 50 mL, diencerkan dengan akuades
sampai garis tanda dan dihomogenkan.
3.3.2. Preparasi Sampel
3.3.2.1.Penyediaan larutan sampel untuk penentuan Ag dan Cu
Sampel dihaluskan, kemudian dikeringkan di dalam oven dan ditanurkan kemudian
lalu ditambahkan 25 mL HNO3 pekat dan ditambahkan H2O2 secukupnya. Ditutup
dengan kaca arloji lalu dipanaskan hingga setengah volume awal. Didinginkan dan
disaring. Dicuci residunya dengan akuades dan dicampur dengan filtratnya dan
dimasukkan ke dalam labu ukur 100 mL kemudian diatur pHnya 2-4 dan
diencerkan dengan akuades sampai garis tanda.
3.3.2.2.Penyediaan larutan sampel untuk penentuan Fe
Sebanyak 10 gram sampel dihaluskan, dimasukkan ke dalam oven, ditanur, dan
ditimbang secara teliti sebanyak 5 gram dengan menggunakan neraca analitis.
Sampel dimasukkan ke dalam beaker glass 250 mL ditambahkan 10 mL akuades
lalu ditambahkan 10 mL HNO3 pekat kemudian ditambahkan 30 mL HCl pekat.
Ditutup dengan kaca arloji lalu dipanaskan hingga setengah volume awal.
Didinginkan dan disaring. Dibilas endapan dengan akuades dan digabungkan
dengan filtrat penyaringan lalu dimasukkan ke dalam labu ukur 100 mL kemudian
diatur pHnya 2-4 dan diencerkan dengan akuades sampai garis tanda.
3.3.3. Pembuatan Kurva Kalibrasi Larutan Standar Ag
Larutan blanko Ag 0,00 mg/L ditentukan absorbansinya dengan menggunakan Spektrofotometer Serapan Atom pada λ = 328,1 nm dan dilakukan hal yang sama untuk larutan seri standar Ag 0,05; 0,10; 0,50; 1,00; 2,00; 3,00; 4,00 dan 5,00
mg/L.
3.3.4. Pembuatan Kurva Kalibrasi Larutan Standar Cu
3.3.5. Pembuatan Kurva Kalibrasi Larutan Standar Fe
Larutan blanko Fe 0,0 mg/L ditentukan absorbansinya dengan menggunakan Spektrofotometer Serapan Atom pada λ = 248,3 nm dan dilakukan hal yang sama untuk larutan seri standar Fe 0,5; 1,0; 1,5; 2,0; 2,5; 3,0 mg/L.
3.3.6.Penentuan kadar Ag pada sampel dengan menggunakan Spektrofotometer Serapan Atom
Larutan sampel yang telah didestruksi ditentukan absorbansinya pada λ= 328,1
nm dengan menggunakan alat Spektrofotometer Serapan Atom.
3.3.7.Penentuan kadar Cu pada sampel dengan menggunakan Spektrofotometer Serapan Atom
Larutan sampel yang telah didestruksi ditentukan absorbansinya pada λ = 324,7
nm dengan menggunakan alat Spektrofotometer Serapan Atom.
3.3.8.Penentuan kadar Fe pada sampel dengan menggunakan Spektrofotometer Serapan Atom
Larutan sampel yang telah didestruksi ditentukan absorbansinya pada λ = 248,3
3.4.Bagan Penelitian
3.4.1. Pembuatan Kurva Kalibrasi Perak (Ag)
larutan blanko Perak (Ag) 0,00 mg/L
ditentukan absorbansinya pada
panjang gelombang = 328,1 nm dengan
menggunakan alat Spektrofotometer Serapan Atom
Hasil
NB: dilakukan prosedur yang sama untuk larutan seri standar perak (Ag) 0,05;
0,10; 0,50; 1,00; 2,00; 3,00; 4,00 dan 5,00 mg/L.
3.4.2. Pembuatan Kurva Kalibrasi Tembaga (Cu)
larutan blanko Tembaga (Cu) 0,0 mg/L
ditentukan absorbansinya pada
panjang gelombang = 324,7 nm dengan
menggunakan alat Spektrofotometer Serapan Atom
Hasil
NB: dilakukan prosedur yang sama untuk larutan seri standar tembaga (Cu) 0,5;
3.4.3. Pembuatan Kurva Kalibrasi Besi (Fe)
larutan blanko Besi (Fe) 0,0 mg/L
ditentukan absorbansinya pada
panjang gelombang = 248,3 nm dengan
menggunakan alat Spektrofotometer Serapan Atom
Hasil
NB: dilakukan prosedur yang sama untuk larutan seri standar besi (Fe ) 0,5; 1,0;
3.4.4. Penyediaan larutan sampel untuk penentuan Ag dan Cu
sampel batu
dihaluskan dengan alu dan lumpang
serbuk batu
ditimbang sebanyak 5 gram
dimasukkan ke dalam beaker glass 250 mL
ditambahkan 10 mL akuades
ditambahkan 25 mL HNO3 pekat
ditutup dengan kaca arloji
disaring dengan kertas saring whatman no 42
dibilas dengan akuades
dikumpulkan dalam labu ukur 100 mL ditambahkan H2O2 secukupnya
3.4.5.Penyediaan larutan sampel untuk Fe
sampel batu
dihaluskan dengan alu dan lumpang
serbuk batu
ditimbang sebanyak 5 gram
dimasukkan ke dalam beaker glass 250 mL
ditambahkan 10 mL akuades
ditambahkan 10 mL HNO3 pekat
ditutup dengan kaca arloji
disaring dengan kertas saring whatman no 42
dibilas dengan akuades
dikumpulkan dalam labu ukur 100 mL
3.4.6.Penentuan kadar Ag dengan menggunakan Spektrofotometer Serapan Atom
Larutan Ag
Hasil
ditentukan absorbansinya pada
panjang gelombang = 328,1 nm dengan
menggunakan alat Spektrofotometer Serapan Atom
3.4.7.Penentuan Kadar Cu dengan menggunakan Spektrofotometer Serapan Atom
Larutan Cu
ditentukan absorbansinya pada
panjang gelombang = 324,7 nm dengan
menggunakan alat Spektrofotometer Serapan Atom
Hasil
3.4.8.Penentuan Kadar Fe dengan menggunakan Spektrofotometer Serapan Atom
Larutan Fe
ditentukan absorbansinya pada
panjang gelombang = 248,3 nm dengan
menggunakan alat Spektrofotometer Serapan Atom
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil dan Pengolahan Data
4.1.1. Logam Perak
Tabel 4.1. Kondisi alat SSA Merek Hitachi Z-2000 pada pengukuran konsentrasi logam Perak (Ag)
No Parameter Logam Perak
1 Panjang gelombang (nm) 328,1
2 Tipe nyala Udara-C2H2
3 Kecepatan aliran gas pembakar (L/min) 2,0
4 Kecepatan aliran udara (L/min) 15,0
5 Lebar celah (nm) 1,3
6 Ketinggian tungku (mm) 7,5
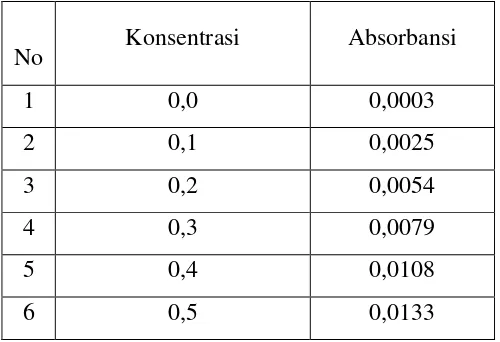
Tabel 4.2. Data Absorbansi Larutan Standar Perak (Ag)
No Konsentrasi Absorbansi
1 0,0 0,0003
2 0,1 0,0025
3 0,2 0,0054
4 0,3 0,0079
5 0,4 0,0108
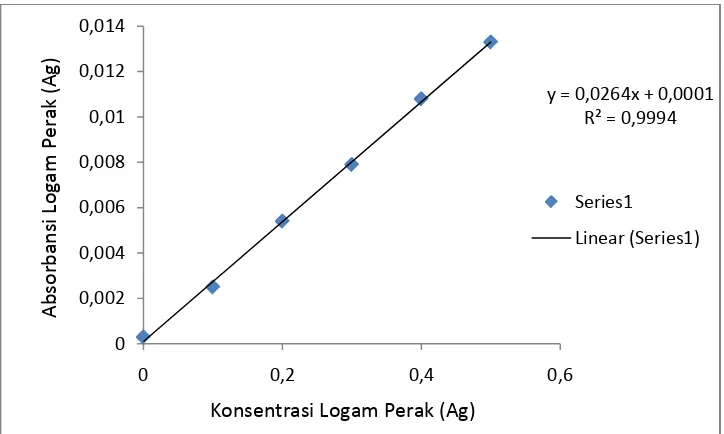
Gambar 4.1. Kurva Kalibrasi Larutan Standar Perak (Ag)
4.1.2. Pengolahan Data Logam Perak (Ag)
4.1.2.1. Penurunan Persamaan Garis Regresi dengan Metode Least Square
Hasil pengukuran absorbansi larutan seri standar logam Perak (Ag) pada tabel 4.2.
diplotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi berupa
garis linier. Persamaan garis regresi untuk kurva kalibrasi ini dapat
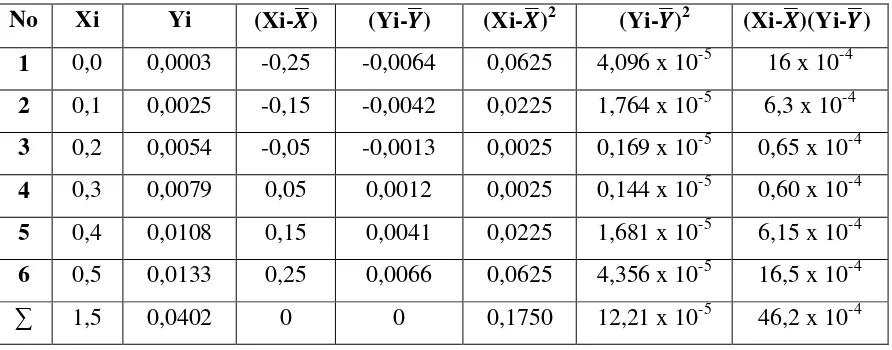
Tabel 4.3. Penurunan Persamaan Garis Regresi untuk Penentuan Konsentrasi Logam Perak (Ag) Berdasarkan Pengukuran Absorbansi Larutan Standar Perak (Ag)
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
garis:
y = ax + b
dimana:
a = slope
b = intersept
selanjutnya harga slope dapat ditentukan dengan menggunakan metode least square
sebagai berikut:
� =∑(Xi−X�)(Yi−Y�)
Dengan mensubstitusikan harga-harga yang tercantum pada tabel 4.9. pada
persamaaan ini maka diperoleh:
� =46,2 x 10
Maka persamaan garis yang diperoleh adalah:
y = 0,0264x + 0,0001
4.1.2.2. Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut:
�= ∑(Xi−X�)(Yi−Y�) [∑(Xi−X�)2∑(Yi−Y�)2 ]1/2
Koefisien korelasi untuk logam Perak (Ag) adalah:
�= 46,2 x 10
−4
[(0,1750)(1,221x10−4)]1/2
r = 0,9994
4.1.2.3.Penentuan Kadar Logam Perak (Ag) Dari Sampel Batuan Mineral Dari Dusun Jambu Dolok Kabupaten Toba Samosir
Kadar perak (Ag) dapat ditentukan dengan menggunakan metode kurva kalibrasi
dengan mensubstitusikan nilai Y (absorbansi) yang diperoleh dari hasil
Dari data pengukuran absorbansi logam perak untuk sampel batuan mineral,
diperoleh serapan (A) sebesar 0,0058.
Dengan mensubstitusikan nilai Y (Absorbansi) kepersamaan garis regresi
Maka diperoleh konsentrasi logam perak (Ag) 0,2159 mg/L.
4.1.2.4. Perhitungan Kadar Logam Perak (Ag) dalam mg/Kg
��������������� (��) = X �
Maka diperoleh kadar logam perak (Ag) pada sampel batuan mineral dari Dusun
4.1.3. Logam Tembaga
Kondisi alat Spektrofotometer Serapan Atom (SSA) pada pengukuran konsentrasi
logam tembaga (Cu) dapat dilihat pada Tabel 4.1.
Tabel 4.4.Kondisi alat SSA Merek Hitachi Z-2000 pada pengukuran konsentrasi logam Tembaga (Cu)
No Parameter Logam Tembaga
1 Panjang gelombang (nm) 324,8
2 Tipe nyala Udara-C2H2
3 Kecepatan aliran gas pembakar (L/min) 2,0
4 Kecepatan aliran udara (L/min) 15,0
5 Lebar celah (nm) 1,3
6 Ketinggian tungku (mm) 7,5
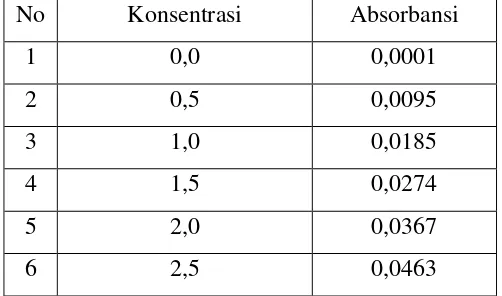
Tabel 4.5. Data Absorbansi Larutan Standar Tembaga (Cu)
No Konsentrasi Absorbansi
1 0,0 0,0001
2 0,5 0,0095
3 1,0 0,0185
4 1,5 0,0274
5 2,0 0,0367
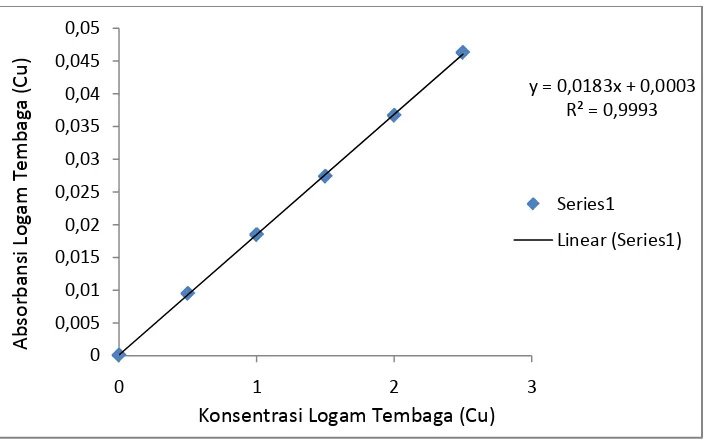
Gambar 4.2. Kurva Kalibrasi Larutan Standar Tembaga (Cu)
4.1.4. Pengolahan Data Logam Tembaga (Cu)
4.1.4.1. Penurunan Persamaan Garis Regresi dengan Metode Least Square
Hasil pengukuran absorbansi larutan seri standar logam Tembaga (Cu) pada tabel
4.8. diplotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi
berupa garis linier. Persamaan garis regresi untuk kurva kalibrasi ini dapat
Tabel 4.6. Penurunan Persamaan Garis Regresi untuk Penentuan Konsentrasi Logam Tembaga (Cu) Berdasarkan Pengukuran Absorbansi Larutan Standar Tembaga (Cu)
No Xi Yi (Xi-��) (Yi-��) (Xi-��)2 (Yi-��)2 (Xi-��)(Yi-��)
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
garis:
y = ax + b
dimana:
a = slope
b = intersept
selanjutnya harga slope dapat ditentukan dengan menggunakan metode least square
� =∑(Xi−X�)(Yi−Y�)
∑(Xi−X�)2
b = y- ax
Dengan mensubstitusikan harga-harga yang tercantum pada tabel 4.9. pada
persamaaan ini maka diperoleh:
� =0,0803
4,3750 = 0,0183
b = 0,0231 – (0,0183)(1,25)
= 0,0231 – 0,0228
= 0,0003
Maka persamaan garis yang diperoleh adalah:
y = 0,0183x + 0,0003
4.1.4.2. Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut:
�= ∑(Xi−X�)(Yi−Y�) [∑(Xi−X�)2∑(Yi−Y�)2 ]1/2
Koefisien korelasi untuk logam Tembaga (Cu) adalah:
�= 0,0803
[(4,3750)(14,76 x 10−4)]1/2
4.1.4.3.Penentuan Kadar Logam Tembaga (Cu) Dari Sampel Batuan Mineral Dari Dusun Jambu Dolok Kabupaten Toba Samosir
Kadar tembaga (Cu) dapat ditentukan dengan menggunakan metode kurva kalibrasi
dengan mensubstitusikan nilai Y (absorbansi) yang diperoleh dari hasil
pengukuran terhadap garis regresi dari kurva kalibrasi.
Dari data pengukuran absorbansi logam tembaga untuk sampel batuan mineral,
diperoleh serapan (A) sebesar 0,0393.
Dengan mensubstitusikan nilai Y (Absorbansi) kepersamaan garis regresi
Hasil ini dikalikan dengan faktor pengencerannya yaitu 500 kali sehingga diperoleh
konsentrasi logam tembaga (Cu) yang sebenarnya 1065,55 mg/L.
4.1.4.4. Perhitungan Kadar Logam Tembaga (Cu) dalam mg/Kg
Maka diperoleh kadar logam tembaga (Cu) pada sampel batuan mineral dari Dusun
Jambu Dolok Kabupaten Toba Samosir adalah 21.311 mg/Kg.
4.1.5. Logam Besi
Tabel 4.7. Kondisi alat SSA Merek Hitachi Z-2000 pada pengukuran konsentrasi logam Besi (Fe)
No Parameter Logam Besi
1 Panjang gelombang (nm) 248,3
2 Tipe nyala Udara-C2H2
3 Kecepatan aliran gas pembakar (L/min) 1,8
4 Kecepatan aliran udara (L/min) 15,0
5 Lebar celah (nm) 0,2
6 Ketinggian tungku (mm) 7,5
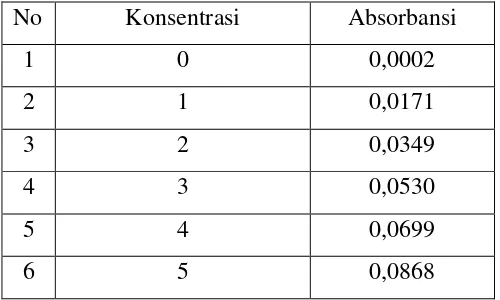
Tabel 4.8. Data Absorbansi Larutan Standar Besi (Fe)
No Konsentrasi Absorbansi
1 0 0,0002
2 1 0,0171
3 2 0,0349
4 3 0,0530
5 4 0,0699
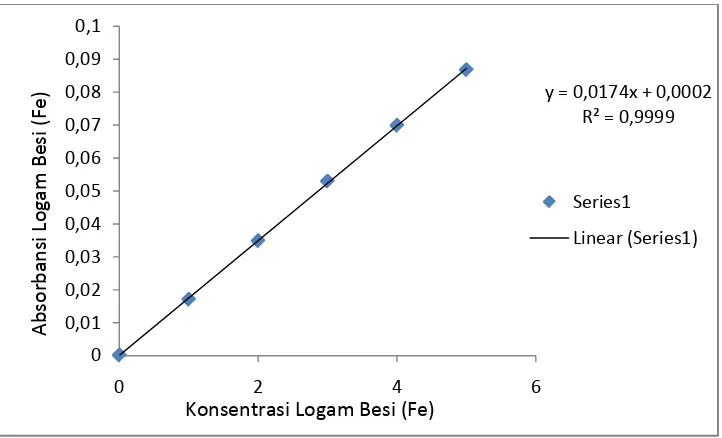
Gambar 4.3. Kurva Kalibrasi Larutan Standar Besi (Fe)
4.1.6. Pengolahan Data Logam Besi (Fe)
4.1.6.1. Penurunan Persamaan Garis Regresi dengan Metode Least Square
Hasil pengukuran absorbansi larutan seri standar logam Besi (Fe) pada tabel 4.2.
diplotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi berupa
garis linier. Persamaan garis regresi untuk kurva kalibrasi ini dapat
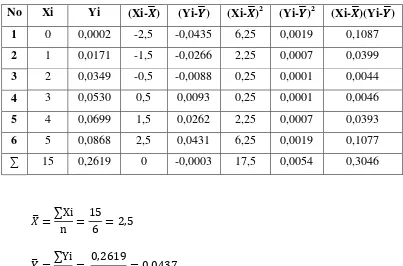
Tabel 4.9. Penurunan Persamaan Garis Regresi untuk Penentuan Konsentrasi Logam Besi (Fe) Berdasarkan Pengukuran Absorbansi Larutan Standar Besi (Fe)
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan
garis:
y = ax + b
dimana:
a = slope
b = intersept
selanjutnya harga slope dapat ditentukan dengan menggunakan metode least square
sebagai berikut:
� =∑(Xi−X�)(Yi−Y�)
b = y- ax
Dengan mensubstitusikan harga-harga yang tercantum pada tabel 4.9. pada
persamaaan ini maka diperoleh:
� =0,3046
17,5 = 0,0174
b = 0,0437 – (0,0174)(2,5)
= 0,0437 – 0,0435
= 0,0002
Maka persamaan garis yang diperoleh adalah:
y = 0,0174 x + 0,0002
4.1.6.2. Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai
berikut:
�= ∑(Xi−X�)(Yi−Y�) [∑(Xi−X�)2∑(Yi−Y�)2 ]1/2
Koefisien korelasi untuk logam Besi (Fe) adalah:
�= 0,3046
[(17,5)(0,0053)]1/2
4.1.6.3. Penentuan Kadar Logam Besi (Fe) Dari Sampel Batuan Mineral Dari Dusun Jambu Dolok Kabupaten Toba Samosir
Kadar besi (Fe) dapat ditentukan dengan menggunakan metode kurva kalibrasi
dengan mensubstitusikan nilai Y (absorbansi) yang diperoleh dari hasil
pengukuran terhadap garis regresi dari kurva kalibrasi.
Dari data pengukuran absorbansi logam besi untuk sampel batuan mineral,
diperoleh serapan (A) sebesar 0,0263.
Dengan mensubstitusikan nilai Y (Absorbansi) ke persamaan garis regresi
y = 0,0174 x + 0,0002
Hasil ini dikalikan dengan faktor pengencerannya yaitu 10.000 kali sehingga
diperoleh konsentrasi logam besi (Fe) yang sebenarnya 15.000 mg/L.
4.1.6.4. Perhitungan Kadar Logam Besi (Fe) dalam mg/Kg
Maka diperoleh kadar logam besi (Fe) pada sampel batuan mineral dari Dusun
Jambu Dolok Kabupaten Toba Samosir adalah 150.000 mg/Kg.
4.2. Pembahasan
Perak, tembaga dan besi merupakan logam-logam yang mempunyai nilai komoditi
yang tinggi. Perak, tembaga dan besi dapat ditemukan pada lapisan litosfer
bumi misalnya pada tanah dan bebatuan. Dusun jambu Dolok merupakan
daerah yang memiliki potensi bebatuan yang mengandung mineral yang
berharga.
Penentuan kadar logam Perak (Ag), Tembaga (Cu) dan besi (Fe) di dalam
batuan mineral yang terdapat di Dusun Jambu Dolok dilakukan dengan
mendestruksi sampel denga metode destruksi basah. Penentuan logam perak
(Ag) dan tembaga (Cu) dengan menggunakan HNO3 dan penentuan logam
besi (Fe) dengan menggunakan HNO3 dan HCl. Kemudian ditentukan nilai
absorbansi dan konsentrasi dari sampel menggunakan alat Spektrofotometer
Serapan Atom pada panjang gelombang untuk perak (Ag) = 328,1 nm;
tembaga (Cu) = 324,7 nm dan besi (Fe) = 248,3 nm.
Kurva standar larutan seri standar logam perak (Ag), tembaga (Cu) dan besi
(Fe) dibuat dengan memvariasikan konsentrasi larutan seri standar dengan
menggunakan Metode Least Square sehingga diperoleh persamaan garis
linear untuk logam perak (Ag) Y = 0,0264X + 0,0001; tembaga (Cu) Y =
0,0183X + 0,0003 dan besi (Fe) Y = 0,0174 + 0,0002.
Dalam penelitian ini diperoleh koefisien korelasi untuk logam perak (Ag) =
0,9994; tembaga (Cu) = 0,9993 dan besi (Fe) = 0,9999. Hal ini
menunjukkan adanya hubungan atau korelasi positif antara konsentrasi
dengan absorbansi. Pada penelitian analitik, grafik kurva standar yang baik
Dari hasil penelitian yang dilakukan diperoleh kadar logam perak (Ag),
tembaga (Cu) dan besi (Fe) masing – masing adalah 2,1590 mg/Kg; 21.311
mg/Kg dan 150.000 mg/Kg.
Adanya logam perak (Ag), tembaga (Cu) dan besi (Fe) di dalam batuan
terbentuk dengan adanya beberapa proses. Batuan terbentuk dari dua
mineral atau lebih yang terbentuk di bawah permukaan bumi (intrusive)
yang berasal dari magma yang mendingin atau membeku dan terbentuk di
atas permukaan bumi (ekstrusive) akibat proses pelapukan dan erosi
sehingga menyebabkan presipitasi mineral bijih. Proses pembentukan bijih
logam secara umum dapat di bagi menjadi empat kelompok, yaitu proses
magmatik, proses hidrotermal, proses metamorfik dan proses permukaan.
Mineral-mineral bijih seperti magnetit, limenit, kromit terbentuk pada fase
awal diferensiasi magma. Semua mineral bijih yang terbentuk pada fase ini disebut
sebagai endapan magmatik. Sistem hidrotermal dapat didefinisikan sebagai
sirkulasi fluida panas (50° sampai >500°C), secara lateral dan vertikal pada
temperatur dan tekanan yang bervarisasi, di bawah permukaan bumi. Sistem
ini mengandung dua komponen utama, yaitu sumber panas dan fase fluida.
Sirkulasi fluida hidrotermal menyebabkan himpunan mineral pada batuan
dinding menjadi tidak stabil dan cenderung menyesuasikan kesetimbangan
baru dengan membentuk himpunan mineral yang sesuasi dengan kondisi
yang baru, yang dikenal sebagai alterasi (ubahan) hidrotermal. Endapan
bijih hidrotermal terbentuk karena sirkulasi
fluida hidrotermal yang melindi (leaching), mentransport, dan mengendapkan
mineral-mineral baru sebagai respon terhadap perubahan kondisi fisik
maupun kimiawi. Interaksi antara fluida hidrotermal dengan batuan yang
dilewatinya (batuan dinding) akan menyebabkan terubahnya
mineral-mineral primer menjadi mineral-mineral ubahan. Semua mineral-mineral bijih yang
terbentuk sebagai mineral ubahan pada fase ini disebut sebagai endapan
Suatu tubuh batuan yang diterobos magma umumnya akan
mengalami rekristalisasi, alterasi, mineralisasi, penggantian (replacement),
pada bagian kontaknya. Perubahan ini disebabkan oleh adanya panas dan
fluida yang berasal dari aktifitas magma tersebut. Selama berlangsung
pengangkatan dan erosi, suatu endapan bijih terekspos di dekat permukaan,
kemudian mengalami proses pelapukan, pelindian (leaching), maupun
oksidasi pada mineral-mineral bijih. Proses tersebut menyebabkan banyak
unsur logam (Cu2+, Pb2+, Zn2+ dll.) akan terlarut (umumnya sebagai
senyawa sulfat) dalam air yang bergerak ke dalam air tanah atau bahkan
sampai ke kedalaman dimana proses oksidasi tidak berlangsung.
Daerah dimana terjadi proses oksidasi disebut sebagai zona oksidasi.
Sebagian larutan yang mengandung logam-logam yang terlarut bergerak
terus hingga di bawah muka air tanah, kemudian logam-logam tersebut
mengendap kembali membentuk sulfida sekunder. Zona ini dikenal sebagai
zona pengkayaan supergen. Di bawah zona pengkayaan supergen terdapat
daerah dimana mineralisasi primer tidak terpengaruh oleh proses oksidasi
maupun pelindian, yang disebut sebagai zona hipogen. Logam yang paling
banyak terbentuk karena proses ini adalah tembaga (Cu) (Hartosuwarno,
2011)
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Dari hasil penelitian yang telah dilakukan diperoleh kesimpulan sebagai
berikut:
Kadar Ag, Cu dan Fe yang terdapat di dalam batuan mineral di Dusun jambu Dolok
Kabupaten Toba Samosir masing-masing adalah 2,1590 mg/Kg, 21.311
mg/Kg dan 150.000 mg/Kg.
2. Dari hasil analisis Ag dan Fe dapat disimpulkan bahwa batuan mineral yang
dijadikan sebagai sampel dalam penelitian ini tidak potensial untuk
dijadikan sumber Ag dan Fe.
5.2. Saran
1. Untuk penelitian selanjutnya disarankan untuk melakukan analisis terhadap
kandungan logam-logam lain yang bernilai ekonomis.
DAFTAR PUSTAKA
Clark, D.V., 1979. Approach to Atomic Absorption Spectroscopy. Sidney-Australia: Anal. Chem Consultants Pty, Ltd.
Harris, D., 1982. Quantitative Chemical Analysis. USA: W. H. Freeman and Company.
Hartosuwarno, S., 2011. Endapan Mineral. Yogyakarta: Fakultas Teknik Mineral Universitas Pembangunan Nasional “Veteran”.o
Keenan, C.W., 1980. General College Chemistry. Sixth Edition. Manhattan: Harper & Row, Publisher, Inc.
Khopkar, S.M., 1984. Konsep Dasar Kimia Analitik. Bombay: Indian Institute of Technology.
Kolthoff, M., 1952. Textbook of Quantitative Inorganic Analysis. Third Edition. New York: The MacMillan Company.
Lewis, G.F., 1985. Analytical Chemistry an Introduction. Second Edition. London: Macmillan publisher Ltd.
Lindgren, W., 1933. Mineral Deposits. Fourth Edition. London: McGraw-Hill book Company, Inc.
Mahan, B., 1966. College Chemistry. USA: Addison-Wesley Series in Chemistry.
Markham, E., 1955. General Chemistry. Boston: Houghton Mifflin Company.
PerkinElmer, 1996. Analitycal Methods for Atomic Absorption Spectroscopy. United States: PerkinElmer, Inc.
Scarlett, A., 1956. College Chemistry. New York: Henry Holt and Company.
Smith, A., 2001. Pustaka Sains Material. London: Usborne Publishing Ltd.
Sommer, L., 1989. Analytical Absorption Spectrophotometry In the Visible And Ultraviolet. Amsterdam: Elsevier.
Tennisen, A., 1974. Nature of Earth Materials. Second Edition. USA: Prentice Hall Inc.
Underwood, A., 1980. Analisa Kimia Kuantitatif. Edisi Keempat. Jakarta: Penerbit Erlangga.
Vogel., 1991. Buku Teks Kimia Analisis Kuantitatif Anorganik. Jakarta: Penerbit Buku Kedokteran EGC.