STUDI KEMAMPUAN PENYERAPAN
UNSUR HARA (N DAN P) OLEH
Gracillaria
sp.
DALAM SKALA LABORATORIUM
DIAN ARY KURNIAWAN
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa Skripsi yang berjudul :
STUDI KEMAMPUAN PENYERAPAN UNSUR HARA
(N DAN P ) OLEH
Gracillaria
sp. DALAM
SKALA LABORATORIUM
Adalah benar merupakan hasil karya sendiri dan belum diajukan dalam bentuk
apapun kepada perguruan tinggi manapun. Semua sumber data dan informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar
Pustaka di bagian akhir Skripsi ini
Bogor, Januari 2006
Dian Ary Kurniawan. C24101020. Studi Kemampuan Penyerapan Unsur Hara (N dan P) oleh Gracillaria sp. dalam Skala Laboratorium. Dibawah bimbingan Ario Damar, Sutrisno Sukimin dan Wage Komarawidjaja.
RINGKASAN
Untuk mengurangi kandungan unsur hara dilakukan dengan cara biofiltrasi (penyerapan unsur hara oleh organisme) yaitu dengan menggunakan rumput laut untuk menyerap nutrien (nitrogen dan fosfor) tersebut. Untuk mengkaji keefektifan penyerapan nitrogen dan fosfor oleh Gracillaria sp. pada selang waktu tertentu, dan pertumbuhan Gracillaria sp. pada selang waktu tertentu.
Dalam penelitian untuk mengetahui laju penyerapan Gracillaria sp. dic obakan tiga konsentrasi nutrien, yaitu perlakuan A(N 100 ppm, P 2 ppm), perlakuan B(N 13,09 ppm, P 1 ppm), dan perlakuan C(N 10 ppm, P 0,528 ppm).
Gracillaria sp. dimasukkan pada masing-masing akuarium pada hari keenam sesudah nutrien dimasukkan dan diharapkan dapat mengurangi kandungan nutrien yang tersedia dalam air dan menggunakan nutrien tersebut untuk pertumbuhan.
STUDI KEMAMPUAN PENYERAPAN
UNSUR HARA (N DAN P) OLEH
Gracillaria
sp.
DALAM SKALA LABORATORIUM
DIAN ARY KURNI AWAN
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Manajemen Sumberdaya Perairan
DEPARTEMEN MANAJEMEN SUMBERDAYA PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul : Studi Kemampuan Penyerapan Unsur Hara (N dan P) oleh
Gracillaria sp. dalam Skala Laboratorium
Nama : Dian Ary Kurniawan
NIM : C24101020
Disetujui
Pembimbing I Pembimbing II
Dr. Ir. Ario Damar. M. Si. Dr.Ir.Sutrisno Sukimin
NIP. 131878933 NIP. 130674522
Pembimbing III
Drh. Wage Komarawidjaja, M.Sc. NIP. 680000427
Mengetahui,
Dekan Fakultas Perikanan dan Ilmu Kelautan
Dr. Ir. Kadarwan Soewardi. NIP. 130805031
PRAKATA
Puji syukur kehadirat Allah SWT atas rahmat, taufik, dan hidayah-Nya sehingga penulis mampu menyelesaikan tugas akhir ini dengan baik.
Tugas akhir ini berjudul “Studi Kemampuan Penyerapan Unsur Hara (N dan P) oleh Gracillaria sp. dalam Skala Laboratorium” yang disusun
sebagai salah satu syarat dalam memperoleh Sarjana Perikanan pada Departemen Manajemen Sumberdaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut
Pertanian Bogor. Penelitian ini berlangsung selama dua bulan yaitu pada bulan Juli-Agustus 2005 di Laboratorium Pollutant Control BIOTROP, Bogor. Dalam penelitian ini penulis mengambil bagian dari penelitian Pusat Pengkajian dan Penerapan Teknologi Lingkungan (P3TL)-BPPT.
Pada kesempatan ini, penulis mengucapkan terima kasih kepada :
1. Bapak, ibu serta adik-adikku, serta om Agus dan Bulek tyo yang telah memberikan bimbingan serta dorangannya selama ini.
2. Bapak Sigit Damiri sekeluarga, Dhina Maretha atas kedewasaannya dalam memberikan nasehat serta motivasi dan sayangnya.
3. Dr. Ir. Ario Damar. M. Si, Dr. Ir. Sutrisno Sukimin, dan Drh. Wage Komarawidjaja, M.Sc selaku dosen pembimbing atas arahan, bimbingan, nasehat dan dorongan semangat kepada penulis.
5. Pusat penelitian Biotrop atas pemberian izin pemakaian tempat serta fasilitas peralatan salama penelitian.
6. Pusat Pengkajian dan Penerapan Teknologi Lingkungan (P3TL) - BPPT yang memberikan fasilitas serta dana sehingga terlaksananya penelitian.
7. Gong-li serta kawan di dalamnya, Kaka, Kus -kus, Dede, Suw, Rekan-rekan
MSP 38 atas kekompakkannya. Tabis, Anton, Idham, Bram, Matsi Production, dan Cosmo atas pertimbangan-perimbangannya. Terimakasih semuannya.
Bogor, Januari 2006
DAFTAR ISI
3. Metode Pengambilan Contoh dan Parameter yang Dianalisis ... 16
D. Analisa Data ... 17
1. Laju Penurunan konsentrasi nutrien... 17
2. Percobaan dengan Metode RAL ... 18
3. Analisis biomassa Gracillaria sp... 20
4. Analisis pertumbuhan Gracillaria sp. ... 20
IV. HASIL DAN PEMBAHASAN A. Hasil Penelitian Pendahuluan ... 21
1. Amonia ... 22
2. Nitrit ... 25
3. Nitrat ... 29
4. Ortofosfat ... 31
C. Parameter Biologis ... 35
1. Berat basah dan laju pertumbuhan relatif ... 35
D. Parameter Fisika-Kimia Lingkungan ... 37
KESIMPULAN DAN SARAN... 39
DAFTAR PUSTAKA ... 40
DAFTAR TABEL
Tabel Halaman 1. Nilai baku mutu TSS berdasarkan KEPMEN LH No. 51 Tahun
2004. ... 8
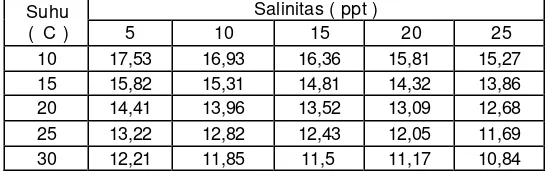
2. Kandungan N pada suhu dan salinitas yang berbeda ... 10
3. Klasifikasi kesuburan perairan berdasarkan kandungan PO4-P ... 11
4. Parameter Fisika-Kimia yang dianalisis ... 17
5. Sidik Ragam Rancangan Acak Lengkap ... 18
6. Pengamatan konsentrasi nutrien selama penelitian pendahuluan ... 21
7. Laju perubahan ammonia pada konsentrasi A ... 24
8. Laju perubahan ammonia pada konsentrasi B ... 24
9. Laju perubahan ammonia pada konsentrasi C ... 24
10. Laju penurunan ammonia pada tiap perlakuan selama pengamatan ... 25
11. Laju penurunan nitrit pada konsentrasi A ... 27
12. Laju penurunan nitrit pada konsentrasi B ... 27
13. Laju penurunan nitrit pada konsentrasi C ... 27
14. Laju penurunan nitrit pada tiap perlakuan ... 28
15. Laju penurunan nitrat pada konsentrasi A ... 30
16. Laju penurunan nitrat pada konsentrasi B ... 30
17. Laju penurunan nitrat pada konsentrasi C ... 30
18. Persentase pe nurunan nitrat pada tiap perlakuan ... 31
19. Laju penurunan ortofosfat pada konsentrasi A ... 33
20. Laju penurunan ortofosfat pada konsentrasi B ... 33
21. Laju penurunan ortofosfat pada konsentrasi C ... 33
23. Berat basah (g) dan RGR Gracillaria sp. ... 37
DAFTAR GAMBAR
Gambar Halaman
1. Skema perumusan masalah dalam penyerapan nutrien oleh
Gracillaria sp. ... 2
2. Gambar Gracillaria sp. yang digunakan pada penelitian ... 4
3. Bentuk-bentuk thallus alga ... 5
4. Gambar siklus reproduksi generatifGracillaria sp. ... 6
5. Rancangan penelitian ... 14
6. Diagram alir pembuatan larutan Urea dan TSP serta volume penambahan larutan Urea dan TSP untuk tiap perlakuan ... 15
7. Parameter-parameter kimia yang diamati pada masing-masing perla kuan dan kontrol... 16
8. Pengamatan konsentrasi nitrogen ... 21
9. Nilai ammonia air laut pada perlakuan konsentrasi A, B, C dan kontrol A, kontrol B, kontrol C dan kontrol D ... 22
10 Nilai nitrit air laut pada perlakuan konsentrasi A, B, C dan kontrol A, kontrol B, kontrol C dan kontrol D ... 26
11. Nilai nitrat air laut pada perlakuan konsentrasi A, B, C dan kontrol A, kontrol B, kontrol C dan kontrol D ... 29
12. Nilai ortofosfat air laut pada perlakuan konsentrasi A, B, C dan kontrol A, kontrol B, kontrol C dan kontrol D ... 32
13. Biomassa Gracillaria sp. pada perlakuan A, B, C ... 36
DAFTAR LAMPIRAN
Lampiran Halaman
1. Gambar alat-alat yang digunakan dalam pengambilan data ... 44
2. Gambar rancangan penelitian ... 45
3. Bahan-bahan yang digunakan dalam pengambilan data ... 46
4. Perhitungan pupuk ... 46
5. Data volume penambahan larutan Urea dan Larutan TSP ... 47
6. Data lengkap parameter fisika -kimia air selama penelitian ... 49
7. Data biomassa Gracillaria sp ... 51
8. Uji statistik kandungan unsur hara air ... 52
I. PENDAHULUAN
A. Latar Belakang
Sisa pakan dari kegiatan budidaya bandeng ataupun budidaya udang yang
terdekomposisi dalam jumlah tinggi pada suatu perairan dapat mengakibatkan meningkatnya kandungan unsur hara pada suatu perairan. Peningkatan nutrien (nitrogen dan fosfor) dapat mengakibatkan terjadinya eutrofikasi. Dampak dari
eutrofikasi yaitu bisa menimbulkan peningkatan kekeruhan dan bisa menimbulkan kondisi anoksik pada perairan tersebut (Mason,1993).
Peningkatan unsur hara akan mengakibatkan peningkatan pesat jumlah plankton di perairan. Plankton dalam jumlah besar akan menyebabkan terjadinya kompetisi dalam memanfaatkan unsur hara,sehingga kandungan unsur hara akan
berkurang. Dampak dari penurunan kandungan unsur hara akan menyebabkan terjadinya kematian plankton, yang menimbulkan proses dekomposisi. Apabila kandungan oksigen dalam perairan kurang mencukupi untuk proses dekomposisi maka akan terjadi proses dekomposisi anaerob yang menghasilkan gas racun yang
menyebabkan perairan menjadi toksik, akan menyebabkan terjadinya kematian ikan dan biota lainnya. Plankton yang mati akan mengendap pada dasar perairan sehingga kandungan bahan organik pada sedimen akan meningkat, sehingga
mengakibatkan penurunan pH pada sedimen. Tingkat asam yang rendah pada sedimen akan membahayakan biota air yang dibudidayakan pada perairan tersebut.
Untuk mencegah terjadinya proses eutrofikasi maka diperlukan suatu cara untuk menanggulanginya. Upaya -upaya yang dilakukan antara lain dengan
menggunkan kincir untuk meningkatan oksigen pada proses budidaya, cara yang lain yaitu dengan menggunakan tanaman air untuk menyerap kandungan unsur
hara dalam perairan.
Gracillaria sp. merupakan salah satu jenis dari kelas ganggang merah yang bentuk luarnya tidak mempunyai perbedaan akar dan batang serta memiliki
proses difusi dengan bantuan arus (Soegiarto et al. 1979). Unsur fosfor dan nitrogen pada perairan diperlukan Gracillaria sp. untuk melakukan pertumbuhannya.
.
B. Pendekatan Masalah
Sisa pakan ikan dan udang atau pun hasil dekomposisi bahan organik pada
suatu perairan menyebabkan kandungan nutrien dalam badan perairan menjadi tinggi dan dapat menimbulkan terjadi eutrofikasi. Salah satu upaya mengurangi
kandungan nutrien tersebut adalah dengan memanfaatkan tanaman air (makrofit) yang berfungsi sebagai biofilter, yaitu dengan menggunakan Gracillaria sp. untuk menye rap nutrien pada perairan tersebut.
Gracillaria sp. mempunyai kemampuan untuk mengurangi kandungan nutrien pada perairan dan menggunakan nutrien tersebut untuk pertumbuhan.
Gracillaria sp. mempunyai jaringan klorofil sehingga mampu untuk melakukan proses fotosintesis, sumber nutrien yang digunakan Gracilla ria sp. Untuk berfotosintesis berasal dari air dalam hal ini N dan P. Oleh karena itu digunakan
Gracillaria sp. Untuk menyerapa nutrient pada perairan tersebut.
Untuk mengetahui kemampuan Gracillaria sp. dalam menyerap nutrien diperlukan uji/pengamatan da lam skala laboratorium. Proses perumusan masalah
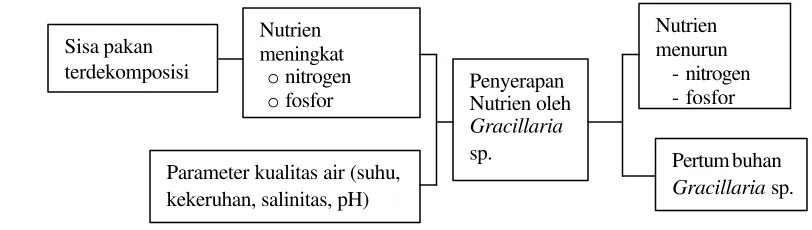
digambarkan pada diagram alir pada Gambar 1.
Gambar 1. Skema perumusan masalah dalam penyerapan nutrien oleh Gracillaria
sp.
Nutrien meningkat
onitrogen ofosfor
Parameter kualitas air (suhu, kekeruhan, salinitas, pH)
C. Tujuan
II. TINJAUAN PUSTAKA
A. Aspek Biologi
Rumput laut adalah tana man yang termasuk dalam suatu kelompok yang
dikenal dengan alga dan kelompok tanaman ini tidak dapat dibagi menjadi batang, akar dan daun (Duddington, 1971). Tumbuhan ini memiliki bentuk yang hampir sama secara keseluruhan, bentuk-bentuk yang mirip itu dikenal dengan istilah
thallus (Aslan, 1991). Untuk memberikan contoh bentuk rumput laut, pada Gambar 2 di bawah ini disajikan gambar Gracillaria sp.
Gambar 2. Gracillaria sp. yang digunakan pada penelitian
Menurut Soegiarto et al. (1979), bentuk thallus bermacam-macam. Ada yang berbentuk bulat seperti tabung, pipih, gepeng, bulat seperti kantung, rambut
dan lain sebagainya. Thallus ini ada yang tersusun oleh hanya satu sel dan banyak sel (uniseluler dan multi seluler). Percabangan thallus ada yang dichotomus (bercabang dua terus-menerus), pectinate (berderet searah pada satu sisi thallus utama), pinnate (bercabang dua -dua sepanjang thallus utama secara
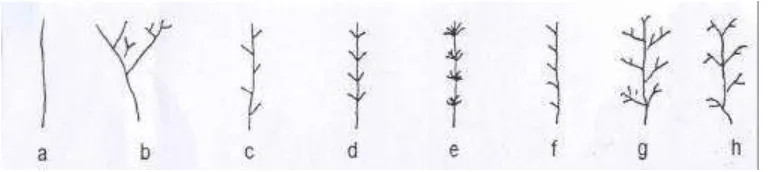
Gambar 3. Bentuk-Bentuk Thallus Alga ( Soegiarto et al. 1979) Keterangan :
a.Tidak bercabang b. Dichotomus c. Pinnate alternate d. Pinnate e. Vertillicate f. Pectinate g. Monopoidal h. sympoidal
Penampakan luar rumput laut terdiri dari berbagai warna yaitu merah, hijau, ataupun coklat kemerahan. Perbedaan warna yang diberikan dipengaruhi oleh kandungan pigmen yang ada. Keanekaragaman pigmen pada rumput laut menjadi ciri yang mencolok, meskipun hampir semua rumput laut mengandung klorofil (Soegiarto et al.1979).
Pigmen yang terkandung pada thallus rumput laut dapat digunakan untuk membedakan berbagai kelas. Perbedaan warna thallus menimbulkan adanya ciri pada alga yang berbeda seperti alga hijau, alga coklat, alga merah (Aslan, 1991). Akan tetapi menurut Soegiato et al. (1979) sebenarnya sangat sulit untuk menentukan salah satu kelas hanya hanya berdasarkan warna thallus, karena alga
kadang-kadang berwarna hijau kekuning-kuningan, coklat kehitam-hitaman atau kuning kecoklatan.
Rumput laut mampu mengurangi kandungan nutrien pada perairan sebesar 66% dari jumlah total N yang ada pada perairan tersebut. Rumput laut juga
mampu mengurangi total fosfor sebesar 56% dari total fosfor pada perairan (Jones et al., 2002). Berdasarkan Kinne et al. (2001) dijelaskan bahwa rumput laut mampu menyerap nitrogen dalam ammonium sebesar 10-14%.
Rumput laut memamfaatkan nutrien untuk pertumbuhan. Berdasarkan Marinho et al., 2002) pertumbuhan Gracillaria sp. pada tambak udang berkisar antara 1.8% -8.8% perhari.
Reproduksi merupakan suatu proses dimana organisme hidup
berkembangbiak, memperbanyak dan meningkatkan jumlah individunya.
vegetatif, generatif. Reproduksi secara generatif terjadi dengan adanya peleburan
antara gamet-gamet yang berbeda yaitu antara spermatozoid yang dihasilkan antheredia dengan sel telur atau ovum yang dihasilkan oleh oogonium.
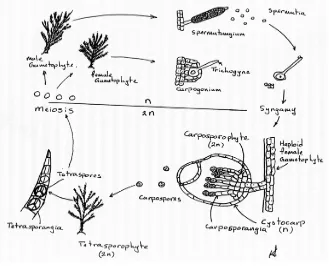
Gambar 4. Siklus Reproduksi Generatif Gracillaria sp.(Raven et al, 1992)
B. Parameter Fisika 1. Cahaya
Fotosintesis bagi tumbuhan, baik tumbuhan darat maupun laut seperti alga, bergantung pada adanya cahaya matahari. Laju fotosintesis tinggi apabila intensitas cahaya tinggi dan sebaliknya (Nybakken, 1992).
Cahaya sangat berpengaruh terhadap fotosintesis pada alga. Laju fotosintesis akan tinggi apabila intensitas cahaya tinggi dan sebaliknya. Penetrasi cahaya dalam air sangat dipengaruhi oleh intensitas dan sudut datang cahaya pada permukan air, kondisi permukaan air, dan bahan-bahan terlarut dan tersuspensi di
2. Suhu
Pengaruh suhu dalam lingkungan perairan saling berinteraksi dengan faktor lingkungan lainnya, demikian pula pengaruhnya dalam membatasi penyebaran suatu organisme (Krebs, 1972). Temperatur juga merupakan faktor
sekunder bagi kehidupan rumput laut dan fluktuasi yang tinggi akan dapat terhindar dengan adanya water mixing (Mubarak, 1981).
Rumput laut akan tumbuh subur pada daerah yang suhunya sesuai dengan suhu di laut. Pada daerah tropis, rumput laut dapat tumbuh pada kisaran suhu 20–
30 ºC, dan untuk jenis Gracillaria sp. tumbuh optimal pada suhu 20–28 ºC (Luning, 1990).
3. Kekeruhan
Kekeruhan menggambarkan sifat optik air yang ditentukan berdasarkan banyaknya cahaya yang diserap dan dipancarkan oleh bahan-bahan yang terdapat dalam air. Kekeruhan disebabkan bahan organik dan bahan anorganik baik
tersuspensi maupun terlarut seperti lumpur, pasir halus, bahan anorganik dan organik seperti plankton dan mikroorganisme lainnya (APHA, 1976; Davis dan Cornwell, 1991). Kekeruhan merupakan faktor pembatas bagi proses fotosintesis dan produksi primer perairan karena mempengaruhi penetrasi cahaya matahari
(Boyd, 1988).
4. Substrat
Menurut Dawson (1956), pantai berkarang merupakan tempat hidup yang
baik bagi sejumlah besar spesies rumput laut dan hanya sedikit yang hidup di pantai berpasir. Hal ini juga didukung oleh pernyataan Nontji (1987) yang mengatakan bahwa sedikitnya alga di perairan yang dasarnya berlumpur atau
berpasir karena sangat terbatasnya benda-benda keras yang cukup kokoh untuk tempatnya melekat.
5. Gerakan Air
Arus dan pergerakan air mempunyai pengaruh yang besar terhadap aerasi, transportasi nutrien, dan pengadukan air yang besar pengaruhnya terhadap keberadaan oksigen terlarut (Trono dan Fortes, 1988). Peranan yang lain yaitu
untuk menghindarkan akumulasi silt dan epifit yang melekat pada thallus yang dapat menghalangi pertumbuhan rumput laut. Semakin kuat arusnya,
pertumbuhan rumput laut akan semakin cepat besar karena difusi nutrien ke dalam sel tanaman semakin banyak sehingga metabolisme dipercepat (Soegiarto et al. 1979).
6. Padatan Tersuspensi Total
Padatan Tersuspensi Total (Total Suspended Solid/TSS) adalah bahan-bahan tersuspensi (diameter > 1 ì m) yang tertahan pada saringan millipore dengan diameter pori 0.45 ì m. TSS terdiri dari lumpur dan pasir halus serta jasad-jasad renik. Penyebab nilai TSS adalah kikisan tanah atau erosi tanah yang
terbawa ke badan air.
Berikut adalah nilai padatan tersuspensi total perairan berdasarkan baku mutu yang dikeluarkan oleh Kementrian Lingkungan Hidup. Nilai padatan
tersuspensi total ini mencakup untuk berbagai habitat.
Tabel 1. Nilai baku mutu TSS berdasarkan KEPMEN LH No. 51 Tahun 2004.
Habitat Nilai TSS (Total Suspended Solid)
Coral 20 mg/l
Mangrove 80 mg/l
Lamun 20 mg/l
C. Parameter Kimia 1. Salinitas
Salinitas adalah ukuran dari total garam dalam gram air laut. Salinitas menggambarkan padatan total di dalam air, setelah semua karbonat dikonversi
Salinitas laut dipengaruhi oleh berbagai faktor seperti sirkulasi air,
penguapan, curah hujan dan aliran sungai (Nontji, 1987). Masing-masing rumput laut dapat tumbuh dengan baik pada kisaran salinitas tertentu tergantung pada toleransi dan adaptasinya terhadap lingkungan (Trono dan Fortes, 1988).
Gracillaria sp. dapat tumbuh pada kisaran salinitas yang tinggi dan dapat tahan sampai 50‰.
2. Derajat keasaman
Derajat keasaman (pH) merupakan hasil pengukuran aktivitas ion hidrogen dalam perairan dan menunjukkan keseimbangan antara asam dan basa air. pH juga merupakan faktor lingkungan yang mengendalikan fitoplankton dalam proses
pengambilan nutrien, keseimbangan nutrien (karbondioksida, fosfat, dan nitrogen) sangat sensitif terhadap perubahan pH menurut Smith in Muntsji (1972).
Nilai pH dipengaruhi oleh beberapa faktor antara lain aktivitas biologi seperti fotosintesis dan respirasi organisme, suhu, dan keberadaan ion-ion dalam
perairan tersebut (Pescod, 1973). Menurut Smith in Muntsji (1972), pH air laut berkisar antara 7.9 - 8.3. Dengan meningkatnya pH akan berpengaruh terhadap kehidupan rumput laut. Kisaran toleransi pH dimana alga ditemukan adalah sebesar 6.8 - 9.6 (Luning, 1990).
3. Nutrien
Rumput laut sebagai tanaman berklorofil memerlukan nutrien sebagai
bahan baku fotosintesis. Dawes (1981) menyatakan bahwa unsur nitrogen dan fosfor diperlukan rumput laut bagi pertumbuhannya dan umumnya unsur fosfor diserap dalam bentuk ortofosfat sedangkan nitrogen diserap dalam bentuk nitrat, nitrit maupun a mmonium.
a. Nitrogen
Ammonia di perairan merupakan hasil pemecahan nitrogen organik
(protein dan urea) dan nitrogen anorganik yang terdapat dalam tanah dan air, berasal dari dekomposisi bahan organik (tumbuhan dan biota akuatik yang telah mati) yang dilakukan oleh mikroba dan jamur. Proses ini dikenal dengan istilah
ammonifikasi (Effendi, 2003), ditunjukkan dalam persamaan reaksi sebagai berikut:
CO(NH2) + H2O 2NH3 + CO2
4NH3 + 7O2 4NO2 + 6H2O Ammonifikasi 2NO2 + O2 2 NO3 Nitrifikasi
Nitrat (NO3) adalah bentuk nitrogen utama di perairan alami yang merupakan nutrien utama bagi pertumbuhan tanaman dan alga. Nitrat sangat
mudah larut dalam air dan bersifat stabil. Senyawa ini dihasilkan dari proses oksidasi sempurna senyawa nitrogen di perairan. Konsentrasi nitrat di perairan
terbentuk dalam proses nitrifikasi. Proses ini adalah proses oksidasi ammonia menjadi nitrit dan nitrat oleh bakteri ototrof yang berlangsung dalam kondisi
aerob.
Nitrit (NO2) biasanya ditemukan dalam jumlah yang sangat sedikit, kadarnya lebih kecil daripada nitrat, karena bersifat tidak stabil dengan keberadaa n oksigen (Novotny dan Olem, 1994). Nitrit merupakan bentuk peralihan antara ammonia dan nitrat (nitrifikasi), dan antara nitrat dan gas
nitrogen (denitrifikasi). Kadar nitrit diperairan alami sekitar 0.001 mg/l dan sebaiknya kadar nitrit tidak melebihi 0.05 mg/l karena dapat bersifat toksik bagi organisme perairan yang sangat sensitif (Moore, 1991).
b. Ortofosfat
Di perairan tidak ditemukan uns ur fosfor dalam bentuk bebas sebagai elemen tetapi dalam bentuk anorganik yang terlarut seperti ortofosfat (PO4-P) dan polifosfat. Keberadaan fosfor di perairan alami biasanya relatif kecil, kadarnya
lebih sedikit daripada nitrogen, karena sumber fosfor yang lebih sedikit dibandingkan dengan sumber nitrogen di perairan. Sumber alami fosfor adalah
dari pelapukan bahan mineral dan berasal dari dekomposisi bahan organik. Sedangkan bentuk fosfor yang dimanfaatkan secara langsung oleh tumbuhan
akuatik adalah ortofosfat.
Tabel 3. Klasifikasi Kesuburan Perairan Berdasarkan Kandungan PO4-P (Boyd, 1988)
Kisaran Nilai Satuan Tingkat Kesuburan
0,000 – 0,020 Ppm PO4-P Rendah
0,021 – 0,050 Ppm PO4-P Sedang
0,051 – 0,100 Ppm PO4-P Tinggi
> 0,201 Ppm PO4-P Sangat Tinggi
4. Oksigen Terlarut (DO)
Oksigen terlarut merupakan unsur penting yang sangat diperlukan dalam melakukan respirasi dan menguraikan zat organik oleh mikroorganisme (Harvey, 1992). Oksigen terlarut adalah besarnya kandungan oksigen yang terlarut da lam
air yang biasa dinyatakan dalam satuan mg/l. Kelarutan oksigen di perairan dipengaruhi oleh suhu, tekanan parsial gas-gas yang ada di udara maupun di air,
kadar garam dan unsur-unsur yang mudah teroksidasi di dalam perairan. Semakin meningkat suhu air, kadar garam, dan tekanan gas-gas terlarut maka semakin berkurang kelarutan oksigen dalam air (Wardoyo, 1981). Peningkatan suhu
sebesar 1 ºC akan meningkatkan konsumsi oksigen sekitar 10 % (Brown, 1987 in
III. METODE PENELITIAN
A. Lokasi dan Waktu Penelitian
Penelitian ini dilakukan dengan skala laboratorium dan dilaksanakan pada
bulan April 2005 sampai Juni 2005 di Laboratorium Pollutant Control Biotrop. Analisa fisika dan kimia dilakukan di Laboratorium tanah di Biotrop dan Laboratorium Lingkungan Dept. BDP, FPIK, IPB.
B. Bahan Uji Penelitian 1. Rumput Laut
Rumput laut yang digunakan dalam penelitian ini diperoleh dari hasil budidaya tambak di Brebes. Rumput laut dibawa ke Bogor dengan menggunakan sterofoam, dimana air laut dimasukkan ke dalam sterofoam sehingga rumput laut
akan tetap segar. Penutup sterofoam dibuka dengan tujuan supaya rumput laut tetap mendapat pasokan oksigen. Rumput laut ditampung dengan menggunakan bak penampungan yang mendapat aerasi dengan tujuan agar rumput laut tetap
terjaga dalam kondisi yang segar.
Pemilihan Gracillaria sp. uji dalam penelitian utama ini diupayakan seragam dan masih berumur muda. Hal ini dikarenakan menurut Widyanto dan Susilo (1997), kecepatan penyerapan mineral per satuan berat kering tumbuhan
lebih besar pada permulaan pertumbuhan dibandingkan bila tumbuhan itu sudah tua. Gracillaria sp .yang digunakan memiliki umur yang sama serta memiliki berat basah dan kondisi yang sama.
2. Air Laut
Air laut yang digunakan berasal dari toko akuarium ikan hias, dimana air laut tersebut mengalami proses pengendapan serta penyaringan terlebih dahulu. Proses penyaringan dilakukan dengan menggunakan planktonnet dengan tujuan
C. Metode penelitian 1. Penelitian Pendahuluan
Penelitian pendahuluan ini terbagi atas kegiatan :
a. Menentukan waktu dekomposisi optimal dari pupuk.
Penelitian pendahuluan ini bertujuan untuk mengetahui waktu pupuk
terdekomposisi menjadi ammonia, nitrit, nitrat, ortofosfat. Konsentrasi nutrien yang digunakan 13,09 mg/l N dan 0,2 PO4 dengan volume air laut 70 liter. Hasil
dari penelitian ini akan digunakan untuk menentukan waktu untuk memasukkan rumput laut setelah pemberian pupuk.
Berdasarkan data pendahuluan pada Tabel 6 dapat diketahui bahwa proses
dekomposisi pupuk urea dan TSP akan mencapai maksimal pada hari ke -6 setelah pupuk dimasukkan ke dalam air laut. Berdasarkan hasil tersebut maka pemberian rumput laut ke dalam akuarium dilakukan pada hari ke-6, karena penyerapan nutrien oleh rumput laut terjadi pada saat proses dekomposisi mencapai
maksimum.
2. Penelitian Utama
a. Persiapan alat dan bahan
Persiapan dimulai dengan menimbang rumput laut dengan bobot 0,5 kg pada masing-masing akuarium, sehingga untuk 6 akuarium dibutuhkan rumput laut dengan bobot 3 kg. Untuk medianya digunakan air laut dengan salinitas 18– 30‰ yang terlebih dahulu disaring dengan planktonnet untuk mengurangi jumlah
plankton. Air laut yang digunakan untuk masing-masing akuarium sebanya k 70 liter dan dengan tinggi 25 cm dari dasar akuarium sehingga rumput laut dengan berat 0,5 kg dapat terendam semua. Pada masing-masing akuarium diberikan
aerasi terlebih dahulu untuk meningkatkan kadar oksigen di dalam air. Untuk
b. Rancangan Penelitian
Dalam penelitian ini digunakan Gracillaria sp. untuk setiap akuarium. Masing-masing akuarium diberikan kadar nutrien dengan perbandingan tertentu. Nutrien yang digunakan yaitu larutan pupuk Urea dan pupuk TSP. Berikut ini
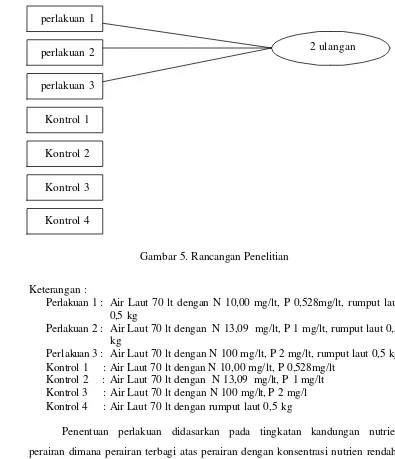
adalah rancangan percobaan pada penelitian ini :
Gambar 5. Rancangan Penelitian
Keterangan :
Perlakuan 1 : Air Laut 70 lt dengan N 10,00 mg/lt, P 0,528mg/lt, rumput laut 0,5 kg
Penentuan perlakuan didasarkan pada tingkatan kandungan nutrien perairan dimana perairan terbagi atas perairan dengan konsentrasi nutrien rendah, sedang, dan tinggi. Gracillaria sp. diadaptasikan terlebih dahulu dengan tingkatan nutrien tersebut, sehingga pada saat dilakukan penelitian Gracillaria sp. telah beradaptasi dengan kondisi lingkungan.
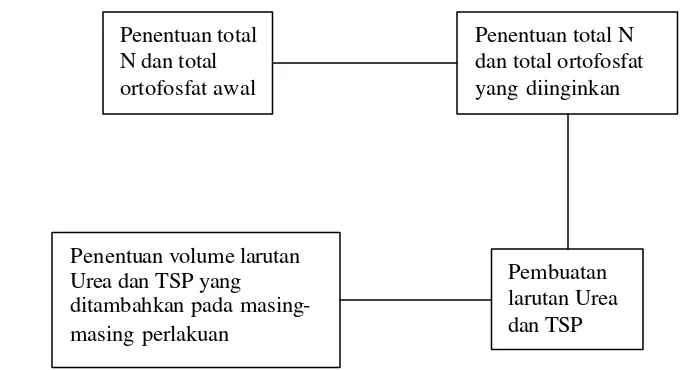
Untuk menentukan volume larutan Urea dan larutan TSP yang perlu
ditambahkan pada masing-masing perlakuan akan diuraikan pada diagram alir pada Gambar 5. Sedangkan untuk perhitungan lebih lanjut dijelaskan pada Lampiran 4.
Gambar 6. Diagram alir pembuatan larutan Urea dan TSP serta volume penambahan larutan Urea dan TSP untuk tiap perlakuan.
Jumlah nutrien yang ditambahkan kedalam media dihitung dengan mengukur kandungan nutrien awal pada air laut, misalnya kandungan total N awal air laut sebesar 3 ppm dan kandungan total P awal 0,05 ppm sehingga untuk
mendapatkan media dengan kandungan total N 13,09 dan total P 0,1 ppm maka penambahan nutrien dapat dihitung dengan cara :
(total N yang diinginkan – total N awal) x 70 liter = V1 x 10000 mg/lt larutan urea (total P yang diinginkan – total P awal) x 70 liter = V1 x 1000 mg/lt larutan TSP
Proses pembuatan larutan Urea dan larutan TSP lebih lanjut dijelaskan di Lampiran 4. Sedangkan untuk volume larutan Urea dan larutan TSP dapat dilihat pada Lampiran 5.
Penentuan total N dan total ortofosfat awal
Penentuan total N dan total ortofosfat yang diinginkan
Pembuatan larutan Urea dan TSP Penentuan volume larutan
Dengan perlakuan seperti di atas maka data kandungan nutrie n yang akan
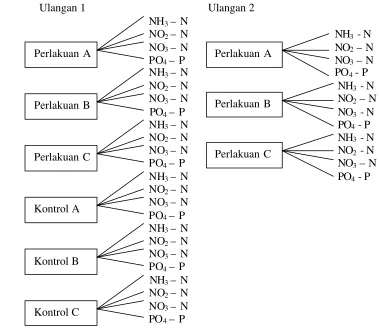
didapat dari tiap perlakuan dapt dilihat pada Gambar 6. Pada tiap perlakuan parameter yang diamati sama dengan di kontrol.
Ulangan 1 Ulangan 2
Gambar 7. Parameter-parameter kimia yang diamati pada masing-masing perlakuan dan kontrol.
3. Metode Pengambilan contoh dan Parameter yang Dianalisis
Pengambilan contoh air untuk pengukuran nitrat, nitrit, ammonia, ortofosfat dilakukan dengan cara mengambil air dalam akuarium, kemudian dimasukkan ke dalam wadah yang telah disediakan untuk analisis kualitas air.
Pengambilan contoh air dilakukan pada hari T1-T7, selang waktu antara T1-T2 adalah 3 hari. Pada T0 ditimbang berat awal dari rumput laut tiap akuarium dan pada T6 di ukur berat akhir tiap akuarium.
Metode peneraan kualitas air dilakukan secara in situ untuk parameter suhu, pH, salinitas, dan oksigen terlarut. Sedangkan untuk metode peneraan
kandungan unsur hara yang terdapat dalam air media, dilakukan pengukuran di
laboratorium terhadap contoh air yang meliputi kandungan nitrat, nitrit, ammonia, ortofosfat (APHA, 1989).
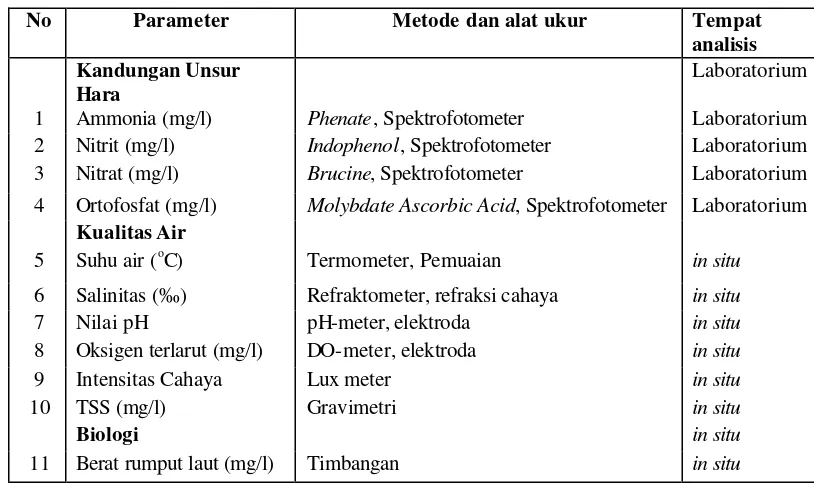
Tabel 4. Parameter fisika kimia yang dianalisis
No Parameter Metode dan alat ukur Tempat
analisis Kandungan Unsur
Hara
Laboratorium
1 Ammonia (mg/l) Phenate, Spektrofotometer Laboratorium
2 Nitrit (mg/l) Indophenol, Spektrofotometer Laboratorium
3 Nitrat (mg/l) Brucine, Spektrofotometer Laboratorium
4 Ortofosfat (mg/l) Molybdate Ascorbic Acid, Spektrofotometer Laboratorium
Kualitas Air
5 Suhu air (oC) Termometer, Pemuaian in situ
6 Salinitas (‰) Refraktometer, refraksi cahaya in situ
7 Nilai pH pH-meter, elektroda in situ
8 Oksigen terlarut (mg/l) DO-meter, elektroda in situ
9 Intensitas Cahaya Lux meter in situ
10 TSS (mg/l) Gravimetri in situ
Biologi in situ
11 Berat rumput laut (mg/l) Timbangan in situ
D. Analisis data
1. Laju Penurunan Konsentrasi Nutrien
KemampuanGracillaria sp. dalam menurunkan nutrien di dalam air laut dapat dilihat berdasarkan persentase tingkat perubahannya. Laju penurunan nutrien antar waktu pengambilan contoh diperoleh dengan rumus :
Konsentrasi nutrien T1 – konsentrasi nutrien T2
Laju Penurunan = T2 – T1
Keterangan = T1 = waktu awal
T2 = Tiga hari setelah waktu awal
Laju penurunan nutrien selama selang waktu penelitian diperoleh dengan rumus :
Konsentrasi nutrien tawal – konsentrasi nutrien takhir Laju Penurunan =
ijk
2. Percobaan dengan Metode Rancangan Petak Terpisah
Data yang diperoleh dari hasil pengamatan disajikan dalam bentuk tabel dan grafik. Analisis secara deskriptif digunakan untuk mendapatkan informasi mengenai pola penyerapan unsur hara dari air oleh Gracillaria sp. dan untuk melihat pertumbuhan pada Gracillaria sp., sedangkan untuk melihat pengaruh perbedaan konsentrasi nutrien terhadap penyerapan unsur hara digunakan
digunakan Rancangan Petak Terpisah (Split Plot in time) (Steel dan Torrie, 1989). Model Rancangan Petak Terpisah (Split Plot in time) sebagai berikut:
Keterangan :
ijk
Y = Nilai pengamatan dari kelompok ke -i dari suatu rancangan kelompok teracak, pada perlakuan petak utama ke-j dengan perlakuan anak petak ke-k.
Untuk melihat pengaruh perbedaan konsentrasi nutrien terhadap penyerapan unsur hara digunakan perlu dilakukan uji Ftabel pada taraf nyata
tertentu menggunakan Analisis Sidik Ragam dari Rancangan Petak Terpisah (Split Plot in time) (Tabel 2) dihitung berdasarkan Steel dan Torrie (1989) sebagai berikut :
Tabel 5. Tabel sidik ragam dari rancangan petak terpisah (Split Plot in times)
Untuk mengetahui apakah ada perbedaan dari masing-masing perlakuan,
perlu dilakukan uji F (tabel) pada taraf nyata tertentu. Hipotesis dari kaidah uji yang digunakan dalam uji ini adalah:
Hipotesis:
H0 = Tingkat perbedaan konsentrasi pupuk tidak memberi pengaruh terhadap kandungan nutrien.
H1 = Tingkat perbedaan konsentrasi pupuk memberi pengaruh terhadap kandungan nutrien.
Kaidah keputusan:
• Fhitung < Ftabel atau probabilitasnya (P) > 0,05 maka perbedaan konsentrasi pupuk tidak memberi pengaruh terhadap kandungan nutrien atau nila inya tidak berbeda nyata.
• Fhitung > Ftabel atau probabilitasnya (P) < 0,05 maka perbedaan konsentrasi pupuk memberi pengaruh terhadap kandungan nutrien atau nilainya tidak berbeda nyata.
• Fhitung > Ftabel atau probabilitasnya (P) <0,01 maka nilainya berbeda sangat nyata.
Jika dari TSR diperoleh Fhitung < Ftabel, maka sedikitnya ada satu pasang perlakuan ke -I yang mempunyai pengaruh terhadap penyerapan unsur hara yang mendapatkan perlakuan tingkat rasio ke -j, maka dilakukan uji lanjutan Beda
Nyata Terkecil (BNT). BNT mempunyai kriteria uji sebagai berikut:
3. Analisis Biomassa Gracillaria sp.
Pada pengukuran biomassa (berat basah), Gracillaria sp. terlebih dahulu ditaruh pada kertas koran selama ± 5 menit agar air yang terdapat pada
Gracillaria sp. dapat diserap. Pengukuran biomassa dari Gracillaria sp. dengan menggunakan timbangan. Pengamatan biomassa dilakukan pada saat pengambilan contoh.
4. Analisis Pertumbuhan Gracillaria s p.
Analisis parameter pertumbuhan Gracillaria sp. dihitung dengan menentukan besarnya laju pertumbuhan relatif (Relative Growth Rate, RGR) (Mitchell, 1974) :
% 100 ln
ln
× −
=
t Xo Xt
RGR
Xo = Berat basah awal
IV. HASIL DAN PEMBAHASAN
A. Hasil Penelitian Pendahuluan
Penelitian pendahuluan dilakukan untuk mendapatkan data yang digunakan dala m penelitian utama. Penelitian pendahuluan yang dilakukan pada penelitian ini bertujuan untuk mengetahui waktu nilai N dan P maksimum.
1. Konsentrasi nutrien selama penelitian pendahuluan
Kandungan unsur hara yang terdapat selama penelitian pendahuluan dapat terlihat dari tabel dan grafik di bawah ini.
Tabel 6. Pengamatan konsentrasi nutrien selama penelitian pendahuluan
Konsentrasi Nutrien (mg/l)
Gambar 8. Pengamatan konsentrasi nitrogen
Berdasarkan Gambar 8 dapat diketahui bahwa konsentrasi nitrit dan fosfat mencapai maksimal pada hari keenam setelah pupuk dimasukkan ke dalam air
penelitian ini digunakan untuk mengetahui waktu rumput laut dimasukkan ke
dalam akuarium. Pada penelitian utama rumput laut akan dimasukkan ke dalam akuarium enam hari setelah pupuk diberikan ke dalam air laut.
C. Hasil Penelitian Utama 1. Ammonia
Kadar ammonia merupakan salah satu parameter kimia yang penting, karena ammonia merupakan bentuk awal dari N-anorganik dalam air.
0
Gambar 9. Konsentrasi ammonia air laut pada perlakuan A, B, C dan kontrol A, kontrol B, kontrol C dan kontrol D
Keterangan : KA = Perlakuan pemberian pupuk 700 ml urea dan 103 ml TSP KB = Perlakuan pemberian pupuk 91 ml urea dan 33 ml TSP KC = Perlakuan pemberian pupuk 70 ml urea dan 0 ml TSP KD = Perlakuan tanpa pupuk dan rumput laut
Berdasarkan Gambar 9 dapat diketahui bahwa kadar ammonia pada
ammonia terjadi pada hari ke-3, hal ini diduga terjadi karena pr oses oksidasi
ammonia menjadi nitrit dan nitrat melalui peran bakteri-bakteri “chemoautotroph”. Reaksi oksidasi dapat dituliskan seperti berikut (Effendi, 2003).
2 NH3 + 3 O2 2 HNO2 + 2H2O + energi 2 HNO2 + O2 2 HNO3 + energi
Pada hari ke-12 dan ke-15 terjadi kenaikan kandungan ammonia pada tiap
perlakuan, hal ini diduga terjadi karena kandungan oksigen pada hari ke-12 dan ke-15 mengalami penurunan sehingga perubahan ammonia menjadi nitrit lebih sedikit jika dibandingkan dengan penambahan kandungan ammonia dari pupuk
urea. Selain itu pada hari ke -11 terdapat thallus Gracillaria sp. yang mati sehingga diduga menambah kandungan ammonia.
Berdasarkan uji statistik terhadap nilai ammonia antara tiap perlakuan menghasilkan kesimpulan bahwa pada selang kepercayaan 95% pemberian
konsentrasi pupuk yang berbeda memberi ammonia antara tiap perlakuan menunjukkan perbedaan yang nyata. Perbedaan nyata terjadi antara konsentrasi A terhadap konsentrasi B, dan konsentrasi B terhadap konsentrasi C. Sedangkan antara konsentrasi A dengan konsentrasi C tidak terjadi perbedaan yang nyata, hal
ini disebabkan karena pemberian dosis pupuk antara perlakuan B dan perlakuan C tidak berbeda jauh.
Berdasarkan uji statistik (uji BNT) hari terhadap kandungan ammonia dapat diketahui bahwa kandungan ammonia pada tiap hari memiliki perbedaan
Tabel 7. Laju perubahan ammonia pada konsentrasi A
Tabel 8. Laju perubahan ammonia pada konsentrasi B
Konsentrasi B
Tabel 9. Laju perubahan ammonia pada konsentrasi C
Konsentrasi C
Pengamatan awal akhir laju penurunan
1 0,6155 0,3205 0,0983 ppm/hari
2 0,3205 0,1725 0,0493 ppm/hari
3 0,1725 0,1425 0,0100 ppm/hari
4 0,1425 0,206 -0,0212 ppm/hari
5 0,206 0,2914 -0,0285 ppm/hari
Berdasarkan Tabel 8, Tabel 9, dan Tabel 10 tiap perlakuan laju penurunan
ammonia paling tinggi terjadi pada 3 hari pertama, hal ini terjadi karena kandungan oksigen yang tinggi dari proses aerasi sehingga mengakibatkan perubahan ammonia menjadi nitrit dan nitrat menjadi cepat.
Pada perlakuan A penurunan terjadi dengan laju 0,3215 ppm/hari pada
hari ke-0 sampai hari ke-3 dan pada hari ke-3 sampai hari ke-6 laju penurunan sebesar 0,1057 ppm/hari, kemudian pada hari ke-6 sampai hari ke-9 laju penurunannya 0,0248 ppm/hari. Terjadi peningkatan kandungan ammonia pada perlakuan A dengan laju peningkatan sebesar 0,0412 ppm/hari pada hari ke-9 sampai hari 12, dan sebesar 0,0368 ppm/hari pada hari 12 sampai hari
ke-15. Pada perlakuan B terjadi penurunan ammonia dari hari ke-1 sampai hari ke-9
sampai hari ke-6, dan pada hari ke-6 sampai hari ke-9 sebesar 0,0392 ppm/hari.
Perlakuan B terjadi peningkatan ammonia pada hari ke-9 sampai hari ke -15 sebesar 0,0250 ppm/hari pada hari ke -9 sampai hari ke-12 dan 0,0115 ppm/hari pada hari ke-12 sampai hari ke-15. Pada perlakuan C penurunan terjadi pada hari
ke-1 sampai hari ke-9 dan terjadi peningkatan pada hari ke-9 sampai hari ke-15.
Tabel 10. Laju penurunan ammonia pada tiap perlakuan selama pengamatan
Perlakuan
Berdasarkan tabel 10 laju penurunan terbesar terdapat pada perlakuan A sebesar 0.0301 ppm/hari. Hal ini diduga terjadi karena kandungan awal ammonia yang terdapat pada perlakuan A lebih besar jika dibandingkan dengan perlakuan yang lain, sehingga kandungan ammonia yang teroksidasi menjadi nitrit lebih
besar dibandingkan perlakuan B dan perlakuan C.
2. Nitrit
Berdasarkan Gambar 10 kandungan nitrit dari hari ke-0 sampai hari ke-15
memiliki kecenderungan menurun, hal ini diduga karena terjadi oksidasi nitrit menjadi nitrat yang mengakibatkan berkurangnya kandungan nitrit pada air laut. Kandungan nitrit pada perlakuan A ulangan 2 terjadi peningkatan kandungan
nitrit pada hari ke-9, hal ini diduga karena kandungan oksigen pada perlakuan tersebut mengalami penurunan sehingga oksidasi nitrit juga lebih sedikit.
Perlakuan B kandungan nitrit mengalami penurunan pada hari ke-0 sampai hari ke-3, sedangkan pada hari ke-3 sampai ke-9 te rjadi kenaikan kandungan
nitrit. Hal ini disebabkan karena penambahan jumlah nitrit dari ammonia lebih besar dari oksidasi nitrit menjadi nitrat. Pada hari ke-9 sampai ke-15 terjadi penurunan kandungan nitrit.
0
Gambar 10. Konsentrasi nitrit air laut pada perlakuan A, B, C dan kontrol A, kontrol B, kontrol C dan kontrol D
Keterangan : KA = Perlakuan pemberian pupuk 700 ml urea dan 103 ml TSP KB = Perlakuan pemberian pupuk 91 ml urea dan 33 ml TSP KC = Perlakuan pemberian pupuk 70 ml urea dan 0 ml TSP KD = Perlakuan tanpa pupuk dan rumput laut
Pada perlakuan A memiliki kandungan nitrit yang lebih besar jika dibandingkan dengan konsentrasi B dan C. Hal ini diduga terjadi karena perubahan ammonia menjadi nitrit pada perlakuan A lebih besar. Perlakuan B
kandungan nitrit pada pengamatan awal hampir sa ma dengan konsentrasi C. Berdasarkan uji statistik terhadap nilai nitrit antara tiap perlakuan menghasilkan kesimpulan bahwa pada selang kepercayaan 95% pemberian konsentrasi pupuk yang berbeda tidak memberi pengaruh terhadap nilai nitrit.
Pemberian pupuk yang berbeda tidak memberi pengaruh karena nitrit adalah bentuk transisi dari ammonia dan nitrat, perubahan ammonia menjadi nitrat terjadi secara cepat.
Berdasarkan uji statistik (Uji BNT) terhadap kandungan nitrit tiap
statistik (Uji BNT) hari terhadap kandungan nitrit, dapat diketahui bahwa hari
memberikan memberikan pengaruh yang nyata terhadap kandungan nitrit.
Tabel 11. Laju pe nurunan nitrit pada konsentrasi A
Konsentrasi A Pengamatan
awal akhir laju penurunan (ppm/hari)
1 0,789 0,657 0,0440
2 0,657 0,291 0,1220
3 0,291 0,411 -0,0400
4 0,411 0,140 0,0905
5 0,140 0,200 -0,0202
Tabel 12. Laju pe nurunan nitrit pada konsentrasi B
Konsentrasi B Pengamatan
awal akhir laju penurunan (ppm/hari)
1 0,6311 0,485 0,0487
2 0,485 0,5616 -0,0255
3 0,5616 0,5185 0,0144
4 0,5185 0,1085 0,1367
5 0,1085 0,1115 -0,0010
Tabel 13. Laju pe nurunan nitrit pada konsentrasi C
Konsentrasi C Pengamatan
awal akhir laju penurunan (ppm/hari)
1 0,603 0,499 0,0347
2 0,499 0,475 0,0080
3 0,475 0,4045 0,0235
4 0,4045 0,0965 0,1027
5 0,0965 0,1535 -0,0190
Berdasarkan Tabel 11, Tabel 12, dan Tabel 13 pada perlakuan A
penurunan nitrat terjadi pada hari ke-0 sampai hari ke-3 sebesar 0,0440 ppm/hari, hari ke-3 sampai hari ke-6 sebesar 0,1220 ppm/hari, dan pada hari ke -9 sampai hari ke -12 sebesar 0,0905 ppm/hari. Penurunan nitrat dapat terjadi karena
oksidasi nitrit lebih besar daripada oksidasi ammonia sehingga jumlah nitrit mengalami penurunan.
Perlakuan B penurunan terjadi pada hari ke -0 sampai hari ke -3 sebesar 0,0487 ppm/hari, hari ke-6 sampai hari ke -9 sebesar 0,0144 ppm/hari, dan pada
C penurunan nitrit terjadi pada hari ke -0 sampai hari ke-12 sebesar 0,0347
ppm/hari, 0,0080 ppm/hari, 0,0235 ppm/hari, dan 0,1027 ppm/hari.
Berdasarkan uji statistik (uji BNT) hari terhadap nilai kandungan nitrit. Dapat diketahui bahwa hari memberikan pengaruh yang nyata terhadap
kandungan nitrit dalam air laut.
Tabel 14. Laju penurunan nitrit pada tiap perlakuan selama pengamatan
Perlakuan
Konsentrasi A Konsentrasi B Konsentrasi C
laju penurunan
(ppm/hari)
0,0171 0,0133 0,0113
Berdasarkan Tabel 14 laju penurunan nitrit pada perlakuan A sebesar 0,0171 ppm/hari, perlakuan B 0,0133 ppm/hari, dan perlakuan C 0,0113 ppm/hari. Penurunan nitrit dapat terjadi karena adanya perubahan nitrit menjadi nitrat.
3. Nitrat
Nitrat (NO3) adalah bentuk nitrogen utama di perairan alami yang merupakan nutrien utama bagi pertumbuhan tanaman. Berdasarkan Gambar 11 kandungan nitrat awal yang paling tinggi terdapat pada konsentrasi A yaitu berada
pada kisaran 4,251-5,25mg/l, hal ini terjadi karena konsentrasi pupuk urea yang diberikan paling besar pada konsentrasi A yaitu sebesar 100 mg/l. Sedangkan kandungan nitrat awal pada konsentrasi B dan konsentrasi C berada pada kisaran yang relatif sama yaitu pada kisaran 1,703-3,257 mg/l, hal ini disebabkan karena
penurunan kandungan nitrat pada perlakuan sedangkan pada kontrol tidak terjadi
Gambar 11. Konsentrasi nitrat air laut pada perlakuan A, B, C dan kontrol A, kontrol B, kontrol C dan kontrol D
Keterangan : KA = Perlakuan pemberian pupuk 700 ml urea dan 103 ml TSP KB = Perlakuan pemberian pupuk 91 ml urea dan 33 ml TSP KC = Perlakuan pemberian pupuk 70 ml urea dan 0 ml TSP KD = Perlakuan tanpa pupuk dan rumput laut
Berdasarkan uji statistik terhadap nilai nitrat antara tiap perlakuan menghasilkan kesimpulan bahwa pada selang kepercayaan 95% pemberian konsentrasi pupuk yang berbeda memberi pengaruh terhadap nilai nitrat.
Berdasarkan uji statistik (uji BNT) terhadap kandungan nitrat antara tiap
perlakuan menunjukkan perbedaan yang nyata. Perbedaan nyata terjadi antara Konsentrasi A terhadap konsentrasi B, dan konsentrasi A terhadap konsentrasi C. Sedangkan antara konsentrasi B dengan konsentrasi C tidak terjadi perbedaan
yang nyata, hal ini disebabkan karena pemberian dosis pupuk antara perlakuan B dan perlakuan C tidak berbeda jauh.
dan hari ke-9 berbeda nyata dengan hari ke -12, serta hari ke-12 berbeda nyata
dengan hari ke-15.
Tabel 15. Laju pe nurunan nitrat pada konsentrasi A
Konsentrasi A
Tabel 16. Laju pe nurunan nitrat pada konsentrasi B
Konsentrasi B
Tabel 17. Laju pe nurunan nitrat pada konsentrasi C
Konsentrasi C
Berdasarkan Tabel 15, Tabel 16, Tabel 17 peningkatan kandungan nitrat pada perlakuan A terjadi pada hari ke-1 sampai hari ke-3 sebesar 0,9110 ppm/hari,
hari ke6 sampai hari ke9 sebesar 1,2042 ppm/hari dan hari ke 12 sampai hari ke
-15 sebesar 0,1707 ppm/hari, penambahan nitrat ini disebabkan berasal dari oksidasi ammonia dan nitrit hal ini dapat terjadi karena kandungan oksigen pada hari ke-1 sampai hari ke-3 mengalami peningkatan. Akan tetapi pada hari ke-3 sampai hari ke-6 terjadi penurunan konsentrasi nitrat sebesar 1,0280 ppm/hari dan
Pada konsentrasi B terjadi peningkatan konsentrasi nitrat dengan pola
yang sama dengan konsentrasi A yaitu pada hari ke-1 sampai hari ke-3 terjadi peningkatan sebesar 0,6125 ppm/hari, hari ke-6 sampai hari ke-9 sebesar 1,1705 ppm/hari dan hari ke-12 sampai ha ri ke-15 sebesar 0,6045 ppm/hari. Penurunan
konsentrasi nitrat terjadi pada hari ke-3 sampai hari ke-6 sebesar 0,5762 ppm/hari dan hari ke-9 sampai hari ke-12 sebesar 1,2522 ppm/hari.
Peningkatan kandungan nitrat pada konsentrasi terjadi pada hari ke -1 sampai hari ke -3 sebesar 0,0590 ppm/ hari, hari ke-6 sampai hari ke -9 sebesar
1,1942 ppm/hari dan hari ke-12 sampai hari ke-15 sebesar 0,5790 ppm/hari. Penurunan nitrat terjadi pada hari ke -3 sampai hari ke-6 sebesar 0,2508 ppm/hari dan hari ke-9 sampai hari ke-12 sebesar 1,2882 ppm/hari.
Tabel 18. Persentase pe nurunan nitrat pada tiap perlakuan
perlakuan
Konsentrasi A Konsentrasi B Konsentrasi C
laju
penurunan 2,7085 % 13,9674 % 15,3917 %
Berdasarkan Tabel 18 penurunan yang terukur pa da perlakuan A sebesar
2,7085 %, perlakuan B sebesar 13,9674 %, dan perlakuan C sebesar 18,3917 %. Persentase penurunan yang paling besar terjadi pada perlakuan C hal ini dapat terjadi karena kandungan unsur hara awal pada perlakuan C lebih kecil.
Berdasarkan Kinne et al. (2001) dijelaskan bahwa rumput laut mampu menyerap nitrogen dalam ammonium sebesar 10-14%. Maka penurunan nitrat yang terjadi pada penelitian ini memiliki persentase yang hamper sama.
4. Ortofosfat
0
Gambar 12. Konsentrasi ortofosfat air laut pada pe rlakuan A, B, C dan kontrol A, kontrol B, kontrol C dan kontrol D
Keterangan : KA = Perlakuan pemberian pupuk 700 ml urea dan 103 ml TSP KB = Perlakuan pemberian pupuk 91 ml urea dan 33 ml TSP KC = Perlakuan pemberian pupuk 70 ml urea dan 0 ml TSP KD = Perlakuan tanpa pupuk dan rumput laut
Berdasarkan Gambar 12 ortofosfat pada konsentrasi A memiliki konsentrasi yang lebih tinggi pada awal pengamatan jika dibandingkan dengan perlakuan B dan perlakuan C. Hal ini disebabkan pemberian pupuk TSP pada
perlakuan A lebih besar jika dibandingkan dengan perlakuan yang lainnya.
Penurunan konsentrasi ortofosfat terjadi dari hari ke-1 sampai hari ke-12
pada setiap perlakuan, karena jumlah penambahan ortofosfat dari dekomposisi pupuk TSP lebih kecil jika dibandingkan dengan penyerapan ortofosfat oleh
Gracillaria sp. Penambahan ortofosfat dari dekomposisi pupuk dapat ditunjukkan dari kontrol masing-masing perlakuan yang menunjukkan kenaikan jumlah kandungan ortofosfat pada tiap hari, terutama pada kontrol A yang mengalami kenaikkan pada hari ke-6 sampai hari ke-12 sebesar 0,167 ppm dan pada kontrol B sebesar 0,134 ppm pada hari ke -1 sampai hari ke-3. Penurunan yang paling
Pada hari ke-12 sampai hari ke-15 pada masing-masing perlakuan terjadi
kenaikkan kandungan ortofosfat yang disebabkan oleh dekomposisi dari sisa pupuk TSP yang belum terdekomposisi, sehingga meningkatkan kandungan ortofosfat didalam air.
Pada kontrol D konsentrasi ortofosfat tidak banyak terjadi perubahan, karena pada kontrol D tidak ditambahkan pupuk TSP dan Gracillaria sp. sehingga kandungan ortofosfat di dalam air tidak terjadi penambahan dan tidak terjadi penyerapan.
Berdasarkan uji statistik terhadap nilai ortofosfat antara tiap perlakuan menghasilkan kesimpulan bahwa pada selang kepercayaan 95% pemberian konsentrasi pupuk yang berbeda memberi pengaruh terhadap nilai ortofosfat.
Tabel 19. Laju penurunan ortofosfat pada konsentrasi A
Konsentrasi A
Tabel 20. Laju penurunan ortofosfat pada konsentrasi B
Konsentrasi B
Tabel 21. Laju penurunan ortofosfat pada konsentrasi C
Berdasarkan Tabel 19, Tabel 20, Tabel 21 laju penurunan ortofosfat pada
perlakuan A me miliki laju penurunan sebesar 0,1348 ppm/hari pada hari 0 sampai 3 dan pada hari 3 sa mpai 6 laju penurunan sebesar 0,0802 ppm/hari. Pada hari 9 sampai 12 perla kuan A laju penurunan sebesar 0,0082 ppm/hari. Peningkatan
kandungan ortofosfat pada perlakuan A terjadi pada hari 6 sampai 9 de ngan laju peningkatan sebesar 0,0012 ppm/hari dan 0,0717 ppm/hari pada hari 12 sampai
15.
Pada perlakuan B penurunan ortofosfat terjadi pada hari 0 sampai 3
sebesar 0,115 ppm/hari, hari ke-3 sampai hari ke -6 sebesar 0,0002 ppm/hari, dan pada hari ke-9 sampai hari ke-12 sebesar 0,0068 ppm/hari. Peningkatan ortofosfat pada perlakuan B ter jadi pada hari ke -6 sampai hari ke-9 sebesar 0,0042 ppm/hari,
dan hari ke-12 sampai hari ke -15 sebesar 0,0763 ppm/hari.
Perlakuan C pada hari ke -0 sampai ke-3 memiliki laju penurunan sebesar 0,0947 ppm/hari, hari ke-3 sampai ke -6 sebesar 0,0033 ppm/hari, dan hari ke -9 sampai ke -12 dengan laju penurunan sebesar 0,0052 ppm/hari. Peningkatan
ortofosfat terjadi pada hari ke-6 sampai ke-9 dengan laju sebesar 0,0078 ppm/hari, dan hari ke -12 sampai ke -15 sebesar 0,0735 ppm/hari.
Laju penurunan kandungan ortofosfat yang paling tinggi terjadi pada hari ke-0 sampai ke-3 untuk semua perlakuan, hal ini diduga terjadi karena ortofosfat
yang terdapat dalam air langsung diserap oleh Gracillaria sp. dan mengakumulasi ortofosfat tersebut didalam sel. Penyerapan ortofosfat secara cepat dan dalam jumlah yang besar dapat dilakukan oleh Gracillaria sp., ortofosfat diakumulasi dalam sel dan akan digunakan jika kandungan ortofosfat di air dalam jumlah yang
sedikit.
Berdasarkan uji statistik (BNT) terhadap nilai laju penurunan ortofosfat antara tiap perlakuan menunjukkan perbedaan yang nyata (P<0,05) antara tiap
perlakuan. Perbedaan yang nyata terjadi antara perlakuan A dan B, perlakuan A dan C. Sedangkan antara perlakuan B dan C tidak terjadi perbedaan yang nyata.
Berdasarkan uji statistik (uji BNT) hari terrhadap kandungan ortofosfat,
dapat diketahui bahwa hari memberikan pengaruh yang nyata terhadap kandungan ortofosfat. Pada hari ke-0 terdapat perbedaan dengan hari ke-3, hari ke-3 terdapat perbedaan yang nyata dengan ha ri ke-6, hari ke-6 tidak berbeda nyata dengan hari
ke-9, dan hari ke-9 tidak berbeda nyata dengan hari ke12, serta hari ke -12 berbeda nyata dengan hari ke -15.
Tabel 22. Persentase penurunan ortofosfat pada tiap perlakuan
perlakuan
Konsentrasi A Konsentrasi B Konsentrasi C
persentase
penurunan 11.1583 % 12.2500 % 16.5066 %
Berdasarkan Tabel 22 penurunan yang paling tinggi terdapat pada perlakuan A sebesar 11,1583% . Perlakuan B me miliki penurunan sebesar 12,25%, sedangkan pada perlakuan C penurunan sebesar 16,5066. Penurunan ortofosfat yang terjadi pada penelitian ini lebih kecil jika dibandingkan penurunan
fosfat menurut Jones et al (2002) yang sebesar 56%.
C. Parameter Biologis
Selain parameter fisika dan kimia, parameter biologis juga memegang
peranan penting. Parameter biologis ini penting untuk diketahui karena proses penyerapan nutrien dapat diketahui dengan adanya penambahan berat dari
Gracillaria sp. Parameter biologis yang diamati dalam percobaan ini akan meliputi analisa pertambahan biomassa Gracillaria sp.
1. Berat Basah dan laju Pertumbuhan Relatif (Relative Growth Rate/RGR)
Berdasarkan Gambar 13 pada Konsentrasi A terlihat berat basah
mengalami peningkatan dari hari ke -0 hingga hari ke -15. Peningkatan yang cukup besar terjadi dari hari ke-9 hingga hari ke-15, hal ini diduga terjadi karena
Penambahan berat basah yang paling tinggi terjadi pada perlakuan A, hal ini
diduga terjadi karena unsur hara yang diberikan paling besar pada perlakuan A. Pada perlakuan B dan C, peningkatan berat basah tidak terjadi perbedaan hal ini terjadi karena pemberian pupuk pada perlakuan B dan C tidak terlalu berbeda.
Berdasarkan uji statistik terhadap biomassa Gracillaria sp. antara tiap perlakuan menghasilkan kesimpulan bahwa pada selang kepercayaan 95%
pemberian konsentrasi pupuk yang berbeda tidak memberi pengaruh terhadap biomass Gracillaria sp., hal ini terjadi karena Gracillaria sp. membutuhkan waktu yang lama untuk pertumbuhannya. Sedangkan uji st atistik terhadap biomassa Gracillaria sp. antara tiap hari menghasilkan kesimpulan bahwa pada selang kepercayaan 95% pada hari yang berbeda berpengaruh terhadap biomass
Gracillaria sp.
Sedangkan uji statistik lanjutan(uji BNT) hari terhadap biomassa
Gracillaria sp., dapat diketahui bahwa hari memberikan pengaruh yang nyata terhadap biomassa Gracillaria sp. Pada hari ke-0 tidak terda pat perbedaan dengan hari ke-3, hari ke -3 tidak terdapat perbedaan yang nyata dengan hari ke-6, hari ke-6 tidak berbeda nyata dengan hari ke -9, dan hari ke -9 berbeda nyata dengan hari ke12, serta hari ke -12 berbeda nyata dengan hari ke-15.
500
Gambar 13. Biomassa Gracillaria sp. pada perlakuan A, B, C
Tabel 23. Berat basah (g) dan RGR Gracillaria sp.
Nilai RGR merupakan cerminan dari kemampuan Gracillaria sp. dalam menyerap unsur hara untuk pertumbuhannya selain daripada pengukuran
biomassa. Berdasarkan Tabel 23 perlakuan A memiliki nilai RGR sebesar 0,1 % perhari, perlakuan B sebesar 0,03 % perhari, dan perlakuan C sebesar 0,03 % perhari. Artinya peningkatan berat basah Gracillaria sp. pada perlakuan A sebesar 0,1 % per hari, perlakuan B 0,03 % per hari, dan perlakuan C 0,03% perhari.
Nilai RGR yang diperoleh pada penelitian ini berkisar antara 0.03 %-0.1 % perhari. Nilai ini masih rendah jika dibandingkan dengan nilai RGR rumput laut pada kondisi di alam yang berkisar pada 1.8 %-8.8 % perhari (Marinho et al, 2002).
D. Parameter Fisika-Kimia Lingkungan
Parameter fisika-kimia yang diamati pada penelitian ini dijadikan sebagai data pendukung untuk mengetahui proses penyerapan nutrien serta untuk
mengetahui proses perubahan nutrien. Berikut adala h data parameter fisika-kimia selama pengamatan.
Tabel 24. Parameter Fisika-Kimia Selama Penelitian
Parameter Kisaran Selama
Penelitian
Suhu 22-24 ºC
DO (Dissolved Oxygen) 5,4-5,59 mg/l
pH 7,5-7,8
Salinitas 33-36 ‰
TSS (Total Suspended Solid) 0-3 mg/l
adalah 20-28 ºC. Kandungan oksigen berada pada kisaran 5,4-5,59 mg/l. Kisaran
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Kemampuan Gracillaria sp. untuk menyerap nitrat adalah sebesar 0,1806 mg/l, untuk menyerap ortofosfat sebesar 0,0149 mg/l
2. Gracillaria sp. dapat digunakan untuk mengurangi kadar nutrien dalam perairan yang terlalu subur.
3. Nutrien yang diserap oleh Gracillaria sp. tidak langsung digunakan untuk pertumbuhan. Pertumbuhan Gracillaria sp. yang maksimal pada penelitian ini sebesar 0,1 %/hari.
B. Saran
1. Perlu dilakukan penelitian lanjutan untuk mengetahui berapa kadar nutrien yang bersifat lethal bagi Gracillaria sp.
2. Untuk mendapatkan konsentrasi nutrien yang sesuai dengan yang diharapkan maka lebih baik sumber nutrien berasal dari nitrit murni, nitrat murni, ammonia murni, ortofosfat murni.
DAFTAR PUSTAKA
APHA (American Public Health Association). 1989. Standard Method For The Examinition of Water and Wastewater. American Public Health Association. Water Pollution Control Federation. Port City Press. Baltimore, Mariland.
Aslan, L.M. 1991. Budidaya Rumput Laut. Kanisius. Yogyakarta. 96 hal
Boyd, C.E. 1988. Water Quality in Ponds for Aquaculture. Agricultural Experiment Station, Auburn University. Auburn, Alabama, USA. 482 p.
Colt, J. 1984. Computation of Dissolved Gas Concentration in Water as Functions of Temperature, Salinity, and Pressure. Amer. Fish. Soc., Spec. Publ. No. 14. 154 pp.
Davis, M.L. dan D.A. Cornwell. 1991. Introduction To Environmental Engineering. Second Edition. Mc-Graw-Hill, Inc.New York. 822p.
Dawes, C.J. 1981. Marine Botany. John Willey and Sons. New York. 497 p.
Dawson, E.Y. 1956. How to Know The Seaweed. W.M.C. Brown Company Publisher. Dubuque, Iowa. 270 p.
Duddington, C.L. 1971. Beginers Guide to Seaweed. Pelhams books Ltd, 52 Bedford Square. London. 187 hal.Kumar, H.D, and Singh, H.N. 1979. A Textbook On Algae. Second Edition. The Macmillan Press, LTD. London. 216 hal.
Effendi, H. 2003. Telaah Kualitas Air : Bagi Pengelolaan Sumberdaya dan Lingkungan Perairan. Jurusan Manajemen Sumberdaya Perairan Fakultas Perikanan dan Ilmu Kelautan. IPB. Bogor. Tidak dipublikasikan. 259 hal.
Harvey, J.W. 1982. Atmosphere and Ocean. Vision Pretd. London. 143 p.
Jones, A.B., N.P. Preston, dan W.C. Dennison. 2002. The Efficiency and Condition of Oysters and Macroalgae used as Biological Filters of Shrimp Pond Effluent. http://www.blackwell-synergy .com/doi/abs.
Krebs, C.J. 1972. Ecology : The Experimental Anallysis of Distribution and Abundance. Harper and Ron. London. 694 p.
Keputusan Menteri Lingkungan Hidup No 51 tahun 2004 Tentang Kualitas Baku Air Laut.
Luning, K. 1990. Seaweed : The Environmental, Biogeography, and Ecophysiology. John Wiley & Son, Inc. Canada. 527 p.
Mason, C.F. 1993. Biology of Freshwater Pollution. Second Edition. Longman Scientific and Technical. New York. 351 p.
Marinho, E. Soriano, C. Morales, dan W.S.C. Moreira. 2002. Cultivation of Gracillaria (Rhodophyta) in Shrimp Pond Effluent in Brazil. Aquaculture Research. 33(13):1081.
Mitchell, D.S. 1974. Aquatic Vegetation and Its Use and Control. UNESCO. Paris. 42pp
Moore, J.W. 1991. Inorganic Contaminants of Surfacewater. Springler-Verlag. New York. 334p.
Mubara k, H. 1981. Budidaya Rumput Laut. Materi Lokakarya Budidaya Laut di Denpasar Bali. Direktorat Jenderal Perikanan dan UNDP/FAO. 12 hal.
Muntsji, A.R. 1972. Beberapa Aspek Biologi Rumput Laut, Skripsi Dalam Mata Ajaran Pokok Hidrologi. Institut Pertanian Bogor. Fakultas Pertanian.
Nontji, A. 1987. Laut Nusantara. Penerbit Djambatan. Jakarta. 368 hal.
Novotny, N. dan Olem, H. 1994. Water Quality, Prevention, Identification, and Management of Diffuse Pollution. Van Nostrans Reinhold. New York. 1054 p.
Nyba kken, J.W. 1992. Biologi Laut Suatu Pendekatan Ekologis. Alih Bahasa H.M. Eidman, Koesoebiono, D.G. Bengen, M. Hutomo dan S. Sukardjo. PT. Gramedia Pustaka Utama. Jakarta. 205 hal.
Kinne, P.N, T.M. Samocha, E.R. Jones, dan C.L. Browdy. 2000. Characteriza tion of Intensive Shrimp Pond Effluent and Preliminary Studies on Biofiltration. North American Journal of Aquaculture. 63(1):25-33.
Pescod, N. B. 1973. Investigation of Rational Effluent and Stream For Tropical Countries. AIT. Bangkok.
Raven, P.H, R.F. Evert, Dan S.E. Elchhorn. 1992. Biology of Plants, 5th edition. Worth Publishers. New York.
Soegiarto, A. Sulistijo, W.W. Atmadja . dan H. Mubarak. 1979. Rumput Laut (Alga), Manfaat, Potensi dan Usaha Budidaya. LON LIPI, Jakarta. 61 hal.
Trono, G. C, dan Fortes. 1974. Euchema Farming in The Phillipine. U: p. National Science Research Center
Wardoyo, S.T.H. 1981. Kriteria Kualitas Air Untuk Pertanian dan Perikanan. Training Analisa Dampak Lingkungan. PPLH-IPB, PUSDI. PSL. IPB. Bogor.
Welch, E.B. 1980. Ecology Effects of Wastewater. Cambridge University Press. London. 337p.
LAMPIRAN
Lampiran 1. Gambar alat-alat yang digunakan dalam pengambilan data
DO-meter
Spectrofotometer
pH-meter
Lampiran 3. Bahan-bahan Yang Digunakan Dalam Pengambilan Data
Parameter Unit Bahan
Biologi
Gracilaria sp. gr
Kimia
Nitrat mg/l Brucine, H2SO4, Larutan standar nitrat
Ortofosfat mg/l Amonium molybdate, Asorbic acid, Larutan standar fosfat
Nitrit mg/l Sulfanilamide, NED, Larutan standar nitrit
Amonia mg/l Phenol solution, Sod. Nitroprosside, Oxidizing solution, Larutan standar amonia
Lampiran 4. Perhitungan Pupuk
1. Pupuk TSP yang digunakan mengandung 32 % P2O5, maka untuk 1000 mg TSP = 320 mg P2O5. Sehingga jika akan dibuat pupuk induk TSP dengan konsentrasi 1000 ppm P2O5 dibutuhkan pupuk TSP sebesar :
3125
atau 3,125 gram TSP dalam satu liter
akuades.
2. Pupuk Urea yang digunakan mengandung 46 % N maka untuk 10000 mg
Urea = 4600 mg N. Sehingga jika akan dibuat pupuk induk Urea dengan konsentrasi 10000 ppm N dibutuhkan pupuk Urea sebesar :
21739
atau 21,739 gram Urea dalam satu
liter akuades.
Untuk menghitung larutan Urea dan larutan TSP yang perlu ditambahkan
untuk masing-masing perlakuan digunakan perumusan sebagai berikut :
Lampiran 5. Data volume penambahan larutan Urea dan Larutan TSP
Larutan Urea 700ml
ka
Larutan TSP 103,14ml
Larutan Urea 91,63ml
k b
Larutan TSP 33,08ml
Larutan Urea 70ml
kc
Larutan TSP 0ml
konsentrasi NO3 (mg/l)
Lampiran 7. Data Biomassa Gracillaria s p.
Lampiran 8. Uji Statistik Kandungan Unsur Hara Media 1. Uji statistik kandungan NO3
SK db JK KT Pr
Kelompok 1 0.040154 0.04015438 -
Perlakuan 2 0.412742 0.206370795 0.0001
Kelompok (Perlakuan) 2 0.031653 0.01582645 -
Waktu 5 0.793392 0.158678368 0.0001
Perlakuan*Waktu 10 0.078056 0.007805573 -
Sisa 15 0.1406 0.009373343 -
Total 35 1.496597 - -
Uji lanjutan Beda Nyata Terkecil (BNT)
a. Uji BNT terhadap tiga perlakuan
Grup µ Perlakuan
A 1,73717 KA
B 1,51352 KC
B 1,5067 KB
b. Uji BNT terhadap hari penelitian
Grup µ Hari
2. Uji statistik kandungan NH3
SK db JK KT Pr
Kelompok 1 0,00130653 0,00130653 -
Perlakuan 2 0,0115173 0,00575865 0,0108
Kelompok (Perlakuan) 2 0,00003587 0,00001793 -
Waktu 5 0,20888601 0,0417772 0,0001
Perlakuan*Waktu 10 0,05043965 0,00504397 -
Sisa 15 0,0139001 0,00092667 -
Total 35 0,28608546 - -
Uji lanjutan Beda Nyata Terkecil (BNT) a. Uji BNT terhadap tiga perlakuan
Grup µ Perlakuan
A 0,15381 KA
B 0,1258 KC
b. Uji BNT terhadap hari penelitian
3. Uji statistik kandungan NO2
SK db JK KT Pr
Kelompok 1 0,00076544 0,00076544 -
Perlakuan 2 0,01163709 0,005818545 0,3904
Kelompok (Perlakuan) 2 0,00723772 0,00361886 -
Waktu 5 1,45174532 0,290349064 0,0001
Perlakuan*Waktu 10 0,16766222 0,016766222 -
Sisa 15 0,08710588 0,005807059 -
Total 35 1,72615367 - -
Uji lanjutan Beda Nyata Terkecil (BNT)
a. Uji BNT terhadap hari penelitian
Grup µ Hari
4. Uji statistik kandungan PO4
SK db JK KT Pr
Kelompok 1 0,005776 0,005776 -
Perlakuan 2 0,10224201 0,051121005 0,0001
Kelompok (Perlakuan) 2 0,00250467 0,001252335 -
Waktu 5 0,88463807 0,176927614 0,0001
Perlakuan*Waktu 10 0,16551802 0,016551802 -
Sisa 15 0,02193033 0,001462022 -
Uji lanjutan Beda Nyata Terkecil (BNT)
a. Uji BNT terhadap tiga perlakuan
Grup µ Perlakuan
A 0,316 KA
B 0,208 KB
B 0,1985 KC
b. Uji BNT terhadap hari penelitian
Grup µ Hari
Lampiran 9. Uji Statistik Biomassa Gracillaria sp.
SK db JK KT Pr
Kelompok 1 0,00001184 0,00001184 -
Perlakuan 2 0,00000548 0,00000274 0,3097
Kelompok (Perlakuan) 2 0,00002694 0,00001347 -
Waktu 5 0,00007062 0,000014124 0,002
Perlakuan*Waktu 10 0,00000709 0,000000709 -
Sisa 15 0,00003239 2,15933E-06 -
Total 35 0,00015436 - -
Uji lanjutan Beda Nyata Terkecil (BNT)
a. Uji BNT hari penelitian terhadap biomassa Gracillaria sp.