SKRIPSI
PEMBUATAN MINUMAN TEH HIJAU DALAM BOTOL DENGAN PENAMBAHAN EKSTRAK KLOROFIL DAUN SUJI (Pleomele angustifolia N. E. Brown) DAN EVALUASI MUTUNYA SELAMA
PENYIMPANAN
Oleh :
WAHYU HARYATI MASER F24060090
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PEMBUATAN MINUMAN TEH HIJAU DALAM BOTOL DENGAN PENAMBAHAN EKSTRAK KLOROFIL DAUN SUJI (Pleomele angustifolia N. E. Brown) DAN EVALUASI MUTUNYA SELAMA
PENYIMPANAN
SKRIPSI
Sebagai salah satu syarat untuk mendapatkan gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Ilmu dan Teknologi Pangan
Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh :
WAHYU HARYATI MASER F24060090
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
Wahyu Haryati Maser. F24060090. Production of Green Tea Drink in Bottle with Increment Chlorophyll Extract Suji Laef (Pleomele angustifolia N. E. Brown) and Evaluation of Quality during Storage. Supervised by Deddy Muchtadi and Sutrisno Koswara.
ABSTRACT
Green tea is the most famous health drink in the world. Polyphenolic compounds contained in green tea have many usages, so that also with suji leaf (Pleomele angustifolia). Production of green tea drink with the addition of chlorophyll extract of suji leaf was increased its antioxidant content. The objective of this research was established the formulation of green tea drink product which combined with chlorophyll extracts from suji leaf, the long time of heating process, and the shelf life of drink product. The storage evaluate had been performed by ASLT (Accelerated Shelf Life Testing) method or acceleration method which was applied Arrhenius model with zero reaction orde and one reaction orde.
This research had been done by two steps including preliminary research and main research. The experiment reported the best resulted of chlorophyll content analyze and antioxidant activity on chlorophyll extracts was performed at Cu2+ with 0 ppm concentration, therefore no addition Cu2+ on the chlorophyll extract drink. The best combination of tea amount and boil water at 85˚C to phenol total analyze and antioxidant activity was identified on 1.25: 100 (w/v). The formulation of ingredient consist of refined sugar 12 % (w/v), sitric acid 0,018 % (w/v), CMC 0,05 % (w/v), green tea 1,25 g/100 ml water, and chloropyll extract (10; 20; 30) ml/100 ml for each product. The first, second, and third sample were indicated 2.9; 2.9; and 2.9 for flavor score, 3.6; 3.5; and 3.4 for taste score, 3.5; 3.2; and 3.1 for color score; 3.6; 3.3; and 3.2 for overall score of organoleptic test. Organoleptic test had shown no significant effect. The experiment reported the best resulted of antioxidant activity was performed at third sample. The total bacterial analysis indicated that both of them period was
described the value of Standard Plate Count < 2.5 x 102 colony/ml. The variable of ASLT (Accelerated Shelf Life Testing) was used
including antioxidant activity value for sample which was sterilized until 10 min have shelf life 223 days at 25 oC respectively and in 15 min have shelf life 235 days at 25 oC respectively. Therefore the sterilization time was using sterilization 15 min than 10 min caused the shelf life was a long time. Based on the experiment indicated the optimal combination value of green tea to boil water was 1.25: 100 (w/v) at 85 oC. It also known the best ingredient formulation were refined sugar 12 % (w/v), sitric acid 0,018 % (w/v), CMC 0,05 % (w/v), green tea 1,25 g/100 ml water, and chloropyll extract 30 ml/100 ml to product based on organoleptic test and antioxidant activity. The sterilization processed of product for 15 min with 121 oC was better than product which was sterilized for 10 min with 121 oC.
Wahyu Haryati Maser. F24060090. Pembuatan Minuman Teh Hijau dalam Botol dengan Penambahan Ekstrak Klorofil Daun Suji (Pleomele angustifolia N. E. Brown) dan Evaluasi Mutunya selama Penyimpanan. Di bawah bimbingan Deddy Muchtadi dan Sutrisno Koswara.
RINGKASAN
Tujuan penelitian ini yaitu menentukan formulasi minuman teh hijau dengan penambahan ekstrak klorofil daun suji, menentukan lama proses pemanasan, dan menentukan umur simpan produk minuman. Metode uji penyimpanan menggunakan metode ASLT (Accelerated Shelf Life Testing) atau metode akselerasi. Model ASLT yang digunakan adalah model Arrhenius. Metode ini menggunakan ordo reaksi nol dan ordo reaksi satu.
Penelitian ini dilakukan dalam dua tahapan yaitu penelitian pendahuluan dan penelitian utama. Analisis yang digunakan mencakup analisis total bakteri, analisis warna, analisis kadar klorofil, analisis total polifenol (Metode Folin-Denis), dan analisis aktivitas antioksidan. Penelitian pendahuluan dilakukan untuk memperoleh ekstrak klorofil daun suji yang stabil dengan menentukan jumlah Cu2+ (CuSO4) pada ekstrak klorofil dan menentukan jumlah teh. Hasil analisis
kadar klorofil dan aktivitas antioksidan pada ekstrak klorofil yang paling baik adalah pada Cu2+ dengan konsentrasi 0 ppm sehingga untuk formulasi minuman ekstrak klorofil tidak dilakukan penambahan Cu2+. Jumlah teh hijau terbaik dari analisisi total fenol dan aktivitas antioksidan adalah perbandingan 1,25 : 100 (b/v) terhadap jumlah teh dan air panas seduhan dengan suhu 85 oC.
Penelitian utama terdiri dari formulasi minuman teh hijau berklorofil dari ekstrak daun suji, pengemasan dengan pembotolan, dan penentuan umur simpan minuman. Formulasi minuman dilakukan dengan tiga macam formula dengan perbedaan pada persentase jumlah ekstrak klorofil. Formula pertama menggunakan gula pasir 12 % (b/v), asam sitrat 0,018 % (b/v), CMC 0,05 % (b/v), teh hijau 1,25 g/100 ml air, dan ekstrak klorofil 10 ml/100 ml minuman. Formula kedua menggunakan gula pasir 12 % (b/v), asam sitrat 0,018 % (b/v), CMC 0,05 % (b/v), teh hijau 1,25 g/100 ml air, dan ekstrak klorofil 20 ml/100 ml minuman. Formula ketiga menggunakan gula pasir 12 % (b/v), asam sitrat 0,018 % (b/v), CMC 0,05 % (b/v), teh hijau 1,25 g/100 ml air, dan ekstrak klorofil 30 ml/100 ml minuman.
Formula yang didapatkan kemudian diproses untuk pembuatan minuman yang selanjutnya dilakukan pengemasan dengan pembotolan. Proses sterilisasi dilakukan pada dua waktu yaitu 10 menit dan 15 menit. Hasil analisis total bakteri menunjukkan kedua waktu sterilisasi memberikan nilai Standard Plate Count sebesar < 2,5 x 102 koloni/ml. Syarat mutu minuman teh dalam kemasan sesuai dengan SNI 01-3143-1992 adalah 2,0 x 102 koloni/ml. Dengan demikian, proses sterilisasi cukup memenuhi syarat mutu minuman teh dalam kemasan. Penetuan waktu sterilisasi yang dipilih selanjutnya ditentukan dengan umur simpan yang lebih lama.
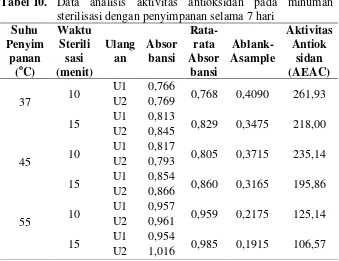
Hasil uji penyimpanan menggunakan metode ASLT (Accelerated Shelf Life Testing) atau metode akselerasi menunjukkan evaluasi mutu minuman selama penyimpanan yang disterilisasi dengan waktu 10 menit pada perubahan aktivitas antioksidan memiliki umur simpan 223 hari pada suhu simpan 25 oC. Evaluasi mutu minuman selama penyimpanan yang disterilisasi dengan waktu 15 menit pada perubahan aktivitas antioksidan memiliki umur simpan 235 hari pada suhu simpan 25 oC. Dengan demikian, waktu sterilisasi lebih baik menggunakan waktu sterilisasi 15 menit dari pada 10 menit karena memberikan umur simpan yang lebih lama.
ii
Judul : PEMBUATAN MINUMAN TEH HIJAU DALAM BOTOL DENGAN PENAMBAHAN EKSTRAK KLOROFIL DAUN SUJI (Pleomele angustifolia N. E. Brown) DAN EVALUASI MUTUNYA SELAMA PENYIMPANAN
Nama : Wahyu Haryati Maser NIM : F24060090
Menyetujui,
Bogor, Desember 2010
Dosen Pembimbing I Dosen Pembimbing II
(Prof. Dr. Ir. Deddy Muchtadi, Ms) (Ir. Sutrisno Koswara, M.Si)
NIP : 19460711 197603 1 001 NIP : 19460505 199103 1 003
Mengetahui
Ketua Departemen,
(Dr. Ir. Dahrul Syah)
NIP : 19650814.199002.1.001
iii
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER INFORMASI
Saya menyatakan dengan sebenar-benarnya bahwa skripsi dengan judul
Pembuatan Minuman Teh Hijau dalam Botol dengan Penambahan Ekstrak Klorofil Daun Suji (Pleomele angustifolia N. E. Brown) dan Evaluasi Mutunya Selama Penyimpanan adalah hasil karya saya sendiri dengan arahan Dosen Pembimbing Akademik, dan belum diajukan dalam bentuk apapun pada
perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya
yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam
teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, Desember 2010
Yang membuat pernyataan,
iv
BIODATA PENULIS
Penulis dilahirkan di Pekanbaru, Riau pada tanggal 27
April 1989, anak ketiga dari tiga bersaudara dari pasangan Bapak Mas’ud dan Ibu Ermi.
Penulis memulai pendidikan di Sekolah Dasar Negeri
018 Simpang Tiga pada tahun 1994 dan lulus pada tahun 2000.
Pada tahun 2000 penulis melanjutkan studi ke Sekolah Lanjutan Tingkat Pertama
Negeri 5 Pekanbaru dan lulus pada tahun 2003. Selanjutnya penulis melanjutkan
ke Sekolah Menengah Atas Negeri 9 Pekanbaru pada tahun 2003 dan berhasil
lulus pada tahun 2006. Penulis diterima di Institut Pertanian Bogor pada tahun
2006 melalui jalur BUD (Beasiswa Utusan Daerah) Provinsi Riau. Pada tahun
2007 penulis diterima sebagai mahasiswa di Departemen Ilmu dan Teknologi
Pangan Fakultas Teknologi Pertanian Institut Pertanian Bogor.
Selama dibangku perkuliahan, penulis pernah aktif di Musholla Al-Quds
Gedung A1 Asrama Putri TPB (Tingkat Persiapan Bersama) selama satu tahun
kepengurusan (2006-2007). Selain itu, penulis juga aktif di Divisi Gerakan
Membangun Nurani Mahasiswa (GAMA) LDK DKM Al-Hurriyyah IPB selama
dua tahun kepengurusan (2006-2008).
v
KATA PENGANTAR
Assalamu’alaykum wa rahmatullahi wa barakatuh
Alhamdulillah, segala puji milik Allah yang telah memberikan
keberkahan, limpahan rahmat, dan hidayah-Nya sehingga penulis dapat
menyelesaikan skripsi ini. Shalawat serta salam senantiasa tercurah kepada
Rasulullah Muhammad SAW beserta para sahabat, keluarga, dan para
pengikutnya.
Penulis membuat skripsi yang berjudul “Pembuatan Minuman Teh Hijau
dalam Botol dengan Penambahan Ekstrak Klorofil Daun Suji (Pleomele
angustifolia N. E. Brown) dan Evaluasi Mutunya Selama Penyimpanan” sebagai
salah satu syarat untuk mendapatkan gelar Sarjana Teknologi Pertanian di Institut
Pertanian Bogor.
Penulis berharap semoga tulisan ini dapat bermanfaat bagi penulis dan
bagi yang membutuhkan. Amin ya Rabb.
Wassalamu’alaykum wa rahmatullahi wa barakatuh
Bogor, Desember 2010
vi
UCAPAN TERIMA KASIH
Segala puji syukur penulis ucapkan kehadirat Allah SWT yang telah
memberikan keberkahan, kekuatan, kenikmatan, dan karunia-Nya sehingga
penulis dapat menyelesaikan karya ilmiah ini. Penelitian ini diselesaikan atas
bantuan dan bimbingan dari berbagai pihak oleh karena itu pada kesempatan ini
penulis ingin mengucapkan terima kasih kepada :
1. Kedua orang tua tercinta dan seluruh keluarga atas segala dorongan, doa, dan
kasing sayang yang tidak pernah terputus terutama untuk Silvia Elsih Maser
dan Istifhar Maser;
2. Bapak Prof. Dr. Ir. Deddy Muchtadi, Ms dan Bapak Ir. Sutrisno Koswara,
M.Si selaku dosen pembimbing atas segala bimbingan, nasehat, dan
arahannya dalam penyelesaian pendidikan sarjana yang ditempuh oleh
penulis;
3. Ibu Dian Herawati, STP, M.Si selaku dosen penguji yang telah memberikan
koreksi dalam penulisan karya ini dan beberapa arahan serta nasihat untuk
perbaikan diri penulis;
4. Seluruh Staf Pengajar, Staf Jurusan, dan Staf Perpustakaan yang telah
membantu penulis secara langsung maupun tidak langsung;
5. Para laboran yang membantu selama penelitian: Pak Rozak, Pak Wahid, Pak
Sobirin, Pak Taufik, Mas Aldi, Pak Edi, Pak Gatot, Bu Rubiyah, Bu Antin,
Pak Sidik;
6. Guru spritual saya dan teman-teman seperjuangan tersayang “Humairoh”
yang telah banyak menyemangati saya;
7. Kepada teman-teman LDK DKM Al-Hurriyyah, Wisma Balsem, dan Asrama
Riau yang telah banyak menginspirasi saya;
8. Kepada teman-teman ITP 43 terutama Sarah, Anna, Angga, Anis, Dedi,
Syaiha, dan yang lainnya yang tidak tertulis namanya, atas segala bantuan dan
dukungannya selama saya melaksanakan penelitian;
Semoga Allah Ta’ala memberkahi dan membalas kebaikan mereka semua dengan kebaikan pula. Amin ya Rabb.
vii
DAFTAR ISI
Halaman
KATA PENGANTAR ... v
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... x
DAFTAR LAMPIRAN ... xi
I. PENDAHULUAN ... 1
A. LATAR BELAKANG ... 1
B. TUJUAN ... 2
II. TINJAUAN PUSTAKA ... 3
A. TEH HIJAU ... 3
B. KLOROFIL ... 4
C. PROSES TERMAL PRODUK MINUMAN ... 6
D. EVALUASI MUTU METODE AKSELERASI DALAM PENYIMPANAN ... 9
1. Reaksi Ordo Nol ... 10
2. Reaksi Ordo Satu ... 11
III. METODOLOGI PENELITIAN ... 14
A. BAHAN DAN ALAT ... 14
1. Bahan ... 14
2. Alat ... 14
B. METODE PENELITIAN ... 15
1. Penelitian Pendahuluan ... 15
2. Penelitian Utama ... 16
3. Analisis Total Bakteri ... 21
4. Analisis Kadar Klorofil ... 21
5. Analisis Total Polifenol (Metode Folin-Denis) ... 22
6. Analisis Aktivitas Antioksidan ... 22
IV. HASIL DAN PEMBAHASAN ... 24
A. PENELITIAN PENDAHULUAN ... 24
viii
2. Penentuan Jumlah Teh ... 26
B. PENELITIAN UTAMA ... 28
1. Formulasi Minuman Teh Hijau Berklorofil ... 28
2. Pengemasan dengan Pembotolan ... 31
3. Penentuan Umur Simpan Minuman ... 32
V. KESIMPULAN DAN SARAN ... 40
A. KESIMPULAN ... 40
B. SARAN ... 41
ix
DAFTAR TABEL
Halaman
Tabel 1. Komposisi teh hijau ... 4
Tabel 2. Kombinasi suhu dan waktu yang diperlukan untuk menurunkan jumlah mikroba pada level yang sama... 8
Tabel 3. Rancangan Formula ... 16
Tabel 4. Data tingkat kadar klorofil pada daun suji... 25
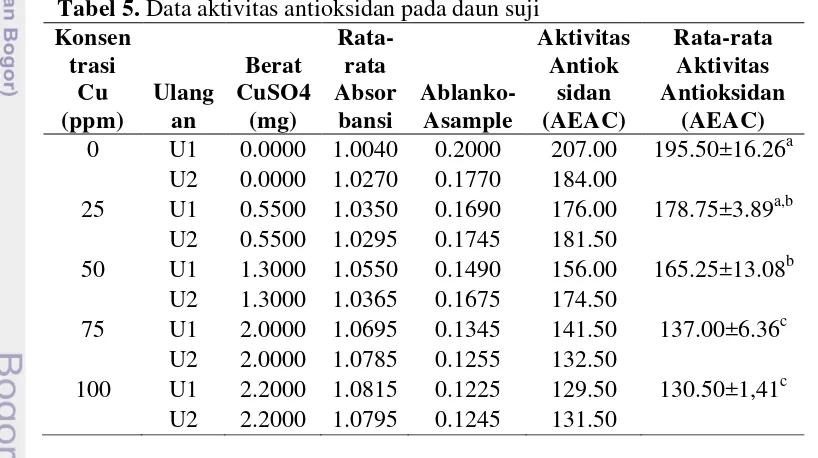
Tabel 5. Data aktivitas antioksidan pada daun suji ... 26
Tabel 6. Data tingkat total fenol pada teh ... 27
Tabel 7. Data aktivitas antioksidan pada seduhan teh hijau ... 28
Tabel 8. Data aktivitas antioksidan pada minuman teh hijau dengan penambahan ekstrak klorofil ... 31
Tabel 9. Data analisis aktivitas antioksidan pada minuman sterilisasi ... 33
Tabel 10. Data analisis aktivitas antioksidan pada minuman sterilisasi dengan penyimpanan selama 7 hari ... 33
Tabel 11. Data analisis aktivitas antioksidan pada minuman sterilisasi dengan penyimpanan selama 14 hari ... 34
Tabel 12. Data analisis aktivitas antioksidan pada minuman sterilisasi dengan penyimpanan selama 21 hari ... 35
Tabel 13. Persamaan ordo nol dan ordo satu ... 36
x
DAFTAR GAMBAR
Halaman Gambar 1. Struktur kimia klorofil a dan klorofi b ... 5
Gambar 2. Tahapan proses pembuatan minuman teh hijau dengan ekstrak
berklorofil ... 17
Gambar 3. Diagram alir analisis total polifenol ... 22
Gambar 4. Plot Arhenius pada aktivitas antioksidan dengan waktu sterilisasi 10
menit ... 37
Gambar 5. Plot Arhenius pada aktivitas antioksidan dengan waktu sterilisasi 15
xi
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data analisi kadar klorofil pada ekstrak klorofil ... 45
Lampiran 2. Hasil oneway ANOVA pengaruh konsentrasi Cu terhadap total klorofil ... 46
Lampiran 3. Data kurva standar asam askorbat pada ekstrak klorofil ... 46
Lampiran 4. Kurva standar asam askorbat pada ekstrak klorofil ... 47
Lampiran 5. Contoh perhitungan aktivitas antioksidan pada ekstrak klorofil ... 47
Lampiran 6. Hasil oneway ANOVA pengaruh konsentrasi Cu terhadap aktivitas antioksidan ... 48
Lampiran 7. Data kurva asam tanat pada analisis total fenol ... 48
Lampiran 8. Kurva standar asam tanat... 49
Lampiran 9. Contoh perhitungan analisi total fenol pada seduhan teh hijau (dalam 100 ml air panas 85 oC) ... 49
Lampiran 10. Hasil oneway ANOVA pengaruh berat teh hijau terhadap total fenol ... 49
Lampiran 11. Data kurva standar asam askorbat pada teh hijau ... 50
Lampiran 12. Kurva standar asam askorbat pada teh hijau ... 50
Lampiran 13. Contoh perhitungan analisis aktivitas antioksidan pada seduhan teh hijau (dalam 100 ml air panas 85 oC) ... 51
Lampiran 14. Hasil oneway ANOVA pengaruh berat teh hijau terhadap aktivitas antioksidan ... 51
Lampiran 15. Kuisioner Organoleptik ... 52
Lampiran 16. Data Uji Organoleptik untuk aroma ... 53
Lampiran 17. Hasil oneway ANOVA pengaruh aroma terhadap ketiga sampel ... 54
Lampiran 18. Data Uji Organoleptik untuk rasa ... 55
Lampiran 19. Hasil oneway ANOVA pengaruh rasa terhadap ketiga sampel ... 56
Lampiran 20. Data Uji Organoleptik untuk Warna ... 57
Lampiran 21. Hasil oneway ANOVA pengaruh warna terhadap ketiga sampel ... 58
Lampiran 22. Data Uji Organoleptik untuk Overall ... 59
xii
Lampiran 24. Data kurva standar pada minuman teh hijau ... 61
Lampiran 25. Kurva standar asam askorbat pada minuman ... 61
Lampiran 26. Contoh perhitungan analisis aktivitas antioksidan pada minuman .... 62
Lampiran 27. Hasil oneway ANOVA pengaruh aktivitas antioksidan terhadap ketiga formula minuman... 62
Lampiran 28. Data total bakteri ... 62
Lampiran 29. Data kurva standar asam askorbat pada minuman sterilisasi ... 63
Lampiran 30. Data kurva standar asam askorbat pada minuman sterilisasi dengan penyimpanan selama 7 hari ... 64
Lampiran 31. Data kurva standar asam askorbat pada minuman sterilisasi dengan penyimpanan selama 14 hari ... 65
Lampiran 32. Data kurva standar asam askorbat pada minuman sterilisasi dengan penyimpanan selama 21 hari ... 66
Lampiran 33. Grafik plot ordo nol suhu 37 oC sterilisasi 10 menit ... 67
Lampiran 34. Grafik plot ordo nol suhu 37 oC sterilisasi 15 menit ... 67
Lampiran 35. Grafik plot ordo nol suhu 45 oC sterilisasi 10 menit ... 67
Lampiran 36. Grafik plot ordo nol suhu 45 oC sterilisasi 15 menit ... 68
Lampiran 37. Grafik plot ordo nol suhu 55 oC sterilisasi 10 menit ... 68
Lampiran 38. Grafik plot ordo nol suhu 55 oC sterilisasi 15 menit ... 68
Lampiran 39. Grafik plot ordo satu suhu 37 oC sterilisasi 10 menit ... 69
Lampiran 40. Grafik plot ordo satu suhu 37 oC sterilisasi 15 menit ... 69
Lampiran 41. Grafik plot ordo satu suhu 45 oC sterilisasi 10 menit ... 69
Lampiran 42. Grafik plot ordo satu suhu 45 oC sterilisasi 15 menit ... 70
Lampiran 43. Grafik plot ordo satu suhu 55 oC sterilisasi 10 menit ... 70
Lampiran 44. Grafik plot ordo satu suhu 55 oC sterilisasi 15 menit ... 70
1 I. PENDAHULUAN
A. LATAR BELAKANG
Perkembangan ilmu pengetahuan dan teknologi menyebabkan
berkembangnya pemahaman masyarakat tentang pangan. Pola konsumsi
pangan masyarakat yang berkembang menunjukkan pengaruh besar terhadap
kebutuhan makanan yang menyehatkan. Kesadaran pentingnya kesehatan
memberikan dampak pemilihan pangan yang tidak hanya mempertimbangkan
nilai gizi dan lezatnya makanan, tetapi juga pengaruh makanan tersebut
terhadap kesehatan. Timbulnya pemahaman ini menyebabkan adanya industri
makanan dan minuman menonjolkan produk yang mengandung antioksidan.
Antioksidan perlu dikonsumsi setiap hari dalam jumlah cukup supaya
dapat bekerja menangkap atau menghancurkan radikal bebas. Antioksidan
yang telah banyak diketahui masyarakat antara lain polifenol dan klorofil.
Polifenol banyak terkandung dalam salah satu tanaman Indonesia yaitu teh
yang merupakan salah satu bahan minuman alami yang sangat populer di
masyarakat.
Teh yang paling baik dari segi visual dan komposisinya adalah teh
hijau. Teh hijau sudah dikenal sebagai salah satu minuman sehat di penjuru
dunia selama berabad-abad. Teh hijau dibuat dari daun teh (Camellia
sinensis) yang mengalami proses pemanasan. Jenis antioksidan yang juga
telah diketahui yaitu klorofil. Menurut Breinholt et al. (1995) diacu dalam
Alsuhendra (2004), beberapa penelitian memperlihatkan bahwa klorofil dan
turunannya memiliki kemampuan sebagai antioksidan dan antikanker. Selain
itu, klorofil juga mempunyai aktivitas sebagai anti peradangan (Okai dan
Okai, 1998).
Daun suji biasa digunakan masyarakat sebagai pewarna makanan
karena kandungan klorofilnya yang cukup tinggi untuk pewarnaan. Menurut
Prangdimurti et al. (2006), ekstrak daun suji memiliki aktivitas antioksidan
dan daya hipokolesterolemik dalam sistem pencernaan in vivo menggunakan
2 kemampuan pengikatan kolesterol dalam simulasi sistem pencernaan in vitro
(Sari, 2005). Oleh karena itu, dalam upaya meningkatkan daya terima daun
suji sebagai produk pangan yang bermanfaat bagi kesehatan, berbagai produk
olahan daun suji perlu dikembangkan.
Perpaduan antara teh hijau dan klorofil dari daun suji merupakan
sebuah inovasi pangan kaya antioksidan yang bermanfaat bagi kesehatan.
Salah satu alternatif pengolahannya adalah pembuatan minuman teh hijau
berklorofil. Dengan demikian, manfaat teh hijau dan klorofil dapat diperoleh
sekaligus.
B. TUJUAN
Tujuan penelitian ini yaitu menentukan formulasi minuman teh hijau
dengan penambahan ekstrak klorofil daun suji, menentukan lama proses
3 II. TINJAUAN PUSTAKA
A. TEH HIJAU
Tanaman teh merupakan spesies tunggal dengan nama Latin
Camellia sinensis. Teh juga memiliki beberapa varietas khusus, yaitu
sinensis, assamica dan irrawadiensis. Menurut Tuminah (2004), teh
diklasifikasikan sebagai berikut:
Divisi : Spermatophyta (tumbuhan biji)
Sub divisi : Angiospermae (tumbuhan biji terbuka)
Kelas : Dicotyledoneae (tumbuhan biji belah)
Sub kelas : Dialypetalae
Ordo (bangsa) : Guttiferales (Clusiales)
Familia (suku) : Camelliaceae (Theaceae)
Genus (marga) : Camellia
Spesies (jenis) : Camellia sinensis
Teh hijau merupakan salah satu jenis teh berdasarkan penanganan
pasca panen. Daun teh yang dijadikan teh hijau biasanya langsung diproses
setelah dipetik. Setelah daun mengalami oksidasi dalam jumlah minimal,
proses oksidasi dihentikan dengan pemanasan. Teh yang sudah dikeringkan
bisa dijual dalam bentuk lembaran daun teh atau digulung rapat berbentuk
seperti bola-bola kecil. Komposisi teh hijau disajikan pada Tabel 1.
Kandungan polifenol teh hijau menyebabkannya memiliki banyak
manfaat. Salah satu jenis polifenol teh adalah flavonoid. Flavonoid teh,
seperti katekin dan turunannya, merupakan antioksidan. Mekanisme
penghambatan oksidasi oleh katekin adalah dengan mendonorkan atom
hidrogennya untuk mereduksi radikal bebas, menjaga, dan meregenerasi
-tokoferol dan atau antioksidan lainnya, serta mengkelat ion logam yang
menginisiasi terbentuknya radikal bebas (Zhang et al., 1997).
Peneliti lain menyebutkan bahwa teh dapat bekerja sebagai
4 Malik (2007), teh hijau efektif menghindarkan kasus tumor sebagaimana
kemampuannya mengurangi penyakit kanker.
Tabel 1. Komposisi teh hijau
No. Komposisi Berat Kering
(%)
Bahan yang dapat diendapkan alkohol Kalium (potasium)
Klorofil adalah pigmen berwarna hijau yang terdapat dalam kloroplas
bersama-sama dengan karoten dan xantofil. Klorofil merupakan suatu porfirin
yang mengandung cincin dasar tetrapirol. Keempat cincinnya berikatan
dengan Mg2+. Cincin isosiklik yang kelima berada dekat dengan cincin pirol ketiga. Subsituen asam propionat diesterifikasi oleh diterpen alkohol fitol
(C20H39OH) yang bersifat hidrofobik dalam cincin keempat. Klorofil ini
banyak terdapat pada tumbuhan berwarna hijau seperti daun suji.
Daun suji mempunyai intensitas warna hijau yang lebih tinggi jika
dicampur dengan adonan makanan dibandingkan dengan daun yang lain.
Kadar klorofil total daun suji segar sebesar 3773.9 ppm yang terdiri dari
klorofil a sebesar 2524.6 ppm dan klorofil b sebesar 1250.3 ppm. Penggunaan
larutan pengekstrak NaHCO3 0.5 % pada daun suji memberikan nilai kadar
5 sebesar 73.25% dan kadar klorofil basis keringnya sebesar 1.4%
(Prangdimurti et al., 2006). Menurut Winarno (1992), ada dua jenis klorofil
yang telah berhasil diisolasi yaitu klorofil a dan klorofil b. Keduanya terdapat
pada tanaman dengan perbandingan 3 : 1. Kedua jenis klorofil tersebut secara
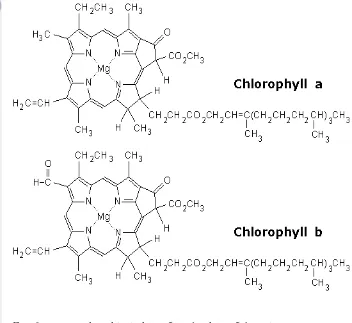
kimiawi sangat mirip. Struktur kimia klorofil dapat dilihat pada Gambar 1.
Gambar 1. Struktur kimia klorofil a dan klorofi b (Winarno, 1992)
Klorofil terdapat dalam bentuk ikatan kompleks dengan molekul
protein. Jika daun yang mengandung klorofil direbus, protein dari senyawa
kompleks tersebut akan mengalami denaturasi. Dengan demikian, klorofil
akan dibebaskan. Klorofil bebas bersifat tidak stabil, sehingga ion magnesium
(Mg2+) yang terdapat di dalamnya dapat dengan mudah diganti oleh ion hidrogen (H+). Warna daun yang semula hijau dapat berubah menjadi kecoklatan akibat terbentuknya feofitin (Alsuhendra, 2004). Warna coklat
6 Pembentukan kompleks turunan klorofil dengan mineral tertentu
(metallo-kompleks) dilakukan untuk mempertahankan warna hijau klorofil.
Menurut Alsuhendra (2004), pemberian mineral selama proses pengolahan
dan penyimpanan menunjukkan warna hijau yang dapat bertahan dengan
baik. Porfirin dapat membentuk kompleks stabil 1:1 dengan berbagai ion
logam seperti tembaga (Cu), besi (Fe), nikel (Ni), dan kobalt (Co). Kompleks
cincin porfirin klorofil dengan ion logam dapat membentuk suatu ikatan kuat
yang lebih tahan terhadap asam dan panas dibandingkan dengan klorofil asal
(porfirin berikatan dengan Mg).
Sodium-copper-chlorophyllin (SCC) merupakan suatu kompleks
antara tembaga (Cu)-turunan klorofil yang larut air, berwarna hijau terang,
dan berpotensi sebagai antioksidan. SCC komersial dibuat dari ekstrak kasar
klorofil menggunakan NaOH-metanol yang diikuti dengan penggantian atom
Mg oleh logam Cu. Terkelatnya logam menyebabkan klorofil lebih tahan
terhadap pemanasan (Rufaida, 2008). Densitas elektron di pusat cincin pun
lebih terkonsentrasi dan menjauhi kerangka porfirinnya. Hal ini dapat
meningkatkan kemampuan mendonorkan elektron dari sistem porfirin yang
terkonjugasi. Klorofil yang kehilangan grup fitilnya menampakkan
peningkatan antioksidasi. Menurut Rufaida (2008), kerangka porfirin dan
keberadaan logam yang terkelat adalah dua hal penting yang menentukan
aktivitas antioksidan klorofil.
C. PROSES TERMAL PRODUK MINUMAN
Pengolahan pangan dengan proses termal dilakukan dengan
menggunakan suhu tinggi untuk membunuh atau menginaktifkan
mikroorganisme yang dapat menyebabkan pembusukan pada produk pangan.
Pembusukan pada produk pangan ini dapat membahayakan kesehatan
manusia ketika dikonsumsi. Menurut Fellows (2000), proses termal
merupakan proses yang dilakukan dengan tujuan membunuh mikroba,
inaktivasi enzim, pembentukan warna, tekstur dan flavor yang baru,
7 Berdasarkan kriteria suhu, waktu, dan tujuan pemanasan, proses
pengolahan pangan dengan suhu tinggi dapat dibagi menjadi beberapa operasi
yaitu proses blansir, pasteurisasi, sterilisasi, dan hot filling (Hariyadi, 2000).
Proses termal yang digunakan pada pengolahan produk minuman teh hijau
dengan penambahan ekstrak klorofil daun suji dalam kemasan yaitu
sterilisasi.
Spora bakteri umumnya mempunyai ketahanan panas yang lebih
tinggi dari pada sel vegetatifnya. Oleh karena itu, proses pemanasan pada
sterilisasi komersial bertujuan untuk menginaktifkan spora bakteri, terutama
spora bakteri patogen yang tahan panas. Sel vegetatif, khamir dan kapang
dapat diinaktifkan pada suhu yang lebih rendah (60-88 oC), sedangkan bakteri termofilik dan mesofilik perlu suhu yang lebih tinggi untuk membunuhnya
(umumnya pada suhu standar 121 oC). Menurut Muchtadi (1995), penangas yang berisi air mendidih dapat digunakan untuk sterilisasi bahan pangan asam
karena suhu 212 oF (100 oC) dianggap cukup untuk menghancurkan mikroba pembusuk dan patogen yang terdapat dalam pangan tersebut.
Keasaman (pH) sangat menentukan suhu sterilisasi yang digunakan.
Proses sterilisasi untuk bahan pangan yang mempunyai pH lebih kecil dari
4.5 cukup dilakukan dengan suhu di bawah 100 oC, sedangkan untuk bahan
pangan yang memiliki pH di atas 4.5 maka suhu sterilisasi harus lebih dari
100 oC dan umumnya 121 oC (Kyle et al., 1956). Menurut Woodroof dan Luh (1982), pangan yang tergolong sebagai pangan asam dan pangan sangat asam,
proses pemanasan di bawah suhu 100 oC selama beberapa menit sudah dianggap memadai. Spora bakteri termofilik yang dikhawatirkan dapat
tumbuh pada proses pemanasan di bawah 100 oC ternyata memiliki resistensi panas yang rendah bila spora tersebut berada dalam suasana pH yang rendah.
Ketahanan panas mikroorganisme biasanya dinyatakan dengan istilah
waktu reduksi termal (decimal reduction time) atau waktu yang dibutuhkan
pada suhu tertentu untuk menurunkan jumlah sel atau spora sebasar satu
siklus log. Waktu reduksi termal juga dapat diartikan sebagai waktu yang
diperlukan pada suhu tertentu untuk membunuh organisme atau sporanya
8 terjadinya penambahan atau pengurangan sepuluh kali lipat dalam waktu
yang dibutuhkan, baik untuk menurunkan sampai 90 % atau pembinasaan
seluruhnya (Subarna et al., 2008).
Parameter kecukupan proses termal dinyatakan dengan nilai
sterilisasi (Fo). Secara umum, Fo didefenisikan sebagai waktu (biasanya dalam
menit) yang dibutuhkan untuk membunuh mikroba target hingga mencapai
level tertentu pada suhu tertentu. Pada sterilisasi, nilai Fo diartikan sebagai
nilai sterilisasi (Hariyadi, 2000).
Terpenuhinya kecukupan panas untuk inaktivasi mikroba yang
menyebabkan kebusukan dan keracunan merupakan keberhasilan proses
pemanasan produk. Ketahanan mikroba terhadap panas diperlukan untuk
mengetahui kecukupan panas yang diberikan pada proses sterilisasi.
Ketahanan mikroba terhadap panas dapat diketahui dengan kombinasi suhu
dan waktu yang tepat. Kombinasi suhu dan waktu yang diperlukan untuk
menurunkan jumlah mikroba pada level yang sama dapat dilihat pada Tabel
2.
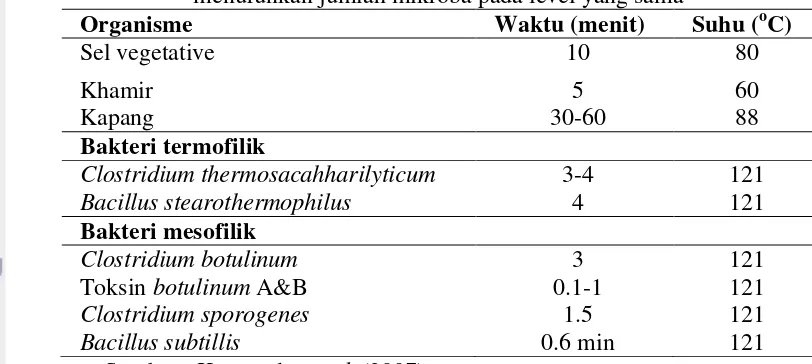
Tabel 2. Kombinasi suhu dan waktu yang diperlukan untuk menurunkan jumlah mikroba pada level yang sama
Organisme Waktu (menit) Suhu (oC)
Sel vegetative 10 80
Khamir 5 60
Kapang 30-60 88
Bakteri termofilik
Clostridium thermosacahharilyticum 3-4 121
Bacillus stearothermophilus 4 121
Bakteri mesofilik
Clostridium botulinum 3 121
Toksin botulinum A&B 0.1-1 121
Clostridium sporogenes 1.5 121
Bacillus subtillis 0.6 min 121
9
D. EVALUASI MUTU METODE AKSELERASI DALAM
PENYIMPANAN
Hasil atau akibat dari berbagai reaksi kimiawi yang terjadi di dalam
produk makanan bersifat akumulatif dan tidak dapat kembali selama
penyimpanan, sehingga pada saat tertentu hasil reaksi tersebut mengakibatkan
mutu makanan tidak dapat diterima lagi (Syarief dan Halid, 1993). Makanan
yang telah lampau masa simpan optimumnya dan menurun mutu gizinya
meskipun penampakannya masih baik maka makanan tersebut telah
kadaluarsa. Jangka waktu kadaluarsa merupakan waktu akumulasi reaksi
yang mengakibatkan mutu makanan tidak dapat lagi diterima.
Penentuan kadaluarsa berkaitan dengan tingkat keyakinan industri
terhadap tingkah laku mutu yang diproduksinya (Hariyadi, 2004). Menurut
National Food Processor Association, umur simpan produk merupakan
produk yang dianggap berada pada kisaran umur simpannya yaitu kualitas
produk tersebut secara umum dapat diterima untuk tujuan yang diinginkan
oleh konsumen dan selama bahan pengemas masih memiliki integritas serta
memproteksi isi kemasan (Arpah, 2001).
Penurunan mutu makanan dapat diketahui dari perubahan faktor
atribut mutu (Syarief dan Halid, 1993). Menurut Ellis (1994), penetuan umur
simpan suatu produk dilakukan dengan mengamati produk selama
penyimpanan sampai terjadi perubahan yang tidak dapat lagi diterima oleh
konsumen. Jenis atribut mutu yang diuji tergantung pada jenis produknya.
Metode evaluasi mutu selama penyimpanan yang digunakan yaitu
metode akselerasi. Untuk mempercepat waktu penentuan umur simpan
makanan, maka dapat menggunakan metode ASLT (Accelerated Shelf Life
Testing) atau metode akselerasi. Metode ini mengkondisikan penyimpanan
yang diatur di luar kondisi normal sehingga produk dapat lebih cepat rusak
dan penentuan umur simpan dapat ditentukan (Arpah dan Syarief, 2000).
Penggunaan metode akselerasi harus disesuaikan dengan keadaan
dan faktor yang mempercepat kerusakan produk yang bersangkutan. Umur
simpan produk yang dikemas dapat ditetapkan dengan metode ASLT. Salah
10 ini dilakukan dengan menyimpan bahan atau produk pangan dengan kemasan
akhir pada minimal tiga suhu. Tabulasi data dari penurunan mutu berdasarkan
atribut mutu tertentu diplotkan ke persamaan Arrhenius. Dari persamaan
tersebut dapat ditentukan nilai k (konstanta penurunan mutu) dan umur
simpan masing-masing bahan atau produk pangan pada berbagai suhu
penyimpanan.
Menurut Labuza (1982), reaksi kehilangan mutu pada makanan dapat
dijelaskan oleh ordo nol dan satu, sedangkan ordo lain hanya sedikit yang
menjelaskan tentang reaksi kehilangan mutu pada bahan pangan.
1. Reaksi Ordo Nol
Penurunan mutu ordo reaksi nol adalah penurunan mutu yang
konstan, kecepatan penurunan mutu tersebut berlangsung tetap pada suhu
konstan. Tipe kerusakan yang mengikuti kinetika reaksi ordo nol meliputi
reaksi kerusakan enzimatik, pencoklatan, dan reaksi oksidasi.
Perhitungan umur simpan Arrhenius dilakukan dengan
menganalisis aktivitas antioksidan pada setiap suhu penyimpanan. Hasil
yang diperoleh kemudian diplotkan dalam dua grafik hubungan antara
hasil analisis aktivitas antioksidan sebagai sumbu y dan waktu
penyimpanan sebagai sumbu x pada masing-masing suhu penyimpanan.
Kemudian dicari nilai k atau nilai konstanta penurunan mutu per hari yang
diperoleh dari kemiringan persamaan regresi kedua grafik tersebut. Setelah
diperoleh nilai k, maka dicari nilai ln k untuk masing-masing suhu
penyimpanan.
Selanjutnya dibuat plot Arrhenius, dengan sumbu x menyatakan
nilai 1/T (K-1) dan sumbu y menyatakan nila ln k pada masing-masing suhu penyimpanan yang digunakan (37 oC, 45 oC, dan 55 oC atau 310 oK, 318 oK, dan 328 oK). Nilai k merupakan gradien dari regresi linier yang didapat dari ketiga suhu penyimpanan. Dari regresi linier yang diperoleh
pada kurva Arrhenius ini dapat diprediksi umur simpan produk dengan
menggunakan rumus :
11 Keterangan :
k = konstanta penurunan mutu
ko = konstanta (tidak tergantung pada suhu)
Ea = energi aktivasi
T = suhu mutlak (K)
R = konstanta gas (1.986 kal/mol K)
Dengan mengubah persamaan di atas menjadi :
ln k = ln ko + (-Ea/R) 1/T
ko merupakan konstanta penurunan mutu produk yang tidak
tergantung pada suhu, sedangkan k merupakan konstanta penurunan mutu
dari salah satu kondisi suhu yang digunakan (20 oC, 25 oC, 30 oC atau 40
o
C) dan Ea/R merupakan gradien yang diperoleh dari plot Arrhenius.
Dengan perhitungan menggunakan rumus ini, akan diperoleh nilai ko.
Umur simpan diperoleh dengan rumus :
Keterangan :
t = prediksi umur simpan (hari)
Ao = nilai mutu awal
At = nilai mutu produk yang tersisa setelah waktu t
ko = konstanta
Dari rumus di atas dapat diprediksi umur simpan dalam hari atau bulan.
2. Reaksi Ordo Satu
Penurunan mutu bahan pangan banyak yang mengikuti ordo
reaksi satu dari pada ordo lain. Tipe-tipe kerusakan yang mengikuti reaksi
ordo satu adalah ketegikan, pertumbuhan mikroba, produksi off flavor oleh
mikroba pada daging, ikan, dan unggas, kerusakan vitamin, dan penurunan
mutu ptotein.
Perhitungan umur simpan Arrhenius dilakukan dengan
12 yang diperoleh kemudian diplotkan dalam dua grafik hubungan antara
hasil analisis aktivitas antioksidan sebagai sumbu y dan waktu
penyimpanan sebagai sumbu x pada masing-masing suhu penyimpanan.
Kemudian dicari nilai k atau nilai konstanta penurunan mutu per hari yang
diperoleh dari kemiringan persamaan regresi kedua grafik tersebut. Setelah
diperoleh nilai k, maka dicari nilai ln k untuk masing-masing suhu
penyimpanan.
Selanjutnya dibuat plot Arrhenius, dengan sumbu x menyatakan
nilai 1/T (K-1) dan sumbu y menyatakan nila ln k pada masing-masing suhu penyimpanan yang digunakan (37 oC, 45 oC, dan 55 oC atau 310 oK, 318 oK, dan 328 oK). Nilai k merupakan gradien dari regresi linier yang didapat dari ketiga suhu penyimpanan. Dari regresi linier yang diperoleh
pada kurva Arrhenius ini dapat diprediksi umur simpan produk dengan
menggunakan rumus :
Keterangan :
k = konstanta penurunan mutu
ko = konstanta (tidak tergantung pada suhu)
Ea = energi aktivasi
T = suhu mutlak (K)
R = konstanta gas (1.986 kal/mol K)
Dengan mengubah persamaan di atas menjadi :
ln k = ln ko + (-Ea/R) 1/T
ko merupakan konstanta penurunan mutu produk yang tidak
tergantung pada suhu, sedangkan k merupakan konstanta penurunan mutu
dari salah satu kondisi suhu yang digunakan (20 oC, 25 oC, 30 oC atau 40
o
C) dan Ea/R merupakan gradien yang diperoleh dari plot Arrhenius.
Dengan perhitungan menggunakan rumus ini, akan diperoleh nilai ko.
Umur simpan diperoleh dengan rumus :
13 Keterangan :
t = prediksi umur simpan (hari)
Ao = nilai mutu awal
At = nilai mutu produk yang tersisa setelah waktu t
ko = konstanta
14 III. METODOLOGI PENELITIAN
A. BAHAN DAN ALAT
1. Bahan
Bahan-bahan yang digunakan dalam pembuatan ekstrak daun suji
adalah daun suji segar (Pleomele angustifolia N. E. Brown) yang diperoleh
dari Darul Falah Desa Ciampea, NaHCO3, dan CuSO4. Daun yang
digunakan adalah daun tua, yaitu 5-7 helai di bawah pucuk daun (Rufaida,
2008). Pembuatan formulasi minuman menggunakan teh hijau kering yang
diproleh dari Perkebunan Teh Pasir Sarongge Desa Cianjur, ekstrak daun
suji, air, gula pasir, asam sitrat, dan CMC. Bahan-bahan yang digunakan
untuk analisis adalah akuades, alkohol, aseton 99.5 %, buffer asetat, asam
tanat, pereaksi Folin-Dennis, larutan Na2CO3, Sodium Copper
Chlorophyllin (SCC), 1,1-diphenyl-2-picrylhydrazyl (DPPH), metanol,
asam askorbat, dan Nutrient Agar (NA).
2. Alat
Peralatan yang digunakan dalam penelitian ini terdiri dari alat
untuk membuat minuman teh hijau berklorofil dan alat untuk analisis.
Peralatan yang digunakan untuk membuat minuman teh hijau berklorofil
yaitu blender, peralatan dapur (panci, kompor, talenan, dan sebagainya),
kain batis, penangas air, refrigerator, dan botol minuman tahan panas 121
o
C dengan volume 150 ml dan tutup tahan panas yang terbuat dari kaleng.
Peralatan yang digunakan untuk analisis yaitu labu takar, gelas piala, gelas
ukur, tabung reaksi, cawan petri, erlenmeyer, pipet, neraca analitik,
mikropipet, termometer, spektrofotometer, retort, inkubator, sentrifuse,
15 B. METODE PENELITIAN
Penelitian ini dilakukan dalam dua tahapan yaitu penelitian
pendahuluan dan penelitian utama. Analisis yang digunakan mencakup
analisis total bakteri, analisis kadar klorofil, analisis total polifenol (Metode
Folin-Denis), dan analisis aktivitas antioksidan. Keseluruhan analisis
dilakukan secara duplo (dua kali ulangan).
1. Penelitian Pendahuluan
Penelitian pendahuluan dilakukan untuk memperoleh ekstrak
klorofil daun suji yang stabil dengan menentukan jumlah Cu2+ (CuSO4)
pada ekstrak klorofil dan menentukan jumlah teh.
a. Penentuan Jumlah Cu2+ pada Ekstrak Daun Suji
Ekstrak klorofil dengan NaHCO3 0,5 % akan diberi
penambahan berbagai konsentrasi ion Cu2+. Sumber ion Cu2+ yang digunakan yaituCuSO4 dengan konsentrasi ion Cu2+ yang ditambahkan
sebesar 0 ppm, 50 ppm, 100 ppm, dan 150 ppm ekstrak daun suji.
Perhitungan mg Cu2+ dalam CuSO4 menggunakan rumus:
Sebagai contoh, untuk membuat 100 ppm ion Cu2+ dalam ekstrak daun suji atau 100 mg/1L ekstrak daun suji, maka mg CuSO4
yang dibutuhkan adalah :
mg CuSO4 = 251.1408 mg
Ekstrak yang ditambahkan ionCu2+ didiamkan di dalam lemari pendingin selama 18 jam. Kemudian dilakukan analisis terhadap
16 b. Penentuan Jumlah Teh
Daun teh hijau kering terlebih dahulu diekstrak dengan cara
didiamkan dalam air panas suhu 85 oC selama 5 menit (Winarno, 1992). Perbandingan teh hijau dan air panas yang digunakan yaitu 0.75 : 100, 1
: 100, dan 1.25 : 100. Air seduhan kemudian disaring dan diambil
filtratnya. Hasil seduhan digunakan untuk analisis total polifenol
(Metode Folin-Denis) dan analisis aktivitas antioksidan.
2. Penelitian Utama
Penelitian utama terdiri dari formulasi minuman teh hijau
berklorofil dari ekstrak daun suji, pengemasan dengan pembotolan, dan
penentuan umur simpan minuman.
a. Formulasi Minuman Teh Hijau Berklorofil
Ekstrak yang telah dipilih dari tahap penelitian pendahuluan
dapat diformulasikan menjadi minuman ringan agar dapat diterima
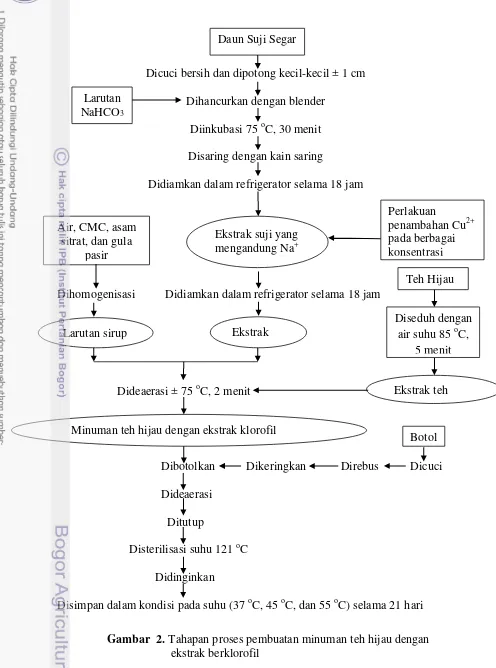
secara organoleptik. Tahapan proses pembuatan minuman terlihat pada
Gambar 2. Bahan-bahan yang digunakan untuk formulasi adalah teh
hijau dengan formulasi, gula pasir 12 % (b/v), asam sitrat 0.018 %
(b/v), dan CMC 0.05 % (b/v). Penambahan gula pasir, asam sitrat, dan
CMC berdasarkan jumlah air yang digunakan untuk pembuatan larutan
sirup. Rancangan Formula yang dilakukan ditunjukkan pada Tabel 3.
Tabel 3. Rancangan Formula
Bahan-bahan Formulasi
I II III
Gula pasir (b/v) 12 % 12 % 12 %
Asam sitrat (b/v) 0.018 % 0.018 % 0.018 %
CMC (b/v) 0.05 % 0.05 % 0.05 %
Teh hijau (g/100 ml air) 1.25 1.25 1.25
17 Dicuci bersih dan dipotong kecil-kecil ± 1 cm
Dihancurkan dengan blender
Diinkubasi 75 oC, 30 menit
Disaring dengan kain saring
Didiamkan dalam refrigerator selama 18 jam
Dihomogenisasi Didiamkan dalam refrigerator selama 18 jam
Dideaerasi ± 75 oC, 2 menit
Dibotolkan Dikeringkan Direbus Dicuci
Dideaerasi
Ditutup
Disterilisasi suhu 121 oC
Didinginkan
Disimpan dalam kondisi pada suhu (37 oC, 45 oC, dan 55 oC) selama 21 hari
Gambar 2. Tahapan proses pembuatan minuman teh hijau dengan ekstrak berklorofil
Minuman teh hijau dengan ekstrak klorofil
18 Selanjutnya dilakukan pengujian organoleptik terhadap aroma,
rasa, dan warna. Jenis uji organoleptik yang dilakukan adalah uji
hedonik atau uji kesukaan yang merupakan pengujian penerimaan
produk. Pengujian dilakukan pada 38 panelis dari mahasiswa. Panelis
diminta mengungkapkan kesukaannya terhadap sampel. Penyajian
sampel dilakukan satu per satu sampel tanpa adanya perbandingan antar
sampel. Atribut yang diujikan yaitu aroma, rasa, dan warna. Skala
hedonik yang digunakan yaitu 1-5. Angka 1 menunjukkan sangat tidak
suka, angka 2 menunjukkan tidak suka, angka 3 menunjukkan netral,
angka 4 menunjukkan suka, dan angka 5 menunjukkan sangat suka
(Soekarto, 1985). Analisis lanjutan setelah organopetik yaitu melihat
aktivitas antioksidan terbaik pada ketiga formula.
b. Pengemasan dengan pembotolan
Proses pengemasan dengan pembotolan di awali dengan
tahap proses deaerasi yakni larutan sirup dipanaskan sampai suhu 75 oC dalam tempat terbuka, kemudian ditambahkan ekstrak daun suji dan
ekstrak teh hijau dan diaduk selama 2 menit. Dengan pemanasan
tersebut oksigen dapat menguap sehingga mencegah kerusakan warna
dan flavor. Menurut Haryadi (2000), deaerasi dapat dilakukan dengan
cara sederhana yaitu dengan memanaskan minuman dalam tempat
terbuka pada suhu 70-80 oC.
Minuman dimasukkan dengan teknik hot filling ke dalam
botol bersih, kemudian ditutup dengan segera untuk menciptakan
kondisi anaerob dalam botol. Tujuannya untuk mengurangi risiko
produk terkontaminasi oleh mikroorganisme lingkungan. Minuman
yang telah dibotolkan kemudian disterilisasi pada suhu 121 oC dengan dua taraf lama pemanasan yaitu 10 menit dan 15 menit. Setelah
sterilisasi, dilakukan pengujian total mikroba untuk melihat hasil
sterilisasi pada waktu 10 menit dan 15 menit. Sebagian lagi minuman
kemudian disimpan pada suhu kamar untuk melihat mutunya selama
19 c. Penentuan Umur Simpan Minuman
Minuman yang telah disterilisasi dan disimpan pada suhu 37
o
C, 45 oC, dan 55 oC. Uji parameter mutu yang dilakukan untuk pendugaan umur simpan adalah aktivitas antioksidan. Batas umur
simpan atau penolakan produk ditetapkan besar aktivitas antioksidan 0
%.
Hasil pengamatan bagi setiap parameter aktivitas antioksidan
dihitung laju penurunan mutunya per hari (penurunan unit mutu per hari
atau k) dengan memplotkan dalam grafik hubungan antara nilai ln
aktivitas antioksidan apabila mengikuti ordo reaksi satu dan nilai
aktivitas antioksidan saja apabila mengikuti ordo reaksi nol. Nilai ini
sebagai sumbu y dan waktu penyimpanan yaitu hari ke-0, 7, 14, dan 21
sebagai sumbu x pada masing-masing suhu penyimpanan (37 oC, 45 oC, dan 55 oC).
Kemudian dicari nilai k atau nilai konstanta penurunan mutu
per hari yang diperoleh dari kemiringan persamaan regresi kedua grafik
tersebut. Setelah diperoleh nilai k, maka dicari nilai ln k untuk
masing-masing suhu penyimpanan.
Selanjutnya dibuat plot Arrhenius, dengan sumbu x
menyatakan nilai 1/T (K-1) dan sumbu y menyatakan nila ln k pada masing-masing suhu penyimpanan yang digunakan (37 oC, 45 oC, dan 55 oC atau 310 oK, 318 oK, dan 328 oK). Nilai k merupakan gradien dari regresi linier yang didapat dari ketiga suhu penyimpanan. Dari regresi
linier yang diperoleh pada kurva Arrhenius ini dapat diprediksi umur
simpan produk dengan menggunakan rumus :
Keterangan :
k = konstanta penurunan mutu
ko = konstanta (tidak tergantung pada suhu)
20 T = suhu mutlak (K)
R = konstanta gas (1.986 kal/mol K)
Dengan mengubah persamaan di atas menjadi :
ln k = ln ko + (-Ea/R) 1/T
ko merupakan konstanta penurunan mutu produk yang tidak
tergantung pada suhu, sedangkan k merupakan konstanta penurunan
mutu dari salah satu kondisi suhu yang digunakan (20 oC, 25 oC, 30 oC atau 40 oC) dan Ea/R merupakan gradien yang diperoleh dari plot Arrhenius. Dengan perhitungan menggunakan rumus ini, akan
diperoleh nilai ko. Umur simpan menurut ordo reaksi satu diperoleh
dengan rumus :
Keterangan :
t = prediksi umur simpan (hari)
Ao = nilai mutu awal
At = nilai mutu produk yang tersisa setelah waktu t
ko = konstanta
Dari rumus di atas dapat diprediksi umur simpan dalam hari
atau bulan.
Jika reaksi mengikuti ordo reaksi nol, maka umur simpan
dapat diperoleh dengan menggunakan rumus :
Keterangan :
t = prediksi umur simpan (hari)
Ao = nilai mutu awal
At = nilai mutu produk yang tersisa setelah waktu t
ko = konstanta
Dari rumus di atas dapat diprediksi umur simpan dalam hari
21 3. Analisis Total Bakteri (Fardiaz, 1992)
Pengukuran dilakukan dengan pencawanan sampel minuman
hasil sterilisasi 121 oC pada lama pemanasan 10 menit dan 15 menit dengan kontrol sampel minuman yang tidak disterilisasi pada media agar
yaitu Nutrient Agar (NA). Sampel dimasukkan pada cawan petri steril
dengan beberapa pengenceran. Setiap pengenceran digunakan dua cawan
(duplo). Selanjutnya, media NA steril yang suhunya 47-50 oC dituang ke dalam cawan sebanyak 10-15 mL. Kemudian, digoyang mendatar di atas
meja supaya contoh menyebar rata. Setelah agar membeku, cawan
diinkubasi dengan posisi terbalik pada suhu 30 oC selama 2 hari. Total bakteri ditentukan dengan Standard Plate Count (SPC).
4. Analisis Kadar Klorofil (Gross, 1991)
Analisis kadar klorofil terdiri dari dua tahap yaitu analisis kadar
klorofil ekstrak dan analisis kadar klorofil minuman.
a. Kadar Klorofil Ekstrak
Pengukuran dilakukan dengan mengambil sejumlah ekstrak
(1.5 mL) yang dicampur dengan 8.5 mL aseton 99.5%. Selanjutnya
dibiarkan selama satu malam dalam refrigerator. Kemudian campuran
disentrifugasi pada 3000 rpm selama 10 menit. Absorbansi supernatan
diukur pada 645 nm dan 663 nm.
Total Klorofil (mg/L) = 20.2 A645 nm + 8.02 A663 nm
b. Kadar Klorofil Minuman
Pengukuran dilakukan dengan mengambil sejumlah sampel
minuman (1.5 mL) dan SSC 500 ppm (0.5 mL) yang dicampur dengan
11.2 mL aseton 99.5%. Selanjutnya dibiarkan selama satu malam dalam
refrigerator. Larutan blanko yang digunakan adalah 1.5 mL akuades
sebagai pengganti larutan sampel. Kemudian, campuran disentrifugasi
22 pengukuran langsung terhadap absorbansi supernatan pada 645 nm dan
663 nm.
Total Klorofil(mg/L)=20.2ASampel-Blanko645nm+8.02ASampel-Blanko663nm
5. Analisis Total Polifenol (Metode Folin-Denis) (Prangdimurti et al., 2009)
Minuman dengan formula optimal digunakan sebagai sampel
pengujian total polifenol. Asam tanat digunakan sebagai standar. Hasil
pengukuran total polifenol minuman kemudian dihitung berdasarkan
kesetaraannya dengan total polifenol pada asam tanat yang dinyatakan
dalam ppm TAE (Tannic Acid Equivalen). Secara spesifik, metode
pengukuran total polifenol dapat dilihat pada Gambar 3.
Diambil 1 ml sampel (diencerkan 2-4 kali dengan aquades)
Ditambah pereaksi Folin-Dennis sebanyak 1 ml
Diinkubasi dalam ruang gelap suhu kamar selama 5 menit
Ditambah 0.25 ml larutan Na2CO3 (60 g/L) dan 1.75 ml aquades
Diinkubasi sampel dalam ruang gelap suhu kamar selama 30 menit
Dibaca absorbansi sampel dengan spektrofotometer pada λ = 760 nm
Gambar 3. Diagram alir analisis total polifenol
6. Analisis Aktivitas Antioksidan (Kubo et. al., 2002)
Pengukuran dengan menggunakan buffer asetat 100 mM (pH
5.5), 1.87 ml metanol, dan 0.1 mL radikal bebas DPPH 3 mM dalam
metanol yang dimasukkan ke dalam tabung reaksi. Larutan DPPH dibuat
segar setiap akan digunakan. Selanjutnya, sebanyak 0.03 mL larutan
sampel ditambahkan ke dalam tabung tersebut dan diinkubasi 25 oC selama 20 menit. Larutan blanko yang digunakan adalah 0.03 mL metanol
23 517 nm. Absorbansi menunjukkan adanya aktivitas scavenging atau
aktivitas antioksidan. Pembuatan kurva standar menggunakan asam
askorbat. Dengan demikian, satuan pengukuran dapat dinyatakan sebagai
Absorbic acid Equivalent Antioxidant Capacity (AEAC).
[
24 IV. HASIL DAN PEMBAHASAN
A. PENELITIAN PENDAHULUAN
1. Penentuan Jumlah Cu2+ pada Ekstrak Daun Suji
Pengekstrakan daun suji diawali dengan pengambilan daun suji
segar yang selanjutnya diekstraksi dengan menggunakan NaHCO3 pada
konsentrasi 0.5 %. Menurut Rufaida (2008), pada pengekstrak NaHCO3
dengan konsentrasi 0.5 % memiliki kadar total klorofil yang optimum.
Dengan demikian, pengekstrakan klorofil dilakukan dengan NaHCO3 0.5 %.
Setelah mendapatkan hasil ekstrak dengan penambahan NaHCO3 maka
dilakukan penentuan jumlah Cu2+ untuk mendapatkan nilai aktivitas antioksidan dan kadar klorofil terbaik. Penggunaan ion Cu2+ pada ekstrak daun suji bertujuan untuk memperoleh warna hijau yang stabil dan
meningkatkan aktivitas antioksidan klorofil. Cu merupakan antioksidan
oligoelemen yang merupakan kofaktor enzim-enzim yang dapat
mendegradasi senyawa-senyawa reactive oxygen species (ROS) (Muchtadi,
2000).
Penentuan kadar klorofil dengan spektrofotometer merupakan cara
paling umum yang digunakan. Menurut Prangdimurti et al., (2006), hasil
pengukuran dengan spektrofotometer diperoleh rata-rata kadar total klorofil
dari daun suji segar dengan larutan pengekstrak NaHCO3 0.5 % sebesar
2.575 ± 0.016 mg/10 ml. Kadar total klorofil menunjukkan hasil yang lebih
besar nilainya dibandingakn dengan pengukuran peneliti sebelumnya. Hal
ini dapat disebabkan oleh konidsi daun yang digunakan berbeda dengan
peneliti sebelumnya sehingga total klorofil yang didapatkan cukup tinggi.
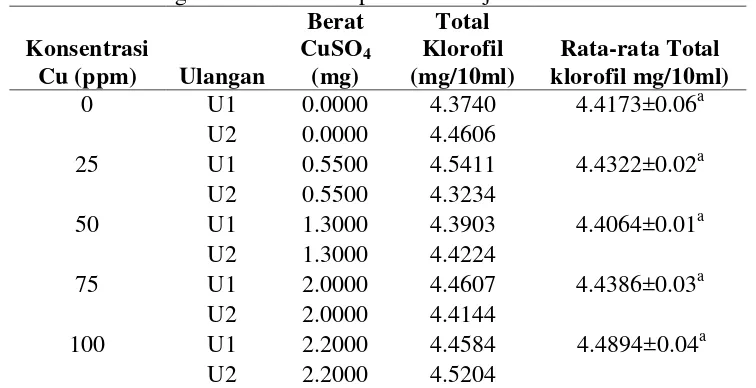
Hasil analisis total klorofil dapat dilihat pada Tabel 4.
Berdasarkan analisis varian (ANOVA) menunjukkan bahwa
ekstrak klorofil daun suji dengan penambahan Cu pada konsentrasi 0 ppm,
25 ppm, 50 ppm, 75 ppm, dan 100 ppm tidak berpengaruh nyata terhadap
kadar total klorofil (p<0.05) (Lampiran 1). Dengan uji lanjut Duncan,
25 menunjukkan nilai tidak berbeda nyata kadar total klorofilnya (Lampiran 2).
Hal ini menunjukkan bahwa pada berbagai konsentrasi Cu yang digunakan
terlihat nilai total klorofil yang hampir sama, sehingga penambahan Cu
tidak memberikan pengaruh terhadap peningkatan atau penurunan kadar
klorofil.
Tabel 4. Data tingkat kadar klorofil pada daun suji
Konsentrasi
Pada analisis antioksidan dilakukan penentuan kurva standar
terlebih dahulu. Kurva standar menggunakan asam askorbat. Konsentrasi
yang digunakan untuk mendapatkan kurva standar asam askorbat yaitu
menggunakan dari 0 ppm sampai 1000 ppm agar mendapatkan rentang nilai
yang luas. Dari kurva standar asam askorbat didapatkan persamaan y =
0.0005x + 0.001 (Lampiran 4). Hasil perhitungan aktivitas antioksidan
menunjukkan semakin tinggi jumlah konsentrasi Cu yang digunakan
semakin kecil nilai antioksidan.
Berdasarkan analisis varian (ANOVA) menunjukkan bahwa
ekstrak klorofil daun suji dengan penambahan Cu pada konsentrasi 0 ppm,
25 ppm, 50 ppm, 75 ppm, dan 100 ppm berpengaruh sangat nyata terhadap
aktivitas antioksidan (p<0.05) (Lampiran 6). Pada penggunaan Cu 0 ppm
tidak berbeda nyata dengan 25 ppm dan penggunaan Cu 25 ppm tidak
26 nyata dengan 100 ppm. Hal ini ditunjukkan pada Tabel 5. Penggunaan Cu
memberikan penurunan terhadap aktivitas antioksidan. Hal ini dapat
disebabkan oleh kelebihan Cu yang digunakan. Cu bebas yang terionisasi di
dalam ekstrak klorofil menurunkan aktivitas antioksidan karena atom Cu
bersifat sebagai oksidator.
Dengan demikian, tujuan penggunaan Cu hanya tercapai untuk
stabilnya warna. Warna hijau yang dihasilkan pada berbagai konsentrasi
hampir sama. Hal ini terlihat dari kadar klorofil yang tidak berbeda nyata.
Pada penentuan aktivitas antioksidan, menunjukkan penurunan sehingga
tujuan penambahan Cu untuk meningkatkan aktivitas antioksidan tidak
tercapai. Selain itu, pada ekstrak klorofil yang tidak ditambahkan Cu
memiliki nilai aktivitas antioksidan tertinggi. Oleh karena itu, selanjutnya
ekstrak klorofil yang digunakan untuk pembuatan minuman tidak dilakukan
penambahan Cu.
Tabel 5. Data aktivitas antioksidan pada daun suji
27 1 : 100 (b/v), dan 1.25 : 100 (b/v). Air seduhan kemudian disaring dan
diambil filtratnya.
Penentuan total polifenol (Metode Folin-Denis) digunakan kurva
standar asam tanat. Konsentrasi yang digunakan untuk mendapatkan kurva
standar asam tanat yaitu menggunakan dari 0 ppm sampai 50 ppm agar
mendapatkan rentang nilai yang luas sesuai dengan nilai yang diharapkan.
Dari kurva standar asam tanat didapatkan persamaan y = 0.0013x - 0.007
(Lampiran 8). Hasil perhitungan total fenol menunjukkan semakin tinggi
jumlah teh yang digunakan semakin besar total fenol.
Berdasarkan analisis varian (ANOVA) menunjukkan bahwa total
fenol pada perbandingan 0,75 : 100 (b/v), 1 : 100 (b/v), dan 1,25 : 100 (b/v)
berpengaruh nyata terhadap total fenol (p<0.05) (Lampiran 10). Pada
perbandingan 0,75 : 100 (b/v) berbeda nyata pada semua perbandingan dan
1 : 100 (b/v) dengan 1,25 : 100 (b/v) tidak berbeda nyata. Hal ini
ditunjukkan pada Tabel 6.
Tabel 6. Data tingkat total fenol pada teh
Berat teh
(gram) Ulangan Absorbansi
Total Fenol
Pada analisis antioksidan dilakukan penentuan kurva standar
terlebih dahulu. Kurva standar menggunakan asam askorbat. Konsentrasi
yang digunakan untuk mendapatkan kurva standar asam askorbat yaitu
menggunakan dari 0 ppm sampai 1000 ppm agar mendapatkan rentang nilai
yang luas. Dari kurva standar asam askorbat didapatkan persamaan y =
28 menunjukkan semakin tinggi jumlah teh hijau yang digunakan semakin
besar aktivitas antioksidan.
Berdasarkan analisis varian (ANOVA) menunjukkan bahwa
penggunaan jumlah teh pada perbandingan 0,75 : 100 (b/v), 1 : 100 (b/v),
dan 1,25 : 100 (b/v) berpengaruh nyata terhadap aktivitas antioksidan
(p<0.05) (Lampiran 14). Pada perbandingan 0,75 :100 (b/v) tidak berbeda
nyata dengan perbandingan 1 : 100 (b/v) dan perbandingan 1 : 100 (b/v)
tidak berbeda nyata dengan perbandingan 1,25 : 100 (b/v). Hal ini
ditunjukkan pada Tabel 7.
Tabel 7. Data aktivitas antioksidan pada seduhan teh hijau
Berat
Dengan demikian, diketahui bahwa jumlah teh pada perbandingan
1,25 : 100 (b/v) memiliki total fenol tertinggi dan aktivitas antioksidan
tertinggi. Oleh karena itu, formulasi minuman akan menggunakan
perbandingan 1,25 : 100 (b/v).
B. PENELITIAN UTAMA
1. Formulasi Minuman Teh Hijau Berklorofil
Tahapan formulasi dilakukan dengan pengujian organoleptik agar
dapat diterima oleh konsumen dan analisis aktivitas antioksidannya.
Formulasi minuman menggunakan gula atau pemanis untuk
29 minuman. Penggunaan gula pasir 12 % sesuai dengan kebiasaan minuman
yang dikonsumsi oleh orang Indonesia.
Asam sitrat berfungsi sebagai penegas rasa dan warna serta
menyelubungi after taste yang tidak disukai. Selain itu, sifat sinergisnya
terhadap antioksidan dalam mencegah ketengikan dan browning. Dengan
penurunan pH, maka suhu sterilisasi yang dibutuhkan juga akan lebih
rendah dan kemungkinan tumbuhnya mikroba berbahaya akan lebih kecil
(Winarno, 1992). Menurut Furia (1981), asam sitrat serta garam natrium dan
kalsium sitrat diklasifikasikan oleh FDA (Food and Drug Administration)
sebagai GRAS (Generally Recognized As Safe).
CMC (Carboxy Methyl Celllose) adalah zat penstabil dalam
pembuatan minuman. CMC merupakan turunan selulosa yang sering dipakai
dalam industri makanan untuk mendapatkan tekstur yang baik. Karena
CMC mempunyai gugus karbonil, maka viskositas larutan CMC
dipengaruhi oleh pH larutan. pH optimum adalah 5 dan jika pH terlalu
rendah yaitu di bawah 3 maka CMC akan mengendap (Winarno, 1992).
Setelah melakukan proses formulasi maka dapat dilakukan
pengujian organoleptik. Uji organoleptik terhadap produk minuman
dilakukan setelah tahap deaerasi pertama. Uji organoleptik yang dilakukan
adalah uji hedonik (kesukaan). Uji ini dilakukan untuk mengukur
penerimaan atau kesukaan panelis terhadap suatu produk. Pada uji ini
panelis diminta mengungkapkan tanggapan pribadinya terhadap skor warna,
rasa, aroma, dan over all berdasarkan intensitas kesukaannya. Penyajian
dilakukan satu persatu tanpa melakukan perbandingan antar sampel tetapi
merupakan respon spontan terhadap kesukaan produk yang diuji. Format
contoh penilaian uji hedonik dapat dilihat pada Lampiran 15.
Hasil organoleptik aroma menunjukkan ketiga sampel yaitu
penambahan ekstrak klorofil 10 % (v/v), 20 % (v/v), dan 30 % (v/v)
memiliki skor yang sama sebesar 2,9 (Lampiran 16). Hal ini dapat diketahui
bahwa panelis memiliki tingkat kesukaan menuju netral. Berdasarkan
30 Hasil organoleptik rasa menunjukkan ketiga sampel yaitu
penambahan ekstrak klorofil 10 % (v/v), 20 % (v/v), dan 30 % (v/v)
memiliki skor yang hampir sama sebesar 3,4 sampai 3,6 (Lampiran 18). Hal
ini dapat diketahui bahwa panelis memiliki tingkat kesukaan menuju suka.
Berdasarkan analisis varian (ANOVA) dapat disimpulkan bahwa rasa ketiganya tidak berbeda nyata pada taraf α = 0.05 (Lampiran 19).
Hasil organoleptik warna menunjukkan ketiga sampel yaitu
penambahan ekstrak klorofil 10 % (v/v), 20 % (v/v), dan 30 % (v/v)
memiliki tingkat kesukaan menuju suka. Berdasarkan analisis varian
(ANOVA) dapat disimpulkan bahwa warna ketiganya tidak berbeda nyata pada taraf α = 0.05 (Lampiran 21).
Hasil organoleptik overall menunjukkan ketiga sampel yaitu
penambahan ekstrak klorofil 10 % (v/v), 20 % (v/v), dan 30 % (v/v)
memiliki tingkat kesukaan menuju suka. Berdasarkan analisis varian
(ANOVA) dapat disimpulkan bahwa overall ketiganya tidak berbeda nyata pada taraf α = 0.05 (Lampiran 23).
Penambahan ekstrak klorofil pada 10 % (v/v), 20 % (v/v), dan 30
% (v/v) tidak berbeda nyata hasil organoleptiknya. Sehingga pengujian
selanjutnya dilihat aktivitas antioksidan terbaik dari ketiga sampel untuk
dijadikan formula terbaik.
Pada analisis antioksidan dilakukan penentuan kurva standar
terlebih dahulu. Kurva standar menggunakan asam askorbat. Konsentrasi
yang digunakan untuk mendapatkan kurva standar asam askorbat yaitu
menggunakan dari 0 ppm sampai 2000 ppm agar mendapatkan rentang nilai
yang lebih luas. Dari kurva standar asam askorbat didapatkan persamaan y =
0.0008x + 0.034 (Lampiran 25). Hasil perhitungan aktivitas antioksidan
menunjukkan semakin tinggi jumlah penambahan ekstrak klorofil yang
digunakan semakin besar aktivitas antioksidan .
Berdasarkan analisis varian (ANOVA) menunjukkan bahwa
penambahan ekstrak klorofil pada 10 % (v/v), 20 % (v/v), dan 30 % (v/v)
berpengaruh nyata terhadap aktivitas antioksidan (p<0.05) (Lampiran 27).
31 penambahan 20 % (v/v) dan perbandingan 30 % (v/v) berbeda nyata pada
sampel lainnya. Hal ini ditunjukkan pada Tabel 8.
Tabel 8. Data aktivitas antioksidan pada minuman teh hijau dengan penambahan ekstrak klorofil
Persentase
Dengan demikian, diketahui bahwa penambahan ekstrak klorofil 30
% (v/v) memiliki aktivitas antioksidan tertinggi dan secara organoleptik
tidak berbeda nyata dengan sampel lainnya. Oleh karena itu, minuman yang
akan dibotolkan adalah formula III dengan formulasi penambahan ekstrak
klorofil 30 %.
2. Pengemasan dengan Pembotolan
Pembuatan minuman dilakukan dengan menggunakan formula
ketiga. Minuman yang telah jadi selanjutnya dilakukan pengemasan dengan
pembotolan. Pengemasan dengan pembotolan dilakukan pada dua waktu
sterilisasi yaitu pada 10 menit dan 15 menit dengan suhu 121 oC. Minuman yang telah dibotolkan dan disterilisasi akan dianalisis total bakterinya. Pada
proses sterilisasi diharapkan dapat menghancurkan mikroba pembusuk dan
patogen yang terdapat dalam pangan. Jumlah total bakteri pada waktu
sterilisasi 10 menit dengan suhu 121 oC sebesar kurang dari 2,5 x 102. Jumlah total bakteri pada waktu sterilisasi 15 menit dengan suhu 121 oC