TETRAPLOIDISASI IKAN PATIN SIAM
(
Pangasianodon hypophthalmus)
DENGAN KEJUTAN SUHU
PANAS
AGUSTINA BUULOLO
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa tesis berjudul “Tetraploidisasi Ikan Patin Siam (Pangasianodon hypophthalmus) dengan Kejutan Suhu Panas’’ adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, November 2016
RINGKASAN
AGUSTINA BUULOLO. Tetraploidisasi Ikan Patin Siam (Pangasianodon
hypophthalmus) dengan Kejutan Suhu Panas. Dibimbing oleh ODANG
CARMAN dan DINAR TRI SOELISTYOWATI.
Ikan patin siam (Pangasianodon hypophthalmus) adalah salah satu komoditas ikan air tawar yang bernilai ekonomis tinggi, prospektif dikembangkan untuk memenuhi permintaan pasar domestik yang selalu meningkat setiap tahun. Spesies ini berasal dari sungai Mekong Vietnam atau sungai Chao Phraya Thailand, menyebar ke beberapa negara seperti Malaysia, Indonesia dan Cina (Ahmed dan Hasan 2007). Ikan ini diintroduksi masuk ke Indonesia pada tahun 1972 dikenal dengan nama Lele Bangkok (Sunarma 2007). Budidaya ikan patin tergolong inefisien karena biaya operasional produksi tinggi yang tidak sebanding dengan harga jual produk yang salah satunya diakibatkan oleh lambatnya pertumbuhan ikan. Perbaikan pertumbuhan di antaranya dapat dilakukan dengan memproduksi ikan triploid yang bersifat steril karena energi reproduksi dapat dialihkan pada pertumbuhan somatik sehingga pertumbuhannya lebih cepat.
Produksi triploid dalam budidaya sangat penting dilakukan dan diharapkan mampu meningkatkan efisiensi produksi. Individu tetraploid dapat dibuat melalui penghambatan pembelahan sel pertama (mitosis I) dengan induksi kejutan suhu panas (heat shock), kejutan dingin (cold shock) atau tekanan (hydrostatic pressure) maupun bahan kimia berupa colchicine, cytochalacin dan vincristine. Metode kejutan suhu panas (heat shock) adalah salah satu metode paling murah dan mudah, keberhasilannya dipengaruhi oleh umur zigot, intensitas perlakuan suhu kejutan dan lama pemberian kejutan (Herbst 2002; Shelton 2006). Induksi tetraploid dengan heat shock dilakukan setelah fertilisasi sebelum pembelahan sel pertama (Fitria et al.2013) dan terjadi karena adanya penekanan pembelahan sel (Zhang et al. 2007). Tetraploidisasi diharapkan dapat menyediakan induk tetraploid untuk produksi massal triploid.
Penelitian ini terdiri dari enam perlakuan dengan tiga ulangan yaitu (A) perlakuan kejutan suhu 42 ᴼC pada umur zigot 28 menit setelah fertilisasi (msf) selama 2,0 menit dan (B) selama 2,5 menit, (C) perlakuan kejutan suhu 42 ᴼC pada umur zigot 30 msf selama 2,0 menit dan (D) selama 2,5 menit, (E) perlakuan kejutan suhu 42 ᴼC pada umur zigot 32 msf selama 2,0 menit dan (F) selama 2,5 menit. Dibuat juga kontrol sebagai pembanding tanpa perlakuan kejutan. Hasil penelitian menunjukkan bahwa tetraploidisasi ikan patin siam Pangasianodon hypophthalmus melalui kejutan suhu panas 42 ᴼC selama 2,0 dan 2,5 menit pada umur zigot 30 msf berhasil menginduksi ikan tetraploid. Kondisi optimum yang dapat menghasilkan tetraploid tertinggi (26,67%) dengan kelangsungan hidup 40,17% adalah kejutan suhu 42 ᴼC selama 2,5 menit pada umur zigot 30 msf.
SUMMARY
AGUSTINA BUULOLO. Tetraploidization of Stripped Catfish
Pangasianodon hypophthalmus using Heat Shock. Supervised by ODANG
CARMAN and DINAR TRI SOELISTYAWATI.
Stripped catfish (Pangasianodon hypophthalmus) is one of the freshwater fish that have highly economic value, prospectively to be developed to meet yearly increasing domestic market demand. this species originated from Mekong river Vietnam or Chao Phraya river Thailand, than distributed to several countries such as Malaysia, Indonesia and China (Ahmed and Hasan 2007). This fish was introduced into Indonesia in 1972 known as Lele Bangkok (Sunarma 2007). Culture of this species was inefficien due to high operational production costs which unbalance compared to the selling price caused by the low growth rate of the fish. The low growth rate can be improved by producing a sterile triploid fish as the reproductive energy can be allocated for somatic growth so that higher growth rate will be achieved.
Triploid production in aquaculture is very important to be developed and it is expected to improve production efficiency. Tetraploid individuals can be induced through the suppression of the firs cell division (mitosis I) using heat shock, cold shock or hydrostatic pressure as well as chemicals such as colchicine, cytochalacin and vincristine. The heat shock treatment is one of the most inexpensive and convenient method, while the success is influenced by zygote's age, temperature shock and duration of the shock treatment (Herbst 2002; Shelton 2006). Tetraploid induction using heat shock is applied after fertilization before the first mitosis (Fitria et al. 2013) and occurs because of the suppression of the cell division (Zhang et al. 2007). Tetraploidization is expected can provide tetraploid broodstock for triploid mass production.
This study consisted of six treatments with three replicates, namely (A) heat shock at 42 ᴼC, 28 minutes after fertilization the (maf) for 2.0 minutes and (B) for 2.5 minutes, (C) heat shock at 42 ᴼC, 30 maf for 2.0 minutes and (D) for 2.5 minutes, (E) heat shock at 42 ᴼC, 32 maf for 2.0 minutes and (F) for 2.5 minutes. A group of untreated zygotes were also produce as control. The results showed that tetraploidization of stripped catfish Pangasianodon hypophthalmus using heat shock treatments at 42 ᴼC for 2.0 minutes and 2.5 minutes at 30 maf of zygote successfully induced tetraploid fish. The highest tetraploid percentage (26.67%) with 40.17% of survival rate was achieved when heat shock treatment at 42 ᴼC for 2.5 minutes at 30 maf was applied.
© Hak Cipta Milik IPB, Tahun 2016
Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan IPB
TETRAPLOIDISASI IKAN PATIN SIAM
(
Pangasianodon hypophthalmus
) DENGAN KEJUTAN SUHU
PANAS
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
BOGOR
2016
AGUSTINA BUULOLO
Tesis
sebagai salah satu syarat untuk memperoleh gelar Magister Sains
ii
iii Judul Tesis : Tetraploidisasi Ikan Patin Siam (Pangasianodon hypophthalmus)
Dengan Kejutan Suhu Panas Nama : Agustina Buulolo
NIM : C151140431
Disetujui oleh
Komisi Pembimbing
Dr Ir Odang Carman, MSc Ketua
Dr Ir Dinar Tri Soelistyowati, DEA Anggota
Diketahui oleh
Ketua Program Studi Ilmu Akuakultur
Dr Ir Widanarni, MSi
Dekan Sekolah Pascasarjana
Dr Ir Dahrul Syah, MScAgr
iv
PRAKATA
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Esa atas segala karunia dan berkah-Nya sehingga serangkaian karya ilmiah yang berjudul
“Tetraploidisasi ikan Patin Siam (Pangasianodon hypophthalmus) Dengan Kejutan Suhu Panas” ini dapat diselesaikan dengan baik.
Terima kasih penulis ucapkan dengan hormat kepada Dr Ir Odang Carman, MSc dan Dr Ir Dinar Tri Soelistyowati, DEA selaku pembimbing yang telah banyak memberikan arahan dan masukan baik tekhnis maupun non tekhnis kepada penulis sehingga karya ilmiah ini dapat diselesaikan. Terimakasih juga penulis ucapkan kepada Dr Dinamella Wahjuningrum SSi, MSi selaku dosen penguji luar komisi pada ujian tesis, atas segala saran yang diberikan sehingga tesis ini menjadi lebih baik.
Penulis juga mengucapkan terima kasih dan rasa hormat kepada ayahanda Demikian Buulolo serta ibunda Ferimawati Halawa dan juga adik-adik Nasib Niat Buulolo Amd Keb, Juliaman Buulolo S.Kep, Suryani Buulolo, dan Krismaryani Buulolo beserta keluarga besar atas segala dukungan, kesabaran, pengertian, doa dan kasih sayangnya selama penulis menjalani masa studi.
Ucapan terima kasih tak lupa penulis sampaikan kepada rekan rekan yang selama masa studi dapat menjadi motivasi dan memberikan pengaruh yang positif bagi penulis; Jannesa Nasmi MSi; Anny Hariayu SPi; Rozana MSi; Liling Palinggi SKel; Shella Marlinfa MSi; Asih Makarti MSi, Teman-teman peneliti di Cijengkol; Nunun Ainun Sari Banun Kaliki Ssi, Dr Cut Tara Dewi MSi; Yusran Ibrahim MSi dan para tenaga tekhnis lapangan Balai Pengembangan Budidaya Ikan Patin dan Lele (BPBIPL) Cijengkol, Provinsi Jawa Barat yang namanya tidak disebutkan satu persatu; keluarga besar Program Studi Ilmu Akuakultur yang tidak bisa disebutkan satu persatu, teman-teman di Wisma Kartika (Rozana MSi; Nuraini MSi, calon Drh Vicho permata kasih putri, Christy Lopulisa SPi, Lusiani ST, dan keluarga besar Ikatan Mahasiswa Kepulauan Nias (IMKN) IPB, serta ucapan terima kasih yang sebesar-besarnya kepada Politeknik Pertanian Payakumbuh selaku penjamin biaya perkuliahan melalui dana DIPA di Institut Pertanian Bogor untuk staf pengajar tetap di Akademi Komunitas Kabupaten Nias Utara.
Semoga karya ilmiah ini bermanfaat.
Bogor, November 2016
v
DAFTAR ISI
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN vii
1 PENDAHULUAN 1
Latar Belakang 1
Rumusan Masalah 2
Tujuan 2
Hipotesis 2
2 METODE 2
Waktu dan Tempat 2
Rancangan Percobaan 3
Pelaksanaan Penelitian 3
Pemijahan Induk 3
Kejutan Suhu 4
Identifikasi Tetraploid 4
Parameter Uji 5
Persentase Tetraploid 5
Derajat Pembuahan (DPh) 5
Derajat Penetasan (DPt) 6
Tingkat Kelangsungan Hidup (TKH) 6
Analisis Data 6
3 HASIL DAN PEMBAHASAN 7
Hasil 7
Derajat pembuahan (DPh) dan Derajat Penetasan (DPt) 7
Tingkat Kelangsungan Hidup (TKH) 8
Keberhasilan tetraploidisasi 8
Pembahasan 9
4 SIMPULAN DAN SARAN 12
Simpulan 12
Saran 12
DAFTAR PUSTAKA 13
LAMPIRAN 15
RIWAYAT HIDUP 20
vi
DAFTAR GAMBAR
1. Skema induksi tetraploid pada ikan (Herbst 2002) 2 2. Proses penyuntikan (a), koleksi sperma (b), stripping telur (c), proses
membuahi telur (d), menghilangkan daya rekat telur dengan suspensi
tanah (e) dan pembilasan telur (f) 3
3. Proses Kejutan suhu (a) corong penetasan (b) dan toples wadah
pemeliharaan (d) 4
4. Proses identifikasi tetraploid dengan analisis nukleus 5 5. Derajat penetasan ikan patin pada semua perlakuan dan kontrol 7 6 Tingkat kelangsungan hidup larva ikan patin selama 15 hari
pemeliharaan pada semua perlakuan dan kontrol. 8 7. Persentas tetraploid ikan patin yang dihasilkan dengan kejutan suhu
42 ᴼC pada umur zigot dan lama kejutan yang berbeda 9 8. Sel ikan patin diploid dengan jumlah maksimum 2 nukleolus per sel
(tanda panah, a) dan ikan patin tetraploid dengan jumlah maksimum 4
nukleolus (tanda panah, b) 9
DAFTAR LAMPIRAN
1 PENDAHULUAN
Latar Belakang
Ikan patin siam (Pangasianodon hypophthalmus) adalah salah satu komoditas ikan air tawar yang bernilai ekonomis prospektif dikembangkan untuk memenuhi permintaan pasar domestik yang selalu meningkat setiap tahun. Spesies ini berasal dari sungai Mekong Vietnam atau sungai Chao Phraya Thailand, menyebar ke beberapa negara seperti Malaysia, Indonesia dan Cina (Ahmed dan Hasan 2007). Ikan ini diintroduksi masuk ke Indonesia pada tahun 1972 dikenal dengan nama Lele Bangkok (Sunarma 2007). Budidaya ikan patin tergolong inefisien karena biaya operasional produksi tinggi yang tidak sebanding dengan harga jual produk yang salah satunya diakibatkan oleh lambatnya pertumbuhan ikan. Menurut Widodo et al. (2010) ikan patin dari bobot 7,4 g membutuhkan waktu pemeliharaan 8-9 bulan untuk mencapai ukuran filet yaitu bobot 600-700 g. Perbaikan pertumbuhan di antaranya dapat dilakukan dengan memproduksi ikan triploid karena bersifat steril dan energi reproduksi dapat dialihkan pada pertumbuhan somatik sehingga pertumbuhannya lebih cepat. Triploidisasi dapat dilakukan dengan persilangan antara diploid (2n) dengan tetraploid (4n) sehingga dihasilkan ikan triploid (3n) secara massal. Sterilitas pada ikan triploid berhubungan dengan tidak berkembangnya gonad yang disebabkan kromosom homolog tidak bersinapsis.
Produksi triploid dalam budidaya sangat penting dilakukan dan diharapkan mampu meningkatkan efisiensi produksi. Individu tetraploid dapat dibuat melalui penghambatan pembelahan sel pertama (mitosis I) dengan ind uksi kejutan suhu panas (heat shock), kejutan dingin (cold shock) atau tekanan (hydrostatic pressure) maupun bahan kimia berupa colchicine, cytochalacin dan vincristine. Metode kejutan suhu panas (heat shock) adalah salah satu metode paling murah dan mudah, keberhasilannya dipengaruhi oleh umur zigot, intensitas perlakuan suhu kejutan dan lama pemberian kejutan (Herbst 2002; Shelton 2006). Induksi tetraploid dengan heat shock dilakukan setelah fertilisasi sebelum fase pembelahan sel pertama (mitosis I) (Fitria et al. 2013) dan terjadi karena adanya penekanan pembelahan sel (Zhang et al. 2007).
Keberhasilan induksi tetraploid melalui heat shock pada beberapa spesies ikan di antaranya; ikan Oncorhynchus mykiss diperoleh tetraploid 66,67% pada suhu kejut 28 ᴼC selama 15 menit setelah enam jam dibuahi (Bencsik et al. 2011) dan sebesar 100% ikan tetraploid didapatkan di ikan nila pada suhu kejut 41 ᴼC selama sembilan menit dengan umur zigot 17,5-22,5 menit setelah fertilisasi (Muller et al. 2004). Kejutan suhu 32 dan 35 ᴼC pada Crassostrea iredalei (Faustino), C. belcheri (Sowerby) menghasilkan individu tetraploid masing-masing sebesar 29,9% dan 25,7% selama 8-10 menit setelah pembuahan (Tan et al. 2016). Induksi tetraploid juga ditemukan pada perlak uan kejutan suhu 35 dan 36 ᴼC selama 5-10 menit dengan umur zigot 18-23 menit setelah pembuahan masing- masing 98,12% dan 61,02% (Sellars et al. 2006).
2
Gambar 1. Skema induksi tetraploid pada ikan (Herbst 2002)
Rumusan Masalah
Kepopuleran ikan patin terus meningkat setiap tahunnya baik dalam maupun luar negeri seiring dengan terus berkembangnya industrialisasi filet ikan. Namun, industri filet ikan mengalami inefisiensi biaya produksi di antaranya karena pertumbuhan ikan yang lambat. Ketersediaan ikan tetraploid diperlukan untuk memproduksi ikan triploid secara massal dengan performa pertumbuhan yang lebih baik dan filet yang berkualitas. Oleh karena itu, pengembangan protokol tetraploidisasi pada ikan patin perlu dilakukan.
Tujuan
Tujuan penelitian ini adalah mengevaluasi kondisi optimum tetraploidisasi pada ikan patin siam Pangasianodon hypophthalmus melalui kejutan pada suhu 42 ᴼC dengan lama kejut dan umur zigot yang berbeda.
Hipotesis
Hipotesis yang diajukan dalam penelitian ini adalah kejutan suhu pada 42
ᴼC dengan variabel lama kejut 2,0 dan 2,5 menit pada umur zigot 28, 30 dan 32 menit setelah fertilisasi akan mendapatkan salah satu kondisi terbaik dalam menginduksi tetraploid ikan patin siam (Pangasianodon hypophthalmus).
2 METODE
Waktu dan Tempat
3
Rancangan Percobaan
Penelitian ini dilakukan dengan metode eksperimental. Rancangan percobaan yang digunakan adalah Rancangan Acak Lengkap (RAL) One Way Anova dengan enam perlakuan dan tiga ulangan, yaitu :
(A) Perlakuan kejut suhu 42 ᴼC pada umur zigot 28 menit setelah fertilisasi (msf) selama 2,0 menit
(B) Perlakuan kejut suhu 42 ᴼC pada umur zigot 28 msf selama 2,5 menit (C) Perlakuan kejut suhu 42 ᴼC pada umur zigot 30 msf selama 2,0 menit (D) Perlakuan kejut suhu 42 ᴼC pada umur zigot 30 msf selama 2,5 menit (E) Perlakuan kejut suhu 42 ᴼC pada umur zigot 32 msf selama 2,0 menit (F) Perlakuan kejut suhu 42 ᴼC pada umur zigot 32 msf selama 2,5 menit (G) Kontrol sebagai pembanding tanpa perlakuan kejutan suhu.
Pelaksanaan Penelitian
Pemijahan Induk
Pemijahan dilakukan menggunakan induk betina umur 2,5 tahun dengan berat 3-6 kg ekor-1 dan induk jantan umur 2 tahun dengan berat 1,5-2 kg ekor-1
masing- masing 6 ekor. Gambar 2 berikut menjelaskan tentang proses pemijahan meliputi penyuntikan induk, koleksi sperma, stripping telur, proses pembuahan, penghilangan daya rekat telur menggunakan suspensi tanah, dan pembilasan telur.
Gambar 2 Proses penyuntikan (a), koleksi sperma (b), stripping telur (c), proses membuahi telur (d), menghilangkan daya rekat telur dengan suspensi tanah (e) dan pembilasan telur (f)
Proses pemijahan dilakukan dengan metode induced breeding yaitu melalui penyuntikan hormon HCG dan ovaprim. Penyuntikan dilakukan 2 kali pada induk betina; penyuntikan pertama menggunakan hormon HCG dosis 500 IU kg-1 induk, penyuntikan kedua dilakukan setelah 24 jam menggunakan ovaprim
(GnRH + anti dopamin) dosis 0,6 mL kg-1 induk, bersamaan dengan itu ovaprim
0,3 mL kg-1 induk disuntikkan pada jantan.
Selanjutnya ditunggu hingga induk betina ovulasi. Setelah induk betina ovulasi, sperma jantan ditampung dalam wadah dan diencerkan dengan 50 mL
a b
c
d e
4
b c
a
larutan NaCl 0,9%. Induk betina di-stripping dan telur diletakkan dalam mangkok kering dan bersih. Fertilisasi dilakukan secara buatan dengan mencampur sperma dan telur secara merata, di aktivasi dengan penambahan 200 mL air mineral selama 1 menit, dihilangkan daya rekat telurnya menggunakan suspensi tanah, kemudian dibilas dengan air bersih. Telur yang telah dibilas dikoleksi untuk dilakukan kejutan suhu.
Kejutan Suhu
Perlakuan kejut suhu panas dilakukan dengan cara merendam telur menggunakan saringan teh dalam wadah styrofoam berisi air bersuhu 42 ᴼC dengan lama perendaman dan umur zigot sesuai perlakuan. Kemudian telur diinkubasi dalam corong penetasan (hatching jar) pada suhu 28-29 ᴼC hingga menetas (20-22 jam). Pemeliharaan larva dilakukan dalam toples bervolume 20 L dengan kepadatan 200 ekor toples-1. Larva diberi naupli artemia setelah kuning
telur habis (30-36 jam) selama 5 hari dengan frekuensi 2 jam sekali. Umur larva 6-10 hari diberi cacing Tubifex 4 jam sekali dan pakan tepung (Feng Li) diberikan pada saat larva berumur 11-15 hari. Penghitungan jumlah nukleolus dilakukan untuk mengidentifikasi individu tetraploid pada akhir pemeliharaan. Parameter yang diamati selama penelitian adalah derajat pembuahan, derajat penetasan, kelangsungan hidup dan keberhasilan tetraploidisasi. Gambar 3 berikut menjelaskan tentang proses perlakuan kejutan suhu, penetasan dalam corong dan pemeliharaan larva.
Gambar 3 Proses kejutan suhu (a) corong penetasan (b) dan toples wadah pemeliharaan (d)
Identifikasi Tetraploid
5 berdiameter 1-2 cm. Gelas objek yang digunakan, sebelumnya telah direndam dalam etanol 96% selama dua jam. Pada setiap gelas objek, dibuat 2-3 buah ring, dikering- udarakan, lalu diwarnai menggunakan larutan A (10 gr AgNO3 dilarutkan
dalam 20 mL akuades) dan B (2 gr gelatin dalam 50 mL air hangat ditambah 50 mL larutan gliserin, dan pada setiap 10 mL ditambahkan 2 tetes asam formiat) masing- masing sebanyak 1 dan 2 tetes kemudian dicampur dan disebar menggunakan tusuk gigi. Langkah berikutnya, preparat dimasukkan ke dalam box staining bersuhu 45-50 ᴼC selama 25 menit hingga preparat berwarna kuning kecoklatan, seterusnya dibilas menggunakan akuades dan preparat diamati
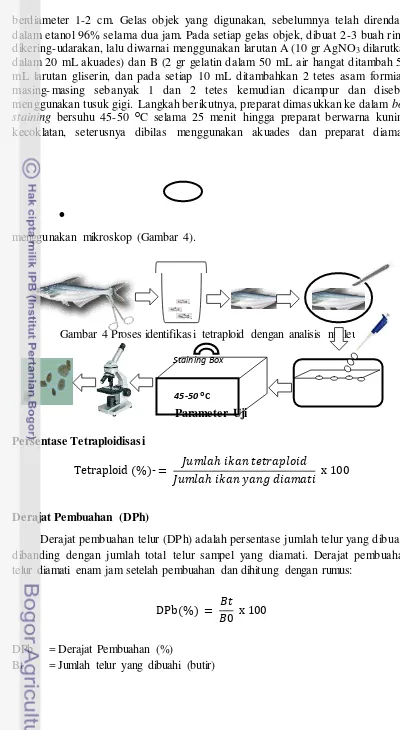
menggunakan mikroskop (Gambar 4).
Gambar 4 Proses identifikasi tetraploid dengan analisis nukleus
Parameter Uji
Persentase Tetraploidisasi
Tetraploid % - = � �ℎ � � �� �
� �ℎ � � �� � �� � � x
Derajat Pembuahan (DPh)
Derajat pembuahan telur (DPh) adalah persentase jumlah telur yang dibuahi dibanding dengan jumlah total telur sampel yang diamati. Derajat pembuahan telur diamati enam jam setelah pembuahan dan dihitung dengan rumus:
DPb % = �� x
DPb = Derajat Pembuahan (%)
Bt = Jumlah telur yang dibuahi (butir)
.
…
…
Staining Box
6
B0 = Jumlah telur sampel yang diamati (butir)
Telur yang terbuahi dapat dilihat dengan tidak adanya warna pada telur atau transparan, telur yang mati karena tidak terbuahi ditandai dengan warnanya yang putih keruh, sedangkan telur terbuahi tapi mati terlihat di bagian dalam telur terbentuk putih bercak-bercak.
Derajat Penetasan (DPt)
Derajat penetasan telur (DPt) adalah persentase jumlah telur yang menetas dibanding dengan jumlah total telur yang dibuahi. Derajat penetasan telur diamati 22 jam setelah terbuahi dihitung dengan rumus:
DPt % = �� x
DPt = Derajat Penetasan (%)
Tt = Jumlah telur yang menetas (ekor) T0 = Jumlah telur yang dibuahi (butir)
Tingkat Kelangsungan Hidup (TKH)
Tingkat kelangsungan hidup (TKH) selama pemeliharaan dihitung dengan melakukan sampling setiap 5 hari sekali sampai umur 15 hari dari jumlah total larva menetas. Pengamatan kelangsungan hidup ikan dilakukan pada fase benih. Tingkat kelangsungan hidup ikan dihitung dengan rumus berikut:
TKH
(%) =
NtNo
x 100
Keterangan :
TKH = Tingkat kelangsungan hidup (%)
Nt = Jumlah ikan hidup pada akhir pemeliharaan (ekor) N0 = Jumlah ikan hidup pada awal pemeliharaan (ekor)
Analisis Data
7
3 HASIL DAN PEMBAHASAN
Hasil
Derajat Pembuahan (DPh) dan Derajat Penetasan (DPt)
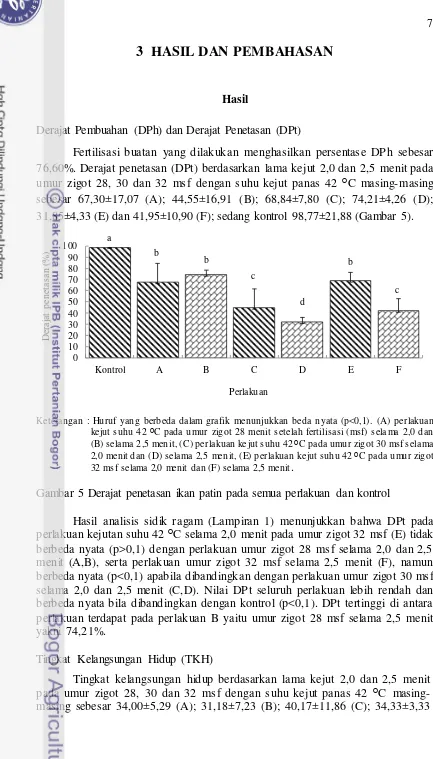
Fertilisasi buatan yang dilakukan menghasilkan persentase DPh sebesar 76,60%. Derajat penetasan (DPt) berdasarkan lama kejut 2,0 dan 2,5 menit pada umur zigot 28, 30 dan 32 msf dengan suhu kejut panas 42 ᴼC masing- masing sebesar 67,30±17,07 (A); 44,55±16,91 (B); 68,84±7,80 (C); 74,21±4,26 (D); 31,85±4,33 (E) dan 41,95±10,90 (F); sedang kontrol 98,77±21,88 (Gambar 5).
Keterangan : Huruf yang berbeda dalam gra fik menunjukkan beda nyata (p<0,1). (A) perlakuan berbeda nyata (p<0,1) apabila dibandingkan dengan perlakuan umur zigot 30 msf selama 2,0 dan 2,5 menit (C,D). Nilai DPt seluruh perlakuan lebih rendah dan berbeda nyata bila dibandingkan dengan kontrol (p<0,1). DPt tertinggi di antara perlakuan terdapat pada perlakuan B yaitu umur zigot 28 msf selama 2,5 menit yakni 74,21%.
Tingkat Kelangsungan Hidup (TKH)
8
(D); 29,33±2,36 (E) dan 39,17±5,20 (F); sedang kontrol 97,00±2,45. Berdasarkan analisis sidik ragam (Lampiran 2) menunjukkan bahwa TKH pada perlakuan kejutan suhu 42 ᴼC selama 2,0 menit pada umur zigot 32 msf (E) berbeda nyata (p<0,1) dengan perlakuan kejutan suhu 42 ᴼC selama 2,0 dan 2,5 menit baik pada umur zigot 28 maupun 30 msf (A,B; C,D), tetapi tidak berbeda nyata (p>0,1) dengan perlakuan kejutan suhu 42 ᴼC selama 2,5 menit pada umur zigot 32 msf (F). Sedangkan perlakuan kejutan suhu 42 ᴼC selama 2,0 menit pada umur zigot 30 msf (C) juga tidak berbeda nyata (p>0,1) dengan perlakuan kejutan suhu 42
ᴼC selama 2,0 dan 2,5 menit pada umur zigot 28 msf (A,B) dan umur zigot 32 menit selama 2,5 menit (F) serta umur zigot 30 menit selama 2,5 menit (D), namun berbeda nyata (p<0,1) apabila dibandingkan dengan perlakuan umur zigot 32 msf selama 2,0 menit (E). Selain itu nilai TKH pada semua perlakuan menunjukkan nilai yang lebih rendah dan berbeda nyata (p<0,1) bila dibandingkan dengan kontrol seperti terlihat pada (Gambar 6).
Keterangan : Huruf yang berbeda dalam grafik menunjukkan beda nyata (p<0,1). (A) perlakuan kejut suhu 42 ᴼC pada u mur zigot 28 menit setelah fe rtilisasi (msf) sela ma 2,0 men it dan (B) sela ma 2,5 menit, (C) perla kuan ke jut suhu 42 ᴼC pada u mur zigot 30 msf selama 2,0 menit dan (D) sela ma 2,5 menit, (E) perlakuan ke jut suhu 42 ᴼC pada umur zigot 32 msf selama 2,0 menit dan (F) selama 2,5 menit.
Gambar 6 Tingkat kelangsungan hidup larva ikan patin selama 15 hari pemeliharaan pada semua perlakuan dan kontrol.
Keberhasilan Tetraploidisasi
9
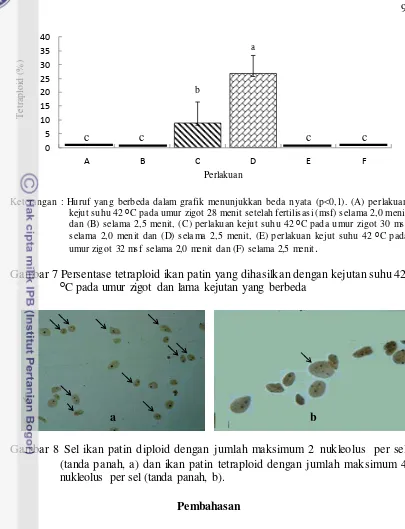
Keterangan : Huruf yang berbeda dalam gra fik menunjukkan beda nyata (p<0,1). (A) perlakuan kejut suhu 42 ᴼC pada umur zigot 28 menit setelah fertilisasi (msf) sela ma 2,0 menit dan (B) sela ma 2,5 menit, (C) perlakuan ke jut suhu 42 ᴼC pada u mur zigot 30 msf selama 2,0 menit dan (D) sela ma 2,5 menit, (E) perlakuan ke jut suhu 42 ᴼC pada umur zigot 32 msf selama 2,0 menit dan (F) selama 2,5 menit.
Gambar 7 Persentase tetraploid ikan patin yang dihasilkan dengan kejutan suhu 42
ᴼC pada umur zigot dan lama kejutan yang berbeda
Gambar 8 Sel ikan patin diploid dengan jumlah maksimum 2 nukleolus per sel (tanda panah, a) dan ikan patin tetraploid dengan jumlah maksimum 4 nukleolus per sel (tanda panah, b).
Pembahasan
10
msf menghasilkan derajat penetasan sebesar 75% (Gill et al. 2016). Perlakuan kejutan 40 ᴼC selama dua menit pada umur zigot 24 msf menghasilkan embrio menetas ikan Cyprinus carpio Linn sebesar 49,51% dan lebih rendah dibandingkan kontrol (Mustami 2013).
Rendahnya DPt ini diduga disebabkan efek pemberian kejutan suhu panas (heat shock) yang menyebabkan kerusakan membran pada embrio, kerusakan pada embrio yang sensitif terhadap perubahan suhu sehingga mengalami kerusakan fisik dan mengakibatkan gangguan pembelahan mitosis; merusak benang-benang spindel, terjadinya depolimerisasi tubulin dalam pembentukan benang-benang spindel, mengganggu aktivitas enzim, pengerasan korio n, dan hilangnya beberapa jumlah dan informasi genetik dalam kromosom (Gill et al. 2016; Nugraha et al. 2012; Solar et al. 1984; Chinjiang et al. 1986), sedangkan intensitas kejutan dan lama kejutan suhu pada telur dapat menimbulkan kematian yang tinggi (Solar et al. 1984). Penjelasan tambahan mengenai fenomena ini dikemukakan oleh Mair (1993) dan Tave (1985) bahwa kejutan panas juga dapat mengganggu aspek-aspek dalam embrio dan perkembangan dalam blastula pada embriogenesis dan beberapa embrio mati sebelum atau sesaat setelah menetas (Pandian dan Varadaraj 1990).
Walaupun demikian, sebagian embrio masih bertahan hidup karena air dalam rongga perivitelin masih mampu menyangga suhu air panas yang mulai masuk ke dalam embrio melalui osmosis (Sastrawibawa 1997). Hasil yang sama dilaporkan oleh Lebeda and Flajshans (2015) pada ikan Acipenser baerii dan Kumar and Hannifa (2012) pada ikan Cyprinus carpio L yang menyebutkan bahwa kejutan suhu mengakibatkan rendahnya DPt. Hal ini berkaitan dengan intensitas suhu kejutan dan lama kejutan yang diterima telur. Carman et al. (1991) menyebutkan bahwa perlakuan triploid dengan suhu kejutan panas 42 ᴼC selama 2,0 menit pada ikan maskoki menghasilkan persentase penetasan terendah, yaitu 13%. Berdasarkan uraian di atas, dapat dikemukakan bahwa selain efektif menginduksi tetraploid perlakuan kejutan suhu menyebabkan tingkat kematian yang cukup signifikan sebelum dan sesaat menjelang penetasan.
Beberapa penelitian mengenai tetraploid hasil induksi menunjukkan bahwa tingkat kelangsungan hidupnya normal. Dalam penelitian ini didapatkan bahwa ikan patin tetraploid memiliki kelangsungan hidup yang relatif sama dengan kontrol diploid, meskipun beberapa perlakuan menunjukkan hasil lebih rendah (Gambar 5). Rendahnya kelangsungan hidup ikan patin tetraploid besar dugaan disebabkan karena menurunnya daya tahan tubuh ikan terhadap kondisi lingkungan selama pemeliharaan. Selain itu, diduga karena terjadinya peningkatan jumlah dan ukuran sel yang mengakibatkan ikan tetraploid membutuhkan energi besar untuk proses metabolisme tubuh. Kebutuhan untuk metabolisme dan energi yang diperlukan ikan tetraploid lebih tinggi dari ikan diploid normal.
11 2006). Induksi tetraploid yang dihasilkan pada Oncorhynchus mykiss menunjukkan kelangsungan hidup sebesar 39,86% (Bencsik 2011) dan sebesar 40% untuk kelangsungan hidup Marsupenaeus japonicus (Sellars et al. 2006). Pada akhir pemeliharaan larva, perlakuan yang menghasilkan TKH tertinggi (40,17%) adalah perlakuan kejutan suhu 42 ᴼC selama 2,0 menit pada umur zigot 32 msf.
Hasil pengamatan nukleolus (Gambar 7) menunjukkan perbedaan warna antara nukleolus (anak inti) dengan nukleus (inti). Nukleus tampak berwarna kuning kecoklatan, sedangkan nukleolus berwarna hitam. Pada penelitian ini ditemukan adanya variasi jumlah nukleolus dalam setiap selnya. Menurut Carman et al. (1997) variasi jumlah tersebut ada hubungannya dengan kemampuan pewarna AgNO3 yang hanya mewarnai nukleolus (NORs/nucleoli organizer
regions) yang sedang aktif melakukan sintesis ribosom, dan jumlah maksimum nukleolus berkorelasi dengan level ploidi. Dengan kata lain, jumlah maksimum nukleolus pada diploid (2 nukleolus per sel) menunjukkan level ploidi 2n sedangkan jumlah maksimum nukleolus individu tetraploid (4 nukleolus per sel) menunjukkan level ploidi 4n.
Keberhasilan induksi tetraploid melalui kejutan suhu 42 ᴼC berdasarkan pengamatan jumlah nukleolus menunjukkan bahwa, ikan patin tetraploid dapat diinduksi melalui kejutan suhu panas meskipun dengan persentase yang berbeda, artinya perlakuan kejutan pada suhu tertentu mampu mencegah terjadinya fisi sel pada tahap mitosis, tidak mengakibatkan kematian total pada zigot dan kemudian dapat digunakan sebagai alternatif untuk menghasilkan induk tetraploid yang dapat digunakan dalam produksi triploid secara massal.
Umumnya keberhasilan persentase tetraploidisasi yang tinggi dari perlakuan kejutan suhu dan lama kejutan berbeda diikuti dengan rendahnya kelangsungan hidup ikan (Bencsik et al. 2011; Sellars et al. 2006; Sakao et al. 2006). Hasil yang didapat dalam penelitian ini (Gambar 5, 6 dan 8) mencerminkan kecenderungan yang sama. Rendahnya TKH menunjukkan pola yang serupa dengan rendahnya DPt dan menunjukkan bahwa selain mempengaruhi proses penetasan, kejutan suhu panas juga berpengaruh terhadap kemampuan larva untuk bertahan hidup.
Induksi tetraploidisasi pada spesies ikan berbeda telah berhasil dilakukan oleh beberapa peneliti seperti pada ikan Acipenser baerii (Lebeda and Flajshans 2015), Cyprinus carpio L (Kumar and Hannifa 2012), Mulinia lateralis Say (Yang et al. 2006), dan Danio rario (Herbst 2002). Keberhasilan tetraploidisasi pada ikan sangat ditentukan oleh faktor perlakuan kejutan suhu, lama kejutan dan umur zigot serta teknik untuk fertilisasi buatan dan didukung oleh kualitas air selama penanganan. Homogenitas perkembangan telur merupakan suatu syarat yang diduga sangat penting untuk keberhasilan perlakuan, sebab perkembangan telur secara merata akan menghasilkan masa pembelahan telur yang sama sehingga waktu pembelahan pun sama dan tetraploid yang dihasilkan tinggi. Selain itu kondisi ini juga akan berkaitan erat dengan aspek-aspek perkembangan blastula ikan.
12
keberhasilan perlakuan kejutan suhu sangat dipengaruhi oleh waktu awal kejut, suhu kejut dan lama kejut yang diterapkan (Don dan Avtalion 1986) serta umur dan kualitas telur (Pandian dan Varadaraj 1990). Keberhasilan tetraploidisasi menunjukkan bahwa perlakuan kejutan suhu panas yang diberikan mampu menghambat pembentukan spindel (mikrotubulus) pada saat pembelahan inti sel (nukleus).
Dalam penelitian ini, induksi tetraploid hanya berhasil dilakukan bila perlakuan kejutan panas pada suhu 42 ᴼC diaplikasikan pada umur zigot 30 msf selama 2,0 dan 2,5 menit. Sedangkan perlakuan lainnya tidak menghasilkan tetraploid. Hal ini diduga bahwa perlakuan kejutan suhu pada umur zigot kurang dari 30 msf (28 msf) waktu kejut awal terlalu awal untuk menghambat pembelahan mitosis I dan perlakuan kejutan suhu pada umur zigot lebih dari 30 msf (32 msf) terlambat untuk menghambat pembelahan mitosis I. Dari referensi yang tersedia, keberhasilan induksi tetraploid melalui kejutan suhu menunjukkan kondisi yang berbeda untuk setiap jenis ikan seperti pada rainbow trout (Hershberger dan Hostuttler 2007).
Menurut Corely-Smith et al. (1996) kejutan suhu selama dua menit merupakan waktu yang efektif untuk menghambat fisi mitosis pertama dalam produksi androgen dan gynogens pada ikan zebra (Danio rario). Dalam penelitian ini menunjukkan bahwa ikan patin siam tetraploid dapat diinduksi pada kejutan suhu panas selama 2,0 dan 2,5 menit.
Berdasarkan hasil persentase tetraploid tertinggi (26,67%) dan kelangsungan hidupnya (40,17%) maka, perlakuan kejutan suhu 42 ᴼC selama 2,5 menit pada umur zigot 30 msf merupakan kondisi optimum untuk menginduksi tetraploid pada ikan patin siam (Pangasianodon hypophthalmus).
4 SIMPULAN DAN SARAN
Simpulan
Tetraploidisasi ikan patin siam Pangasianodon hypophthalmus melalui
kejutan suhu panas 42 ᴼC selama 2,0 dan 2,5 menit pada umur zigot 30 menit setelah fertilisasi berhasil menginduksi ikan tetraploid. Kondisi optimum yang dapat menghasilkan tetraploid tertinggi (26,67%) dengan kelangsungan hidup 40,17% adalah kejutan suhu 42 ᴼC selama 2,5 menit pada umur zigot 30 menit setelah fertilisasi.
Saran
Optimasi kejutan suhu pada umur zigot yang tepat perlu ditelusuri lebih lanjut untuk meningkatkan keberhasilan tetraploid yang lebih tinggi.
13
DAFTAR PUSTAKA
Ahmed N and Hasan MR. 2007. Sustainable Livelihoods of Pangus Farming in Rural Bangladesh. Aquaculture Asia 12 (4): 6-11.
Bencsik I, N Pacala G, Dumitrescu D, Dronca J, Stanculet LP, Ciochina, Boca L. 2011. The rate of Tetraploidy Determination in Rainbow trout (Oncorhynchus mykiss) in Embryonated Eggs. Scientific Papers: Animal Science and Biotechnologies 44 (1): 158-161.
Carman O, Alimuddin, Sastrawibawa S, Arfah H. 1997. Determinasi Kromosom dan Nukleoli pada Ikan Nila Merah (Oreochromis sp.). Zuriat, 8 (2): 83-89. Carman O, Oshiro T, Takashima F. 1991. Estimation of Effective Condition for
Induction of Triploid in Goldfish Carassius auratus Linnaeus. J Tokyo Univ Fish. 78(2):127-135.
Chinjiang W, Yuszen Y, Ronde C. 1986. Genome Manipulation In Carp Ciprinus carpio L. Aquaculture 54:57-61
Corely-Smith GE, Lim CJ, Brandhorst BP. 1996. Production of androgenetic zebrafish (Danio rerio). Genetics 142:1265-1276.
Don J, Avtalion RR. 1986. The Induction of Triploid in Oreochromis aureus by Heat Shock. Theor Appl Genet. 72:186-192.
Fitria S, Sistina Y, Sulistyo I. 2013. Poliploidisasi Ikan Nilem (Osteochilus hasselti Valenciennes, 1842) dengan Kejut Dingin 4 ᴼC. Di dalam: Rinanti Y, Ramli Y, Nurmiyati, Payitno BA, Karyanto P, Widoretno S, Suciati, Maridi, Sugiharto B, Editor. Biologi, Sains, Lingkungan, dan Pembelajarannya. Seminar Nasional X Pendidikan Biologi; 2013 Jul 06; Surakarta, Indonesia. Surakarta (ID): Universitas Sebelas Maret. hlm 7-17. Gill HW, Kong HJ, An CN, Kim BS, Lim SG, Park IS. 2016. Cytogyenetic Study of Diploid and Induced Tetraploid in Korean Rose bitterling, Rhodeus uyekii. Journal a Springer Plus 5:186-195.
Herbst EC. 2002. Induction of Tetraploidy In Zebrafish Danio rerio and Nile Tilapia Ochromis niloticus. [Thesis]. University of North Carolina At Charlotte. 139
Hershberger WK, Hostuttler MA. 2007. Protocols for More Effective Induction of Tetraploid. Aquaculture 69: (4) 367-372.
Howell WM and Black DA. 1980. Controlled Silver Staining of Nucleolus Organizer Region with Protective Colloidal Developer: a 1 – Step Methods. Experientia. 36:1014-1015
Kumar A and Haniffa MAK. 2012. Induction of Tetraploidy in an Ornamental Fish koicarp Cyprinus carpio L, using Heat Shock. Journal of Research in Animal Sciences 1: 013-019.
Lebeda I and Flajshans M. 2015. Technical note: Production of Tetraploid Sturgeons. Journal of Animal Science 93:3759-3764.
Mair GC. 1993. Chromosome-set Manipulation In Tilapia – Techniques, Problems and Prospects. Aquaculture 111:313-322.
14
Mustami MK. 2013. Tingkat Penetasan Relatif Telur Ikan Mas ( Cyprinus carpio Linn.) Ras Punten yang diberikan Kejutan Suhu Panas untuk Memproduksi Ikan poliploid. Jurnal Bionature, hlm.7-10
Nugraha D, Supardjo MN, Subiyanto. 2012. Pengaruh Perbedaan Suhu Terhadap Perkembangan Embrio, Daya Tetas Telur dan Kecepatan Penyerapan Kuning Telur ikan Black Ghost (Apteronotus albifrons) pada Skala Laboratorium. Semarang. Jurnal of Management of Aquatic Resources 1 (1): 1-6.
Pandian TJ and Varadaraj K. 1990. Techniques to Produce 100% Male Tilapia. AGA. The ICLARM Quarterly 13(34):3-5.
Sakao S, Fujimoto T, Kimura S et al (2006) Drastic mortality in tetraploid induction result from the elevation of ploidy in masu salmon Oncorhynchus masou. Aquaculture 252: 147-160
Sastrawibawa S. 1997. Triploidisasi Ikan Tawes (Puntius gonionotus Blkr.) Dengan Menggunakan Kejutan Panas. [Disertasi]. Fakultas Pertanian. UNPAD, Bandung.
Sellars MJ, Coman FE, Degnan BM, Preston NP. 2006. The Effectiveness of Heat, Cold and 6-Dimethylaminopurine Shock for Inducing Tetraploidy In Kuruma Shrimp, Marsupenaeus japonicus (BETE). Journal of Shellfish Research. 25(2):631-637. hypophthalmus. BBPBAT Sukabumi. Hal. 1-12.
Tan SHA, Teh CP, Chang GO, Yasin Z. 2016. Tetraploid Induction in Tropical Oysters, Crassostrea belcheri (Sowerby) and Crassostrea iredalei (Faustino). Aquaculture Research 1-7.
Tave D. 1985. Genetic for Fish Hatchery Managers. Connecticut [NL]: Avi Publishing. 368 hlm.
Weber GM and Hostuttler MA, Semmens KJ, Beers BA. 2015. Induction and Viabillity of Tetraploids in Brook Trout (Salvelinus fontinalis). National Center for Cool and Cold Water. Aquaculture. USDA/ARS 1-27.
Widodo P, Akmal, Syafrudin. 2010. Budidaya Ikan Patin (Pangasius hypophthalmus) pada Lahan Marjinal di Kabupaten Pulang Pisau Provinsi Kalimantan Tengah. Prosiding Forum Inovasi Teknologi Akuakultur. 43 (1): 12
Yang H and Guo X. 2006. Polyploid Induction by Heat Shock-Induced Meiosis and Mitosis Inhibition in the Dwaft Surf Clam, Mulinia lateralis Say. Aquaculture 252; 171-182.
15
16
Lampiran 1 Hasil analisis ragam derajat penetasan (DPT) ANOVA
17
Lampiran 2 Hasil analisis ragam tingkat kelangsungan hidup (TKH)
ANOVA
19
Lampiran 3 Hasil analisis ragam persentase keberhasilan tetraploid (4N)
ANOVA
20
28 6 0,0000 a
30 6 0,0000 a
32 6 17,7778 b
Sig. 1,000 1,000
Uji BNT untuk Lama Kejutan
Waktu (menit) 28 30 32
2,0
0 13.33 0
0 13.33 0
0 0 0
Rata-rata 0 8.88 0
2,5
0 20 0
0 33,33 0
0 26,67 0
Rata-rata 0 26.67 0
BNT = α
2;dBS √
� �
= 0,922√ ∗ , = 0,922* 5, 42 = 4.99
Uji BNT untuk Lama Kejutan Lama kejut
(menit) d c a b e f Pengelompokan
d 0 a
c 17.78 0 b
A 26.67 8.89 0 c
b 26.67 8.89 26.67 0 c
e 26.67 8.89 26.67 8.89 0 c
21