HEWA
SE
INST
EWAN MODEL PASCARUMEN
SITTI WAJIZAH
SEKOLAH PASCASARJANA
STITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa disertasi Ketahanan Amida dalam Sistem Rumen dan Efektivitasnya Memodifikasi Komposisi Asam Lemak pada Tikus sebagai Hewan Model Pascarumen adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka pada bagian akhir disertasi ini.
Bogor, Januari 2012
Effectiveness in Modifying Fatty Acid Composition in Rat as Post Ruminal Model. Under supervision of KOMANG G. WIRYAWAN, WASMEN MANALU, and DWI SETYANINGSIH.
Dietary n-3 polyunsaturated fatty acids (PUFA n-3), such as fish oil in ruminant potentially decrease cholesterol concentration in meat. Due to extensive lipolysis and hydrogenation of n-3 PUFA by rumen microorganism, n-3 PUFA was reacted with butylamine to produce fish oil amides that resist microbial breakdown in the rumen. Three in vitro trials were conducted to determine whether fish oil amides were degraded and hydrogenated by ruminal organism. The treatments consisted of ground corn hay supplemented with either no lipid, fish oil, combination of fish oil and amide, and amide alone. After 24 hours incubation, the degradation of amide was lower for 10% supplementation than for 5% supplementation (13% and 30% respectively). Fish oil amides had no effect on VFA, acetat:propionate, NH3, microbial protein, and gas production. Relative to control, fish oil amide significantly reduced the degradabilities of dry and organic matters, and protozoa population in cultures. In in vivo experiment, fish oil amide was added to rat diets as post ruminal model. This experiment was conducted to study the effectiveness of fish oil amide in decreasing plasma cholesterol and triglyceride concentrations, increasing PUFA in rat muscle and its effect on blood hematological status. Thirty five male Sprague Dawley rats of 7 weeks old were randomly divided into 5 (five) treatment groups. Control group (A) was fed with semi-purified diet containing of 8% corn oil. Treatment groups were supplemented with 4.5% fish oil (B), 3% fish oil+1.5% fish oil amide (C), 1,5% fish oil+3% fish oil amide (D), and 4.5% fish oil amide (E), respectively. The result showed that fish oil amide supplementation could maintain the number of erythrocytes and hemoglobin, while hematocrit value began to decrease with 3% amide supplementation compared to fish oil supplementation (B) and 1.5% amide supplementation (C). The number of leucocytes in group with 4.5% amide supplementation significantly increased (P<0,05) compared to the group supplementing fish oil (B). Fish oil amide supplementation had no effect on plasma cholesterol and HDL concentrations, but began markedly increased (P<0,05) plasma triglyceride, LDL concentrations, and muscle cholesterol at 3% amide supplementation. There was no enriched levels of n-3 PUFA in rat muscle with amide supplementation. It was concluded that 3% amide supplementation gave negative impact on hematological status, plasma lipid profile, mucle and adipose tissue.
dan Efektivitasnya Memodifikasi Komposisi Asam Lemak pada Tikus Sebagai Hewan Model Pascarumen. Dibimbing oleh: Prof. Dr. Komang G. Wiryawan, Prof. Wasmen Manalu, PhD, dan Dr. Dwi Setyaningsih, M.Si.
Pemberian pakan tinggi asam α-linolenat dan khususnya asam lemak
dengan rantai yang lebih panjang, yaitu EPA dan DHA, dapat memperbaiki kandungan asam lemak tak jenuh rantai ganda atau polyunsaturated fatty acids (PUFA) n-3 dalam jaringan daging domba untuk memenuhi standar kesehatan yang optimal bagi diet manusia. Pada ruminansia, diet asam lemak mengalami biohidrogenasi yang ekstensif oleh mikroorganisme rumen sehingga penyerapan didominasi oleh asam lemak jenuh yang mengarah pada pembentukan lipoprotein berdensitas sangat rendah atau very-low-densitylipoprotein (VLDL).
Biohidrogenasi asam lemak dalam rumen dapat diatasi dengan melindungi asam lemak, terutama PUFA n-3 dalam bentuk amida. Penelitian ini dimulai dari tahap pembuatan amida minyak ikan, uji ketahanan dalam sistem rumen, dan efektivitasnya dalam mengubah profil lemak pada hewan model. Identifikasi gugus amida yang terbentuk dilakukan dengan spektroskopi inframerah, sedangkan GC-MS digunakan untuk mengetahui kadar senyawa amida yang terbentuk.
Percobaan pada tikus sebagai hewan model pascarumen menunjukkan bahwa amida tidak dapat memasok EPA dan DHA dalam saluran pencernaan yang ditunjukkan oleh kecilnya proporsi EPA dan DHA dalam jaringan otot dibandingkan dengan pemberian minyak ikan. Tampaknya proses amidasi memutuskan ikatan rangkap pada minyak sehingga jumlahnya berkurang, dan sebagian mengalami penjenuhan. Hal ini terlihat dari kenaikan trigliserida dan LDL plasma, serta kolesterol jaringan otot pada pemberian amida. Hal ini tidak terlihat pada pemberian minyak ikan, karena EPA dan DHA bersifat menurunkan sintesis kolesterol dalam hati, serta menekan produksi lipoprotein endogen, meningkatkan eliminasi lipoprotein, atau meningkatkan aktivitas lipoprotein lipase.
Pemberian amida menurunkan konsumsi dan kecernaaan bahan kering, serta kecernaan lemak. Hal ini mengakibatkan turunnya pertambahan bobot badan harian. Penurunan konsumsi bahan kering dapat disebabkan oleh faktor fisiologis atau palatabilitas, karena bau amida yang agak menyengat. Suplementasi amida tidak berpengaruh nyata pada konsentrasi kolesterol total dan HDL, tetapi mulai meningkatkan konsentrasi trigliserida, LDL, kolesterol daging pada pemberian 3% dalam ransum.
Meskipun masih berada dalam kisaran normal, suplementasi 3% amida dalam ransum mulai memperlihatkan peningkatan jumlah leukosit, yang diikuti dengan menurunnya kadar Hb darah.
© Hak Cipta milik IPB, tahun 2012 Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik dan tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
HEWAN MODEL PASCARUMEN
SITTI WAJIZAH
Disertasi
sebagai salah satu syarat untuk memperoleh gelar
Doktor pada
Program Studi Ilmu Ternak
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Penguji pada Ujian Tertutup : Prof. Dr. Ir. Dwi Apri Astuti, M.S.
Dr. Ir. Asep Sudarman, M.Rur.Sc.
Penguji pada Ujian Terbuka : Dr. Ir. Jajat Jachja, M.Sc.Agr.
Dr. Ir. Moh. Yamin, M.Agr.Sc.
Judul Disertasi : Ketahanan Amida dalam Sistem Rumen dan Efektivitasnya Memodifikasi Komposisi Asam Lemak pada Tikus sebagai Hewan Model Pascarumen
Nama : Sitti Wajizah
NRP : D061040031
Disetujui Komisi Pembimbing
Prof. Dr. Ir. Komang G Wiryawan Ketua
Prof. Wasmen Manalu, PhD. Anggota
Dr. Ir. Dwi Setyaningsih, M.Si. Anggota
Diketahui
Ketua Departemen
Ilmu Nutrisi dan Teknologi Pakan
Dr. Ir. Idat Galih Permana M.Sc.Agr.
Dekan Sekolah Pascasarjana IPB
Dr. Ir. Dahrul Syah, M.Sc.Agr.
kesehatan dan kekuatan sehingga penulis akhirnya mampu menyelesaikan penulisan disertasi ini. Tema yang dipilih dalam penelitian yang mulai dilaksanakan sejak tahun 2009 ini ialah perlindungan PUFA n-3 dalam sistem rumen. Penelitian ini berjudul Ketahanan Amida Minyak Ikan dalam Sistem Rumen dan Efektivitasnya Memodifikasi Komposisi Lemak pada Tikus sebagai Hewan Model Pascarumen.
Ungkapan terima kasih dan penghargaan yang tinggi penulis sampaikan kepada Bapak Prof. Dr. Komang G. Wiryawan, Prof. Wasmen Manalu, PhD, dan Dr. Ir. Dwi Setyaningsih, M.Si selaku komisi pembimbing yang telah memberi arahan serta bimbingan kepada penulis dalam pelaksanaan penelitian hingga penyusunan disertasi ini. Rasa terima kasih yang dalam juga penulis sampaikan kepada ibu Dr. Ir. Dwierra Evvyernie A., MS. M.Sc selaku Ketua Program Studi Ilmu Nutrisi beserta para staf yang telah sekuat tenaga membantu penyelesaian studi penulis di saat-saat terakhir ini.
Ucapan terima kasih juga penulis sampaikan kepada Dirjen Dikti beserta jajarannya, Rektor Unsyiah beserta jajarannya, Rektor IPB beserta jajarannya, Pemerintah Provinsi Aceh yang telah mendukung penulis dengan beasiswa NAD, Toyota Astra yang telah memberikan bantuan dana untuk membantu penyelesaian studi, serta seluruh instansi dan perseorangan yang telah menyediakan fasilitas dan bantuan bagi penulis, mulai dari masa kuliah hingga selesainya disertasi ini.
Kepada ayahanda dan ibunda tercinta penulis menghaturkan terima kasih yang tulus atas doa yang tak pernah putus, kasih sayang yang tak pernah pupus, dan dorongan semangat yang membuat penulis kembali bangkit. Kepada adik-adikku terima kasih atas segala pengertian dan kasih sayang. Kepada suamiku terkasih, terima kasih atas segala kesabaran dalam penantian yang panjang, semoga kita dapat membangun harapan bersama ke depan.
Terima kasih kepada sahabat-sahabat setiaku Dr. drh. Nurliana, M.Si, dan Dr. drh. Ummu Balqis, M. Si, serta adik-adikku di Radar 6 yang telah mendukung penulis dalam penyelesaian studi ini. Kepada teman-teman pascasarjana PTK yang senasib seperjuangan terima kasih atas segala kebersamaan, bantuan, dan dukungan semangat yang senantiasa ada terutama di masa-masa sulit ini. Semoga persahabatan kita tetap indah.
Disertasi ini masih penuh kekurangan, saran dan kritik yang membangun sangat diharapkan untuk menjadikan karya ini bermanfaat. Semoga Allah SWT meridhai. Amiin
Bogor, Januari 2012
Penulis dilahirkan di Banda Aceh pada tanggal 28 Pebruari 1969 dari Bapak Amiruddin Abdul Wahab dan Ibu Sitti Halimah Hamzah. Penulis merupakan putri pertama dari tiga bersaudara.
Tahun 1987 penulis lulus dari SMA Negeri 3 Banda Aceh dan pada tahun yang sama penulis diterima sebagai mahasiswa Jurusan Peternakan, Fakultas Pertanian, Universitas Syiah Kuala melalui jalur PMDK, dan lulus pada tahun 1992. Pada tahun 1996 penulis menjalani program magister (S-2) pada Sekolah Pascasarjana IPB, Program Studi Ilmu Ternak dan lulus pada tahun 1999. Selanjutnya di tempat yang sama, pada tahun 2004 penulis menempuh program pendidikan doktoral (S-3).
Sebuah artikel berjudul Profil Lemak Plasma dan Nilai Hematologi Tikus
Sprague Dawley dengan Suplementasi Amida Minyak Ikan telah disetujui untuk
diterbitkan pada Jurnal Fakultas Kedokteran Hewan Universitas Syiah Kuala edisi 2012.
x
DAFTAR ISI
Halaman
DAFTAR TABEL ………... xii
DAFTAR GAMBAR ……….. xiv
DAFTAR LAMPIRAN………... xv
PENDAHULUAN……… 1
Latar Belakang………. 1
Tujuan Penelitian……….. 3
Manfaat Penelitian……… 3
Hipotesis Penelitian……….. 3
TINJAUAN PUSTAKA Suplementasi Lemak dalam Pakan Ruminansia………... 5
Metabolisme Lemak dalam Rumen……….. 9
Tipe Lemak dan Kolesterol……….. 13
Minyak Ikan dan Peranannya………... 15
Perlindungan Asam Lemak dalam Rumen………... 19
MATERI DAN METODE Sintesis Amida Minyak Ikan……… 23
Metode Analisis Minyak Ikan dan Amida Minyak Ikan………. 23
Uji Ketahanan Minyak Ikan secara In Vitro………. 26
Metode Analisis In Vitro……….. 27
Efektivitas Suplementasi Amida Minyak Ikan pada Tikus sebagai Hewan Model Pascarumen………. 30
Pengambilan Data dan Sampel ……….. 31
Metode Analisis In Vivo……….. 32
xi HASIL DAN PEMBAHASAN
Produk Amida Minyak Ikan……… 37
Uji Ketahanan Amida Minyak Ikan secara In Vitro………. 41
Uji Efektivitas Amida Pascarumen……….. 51
Pembahasan Umum……….. 64
SIMPULAN DAN SARAN……… 69
DAFTAR PUSTAKA……….. 71
xii
DAFTAR TABEL
Halaman
1 Asam lemak utama dalam diet………. 5
2 Asam lemak komponen lemak depo ternak (%)……… 7
3 Komposisi lemak berbagai jenis ternak (%)……… 14
4 Tempat sintesa dan pengaruh prostaglandin terhadap agregasi platelet……….. 17
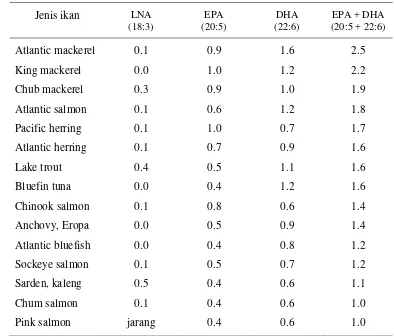
5 Kandungan PUFA n-3 pada beberapa jenis ikan (%)……… 18
6 Komposisi minyak ikan dan minyak jagung (%)……… 30
7 Susunan ransum percobaan in vivo……… 31
8 Karakteristik minyak ikan untuk amidasi……….. 37
9 Karakteristik amida minyak ikan………... 38
10 Komposisi kimia utama hasil amidasi minyak ikan……….. 39
11 Rataan pH cairan rumen in vitro pada perlakuan penambahan minyak ikan dan amida minyak ikan……… 42
12 Rataan populasi protozoa/ml sampel rumen secara in vitro pada perlakuan penambahan minyak ikan dan amida minyak ikan………... 43
13 Rataan N-NH3, VFA total, produksi gas, dan protein mikrob secara in vitro pada perlakuan penambahan minyak ikan dan amida minyak ikan………... 44
14 Rataan VFA parsial (mM) secara in vitro pada perlakuan penambahan minyak ikan dan amida minyak ikan……… 45
15 Rataan DBO(%) dan DBK (%) secara in vitro pada perlakuan penambahan minyak ikan dan amida minyak ikan……… 48
16 Senyawa amida (%) pada kultur in vitro pada perlakuan penambahan minyak ikan dan amida minyak ikan……… 50
17 Nilai rata-rata hematologi darah tikus pada perlakuan suplementasi minyak ikan dan amida minyak ikan………. 52
xiii 18 Rataan konsentrasi lemak plasma dan daging tikus pada perlakuan
suplementasi minyak ikan dan amida minyak ikan……….. 54
xiv
DAFTAR GAMBAR
Halaman
1 Lipolisis dan biohidrogenasi ………. 10
2 Fraksi lipida dalam duodenum ruminansia……… 11
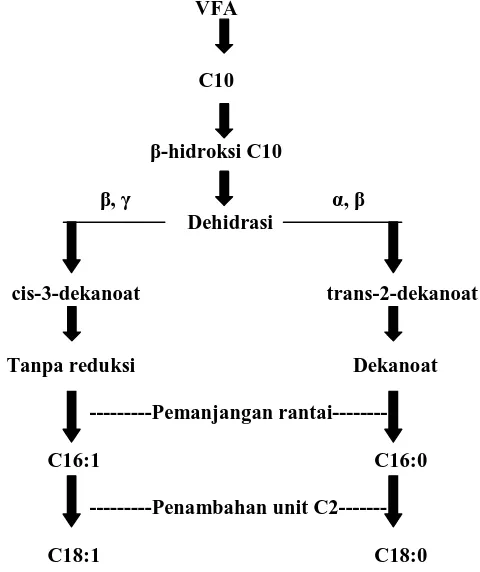
3 Sintesis asam lemak jenuh dan asanm lemak tak jenuh tunggal oleh mikrob……… 12
4 Jalur metabolisme asam lemak esensial dari prekursor n-3 dan n-5 ……… 16
5 Spektra IR hasil reaksi minyak ikan dan butilamina………. 38
6 Spektra IR hasil reaksi minyak ikan dan urea ……….. 40
7 Spektra IR hasil reaksi ester minyak ikan dan urea ………. 40
8 Spektra IR minyak ikan………... 41
xv
DAFTAR LAMPIRAN
Halaman
1 Analisis sidik ragam populasi protozoa pada inkubasi 0 jam ………. 81
2 Analisis sidik ragam dan uji BNTpopulasi protozoa pada inkubasi 12 jam……… 81
3 Analisis sidik ragam populasi protozoa pada inkubasi 24 jam……… 81
4 Analisis sidik ragam produksi gas……… 82
5 Analisis sidik ragam nilai pH pada inkubasi 0 jam……….. 82
6 Analisis sidik ragam nilai pH pada inkubasi 24 jam……… 82
7 Analisis sidik ragam nilai pH pada inkubasi 48 jam……… 82
8 Analisis sidik ragam konsentrasi N-NH3………. 83
9 Analisis sidik ragam konsentrasi VFA total……… 83
10 Analisis sidik ragam konsentrasi asetat……… 83
11 Analisis sidik ragam konsentrasi propionat……… 83
12 Analisis sidik ragam konsentrasi isobutirat………. 83
13 Analisis sidik ragam konsentrasi n-butirat……….. 84
14 Analisis sidik ragam konsentrasi isovalerat………. 84
15 Analisis sidik ragam rasio A:P……… 84
16 Analisis sidik ragam dan uji BNT degradasi bahan organik pada inkubasi 0 jam………. 84
17 Analisis sidik ragam dan uji BNT degradasi bahan organik pada inkubasi 24 jam……… 85
18 Analisis sidik ragam dan uji BNT degradasi bahan organik pada inkubasi 48 jam……… 85
xvi 20 Analisis sidik ragam dan uji BNT degradasi bahan kering
pada inkubasi 24 jam……… 86
21 Analisis sidik ragam dan uji BNT degradasi bahan kering pada inkubasi 48 jam……… 87
22 Analisis sidik ragam protein mikrob……… 87
23 Analisis sidik peragam dan uji BNT PBBH……… 88
24 Analisis sidik peragam eritrosit……… 88
25 Analisis sidik peragam nilai hematokrit……….. 89
26 Analisis sidik peragam kadar hemoglobin 89 27 Analisis sidik peragam dan uji BNT jumlah leukosit……….. 90
28 Analisis sidik peragam jumlah neutrofil 90 29 Analisis sidik peragam jumlah jumlah limfosit……… 91
30 Analisis sidik peragam jumlah monosit………... 91
31 Analisis sidik peragam jumlah eosinofil………. 91
32 Analisis sidik peragam konsentrasi kolesterol plasma………. 92
33 Analisis sidik peragam dan uji BNT konsentrasi trigliserida plasma.. 92
34 Analisis sidik peragam konsentrasi HDL plasma……… 93
35 Analisis sidik peragam dan uji BNT konsentrasi LDL plasma……… 93
36 Analisis sidik peragam dan uji BNT konsentrasi kolesterol daging… 94 37 Analisis sidik peragam dan uji BNT kandungan lemak daging……... 95
38 Analisis sidik peragam dan uji BNT kandungan asam laurat……….. 96
39 Analisis sidik peragam dan uji BNT kandungan asam miristat……. 97
40 Analisis sidik peragam dan uji BNT kandungan asam palmitat…… 98
xvii
43 Analisis sidik peragam dan uji BNT kandungan asam oleat………… 101
44 Analisis sidik peragam dan uji BNT kandungan asam linoleat……... 102
45 Analisis sidik peragam dan uji BNT kandungan asam linolenat……. 103
46 Analisis sidik peragam dan uji BNT kandungan asam arakidonat…... 104
47 Analisis sidik peragam dan uji BNT kandungan EPA………. 105
48 Analisis sidik peragam dan uji BNT kandungan DHA……… 106
49 Analisis sidik peragam dan uji BNT konsumsi bahan kering……….. 106
50 Analisis sidik peragam dan uji BNT kecernaan bahan kering………. 107
51 Analisis sidik peragam konsumsi protein………. 107
52 Analisis sidik peragam dan uji BNT kecernaan protein……….. 108
53 Analisis sidik peragam dan uji BNT konsumsi lemak………. 108
Latar Belakang
Domba merupakan salah satu sumber daging yang paling banyak dikonsumsi di dunia. Produksi daging domba terus meningkat karena memiliki nilai ekonomis yang tinggi, dan sangat efisien dalam mengubah hijauan yang berkualitas rendah menjadi daging yang berkualitas tinggi. Karakteristik daging domba didominasi oleh kandungan asam lemak jenuh atau saturated fatty acids (SFA) yang tinggi, dan memiliki rasio asam lemak tak jenuh ganda atau
polyunsaturated fatty acids (PUFA) : SFA yang rendah (Cooper et al. 2004).
Berdasarkan hal tersebut maka Lee et al. (2004) menyatakan bahwa konsumsi daging merah termasuk daging domba berisiko pada kesehatan, karena tingginya kandungan SFA (40-50%) dan rendahnya kandungan PUFA. Konsumsi SFA yang tinggi merupakan salah satu faktor pemicu berkembangnya beberapa jenis kanker, penyakit jantung koroner atau coronary heart disease (CHD), diabetes, dan obesitas. Asam lemak jenuh, terutama C14:0 dan C16:0, yang berlebihan mengakibatkan otot rentan terhadap resistensi insulin sehingga timbul hiperinsulinemia, atau meningkatkan produksi trigliserida dan kolesterol oleh hati yang meningkatkan faktor risiko aterosklerosis kronis (Moibi & Christopherson 2001).
Manipulasi nutrisi merupakan salah satu jalan untuk mendapatkan komposisi lemak daging yang lebih sehat. Pakan ternak berbasis hijauan menghasilkan daging dengan sedikit lemak intramuskular dan kandungan PUFA yang lebih tinggi dibandingkan pakan ternak berbasis konsentrat. Aktivasi enzim
∆-desaturase juga dapat meningkatkan kandungan asam lemak tak jenuh tunggal atau monounsaturated fatty acids (MUFA), yang berperan menurunkan penyakit metabolis pada manusia. Pemberian asam linoleat dan asam α-linolenat juga akan meningkatkan kandungan asam linoleat terkonjugasi atau conjugated linoleic
acids (CLA), yang mempunyai aktivitas antikarsinogenik (Hausman et al. 2009).
ikan laut yang mengandung asam eikosapentanoat (EPA; 20:5) dan asam dokosaheksanoat (DHA; 22:6). Kecukupan EPA dan DHA dapat mencegah terjadinya aterosklerosis dan penyakit jantung pada manusia dewasa. Minyak ikan mengandung PUFA n-3, seperti EPA dan DHA, dalam jumlah yang berlimpah, tetapi jarang terdapat pada lemak hewan (Irie & Sakimoto 1992).
Penelitian terakhir menunjukkan bahwa pemberian pakan tinggi asam α -linolenat, khususnya asam lemak dengan rantai yang lebih panjang, yaitu EPA dan DHA, dapat memperbaiki kandungan PUFA n-3 dalam jaringan daging domba untuk memenuhi standar kesehatan yang optimal bagi diet manusia. Namun demikian, pada ruminansia, diet asam lemak mengalami hidrogenasi yang ekstensif oleh mikroorganisme rumen sehingga penyerapan didominasi oleh asam lemak jenuh yang mengarah pada pembentukan lipoprotein berdensitas sangat rendah atau very-low-density lipoprotein (VLDL). Trans-asam lemak tak jenuh tunggal atau monounsaturated fatty acids (MUFA) dan SFA yang merupakan bagian dari VLDL selanjutnya tergabung ke dalam lemak otot, yang berimplikasi pada rendahnya rasio PUFA : SFA pada daging domba (Jenkins 1993; Cooper et al. 2004).
Gulati et al. (1999) melaporkan bahwa meskipun pada beberapa penelitian didapatkan bahwa EPA dan DHA hanya mengalami modifikasi sebagian oleh mikroorganisme rumen secara in vitro, hidrogenasi ruminal yang ekstensif terjadi pada asam-asam lemak tersebut secara in vivo. Selain itu, pakan yang mengandung PUFA memiliki beberapa pengaruh inter-relasi (baik positif maupun negatif) terhadap metabolisme rumen yang mempengaruhi pola fermentasi, jumlah protozoa, kecernaan pakan, efisiensi pertumbuhan mikrob, serta situs dan kinetika pencernaan (Chikunya et al. 2004).
bahwa meskipun perlindungannya belum sempurna, ternyata linolamida dapat bertahan dari biohidrogenasi dalam rumen jauh lebih baik dari asam linoleat. Namun demikian, perlindungan dalam bentuk amida dari EPA dan DHA dalam minyak ikan masih jarang dilakukan.
Berdasarkan pernyataan di atas, perlu dikaji pengaruh amida minyak ikan pada pola fermentasi rumen, dan efektivitasnya dalam meningkatkan aliran EPA dan DHA pascarumen, memperbaiki profil asam lemak plasma, dan deposisinya dalam jaringan otot tikus sebagai hewan model pascarumen. Penggunaan tikus didasarkan asumsi bahwa pencernaan pascarumen mempunyai kemiripan dengan pencernaan monogastrik pada nonruminan.
Tujuan Penelitian
1. Mempelajari pembuatan amida minyak ikan.
2. Mengevaluasi ketahanan amida minyak ikan dalam rumen secara in vitro.
3. Mengevaluasi efektivitas amida minyak ikan pascarumen menggunakan hewan model tikus.
Manfaat Penelitian
1. Mendapatkan teknologi pembuatan amida minyak ikan.
2. Menentukan kemampuan melindungi PUFA n-3 dari degradasi sistem rumen.
3. Menentukan profil lemak pada tikus sebagai hewan model.
Hipotesis Penelitian
1. Amida minyak ikan dapat melindungi PUFA n-3 dari biohidrogenasi dalam rumen untuk pencernaan pascarumen.
2. Pemberian amida minyak ikan dapat meningkatkan kandungan PUFA n-3 dalam jaringan otot tikus.
TINJAUAN PUSTAKA
Suplementasi Lemak dalam Pakan Ruminansia
Lipid adalah suatu substansi yang tidak larut air, tetapi larut dalam pelarut organik (eter, kloroform, heksan, dll). Lipid dalam bahan pakan biasanya dalam bentuk trigliserida yang terutama ditemukan dalam biji-bijian sereal, biji-bijian penghasil minyak, dan lemak hewan. Selain itu, lipid dalam bahan pakan juga terdapat dalam bentuk glikolipida yang terutama ditemukan dalam hijauan rumput-rumputan dan leguminosa, dan sejumlah kecil terdapat dalam bentuk fosfolipid (Wattiaux & Grummer 2006).
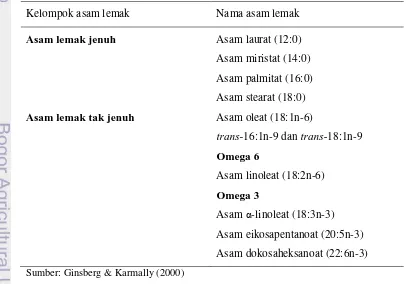
Ginsberg dan Karmally (2000) membagi asam lemak dalam diet menjadi 3 kelompok utama, yaitu asam lemak jenuh atau saturated fatty acids (SFA), asam lemak tak jenuh tunggal atau monounsaturated fatty acids (MUFA), dan asam lemak tak jenuh ganda atau polyunsaturated fatty acids (PUFA). Perbandingan berdasarkan bobot antara PUFA dan SFA dikenal dengan rasio PUFA : SFA. Asam lemak utama yang terdapat dalam triasilgliserol diet (lemak dan minyak) dapat dilihat pada Tabel 1.
Tabel 1 Asam lemak utama dalam diet
Kelompok asam lemak Nama asam lemak
Asam lemak jenuh Asam laurat (12:0)
Asam miristat (14:0) Asam palmitat (16:0) Asam stearat (18:0) Asam lemak tak jenuh Asam oleat (18:1n-6)
trans-16:1n-9 dan trans-18:1n-9 Omega 6
Asam linoleat (18:2n-6) Omega 3
Asam α-linoleat (18:3n-3) Asam eikosapentanoat (20:5n-3) Asam dokosaheksanoat (22:6n-3)
Lazimnya, pakan ternak produksi mengandung sedikit atau tanpa penambahan lemak. Sumber asam lemak satu-satunya terdapat secara alami dalam bahan pakan. Penggunaan lemak terutama terbatas pada pakan unggas dan pengganti susu pada ruminansia muda. Namun demikian, akhir- akhir ini terjadi perkembangan yang pesat dalam penambahan lemak pada pakan ternak produksi. Pemberian lemak biasanya dimaksudkan untuk meningkatkan kepadatan energi dalam pakan, di samping memiliki keuntungan lain, seperti meningkatkan penyerapan nutrien larut lemak dan mengurangi debu pada pakan (Palmquist 1988).
Sejalan dengan meningkatnya pengetahuan tentang pengaruh asam lemak tertentu pada kandungan lemak darah, dikeluarkanlah rekomendasi internasional menyangkut jumlah dan komposisi lemak diet yang dikonsumsi. Lemak hewan ternyata tidak direkomendasikan karena terlalu banyak mengandung SFA dan terlalu sedikit PUFA. Di samping itu, pentingnya PUFA n-3 telah lama diketahui sehingga rasio n-3: n-6 menjadi penting. Usaha untuk mendapatkan pangan asal hewan yang lebih sehat bertujuan untuk mengubah pola asam lemak produk, agar sedapat mungkin sesuai dengan rekomendasi kesehatan (Leibetseder 1997).
Ponnampalan et al. (2001) menambahkan bahwa tipe lemak pada pakan ternak domestikasi dapat mempengaruhi komposisi asam lemak total dan lemak netral pada jaringan otot. Asam lemak jenuh bila diberikan melebihi kebutuhan akan dideposit pada jaringan lemak sebagai trigliserida cadangan, sedangkan PUFA terutama n-3 sebagian besar dideposit dalam fosfolipid struktural. Mayoritas lipid sel terdiri atas fosfolipid dan kolesterol, yang memainkan peranan penting dalam menentukan struktur lipoprotein plasma, juga sangat mempengaruhi fungsi protein membran seperti aktivitas insulin pada jaringan lemak otot.
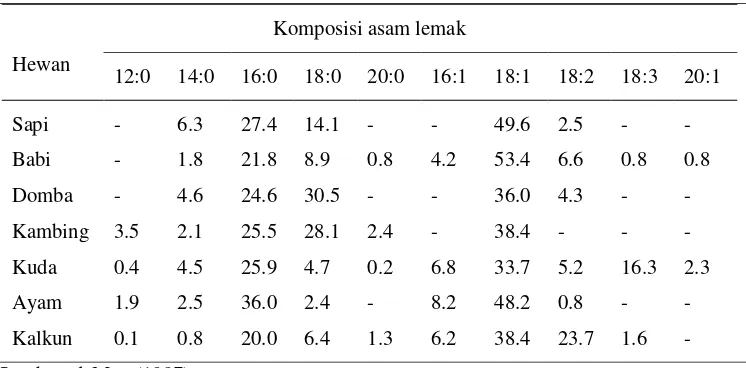
namun terdapat perbedaan yang besar antara komposisi asam lemak subkutan pada domba jantan dan domba jantan kastrasi. Perbedaan ini disebabkan domba betina dan domba jantan kastrasi lebih gemuk daripada domba jantan pada umur yang sama. Pengaruh penambahan lemak pada pakan relatif kecil dalam mempengaruhi komposisi lemak karena asam lemak segera terhidrogenasi dalam rumen, kecuali bila diberikan dalam bentuk terproteksi. Komponen pakan selain lemak mempunyai pengaruh yang besar pada jenis asam lemak dalam depot lemak, dalam kaitannya dengan sintesis asam lemak de nuvo (Enser 1991). Komposisi asam lemak depo dari beberapa jenis ternak dapat dilihat pada Tabel 2 berikut ini.
Tabel 2 Asam lemak komponen lemak depo ternak (%)
Komposisi asam lemak
Hewan
12:0 14:0 16:0 18:0 20:0 16:1 18:1 18:2 18:3 20:1
Sapi - 6.3 27.4 14.1 - - 49.6 2.5 -
umum untuk kandungan lemak dalam ransum tidak melebihi 6-7% dari bahan kering ransum (Jenkins 1998; Bauman et al. 2003).
Penambahan lemak dalam pakan ruminansia dapat mengganggu fermentasi dalam rumen, sehingga menyebabkan menurunnya kecernaan energi dari sumber bukan lemak. Kecernaan karbohidrat struktural dalam rumen dapat menurun 50% atau lebih dengan penambahan lemak kurang dari 10%. Penurunan kecernaan berbarengan dengan turunnya produksi metan, hidrogen, dan VFA, serta turunnya rasio asetat:propionat. Metabolisme protein dalam rumen juga mengalami perubahan dengan terganggunya fermentasi rumen akibat penambahan lemak. Penurunan kecernaan protein dalam rumen berbarengan dengan turunnya konsentrasi amonia, dan meningkatnya aliran N ke dalam duodenum (Jenkins 1993).
Sintesis asam lemak de novo dipengaruhi oleh densitas energi pakan. Pakan hijauan mempunyai densitas yang rendah, sehingga membatasi deposisi lemak. Penambahan konsentrat biji-bijian yang kaya pati pada hijauan akan meningkatkan densitas energi. Pati akan difermentasi dalam rumen menjadi asam lemak terbang atau volatile fatty acids (VFA), terutama asam asetat dan asam propionat yang segera diserap dan digunakan sebagai substrat dalam sintesis asam lemak (Enser 1991)
Penambahan lemak dalam ransum ruminansia juga dapat mengakibatkan turunnya kecernaan asam lemak, yang umumnya berhubungan dengan sifat dari komposisi asam lemak itu sendiri. Pada kondisi tertentu, kecernaan SFA dapat lebih rendah dibandingkan kecernaan PUFA. Bilangan Iod atau Iodine Value (IV) 50 atau lebih berpengaruh kecil pada kecernaan asam lemak. Namun demikian, kecernaan menurun bila IV menurun di bawah 50, terutama bila IV jatuh dari nilai 27 menjadi 11. Pada asupan asam lemak yang rendah, kecernaan asam lemak sejati masing-masing mencapai 89% untuk lemak dengan IV>40 dan 74% untuk lemak dengan IV<40. Namun demikian, kecernaan asam lemak semakin menurun dengan meningkatnya asupan asam lemak dengan IV>40 (Jenkins 1998).
rumen. Untuk mendapatkan produk daging yang lebih sehat, terutama dengan peningkatan PUFA dan mendapatkan rasio n-3:n-6 yang lebih baik, dilakukan penambahan sumber PUFA n-3 dalam pakan ternak, terutama yang berasal dari minyak ikan. Minyak ikan mengandung dua jenis asam lemak rantai panjang atau
long chain fatty acids (LCFA), yaitu EPA dan DHA yang biasanya diberikan
dalam bentuk lemak terlindungi (Chilliard et al. 2000; Bauman et al. 2003).
Metabolisme Lemak dalam Rumen
Demeyer dan Doreau (1999) menjelaskan bahwa hidrolisis merupakan langkah pertama metabolisme lipid dalam rumen. Triasilgliserol, fosfolipid, dan galaktosil lipid dalam pakan hijauan dan konsentrat segera mengalami hidrolisis dalam rumen oleh lipase ekstraselular yang dihasilkan oleh sejumlah kecil bakteri. Beberapa aktivitas kemungkinan berhubungan dengan fraksi protozoa. Produk akhir yang dihasilkan berupa asam lemak bebas, selain itu juga gliserol dan galaktosa yang diubah menjadi VFA. Tingkat hidrolisis sangat tinggi terutama pada lemak yang tidak terproteksi mencapai 85-95%, persentase hidrolisis lebih tinggi pada pakan kaya lemak dibandingkan dengan pakan konvensional, dimana sebagian besar lemak terdapat dalam struktur sel (Tamminga & Doreau 1991).
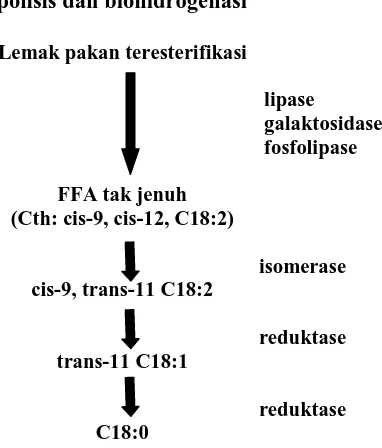
Hidrogenasi terjadi oleh berbagai jenis bakteri, dimulai dengan isomerisasi oleh enzim bakteri (Gambar 1). Asam linolenat (C18:3 n-3) umumnya mengalami hidrogenasi sempurna menjadi asam stearat (C18:0). Sebaliknya hidrogenasi asam linoleat (C18:2 n-6) berlangsung tidak sempurna. Hidrogenasi menghasilkan asam stearat dan asam trans-vaksenat (C18:1 n-7), menunjukkan tingkat hidrogenasi yang tinggi terhadap asam linoleat dan asam linolenat. Rata-rata hanya kurang dari 10% asam linoleat dan kurang dari 5% asam linolenat yang terbebas dari hidrogenasi. Tingkat hidrogenasi asam trans-vaksenat menjadi asam stearat bergantung pada kondisi rumen. Hidrogenasi menjadi asam stearat dipacu oleh adanya cairan rumen bebas sel dan partikel pakan, tetapi dihambat oleh asam linoleat dalam jumlah besar (Tamminga & Doreau 1991; Jenkins 1993)
Lipolisis dan biohidrogenasi
Gambar 1 Tahap kunci lemak pakan teresterifikasi menjadi asam lemak jenuh oleh lipolisis dan biohidrogenasi dalam rumen (Jenkins 1993).
Jenkins (1993) juga menambahkan bahwa tingkat hidrogenasi pada asam lemak tak jenuh bergantung pada derajat ketidakjenuhan suatu asam lemak serta jumlah dan frekuensi pemberiannya dalam pakan. Hidrogenasi yang dialami PUFA dalam rumen diperkirakan berkisar 60-90%, sedangkan asam lemak rantai panjang hanya mengalami sedikit degradasi dalam rumen. Sebagian besar asam lemak yang disintesis oleh mikrob rumen bergabung dalam fosfolipid. Kira-kira 85-90% asam lemak yang meninggalkan rumen merupakan asam lemak bebas, dan sekitar 10-15% adalah fosfolipid mikrob. Karena asam lemak bersifat hidrofobik, maka akan terikat pada partikel pakan dan mengangkutnya menuju duodenum. Lipolisis dalam rumen berlangsung sangat efisien. Oleh sebab itu, hampir semua lemak yang teresterifikasi yang mencapai duodenum dalam bentuk sel mikrob. Namun demikian, lipolisis dan biohidrogenasi menurun pada pH rumen yang rendah, seperti pada pakan kaya biji-bijian (Palmquist 1988).
mengalami transformasi dan lipid mikrob dalam isi duodenum tersimpan dalam jaringan ruminansia (Jenkins 1994).
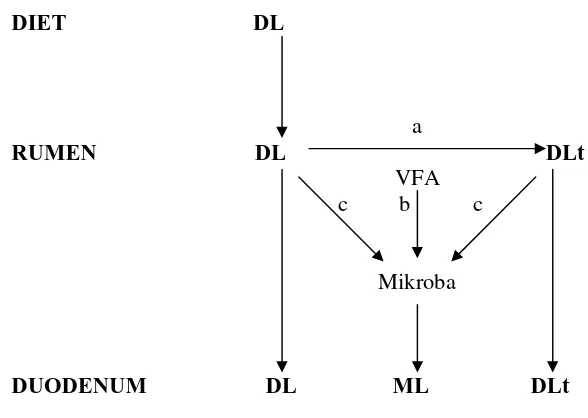
Fraksi lipid dalam duodenum ruminansia
DIET DL
a
RUMEN DL DLt VFA
c b c
Mikroba
DUODENUM DL ML DLt
Gambar 2 Lipid dalam duodenum ruminansia terdiri atas lipid pakan yang mencapai duodenum tanpa perubahan (DL), lipid pakan setelah hidrogenasi oleh mikrob rumen (DLt), dan lipida mikrobial (ML). Huruf merujuk pada a) konversi DL menjadi DLt oleh biohidrogenasi, b) sintesis lipid secara de novo oleh mikrob rumen dari VFA, dan c) asupan langsung DL dan DLt oleh mikrob rumen (Jenkins 1994).
Jenkins (1993) melaporkan bahwa kandungan lipid total dari massa bakteri kering dalam rumen berkisar antara 10-15%, baik yang berasal dari sumber eksogen (asupan diet LCFA) maupun sumber endogen (sintesis de novo). Sebagian asam lemak yang ditemukan dalam rumen merupakan komponen fosfolipid membran mikrob. Asam lemak yang disintesis secara de novo terutama terdiri atas C18:0 dan C16:0. Asam lemak bakteri mengandung 15-20% MUFA, yang disintesis melalui jalur anaerobik (Gambar 3).
Bakteri rumen biasanya tidak mensintesis PUFA, kecuali dari kelompok
cyanobacteria. Namun demikian, PUFA yang dilaporkan terdapat dalam mikrob
Non-esterified Fatty Acids (NEFA) yang berasal dari pakan dan mikrob (70%), dan sejumlah kecil (10%-20%) fosfolipid mikrob. Umumnya, koefisien penyerapan asam lemak individual dalam usus halus berkisar antara 80% (untuk SFA) sampai 92% (untuk PUFA) pada pakan konvensional dengan kandungan lemak rendah (2-3% bahan kering) (Bauchart 1993).
Gambar 3 Sintesis MUFA oleh mikrob rumen melalui jalur anaerob (Jenkins 1993).
Tipe Lemak dan Kolesterol
Tingginya konsumsi lemak dan SFA dipercaya secara luas berkonstribusi terhadap meningkatnya kasus penyakit jantung koroner atau coronary heart
disease (CHD), yang merupakan penyebab kematian utama pada sebagian negara
industri. Adanya korelasi positif antara konsumsi lemak asal hewan dan kematian yang disebabkan CHD, tampaknya sangat dipengaruhi oleh konsentrasi lipoprotein berdensitas rendah atau low density lipoproteins (LDL) yang merupakan faktor risiko timbulnya CHD. Lipoprotein merupakan kompleks protein-lipid dalam darah, yang terdiri atas tiga tipe: lipoprotein berdensitas rendah atau low density lipoproteins (LDL) yang molekulnya terdiri atas 46% kolesterol; lipoprotein berdensitas tinggi atau high density lipoproteins (HDL) yang mengandung 20% kolesterol, dan lipoprotein berdensitas sangat rendah atau
very low density lipoproteins (VLDL) yang mengandung 8% kolesterol.
Tingginya kandungan kolesterol dalam LDL merupakan penyebab utama timbulnya CHD, sebaliknya HDL berperan sebagai pelindung (Bender 1992; Bandara 1997).
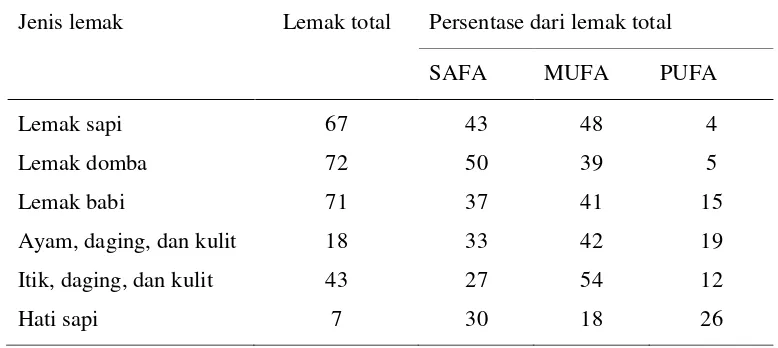
Tabel 3 Komposisi lemak berbagai jenis ternak (%)
Jenis lemak Lemak total Persentase dari lemak total
SAFA MUFA PUFA
Lemak sapi 67 43 48 4
Lemak domba 72 50 39 5
Lemak babi 71 37 41 15
Ayam, daging, dan kulit 18 33 42 19
Itik, daging, dan kulit 43 27 54 12
Hati sapi 7 30 18 26
Sumber: Bender (1992).
Gurr (1992) mendeskripsikan CHD sebagai suatu kondisi ketika arteri utama (coronary) yang memasok darah ke jantung kehilangan kemampuan untuk memasok darah dan oksigen dalam jumlah yang cukup ke otot jantung
(myocardium). Tahapan perkembangan penyakit ini dimulai dengan
menyempitnya arteri utama oleh endapan campuran kompleks lemak pada dinding arteri, proses tersebut dikenal dengan asteriosklerosis. Tahapan yang fatal ketika terbentuknya gumpalan darah (thrombosis) yang menghambat aliran darah melalui arteri yang telah menyempit. Menurunnya aliran darah ke otot jantung menyebabkan otot jantung kekurangan oksigen sehingga terjadi kerusakan yang ekstensif, yang dikenal dengan serangan jantung (myocardial infraction).
Asam lemak tak jenuh ganda (PUFA) terutama dari seri n-3 mempunyai pengaruh yang menguntungkan dalam menekan kejadian CHD, karena dapat mencegah terjadinya asteriosklerosis dan komplikasi karena trombosis. Asam lemak n-3 yang berasal dari laut memiliki pengaruh antitrombosis, memodifikasi agregasi platelet, menurunkan kekentalan darah, dan meminimalisir respons inflamasi dalam dinding pembuluh darah. Pemberian PUFA n-3 pada ruminansia bertujuan meningkatkan konsentrasinya dalam jaringan tubuh untuk meningkatkan produksi dan kesehatan, serta meningkatkan asam lemak
Minyak Ikan dan Peranannya
Ditemukannya hubungan antara lemak diet dengan penyakit pembuluh darah jantung atau cardiovascular (CVD), telah menelurkan rekomendasi yang menyarankan penggantian kolesterol dan SFA dalam diet dengan PUFA. Kelompok PUFA ditandai dengan adanya ikatan rangkap pada rantai karbonnya. Dua kelompok PUFA yang penting adalah PUFA n-6 dan PUFA n-3, yang masing-masing posisi ikatan rangkap pertamanya pada atom karbon keenam dan ketiga dari ujung metil rantai karbon. Kelompok PUFA n-6 penting dalam diet dan terutama terdapat dalam minyak tumbuhan. Asam linoleat (18:2n-6) yang merupakan sumber PUFA n-6 dalam diet terdapat dalam jumlah yang melimpah dalam minyak tumbuhan (kedelai, jagung, dan safflower), dan merupakan prekursor asam arakidonat (20:4n-6). Kelompok PUFA n-3 terkandung dalam jumlah yang sedikit dalam kebanyakan bahan makanan, kecuali ikan. Asam linolenat (18:3n-3) terdapat dalam konsentrasi yang rendah dalam jaringan tumbuhan dan minyak kedelai. Ikan laut merupakan sumber yang kaya asam eikosapentanoat atau EPA (20:5n-3) dan asam dokosaheksanoat atau DHA (22:6n-3). Asam linolenat juga merupakan prekursor EPA dan DHA (Kinsella 1987; Cunnane & Griffin 2002).
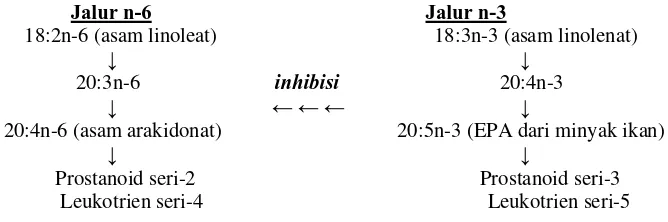
Menyangkut fungsinya sebagai prekursor eikosanoid, EPA mendapat perhatian khusus yang penting secara fisiologis. Asam ini termasuk kelompok substansi yang secara fisiologis potensial, yaitu prostaglandin, tromboksan, dan leukotrien. Ketiga substansi ini terbentuk dari prekursor asam lemak dengan masuknya atom oksigen ke dalam rantai asam lemak. Asam lemak terpenting yang bertindak sebagai prekursor untuk sintesis eikosanoid adalah asam arakidonat. Proses oksigenasi terjadi dalam dua jalur utama, yaitu jalur siklik yang membentuk prostaglandin dan tromboksan, dan jalur linear yang menghasilkan leukotrien. Pembentukan prostaglandin dan tromboksan menjadi penting karena perannya dalam agregasi platelet. Ada dua jenis PUFA yang terlibat dalam produksi kedua substansi tadi, yaitu asam linoleat sebagai prekursor asam arakidonat dan asam linolenat sebagai prekursor EPA dan DHA (Gambar 4)(Groff & Gropper 2000; McCowen & Bistrian 2003).
Gambar 4 Jalur metabolisme asam lemak esensial dari prekursor n-3 dan n-6 (McCowen & Bistrian 2003)
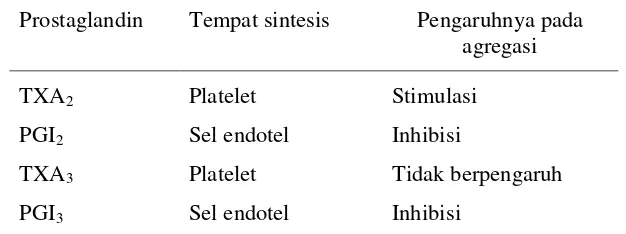
Tabel 4 Tempat sintesis dan pengaruh prostaglandin pada agregasi platelet
Pemberian minyak ikan juga diketahui dapat menekan produksi prostaglandin dan tromboksan dari asam arakidonat, sehingga membatasi pengaruh inflamasi dengan menghasilkan prostaglandin dan leukotrien seri 3 dan 5. Meningkatnya asupan EPA dan DHA dari minyak ikan akan meningkatkan proporsi EPA dan DHA dalam plasma dan fosfolipid eritrosit, berbarengan dengan menurunnya proporsi asam arakidonat dalam plasma dan fosfolipid eritrosit dan menurunnya asam linoleat dalam fosfolipid eritrosit. Selain menghambat agregasi platelet, minyak ikan juga berpengaruh dalam hipolipidemia dan menurunkan kolesterol plasma, yang pada akhirnya akan meminimalisir pembentukan plak. EPA dalam minyak ikan juga dapat menurunkan produksi faktor pengaktif platelet atau platelet activating-factor (PAF), dan bersifat antiinflamasi karena menekan produksi leukotrien-B4 dalam leukosit yang menyebabkan respons inflamasi pada leukosit (Marinetti 1990; McCowen & Bistrian 2003; Trebble et al. 2003).
Minyak ikan mengandung berbagai jenis asam lemak, terutama dari kelompok PUFA n-3. Ikan menyerap dan menyimpan berbagai asam lemak yang tersedia dalam pakannya, selanjutnya juga mengubah komponen lain dari diet seperti alkohol dari ester lilin menjadi asam lemak dan menyimpannya dalam jaringan tubuh. Ikan juga mampu mensintesis asam lemak secara de novo serta melakukan desaturasi dan perpanjangan dari asam lemak yang tersedia. Asam lemak utama dalam minyak ikan adalah EPA dan DHA, yang jumlahnya mencapai 20% atau lebih pada beberapa minyak, di samping sejumlah kecil asam
Tabel 5 Kandungan PUFA n-3 pada beberapa jenis ikan (%)
Dalam tinjauannya Azain (2004) mengungkapkan bahwa pemberian minyak ikan untuk nonruminan dapat meningkatkan kandungan PUFA n-3 dalam jaringan tubuh. Irie dan Sakimoto (1992) melaporkan bahwa pemberian diet dengan 6% minyak ikan untuk babi selama 4 minggu, dapat meningkatkan kandungan EPA dan DHA dalam daging masing-masing 5 dan 10 kali lipat. Untuk memanipulasi profil asam lemak dalam jaringan tubuh ruminansia lebih sulit. Meskipun ada peningkatan PUFA n-3 dalam fosfolipid otot pada pemberian minyak ikan, fraksi tersebut hanya sejumlah kecil dari keseluruhan lemak daging. Namun demikian, peningkatan PUFA n-3 pada daging tanpa lemak (lean) masih dimungkinkan untuk mendapat daging yang mengandung PUFA n-3 dalam jumlah yang cukup berarti (Nettleton 1994).
ini mencerminkan aktivitas dari lechitin cholesteryl acyl transferase. Fraksi cholesteryl ester mengandung sekitar 80% asam lemak tak jenuh atau unsaturated fatty acids (UFA). Komposisi asam lemak dari triasilgliserol dan asam lemak bebas dalam plasma serupa dengan dalam digesta abomasum, yang mencerminkan pencernaan dan transfer lemak diet. Kandungan EPA dan DHA dalam triasilgliserol plasma tidak tercermin dalam triasilgliserol jaringan lemak. Tidak adanya inkorporasi EPA atau DHA ke dalam triasilgliserol jaringan adiposa menunjukkan bahwa pada tingkat intestinal asam lemak tersebut tergabung ke dalam kilomikron triasilgliserol, tetapi tidak ditransfer dari pool plasma ke dalam jaringan adiposa. Hal ini berbeda dari EPA dan DHA yang diserap oleh kelenjar susu dan terinkorporasi ke dalam triasilgliserol susu. Suplementasi minyak ikan tuna pada ruminansia menurunkan kandungan triasilgliserol dan kolesterol plasma karena adanya penghambatan sintesis dalam usus dan hati (Kitessa et al. 2001).
Demirel et al. (2004) melaporkan bahwa perlakuan minyak linseed bersama minyak ikan pada domba meningkatkan konsentrasi EPA dan DHA secara nyata dalam fosfolipid otot dan fraksi lemak netral dan polar dalam hati, dibandingkan dengan pemberian minyak linseed secara tunggal. Perlakuan tersebut juga meningkatkan rasio PUFA:SFA dalam hati dan jaringan adiposa tetapi tidak dalam otot dan memperbaiki rasio PUFA n-6:n-3. Percobaan Gulati et al. (1999) terhadap dosis minyak ikan yang diberikan pada domba menunjukkan adanya hidrogenasi yang cukup besar terhadap EPA dan DHA bila konsentrasi minyak ikan kurang dari 1 mg/ml cairan rumen, sedangkan produksi asam lemak
trans-C18:1 sangat tinggi. Pada konsentrasi minyak ikan yang lebih tinggi, isomer
ini menurun yang menandai adanya penghambatan biohidrogenasi.
Perlindungan Asam Lemak dalam Rumen
Turunnya kecernaan serat kasar karena lemak melapisi partikel pakan, sehingga mencegah pelekatan bakteri selulolitik. Pengaruh penghambatan meningkat seiring tingkat kelarutan, karenanya asam lemak dengan rantai sedang (C 12-14) dan asam lemak tak jenuh (minyak tumbuhan, minyak ikan) merupakan penghambat yang kuat. Asam lemak yang tidak teresterifikasi memiliki efek hambat yang lebih tinggi dari bentuk teresterifikasi, dan minyak bebas lebih menghambat dibandingkan biji-bijian yang diberi utuh (Palmquist 1988; Van Nevel 1991).
Pemberian minyak ikan yang kaya PUFA n-3 dapat mengubah profil asam lemak pada jaringan dan organ tubuh ruminansia, terutama dengan penggabungan EPA dan DHA, sehingga didapatkan produk ternak yang menguntungkan bagi kesehatan manusia. Namun demikian, adanya biohidrogenasi asam lemak yang ekstensif dalam rumen dapat menurunkan keuntungan pemberian PUFA n-3 seperti yang diharapkan. Untuk itu dilakukan perlindungan asam lemak yang dapat mencegah PUFA n-3, terutama EPA dan DHA, mengalami perubahan dalam rumen, sehingga memungkinkan penggabungannya dalam jaringan tubuh ruminansia (Jones et al. 2005).
demikian, dilaporkan adanya hidrogenasi parsial terhadap asam lemak dalam rumen, karena sabun yang terbentuk mengalami disosiasi dalam rumen. Disosiasi meningkat jika pH rumen menurun dan kejadian ini lebih tinggi pada PUFA dibandingkan asam lemak jenuh. Teknik terbaru yang mulai dikembangkan adalah perlindungan asam lemak dalam bentuk amida asam lemak (Palmquist 1988; Tamminga & Doreau 1991; Chilliard et al. 2000).
Amida asam lemak dihasilkan dengan mereaksikan asam lemak dengan amina. Berdasarkan laju degradasi amida yang rendah oleh suspensi populasi bakteri dan kebutuhan gugus karboksil bebas untuk biohidrogenasi oleh mikrob rumen, Fotouhi dan Jenkins (1992a) menyatakan bahwa amida dari UFA akan tahan terhadap biohidrogenasi oleh mikrob rumen. Mikrob rumen memerlukan gugus karboksil bebas untuk menghilangkan ikatan rangkap dari UFA. Dari dua percobaan in vitro terlihat penurunan kehilangan asam linoleat pada kultur rumen jika UFA diberikan sebagai amida dibandingkan sebagai asam lemak bebas. Pemberian linoleamida juga mengurangi destruksi ruminal dari asam linoleat dibandingkan dengan pemberian asam linoleat tidak terlindungi atau kalsium linoleat (Fotouhi & Jenkins 1992b).
Jenkins (1995) mensintesis amida skunder dari butilamina dan minyak kedelai mengikuti metode Feairheller et al. (1994), untuk mengukur ketahanannya terhadap biohidrogenasi dalam rumen. Dengan penambahan masing-masing 5% butilsoyamida dan minyak kedelai pada pakan, ternyata dapat meningkatkan konsentrasi asam linoleat plasma 22% pada pemberian minyak kedelai dan 58% pada pemberian butilsoyamida dibandingkan kontrol. Jenkins (1997) juga mensintesis amida dengan mereaksikan minyak kedelai dengan ethanolamina
menghasilkan N-hidroksietilsoyamida. Butilsoyamida dan
Pada percobaan in vivo, Lundy et al. (2004) mengevaluasi biohidrogenasi asam oleat dan linoleat dalam bentuk minyak kedelai, kalsium minyak kedelai, dan amida minyak kedelai pada sapi perah laktasi. Aliran asam lemak pascarumen dan laju biohidrogenasi diukur dari sampel omasal, dan didapatkan bahwa pemberian minyak kedelai dalam bentuk garam kalsium dan amida belum mampu menurunkan biohidrogenasi asam linoleat secara berarti, namun amida mampu menurunkan biohidrogenasi asam oleat secara nyata. Tampaknya efektivitas ketahanan garam kalsium atau amida terhadap biohidrogenasi bergantung pada jenis asam lemak dan komposisi asam lemak.
MATERI DAN METODE
Penelitian ini dilaksanakan di Laboratorium Biologi Hewan Pusat Penelitian Sumberdaya Hayati dan Bioteknologi, Pusat Antar Universitas (PPSHB-PAU), Laboratorium Ternak Perah Fakultas Peternakan, dan Laboratorium Hewan Percobaan Southeast Asian Food and Agricultural Science
and Technology Center (SEAFAST Center) Institut Pertanian Bogor. Penelitian
ini terdiri atas tiga tahap, yaitu pembuatan amida minyak ikan, uji ketahanan amida minyak ikan secara in vitro, dan uji efektivitas suplementasi amida minyak ikan pada tikus sebagai hewan coba pascarumen.
Sintesis Amida Minyak Ikan
Minyak ikan yang digunakan untuk pembuatan amida minyak ikan lemuru yang diperoleh dari Desa Muncar Banyuwangi, Jawa Timur. Selama penyimpanan, minyak ikan ditambahkan butylated hydroksitoluen (BHT) untuk melindungi minyak dari ketengikan oksidatif. Sebelum dilakukan reaksi amidasi ditentukan dahulu bilangan iod, bilangan penyabunan, dan bilangan asam minyak ikan yang digunakan. Kandungan asam lemak utama dalam minyak ikan ditentukan menggunakan kromatografi gas dengan detektor ionisasi nyala atau
gas liquidchromatography flame ionized detector (GLC FID).
Proses amidasi dilakukan dengan tiga cara berbeda untuk mendapatkan hasil yang terbaik yaitu:
1. Sintesis amida minyak ikan dengan mereaksikan minyak ikan dan urea, dengan perbandingan 1:1 (w/w) menurut prosedur Jenkins dan Adams (2002). Reaksi dilakukan dalam reaktor amidasi vakum dengan kapasitas 500 ml dengan diameter 10 cm, yang dilengkapi dengan pengaduk. Suhu pemanasan selama reaksi berlangsung dikontrol dengan menggunakan termokopel. Pembuatan amida minyak ikan dilakukan pada suhu 90⁰C dengan lama reaksi 4 jam. Produk yang dihasilkan disaring dengan kertas saring.
suhu 75⁰C selama 2 jam, dengan flushing N2. Etil ester minyak ikan yang terbentuk direaksikan dengan urea dengan rasio molar 1:2, pada suhu 90⁰C dengan pengadukan. Produk yang dihasilkan disaring dengan kertas saring.
3. Sintesis amida minyak ikan dengan mereaksikan minyak ikan dan n-butilamin mengikuti metode Feairheller et al. (1994). Minyak ikan direaksikan dengan n-butilamin dengan rasio molar 1 :8. Ke dalam bahan juga ditambahkan Na-EDTA sebanyak 0.5% (w/w) dan BHT sebanyak 0.05% (w/w), sebagai antioksidan selama proses amidasi berlangsung. Bahan dipanaskan dengan hot plate dalam labu empat leher yang dihubungkan dengan kondensor refluks dan dilakukan flushing N2 untuk mengusir O2. Suhu dipertahankan pada kisaran 77-78⁰C, yang merupakan titik didih n-butilamin, dengan kecepatan pengadukan 150 rpm selama 5 jam. Setelah proses berakhir, produk dilarutkan kembali dengan heksan, selanjutnya dicuci dengan akuades 70⁰C 3-4 kali untuk membuang kelebihan butilamin dan gliserol. Kemudian produk dievaporasi dengan rotavapor dan selanjutnya dikompressor untuk menguapkan dan menghilangkan sisa heksan. Analisis kualitatif dilakukan untuk mengidentifikasi terbentuknya senyawa amida dengan menggunakan spektroskopi inframerah atau infra red (IR). Analisis semi kuantitatif untuk mengetahui jumlah senyawa amida yang dihasilkan dilakukan dengan menggunakan kromatografi gas dengan spektrometer massa atau gas chromatography mass spectrometry GC-MS. Analisis proksimat dilakukan untuk mengetahui kadar lemak dan N dari produk. Pengukuran bilangan iod setelah reaksi juga dilakukan untuk mengetahui derajat ketidakjenuhan yang masih bisa dipertahankan.
Metode Analisis Minyak ikan dan Amida Minyak Ikan Bilangan iod
ml kloroform untuk melarutkan sampel, dan 25 ml pereaksi Hanus kemudian dibiarkan selama 1 jam di tempat gelap sambil sekali-sekali dikocok. Kemudian ditambahkan 10 ml larutan KI 15 % lalu dikocok. Erlenmeyer dan tutupnya dicuci dengan 100 ml akuades. Titrasi dengan larutan standar Na2S2O3 0.1 N sampai warna kuning iod hampir hilang, kemudian ditambahkan 2 ml larutan pati 1% sebagai indikator. Titrasi dilanjutkan sampai warna biru hilang. Di samping itu juga dilakukan penetapan blanko.
ml titrasi (blanko-sampel) x N Na2S2O3 x 12.69 Bilangan Iod = --- berat sampel (gram)
Bilangan penyabunan
Bilangan penyabunan adalah jumlah miligram KOH yang diperlukan untuk menyabunkan satu gram minyak atau lemak. Penentuan bilangan penyabunan dilakukan dengan metode titrasi (Apriyantono et al. 1989). Sejumlah bahan ditimbang (1-5 gram) dalam erlenmeyer 300 ml dan ditambahkan 50 ml KOH beralkohol. Kemudian dihubungkan dengan pendingin tegak dan direfluks hingga tersabunkan sempurna. Larutan didinginkan dan ditambahkan 1 ml indikator fenolftalen. Kemudian dititrasi dengan HCl 0.5 N sampai warna merah jambu hilang. Buat penetapan blanko seperti penetapan contoh.
ml titrasi (blanko-sampel) x N HCl x 56.1 Bilangan Penyabunan = --- bobot sampel (gram)
Bilangan asam
penghitungan jumlah miligram KOH yang digunakan untuk menetralkan asam lemak bebas dalam 1 gram minyak atau lemak.
ml titrasi sampel x KOH x 56.1 Bilangan Asam = --- bobot sampel (gram)
Uji Ketahanan Amida Minyak Ikan secara In Vitro
Percobaan in vitro dilakukan menurut metode Tilley dan Terry (1963), untuk mengetahui ketahanan amida asam lemak minyak ikan terhadap biohidrogenasi oleh bakteri rumen dengan inkubasi menurut perlakuan untuk mengetahui pelepasan asam lemak pascarumen. Unit percobaan dilakukan secara terpisah. Penambahan lemak baik dalam bentuk minyak ikan maupun amida minyak ikan, sebanyak 10% dari ransum. Senyawa amida yang tersisa dalam kultur dianalisis menggunakan GC-MS. Percobaan in vitro juga dilakukan untuk mengetahui pengaruh pemberian amida asam lemak pada pH cairan rumen, konsentrasi N-NH3, VFA total cairan rumen, VFA parsial, produksi gas, jumlah protozoa, protein mikrob, degradasi bahan kering (DBK) dan bahan organik (DBO) pakan.
Sumber inokulum yang digunakan adalah cairan rumen domba, dan sebagai substrat adalah hijauan jagung yang telah digiling halus. Berdasarkan analisis proksimat, substrat hijauan jagung mengandung 91.82% bahan kering, 7.68% protein, 1.54% lemak, 28.88% serat kasar, 9.81% abu, dan 52.09% BETN.
Percobaan menggunakan Rancangan Acak Kelompok yang terdiri atas 4 perlakuan, dengan masing-masing 3 kelompok pengambilan cairan rumen sebagai berikut:
R0 = Substrat hijauan jagung
R1 = R0 yang mengandung 10% minyak ikan
Metode Analisis In Vitro
Degradasi bahan kering (DBK) dan bahan organik (DBO) in vitro
Inkubasi in vitro dilakukan dengan metode Tilley dan Terry (1963). Sampel yang telah disiapkan ditimbang sebanyak 0.5 gram dan dimasukkan ke dalam tabung fermentor berkapasitas 100 ml. Larutan medium buffer yang terdiri atas 2 gram trypticase, 400 ml air, 0.1 ml larutan mikromineral ditempatkan di dalam erlenmeyer dan diaduk hingga larut. Selanjutnya ditambahkan 200 ml larutan buffer, 200 ml larutan mikromineral, dan 1 ml resazurin dan 40 ml larutan pereduksi. Medium lalu ditempatkan ke dalam water bath pada suhu 39⁰ C sambil dialirkan gas CO2 dan diaduk dengan magnetic stirrer, hingga terjadi perubahan warna medium dari biru ke merah muda hingga menjadi bening tidak berwarna yang menandai medium telah tereduksi dengan sempurna. Selanjutnya 1 bagian rumen dicampur dengan 4 bagian medium di bawah aliran gas CO2 di dalam
water bath sambil terus diaduk. Sebanyak 50 ml campuran medium diambil dan
dimasukkan ke dalam masing-masing tabung fermentor yang telah berisi sampel dan 2 tabung fermentor yang tidak berisi sampel (blanko). Tabung fermentor ditutup dengan tutup karet berventilasi, dan diinkubasi secara anaerob menurut perlakuan, yaitu selama 0, 24 dan 48 jam dalam shaker water bath pada suhu 39⁰ C. Setelah inkubasi berakhir kultur ditetesi 2-3 tetes asam sulfat pekat, H2SO4 9M kemudian disentrifus dengan kecepatan 3000 rpm. Supernatan diambil untuk analisis VFA, N-NH3, dan senyawa amida, sisanya disaring menggunakan kertas saring Whatman no. 41, lalu ditentukan kadar bahan kering dan bahan organiknya. Degradasi bahan kering (DBK) dan bahan organik (DBO) dihitung dengan persamaan :
Pengukuran VFA parsial
Untuk analisis VFA, supernatan diambil sebanyak 2 ml dan dimasukkan ke dalam tabung sampel yang bertutup. Ke dalam tabung tersebut ditambahkan 30 mg 5-sulphosalicylic acid (C6H3(OH)SO3H H2O) lalu dikocok. Kemudian disentrifus dengan kecepatan 3000 rpm selama 10 menit dan disaring dengan milipore hingga diperoleh cairan jernih. Sebanyak 1 µl cairan jernih diinjeksikan ke gas kromatografi (AOAC 1995). Sebelum injeksi sampel, terlebih dahulu
Kadar VFA total ditentukan dengan metode destilasi uap (General Laboratory Procedure 1966). Sebanyak 5 ml supernatan dimasukkan ke dalam tabung destilasi yang dipanaskan dengan uap air. Tabung segera ditutup rapat setelah ditambahkan 1 ml H2SO4 15%. Uap air panas akan mendesak VFA melewati tabung destilasi yang terkondensasi dan ditampung dengan erlenmeyer yang berisi 5 ml NaOH 0.5 N sampai mencapai volume sekitar 300 ml. Selanjutnya ditambahkan indikator penophtalein sebanyak 2 tetes dan dititrasi dengan HCl 0.5 N. Titrasi berakhir pada saat titik awal perubahan warna dari
dengan asam borat berindikator metil red dan brom kressol green sebanyak 1 ml. Kemudian cawan Conway ditutup rapat dengan tutup bervaselin, digoyang dengan perlahan hingga supernatan tercampur dengan larutan Na2CO3. Amonia yang dibebaskan dari reaksi antara kedua bahan tersebut, selanjutnya akan ditangkap oleh asam borat yang diperlihatkan dengan adanya perubahan warna. Setelah dibiarkan selama 24 jam dalam suhu kamar, amonium borat dititrasi dengan H2SO4 0.005 N sampai terjadi perubahan warna ke warna asal asam borat (merah muda).
Volume titran dicatat, dan kadar N-NH3 dapat dihitung dengan rumus: N-NH3 = (ml H2SO4 x N H2SO4 x 1000) mM
Pengukuran Produksi Gas
Pengukuran produksi gas mengikuti prosedur Close dan Menke (1986) sebagai berikut: Syringe kapasitas 100 ml diisi dengan 0.2 g sampel, kemudian ditambahkan 30 ml cairan rumen yang telah dicampur dengan larutan buffer dengan perbandingan 1:2. Selanjutnya syringe diinkubasi dalam shaker waterbath Pada suhu 39⁰C. Pengamatan dilakukan pada 0, 12, dan 48 jam dengan mencatat volume gas yang terbentuk selama proses fermentasi.
Pengukuran sintesis protein mikrob
Sebanyak dua ml supernatan dimasukkan ke dalam tabung eppendorf, kemudian disentrifus dengan kecepatan 15 000 rpm pada suhu 4⁰C selama 30 menit. Endapan yang terbentuk dibilas dengan akuades selanjutnya disentrifus lagi pada kondisi yang sama. Selanjutnya, endapan disuspensikan dengan 2 ml NaOH 1 N, divortex lalu dipanaskan pada air bersuhu 60-70⁰C selama 10 menit. Analisis protein mikrob dilakukan menurut Lowry et al. (1951). Pembacaan absorbansi dilakukan pada 660 nm dan kadar protein sampel (mg/L) dapat dihitung berdasarkan persamaan regresi kurva standar.
Perhitungan jumlah protozoa
hemositometer dan jumlah protozoa dapat dilihat di bawah mikroskop dengan pembesaran 400 kali.
Efektivitas Suplementasi Amida Minyak Ikan pada Tikus sebagai Hewan Model Pascarumen
Percobaan in vivo bertujuan untuk mempelajari efektivitas suplementasi amida minyak ikan, dengan menggunakan hewan coba tikus sebagai model pascarumen. Percobaan ini menggunakan 35 ekor tikus jantan strain Sprague Dawley, yang berumur 7 minggu dengan kisaran bobot badan 120-160 g, yang diperoleh dari Balai Penelitian Veteriner Bogor.
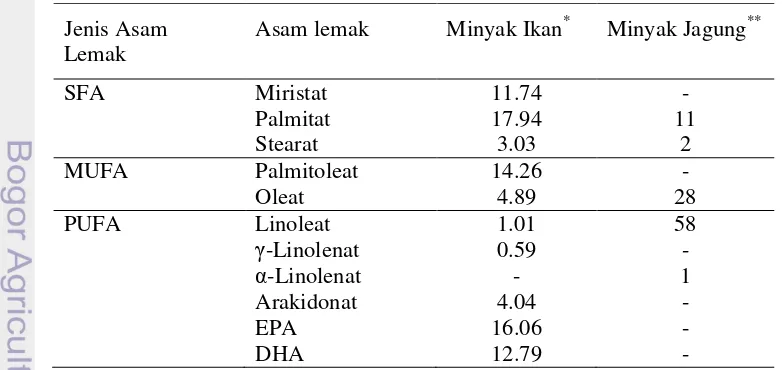
Tikus ditempatkan di kandang individu berupa bak plastik yang dilengkapi dengan panggung kasa , dasarnya beralas koran yang diganti setiap hari. Kandang dibersihkan dua kali seminggu. Ransum tikus diformulasi berdasarkan metode AOAC (1990) berupa ransum semi purified yang mengandung minyak jagung sebagai ransum standar, dengan suplementasi minyak ikan dan amida minyak ikan menurut perlakuan (Tabel 7). Masa adaptasi dilakukan selama 7 hari dengan pemberian ransum standar. Tikus dibagi secara acak ke dalam 5 perlakuan dengan jumlah masing-masing perlakuan sebanyak 7 ekor. Ransum percobaan dan air minum diberikan secara ad libitum selama 6 minggu. Komposisi minyak ikan dan minyak jagung, tersaji pada Tabel 6 berikut.
Tabel 6 Komposisi minyak ikan dan minyak jagung (%)
Jenis Asam
Keterangan : * Hasil Analisis Laboratorium Kimia Terpadu IPB (2010)
Penelitian ini menggunakan rancangan acak lengkap (RAL), dengan perlakuan sebagai berikut:
A= Kontrol (sumber lemak 8% minyak jagung) B= Suplementasi 4,5% minyak ikan
C= Suplementasi 3% minyak ikan dan 1,5% amida minyak ikan D= Suplementasi 1,5% minyak ikan dan 3% amida minyak ikan E = Suplementasi 4,5% amida minyak ikan
Tabel 7 Susunan ransum percobaan in vivo
Sumber: Hasil Analisis Laboratorium Biologi Hewan, PPSHB IPB (2011)
Pengambilan Data dan Sampel
Pada akhir percobaan, dilakukan pengambilan darah melalui jantung menggunakan alat suntik setelah tikus dibius dengan eter, kemudian darah dimasukkan ke dalam tabung yang berisi antikoagulan EDTA. Sampel darah dibagi menjadi dua, yaitu untuk analisis hematologi dan untuk analisis profil lemak darah. Tikus dibunuh, daging paha belakang diambil untuk analisis kadar lemak daging, komposisi asam lemak, dan kadar kolesterol daging.
Metode Analisis In Vivo
Pertambahan bobot badan
Dihitung berdasarkan selisih bobot badan akhir dengan bobot badan awal dibagi lama waktu pengamatan. Penimbangan bobot badan tikus dilakukan setiap minggu.
Konsumsi ransum
Dihitung berdasarkan jumlah ransum yang disediakan dikalikan dengan kandungan bahan keringnya, dikurangi sisa ransum dikalikan dengan bahan kering sisa ransum tersebut.
Konversi pakan
Diperoleh berdasarkan jumlah konsumsi bahan kering pakan dibagi dengan kenaikan bobot badan per satuan waktu.
Kecernaan zat makanan
Dihitung berdasarkan selisih zat-zat makanan dari konsumsi ransum yang diukur dengan zat makanan yang terkandung dalam feses, dibagi dengan zat-zat makanan yang dikonsumsi, selama masa koleksi feses (10 hari).
Pengukuran nilai hematologi darah.
dan angka hematokrit dicatat (Sastradipraja et al., 1989). Pengukuran kadar hemoglobin (Hb) dengan metode Cyanmethemoglobin (Merck, 1987).
Pengukuran kadar kolesterol dan trigliserida serum
Kolesterol serum ditentukan dengan metode CHOD-PAP (Cholesterol
Oxidase Phenol Amino Phenazone), yang merupakan enzymatic photometric test.
Prinsip pengukuran kolesterol dengan metode ini melibatkan enzim cholesterol
esterase yang memecah ikatan ester kolesterol menjadi kolesterol dan asam
lemak. Selanjutnya enzim cholesterol oksidase mengoksidasi kolesterol menjadi
cholest-3-one dan hidrogen peroksida. Hidrogen peroksida bereaksi dengan
4-aminoantipyrine dan fenol dengan adanya enzim peroksidase membentuk pigmen quinoneimine sebagai indikator colorimetri. Spesimen yang digunakan adalah serum atau standar sebanyak 10 µl ditambah 1 ml reagensia, kemudian dikocok sampai homogen. Sebagai blanko digunakan air suling sebanyak 10 µl yang ditambah 1 ml reagensia. Selanjutnya diinkubasi selama 20 menit pada suhu 20-25⁰C, dan dibaca absorbansinya pada panjang gelombang 500 nm dengan alat
spektrofotometer. Sebagai blanko digunakan air suling sebanyak 50 µl yang ditambah 1 ml reagensia.
Konsentrasi kolesterol dalam supernatan dapat dihitung dengan rumus:
A sampel
Kolesterol (mg/dl) = --- x kons. Standar (mg/dl) A standar
Kolesterol-LDL = Kolesterol total – kolesterol dalam supernatan
Prinsip penentuan kolesterol HDL didasarkan pada pengendapan kolesterol LDL, VLDL dan kilomikron dengan penambahan phosphotungstic acid dengan adanya ion magnesium. Setelah disentrifus, konsentrasi kolesterol dalam fraksi HDL yang berada dalam supernatan dapat diukur. Serum sebanyak 500 µl dimasukkan ke dalam tabung sentrifuse, ditambahkan 1 ml reagen pengendap, kemudian dikocok sampai homogen. Campuran dibiarkan selama 10 menit pada suhu kamar, kemudian disentrifus selama 2 menit dengan kecepatan 12.000 rpm. Supernatan yang jernih dipisahkan untuk dilakukan penentuan kadar kolesterol dengan metode CHOD-PAP.
Supernatan atau standar sebanyak 100 µl selanjutnya dimasukkan ke dalam tabung, ditambahkan 1 ml reagensia dan dikocok hingga homogen. Campuran diinkubasi selama 10 menit pada suhu 20-25⁰C, dan dibaca absorbansinya pada panjang gelombang 500 nm dengan alat spektrofotometer. Sebagai blanko digunakan air suling sebanyak 100 µl yang ditambah 1 ml reagensia.
Konsentrasi kolesterol-HDL dalam supernatan adalah:
A sampel
Kolesterol-HDL (mg/dl) = --- x kons. Standar (mg/dl) A standar
4-chlorophenol dengan adanya enzim peroksidase membentuk pigmen quinoneimine sebagai indikator colorimetri. Spesimen yang digunakan adalah serum atau standar sebanyak 10 µl ditambah 1 ml reagensia, kemudian dikocok sampai homogen. Sebagai blanko digunakan air suling sebanyak 10 µl yang ditambah 1 ml reagen. Selanjutnya diinkubasi selama 20 menit pada suhu 20-25⁰ C, dan dibaca absorbansinya pada panjang gelombang 500 nm dengan alat
Untuk mengoreksi gliserol bebas, konsentrasi trigliserida dari perhitungan di atas dikurangi 10 mg/dl.
Komposisi asam lemak daging
Lemak daging diekstraksi dengan petroleum eter dengan metode soxhlet. Komposisi asam lemak dianalisis sesuai dengan AOAC (1995). Sampel hasil ekstraksi sebanyak 100 mg ditambah 4 ml NaOH 0.5 N di bawah gas nitrogen, dikocok, tutup rapat dan dipanaskan pada suhu 100⁰C selama 5 menit. Kemudian 5 ml BF3 - metanol (boron triflouride 7% dalam metanol). Kemudian ditutup (heksan) diambil dan ditambahkan Na2SO4 anhidrat, kemudian didiamkan selama 10 menit. Heksan dipekatkan, lalu diinjeksikan 2 µl ke dalam Gas Chromatography.
Kolesterol daging dan feses
ml, dan diuapkan di penangas air. Residu diuapkan dengan kloroform sedikit demi sedikit, sambil dituangkan ke dalam tabung berskala sampai volume 5 ml, ditambahkan asam asetat anhidrat, lalu ditambahkan 0.2 ml H2SO4 pekat (p.a). Campuran dikocok dan dibiarkan di tempat gelap selama 15 menit. Kemudian absorbansinya dibaca pada gelombang 420 nm dengan standar yang digunakan 0.4 mg/ml.
Kadar kolesterol daging dapat dihitung dengan rumus :
(A sampel x konsentrasi sampel)/bobot sampel Kadar kolesterol = ---
A standar
Analisis Data