ABSTRAK
KUALITAS SEMEN BEKU SAPI BALI DENGAN PENAMBAHAN BERBAGAI DOSIS VITAMIN C PADA BAHAN PENGENCER
SKIM KUNING TELUR
Oleh
FARADINA KUSUMA SAVITRI
Penelitian yang dilaksanakan di Unit Pelayanan Teknis Daerah Balai Inseminasi Buatan Daerah (UPTD-BIBD) Lampung, Kecamatan Terbanggi Besar, Kabupaten Lampung Tengah, Provinsi Lampung pada 18--25 April 2014, bertujuan untuk mengetahui pengaruh penambahan antioksidan vitamin C (asam askorbat) dalam pengencer skim kuning telur terhadap persentase motilitas dan persentase hidup spermatozoa. Rancangan percobaan yang digunakan pada penelitian ini adalah Rancangan Acak Lengkap (RAL) dengan perlakuan yang diberikan yaitu P1 (tanpa penambahan vitamin C), P2 (penambahan 1,50 mM vitamin C), P3 (penambahan 2,50 mM vitamin C), P4 (penambahan 3,50 mM vitamin C), P5 (penambahan 4,50 mM vitamin C) dalam pengencer susu skim kuning telur dan masing-masing perlakuan dilakukan pengulangan sebanyak tiga kali. Data yang diperoleh dianalisis ragam pada taraf nyata 5%. Hasil penelitian menunjukkan bahwa penambahan berbagai dosis vitamin C ke dalam pengencer susu skim kuning telur menghasilkan pengaruh yang tidak berbeda nyata (P>0,05) terhadap persentase motilitas spermatozoa dan persentase spermatozoa hidup.
RIWAYAT HIDUP
Penulis dilahirkan di Pringsewu pada 28 November 1992 sebagai anak pertama
dari dua bersaudara, putri pasangan Bapak drh. Nur Rokhmad dan Ibu Dra. Titie
Widowati Prayogani.
Penulis menyelesaikan pendidikan taman kanak-kanak (TK) pada tahun 1998 di
TK. AB, Poncowarno, Lampung Tengah; pendidikan sekolah dasar (SD) pada
tahun 2004 di SD Negeri 1 Poncowati, Lampung Tengah; pendidikan sekolah
menengah pertama (SMP) pada tahun 2007 di SMP Negeri 1 Terbanggi Besar,
Lampung Tengah; dan pendidikan sekolah menengah atas (SMA) pada tahun
2010 di SMA Negeri 1 Terbanggi Besar, Lampung Tengah. Ditahun yang sama
penulis terdaftar sebagai mahasiswa Jurusan Peternakan, Fakultas Pertanian,
Universitas Lampung melalui jalur Seleksi Nasional Masuk Perguruan Tinggi
Negeri (SNMPTN).
Selama masa perkuliahan penulis pernah melakukan magang kerja di Farm
Sidomulyo, Lampung Selatan milik PT. Rama Jaya Lampung; Praktik Umum
(PU) di Balai Inseminasi Buatan (BIB) Ungaran, Jawa Tengah; dan Kuliah Kerja
Nyata (KKN) di Desa Karya Mulya Sari, Lampung Selatan. Penulis aktif dalam
kegiatan Himpunan Mahasiswa Peternakan (HIMAPET) FP UNILA sebagai
Anggota bidang Pengabdian Masyarakat periode 2012--2013 dan Sekretaris
Ku persembahkan Skripsi ini kepada :
Mama, Papa, Adik,
Tante, Om, Sepupu,
Guru, dan Sahabat,
Almamater,
Indonesia
Atas salah satu bukti
Rasa terimakasih, kerja keras, dan
Ingatlah Allah ketika kamu bahagia,
maka Allah akan mengingatmu ketika kamu sengsara,
jadilah kamu pengajar atau pelajar atau pendengar,
janganlah sekali-kali kamu menjadi orang yang bodoh (tidak mau belajar)
karena kamu pasti celaka.
(Abu Darda’)
KATA PENGANTAR
Bismillahirrahmaanirrahiim
Segala puji bagi Allah SWT, karena berkat rahmat, hidayah, dan kehendak-Nya
lah sehingga penulis dapat menyelesaikan skripsi ini, dalam kesempatan ini
penulis mengucapkan terimakasih kepada :
1. Ibu Sri Suharyati, S.Pt, M.P.— selaku Pembimbing Utama — atas
bimbingan, kesabaran, saran dan arahan dalam menyelesaikan skripsi;
2. Bapak Siswanto, S.Pt., M.Si.— selaku Pembimbing Anggota — atas
bimbingan, saran dan arahan dalam menyelesaikan skripsi;
3. Bapak drh. Madi Hartono, M.P.— selaku Penguji Utama — atas bimbingan,
saran dan arahan dalam menyelesaikan skripsi;
4. Bapak Ir. Yusuf Widodo, M.P.— selaku Pembimbing Akademik — atas
bimbingan, saran dan arahan selama masa perkuliahan;
5. Bapak Prof. Dr. Ir. Muhtarudin, M.S.— selaku Ketua Jurusan Peternakan,
Fakultas Pertanian, Universitas Lampung;
6. Bapak Prof. Dr. Ir. Wan Abbas Zakaria, M.S.— selaku Dekan Fakultas
Pertanian, Universitas Lampung;
7. Ibu dan Bapak Dosen di Jurusan Peternakan atas ilmu dan dukungannya;
8. Bapak Ir. Agust A. Arabusman — selaku Kepala Balai Inseminasi Buatan
9. Mas drh. Akbar , Mba Murtiawan, S.Pt., Bapak Ir. Joko, dan Mas Vivid
Bambang SN, S.Pt. —atas bimbingan, saran dan arahan selama pelaksanaan
penelitian;
10. Mama, Papa, Fariz Kusuma Aditya, Om, Bulek, dan Sepupu-sepupu —atas
doa, nasehat, perhatian, kesabaran, kasih sayang, materil serta dukungan yang
tak henti-hentinya;
11. Ajrul Mukminat —atas kesabaran, pengertian, perhatian, dukungan,
kerjasama, bantuan, pelajaran, kasih sayang, dan persaudaraan, semoga tetap
bertahan;
12. Nano Setiono, Febi Aditya, Heru Yoga Prawira, Rahmadhanil Putra Rusadi,
Rangga Saputra, Tri Haryanto Saputra, dan Yuli Prasetiyo —atas kesabaran,
pengertian, perhatian, dukungan, kerjasama, bantuan, pelajaran, dan
persaudaraan, semoga tetap bertahan;
13. Saudara peternakan angkatan 2010 (Rizki Indah, Fandi, Nurma, Sekar, Irma,
Nani, Sherly, Tiwi, Anung, Dian, Repi, Dewa, Afrizal, Etha, Gaby, Nova,
Alm. Anggiat, Fauzan, Fajar, Rahmat, Rohmat, Repki, Aini, dkk) —atas
persaudaraan, bantuan, semangat, dukungan dan kebersamaan yang selalu
diberikan, semoga tetap bertahan;
Semoga segala kebaikan yang telah diberikan kepada penulis menjadi amal baik
dan mendapat balasan yang berlipat dari Allah SWT. Semoga bermanfaat.
Bandar Lampung, 2014
Penulis,
I. PENDAHULUAN
A. Latar Belakang
Berdasarkan Data Statistik 2013 jumlah penduduk Indonesia mencapai
242.013.800 jiwa yang akan bertambah sebesar 1,49% setiap tahunnya
(Anonim,2013). Jumlah penduduk yang terus meningkat berkorelasi positif
dengan kebutuhan protein hewani, semakin banyak jumlah penduduk Indonesia
maka semakin tinggi pula kebutuhan protein hewani. Pemenuhan protein hewani
dapat dilakukan dengan cara meningkatkan produksi daging ternak. Salah satu
ternak penghasil daging adalah sapi potong.
Sapi Bali adalah jenis sapi potong asli Indonesia yang berpotensi besar untuk terus
dikembangkan. Menurut Suryana (2009) Sapi Bali memiliki daya adaptasi baik
terhadap berbagai kondisi lingkungan kering maupun hujan. Wahyuni (2000),
mengatakan bahwa Sapi Bali memiliki beberapa keunggulan karakteristik yaitu
mempunyai fertilitas tinggi, lebih tahan terhadap kondisi lingkungan yang kurang
baik, cepat beradaptasi apabila dihadapkan dengan lingkungan baru, dan cepat
berkembang biak. Keunggulan-keunggulan ini harus didorong dengan kemajuan
teknologi khususnya teknologi reproduksi. Teknologi reproduksi yang sangat
menunjang dan cocok diaplikasikan di lapangan untuk pengembangan Sapi Bali
2
Teknologi IB memanfaatkan semen pejantan unggul yang telah dibekukan serta
telah mengalami evaluasi dan pengenceran. Menurut Toelihere (2006),
keberhasilan program IB ditentukan oleh empat faktor utama yaitu kualitas semen,
kesuburan ternak betina, keterampilan teknisi, dan pengetahuan zooteknik
peternak. Toelihere (1985) mengatakan bahwa proses pengolahan seperti
penampungan semen, pengenceran, ekuilibrasiatau penyesuaian suhu, dan
pembekuan memengaruhi kualitas semen beku yang akan diaplikasikan pada
ternak.
Goldman dkk., (1991) mengatakan bahwa selama proses pembekuan semen,
terjadi kematian spermatozoa sampai 30% dari jumlah spermatozoa segar, karena
spermatozoa memiliki sifat sangat peka terhadap lingkungan seperti perubahan
suhu. Kematian spermatozoa yang tinggi pada proses pengolahan semen menurut
Herdis (2005) disebabkan oleh rusaknya membran plasma spermatozoa akibat
peroksida lipid. Maxwell dan Watson (1996) juga berpendapat bahwa kematian
spermatozoa terjadi karena membran spermatozoa banyak mengandung lemak tak
jenuh yang sangat rentan terhadap reaksi peroksida lipid.
Reaksi peroksida lipid yang dapat merusak spermatozoa dalam proses pengolahan
semen terjadi karena kontak antara semen dan oksigen (O2). Menurut Siregar
(1992), oksigen merupakan unsur yang esensial, tetapi kelebihan oksigen
menyebabkan kerusakan peroksidatif. Rizal dan Herdis (2010) mengatakan bahwa
selama proses respirasi oksigen mengalami reduksi dalam rangkaian elektron
dan hidrogen peroksida. Radikal bebas jika bereaksi dengan asam lemak tak jenuh
akan menghasilkan lipid peroksida.
Menurut Rizal dan Herdis (2010) radikal bebas adalah senyawa kimia yang
memiliki elektron tak berpasangan dan bersifat sangat reaktif. Siswono (2005)
mengatakan bahwa sumber radikal bebas bisa berasal dari proses metabolisme
dalam tubuh dan dapat berasal dari luar tubuh. Maxwell dan Watson (1996)
berpendapat bahwa kerusakan yang diakibatkan oleh radikal bebas dan peroksida
lipid ini dapat menurunkan tingkat motilitas dan daya hidup spermatozoa.
Penambahan antioksidan dalam pengencer semen dilakukan untuk meminimalisir
atau menekan kerusakan membran spermatozoa akibat radikal bebas. Widiastuti
(2001) mengatakan bahwa penambahan antioksidan dalam pengencer semen
berfungsi untuk memutus atau menekan reaksi radikal bebas dan mampu untuk
mengakhiri siklus reaksi. Berakhirnya siklus reaksi radikal bebas dapat
menghentikan kerusakan membran spermatozoa akibat peroksida lipid yang dapat
menurunkan kemampuan fertilitas semen beku. Beconi dkk., (1993) mengatakan
bahwa vitamin C dan E mampu melindungi membran plasma spermatozoa sapi
selama proses pembekuan dan pencairan kembali.
Almatsier (2009) mengatakan bahwa vitamin C berbentuk kristal putih yang
memiliki sifat mudah larut dalam air. Suryohudoyo (2000) menambahkan bahwa
vitamin C atau asam askorbat termasuk dalam antioksidan yang mampu memutus
rantai reaksi radikal bebas. Vitamin C mempunyai kemampuan menguatkan
kestabilan jaringan pelindung membran plasma terhadap peroksida lipid, sehingga
4
yang asam oleh karena itu penambahannya ke dalam pengencer harus
memperhatikan perubahan pH yang akan terjadi.
Berdasarkan uraian di atas perlu dilakukanya penelitian tentang pengaruh
penambahan vitamin C sebagai antioksidan ke dalam pengencer semen sapi
terhadap persentase motilitas dan persentase hidup spermatozoa
B. Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. mengetahui pengaruh penambahan antioksidan vitamin C (asam askorbat)
dalam pengencer semen sapi terhadap persentase motilitas dan persentase
hidup spermatozoa;
2. mengetahui dosis penambahan antioksidan vitamin C yang terbaik dalam
pengencer semen sapi yang dapat mempengaruhi persentase motilitas dan
persentase hidup spermatozoa.
C. Kegunaan Penelitian
Hasil dari penelitian ini diharapkan mampu memberikan informasi tentang
manfaat penambahan vitamin C dalam pengencer semen sapi terhadap persentase
motilitas dan persentase hidup spermatozoa yang dapat memengaruhi fertilitas
D. Kerangka Pemikiran
Semen beku adalah semen segar dari pejantan yang sudah mengalami proses
pengenceran dan diproses dengan cara tertentu lalu mengalami penyimpanan
dalam nitrogen cair dengan suhu -196 ºC. Goldman dkk., (1991) mengatakan
bahwa selama proses pembekuan semen, terjadi kematian spermatozoa sampai
30% dari jumlah spermatozoa segar dan menurut Wahyadin (2012) 50 %
spermatozoa mati selama proses pembekuan, maka setiap dosis IB semen sapi
paling sedikit harus mengandung 25 juta sel spermatozoa.
Kematian spermatozoa selama proses pengenceran disebabkan oleh peroksida
lipid yang terjadi karena radikal bebas saat semen berinteraksi langsung dengan
oksigen. Peroksida lipid adalah kerusakan oksidatif dari minyak dan lemak yang
mengandung ikatan karbon-karbon rangkap. Pazil (2009) mengatakan bahwa
peroksida lipid merupakan reaksi berantai yang memberikan pasokan radikal
bebas secara terus-menerus yang menimbulkan peroksida lebih lanjut.
Tingginya tingkat kematian spermatozoa saat proses pengenceran dan pembekuan
karena radikal bebas yang menimbulkan peroksida lipid menyebabkan
ketidakstabilan membran plasma spermatozoa. Kerusakan membran plasma
spermatozoa menurunkan tingkat motilitas dan mematikan spermatozoa yang
akan menurunkan kemampuan spermatozoa untuk membuahi sel telur.
Peningkatan reaksi radikal bebas dapat diminimalisir dengan penambahan
antioksidan dalam pengencer semen. Antioksidan menurut Hemmerstedt (1993)
6
atau menekan radikal bebas dan mampu untuk mengakhiri siklus reaksi. Winarno
dkk., (1984) mengatakan bahwa antioksidan dapat mencegah oksidasi lemak dan
adanya antioksidan dalam lemak dapat mengurangi kecepatan proses oksidasi.
Maxwell dan Watson (1996) mengatakan salah satu manfaat dari antioksidan
adalah dapat memperlambat ketidakstabilan membran yang dihubungkan dengan
penuaan spermatozoa. Menurut Widiastuti (2001) antioksidan hanya mampu
memperbaiki fertilitas spermatozoa yang dibekukan dan tidak bekerja pada semen
segar. Oleh karenanya, penambahan antioksidan dalam pengencer semen sangat
dianjurkan dilakukan untuk mempertahankan keutuhan membran plasma dan
dapat meningkatkan kemampuan fertilisasi spermatozoa.
Salah satu antioksidan yang memiliki kemampuan tinggi untuk mengatasi radikal
bebas adalah vitamin C atau asam askorbat. Winarno (1997) mengatakan bahwa
peranan utama vitamin C adalah dalam pembentukan kolagen interseluler
sehingga vitamin C dapat digunakan untuk mempertahankan dan menjaga fungsi
membran. Menurut Sauberlich (1991), asam askorbat siap untuk diabsoprsi oleh
jaringan jika terdapat dalam dosis yang rendah.
Vitamin C memiliki sifat asam sedangkan spermatozoa sangat peka terhadap
perubahan pH. Penambahan vitamin C harus sangat diperhatikan untuk menjaga
keadaan pH dalam semen cair. Sumarsono (1998) mengatakan bahwa pada semen
beku kerbau lumpur penambahan 1,5 mM vitamin C nyata mempertahankan
motilitas setelah pembekuan , tetapi dalam penambahan 3 dan 5 mM cenderung
Penggunaan vitamin C sebagai antioksidan menurut penelitian pendahulu mampu
mengatasi dan menghentikan radikal bebas yang dapat merusak dan menurunkan
kualitas spermatozoa namun penambahanya harus pada dosis yang tepat untuk
menjaga pH semen. Oleh karena itu, penelitian ini diharapkan dapat menghasilkan
pengetahuan tentang dosis penambahan vitamin C yang paling tepat untuk
ditambahkan dalam pengencer semen sehingga dapat mempertahankan
kualitasnya.
E. Hipotesis
Hipotesis yang dapat diajukan dalam penelitian ini yaitu :
1. penambahan vitamin C dalam pengencer semen dapat mempertahankan
persentase motilitas dan hidup spermatozoa setelah proses pembekuan;
2. terdapat dosis penambahan vitamin C yang optimal dalam pengencer semen
II. TINJAUAN PUSTAKA
A. Sapi Bali
Hasnawati (2008) mengatakan bahwa Sapi Bali adalah keturunan sapi liar yang
disebut banteng (Bos sondaicus) yang telah mengalami domestikasi berabad-abad
lamanya. Klasifikasi Sapi Bali menurut Blakely dan Bade (1992), yaitu:
phylum : Chordata;
sub-Phylum : Vertebrata;
class : Mamalia;
sub-Class : Theria;
ordo : Artiodactyla;
sub-Ordo : Ruminantia;
infra-Ordo : Pecora;
family : Bovidae;
genus : Bos;
group : Taurinae;
species : Bos sondaicus
Ciri-ciri Sapi Bali menurut Sugeng (1992) yaitu berwarna merah bata atau seperti
kehitam-hitaman sedangkan sapi betina tetap berwarna merah bata. Baik jantan
maupun betina bagian belakang tubuh dan keempat kakinya berwarna putih.
Hardjosubroto (1994) mengatakan bahwa ada tanda-tanda khusus yang harus
dipenuhi sebagai Sapi Bali murni, yaitu warna putih pada bagian belakang paha,
pinggiran bibir atas, dan pada paha kaki bawah mulai tarsus dan karpus sampai
batas pinggir atas kuku. Bulu pada ujung ekor hitam, bulu pada bagian dalam
telinga putih, terdapat garis belut (garis hitam) yang jelas pada bagian atas
punggung. Bentuk tanduk pada jantan yang paling ideal disebut bentuk tanduk
silak congklok yaitu jalannya pertumbuhan tanduk mula-mula dari dasar sedikit
keluar lalu membengkok keatas, kemudian pada ujungnya membengkok sedikit
keluar. Pada yang betina bentuk tanduk yang ideal yang disebut manggul gangsa
yaitu jalannya pertumbuhan tanduk satu garis dengan dahi arah kebelakang sedikit
melengkung kebawah dan pada ujungnya sedikit mengarah kebawah dan ke
dalam, tanduk ini berwarna hitam.
Sapi Bali memiliki karakteristik fertilisasi yang baik. Bandini (1999) mengatakan
bahwa umur pubertas Sapi Bali berkisar antara 18--24 bulan, tingkat fertilitas
23--26%, siklus estrus 20--21 hari, masa subur 18--19 jam, persentase kebuntingan
86,56%. Bobot jantan pada sapi dewasa 375--400 kg, bobot betina dewasa
275--300 kg. Wahyuni (2000) menambahkan bahwa Sapi Bali memiliki periode
kebuntingan 280-294 hari, tingkat kematian kelahiran anak sapi hanya 3,65%,
10
B. Semen
Toelihere (1985) mengatakan bahwa semen adalah sekresi kelamin jantan,
disekresikan secara normal yang terdiri atas spermatozoa dan plasma semen.
Evans dan Maxwell (1987) mengatakan bahwa semen mengandung dua bagian
utama yaitu plasma seminal dan spermatozoa, komposisi keduanya berbeda antar
spesies. Semen secara normal diejakulasikan ke dalam saluran kelamin betina
sewaktu kopulasi tetapi dapat pula ditampung dengan berbagai cara untuk
keperluan inseminasi buatan.
Spermatozoa yaitu sel kelamin jantan yang tersuspensi di dalam plasma semen
yang dihasilkan oleh epididemis dan kelenjar-kelenjar kelamin pelengkap.
Patodiharjo (1982) mengatakan bawa Spermatozoa dihasilkan di dalam testes
sedangkan plasma semen adalah campuran sekresi yang dibuat oleh kelenjar
epididemis, vasdeferens, prostat, vesika seminalis, dan kelenjar cowper.
Toelihere (1993) menyebutkan bahwa spermatozoa merupakan sel kecil, kompak,
dan khas yang tidak bertumbuh atau membagi diri. Spermatozoa tidak memiliki
sitoplasma yang khas seperti sel umumnya, contohnya adalah sel spermatozoa
sapi, hanya ± 0,00005 kali dari volume satu sel ovum, namun keduanya memiliki
nilai herediter yang sama. Spermatozoa dihasilkan dalam jumlah yang jauh lebih
banyak dan satu kali ejakulasi sapi yang baik mengandung 10 x 10 9spermatozoa
yang cukup untuk diinseminasikan pada 1.000 ekor betina.
Plasma semen terdiri dari zat-zat organik dan non organik. Fungsi plasma semen
melewati saluran reproduksi jantan ketika ejakulasi, mengaktifkan medium untuk
sperma non motil, dan sebagai bahan penyangga yang kaya kandungan nutrsi serta
bereperan membantu sperma tetap hidup setelah di pindahkan ke dalam saluran
kelamin betina.
C. Struktur Spermatozoa
Salisbury dan Van Demark (1985) menyebutkan bahwa Spermatozoa terdiri atas
kepala, leher, dan ekor. Panjang spermatozoa sapi 68±3 µm, panjang kepala
sekitar 10 µm, ekor 50 µm, leher 1 µm, dan badan 8--10 µm. Bagian leher
spermatozoa yang berisi sentriol proksimal kadang dinyatakan sebagai pusat
kinetik aktivitas sperma. Ekor sperma berfungsi sebagai motor dalam pergerakan
sperma.
Sumber : Anonim(2009)
Gambar 1.Bagian-bagian dari spermatozoa
Permukaan Spermatozoa diselubungi oleh lapisan membran lipoprotein. Asam
12
di bagian kepala. Mukopolisakarida berada di bagian akrosom yang memiliki
fungsi membungkus kepala sperma, terikat di dalam molekul protein. Ikatan
molekul protein tersebut menurut Cole dan Cupps (1977) mengandung beberapa
enzim yang penting dalam proses fertilisasi serta mudah rusak karena pengaruh
suhu.
Salisbury dan Van Demark (1985) menyebutkan bahwa plasmalogen atau lemak
terdapat pada leher, badan, dan ekor sperma yang memiliki fungsi sebagai alat
respirasi yang ditutup oleh selubung protein berbentuk keratin. Lemak juga
terdapat pada membran plasma yang sangat penting dalam fertilisasi. Linder
(1992) mengatakan lemak dalam tubuh manusia berperan sebagai komponen
struktur membran sel, bentuk penyimpanan energi, bahan bakar metabolik, dan
sebagai bahan pengemulsi.
D. Proses Pembuatan Semen Beku
Semen beku adalah semen yang berasal dari pejantan terpilih yang diencerkan
sesuai prosedur proses produksi sehingga menjadi semen beku dan disimpan di
dalam rendaman nitrogen cair pada suhu -196ºC pada kontainer (SNI, 2005).
Menurut Widiastuti (2001) fertilitas Spermatozoa semen beku yang lebih rendah
dari Spermatozoa semen segar dapat disebabkan oleh kerusakan membran yang
terjadi selama proses pembekuan dan pencairan kembali. Oleh karena itu, proses
pembuatan semen beku harus memperhatikan dan menjaga faktor-faktor yang
1. Penampungan
Toelihere (1993) menyebutkan bahwa pengkoleksian atau penampungan semen
dapat dilakukan dengan tiga metode yaitu metode pemijatan, metode dengan
bantuan elektroejakulator, metode vagina buatan. Menurut Evans dan Mexwell
(1987) semen dapat dikoleksi beberapa kali per hari dengan vagina buatan. Hafez
(1987) juga mengatakan bahwa dengan menggunakan vagina buatan dapat
merangsang kopulasi secara normal sehingga tidak mengakibatkan stress pada
sapi dan hasil ejakulasinya cukup baik, oleh karena itu penggunaan vagina buatan
sangat dianjurkan dalam penampungan semen.
Temperatur vagina buatan menurut Widiasuti (2001) sebelum digunakan harus
berkisar 42--45 ºC dan tabung semen harus bersuhu 30--37 ºC untuk mencegah
coolshock pada Spermatozoa . Pejantan donor harus di pancing terlebih dahulu
dengan teaser untuk meningkatkan libido. Hal tersebut sesuai dengan pendapat
Salisbury dan VanDenmark (1985) yang menyatakan bahwa rangsangan seksual
akan menambah jumlah spermatozoa yang ditampung. Hartono dkk., (2008)
mengatakan bahwa usaha untuk mempertinggi libido pejantan yang akan dikoleksi
dilakukan dengan cara melakukan pengekangan (false mount). Cara ini mampu
meningkatkan konsentrasi sperma 50% dan dua kali false mount dapat
meningkatkan konsentrasi Spermatozoa hingga dua kali lipat.
2. Pengenceran semen
Menuru Farstadt (1996) pengencer adalah yang mengawetkan Spermatozoa dan
14
sebagaimana menyediakan energi untuk spermatozoa selama penyimpanan antara
pendinginan, ekuilibrasi, dan pembekuan. Syarat pengencer semen dalam SNI
(2005) yaitu:
mempunyai sifat isotonik terhadap semen;
mempunyai sifat sebagai buffer;
dapat melindungi spermatozoa dalam proses pendinginan, pembekuan,
dan pencairan kembali (thawing);
bersifat sebagai sumber nutrisi;
mempunyai efek anti bakterial;
menjaga fertilitas spermatozoa;
tidak boleh mengandung zat-zat yang bersifat toksik atau racun, baik
terhadap spermatozoa maupun terhadap saluran reproduksi sapi betina.
Susu skim kuning telur adalah salah satu jenis pengencer semen sapi yang banyak
digunakan. Kuning telur mengandung asam-asam amino, karbohidrat, vitamin,
dan mineral untuk memenuhi kebutuhan hidup spermatozoa. Djanuar (1985)
mengatakan bahwa di dalam kuning telur mengandung senyawa anti kejut yang
berperan melindungi spermatozoa dari kejutan dingin. Kuning telur juga
mengandung glukosa bermacam-macam protein dan vitamin yang larut dalam air
dan lemak serta viskositasnya yang dapt menguntungkan spermatozoa.
Susu skim mengandung zat nutrisi yang dapat dimanfaatkan oleh spermatozoa
sebagai sumber energi. Widjaja (2011) mengatakan bahwa susu skim mengandung
zat lipoprotein dan lesitin sehingga bisa digunakan dalam pengencer semen untuk
mengandung enzim yang hancur pada waktu pemanasan dimana pemanasan susu
diatas 80ºC akan melepaskan gugus sulfihidril (-SH) yang berfungsi sebagai zat
reduktif yang mengatur metabolisme oksidatif sperma.
Penambahan antibiotik seperti Penicillin dan Streptomycin menurut Toelihere
(1993) untuk mengahambat pertumbuhan mikroorganisme serta penambahan
gliserol untuk melindungi Spermatozoa terhadap efek letal pembekuan. Toelihere
(1993) mengatakan bahwa pemberian gliserol sebaiknya dilakukan secara
bertahap untuk mencegah osmotic shock.
3. Ekuilibrasi
Toelihere (1993) mengetakan bahwa ekuilibrasi adalah waktu yang dibutuhkan
spermatozoa untuk menyesuaikan diri sebelum dilakukan pembekuan sehingga
kematian spermatozoa yang berlebihan dapat dicegah. Ekuilibrasi dilakukan
setelah semen dicampur dengan beberapa pengencer. Ekuilibrasi dilakukan
dengan cara meletakan semen dalam straw pada temperatur 5 ºC selama 4--6 jam.
Hal tersebut sesuai dengan pendapat Hafez (1987) yang mengatakan bahwa
ekuilibrasi dapat mencegah pengaruh negatif gliserol terhadap antibiotik yang
ditambahkan kedalam pengencer dan lama waktu yang disarankan berkisar antara
4--6 jam.
4. Penyimpanan
Pembekuan dan penyimpanan semen dapat dilakukan dengan berbagai cara.
Menurut Toelihere (1993) penyimpanan semen dapat dilakukan dengan cara
16
umumnya semen yang beredar dalam bentuk straw. Jerami plastik atau straw yang
digunakan umumnya berukuran 12 cm .
Toelihere (1993) mengatakan bahwa jumlah semen dalam straw biasa (midistraw)
adalah 0,5 ml dan ministraw 0,25 ml. Konsentrasi Spermatozoa harus jauh lebih
tinggi agar tetap mengandung minimal 25 juta sel untuk setiap straw 0,25 ml.
Kelebihan dari penggunaan straw yaitu menghemat tempat; ringan dan praktis;
dapat dibuat dalam berbagai warna yang mengidentifikasikan jenis pejantan
tertentu.
Menurut Witarsa (1997) semen beku adalah produk peternakan yang mudah
rusak. Oleh karena itu, diperlukan teknik penyimpanan dan perawatan yang tepat
terhadap semen beku agar tetap dapat digunakan meski disimpan dalam jangka
waktu yang lama sebelum pengaplikasiannya. Pada dasarnya pembekuan semen
bertujuan untuk menghambat metabolisme spermatozoa tanpa merusak dan
mempertahankan daya hidupnya dalam jangka waktu yang tidak ditentukan dan
dapat dikembalikan metabolismenya seperti semula serta dapat berfungsi seperi
sediakala.
Semen beku harus disimpan pada suhu yang sangat dingin dan yang paling sering
dilakukan adalah dengan menyimpanya di dalam kontainer berisi nitrogen cair.
Telah diemukan hubungan yang terbaik antara pengawetan Spermatozoa dengan
temperatur penyimpanan . Hasil penelitian Cole dan Cupps(1977) Spermatozoa
sapi menunjukkan penurunan kemampuan fertilisasi dan peningkatan kematian
E. Pemeriksaan Semen Beku
Semen yang telah ditambahkan pengencer dan dibekukan harus melalui proses
evaluasi untuk melihat kualitas dan kemampuan spermatozoa dalam membuahi.
Penilaian yang dilakukan yaitu uji Before Freezing dan uji Post Thawing Motility.
Aminasari (2009) mengatakan bahwa pemeriksaan Before Freezing (BF) adalah
pemeriksaan terhadap semen segar yang telah ditambahkan pengencer dan
didinginkan pada temperatur 5°C selama 1--2 jam. Aminasari (2009) juga
menyatakan bahwa motilitas semen yang telah didinginkan pada suhu 5°C tidak
boleh berada di bawah 55%. Uji BF ini dilakukan sebagai penilaian awal untuk
melihat penyesuaian penegencer dengan semen.
Persentase motilitas spermatozoa dihitung dengan cara menilai gerakan individu
spermatozoa. Penilaian ini menggunakan standar yang dilakukan Rice dkk.,
(1975), yaitu :
a. 0 : tidak ada gerakan;
b. 1 : 20% atau kurang bergerak di tempat;
c. 2 : 20--40% spermatozoa menunjukkan gerakan terbatas;
d. 3 : 40--60% spermatozoa motil progresif, bergerak terbatas pada
spermatozoa secara individu;
e. 4 : 60--80% spermatozoa motil progresif, bergerak bebas dan kadang-
kadang lambat;
f. 5 : 80--100% spermatozoa motil progresif, bergerak bebas kesemua arah;
Pencairan kembali atau thawing semen beku merupakan prosedur yang sangat
18
fertilitasnya. Menurut Toelihere (1993) setelah pencairan kembali semen beku
merupakan barang rapuh dan tidak dapat tahan hidup seperti semen cair,
menurutnya semen beku yang sudah dicairkan kembali tidak dapat dibekukan
kembali.
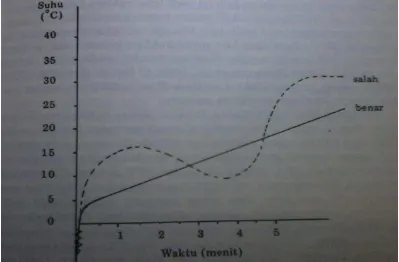
Salisbury dan Van Demark (1985) mengatakan bahwa pencairan kembali semen
setelah dibekukan dapat dilakukan dengan berbagai cara selama dengan prinsip
bahwa kurva peningkatan suhu semen harus naik secara konstan sampai waktu
inseminasi. Menurut Cole dan Cupps (1977) thawing pada suhu 37°C dan 50°C
cukup efektif dan menurut Sanjaya (1976) untuk Indonesia metode thawing yang
mungkin paling praktis adalah thawing di dalam air kran, dengan catatan bahwa
semen yang sudah diencerkan kembali harus dipakai untuk inseminasi dalam waktu
kurang dari 5 menit.
Sumber: Toilehere (1993)
F. Pengaruh Pembekuan Terhadap Spermatozoa
Menurut Toelihere (1993) beberapa sapi jantan, kira-kira 10--20% menghasilkan
semen yang tidak tahan terhadap pembekuan rata-rata 50% spermatozoa akan
mati sehingga jumlah sel kelamin janta perlu dipertinggi untuk setiap dosis IB.
Menururt Widiastuti (2001) penurunan kemampuan spermatozoa selama
pembekuan dapat diakibatkan oleh proses penambahan gliserol, perlakuan
pendinginan, temperatur yang sangat rendah di bawah titik beku yang dapat
mengakibatkan coldshock, proses thawingserta dari komposisi membran itu
sendiri yang sangat rentan terhadap perubahan.
Toelihere (1993) mengatakan bahwa pada sapi, satu dosis inseminasi dengan
semen cair harus mengandung minimal 5 juta spermatozoa sedangkan dengan
semen beku paling sedikit harus mengandung 12 juta spermatozoa. Hal tersebut
karena banyak spermatozoa yang mati selama pembekuan, umumnya dikarenakan
coldshock. Goldman (1991) mengatakan bahwa pada pembekuan semen akan
terjadi kematian spermatozoa sampai 30% dari jumlah spermatozoa segar atau
setelah diencerkan dan kerusakan akibat pengaruh pendinginan (coldshock).
White (1993) mengatakan bahwa tanda yang paling jelas dari coldshock adalah
hilangnya motilitas yang permanen ketika semen dihangatkan kembali, juga
terdapat penurunan angka fruktolisis dan respirasi. Hal ini disebabkan karena
tingginya rasio asam lemak jenuh dan tidak jenuh dalam fosfolipid dan kandungan
kolesterol yang rendah. Besarnya pengaruh coldshock terhadap kualitas
spermatozoa menyebabkan ditambahkanya krioprotektan seperti gliserol dengan
20
Wijaya (1996) mengatakan bahwa selain rentan terhadap coldshock, spermatozoa
juga rentan terhadap pengaruh radikal bebas terutama radikal hidroksil (OH).
Menururt Rizal dan Herdis (2010) radikal bebas adalah senyawa kimia yang
memiliki elektron tak berpasangan dan bersifat sangat reaktif. Kerusakan yang
dapat ditimbulkan oleh serangan radikal bebas menurut Muhilal (1991) antara lain
kerusakan membran sel, protein, DNA, penuaan, dan terjadinya peroksida lipid.
Reaksi peroksida lipid yang dapat merusak spermatozoa dalam proses pengolahan
semen terjadi karena kontak antara semen dan oksigen (O2). Radikal bebas jika
bereaksi dengan asam lemak tak jenuh akan menghasilkan lipid peroksida.
Kecepatan reaksi peroksida menurut Hammerstedt (1993) pada awalnya akan
rendah dan kemudian meningkat dengan cepat sebagaimana oksigen mendekati
konsentrasi yang jenuh. Widiastuti (2001) mengetakan bahwa lipid peroksida
yang berkepanjangan akan merusak struktur matrik lipid dan akhirnya
menyebabkan instabilitas pada membran.
G. Radikal Bebas dan Peroksida lipid
Radikal adalah bentuk radikal bebas yang sangat aktif dan memiliki waktu paruh
yang sangat pendek. Pazil (2009) mengatakan bahwa jika radikal bebas tidak
diinaktivkan, reaktivitasnya dapat merusak seluruh tipe makromolekul seluler,
termasuk karbohidrat, protein, lipid, dan asam nukleat. Rizal dan Herdis (2010)
mengatakan bahwa radikal bebas muncul akibat tekanan yang berat karena
metabolisme yang meningkatkan konsentrasi reaksi radikal bebas sebagai salah
satu produk akhir metabolisme.
Menurut Siregar (1992) reaksi radikal bebas yang berkelanjutan akan membentuk
reaksi berantai dan berlangsung terus menerus karena setiap reaksi menghasilkan
radikal bebas baru yang mengakibatkan reaksi peroksida lipid baru, sehingga
disebut reaksi rantai atau reaksi autokatalitik. Reaksi autokatalitik sebagai berikut:
Pencetusan : RH + OH● → R● + H2O
Perambatan : R● + O2 → ROO●
ROO● + RH → ROOH + O2
Terminasi : R● + R● → R R●
ROO● + ROO● → ROOR + O2
Menurut Candra (2008) radikal bebas jika bereaksi dengan asam lemak tak jenuh
akan menghasilkan lipit peroksida. Peroksidasi lipid tergantung pada konsentrasi
oksigen. Peroksida lipid adalah kerusakan oksidatif dari minyak dan lemak yang
mengandung ikatan karbon-karbon rangkap. Rizal dan Herdis (2010) mengatakan
bahwa asam lemak tak jenuh merupakan komponen utama fosfolipida penyusun
membran plasma sel dan protein yang memegang berbagai peranan penting
sebagai enzim, reseptor, antibodi, pembentuk metriks, dan sitokeleton.
Jones dan Martin (1973) mengatakan bahwa reaksi peroksida lipid akan merubah
struktur spermatozoa terutama pada bagian akrosom, kehilangan motilitas,
perubahan metabolisme yang cepat, dan pelepasan komponen intraseluler dan
22
dapat menurunkan daya tahan spermatozoa selama proses pengawetan
berlangsung.
H. Antioksidan
Menurut Pazil (2009) antioksidan adalah substansi yang diperlukan tubuh untuk
menetralisir radikal bebas dan mencegah kerusakan yang ditimbulkan oleh radikal
bebas terhadap sel normal, protein, dan lemak. Antioksidan menurut Winarno
(1984) adalah bahan yang digunakan untuk mencegah oksidasi lemak dan adanya
antioksidan dalam lemak akan mengurangi kecepatan proses oksidasi. Anggorodi
(1994) mengatakan bahwa antioksidan yang efektif dapat menghalangi peroksida
dengan menyediakan hidrogen kepada radikal bebas pertama yang terbentuk dan
mengubah kembali ke asam lemak semula. Menurut Gordon (1990) reaksi
penghambatan radikal bebas pertama oleh antioksidan (AH) adalah sebagai
berikut :
Pencetusan : R● + AH → RH + A●
Perambatan : ROO● + AH → ROOH + A●
Vitamin C atau asam askorbat adalah vitamin yang tidak bisa diproduksi oleh
tubuh. Anonim (2013) vitamin C sangat mudah larut dalam air dan termasuk
golongan antioksidan yang mampu menangkal berbagai radikal bebas
ekstraselular, vitamin C memiliki karakteristik antara lain sangat mudah
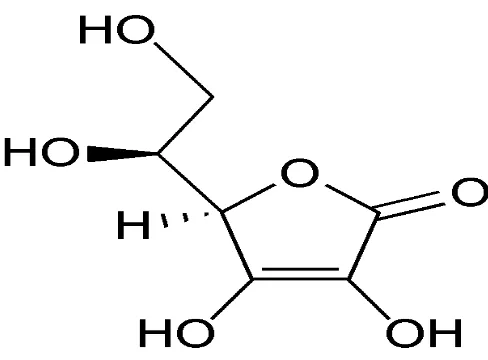
Sumber: Anonim (2013)
Gambar 3. Struktur kimia asam askorbat
Winarno (1984) mengatakan bahwa peranan utama vitamin C adalah dalam
pembentukan kolagen interseluler, oleh kerena itu vitamin C dapat digunakan
untuk mempertahankan dan menjaga fungsi membran. Asam askorbat siap
diabsorbsi oleh jaringan jika terdapat dalam jumlah yang kecil. Namun, menurut
Beconi dkk., (1993) pada semen berkualitas baik penambahan vitamin C dan E
terbukti dapat mengurangi kerentanan membran plasma terhadap peroksidasi,
tetapi penambahanya pada Spermatozoa dengan kualitas jelek tidak memberikan
III. BAHAN DAN METODE
A. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada tanggal 18--25 April 2014 di Unit Pelayanan
Teknis Daerah Balai Insemninasi Buatan Daerah Lampung, Kecamatan Terbanggi
Besar, Kabupaten Lampung Tengah, Provinsi Lampung.
B. Alat dan Bahan Penelitian
Alat yang digunakan dalam penelitian ini adalah labu didih dan penangas;
timbangan elektrik; termometer; spatula; corong; gelas ukur dan tutupnya; kertas
label dan kertas whatman; waterbath; object dan cover glass; spektrofotometer;
micropipet; beaker glass; mesin filling dan sealing; pH meter; boks tempat
pre-freezing dan freezing; mikroskop; counter number, stopwatch, dan hairdrye;
kontainer; gunting; pinset; alat tulis; kamera; tisu.
Bahan yang digunakan dalam penelitian ini adalah semen yang dikoleksi dari satu
ekor pejantan Sapi Bali; susu skim bebas lemak (non fat); aquabidestilata;
penicilin dan streptomicyn; gliserol; kuning telur; glukosa; Vitamin C (Asam
Askorbat); nitrogen cair (N2 cair), NaCl Fisiologis dan pewarna eosin 2%; air
C. Metode Penelitian
Rancangan percobaan yang digunakan pada penelitian ini adalah Rancangan Acak
Lengkap (RAL) dengan lima perlakuaan penambahan dosis vitamin C dalam
pengencer semen Sapi Bali. Setiap perlakuan akan diulang tiga kali, perlakuan
yang diberikan sebagai berikut :
P1 : pengencer skim kuning telur tanpa penambahan vitamin C
P2 : pengencer skim kuning telur dengan penambahan 1,50 mM vitamin C
P3 : pengencer skim kuning telur dengan penambahan 2,50 mM vitamin C
P4 : pengencer skim kuning telur dengan penambahan 3,50 mM vitamin C
P5 : pengencer skim kuning telur dengan penambahan 4,50 mM vitamin C
Data yang diperoleh dianalisis ragam pada taraf nyata 5% dan apabila berbeda
nyata akan dilanjutkan dengan uji polinomial ortogonal (Steel dan Torrie 1993).
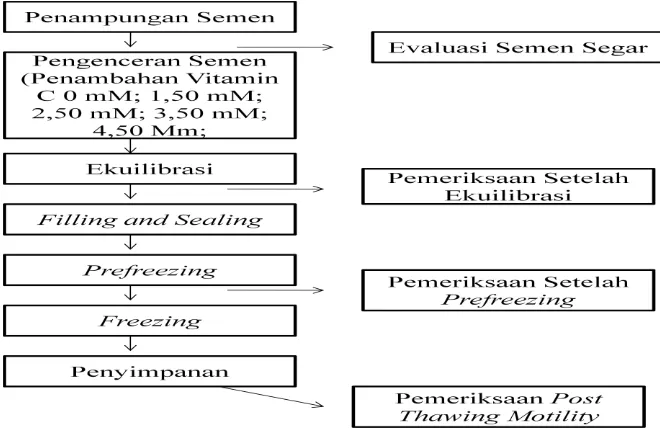
D. Prosedur Penelitian
Penelitian ini dilaksanakan di laboratorium UPTD-BIBD Lampung yang meliputi
proses pembuatan pengencer skim kuning telur, pemeriksaan kualitas semen Sapi
Bali segar, proses pembuatan semen beku Sapi Bali, dan pemeriksaan kualitas
semen beku Sapi Bali berupa persentase motilitas spermatozoa dan persentase
26
1. Pembuatan pengencer semen
Pembuatan pengencer yang dilakukan yaitu pembuatan bufferskim, pembuatan
buffer antibiotik, pembuatan pengencer bagian A, dan pembuatan pengencer
bagian B.
a. Pembuatan bufferskim
Cara pembuatan buffer skim yaitu dengan menyiapkan alat (penangas, labu didih,
beaker glass, corong, kertas saring, gelas ukur , spatula, termometer, timbangan
analitik, dan tisu) dan bahan (skim bubuk, dan aquabidestilata); menimbang skim
bubuk; menyiapkan aquabidestilata dan memasukkan sebagian dalam labu didih;
menyalakan pemanas listrik; mencairkan skim bubuk dengan sisa bagian
aquabidestilata; mengaduk rata sampai suhu mencapai 92oC; mematikan pemanas
setelah suhu 92oC, kemudian menyaring larutan skim tersebut ke dalam gelas ukur
perlahan-lahan; mendinginkan larutan skim dan selanjutnya menyimpan larutan
dalam refigrator (BIB Ungaran, 2011).
Pemakaian bubuk susu skim yang dipanaskan dengan temperatur tinggi dipakai
sebanyak 9%. Salisburry dan Van Denmark (1985) mengatakan bahwa pemakaian
pengencer susu skim menghasilkan fertilitas yang sedikit lebih tinggi daripada
kuning telur sitrat. Susu skim yang sudah diencerkan dipanaskan secara hati-hati
b. Pembuatan buffer antibiotik
Cara pembuatannya yaitu menyiapkan alat (gelas ukur bertutup, pembuka tutup
botol) dan bahan (penicillin 1 flc, streptomycin 3 flc, aquabidestilata, larutan
buffer skim); mencampur 3 flc streptomicyn dan 1 flc penicillin, kemudian
ditambah aquabidestilata sampai volume 30 cc; menghomogenkan larutan,
kemudian mencampur larutan tersebut dengan bufferskim, perbandingan 1 bagian
buffer antibiotik dengan 100 bagian buffer skim; menghomogenkan larutan (BIB
Ungaran, 2011).
c. Pembuatan pengencer bagian A
Pengencer bagian A adalah pengencer semen yang terdiri atas 90% buffer skim
antibiotik dan kuning telur dengan persentase kuning telur sebanyak 10% dari
total volume pengencer. Cara pembuatan 100 ml Pengencer bagian A yaitu
menyiapkan alat (gelas ukur bertutup, beaker glass, kertas saring, tissue, dan
pinset) dan bahan (buffer antibiotik, telur ayam ras, dan alkohol); menuangkan
buffer antibiotik ke dalam gelas ukur sebanyak 90 ml; menyiapkan telur segar dan
membersihkan cangkangnya dengan alkohol; menyiapkan kuning telur,
membersihkan kuning telur dari selaput fitelin menggunakan kertas saring,
memecah kuning telur; memasukkannya ke dalam beaker glass; menuangkan
kuning telur ke dalam gelas ukur yang berisi buffer antibiotik sebanyak 10 ml
perlahan agar tidak terkena dinding tabung; menambahkan vitamin C dengan
dosis 0 mM; 1,50 mM; 2,50 Mm; 3,50 mM; dan 4,50 mM ke dalam tabung yang
berbeda; menghomogenkan larutan dengan cara dikocok selama 30 menit (BIB
28
dalam proses pengenceran semen sebelum ditambahkannya pengencer bagian B
yang mengandung lebih banyak energi.
d. Pembuatan pengencer bagian B
Pengencer bagian B merupakan pengencer A yang sudah ditambah gliserol dan
glukosa. Pengencer B terdiri atas 72% buffer skim antibiotik, 10% kuning telur,
16% gliserol, dan 2% glukosa (BIB Ungaran, 2011).
Prosedur pembuatannya 100 ml pengencer bagian B yaitu menyiapkan alat (gelas
ukur bertutup, timbangan analitik, beaker glass, kertas saring, tissue, pinset) dan
bahan (buffer antibiotik, telur ayam ras, glukosa, gliserol, dan alkohol 70 %);
menuang buffer antibiotik ke dalam gelas ukur sebanyak 72 ml; menuang gliserol
ke dalam gelas ukur berisi buffer antibiotik sebanyak 16 ml; menyiapkan kuning
telur, membersihkan kuning telur dari putih telur menggunakan kertas saring,
memecah selaput kuning telur dan diambil kuning telurnya kemudian dimasukkan
ke dalam beaker glass; menambahkan kuning telur ke dalam gelas ukur yang
berisi buffer antibiotik dan gliserol sebanyak10 ml perlahan agar tidak terkena
dinding tabung; menambahkan glukosa sebanyak 2 gr; menghomogenkan larutan
dengan cara dikocok selama 30 menit (BIB Ungaran, 2011).
2. Penampungan semen
Pejantan donor harus dipancing terlebih dahulu dengan teaser untuk
meningkatkan libido. Ridwan ( 2009) mengatakan bahwa pengekangan (false
Cara ini mampu meningkatkan konsentrasi Spermatozoa 50% dan dua kali false
mount konsentrasi sperma meningkat dua kali lipat.
Semen dapat segera ditampung menggunakan artivicial vagina (AV) pada saat
terjadi ejakulasi, penis harus masuk tepat pada AV dan semen jangan sampai
tercecer di luar. Hafez (1987) mengatakan bahwa dengan menggunakan vagina
buatan dapat merangsang kopulasi secara normal sehingga tidak mengakibatkan
stress pada sapi dan hasil ejakulasinya cukup baik, oleh karena itu penggunaan
vagina buatan sangat dianjurkan dalam penapungan semen.
3. Evaluasi semen segar
Semen segar yang telah ditampung segera dibawa ke laboratorium uji untuk
dilakukan penilaian secara makroskopis (warna, bau, volume, konsistensi, dan
pH) dan penilaian mikroskopis (gerakan massa, persentase motil progresif,
konsentrasi spermatozoa, dan persentase spermatozoa hidup).
4. Pengenceran semen
Penambahan pengencer yang dilakukan pada semen segar tidak dapat dilakukan
secara langsung karena akan menimbulkan coldshock yang dapat menurunkan
kualitas semen. Ada tiga tahapan penambahan pengencer yang dilakukan,
pemberian pengenceran A dibagi dalam dua kali pemberian yaitu pengencer A1
(Part A primer) dan pengenceran A2 (Part A Extra), serta pengenceran B yang
diberikan kemudian. Volume pengencer yang ditambahkan sesuai dengan output
30
diberikan yaitu 1:1. Pemberian pengencer A1, pengencer A2, dan pengencer B
ditentukan dengan rumus berikut:
Pengencer A (Part A) = 0,5 x pengencer total
Pengencer A1 (Part A primer) = berkisar 5--10 ml
Pengencer A2 (Part A Extra) = pengencer A – pengencer A1
Pengencer B (Part B) = 0,5 x pengencer total
Cara pencampurannya yaitu mempersiapkan alat (cool top, water bath, dan gelas
ukur) dan bahan (pengencer A1 diletakkan di dalam water bath bersuhu 27oC);
mengambil semen segar hasil evaluasi; mempersiapkan pengencer (volume
pengencer sesuai output dari spektrofotometer); menghitung kompisisi pengencer
dengan rumus; mencampur semen segar dengan pengencer A1; memasukkan
tabung ke dalam beaker glass yang berisi air bersuhu 27oC (water jacket);
memasukkan tabung yang telah dilindungi water jacket ke dalam cooltop;
melepaskan water jacket setelah 35 menit; menuangkan pengencer A2 dalam
tabung 50 menit setelah water jacket dilepas, dan menghomogenkan hasil kerja;
setelah 15 menit, pengencer B diberikan 4 tahap dengan selang waktu 15 menit;
melakukan proses ekulibrasi selama 4 jam di dalam cool top (BIB Ungaran,
2011).
5. Ekuilibrasi
Proses ekuilibrasi dilakukan setelah sampel semen dicampur dengan
masing-masing bahan pengencer. Toelihere (1993) menjelaskan bahwa ekuilibrasi adalah
dilakukan pembekuan sehingga kematian spermatozoa yang berlebihan dapat
dicegah. Ekuilibrasi dilakukan dengan cara menempatkan straw pada temperatur
5oC dalam cooltop selama 4 jam.
6. Pemeriksaan setelahekuilibrasi
Aminasari (2009) mengatakan bahwa pemeriksaan setelahekuilibrasi, atau biasa
disebut dengan uji Before Freezing (BF) adalah pemeriksaan terhadap semen
segar yang telah ditambahkan pengencer dan didinginkan pada temperatur 5°C
selama 1--2 jam. Dalam pemeriksaan BF kualitas yang akan dinilai adalah persentase
motilitas dan persentase hidup. Aminasari (2009) melanjutkan bahwa motilitas
semen yang telah didinginkan pada suhu 5°C tidak boleh berada di bawah 55%.
7. Filling, sealing dan printing
Filling, sealing, dan printing merupakan proses pengisian semen cair yang telah
lolos pemeriksaan post ekuilibrasi atau before freezing ke dalam straw
menggunakan mesin otomatis di dalam cool top.
8. Prefreezing
Proses prefreezing dilakukan dengan cara meletakan straw pada permukaan
nitrogen cair (4 cm di atas permukaan) yang bersuhu -110 -- -120ºC selama
32
9. Pemeriksaan setelah prefreezing
Setelah proses prefreezing selama sembilan menit dilakukan pemeriksaan kualitas
spermatozoa yang meliputi penilaian persentase motilitas dan persentase hidup
spermatozoa.
10. Freezing
Proses freezing dilakukan dengan cara merendam straw yang telah melalui proses
prefreezing kedalam nitrogen cair yang bersuhu -196 ºC.
11. Penilaian Post Thawing Motility
Setelah semen sapi dibekukan pada suhu - 196ºC maka untuk menilai kualitasnya
dilakukan pemeriksaan PTM atau Post Thawing Motility, dalam PTM ini kualitas
spermatozoa yang dinilai adalah persentase motilitas dan persentase hidup setelah
mengalami pencairan. Post Thawing Motility dilakukan pada air sumur bersuhu
37ºC selama 29 detik. SNI (2005) yang menyatakan bahwa sperma sapi yang
motil progresif minimal 40% dan gerak maju individu spermatozoa minimal 2 +.
E. Peubah yang Diamati
1. Persentase motilitas spermatozoa
Persentase motilitas spermatozoa dihitung dengan cara menilai gerakan individu
spermatozoa. Penilaian ini menggunakan standar yang dilakukan Rice dkk.,
(1975), yaitu dengan menggunakan penilaian persentase pergerakan spermatozoa
yang ditunjukan dengan angka 0--100%.
2. Persentase spermatozoa hidup
Persentase spermatozoa hidup dilihat pada preparat ulas yang dibuat dengan cara
meneteskan satu tetes eosin 2% pada ujung object glass, meneteskan semen
dengan ukuran yang sama pada object glass tersebut, menempelkan ujung cover
glass pada kedua cairan sehingga tercampur, kemudian dorong ke ujung object
glass sehingga terbentuk lapisan tipis, mengeringkannya menggunakan hairdryer.
Pemeriksaan dilakukan di bawah mikroskop dengan pembesaran 10 x 40.
Spermatozoa dihitung dengan cara berurutan atau zik-zak sampai sepuluh lapang
pandang (200 spermatozoa). Spermatozoa yang hidup tidak berwarna atau
berwarna merah muda dan yang telah mati akan berwarna merah pada bagian
kepalanya.
Persentase spermatozoa hidup dapat ditentukan dengan rumus :
Spermatozoa hidup (%) =
x 100
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan hasil penelitian kualitas semen beku Sapi Bali dengan penambahan
berbagai dosis vitamin C dalam pengencer skim kuning telur dapat disimpulkan
bahwa dosis penambahan vitamin C yang berbeda (0 mM; 1,50 mM; 2,50 mM;
3,50 mM; 4,50 mM) dalam pengencer susu skim kuning telur menunjukkan hasil
yang tidak berbeda nyata (P>0,05) terhadap persentase motilitas spermatozoa dan
persentase spermatozoa hidup.
B. Saran
Berdasarkan hasil penelitian ini, perlu dilakukanya penelitian lebih lanjut terhadap
dosis penambahan vitamin C yang berbeda dalam berbagai jenis pengencer semen
DAFTAR ISI
Halaman
DAFTAR ISI……….………... i
DAFTAR TABEL………... ii
DAFTAR GAMBAR……… ii
I. PENDAHULUAN……...………..…. 1
A. Latar Belakang……...……… 1
B. Tujuan Penelitian…...……… 4
C. Keguanaan Penelitian.……… 4
D. Kerangka Pemikiran...……… 5
E. Hipotesis…….……… 7
II. TINJAUAN PUSTAKA……….……….….… 8
A. Sapi Bali…….………. 8
B. Semen……….……….... 10
C. Struktur Spermatozoa……….……….... 11
D. Proses Pembuatan Semen Beku…….………... 12
1. Penampungan………..… 13
2. Pengenceran semen……...………..…. 13
3. Ekuilibrasi………..……….…. 15
E. Pemeriksaan Semen Beku…..……….………...….. 17
F. Pengaruh Pembekuan Terhadap Spermatozoa……...…….………... 19
G. Radikal Bebas dan Peroksida Lipid...………...………..…….. 20
H. Antioksidan………..…. 23
III. BAHAN DAN METODE……..……….. 24
A. Waktu dan Tempat Penelitian……… 24
B. Alat dan Bahan Penelitian…..……… 24
C. Metode Penelitian…...……… 25
D. Prosedur Penelitian….……… 25
1. Pembuatan pengencer...………. 26
a. Pembuatan buffer skim………………. 26
b. Pembuatan buffer antibiotik..……….. 27
c. Pembuatan pengencer bagian A……….. 27
d. Pembuatan pengencer bagian B………... 28
2. Penampungan semen…...………... 28
3. Evaluasi semen segar…..……….. 29
4. Pengenceran semen…….……….. 29
5. Ekuilibrasi………. 30
6. Pemeriksaan setelahekuilibrasi……………. 31
7. Felling, sealing, dan printing………………. 31
8. Prefreezing……...………. 31
9. Pemeriksaan setelah prefreezing……….……..………..…….. 32
E. Peubah yang Diamati………... 33
1. Persentase motilitas spermatozoa……….……….……….. 33
2. Persentase spermatozoa hidup………….……….…… 33 IV. HASIL DAN PEMBAHASAN.……….……… 34
A. Penilaian Kualitas Semen Segar Sapi Bali….……….……… 34
B. Pengaruh Penambahan Vitamin C Terhadap Motilitas Spermatozoa Semen Beku………...……… 38
C. Pengaruh Penambahan Vitamin C Terhadap Persentase Spermatozoa Hidup Semen Beku……….………….……… 42
V. SIMPULAN DAN SARAN…...………. 46
A. Simpulan………. 46
B. Saran……….………. 46
DAFTAR PUSTAKA……...……… 47
DAFTAR PUSTAKA
Almatsier, S. 2009. Prinsip Dasar Ilmu Gizi. PT Gramedia Pustaka Utama. Jakarta
Alvarez, J.G. and B.T Storey. 1982. Spontaneous lipid peroxidation in rabbit epididymal spermatozoa: its effect on sperm motility. Biol. Reprod. 22:1102--1108
Asada, K. 1992. Ascorbate Peroxidase-Hydrogen Peroxydescavenging Enzyme in Plants dalam: Physiologia Plantarum. 85:23--24
Aminasar, D.P. 2009. Pengaruh umur pejantan terhadap kualitas semen beku sapi limousin.
http://elibrary.ub.ac.id/bitstream/123456789/21674/1/Pengaruh-umur-pejantan-terhadap-kualitas-semen-beku-sapi-limousin.pdf .akses 9 September 2013
Anggorodi. 1994. Ilmu Makanan Ternak Umum, Edisi ke Lima. PT. Gramedia Pustaka Utama. Jakarta
Anonim. 2009. Struktur Spermatozoa Sapi.
https://figures.boundless.com/3690/raw/ified-spermatozoon-diagram.svg. Akses November 2013
Anonim. 2013. Data statistik Indonesia.
http://www.datastatistik-indonesia.com/portal/index.php?option=com_proyeksi&task=show&Itemi d=172. Akses November 2013
Anonim. 2013. Vitamin C. http://id.wikipedia.org/wiki/Vitamin C. Akses November 2013
Bandini. 1999. Sapi Potong . Penebar Swadaya. Jakarta
Beconi, M.T., C.R. Francia, N.G. Mora, and M.A. Affranchino. 1993. Effect of natural antioxidants on frozen bovine semen preservation.
Theriogenology. 40: 841--851
BIB Ungaran. 2011. Instruksi Kerja. Balai Inseminasi Buatan Ungaran. Jawa Tengah
BSN. 2005. Semen Beku Sapi (SNI.01-4869-2005). Badan Standarisasi Nasional. Jakarta
Butar, E. 2009. Efektifitas Frekuensi Exercise Terhadap Peningkatan Kualitas Semen Sapi Simmental. http://repository.usu.ac.id/bitstream/1/09E00898.pdf . Diakses pada 5 November 2013
Candra, K.P. 2008. Kerusakan oksidatif (peroksidasi) minyak dan lemak. THP, Faperta UNMUL.
http://krishnapcandra.files.wordpress.com/2012/04/11-th-lecture.pdf. Akses 7 November 2013
Cole, H.H. and P.T Cupps. 1977. Reproduction On Domestic Animal, 3th Ed. Academic Press. New York
Connors, K.A.G. C.Amidon, and J.J Stella. 1992. Stabilitas Kimiawi Sediaan Farmasi Terjemahan Didik Gunawan Jilid 1 Edisi 2 IKIP. Semarang Press. Semarang
Direktorat Jendral Peternakan. 2000. SNI DI. 4869.1.2005 Semen Beku Sapi. Jakarta
Direktorat Jendral Peternakan. 2007. Petunjuk teknis produksi dan distribusi semen beku. Jakarta
Djanuar. 1985. Fisiologi Reproduksi dan Inseminasi Buatan pada Sapi. Gadjah Mada University Press. Yogyakarta.
Dody. 2008. Bangsa-bangsa sapi.
http://dodee88.wordpress.com/2008/10/10/bangsa-bangsa-sapi/. Akses 19 November 2013
Evans, G.W. and M.C Maxwell. 1987. Salamons Artificial Insemination Of Sheep and Goats.Butterworths. London
Farstadt, W. 1996. Semen cryopreservation in dogs and foxs. Anim. Reprod. 70: 218--219
Fathul.F. Liman, N. Purwaningsih, dan S.Tantalo. 2013. Pengetahuan Bahan Pakan dan Formulasi Ransum. Universitas Lampung. Bandar Lampung
49
__________. 2010. Bioteknologi Reproduksi pada Ternak. Alfabeta. Bandung
Garner, D.L., and E.S.E. Hafez. 2000. Spermatozoa and Seminal Plasma. In Reproduction in Farm Animal. Hafez E.S.E. and B. Hafez (eds.) 7th ed. Lippincott & Williams. Baltimore, Marryland. USA
Goldman, E.E. J.E Ellington. F.B Farrel. and R.H Foote. 1991. Use of fresh and frozen thawed bull sperm in vitro. Theriogenology 35: 20--24
Gordon, M.H. 1990. The Mechanism Of Antioxidants Action In Vitro. Elvesier Applied Science. London
Hafez, E.S.E. 1987. Reproduction In Farm Animal. 5th Ed. Lea and Febiger. Philadelphia
Hafez, E.S.E. 2000. Semen Evaluation in Reproduction In Farm Animals. 7th edition. Lippincott Wiliams and Wilkins. Maryland. USA
Hardjosubroto, W. 1994. Aplikasi Pemuliaan Ternak di Lapang. PT Gramedia Widiasarana Aksara Indonesia. Jakarta
Hartono, M. S. Suharyati. dan P.E Santosa. 2008. Penuntun Praktikum Teknologi Reproduksi Ternak. Jurusan Peternakan Fakultas Pertanian Universitas Lampung. Bandar Lampung
Hasnawati,M. 2008. Faktor-faktor yang Mempengaruhi Servic Per
Conception pada Sapi Potong di Kecamatan Terbanggi Besar, Kabupaten Lampung Tengah. Skripsi. Universitas Lampung. Bandar Lampung
Hammerstedt, R.H. l993. Maintenance of bioenergetic balance in sperm and prevention of lipid peroxidation A review of the effects on design and storage preservation system. Reprod. 5: 675--690
Herdis. 2005. Optimalisasi Inseminasi Buatan Melalui Aplikasi Teknologi Laserpunktur pada Domba Garut (Ovis aries). Makalah Ilmiah. Institut Pertanian Bogor. Bogor
Hertoni, N. 2007. Faktor-Faktor Yang Mempengaruhi Motilitas Spermatozoa Semen Beku Sapi Pada Berbagai Inseminator Di Lampung Tengah. Skripsi. Fakultas Pertanian. Universitas Lampung. Bandar Lampung
Jones, R.C. and I.C.A Martin. 1973. The effects of dilution, egg yolk and cooling to 5ºC on the ultrastructure of ram spermatozoa. J Reprod. Fertil.
35: 311--320
Linder, M.C. 1992. Biokimia Nutrisi dan Metabolisme. UI Press. Jakarta
Maxwell, W.M.C and P.F. Watson. 1996. Recent progress in the preservation of ram semen. J. Anim. Reprod. Sci 42: 55--65
Muhilal. 1991. Teori Radikal Bebas dalam Gizi dan Kedokteran. Cermin Dunia Kedokteran
Mumu, M. I. 2009. Viabilitas Semen Sapi Simmental yang Dibekukan Menggunakan Krioprotektal Gliserol. Skripsi. Universitas Tadulako. Sulawesi Tengah
Nursyam. 2007. Perkembangan iptek bidang reproduksi ternak untuk meningkatkan produktivitas ternak.
http//:www.unlam.ac.id./journal/pdf_file. Diakses pada 5 November 2013
Park J.E. and J.K Graham. 1992. Effects of cryopreservation procedur on sperm membranes. Theriogenology. 38: 209--222
Partodiharjo, S. 1982. Ilmu Reproduksi Hewan. Mutiara. Jakarta
Pazil, S.N.BT. 2009. Perbandingan Aktifitas Antioksidan Ekstrak Daging Pisang Raja (Musa AAB ‘Pisang Raja’)dengan Vitamin A, Vitamin C, dan Katekin Melalui Penghitungan Bilangan Peroksida. Skripsi. Fakultas Kedokteran. Universitas Indonesia
Purwasih, Y. S. Ondho. dan Sutopo. 2013. Efektivitas prefreezing semen Sapi Jawa sebagai parameter keberhasilan processing semen beku. Jurnal Ilmiah. http://ejournal-s1.undip.ac.id/index.php/aaj. 2: 44--50
Ridwan. 2009. Pengaruh Pengencer Semen Terhadap Abnormalitas dan Daya Tahan Hidup Spermatozoa Kambing Lokal Pada Penyimpanan Suhu 5ºC. Fakultas Pertanian. Universitas Tadulako
Rizal, M. dan Herdis. 2010. Peranan antioksidan dalam meningkatkan kualitas semen beku. Makalah Ilmiah. Jakarta
Rice, V.A, F.N Andrews, E.J Warwick, and J.E Legates. 1957. Breeding and Improvement Of Farm Animals. McGraw-Hill Book Company, Inc. New York
51
Salisbury, G.W.N.L. dan VanDenmark. 1985. Fisiologi Reproduksi dan
Inseminasi Buatan pada Sapi. Gadjah Mada University Press. Yogyakarta
Sanjaya. 1976. Penggunaan katalase dalam produksi semen dingin sapi. pros. Seminar Nasional Teknologi Peternakan dan Veteriner Puslitbang Peternakan. Bogor 4-5 Agustus 2004
Sauberlich, H.A. 1991. Pengetahuan Gizi Mutakhir. PT. Gramedia Pustaka Utama. Jakarta
Siregar, P. 1992. Metabolit Oksigen Radikal Bebas dan Kerusakan Jaringan. Cermin Dunia Kedokteran. 80: 112—115
Siswono, 2005. Konsumsi protein hewani di bawah standar. http://www.republika.co.id/. Diakses 01 Maret 2014
Steel,R.G.D, dan J.H. Torrie. 1993. Prinsip-Prinsip dan Prosedur Statistika. Diterjemahkan oleh Bambang Sumantri. PT Gramedia Pustaka Utama. Jakarta
Sugeng, Y.B. 1992. Sapi Potong. Penebar Swadaya. Jakarta
Suhartono E, Fachir H dan Setiawan B. 2007. Kapita Sketsa Biokimia Stres Oksidatif Dasar dan Penyakit. Pustaka Benua. Banjarmasin
Sulistyowati, Y. 2006. Pengaruh Pemberian Likopen Terhadap Status
Antioksidan (Vitamin C, Vitamin E dan Gluthation Peroksidase) Tikus (Rattus norvegicus Galur Sprague Dawley) Hiperkolesterolemik. Skripsi Universitas Dipenogoro. Semarang
Susilawati, T. 2011. Spermatozoatology. Universitas Brawijaya Press. Malang
Sumarsono, T. 1998. Peningkatan Kualitas Spermatozoa Kerbau Lumpur dengan Penambahan Asam Askorbat dalam Pengencer Semen Beku. Tesis. Institut Pertanian Bogor. Bogor
Sorenson Jr., A.M. 1979. Laboratory Manual for Animal Reproduction. 4 th Ed. American Press. Boston. USA
Suryana. 2009. Pengembangan usaha ternak sapi potong berorientasi agribisnis dengan pola kemitraan . Jurnal Litbang Pertanian, 28: 29--37
Suryohudoyo, P. 2000. Oksidan, Antioksidan, dan Radikal Bebas. CV Sagung Seto. Jakarta
Toelihere, M. R. 1985. Fisiologi Reproduksi pada Ternak. Angkasa. Bandung.
_______________. 2006. Pokok-pokok pikiran tentang perkembangan (bio) teknologi reproduksi di masa lalu, masa kini, dan masa yang akan datang dalam menunjang pembangunan peternakan di Indonesia. Makalah Ilmiah Fakultas Kedokteran Hewan. Institut Pertanian Bogor. Bogor
UPTD BIBD Lampung. 2013. Standar Oprasional Pemberian Pakan Pejantan. Bandar Lampung
Wahyuni. D. 2000. Populasi sapi bali dan pemenuhan daging.
http://suharjawanasuria.tripod.com/sapi_potong_01.htm. akses: 9 Maret 2014
Werdhany, I.W., M.R. Toelihere, I. Supriatna, dan I.K. Sutama. 2000. Efek pemberian berbagai konsentrasi a-tokoferol sebagai antioksidan dalam pengencer Tris sitrat terhadap motilitas sperma kambing peranakan Etawah. Prosiding Seminar Nasional Peternakan dan Veteriner. Puslitbang Peternakan. Bogor, 18-19 Oktober 1999. Hlm 244-252.
Whit, I.G. 1993. Lipids and calcium uptake of sperm in relation to cold shock and preservation: A Review. Repod. Fertil. Dev. 5: 639--658
Widiastuti, E. 2001. Kualitas Semen Beku Sapi FH dengan Penambahan Antioksidan Vitamin C dan E. Skripsi. Fakultas Peternakan. Institut Pertanian Bogor. Bogor
Widjaja, N. 2011. Pengaruh Pemberian Susu Skim dengan Pengencer Tris Kuning Telur Terhadap Daya Tahan Hidup Spermatozoa Sapi pada Suhu Penyimpanan 5ºC. Skripsi. Fakultas Pertanian. Universitas Bandung Raya. Bandung
Wijaya, A. 1996. Radikal bebas dan parameter status antioksidan.forum diagnostikum no.1.Lab. Klinik Prodia. Jakarta
Witarsa, A. 1997. Pemindahan semen beku. Diklat Pelatihan dan Penanganan Semen Beku. Balai Inseminasi Lembang. Bandung
_______________. 1997. Kimia Pangan dan Gizi. PT.Gramedia Pustaka Utama. Jakarta
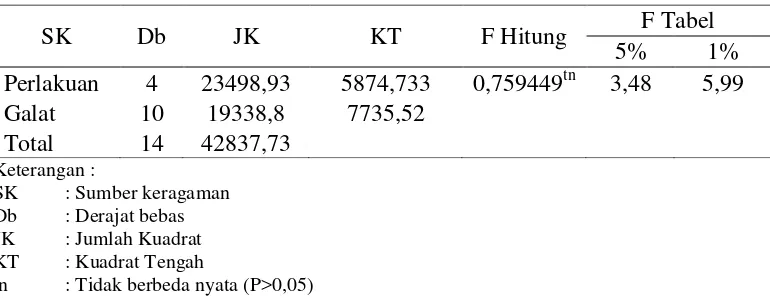
Tabel 4. Hasil analisis ragam motilitas spermatozoa Sapi Bali setelah ekuilibrasi
tn : Tidak berbeda nyata (P>0,05)
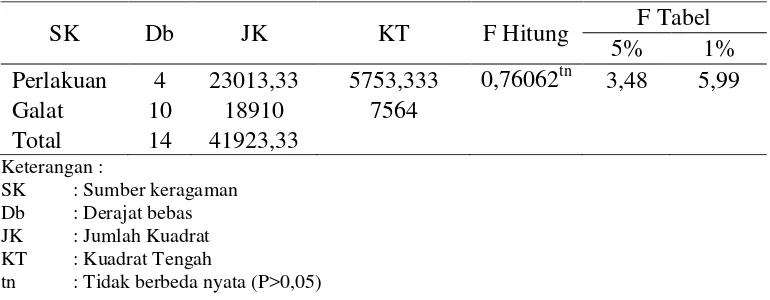
Tabel 5. Hasil analisis ragam motilitas spermatozoa Sapi Bali setelah prefreezing
Keterangan :
SK : Sumber keragaman Db : Derajat bebas JK : Jumlah Kuadrat KT : Kuadrat Tengah
tn : Tidak berbeda nyata (P>0,05)
Tabel 6. Hasil analisis ragam motilitas spermatozoa Sapi Bali PTM (Post Thawing Motility)
tn : Tidak berbeda nyata (P>0,05)
55
Tabel 7. Hasil analisis ragam persentase spermatozoa hidup Sapi Bali setelah ekuilibrasi
tn : Tidak berbeda nyata (P>0,05)
Tabel 8. Hasil analisis ragam persentase spermatozoa hidup Sapi Bali setelah
prefreezing
tn : Tidak berbeda nyata (P>0,05)
Tabel 9. Hasil analisis ragam persentase spermatozoa hidup Sapi Bali PTM (Post Thawing Motility)
tn : Tidak berbeda nyata (P>0,05)