i
UIN SYARIF HIDAYATULLAH JAKARTA
KARAKTERISASI EKSTRAK ETANOL TANAMAN
RUMPUT ISRAEL (
Asystasia gangetica
) DARI TIGA
TEMPAT TUMBUH DI INDONESIA
SKRIPSI
ARSYADANIE SAIFI ADLI
(1110102000031)
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
ii Skripsi ini adalah karya sendiri,
dan semua sumber yang dikutip maupun dirujuk telah saya nyatakan dengan benar
Nama : Arsyadanie Saifi Adli
NIM : 1110102000031
Tanda Tangan :
iii
NAMA : ARSYADANIE SAIFI ADLI
NIM : 1110102000031
JUDUL : KARAKTERISASI EKSTRAK ETANOL TANAMAN RUMPUT
ISRAEL (Asystasia gangetica) DARI TIGA TEMPAT TUMBUH
DI INDONESIA
Menyetujui,
Pembimbing I Pembimbing II
Puteri Amelia, M. Farm., Apt Marissa Angelina, M.Farm., Apt
NIP. 198012042011012004 NIP. 198212312005022001
Mengetahui,
Ketua Program Studi Farmasi
UIN Syarif Hidayatullah Jakarta
iv
Skripsi ini diajukan oleh :
Nama : Arsyadanie Saifi Adli
NIM : 1110102000031
Program studi : Farmasi
Judul : KARAKTERISASI EKSTRAK ETANOL TANAMAN
RUMPUT ISRAEL (Asystasia gangetica) DARI TIGA
TEMPAT TUMBUH DI INDONESIA
Telah berhasil dipertahankan didepan Dewan Penguji dan diterima sebagai bagian persyaratan yang diperlukan untuk memperoleh gelar Sarjana Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan (FKIK) UIN Syarif Hidayatullah Jakarta
DEWAN PENGUJI
Pembimbing 1 : Puteri Amelia, M.Farm., Apt. ( )
Pembimbing 2 : Marissa Angelina, M.Farm., Apt. ( )
Penguji 1 : Ismiarni Komala, Ph.D., Apt ( )
Penguji 2 : Prof. Dr. Atiek Soemiati, MS., Apt ( )
Ditetapkan di : Ciputat
v
Nama : Arsyadanie Saifi Adli
Program studi : Farmasi
Judul : KARAKTERISASI EKSTRAK ETANOL TANAMAN
RUMPUT ISRAEL (Asystasia gangetica) DARI TIGA TEMPAT TUMBUH DI INDONESIA
Rumput Israel (Asystasia gangetica) merupakan tanaman yang tumbuh di daratan Afrika, Arab, dan Asia. Rumput Israel digunakan secara tradisional untuk mengobati asma, rematik, batuk kering, dan gangguan pencernaan. Aktivitas farmakologis dari tanaman Rumput Israel diantaranya efek bronkopasmolitik, anti inflamasi, anti hipertensi, anti artritis, dan antiviral dengue. Karakterisasi dari ekstrak tanaman Rumput Israel perlu dilakukan untuk memperoleh data parameter spesifik dan non spesifik sebagai langkah awal standardisasi untuk menjamin keseragaman khasiat, mutu, dan keamanan. Karakterisasi dilakukan terhadap ekstrak etanol tanaman Rumput Israel dari tiga daerah yang berbeda yaitu Tangerang Selatan, Depok, dan OKU timur. Dari proses ektraksi pada tanaman Rumput Israel didapat rendemen masing-masing sebesar 20,6 %, 18,58 %, dan 20,17 % pada ekstrak Rumput Israel asal Tangsel, Depok, dan OKU Timur. Uji parameter spesifik menunjukkan ekstrak berbentuk kental, berwarna coklat kehijauan, berbau khas, dan berasa pahit dengan kadar senyawa larut air sebesar 60,810 % + 0,37 sampai 74,485%+2,27. Kadar senyawa larut etanol sebesar 36,063%+0,75 sampai 44,065%+0,78. Fase gerak terbaik pada KLT yakni kloroform : metanol (9:1) dan HPLC air : metanol (8:2). Kandungan kimia yakni flavonoid, alkaloid, tanin, dan steroid, dengan kadar total flavonoid 4,3 % sampai 8,162 %. Hasil uji parameter non spesifik menunjukkan susut pengeringan 18,098 % + 0,04 sampai 19,065 % + 0,55, bobot jenis 1,0165 g/mL + 0,0001 sampai 1,0184 g/mL + 0,0001, kadar air 7,573 % + 0,13sampai9,742 % + 0,10. Kadar abu 18,604 % + 1,33 sampai 32,153 % + 0,79, kadar abu tidak larut asam 3,061 % + 0,72 sampai 3,506 % + 0,34. Sisa pelarut (etanol) tidak terdeteksi dengan GCMS. Cemaran Pb (Timbal) tidak terdeteksi sedangkan cemaran Cd (Kadmium) 4,96 ppm sampai 6,52 ppm dan cemaran As (Arsen) ketiga ekstrak <0,005 ppm.
Kata kunci : Karakterisasi, Asystasia gangetica, Rumput Israel, Parameter spesifik, Parameter non spesifik.
vi
Name : Arsyadanie Saifi Adli
Department : Pharmacy
Judul : CHARACTERIZATION OF ETHANOL EXTRACT OF
RUMPUT ISRAEL (Asystasia gangetica) FROM THREE PLACES IN INDONESIA
Rumput Israel (Asystasia gangetica) is a plant that grows in mainland Africa, Arabia, and Asia. Rumput Israel traditionally used to treat asthma, arthritis, dry cough, and digestive disorders. Pharmacological activites Rumput Israel including broncopasmolitic effects, anti-inflammatory, anti-hypertensive, anti-arthritis, and antiviral dengue. Characterization of Rumput Israel needs to be done to obtain data on specific and non-specific parameters as a first step to ensure uniform standardization of efficacy, quality, and safety. Characterization made to ethanol extract of Rumput Israel from three different regions of the South Tangerang, Depok, and East OKU. Extraction process in the Rumput Israel yield obtained respectively by 20.6%, 18.58%, and 20.17% in Rumput Israel from South Tangerang, Depok, and East OKU. Specific test parameters showed extracts shaped thick, greenish brown, characteristic odor and a bitter taste with the levels of water-soluble compounds 60,810 % + 0,37 to 74,485 % + 2,27. Levels of ethanol-water-soluble compounds by 36,063 % +0,75 to 44,065% + 0,78. The best mobile phase in TLC is chloroform : methanol (9 : 1) and HPLC is water : methanol (8 : 2). The chemical constituents of flavonoids, alkaloids, tannins, and steroids, with levels of total flavonoids 4.3% to 8.162%. The test results of non-specific parameters indicate of drying shrinkage 18,098 % + 0,04 to 19,065 % + 0,55, a specific gravity of 1,0165 g/mL + 0,0001 to 1,0184 g/mL + 0,0001, the water content of 7,573 % + 0,13 to
9,742 % + 0,10. Ash content is 18,604 % + 1,33 to 32,153 % + 0,79, acid insoluble
ash content 3,061 % + 0,72 to 3,506 % + 0,34. Residual solvent (ethanol) was not
detected by GCMS. Contamination Pb (Lead) not detected while the contamination of Cd (Cadmium) 4.96 ppm to 6.52 ppm and contamination of As (Arsenic) all extract <0.005 ppm.
vii
Alhamdulillah, Puji dan syukur penulis panjatkan kehadirat Allah SWT
yang telah melimpahkan nikmat dan karunia-Nya sehingga penulis dapat
menyelesaikan penelitian dan penyusunan skripsi ini. Shalawat dan salam selalu
tercurah kepada Nabi Muhammad SAW.
Skripsi dengan judul “Karakterisasi Ekstrak Etanol Tanaman Rumput Israel
(Asystasia gangetica) dari Tiga Tempat Tumbuh di Indonesia” ini disusun untuk
memenuhi salah satu syarat menempuh ujian akhir guna mendapatkan gelar Sarjana
Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan
Universitas Islam Negeri Syarif Hidayatullah Jakarta.
Dalam proses penelitian dan penyusunan skripsi ini penulis menyadari ada
beberapa pihak yang sangat memberikan kontribusi kepada penulis. Maka
perkenankanlah penulis menyampaikan rasa terima kasih yanng sebesar-besarnya
khususnya kepada :
1. Allah SWT, atas rahmat, nikmat, dan karuni-Nya sehingga dengan izinnya
penulis dapat menyelesaikan skripsi ini.
2. Kedua orang tua, Abah tercinta dr. Suriadie dan Mama tercinta dr. Siti
Nurjanah yang tiada henti memberikan kasih sayang, nasihat, dan do’a serta
dukungan kepada ananda baik moril maupun materil.
3. Ibu Puteri Amelia, M. Farm., Apt. sebagai pembimbing I dan Ibu Marissa
Angelina, M. Farm., Apt. sebagai pembimbing II yang telah rela meluangkan
waktu, pikiran dan tenaganya untuk membimbing serta memotivasi penulis
selama penelitian.
4. Ibu Lia, Ibu Tatik, Mas Lili, Ibu Lisna, Ibu Mimin, Ibu Lala, Ibu Mega, Mas
Udin, Pak Rokib, Pak Wakhidi atas segala bantuan yang telah diberikan
selama penelitian.
5. Prof. Dr. (hc) dr. M. K. Tadjudin, Sp.And selaku Dekan Fakultas Kedokteran
dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
6. Drs. Umar Mansur, M.Sc., Apt. selaku Ketua Program Studi Farmasi Fakultas
viii
menyelesaikan studi di program studi farmasi FKIK UIN Syarif Hidayatullah
Jakarta.
7. Sahabat penulis, Andalusia, yang selalu satu dalam langkah, erat dalam
ukhuwah, dan saling menyukseskan. The paviliun, yang susah senang
bersama, dan semua cowo Andalusia, Arum, Fikry, Dwikky, Fahrur, Erwin,
Chandra, Atras, Hafit, Denny, Anas, Iid, Luther, Rendy, Hadi, Mirza.
8. Kakakku tercinta drg. Ichda Nabiela, dan adikku tersayang Faiq Fadhil
Dzulfiqar Bariq, Mirza Zuffar Al-Haq Firdausi, Gharizza Nayla.
9. Keluarga besar Bani Amir dan Bani Taberani yang selalu memberikan
motivasi dan dukungannya.
10.Seluruh pihak yang telah membantu penulis selama ini yang tidak bisa penulis
sebut satu persatu.
Jakarta, 3 September 2014
ix
Sebagai civitas akademik Universitas Islam Negeri (UIN) Syarif
Hidayatullah Jakarta, saya yang bertanda tangan dibawah ini :
Nama : Arsyadanie Saifi Adli
NIM : 1110102000031
Program Studi : Farmasi
Fakultas : Kedokteran dan Ilmu Kesehatan (FKIK)
Jenis Karya : Skripsi
Demi pengembangan ilmu pengetahuan, saya menyetujui skripsi/karya
ilmiah saya dengan judul :
KARAKTERISASI EKSTRAK ETANOL TANAMAN RUMPUT ISRAEL
(Asystasia gangetica) dari TIGA TEMPAT TUMBUH DI INDONESIA
untuk dipublikasikan atau ditampilkan di internet atau media lain yaitu Digital
Library Perpustakaan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta
untuk kepentingan akademik sebatas sesuai dengan Undang-Undang Hak Cipta.
Dengan demikian persetujuan publikasi karya ilmiah ini saya buat dengan
sebenarnya.
Dibuat di : Ciputat
Pada Tanggal : 3 September 2014
Yang menyatakan
x
HALAMAN JUDUL ... i
HALAMAN PERNYATAAN ORISINALITAS ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN SKRIPSI ... iv
ABSTRAK ... v
ABSTRACT ... vi
KATA PENGANTAR ... vii
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI TUGAS AKHIR UNTUK KEPENTINGAN AKADEMIK ... ix
DAFTAR ISI ... x
2.2. Karakterisasi Sebagai Langkah Awal Standardisasi ... 10
2.2.1. Pengertian Standardisasi ... 10
2.2.2. Standardisasi Menjamin Keseragaman Khasiat ... 11
2.2.3. Standardisasi untuk Uji Klinik ... 11
xi
2.3. Parameter-Parameter Standar Ekstrak ... 12
2.3.1. Parameter Spesifik ... 13
2.7. Faktor yang Mempengaruhi Mutu Ekstrak ... 19
2.7.1. Faktor Biologi ... 19
2.11. Kromatografi Gas-Spektrometri Massa ... 30
BAB III METODE PENELITIAN ... 33
3.3.2. Karakterisasi Ekstrak Rumput Israel ... 35
xii
BAB IV HASIL DAN PEMBAHASAN ... 44
4.1. Determinasi Tanaman ... 44
4.2. Rendemen Ekstrak ... 44
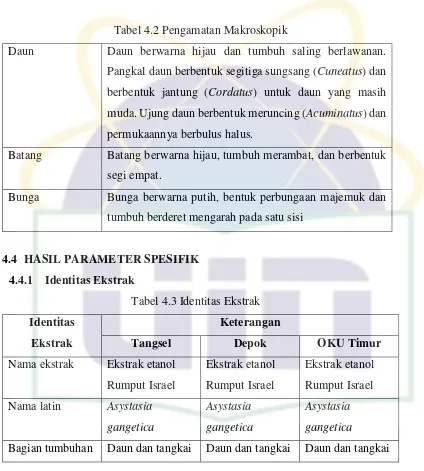
4.3. Pengamatan Makroskopik ... 44
4.4. Hasil Parameter Spesifik ... 45
4.4.1. Identitas Ekstrak ... 45
4.4.2. Organoleptik Ekstrak ... 45
4.4.3. Senyawa Terlarut Dalam Pelarut Tertentu ... 46
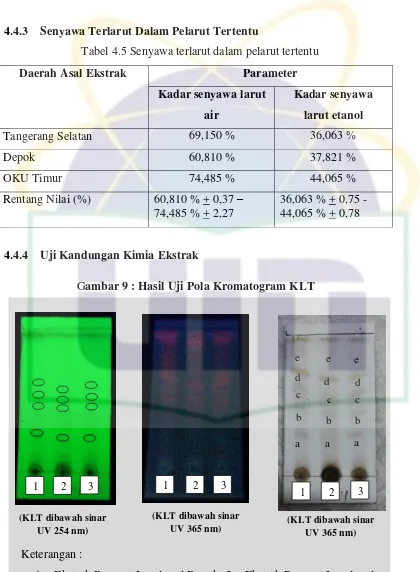
4.4.4. Uji Kandungan Kimia Ekstrak ... 46
4.5. Hasil Parameter Non Spesifik ... 49
4.6. Pembahasan ... 50
BAB V KESIMPULAN DAN SARAN ... 59
5.1. Kesimpulan ... 59
5.2. Saran ... 60
DAFTAR PUSTAKA ... 61
xiii
Gambar 1 : Asystasia gangetica ... 7
Gambar 2 : Asystasia gangetica ... 8
Gambar 3 : Asystasia gangetica ... 8
Gambar 4 : Skema Kromatografi Lapis Tipis ... 20
Gambar 5 : Skema Spektrofotometer UV-Vis ... 24
Gambar 6 : Skema Spektrofotometer Serapan Atom ... 26
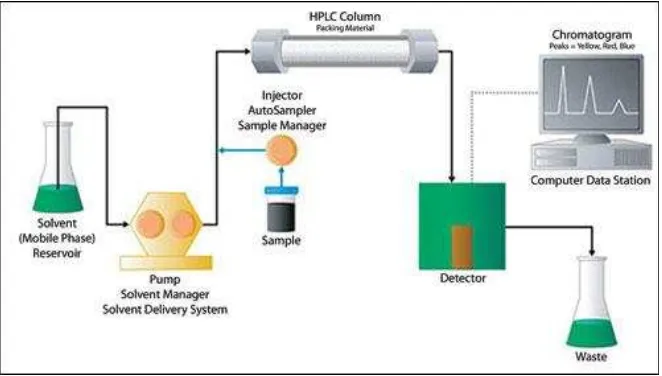
Gambar 7 : Skema Kromatografi Cair Kinerja Tinggi ... 28
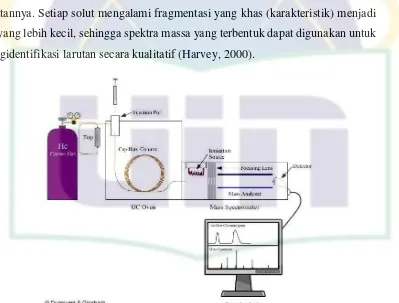
Gambar 8 : Skema GCMS ... 31
Gambar 9 : Hasil Uji Pola Kromatogram KLT ... 46
Gambar 10 : Hasil Uji Pola Kromatogram KCKT ... 47
Gambar L.1 : Ekstrak etanol Asystasia gangetica asal Tangsel ... 68
Gambar L.2 : Ekstrak etanol Asystasia gangetica asal Depok ... 68
Gambar L.3 : Ekstrak etanol Asystasia gangetica asal OKU Timur ... 68
Gambar L.4 : Spektrofotometri UV-Vis ... 68
Gambar L.5 : Desikator ... 68
Gambar L.6 : Muffle Furnace ... 68
Gambar L.7 : Pilot Plant ... 69
Gambar L.8 : Mikroskop ... 69
Gambar L.9 : GCMS ... 69
Gambar L.10 : HPLC ... 69
xiv
Tabel 4.1 : Rendemen Ekstrak ... 44
Tabel 4.2 : Pengamatan Makroskopik ... 45
Tabel 4.3 : Identitas Ekstrak ... 45
Tabel 4.4 : Organoleptik Ekstrak ... 45
Tabel 4.5 : Senyawa Terlarut Dalam Pelarut Tertentu ... 46
Tabel 4.6 : Nilai Rf KLT ... 47
Tabel 4.7 : Data Puncak Kromatogram KCKT ... 48
Tabel 4.8 : Penapisan Golongan Kimia... 48
Tabel 4.9 : Kadar Flavonoid ... 48
Tabel 4.10 : Parameter Non Spesifik ... 49
Tabel 4.11 : Parameter Non Spesifik Cemaran ... 49
Tabel L.1 : Senyawa Terlarut Air ... 80
Tabel L.2 : Senyawa Terlarut Etanol ... 82
Tabel L.3 : Susut Pengeringan ... 84
Tabel L.4 : Bobot Jenis ... 86
Tabel L.5 : Kadar Abu ... 88
Tabel L.6 : Kadar Abu Tidak Larut Asam ... 90
xv
Lampiran 1 : Alur Penelitian ... 65
Lampiran 2 : Determinasi Tanaman Rumput Israel ... 66
Lampiran 3 : Alat dan Bahan Penelitian ... 68
Lampiran 4 : Hasil Uji Cemaran Logam ... 70
Lampiran 5 : Uji Sisa Pelarut Dan Pola Kromatogram GCMS ... 75
Lampiran 6 : Perhitungan Rendemen Ekstrak ... 79
Lampiran 7 : Perhitungan Senyawa Terlarut Air ... 80
Lampiran 8 : Perhitungan Senyawa Terlarut Etanol ... 82
Lampiran 9 : Perhitungan Susut Pengeringan ... 84
Lampiran 10 : Perhitungan Bobot Jenis ... 86
Lampiran 11 : Perhitungan Kadar Abu ... 88
Lampiran 12 : Perhitungan Kadar Abu Tidak Larut Asam ... 90
Lampiran 13 : Perhitungan Kadar Air ... 92
Lampiran 14 : Perhitungan Kadar Total Flavonoid ... 94
UIN Syarif Hidayatullah Jakarta
BAB I PENDAHULUAN
1.1. LATAR BELAKANG
Indonesia dikenal sebagai negara dengan sumber daya hayati kedua
terbesar setelah Brasil. Di Indonesia terdapat lebih kurang 30.000 jenis
tumbuh-tumbuhan yang hidup di kepulauan Indonesia, diketahui sekurang-kurangnya 9.600
spesies tumbuhan berkhasiat sebagai obat dan kurang lebih 300 spesies telah
digunakan sebagai bahan obat tradisional oleh industri obat tradisional
(Kotranas, 2007).
Berdasarkan data Badan Penelitian dan Pengembangan Pertanian (2005),
Indonesia memiliki ketergantungan yang besar terhadap bahan baku dan obat
konvensional impor senilai 160 juta USD/tahun, padahal berdasar kekayaan
tanaman yang dimiliki Indonesia berpotensi besar menjadi sumber daya tanaman
obat bagi dunia. Tren global “back to nature” menunjukkan pertumbuhan pesat,
termasuk di Indonesia, sehingga produk tanaman obat (TO) memiliki arti strategis
di bidang kesehatan.
Faktor pendorong terjadinya peningkatan penggunaan obat herbal di
negara maju adalah usia harapan hidup yang lebih panjang pada saat prevalensi
penyakit kronik meningkat, adanya kegagalan penggunaan obat modern untuk
penyakit tertentu di antaranya kanker serta semakin luas akses informasi mengenai
obat herbal di seluruh dunia (Sukandar EY, 2006).
Obat herbal telah diterima secara luas di hampir seluruh Negara di dunia.
Menurut WHO, negara negara di Afrika, Asia dan Amerika Latin menggunakan
obat herbal sebagai pelengkap pengobatan primer yang mereka terima. Bahkan di
Afrika, sebanyak 80% dari populasi menggunakan obat herbal untuk pengobatan
primer. WHO merekomendasi penggunaan obat tradisional termasuk herbal dalam
pemeliharaan kesehatan masyarakat, pencegahan dan pengobatan penyakit,
terutama untuk penyakit kronis, penyakit degeneratif dan kanker. WHO juga
mendukung upaya-upaya dalam peningkatan keamanan dan khasiat dari obat
UIN Syarif Hidayatullah Jakarta Fakta bahwa penggunaan obat berbasis tumbuhan semakin berkembang
pesat di masyarakat seiring dengan kekayaan biodiversitas yang dimiliki Indonesia,
serta dukungan dari WHO perihal upaya pengembangan obat herbal, menjadikan
tugas bagi pemerintah untuk menjamin obat berbasis herbal memiliki mutu yang
terukur, mampu mendukung derajat kesehatan, terjamin keamanannya dengan
terbebas dari bahan mikroba berbahaya, serta meningkatkan nilai ekonomi produk
alam Indonesia.
Berdasarkan Farmakope Herbal (2009), Obat herbal terstandar merupakan
sediaan obat bahan alam yang telah dibuktikan keamanan dan khasiatnya secara
ilmiah dengan uji praklinik dan bahan bakunya telah distandardisasi. Salah satu
tanaman yang sedang dikembangkan sebagai obat herbal terstandar adalah Rumput
Israel (Asystasia gangetica).
Rumput Israel (Asystasia gangetica) merupakan tanaman yang tumbuh di
daratan Afrika, Arab, dan Asia. Di Kenya dan Uganda, tanaman ini dikonsumsi
sebagai sayuran, sedangkan di Nigeria, daun dari tanaman ini digunakan untuk
mengobati asma. Di India, tanaman ini digunakan untuk mengobati penyakit
rematik, sedangkan di Maluku, tanaman ini diolah menjadi jus dan dicampur
dengan jeruk dan bawang putih untuk mengobati batuk kering. Sedangkan di
Filipina, tanaman ini digunakan untuk mengobati gangguan pencernaan
(Grubben G.J.H, 2004).
Menurut Ezike et al (2008), penggunaan Asystasia gangetica sebagai obat
tradisional asma dikarenakan adanya kandungan terpenoid pada tanaman tersebut
yang dapat memberikan efek bronkopasmolitik
Berdasarkan penelitian Mohan Khrisna (2011), ekstrak metanol Asystasia
gangetica memiliki aktivitas anti inflamasi yang signifikan dengan perkiraan
mekanisme yakni menghambat sintesis prostaglandin dengan menstabilkan
membran lisosom.
Antosianin yang diisolasi dari ekstrak etanol Asystasia gangetica memiliki
aktivitas menghambat alfa-amilase yang cukup baik sehingga dapat dikembangkan
sebagai obat anti diabetes (Rajeshwari Sivaraj et al, 2013)
Menurut penelitian Mugabo Pierre dan Raji Ismaila (2013), ekstrak air
UIN Syarif Hidayatullah Jakarta
SHR (Spontaneously Hypertensive Rats) dengan perkiraan mekanisme yakni
melalu penghambatan ACE (Angiotensin Converting Enzyme) dan sebagai
antagonis reseptor Angiotensin II, sehingga dapat dikembangkan sebagai obat anti
hipertensi.
Ekstrak metanol dari Asystasia gangetica dengan konsentrasi 200 µg/mL
menunjukkan aktivitas penghambatan yang denaturasi protein yang cukup baik,
yakni sebesar 42,7 % sedangkan Natrium diklofenak sebagai standar dengan
konsentrasi yang sama, memiliki aktivitas penghambatan denaturasi protein sebesar
84,47 %. Hal ini menunjukkan peluang digunakannya tanaman Asystasia gangetica
sebagai obat anti artritis.
Albendazole digunakan sebagai standar untuk mengetahui aktivitas
anthelmintic dari ekstrak metanol Asystasia gangetica dengan Pheretima posthuma
sebagai objek. Ekstrak metanol Asystasia gangetica dengan konsentrasi 10 mg/ml
menunjukkan aktivitas yang baik, dimana membutuhkan waktu 54 menit untuk
mematikan Pheretima posthuma, sedangkan albendazole dengan konsentrasi yang
sama membutuhkan waktu 56 menit (Gopal T.K et al, 2013).
Bedasarkan penelitian yang dilakukan oleh LIPI (Lembaga Ilmu
Pengetahuan Indonesia) dengan metode foccus forming assay, tanaman Rumput
Israel (Asystasia gangetica) memiliki aktivitas antiviraldengue dengan nilai IC50
sebagai parameternya. Berbagai manfaat yang ada dalam tanaman Asystasia
gangetica tentu berasal dari senyawa kimia yang dikandungnya, dimana
berdasarkan penelitian Kensa Mary (2011), Asystasia gangetica diketahui
mengandung senyawa fenol, alkaloid, flavonoid, tanin, saponin, dan steroid.
Kandungan kimia yang terdapat dalam tanaman Asystasia gangetica tidak
dapat dijamin konstan karena adanya faktor-faktor yang mempengaruhi,
diantaranya bibit, umur tanaman, tempat tumbuh, iklim, serta cara panen.
Kandungan kimia yang bertanggungjawab terhadap efek biologis harus mempunyai
spesifikasi kimia berupa jenis dan kadar, sedangkan ekstrak sebagai bahan baku
obat harus memenuhi syarat mutu dan keamanan, sehingga harus dilakukan
standardisasi. Sampai saat ini belum ada laporan penelitian baik nasional maupun
UIN Syarif Hidayatullah Jakarta
Untuk menjamin keseragaman khasiat, mutu, dan keamanan dari suatu
ekstrak, perlu dilakukan standardisasi. Standardisasi dalam kefarmasian adalah
serangkaian parameter prosedur dan cara pengukuran yang hasilnya merupakan
unsur-unsur terkait paradigma mutu kefarmasian, mutu dalam artian memenuhi
syarat standar (kimia, biologi, dan farmasi), termasuk jaminan (batas-batas)
stabilitas sebagai produk kefarmasian umumnya. Persyaratan mutu ekstrrak terdiri
dari berbagai parameter standar umum dan parameter standar spesifik (Depkes RI,
2000).
Melihat manfaat dari tanaman Asystasia gangetica berdasarkan beberapa
penelitian yang telah dilakukan, dan banyaknya ketersediaan tanaman Rumput
Israel (Asystasia gangetica) di Indonesia, serta sejalan dengan pengembangan
ekstrak Rumput Israel (Asystasia gangetica) sebagai obat antiviral dengue oleh
Lembaga Penelitian Indonesia (LIPI), maka perlu adanya penelitian tentang
karakterisasi ekstrak etanol tanaman Rumput Israel (Asystasia gangetica) dari 3
tempat tumbuh di Indonesiauntuk mengetahui standar mutu dan keamanan, serta
menjaga kualitas dari ekstrak Asystasia gangetica dalam rangka pengembangan
obat herbal di Indonesia.
1.2. RUMUSAN MASALAH
Berdasarkan latar belakang yang telah dikemukakan, diketahui bahwa
belum ada penelitian mengenai karakterisasi ekstrak etanol Rumput Israel
(Asystasia gangetica) sebagai tahap pengembangan ekstrak terstandar.
1.3. TUJUAN PENELITIAN
Tujuan penelitian ini adalah :
1. Menetapkan parameter non spesifik yang meliputi susut pengeringan, bobot
jenis, kadar air, kadar abu, sisa pelarut, dan cemaran logam berat pada ekstrak
etanol Rumput Israel (Asystasia gangetica)
2. Menetapkan parameter spesifik yang meliputi identitas ekstrak, organoleptik
ekstrak, senyawa terlarut dalam pelarut tertentu, pola kromatogram, dan
kandungan kimia ekstrak pada ekstrak etanol Rumput Israel (Asystasia
UIN Syarif Hidayatullah Jakarta
1.4. MANFAAT PENELITIAN
Dengan penelitian ini diharapkan dapat diperoleh data karakterisasi dari
ekstrak etanol Rumput Israel (Asystasia gangetica) berupa parameter spesifik dan
non spesifik sebagai langkah awal dalam menjamin keseragaman khasiat, mutu, dan
UIN Syarif Hidayatullah Jakarta
BAB II
TINJAUAN PUSTAKA
2.1 RUMPUT ISRAEL (Asystasia gangetica)
2.1.1 Klasifikasi Tanaman
Klasifikasi dari tanaman ini adalah sebagai berikut :
Kingdom : Plantae
Subkingdom : Tracheobionta
Superdivision : Spermatophyta
Division : Magnoliophyta
Class : Magnoliopsida
Subclass : Asteridae
Order : Scrophulariales
Family : Acanthaceae
Genus : Asystasia Blume
Species : Asystasia gangetica (L.) T. Anderson
(Tilloo S.K et al, 2012)
2.1.2 Sinonim dan Nama Daerah
Sinonim : Asystasia coromandeliana Nees (1832)
Nama Daerah : Chinese Violet (Inggris), Herbe le rail (Prancis),
Namu (Liberia), Ara Sungsang, Seri Pagi (Malaysia), Rumput Israel
(Indonesia) (Grubben G.J.H, 2004).
2.1.3 Deskripsi
Asystasia gangetica tumbuh merambat dan bercabang, batangnya
berbentuk segi empat dengan panjang hingga 2 meter. Bentuk daun saling
berlawanan dan tidak terdapat stipula. Panjang tangkai daun 0,5-6 cm dengan
daun yang berbentuk ovutus dengan panjang 4-9 cm dan lebar 2-5 cm. Bentuk
pangkal daun segitiga sungsang (Cuneatus) atau berbentuk jantung (Cordatus)
saat daun masih kecil. Ujung daun berbentuk meruncing (Acuminatus) dan
UIN Syarif Hidayatullah Jakarta
memiliki 4-6 urat daun (vena lateralis) di setiap sisi pelepah. Bentuk perbungaan
majemuk dan berderet mengarah pada satu sisi dengan panjang deret bunga
mencapai 25 cm. Tangkai bunga memiliki panjang hingga 3 mm dan kelopak
bunga dengan panjang 4-10 mm. Bunga biasanya berwarna putih atau putih
dengan bintik-bintik keunguan (Grubben G.J.H, 2004).
Periode dari penyebaran bibit hingga munculnya benih Asystasia
gangetica membutuhkan waktu 8 minggu di daerah terbuka atau terkena sinar
matahari langsung, tetapi bisa memakan waktu 2 minggu lebih lama di daerah
yang sebagian tertutup. Tanpa penyiangan, proporsi Asystasia gangetica dalam
semak dari perkebunan kelapa sawit muda meningkat dalam jangka waktu 2 tahun
dari 25 % menjadi 84 %. Asystasia gangetica memiliki daya serap tinggi terhadap
nutrisi dalam tanah dan mengganggu penyerapan nutrisi spesies lain sehingga
dikategorikan sebagai gulma. Asystasia gangetica memiliki palatabilitas dan daya
cerna yang tinggi sehingga dapat digunakan sebagai pakan hewan
(Grubben G.J.H, 2004).
Gambar 1 : Asystasia Gangetica
UIN Syarif Hidayatullah Jakarta
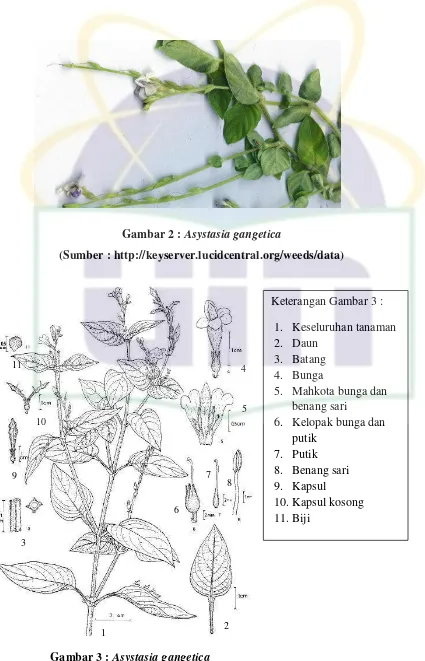
Gambar 2 : Asystasia gangetica
(Sumber :http://keyserver.lucidcentral.org/weeds/data)
Keterangan Gambar 3 :
1. Keseluruhan tanaman 2. Daun
3. Batang 4. Bunga
5. Mahkota bunga dan benang sari
6. Kelopak bunga dan putik
7. Putik 8. Benang sari 9. Kapsul
10.Kapsul kosong 11.Biji
Gambar 3 : Asystasia gangetica
(Sumber : Tsai Wen Hsu et al, 2005)
1 2
3
4
5
6 7
8 9
UIN Syarif Hidayatullah Jakarta
2.1.4 Tempat Tumbuh
Asystasia gangetica berasal dari daratan tropis Afrika, Arabia dan Asia.
Asystasia gangetica biasa ditemukan di pinggir jalan dan tepi sungai, di daerah
yang lembab, dan dapat tumbuh hingga ketinggian 2.500 m dpl. Di daerah dengan
musim kemarau 4 bulan atau lebih, tanaman ini kemungkinan tidak dapat bertahan
hidup. Asystasia gangetica dapat berkembang pada tanah aluvium pantai, tanah
gambut dengan 85 % bahan organik dan pH 3,5-4,5 , dan tanah liat. Dua
subspesies dari Asystasia gangetica dapat dibedakan, dimana Asystasia gangetica.
Subsp. micrantha ( Nees ) Ensermu, dengan panjang mahkota bunga kurang dari
2,5 cm dan panjang tangkai putik kurang dari 1,5 cm biasanya tumbuh di daerah
tropis Afrika, pulau-pulau di Samudera Hindia dan Arab Saudi. Sedangkan
Subsp. gangetica, dengan panjang mahkota bunga lebih dari 2,5 cm dan tangkai
putik lebih dari 1,5 cm biasanya tumbuh di India, Sri Lanka, Asia Tenggara dan
pulau-pulau di Samudera Pasifik, dan terdapat juga di daerah tropis benua
Amerika (Grubben G.J.H, 2004).
2.1.5 Penggunaan dan Khasiat
Rumput Israel (Asystasia gangetica) secara lokal digunakan sebagai
sayuran di Kenya dan Uganda dimana tanaman ini dicampur dengan kacang tanah,
wijen, ataupun sayuran lainnya. Kemampuan tumbuh yang baik dan nilai gizi
yang tinggi menjadikan Asystasia gangetica digunakan sebagai pakan untuk sapi,
kambing dan domba di Asia Tenggara. Di Afrika, larutan dari tanaman ini
digunakan untuk meringankan rasa sakit saat melahirkan, dan getahnya digunakan
untuk mengobati luka, meredakan otot kaku dan pembesaran limpa pada
anak-anak. Serbuk dari akar Asystasia gangetica dipercaya memiliki efek analgesik dan
digunakan dalam mengobati sakit perut dan gigitan ular. Larutan dari daun
Asystasia gangetica digunakan untuk mengobati epilepsi dan gangguan saluran
kemih (Grubben G.J.H, 2004).
Asystasia gangetica telah banyak digunakan sejak zaman kuno di daerah
Babungo, Kamerun untuk mengobati berbagai penyakit. Masyarakat pedesaan di
daerah Sivagangai dari Tamil Nadu, India Selatan, menggunakan Rumput Israel
UIN Syarif Hidayatullah Jakarta
Nadu, menggunakan pasta dari akar Asystasia gangetica untuk mengobati alergi
kulit. Di Kawazu-Natal, Afrika Selatan, penduduk menggunakan Asystasia
gangetica sebagai sayuran. Secara tradisional, jus dari tanaman ini digunakan
sebagai anthelmintik, mengobati pembengkakan, rematik, gonorrhea dan
penyakit pada telinga. Asystasia gangetica juga digunakan sebagai obat
tradisional untuk mengobati diabetes mellitus di beberapa daerah di India Selatan
(Tilloo S.K et al, 2012).
2.1.6 Kandungan Kimia
Asystasia gangetica mengandung senyawa alkaloid, antrakuinon, senyawa
fenolik, steroid, tanin, glikosida, dan xanthoprotein (Daffodil E.D et al, 2013).
Ekstrak metanol Asystasia gangetica mengandung beberapa senyawa flavonoid,
diantaranya Luteolin, Kuersetin, Kaempferol, dan Isorhamnetin
(Gopal T.K et al, 2013).
Senyawa glikosida biflavon dari Asystasia gangetica yang telah berhasil
diisolasi dan dikarakterisasi yakni apigenin 7-0-glukosil (3’-6’’) luteolin 7’’
-0-glukosida (Senthamilselvi M.M et al, 2011). Selain itu, senyawa glikosida
epoksimegastigmane (asygangoside) dari Asystasia gangetica juga telah berhasil
diisolasi (Kanchanapoom T et al, 2007).
2.2 KARAKTERISASI EKSTRAK SEBAGAI LANGKAH AWAL
STANDARDISASI
2.2.1 Pengertian Standardisasi
Standardisasi suatu simplisia tidak lain adalah pemenuhan terhadap
persyaratan sebagai bahan dan penetapan nilai berbagai parameter dari produk
seperti yang ditetapkan sebelumnya. Standardisasi simplisia mempunyai
pengertian bahwa simplisia yang akan digunakan untuk obat sebagai bahan baku
harus memenuhi persyaratan yang tercantum dalam monografi terbitan resmi
Departemen Kesehatan (Materia Medika Indonesia). Sedangkan sebagai produk
yang langsung dikonsumsi, juga harus memenuhi persyaratan produk kefarmasian
UIN Syarif Hidayatullah Jakarta
Mengingat obat herbal dan berbagai tanaman memiliki peran penting
dalam bidang kesehatan bahkan bisa menjadi produk andalan Indonesia, maka
perlu dilakukan upaya penetapan standar mutu dan keamanan ekstrak tanaman
obat. Rangkaian proses melibatkan berbagai metode analisis kimiawi berdasarkan
data farmakologis, melibatkan analisis fisik dan mikrobiologi berdasarkan kriteria
umum keamanan (toksikologi) terhadap suatu ekstrak alam (tumbuhan obat)
disebut standardisasi bahan obat alam (SBOA) atau standardisasi obat herbal
(Saifudin et al, 2011)
2.2.2 Standardisasi Menjamin Keseragaman Khasiat
Mayoritas penggunaan bahan obat berbasis herbal di Indonesia masih
bersifat tidak terukur baik kepastian tanaman, takaran, cara penyiapan sehingga
tidak menjamin konsistensi khasiat. Salah satu tujuan dari standardisasi adalah
menjaga konsistensi dan keseragaman khasiat dari obat herbal. Standardisasi
melibatkan pemastian kadar senyawa aktif farmakologis melalui analisis
kuantitatif metabolit sekunder yang akan menjamin keseragaman khasiat.
Tercatat sekitar 997 industri obat tradisional di Indonesia dan 98
diantaranya adalah produsen dengan skala besar dan sedang. Produsen dengan
skala besar dan sedang telah mampu mengekspor produknya ke negara lain seperti
Malaysia, Singapura, India, Pakistan, negara-negara di Timur Tengah bahkan
beberapa negara di Eropa dan Amerika Serikat. Banyak bahan mentah rempah dan
obat herbal diekspor ke luar negeri tanpa mengalami pengolahan. Masalah yang
seringkali dihadapi adalah belum terstandarnya bahan baku yang diperdagangkan
bahkan dijumpainya kontaminan mikrobiologis pada produk obat herbal
(Saifudin et al, 2011).
2.2.3 Standardisasi untuk Uji Klinik
Uji Klinik adalah uji senyawa kimia obat, obat herbal, ekstrak dan berbagai
sediaan pada dosis tertentu dengan target biologis manusia (atau veteriner jika
targetnya memang binatang), agar memberikan respon biologis berupa
parameter-parameter klinik perbaikan dari kondisi patologis yang terkait dengan penyakit
UIN Syarif Hidayatullah Jakarta
Respon uji klinik sangat ditentukan oleh konsistensi dosis. Jika jumlah zat aktif
yang diberikan tidak konsisten, maka interpretasinya menjadi bias dan justru
merugikan. Disinilah peran besar standardisasi untuk menjaga senyawa-senyawa
aktif selalu konsisten terukur antarperlakuan (Saifudin et al, 2011).
2.2.4 Standardisasi Menjamin Aspek Keamanan dan Stabilitas Ekstrak
Tempat tumbuh tanaman, penanganan pasca panen, proses ekstraksi,
penyimpanan simplisia tanaman dan ekstrak juga mempengaruhi elemen
keamanan terhadap pemakai, misalnya keberadaan logam berat (Pb, Cd,dan As),
pestisida dalam tanah, udara dan air, jenis dan jumlah mikroorganisme dan
metabolit pencemar berbahaya. Keberadaan air di dalam suatu ekstrak juga
mempengaruhi stabilitas bahan baku bahkan bentuk sediaan yang nantinya
dihasilkan. Untuk itu dilakukan berbagai analisis untuk menentukan batas
minimal kadar air, zat dan jumlah mikroba pencemar yang disebut parameter non
spesifik. Proses standardisasi yang meliputi aspek kimiawi metabolit sekunder,
jumlah cemaran mikroba minimal, cemaran logam berat, sisa pelarut, dan
lain-lain sangatlah penting karena terkait dengan efikasi dan keamanan pada konsumen
(Saifudin et al, 2011).
2.2.5 Standardisasi Meningkatkan Nilai Ekonomi
Tanaman obat dan rempah Indonesia mempunyai potensi besar sebagai
produk unggulan. Belum tingginya upaya lintas sektoral dan terpadu antara
swasta-pemerintah-perguruan tinggi untuk mengangkat secara sistematis natural
product Indonesia mengakibatkan banyak produk ekspor herbal berdaya tawar
rendah. Standardisasi adalah upaya penting untuk menaikkan nilai ekonomi
produk alam Indonesia dimana dampak positifnya sebenarnya menguntungkan
semua pihak, yakni konsumen, produsen, dan juga pemerintah
(Saifudin et al, 2011).
2.3 PARAMETER-PARAMETER STANDAR EKSTRAK
Parameter-parameter standar ekstrak terdiri dari parameter spesifik dan
UIN Syarif Hidayatullah Jakarta
2.3.1 Parameter Spesifik
Parameter spesifik berfokus pada senyawa atau golongan senyawa yang
bertanggung jawab terhadap aktivitas farmakologis. Analisis kimia yang
dilibatkan ditujukan untuk analisa kualitatif dan kuantitatif terhadap senyawa
aktif. Berdasarkan Depkes RI (2000), parameter spesifik meliputi :
1. Identitas
Identitas ekstrak meliputi deskripsi tata nama ekstrak, nama lain tumbuhan
(sistematika botani), nama Indonesia tumbuhan, dan bagian tumbuhan yang
digunakan.
2. Organoleptik
Organoleptik ekstrak meliputi penggunaan panca indera dalam
mendeskripsikan bentuk, warna, bau, rasa untuk pengenalan awal yang
sederhana dan seobjektif mungkin.
3. Senyawa terlarut dalam pelarut tertentu
Penentuan jumlah senyawa terlarut dalam pelarut tertentu dilakukan dengan
melarutkan ekstrak dengan pelarut (alkohol/air) untuk ditentukan jumlah
larutan yang identik dengan jumlah senyawa kandungan secara gravimetrik.
Dalam hal tertentu dapat diukur senyawa terlarut dalam pelarut lain misalnya
heksana, diklorometan, metanol. Tujuannya untuk memberikan gambaran awal
jumlah senyawa kandungan.
4. Uji kandungan kimia ekstrak
a) Pola Kromatogram
Pada penentuan pola kromatogram, ekstrak ditimbang dan diekstraksi
dengan pelarut dan cara tertentu, kemudian dilakukan analisis kromatografi
sehingga memberikan pola kromatogram yang khas. Pengujian ini
bertujuan untuk memberikan gambaran awal komposisi kandungan kimia
berdasarkan pola kromatogram (KLT/KCKT).
b) Kadar Total Golongan Kandungan Kimia
Kadar kandungan golongan kimia ditetapkan dengan penerapan metode
spektrofotometri, titrimetri, volumetri, gravimetri, atau lainnya. Metode
yang digunakan harus sudah teruji validitasnya, terutama selektivitas dan
UIN Syarif Hidayatullah Jakarta
memberikan informasi golongan kimia sebagai parameter mutu ekstrak
dalam kaitannya dengan efek farmakologis.
c) Kadar Kandungan Kimia Tertentu
Adanya kandungan kimia yang berupa senyawa identitas atau senyawa
kimia utama ataupun kandungan kimia lainnya, maka secara kromatografi
instrumental dapat dilakukan penetapan kadar kandungan kimia tersebut.
Instrumen yang dapat digunakan adalah densitometer, kromatografi gas,
kromatografi cair kinerja tinggi, atau instrumen lain yang sesuai.
Metode penetapan kadar harus diuji dahulu validitasnya, yaitu batas
deteksi, selektivitas, linearitas, ketelitian, ketepatan, dan lain-lain.
Tujuannya memberikan data kadar kandungan kimia tertentu sebagai
senyawa identitas atau senyawa yang diduga bertanggung jawab pada efek
farmakologis (Depkes RI, 2000).
2.3.2 Parameter Non Spesifik
Parameter non spesifik merupakan aspek yang berfokus pada aspek kimia,
mikrobiologi dan fisis yang akan mempengaruhi keamanan konsumen dan
stabilitasnya. Berdasarkan Depkes RI (2000), parameter non spesifik meliputi :
1. Susut Pengeringan
Parameter susut pengeringan diukur dengan pengukuran sisa zat setelah
pengeringan pada temperatur 105°C selama 30 menit atau sampai berat konstan
yang dinyatakan sebagai nilai persen. Dalam hal khusus (jika bahan tidak
mengandung minyak menguap/atsiri dan sisa pelarut organik menguap) identik
dengan kadar air, yaitu kandungan air karena berada di atmosfer/lingkungan
terbuka. Adapun tujuan menentukan susut pengeringan untuk memberikan
batasan maksimal (rentang) tentang besarnya senyawa yang hilang pada proses
pengeringan.
2. Bobot Jenis
Parameter bobot jenis diukur dengan mengetahui masa per satuan volume
pada suhu kamar tertentu (25°C) yang ditentukan dengan alat khusus
piknometer atau alat lainnya. Adapun tujuan menentukan bobot jenis ekstrak
UIN Syarif Hidayatullah Jakarta
merupakan parameter khusus ekstrak cair sampai ekstrak pekat (kental) yang
masih dapat dituang.
3. Kadar air
Kandungan air yang berada di dalam bahan dapat diukur dengan cara yang
tepat diantaranya dengan titrasi, destilasi atau gravimetrik. Tujuan penentuan
kadar air adalah untuk mengetahui tercapainya batasan minimal atau rentang
kandungan air di dalam bahan.
4. Kadar Abu
Pada penentuan kadar abu, bahan dipanaskan pada temperatur dimana
senyawa organik dan turunannya terdestruksi dan menguap, sehingga tinggal
unsur mineral dan anorganik. Uji ini bertujuan untuk memberikan gambaran
kandungan mineral internal dan eksternal yang berasal dari proses awal sampai
terbentuknya ekstrak.
5. Sisa pelarut
Dalam penentuan sisa pelarut, yang ditentukan adalah kandungan sisa
pelarut tertentu (yang memang ditambahkan). Pada ekstrak cair berarti
kandungan pelarutnya, misalnya kadar alkohol. Tujuan dalam menentukan sisa
pelarut adalah memberikan jaminan bahwa selama proses tidak meninggalkan
sisa pelarut yang memang seharusnya tidak boleh ada, sedangkan untuk ekstrak
cair menunjukkan jumlah pelarut (alkohol) sesuai dengan yang ditetapkan.
6. Cemaran logam berat
Penentuan kandungan logam berat dilakukan dengan metode spektroskopi
serapan atom yang lebih valid dan bertujuan untuk menguji cemaran logam
berat untuk memberikan jaminan bahwa ekstrak tidak mengandung logam berat
tertentu (As, Pb, Cd) melebihi nilai yang ditetapkan karena berbahaya (toksik)
bagi kesehatan.
2.4 SIMPLISIA
Simplisia atau herbal adalah bahan alam yang telah dikeringkan yang
digunakan untuk pengobatan dan belum mengalami pengolahan. Kecuali
dinyatakan lain suhu pengeringan simplisia tidak lebih dari 60o C. Simplisia segar
UIN Syarif Hidayatullah Jakarta
yang berupa tumbuhan utuh, bagian tumbuhan atau eksudat tumbuhan. Eksudat
tumbuhan adalah isi sel yang secara spontan keluar dari tumbuhan atau dengan cara
tertentu dipisahkan dari tumbuhannya. Serbuk simplisia nabati adalah bentuk
serbuk dari simplisia nabati, dengan ukuran derajat kehalusan tertentu. Sesuai
dengan derajat kehalusannya, dapat berupa serbuk sangat kasar, agak kasar, halus
dan sangat halus (Farmakope Herbal, 2009).
Serbuk simplisia nabati tidak boleh mengandung fragmen jaringan dan
benda asing yang bukan merupakan komponen asli dari simplisia yang
bersangkutan antara lain telur nematoda, bagian dari serangga dan hama serta sisa
tanah. Nama latin simplisia ditetapkan dengan menyebut nama marga (genus),
nama jenis (spesies) dan bila memungkinkan petunjuk jenis (varietas) diikuti
dengan bagian yang digunakan. Nama latin dengan pengecualian ditetapkan dengan
menyebut nama marga untuk simplisia yang sudah lazim disebut dengan marganya.
Nama lain adalah nama Indonesia yang paling lazim, didahului dengan bagian
tumbuhan yang digunakan (Farmakope Herbal, 2009).
2.5 EKSTRAK
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat
aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai,
kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang
tersisa diperlakukan sedemikian hingga memenuhi baku yang telah ditetapkan.
(Farmakope Indonesia IV, 1995)
Ekstrak adalah sediaan kering, kental, atau cair dibuat dengan menyari
simplisia nabati atau hewani menurut cara yang cocok, di luar pengaruh cahaya
matahari langsung (Farmakope Indonesia III, 1979)
Ekstrak kering adalah sediaan padat yang memiliki bentuk serbuk yang
didapatkan dari penguapan dari pelarut yang digunakan untuk ekstraksi. Ekstrak
kering dapat ditambahkan bahan tambahan, yaitu bahan pengisi, bahan penstabil
(stabilizers), dan bahan pengawet (preservative). Ekstrak kering yang telah
distandardisasi adalah ekstrak kering yang telah diukur kandungannya, dan
UIN Syarif Hidayatullah Jakarta
untuk pengolahan. Penggunaan pelarut disesuaikan dengan jumlah dan
monografinya (US Pharmacopeia, 2009).
Ekstrak kental didapatkan dari penguapan sebagian dari pelarut, air,
alkohol, atau campuran hidroalkohol yang digunakan sebagai pelarut dalam
ekstraksi. Ekstrak kental dapat ditambahkan antimikroba atau bahan pengawet
lainnya yang sesuai. Ekstrak kental dan ekstrak kering yang berasal dari bahan yang
sama dapat digunakan sebagai obat-obatan atau suplemen, tetapi memiliki
keuntungan dan kerugian masing-masing (US Pharmacopeia, 2009).
2.6 EKSTRAKSI
2.6.1 Pengertian Ekstraksi
Ekstraksi adalah penyarian zat-zat berkhasiat atau zat-zat aktif dari bagian
tanaman obat, hewan dan beberapa jenis ikan termasuk biota laut. Zat-zat aktif
terdapat di dalam sel, namun sel tanaman dan hewan berbeda demikian pula
ketebalannya, sehingga diperlukan metode ekstraksi dengan pelarut tertentu
dalam mengekstraksinya.
Tujuan ekstraksi adalah untuk menarik semua komponen kimia yang
terdapat dalam simplisia. Ekstraksi ini didasarkan pada perpindahan massa
komponen zat padat ke dalam pelarut dimana perpindahan mulai terjadi pada
lapisan antar muka, kemudian berdifusi masuk ke dalam pelarut
(Dirjen POM, 1986).
2.6.2 Metode Ekstraksi
Menurut Departemen Kesehatan RI (2000), terdapat beberapa metode
ekstraksi dengan menggunakan pelarut yaitu:
1. Cara dingin
a) Maserasi
Maserasi adalah proses pengekstrakan simplisia dengan menggunakan
pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur
ruangan (kamar). Secara teknologi termasuk ekstraksi dengan prinsip
metode pencapaian konsentrasi pada keseimbangan. Maserasi kinetik
UIN Syarif Hidayatullah Jakarta
berarti dilakukan pengulangan penambahan pelarut setelah dilakukan
penyaringan maserat pertama, dan seterusnya.
b) Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai
sempurna (exhaustive extraction) yang umumnya dilakukan pada
temperatur ruangan. Proses ini terdiri dari tahapan pengembangan bahan,
tahap maserasi antara, tahap perkolasi sebenarnya
(penetesan/penampungan ekstrak), terus menerus sampai diperoleh ekstrak
(perkolat) yang jumlahnya 1-5 kali bahan.
2. Cara Panas
a) Refluks
Refluks merupakan ekstraksi dengan pelarut pada temperatur titik
didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif
konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan
proses pada residu pertama sampai 3-5 kali sehingga dapat termasuk proses
ekstraksi sempurna.
b) Sokletasi
Sokletasi ialah ekstraksi dengan menggunakan pelarut yang selalu baru
yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi
kontinyu dengan jumlah pelarut relatif konstan dengan adanya pendinginan
balik.
c) Digesti
Digesti merupakan maserasi kinetik (dengan pengadukan kontinyu)
pada temperatur yang lebih tinggi dari temperatur ruangan (kamar), yaitu
secara umum dilakukan pada temperatur 40-50oC.
d) Infusa
Infusa adalah ekstraksi dengan pelarut air pada temperature penangas
air mendidih, temperatur terukur 96oC-98oC selama waktu tertentu
(15-20 menit).
e) Dekok
Dekok adalah infus yang waktunya lebih lama (lebih dari 30 menit) dan
UIN Syarif Hidayatullah Jakarta
2.7 FAKTOR YANG MEMPENGARUHI MUTU EKSTRAK
2.7.1 Faktor Biologi
Mutu ekstrak dipengaruhi oleh bahan asal yaitu tumbuhan obatnya, dan
dipandang dari beberapa faktor biologi, baik untuk tumbuhan liar maupun
tumbuhan obat hasil budidaya yang meliputi :
1. Identitas Jenis
Jenis tumbuhan dari sudut keragaman hayati dapat dikonfirmasi sampai
informasi genetik sebagai faktor internal untuk validasi jenis (spesies)
2. Lokasi Tumbuhan Asal
Lokasi berarti faktor eksternal, yaitu lingkungan (tanah dan atmosfer)
dimana tumbuhan berinteraksi berupa energi (cuaca, temperatur, cahaya) dan
materi (air, senyawa organik dan anorganik)
3. Periode Pemanenan Hasil Tumbuhan
Faktor ini merupakan dimensi waktu dari proses kehidupan tumbuhan
terutama metabolisme sehingga menentukan senyawa yang dikandung. Ada
waktu dimana senyawa kandungan mencapaii kadar optimal dari proses
biosintesis dan sebaliknya ada waktu dimana senyawa tersebut dikonversi
ataupun dibiotransformasi menjadi senyawa lain.
4. Penyimpanan Bahan Tumbuhan
Merupakan faktor eksternal yang dapat diatur karena dapat berpengaruh
pada stabilitas bahan serta adanya kontaminasi (biotik dan abiotik)
5. Umur Tumbuhan dan Bagian yang Digunakan (Depkes RI, 2000)
2.7.2 Faktor Kimia
Mutu ekstrak dipengaruhi oleh bahan asal yaitu tumbuhan obatnya,
khususnya dipandang dari segi kandungan kimianya. Faktor kimia, baik untuk
bahan dari tumbuhan liar maupun tumbuhan hasil budidaya, meliputi beberapa
hal, yaitu :
1. Faktor Internal
Meliputi jenis, komposisi kualitatis, komposisi kuantitatif, dan kadar total
UIN Syarif Hidayatullah Jakarta
2. Faktor Eksternal
Meliputi metode ekstraksi, perbandingan ukuran alat ekstraksi, ukuran,
kekerasan, serta kekeringan bahan, pelarut yang digunakan, kandungan logam
berat, dan kandungan pestisida (Depkes RI, 2000).
2.8 KROMATOGRAFI LAPIS TIPIS
2.8.1 Deskripsi
Kromatografi lapis tipis (KLT) dikembangkan oleh Izmailoff dan
Schraiber pada tahun 1938. KLT merupakan bentuk kromatografi planar, selain
kromatografi kertas dan elektroforesis. Berbeda dengan kromatografi kolom yang
mana fase diamnya diisikan atau dikemas di dalamnya, pada kromatografi lapis
tipis, fase diamnya berupa lapisan yang seragam (uniform) pada permukaan
bidang datar yang didukung oleh lempeng kaca, pelat aluminium atau pelat
plastik. Meskipun demikian, kromatografi planar ini dapat dikatakan sebagai
bentuk terbuka dari kromatografi kolom (Gandjar dan Rohman, 2007).
KLT dapat dipakai dengan dua tujuan. Pertama, dipakai selayaknya
sebagai metode untuk mencapai hasil kualitatif, kuantitatif, atau preparatif.
Kedua, dipakai untuk menjajaki sistem pelarut dan sistem penyangga yang akan
dipakai dalam kromatografi kolom atau kromatografi cair kinerja tinggi
(Roy, James, dan Arthur, 1991).
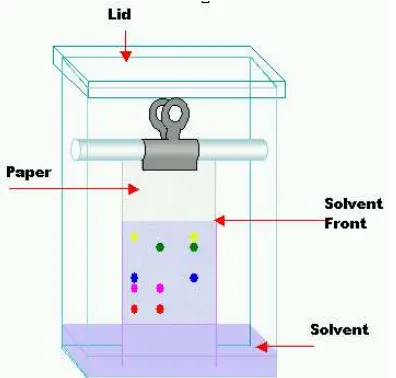
Gambar 4 : Skema Kromatografi Lapis Tipis
UIN Syarif Hidayatullah Jakarta
Fase gerak yang dikenal sebagai pelarut pengembang akan bergerak
sepanjang fase diam karena pengaruh kapiler pada pengembangan secara menaik
(ascending) atau karena pengaruh gravitasi pada pengembangan secara menurun
(descending). Kromatografi lapis tipis dalam pelaksanaannya lebih mudah dan
lebih murah dibandingkan dengan kromatografi kolom. Demikian juga peralatan
yang digunakan. Dalam kromatografi lapis tipis, peralatan yang digunakan lebih
sederhana dan dapat dikatakan hampir semua laboratorium dapat melaksanakan
setiap saat secara cepat (Gandjar dan Rohman, 2007).
2.8.2 Fase Diam
Fase diam yang digunakan dalam KLT merupakan penjerap berukuran
kecil dengan diameter partikel antara 10-30 m. Semakin kecil ukuran rata-rata
partikel fase diam dan semakin sempit kisaran ukuran fase diam, makasemakin
baik kinerja KLT dalam hal efisiensi dan resolusinya.Penjerap yang paling sering
digunakan adalah silica dan serbuk selulosa, sementara mekanisme penyerapan
yang utama pada KLT adalah adsorpsi danpartisi (Gandjar dan Rohman, 2007).
2.8.3 Fase Gerak
Fase gerak pada KLT dapat dipilih berdasarkan pustaka, tetapi lebih sering
dengan mencoba-coba. Sistem yang paling sederhana ialah campuran 2 pelarut
organik karena daya elusi campuran kedua pelarut ini dapat mudah diatur
sedemikian rupa sehingga pemisahan dapat terjadi secara optimal. Berikut adalah
beberapa petunjuk dalam memilih dan mengoptimasi fase gerak :
1. Fase gerak harus mempunyai kemurnian yang sangat tinggi karena KLT
merupakan teknik yang sensitif.
2. Daya elusi fase gerak harus diatur sedemikian rupa sehingga harga Rf
terletak antara 0,2-0,8 untuk memaksimalkan pemisahan.
3. Untuk pemisahan dengan menggunakan fase diam polar seperti silika gel,
polaritas fase gerak akan menentukan kecepatan migrasi senyawa yang
berarti juga menentukan nilai Rf. Penambahan pelarut yang bersifat sedikit
UIN Syarif Hidayatullah Jakarta
akan meningkatkan harga Rf secara signifikan (Gandjar dan Rohman,
2007).
2.8.4 Deteksi Bercak
Deteksi bercak pada KLT dapat dilakukan secara kimia dan fisika. Cara
kimia yang biasa digunakan adalah dengan mereaksikan bercak dengan suatu
pereaksi melalui cara penyemprotan sehingga bercak menjadi jelas. Cara fisika
yang dapat digunakan untuk menampakkan bercak adalah dengan dengan cara
pencacahan radioaktif dan fluorosensi sinar ultraviolet. Fluorosensi sinar
ultraviolet terutama untuk senyawa yang dapat berfluorosensi, membuat bercak
akan terlihat jelas. Berikut adalah cara-cara kimiawi untuk mendeteksi bercak :
1. Menyemprot lempeng KLT dengan reagen kromogenik yang akan bereaksi
secara kimia dengan senyawa yang mengandung gugus fungsional tertentu
sehingga bercak menjadi berwarna. Kadang-kadang dipanaskan terlebih
dahulu untuk mempercepat reaksi pembentukan warna dan intensitas warna
bercak.
2. Mengamati lempeng dibawah lampu ultraviolet yang dipasang panjang
gelombang emisi 254 nm atau 366 nm untuk menampakkan fraksi sebagai
bercak yang gelap atau bercak yang berfluorosensi terang pada dasar yang
berfluorosensi seragam. Lempeng yang diperdagangkan dapat dibeli dalam
bentuk lempeng yang sudah diberi dengan senyawa fluorosensi yang tidak
larut yang dimasukkan ke dalam fase diam untuk memberikan dasar
fluorosensi atau dapat pula dengan menyemprot lempeng dengan reagen
fluorosensi setelah dilakukan pengembangan.
3. Menyemprot lempeng dengan asam sulfat pekat atau asam nitrat pekat lalu
dipanaskan untuk mengoksidasi solut-solut organik yang akan nampak
sebagai bercak hitam sampai kecoklat-coklatan.
4. Memaparkan lempeng dengan uap iodium dalam chamber tertutup.
5. Melakukan scanning pada permukaan lempeng dengan densitometer, suatu
instrumen yang dapat mengukur intensitas radiasi yang direfleksikan dari
UIN Syarif Hidayatullah Jakarta
tampak. Solut-solut yang mampu menyerap sinar akan dicatat sebagai
puncak (peak) dalam pencatatan (recorder) (Gandjar dan Rohman, 2007).
2.8.5 Perhitungan Nilai Rf
Retardation Factor (Rf) adalah parameter karakteristik kromatografi
kertas dan kromatografi lapis tipis. Harga Rf merupakan ukuran kecepatan migrasi
suatu komponen pada kromatografi dan pada kondisi tetap marupakan besaran
karakteristik dan reproduksibel. Nilai Rf bersifat karakteristik dan menunjukkan
identitas masing-masing komponen. Komponen yang paling mudah larut dalam
pelarut harganya akan mendekati satu, sedangkan komponen yang kelarutannya
rendah akan mempunyai Rf hampir nol. Perhitungan nilai Rf didasarkan pada
rumus :
Nilai Rf dinyatakan hingga angka 1,0 beberapa pustaka menyatakan nilai Rf yang
baik yang menunjukkan pemisahan yang cukup baik adalah berkisar antara
0,2-0,8 (Gandjar dan Rohman, 2007).
2.9 SPEKTROFOTOMETRI
2.9.1 Spektrofotometri UV-Vis
Spektrofotometri UV-Vis merupakan salah satu teknik analisis
spektroskopi yang memakai sumber radiasi elektromagnetik ultraviolet dekat
(190-380 nm) dan sinar tampak (380-780 nm) dengan memakai instrumen
spektrofotometer. Spektrofotometri UV-Vis melibatkan energi elektronik yang
cukup besar pada molekul yang dianalisis, sehingga spektrofotometri UV-Vis
lebih banyak dipakai untuk analisis kuantitatif ketimbang kualitatif
(Mulja dan Suharman, 1995).
Spektrofotometer terdiri atas spektrometer dan fotometer.
Spektrofotometer menghasilkan sinar dari spektrum dengan panjang gelombang
tertentu dan fotometer adalah alat pengukur intensitas cahaya yang ditranmisikan
atau yang diabsorpsi. Spektrofotometer tersusun atas sumber spektrum yang Jarak yang ditempuh oleh komponen
UIN Syarif Hidayatullah Jakarta
kontinyu, monokromator, sel pengabsorpsi untuk larutan sampel atau blangko dan
suatu alat untuk mengukur pebedaan absorpsi antara sampel dan blangko ataupun
pembanding (Khopkar, 1990).
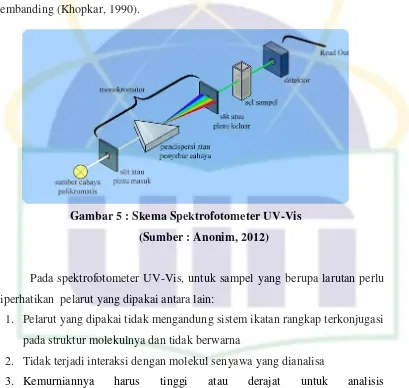
Gambar 5 : Skema Spektrofotometer UV-Vis (Sumber : Anonim, 2012)
Pada spektrofotometer UV-Vis, untuk sampel yang berupa larutan perlu
diperhatikan pelarut yang dipakai antara lain:
1. Pelarut yang dipakai tidak mengandung sistem ikatan rangkap terkonjugasi
pada struktur molekulnya dan tidak berwarna
2. Tidak terjadi interaksi dengan molekul senyawa yang dianalisa
3. Kemurniannya harus tinggi atau derajat untuk analisis
(Mulja dan Suharman, 1995).
Komponen-komponen pokok dari spektrofotometer meliputi :
1. Sumber tenaga radiasi yang stabil, sumber yang biasa digunakan adalah
lampu wolfram.
2. Monokromator untuk memperoleh sumber sinar yang monokromatis.
3. Sel absorpsi, pada pengukuran di daerah visibel menggunakan kuvet kaca
atau kuvet kaca corex, tetapi untuk pengukuran pada UV menggunakan sel
kuarsa karena gelas tidak tembus cahaya pada daerah ini.
4. Detektor radiasi yang dihubungkan dengan sistem meter atau pencatat.
Peranan detektor penerima adalah memberikan respon terhadap cahaya pada
UIN Syarif Hidayatullah Jakarta
Serapan cahaya oleh molekul dalam daerah spektrum ultraviolet dan
visibel tergantung pada struktur elektronik dari molekul. Serapan ultraviolet dan
visibel dari senyawa-senyawa organik berkaitan erat transisi-transisi diantara
tingkatan-tingkatan tenaga elektronik. Disebabkan karena hal ini, maka serapan
radiasi ultraviolet atau terlihat sering dikenal sebagai spektroskopi elektronik.
Transisi-transisi tersebut biasanya antara orbital ikatan atau orbital pasangan
bebas dan orbital non ikatan tak jenuh atau orbital anti ikatan. Panjang gelombang
serapan merupakan ukuran dari pemisahan tingkatan-tingkatan tenaga dari orbital
yang bersangkutan. Spektrum ultraviolet adalah gambar antara panjang
gelombang atau frekuensi serapan lawan intensitas serapan (transmitasi atau
absorbansi). Sering juga data ditunjukkan sebagai gambar grafik atau tabel yang
menyatakan panjang gelombang lawan serapan molar atau log dari serapan molar,
Emax atau log Emax (Sastrohamidjojo, 2001).
Sumber tenaga radiasi terdiri dari benda yang tereksitasi menuju ke tingkat
yang lebih tinggi oleh sumber listrik bertegangan tinggi atau oleh pemanasan
listrik. Monokromator adalah suatu piranti optis untuk memencilkan radiasi dari
sumber berkesinambungan. Digunakan untuk memperoleh sumber sinar
monokromatis. Alat dapat berupa prisma atau grating (Khopkar, 1990).
Pengukuran pada daerah UV harus menggunakan sel kuarsa karena gelas
tidak tembus cahaya pada daerah ini. Sel yang biasa digunakan berbentuk persegi
maupun berbentuk silinder dengan ketebalan 10 mm. Sel tersebut adalah sel
pengabsorpsi, merupakan sel untuk meletakkan cairan ke dalam berkas cahaya
spektrofotometer. Sel haruslah meneruskan energi cahaya dalam daerah spektral
yang diminati. Sebelum sel dipakai dibersihkan dengan air atau dapat dicuci
dengan larutan detergen atau asam nitrat panas apabila dikehendaki
(Sastrohamidjojo, 2001).
2.9.2 Spektrofotometri Serapan Atom
Spektrometri merupakan suatu metode analisis kuantitatif yang
pengukurannya berdasarkan banyaknya radiasi yang dihasilkan atau yang diserap
oleh spesi atom atau molekul analit. Salah satu bagian dari spektrometri ialah
UIN Syarif Hidayatullah Jakarta
kuantitatif yang pengukurannya berdasarkan penyerapan cahaya dengan panjang
gelombang tertentu oleh atom logam dalam keadaan bebas (Skoog et al, 2000).
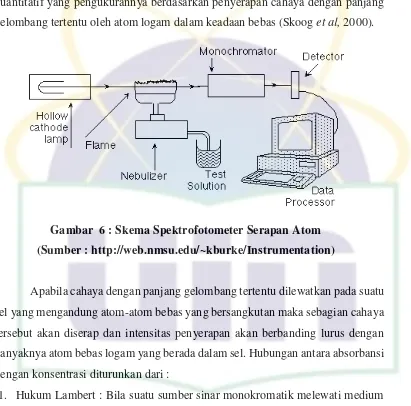
Gambar 6 : Skema Spektrofotometer Serapan Atom (Sumber : http://web.nmsu.edu/~kburke/Instrumentation)
Apabila cahaya dengan panjang gelombang tertentu dilewatkan pada suatu
sel yang mengandung atom-atom bebas yang bersangkutan maka sebagian cahaya
tersebut akan diserap dan intensitas penyerapan akan berbanding lurus dengan
banyaknya atom bebas logam yang berada dalam sel. Hubungan antara absorbansi
dengan konsentrasi diturunkan dari :
1. Hukum Lambert : Bila suatu sumber sinar monokromatik melewati medium
transparan, maka intensitas sinar yang diteruskan berkurang dengan
bertambahnya ketebalan medium yang mengabsorpsi.
2. Hukum Beer : Intensitas sinar yang diteruskan berkurang secara eksponensial
dengan bertambahnya konsentrasi spesi yang menyerap sinar tersebut.
Dari kedua hukum tersebut diperoleh suatu persamaan :
Keterangan : Io = Intensitas sumber sinar
It = Intensitas sinar yang diteruskan
ε = Absortivitas molar It = Io.e-(εbc)
UIN Syarif Hidayatullah Jakarta
b = Panjang medium
c = Konsentrasi atom-atom yang menyerap sinar
A = Absorbansi
Dari persamaan di atas, dapat disimpulkan bahwa absorbansi cahaya berbanding
lurus dengan konsentrasi atom (Day dan Underwood, 1989).
Instrumen pada spektrofotometer serapan atom terdiri dari :
1. Sumber Sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow
cathode lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Bila antara anoda dan katoda diberi suatu selisih
tegangan yang tinggi (600 volt), maka katoda akan memancarkan
berkas-berkas elektron yang bergerak menuju anoda yang memiliki kecepatan dan
energi yang tinggi lalu akan bertabrakan dengan gas-gas yang diisikan
sehingga gas menjadi ion bermuatan positif. Ion positif akan bertabrakan
dengan katoda dan menghasilkan pancaran spektrum yang disesuaikan
dengan unsur yang akan dianalisis.
2. Tempat sampel
Dalam analisis dengan spektrofotometer serapan atom, sampel yang
dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam
keadaan asas. Ada berbagai macam alat yang dapat digunakan untuk
mengubah sampel menjadi uap atom-atom yaitu dengan nyala (flame) atau
tanpa nyala (flameless).
3. Monokromator
Pada spektrofotometer serapan atom, monokromator dimaksudkan untuk
memisahkan dan memilih panjang gelombang yang digunakan dalam
analisis. Disamping sistem optik, dalam monokromator juga terdapat suatu
alat yang digunakan untuk memisahkan radiasi resonansi yang disebut
chopper.
4. Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat
atomisasi. Biasanya digunakan tabung penggandaan foton (photomultiplier
UIN Syarif Hidayatullah Jakarta
radiasi resonansi dan radiasi kontinyu atau hanya memberikan respon
terhadap radiasi resonansi.
5. Readout
Readout merupakan suatu alat petunjuk atau sistem pencatatan hasil yang
dilakukan dengan suatu alat yang telah terkalibrasi untuk pembacaan sutu
transmisi atau absorbsi. Hasil pembacaan dapat berupa angka atau berupa
kurva dari suatu recorder yang menggambarkan absorbansi atau intensitas
emisi (Gandjar dan Rohman, 2007).
2.10 KROMATOGRAFI CAIR KINERJA TINGGI
Kromatografi cair kinerja tinggi atau KCKT atau biasa juga disebut
dengan HPLC (High Performance Liquid Chromatography) dikembangkan pada
akhir tahun 1960-an dan awal tahun 1970-an. Saat ini KCKT merupakan teknik
pemisahan yang diterima secara luas untuk analisis dan pemurnian senyawa tertentu
dalam suatu sampel. Kromatografi merupakan teknik yang mana zat terlarut
terpisah oleh perbedaan kecepatan elusi. Pemisahan zat-zat terlarut diatur oleh
distribusi solut dalam fase gerak dan fase diam. Penggunaan KCKT membutuhkan
penggabungan secara tepat dari berbagai kondisi operasional seperti jenis kolom,
fase gerak, panjang dan diameter kolom, kecepatan alir fase gerak, suhu kolom, dan
ukuran sampel (Indira, 2010).
UIN Syarif Hidayatullah Jakarta
Beberapa komponen pada Kromatografi Cair Kinerja Tinggi diantaranya adalah :
1. Wadah Fase Gerak
Wadah fase gerak terbuat dari bahan yang inert terhadap fase gerak. Bahan
yang umum digunakan adalah gelas dan baja anti karat. Daya tampung wadah
harus lebih besar dari 500 mL, yang dapat digunakan selama 4 jam untuk
kecepatan alir yang umumnya 1-2 mL/menit (Pasri, 2010).
2. Pompa
Untuk mengerakkan fase gerak melalui kolom diperlukan pompa. Pompa harus
mampu menghasilkan tekanan 6000 psi pada kecepatan alir 0,1–10 mL/menit.
Pompa ada 2 jenis yaitu pompa volume konstan dan pompa tekanan konstan.
Pompa terbuat dari bahan yang inert terhadap semua pelarut. Bahan yang
umum digunakan adalah gelas baja antikarat dan teflon. Aliran pelarut dari
pompa harus tanpa denyut untuk menghindari hasil yang menyimpang pada
detektor (Pasri, 2010).
3. Injektor
Ada beberapa tipe injektor dalam KCKT, diantaranya adalah Stop-Flow,
Septum, dan Loop Valve. Teknik yang umum digunakan adalah Stop-Flow,
yaitu aliran dihentikan, injeksi dilakukan pada kinerja atmosfir, sistem tertutup,
dan aliran dilanjutkan lagi. Teknik ini bisa digunakan karena difusi di dalam
cairan kecil dan resolusi tidak dipengaruhi (Putra, 2004).
4. Kolom
Kolom adalah jantung kromatografi. Berhasil atau gagalnya suatu analisis
tergantung pada pemilihan kolom dan kondisi percobaan yang sesuai. Kolom
dapat dibagi menjadi dua kelompok :
a. Kolom analitik
Diameter dalam 2 -6 mm. Panjang kolom tergantung pada jenis material
pengisi kolom. Untuk kemasan pellicular, panjang yang digunakan adalah
50 -100 cm. Untuk kemasan poros mikropartikulat, 10 -30 cm.
b. Kolom preparatif
umumnya memiliki diameter 6 mm atau lebih besar dan panjang kolom