Lampiran 1. Hasil Ekstraksi Galaktomanan Kolang-kaling
% Galaktomanan = 5,7867 ���� ������������
100,44 ���� ������ −������x 100% = 5,7613 %
Lampiran 3. Hasil Spektrum FTIR Galaktomanan
Lampiran 7. Hasil Penentuan Kadar Vitamin E Yang Ditambahkan Pada Matriks GIF Dengan Alat Spektrofotometer Uv-Vis
Sampel Standar yang
dtambahkan Absorbansi (y) Slope c
Konsentrasi
Lampiran 8. Hasil Penentuan Kadar Vitamin E Yang Terlepas Dengan UV-Vis Sample Absorbansi
(A)
Diagram Konsentrasi Vit.E Hasil Cucian GIFVE
Lampiran 9. Perhitungan % Efisiensi Vit.E Yang Terikat Pada Matriks GIF % Efisiensi Vitamin E yang terperangkap pada matriks:
% Efisiensi Vit.E yang terperangkap pada matriks =
konsentrasi vit. E yang ditambahkan−konsentrasi vit. E yang tidak terperangkap
konsentrasi vit. E yang ditambahkan �100%
Lampiran 10. Hasil Penentuan Kadar Vitamin E 50% Dan Vitamin E 70% Dengan HPLC
NO Sample PARAMETER
α-Tokoperol α-Tokotrienol β-Tokotrienol γ-Tokotrienol δ-Tokotrienol
1 Vitamin E 50% 12.91 15.53 1.83 17.77 7.05
2 Vitamin E 70% 20.97 15.83 2.43 22.31 8.48
-1:2 GIF Vit E 70% 0.05gram
-1:2 GIF Vit E 50% 0.05 gram
- 1:250% 0,1gram
- 1:2 GIF 50% 0,15gram
-- 1:2 GIF 70% 0,1gram
- 1:3 70% 0,1gram
DAFTAR PUSTAKA
Anonim. 2009,Aren Sumber Alternatif. Warta Penelitian dan Pengembangan Pertanian, 31,2.
Banegas, R., Zornio, C.F., Borges A.M., Porto, L. C., and Soldi, V. 2013.Preparation, Characteristization and Properties of Films Obtained from Cross-linked Guar Gum.
Cerqueira, M. A., Lima, A. M., Teixeira, J. A., Moreira, R. A., & Vicente, A. A., 2009a, Suitability of novel galactomannans as edible coatings for
tropical fruits, Journal of Food Engineering, 94, 372-378.
Christie W.W.2011, Structure, Composition, Biology and Analysis Tocopherols
and Tokotrienols.James Hutton Research Institut. Scotland
Chudzikowski, R.J., 1971. Guar Gumand Its Applications. Society of Cosmetic Chemists of great Britain, 22 : 43-60
Evans, J.C.D.R., Kodali, and Addis, P.B., 2002, Optimal Tocoperol
Concentration to Inhibitor Soybean Oil Oxidation, JAOCS 79: 47-51.
Gliko-Kabir, B. Yagen, A. Penhasi,.and A. Rubinstein., 1998,Phar, Res. 15 : 1019-1025.
Gliko-Kabir, B. Yagen, A. Penhasi,.and A. Rubinstein, A., 2000,Phosphate Crosslinked Guar for Colon-Spesific Drug Delivery. I. Preparation and Physicochemical Characterization.
Gowda, D.W., Khan, M.S., and Vineela S. 2012,Development and Evaluation Crosss-Linked Guar Gum Microspheres for Improved Delivery of Anticancer to Colon,Taylor & Francis Group, LLC, 51 : 1395-1404. Kesavan, S., and Robert, K. Prud’homme., 1992, Rheology of Guar and HPG
Cross-Linked by Borate, J. Amer. Soc. Macromolecule, 25 (7) : 2026-2032.
Koiman, P., 1971, Structures of The Galactomannan Seeds of Annona muricata,
Mathur, N.K., 2012, Industrial Galactomannan Polysaccharide, CRC Press, Boca Raton,Florida.
Mogea. J., Seibert, B., and Smits, W., 1991, Multipurpose Palms: The Sugar Palm
(ArengaPinnata (Wurmb) Merr), Argoforestry Systems, 13: 111 – 129.
Mohini, C., Manish, K.C., Nitin, K.J., Aviral, J., Vandana, S., Yashwant, G., and Sanjay, K.J.,2006,Cross Linked Guar-Gm Microsphere : Aviable
Approach for Improved Delivery of Anticancer Drugs for The Treatment of Colorectal Cancer, AAPS Phar, Sci, Tech, 7 (3), 1-8.
Morris, E.R., Rees, D.A., Young, G., Walkinshaw, M.D. and Darke, A., 1997, A
Role for Polysaccharide Conformation in Recognition Between Xanthomonas Pathogen and its Plant Host, J. Mol. Biol., 110: 1 – 16.
Nasaretman, K., Amba, R., Sellvaduray, K.R., Radhakhrishnan, R., Reiman, K., Razak, G. And Virgall, F., 2004, Tocotrienol Rich Fraction from Palm
Oil Affects Gene Expression in TumorResulting From MCF-7 Cell Inoculation in AthymicMice, Lipid 39:459-467.
Nisa, C.T., 1996, Masalah Dorminasi pada Biji Aren ( Arenga pinnata merr )
serta Pemecahannya untuk Meningkatkan Perkecambahan, Pidato
Pengukuhan Guru Besar USU. Medan.
Orwa, C., Mutua, A., Kindt R., Jamnadass R. and Anthony, S., 2009,
Agroforestree Database tree reference and selection guide version 4.0,
Rimm, E.B., Stampfer, M.J., Ascherio, A., Giovannucci, E., Colditz, G. And Willet,
W.C.,1993, Vitamin E Consumption and the risk of coronary disease in man, N.Eng 1 J, Med.328,1450-1456.
Srivastava, M., and Kapoor, V.P., 2005, Seed Galactomannans An Overview.
Chemistry & Biodiversity, 2: 295 – 317.
Song, B.Y., and Lee, H.G., 2009,Α Tocopherol- Loaded Ca-Pectinate Microcapsules : Optimization, in vitro release, and bioavailability.
Tarigan, J.,Barus, T., Marpongahtun, 2012. Asian International Conference on Materials,Minerals, and Polymer.
BAB 3
METODE PENELITIAN
3.1. Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah :
- Gelas Erlenmeyer 250 ml Pyrex
- Neraca Analitis Shimadzu
- Blender National Super
- Magnetik Bar
- Alat Sentrifugator Hitachi
- Batang Pengaduk
- Hotplate Stirer Ika
- Plat Kaca 13cmsx7cmx3cm
- Spektrofotometer FT-IR Perkin Elmer
- Scanning Electron Microscope Hitachi
- Oven Blower Memmert
- Indikator Universal - Desikator
- Corong Pisah Pyrex
- Labu Takar Pyrex
- Neraca Kaki Tiga Ohauss
- Lemari Pendingin - Tabung Sentrifugator
-Spektrofotometer UV-Visible Perkin Elmer
3.2. Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah :
- Kolang-kaling
- Trinatrium Trimetafosfat Aldrich
- NaOH p.a E’ Merck
- Kalium Dihidrogen Fosfat Merck
3.3. Prosedur Penelitian
3.3.1. Ekstraksi Galaktomanan dari Kolang-Kaling
Sebanyak 100,44 gram kolang-kaling dibersihkan dan di rajang. Kemudian kolang-kaling dihaluskan dengan blender selama ± 3-5 menit dengan penambahan air suling sebanyak 1000 ml, dan disimpan dalam lemari pendingin selama 24 jam.Kemudian disentrifugasi pada kecepatan rata-rata 8500 rpm selama 50 menit.Supernatan ditambahkan etanol 96% dengan perbandingan volume 1:2, kemudian disimpan dalam lemari pendingin selama 24 jam. Endapan yang terbentuk disaring kemudian direndam dengan etanol p.a. Endapan disaring dan dikeringkan didalam desikator.
3.3.2. Pembuatan Galaktomanan Ikat Silang Fosfat
3.3.2.1. Pembuatan Larutan Trinatrium Trimetafosfat
3.3.3.2. Pembuatan Galaktomanan Ikat Silang Fosfat
Sebanyak 80 ml air suling dimasukkan kedalam gelaserlenmeyer. Kemudian ditambahkan 1 gram galaktomanan secara perlahan hingga larut, kemudian ditambahkan NaOH 2M secara perlahan-lahan hingga pH 12. Ditambahkan larutan 2 gram trinatrium trimetafosfat secara perlahan-lahan.Kemudian diaduk selama 2 jam. Dengan prosedur yang sama dilakukan untuk variasi perbandingan galaktomanan : TMP = 1:3.
Untuk analisis FT-IR dan SEM maka matriks terlebih dahulu dicuci dengan air suling hingga pH = 7 (netral) dan selanjutnya dikeringkan.
3.3.3. Inkorporasi Vitamin E 50% dan 70% pada Matriks GIFVE dengan
Perbandingan 1:2 dan 1:3
Sebanyak 0,05 gram vitamin E 50%dimasukkan kedalam beaker glass, kemudian ditambahkan 20 ml etanol p.a, dan 0,5 gram twin 20 sambil di aduk selama 30 menit dalam ruang gelap. Secara perlahan dituangkan kedalam larutan matriks ikat silang fosfat perbandingan 1:2 dan diaduk selama 2 jam.
Dituang kedalam plat kaca yang berukuran panjang 13cm, lebar 7 cm, tinggi 3 cm. Dikeringkan didalam oven blower pada suhu 37oC selama 24jam. Kemudian film dicuci dengan air suling hingga pH 7,dikeringkankembalididalamoven blower pada suhu 37oC selama 5 jam, setelah film kering dilepaskan dari plat secara perlahan-lahan kemudian dimasukkan kedalam wadah tertutup hingga digunakan selanjutnya. Dengan prosedur yang sama dilakukan untuk vitamin E 50% dengan variasi berat 0,1 dan 0,15 gram dan vitamin E 70% pada variasi berat 0,05; 0,1 dan 0,15 gram serta perbandingan galaktomanan : TMP = 1:3. Matriks galaktomanan ikat silang fosfat dengan vitamin E yang terbentuk dianalisis dengan spektrofotometer FT-IR dan SEM (Scanning Electron Microscopic).
3.3.4 Ekstraksi Vitamin E yang tidak terperangkappada matriks
galaktomanan ikat silang fosfat
3.4 Bagan Penelitian
3.4.2. Pembuatan Galaktomanan Ikat Silang Fosfat
3.4.2.1. Pembuatan Larutan Trinatrium Trimetafosfat
Dilakukan prosedur yang sama untuk variasi berat trinatrium trimetafosfat pada perbandingan galaktomanan : TMP =1:2 dan 1:3 dan vitamin 50% dan 70%.
3.4.2.2. Pembuatan Galaktomanan Ikat Silang Fosfat
3.4.3. Pembuatan Matriks Galaktomanan Ikat Silang Fosfat sebagai Pembawa Vitamin E
Dilakukan perlakuan yang sama untuk variasi galaktomanan : TMP 1:2 untuk 0,1 gram; 0,15 gram dan 1:3 pada Vitamin E untuk 0,05 gram; 0,1 gram dan 0,15 gram.
3.4.4. Ekstraksi Vitamin E yang tidak Terperangkap pada Matriks Galaktomanan Ikat Silang Fosfat
Dilakukan prosedur yang sama untuk variasi galaktomanan : TMF 1:2 untuk 0,1 gram; 0,15 gram dan 1:3 pada vitamin E untuk 0,05 gram; 0,1 gram dan 0,15 gram.
Larutan Cucian Film
(GIF 1:2 0,05 gram Vitamin E 50%)
Dimasukkan kedalam corong pisah Ditambahkan 50 ml n-heksan Terbentuk 2 lapisan, dipisahkan
Lapisan n-heksan Lapisan air
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Hasil Ekstraksi Galaktomanan Dari Kolang-Kaling
Hasil ekstraksi 100,44 gram kolang kaling dengan menggunakan air suling sebagai pelarut diperoleh serbuk putih sebanyak 5,7867 gram, persentase galaktomanan diperoleh sebesar 5,7613%.
4.1.2. Hasil Analisis FT-IR
4.1.2.1. Hasil Analisis Gugus Fungsi Galaktomanan Kolang Kaling
dengan Spektrofotometer FT-IR
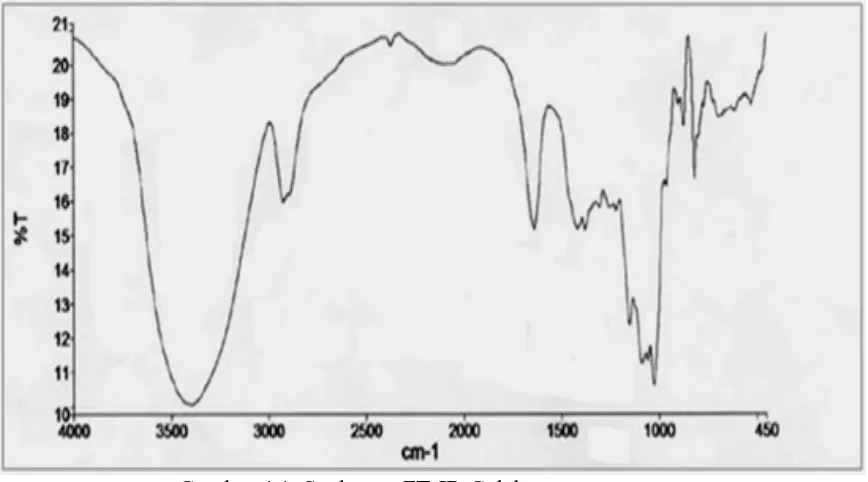
Data spektroskopi FT-IR memberikan puncak-puncak vibrasi pada bilangan gelombang 3348 cm-1; 2915 cm-1; 1437 cm-1; 1319 cm-1; 1030 cm-1. Hasil spektrum FT-IR galaktomanan kolang kaling dapat dilihat pada gambar 4.1.
Gambar 4.1. Spektrum FT-IR Galaktomanan
Hasil analisis gugus fungsi galaktomanan kolang kaling ditunjukkan pada tabel 4.1.
Tabel 4.1. Hasil Analisis Gugus Fungsi Galaktomanan dengan
Parameter Bilangan Gelombang (cm-1)
Vibrasi streaching O-H 3348
VibrasistreachingC-H sp3 2915
Vibrasibending C-H sp3 1437, 1319
VibrasistreachingC-O 1030
4.1.2.2.1. Hasil Analisis Gugus Fungsi GIF dengan Spektrofotometer FT-IR
Data spektroskopi FT-IR memberikan puncak-puncak vibrasi pada bilangan gelombang 3407 cm-1; 2895 cm-1; 1270 cm-1; 1030 cm-1;875 cm-1. Hasil spektrum FT-IR galaktomanan ikat silang fosfat dapat dilihat pada gambar 4.2.
Gambar 4.2. Spektrum FT-IR GIF
Tabel 4.2. Hasil Analisis Gugus Fungsi GIF dengan Spektrofotometer FT-IR
Parameter Bilangan Gelombang (cm-1)
Vibrasi streaching O-H 3407
VibrasistreachingC-H sp3 2895
Vibrasibending C-O 1270
VibrasistreachingP=O Vibrasi P-O-C alifatik
4.1.2.3. Hasil Analisis Gugus Fungsi GKK:TMF 1:2 + 0.05 g Vitamin E 70% dengan Spektrofotometer FT-IR
Data spektroskopi FT-IR memberikan puncak-puncak vibrasi pada bilangan gelombang 3407 cm-1; 2899 cm-1; 1652 cm-1; 1120 cm-1; 892 cm-1. Hasil spektrum FT-IR galaktomanan ikat silang fosfat vitamin E (GIFVE) dapat dilihat pada gambar 4.3.
Gambar 4.3. Spektrum FT-IR GIFVE
Tabel 4.3 . Hasil Analisis Gugus Fungsi Galaktomanan + Vitamin E dengan Spektrofotometer FT-IR
Parameter Bilangan Gelombang (cm-1)
Vibrasi streaching O-H 3407
VibrasistreachingC-H Vibrasistreaching C=C
2899 1652
Vibrasi Streaching C-O 1120
4.1.3. Hasil Analisis Morfologi Permukaan Scanning Electron Microscopic (SEM)
Analisis morfologi permukaan dilakukan terhadap galaktomanan ditunjukkan pada gambar 4.4, galaktomanan ikat silang posfat pada gambar 4.5, dan galaktomanan ikat silang posfat dengan penambahan vitamin E ditunjukkan pada gambar 4.6.
Gambar 4.4. Hasil Uji Morfologi Permukaan Galaktomanan Kolang Kaling
Gambar 4.6. Hasil Morfologi Permukaan GIF 1:2 + Vitamin E 70%
4.1.4. Hasil Inkorporasi Vitamin E pada Galaktomanan Kolang-Kaling
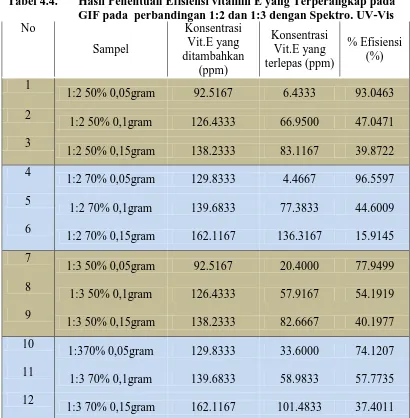
Tabel 4.4. Hasil Penentuan Efisiensi vitamin E yang Terperangkap pada GIF pada perbandingan 1:2 dan 1:3 dengan Spektro. UV-Vis
No
1:2 50% 0,15gram 138.2333 83.1167 39.8722 4
1:2 70% 0,05gram 129.8333 4.4667 96.5597 5
1:2 70% 0,1gram 139.6833 77.3833 44.6009 6
1:2 70% 0,15gram 162.1167 136.3167 15.9145 7
1:3 50% 0,05gram 92.5167 20.4000 77.9499 8
1:3 50% 0,1gram 126.4333 57.9167 54.1919 9
1:3 50% 0,15gram 138.2333 82.6667 40.1977 10
1:370% 0,05gram 129.8333 33.6000 74.1207 11
1:3 70% 0,1gram 139.6833 58.9833 57.7735 12
4.4. Hasil Analisis Kandungan Vitamin E Setelah Diinkorporasi
Menggunakan Alat HPLC
Komponen senyawa vitamin E yang tidak terperangkap pada matriks GIF ditunjukkan pada tabel 4.5.
Table 4.5Hasil Penentuan Vitamin E yang Tidak Terperangkap Pada Matriks GIF dengan HPLC
NO Sampel
Komposisi Vitamin E (%) α
-4.2. Pembahasan
4.2.1. Hasil Ekstraksi Galaktomanan Dari Kolang-Kaling
Sebanyak 100,44 gram kolang kaling diekstraksi menggunakan air suling dan penambahan etanol p.a dengan perbandingan 1:2, maka diperoleh galaktomanan sebanyak 5,7867 gram (5,7613%).
galaktomanan dengan etanol p.a menghasilkan galaktomanan yang lebih tahan lama disimpan. Dimana air dapat mempercepat proses pelapukan atau tumbuhnya jamur yang menyebabkan kerusakan pada galaktomanan.
4.2.2. Hasil Inkorporasi vitamin E pada Galaktomanan Ikat Silang Fospat
Vitamin E yang diperoleh memiliki nilai antioksidan tinggi yang memainkan peranan penting untuk mencegah terjadinya reaksi radikal bebas, namun demikian antioksidan alami sukar larut dalam air dan secara biologi tidak stabil, karena sensitif terhadap faktor lingkungan ataupun pada saat pengolahan seperti cahaya, dan suhu ( Evanset al., 2002). Untuk mengurangi kelemahan tersebut maka vitamin E sebaiknya diinkorporasi kedalam suatu matriks polimer galaktomanan kolang-kaling sehingga vitamin E dapat terserap dalam matrik tersebut.
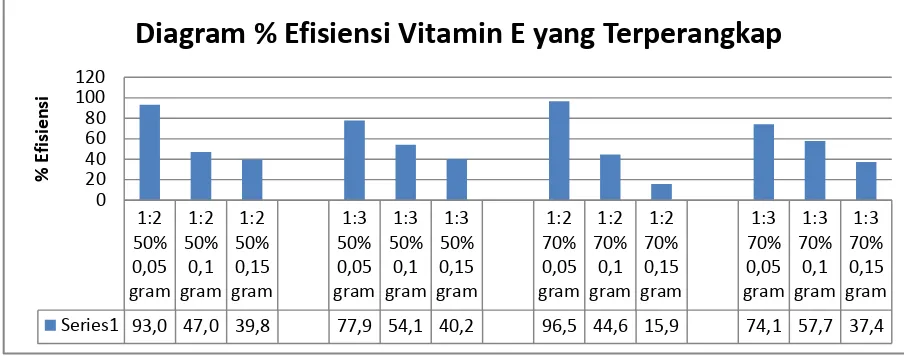
Gambar 4.7 Diagram % Efisiensi Vitamin E yang terperangkap pada GIFVE
Hasil data HPLC (lampiran 11) menunjukkan bahwa vitamin E yang terperangkap dalam matriks dapat diketahui melalui pengujian hasil cucian matriks. Setelah dilakukannya uji vitamin E dengan HPLC, maka diperoleh komposisi vitamin e yang terlepas dari vitamin E 70% dengan berat 0.05 gram pada perbandingan GIF 1:2 adalah yang terkecil. Dikarenakan vitamin E yang ditambahkan kedalam matriks terperangkap dengan sangat baik, ditinjau dari komposisi tokoferol dan tokotrienol yang relatif sedikit dibandingkan dengan sampel yang lain. Data ini sangat mendukung data spektrofotometer UV-Vis. Diagram % vitamin E yang tidak terperangkap dengan alat HPLC ditunjukkan pada gambar 4.8.
Gambar 4.8 Diagram % vitamin E yang tidak terperangkap pada matriks GIFVE
1:2
Series1 93,0 47,0 39,8 77,9 54,1 40,2 96,5 44,6 15,9 74,1 57,7 37,4
0
Diagram % Efisiensi Vitamin E yang Terperangkap
0
tokotrienol 0,16 7,65 9,67 0,16 0,27 8,27 0,1 8,26 29,5 0,21 2,25 20,6
%
4.2.3. Hasil Analisis Gugus Fungsi dengan Spektrofotometer FT-IR
Tarigan, 2014 telah melakukan penelitian terhadap stabilitas vitamin E dari PFAD yang diinkorporasi pada galaktomanan kolangkaling untuk mengetahui interaksi antara galaktomanan dan vitamin E adanya puncak bilangan gelombang pada 1640 cm-1 (GKK dan vitamin E) dan 1639 cm-1menunjukkan vibrasi
streachingikatan rangkap C=C. Interaksi antara galaktomanan dan vitamin E
terjadi karena galaktomanan memilki pori pori dan galaktomanan juga bersifat hidrofilik karena adanya cabang galaktosa dan manosa sebagai rantai utama bersifat hidrofobik sehingga gaya yang terjadi antara senyawa polar dan non polar adalah gaya dipol dipol, yang menunjukkan bahwa vitamin E telah terperangkap pada galaktomanan.
O
Terjadinya inkorporasi vitamin E pada GIF ditunjukkan dengan adanya perubahan puncak vibrasi regangan gugus OH dari gelombang 3348 cm-1menjadi 3407 cm-1; vibrasi regangan C-H pada GIF dari gelombang 2895 menjadi 2899 pada GIFVE, demikian juga terjadi vibrasi regangan C=C pada GIFVE di gelombang 1652 cm -1
yang menunjukkan adanya interaksi antara vitamin E dengan galaktomanan (Tarigan,2004). Semakin tajamnya intensitas spektrum pada bilangan gelombang 875 cm-1menjadi 892 cm-1menunjukkan vibrasi gugus P-O-C alifatik.
4.2.4. Hasil Data SEM Galaktomanan, GIF, dan GIFVE
Dari gambar 4.4 ditunjukkan morfologi permukaan Galaktomanan. Dimana ditunjukkan bahwa terdapatnya ruang-ruang kosong (dark cave) yang tidak teratur. Dari gambar 4.5 ditunjukkkan bentuk morfologi permukaan GIF (Galaktomanan ikat silang fosfat) yang sudah teratur dibandingkan dengan gambar 4.4.
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Efisiensi vitamin yang terikat kedalam matriks galaktomanan kolang-kaling (Arengapinnata) yang diikat silang dengan trinatrium trimetafosfat dengan perbandingan 1:2 dan 1:3 (galaktomanan : TMF) dengan variasi berat 0,05; 0,1; 0,15 gram diperoleh sebesar 15.91448% - 96.55969%. Pengikatan vitamin E oleh matriks galaktomanan ikat silang fosfat yang lebih efisien yaitu vitamin E 70% dengan berat 0,05 gram pada perbandingan galaktomanan : TMF = 1:2 sebesar 96.55969%.
5.2 Saran
BAB 2
TINJAUAN PUSTAKA
2.1. Tanaman Aren (Arenga pinnata)
Aren (Arenga pinnata) merupakan tanaman serba guna yang dapat hidup didaerah tropis basah serta mampu beradaptasi dengan baik pada berbagai agroklimat mulai dari dataran rendah hingga 1.400 meter diatas permukaan laut. Aren merupakan tumbuhan berbiji tertutup dimana biji buahnya terbungkus daging buah.
Aren banyak ditanam di Indonesia termasuk di propinsi Sumatera Utara, Aceh, Sumatera Barat, Bengkulu, Jawa barat, Banten, Jawa Tengah, Kalimantan Selatan dan Sulawesi Selatan. Tanaman aren belum dibudidayakan dan sebagian besar masih menerapakan teknologi yang minim (Anonim, 2009). Adapun sistematika tanaman aren adalah sebagai berikut:
Kingdom : Plantae
Tinggi batang tanaman aren berkisar antara 8-20 m sehingga untuk
menyadap nira diperlukan tangga. Tanaman berbunga setelah berumur 7-12 tahun.
Tandan bunga muncul dari setiap pelepah atau bekas pelepah daun, mulai dari atas
kira-kira seperempat dari pucuk kearah bawah. Bunga pada tandan pertama
hingga kelima atau enam adalah bunga betina, baru disusul bunga jantan yang
muncul secara bertahap hingga ke pangkal batang atau 2-3 m di atas tanah.
Seluruh bunga betina akan masak dalam 1-3 tahun. Bunga betina yang
masih muda dapat diolah menjadi buah aren atau kolang-kaling. Buah aren
serangga. Buah aren berbentuk bulat berdiameter 4 – 5 cm, di dalamnya berisi biji 3 buah, masing masing terbentuk seperti satu siung bawang putih.
Bagian – bagian dari buah aren terdiri dari :
1. Kulit luar, halus berwarna hijau pada waktu masih muda, dan menjadi kuning setelah masak.
2. Daging buah, berwarna putih kekuning – kuningan.
3. Kulit biji, berwarna kuning dan tipis pada waktu masih muda, dan berwarna hitam yang keras setelah buah masak.
4. Endosperm, berbentuk lonjong agak pipih berwarna putih agak bening dan lunak pada waktu buah masih muda; dan berwarna putih, padat atau agak keras pada waktu buah sudah masak.
Buah yang masih muda adalah keras dan melekat sangat erat pada untaian buah, sedangkan buah yang sudah masak daging buahnya agak lunak. Daging buah aren yang masih muda mengandung lendir yang sangat gatal jika mengenai kulit, karena lendir ini mengandung asam oksalat. Buah yang setengah masak dapat dibuat kolang-kaling.
Kolang-kaling adalah endosperm biji buah aren yang berumur setengah masak setelah melalui proses pengolahan. Setelah diolah menjadi kolang-kaling, maka benda ini mejadi lunak, kenyal, dan berwarna putih agak bening (Sunanto, 1993).Tiap buah aren mengandung tiga biji. buah aren yang setengah masak, kulit biji buahnya tipis, lembek dan berwarna kuning, inti biji (endosperm) berwarna putih agak bening dan lembek, endosperm inilah yang diolah menjadi kolang-kaling (Mogea et al, 1991).
Adapun cara untuk membuat kolang-kaling sebagai berikut:
dengan air sampai dihasilkan inti biji yang bersih.Buah aren direbus dalam belanga/kuali sampai mendidih selama 1-2 jam, sehingga kulit biji menjadi lembek dan memudahkan untuk melepas/memisahkan dari inti biji. Inti biji ini dicuci berulang-ulang sehingga menghasilkan kolang-kaling yang bersih.
Untuk menghasilkan kolang-kaling yang baik, bersih dan kenyal, inti biji yang sudah dicuci diendapkan dalam air kapur selama 2 – 3 hari. Setelah direndam dalam air kapur, maka kolang-kaling yang terapung inilah yang siap untuk dipasarkan.Analisis terhadap kolang-kalingmemperlihatkan komposisi kimia yang dikandung berdasarkan berat keringnya adalah 5,2% protein, 0,4% lemak, 2,5% abu, 39% serat kasar dan 52.9% karbohidrat (Nisa, 1996). Kolang-kaling memiliki kadar air sangat tinggi, hingga mencapai 93,8% dalam setiap 100 gram-nya. Kolang-kaling juga mengandung kasar.
Selain memiliki rasa yang menyegarkan, mengkonsumsi kolang-kaling juga membantu memperlancar kerja saluran cerna manusia. Kandungan karbohidrat yang dimiliki kolang kaling bisa memberikan rasa kenyang bagi orang yang mengkonsumsinya, selain itu juga menghentikan nafsu makan dan mengakibatkan konsumsi makanan jadi menurun, sehingga cocok dikonsumsi sebagai makanan diet. Kolang-kaling juga dapat digunakan sebagai coktail dan makanan ringan lokal seperti kolak (Orwa et al., 2009). Karbohidrat di dalam kolang-kaling pada umumnya adalah galaktomanan dengan berat molekul beragam dari 6000 sampai dengan 17000 (Koiman, 1971).
2.2. Galaktomanan
Kebanyakan tumbuh-tumbuhan memiliki cadangan polisakarida yang secara biologis tidak memiliki fungsi apapun terkecuali sebagai cadangan sumber karbon untuk bertumbuh. Tumbuhan dari famili Poaceae seperti misalnya gandum, padi,
Tumbuhan lainnya dari keluarga legume memiliki cadangan polisakarida dalam bentuk galaktomanan. Hasil penelitian sebelumnya menunjukkan dari 163 spesies tumbuhan dari keluarga legume ini, 119 diantaranya menyimpan cadangan polisakaridanya dalam bentuk galaktomanan (Mathur, 2012). Galaktomanan ini memiliki selain sebagai cadangan makanan juga berfungsi menyimpan air untuk mencegah terjadinya kekeringan pada tumbuhan (Srivastava et al., 2005).
Galaktomanan merupakan polisakarida heterogen yang terdiri dari rantai utama β-(1-4)-D-manopiranosa dengan satu unit cabang α-D-galaktopiranosa yang terikat pada posisi α-(1-6). Galaktomanan dari masing-masing tanaman berbeda-beda pada rasio manosa dan galaktosa, distribusi galaktosa pada rantai manosa dan berat molekulnya.
Gambar 2.1. Struktur umum gaktomanan (Cerqueira et al., 2009).
Viskositas galaktomanan sangat konstan sekali pada kisaran pH 1 – 10,5 yang kemungkinan disebabkan oleh karakter molekulnya yang bersifat netral. Namun demikian apabila galaktomanan akan mengalami degradasi pada kondisi yang sangat asam atau basa pada suhu tinggi.
Sifat fisikokimia galaktomnan dapat dikarakterisasi dengan menggunakan beberapa peralatan dan teknik yang berbeda. Parameter-parameter yang penting dalam karakterisasi galaktomanan adalah perbandingan manosa dan galaktosa, berat molekul rata-rata, bentuk struktur dan viskositas intrinsiknya. Rasio manosa dan galaktosa dapat ditentukan dengan menggunakan kromatografi gas atau dengan kromatografi pertukaran anion tekanan tinggi setelah terlebih dahulu dihidrolisis dengan menggunakan asam.
Berat molekulnya dapat ditentukan dengan menggunakan size exclusion
chromatography sedangkan distribusi galaktosa pada rantai manannya dapat
dikarakterisasi dengan menggunakan spektroskopi13 C-NMR atau dengan menggunakan metode enzimatis dengan enzim β-D-mannanase yang akan mendegradasi galaktomanan secara spesifik. Viskositas intrinsik dapat ditentukan dengan menggunakan viskometer kapiler dan persamaan Huggins & Kramer’s untuk menentukan viskositasnya (Cerqueira et al., 2009b).
Rasio manosa dan galaktosa tergantung pada sumber galaktomanan tersebut dan umumnya berkisar pada 1,1 sampai dengan 5,0. Galaktomanan dengan kandungan galaktosa yang besar umumnya mudah larut dalam air dan kecenderungannya untuk membentuk gel sangat rendah dibandingakn galaktomanan dengan rasio galatosa yang rendah.Kelarutan yang sangattinggitersebutolehbanyaknyarantaicabangsehinggarantaimanosamenjadisuk aruntukberinteraksisecaraintermolekuler (Srivastavaand Kapoor, 2005).
2.3. Galaktomanan Kolang Kaling Ikat Silang
silang hampir sama dengan metode asetilasi yaitu samasama mengganti gugus -OH dengan gugus fungsi yang lain. Pada metode ikat silang gugus –-OH di ganti dengan gugus eter, ester, atau fosfat.Trinatrium trimetafosfat (TMP) merupakan bahan tidak beracun yang dapat digunakan untuk reaksi ikat silang pada galaktomanan untuk meningkatkan kualitas darifilm galaktomanan yang dihasilkan, hal ini dikarenakan trinatrium trimetafosfat akan mengurangi sifat pengembangannya (Mohini, et al., 2006).
Pada pH basa, senyawa kompleks ester dipolimer fosfat dibentuk dari guar gum dan trinatrium trimetafosfat yang mengalami reaksi ikat silang. Sifat mengembang pada polimer yang terikat silang menurun secara jelas (29-35 kali lipat) (Gowda et al., 2012).
Untuk reaksi ikat silang antara Guar Gum dan Ion borat, dan guar gum dengan gluteraldehida dapat dilihat pada gambar 2.2 dan 2.3.
C
Guar ion borat Guar ikat silang
Gambar 2.2 Reaksi ikat silang galaktomanan dan ion borat(Chudzikowski, 1971)
HC(CH2)3CH
Gambar 2.3 Reaksi antara gluteraldehida dan gugus hidroksil Guar Gum (Kabir et al., 1998).
Lim dan Seib (1993) menyelidiki bahwa modifikasi ikat silang akanmemberikan hasil lebih baik dalam mempertahankan viskositas bila guar
menggunakancampuran garam fosfat Sodium trimetaphosphat (STMP) dan Sodium tripoliphosphat (STPP) dibandingkan hanya menggunakan STMP.
Hasil penelitian Wattanachant et al., (2002), menunjukkan bahwa campuran garam fosfat 2% STMP dan 5% STPP lebih efisien dalam hidroksipropilasi ikat silang pati sagu dibandingkan dengan menggunakan POCl3 atau epiklorohidrin.
Kabir, et al., (2000) melakukan penelitian guar gum ikat silang dengan trinatrium trimetafosfat mampu mereduksi sifat mengembang sehingga dapat digunakan sebagai pembawa untuk mencapai target yang dituju, kemampuan mengembang gum dalam matriks yang tinggi tidak dapat digunakan sebagai pembawa sehingga dilakukan modifikasi dan mampu dilepas pada bagian yang rusak.
2.4. Spektrofotometer Ultraviolet Visibel (UV-Vis)
Spektrofotometer UV-Vis adalah pengukuran panjang gelombang dan intensitas sinar ultraviolet dan cahaya tampak yang diabsorbsi oleh sampel. Sinar ultraviolet dan cahaya tampak memiliki energi yang cukup untuk mempromosikan elektron pada kulit terluar ke tingkat energi yang lebih tinggi. Spekroskopi UV-Vis biasanya digunakan umtuk molekul dan ion anorganik atau kompleks didalam larutan. Spektrum UV-Vis mempunyai bentuk yang lebar dan hanya sedikit informasi tentang struktur yang bisa didapatkan dari spektrum ini. Tetapi spektrum ini sangat berguna untuk pengukuran secara kuantitatif. Konsentrasi dari analit didalam larutan bisa ditentukan dengan mengukur absorban pada panjang gelombang tertentu dengan menggunakan hukum Lambert-Beer.
suatu senyawa, serta mampu untuk menganalisa senyawa organik secara kuantitatif (Dachriyanus, 2004).
2.5. Scanning Electron Microscopy (SEM)
Scanning Electron Microscopy (SEM) merupakan alat yang dapat
membentuk bayangan permukaan. Struktur permukaan suatu benda yang akan diuji dapat dipelajari dengan mikroskop elektron pancaran karena jauh lebih mudah untuk mempelajari struktur permukaan itu secara langsung. Pada dasarnya, SEM menggunakan sinyal yang dihasilkan elektron dan dipantulkan atau berkas sinar elektron sekunder.
SEM menggunakan prinsip scanning yaitu berkas elektron diarahkan pada titik permukaan spesimen. Gerakan elektron diarahkan dari satu titik ke titik lain pada permukaan spesimen. Jika seberkas sinar elektron ditembakkan pada permukaan spesimen maka sebagian dari elektron itu akan dipantulkan kembali dan sebagian lagi diteruskan. Jika permukaan spesimen tidak merata, banyak lekukan, lipatan atau lubang-lubang, maka tiap bagian permukaan itu akan memantulkan elektron dengan jumlah dan arah yang berbeda dan kemudian akan ditangkap oleh detektor dan akan diteruskan ke sistem layar. Hasil yang diperoleh merupakan gambaran yang jelas dari permukaan spesimen dalam bentuk tiga dimensi.
Dalam penelitian morfologi permukaan dengan menggunakan SEM, pemakaiannya sangat terbatastetapi memberikan informasi yang bermanfaat mengenai topologi permukaan dengan resolusi sekitar 100 Å (Stevens, 2001).
2.6. Vitamin E
(Colombo, 2010). Perbedaan struktur molekul antara tokoferol dan tokotrienol menyebabkan perbedaan aktivitas antioksidan keduanya. Tokotrienol memiliki aktivitas antioksidan yang tinggi. Karena tokotrienol memiliki 3 ikatan rangkap yang menyebabkan lebih cepat teroksidasi dibandingkan tokoferol (Suzuki et
al.,1993).
Vitamin E melindungi membran sel, terutama di paru-paru dan sel darah merah terhadap kerusakan yang disebabkan oleh berbagai polutan, peroksida,dan radikal bebas yang terbentuk selama proses metabolisme, dapat bekerja secara sinergis dengan nutrisi antioksidan lain seperti vitamin C, beta-karoten untuk memuaskan radikal bebas atau peroksida, dan sangat penting untuk saraf dan otot fungsi sel. Vitamin E bisa sebagai antioksidan (Constantinides,2006).
Gambar 2.4. A. Tokoferol ; B. Tokotrienol (Duhem et al., 2014)
2.7 Kromatografi Cair Kinerja Tinggi (HPLC)
Kromatografi Cair Tenaga Tinggi (KCKT) atau biasa juga disebut dengan High Performance Liquid Chromatography (HPLC) merupakan metode yang tidak destruktif dan dapat digunakan baik untuk analisis kualitatif dan kuantitatif. HPLC secara mendasar merupakan sebuah perkembangan tingkat tinggi dari kromatografi kolom. Selain dari pelarut yang menetes melalui kolom di bawah pengaruh gravitasi, HPLC didukung oleh pompa yang dapat memberikan tekanan tinggi sampai dengan 400 atm. Hal ini membuat HPLC dapat memisahkan komponen sampel lebih cepat. Saat ini, HPLC merupakan teknik pemisahan yang diterima secara luas untuk analisis dan pemurnian senyawa tertentu dalam suatu sampel dalam berbagai bidang, antara lain farmasi, lingkungan, bioteknologi, polimer, dan industri-industri makanan. Beberapa perkembangan HPLC terbaru antara lain miniaturisasi sistem HPLC, penggunaan HPLC untuk analisis asam-asam nukleat, analisis protein, analisis karbohidrat, dan analisis senyawa-senyawa kiral.
dalam kolom terjadi pemisahan komponen-komponen campuran. Karena perbedaan kekuatan interaksi antara solut-solut terhadap fasa diam. Solut-solut yang kurang kuat interaksinya dengan fasa diam akan keluar dari kolom lebih dulu. Sebaliknya, solut yang kuat berinteraksi dengan fasa diam maka solut-solut tersebut akan keluar kolom dideteksi oleh detektor kemudian direkam dalam bentuk kromatogram kromatografi gas. Seperti pada kromatografi gas, jumlah peak menyatakan konsentrasi komponen dalam campuran. Komputer dapat digunakan untuk mengontrol kerja sistem HPLC dan mengumpulkan serta mengolah data hasil pengukuran HPLC (Anonim, 2014).
2.8. Fourier Transform Infrared (FT-IR)
Instrumen yang digunakan untuk mengukur resapan radiasi infra merah pada pelbagai panjang gelombang disebut spektrometer inframerah. Pancaran inframerahumumnya mengacu pada bagian spektrum elektromagnet yang terletak di antara daerah tampak dan daerah gelombang mikro. Pancaran inframerah yang kerapatannya kurang dari pada 100 cm-1 (panjang gelombang lebih dari 100 µm) diserap oleh sebuah molekul organik dan diubah menjadi energi putaran molekul. Penyerapan itu tercatu dan demikian spektrum rotasi molekul terdiri dari garis-garis yang tersendiri.
Atom molekul bergerak dengan berbagai cara, tetapi selalu pada tingkat energi tercatu. Energi getaran rentang untuk molekul organik bersesuaian dengan radiasi inframerah dengan bilangan gelombang antara 1200 dan 4000 cm-1. Bagian tersebut dari spektrum inframerah khususnya berguna untuk mendeteksi adanya gugus fungsi dalam senyawa organik. Memang daerah ini sering dinyatakan sebagai daerah gugus fungsi karena kebanyakan gugus fungsi yang dianggap penting oleh para kimiawan organik mempunyai serapan khas dan nisbi tetap pada panjang gelombang tersebut.
Identifikasi pita absorpsi khas yang disebabkan oleh berbagai gugus fungsi merupakan dasar penafsiran spektrum inframerah. Hadirnya sebuah puncak serapan dalam daerah gugus fungsi dalam sebuah spektrum inframerah hampir selalu merupakan petunjuk pasti bahwa beberapa gugus fungsi tertentu terdapat dalam senyawa cuplikan. Demikian pula, tidak adanya puncak dalam bagian tertentu dari daerah gugus fungsi sebuah spektrum inframerah biasnya berarti bahwa gugus tersebut yang menyerap pada daerah itu tidak ada (Pine, 1980). Asam karboksilat mempunyai dua karakteristik absorbsi IR yang membuat senyawa -CO2H dapat diidentifikasi sengan mudah. Ikatan O-H dari golongan karboksil diabsorbsi pada daerah 2500 sampai 3300 cm-1, dan ikatan C=O yang ditunjukkan diabsorbsi di antara 1710 sampai 1750 cm-1 (McMurry, 2007).
Sistim optik Spektrofotometer FTIR seperti pada gambar dibawah ini dilengkapi dengan cermin yang bergerak tegak lurus dan cermin yang diam. Dengan demikian radiasi infra merah akan menimbulkan perbedaan jarak yang ditempuh menuju cermin yang bergerak ( M ) dan jarak cermin yang diam ( F ). Perbedaan jarak tempuh radiasi tersebut adalah 2 yang selanjutnya disebut sebagai retardasi ( δ ). Hubungan antara intensitas radiasi IR yang diterima detektor terhadap retardasi disebut sebagai interferogram. Sedangkan sistim optik dari Spektrofotometer IR yang didasarkan atas bekerjanya interferometer disebut sebagai sistim optik Fourier Transform Infra Red.
BAB 1 PENDAHULUAN
1.1. Latar Belakang
Polisakarida dialam telah digunakan secara luas sebagai pengental pada produk makanan, obat-obatan dan matriks pelepasan obat-obatan yang dikonsumsi secara oral. Akhir-akhir ini polisakarida yang terbiodegradasi, seperti pektin, dekstran, dan galaktomanan dapat digunakan sebagai pembawa obat kedalam usus manusia jika dimodifikasi sebagaimanan mestinya (misalnya : ikat silang untuk membentuk hidrogel)untuk mengurangi sifat kelarutan/mengembangnya dalam air (Gliko-Kabir et al.,1998).
Peneliti sebelumnya telah meneliti penurunan sifat mengembang galaktomanan guar gum yakni guar gum terikat silang gluteraldehida (Gliko-Kabir
et al.,1998), guar gum (GG) dengan 1-etil 3-(3-dimetil amino propil) (Banegas et al.,2013), guar gum dengan Trinatrium trimetafosfat (Gliko-kabir et al.,2000a,b)
guar gum dengan borak (Kesavan et al.,1992).Penguraian sifat mengembang sangat dibutuhkan untuk mencegah obat yang terperangkap tidak dilepas lebih awal sebelum sampai ke tujuan setelah dikonsumsi secara oral (Gliko Kabir et al., 1998).Novalia, 2015 telah melakukan modifikasi galaktomanan kolang kaling (GKK) melalui proses ikat silang dengan trinatriumtrimetafosfat, hasil indeks swelling galaktomanan ikat silang didalam larutan NaCl 0,9% dan air suling masih terlalu besar.
Vitamin E umumnya dikenal sebagai tokoferol dan tokotrienol, merupakan antioksidan alami larut dalam lemak yang dapat mencegah terjadinya oksidasi asam lemak tidak jenuh pada produk makanan (Nasaretman et al., 2008).Vitamin E memainkan peranan penting untuk mencegah terjadinya reaksi radikal bebas yang menyebabkan penyakit seperti jantung koroner dan kanker (Rimm et al., 1993), namun demikian antioksidan alami sukar larut dalam air dan secara biologi tidak stabil, karena sensitif terhadap faktor lingkungan ataupun pada saat pengolahan seperti cahaya, oksigen, dan suhu (Evans et al., 2002).Untuk menanggulangi kelemahan tersebut maka vitamin E sebaiknya diinkorporasi kedalam suatu matriks.
Salah satu matriks yang dapat digunakan adalah galaktomanan kolang kaling ikat silang fosfat. Galaktomanan kolang kaling diperoleh dari endosperm biji aren yang berumur setengah matang (Sunanto, 1993) dan pemanfaatan kolang kaling ini juga masih terbatas.
Peneliti sebelumnya telah menggunakan beberapa matriks sebagai pembawa pembawa tokoferol antara lain calsium alginat (Yoo et al., 2006), calsium pektinat (Song et al.,2009),oktenil suksinat anhidrida (Hategekimana,2015), xantan (Anca
et al.,2009). Namun demikian galaktomanan ikat silang fosfat belum digunakan
dengan TMP dimana pada perbandingan 1:2 dan 1:3 banyak vitamin yang terperangkap dalam matriks.
Berdasarkan uraian diatas peneliti tertarik untuk membuat inkorporasi vitamin E dari matriks galaktomanan kolang kaling yang terikat silang dengan fosfat dengan variasi berat vitamin E 0,05 gram, 0,1 gram, dan 0.15 gram dengan perbandingan galaktomanan dan TMP 1:2 dan 1:3, agar semakin efektifnya vitamin E yang terperangkap pada GIFVE. Vitamin E yang telah terperangkap pada matriks dianalisis dengan SEM (Scanning Electron Microscopic), Spektrofotometer FT-IR, selanjutnya ditentukan vitamin E yang tidak terperangkap dengan spektrofotometer UV-Visibel dan HPLC dari hasil cucian matriks.
1.2Permasalahan
Bagaimanakah efisiensi vitamin E 50% dan 70% yang terperangkap kedalam matriks galaktomanan kolang kaling (Arengapinnata) yang diikat silang dengan trinatrium trimetafosfat pada perbandingan 1:2 dan 1:3.
1.3Pembatasan Masalah
1. Vitamin yang digunakan adalah vitamin E 50% dan 70%
2. Variasi perbandingan galaktomanan dan trinatrium trimetaposfat yang digunakan adalah 1:2 dan 1:3
3. Digunakan variasi berat vitamin 0,05, 0,1, dan 0,15 pada masing-masing konsentrasi vitamin E 50% dan 70%
4. Efisiensi vitamin yang tidak terperangkap diuji dengan menggunakan Spektrofotometer UV-Vis dan juga HPLC.
1.4 Tujuan Penelitian
Untuk mengetahui efisiensi vitamin E 50% dan 70% yang terperangkap kedalam matriks galaktomanan kolang kaling (Arengapinnata) yang diikat silang dengan trinatrium trimetafosfat pada perbandingan 1:2 dan 1:3.
1.5 Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan informasi tentang efisiensi penggunaan vitamin E yang diikat silang fosfat melalui matriks galaktomanan kolang kaling (Arengapinnata).
1.6 Lokasi Penelitian
1.7 Metodologi Penelitian
INKORPORASI VITAMIN E 50% DAN 70% PADA MATRIKS
GALAKTOMANAN IKAT SILANG FOSFAT
ABSTRAK
Telah dilakukan penelitian tentang inkorporasi vitamin E 50% dan 70% pada matriks galaktomananikat silang fosfat. Penelitian ini bertujuan untuk menganalisis vitamin E yang terperangkap kedalam matriks galaktomanan kolang-kaling yang diikat silang dengantri natrium trimeta fosfat. Pembuatan galaktomananikat silang fospat dilakukan dengan mereaksikan galaktomanan kolang-kaling (GKK) denganTrinatriumtrimetafosfatdenganperbandingan 1:2 dan 1:3 (b/b) diadukselama 2 jam dalamsuhukamarpada pH 12. PembuatanGalaktomananIkatSilangFosfat vitamin E (GIFVE) dilakukandenganmenambahkan vitamin E denganvariasi berat 0.05 gram; 0.1 gram; dan 0.15 gram pada matriks GIF dengan perbandingan GKK:TMF = 1:2 serta 1:3. Kadar vitamin E yang terperangkap diperoleh dari hasil perhitungan jumlah vitamin E yang ditambahkan, dikurang vitamin E hasil pencucian film GIFVE. Hasil analisa FT-IR menunjukkan telah terbentuknya ikat silang fosfat ditandai dengan adanya perbedaan puncak gugus OH dari yang melebar dan tajam pada galaktomanan menjadi lemah. Demikian juga setelah penambahan vitamin E pada GIF muncul puncak pada bilangan gelombang 1652 cm-1 merupakan vibrasi
streaching C=C dan puncak tajam pada bilangan gelombang 1120 cm-1 dan 1270 cm-1 merupakan vibrasi bending C-O. Hasil SEM menunjukkan telah terjadi perubahan morfologi permukaan dari yang berongga pada GIF menjadi halus pada GIFVE. Hasilspektrofotometer UV-Vis menunjukkanbahwa vitamin E yang terikatbaikpadamatriks GIF adalah vitamin E 70% denganberat 0,05 gram padaperbandingan TMF : GKK 1:2 yaitusebesar96.5597% dan data HPLC menunjukkanbahwa GIFVE 70% denganberat 0.05 gram memiliki sedikit kandungan vitamin E yang terlepassaatpencucian.
INCORPORATION OF VITAMIN E 50% AND 70% ON THE MATRIX GALACTOMANAN CROSSLINKED PHOSPHATE
ABSTRACT
A research on the incorporation of vitamin E 50% and 70% on the matrix galaktomanan crosslink phosphate. This study aimed to analyze the vitamin E is trapped into the matrix galaktomanan fro crosslinked with trisodium trimetafosfat. Making galaktomanan crosslink fospat carried out by reacting galaktomanan fro (GKK) with trisodium trimetafosfat the ratio of 1: 2 and 1: 3 (w / w) was stirred for 2 hours at room temperature at pH 12. Making Galaktomanan Tie Cross Phosphate vitamin E (GIFVE) is done by adding vitamin E to the gram weight variation 0:05; 0.1 grams; and 0:15 gram on the matrix GIF with the comparison GKK: TMF = 1: 2 and 1: 3. Levels of vitamin E were trapped obtained from the calculation of the amount of vitamin E added, subtracted vitamin E washery GIFVE movie. FT-IR analysis results showed the formation of crosslink phosphate has been characterized by the difference in the peak of the OH group is widened and sharp on galaktomanan becoming weaker. Likewise, after the addition of vitamin E in the GIF appears peak at wave number 1652 cm-1 is vibration streaching C = C and a sharp peak at wave number 1120 cm -1 and 1270 cm-1 is a C-O bending vibration. SEM results indicate there has been a change in the morphology of the surface of the hollow on the GIF to be smooth on GIFVE. UV-Vis spectrophotometer results showed that vitamin E is committed to neither vitamin E matrix GIF is 70% by weight of 0.05 grams in comparison TMF: GKK 1: 2 in the amount of 96.5597% and data GIFVE HPLC showed that 70% by weight of 12:05 gram have smaller amounts of vitamin E are released during laundering.
INKORPORASI VITAMIN E 50% DAN 70% PADA MATRIKS
GALAKTOMANAN KOLANG-KALING
IKAT SILANG FOSFAT
SKRIPSI
RENAL BERNADI NAPITUPULU
130822036
DEPARTEMEN KIMIA
PROGRAM STUDI KIMIA EKSTENSI
FAKULTAS MATEMATIKA DAN ILMUPENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
MEDAN
PERSETUJUAN
Judul : Inkorporasi Vitamin E 50% dan 70%
Padamatriks Galaktomanan Kolang-Kaling Ikat Silang Fosfat
Kategori : Skripsi
Nama : Renal BernadiNapitupulu
NomorIndukMahasiswa : 130822036
Program : Sarjana (S1) Ekstensi Kimia
Departemen : Kimia
Fakultas : Matematika Dan IlmuPengetahuanAlam (Fmipa) Universitas Sumatera Utara
Disetujui di
Medan, September 2016
KomisiPembimbing :
Pembimbing 2 Pembimbing 1
SabarminPerangin-angin,S.Si, M.Si Dr. JuliatibrTarigan,S.Si,M.Si NIP : 196912131997022001 NIP: 197205031999032001
Diketahui/ Disetujuioleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
INKORPORASI VITAMIN E 50% DAN 70% PADA MATRIKS
GALAKTOMANAN KOLANG-KALING
IKAT SILANG FOSFAT
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil karya saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, September 2016
PENGHARGAAN
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa, atas berkat dan penyertaanNya penulis dapat menyelesaikan skripsi dengan judul “inkorporasi vitamin e 50% dan 70% pada matriks galaktomananikat silang fosfat”. Dalam penyelesaian skripsi ini penulis senantiasa berterimakasih kepada:
1. Dekan FMIPA USU BapakDr. Krista Sebayang, M.S
2. Ibu Dr. Rumondang Bulan, MS dan Bapak Drs. Albert Pasaribu, M.Sc selaku Ketua dan Sekretaris Departemen Kimia FMIPA USU.
3. Ibu Dr. Juliati Br. Tarigan, M.Si selaku pembimbing I dan Ibu Sabarmin Perangin-angin, M.Si selaku pembimbing II yang telah banyak meluangkan waktu dan selalu membimbing penulis selama melakukan penelitian dan penyusunan skripsi ini hingga selesai.
4. Bapak Prof. Dr. Jamaran Kaban, M.Sc selaku ketua bidang Kimia Organik FMIPA USU
5. Bapak Dr. Mimpin Ginting, M.S selaku Kepala Laboratorium Kimia Organik FMIPA USU beserta Dosen dan Staf Laboratorium Kimia Organik FMIPA USU 6. Ayahanda tercinta M. Napitupulu dan Ibunda tercinta R. Silalahi serta pasangan
terkasih Narta Lena Br. Ginting yang senantiasa memberikan dukungan moril maupun materil kepada penulis.
7. Dan semuaPihak yang terlibat yang tidak dapat disebutkan satu persatu.
Penulis menyadari bahwa skripsi ini masih jauh dari sempurna karena keterbatasan penulis, oleh karena itu penulis mengharapkan kritik dan saran yang dapat menunjang kesempurnaans kripsi ini untuk masa yang akan datang.
Semoga skirpsi ini dapat bermanfaat bagi penelitian selanjutnya, pembaca dan penulis sendiri. Akhir kata penulis mengucapkan banyak terimakasih atas berbagaid ukungan semua pihak dalam penyelesaian skripsi ini.
DAFTAR ISI
Daftar Tabel viii
Daftar Gambar ix
Daftar Lampiran Daftar Singkatan
x xi Bab 1 Pendahuluan
1.1 Latar Belakang 1.2 Permasalahan 1.3 Pembatasan Masalah 1.4 Tujuan Penelitian 1.5 Manfaat Penelitian 1.6 Lokasi Penelitian 1.7 Metodologi Penelitian
1 Bab 2 Tinjauan Pustaka
2.1 Tanaman Aren(Arengapinatta) 2.2 Galaktomanan
2.3 Galaktomanan Kolang Kaling Ikat Silang 2.4 Spektrofotometer UV-Visible
2.5 Scanning Electron Microscopy (SEM) 2.6 Vitamin E
2.7 Kromatografi Cair Kinerja Tinggi (HPLC) 2.8 Fourier Transform Infrared (FT-IR)
4 Bab 3 Metode Penelitian
3.1 Alat-alat 3.2 Bahan-bahan 3.3 Prosedur Penelitian
3.3.1 EkstraksiGalaktomanandariKolang-Kaling 3.3.2 PembuatanGalaktomananIkatSilangFosfat
3.3.2.1 PembuatanLarutanTrinatriumTrimetafosfat 3.3.2.2 PembuatanGalaktomananIkatSilang
Fosfat
3.3.3 Inkorporasi Vitamin E 50% dan 70% pada Matriks GIFVE dengan Perbandingan 1:2 dan 1:3
3.3.4 Ekstraksi Vitamin E yang tidak Terperangkap pada Matriks Galaktomanan Ikat Silang Fosfat
3.4 Bagan Penelitian
3.4.1 EkstraksiGalaktomanandariKolang-Kaling 3.4.2 PembuatanGalaktomananIkatSilangFosfat
3.4.2.1 Pembuatan LarutanTrinatriumTrimetafosfat 3.4.2.2 PembuatanGalaktomananIkatSilang
Fosfat
3.4.3 Pembuatan Matriks Galaktomanan Ikat Silang Fosfatsebagai Pembawa Vitamin E 3.4.4Ekstraksi Vitamin Eyangtidak Terperangkap pada MatriksGalaktomanan IkatSilangFosfat
Bab 4 Hasil dan Pembahasan 4.1 Hasil Penelitian 4.2 Pembahasan
25 31 Bab 5 Kesimpulan dan Saran
DAFTAR TABEL
Nomor Judul Tabel
Halaman
4.1Hasil Analisis Gugus Fungsi Galaktomanan Dengan Spektrofotometer FT-IR
26
4.2 Hasil Analisis Gugus Fungsi GIF Dengan Spektrofotometer FT-IR
4.3 Hasilanalisis Gugus Fungsi Galaktomanan + Vitamin E Dengan Spektrofotometer FT-IR
4.4 Hasil Penentuan Efisiensi Vitamin E yang Terperangkap pada GIF Perbandingan 1:2 dan 1:3 Dengan Spekto. UV-Vis 4.5 Hasil Penentuan Vitamin E yang Tidak Terperangkap Pada MatriksGIF dengan HPLC
27
28
30
DAFTAR GAMBAR
Nomor Judul Gambar
Halaman
2.1 Struktur Umum Galaktomanan 7
2.2 Reaksi Ikat Silang Galaktomanan dan Ion Borat 9 2.3 Proses Isomerasi Glutaraldehida dalam Suasana Asam dan Reaksi
Antara Glutaraldehida dan GugusHidroksil
10
2.4 A. Tokoferol ; B. Tokotrienol 13
4.1 Spektrum FT-IR Galaktomanan 25
4.2 Spektrum FT-IR GIF 26
4.3 Spektrum FT-IR GIFVE
4.4 Hasil Uji Morfologi Permukaan Galaktomanan Kolang Kaling 4.5 Hasil Uji Morfologi Permukaan GIF 1:2
4.6 Hasil Morfologi Permukaan GIF 1:2 + Vitamin E 70%
4.7 Diagram % Efisiensi Vitamin E yang Terperangkap pada GIFVE 4.8 Diagram % vitamin E yang tidak terperangkap pada matriks GIFVE
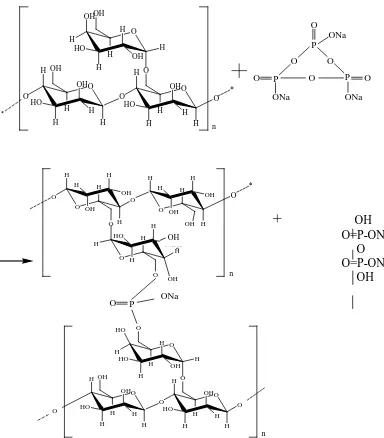
4.9 Reaksi Ikat Silang Galaktomanan dan TMF
DAFTAR LAMPIRAN
Nomor Judul Lampiran
1. Hasil Ekstraksi Galaktomanan Kolang-kaling
2. Hasil Galaktomanan Ikat Silang Fosfat Pembawa Vitamin E
3. Hasil Spektrum FT-IR Galaktomanan
4. Hasil Spektrum GIF
5. Hasil Spektrum FT-IR + Vitamin E 70% 0,05 gram
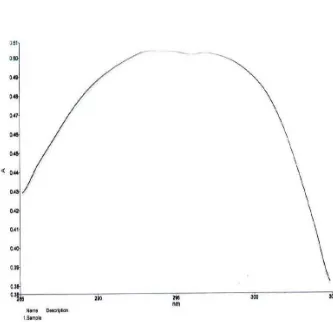
6. Grafik Panjang Gelombang Maksimum Vitamin E
7. Hasil Penentuan Kadar Vitamin E yang Ditambahkan Pada
DAFTAR SINGKATAN
FT-IR : Fourier Transform Infrared GIF : Galaktomanan Ikat Silang Fosfat
GIFVE : Galaktomanan Ikat Silang Fosfat Vitamin E GKK : Galaktomanan Kolang Kaling
HPLC : High Performance Liquid Cromatography SEM : Scanning Electron Microscopy