TUBUH IKAN NOMEI (HORPODON NEHEREUS) DI PERAIRAN
TARAKAN
RATNO ACHYANI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Dengan ini saya menyatakan bahwa tesis yang berjudul:
Kharakteristik Polycyclic Aromatic Hydrocarbons (PAH) di Air dan Sedimen Serta Akumulasinya pada Tubuh Ikan Nomei (Horpodon nehereus) di Kota Tarakan, adalah karya saya sendiri dengan arahan komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau yang dikutip dari karya yang telah diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka dibagian akhir tesis ini.Bogor, Mei 2011
RATNO ACHYANI. Characteristics of the Polycyclic Aromatic Hydrocarbons (PAHs) in Water, Sedimen and their accumulation in the Nomei fish (Horpodon nehereus) in Tarakan Waters. Under direction of TRI PRARTONO, ETTY RIANI.
PAHs are important pollutant in the marine environment because of their mutagenic and carcinogenic properties. PAHs are the most toxic among the hydrocarbon families. The purpose of this study was to identify the component of PAHs and their concentration in water, sediment and their accumulation in the tissue and liver of the fish Horpodon neherus. The study was conducted from June-December 2010. Water was analyzed using by liquid-liquid extraction, while the sediment and fish tissue sampel was carried out using soxhlet extraction. All of extracts were analyzed by GC-MS (Gas Chromatograph Mass Spectrometyr). Lipid content of the fish tissue was ditermined by gravimetric method. Two compounds of PAHs were found with total concentration ranged from 6-248 µg/l in the waters, and 5 component of those were found with total concentration ranged from 7-69 ng/g in the sediment. The content PAH in tissue ranged from 27-422 ng/g and those in liver 6 ranged from121-833 ng/g. The lipid content varied based on the size of body fish, 200 µg/g for <20 cm, 600 µg/g for 21-25 cm and 1700 µg/g for >25 cm size.
RATNO ACHYANI. Karakteristik Polycyclic Aromatic Hydrocarbons (PAHs) di Air dan Sedimen Serta Akumulasinya pada Tubuh Ikan Nomei (Horpodon nehereus) Di Kota Tarakan. Dibimbing oleh TRI PRARTONO, ETTY RIANI.
Kegiatan-kegiatan pembangunan yang berasal dari daratan berpotensi mempengaruhi perairan di sekitarnya. Pembangunan yang cukup signifikan di Kota Tarakan Propinsi Kalimantan Timur yang wilayahnya berupa pulau saat ini dapat menjadi sumber pencemar perairan di sekitarnya. Salah satu yang akhir-akhir ini menjadi perhatian adalah pencemar PAH. PAH masuk ke lingkungan khususnya di perairan laut melalui hujan, buangan industri, tumpahan minyak dan aliran permukaan. Keberadaan senyawa ini di lingkungan menjadi penting karena bersifat karsinogenik dan mutagenik. Tujuan utama penelitian ini menentukan komponen PAH dan konsentrasinya yang ada di air laut, sedimen dan tingkat akumulasinya pada tubuh ikan Nomei. Manfaat dari penelitian ini adalah menduga sumber potensi pencemar dan tingkat bahayanya terhadap kondisi lingkungan perairan.
Jenis dan banyaknya sampel yang digunakan adalah air (3 sampel), sedimen (3 sampel), daging (3 sampel) dan hati ikan Nomei (3 sampel). Stasiun pengambilan contoh air dan sedimen ditentukan berdasarkan 3 lokasi keterwakilan yaitu wilayah yang mewakili daerah kurang banyak kegiatan, mewakili daerah yang aktif/banyak kegiatan dan lokasi pengambilan contoh ikan Nomei. Prosedur analisis PAH dalam air dilakukan dengan metode liquid-liquid extraction. Analisa PAH dalam sedimen, daging dan hati ikan Nomei dilakukan dengan metode soxhlet dan prosedur analisis yang digunakan untuk mengetahui kandungan lemak pada daging ikan Horpodon nehereus dengan metode gravimetri. Analisa jenis PAH pada sampel sedimen, air, daging dan hati ikan Nomei dilakukan dengan menggunakan GCMS tipe Shimadzu QP2010.
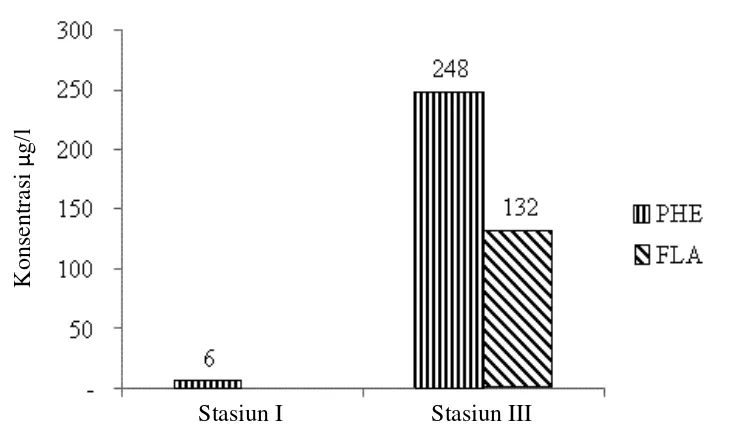
Secara umum jenis PAH yang ditemukan pada cuplik air adalah 2 jenis yaitu fenantrena (PHE) dan fluorantena (FLA). Pada Stasiun 1 hanya ditemukan PHE dengan konsentrasi rendah yaitu 6 µg/l. Pada Stasiun 3 ditemukan FLA mencapai 132 µg/l dan PHE yang mencapai 248 µg/l, tetapi PAH tidak diterdeteksi di Stasiun dua. Pada cuplik sedimen terdapat 5 jenis senyawa PAH. Konsentrasi cuplik sedimen berkisar antara 7-69 ng/g. Konsentrasi maksimum ditemukan pada Stasiun 1 yaitu PHE-C1 69 ng/g dan konsentrasi terendah pada Stasiun 3 yaitu ANT-C1 7 ng/g. Level konsentrasi PAH di air adalah sedang dan sedimen adalah kecil-sedang.
konsentrasi 73 ng/g dan 116 ng/g. NAP-C1 hanya ditemukan pada ukuran besar yaitu 74 ng/g. FLA dan BPH terdeteksi pada ukuran kecil dan sedang. Konsentrasi terbesar FLA 64 ng/g dan BPH 68 ng/g pada ukuran kecil. Jenis PHE hanya terdeteksi pada ukuran ikan sedang dan besar yaitu 115 ng/g dan 203 ng/g.
Pada cuplik hati ikan Nomei teridentifikasi 6 jenis senyawa PAH yang terakumlasi. Kandungan PAH total pada hati ikan Nomei kecil adalah 1679 ng/g, ukuran sedang 977 ng/g, dan ukuran besar 1445 ng/g. NAP-C2 dan PHE adalah jenis PAH yang ditemukan pada setiap ukuran ikan. NAP-C2 mempunyai konsentrasi 833 ng/g pada ukuran kecil, 573 ng/g pada ukuran sedang, dan 660 ng/g pada ukuran besar. PHE mempunyai konsentrasi 427 ng/g pada ukuran kecil, 215 ng/g pada ukuran sedang, dan 176 ng/g pada ukuran besar. Akumulasi total kandungan PAH dalam tubuh ikan Nomei adalah terkontaminasi sangat tinggi.
Jenis PAH FLA hanya ditemukan pada hati ikan Nomei kecil dengan konsentrasi 298 ng/g. NAP-C1 hanya ditemukan pada hati ukuran sedang dengan konsentrasi 190 ng/g dan NAP hanya ditemukan pada hati ukuran besar dengan konsentrasi 381 ng/g. BPH adalah senyawa PAH yang hanya terdapat pada hati ukuran kecil dan besar dengan konsentrasi 121 ng/g dan 227 ng/g. Kandungan lipid pada ikan menunjukkan adanya peningkatan persentasi jumlah lipid berdasarkan ukuran tubuh. Hasil ini menunjukkan bahwa semakin besar tubuh ikan semakin besar pula kandungan lipidnya, namun konsentrasi PAH pada daging tidak berkorelasi positif.
Karakteristik PAH di perairan dan sedimen menunjukkan PAH pirogenik dan petrogenik. Level konsentrasi PAH di air adalah sedang dan sedimen adalah kecil-sedang. Akumulasi total kandungan PAH dalam tubuh ikan Nomei adalah terkontaminasi sangat tinggi.
© Hak cipta milik Institut Pertanian Bogor, Tahun 2011 Hak cipta dilindungi undang-undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebarkan sumbernya. Pengutip hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah dan pengutipan tidak merugikan kepentingan yang wajar IPB
TUBUH IKAN NOMEI (HORPODON NEHEREUS) DI PERAIRAN
TARAKAN
RATNO ACHYANI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Ilmu Kelautan
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
(Harpodon Nehereus) Di Perairan Tarakan Nama : Ratno Achyani
NIM : C551080111
Disetujui
Komisi Pembimbing
Ketua
Dr. Ir. Tri Prartono, M.Sc
Anggota Dr. Ir. Etty Riani, MS
Diketahui,
Ketua Mayor Ilmu Kelautan
Dr. Ir. Neviaty P. Zamani, M.Sc
Dekan Sekolah Pasca Sarjana IPB
Dr. Ir. Dahrul Syah, M.Sc.Agr
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesesaikan. Tema yang dipilh dalam penelitian yang dilaksanakan sejak bulan juni 2010 ini adalah environment investigation, dengan judul Karakteristik Polycyclic Aromatic Hidrocarbons
(PAH) Di Air dan Sedimen Serta Akumulasinya Pada Tubuh Ikan Nomei (Harpodon Nehereus) Di Kota Tarakan
Terima kasih penulis ucapkan kepada Bapak Dr. Ir. Tri Prartono. M.Sc dan Ibu Dr. Ir. Etty Riani. MS selaku pembimbing yang dengan sabar memberi pencerahan. Di samping itu, penghargaan penulis sampaikan kepada Saudari Pipiet dan Prita dari Laboratorium Pangan Universitas Islam Negeri (UIN) Syarif hidayatullah Ciputat Jakarta, yang telah membantu selama analasis sampel. Penghargaan juga disampaikan kepada Almarhum Ayah yang selalu bekerja keras untuk anak-anaknya dan keluarga, Ibu tercinta dan adik-adikku Rita, Tri, Wahyu yang penuh perhatian, istriku tersayang Endah Wanti Hastuti dan anakku Ra’id
Eshan Nawfal Ali penyemangatku, atas segala doa dan kasih sayangnya. Ungkapan terima kasih juga disampaikan kepada saudara-saudara saya senasib dan sepenanggungan, Agung, Sabam, Afdal dan semua teman-teman IKL 2008 yang mencerahkan.
Semoga karya ilmiah ini bermanfaat.
Bogor, Mei 2011
Penulis dilahirkan di Balikpapan pada 29 Juli 1981 dari Ayah Alm. Ngatman dan Ibu Sutrisnani. Penulis merupakan putra pertama dari empat bersaudara. Mempunyai istri bernama Endah Wanti Hastuti dan dikaruniai seorang putra bernama Ra’id Eshan Nawfal Ali.
Pendidikan SD, SMP dan SMA ITCI ditempuh di Penajam Pasir Utara. Pada tahun 2000 meneruskan pendidikan sarjana di Universitas Mulawarman pada Fakultas Perikanan dan Ilmu Kelautan Program Studi Manajemen Sumber Daya Perairan dimana lulus tahun 2005 dan pada tahun yang sama menjadi Dosen pada Fakultas Perikanan dan Ilmu Kelautan Universitas Borneo Tarakan pada Program Studi Manajemen Sumber Daya Perairan.
Penulis menjadi peneliti di Pusat Penelitian Lingkungan Hidup Univ. Borneo Tarakan, sempat menjabat menjadi Kepala Laboratorium Kualitas Air dan terakhir menjadi Sekretaris Jurusan Manajemen Sumber Daya Perairan. Tahun 2008 penulis diterima di Program Studi Ilmu Kelautan pada Program Pascasarjana
DAFTAR ISI
2.8 Karakteristik Perairan Pesisir dan Laut………... 27
3.4.2 Polycyclic Aromatic Hydrocarbon (PAH)………. 34
3.4.3 Analisis lipid……….. 36
3.5 Analisis Data………... 36
4 HASIL DAN PEMBAHASAN………. 39
4.1 Hasil Penelitian………... 39
4.1.1 Kandungan PAH Di Air………. 39
4.1.2 Kandungan PAH Di Sedimen……… 44
4.1.3 Kandungan PAH di Daging dan Hati Ikan Nomei………. 48
4.1.4 Kandungan Lipid……… 59
4.2 Pembahasan………. 60
4.2.1 Sumber PAH……….. 60
4.2.2 Tingkat Konsentrasi PAH……….. 62
4.2.3 Status Ekotoksikologi PAH……… 64
5 KESIMPULAN DAN SARAN………. 69
5.1 Kesimpulan………. 69
5.2 Saran……… 70
DAFTAR TABEL
Hal
1 Penelitan PAH terkait dengan distribusi, karakteristik dan akumulasinya pada beberapa biota perairan di beberapa wilayah dunia.
3
2 Jenis PAH yang biasa digunakan dalam studi environmental forensic
investigations (∑ PAH50) dengan 16 jenis PAH sebagai polutan
prioritas menurut USEPA (∑ PAH16
5
) (Boehm 2006).
3 Pengelompokan PAH berdasarkan berat molekul dan jumlah ring (USEPA).
8
4 Besaran potensi 16 bahan pencemar PAH, terikat pada sedimen (KOC) dan air (KOW
9 ).
5 Total konsentrasi PAH pada sedimen laut pada beberapa wilayah Amerika Utara, Eropa, Afrika dan Asia (dimodifikasi dari Latimer dan Jinshu 2003).
13
6 Konsentrasi PAH di perairan laut beberapa wilayah dunia. 14
7 Konsentrasi PAH dari beberapa biota bivalva laut dan invertebrata (dimodifikasi dari Meador 2006).
15
8 Rasio individu PAH sebagai penduga sumber. 17
9 Rangkuman sensitifitas sifat kronis pada organisme air tawar dan laut (dimodifikasi dari EPA/600/R-02/013).
24
10 Beberapa individu PAH yang bersifat karsinogenik (Neff 1979). 27
11 Daftar 28 jenis PAH, kuantifikasi ion dan konfirmasi ion untuk SIM
(single ion monitoring) GC-MS yang digunakan dalam
mengidentifikasi senyawa PAH selain menggunakan library internal
GC-MS (Orecchio et al. 2009).
35
12 Ratio individu PAH penentu sumber pencemar. 36
13 Tingkatan level konsentrasi PAH pada sedimen (Baumard et al. 1998). 37
14 Konsentrasi ERL (effect range low) dan ERM (effect range
median)untuk menentukan status kontaminasi PAH di sedimen
terhadap organisme laut (Woodhead et al. 1999, O’connor dan john 2000, Burton 2002).
15 Klasifikasi status jaringan ikan yang terkontaminasi PAH (Varanasi et al. 1993 dalam Gomes et al. 2010).
37
16 Kriteria kualitas PAH di perairan laut menurut USEPA (Irwin 1997). 38
17 Sumber pencemar PAH dari beberapa wilayah dunia. 61
18 Diagnosis sumber PAH berdasarkan ratio. 62
19 Tingkatan level konsentrasi PAH di sedimen pada setiap stasiun. 62
20 Konsentrasi ∑PAH pada permukaan sedimen di beberapa wilayah dunia (dimodifikasi dari Mosatafa et al. 2009).
63
21 Konsentrasi ∑PAH pada air laut di beberapa wilayah dunia. 64
22 Status kontaminasi PAH pada ikan Nomei. 64
23 Konsentrasi ∑PAH beberapa jenis ikan di beberapa wilayah dunia. 65
24 Status kontaminasi PAH di sedimen terhadap organisme laut berdasarkan konsentrasi ERL dan ERM pada setiap stasiun.
67
25 Rangkuman sensitifitas sifat kronis pada organisme air tawar dan laut terhadap FLA (dimodifikasi dari EPA/600/R-02/013).
67
DAFTAR GAMBAR
Hal
1 Analisis PAH (∑PAH50) pada cuplikan minyak mentah (Boehm 2006). 6
2 Stuktur 16 jenis polutan utama PAH menurut United State Environmental Protection Agency (USEPA) (Amir et al. 2005).
7
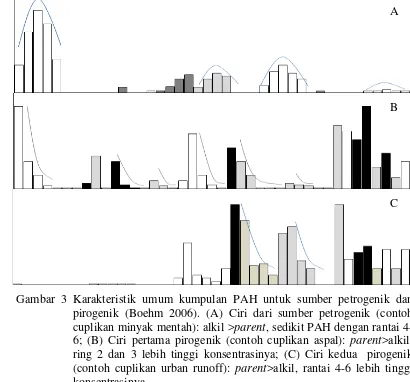
3 Karakteristik umum kumpulan PAH untuk sumber petrogenik dan pirogenik (Boehm 2006). (A) Ciri dari sumber petrogenik (contoh cuplikan minyak mentah): alkil >parent, sedikit PAH dengan rantai 4-6; (B) Ciri pertama pirogenik (contoh cuplikan aspal): parent>alkil, ring 2 dan 3 lebih tinggi konsentrasinya; (C) Ciri kedua pirogenik (contoh cuplikan urban runoff): parent>alkil, rantai 4-6 lebih tinggi konsentrasinya.
12
4 Kurva hubungan antara konsentrasi bahan toksik terhadap respon hewan
uji.
20
5 LC50 Menggambarkan nilai tengah respon dari populasi. 21
6 Proses mixed function oxidase (MFO) dalam metabolisme benzo[a]pirena. 23
7 Ikan Nomei (Horpodon nehereus) dengan nama lokal ikan Pepija atau Lembe-Lembe.
29
8 Persentasi jenis makanan yang ditemukan pada perut Horpodon nehereus
(Pillay 1953).
30
9 Histogram yang menunjukkan variasi bulanan volume beberapa jenis makanan yang dimakan ikan nomei berdasarkan perbedaan bulan (Pilay 1952). (a) Udang dan udang-udangan, (b) Ikan nomei, (c) Ikan yang lain, (d) Larva megalopa, (e) Bahan tumbuhan, (f) Detritus.
30
10 Peta lokasi pengambilan cuplikan. Cuplikan air dan sedimen (Stasiun 1, 2, dan 3), cuplikan ikan (Stasiun 2).
32
11 Histogram konsentrasi individu PAH (ug/l) dalam cuplikan air. 39
12 TIC (total ionic current) pada cuplikan air 1. ( [1] fluorantena), [O] series dari hidrokarbon alkana).
40
13 TIC (total ionic current) pada cuplikan air 2 yang tidak terdeteksi adanya PAH. ([O] series dari hidrokarbon alkana).
41
14 TIC (total ionic current) pada cuplikan air 3. ( [1] fluorantena, [2]
fenantrena (PHE), [O] series dari hidrokarbon alkana).
15 Histogram konsentrasi individu PAH (ng/g) dalam cuplikan sedimen. 44
16 TIC (total ionic current) pada cuplikan sedimen 1. [1]
1,3-dimetilnaftalena (1,3-D-NAP (NAP-C1)), [4] fenantrena (PHE), [5] 2-metil-fenantrena (2-M-PHE (PHE-C1)), [6] 4- 2-metil-fenantrena (4-M-PHE ((4-M-PHE-C1)).
45
17 TIC (total ionic current) pada cuplikan sedimen 2. [3] 1,6-dimetil-4-(1-metilethil)-naftalena (1,6-D-4-NAP (NAP-C1)), [4] fenantrena (PHE).
46
18 TIC (total ionic current) pada cuplikan sedimen 3. [1]
1,3-dimetilnaftalena (1,3-D-NAP (NAP-C1)), [2] 1,2,3,4-tetrahidro-1,6 dimetil-4-(1-metiletil)-(1S-cis) naftalena (1T-1D-4M-1S-NAP (NAP-C1)), [4] fenantrena (PHE), [7] 9-metil-fenantrena (9-M-PHE (PHE-(NAP-C1)), [8] 9-metil-antrasena (9-M-ANT (ANT-C1)), [9] fluorantena (FLA).
47
19 Diagram konsentrasi individu PAH (ng/g) dalam daging ikan Nomei. 48
20 TIC (total ionic current) pada cuplikan daging ikan Nomei kecil. [1] 1,3-dimetilnaftalena (1,3-D-NAP (NAP-C1)), [2] 1,6- 1,3-dimetilnaftalena (1,6-D-NAP (NAP-C1), [5] 4-metil-bifenil (4-M-BL (BPH), [10] antrasena (ANT), [11] 4-metilfenantrena (4-M-PHE (PHE-C1)), [13] fluorantena (FLA), [14] pirena (PYR).
49
21 TIC (total ionic current) pada cuplikan daging ikan Nomei sedang. [1]
1,3-dimetilnaftalena (1,3-D-NAP (NAP-C1)), [2] 1,6- dimetilnaftalena (1,6-D-NAP (NAP-C2), [4] 3-metilbifenil (3-M-BL (BPH)), [7] n-cycloheptyl-2,2-diphenylacetamid (N-C-2,2-D- asenaftena (ACE)), [9] fenantrena (PHE), [12] 9-metilantrasena (9-M-ANT (ANT-C1)), [13] fluorantena (FLA).
50
22 TIC (total ionic current) pada cuplikan daging ikan Nomei besar. [1] 1,3-dimetilnaftalena (1,3-D-NAP (NAP-C2)), [2] 1,6-1,3-dimetilnaftalena (1,6-D-NAP (NAP-C2)), [3] 1,7-dimetilnaftalena (1,7-(1,6-D-NAP (NAP-C2)), [4] 3-metilbifenil (3-M-BL (BPH)), [6] 1-allyl- naftalena (1-A-NAP (NAP-C1)), [8] fluorena (FLU), (9) fenantrena (PHE), [11] 4-metilfenantrena (4-M-PHE (PHE-C1)).
51
23 Diagram konsentrasi individu PAH (ng/g) dalam hati ikan Nomei. 52
24 TIC (total ionic current) pada cuplikan hati ikan Nomei kecil. [2] 1,3-dimetilnaftalena (1,3-D-NAP (NAP-C2)), [3] 1,4-1,3-dimetilnaftalena (1,4-D-NAP ((1,4-D-NAP-C2)), [4] 1,5-dimetilnaftalena (1,5-D-(1,4-D-NAP ((1,4-D-NAP-C2)), [7] 3-metilbifenil (3-M-BL (BPH)), [10] fenantrena (PHE), [11] fluorantena (FLA).
53
25 TIC (total ionic current) pada cuplikan hati ikan Nomei sedang. [2] 1,3-dimetilnaftalena (1,3-D-NAP (NAP-C2)), [3] 1,4-1,3-dimetilnaftalena (1,4-D-NAP ((1,4-D-NAP-C2)), [5] 1,7-dimetilnaftalena (1,7-D-(1,4-D-NAP ((1,4-D-NAP-C2)), [8] 1-allyl-naftalena (1-A-NAP (NAP-C1)), [10] fenantrena (PHE).
26 TIC (total ionic current) pada cuplikan hati ikan Nomei besar. [1] naftalena (NAP), [2] 1,3-dimetilnaftalena (1,3-D-NAP (NAP-C2)), [3] 1,4-dimetilnaftalena (1,4-D-NAP (NAP-C2)), [6] 2,6-dimetilnaftalena (2,6-D-NAP (NAP-C2)), [7] 3-metilbifenil (3-M-BL (BPH)), [9] diphenylmethan (D-MTH (BPH)), [10] fenantrena (PHE).
55
27 Perbedaan jenis dan konsentrasi PAH pada daging dan hati ikan Nomei kecil.
57
28 Perbedaan jenis dan konsentrasi PAH pada daging dan hati ikan Nomei sedang.
57
29 Perbedaan jenis dan konsentrasi PAH pada daging dan hati ikan Nomei besar.
58
30 Perbedaan senyawa dan konsentrasi PHE dan 1,3-D-NAP pada daging dan hati ikan Nomei berdasarkan ukuran.
58
31 Konsentrasi jumlah lipid berdasarkan ukuran tubuh ikan Nomei (A), total konsentrasi PAH dalam daging berdasarkan ukuran tubuh ikan Nomei (B).
59
32 Penentuan sumber pencemar PAH di air dan sedimen berdasarkan persentasi konsentrasi antara berat molekul rendah, berat molekul tinggi dan alkil PAH. Pada air sumber pencemar PAH berasal dari sumber petrogenik dan pirogenik dengan persentasi berat molekul rendah (sumber petrogenik) lebih besar. Pada sedimen sumber pencemar PAH juga berasal dari sumber petrogenik dan pirogenik, dengan persentasi jumlah alkil lebih besar dari parent (sumber petrogenik).
DAFTAR LAMPIRAN
Hal
1 Bagan alir ekstraksi PAH dalam air laut menurut Yu et al. 2009 yang telah dimodifikasi
79
2 Bagan alir ekstraksi PAH pada sedimen, daging dan hati ikan
Horpodon nehereus menurut Liu et al. 2007 yang telah dimodifikasi
80
3 Prosedur SEAMIC IMFJ (Southeast Asian Medical Information
Center International Medical Foundation of Japan) Tahun 1985
81
4 Spektrum fenantrena 82
5 Spektrum pirena 82
6 Spektrum 1,3-dimetilnaftalena 82
7 Spektrum 1,6 dimetilnaftalena 83
8 Spektrum 3-metilbifenil 83
9 Spektrum antrasena 83
10 Spektrum 4-metifenantrena 84
11 Spektrum 9-metilantrasena 84
12 Spektrum fluorantena 84
13 Spektrum 1,3-dimetilnaftalena 85
14 Spektrum 1,7 dimetilnaftalena 85
15 Spektrum 1,5-dimetilnaftalena 85
16 Spektrum 1,4-dimetilnaftalena 86
17 Spektrum 2,6-dimetilnaftalena 86
18 Spektrum 1,2,3,4-tetrahidro-1,6 dimetil -4-(1-metil etil)-(1S-cis) naftalena
86
19 Spektrum 9-metilantrasena 87
20 Spektrum 4-metilbipenil 87
22 Spektrum 2-metilfenantrena 88
23 Spektrum 1,6-dimetil -4-(1-metil etil)-naftalena 88
24 Spektrum naftalena 88
25 Spektrum difenilmethan 89
1
PENDAHULUAN
1.1Latar Belakang
Wilayah Kota Tarakan Propinsi Kalimantan Timur wilayahnya berupa pulau
dan saat ini mengalami perkembangan yang cukup signifikan, namun
kegiatan-kegiatan pembangunan yang berasal dari daratan tersebut berpotensi
mempengaruhi perairan di sekitarnya. Hal ini ditunjukkan berbagai material
daratan termasuk limbah yang masuk ke laut, dan diantaranya adalah limbah
berupa minyak yang mampu dialirkan dengan melalui ± 20 anak sungai.
Komponen minyak sebagai sumber pencemar antara lain berasal dari buangan
air balast, ceceran bahan bakar mesin-mesin kapal dan buangan oli bekas di
daratan. Salah satu bahan pencemar komponen minyak yang berbahaya adalah
polycyclic aromatic hydrocarbons (PAH). PAH terdiri dari 2 atau lebih rantai
karbon siklik yang memiliki stabilitas yang tinggi di lingkungan, mempunyai sifat
hidrophobik yang tinggi dan struktur kimia yang stabil, sifatnya tidak mudah larut
dan dapat dengan cepat terserap melalui partikel tanah, terutama pada
bahan-bahan organik (Tang et al. 2005).
Distribusi dan fate PAH sebagai kontaminan organik di sedimen pada
ekosistem perairan sangat perlu diperhatikan karena mempunyai efek mutagenik
dan karsinogenik. Konsentrasi PAH dalam tingkat tertentu di air laut dan sedimen
dapat bersifat toksik terhadap organisme laut bentik dan pelagik (Arias et al.
2009). Konsentrasi PAH di lingkungan 1-50 ppb dapat menyebabkan respon
subletal pada beberapa organisme yang sensitif (Neff 1979). Kandungan benzena
108 ppm, toulena 28 ppm, naftalena 3.8 ppm, dapat memberikan efek toksik pada
Cancer magister (Dungeness crab) (Caldwell et al. 1977). Efek toksik PAH
benzena 386 ppm dan toulena 1180 ppm juga berpengaruh pada Gambusia affinis
(Mosquito fish) serta pada Carassius auratus (goldfish) yaitu toluena 22.80 ppm,
xilin 16.94 ppm dan 1,3,5-trimetilbenzena 12.52 ppm (Brenniman et al. 1976).
Banyak kegiatan-kegiatan yang ada di Kota Tarakan berpotensi sebagai
sumber polutan PAH, diantaranya kegiatan-kegiatan eksplorasi dan eksploitasi
pesisir utara, selatan dan barat, pembuangan limbah-limbah oli dari usaha bengkel
yang banyak tersebar, lalu lintas aktivitas kapal serta kegiatan pembakaran
sampah dengan incenerator di TPAS (tempat pembuangan akhir sampah).
Penelitian tentang senyawa organik PAH sudah banyak dilakukan baik berupa
distribusi, karakteristik dan akumulasinya pada sedimen, air dan biota laut (Tabel
1). Di wilayah Indonesia informasi saat ini hanya sebatas pada perairan laut dalam
dan beberapa perairan seperti Teluk Jakarta, sehingga data tentang efek PAH di
Indonesia masih sangat sedikit.
1.2 Perumusan Masalah
Kegiataan pembangunan akhir-akhir ini meningkat dengan pesat terutama
infrastruktur, mulai dari pembukaan lahan untuk pemukiman, jalan dan industri
yang dibangun untuk meningkatkan kesejahteraan. Peningkatan pembangunan di
berbagai bidang khususnya industri dan perdagangan, penggunaan bahan
berbahaya dan beracun (B3) di dalam proses industri akan semakin meningkat.
Konsekuensinya limbah berbahaya dan beracun yang dikeluarkan oleh kegiatan
tersebut akan menimbulkan pencemaran lingkungan apabila tidak dikelola dengan
baik. Pencemaran lingkungan ini khususnya di perairan, tentunya akan berdampak
negatif terhadap lingkungan, biota dan manusia.
Salah satu yang akhir-akhir ini menjadi perhatian adalah pencemar PAH.
PAH masuk ke lingkungan khususnya di perairan laut melalui hujan, buangan
industri, tumpahan minyak dan aliran permukaan yang masuk melalui sungai.
Senyawa ini terutama keberadaannya di lingkungan menjadi penting karena
sifatnya yang/dapat bersifat karsinogenik dan mutagenik. Informasi mengenai
keberadaan, jenis, konsentrasi dan akumulasinya terutama pada biota di
lingkungan perairan laut khususnya di Kota Tarakan tidak tersedia.
1.3 Tujuan dan Manfaat Penelitian
Tujuan utama penelitian ini menentukan jenis PAH dan konsentrasinya yang
ada di air laut, sedimen dan tingkat akumulasinya pada tubuh ikan Nomei.
Manfaat dari penelitian ini adalah mengetahui sumber potensi pencemar dan
Tabel 1 Penelitan PAH terkait dengan distribusi, karakteristik dan akumulasinya pada beberapa biota perairan di beberapa wilayah dunia.
Uraian Jenis cuplikan Lokasi Referensi
Sumber pencemar
Sedimen pesisir Cotonou (Benin) dan Aquitaine
Air Pantai Alexandria,
Mesir
Crustacea (Nephrops norvegicus)
Ikan (Mullus barbatus, Scomber scombrus, Micromesistius poutassou,
Merluccius merluccius)
Laut Adriatic, Italia Perugini et al. 2007
Air, remis (Brachidontes
sp, Tagelus sp), ikan
Sedimen Daerah pesisir
Hadhramout, Teluk Aden, Yaman
Mostafa et al. 2009
Konsentrasi Air laut, suspended particulate matter (SPM), permukaan sedimen dan
2
TINJAUAN PUSTAKA
2.1Minyak Bumi
Minyak bumi adalah suatu campuran komplek yang sebagian besar
komponen dan hidrokarbon mengandung karbon dan hidrogen serta sejumlah
kecil unsur-unsur yaitu nitrogen, sulfat, oksigen termasuk unsur-unsur logam
seperti vanadium, ferrum dan nikel (Sanusi dan Sugeng 2009). Berdasarkan
perbedaan hidrokarbon yang terkandung di dalamnya, baik perbedaan jenis,
struktur maupun komposisi campurannya, minyak bumi dibedakan dalam 3 jenis
yaitu minyak bumi parafinik (alkana), minyak bumi aspaltik
(naftenik/sikloparafin/sikloalkana) dan minyak bumi campuran (Sanusi dan
Sugeng 2009).
Minyak mentah mengandung senyawa hidrokarbon sekitar 50-98%. Minyak
berdasarkan kelarutannya dalam pelarut organik dapat dibedakan : 1) Hidrokarbon
jenuh yaitu alkana dengan struktur CnH2n+2 (alifatik) dan CnH2n (alisiklik)
dengan n<40. Hidrokarbon jenuh paling banyak terkandung dalam minyak
mentah. 2) Hidrokarbon aromatik, yaitu kelas monosiklik aromatik BTEX
(benzena, toluena, etilbenzena, xilen) dan PAH ( naftalena, antrasena, fenantrena).
PAH bersifat karsinogenik atau dapat ditransformasi oleh mikroba menjadi
senyawa karsinogen, sehingga menjadi senyawa penting dalam menjaga kualitas
lingkungan; 3) Resin, yaitu senyawa polar mengandung nitrogen, sulfur, oksigen
(piridin dan thiopen), sehingga disebut juga senyawa NSO; 4) Aspalth, yaitu
senyawa dengan berat molekul besar dan mengandung logam berat nikel,
vanadium dan besi. Namun variasi minyak mentah berbeda di berbagai tempat
(Mangkoedihardjo 2005).
2.2Karakteristik PAH
PAH adalah kelompok pencemar organik persisten (POP) khas yang terdiri
dari ratusan kandungan individual. Komponen ini terdiri dari 2 atau lebih rantai
benzena yang terdiri dari atom hidrogen dan karbon (Douben 2006). Secara umum
forensic investigations. Namun hanya 16 senyawa yang menurut USEPA (united
states environmental protection agency) sangat berbahaya keberadaannya di
lingkungan (Tabel 2). Beberapa senyawa tersebut adalah PAH yang tidak
tersubstitusi (parent) dan non-alkil (Gambar 1dan 2)
Tabel 2 Jenis PAH yang biasa digunakan dalam studi environmental forensic investigations (∑PAH50) dengan 16 jenis PAH sebagai polutan prioritas menurut USEPA (∑PAH16) (Boehm 2006).
Jenis PAH Singkatan Jenis PAH Singkatan
Naftalena* NAP Pirena* PYR
C1-naftalena NAP-C1 C1-Fluorantena/pirena FLA/PYR-C1 C2-naftalena NAP-C2 C2-Fluorantena/pirena FLA/PYR-C2 C3-naftalena NAP-C3 C3-Fluorantena/pirena FLA/PYR-C3
C4-naftalena NAP-C4 Benz(a)antrasena* BaA
Bifenil BPH Krisena* CHR
Asenaftilena* ACL C1-krisena CHR-C1
Asenaftena* ACE C2-krisena CHR-C2
Dibenzofuran DBF C3-krisena CHR-C3
Fluorena* FLU C4-krisena CHR-C4
C1-Fluorena FLU-C1 Benzo(a)Fluorantena BaF C2-Fluorena FLU-C2 Benzo(b)Fluorantena* BbF C3-Fluorena FLU-C3 Benzo(j,k)Fluorantena* BkF
Antrasena* ANT Benzo(e)pirena BeP
Fenantrena* PHE Benzo(a)pirena* BaP
C1-fenantrena/antrasena PHE-C1 Perylene Per C2-fenantrena/antrasena PHE-C2 Indeno(1,2,3-c,d)pirena* ID-PYR C3-fenantrena/antrasena PHE-C3 Dibenzo(a,h)antrasena* DaA C4-fenantrena/antrasena PHE-C4 Benzo(g,h,i)perylene* BgP
Dibenzotiofena DBT Dibenzo(a,e)pirena DeP
C1- dibenzotiofena DBT-C1 Dibenzo(a,h)pirena DhP C2- dibenzotiofena DBT-C2 Dibenzo(a,1)pirena D1P C3- dibenzotiofena DBT-C3 Dibenzo(a,i)pirena DiP C4- dibenzotiofena DBT-C4 Dibenzo(a,e)Fluorantena DeF
Fluorantena* FLA Anthanthren ANTr
Gambar 1 Analisis PAH (∑PAH50) pada cuplikan minyak mentah (Boehm 2006). Ket : (*) ∑PAH16 polutan utama menurut USEPA
PAH dihasilkan dari proses alami dan proses antropogenik. Menurut Boehm
(2006) PAH secara umum dihasilkan melalui 4 proses :
1. Lambat, perubahan suhu rendah (<70o
2. Relatif cepat (hari-tahun), perubahan yang panjang, temperatur sedang
(100-300
C)/diagenesis dari partikel organik
sebagai bagian dari perubahan yang dijalani oleh biomolekul dan
hubungan organik setelah pertama kali terdeposit di sedimen;
o
3. Cepat, temperatur tinggi (>500
C) membentuk minyak fosil yaitu petroleum dan batu bara
(contoh dari petrogenik);
o
4. Biosintesis oleh tumbuhan dan binatang dari komponen PAH individu atau
gabungan yang relatif sederhana.
C), pembakaran yang tidak sempurna/tidak
efisien (contohnya oksigen yang sedikit) dari biomasa bahan organik
(pirolisis) seperti kebakaran hutan dan rumput serta kegiatan antropogenik
Gambar 2 Stuktur 16 jenis polutan utama PAH menurut United State Environmental Protection Agency (USEPA) (Amir et al. 2005).
PAH bersifat hidrofobik (log KOW
Secara umum kelarutan PAH bervariasi, yaitu tingkat kelarutan rendah ke
sangat rendah dan tingkat kelarutan rendah ke moderat. Daya larut PAH bervariasi
berdasarkan kondisi media, 1-2 bulan di lingkungan perairan, 2 bulan sampai 2
tahun di tanah, dan 8 bulan sampai 6 tahun di sedimen. Log n-octanol/water
partition coefficients (log K
3–8) dengan daya larut yang sangat
rendah, sehingga konsentrasi PAH di lingkungan perairan sangat rendah (Nemr
dan Aly 2003). Selain bersifat hidrofobik, PAH memiliki struktur stabil, sehingga
PAH tidak mudah larut dan dapat diabsorsi dengan cepat ke dalam tanah termasuk
di lingkungan perairan seperti sedimen (Tang et al. 2005).
OWS) dari PAH meningkat dengan peningkatan massa
molekul dengan kisaran kira-kira 3.0-7.0, mengindikasikan sifat hidropobik tinggi
untuk PAH dengan berat molekul tinggi (Kalf et al. 1996).
1. naftalen 5. fenantrena 9. benzo(a)antrasena 3. benzo(a)piren
2. asenaftilen 6. antrasena 10. krisenae 14. dibenzo(a,h)antrasena
3. asenaftena 7. fluorantena 11. benzo(b)fluoranten 15. dibenzo(g,h,i)piren
Antrasena, fluorena dan fenantrena adalah senyawa PAH yang memiliki 2
rantai benzena yang dikelompokkan dalam PAH dengan berat molekul rendah
(BMR). Fluorantena memiliki 4 rantai benzena yang digolongkan pada PAH
dengan berat molekul tinggi (BMT) (Tabel 3). Semakin besar berat molekulnya
maka semakin persisten keberadaannya di lingkungan.
Tabel 3 Pengelompokan PAH berdasarkan berat molekul dan jumlah ring (USEPA).
Berat molekul rendah (BMR; <202) Berat molekul tinggi (BMT; >202)
2-ring 3-ring 4-ring 5-ring
Fenantrena dan fluorena memiliki sifat karsinogenik. Antrasena tidak
bersifat karsinogenik namun sangat fototoksik (peningkatan sifat toksik ketika
terkena cahaya, khususnya sinar UV) sehingga dapat berubah menjadi
karsinogenik. Fluorantena adalah PAH tidak bersifat toksik namun berpotensi
menjadi karsinogenik. Fluorena bukan PAH yang bersifat phototoksik. Antrasena,
fluorantena dan fenantrena sering digunakan dalam menduga sumber dari PAH
(Irwin 1997). Fenantrena lebih stabil dari pada antrasena. Ketika temperatur
rendah fenantrena memproduksi fraksi molal lebih banyak dari pada antrasena
(Tang et al. 2005).
2.3PAH di Lingkungan Perairan
PAH masuk ke lingkungan secara umum melalui tiga proses; (1)
pembakaran bahan organik pada saat suhu sangat tinggi; (2) tumpahan minyak;
(3) proses diagenesis (perubahan bahan organic sedimen secara fisik, kimia dan
biologi) (Neff 1979). Pergerakan PAH di lingkungan tergantung pada propertinya
seperti mudahnya PAH larut di air dan mudahnya PAH menguap ke atmosfir.
air atau terperangkap pada partikel kecil. PAH dapat berpindah dengan jarak yang
jauh sebelum mereka kembali ke bumi melalui hujan atau partikel yang
tersuspensi (Irwin 1997).
Nilai KOC mengindikasikan besarnya potensi terikat pada organik karbon di
tanah dan sedimen secara kimia (Tabel 4). PAH dengan berat molekul rendah
mempunyai kisaran nilai dari 3-4 yang mengindikasikan potensi moderate
terserap pada karbon organik di tanah dan sedimen. Potensi medium nilai KOC
adalah 4. PAH dengan berat molekul tinggi mempunyai nilai KOC berkisar antara
5-6, mengindikasikan kecenderungan yang kuat terserap pada karbon organik.
Penyerapan PAH di tanah dan sedimen meningkat dengan meningkatnya
kandungan orgnik karbon dan juga tergantung pada ukuran partikel (Irwin1997).
Tabel 4 Besaran potensi 16 bahan pencemar PAH terikat pada sedimen (KOC) dan air (KOW).
: Octanol: water partition coefficients
OC
Kegiatan antropogenik adalah sumber utama dari PAH, besaran PAH di
al. 2005). PAH terbentuk selama proses pirolisis pada semua bahan organik dan
bahan kontaminan organik yang tersebar di sedimen perairan. PAH di permukaan
tanah dapat disebarkan oleh aliran air permukaan dan debu. Permukaan tanah
adalah salah satu sumber dari kontaminasi PAH yang berada di udara dan
sedimen. Bentuk tanah dan strukturnya seperti organik karbon memainkan fungsi
penting ketika PAH terabsorpsi di tanah (Tang et al. 2005).
Partisi dari bahan kontaminan yang hidropobik, yaitu yang tersuspensi dan
terlarut mengontrol fate PAH di lingkungan dan bioaviability pada organisme
akuatik. Konsentrasi PAH di air dapat dipengaruhi oleh durasi dari jumlah partikel
PAH yang terabsorbsi. Kandungan karbon organik di air dan sedimen memainkan
peran penting dalam distribusi PAH (Menon dan Menon 1999). PAH dengan berat
molekul rendah dapat hilang dengan cepat di sedimen, sedangkan PAH dengan
berat molekul tinggi lebih persisten (Wilcock et al.1996, diacu dalam Amir et al.
2005). Fate dari sedimen dan air yang terkontaminasi oleh PAH, konsentrasinya
akan berkurang seiring dengan waktu. Hal ini disebabkan oleh adanya
biodegradasi oleh bakteri atau mikroorganisme.
Biodegradasi PAH berhubungan dengan berat molekul. Rantai 2 dan 3 dari
PAH (naftalena, fluorena dan fenantrena) dengan cepat terdegradasi. PAH dengan
4 rantai (fluorantena, pirena, benz(a)antrasena dan krisena) umumnya terdegradasi
50% dalam beberapa bulan. PAH dengan rantai 5 (benzo(b)fluorantena dan
benzo(a)pirena) berkurang lambat selama beberapa tahun (Irwin1997).
Sedimen di rawa manggrove yang terkontaminasi PAH dari 2135 ng/g
menjadi 1196 ng/g (120 hari) (Ke et al. 2002). PAH dari tumpahan minyak
memiliki reaktivitas yang terjadi dari komponen minyak selama biodegradasi
yaitu: n-alkana (berat molekul rendah) > fenantrena > 3-2-metilfenantrena> n
-alkana dengan panjang rantai intermediate > n--alkana dengan rantai lebih
panjang > isoprenoids 9-1-metilfenantrena (Juan et al. 1996).
2.4Sumber PAH
PAH masuk ke dalam air melalui berbagai sumber yang dengan cepat
diabsorpsi oleh partikel organik dan anorganik. Level PAH yang terakumulasi
melalui beberapa kegiatan seperti fotooksidasi, oksidasi kimia, metabolisme
mikroba dan metabolisme oleh metazoan yang lebih tinggi. Konsentrasi relatif
dari PAH pada ekosistem perairan secara umum adalah lebih tinggi pada sedimen,
intermediate di biota akuatik, dan rendah di kolom perairan (Neff 1979).
Secara umum sumber PAH yang masuk ke lingkungan perairan dapat
dibedakan berdasarkan 2 sumber :
a. Pirogenik. PAH yang terbentuk karena peningkatan suhu secara alami dan
proses antropogenik. Selama proses peningkatan suhu, bahan organik
tersebut lolos dari pembakaran sempurna (oksidasi menjadi karbon
dioksida dan air). PAH pirogenik terbentuk selama pembakaran
menggunakan kayu (kompor), dan pembakaran dari bahan bakar fosil
(bensin, solar, oli mesin).
b. Petrogenik. Minyak dan batu bara yang ada di dalam stuktur geologi dan
terbentuk pada waktu yang lama menghasilkan PAH petrogenik. Batu bara
terbentuk dari sisa-sisa tumbuhan yang terakumulasi. Selama terkubur
jutaan tahun, bahan ini berubah menjadi batu bara, membentuk senyawa
aromatik dengan struktur 3 dimensi. Jumlah rantai aromatik yang
terbentuk per unit struktur batu bara bervariasi. Sebagian besar batu bara
terdiri dari 3-5 rantai per unit struktur, dengan beberapa unit dapat
mencapai 10 rantai aromatik.
PAH petrogenik secara umum dicirikan dengan alkil PAH lebih banyak
daripada non-alkil dari PAH utama dan sebaliknya merupakan sumber pirogenik.
Selain itu sumber dari petrogenik lebih banyak PAH dengan rantai 2 dan 3, dan
sumber dari pirogenik lebih banyak PAH dari rantai 4-6 (Gambar 3). PAH dengan
jumlah rantai karbon 4-6 merupakan berat molekul tinggi >202 seperti naftalena,
fluorantena dan pirena biasanya terdeteksi sebagai sumber pirogenik seperti dari
pembakaran batu bara, kayu, dan bahan bakar kendaraan. PAH dengan berat
molekul rendah <202 yaitu PAH dengan jumlah rantai karbon
2-3/alkil-susbstituted PAH berasal dari sumber petrogenik seperti 2-metilnaftalena,
asenaftena, fenantrena dan fluorena (Arias et al. 2009). PAH seperti fenantrena
berasal dari sumber petrogenik dan pirogenik (mixed sources) (Boehm 2006).
A
B
C proses pirolitik lebih sering berasosiasi dengan sedimen dan sebagian besar
resistan terhadap degradasi oleh mikroba dibandingkan dengan PAH yang berasal
dari petrogenik (Mostafa et al. 2009).
Gambar 3 Karakteristik umum kumpulan PAH untuk sumber petrogenik dan pirogenik (Boehm 2006). (A) Ciri dari sumber petrogenik (contoh cuplikan minyak mentah): alkil >parent, sedikit PAH dengan rantai 4-6; (B) Ciri pertama pirogenik (contoh cuplikan aspal): parent>alkil, ring 2 dan 3 lebih tinggi konsentrasinya; (C) Ciri kedua pirogenik (contoh cuplikan urban runoff): parent>alkil, rantai 4-6 lebih tinggi konsentrasinya.
2.5Konsentrasi PAH
Secara global, konsentrasi PAH baik di sedimen, air dan biota telah banyak
diteliti. Distribusi PAH di lingkungan sebagian besar dipengaruhi oleh sifat
solibilitas dan hidropobik, yang membuat PAH dapat dengan mudah ditemukan di
sedimen. PAH di sedimen telah diketahui nilainya dari banyak bagian di dunia
(Tabel 5). Konsentrasi total PAH di perairan laut adalah kecil (Tabel 6). Batasan
konsentrasi sangat besar walaupun relatif berada dalam satu kawasan, sehingga
Tabel 5 Total konsentrasi PAH pada sedimen laut pada beberapa wilayah Amerika Utara, Eropa, Afrika dan Asia (dimodifikasi dari Latimer dan Jinshu 2003).
Lokasi Konsentrasi (ng/gDw)
Amerika utara
Seluruh pantai amerika 13.4-40 453
Seluruh pantai amerika 4.87-30 674
Pelabuhan New Bedford, MA 14 000-170 000
Selat Pales verdes, CA, USA 1 252-7 037
Teluk Naragansett, RI 100-29 300
Teluk Alaska (sebelum kasus Exxon Valdez) 1 096 Daerah estuari Carolina utara 33-9 630
Stasiun Alaska 2.17-733
Daerah barat laut Beaufort (sedimen Polar Star) 159-1 092
Daerah estuari Fraser (BC, Canada) 180-620 (pembakaran) 220-660 (petroleum) Pintu masuk Burrard (BC, Canada) 430-91 800 (pembakaran)
70-39 500 (petroleum) Selat Georgia (BC, Canada) 300-8 470 (pembakaran)
560-4 300 (petroleum) Teluk San Francisco embayments (1800an-1999) 40-6 300 (pirogenik) Eropa
Teluk Bay (wilayah tengah Mediterania) 86.5-48 060 Bagian selatan Laut Mediterania 20-18 700 Dekat daerah pantai Spanyol dan Perancis (Laut
Mediterania)
0.32-8 400
Laut Baltic 3.16-30 100
Wilayah Estuari Gironde (Perancis) 3.5-853
Teluk Arcachon (Perancis) 293
Laut Cretan (wilayah timur Mediterania 14.6-158.5 (73% pembakaran)
Wilayah Estuari Irish 83-22 960
Afrika
Pantai Cotonou (Benin) 80-1411
Asia
Laut Kuning 20-5 734
Teluk Kyeonggi (Korea) 9.1-1 400
Hong Kong (permukaan) 7.25-4 420
Laut Putih (Rusia, Laut Artic) 13-208
Laut Cina Selatan 24.7-275.4
Daerah estuari Sungai Yangtze (core) 122-11 740
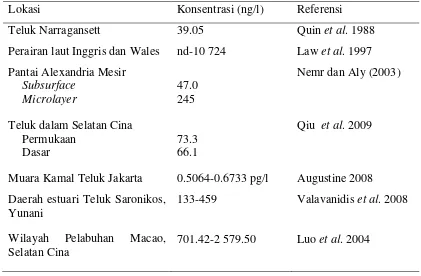
Tabel 6 Konsentrasi PAH di perairan laut beberapa wilayah dunia.
Lokasi Konsentrasi (ng/l) Referensi
Teluk Narragansett 39.05 Quin et al. 1988
Perairan laut Inggris dan Wales nd-10 724 Law et al. 1997
Pantai Alexandria Mesir Nemr dan Aly (2003)
Subsurface 47.0
Microlayer 245
Teluk dalam Selatan Cina Qiu et al. 2009
Permukaan 73.3
Dasar 66.1
Muara Kamal Teluk Jakarta 0.5064-0.6733 pg/l Augustine 2008
Daerah estuari Teluk Saronikos, Yunani
133-459 Valavanidis et al. 2008
Wilayah Pelabuhan Macao, Selatan Cina
701.42-2 579.50 Luo et al. 2004
Secara umum berdasarkan lokasi, terdapat perbedaan konsentrasi PAH yaitu
konsentrasi pada daerah lepas pantai adalah kecil, diikuti oleh daerah dekat pantai
dan terakhir pada lapisan mikro permukaan laut/surface micro layer (SSM).
Akumulasi PAH dari lingkungan juga terjadi pada organisme laut. Namun nilai
konsentrasi yang besar dari jaringan di tubuh organisme, diperoleh dari variasi
konsentrasinya di alam, lamanya terekspose, dan kemampuan spesies dalam
memetabolisme senyawa tersebut.
Pada biota invertebrata, konsentrasi tertinggi dapat ditemukan pada organ
dalam seperti hepatopankreas, dan di jaringan yang terikut dalam siklus umum,
hal ini mungkin berhubungan dengan variasi kandungan lipid, siklus bertelur, atau
flux lingkungan (Jovanovich dan Marion 1987; Maruya et al. 1997; Miles dan
Roster 1999 diacu dalam Latimer dan Jinshu 2003). Konsentrasi PAH pada
bivalva dan inveterbrata laut dari berbagai wilayah di dunia di tunjukkan pada
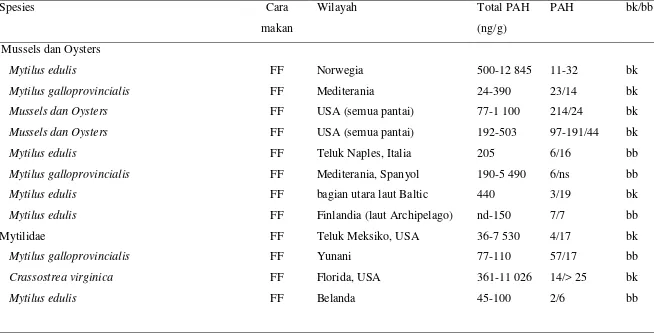
Tabel 7 Konsentrasi PAH dari beberapa biota bivalva laut dan invertebrata (di modifikasi dari Meador 2006).
Spesies Cara
makan
Wilayah Total PAH
(ng/g)
PAH bk/bb
Mussels dan Oysters
Mytilus edulis FF Norwegia 500-12 845 11-32 bk
Mytilus galloprovincialis FF Mediterania 24-390 23/14 bk
Mussels dan Oysters FF USA (semua pantai) 77-1 100 214/24 bk
Mussels dan Oysters FF USA (semua pantai) 192-503 97-191/44 bk
Mytilus edulis FF Teluk Naples, Italia 205 6/16 bb
Mytilus galloprovincialis FF Mediterania, Spanyol 190-5 490 6/ns bb
Mytilus edulis FF bagian utara laut Baltic 440 3/19 bk
Mytilus edulis FF Finlandia (laut Archipelago) nd-150 7/7 bb
Mytilidae FF Teluk Meksiko, USA 36-7 530 4/17 bk
Mytilus galloprovincialis FF Yunani 77-110 57/17 bb
Crassostrea virginica FF Florida, USA 361-11 026 14/> 25 bk
Tabel 7 (lanjutan)
M. edulis, M. galloprovincialis dan C. Gigas FF Perancis tt-300 000 110/td bk
Mytilus edulis FF Skotlandia 54-2 803 27/10 bb
Mytilus edulis FF Puget Sound, WA 40.63-600 9/24 bk
Mytilus spp FF Teluk San Francisco 180-4 100 6/34 bk
Benthik invertebrata
Macoma balthica DF/FF Scheldt, Belanda 947 (449) 2/12 bk
Crangon crangon Scav Scheldt, Belanda 410 (285) 2/12 bk
Nereis diversicolor Omn Scheldt, Belanda 785 (409) 2/12 bk
Homarus americanus Scav Nova Scotia, Kanada 235-73 000 1/10 bb
Littorina littorea Herb Bagian Selatan Norwegia 595-1 430 4/27 bk
Patella vulgata Herb Bagian Selatan Norwegia 674-15 462 2/31 bk
Asterias rubens Pred Bagian Selatan Norwegia 325-458 2/19 bk
Macropipus tubrculatus Omn spanyol 60-930 6/td bb
(tt) tidak terdeteksi; (td) tidak dilaporkan; (bk) berat kering; (bb) berat basah
Ikan mengakumulasi bahan kontaminan khususnya PAH melalui kulit, tapi
sebagian besar melalui insang (Irwin 1997). Secara umum, meskipun antara PAH
dengan berat molekul rendah dan berat molekul tinggi terserap relatif cepat pada
spesies perairan seperti ikan, metabolisme dan depurasinya juga cepat. PAH dapat
masuk ke semua jaringan tubuh yang terdapat lemak. Biasanya terserap di ginjal,
hati dan lemak. Jumlah yang kecil tersimpan pada limpa, kelenjar ginjal dan
indung telur.
2.6PAH Sebagai Indikator Sumber Pencemar
Senyawa PAH dapat digunakan sebagai salah satu indikator status
lingkungan. Distribusi dan fate dari PAH sebagai bahan kontaminasi organik di
sedimen ekosistem perairan sangat perlu diperhatikan karena mempunyai efek
mutagenik dan karsinogenik. Konsentrasi PAH dalam tingkat tertentu di air laut
dan sedimen dapat bersifat toksik terhadap organisme laut bentik dan pelagik,
sehingga keberadaannya perlu diperhatikan.
Sifatnya yang tidak mudah larut, dapat menghilang dengan cepat di
perairan, mampu meningkatkan konsentrasi dan berat molekulnya sendiri, mudah
terakumulasi dan terabsorpsi pada biota dan sedimen, menunjukkan perlunya
perhatian khususnya pada lingkungan perairan pesisir. Pendugaan sumber PAH
dilakukan dengan menggunakan rasio dari beberapa individu PAH (Tabel 8).
Tabel 8 Rasio individu PAH sebagai penduga sumber.
Diagnostik ratio Pirolitik Petrogenik
BMR/BMT Low high
∑MP/PHE <1 >1
FLA(FLA+PYR) >0.5 <0.5
Double ratio PHE/ANT, FLA/ANT dan
PHE/ANT, FLA/PYR
<10 / >1 >15 / <1
BMR : berat molekul rendah; BMT : berat molekul tinggi; MP : metilfenantrena; PHE : fenantrena; FLA : fluorantena; PYR : pirena; ANT : antrasena
Rasio dari FLA/PYR dapat mengindikasikan asal sumber dari PAH. Sumber
sumber pirolitik (Sicre et al. 1987, diacu dalam Ke et al. 2002). Menentukan
sumber pencemar PAH dalam air dapat menggunakan rasio FLA/(FLA+PYR).
Jika rasionya adalah 1, dapat diduga sumber pencemar berasal dari petrogenik.
Rasio FLA/(FLA+PYR) <0.40 mengindikasikan sumber pencemar PAH berasal
dari sumber petroleum (oli, mesin diesel, batu bara, dsb), rasio antara 0.4-0.5
mengindikasikan sumber dari pembakaran bahan bakar fosil (kendaraan dan
minyak mentah) dan rasio >0.5 berasal dari pembakaran rumput,
kayu/pembakaran batu bara (Zhang et al. 2006; Arias et al. 2009).
Sumber dari PAH dari sedimen dapat diperoleh berdasarkan rasio total
antara isomer metilfenantrena terhadap fenantrena (MP/P). Rasio MP/P <1
menunjukkan sumber dari pirogenik dan MP/P >1 menunjukkan sumber dari
petrogenik (Blumer dan Youngblood 1975, diacu dalam Yim et al. 2007;
Boonyatumanond et al. 2006).
Pendugaan sumber PAH pada biota dapat menggunakan rasio fenantrena,
ANT, fluorantena dan pirena yaitu rasio antara PHE/ANT, FLA/ANT dan
FLA/PYR. Rasio PHE/ANT <10 dan FLA/PYR >1, mencirikan sumber pirogenik
dan rasio PHE/ANT >15 dan FLA/PYR <1 mencirikan sumber petrogenik
(Steinhauer dan Boehm 1992; Budzinski et al. 1997; Baumard et al. 1998, diacu
dalam Yim et al. 2007). Fluorantena dan pirena adalah penanda khusus untuk
sumber pirolisis/pembakaran yang tidak sempurna. Di lain pihak pada emisi hasil
pembakaran bahan bakar sepert mesin diesel, profilnya predominan oleh
fenantrena, fluorantena dan pirena (Li et al. 2003; Wang et al. 2009, diacu dalam
Arias et al. 2009).
Beberapa PAH seperti fenantrena berasal dari sumber petrogenik dan
pirogenik (mixed sources) (Irwin 1997). Rasio jumlah berat molekul rendah
(BMR) dengan berat molekul tinggi (BMT) adalah bila nilainya kecil
menggambarkan sumber dari pirolitik dan bila nilainya besar bersumber dari
petrogenik (Budzinski et al. 1997, Sicre et al. 1987, Mostafa et al. 2009). Sumber
petrogenik secara umum alkil PAH lebih banyak dari pada non alkil dari PAH
utama dan sebaliknya merupakan sumber petrogenik.
Sumber dari petroleum biasanya berupa krisena, fluorena, naftalena,
naftalena, benzo(a)pirena, fluorena dan fenantrena. Petroleum lebih besar
menyumbang PAH jenis berat molekul rendah seperti naftalena, asenaftena dan
fluorin, dan juga alkil PAH seperti metilnaftalen. Pembakaran (pirolitik)
menyumbang PAH jenis berat molekul tinggi lebih besar seperti fenantrena,
fluorantena, pirena dan benzo(a)pirena, juga termasuk sedikit PAH jenis berat
molekul rendah seperti naftalena (Irwin 1997).
2.7Toksisitas
2.7.1 Uji toksisitas (Bioassay)
Semua bahan atau senyawa kimia yang terbuang diduga sebagai bahan
pencemar beracun (Poisonous pollutant), kecuali apabila terbukti melalui uji
biologis (bioassay/toxicity test) senyawa atau bahan tersebut tidak meracuni
organisme yang hidup di dalamnya beserta penghuninya (hewan dan manusia)
khususnya PAH. Toksisitas suatu senyawa dapat digolongkan berdasarkan efek
yang terjadi pada konsentrasi tertentu, yaitu : 1) Letal, langsung menyebabkan
kematian atau cukup mematikan. 2) Sub-letal, diatas kadar yang langsung
menyebabkan kematian. 3) Akut, dimana menimbulkan suatu rangsangan syaraf
yang cukup hebat sehingga menghasilkan respon yang cepat (untuk ikan biasanya
dalam waktu 4 hari). 4) Sub-akut, menimbulkan respon setelah waktu yang lama
dan mungkin menjadi menahun/kronik. 5) Kronik, menimbulkan rangsangan yang
lambat atau menerus dalam selang waktu yang lama, dan 6) Kumulatif yaitu
peningkatan kadar pada waktu yang lama.
Pengaruh bahan toksik terhadap suatu organisme dapat di amati berdasarkan
beberapa kondisi hidupnya yaitu; 1) siklus hidup (life cycle) hewan uji yaitu
pengamatan yang dilakukan mulai dari fase larva sampai hewan tersebut mati. 2)
Sebagian dari siklus hidupnya (partial life cycle), pengamatan yang dilakukan
pada fase larva sampai dewasa, dan 3) Awal siklus hidup (early life cycle),
pengamatan hanya pada fase larva.
Uji toksisitas secara kuantitatif dapat ditinjau dari lamanya waktu, yang
dapat diklasifikasikan menjadi toksisitas letal, sub-letal, kronis. Toksisitas akut
adalah efek total yang didapat pada dosis tunggal/banyak dalam 24 jam
reversibel. Toksisitas kronis sifatnya permanen, lama, konstan, kontinyu,
irreversible. Uji toksisitas atas dasar dosis dan waktu berarti spesifik toksisitas
akut/kronis. Dosis adalah jumlah racun yang masuk ke dalam tubuh, besar,
kecilnya menentukan efek. Sedangkan efek dosis ini merupakan fungsi dari usia,
jenis kelamin, berat badan, cara masuk ke tubuh, frekuensi, interval waktu,
kecepatan eksresi, kombinasi dengan zat lain. Uji toksisitas letal biasanya
dijalankan dalam jangka waktu 24, 48, 72 dan 96 jam.
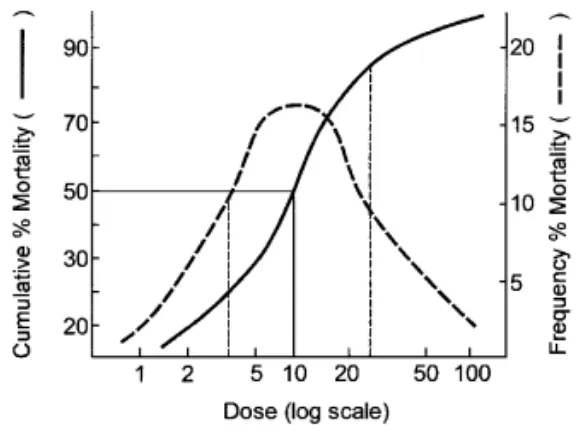
LD yaitu dosis yang menyebabkan kematian. Semakin tinggi konsentrasi
semakin tinggi tingkat kematiannya (Gambar 4). LD50 atau LC50 (konsentrasi letal
50%) atau TLm (toleransi limit median) atau TL50 (toleransi limit 50%) yaitu dosis
yang menyebabkan kematian 50% hewan uji dalam waktu uji (inkubasi) 12, 24,
48, 72, dan 96 jam. Menurut Wrigh dan Pamela (2002) LC50 adalah konsentrasi
bahan toksik yang menyebabkan kematian 50% (nilai tengah respon) dari
hewan/populasi tes pada waktu tertentu (Gambar 5). Ketika konsentrasi letal
median (LC50) dihitung, keyakinan 95% limit yang terkait dengan nilai (DO, pH,
Suhu) juga dilaporkan (Zakrzewski 2002).
Gambar 4 Kurva hubungan antara konsentrasi bahan toksik terhadap respon hewan uji
EC (konsentrasi efektif) yaitu konsentrasi bahan uji yang mengakibatkan
suatu tingkah laku atau respon hewan uji yang tidak normal. Angka indeks
yang terjadi selama waktu uji (EC50 – 48 Jam) (Sanusi dan Sugeng 2009).
Menurut Philp (2001) EC50 adalah dosis efektif yang menyebabkan 50%
perubahan efek maksimum dari hewan uji.
Gambar 5 LC50 Menggambarkan nilai tengah respon dari populasi.
Selain hal tersebut diatas juga digunakan evaluasi seperti NOEC (No
Observed Effect Concentration) yaitu konsentrasi tertinggi yang tidak
berpengaruh secara signifikan terhadap hewan uji dari control. LOEC (lowest
observed effect concentrations) yaitu konsentrasi terendah yang secara signifikan
berpengaruh terhadap ketahanan, pertumbuhan/reproduksi dari hewan uji terhadap
kontrol (Wrigh dan Pamela 2002), untuk mengevaluasi tingkat bahan toksik
khususnya PAH.
2.7.2 Toksisitas PAH
Material organik di perairan alami mempunyai efek yang kuat pada
ketersediaan pencemar organik. Ketersediaan dari beberapa pencemar organik
meningkat dengan peningkatan konsentrasi materi organik yang terlarut di air
(Kukkonen 1991 diacu dalam Tuvikene 1995). Toksisitas adalah senyawa yang
dapat bersifat racun yang dapat membahayakan makhluk dan lingkungan
disekitarnya pada konsentrasi tertentu. PAH termasuk senyawa organik yang
adalah karakteristiknya, kadar PAH, jenis biota laut, aktivitas mikroba dan lama
pemaparannya (Sanusi dan Sugeng 2009).
Kelimpahan alkil PAH yang lebih banyak (terutama pada sumber
petrogenik) persisten untuk waktu yang lebih lama, dan beberapa lebih toksik dari
senyawa utamanya. Metilfenantrena lebih toksik dari pada fenantrena. PAH yang
terurai tidak berarti mengurangi potensi dampaknya secara biologi terhadap
komponen biologi, PAH yang terurai dapat lebih berbahaya (Irwin 1997).
Menurut karakteristik senyawa PAH, toksisitasnya dapat dibagi menjadi 2 yaitu :
1. Senyawa PAH dengan jumlah karbon rendah (C8-C14) memberikan
toksisitas akut (2.35-970 µg/l di perairan (Irwin 1997)) terhadap biota laut.
Hal ini dikarenakan kelarutan dari senyawa tersebut tinggi (KOW
2. Senyawa PAH dengan jumlah karbon tinggi (>C
1.40-4.15).
14) memberikan toksisitas
kronis (10-710 µg/l di perairan (Irwin 1997)) terhadap biota laut, karena
kelarutan dari senyawa tersebut rendah (KOW 4.15-6.20).
2.7.3 Dampak PAH terhadap Organisme
PAH yang terakumulasi dalam tubuh organisme, dapat mempengaruhi
kehidupannya. Beberapa PAH, yang terakumulasi dalam biota, mempunyai
kemampuan untuk menyerap energi cahaya ultraviolet (UV) yang dapat
mempengaruhi sifat toksisitasnya seperti antrasena dan fluorantena. Peningkatan
potensi toksisitas bersamaan dengan pemaparan cahaya disebut fototoksisitas
(Irwin 1997). Efek toksik PAH pada biota laut bersifat lokal dan sementara dan
tidak berdampak nyata dalam jangka panjang, Selain itu, efeknya juga dapat pulih
kembali (reversible). Perbedaan jenis individu maupun campuran senyawa PAH,
lama pemaparan, besaran dan efeknya berbeda pada masing-masing biota, baik
yang bersifat akut maupun Kronis (Tabel 9).
2.7.4 Jenis PAH Bersifat Racun
Secara umum sifat toksik, mutagenik dan karsinogenik dari PAH
disebabkan oleh transformasi dari metabolisme PAH karena adanya sistem MFO
metabolisme PAH. Proses penting ini pada populasi dan ekosistem tidak jelas,
karena masih diabaikan ketika mengelola lingkungan (Kalf et al. 1996). Sistem
MFO bertindak untuk mendegradasi aromatik dan sejumlah senyawa organik
(termasuk PAH) oleh hidroksilasi (fase 1) dan konjugasi dengan glucuronic acid
(fase 2). Reaksi antara bahan kontaminan organik dengan uridine diphosphate
glucuronic acid (UDPGA) disebut glucuronisasi atau glucuronid konjugasi
sebagai bagian dari fase 2 pada proses metabolisme (Gambar 6). Beberapa PAH
berubah menjadi bentuk lebih water soluble oleh glucuronisasi (Irwin 1997). Sifat
karsinogenik individu PAH berbeda-beda (Tabel 10).
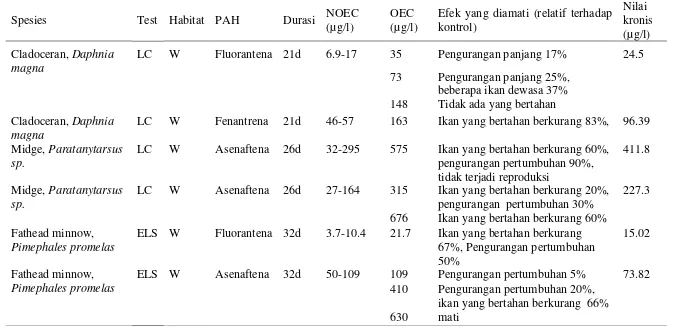
Tabel 9 Rangkuman sensitifitas sifat kronis pada organisme air tawar dan laut (dimodifikasi dari EPA/600/R-02/013).
Spesies Test Habitat PAH Durasi NOEC
(µg/l)
OEC (µg/l)
Efek yang diamati (relatif terhadap kontrol)
73 Pengurangan panjang 25%, beberapa ikan dewasa 37% 148 Tidak ada yang bertahan Cladoceran, Daphnia pengurangan pertumbuhan 30%
227.3
676 Ikan yang bertahan berkurang 60% Fathead minnow, 410 Pengurangan pertumbuhan 20%,
Tabel 9 (lanjutan)
Fathead minnow,
Pimephales promelas
ELS W Asenaftena 32-35d
67-332 495 Pengurangan pertumbuhan 54% 405
Rainbow trout,
14 Ikan yang bertahan berkurang 48%, pengurangan pertumbuhan 44%
32 Ikan yang bertahan berkurang 52%, Pengurangan pertumbuhan 75%
66 mati Mysid, Americamysis
bahia
LC B/W Asenaftena 35d 100-240 340 Terjadi pengurangan ikan muda 93%
285.7
510 Tidak ada yang bertahan Mysid, Americamysis
bahia
LC B/W Asenaftena 25d 20.5-44.6 91.8 Terjadi pengurangan ikan muda 91%
63.99
168 Tidak terjadi reproduksi,
pengurangan pertumbuhan 34% 354 Ikan yang bertahan berkurang
96%, Tidak terjadi reproduksi Mysid, Americamysis
bahia
LC B/W Fluorantena 28d 3592 621 Ikan yang bertahan berkurang 26.7%, terjadi pengurangan ikan muda 91.7%
15.87
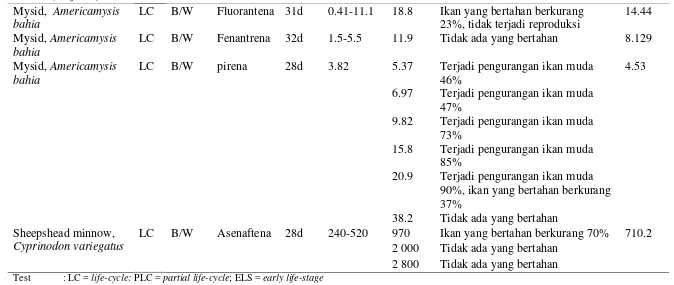
Tabel 9 (lanjutan)
Mysid, Americamysis bahia
LC B/W Fluorantena 31d 0.41-11.1 18.8 Ikan yang bertahan berkurang 23%, tidak terjadi reproduksi
14.44
6.97 Terjadi pengurangan ikan muda 47%
9.82 Terjadi pengurangan ikan muda 73%
15.8 Terjadi pengurangan ikan muda 85%
20.9 Terjadi pengurangan ikan muda 90%, ikan yang bertahan berkurang 37%
38.2 Tidak ada yang bertahan Sheepshead minnow,
Cyprinodon variegatus
LC B/W Asenaftena 28d 240-520 970 Ikan yang bertahan berkurang 70% 710.2 2 000 Tidak ada yang bertahan
2 800 Tidak ada yang bertahan
Test : LC = life-cycle; PLC = partial life-cycle; ELS = early life-stage
Habitat : I = infauna; B = epibenthic; W = water column
NOEC : No Observed Effect Concentration
Tabel 10 Beberapa individu PAH yang bersifat karsinogenik (Neff 1979). Fenantrena -- Benz[j]aceantirilen + + Benz[a]antrasena + 3-metilkolantren + + + + 7,12-dimetilbenz[a]antrasena + + + + Napthasen -- Dibenz[aj]antrasena + Pirena -- Dibenz[ah]antrasena + + + Benzo[a]pirena + + + Dibenz[ac]antrasena + Benzo[e]pirena -- Benzo[a]fenantrena + + + Dibenzo[al]pirena ± Fluorena -- Dibenzo[ah]pirena + + + Benzo[a]fluorena -- Dibenzo[ai]pirena + + + Benzo[b]fluorena -- Dibenzo[cd,jk]pirena -- Benzo[c]fluorena -- Indeno[1,2,3-cd]pirena + Dibenzo[ag]fluorena + Krisena ± Dibenzo[ah]fluorena ± Dibenzo[b,def]krisena + + Dibenzo[ac]fluorena ± Dibenzo[def,p]krisena + Fluorantena -- Dibenzo[def,mno]krisena -- Benzo[b]fluorantena + + Perilen -- Benzo[i]fluorantena + + Benzo[ghi]perilen -- Benzo[k]fluorantena -- koronen -- Benzo[mno]fluorantena --
Ket : (--) tidak bersifat karsinogenik; (±) sifat karsinogeniknya lemah; (+) bersifat karsinogenik; (++, +++, ++++) sifat kasinogeniknya tinggi
2.8Karakteristik Perairan Pesisir dan Laut
Pesisir merupakan suatu wilayah yang menjadi peralihan antara daratan dan
laut. Pesisir memiliki peran antara lain sebagai sumber penyedia sumber daya
alam, jasa pendukung kehidupan dan kenyamanan dan sebagai mitigasi bencana.
Pesisir dan daratan memiliki keterkaitan. Keterkaitan daratan (DAS) dengan
pesisir adalah sebagai penghubung antara daratan di hulu dengan pesisir,
penghantar bahan pencemar dari hulu ke pesisir dan dampak yang dihulu akan
dirasakan di pesisir karena peran DAS.
Batasan wilayah pesisir di daratan yaitu wilayah dimana daratan berbatasan
dengan laut, masih dipengaruhi oleh proses-proses seperti pasang surut, angin laut
dan intrusi garam. Batasan wilayah pesisir di laut adalah daerah yang dipengaruhi
serta daerah laut yang dipengaruhi oleh kegiatan-kegiatan manusia di daratan
(Bengen 2004).
Daratan dan proses-proses yang terjadi di daratan (misalnya aliran air besar
dengan zat partikel yang dibawanya menuju laut) akan mempengaruhi salinitas,
turbiditas, kesuburan dan kecerahan perairan pantai. Iklim setempat seperti curah
hujan akan mempengaruhi salinitas dan angin yang kencang akan menyebabkan
berkembangannya arus dan gelombang laut. Pengaruh dari faktor setempat ini
akan menyebabkan sifat atau keadaan oseanografi menjadi lebih kompleks dan
unik bagi suatu daerah perairan pantai/pesisir yang berlainan dari sifat/pola umum
di laut lepas yang banyak ditentukan baik oleh pengaruh musim maupun pengaruh
samudera yang berdekatan.
Wilayah pesisir dan laut juga rentan terhadap dampak pencemaran akibat
aliran limbah dari daratan melalui sungai, saluran yang menuju ke laut (ocean
outfall)/pembuangan langsung ke laut. Secara fisik, kondisi pesisir dan laut lepas
di pengaruhi oleh siklus hidrologi, hidrodinamika, topografi wilayah pesisir dan
laut, zonasi dan intensitas kegiatan pemanfaatan sumberdaya alam serta teknologi
yang dipakai dalam kegiatan tersebut. Kondisi ini mempengaruhi sifat, pola dan
intensitas pencemaran yang mungkin terjadi akibat kegiatan sosial ekonomi di
wilayah pesisir dan laut.
Ketika masuk ke perairan pesisir dan laut, limbah akan berinteraksi dengan
air laut dan menghasilkan perilaku limbah yang khas. Perilaku tersebut bisa
berupa menguap, terlarut, terdispersi, dsb. Hal ini selanjutnya akan berpengaruh
pada konsentrasi limbah dan intensitas serta besaran dampak terhadap lingkungan
yang mungkin ditimbulkan (Mukhtasor 2007).
2.9Ikan Nomei (Horpodon nehereus)
Tarakan adalah salah satu pulau yang berada di Propinsi Kalimantan Timur
yang mempunyai luas wilayah ± 657.33 km2, dengan luas kawasan pesisir pantai
± 70 km2. Luas laut Pulau Tarakan 406.53 km2 (61.85%). Salah satu potensi
sumberdaya hayati perairan yang ada di Pulau Tarakan adalah ikan Nomei
(Gambar 7). Ikan Nomei merupakan ikan komersial yang banyak dipasarkan
dalam bentuk ikan kering yang menjadi satu makanan khas Kota Tarakan.
Gambar 7 Ikan Nomei (Horpodon nehereus) dengan nama lokal ikan Pepija atau Lembe-Lembe.
Ikan Nomei hidup di perairan lepas pantai yang dalam pada sedimen lumpur
berpasir sepajang tahun. Namun ikan ini juga berkumpul di wilayah yang luas di
daerah delta sungai untuk mencari makan pada musim angin monsun. Ikan ini
adalah predator yang agresif dan sangat pendar. Mempunyai 6 telur pada sekali
bertelur dalam setahun. Ikan Nomei mempunyai kebiasaan makan sebagai
karnivora dengan udang-udangan yang merupakan sumber makanan. Menurut
Pillay (1953) ikan ini juga memakan ikan, detritus, larva megalopa dan tumbuhan
(Gambar 8).
Daging ikan Nomei seperti jeli, tubuhnya terkandung banyak sekali air dan
merupakan media yang baik untuk pertumbuhan bakteri. Mulut yang menganga,
gigi besar, mata kecil dan badan yang lembut, ikan Nomei mirip dengan
Chauliodontidae yang mencirikan ikan laut dalam (Haneda 1950). Jenis makanan
Gambar 8 Persentasi jenis makanan yang ditemukan pada perut Horpodon nehereus (Pillay 1953).
Gambar 9 Histogram yang menunjukkan variasi bulanan volume beberapa jenis makanan yang dimakan ikan Nomei berdasarkan perbedaan bulan (Pilay 1953). (a) Udang dan udang-udangan, (b) Ikan Nomei, (c) Ikan yang lain, (d) Larva megalopa, (e) Bahan tumbuhan, (f) Detritus.
Jum
la
h or
ga
ni
sm
e
Bulan
a
b
c d
3
BAHAN DAN METODE
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan Juni-Juli 2010 untuk pengambilan
cuplikan di perairan laut Kota Tarakan, dan bulan Juli-Desember 2010 untuk
analisis cuplikan di laboratorium. Cuplikan dianalisis di Laboratorium Kualitas
Air Universitas Borneo Tarakan dan Laboratorium Pangan Universitas Islam
Negeri (UIN) Syarif Hidayatullah Tanggerang Selatan.
3.2 Bahan dan Alat
Bahan yang digunakan selama penelitian adalah cuplikan sedimen, air, ikan
Nomei (daging dan hati). Alat yang digunakan adalah ekman grab, dissecting set,
frezee dried, van dorn water sampler dan pendeteksi PAH spektrometry massa
gas kromatograf (GC-MS) tipe Shimadzu QP2010, detection limit 0.001 ppb.
3.3 Pengumpulan Data
3.3.1 Penentuan Stasiun Pengambilan Cuplikan
Stasiun pengambilan cuplikan air dan sedimen ditentukan berdasarkan 3
lokasi keterwakilan. Lokasi pertama adalah wilayah yang mewakili daerah kurang
banyak kegiatan. Lokasi kedua merupakan lokasi pengambilan cuplikan ikan dan
lokasi ketiga mewakili daerah yang aktif/banyak kegiatan. Pengambilan cuplikan
ikan hanya dilakukan pada 1 stasiun yaitu lokasi penangkapan di utara (Stasiun 2)
karena hanya di wilayah tersebut cuplikan ikan dapat ditemukan (Gambar 10) dan
ditangkap pada saat kondisi air laut pasang.
3.3.2 Teknik Pengambilan Cuplikan
1. Air
Cuplikan air diambil dengan menggunakan van dorn water sampler
berkapasitas 2 liter, kedalaman 1 meter dari permukaan air dan 1 meter