KAJIAN ABNORMALITAS PRIMER SPERMATOZOA PADA
BEBERAPA BANGSA SAPI DENGAN UMUR BERBEDA
MENGGUNAKAN PEWARNAAN CARBOLFUCHSIN
(WILLIAMS)
NURUL HAFSARI
FAKULTAS KEDOKTERAN HEWAN INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Kajian Abnormalitas Primer Spermatozoa pada Beberapa Bangsa Sapi dengan Umur Berbeda Menggunakan Pewarnaan Carbolfuchsin (Williams) adalah benar karya saya dengan arahan dari dosen pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juli 2014
Nurul Hafsari
ABSTRAK
NURUL HAFSARI. Kajian Abnormalitas Primer Spermatozoa pada Beberapa Bangsa Sapi dengan Umur Berbeda Menggunakan Pewarnaan Carbolfuchsin (Williams). Dibimbing oleh R IIS ARIFIANTINI dan MUCHIDIN NOORDIN.
Morfologi spermatozoa yang abnormal telah lama diketahui berhubungan erat dengan peningkatan umur dan sterilitas. Tujuan penelitian adalah untuk mempelajari morfologi spermatozoa di Balai Inseminasi Buatan (BIB) Lembang dari berbagai bangsa dan umur yang berbeda menggunakan pewarnaan carbolfuchsin (Williams). Sebanyak 24 ekor sapi milik BIB Lembang digunakan dalam penelitian ini. Sapi dikelompokkan menjadi dua kelompok, sapi berumur 3-5 tahun dan 7-11 tahun ayng terdiri dari sapi Ongole, Frisien Holstein (FH), Simental, dan Limosin. Semen dikoleksi menggunakan vagina buatan dan dievaluasi secara makroskopis dan mikroskopis. Untuk pengujian morfologi semen dibuat preparat ulas dari semen segar dan dikeringudarakan kemudian diwarnai dengan pewarnaan carbolfuchsin. Pengujian abnormalitas spermatozoa dilakukan dari total 500 sel spermatozoa. Hasil penelitian menunjukkan abnormalitas spermatozoa sapi Limosin lebih tinggi (2.8%), dibandingkan sapi Simmental (1.83%), FH (1.77%), dan Ongole (1.5%). Jumlah abnormalitas tidak dipengaruhi oleh umur. Jumlah abnormalitas pada sapi berumur 3-5 tahun dan sapi berumur 7-11 tahun adalah (0.35%) dan (0.34%). Kesimpulan dari penelitian ini adalah bahwa semen sapi yang digunakan dalam penelitian memiliki kualitas yang baik berdasarkan hasil evaluasi karena jumlah abnormalitas pada semua breed menunjukkan hasil <20%.
Kata kunci: abnormalitas spermatozoa, balai inseminasi buatan, pewarnaan Williams
ABSTRACT
NURUL HAFSARI. Study of Bulls Sperm Morphology of Different Breed and Age Using Carbolfuchsin Stain (Williams). Supervised by R IIS ARIFINTINI and MUCHIDIN NOORDIN.
KAJIAN ABNORMALITAS PRIMER SPERMATOZOA PADA
BEBERAPA BANGSA SAPI DENGAN UMUR BERBEDA
MENGGUNAKAN PEWARNAAN CARBOLFUCHSIN
(WILLIAMS)
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Kedokteran Hewan
pada
Fakultas Kedokteran Hewan
FAKULTAS KEDOKTERAN HEWAN INSTITUT PERTANIAN BOGOR
BOGOR 2014
PRAKATA
Puji syukur kehadirat Allah SWT yang telah melimpahkan rahmat dan hidayah-Nya serta ilmu yang bermanfaat sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini.
Ucapan terima kasih kepada Ibu Prof Dr Dra R Iis Arifiantini, MSi dan Bapak Drh Muchidin Noordin atas kesediaan dan kesabarannya membimbing penulis pada saat penelitian, penyusunan dan selama penyelesaian skripsi ini. Terima kasih untuk Bapak Dr Drh Chusnul Choliq, MS, MM, selalu pembimbing akademik atas bimbingan dan arahannya selama penulis berada di FKH. Selain itu, penulis juga berterima kasih pada Ibu Ros dan Pak Langgeng serta seluruh staf Balai Inseminasi Buatan Lembang yang telah membantu pada saat penulis melakukan pengambilan data. Terima kasih pula kepada Anis STK yang telah membantu penulis dalam menganalisis data sehingga penulis dapat menyelesaikan skripsi ini.
Kepada Mamah Helga dan Ayah Hilman, terima kasih atas doa, dukungan, dan kasih sayangnya selama ini. Untuk Aa Fahmi dan Akang Hafiz, terima kasih atas bantuan dan dukungan yang diberikan selama ini.
Kepada teman perjuangan penulis sejak awal penelitian, Donny dan Yani, terima kasih atas kerjasamanya selama ini. Untuk sahabat-sahabat, Deka, Ghina, Gamma, Erlan, Koko, Tiwa, Faisal, Mba Choti dan teman-teman Acromion lainnya, terima kasih sudah menjadi teman yang baik. Bagi teman-teman semasa SMA, Barisan Heboh, terima kasih atas dukungan dan motivasinya.
Menyadari banyaknya kekurangan dalam penelitian ini, maka penulis mengharapkan saran dan kritik guna penyempurnaan skripsi ini. Akhir kata penulis meminta maaf atas segala kekurangan dan kesalahan, semoga skripsi ini bermanfaat bagi kita semua.
Bogor, Juli 2014
DAFTAR ISI
Jenis Sapi di Balai Inseminasi Buatan 3
Sapi Peranakan Ongol 3
Sapi Friesian Holstein 3
Sapi Simental 4
Sapi Limosin 4
Morfologi Spermatozoa 4
Teknik Pengujian dan Pewarnaan Morfologi 5
METODE 6
Koleksi Sampel Preparat Ulas 7
Pewarnaan Carbolfuchsin 7
Abnormalitas Primer Spermatozoa Berdasarkan Umur Sapi 11 Abnormalitas Primer Spermatozoa Berdasarkan Bangsa Sapi 12
DAFTAR TABEL
1 Karakteristik semen segar sapi 9
2 Persentase abnormalitas primer spermatozoa berdasarkan bangsa sapi 11 3 Abnormalitas primer spermatozoa berdasarkan umur 12 4 Abnormalitas primer spermatozoa berdasarkan bangsa sapi 13
DAFTAR GAMBAR
1 Abnormalitas primer spermatozoa 10
DAFTAR LAMPIRAN
1 Data deskriptif persentase abnormalitas spermatozoa berdasarkan
bangsa sapi 18
2 Data deskriptif abnormalitas primer spermatozoa berdasarkan umur 18 3 Data deskriptif abnormalitas primer spermatozoa berdasarkan bangsa
sapi 19
4 Hasil uji lanjut Duncan persentase abnormalitas spermatozoa
berdasarkan bangsa sapi 20
5 Hasil uji lanjut Duncan abnormalitas spermatozoa berdasarkan bangsa
sapi 20
6 Hasil uji lanjut Duncan abnormalitas spermatozoa berdasarkan umur 22 7 Data deskriptif volume, motilitas, dan konsentrasi spermatozoa 22
8 Hasil uji lanjut Duncan volume spermatozoa 23
PENDAHULUAN
Latar Belakang
Balai Inseminasi Buatan (BIB) adalah suatu balai yang bertugas untuk melaksanakan produksi dan pemasaran semen beku ternak unggul (Kementan 2013). Saat ini yang resmi tercatat ada 2 BIB berskala nasional dan 15 Balai Inseminasi Buatan Daerah (BIBD) berskala lokal (Ditjennak 2008). Kegiatan produksi semen meliputi penampungan dan pengolahan semen seperti pengenceran, pengemasan, ekuilibrasi, pembekuan, dan penyimpanan (Arifiantini
et al. 2005).
Semen adalah cairan ejakulat yang terdiri dari plasma protein dan spermatozoa. Spermatozoa merupakan sel kecil yang kompak dan sangat khas serta tidak tumbuh dan membelah diri. Secara garis besar, spermatozoa terbagi atas bagian kepala dan ekor (Hafez dan Hafez 2000). Kepala spermatozoa dibagi menjadi dua daerah yaitu daerah akrosom anterior yang dibungkus oleh tudung akrosom dan daerah post akrosom posterior yang berbatasan dengan ekor. Tudung akrosom berasal dari apparatus golgi selama tahap awal spermiogenesis, yang mengandung akrosin, hyaluronidase, dan enzim-enzim hidrolitik lainnya yang terlibat pada proses fertilisasi (Arthur 2001). Ekor spermatozoa berasal dari sentriol spermatid selama proses spermiogenesis yang berfungsi untuk memberikan gerakan maju atau lokomosi kepada spermatozoa, ekor ini terbagi atas tiga bagian, yaitu bagian tengah (mid piece), bagian utama (principal piece) dan bagian ujung atau end piece (Barth dan Oko 1989).
Pengujian kualitas semen yang dilakukan di BIB meliputi makroskopis dan mikroskopis. Pengujian secara makroskopis meliputi volume, konsistensi dan warna semen, sedangkan secara mikroskopis meliputi gerakan massa, motilitas, skor individu dan konsentrasi (Arifiantini 2012), sedangkan pengujian morfologi jarang dilakukan. Menurut Morrel dan Rodriguez-Martinez (2009) untuk dapat melakukan fertilisasi, spermatozoa harus memiliki viabilitas, motilitas dan kromatin yang intact, serta mempunyai morfologi yang normal. Al-Makhzoomi et al. (2008) melaporkan adanya korelasi antara morfologi dengan fertilitas.
Sapi jantan mengalami perkembangan organ reproduksi selaras dengan tambahan umur dan perkembangan kondisi tubuh ternak itu sendiri yang terjadi dalam perjalanan masa pubertas sampai mencapai dewasa tubuh. Peningkatan kapasitas reproduksi terlihat dari volume ejakulat, jumlah spermatozoa motil dan konsentrasi spermatozoa. Hal ini baru terjadi 6 sampai 9 bulan sesudah awal pubertas (Lestari et al. 2013a). Awal pubertas merupakan salah satu tolak ukur bahwa sapi sudah mulai memasuki usia produktif yang akan diikuti dengan peningkatan kapasitas reproduksi. Brito et al. (2002) menyatakan umur dan kelompok genetik memengaruhi karakteristik skrotum, testes, dan Testicular Vascular Cones (TVC). Selain itu, karakteristik skrotum, testes dan TVC berhubungan dengan produksi sperma dan kualitas spermatozoa pada sapi jantan.
2
Perumusan Masalah
Balai Inseminasi Buatan yang menyediakan fasilitas semen beku harus selalu memperhatikan kualitas semen beku yang diproduksinya. Spermatozoa abnormal merupakan salah satu penyebab infertilitas akibat kegagalan spermatozoa untuk mencapai tempat terjadinya fertilisasi. Untuk mengetahui abnormalitas morfologi spermatozoa dapat dilakukan dengan menggunakan teknik pewarnaan Williams.
Tujuan Penelitian
Penelitian ini bertujuan untuk menguji perbedaan morfologi spermatozoa dengan beberapa indikator abnormalitas berdasarkan umur pada beberapa jenis sapi berbeda.
Manfaat Penelitian
3
TINJAUAN PUSTAKA
Jenis Sapi di Balai Inseminasi Buatan
Aplikasi teknologi Inseminasi Buatan (IB) menggunakan semen beku telah dilakukan di Indonesia sejak tahun 1972 menggunakan semen beku hasil impor. Produksi semen beku di Indonesia telah dimulai sejak tahun 1976 di BIB Lembang (Jawa Barat) dan dilanjutkan di Singosari (Jawa Timur) pada tahun 1982 (Feradis 2010). Pejantan yang dipelihara BIB Lembang adalah sapi penghasil susu dan daging, sedangkan menurut pembuktian kualitas pemuliaan ternaknya terbagi atas pejantan proven (terbukti dari produksi turunannya tinggi), pejantan register (tercatat tiga generasi tertuanya), dan pejantan performance
(yang tercatat dari penampakan luarnya saja).
Menurut Prajogo et al. (2002), ternak sapi perah yang potensial di Indonesia adalah sapi FH, sedangkan ternak sapi potong yang potensial adalah sapi Limosin dan Simental. Program peningkatan populasi sapi potong dapat dilakukan melalui pengendalian pemotongan ternak sapi produktif, pengendalian penyakit reproduksi dan penyediaan bibit ternak sapi bermutu (Sodiq dan Nurwakhidiati 2006). Faktor yang menentukan efisiensi maksimum produksi susu sapi perah adalah berapa banyak liter susu yang diproduksi per hari sepanjang hidupnya, sedangkan untuk sapi tipe pedaging faktor yang menentukan adalah kecepatan tumbuh setiap hari dan dari bagian karkas yang dapat dimakan (Philips 2001). Sapi Peranakan Ongol
Bangsa sapi Peranakan Ongol (PO) tersebar luas dan populasi terbesar terdapat di pulau Jawa terutama di Jawa Timur. Bangsa sapi ini baru terbentuk sekitar tahun 1930 melalui sistem persilangan dengan grading up sapi Jawa dengan sapi Sumba Ongol (SO). Persilangan tersebut bertujuan untuk memperoleh ternak sapi yang dapat digunakan bagi keperluan tenaga tarik membantu petani mengolah tanah pertanian dan transportasi.
Sapi PO berwarna putih, mempunyai perawakan besar, bergumba pada pundak, dan mempunyai gelambir yang menjulur sepanjang garis bawah leher, dada, sampai ke pusar. Sapi PO termasuk tipe sapi pekerja yang baik, bertenaga kuat, tahan lapar dan haus, sabar serta dapat menyesuaikan dengan pakan yang sederhana. Sapi PO juga menunjukkan keunggulan sapi tropis yaitu daya adaptasi iklim tropis yang tinggi, tahan terhadap panas, tahan terhadap gangguan parasit seperti gigitan nyamuk dan caplak, disamping itu juga menunjukkan toleransi yang baik terhadap pakan yang mengandung serat kasar tinggi (Soeprapto 2006). Sapi Friesian Holstein
4
Sifat sapi FH yang tenang dan jinak memudahkan pengendalian dan penanganannya saat diberi perlakuan. Sapi FH memiliki kuantitas produksi susu yang paling tinggi dibandingkan dengan bangsa sapi perah lainnya. Di Amerika Serikat produksi susunya dapat mencapai 5755 liter dalam satu masa laktasi (± 10 bulan), sedangkan di Indonesia rata-rata produksi sapi FH adalah 10 liter per ekor per hari (Syarif dan Harianto 2011).
Sapi Simental
Sapi Simental merupakan sapi bangsa Bos taurus yang berasal dari Swiss. Sapi Simental memiliki warna coklat muda kemerahan dengan bagian wajah, tubuh bagian bawah, lutut, hingga ujung ekor berwarna putih. Sapi ini memiliki tubuh besar, kekar, dan berotot. Pertumbuhannya sangat baik dengan persentase karkas tinggi dan sedikit lemak. Bobot badan Simental dewasa dapat mencapai 1200 kg/ekor (Fikar dan Ruhyadi 2010). Sapi ini bukan hanya sapi dwiguna, tetapi triguna karena dapat berfungsi sebagai sapi pekerja, meskipun Simental digolongkan dalam tipe triguna, tetapi pemanfaatan sapi ini umumnya sebagai ternak pedaging karena memiliki pertumbuhan otot yang sangat baik, menghasilkan karkas yang tinggi dan sedikit lemak (Ditjennak 2006).
Sapi Limosin
Sapi Limosin berasal dari Perancis keturunan dari Bos taurus. Sapi Limosin memiliki rambut warna mulai dari kuning sampai merah keemasan dan tanduknya berwarna cerah dengan tanduk jantan tumbuh keluar dan melengkung. Kepala Limosin adalah kecil dan pendek dengan dahi yang lebar dan leher yang pendek. Sapi jantan dewasa berbobot badan 907-998 kg dan bobot badan sapi betina dewasa 544-635 kg. Sapi Limosin dikenal untuk efektivitas mereka dalam efisiensi pakan ternak, karkas yang tinggi dan besarnya daerah loin (Gillespie dan Flanders 2009).
Sapi ini sangat cocok dipelihara di daerah beriklim sedang. Sapi Limosin merupakan sapi pedaging bertipe besar dan mempunyai volume rumen yang besar. Karena itu, sapi ini mampu menambah konsumsi pakan lebih banyak di luar kebutuhan yang sebenarnya. Namun, sapi ini memiliki metabolisme yang cepat sehingga menuntut teknik pemeliharaan yang lebih teratur (Fikar dan Ruhyadi 2010).
Morfologi Spermatozoa
Morfologi spermatozoa adalah salah satu bentuk evaluasi semen secara mikroskopis yang dilakukan dengan menghitung jumlah spermatozoa yang normal dan abnormal secara primer dan sekunder (Arifiantini dan Ferdian 2006). Morfologi spermatozoa juga indikator refleksi normalitas dari tubulus seminiferus dan beberapa bagian dari epididymis (Holroyd et al. 2002).
5 sepenuhnya dengan materi yang homogen sebagai informasi genetik dari pejantan yaitu kromosom. Ekor spermatozoa berasal dari sentriol spermatid selama proses spermiogenesis yang berfungsi untuk memberikan gerakan maju atau lokomosi kepada spermatozoa dengan gelombang-gelombang yang dimulai dari daerah implantasi ekor-kepala dan berjalan ke arah belakang (Barth dan Oko 1989).
Determinasi abnormalitas spermatozoa berbeda-beda diantara peneliti maupun laboratorium. Menurut Chenoweth (2005), abnormalitas spermatozoa terbagi dalam dua katagori, yakni berdasarkan sekuen proses pembentukan spermatozoa (primer dan sekunder) dan berdasarkan dampaknya bagi fertilitas. Katagori kerusakan spermatozoa bersifat primer adalah yang terjadi pada saat spermatogenesis, sedangkan sekunder jika kejadiannya setelah spermiasi. Pengelompokkan kelainan mayor dan minor didasarkan pada dampaknya terhadap fertilitas jantan tersebut. Kelainan mayor akan berdampak besar pada fertilitas, sebaliknya kelainan yang bersifat minor dampaknya kecil pada fertilitas.
Telah dikembangkan suatu metode yang disebut breeding soundness evaluation (BSE) untuk mengukur potensi seekor sapi jantan. Menurut Alexander (2008), BSE atau disebut juga bull breeding soundness evaluation (BBSE) mudah dilakukan dan relatif tidak mahal serta sangat berguna untuk peternakan. Saat ini
Society for Theriogenology (SFT) menggunakan standar BBSE yang diadopsi pada tahun 1993, dimana seekor pejantan harus memenuhi minimum standar 4 katagori yaitu organ reproduksi umum, indeks lingkar skrotum (scrotal circumference indexed) sesuai umurnya, motilitas spermatozoa dan morfologi spermatozoa. Hal ini disebabkan pejantan dengan umur yang semakin tua akan mengalami degenerasi pada sel-sel tubuh, termasuk pada organ reproduksinya. Penelitian sebelumnya oleh Söderquist et al. (1996) dalam Arifiantini dan Ferdian (2006) menyatakan bahwa terdapat pengaruh umur yang sangat signifikan terhadap abnormalitas spermatozoa.
Teknik Pengujian dan Pewarnaan Morfologi
Zat warna yang umum dipakai untuk pengamatan spermatozoa adalah eosin, tinta India dan eosin-negrosin. Menurut Barth dan Oko (1989) teknik fiksasi dan pewarnaan spermatozoa dibedakan atas dua metode yaitu metode kering dan metode basah.
Pengamatan morfologi dapat dilakukan dengan berbagai cara, baik secara komvensional atau manual maupun menggunakan teknologi mutakhir. Cara manual dapat dilakukan dengan menggunakan teknik pewarnaan dan pengamatan dilakukan dengan menggunakan mikroskop cahaya atau mikroskop fase kontras. Sedangkan metode mutakhir yang dapat digunakan antara lain adalah Timed-Exposure Photomicrography (TEP), Multiple Exposure Photomycrography
6
METODE
Waktu dan Tempat Penelitian
Koleksi sampel dilakukan di Balai Inseminasi Buatan Lembang, Bandung pada bulan Agustus sampai September 2013 sedangkan pewarnaan dan pengujian morfologi spermatozoa dilakukan di Laboratorium Unit Rehabilitasi Reproduksi Fakultas Kedokteran Hewan Institut Pertanian Bogor bulan Oktober 2013 sampai dengan Februari 2014.
Bahan
Sumber semen berasal dari 24 ekor pejantan, 12 ekor berumur kurang dari 7 tahun (3-5 tahun) dan 12 ekor berumur lebih dari 7 tahun (7-11 tahun), serta masing-masing 3 ekor dari bangsa FH, Ongol, Limosin, dan Simental. Bahan yang digunakan adalah seperangkat pewarnaan carbolfuchsin diantaranya basic fuchsin, bluish eosin, chloramine 0.5%, destilled water, dan alkohol 95%.
Alat
Peralatan yang digunakan untuk mengamati morfologi menggunakan mikroskop cahaya Olympus CH20 dan dokumentasi menggunakan mikroskop dengan kamera Canon IXUS 220 HS.
Metode Penelitian Koleksi semen
Koleksi semen dilakukan pada pagi hari dengan menggunakan vagina buatan. Pemakaian alat vagina buatan merupakan simulasi yang sempurna terhadap perkawinan secara alami, sehingga semen tertampung dengan kualitas yang jauh lebih baik daripada metoda lainnya (Mardiyah et al. 2001). Vagina buatan adalah alat koleksi semen yang umum dilakukan, kualitas dan kuantitasnya optimal, dan prosesnya berlangsung secara fisiologis (Arifiantini dan Ferdian 2006).
Sebelum penampungan semen dimulai, praeputium dan daerah sekitarnya dicuci dengan air hangat. Penampungan semen dilakukan di tempat penampungan yang dibuat khusus dengan hewan pemancing seekor pejantan. Pejantan yang akan ditampung semennya diberikan rangsangan dengan cara membawa pejantan itu mendekati hewan pemancing lalu membawanya pergi lagi. Membiarkan pejantan menaiki hewan pemancing tetapi tidak ditampung semennya disebut
false mount. Satu false mount akan meninggikan konsentrasi sperma 50% dan dua
7 menaiki pemancing. Dengan telapak tangan kiri yang mengarah ke atas, preputium digenggam dan penis yang ereksi ditarik ke samping ke arah vagina buatan. Ujung penis dikenakan ke mulut vagina buatan. Ejakulasi ditandai dengan adanya suatu dorongan tiba-tiba ke depan dan kedua kaki belakang pejantan terangkat seolah-olah hendak melompati pemancing. Sesudah ejakulasi, pejantan bergerak turun dan vagina buatan ditarik perlahan-lahan ke depan. Setelah penis terlepas keluar, vagina buatan segera dibalikkan vertikal dengan tabung penampung berada dibawah, lalu lubang ventilasi udara dibuka sedikit, atau bisa juga vagina buatan diputar perlahan-lahan membentuk angka 8 agar semen yang tertampung dapat turun dan masuk ke dalam tabung penampung. Setelah kira-kira semua semen turun ke dalam tabung penampung, maka tabung penampung dilepas dari ekor corong karet dan ditutup. Lalu disimpan dalam termos berisi air hangat 37 oC lalu dibawa ke laboratorium untuk dilakukan evaluasi.
Evaluasi makroskopis dan mikroskopis
Evaluasi semen dilakukan secara makroskopis maupun mikroskopis. Evaluasi makroskopis meliputi volume, konsistensi dan warna semen sedangkan evaluasi mikroskopis meliputi persentase hidup mati, persentase abnormalitas, persentase motilitas dan konsentrasi (Freshman 2002).
Koleksi sempel preparat ulas
Semen segar yang dikoleksi di BIB Lembang dilarutkan dengan NaCl fisiologis dengan perbandingan 1:4 lalu dibuat preparat ulas pada gelas objek, diberi identitas dan dikeringudarakan kemudian disimpan pada slide boks sampai waktu pewarnaan.
Pewarnaan carbolfuchsin
Pewarnaan dilakukan dengan cara fiksasi preparat ulas di atas api bunsen dan selanjutnya dicuci dalam alkohol absolut selama 4 menit lalu dikeringudarakan. Preparat dimasukkan ke dalam larutan chloramin 0.5% selama 1-2 menit, sambil diangkat dan dimasukkan kembali berkali-kali dengan tujuan menghilangkan mukus dan ulasan terlihat jernih. Kemudian dicuci dengan
destilled water, selanjutnya dalam alkohol 95% dan diwarnai dengan larutan carbolfuchsin selama 8-10 menit. Terakhir, dicuci dengan air mengalir dan dikeringkan (Arifiantini et al. 2006).
Pengamatan Morfologi Spermatozoa
Morfologi spermatozoa diamati dengan cara melihat kelainan bentuk kepala spermatozoa dan menghitung jumlah spermatozoa sebanyak 500 sel dengan pembesaran 400x. Selanjutnya semua jenis abnormalitas spermatozoa yang ditemukan dicatat, diklasifikasikan, dan didokumentasikan menggunakan kamera. Klasifikasi jenis abnormalitas spermatozoa primer dilakukan berdasarkan temuan yang didapat pada waktu pengamatan (Riyadhi et al. 2012).
Prosedur Analisis Data
8
9
HASIL DAN PEMBAHASAN
Kualitas semen segar
Kualitas semen segar dari keempat bangsa sapi yang digunakan dalam penelitian ini memiliki kualitas yang cukup baik. Warna semen yang diperoleh adalah putih susu. Warna semen sapi yang normal adalah seperti putih susu atau krem keputih-putihan (Feradis 2010).
Volume semen sapi FH adalah 8.110.46 mL paling tinggi dibanding dengan volume sapi Limosin (6.690.39 mL) berbeda nyata pada taraf nyata (alpha) sebesar 5%, dan tidak terdapat perbedaan volume semen antara sapi FH, Ongol dan Simental, demikian juga antara volume semen sapi Ongol, Simental dan Limosin. Secara umum volume semen tersebut masih termasuk normal karena menurut Garner dan Hafez (2000), volume semen sapi berkisar antara 5-8 mL.
Tabel 1 Karakteristik semen segar sapi
Karakteristik FH Ongol Limosin Simental
Warna Putih susu Putih susu Putih susu Putih Susu
Volume (mL) 8.11 0.46a 7.27 0.59ab 6.69 0.39b 6.98 0.39ab
Konsistensi Sedang Sedang Sedang Sedang
Gerak ++ ++ ++ ++
Motilitas (%) 70.50 3.12a 70.31 1.27a 70.20 0.86a 70.00 2.68a Konsentrasi (juta/mL) 1098.26 62.49a 1193.33 85.25a 1190.40 42.80a 1073.33 62.21a Angka-angka pada kolom yang sama yang diikuti oleh huruf yang sama tidak berbeda nyata pada taraf uji 5% (uji selang berganda Duncan).
Konsistensi semen pada keempat bangsa sapi ini termasuk sedang. Semakin kental semen dapat diartikan bahwa semakin tinggi konsentrasi spermatozoa yang terkandung di dalamnya (Feradis 2010). Semen yang baik memiliki kekentalan hampir sama dengan susu (Lestari et al. 2013b). Taurin et al. (2000) melaporkan bahwa konsistensi semen mempunyai korelasi dengan warna, semen yang berwarna krem biasanya memiliki konsistensi yang pekat atau kental, sedangkan semen dengan warna yang jernih atau terang memiliki konsistensi yang encer.
Secara mikroskopis semen segar memiliki gerakan massa spermatozoa ++, ditandai dengan awan hitam yang tidak begitu gelap dengan gerakan yang cepat berpindah. Persentase spermatozoa motil yang diperoleh adalah antara 70.002.68% hingga 70.503.12%, nilai ini masih berada dalam kisaran normal. Menurut Garner dan Hafez (2000), kisaran normal gerakan massa spermatozoa yaitu antara 40-75%. Campbell et al. (2003), menyatakan bahwa spermatozoa dengan motilitas yang sangat baik berkisar antara 70-80%. Motilitas merupakan uji kualitas yang penting karena fertilitas erat kaitannya dengan spermatozoa motil yang diinseminasikan.
10
konsentrasi spermatozoa pada sapi jantan dewasa berkisar antara 800-1200 juta/mL semen.
Abnormalitas Primer Spermatozoa
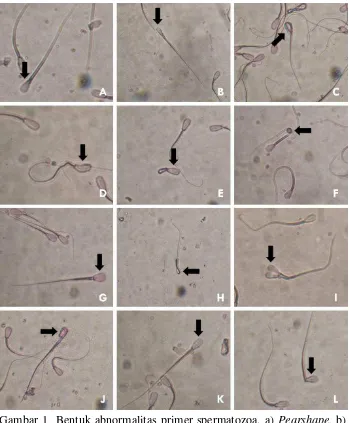
Parameter yang dianggap penting bagi spermatozoa yang akan menentukan fertilitasnya antara lain adalah: kapasitas produksi, daya tahan dan morfologi spermatozoa termasuk jumlah spermatozoa yang abnormal (Arifiantini et al. 2006). Pada penelitian ini, ditemukan 12 jenis kelainan primer spermatozoa yaitu
pearshape, narrow at the base, narrow, abnormal contour, undeveloped, round head, macrocephalus, microcephalus, double head, abaxial, knobbed acrosome defect, detached head (Gambar 1).
Gambar 1 Bentuk abnormalitas primer spermatozoa. a) Pearshape, b)
Narrow at the base, c) Narrow, d) Abnormal contour, e)
Undeveloped, f) Round head, g) Macrocephalus, h)
11 Abnormalitas spermatozoa merupakan kelainan struktur spermatozoa dari struktur normal yang dapat disebabkan oleh beberapa faktor, yaitu lingkungan, genetik, atau kombinasi dari keduanya (Chenoweth 2005). Morfologi spermatozoa yang abnormal ini memiliki korelasi positif dengan fertilitas sehingga berpengaruh terhadap kemampuan spermatozoa untuk membuahi ovum (Barth dan Oko 1989). Abnormalitas spermatozoa berdasarkan kejadiannya dibedakan menjadi abnormalitas primer dan abnormalitas sekunder (Chenoweth 2005). Abnormalitas sekunder umumnya terjadi pada bagian ekor dan akan mudah terseleksi pada saat pengujian motilitas, sedangkan abnormalitas primer terjadi pada bagian kepala dan sebagian bersifat genetik dan berdampak pada fertilitas (Riyadhi et al. 2012).
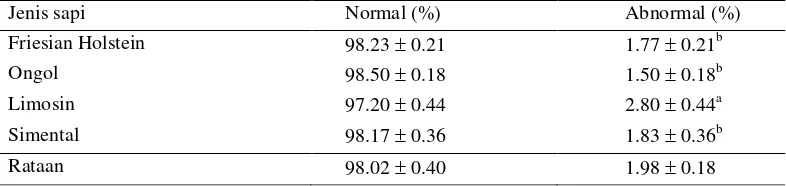
Hasil penelitian menunjukkan jumlah abnormalitas spermatozoa pada keempat bangsa yang diuji sangat rendah. Jumlah abnormalitas spermatozoa Limosin berbeda nyata pada taraf nyata (alpha) sebesar 5% dibandingkan bangsa sapi lain yaitu sebesar 2.80.44%, disusul dengan Simental yaitu 1.830.36%. Jumlah abnormalitas ini masih termasuk sedikit, karena menurut Barth dan Oko (1989), abnormalitas akan dianggap serius apabila abnormalitas primer mencapai 18-20% karena dapat menyebabkan penurunan fertilitas.
Tabel 2 Persentase abnormalitas spermatozoa berdasarkan bangsa sapi
Jenis sapi Normal (%) Abnormal (%) pada taraf uji 5% (uji selang berganda Duncan).
Sedikitnya jumlah abnormalitas primer spermatozoa disebabkan sapi yang digunakan merupakan sapi hasil seleksi secara genetik unggul dan dipelihara dengan manajemen yang baik dan telah terlatih untuk dikoleksi semennya. Teknik koleksi semen akan memengaruhi kualitas semen yang dihasilkan. Hewan yang belum terbiasa atau pertama kali dikoleksi semennya akan memperlihatkan abnormalitas primer spermatozoa yang tinggi. Abnormalitas spermatozoa juga akan dipengaruhi oleh teknik koleksi semen yang dilakukan.
Abnormalitas spermatozoa dengan teknik masase pada kerbau lumpur dapat mencapai 31.86% (Arifiantini dan Ferdian 2006), pada anoa menggunakan teknik koleksi elektroejakulator menunjukkan persentase 33.64% (Yudi et al. 2010) bahkan O’brien dan Roth (2000) melaporkan abnormalitas spermatozoa yang tinggi hingga mencapai 60% pada badak sumatera (Dicerorhinus sumatrensis) yang dikoleksi menggunakan teknik recovery postcoital dari vagina.
Abnormalitas Primer Spermatozoa Berdasarkan Umur Sapi
12
perkembangan sempurna sehigga dapat berbentuk kecil, ekor pendek, dan dengan pemeriksaan lanjut diperoleh bahwa sel tersebut tidak disusun oleh materi yang lengkap (Barth dan Oko 1989). Liu et al (2005) menyatakan bahwa persentase spermatozoa undeveloped dalam jumlah besar akan menyebabkan kemandulan (sterilitas) dan penyebab utama kelainan ini adalah pengaruh genetik.
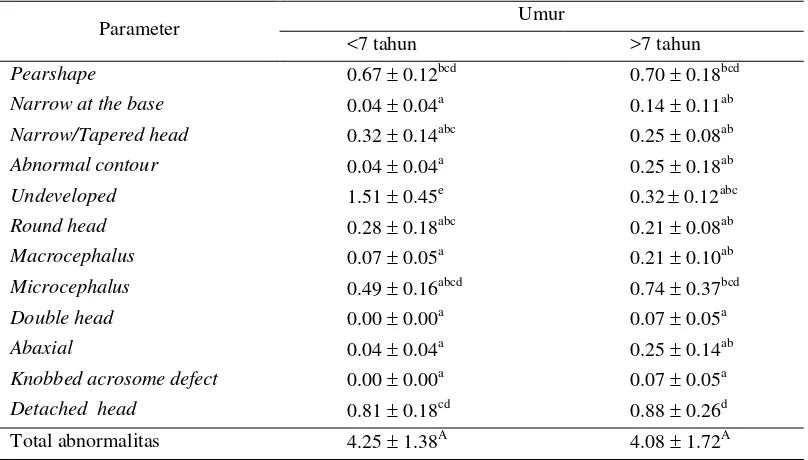
Berdasarkan hasil penelitian, total abnormalitas primer spermatozoa pada sapi berumur <7 tahun adalah 4.251.38% dan pada sapi berumur >7 tahun adalah 4.081.72%. Hasil penelitian ini hampir sama dengan yang dilaporkan oleh Riyadhi et al. (2012) bahwa umur tidak memengaruhi abnormalitas primer yang ditemukan pada sapi pejantan berumur 3-5 tahun milik BIB.
Tabel 3 Abnormalitas primer spermatozoa berdasarkan umur
Parameter Umur
Angka-angka pada kolom yang sama yang diikuti oleh huruf yang sama tidak berbeda nyata pada taraf uji 5% (uji selang berganda Duncan).
Menon et al. (2011) melaporkan bahwa abnormalitas pada sapi berumur 13-18 bulan memiliki jumlah abnormalitas tinggi (22.7718.57%) dibandingkan sapi berumur >26 bulan (18.2712.79%). Adanya pengaruh genetik, lingkungan, dan manajemen pemeliharaan, memungkinkan abnormalitas spermatozoa dapat ditemukan pada umur yang lebih muda. Oleh karena itu sangat tepat jika batasan umur penggunaan pejantan untuk produksi semen beku di Indonesia telah ditetapkan antara 6-7 tahun (Ditjennak 2007).
Abnormalitas Primer Spermatozoa Berdasarkan Bangsa Sapi
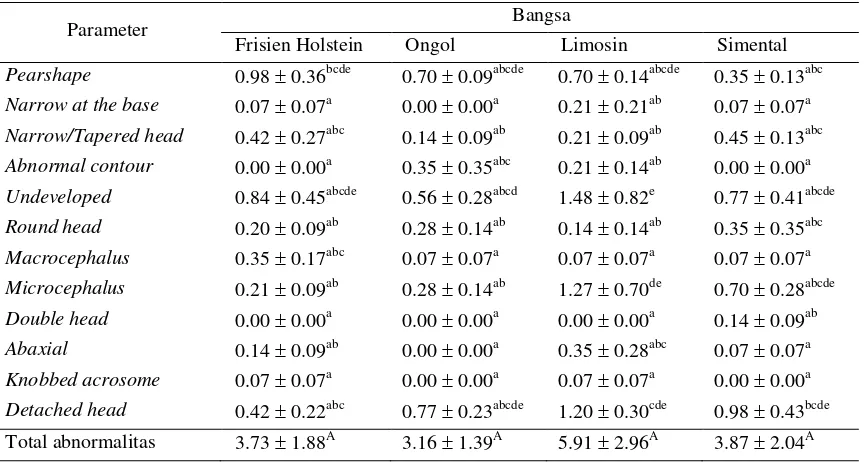
Hasil penelitian menunjukkan tidak adanya perbedaan pada jumlah abnormalitas primer spermatozoa pada empat bangsa sapi yang diuji. Jumlah abnormalitas pada sapi FH, Ongol, Limosin, dan Simental masing-masing adalah 3.731.88%, 3.161.39%, 5.912.96%, dan 3.872.04% (Tabel 4).
Pada bangsa sapi Ongol dan Simental, abnormalitas terbanyak adalah
13 1.480.82%, dan pada sapi FH, kelainan pearshape adalah abnormalitas tertinggi yaitu 0.980.36%. Menurut Barth dan Oko (1989) kelainan pearshape ini bersifat genetik, hal ini terbukti sapi jantan keturunan dari tetua dengan tingkat abnormalitas pearshape yang tinggi memperlihatkan gambaran semen yang sama dengan tetuanya. Spermatozoa yang berbentuk pearshape tidak mampu untuk melakukan fertilisasi. Ketidakmampuan spermatozoa melakukan kontak dengan sel telur (ovum) akibat tudung akrosom yang tidak sempurna untuk menembus zona pelusida.
Tabel 4 Abnormalitas primer spermatozoa berdasarkan bangsa sapi
Parameter Bangsa
Frisien Holstein Ongol Limosin Simental
Pearshape 0.98 0.36bcde 0.70 0.09abcde 0.70 0.14abcde 0.35 0.13abc
Angka-angka pada kolom yang sama yang diikuti oleh huruf yang sama tidak berbeda nyata pada taraf uji 5% (uji selang berganda Duncan).
14
SIMPULAN DAN SARAN
Simpulan
Umur tidak memengaruhi jumlah abnormalitas primer spermatozoa. Bangsa sapi Limosin memiliki abnormalitas yang lebih tinggi dibandingkan sapi Ongol, FH dan Simental.
Saran
15
DAFTAR PUSTAKA
Alexander JH. 2008. Bull breeding soundness evaluation: A practitioner’s perspective. Theriogenology. 70:469–472
Al-Makhzoomi A, Lundeheim N, Haard M, Rodriguez-Martinez H. 2008. Sperm morphology and fertility of progeny-tested AI dairy bull in Sweden.
Theriogenology. 70:682-691.
Arifiantini RI, Yusuf TL, Graha N. 2005. Longivitas dan recoveryrate pasca thawing semen beku sapi Frisien Holstein menggunakan bahan pengencer yang berbeda. Bul Peternakan. 29(2): 53-61.
Arifiantini RI, Wresdiyati T, Retnani EF. 2006. Pengujian morfologi spermatozoa Sapi Bali (Bos sondaicus) menggunakan pewarnaan Williams. J Indon Trop Anim Agric. 31:105-110.
Arifiantini RI, Ferdian F. 2006. Tinjauan aspek morfologi dan morfometri spermatozoa Kerbau Rawa (Bubalus Bubalis) yang dikoleksi dengan teknik masase. J Vet. 17(2): 83-91.
Arifiantini RI. 2012. Teknik Koleksi dan Evaluasi Semen pada Hewan. Bogor (ID): IPB Pr.
Arthur GH. 2001. Veterinary Reproduction and Obstetries 8th ed. London (GB): WB Saunders.
Campbell JR, Campbell KL, Kenealy MD. 2003. Artificial Insemination. In: Anim. Sci. 41th Ed. New York (US): McGraw-Hill.
Chenoweth PJ. 2005. Genetic Sperm Defect. Theriogenology. 64: 457-468.
[Ditjennak] Direktorat Jenderal Peternakan dan Kesehatan Hewan. 2006. Peraturan Direktur Jenderal Peternakan Nomor 121/Kpts/OT.210/F/11.06 tentang Petunjuk Teknis Pengawasan Mutu Semen Beku Sapi dan Kerbau. Jakarta (ID): Ditjennak.
[Ditjennak] Direktorat Jenderal Peternakan dan Kesehatan Hewan. 2007.
Petunjuk Teknis Produksi dan Distribusi Semen Beku. Jakarta (ID): Ditjennak.
[Ditjennak] Direktorat Jenderal Peternakan dan Kesehatan Hewan. 2008. Road Map Perbibitan Ternak. Jakarta (ID): Ditjennak.
Feradis MP. 2010. Bioteknologi Reproduksi Ternak. Bandung (ID): Alphabeta. Fikar S, Ruhyadi D. 2010. Beternak & Bisnis Sapi Potong. Jakarta (ID):
AgroMedia Pustaka.
Freshman JL. 2002. Semen collection and evaluation. Clin Tech Small Anim Pract. 17(3): 104-107.
16
Gillespie R, Flanders FB. 2009. Breeds of Beef Cattle. In: Modern Livestock and Poultry Production 8th ed. New York (US): Delmar Cengage Learning. Hafez ESE, Hafez B. 2000. Reproduction in Farm Animal 7th ed. Philadelphia
(US): Williams & Wilkins.
Holroyd RG, Doogan VJ, De Faveri J, Fordyce G, Mcgowan MR, Bertram JD, Vankam DM, Fitzpatrick LA, Jayawardhana GA, Miller RG. 2002. Bull selection and use in Northern Australia 4. Calfoutput and predictors of fertility of bulls in multiple-sire herds. J Anim Reprod Sci. 71: 67-79. [Kementan] Kementrian Pertanian. 2013. Peraturan Menteri No 58/Permentan/
OT.140/5/2013 Tentang Tugas Pokok Balai Inseminasi Buatan. Jakarta (ID): Kementan.
Kondracki S, Banaszewska D, Wysokinska, and Chomicz J. 2006. Sperm morphology of cattle and domestic pig. J Reprod Bio. 2(6): 99-104.
Lestari S, Saleh DM, Maidaswar. 2013a. Profil kualitas semen segar sapi pejantan Limousin dengan umur berbeda di Balai Inseminasi Buatan Lembang Jawa Barat. J Ilmiah Peternakan. 1(3): 1165-1172.
Lestari SD, Tagama TR, Saleh DM. 2013b. Profil produksi semen segar sapi Simmental pada tingkat umur yang berbeda di Balai Inseminasi Buatan Lembang Jawa Barat. J Ilmiah Peternakan. 1(3): 897-906.
Liu S, Sun Y, Zhou G, Zhang, Feng H, He X, Fang H, Luo C, Zhu G, Yang H, and Liu Y. 2005. The fertility of tetraploid hybrids and the sterility of their triploid offspring. J Taiwan Vet. 1-3.
Mardiyah E, Suarida I, Pustaka IK, Hernawati R. 2001. Penampungan dan evaluasi mutu semen sapi dengan vagina buatan. J Litbang Pertanian. 21: 138-146.
Menon AG, Barkema HW, Wilde R, Katelic JP, Thundathil JC. 2011. Associations between sperm abnormalities, breed, age, and scrotal circumference in beef bulls. J Can Vet. 75:241–247.
Morrell JW, Rodriguez-Martinez H. 2009. Biomimetic Techniques for improving sperm quality in animal breeding: a review. J Andrology. 1: 1-9.
O’brien JK, Roth TL. 2000. Postcoital sperm recovery and cryopreservation in
Sumatran Rhinoceros (Dicerorhinus sumatrensis) and aplication to gamete rescue in the African Black Rhinoceros (Diceros bicornis). J Reprod Fertil. 118(2): 263-271.
Phillips CJC. 2001. Principles of Cattle Production. Wallingford (GB): CABI Publishing.
Prajogo U, Hadi, Ilham N. 2002. Problem dan prospek pengembangan usaha pembibitan sapi potong di Indonesia. J Litbang Pertanian. 21: 148-157. Riyadhi M, Arifiantini RI, Purwantara B. 2012. Korelasi morfologi abnormalitas
primer spermatozoa terhadap umur pada beberapa bangsa sapi potong. J Vet. 19(2): 79-85.
Siregar AR. 2003. Pengembangan sapi perah rumpun unggul pada dataran rendah. Di dalam: Supriyadi, Syahgian S. Kumpulan hasil-hasil penelitian APBN tahun anggaran 2002. Buku 1 Ternak Ruminansia. Bogor (ID): Balai Penelitian Ternak Ciawi.
17 Soeprapto H. 2006. Cara Tepat Penggemukan Sapi Potong. Jakarta (ID):
AgroMedia Pustaka.
Syarif EK, Harianto B. 2011. Buku Pintar Beternak dan Bisnis Sapi Perah. Jakarta (ID): AgroMedia Pustaka.
Taurin B, Santi D, Putri KH. 2000. Inseminasi Buatan. Jakarta (ID): Universitas Terbuka.
18
LAMPIRAN
Lampiran 1 Data deskriptif persentase abnormalitas spermatozoa berdasarkan bangsa sapi
Lampiran 2 Data deskriptif abnormalitas primer spermatozoa berdasarkan umur
Mean Std.
Error
PearShape <7 ,00668167 ,001213586
PearShape >7 ,00703333 ,001824235
NarrowAtTheBase <7 ,00035167 ,000351667
NarrowAtTheBase>7 ,00140667 ,001081313
NarrowTapered <7 ,00316500 ,001386542
NarrowTapered >7 ,00246167 ,000814443
AbnormCon <7 ,00035167 ,000351667
AbnormCon >7 ,00246167 ,001833456
Undev <7 ,01512083 ,004451384
Undev >7 ,00316500 ,001175946
RoundHead <7 ,00281333 ,001824235
RoundHead >7 ,00211000 ,000821316
Macro <7 ,00070333 ,000474187
Macro >7 ,00211000 ,000971795
Micro <7 ,00492333 ,001628887
Micro >7 ,00738417 ,003713334
DoubleHead <7 0E-8 0E-9
DoubleHead >7 ,00070333 ,000474187
Abaxial <7 ,00035167 ,000351667
Abaxial >7 ,00246167 ,001418605
KnobAcro <7 0E-8 0E-9
KnobAcro >7 ,00070333 ,000474187
DetHead <7 ,00808833 ,001758333
DetHead >7 ,00879167 ,002620930
19 Lampiran 3 Data deskriptif abnormalitas primer spermatozoa berdasarkan
20
Lampiran 4 Hasil uji lanjut Duncan persentase abnormalitas spermatozoa berdasarkan bangsa sapi
Means for groups in homogeneous subsets are displayed. a. Uses Harmonic Mean Sample Size = 6,000.
Lampiran 5 Hasil uji lanjut Duncan abnormalitas primer spermatozoa berdasarkan bangsa sapi
knobbed acrosome 24 ,0833
narrow at the base 24 ,2083
abnormal contour 24 ,3333
Macro 24 ,3333
Means for groups in homogeneous subsets are displayed. a. Uses Harmonic Mean Sample Size = 24,000.
nilai_jenis
Means for groups in homogeneous subsets are displayed.
a. Uses Harmonic Mean Sample Size =
21
NarrowTapered_Ongol 6 ,3333 ,3333
RoundHead_Lim 6 ,3333 ,3333
DoubleHead_Sim 6 ,3333 ,3333
Abaxial_FH 6 ,3333 ,3333
NarrowAtTheBase_Lim 6 ,5000 ,5000
NarrowTapered_Lim 6 ,5000 ,5000
AbnormCon_Lim 6 ,5000 ,5000
RoundHead_FH 6 ,5000 ,5000
Micro_FH 6 ,5000 ,5000
RoundHead_Ongol 6 ,6667 ,6667
Micro_Ongol 6 ,6667 ,6667
PearShape_Sim 6 ,8333 ,8333 ,8333
NarrowTapered_Sim 6 ,8333 ,8333 ,8333
AbnormCon_Ongol 6 ,8333 ,8333 ,8333
RoundHead_Sim 6 ,8333 ,8333 ,8333
Macro_FH 6 ,8333 ,8333 ,8333
Abaxial_Lim 6 ,8333 ,8333 ,8333
NarrowTapered_FH 6 1,0000 1,0000 1,0000
DetHead_FH 6 1,0000 1,0000 1,0000
Undev_Ongol 6 1,3333 1,3333 1,3333 1,3333
PeasrShape_Ongol 6 1,6667 1,6667 1,6667 1,6667 1,6667
PearShape_Lim 6 1,6667 1,6667 1,6667 1,6667 1,6667
22
Lampiran 6 Hasil uji lanjut Duncan abnormalitas primer spermatozoa berdasarkan umur
NarrowAtTheBase <7 12 ,0833
AbnormCon <7 12 ,0833
Abaxial <7 12 ,0833
Macro <7 12 ,1667
DoubleHead >7 12 ,1667
KnobAcro >7 12 ,1667
NarrowAtTheBase>7 12 ,3333 ,3333
RoundHead >7 12 ,5000 ,5000 ,5000
Means for groups in homogeneous subsets are displayed. a. Uses Harmonic Mean Sample Size = 12,000.
Lampiran 7 Data deskriptif volume, motilitas, dan konsertrasi spermatozoa Descriptives
simmental 27 1073,3333 62,21001
limousin 25 1190,4000 42,80374
FH 23 1098,2609 62,49001
23 Lampiran 8 Hasil uji lanjut Duncan volume spermatozoa
volume Duncan
jenis N Subset for alpha = 0.05
1 2
limousin 25 6,6920
simmental 27 6,9889 6,9889
ongol 18 7,2722 7,2722
FH 23 8,1174
Sig. ,409 ,107
Lampiran 9 Hasil uji lanjut Duncan motilitas spermatozoa Motilitas
Duncan
jenis N Subset for alpha
= 0.05 1
FH 23 ,7050
simmental 27 ,7000
ongol 18 ,7031
limousin 25 ,7020
Sig. ,230
Lampiran 10 Hasil uji lanjut Duncan konsentrasi spermatozoa Consent
Duncan
jenis N Subset for alpha
= 0.05 1
simmental 27 1073,3333
FH 23 1098,2609
limousin 25 1190,4000
ongol 18 1193,3333
24